Клиническая фармакология и фармакотерапия: учебник. - 3-е изд., перераб. и доп. / под ред. В. Г. Кукеса, А. К. Стародубцева. - 2012. - 840 с.: ил.
|
|
|
|
ЧАСТЬ II. ФАРМАКОТЕРАПИЯ И ЧАСТНЫЕ ВОПРОСЫ ФАРМАКОЛОГИИ. Глава 10. АРТЕРИАЛЬНАЯ ГИПЕРТЕНЗИЯ
10.1. СИНДРОМ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ
Артериальная гипертензия (АГ) - синдром, который заключается в повышении уровня АД (систолическое АД >140 мм рт. ст. и /или диастолическое АД >90 мм рт. ст.).
Синдром АГ может сопровождать целый ряд заболеваний, но чаще единую этиологическую причину повышения АД выявить не удается - это так называемая эссенциальная (первичная или идиопатиче-ская) АГ. Распространены также и другие названия этого заболевания - гипертоническая болезнь, артериальная гипертония. Причины, вызывающие эссенциальную гипертензию, до сих пор недостаточно изучены, хотя среди всех больных с повышенным АД эссенциальная гипертензия встречается в 90-94% случаев.
Если причины повышения АД известны, принято говорить о вторичной или симптоматической АГ.
Эпидемиология АГ. АГ - важнейший фактор риска основных сердечно-сосудистых заболеваний, относится к наиболее частым патологическим состояниям сердечно-сосудистой системы. Повышение АД отмечают примерно у 25% всего взрослого населения в индустриально развитых странах. Повышенное АД диагностировано у 40% взрослого населения РФ. Только в США АГ становится причиной 100 млн обращений за медицинской помощью ежегодно, а на лечение больных АГ расходуют в среднем 31,7 млрд долларов в год. Осведомленность больных АГ о наличии заболевания в РФ составляет 77,9%. Антигипертензивные препараты принимают 59,4% больных АГ, лечение эффективно у 21,5%.
Этиология и патогенез вторичной АГ. Причиной вторичной АГ может быть только какое-либо заболевание (табл. 10-1). Наиболее часто АД повышается при заболеваниях почек, протекающих с задержкой жидкости и ионов натрия в организме. Некоторые опухоли могут продуцировать в большом количестве гормоны (альдостерон, тироксин, адренокортикотропный гормон) или биологически активные вещества (ренин), обладающие выраженным прессорным (повышающим
АД) эффектом. К этой группе заболеваний относят феохромоцито-му1 - опухоль надпочечников, продуцирующую катехоламины. АД при этом заболевании эпизодически повышается до очень высоких цифр. У беременных причиной повышения давления считают увеличение объема циркулирующей жидкости и нарушение функций почек (нефропатия беременных, эклампсия). Вторичная АГ часто обусловлена приемом ЛС - в первую очередь глюкокортикоидов и пероральных контрацептивов.
Таблица 10-1. Типы и причины АГ
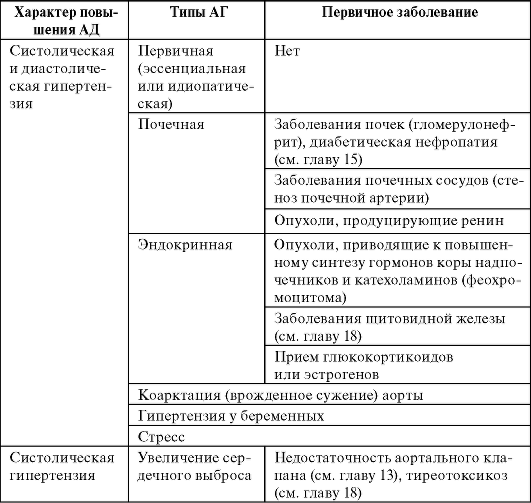
1 Применение БАБ при феохромоцитоме вызывает парадоксальное увеличение АД из-за блокады периферических β-адренорецепторов, расширяющих сосуды.
Этиология и патогенез эссенциальной АГ. Причины этой формы АГ в настоящее время остаются малоизученными. Предполагают, что развитию заболевания способствует ряд факторов, среди которых наибольшее значение имеет избыточное потребление поваренной соли, стресс1, уменьшение количества функционально активных нефронов2, генетические дефекты и ожирение. Таким образом, эссен-циальную АГ можно отнести к полиэтиологичным заболеваниям.
Уровень АД у человека зависит от сердечного выброса и сопротивления периферических сосудов. У больных с АГ увеличение сердечного выброса может быть обусловлено двумя главными причинами:
- увеличением объема жидкости, вызванным избытком ионов натрия (повышенным потреблением натрия, нарушением его выведения почками, повышенным синтезом альдостерона);
- увеличением сократимости сердечной мышцы под воздействием катехоламинов и чрезмерной симпатической иннервации (стрессом).
С другой стороны, катехоламины, ангиотензин II и ионы натрия вызывают сужение периферических сосудов и необратимую гипертрофию мышечного слоя стенки сосудов, что приводит к повышению периферического сосудистого сопротивления и эндотелиальной дисфункции.
В патогенезе АГ в основном участвуют прессорные системы организма - симпатоадреналовая и ренин-ангиотензин-альдостероновая система (РААС) - рис. 10-1. Вместе с тем длительному повышению уровня АД противодействуют центральные (ЦНС) и периферические (калликреин-кининовая система)3 депрессорные системы. Однако длительная существующая высокая активность прессорных факторов приводит к необратимым изменениям структуры почек и сосудистой стенки и к «закреплению» повышенного уровня АД.
РААС имеет особое значение в регуляции АД, она определяет ОЦК, АД и функции сердечно-сосудистой системы. РААС активируется в ответ на уменьшение ОЦК, снижение АД и при повышении активности симпатической нервной системы.
1 Стресс - патологическое состояние, характеризуется чрезмерной активацией симпатоадреналовой системы и повышенной продукцией катехоламинов под воздействием внешних или внутренних раздражителей.
2 Нефрон - структурная и функциональная единица почек.
3 Каллекреин-кининовая система синтезирует кинины (брадикинин) - активные соединения, обладающие гипотензивным действием. Синтез этих соединений происходит в почках.
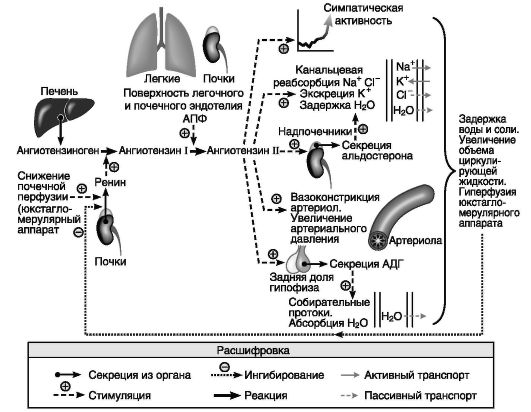
Рис. 10-1. Ренин-ангиотензин-альдостероновая система
РААС участвует в регуляции АД и объема жидкости, так как ренин катализирует превращение ангиотензиногена в ангиотензин I, который с помощью АПФ1 трансформируется в ангиотензин II. Ангиотензин II, действующий через рецепторы четырех типов - AT1, AT2, AT3, AT4, выполняет функцию центрального действующего звена РААС. Наиболее хорошо изучены первые два - рецепторы к ангиотензину II 1-го (АТ1) и 2-го (АТ2) типа. В организме человека рецепторов типа АТ1 значительно больше, чем АТ2, таким образом, эффекты от стимуляции ангиотензином II в основном обусловлены стимуляцией АТ1-рецепторов: артериальная вазоконстрикция и особенно повышение гидравлического давления в почечных клубочках (вазоконстрикция приносящих и в еще большей степени выносящих артериол), сокращение мезанги-альных клеток и снижение почечного кровотока, усиление реабсорбции натрия в проксимальных почечных канальцах, секреция альдостерона
1 АПФ - ангиотензинпревращающий фермент.
корой надпочечников, секреция вазопрессина, эндотелина-1, высвобождение ренина, усиление высвобождения норадреналина из симпатических нервных окончаний, активация симпатоадреналовой системы (центральная на пресинаптическом уровне и периферическая в надпочечниках), стимуляция процессов ремоделирования сосудов и миокарда (пролиферация и миграция гладкомышечных клеток сосудов, гиперплазия интимы, гипертрофия кардиомиоцитов и фиброз миокарда).
Кардиоваскулярные эффекты ангиотензина II, опосредованные АТ2-рецепторами, противоположны эффектам, обусловленным возбуждением АТ1-рецепторов, и менее выражены. Рецепторы типа AT2 в изобилии представлены в тканях плода, в тканях взрослого человека они обнаружены в миокарде, мозговом веществе надпочечников, в почках, репродуктивных органах, мозге, через них регулируется клеточный апоптоз. Стимуляция рецепторов АТ2 сопровождается вазодилатацией, ингибированием клеточного роста, подавлением пролиферации клеток (эндотелиальных и гладкомышечных клеток сосудистой стенки, фибробластов), торможением гипертрофии кар-диомиоцитов. Кроме того, увеличивается продукция оксида азота (NO). Также существует проренин - предшественник ренина, который ранее рассматривали как неактивную молекулу. Однако данные последних исследований свидетельствуют о том, что проренин может обладать ангиотензин I-образующей активностью. Ренин и проренин также обладают прямыми эффектами посредством взаимодействия с недавно открытыми рецепторами к (про)ренину.
Повышенный уровень АД у больных АГ опасен из-за целого ряда осложнений. У таких пациентов увеличен риск атеросклероза и развития ИБС (см. главуу 11) или цереброваскулярных заболеваний [острое нарушение мозгового кровообращения (ОНМК)]. Повышенное АД вызывает повреждение, гибель нефронов и развитие почечной недостаточности; повреждение сосудов сетчатки и заболевания артерий нижних конечностей. Увеличение постнагрузки вызывает гипертрофию миокарда, прогрессирование которой приводит к развитию сердечной недостаточности (см. главу 14). Органы, в которых чаще всего развиваются патологические изменения, получили название органов-мишеней (табл. 10-2).
Факторы риска АГ. Уровень АД считают важнейшим, но далеко не единственным фактором, определяющим тяжесть АГ, ее прогноз и тактику лечения. Большое значение имеет оценка общего сердечнососудистого риска, степень которого зависит от величины АД, а также от наличия или отсутствия сопутствующих факторов риска, поражения органов-мишеней и сопутствующих клинических состояний.
Таблица 10-2. Факторы, наличие которых отрицательно влияет на прогноз у больных АГ
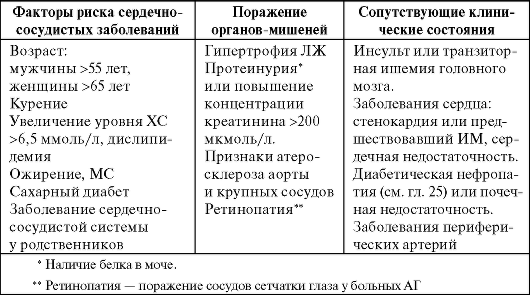
Классификация АГ. Тяжесть течения заболевания оценивают по величине АД. От этого показателя в первую очередь зависит риск осложнений и продолжительность жизни больных (табл. 10-3). Кроме того, наличие поражения органов-мишеней и ряда сопутствующих состояний, а также курение и пожилой возраст отрицательно влияют на прогноз АГ (см. табл. 10-2).
Симптомокомплекс АГ. Обычно заболевание протекает бессимптомно, что затрудняет его своевременную диагностику. Больные АГ чаще всего жалуются на головную боль, головокружение, нарушение зрения, общее плохое самочувствие, также возможны сенсорные и двигательные нарушения, сердцебиение, одышка, сухость во рту, ощущение «приливов», жара, похолодание конечностей. Вместе с тем часто выявляют симптомы других заболеваний (ИБС, ОНМК, почечную недостаточность), осложняющих течение АГ.
Заболевание может протекать с внезапными повышениями АД (ГК) различной продолжительности (от нескольких часов до нескольких суток). ГК1, как правило, развивается у больных, не получающих адекватного лечения, или при резком прекращении приема гипотензивных препаратов, а также при стрессе, резких метеорологических изменениях или вследствие избыточного потребления соли и жидкости.
ГК - гипертонический криз (см. главу 10.12).
Таблица 10-3. Классификация степени повышения АД у больных с АГ, предложенная ВОЗ и Международным обществом по артериальной гипертензии в 1999 г.
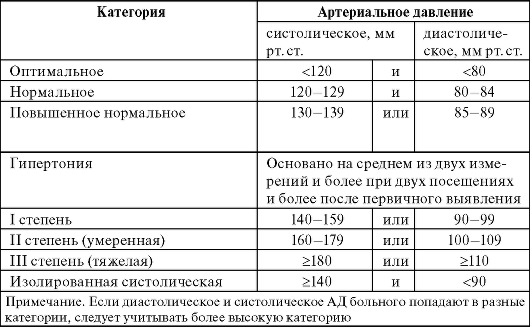
Течение и тяжесть заболевания. Вторичная АГ развивается обычно в молодом возрасте и характеризуется быстрым прогрессированием и частыми кризами. Эссенциальной АГ, напротив, свойственно медленное прогрессирование, заболевание многие годы может протекать бессимптомно (повышение АД у таких больных впервые отмечают после 30-40 лет). Постепенно с прогрессированием заболевания появляются поражения органов-мишеней и развиваются другие заболевания сердечно-сосудистой системы. Появление осложнений свидетельствует о тяжелом течении заболевания и увеличении риска развития
ИМ и ОНМК.
Наиболее прогностически неблагоприятная форма течения АГ, дающая большое количество осложнений, инвалидизации, утраты работоспособности и летальных исходов - кризовое течение.
Диагноз и методы обследования. Диагноз АГ ставят на основании наличия у больного повышенного АД (повышение АД должно быть зарегистрировано не менее двух раз на двух последовательных визитах в положении больного сидя). Исключается употребление кофе и крепкого чая за 1 ч перед исследованием; рекомендуют не курить в течение 30 мин до измерения АД; отменяют прием симпатомимети-
ков, включая назальные и глазные капли; АД измеряют в покое после отдыха в течение 5 мин; если процедуре измерения АД предшествует значительная физическая или эмоциональная нагрузка, период отдыха следует продлить до 15-30 мин.
Обследование больных преследует две основные цели.
• Исключение вторичного характера АГ:
- биохимический анализ крови (повышение концентрации мочевины и креатинина характерно для ХПН);
- ультразвуковое исследование (УЗИ) органов брюшной полости, а также компьютерная томография и сцинтиграфия (позволяет выявить некоторые заболевания почек и надпочечников, вызывающих АГ);
- ультразвуковая допплерография почечных артерий: позволяет выявить стеноз (сужение) почечной артерии (при стенозе снижается приток крови к почкам, что, в свою очередь, вызывает активацию РААС) и контрастные методы исследования (ангиография);
- исследование концентрации гормонов щитовидной железы, кортизола (гормон коры надпочечников), метаболитов катехо-ламинов в моче (увеличивается при феохромоцитоме);
- рентгенография черепа (зона турецкого седла) для исключения опухоли гипофиза1;
- измерение АД на нижних конечностях и УЗИ брюшной аорты для исключения коарктации (врожденного сужения) аорты.
• Определение состояния органов-мишеней:
- эхокардиография (ЭхоКГ) (гипертрофия миокарда) и доппле-рография крупных сосудов (атеросклероз);
- ЭКГ (гипертрофия миокарда, признаки ишемии и /или рубцовых изменений миокарда);
- исследование мочи на наличие белка;
- исследование глазного дна;
- концентрация глюкозы в крови (исключение СД);
- неврологический осмотр (выявление гипертонической энцефалопатии), в том числе магнитно-резонансная томография головного мозга, ультразвуковая допплерография магистральных артерий.
1 Гипофиз - непосредственно связанная с головным мозгом железа внутренней секреции, гормоны, выделяемые этой железой, регулируют функции других желез внутренней секреции.
Важную информацию о состоянии сердечно-сосудистой системы дает суточное мониторирование АД. Посредством этого метода можно определить суточную вариабельность АД, ночную артериальную гипотензию и гипертензию, проследить связь с эмоциональным фоном обследуемого. Все эти факторы имеют значение при выборе антигипертензивных препаратов и при оценке их эффективности. Необходимо также отметить наличие у некоторых пациентов гипертонии «белого халата» с низким риском сердечно-сосудистых заболеваний, которую также можно выявить с помощью данного метода.
Клинико-фармакологические подходы к лечению артериальной гипертензии
Лечение вторичной АГ заключается прежде всего в коррекции основного заболевания, ЛС с гипотензивным действием выполняют функцию симптоматической терапии.
Согласно современным национальным рекомендациям, рекомендациям Европейского общества по артериальной гипертензии и Европейского общества кардиологов, тактика лечения эссенциаль-ной АГ зависит от уровня АД и степени риска кардиоваскулярных осложнений. Основной целью лечения считают максимальное снижение риска развития сердечно-сосудистых осложнений и смерти от них. Основные задачи лечения - нормализация АД, предупреждение осложнений при отсутствии или минимальном уровне НЛР, коррекция всех модифицируемых факторов риска (курение, дисли-пидемия, гипергликемия, ожирение), предупреждение и замедление темпа прогрессирования и /или уменьшение поражения органов-мишеней, а также лечение ассоциированных и сопутствующих заболеваний (ИБС, СД).
При лечении пациентов с АГ необходимо поддерживать АД ниже 140/90 мм рт. ст., что называют целевым уровнем. При хорошей переносимости назначенного лечения целесообразно снижение АД до более низких значений. У пациентов с высоким и очень высоким риском сердечно-сосудистых осложнений необходимо снизить АД до 140/90 мм рт. ст. и менее за 4 нед. Затем при условии хорошей переносимости рекомендуют снижение АД до 130/80 мм рт. ст. и менее. У пациентов с ИБС уровень АД необходимо снижать до целевого значения 130/85 мм рт. ст. У больных СД и /или заболеваниями почек целевой уровень АД должен составлять менее 130/85 мм рт. ст.
При низком риске развития осложнений лечение начинают с мероприятий, направленных на изменение образа жизни больно-
го. Изменение образа жизни и питания следует рекомендовать всем пациентам, независимо от тяжести АГ. Следует попытаться устранить все относительно обратимые факторы, а также повышенные концентрации холестерина (ХС) и /или глюкозы в крови. Среди рекомендаций по изменению образа жизни особенно актуальны следующие:
- снижение избыточной массы тела [индекс массы тела (ИМТ) <25 кг/ м2];
- ограничение потребления поваренной соли до 5 г и менее в сутки;
- отказ от курения;
- снижение потребления алкогольных напитков - <30 г алкоголя в сутки для мужчин и 20 г для женщин;
- регулярные физические упражнения умеренной интенсивности продолжительностью не менее 30-60 мин на открытом воздухе 3-4 раза в неделю;
- изменение режима питания с увеличением потребления растительной пищи, калия, кальция (содержатся в овощах, фруктах, зерновых) и магния (содержится в молочных продуктах), а также уменьшением потребления животных жиров.
Перечисленные меры позволяют, с одной стороны, снизить скорость прогрессирования заболевания, а с другой - уменьшить дозы гипотензивных препаратов.
Необходимо разъяснить больному цели лечения и обучить технике измерения АД (самостоятельно или при помощи близких), научить принимать правильные решения в конкретных клинических ситуациях (например, первая помощь при гипертоническом кризе). Больному следует разъяснить важность немедикаментозных лечебных мероприятий (ограничение поваренной соли, снижение массы тела и т.д.).
Если у больного с низким риском осложнений эти мероприятия не позволяют нормализовать уровень АД на протяжении 6-12 мес, следует переходить к назначению гипотензивных прпаратов. У больных с АГ II-III степени, высоким риском развития сердечно-сосудистых осложнений, поражением органов-мишеней и наличием сопутствующих заболеваний медикаментозное лечение начинают незамедлительно и параллельно проводят немедикаментозное лечение.
Классификация лекарственных средств, применяемых для лечения артериальной гипертензии
В настоящее время для лечения АГ рекомендованы пять основных классов антигипертензивных препаратов:
• ИАПФ1 - каптоприл, эналаприл, периндоприл, лизиноприл, фозиноприл, хинаприл, трандолаприл и др.
• Блокаторы рецепторов AT1 (БРА) - валсартан, лозартан, телми-сартан, кандесартан, ирбесартан и др..
• БМКК2 - нифедипин, амлодипин.
• БАБ3 - карведилол, бисопролол, небиволол, метопролол, атенолол.
• Тиазидные и тиазидоподобные диуретики - гидрохлортиазид, индапамид и др.
В качестве дополнительных классов антигипертензивных препаратов для комбинированного лечения можно использовать α-адреноблокаторы (празозин, доксазозин), агонисты имидазолиновых рецепторов (моксонидин), прямой ингибитор ренина (алискирен).
При выборе антигипертензивного препарата в первую очередь надо оценить эффективность, вероятность развития побочных эффектов и преимущества ЛС в определенной клинической ситуации (табл. 10-4, 10-5).
На выбор препарата оказывают влияние многие факторы, наиболее важными из которых считают:
- наличие у больного факторов риска;
- поражение органов-мишеней;
- сопутствующие клинические состояния, поражения почек, метаболический синдром (МС), СД;
- сопутствующие заболевания, при которых необходимы назначения или ограничения применения антигипертензивных препаратов различных классов;
- предыдущие индивидуальные реакции больного на препараты различных классов;
- вероятность взаимодействия с препаратами, которые пациенту назначены по другим поводам;
- социально-экономические факторы, включая стоимость лечения.
ИАПФ - ингибиторы ангиотензинпревращающегося фермента. БМКК - блокаторы медленных кальциевых каналов. БАБ - блокаторы β-адренорецепторов.
Таблица 10-4. Преимущественные показания к назначению различных групп антигипертензивных препаратов
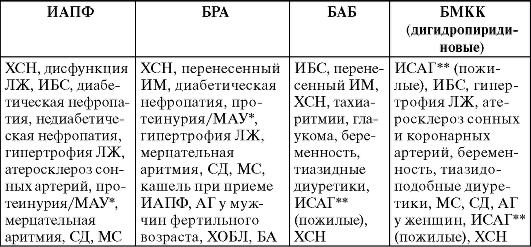
* МАУ - микроальбуминурия.
** ИСАГ - изолированная систолическая артериальная гипертензия.
Таблица 10-5. Абсолютные и относительные противопоказания к назначению различных групп антигипертензивных препаратов
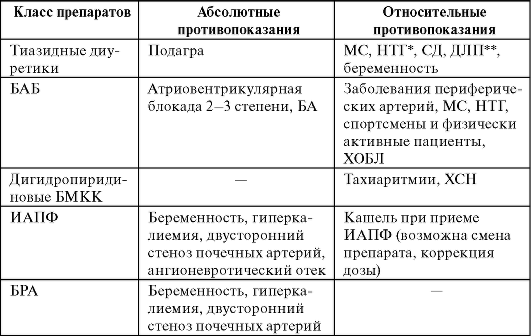
* НТГ - нарушение толерантности к глюкозе. ** ДЛП - дислипопротеидемия.
Начинать лечение необходимо с назначения одного ЛС в минимальной суточной дозе (эта рекомендация не касается больных с тяжелой АГ или лиц, у которых предшествующее лечение было неэффективно). Прием новых препаратов следует начинать с низких доз, целью каждого очередного этапа лечения должно быть снижение уровня АД на 10-15 мм рт. ст. У пациентов с II и III степенью АГ рекомендовано начинать лечение с комбинированного назначения двух (а иногда и трех) рационально подобранных ЛС. Если АД не снижается до желаемого уровня, дальнейшее лечение проводят путем постепенного увеличения доз или присоединения новых ЛС. Неэффективные ЛС (не вызывающие снижение АД на 10-15 мм рт. ст.) и препараты, вызывающие НЛР, следует заменить.
Единых рекомендаций относительно того, с каких именно ЛС следует начинать лечение больного, не существует. Выбор препарата зависит от возраста, пола и наличия сопутствующих заболеваний. У пациентов с АГ тяжелого течения и при неэффективности лечения одним препаратом назначают сочетания ЛС.
Комбинированная антигипертензивная терапия имеет много преимуществ.
• Усиление антигипертензивного эффекта путем разнонаправленного действия препаратов на патогенетические механизмы развития АГ, что увеличивает число пациентов со стабильным снижением АД.
• Уменьшение частоты возникновения побочных эффектов благодаря как меньшим дозам комбинируемых антигипертензивных препаратов, так и взаимной нейтрализации этих эффектов.
• Обеспечение наиболее эффективной органопротекции и уменьшение риска и частоты сердечно-сосудистых осложнений.
Назначение препаратов в виде комбинированного лечения должно отвечать следующим условиям:
• препараты должны иметь взаимодополняющее действие;
• при их совместном применении достигаются лучшие результаты;
• препараты должны иметь близкие фармакодинамические и фар-макокинетические показатели, что особенно важно для фиксированных сочетаний.
Сочетание двух антигипертензивных препаратов делят на рациональные (эффективные), возможные и нерациональные. Все преимущества комбинированного лечения присущи только рациональным комбинациям антигипертензивных препаратов.
К ним относятся:
- ИАПФ + диуретик;
- БРА + диуретик;
- ИАПФ + дигидропиридиновый БМКК;
- БРА + дигидропиридиновый БМКК;
- дигидропиридиновый БМКК + БАБ;
- дигидропиридиновый БМКК + диуретик;
- БАБ + диуретик;
- БАБ + α-адреноблокатор.
Для комбинированного лечения АГ можно использовать как нефиксированные, так и фиксированные комбинации препаратов (два препарата в одной таблетке).
К преимуществам фиксированных (официнальных) сочетаний можно отнести:
- потенцирование антигипертензивного эффекта препаратов;
- простоту назначения и процесса титрования дозы;
- уменьшение частоты возникновения побочных эффектов (низкая доза, взаимная нейтрализация НЛР);
- увеличение приверженности пациентов лечению;
- уменьшение стоимости лечения.
В настоящее время существует достаточно много официнальных комбинированных препаратов: Капозид* (каптоприл + гидрохлор-тиазид), Ко-ренитек* (эналаприл + гидрохлортиазид), Нолипрел* (периндоприл + индапамид), Аккузид* (хинаприл + гидрохлортиазид), Ко-диован* (валсартан + гидрохлортиазид), Гизаар* (лозартан + гидрохлортиазид), Эксфорж* (валсартан + амлодипин), Экватор* (лизиноприл + амлодипин), Логимакс* (метопролол + фелодипин), Тарка* (верапамил + трандолаприл) и др.
Контроль эффективности лечения артериальной
гипертензии
При оценке эффективности лечения АГ выделяют следующие моменты.
• Краткосрочные цели:
- снижение систолического и /или диастолического АД на 10% и более;
- отсутствие гипертонических кризов;
- сохранение или улучшение качества жизни.
• Среднесрочные цели:
- достижение целевых значений АД;
- отсутствие поражения органов-мишеней или обратная динамика имевшихся осложнений;
- устранение модифицируемых факторов риска.
• Наконец, долгосрочной целью лечения считают стабильное поддержание АД на целевом уровне и отсутствие прогрессирования поражения органов-мишеней.
Эффективность лечения контролируют на основании регулярного измерения АД и регулярных медицинских обследований больного (см. раздел «Диагноз и методы обследования»).
Контроль безопасности лечения АГ. При назначении празозина, клонидина, гуанетидина существует опасность развития ортостати-ческого коллапса, и АД измеряют в положении пациента лежа и стоя. Разница в 20 мм рт. ст. свидетельствует о высокой вероятности развития у больного ортостатической гипотензии.
Большинство препаратов, снижающих сосудистый тонус (нитраты, БМКК, неселективные α-адреноблокаторы), вызывают рефлекторную тахикардию, в то же время некоторые препараты способны вызвать брадикардию, снижение силы сердечных сокращений и внутрисер-дечной проводимости (агонисты центральных α-адренорецепторов, симпатолитики, пирроксан).
При назначении ИАПФ, БРА, индапамида следует контролировать концентрацию калия в плазме крови.
При приеме метилдопы, теразозина, ИАПФ возможно развитие анемии, лейкопении, а при назначении нифедипина - еще и тром-боцитопении.
Кроме того, при назначении БАБ, центральных α-адреномиметиков, симпатолитиков, ИАПФ следует помнить о возможности усиления тонуса бронхов и появления бронхоспазма, а при лечении симпатоли-тиками - о появлении боли в эпигастральной области.
10.2. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ ИНГИБИТОРОВ АНГИОТЕНЗИНПРЕВРАЩАЮЩЕГО
ФЕРМЕНТА
Поиск ЛС, регулирующих активность РААС, начался в 60-е годы XX в., сразу же после того как было выяснено ее значение в патогенезе АГ. Первым эффективным регулятором активности РААС стал ИАПФ каптоприл, который используют в клинической практике
с 1979 г.
Существуют пять групп ЛС, регулирующих активность РААС.
• БАБ: блокируют Р1-адренорецепторы юкстагломерулярного аппарата почек, снижают синтез, выделение ренина и косвенно АТ II.
• ИАПФ: снижают концентрацию АТ II, путем блокады основного фермента, катализирующего переход АТ I в АТ II.
• БРА: препятствуют взаимодействию АТ II с тканями-мишенями посредством АТ1-рецепторов, но при этом АТ II взаимодействует с АТ2-рецепторами.
• Блокаторы альдостероновых рецепторов: препятствуют взаимодействию альдостерона с тканями-мишенями.
• Селективный ингибитор ренина: связываясь с молекулой ренина, предотвращает связывание ренина с ангиотензиногеном и тем самым снижает образование АТ II.
Классификация ингибиторов ангиотензинпревращающего фермента
В основу классификации ИАПФ положен фармакокинетиче-ский принцип: различают группу активных препаратов (каптоприл и лизиноприл) и пролекарств (остальные ИАПФ), из которых в печени образуются активные метаболиты, оказывающие лечебные эффекты (табл. 10-6).
Таблица 10-6. Классификация ИАПФ по Opie, 1999

Фармакокинетика ингибиторов ангиотензинпревращающего фермента
Фармакокинетические особенности наиболее часто назначаемых ИАПФ представлены в табл. 10-7.
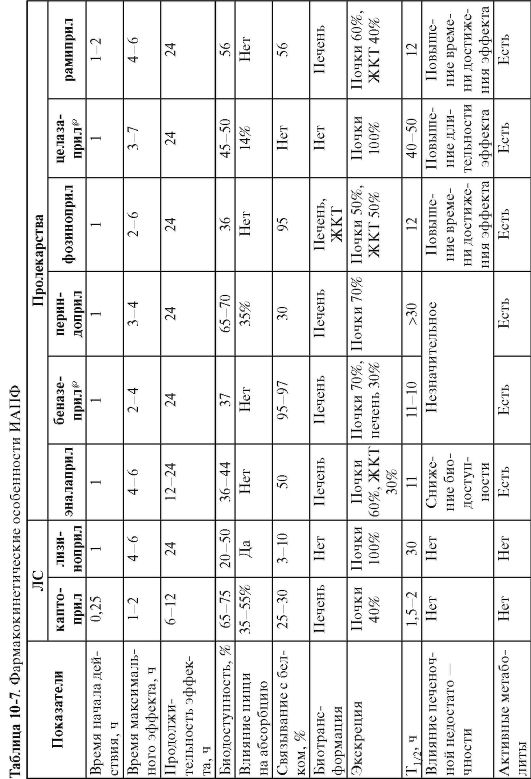
Фармакодинамика ингибиторов ангиотензинпревращающего фермента
Фармакодинамика ИАПФ связана с подавлением основного пути синтеза АТ II, что обусловливает их антигипертензивный эффект, положительное действие на функции сердца при ХСН и ИБС (табл. 10-8).
Таблица 10-8. Основные фармакологические свойства ИАПФ
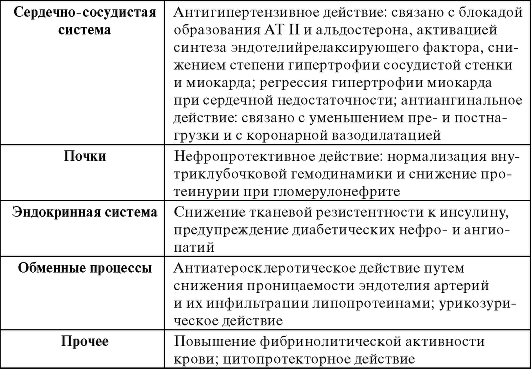
Прием ИАПФ приводит к снижению сосудистого тонуса, а у больных с АГ - системного АД. Следует отметить, что снижение АД под влиянием ИАПФ не сопровождается развитием тахикардии. Различают «острый» и «хронический» антигипертензивный эффект препаратов.
«Острый» эффект обусловлен снижением концентрации АТ II в циркуляторном русле и накоплением брадикинина в эндотелии при снижении скорости его деградации. Брадикинин непосредственно вызывает снижение тонуса гладких мышц сосудистой стенки, а также способствует высвобождению эндотелийрелаксирующих факторов - окиси азота и простагландина E2. Это может привести к падению перфузионного давления в почках и увеличению образования ренина, что вызывает феномен «ускользания» - уменьшение
гипотензивного действия препаратов в течение 7-10 сут. При дальнейшем приеме ИАПФ снижается образование альдостерона, усиливается выведение натрия и воды, что стабилизирует антигипер-тензивное действие.
«Хронический» антигипертензивный эффект препаратов возникает при длительном (несколько месяцев или лет) приеме и обусловлен их способностью снижать выраженность гипертрофии (в основном посредством соединительнотканных компонентов) мышечного слоя сосудистой стенки и миокарда. Торможение роста, пролиферации гладкомышечных клеток и фибробластов в медии артерий приводят к увеличению их просвета, а также восстанавливает или улучшает эластичность артериальной стенки. Восстановление структуры миокарда, с одной стороны, способствует нормализации центральной гемодинамики, с другой - понижает уровень периферического сосудистого сопротивления путем рефлекторных механизмов.
На фоне длительного приема ИАПФ существенно снижаются (примерно на 8% в год) риск развития ИМ и смертность больных.
Поскольку ИАПФ увеличивают экскрецию мочевой кислоты, они должны быть препаратами первого выбора у пациентов с подагрой. Однако следует помнить, что сильный урикозурический эффект может способствовать образованию мочекислых камней.
Клиническое применение ингибиторов ангиотензинпревращающего фермента
К основным показаниям к назначению ИАПФ относят следующие:
• артериальную гипертензию любой этиологии (в качестве монотерапии и в комбинации с диуретиками и антигипертензивными средствами других групп);
• купирование гипертонических кризов (для каптоприла);
• ХСН;
• систолическую и диастолическую дисфункцию ЛЖ;
• ИБС (для уменьшения инфарктной зоны, дилатации коронарных сосудов и снижения дисфункции при реперфузии, снижения риска развития повторного ИМ);
• диабетическую ангиопатию (в частности, для замедления про-грессирования диабетической нефропатии);
• диагностику реноваскулярной гипертензии и первичного альдо-стеронизма (однократный прием каптоприла).
Контроль за эффективностью и безопасностью назначения ингибиторов ангиотензинпревращающего фермента
Эффективность лечения ИАПФ при АГ определяется динамикой
АД.
Для контроля за безопасностью лечения необходимо также измерять АД для исключения возможной гипотонии. Гипотония развивается чаще у больных с ХСН, почечной недостаточностью, стенозом почечных артерий, из-за чего прием первой дозы препарата необходимо проводить сидя или лежа. Развитие гипотонии требует снижения дозы препарата с последующей титрацией под контролем уровня АД.
Для исключения роста уратных камней у больных с мочекаменной болезнью необходимо определять концентрацию уратов в моче, а для исключения гипогликемии у больных с СД - контролировать концентрацию глюкозы в крови.
Нежелательные лекарственные реакции
ИАПФ - одни из наиболее безопасных гипотензивных препаратов. Мужчины лучше переносят длительное лечение этими ЛС, чем женщины.
Наиболее частой НЛР (от 1 до 48% при лечении разными ИАПФ) считают сухой кашель, что в ряде случаев требует отмены препарата. Механизм его возникновения чаще всего связывают с повышением концентрации брадикинина в бронхиальной ткани. Как правило, кашель не зависит от дозы препарата.
Вторая по частоте (от менее 1 до 10-15% при сердечной недостаточности) НЛР ИАПФ - развитие ортостатической гипотензии, так называемого «эффекта первой дозы», который встречается у пациентов с высокой активностью РААС. Также способствует развитию гипотензивной реакции одновременный прием мочегонных и других гипотензивных средств.
У больных с сердечной недостаточностью (реже - с АГ) ИАПФ могут ухудшать клубочковую фильтрацию и другие функции почек, причем частота этих НЛР увеличивается при продолжительном приеме. Чаще всего это происходит на фоне скрытой патологии почек и (или) у больных, получающих мочегонные и НПВС.
Клинически значимая гиперкалиемия (более 5,5 ммоль/л) наблюдается в основном у больных с патологией почек. Так, при почечной недостаточности ее частота колеблется от 5 до 50%.
В 0,1-0,5% случаев на фоне лечения ИАПФ развивается ангио-невротический отек (отек Квинке), причем у женщин в 2 раза чаще, чем у мужчин.
В ряде случаев ИАПФ могут вызвать цитопению (чаще лейкопению, реже тромбо- и панцитопению). Механизм данной НЛР связан с тем, что одним из субстратов для АПФ служит циркулирующий в крови пептид N-ацетил-серил-аспартил-лизил-пролин, выполняющий функцию отрицательного регулятора гемопоэза. При блокаде фермента количество этого пептида в крови может увеличиваться. При приеме ИАПФ могут развиваться и такие неспецифичные побочные эффекты, как головокружение, головная боль, утомляемость, слабость, диспепсические явления (тошнота, диарея), нарушения вкусовых ощущений и кожные высыпания.
Прием ИАПФ в II и III триместрах беременности приводит к развитию артериальной гипотензии, гипоплазии черепа, анурии, обратимой и необратимой почечной недостаточности и смерти плода. Кроме того, возможны уменьшение количества околоплодной жидкости, развитие контрактур суставов, черепно-лицевых деформаций и гипоплазии легких.
Противопоказания к применению ИАПФ
Абсолютные: непереносимость препаратов; аллергические реакции; беременность и лактация; двусторонний стеноз почечных артерий (повышается возможность резкой гипотензии), тяжелая ХПН (концентрация креатинина в сыворотке крови более 300 ммоль/л), выраженная гиперкалиемия (более 5,5 ммоль/л); гипертрофическая кардиомиопатия с обструкцией выносящего тракта ЛЖ, гемодина-мически значимый стеноз аортального или митрального клапанов, констриктивный перикардит, трансплантация внутренних органов.
Относительные: гипотония; умеренная ХПН, умеренная гиперкалие-мия (5,0-5,5 ммоль/л), подагрическая почка (обладая урикозурическим действием, ИАПФ могут ускорить рост уратных камней); цирроз печени, хронический активный гепатит; облитерирующий атеросклероз артерий нижних конечностей; тяжелые обструктивные заболевания легких.
Взаимодействие ИАПФ с другими ЛС
Наиболее значимое фармакокинетическое взаимодействие у ИАПФ отмечается с антацидами, содержащими гидроокись алюминия или (и) магния. Эти антациды нарушают всасывание из пищеварительного тракта каптоприла и фозиноприла.
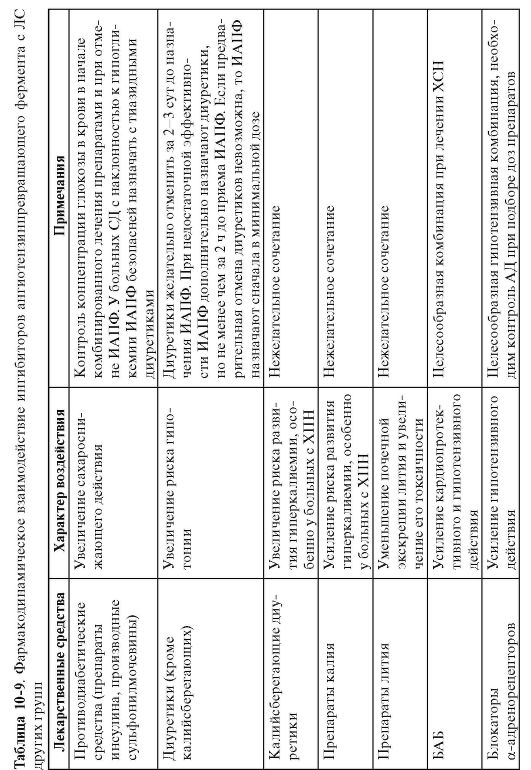
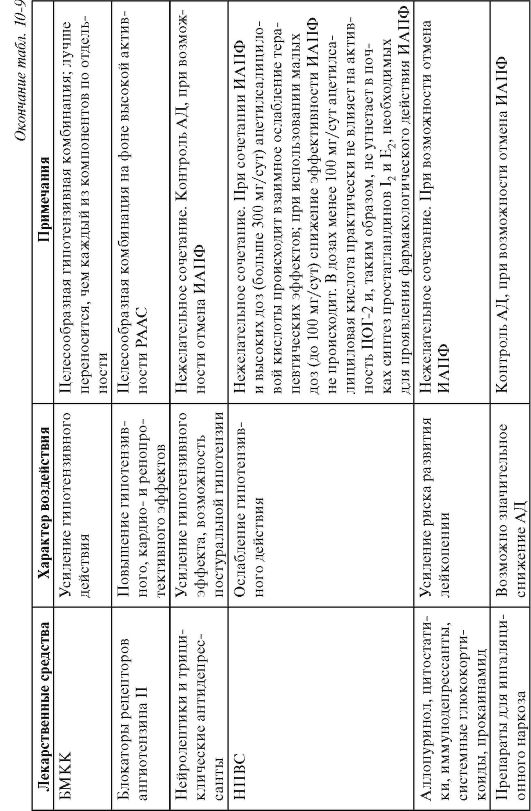
Более важным для клинической практики считают фармакоди-намическое взаимодействие ИАПФ с другими, отличными от них по механизму действия, группами препаратов (табл. 10-9).
Характеристика основных препаратов
Каптоприл (Капотен*). Сила, с которой каптоприл связывается с ангиотензинпревращающим ферментом, невысока, что обусловливает назначение больших доз. У каптоприла в группе ИАПФ наименьшая продолжительность действия (6-8 ч по сравнению с 24 ч у других препаратов), но наиболее раннее наступление эффекта, что позволяет использовать его сублингвально для экстренной помощи при гипертензивных состояниях. При приеме каптоприла под язык антигипертензивный эффект наступает через 5-15 мин. Важным отличием каптоприла от других ИАПФ считают наличие SH-группы, которая определяет его основные побочные эффекты - нефротоксичность и связанную с ней протеинурию (при дозе более 150 мг/сут), холестаз, нейтропению (как правило, у больных с диффузными заболеваниями соединительной ткани и нарушением функций почек при длительном приеме). Вместе с тем наличие у кап-топрила SH-группы способствует проявлению антиоксидантного действия, усиливает коронарный кровоток и повышает чувствительность тканей к инсулину.
Использование каптоприла у больных острым ИМ приводит к достоверному снижению смертности. Длительный прием препарата - более 3 лет - снижает риск развития повторного ИМ на 25%, а риск смерти от него - на 32%.
Пробу с каптоприлом используют в радиоизотопной диагностике реноваскулярной гипертензии и биохимической диагностике первичного гиперальдостеронизма (болезни Кона).
Эналаприл (Ренитек*) в печени трансформируется в эналаприлат (40-60% от принятой внутрь дозы), обладающий высокой степенью связывания с ангиотензинпревращающим ферментом.
При назначении эналаприла для лечения АГ за 2-3 сут следует временно отменить диуретики, при невозможности этого начальную дозу препарата (5 мг) уменьшают в 2 раза. Также первые дозы эна-лаприла должны быть минимальны у больных с исходно высокой активностью РААС. Оценку эффективности назначенной дозы проводят каждые две недели. Препарат назначают 1-2 раза в сутки.
Лизиноприл (Диротон*) - активный метаболит эналаприла. Снижение АД отмечают через 1 ч после приема препарата. При назна-
чении лизиноприла 1 раз в сутки его стабильная концентрация в крови достигается через 3 сут. Препарат выделяется почками в неизмененном виде, при почечной недостаточности обладает выраженной кумуляцией (период полувыведения возрастает до 50 ч). У пожилых пациентов его концентрация в крови в 2 раза выше, чем у молодых. При внутривенном введении лизиноприла его антигипертензивное действие начинается через 15-30 мин, что позволяет использовать его для купирования гипертонических кризов.
Периндоприл (Престариум*) - пролекарство, в печени трансформируется в активный метаболит периндоприлат (20% от введенного периндоприла), обладающий высокой степенью связывания с ангио-тензинпревращающим ферментом. Препарат снижает гипертрофию сосудистой стенки и миокарда. В сердце на фоне его приема уменьшается количество субэндокардиального коллагена.
Рамиприл (Тритаце*) в печени трансформируется в рамиприлат, обладающий высокой степенью связывания с ангиотензинпревра-щающим ферментом. Важное клиническое значение имеют две фар-макокинетические особенности рамиприла - медленное выведение из организма и двойной путь элиминации (до 40% препарата выводится с желчью). Однако при выраженной почечной недостаточности (скорость клубочковой фильтрации 5-55 мл/мин) его дозу рекомендовано снизить вдвое.
Трандолаприл (Гоптен*) по влиянию на тканевой АПФ в 6-10 раз превосходит эналаприл. Хотя трандолаприл считается пролекарством, он сам по себе обладает фармакологической активностью, но тран-долаприлат в 7 раз более активен, чем трандолаприл. Гипотензивное действие препарата при однократном приеме продолжается до 48 ч.
Моэксиприл (Моэкс*) становится активным после биотрансформации в печени в моэксиприлат. В отличие от большинства ИАПФ имеет двойной путь выведения: до 50% моэксиприла выводится с желчью, что делает его более безопасным у больных почечной недостаточностью.
Моэксиприл преимущественно назначают для лечения АГ, его антигипертензивный эффект продолжается до 24 ч.
Фозиноприл (Моноприл*) относится к пролекарствам, превращаясь в печени в активное вещество фозиноприлат.
Препарат имеет двойной путь выведения: его элиминация идет в равной степени и через почки, и через печень. При почечной недостаточности выделение фозиноприла из организма через печень усиливается, а при печеночной - через почки, что позволяет не кор-
ректировать дозу препарата при наличии данных заболеваний у пациентов.
Препарат применяют 1 раз в сутки.
Фозиноприл редко вызывает развитие сухого кашля; при появлении данного осложнения на фоне приема каких-либо ИАПФ рекомендовано переходить на фозиноприл.
10.3. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ БЛОКАТОРОВ РЕЦЕПТОРОВ АНГИОТЕНЗИНА II
Прием ИАПФ не обеспечивает полного прекращения образования АТ II в органах и тканях больных людей из-за существования независимого от АПФ пути образования АТ II из АТ I. Он может происходить при помощи катепсина G, тонина, тканевого активатора плазминогена, эндотелиальной пептидилдипептидазы, почечной карбоксипептидазы, химостатинчувствительного АТ II-образующего фермента (CAGE) и химазы. Последний фермент представляет собой сериновую протеинкиназу сердца и способствует образованию до 80% миокардиального АТ II. Из-за этого у некоторых больных терапевтический эффект ИАПФ недостаточен, и в данном случае большое значение приобретают БРА, ограничивающие его биологическое действие в тканях.
В настоящее время в мировой лечебной практике используют несколько синтетических непептидных селективных АТ1-блокаторов - валсартан, ирбесартан, кандесартан, лозартан, телмисартан и эпросартан.
Существует несколько классификаций антагонистов рецепторов ангиотензина II: по химической структуре, фармакокинетическим особенностям, механизму связывания с рецепторами и т.д.
По механизму связывания с рецепторами БРА (а также их активные метаболиты) разделяют на конкурентные и неконкурентные антагонисты ангиотензина II. Так, лозартан и эпросартан обратимо связываются с АТ1-рецепторами и являются конкурентными антагонистами (т.е. при определенных условиях, например при повышении уровня ангиотензина II в ответ на уменьшение ОЦК, могут вытесняться из мест связывания), тогда как валсартан, ирбесартан, кандесартан, телмисартан, а также активный метаболит лозартана EXP-3174 действуют как неконкурентные антагонисты и связываются с рецепторами необратимо.
Фармакокинетика блокаторов рецепторов ангиотензина
Все БРА действуют постепенно, антигипертензивный эффект развивается плавно, в течение нескольких часов после приема однократной дозы, и продолжается до 24 ч. При регулярном приеме выраженный терапевтический эффект обычно достигается через 2-4 нед (до 6 нед) лечения.
Особенности фармакокинетики ЛС этой группы делают удобным их прием пациентами. Эти препараты можно принимать вне зависимости от приема пищи. Однократного приема достаточно, чтобы обеспечить хороший гипотензивный эффект в течение суток. Они одинаково эффективны у больных разного пола и возраста, включая пациентов старше 65 лет.
Фармакодинамика блокаторов рецепторов ангиотензина
Основной механизм действия ЛС этой группы связан с блокадой АТ1-рецепторов. БРА обладают высокой аффинностью и селективностью к подтипу АТ1-рецепторов, через которые и реализуются основные эффекты ангиотензина II. По данным различных авторов, их аффинность к АТ1-рецепторам превышает таковую к АТ2-рецепторам в тысячи раз: для лозартана и эпросартана более чем в 1 тыс. раз, телмисартана - более 3 тыс., ирбесартана - 8,5 тыс., активного метаболита лозартана EXP-3174 и кандесартана - 10 тыс., валсартана - в 20 тыс. раз.
Они блокируют основные отрицательные эффекты ангиотензина II, лежащие в основе патогенеза сердечно-сосудистых заболеваний: повышение АД, высвобождение альдостерона, ренина, вазопрессина и норадреналина, развитие гипертрофии миокарда ЛЖ и гладких мышц сосудов.
В основе антигипертензивного действия и других фармакологических эффектов БРА лежат несколько механизмов - один прямой и по меньшей мере два косвенных (опосредованных).
Прямой механизм антигипертензивного действия БРА связан с ослаблением эффектов ангиотензина II, которые опосредуются АТ1-рецепторами. Блокируя АТ1-рецепторы, БРА уменьшают вызываемую ангиотензином II артериальную вазоконстрикцию, снижают повышенное гидравлическое давление в почечных клубочках, а также уменьшают секрецию таких вазоконстрикторных и антина-трийуретических веществ, как альдостерон, аргинин-вазопрессин,
эндотелин-1 и норадреналин. При длительном приеме БРА ослабляют пролиферативные эффекты ангиотензина II, а также альдостеро-на, аргинин-вазопрессина, эндотелина-1 и норадреналина в отношении кардиомиоцитов и гладкомышечных клеток сосудистой стенки, а также фибробластов и мезангиальных клеток.
Косвенные механизмы фармакологических эффектов БРА связаны с реактивной гиперактивацией РААС в условиях блокады АТ1-рецепторов, которая ведет, в частности, к повышенному образованию ангиотензина II и ангиотензиногена. Эти эффекторные пептиды РААС в условиях блокады АТ1-рецепторов вызывают дополнительную стимуляцию АТ2- и АТх-рецепторов, вызывая артериальную вазодилатацию, оказывая антипролиферативное действие и увеличивая экскрецию натрия почками.
Недавние исследования дисфункции эндотелия при АГ позволяют предположить, что кардиоваскулярные эффекты БРА могут быть также связаны с модуляцией эндотелия и влиянием на продукцию оксида азота (NO). Полученные экспериментальные данные и результаты отдельных клинических исследований достаточно противоречивы. На фоне блокады АТ1-рецепторов увеличивается эндотелийза-висимый синтез и высвобождение оксида азота, что способствует вазодилатации, уменьшению агрегации тромбоцитов и снижению пролиферации клеток.
Таким образом, специфическая блокада АТ1-рецепторов позволяет обеспечить выраженный антигипертензивный и органопротективный эффект. На фоне блокады АТ1-рецепторов тормозится неблагоприятное воздействие ангиотензина II (и ангиотензина III, обладающего сродством к рецепторам ангиотензина II) на сердечно-сосудистую систему и предположительно проявляется его защитное действие (путем стимуляции АТ2-рецепторов), а также развивается действие ангиотензина- (I-VII) путем стимуляции АТх-рецепторов. Все эти эффекты способствуют вазодилатации и ослаблению пролифератив-ного действия ангиотензина II в отношении клеток сосудов и сердца.
БРА могут проникать через гематоэнцефалический барьер и тормозить активность медиаторных процессов в симпатической нервной системе. Блокируя пресинаптические АТ1-рецепторы симпатических нейронов в ЦНС, они угнетают высвобождение норадреналина и уменьшают стимуляцию адренорецепторов гладкой мускулатуры сосудов, что приводит к вазодилатации. По данным экспериментальных исследований, этот дополнительный механизм вазодилатирую-щего действия более характерен для эпросартана. Данные о действии
лозартана, ирбесартана, валсартана и других препаратов этой группы на симпатическую нервную систему (которое проявлялось при дозах, превышающих терапевтические) весьма противоречивы.
Показания к назначению блокаторов рецепторов
ангиотензина
Показаниями для назначения БРА считают АГ и ХСН.
Нежелательные лекарственные реакции
Результаты мультицентровых плацебоконтролируемых исследований свидетельствуют о высокой эффективности и хорошей переносимости антагонистов АТ1-рецепторов ангиотензина II. БРА - одни из наиболее безопасных антигипертензивных средств. Основные их побочные эффекты (головная боль, головокружение, астения, сухой кашель) сравнимы с таковыми у плацебо. Синдром отмены не наблюдается.
Противопоказания к назначению блокаторов
рецепторов ангиотензина
Противопоказания для БРА - непереносимость препаратов, беременность, лактация.
Характеристика основных препаратов
Валсартан (Диован*). Наиболее изученный препарат группы. Общее число пациентов, включенных в клинические исследования, достигает 100 тыс., из них более 40 тыс. включены в исследования с изучением заболеваемости и смертности (жестких конечных точек).
Биодоступность препарата составляет 23%. Хотя прием пищи замедляет его всасывание, это не приводит к снижению клинической эффективности. Связь с белками плазмы - 94-97%. Выводится валсартан печенью (70%) и почками (30%) в неизмененном виде. Больным с нарушением функций печени и почек коррекции дозы препарата не требуется.
Для лечения АГ валсартан назначают 1 раз в сутки. У большинства пациентов начало его антигипертензивного действия отмечается в пределах 2 ч, максимум - 4-6 ч, продолжительность - более 24 ч.
Проведено более 150 клинических исследований с изучением более 45 точек оценки эффективности. Препарат эффективен как у пациентов с впервые диагностированной АГ, так и при неэффективности предшествующего лечения. Валсартан обладает по меньшей мере сопоставимой эффективностью с антигипертен-зивными препаратами других групп. В ряде исследований валсартан продемонстрировал преимущества перед другими БРА - лозарта-ном, телмисартаном, ирбесартаном и кандесартаном. Число пациентов, ответивших на назначение валсартана в дозе 80-160 мг/сут, достигает 75%. Помимо антигипертензивной эффективности, вал-сартан достоверно уменьшает концентрацию высокочувствительного С-реактивного белка, маркера воспаления и эндотелиальной дисфункции; подтверждены нефропротективные свойства вал-сартана у пациентов с тяжелой ХПН, а также у больных, находящихся на гемодиализе. На фоне приема валсартана отмечены уменьшение риска возникновения СД на 23% по сравнению с амло-дипином и уменьшение риска развития сердечной недостаточности. В исследованиях показано кардиопротективное действие валсарта-на, выражавшееся в уменьшении коэффициента гипертрофии ЛЖ и улучшении диастолической функции ЛЖ. Включение валсар-тана в стандартную схему лечения АГ уменьшает риск развития сердечно-сосудистых осложнений и смертности на 39% по сравнению со схемой лечения, не включавшей БРА. По данным различных исследований, при применении валсартана риск первичного и повторного инсульта уменьшался на 40%.
Лозартан (Козаар*). Препарат хорошо абсорбируется после приема внутрь, в кишечнике подвергается карбоксилированию с образованием активного метаболита Е-3174. Биодоступность препарата 33%, максимальная концентрация в крови достигается в течение 1 ч, с альбуминами связывается 92% лозартана. Выделяется лозартан на 90% печенью.
В сравнительных исследованиях у пожилых пациентов лозартан вызывал относительное снижение риска смерти на 46% больше, чем каптоприл [ELITE, 1997].
У больных с почечной недостаточностью препарат снижает выраженность протеинурии, поддерживает приемлемую скорость клубоч-ковой фильтрации и почечный кровоток.
Лозартан увеличивает экскрецию мочевой кислоты почками (путем угнетения канальцевой реабсорбции), снижая ее концентрацию в крови и тканях.
Ирбесартан (Апровель*). Биодоступность препарата составляет 60-80%. Максимальная концентрация в крови достигается в течение 1,5-2 ч. Т1/2-11-15 ч. Связывание с белками плазмы - 96%. Выводится ирбесартан печенью и почками как в неизмененном виде, так и в виде метаболитов (6%). Больным с нарушением функций печени и почек коррекция дозы не требуется.
Максимальное действие препарата после однократного приема развивается через 3-6 ч. Устойчивый клинический эффект достигается через 1-2 нед приема.
Кандесартан (Атаканд*). Абсолютная биодоступность таблетиро-ванной формы препарата составляет 14%. Прием пищи не оказывает влияния на биодоступность. Максимальная концентрация в крови достигается через 3-4 ч. Т1/2-9 ч, кумуляция не отмечается. Связывание с белками плазмы - более 99%. Выводится кандесартан с желчью и мочой в основном в неизмененном виде и в незначительной степени в виде метаболитов. Больным с тяжелыми нарушениями функций почек и больным на гемодиализе требуется снижение дозы в 2 раза.
Эпросартан (Теветен*) - селективный непептидный блокатор рецепторов ангиотензина II, дающий дополнительный фармакодина-мический эффект, опосредуемый пресинаптическими ангиотензино-выми рецепторами: дополнительная вазодилатация без рефлекторной тахикардии в результате блокады не только РААС, но и симпатоадре-наловой системы. Эпросартан не взаимодействует с изоферментами цитохрома Р-450 и, следовательно, имеет низкий потенциал взаимодействия с другими ЛС. Препарат оказывает выраженное действие на систолическое АД.
После приема внутрь разовой дозы 300 мг биодоступность препарата составляет примерно 13%, прием с пищей снижает абсорбцию. Связывание с белками плазмы высокое (98%) и сохраняется постоянным после достижения терапевтической концентрации. Cmax достигается через 1-2 ч. Практически не кумулируется. Т1/2-5-9 ч. Выводится в основном в неизмененном виде через кишечник и почками.
Телмисартан (Микардис*). Биодоступность препарата составляет около 50%, прием пищи несколько снижает скорость всасывания. Т1 / 2-20 ч. Связывание с белками плазмы - 99%. Выводится телми-сартан печенью. Больным с нарушением функций печени требуется коррекция дозы.
Основное показание - лечение АГ. Действие после однократного приема препарата длится 24-48 ч. Максимальный клинический эффект развивается через 4-8 нед после начала лечения.
10.4. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ β-АДРЕНОБЛОКАТОРОВ
БАБ - препараты, блокирующие β-адренорецепторы.
Первые адреноблокаторы появились в начале 60-х годов XX в., их преимущественно назначали для лечения острых нарушений ритма сердца, а затем - для лечения АГ, стенокардии, острого ИМ, ХСН.
Классификация β-адреноблокаторов
В клинической практике используют более 30 БАБ, которые подразделяют на следующие группы.
• Препараты, действующие на β1- и β2-адренорецепторы или неселективные (пропранолол, надолол) и действующие на β1-адренорецепторы или кардиоселективные (атенолол, мето-пролол, бисопролол, небиволол).
• Препараты с внутренней симпатомиметической активностью (пин-долол) и без внутренней симпатомиметической активности (пропра-нолол, надолол, метопролол, бисопролол, небиволол).
• Препараты с мембраностабилизирующим эффектом (пропра-нолол, пиндолол, талинолол) и без мембраностабилизирующего эффекта (надолол).
• Препараты с комбинированным механизмом действия:
- блокада α- и β-адренорецепторов (лабеталол®);
- неселективная β-блокада + блокада а1-адренорецепторов (кар-ведилол);
- неселективная β-блокада + а2-адреностимуляция (дилевалол);
- высокоселективная блокада β1-рецепторов + прямой вазодила-тирующий эффект, связанный с активацией системы монооксида азота эндотелиального происхождения (небиволол).
Существует и другая классификация, которая характеризует БАБ по поколениям (табл. 10-10).
Таблица 10-10. Классификация БАБ по M.R. Bristow, 1998

Фармакокинетика β-адреноблокаторов
Фармакокинетика БАБ зависит во многом от растворимости в жирах и воде (табл. 10-11). По этому признаку все БАБ разделяют на три группы: жирорастворимые (липофильные); водорастворимые (гидрофильные); жиро- и водорастворимые.
Таблица 10-11. Фармакокинетические характеристики жирорастворимых и водорастворимых БАБ
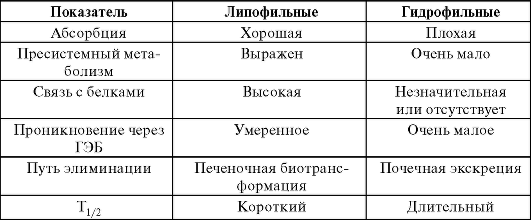
Липофильные БАБ (бетаксолол, карведилол, метопролол, окспре-нолол®, пропранолол, тимолол, небиволол) быстро и хорошо (более 90%) всасываются в ЖКТ, связь с белками плазмы составляет 80-95%. На 80-100% подвергаются метаболической трансформации в печени. Из-за этого у пациентов со сниженным печеночным кровотоком (пожилой и старческий возраст, выраженная сердечная недостаточность) и заболеваниями печени (гепатит, цирроз) дозы липофильных БАБ должны быть снижены. Препараты этой группы сами могут уменьшать печеночный кровоток (например, пропранолол - на 30%), что приводит к замедлению собственного метаболизма в печени, удлинению периода полувыведения, особенно при длительном приеме. Липофильные БАБ обычно имеют короткий период полувыведения (от 1 до 5 ч) и из-за этого их необходимо назначать не реже 2-3 раз в сутки (иногда до 4-6). Липофильные БАБ сильнее связываются с β-адренорецепторами. Недостатком этих препаратов считают способность вызывать легкие депрессивные расстройства, обусловленные их проникновением через гематоэнцефалический барьер.
Гидрофильные БАБ (атенолол, надолол, соталол) всасываются в ЖКТ не полностью (30-70%), экскретируются, как правило, в неизмененном виде (40-70%) или в виде метаболитов почками и только в незначи-
тельной степени (до 20%) подвергаются биотрансформации в печени. Гидрофильные препараты имеют более продолжительный период полувыведения (от 6 до 24 ч). Их обычно назначают 1-3 раза в сутки. Следует отметить, что нет существенных отличий в периоде полувыведения и продолжительности действия гидрофильных и пролонгированных форм липофильных БАБ. Однако сохраняются значительные отличия в путях элиминации, что следует учитывать при выборе препаратов для длительного лечения. Например, период полувыведения гидрофильных БАБ увеличивается при почечной недостаточности, у лиц пожилого и старческого возраста, когда снижается скорость клубочковой фильтрации. У некоторых липофильных БАБ (пропрано-лол) существуют активные метаболиты, которые, как и гидрофильные препараты, выводятся через почки и могут накапливаться при почечной недостаточности. У таких липофильных БАБ, как метопролол или тимолол, активных метаболитов нет. Таким образом, при ХПН они более предпочтительны для длительного лечения. При наклонности к депрессивным состояниям, особенно в пожилом и старческом возрасте, целесообразнее назначать водорастворимые препараты.
Липо - и водорастворимые БАБ хорошо растворяются как в жирах, так и в воде (бисопролол, пиндолол, целипролол®). Эти препараты имеют два примерно равноценных пути элиминации - печеночный и почечный. До 40-60% всосавшегося препарата подвергается биотрансформации в печени, остальная часть выводится через почки в неизмененном виде. Обычно препараты имеют небольшой период полувыведения - от 3 до 12 ч. Однако эффекты, обусловленные блокадой β-адренорецепторов, могут быть более продолжительными, причем степень и длительность адреноблокирующего действия увеличиваются по мере повышения дозы препарата.
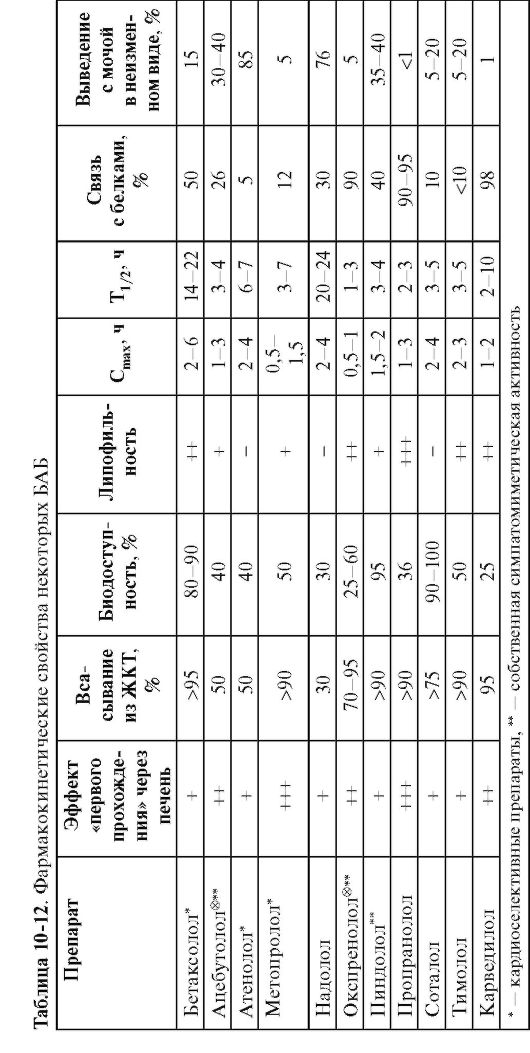
Основные показатели фармакокинетики некоторых БАБ представлены в табл. 10-12.
Перспективными считают БАБ, обладающие большим периодом полувыведения. Это особенно важно при лечении АГ, ХСН, когда необходимы средства, обеспечивающие контроль уровня АД при приеме 1-2 раза в сутки.
Фармакодинамика β-адреноблокаторов
Блокада β-адренорецепторов уменьшает активность аденилатци-клазы, благодаря чему снижается внутриклеточная концентрация кальция, клетка расслабляется, становится менее возбудимой.
Миокард. БАБ - конкурентные антагонисты катехоламинов, снижают симпатические влияния на сердечно-сосудистую систему, уменьшают АД. Уменьшается ЧСС, сократимость миокарда, а значит, и потребность миокарда в кислороде. Это обусловливает антиангиналь-ную активность препаратов, хотя при их применении увеличиваются время изгнания и объем ЛЖ, а коронарный кровоток не изменяется или даже снижается. В ответ на физическую или психоэмоциональную нагрузку БАБ способствуют стабилизации лизосомальных мембран, повышению устойчивости клеток к ишемии. Благодаря блокаде β-адренорецепторов уменьшается ток ионов натрия в фазы 0 и 4, снижается активность синусового узла и эктопических очагов.
Мембраностабилизирующее действие связано со способностью некоторых БАБ влиять на мембранные калиевые каналы и стабилизировать содержание внутриклеточного калия. Однако оно не имеет большого значения и при приеме терапевтических доз препаратов не выражено.
Почки. При блокаде БАБ юкстагломерулярного аппарата на 60% уменьшается продукция ренина.
Сосуды. Блокада β2-адренорецепторов сначала приводит к преобладанию вазоконстрикторных влияний α-адренорецепторов и повышению тонуса периферических сосудов. Затем тонус сосудов возвращается к норме или снижается посредством обратных ауторегуляторных реакций, что также объясняет механизм более долгосрочного гипотензивного действия БАБ.
Кровь. БАБ угнетают агрегацию тромбоцитов и способствуют тому, что эритроциты лучше «отдают» кислород ишемизированным клеткам.
ДЙС. Некоторые БАБ устраняют симптомы тревожности. Возможно развитие депрессивных расстройств, нарушение концентрации внимания, снижение скорости реакции, сонливость. БАБ также уменьшают тремор.
Матка. Препараты усиливают ритмическую и сократительную активность миометрия.
Бронхи. Увеличивают тонус бронхов. Кроме того, БАБ повышают тонус нижнего сфинктера пищевода. Эффект более выражен у неселективных БАБ, его используют для лечения и профилактики рефлюкс-эзофагита. БАБ способны также усиливать моторику ЖКТ, расслаблять мышцу, выталкивающую мочу (нарушение опорожнения мочевого пузыря). Некоторые БАБ (пропранолол) тормозят образование активных форм тиреоидных гормонов на уровне периферических тканей.
В целом, все БАБ обладают сходными фармакологическими свойствами и их различия не всегда значимы. Кардиоселективные препараты оказывают преимущественное действие на β1-адренорецепторы. Однако селективность большинства БАБ относительна, она нивелируется при увеличении доз препарата. Наиболее выражена кар-диоселективность у небиволола. Коэффициент кардиоселективности у небиволола равен 288, у бисопролола - 75, в то время как у ате-нолола только 19. Из-за этого небиволол и бисопролол, в отличие от атенолола, не снижают толерантность к нагрузкам, не вызывают утомляемости и не влияют на максимальную работоспособность, кроме того, препараты мало влияют на бронхиальную проходимость и уровень метаболизма (можно назначать пациентам с МС и СД).
Наличию внутренней симпатомиметической активности долгое время придавали очень большое значение. (Такие препараты, наряду с блокадой рецепторов, способны их несколько возбуждать.) Препараты с внутренней симпатомиметической активностью (пиндолол, ацебуто-лол®) мало влияют на ЧСС в покое, но снижают степень тахикардии при нагрузке. Существовало предположение, что эти препараты меньше снижают сердечный выброс, расширяют периферические артерии, реже вызывают нарушения периферического кровообращения, чем другие БАБ. Однако опыт применения этих препаратов свидетельствует о том, что внутренняя симпатомиметическая активность БАБ не имеет ключевого значения для их эффективности.
Клиническое применение β-адреноблокаторов
Артериальная гипертензия - важнейшее показание к назначению БАБ. Препараты уменьшают риск сердечно-сосудистых осложнений, гипертрофию миокарда, снижают смертность, увеличивают продолжительность жизни больных с АГ. Их можно назначать в качестве монотерапии или в сочетании с другими гипотензивными средствами: диуретиками, блокаторами медленных кальциевых каналов (дигидро-пиридиновыми), а1-адреноблокаторами. Сочетание с ИАПФ в некоторых руководствах расценивают как менее эффективное сочетание, но доказательных клинических исследований по этой теме нет.
При лечении АГ предпочтение необходимо отдавать БАБ с вазо-дилатирующими свойствами (карведилол, небиволол) и кардиоселек-тивным препаратам (бисопролол, метопролол, бетаксолол, атенолол). Первые рекомендуют назначать из-за повышенного периферического сопротивления сосудов у большинства больных. Вторые обладают
меньшим негативным влиянием на тонус сосудов. При АГ целесообразно применение длительно действующих препаратов (неби-волол, бисопролол, метопролол, бетаксолол, талинолол). Во-первых, из-за удобства приема 1 раз в сутки (в редких случаях 2), во-вторых, назначение длительно действующих БАБ дает возможность поддерживать постоянную концентрацию препарата в крови, а следовательно, избегать колебания активности симпатоадреналовой системы.
Стабильное гипотензивное действие БАБ развивается через 3-4 нед после начала приема препарата. Оно устойчиво и не зависит от физической активности и психоэмоционального состояния пациента.
При назначении БАБ в качестве монотерапии они существенно снижают АД у 50-70% больных. Гипотензивное действие БАБ усиливается в сочетании с мочегонными препаратами, блокаторами медленных кальциевых каналов, α-адреноблокаторами, ИАПФ.
Принципы выбора БАБ у больных с АГ в зависимости от сопутствующих заболеваний, синдромов или состояний приведены в табл. 10-13.
Контроль за эффективностью и безопасностью применения БАБ
Поскольку исходный уровень симпатической активности у разных пациентов неизвестен, в начале лечения препараты назначают в минимальных терапевтических дозах, постепенно повышая их до получения клинического эффекта (титрование дозы). Критерием правильно подобранной дозы считают уровень АД. Удлинение интервала PQ на ЭКГ указывает на нарушение атриовентрикулярной проводимости и требует отмены или коррекции дозы препарата. Необходимо контролировать сократительную функцию сердца с помощью дополнительных методов исследования (ЭхоКГ). У больных пожилого и старческого возраста в начале лечения дозу БАБ уменьшают в 2-4 раза от среднетерапевтической. Подобранную дозу можно назначать длительно в качестве поддерживающей терапии благодаря тому, что толерантности к БАБ не наступает.
Критерии эффективности и безопасности
• Клинические:
- ЧСС в покое должна быть около 60 в минуту (не менее 50); при умеренной физической нагрузке (при приседании, велоэр-гометрии) ЧСС не должна возрастать выше 100-120 в минуту;
- снижение АД;
- отсутствие нарастания признаков сердечной недостаточности.

• Лабораторные, функциональные:
- определение концентрации БАБ в крови не имеет практического значения из-за индивидуальной вариабильности ответа на препарат и скорости биотрансформации;
- ЭКГ: увеличение интервала PQ на ЭКГ более, чем на 25% считают опасным;
- исследование функции внешнего дыхания при склонности к бронхоспазму;
- контроль концентрации глюкозы в крови и липидного спектра
(ЛПНП и ЛПОНП, а также ЛПВП). Нежелательные лекарственные реакции
Побочные эффекты отражают неспецифическую блокаду β1-или β2-адренорецепторов. Для их устранения необходима полная отмена препарата или ограничение дозы. Основные НЛР, свойственные БАБ, перечислены ниже.
• Обусловленные в основном блокадой β2-адренорецепторов:
- бронхоспазм;
- расстройства периферической сосудистой системы (похолодание конечностей; обострение синдрома Рейно, перемежающейся хромоты);
- ухудшение церебрального кровотока, проявляющееся в ряде случаев чувством усталости, сонливости;
- возможность гипогликемического состояния у больных СД (БАБ - антагонисты адреналина в отношении его гипергли-кемического действия, в частности угнетается гликогенолиз в печени). Допустимо назначение БАБ, особенно кардиоселек-тивных, больным с компенсированным СД;
- повышение концентрации ХС в крови из-за антагонизма с адреналином, обладающим липолитическим действием (концентрация общего холестерина не меняется, содержание ХС ЛПВП снижается, ХС ЛПОНП повышается). Однако эти изменения не обязательно ведут к атерогенезу.
• Обусловленные в основном блокадой β1-адренорецепторов:
- АВ-блокада.
• Обусловленные блокадой β1- и β2-адренорецепторов:
- прямое влияние на ЦНС (для жироростворимых препаратов) - бессонница, тревожные сны, галлюцинации, редко - депрессия;
- постуральная гипотензия;
- импотенция.
Меньшее значение имеют следующие фармакологические эффекты БАБ.
• Усиление моторики ЖКТ, что может проявляться болями в животе, рвотой, диареей, реже - запором.
• Расслабление мышцы, выталкивающей мочу. Это может доставлять дискомфорт больным с гиперплазией предстательной железы, полезно при лечении недержания мочи, особенно невроген-ного характера.
• Окуломукокутанный синдром. Возможно снижение секреции слезных желез (данный эффект может приводить к развитию конъюнктивита или кератоконъюнктивита, особенно у пациентов, носящих контактные линзы).
Противопоказания к назначению β-адреноблокаторов
• БА.
• Инсулинозависимый СД.
• Обструктивные заболевания периферических сосудов.
• Нарушение сердечной проводимости.
• Кормление грудью - относительное противопоказание. Некоторые БАБ накапливаются в грудном молоке (надолол). Прием БАБ в адекватной дозе, 1-2 раза в сутки, назначение кардиоселективных препаратов уменьшают риск нежелательных эффектов.
• Феохромоцитома. Возможно развитие ГК при назначении препаратов без α-блокирующей активности.
Беременность с появлением высокоселективных БАБ перестала быть противопоказанием для назначения этой группы препаратов.
Следует учитывать возможность резкого ухудшения течения ИБС и АГ при внезапном прекращении приема БАБ (синдром отмены). При этом наблюдаются учащение приступов стенокардии, повышение АД, увеличение агрегации тромбоцитов. БАБ необходимо отменять постепенно, с уменьшением дозы на 50% в неделю.
Взаимодействие β-адреноблокаторов с другими
лекарственными средствами
Усиливается антиангинальный эффект при сочетании БАБ с нитратами, уменьшаются побочные эффекты нифедипина, свя-
занные с активацией симпатоадреналовой системы. Сочетание с верапамилом считают эффективным, но в результате аддитивного действия возможны нежелательные эффекты (брадикардия, АВ-блокада, артериальная гипотензия, сердечная недостаточность). Усиливается брадикардия, вызываемая дигоксином. Усиливается действие барбитуратов. Потенцируется отрицательное инотропное действие хинидина, прокаинамида. При назначении БАБ с клони-дином отмечаются снижение АД и брадикардия, особенно при вертикальном положении больного. Сочетание с амиодароном усиливает антиаритмическое и антиангинальное действие. Рекомендуется избегать ингаляционного наркоза с эфиром диэтиловым, циклопропаном, хлороформом из-за усиления β-блокирующего эффекта (безопасен галотан).
В дополнение к этому необходимо отметить, что препараты, которые уменьшают активность микросомальных ферментов печени (циметидин, хлорпромазин), замедляют элиминацию липофильных БАБ. Средства, повышающие активность микросомальных ферментов печени (барбитураты, фенитоин, рифампицин), а также курение, наоборот, ускоряют элиминацию липофильных БАБ и практически не влияют на метаболизм гидрофильных БАБ.
Характеристика основных препаратов
Неселективные β-адреноблокаторы
Пропранолол (Обзидан*) - своеобразный эталон средств с β-адреноблокирующей активностью. Биодоступность при приеме внутрь составляет 36x10%. Примерно 93% препарата в крови находится в связанном с белками состоянии. Т1/2 составляет 2-3 ч (у больных с печеночной недостаточностью Т1/2 увеличивается). Объем распределения - 3,9 л/кг. Препарат подвергается биотрансформации в печени с образованием активных метаболитов. Только 0,5% от дозы выводится почками. Препарат принимают с интервалом 4-6 ч.
Надолол (Коргард*). Отличается от других препаратов этой группы длительным действием и способностью улучшать функции почек. Антиангинальная активность выше, чем у пропрано-лола. Кардиодепрессивное действие выражено в меньшей степени. Биодоступность надолола при приеме внутрь составляет 30x10%. Только 30% препарата в крови находится в связанном с белками состоянии. Т1 / 2 надолола составляет 20-24 ч (у больных с почечной недостаточностью Т1 / 2 увеличивается). Эффективная концентрация
достигается через 6-9 сут приема. Объем распределения - 2,1 л/кг. В ходе метаболизма неактивные метаболиты не образуются. До 76% от дозы выводится почками.
Пиндолол (Вискен*). Вызывает менее выраженный отрицательный инотропный эффект, чем пропранолол. В меньшей степени, чем другие неселективные БАБ, влияет на β2-адренорецепторы. Более безопасен при бронхоспазме и СД. При АГ эффект пиндолола ниже, чем у пропранолола.
Пиндолол практически полностью всасывается в ЖКТ, его биодоступность при приеме внутрь составляет 95%, только 40% препарата в крови находится в связанном с белками состоянии. Т1/2 пиндолола составляет 3-4 ч. Объем распределения - 2,0 л/кг. В ходе метаболизма неактивные метаболиты не образуются. Около 35-40% от дозы выводится почками. Препарат принимают внутрь 3-4 раза в сутки.
Кардиоселективные БАБ
Атенолол (Теноретик*) - селективный β1-адреноблокатор без собственной симпатомиметической и мембраностабилизирующей активности. Препарат можно принимать 2 раза в сутки, он обладает слабой кардиоселективностью, практически лишен центрального побочного действия. К достоинствам препарата относится низкая стоимость.
Биодоступность атенолола при приеме внутрь составляет 40±10%. Только 5% препарата в крови находится в связанном состоянии. Т1 /2 составляет 6-7 ч, Т1/2 значительно увеличивается у больных с ХПН. Объем распределения - 0,7 л/кг. Около 85% препарата выводится почками, и при ХПН необходима коррекция дозы.
Метопролол (Беталок*, Беталок-ЗОК*). Кардиоселективный β1-адреноблокатор с собственной симпатомиметической активностью. Биодоступность при приеме внутрь составляет 50%, подвергается интенсивному пресистемному метаболизму в печени, активных метаболитов не имеет. Хорошо проникает через гематоэнцефалический барьер, обнаруживается в высоких концентрациях в грудном молоке. Т1/2 колеблется от 3до7 ч, увеличение Т1/2 отмечают у лиц, относящихся к категории «медленных» метаболизаторов (см. гл. 9). Объем распределения - 5,6 л/кг. Только 5% дозы выводится почками, и при почечной недостаточности значимой кумуляции в организме не наблюдается, у больных с циррозом печени биотрансформация замедляется. Гипотензивный эффект наступает быстро: систолическое АД начинает снижаться уже через 15 мин. Назначают при АГ и стенокардии 2 раза в сутки.
Бисопролол (Конкор*) - один из наиболее селективных β1-адреноблокаторов. Оказывает гипотензивное, антиаритмическое,
антиангинальное действие. В терапевтических дозах не обладает внутренней симпатомиметической активностью и клинически значимыми мембраностабилизирующими свойствами. Абсорбция - 80-90%, прием пищи не влияет на абсорбцию, время достижения Стах - 2-4 ч, связь с белками - 26-33%, биотрансформация в печени, Т1/2-9-12 ч, экскреция - почками (50% в неизмененном виде), менее 2% - с фекалиями. Проникновение через гематоэнцефалический барьер (ГЭБ) и плацентарный барьер - низкое, секреция с грудным молоком - низкая.
Бисопролол обеспечивает контролируемое снижение АД, зависящее от дозы препарата, плавно снижает АД на протяжении суток, в том числе в ранние утренние часы, его можно принимать длительное время без развития толерантности. Высокая β-селективность позволяет применять бисопролол у особых групп пациентов: больных СД, нарушением липидного обмена; два пути выведения позволяют назначать бисопролол больным с нарушением функций печени и почек, а также для лечения ХСН (вызывает регрессию гипертрофии миокарда).
Бетаксолол (Локрен*). Не обладает внутренней симпатомиме-тической активностью. При назначении в высоких дозах обладает мембраностабилизирующим действием. Около 89-95% всасывается из ЖКТ, примерно половина препарата в крови находится в связанном с белками состоянии. Т1/2 бетаксолола составляет 14-22 ч. Объем распределения - 6,1 л/кг. Подвергается биотрансформации в печени, метаболиты фармакологической активностью не обладают и выводятся почками. Около 15% дозы выводится почками в неизмененном виде. Бетаксолол назначают 1 раз в сутки.
Препараты с комбинированным механизмом действия
Биодоступность при приеме внутрь составляет 25%, через 2 ч достигая максимальной концентрации в крови. На 50% связывается с белками плазмы. Т1/2 лабетолола® составляет 6-8 ч. Объем распределения - 9,4 л/кг. Подвергается биотрансформации в печени. В ходе метаболизма неактивные продукты не образуются. Только 5% от дозы выводится почками. При почечной недостаточности выведение препарата значимо не меняется.
Карведилол (Дилатренд*) - блокатор α1- и β12-адренорецепторов. Блокада β1-адренорецепторов приводит к снижению частоты и силы сердечных сокращений без резкой брадикардии, снижению проводимости. В результате блокады α1-адренорецепторов расширяются периферические сосуды. Блокада β2-адренорецепторов вызывает некоторое повышение тонуса бронхов, сосудов микроциркуляторно-го русла, усиление тонуса и перистальтики кишечника.
Быстро всасывается при приеме внутрь, прием пищи может уменьшить степень адсорбции, но не уменьшает ее интенсивность. При одновременном приеме с пищей уменьшается риск развития ортостатической гипотензии. Биодоступность карведилола - 25-35%. Имеет место эффект первого прохождения через печень, на интенсивность метаболизма могут оказать влияния ингибиторы CYP2D6. Т1 / 2 составляет 7-10 ч.
Наиболее серьезной НЛР при приеме карведилола считают орто-статическую гипотензию (около 2% случаев), из-за этого после первого назначения препарата больной должен несколько часов находиться в положении сидя или лежа. Иногда после приема карведилола возникают боль в грудной клетке, нарушение толерантности к глюкозе; сонливость, проходящая через 7-10 сут регулярного приема препарата. Карведилол принимают внутрь 1-2 раза в сутки.
Небиволол (Небилет*) - это БАБ нового поколения, обладающий высокой селективностью в отношении β1-адренорецепторов, отличающийся от прочих препаратов этого класса непосредственным сосудорасширяющим действием путем стимуляции выработки эндотелием оксида азота. Его назначают для лечения АГ, ИБС, ХСН. Побочные эффекты, свойственные другим БАБ, наблюдаются значительно реже. Не требуется титрования дозы для получения необходимого эффекта.
10.5. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ БЛОКАТОРОВ МЕДЛЕННЫХ КАЛЬЦИЕВЫХ
КАНАЛОВ
БМКК - ЛС, которые, блокируя мембранные каналы клеток, препятствуют току ионов кальция.
Классификация блокаторов медленных
кальциевых каналов
Существует несколько вариантов классификации БМКК. А. По химической природе.
• Фенилалкиламины (верапамил).
• Бензотиазепины (дилтиазем).
• Дигидропиридины (нифедипин, низолдипин*3, амлодипин).
• Дифенилпиперазины (циннаризин, флунаризин®).
Особенности строения препаратов из разных химических групп определяют различия в тканевой избирательности (табл. 10-14). Так, фенилалкиламины (верапамил) действуют преимущественно на сердце (особенно на проводящую систему) и в меньшей степени на артериальные сосуды. Дилтиазем примерно в равной степени действует на проводящую систему сердца и сосуды. Дигидропиридины (нифедипин), напротив, преимущественно влияют на артериальные сосуды и в незначительной степени на сердце. Дифенилпиперазины (циннаризин, флунаризин®) избирательно влияют на артериальные сосуды головного мозга.
Таблица 10-14. Селективность (сосуды/миокард) и фармакологическое действие различных БМКК
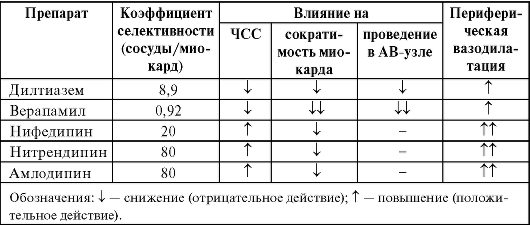
Б. Существует деление БМКК по длительности действия.
• Короткодействующие препараты: верапамил, нифедипин, дил-тиазем.
• Длительно действующие препараты: изоптин SR 240*, алтиазем РР*, адалат SR, амлодипин.
Недостатком БМКК короткого действия считают частое суточное колебание концентрации препарата в крови, следовательно, неустойчивый эффект. Длительно действующие препараты представлены двумя подгруппами.
• Специальные лекарственные формы с замедленным высвобождением короткодействующего препарата:
- ретард формы в виде таблеток или капсул с медленным выходом препарата из лекарственной формы (изоптин SR 240*, алтиазем РР*);
- рапид-ретард формы с двухфазным высвобождением препарата (адалат CL*>);
- лекарственные терапевтические системы суточного действия (адалат GITS*3).
• Новые производные дигидропиридинов: нитрендипин, амлоди-пин и др.
Существует также деление БМКК по поколениям. В частности, к первому поколению относят короткодействующие препараты, а ко второму - длительно действующие ЛС.
Фармакокинетика блокаторов медленных кальциевых каналов
Фармакокинетические параметры основных БМКК представлены в табл. 10-15 и 10-16.
Таблица 10-15. Фармакокинетические параметры некоторых БМКК (часть 1)
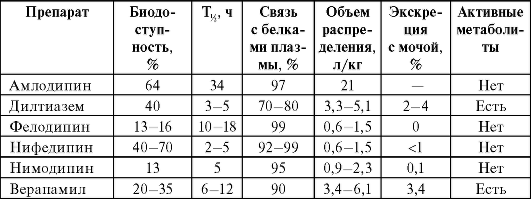
Таблица 10-16. Фармакодинамические параметры некоторых БМКК (часть 2)
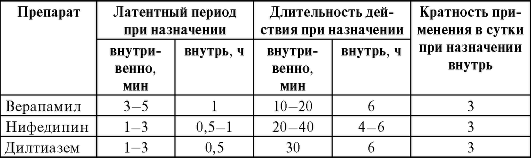
Фармакодинамика блокаторов медленных кальциевых каналов
Ионы кальция выполняют особую функцию в поддержании функциональной активности клеток. Они регулируют сокращение мышечных волокон, выделение медиаторов нервными клетками, секрецию ферментов и гормонов. Значение внеклеточного и внутриклеточного кальция в сокращении различных типов мышц неодинаково. Например, для сокращения скелетной мышцы расходуется только кальций, находящийся в саркоплазматическом ретикулуме. Сокращение сердечной мышцы на 95% обеспечивается кальцием из саркоплазматического ретикулума, на 5% - внеклеточным «затравочным» кальцием. В клетках гладких мышц сосудов саркоплазматический ретикулум не развит, и сокращение почти полностью зависит от внеклеточного кальция. Для поступления кальция в клетку используются ионные каналы: потенци-алзависимые и рецепторзависимые. Потенциалзависимые каналы открываются при изменении мембранного потенциала. Различают несколько типов потенциалзависимых кальциевых каналов: L, Т, N, P, R.
БМКК блокируют L- и T-кальцийпроводящие каналы гладкомы-шечных клеток и снижают поступление в них кальция. Этот механизм приводит к снижению сердечного выброса (фенилалкиламины и бензотиазепины), уменьшению периферического сопротивления артериол (дигидропиридины) и снижению АД. Затем активируется симпатоадреналовая система и РААС. При этом фенилалкиламины и бензотиазепины нейтрализуют стимулирующее влияние катехо-ламинов на миокард путем прямого кардиодепрессивного действия, а применение дигидропиридинов (особенно короткого действия) может привести к тахикардии и увеличению потребности миокарда в кислороде.
Препараты этой группы снижают тонус коронарных сосудов и увеличивают коронарный кровоток. Расслабление артериол под влиянием БМКК существенно снижает постнагрузку на сердце. Перечисленные эффекты создают щадящие условия для сердечной деятельности и увеличивают доставку кислорода к миокарду. Эти ЛС обладают кардиопротективными свойствами: уменьшают повреждение митохондрий в кардиомиоцитах, увеличивают концентрацию АТФ, стимулируют коллатеральный кровоток в ише-мизированном миокарде. При АГ они вызывают обратное развитие гипертрофии ЛЖ.
Верапамил и дилтиазем снижают автоматизм синусового АВ-узла и эктопических очагов, уменьшают проводимость в АВ-узле и увеличивают эффективный рефрактерный период предсердий.
БМКК оказывают благоприятное влияние на почки. Они снижают тонус почечных артерий, улучшают клубочковую фильтрацию и увеличивают выделение почками натрия, что способствует гипотензивному действию.
Препараты этой группы угнетают агрегацию тромбоцитов, обладают антиатерогенными свойствами. БМКК назначают при АГ, ИБС, аритмиях, гипертрофической кардиомиопатии, нарушениях мозгового кровообращения.
Контроль за эффективностью и безопасностью БМКК
При назначении БМКК необходимо контролировать АД, ЧСС, проводимость (дигидропиридины учащают ритм, фенилалкиламины и бензотиазепины - урежают ритм, снижают проводимость и удлиняют интервал PQ), а также сократимость миокарда (ЭхоКГ).
Кроме того, необходимо учесть, что при применении короткодействующих дигидропиридинов (нифедипина) для лечения АГ повышается риск смерти или развития сердечно-сосудистых осложнений. Следует избегать назначения короткодействующих препаратов больным, перенесшим ИМ. Не рекомендовано при гипертонических кризах принимать короткодействующие формы нифедипина, поскольку они вызывают резкое снижение АД и тем самым могут провоцировать развитие ишемии миокарда, головного мозга и почек. Длительно действующие формы верапамила, дилтиазема, нифедипина переносятся лучше. Длительный прием БМКК нежелателен при систолической дисфункции ЛЖ, синдроме слабости синусового узла, АВ-блокаде II-III степени, в начале беременности и в период лактации.
Нежелательные лекарственные реакции
Существенные НЛР при назначении БМКК в терапевтических дозах отмечают редко. Основные НЛР разделяют на три группы.
• Влияние на сосуды: головная боль, головокружение, приливы у 7-10% пациентов, сердцебиение, отеки стоп у 5-15% больных, преходящая гипотония.
• Влияние на сердце: снижение проводимости и силы сердечных сокращений (особенно у верапамила), брадикардия (верапамил и дилтиазем - у 25% больных).
• Желудочно-кишечные расстройства (запор у 20% больных, диарея, тошнота - у 3%).
Противопоказания к применению
Препараты не назначают при кардиогенном шоке, выраженной брадикардии, артериальной гипотонии, сердечной недостаточности.
Взаимодействия блокаторов медленных кальциевых каналов с другими лекарственными
средствами
Лекарственные взаимодействия представлены в табл. 10-17.
Характеристика основных препаратов
Верапамил (Изоптин*) - производное фенилалкиламинов. Первый БМКК. Оказывает антиаритмическое, антиангинальное и гипотензивное действие, снижает потребность миокарда в кислороде путем уменьшения сократимости миокарда и ЧСС. Вызывает расширение коронарных артерий и увеличение коронарного кровотока. Как антиаритмик эффективен при наджелудочковых аритмиях (подробнее см. главу 13).
Дилтиазем - производное бензотиазепинов. По фармакодинами-ческим свойствам дилтиазем занимает промежуточное положение между верапамилом и нифедипином. Он снижает активность синусового узла и угнетает атриовентрикулярную проводимость в меньшей степени, чем верапамил, а на общее периферическое сосудистое сопротивление (ОПСС) влияет меньше, чем нифедипин.
Дилтиазем подвергается биотрансформации в печени с образованием активного метаболита - дезацетилдилтиазема, выводится почками, преимущественно в виде метаболитов и только 2-4% препарата экскретируется в неизмененном виде.
Препарат назначают при АГ, для профилактики приступов стенокардии, в том числе и вазоспастической (стенокардии Принцметала), над-желудочковых аритмий (пароксизмальная наджелудочковая тахикардия, мерцание предсердий, трепетание предсердий, экстрасистолия).
Препарат противопоказан при синдроме слабости синусового узла, нарушении атриовентрикулярной проводимости.
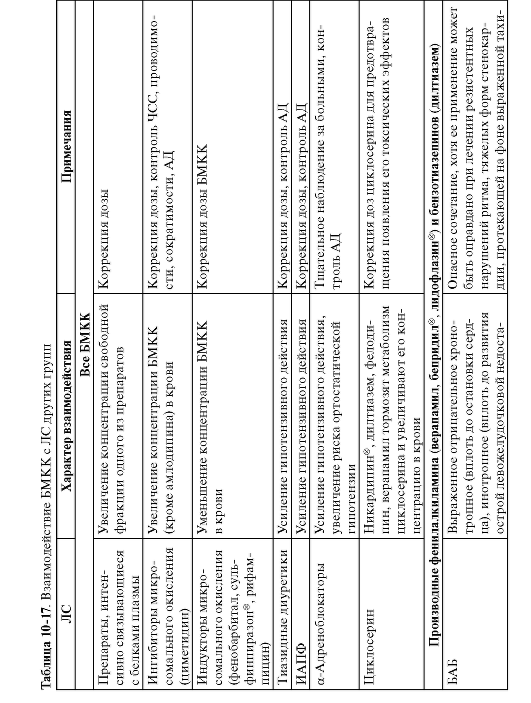
Продолжение табл. 10-17
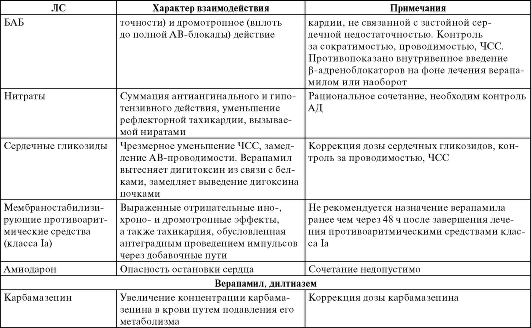
Окончание табл. 10-17
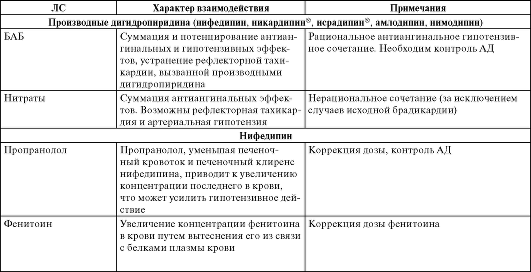
Нифедипин (Адалат*, Коринфар*) - производное дигидропириди-на. Снижает тонус коронарных и периферических сосудов и АД, увеличивает коронарный кровоток при атеросклеротической обструкции. Препарат обладает отрицательным инотропным действием, не влияет на проводимость в миокарде, не имеет противоаритмиче-ских свойств. При длительном приеме снижает частоту образования новых атеросклеротических повреждений коронарных сосудов, блокирует агрегацию тромбоцитов.
У пожилых пациентов препарата в 2 раза больше, чем у молодых. При сублингвальном применении действие начинается через 5-10 мин, достигая максимума через 15-30 мин. Препарат менее липо-филен по сравнению с верапамилом и меньше проникает в ткани. Нифедипин подвергается биотрансформации в печени; неактивные метаболиты выводятся почками.
Назначение короткодействующих форм нифедипина приводит к тахикардии и увеличению потребности миокарда в кислороде, что существенно ограничивает его применение при гипертонической болезни и ИБС. Недостаток нифедипина заключается в малой длительности действия, а также в необходимости его многократного приема, что не только создает неудобства для больных, но и становится причиной значительного суточного колебания АД. Для длительного лечения АГ рекомендовано назначение ретард-форм нифедипина или дигидропиридиновых БМКК второго поколения.
Адалат SL* - лекарственная форма с двухфазным высвобождением нифедипина, содержащая микрогранулы быстровысвобождаю-щегося препарата (5 мг) и нифедипина замедленного высвобождения (15 мг). Результат такого сочетания - быстрое начало действия и увеличенная длительность терапевтического эффекта (до 8-10 ч).
Адалат GITS*3 (GITS - gastrointestinal therapeutic system) - дли-тельнодействующие терапевтические системы. Подобные терапевтические системы основаны на выходе препарата из лекарственной формы под влиянием осмоса. GITS-система состоит из двух слоев: первый содержит препарат, а второй - полимерное осмотически-активное вещество. Такая двухслойная таблетка покрыта водопроницаемой нерастворимой мембраной, в которой со стороны препарата лазером пробито отверстие. При попадании системы в желудок вода, проникая через мембрану, превращает действующее вещество в суспензию, одновременно связываясь с осмотически-активным наполнителем. Наполнитель выталкивает суспензию нифедипина через лазерное отверстие с постоянной скоростью.
Длительность действия такого препарата - 24 ч. В данном случае из-за медленного развития вазодилатирующего эффекта симпатоа-дреналовая система активируется незначительно. При использовании пролонгированных препаратов концентрация норадреналина в крови практически не изменяется. Это позволяет существенно уменьшить выраженность рефлекторной тахикардии и ускорить обратное развитие гипертрофии ЛЖ. В целом назначение пролонгированных препаратов позволяет уменьшить частоту возникновения
НЛР в 3-4 раза.
При приеме нифедипина могут развиваться аллергические реакции (высыпания на коже и лихорадка), нарушения сна, зрения. Очень редко отмечают гематологические нарушения (тромбоцитопению, лейкопению, анемию), аллергический гепатит, гингивит, депрессию и параноидальный синдром, обморок, временное нарушение функций печени. Для короткодействующего нифедипина характерны тахикардия, повышение потребности миокарда в кислороде, колебания АД.
При назначении нифедипина в сочетании с сердечными гликози-дами дозу последних нужно уменьшить на 40-50%. Сочетание нифе-дипина с БАБ может провоцировать развитие гипотонии. Циметидин и дилтиазем повышают концентрацию нифедипина в крови.
Амлодипин (Норваск*) - длительнодействующий БМКК. Препарат хорошо всасывается в ЖКТ. Прием пищи не влияет на всасывание амлодипина. Биодоступность - 60-80%. Максимальная концентрация в крови наблюдается через 6-12 ч, стабильная концентрация в плазме достигается через 7-8 сут постоянного приема препарата. Амлодипин подвергается биотрансформации в печени с образованием неактивных метаболитов, T1/2 - до 50 ч. При ИБС амлодипин можно назначать в качестве монотерапии и в сочетании с другими антиангинальными средствами. Возможно применение амлодипина при диастолической дисфункции миокарда.
Нитрендипин (Октидипин*) - длительно действующее производное дигидропиридина. Обладает гипотензивной и антиангинальной активностью. Биодоступность - 60-70%. T1/2-8-12 ч.
Фелодипин (Плендил*) - препарат с высокой вазоселективно-стью, в 7 раз превышающей таковую нифедипина. Оказывает умеренное диуретическое (натрийуретическое) действие. У препарата низкая биодоступность - 15%. Латентный период при внутривенном введении составляет 10-15 мин, при энтеральном - 45 мин.
10.6. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ α-АДРЕНОБЛОКАТОРОВ
Блокаторы α-адренергических рецепторов применяют для лечения АГ более 40 лет, в настоящее время их рассматривают как дополнительные препараты в сочетании с препаратами основных классов.
Классификация препаратов основана на их избирательности по отношению к различным рецепторам.
• Неселективные α-адреноблокаторы: дигидрированные алкалоиды спорыньи, троподифен, фентоламин;
• Селективные а1-адреноблокаторы: празозин, доксазозин, теразо-зин.
В настоящее время при АГ назначают селективные а1-адрено-блокаторы, которые при длительном применении по гипотензивному действию сопоставимы с тиазидными диуретиками, БАБ, БМКК и ИАПФ. Препараты, блокируя а1-адренорецепторы, снижают системное сосудистое сопротивление, вызывают обратное развитие гипертрофии ЛЖ, улучшают липидный состав крови. Они существенно снижают концентрацию в крови общего ХС за счет ЛПНП и одновременно повышают концентрацию ЛПВП. Препараты повышают чувствительность тканей к инсулину и вызывают небольшое снижение концентрации глюкозы. Наличие большого количества а1-адренорецепторов в гладкой мускулатуре предстательной железы и шейке мочевого пузыря позволяет назначать препараты больным с аденомой предстательной железы для улучшения мочеиспускания.
Празозин - селективный а1-адреноблокатор короткого действия, при приеме внутрь он быстро всасывается в ЖКТ. Биодоступность - 60%. Более 90% празозина связывается с белками плазмы. Максимальная концентрация в крови определяется через 2-3 ч. T1 / 2-3-4 ч. Действие препарата начинается через 30-60 мин, длительность - 4-6 ч. Празозин подвергается биотрансформации в печени. 90% препарата и его метаболитов выводится через кишечник, остальная часть - через почки. Кратность приема - 2-3 раза в сутки. Для празозина характерен эффект «первой дозы» - резкое снижение АД после приема первой дозы препарата, из-за этого его принимают лежа, особенно первый раз, а лечение начинают с малых доз (0,5-1 мг). Препарат вызывает постураль-ную гипотензию, слабость, сонливость, головокружение, головную боль. Из-за малой продолжительности действия и НЛР празозин
не получил широкого распространения для лечения гипертонической болезни.
Доксазозин (Кардура*) - длительно действующий а1-адрено-блокатор, не вызывает эффекта «первой дозы». Доксазозин почти полностью всасывается в ЖКТ. Пища замедляет всасывание препарата примерно на 1 ч. Биодоступность - 65-70%. Максимальная концентрация в крови определяется через 2-3,5 ч после приема. T1 / 2-16-22 ч. Продолжительность действия - 18-36 ч. Доксазозин назначают 1 раз в сутки. При приеме препарата на ночь максимальный эффект наступает в период утреннего подъема АД, который связывают с циркадной активацией симпатоадреналовой системы. По данным многолетних клинических наблюдений, монотерапия доксазозином эффективна у 66% больных. Доксазозин вызывает обратное развитие гипертрофии ЛЖ, снижает повышенный риск развития сердечно-сосудистых осложнений у больных с АГ. Препарат облегчает отхождение мочи у больных с аденомой предстательной железы. Для доксазозина характерны следующие НЛР: головокружение, слабость, сонливость, артериальная гипотония. При недостаточной эффективности доксазозин комбинируют с БМКК, БАБ, ИАПФ, мочегонными средствами.
Фентоламин - неселективный а-адреноблокатор. В основном показан при лечении гипертонических кризов, связанных с гиперпродукцией катехоламинов, например, у больных с феохромоцито-мой. Кроме того, фентоламин назначают с диагностической целью при подозрении на феохромоцитому. Фентоламин и другие неселективные а-адреноблокаторы в настоящее время не применяют для лечения АГ из-за частого развития ортостатической гипотензии, тахикардии, головокружения, слабости.
10.7. ПРИМЕНЕНИЕ ДИУРЕТИКОВ ДЛЯ ЛЕЧЕНИЯ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ
Мочегонные средства назначают при АГ давно, сначала их использовали как вспомогательные. В настоящее время тиазидные и тиази-доподобные диуретики считают препаратами выбора для длительного комбинированного лечения и монотерапии АГ.
Роль увеличения концентрации ионов натрия в плазме и сосудистой стенке в патогенезе гипертонии общеизвестна, и основное значение при лечении АГ имеют салуретики - препараты, механизм
которых связан с угнетением реабсорбции натрия и хлора. К ним относят производные бензотиадиазина и тиазидоподобные диуретики. В качестве монотерапии тиазидные и тиазидоподобные диуретики в низких дозах эффективны у 25-65% больных с мягкой и умеренной АГ. В экстренных ситуациях, например при гипертоническом кризе, применяют «петлевые» диуретики: фуросемид и этакриновую кислоту. Иногда в качестве монотерапии назначают калийсберегаю-щие диуретики. Эта группа чаще выполняет вспомогательную функцию, их обычно назначают с тиазидными и петлевыми диуретиками для уменьшения потери калия.
Первоначальное снижение АД при назначении салуретиков связано с увеличением экскреции натрия, уменьшением объема плазмы и снижением сердечного выброса. Через 2 мес лечения диуретическое действие снижается, нормализуется сердечный выброс. Это связано с компенсаторным повышением концентрации ренина и альдо-стерона, которые препятствуют потере жидкости. Гипотензивное действие диуретиков на этом этапе объясняется снижением периферического сосудистого сопротивления, скорее всего из-за уменьшения концентрации ионов натрия в клетках гладких мышц сосудов. Диуретические средства снижают как систолическое, так и диасто-лическое АД, незначительно влияют на сердечный выброс.
При применении диуретиков в качестве средств, снижающих АД, следует учитывать продолжительность их действия (табл. 10-18) для обеспечения постоянства гипотензивного действия этих ЛС в течение всего дня.
Таблица 10-18. Продолжительность гипотензивного эффекта некоторых диуретиков
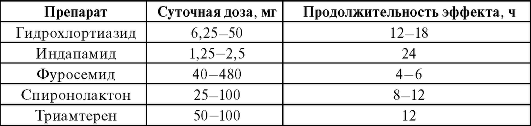
Применение мочегонных средств при АГ снижает вероятность развития ОНМК. Возможность развития инсульта и декомпенсации ХСН более выраженно снижается при длительном приеме сравнимых доз тиазидных и тиазидоподобных диуретиков (не менее 25 мг гидро-хлортиазида в сутки). При назначении тиазидных и тиазидоподоб-
ных диуретиков может снижаться скорость клубочковой фильтрации, и эти препараты (за исключением индапамида) не рекомендовано применять в качестве монотерапии у больных с нарушениями функций почек. Тиазидные диуретики нежелательно назначать для длительной монотерапии АГ у больных инсулинозависимым СД. По данным различных исследований, применение тиазидных диуретиков у таких больных существенно повышает их смертность. При лечении АГ у больных с инсулинонезависимым СД назначение тиазидных диуретиков допустимо в небольших дозах (не более 25 мг гидрохлор-тиазида или клопамида в сутки). Диуретики вызывают обратное развитие гипертрофии ЛЖ. В качестве монотерапии тиазидные и тиази-доподобные диуретики назначают в низких дозах. Увеличение дозы диуретика приводит к усилению гипотензивного эффекта, но и увеличивает риск НЛР. Мочегонные средства усиливают гипотензивное действие БАБ, ИАПФ, блокаторов АТ1-рецепторов.
10.8. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ ГИПОТЕНЗИВНЫХ СРЕДСТВ ЦЕНТРАЛЬНОГО
ДЕЙСТВИЯ
ЛС центрального действия снижают активность сосудодвигатель-ного центра продолговатого мозга, в настоящее время их назначают как дополнительные средства для лечения АГ.
Клонидин (Гемитон*®, клофелин*) - производное имидазолина, стимулятор центральных а2-адрено- и ^-рецепторов. Не рекомендован для постоянного применения, за исключением случаев рефрактерной к лечению или злокачественной АГ.
Фармакокинетика клонидина. Препарат хорошо всасывается из ЖКТ. При приеме внутрь действие препарата наступает через 30-60 мин, внутривенном введении - 3-6 мин. При энтеральном применении максимальная концентрация в крови регистрируется через 3-5 ч, T1/2-12-16 ч, при нарушении функций почек увеличивается до 41 ч. Клонидин выводится из организма почками в основном в виде метаболитов.
Фармакодинамика клонидина. Препарат стимулирует рецепторы ядер солитарного тракта продолговатого мозга, что приводит к угнетению нейронов сосудодвигательного центра и снижению симпатической иннервации. Гипотензивное действие препарата обусловлено снижением сердечного выброса и ОПСС. При внутривенном введении препара-
та гипотензивному действию может предшествовать кратковременное повышение АД из-за стимуляции а2-адренорецепторов сосудов.
НЛР. При прекращении приема препарата возникает синдром «отмены» - резкое повышение АД. Клонидин оказывает седативное и гипногенное действие, потенцирует центральные эффекты алкоголя, седативных средств, депрессантов. При сочетании клонидина с трициклическими антидепрессантами происходит повышение АД. Препарат снижает аппетит, секрецию слюнных желез, задерживает натрий и воду.
Противопоказания. Клонидин противопоказан при атеросклерозе сосудов головного мозга, депрессии, декомпенсации ХСН, а также пациентам, чья профессия требует повышенного внимания.
Метилдопа (Допегит*) превращается в а-метилнорадреналин, который стимулирует центральные а2-адренорецепторы в солитар-ном тракте.
Фармакокинетика метилдопы. При приеме внутрь всасывается 20-50% препарата. Максимальное гипотензивное действие развивается через 4-6 ч, длительность действия - до 24 ч, связывание с белками плазмы - 20%. Подвергается биотрансформации в печени, выводится почками.
Фармакодинамика метилдопы. Опосредованное снижение активности сосудодвигательного центра приводит к уменьшению ОПСС и снижению АД. На сердечную деятельность препарат оказывает незначительное влияние. Увеличивает скорость клубочковой фильтрации и почечный кровоток. Оказывает небольшое седативное действие. В экспериментальных исследованиях не выявлено неблагоприятного влияния препарата на плод, благодаря чему метилдопу можно рассматривать как препарат выбора при лечении АГ у беременных.
НЛР. Метилдопа может вызывать сонливость, сухость во рту, задержку ионов натрия и воды, редко - агранулоцитоз, миокардит, гемолитическую анемию. Метилдопу не комбинируют с трицикли-ческими антидепрессантами и симпатомиметическими аминами из-за возможности повышения АД.
Моксонидин (Физиотенз*) - агонист ^-рецепторов.
Фармакокинетика моксонидина. Препарат хорошо всасывается из ЖКТ и обладает высокой биодоступностью (88%). Максимальную концентрацию в крови регистрируют через 0,5-3 ч. 90% препарата выводится почками, в основном (70%) в неизмененном виде. Несмотря на короткий T1 / 2 (около 3 ч), он контролирует АД в течение суток.
Фармакодинамика. Активация имидазолиновых рецепторов в ЦНС приводит к снижению активности сосудодвигательного центра и уменьшению периферического сопротивления сосудов. Моксонидин эффективен в качестве монотерапии АГ. Он более безопасен, чем клонидин, пропранолол, каптоприл, нифедипин. Седативный эффект выражен значительно меньше, чем у других препаратов центрального действия.
НЛР. Моксонидин может вызывать утомляемость, головные боли, головокружение, нарушения сна.
Противопоказания к применению препарата - синдром слабости синусового узла, АВ-блокада II и III степени, выраженная брадикар-дия, тяжелые аритмии, нестабильная стенокардия.
Взаимодействие моксонидина с другими ЛС. Сочетание моксониди-на с другими гипотензивными средствами усиливает их антигипер-тензивный эффект. Препарат потенцирует эффекты ЛС, угнетающих ЦНС, - этанола, транквилизаторов, барбитуратов.
10.9. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ
ВАЗОДИЛАТАТОРОВ
Вазодилататоры для лечения АГ представлены препаратами двух групп: с преимущественным действием на артерии (гидралазин, минок-сидил) и смешанным действием (нитропруссид натрия) - табл. 10-19. Артериолярные вазодилататоры расширяют резистивные сосуды (арте-риолы и мелкие артерии) и снижают ОПСС. При этом происходит рефлекторное увеличение ЧСС и сердечного выброса. Увеличивается актив-
Таблица 10-19. Эффекты вазодилататоров
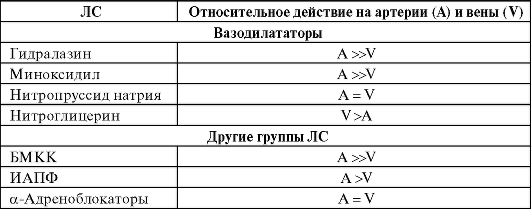
ность симпатоадреналовой системы и секреция ренина. Препараты вызывают задержку натрия и воды. Вазодилататоры смешанного действия вызывают еще и расширение емкостных сосудов (венул, мелких вен) с уменьшением венозного возврата крови к сердцу.
Гидралазин из-за большого количества НЛР (тахикардия, боли в области сердца, покраснение лица, головная боль, волчаночнопо-добный синдром) назначают редко и только в виде готовых сочетаний препаратов (адельфан-эзидрекс*). Он противопоказан при язве желудка, аутоиммунных процессах.
Диазоксид - артериолярный вазодилататор, активатор калиевых каналов. Влияние на калиевые каналы приводит к гиперполяризации мембраны мышечных клеток, что снижает поступление внутрь ионов кальция, необходимых для поддержания сосудистого тонуса. Препарат назначают внутривенно при гипертоническом кризе. Длительность действия - примерно 3 ч. Нежелательными реакциями при применении считают гипергликемию, ишемию мозга или миокарда. Препарат противопоказан при нарушениях мозгового кровообращения, в остром периоде ИМ.
Миноксидил (Регейн*) - артериолярный вазодилататор, активатор калиевых каналов. Препарат хорошо всасывается в ЖКТ. T1 / 2 - 4 ч. Миноксидил принимают внутрь 2 раза в сутки, постепенно увеличивая дозу. При местном применении вызывает активный рост волос, что можно использовать для лечения облысения.
Нитропруссид натрия - смешанный артериовенозный вазодила-татор. Гипотензивное действие связано с освобождением из молекулы препарата окиси азота, которая действует аналогично эндогенному эндотелий-расслабляющему фактору. Таким образом, его механизм действия схож с нитроглицерином. Нитропруссид натрия вызывает увеличение ЧСС, не увеличивая сердечного выброса. Однако при снижении сократительной функции ЛЖ препарат увеличивает сердечный выброс и его можно назначать при сердечной недостаточности и отеке легких. Нитропруссид натрия назначают внутривенно из-за того, что при приеме внутрь он не оказывает гипотензивного действия. При внутривенном введении латентный период препарата - 1-5 мин, после окончания введения действует еще 10-15 мин. Натрия нитропруссид применяют при гипертонических кризах, острой лево-желудочковой недостаточности. Из НЛР отмечают головную боль, беспокойство, тахикардию.
10.10. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ
ИНГИБИТОРА РЕНИНА
В настоящее время прошел клинические исследования и зарегистрирован во многих странах мира, в том числе и в РФ, первый селективный ингибитор ренина непептидной структуры, обладающий выраженной активностью, - алискирен.
Алискирен (Расилез*) действует, связываясь с активным сайтом молекулы ренина, тем самым предотвращая связывание ренина с ангиотензиногеном и блокируя образование ангиотензина I, предшественника ангиотензина II. Оптимальная начальная доза алиски-рена - 150 мг 1 раз в сутки; при необходимости дозу увеличивают до 300 мг. При мягкой и умеренной АГ алискирен можно назначать в качестве монотерапии 1 раз в сутки, обеспечивая достоверное дозо-зависимое снижение АД. Антигипертензивный эффект алискирена сохраняется в течение более чем 24 ч после приема.
Алискирен обладает по меньшей мере сопоставимой эффективностью с антигипертензивными препаратами других групп. Его анти-гипертензивный эффект усиливается при совместном назначении с ИАПФ, БРА, БМКК или диуретиками. Кроме того, в трех исследованиях были продемонстрированы дополнительные кардиопротектив-ные и нефропротективные свойства препарата. Добавление алискирена к стандартному лечению пациентов с АГ и ХСН приводит к достоверно большему снижению концентрации мозгового натрийуретического пептида в плазме крови (маркер тяжести сердечной недостаточности). Алискирен уменьшает гипертрофию миокарда ЛЖ у пациентов с АГ сопоставимо с лозартаном, а при добавлении к лозартану обеспечивает дополнительное уменьшение соотношения альбумин/креатинин в моче по сравнению с плацебо у пациентов с АГ, СД и нефропатией, что свидетельствует о выраженных нефропротективных свойствах препарата. Выраженность антигипертензивного эффекта алискирена не зависит от возраста, пола, расовой принадлежности и индекса массы тела.
10.11. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ
СИМПАТОЛИТИКОВ
В современной кардиологической практике данные ЛС используют редко. К симпатолитикам относят резерпин, гуанетидин. Эти препараты нарушают передачу возбуждения, действуя пресинапти-
чески. Воздействуя на окончания адренергических нервных волокон, эти вещества уменьшают количество норадреналина, выделяющегося в ответ на нервные импульсы. На адренорецепторы они не влияют.
Резерпин - алкалоид раувольфии. Препарат нарушает депонирование норадреналина в везикулах, что приводит к разрушению его цитоплазматической моноаминоксидазой. Резерпин уменьшает содержание норадреналина в сердце, сосудах, ЦНС и других органах. Гипотензивный эффект резерпина при приеме внутрь развивается постепенно в течение 7-10 сут, после внутривенного введения препарата - в течение 2-4 ч. Резерпин оказывает гипотензивное действие только у 25% больных, даже в условиях «мягкой» гипертензии.
НЛР: сонливость, депрессия, боли в желудке, диарея, брадикар-дия, бронхоспазм. Препарат вызывает задержку натрия и воды в организме. При длительном приеме возможно развитие лекарственного паркинсонизма.
Для лечения АГ до сих пор применяют официнальные комбинации ЛС, содержащих симпатолитики: резерпин, гидралазин и гидрохлор-тиазид; резерпин, дигидралазин®, гидрохлортиазид, калия хлорид; резерпин, а-адреноблокаторы - дигидроэргокристин и клопамид.
Гуанетидин нарушает процесс высвобождения норадреналина и препятствует обратному захвату медиатора симпатическими окончаниями. Снижение АД обусловлено уменьшением сердечного выброса и снижением ОПСС. Биодоступность препарата - 50%. T1/2 - около 5 сут.
НЛР: препарат вызывает постуральную гипотензию, резкую бра-дикардию, задержку в организме натрия и воды, головокружение, слабость, отек слизистой оболочки носа, диарею.
Противопоказания: выраженный атеросклероз, ОНМК, ИМ, почечная недостаточность, феохромоцитома.
10.12. ПРИНЦИПЫ ФАРМАКОТЕРАПИИ
ГИПЕРТОНИЧЕСКОГО КРИЗА
ГК - это остро возникшее выраженное повышение АД, сопровождающееся клиническими симптомами, требующее немедленного контролируемого снижения АД для предупреждения или ограничения поражения органов-мишеней.
Гипертонические кризы подразделяют на две большие группы - осложненные (жизнеугрожающие) и неосложненные (нежизнеугро-жающие).
ГК считают осложненным в следующих случаях:
- гипертоническая энцефалопатия;
- ОНМК;
- острый коронарный синдром (ОКС);
- острая левожелудочковая недостаточность;
- расслаивающая аневризма аорты;
- ГК при феохромоцитоме;
- преэклампсия или эклампсия;
- тяжелая АГ, ассоциированная с субарахноидальным кровоизлиянием или травмой головного мозга;
- АГ у больных в послеоперационном периоде и при угрозе кровотечения;
- ГК на фоне приема амфетаминов, кокаина и других препаратов. В большинстве случаев ГК развивается при систолическом
АД >180 мм рт. ст. и /или диастолическом АД >120 мм рт. ст., но возможно развитие этого неотложного состояния и при менее выраженном повышении АД. Всем больным с ГК требуется быстрое снижение АД.
ГК, как правило, сопровождается выраженной головной болью, головокружением, тошнотой, рвотой, ощущением жара, потливостью, сердцебиением, чувством нехватки воздуха. Особенно выраженное повышение АД может привести к развитию гипертонической энцефалопатии (сонливости, оглушенности, нарушению мозгового кровообращения) или развитию острой левожелудочковой недостаточности (отеку легких).
ГК требует неотложного лечения, так как резкое повышение АД создает угрозу нарушения мозгового кровообращения и развития острой сердечной недостаточности.
При неосложненном ГК возможно внутривенное или сублинг-вальное введение и прием антигипертензивных ЛС внутрь (в зависимости от выраженности повышения АД и симптомов). Лечение необходимо начинать немедленно, скорость снижения АД не должна превышать 25% за первые 2 ч, с последующим достижением целевого АД в течение нескольких часов (не более 24-48 ч) от начала лечения. Вводят препараты с относительно быстрым и коротким действием внутрь или сублингвально: каптоприл (25-50 мг), клонидин (0,1-0,2 мг), ранее применяли нифедипин (10-20 мг) и нитроглицерин (0,5 мг). Прием этих ЛС больной может осуществлять самостоятельно, используя инструкции лечащего врача. Однако следует помнить, что при сублингвальном приеме клонидина, нифедипина, каптоприла возможны резкое снижение АД и ухудшение мозгового кровообращения особенно у пожилых больных.
Лечение пациентов с осложненным ГК проводят в отделении неотложной кардиологии или палате интенсивной терапии кардиологического, неврологического или терапевтического отделения.
Применяют следующие препараты для лечения ГК (табл. 10-20):
• Вазодилататоры:
- эналаприл (предпочтителен при острой недостаточности ЛЖ);
- нитроглицерин в дозе 5-100 мкг/мин (предпочтителен при ОКС и острой недостаточности ЛЖ);
- нитропруссид натрия 0,5-10 мкг/кг в минуту (препарат выбора при гипертонической энцефалопатии, но следует учесть, что он может повышать внутричерепное давление).
• БАБ.
• Антиадренергические средства (фентоламин при подозрении на феохромоцитому).
• Диуретики (фуросемид при острой недостаточности ЛЖ).
• Нейролептики (дроперидол).
• Ганглиоблокаторы (пентамин).
Таблица 10-20. Основные препараты, применяемые для купирования гипертонических кризов, в зависимости от поражения органов-мишеней

При лечении пациентов с ГК следует помнить, что быстрое снижение АД может провоцировать развитие недостаточности мозгового кровообращения или другие опасные осложнения.
При впервые выявленном неосложненном ГК у больных с неясным генезом АГ, при некупирующемся ГК, частых повторных кризах показана госпитализация в кардиологическое или терапевтическое отделение стационара.
10.13. РЕФРАКТЕРНАЯ И ЗЛОКАЧЕСТВЕННАЯ
АРТЕРИАЛЬНАЯ ГИПЕРТЕНЗИЯ
Согласно современным национальным рекомендациям, рефрактерной или резистентной к лечению считают АГ, при которой назначенное лечение (изменение образа жизни и рациональное комбинированное антигипертензивное лечение с назначением адекватных доз не менее трех препаратов, включая диуретики) не приводит к достаточному снижению АД и достижению его целевого уровня. В таких случаях показано детальное обследование органов-мишеней - при рефрактерной АГ в них часто наблюдаются выраженные изменения. Необходимо исключить вторичные формы АГ, которые становятся причиной рефрактерности к лечению. Неадекватные дозы ЛС и их нерациональные сочетания также могут привести к недостаточному снижению АД. Рефрактерность АГ может быть связана с псевдогипертензией, например «гипертонией белого халата» или использованием несоответствующей по размеру манжеты.
Основные причины рефрактерной АГ
• Отсутствие приверженности лечению (несоблюдение режима приема и доз назначенных препаратов).
• Нарушение или отказ от рекомендаций по изменению образа жизни: прибавка массы тела, злоупотребление алкоголем, продолжение курения.
• Перегрузка объемом, обусловленная следующими причинами: избыточное потребление поваренной соли, неадекватное лечение диуретиками, прогрессирование ХПН, гиперальдостеронизм.
• Продолжающийся прием ЛС, повышающих АД или снижающих эффективность лечения (глюкокортикоиды, НПВС).
• Недиагностированные вторичные формы АГ.
• Нелеченый синдром обструктивного ночного апноэ.
• Тяжелое поражение органов-мишеней.
Тщательный анализ всех возможных причин рефрактерной АГ способствует рациональному выбору антигипертензивного лечения. Для контроля АД при рефрактерной АГ может потребоваться назначение более трех антигипертензивных препаратов.
Проблема сочетания трех препаратов и более еще недостаточно изучена, поскольку нет результатов рандомизированных, контролируемых, клинических исследований, изучавших тройную комбинацию антигипертензивных ЛС. Однако у многих пациентов, в том
числе у больных с рефрактерной АГ, только с помощью трех препаратов и более можно достичь целевого уровня АД.
Согласно современным национальным рекомендациям, к рациональным комбинациям трех антигипертензивных ЛС относят:
- БРА + дигидропиридиновый БМКК + диуретик;
- ИАПФ + дигидропиридиновый БМКК + диуретик;
- БРА + дигидропиридиновый БМКК + БАБ;
- ИАПФ + дигидропиридиновый БМКК + БАБ;
- БРА + диуретик + БАБ; ИАПФ + диуретик + БАБ;
- дигидропиридиновый БМКК + диуретик + БАБ. Злокачественная АГ встречается редко. При злокачественной АГ
наблюдается крайне высокое АД (>180/120 мм рт. ст.) с развитием тяжелых изменений сосудистой стенки (фибриноидный некроз), что приводит к кровоизлияниям и /или отеку соска зрительного нерва, ишемии тканей и нарушению функций различных органов. Переход АГ в злокачественную форму возможен при всех ее формах, но чаще это происходит у пациентов с вторичной или тяжелой АГ. В развитии злокачественной АГ принимают участие различные нейро-гормональные системы. Активация их деятельности увеличивает экскрецию натрия, гиповолемию, а также повреждает эндотелий и вызывает пролиферацию гладкомышечных клеток сосудов. Все эти изменения сопровождаются продолжающимся выбросом в кровяное русло вазоконстрикторов и еще большим повышением АД. Синдром злокачественной АГ обычно сопровождается симптомами со стороны ЦНС, прогрессированием ХПН, ухудшением зрения, снижением массы тела, изменениями реологических свойств крови, вплоть до развития диссеминированного внутрисосудистого свертывания (ДВС) или гемолитической анемии. Эффективное и своевременное лечение улучшает прогноз, тогда как при его отсутствии 50% пациентов умирают в течение года.
Наличие злокачественной АГ оценивается как тяжелое состояние и требует снижения диастолического АД до 100-110 мм рт. ст. в течение 24 ч. Пациентам со злокачественной АГ показано лечение тремя антигипертензивными препаратами и более. Следует помнить о возможности избыточного выведения из организма натрия, особенно при назначении диуретиков, что сопровождается дальнейшей активацией РААС и повышением АД. Пациента со злокачественной АГ необходимо тщательно обследовать на предмет наличия вторичной АГ.
10.14. АРТЕРИАЛЬНАЯ ГИПЕРТЕНЗИЯ У ЛИЦ ПОЖИЛОГО ВОЗРАСТА
Согласно современным международным и национальным рекомендациям по лечению АГ, принципы лечения пожилых больных такие же, как в общей популяции. Лечение следует начинать с изменения образа жизни. Ограничение потребления поваренной соли и снижение массы тела у этой категории больных оказывают существенный антигипертензивный эффект. Для медикаментозного лечения можно применять ЛС разных классов: тиазидные диуретики, БМКК, БАБ, ИАПФ и БРА. У большинства пожилых пациентов имеются другие факторы риска, сопутствующие заболевания, что необходимо учитывать при выборе ЛС первого ряда.
В целом, как свидетельствуют результаты завершенных крупномасштабных исследований, при лечении АГ в пожилом возрасте наиболее эффективны тиазидные диуретики, БМКК и БРА. Начальная доза антигипертензивных препаратов у некоторых пожилых пациентов может быть снижена; вместе с тем большинству больных этой категории требуется назначение стандартных доз для достижения целевого АД. Пожилым пациентам необходима особая осторожность при назначении и титровании дозы антигипертензивных ЛС из-за большего риска развития побочных эффектов. При этом особое внимание следует обратить на возможность развития ортостатиче-ской гипотонии и измерять АД также и в положении стоя.
Целевой уровень систолического АД должен быть менее 140 мм рт. ст., и для его достижения часто требуется сочетание двух антиги-пертензивных препаратов и более. Оптимальная величина диастоли-ческого АД у пожилых больных точно не определена, но, по результатам анализа ряда исследований, его снижение менее 70 мм рт. ст. и особенно менее 60 мм рт. ст. ухудшает прогноз заболевания.
10.15. АРТЕРИАЛЬНАЯ ГИПЕРТЕНЗИЯ
У БЕРЕМЕННЫХ
АГ и связанные с ней осложнения до настоящего времени остаются одной из основных причин заболеваемости и смертности матери, плода и новорожденных. Цель лечения беременных с АГ - предупредить развитие осложнений, обусловленных высоким АД, обеспечить сохранение беременности, нормальное развитие плода и успешные роды.
Целевой уровень АД для беременных составляет менее 140/90 мм рт. ст., но следует избегать эпизодов гипотонии, предотвращая нарушения плацентарного кровотока. Немедикаментозное лечение целесообразно при АД - 140-149/90-94 мм рт. ст. и активном наблюдении. Следует ограничить физическую активность; данных о целесообразности ограничения потребления соли у беременных недостаточно. Снижение массы тела во время беременности не рекомендуют даже пациенткам с ожирением. У женщин с длительно существующей АГ, сопровождающейся поражением органов-мишеней, а также требовавшей до наступления беременности приема больших доз антигипертензивных препаратов, во время беременности антигипертензивное лечение необходимо продолжить. Женщины, у которых АД хорошо контролировалось до беременности, могут принимать те же препараты, за исключением ИАПФ и БРА. Практически все антигипертензивные препараты проникают через плаценту и потенциально способны оказывать нежелательное влияние на плод, новорожденного и /или дальнейшее развитие ребенка. Таким образом, спектр ЛС, используемых при беременности, ограничен. Препаратами первой линии считают метилдопу, дигидропиридиновые БМКК (нифедипин) и кардиоселективные БАБ. В качестве дополнительных препаратов для комбинированного лечения возможно назначение диуретиков (гипотиазид). Противопоказано назначение ИАПФ, БРА и препаратов раувольфии из-за возможного проявления пороков развития и гибели плода. Следует воздержаться от назначения малоизученных при беременности ЛС, таких, как индапамид и агонисты имидазолиновых рецепторов.
Согласно современным международным и национальным рекомендациям по лечению АГ, систолическое АД >170 и диастоличе-ское АД >110 мм рт. ст. у беременной расценивают как неотложное состояние, требующее госпитализации. Главное правило при лечении ГК - осторожное и контролируемое снижение АД не более 20% от исходного. Внутрь назначают метилдопу или нифедипин; при неэффективности возможно кратковременное назначение нитропруссида натрия или гидралазина. Для лечения преэклампсии с отеком легких препаратом выбора считают нитроглицерин. Его введение возможно на протяжении не более 4 ч, из-за отрицательного воздействия на плод и риска развития отека мозга у матери. Применение диуретиков не оправдано - при преэклампсии уменьшается ОЦК.
10.16. АРТЕРИАЛЬНАЯ ГИПЕРТЕНЗИЯ У ПАЦИЕНТОВ
С МЕТАБОЛИЧЕСКИМ СИНДРОМОМ И САХАРНЫМ
ДИАБЕТОМ
Сочетание СД и АГ заслуживает особого внимания, поскольку оба заболевания существенно увеличивают риск развития микро-и макрососудистых поражений, включая диабетическую нефропа-тию, ОНМК, ИБС, ИМ, ХСН, заболевания периферических сосудов, и способствуют увеличению сердечно-сосудистой смертности.
Мероприятия по изменению образа жизни, особенно соблюдение низкокалорийной диеты, увеличение физической активности и ограничение потребления поваренной соли, должны быть максимально использованы из-за того, что ожирение имеет большое значение в прогрессировании СД II типа. Уменьшение массы тела пациентов с АГ и СД помогает дополнительно снизить АД и увеличить чувствительность тканей к инсулину. Антигипертензивное лечение у больных АГ и СД необходимо начинать при высоком нормальном АД.
Согласно современным международным и национальным рекомендациям по лечению АГ, для больных СД установлен целевой уровень АД менее 130/80 мм рт. ст. При высоком нормальном АД возможно достижение его целевого уровня на фоне монотерапии. Остальным пациентам, как правило, необходимо комбинированное назначение двух ЛС и более. Препаратами первого ряда считают БРА или ИАПФ, что обусловлено их наилучшим нефропротективным эффектом. В качестве комбинированного лечения к ним целесообразно добавить БМКК, агонисты имидазолиновых рецепторов, тиазидные диуретики в низких дозах, небиволол или карведилол. Доказана также эффективность лечения фиксированным сочетанием периндоприла с индапа-мидом у больных СД II типа для снижения риска сердечно-сосудистых осложнений и смерти от них. Учитывая больший риск возникновения ортостатической гипотонии, необходимо дополнительно измерять АД в положении стоя. При лечении больных АГ и СД необходимо контролировать все имеющиеся у пациента факторы риска.
Наличие диабетической нефропатии, в частности микроальбуминурии, у больных АГ связано с очень высоким риском развития сердечно-сосудистых осложнений. Для коррекции нефропатии необходим строгий контроль АД на уровне <130/80 мм рт. ст. и уменьшение протеинурии до минимально возможных значений. Наиболее эффективными классами ЛС для профилактики или лечения диабетической нефропатии в настоящее время считают БРА и ИАПФ.
Метаболический синдром (МС) подробно рассматривается в главе 16.
Согласно современным международным и национальным рекомендациям, основа лечения пациента с МС - немедикаментозные мероприятия, направленные на снижение массы тела, изменение стереотипов питания и повышение физической активности - формирование здорового образа жизни. При недостаточной эффективности немедикаментозных методов лечения или наличии показаний возможна медикаментозная или хирургическая коррекция массы тела. Обязательной считают коррекцию имеющихся нарушений углеводного, липидного и пуринового обмена.
Выбор тактики ведения больных с МС индивидуален и зависит от степени ожирения, наличия или отсутствия АГ и других проявлений МС. У пациентов с высоким и очень высоким риском сердечно-сосудистых осложнений необходимо немедленно назначить антигипертензивные препараты и проводить лечение, направленное на устранение абдоминального ожирения, инсулинорезистентности, гипергликемии, дислипидемии.
При выборе препарата необходимо учитывать его влияние на углеводный и липидный обмены. Преимуществом должны пользоваться метаболически нейтральные ЛС. Препаратами первого ряда для лечения АГ у больных с МС считают БРА или ИАПФ, для которых доказаны метаболическая нейтральность и органопротективное действие. При недостаточной эффективности монотерапии для достижения целевого уровня АД к ним целесообразно присоединять БМКК или агонисты имидазолиновых рецепторов. Доказано, что эти сочетания хорошо снижают АД, благоприятно воздействуют на органы-мишени и снижают риск развития СД.
Без отчетливых показаний больным АГ и МС не следует назначать БАБ, поскольку многие из них негативно влияют на чувствительность к инсулину, углеводный и липидный обмены. Исключением можно считать небиволол и карведилол, обладающие дополнительными вазодилатирующими свойствами, а также высокоселективный бисопролол. Эти препараты можно рекомендовать пациентам с АГ и МС в составе комбинированного лечения.
Тиазидные или петлевые диуретики также можно назначать пациентам с АГ и МС в составе комбинированного лечения с БРА или ИАПФ. Наиболее безопасным мочегонным препаратом считают тиазидоподобный диуретик индапамид. Пациентам с АГ при наличии метаболических нарушений следует избегать сочетания БАБ
и диуретиков из-за того, что оба препарата неблагоприятно влияют на липидный, углеводный и пуриновый обмен.
Таким образом, при коррекции АГ у больных с МС необходимо добиваться полной нормализации АД. Наиболее важное требование при выборе гипотензивной терапии - отсутствие отрицательного метаболического действия препарата.