Клиническая фармакология и фармакотерапия: учебник. - 3-е изд., перераб. и доп. / под ред. В. Г. Кукеса, А. К. Стародубцева. - 2012. - 840 с.: ил.
|
|
|
|
Глава 15. БОЛЕЗНИ ПОЧЕК И КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ ДИУРЕТИКОВ
15.1. СИМПТОМЫ ПОРАЖЕНИЯ ПОЧЕК
Для заболеваний почек характерно наличие некоторых общих симптомов, которые могут присутствовать у больных в различных сочетаниях:
- олигурия - состояние, при котором объем выделяемой мочи у взрослого человека со средней массой тела составляет <500 мл/сут;
- анурия - практически полное отсутствие отделения мочи
(<100 мл/ сут);
- полиурия - увеличение отделения мочи >2500 мл/сут;
- гематурия - присутствие крови в моче (при микрогематурии эритроциты в моче выявляют при микроскопии, макрогематурия - изменение цвета мочи до красного или коричневого);
- отеки - симптом, обусловленный избытком натрия и воды во внеклеточном пространстве. На ранних стадиях избыток воды проявляется только увеличением массы тела больного, но позднее отеки становятся явными. При заболеваниях почек отеки часто (но не всегда) локализуются на лице и более выражены в утренние часы;
- анемия (в почках происходит синтез эритропоэтина, который стимулирует образование эритроцитов в костном мозге) и вторичная АГ.
Прогрессирование почечной недостаточности может приводить к развитию генерализованных отеков - анасарки, кроме того, избыточная жидкость может накапливаться:
- в плевральной полости - гидроторакс;
- полости перикарда - гидроперикард;
- брюшной полости - асцит.
К лабораторным симптомам поражения почек следует отнести:
- протеинурию - наличие белка в моче;
- цилиндрурию - экскрецию с мочой цилиндров, которые представляют собой «слепок», образующийся в просвете канальцев из белка или клеточных элементов; различают гиалиновые, зернистые, восковидные, эритроцитарные и лейкоцитарные цилиндры;
- снижение удельного веса мочи и ее осмолярности;
- увеличение концентрации креатинина в сыворотке крови (скорость образования креатинина в организме относительно постоянна, а экскреция происходит только путем фильтрации); нормальные показатели концентрации креатинина в крови - 0,04-0,13 ммоль/л; по концентрации креатинина можно оценить скорость клубочковой фильтрации.
Основные синдромы поражения почек
К основным синдромам поражения почек относят:
- мочевой;
- отечный;
- нефротический;
- АГ.
Мочевой синдром
Мочевой синдром - наиболее постоянный признак поражения почек и мочевыводящих путей. Его диагностическое значение особенно велико при отсутствии экстраренальных признаков заболевания почек (отеки, гипертензия), когда изменения в моче - единственный диагностический критерий патологии почек или мочевыводящих путей, например при гломерулонефрите с изолированным мочевым синдромом, хроническом пиелонефрите с латентным течением, начальной стадии амилоидоза почек.
В понятие «мочевой синдром» входят протеинурия, гематурия, лейкоцитурия и цилиндрурия.
Отечный синдром
Отеки встречаются при многих заболеваниях почек, прежде всего таких, как острый и хронический гломерулонефрит, нефро-патия беременных, амилоидоз почек, диабетический гломеруло-склероз. Выраженность отечного синдрома может быть различной. В одних случаях отеки бывают незначительными в виде пастоз-ности лица и голеней, в других - умеренными и хорошо разли-
чимыми при осмотре больного, в третьих - резко выраженными, массивными, часто в виде анасарки с асцитом, гидротораксом, гидроперикардом, что в наибольшей степени свойственно нефро-тическому синдрому.
В отличие от сердечных отеков, которые обычно располагаются на отлогих местах (стопах и голенях, в области поясницы), почечные отеки распространяются везде - на лице, туловище, конечностях. В одних случаях они образуются быстро (в течение нескольких часов или суток), в других - медленно, постепенно нарастая в течение многих дней. Они могут быть плотными на ощупь или, наоборот, мягкими, тестоватыми, когда при надавливании пальцем долго остается ямка, например при нефротических отеках. У некоторых больных видимые отеки могут вообще отсутствовать, несмотря на явную задержку жидкости в организме, определяемую по уменьшению количества мочи (олигурия).
Синдром артериальной гипертензии
Артериальная гипертензия - один из наиболее частых и характерных признаков многих первичных и вторичных, дву- и односторонних заболеваний почек. Она занимает ведущее место среди симптоматических артериальных гипертензий.
Этиология
К возникновению ренальной гипертензии приводят:
- диффузный гломерулонефрит;
- хронический пиелонефрит;
- патология сосудов почек;
- диффузные заболевания соединительной ткани - системная красная волчанка, системная склеродермия;
- узелковый периартериит;
- ревматоидный артрит;
- диабетический гломерулосклероз;
- нефропатия беременных;
- амилоидоз почек ;
- мочекаменная болезнь;
- аномалии развития почек (поликистоз, гипо- и дисплазия почек, подковообразная почка);
- аномалии развития мочевыводящих путей (стриктура мочеточника, гидроуретер).
Клинико-фармакологические подходы к лечению синдрома АГ. Лечение ренальной АГ направлено на основной патогенетический процесс: назначение глюкокортикоидов, коррекция гликемии, оперативное лечение и т.д. С симптоматической целью назначают гипотензивные ЛС (см. главу 10), ограничивают потребление поваренной соли.
Нефротический синдром
Нефротический синдром - комплекс симптомов, связанный с длительным и сильно выраженным повышением проницаемости клубочков почек для белка. Главный признак - протеинурия (выделение белка с мочой в количестве >3 г/ м2 в сутки), гипоальбумине-мия (снижение концентрации альбумина в сыворотке ниже 25 г/л), гиперлипидемия и генерализованные отеки.
Этиология и патогенез
Нефротический синдром может развиться в любом возрасте. Описаны случаи наследственного (семейного) Нефротический синдром и нефротический синдром с первичным поражением почек. Этот синдром может возникать при целом ряде заболеваний, приводящих к хроническому поражению ткани почек (нефротический синдром с вторичным поражением почек):
- сахарный диабет;
- амилоидоз;
- хронический гломерулонефрит;
- аутоиммунные заболевания (системная красная волчанка, узелковый периартериит);
- лейкозы, лимфомы, миеломная болезнь;
- лекарственное повреждение почек (препараты золота, пени-цилламин, НПВС, препараты лития, неочищенный героин);
- инфекции (острый гломерулонефрит, вирусный гепатит В, ВИЧ). Симптомокомплекс. Ранний признак нефротического синдрома -
появление пенистой мочи. Затем у больных возникает протеинурия, снижается концентрация белка в плазме, аппетит, появляются отеки, боли в животе и атрофия мышц. Часто выявляются асцит и выпот в плевральной полости.
Диагноз и методы обследования. Диагноз нефротического синдрома основан на характерных симптомах и наличии протеинурии >2 г / м2 в сутки, но окончательный диагноз ставят на основании гистологического исследования ткани почки.
Клинико-фармакологические подходы к лечению нефротического синдрома
Лечение нефротического синдрома направлено на основной патогенетический процесс. При иммунных поражениях почек показано назначение глюкокортикоидов, в некоторых случаях применяют цитостатики. Выбор ЛС зависит от морфологической картины поражения ткани почек, и всем больным с нефротическим синдромом проводят биопсию. В качестве симптоматического лечения назначают гипотензивные ЛС, ограничивают потребление поваренной соли. На поздних стадиях нефротического синдрома показаны гемодиализ, трансплантация почки.
Контроль эффективности проводимого лечения основан на динамике лабораторных показателей (протеинурия, концентрация креа-тинина в плазме).
15.2. ОСТРАЯ ПОЧЕЧНАЯ НЕДОСТАТОЧНОСТЬ
ОПН - состояние, проявляющееся быстро и непрерывно нарастающей азотемией и олигурией.
Этиология и патогенез
К развитию ОПН может приводить целый ряд заболеваний и состояний, которые принято разделять на три группы:
- преренальные (дословно: допочечные), связанные с нарушением нормального кровообращения в почках: массивные кровотечения, гипотония, септический шок, печеночная недостаточность, ожоги (потеря жидкости и электролитов + повреждение нефронов миоглобином и гемоглобином);
- ренальные - собственно связанные с повреждением ткани почек: острое поражение почек (ишемия, воздействие токсинов и рентгеноконтрастных препаратов, аминогликозидов, повреждения, вызванные миоглобином и гемоглобином), тяжелая АГ, острый гломерулонефрит, ДВС-синдром, обструкция почечных артерий или вен, пиелонефрит, подагра, миеломная болезнь;
- постренальные (дословно: послепочечные), связанные с нарушением оттока мочи из почек: простатит, опухоли мочевого пузыря, камни в мочевыводящих путях.
Диагноз и методы обследования
Основные симптомы ОПН - олигурия или анурия, а также прогрессирующее повышение концентрации креатинина в плазме. Затем у больных увеличивается концентрация калия в сыворотке крови, появляются АГ, отеки и геморрагические осложнения.
В тех случаях, когда развитие ОПН связано с шоком, ожогами, ХСН, диагноз, как правило, не вызывает затруднений. Появление гематурии может указывать на наличие опухоли или острого гло-мерулонефрита. При выявлении в крови повышения концентрации мочевой кислоты и наличии поражения суставов можно заподозрить подагру. В каждом случае ОПН следует выяснить, не принимает ли больной нефротоксичные ЛС: аминогликозиды или рентгенокон-трастные препараты.
ОПН - излечимое состояние, выживаемость больных при своевременном лечении составляет 60%. Чаще к смерти больного приводит не сама ОПН, а те заболевания, которые привели к ее развитию (травмы, ожоги, ДВС-синдром).
В течении ОПН выделяют три периода: продромальный (длительность которого зависит от причины ОПН), олигурический период (продолжается от 1-2 сут до 6-8 нед) и постолигурическую фазу.
Диагноз устанавливают при быстром нарастании у больного концентрации креатинина в крови и прогрессирующей олигурии.
Клинико-фармакологические подходы к лечению острой почечной недостаточности
Развитие ОПН часто можно предотвратить путем поддержания нормального ОЦК и адекватного уровня АД. У больных с острой кровопотерей и ожогами для этих целей проводят переливание свежезамороженной плазмы, альбумина человека, солевых растворов. При артериальной гипотонии на фоне нормального объема циркулирующий жидкости (шок, сепсис) применяют сосудосуживающие агенты (допамин).
При заболеваниях, сопровождающихся гемолизом и острым некрозом скелетных мышц, в крови и моче появляются гемоглобин и миоглобин, оказывающие повреждающее действие на почки. При обнаружении этих пигментов в моче необходимо назначение маннитола и фуросемида до нормализации показателей.
При первых симптомах ОПН внутривенное введение высоких доз фуросемида в сочетании с маннитолом или допамином иногда позволяет восстановить нормальный диурез.
Больным с олигурической фазой ОПН показан гемодиализ. Также следует значительно (до 500 мл/сут) ограничить прием жидкости, исключить поваренную соль и продукты, богатые калием. У таких больных необходимо отменить прием всех ЛС, элиминация которых происходит через почки, а также прием рентгеноконтрастных препаратов.
Контроль эффективности и безопасности лечения при ОПН в первую очередь направлен на оценку водно-электролитного состояния организма и требует регулярного мониторирования диуреза, массы тела больного, концентрации в крови креатинина, а также калия и натрия.
15.3. ХРОНИЧЕСКАЯ ПОЧЕЧНАЯ
НЕДОСТАТОЧНОСТЬ
ХПН - состояние, развивающееся в исходе множества патологических процессов, ведущих к нарушению и недостаточности экскреторной и регуляторной функции почек.
Этиология и патогенез
Причины развития ХПН многообразны:
- заболевания почек (гломерулонефрит);
- поражения почек при нарушении обмена веществ (СД, подагра);
- диффузные заболевания соединительной ткани (системная красная волчанка);
- хронические инфекции (пиелонефрит);
- АГ;
- воздействие токсических факторов. Прогрессированию ХПН способствуют снижение ОЦК и гипотония, декомпенсированная ХСН, АГ, инфекционные заболевания, обструкция мочевыводящих путей, тромбоз почечных вен и воздействие нефротоксических веществ.
Течение и тяжесть заболевания
В течение ХПН выделяют три стадии:
- снижение функциональных резервов почек;
- декомпенсированную почечную недостаточность;
- уремию.
ХПН может прогрессировать с различной скоростью. Развитие у больных гиперкалиемии, олигурии и перикардита свидетельствует о терминальной стадии заболевания, но и у этих пациентов применение гемодиализа, а в последующем трансплантация почки может обеспечить благоприятный исход.
Диагноз и методы обследования
На начальных стадиях ХПН (при снижении скорости клубочковой фильтрации >50% от должного) симптомы заболевания могут почти полностью отсутствовать, несмотря на увеличение концентрации креатини-на и мочевины в крови. По мере прогрессирования заболевания пациенты отмечают появление слабости, утомляемости. Прогрессирование ХПН обычно сопровождается появлением нейропатии и мышечных спазмов. Со стороны ЖКТ отмечаются потеря аппетита, тошнота, рвота, у больных с ХПН увеличивается риск развития эрозий и язв желудка. Задержка жидкости в организме проявляется отеками, гидротораксом, гидроперикардом и перегрузкой сердца увеличенным ОЦК, что может привести к развитию или прогрессированию сердечной недостаточности. Увеличение ОЦК сопровождается повышением АД.
Характерные лабораторные симптомы ХПН - увеличение концентрации креатинина, мочевины и калия в крови, умеренный ацидоз, анемия. Осмолярность мочи у таких больных близка к осмоляр-ности плазмы.
Диагностика ХПН основана на лабораторных данных - концентрации креатинина и мочевины в крови и определении СКФ. Кроме того, используют инструментальные методы исследований - урогра-фию, УЗИ. Важным прогностическим критерием считают увеличение концентрации калия в крови.
Клинико-фармакологические подходы к лечению хронической почечной недостаточности
Потребность больных ХПН в гемодиализе в нашей стране удовлетворяется лишь на несколько процентов. Из-за этого консервативное лечение имеет особенно большое значение. Оно включает в себя:
- ограничение потребления поваренной соли;
- ограничение потребления белка для уменьшения накопления в организме азотистых шлаков;
- ограничение поступления фосфора с пищей (увеличение концентрации фосфатов в крови больных ХПН приводит к прогрес-сированию заболевания и развитию дистрофии костной ткани); при выраженном снижении СКФ назначают ЛС, препятствующие всасыванию фосфора в кишечнике (антацидные препараты, содержащие гидроокись алюминия и кальция карбонат);
- для борьбы с гипокальциемией назначают препараты витамина D;
- активная коррекция АГ предполагает назначение гипотензивных ЛС, не уменьшающих почечный кровоток (клонидин, лабетолол®);
- при задержке жидкости в организме назначают петлевые диуретики;
- коррекция ацидоза может потребовать применения натрия бикарбоната;
- при лечении анемии, обусловленной ХПН, назначают эпоэтин бета.
Неэффективность консервативной терапии ХПН требует проведения гемодиализа и трансплантации почки.
Контроль эффективности и безопасности лечения ХПН основан на измерении концентрации креатинина и мочевины в крови. Для мониторинга безопасности диуретиков измеряют концентрацию калия в крови и оценивают кислотно-основное состояние. О развитии у больного такого потенциально опасного осложнения, как гиперка-лиемия, может свидетельствовать изменение зубца Т на ЭКГ.
15.4. ОСТРЫЙ ГЛОМЕРУЛОНЕФРИТ
Острый гломерулонефрит - заболевание, характеризующееся диффузными воспалительными изменениями в клубочках, а клинически - внезапным появлением гематурии, незначительной про-теинурией и во многих случаях гипертензией, отеками и азотемией.
Эпидемиология. Заболевают в основном дети, случаи заболевания во взрослом возрасте редки (5%).
Этиология и патогенез
Острый гломерулонефрит - иммунокомплексное заболевание, наиболее частой причиной его развития считают стрептококко-
вую инфекцию (реже острый гломерулонефрит возникает при других инфекциях: бактериальном эндокардите, пневмонии, абсцессах, ветряной оспе, вирусном гепатите). При этом заболевании антигены стрептококка группы А вызывают продукцию антител, а образовавшиеся иммунные комплексы (антиген - антитело) откладываются в стенках капилляров клубочков, что ведет к их повреждению и повышению проницаемости.
Симптомокомплекс
Латентный период между инфекционным заболеванием и развитием гломерулонефрита составляет около 2 нед. Основные симптомы гломерулонефрита - отеки, олигурия, гематурия, гиперволе-мия и АГ. В моче присутствуют эритроциты в виде эритроцитарных цилиндров и белка. В крови выявляют антитела к стрептококкам (антистрептолизин-О, антистрептокиназы, антигиалуронидазы).
Течение и тяжесть заболевания
Прогноз при остром гломерулонефрите обычно благоприятный, но в 1% случаев у детей и в 10% случаев у взрослых наблюдается про-грессирование заболевания с исходом в ОПН.
Диагностика и методы обследования
Диагноз ставят на основании клинических (предшествующая стрептококковая инфекция) и лабораторных (эритроцитарные цилиндры в моче, антитела к стрептококкам в крови) данных. В сложных случаях для уточнения диагноза проводят биопсию почек.
Клинико-фармакологические подходы к лечению острого гломерулонефрита
Специфического лечения острого гломерулонефрита не существует. Необходима санация хронических очагов инфекции, назначают симптоматическое лечение (гипотензивные ЛС, диуретики), ограничивают потребление поваренной соли, в некоторых случаях при затяжном течении эффективны глюкокортикоиды.
15.5. МОЧЕКАМЕННАЯ БОЛЕЗНЬ
Мочекаменная болезнь - заболевание почек, характеризующееся отложением конкрементов (камней) в чашечно-лоханочной системе.
Этиология и патогенез
В рамках каждого вида мочекаменной болезни различают:
- первичный нефролитиаз, этиология которого связана с особенностями питания (чрезмерное употребление животного белка, гиповитаминозы) и состава питьевой воды;
- вторичный нефролитиаз, развивающийся при заболеваниях, сопровождающихся метаболическими нарушениями, - гипер-кальциурией, гиперкальциемией (первичный гиперпаратиреоз, саркоидоз), гиперурикемией (подагра, миелопролиферативные заболевания), гипероксалурией (хронический энтерит);
- смешанный нефролитиаз всегда вторичный и вызывается инфекцией мочевыводящих путей; содержащая фермент уреазу бактериальная флора (протей) расщепляет мочевину до аммиака, в результате чего происходит резкий сдвиг рН мочи в сторону щелочи, что способствует кристаллизации фосфатов кальция, магния, аммония (триппельфосфатов).
Несмотря на разнообразие механизмов формирования нефроли-тиаза, выделяют общие патогенетические факторы: высокую концентрацию солей в моче (гиперэкскреция, дегидратация, олигу-рия); изменение химических (стойкий сдвиг рН) и стабилизирующих (дефицит ингибиторов кристаллизации) свойств мочи; алиментарный фактор; нарушения уродинамики (пузырно-мочеточниковый рефлюкс, повреждение спинного мозга, беременность, гиподинамия); инфекционный фактор (содержащая уреазу флора, шистосо-моз). В зависимости от химического состава конкрементов различают кальциевый (карбонатный), оксалатный, уратный, цистиновый и смешанный (фосфатный) нефролитиаз.
Симптомокомплекс мочекаменной болезни
Типичное клиническое проявление нефролитиаза - болевой синдром, вызванный мелкими конкрементами. Тупая боль в поясничной области обусловлена большими малоподвижными камнями. Иногда наблюдается безболевое латентное течение болезни, которую диа-
гностируют при инструментальном исследовании по поводу микрогематурии или в связи с присоединением осложнений мочекаменной болезни - пиелонефрита, макрогематурии, гидро- и пионефроза, сморщивания почки с синдромом АГ.
Диагноз и методы обследования
Предварительный диагноз может быть установлен при выявлении типичной клинической картины почечной колики с гематурией и положительным симптомом Пастернацкого: рентгенологического, УЗИ. Для установления вида и формы нефролитиаза необходимо провести исследование состава мочевых камней и обнаружить кри-сталлурию. Для уточнения состояния уродинамики используют экскреторную урографию.
При часто рецидивирующем нефролитиазе необходимо использовать специальные методы исследования мочи (рН, суточную экскрецию кальция, фосфатов, мочевой кислоты, оксалатов, цистина), а также определять уровень кальция, неорганических фосфатов, мочевой кислоты и паратиреоидного гормона в сыворотке крови.
Клинико-фармакологические подходы к лечению мочекаменной болезни
При мелких конкрементах, не нарушающих отток мочи, проводят консервативное лечение, направленное на их изгнание. Для этого используют миотропные спазмолитики (дротаверин, метамизол натрия) и водную нагрузку. При уратном нефролитиазе возможно проведение литолиза цитратными препаратами (солимок*, уралит*®, магурлит*®). В некоторых случаях используют дистанционную ударно-волновую литотрипсию; при развитии ОПН, пиелонефрита показано хирургическое лечение.
15.6. ПИЕЛОНЕФРИТ
Пиелонефрит - неспецифический инфекционно-воспалительный процесс, при котором одновременно или последовательно поражаются паренхима (преимущественно интерстициальная ткань) и лоханка почки.
Этиология
Неосложненные инфекции обычно вызваны одним микроорганизмом из семейства Enterobacteriaceae. Основной возбудитель пиелонефрита - Escherichia coli, реже: Proteus spp., Klebsiella spp. и др. При осложненной инфекции частота выделения E. coli снижается, чаще встречаются другие возбудители: Proteus spp., Pseudomonas spp., Klebsiella spp. и другие энтеробактерии.
Формы заболевания
По характеру течения пиелонефрит подразделяется на неосложнен-ный и осложненный. Неосложненной считается инфекция мочевыво-дящих путей при отсутствии обструктивных изменений почек и моче-выводящих путей, а также у пациентов без серьезных сопутствующих заболеваний. Осложненный пиелонефрит развивается у пациентов с обструктивными изменениями мочевыводящих путей [стриктуры (сужения), камни, опухоли, гипертрофия простаты], а также пиелонефрит, возникший на фоне инструментальных методов обследования и лечения, тяжелых сопутствующих заболеваний (СД, нейтропения).
Симптомокомплекс
Клиническая картина острого пиелонефрита включает в себя общие симптомы (озноб, лихорадку, тахикардию, недомогание, тошноту и рвоту) и специфические признаки (боль в поясничной области, дизурические явления).
Диагноз и методы обследования
При исследовании крови выявляют нейтрофильный лейкоцитоз со сдвигом влево, увеличение СОЭ, концентрации С-реактивного белка, гиперглобулинемию.
Важную информацию для постановки диагноза пиелонефрита дает лабораторное исследование мочи. При микроскопии мочи, как правило, выявляют выраженную пиурию (лейкоцитурию), иногда лейкоцитарные цилиндры, бактериурию. Бактериологическое исследование мочи позволяет выделить возбудителя инфекции. Бактериурию считают диагностически значимой при выделении микроорганизма в количестве >105 КОЕ (колониеобразующих единиц) в 1 мл мочи.
Дополнительные методы исследования (УЗИ почек, рентгенологические методы) не имеют большого значения при неосложненном пиелонефрите, но при осложненной инфекции эти методы позволяют выявить и оценить факторы, осложняющие течение заболевания (камни, гипертрофию предстательной железы).
Клинико-фармакологические подходы к лечению
пиелонефрита
Подходы к лечению пиелонефрита определяются формой заболевания, при этом заболевании обычно назначаются антибиотики, создающие высокие концентрации в моче: фторхинолоны, амокси-циллин, цефалоспорины 2-3-го поколения.
Контроль эффективности проводимого лечения
Критериями эффективности антибактериальной терапии являются нормализация температуры, уменьшение выраженности симптомов заболевания и исчезновения бактерий и лейкоцитов в анализе мочи.
15.7. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ ДИУРЕТИКОВ
Строение нефрона, локализация и механизм действия диуретиков
Структурно-функциональная единица почки - нефрон, состоящий из сосудистого клубочка, окруженного капсулой, системы извитых и прямых канальцев, кровеносных и лимфатических сосудов, а также нейрогуморальных элементов (рис. 15.1).
В результате процесса фильтрации в клубочках почек образуется фильтрат (первичная моча), содержащий воду, глюкозу, аминокислоты, ионы бикарбонатов, фосфатов и другие соединения (ежедневно в организме образуется около 200 л клубочкового фильтрата). В дальнейшем, при продвижении фильтрата по системе канальцев, происходит его концентрирование, при этом 99% воды и электролитов подвергаются обратному всасыванию - реабсорбции. Снижение скорости реабсорбции всего на 1% приводит к увеличению объема мочи в 2 раза. Таким образом, ЛС, обладающие даже незначительным влиянием на процессы обратного всасывания электролитов в канальцах
Корковый слой Собирательные
канальцы
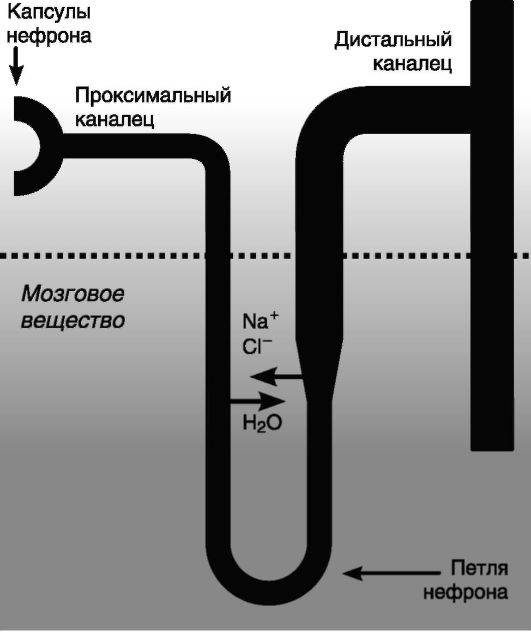
Рис. 15.1. Строение нефрона (схема)
нефрона, способны существенно изменять диурез. С другой стороны, патологические процессы, приводящие к временному или постоянному изменению структуры клубочков и канальцев, способны вызывать серьезные изменения водно-электролитного баланса в организме.
Известные в настоящее время препараты, влияющие на диурез: диуретики обладают различными механизмами действия и влияют на процессы в различных участках нефрона.
Кроме того, существуют внепочечные механизмы регуляции диуреза. При снижении системного АД <90 мм рт. ст. (например, при шоке) происходят уменьшение почечного кровотока, снижение объема фильтрации и уменьшение диуреза. Критической величиной снижения диуреза считают уровень менее 20 мл/час. Классические
диуретики в этой ситуации малоэффективны, так как при снижении фильтрации их проникновение в канальцы нефронов затруднено. С другой стороны, назначение ЛС, увеличивающих системное АД и /или почечный кровоток (добутамин, допамин), приводит к увеличению диуреза.
Действие диуретиков в проксимальных канальцах нефрона
В этом участке нефрона происходит активная реабсорбция натрия, сопровождающаяся изотоническим потоком воды в интерстициаль-ное пространство. На реабсорбцию ионов в этом отделе влияют осмотические диуретики и ингибиторы карбоангидразы.
Осмотические диуретики (маннитол) - группа препаратов, фильтрующихся в клубочках нефрона, но плохо реабсорбирующихся. В проксимальных канальцах нефрона они повышают осмотическое давление фильтрата и выделяются почками в неизмененном виде с изоосмотическим количеством воды.
Ингибиторы карбоангидразы. Препараты этой группы (ацетазо-ламид) уменьшают реабсорбцию бикарбонатов в проксимальных канальцах путем угнетения процессов гидратации СО2:
СО2 + Н2О -- Н2СО3 -- H+ + НСО3-
Образующиеся в результате этого процесса ионы водорода поступают в просвет канальца в обмен на ионы натрия. Таким образом, применение ингибиторов карбоангидразы увеличивают экскрецию Н2О, Na+ и НСО3-. Повышение концентрации Na+ в просвете канальца приводит к увеличению секреции К+. Потеря бикарбоната может приводить к возникновению метаболического ацидоза, но при этом диуретическая активность ингибиторов карбоангидразы также снижается.
Действие диуретиков в восходящих отделах петли нефрона
В восходящем отделе петли Генле ионы хлора активно переходят в интерстициальное пространство, увлекая за собой ионы натрия и калия (Na+:K+:2Cl-котранспортер), кроме того, примерно половина ионов натрия в этом отделе реабсорбируется пассивно. В результате интерстициальная жидкость становится гипертонич-ной по отношению к жидкости в просвете канальца. Для молекул воды восходящий отдел петли нефрона непроницаем, но в параллельно расположенных нисходящих отделах петли происходит активный переход жидкости в интерстициальное пространство
и капилляры. Петлевые диуретики (фуросемид) селективно блокируют №+:К+:2С1-котранспортер, нарушая транспорт ионов, что приводит к увеличению диуреза. Одновременно повышается экскреция ионов магния и кальция.
Действие диуретиков в дистальных канальцах нефрона
В начальной части дистальных канальцев происходит активная реабсорбция Na+ и С1-, в результате чего осмотическое давление фильтрата снижается. Тиазидные диуретики угнетают этот процесс, в результате чего повышается выведение из организма Н2О, Na+ и С1-. Увеличение концентрации Na+ в просвете канальца стимулирует процесс обмена ионов натрия на К+ и Н+, что может привести к гипока-лиемии и алкалозу.
Действие диуретиков в собирательных трубочках
Собирательные трубочки - альдостеронозависимый участок нефрона, в котором происходят процессы, контролирующие гомеостаз калия. Альдостерон регулирует обмен Na+ на Н+ и K+. Калийсберегающие диуретики понижают реабсорбцию Na+, конкурируя с альдостероном за цитоплазматические рецепторы (спиро-нолактон) или блокируя натриевые каналы (амилорид®). Препараты этой группы могут вызывать гиперкалиемию.
Классификация диуретиков
Диуретики классифицируют в зависимости от характера диуретического действия:
- вызывающие преимущественно водный диурез (ингибиторы карбоангидразы, осмотические диуретики) - действуют преимущественно на проксимальные канальцы нефрона;
- петлевые диуретики - оказывают наиболее выраженное диуретическое действие, подавляя реабсорбцию натрия и воды в восходящем отделе петли Генле; увеличивают экскрецию натрия
на 15-25%;
- тиазидные - действуют преимущественно в области дис-тальных канальцев нефрона, увеличивают экскрецию натрия
на 5-10%;
- калийсберегающие - действуют преимущественно в области собирательных трубочек, увеличивают экскрецию натрия не более чем на 5%.
Принципы рационального лечения и выбор диуретического препарата
Принципиальными моментами в лечении мочегонными препаратами считают:
- назначение слабейшего из эффективных у данного больного диуретиков;
- назначение мочегонных средств в минимальных дозах, позволяющих добиться эффективного диуреза (для активного диуреза прибавка должна составлять +800-1000 мл в сутки, для поддерживающей терапии - не более 200 мл в сутки),
- при недостаточной эффективности применение диуретиков с разным механизмом действия.
Выбор диуретического средства зависит от характера и тяжести заболевания. В неотложных ситуациях (отек легких) назначают сильно- и быстродействующие петлевые диуретики внутривенно. При выраженном отечном синдроме (например, у пациентов с декомпенсацией ХСН) лечение также начинают с внутривенного введения петлевых диуретиков, с последующим переходом на прием фуросе-мида внутрь.
При недостаточной эффективности монотерапии используют сочетания диуретиков с разными механизмами действия: фуросемид с гидрохлортиазидом или фуросемид со спиронолактоном. Сочетание фуросемида с калийсберегающими диуретиками назначают также для предупреждения нарушений электролитного баланса.
Для длительного лечения (например, при АГ) применяют тиазид-ные и калийсбергающие диуретики.
Осмотические диуретики назначают для увеличения водного диуреза и предупреждения развития анурии (в частности, при гемолизе), а также для уменьшения внутричерепного и внутриглазного давления.
Ингибиторы карбоангидразы показаны при глаукоме (уменьшают продукцию внутриглазной жидкости), эпилепсии, острой высотной болезни, для повышения выведения с мочой фосфатов при гиперфос-фатемии тяжелого течения.
Контроль эффективности и безопасности лечения диуретиками
Эффективность лечения оценивают по уменьшению выраженности симптомов (одышки при отеке легких, отеков при ХСН), а также по увеличению диуреза. Наиболее надежный способ контроля эффек-
тивности долговременного лечения диуретиками - контроль массы тела больного.
Для контроля безопасности проводимого лечения необходимо регулярно измерять электролитный баланс и АД, в некоторых случаях (при проведении интенсивной терапии и реанимации) может потребоваться контроль центрального венозного давления и состояния свертывающей системы крови.
15.7.1. Клиническая фармакология тиазидных и тиазидоподобных диуретиков
К тиазидным диуретикам относится гидрохлоротиазид. К тиази-доподобным - индапамид.
Фармакокинетика. Тиазиды и тиазидоподобные диуретики хорошо всасываются в ЖКТ при приеме внутрь. Гидрохлоротиазид слабо растворим в липидах. Связывание с белками высокое. Подвергаются в почках активной канальцевой секреции и из-за этого становятся конкурентами секреции мочевой кислоты, которая выводится из организма с помощью этого же механизма, вследствие чего скорость удаления мочевой кислоты снижается и повышается ее уровень в плазме крови. Препараты этой группы почти полностью выводятся почками, индапамид выводится главным образом с желчью, благодаря этому возможен его прием больными почечной недостаточностью.
Показания. Тиазидные и тиазидоподобные диуретики применяют для длительного лечения АГ. Их считают препаратами выбора при изолированной систолической АГ, сочетании АГ с отечным синдромом, ХСН, у больных пожилого и старческого возраста. Показания для применения гидрохлортиазида: задержка жидкости, отеки, связанные с сердечной недостаточностью, циррозом печени, некоторыми нарушениями функции почек, лечением глюкокорти-коидами и эстрогенами, предупреждение образования кальциевых почечных конкрементов, лечение центрального и нефрогенного несахарного диабета.
НЛР. Нарушения солевого баланса: гипонатриемия, гипохлоре-мический алкалоз, гипокалиемия, гипомагниемия и гипокальцие-мия. При применении гидрохлортиазида возможно развитие гипергликемии и гиперлипидемии, что не характерно для индапамида. Тиазидные и тиазидоподобные диуретики могут вызвать повышение концентрации мочевой кислоты. Характерная НЛР для этой группы ЛС - эректильная дисфункция.
Противопоказания. Анурия или тяжелое поражение почек, СД, подагра или гиперурекимия, нарушение функций печени, гипер-кальциемия или гиперлипидемия, гипонатриемия. Повышенная чувствительность к тиазидным диуретикам или другим сульфаниламидным препаратам.
Гидрохлортиазид
Хорошо всасывается в ЖКТ. Практически не подвергается биотрансформации, выводится главным образом с мочой. Начало действия происходит через 30-60 мин, максимум через 4 ч, продолжается 6-12 ч. Период полувыведения быстрой фазы составляет 1,5 ч, медленной - 13 ч.
Индапамид
Оказывает слабое диуретическое действие, а также расширяет почечные артерии. Обладает гипотензивным действием, которое обусловлено снижением концентрации натрия и уменьшением общего периферического сопротивления из-за снижения чувствительности сосудистой стенки к норадреналину и ангиотензину II, повышения синтеза про-стагландина Е2. Может ускорять клубочковую фильтрацию. Индапамид обладает пролонгированным гипотензивным эффектом без значительного влияния на диурез. Латентный период составляет около 2 нед. Максимальное устойчивое действие препарата развивается через 4 нед.
Индапамид хорошо всасывается в ЖКТ, максимальная концентрация в крови определяется через 2 ч. Период полувыведения составляет около 14 ч.
15.7.2. Клиническая фармакология петлевых диуретиков
К петлевым диуретикам относят фуросемид, торасемид, этакри-новую кислоту.
Фармакодинамика. Начало диуретического эффекта петлевых диуретиков при приеме внутрь происходит через 30-60 мин, максимум - через 1-2 ч, продолжительность - 6-8 ч. При внутривенном введении эффект проявляется через несколько минут, пик - через 30 мин, продолжительность действия составляет 2 ч. Препарат сохраняет эффективность при низкой скорости клубочковой фильтрации, и его можно применять при почечной недостаточности.
Показания. Петлевые диуретики особенно показаны при выраженной задержке жидкости: отеках, связанных с декомпенсацией ХСН, циррозом печени, заболеваниями почек (в том числе ОПН), острой левожелудочковой недостаточности (отек легких), острых интоксикациях (форсированный диурез). Их не используют для лечения АГ. Однако эти препараты можно назначать для купирования гипертонических кризов как в виде монотерапии, так и в сочетании с другими антигипертензивными препаратами. Петлевые диуретики также назначают для лечения гипер-кальциемии.
Противопоказания. Тяжелые нарушения функции почек, печени, панкреатит, СД, гиперурикемия, нарушение слуха, повышенная чувствительность к сульфаниламидным препаратам. С осторожностью назначают больным с желудочковыми аритмиями.
НЛР. Нарушения солевого баланса: гипонатриемия, гипохлоре-мический алкалоз, гипокалиемия и гипомагниемия. При применении торасемида электролитные нарушения развиваются реже. Ототоксичность наиболее часто встречается при нарушении функции почек, быстром парентеральном введении больших доз петлевых диуретиков или при совместном приеме с другими ототоксичными препаратами (например, аминогликозидами). Этот эффект наиболее характерен для этакриновой кислоты.
Взаимодействие с другими ЛС. Следует избегать одновременного или последовательного назначения фуросемида и амфотерицина В (усиливается нефротоксическое и ототоксическое действие амфо-терицина В, усугубляются нарушения солевого баланса). При сочетании с ИАПФ возможно развитие артериальной гипотензии при приеме первой дозы, ИАПФ могут ослаблять выраженность вторичного гиперальдостеронизма и гипокалиемии. Фуросемид может повышать концентрацию глюкозы в крови и уменьшать эффекты сахаросни-жающих препаратов. НПВС, особенно индометацин, могут противодействовать натрийурезу и повышению активности ренина, снижать эффективность фуросемида.
Фуросемид
Препарат быстро и полно всасывается при введении любым путем. Биодоступность при приеме внутрь составляет 60-70%. Период полувыведения - 0,5-1 ч. Фуросемид подвергается биотрансформации в печени с образованием неактивных метаболитов.
При приеме внутрь начало диуретического действия отмечается через 30-60 мин, продолжительность - 6-8 ч, при внутривенном введении начало действия - через 30 мин, продолжительность - 2 ч.
Торасемид
Быстро и полно всасывается из ЖКТ. Биодоступность препарата составляет около 80%. Период полувыведения - 3-4 ч, при почечной недостаточности не изменяется. Торасемид подвергается биотрансформации в печени системой цитохрома Р-450 в три неактивных метаболита. Этот препарат в меньшей степени вызывает гипокалие-мию по сравнению с фуросемидом, но при этом проявляет большую активность и его действие более продолжительно. Торасемид противопоказан при беременности и лактации.
15.7.3. Клиническая фармакология калийсберегающих диуретиков
К калийсберегающим диуретикам относят спиронолактон, эпле-ренон*3 и триамтерен.
Показания к применению. Калийсберегающие диуретики относятся к слабо действующим препаратам. Поскольку в дистальных почечных канальцах реабсорбция натрия уменьшена, они могут не вызвать выраженный мочегонный эффект. Однако их можно рационально сочетать с более активными диуретиками из-за того, что они, с одной стороны, уменьшают потери калия, а с другой - повышают эффективность лечения: такие сочетания применяют для преодоления резистентности к диуретикам. Спиронолактон и эплеренон*3 в малых дозах длительно назначают при ХСН в качестве нейрогуморальных модуляторов для снижения активности РААС. Спиронолактон применяют для лечения первичного гиперальдостеронизма, синдрома поликистоза яичников, гирсутизма, предменструального синдрома, угревой сыпи.
Противопоказания. Гиперкалиемия, азотемия, анурия или нарушение работы почек со значительным снижением экскреторной функции. С осторожностью назначают при нарушении функций печени, СД, особенно диабетической нефропатии, предрасположенности к метаболическому ацидозу, гипонатриемии, гиперкальциемии.
НЛР. Аллергические реакции, гиперкалиемия, гипонатриемия, повышение концентрации в крови мочевины, креатинина, мочевой кислоты, диспепсические расстройства, головные боли, головокружение, психические расстройства, фотосенсибилизация, гинеко-
мастия, нарушение эректильной функции, менструального цикла, мегалобластоз, агранулоцитоз, тромбоцитопения. Самыми частыми НЛР при применении спиронолактона считают гинекомастию (анти-андрогенный эффект) и гиперкалиемию. Эплеренон*3 гинекомастию не вызывает. Для триамтерена характерна гепатотоксичность, особенно у лиц пожилого и старческого возраста.
Взаимодействие с другими ЛС. НПВС уменьшают натрийурети-ческий и диуретический эффект этих препаратов, возрастает риск развития почечной недостаточности. При одновременном применении могут снижаться свойства антикоагулянтов путем уменьшения объема плазмы и повышения концентрации факторов свертывания. ИАПФ, препараты калия, калиевые добавки способствуют развитию гиперкалиемии. Спиронолактон может увеличивать период полувыведения дигоксина.
Спиронолактон
Антагонист альдостерона, слабый калийсберегающий диуретик длительного действия. Препарат хорошо всасывается из ЖКТ, период полувыведения составляет 13-24 ч.
Диуретический эффект проявляется с 2-5 сут лечения и продолжается 2-3 сут после прекращения лечения. Препарат оказывает слабое и непостоянное гипотензивное действие, не зависящее от концентрации ренина в плазме. Спиронолактон не влияет на почечный кровоток и клубочковую фильтрацию.
Триамтерен
Калийсберегающий диуретик средней продолжительности действия. Препарат всасывается из ЖКТ быстро, но неполностью, период полувыведения составляет 5-7 ч.
15.7.4. Клиническая фармакология ингибиторов карбоангидразы
К ингибиторам карбоангидразы относится ацетазоламид.
Фармакокинетика. Ацетазоламид хорошо всасывается из ЖКТ, достигая максимальной концентрации через 2 ч, продолжительность действия - до 12 ч. Распределяется главным образом в эритроцитах, почках, мышцах, тканях глазного яблока и ЦНС. Связь с белками крови высокая, проникает через плацентарный барьер, биотрансформации не подвергается, выводится почками в неизмененном виде.
Показания. В настоящее время ингибиторы карбоангидразы в основном назначают при глаукоме, повышении внутричерепного давления, малых приступах эпилепсии. При задержке жидкости и отечном синдроме, связанном с ХСН, легочным сердцем, нарушением функций печени или почек (особенно в сочетании с алкалозом), ацетазоламид применяют в составе комплексного лечения. Кроме того, ингибиторы карбоангидразы назначают при предменструальном синдроме, для профилактики и лечения острой горной болезни.
НЛР. Сонливость, головокружение, головные боли. При длительном приеме возможны парестезии, дезориентация, гемолитическая анемия, гипокалиемия, метаболический ацидоз, нефролитиаз, преходящая гематурия и глюкозурия.
Противопоказания. Метаболический ацидоз и склонность к ацидозу, например при СД, нарушение функций печени и почек (в том числе острая и ХПН), гипокалиемия, беременность.
Взаимодействие с другими ЛС. Мочегонный эффект ацетазоламида усиливается теофиллином, ослабляется кислотообразующими диуретиками. При одновременном приеме повышается риск появления токсических эффектов салицилатов, карбамазепина, эфедрина.
Применение. Препарат не следует назначать более 5 сут подряд из-за риска развития метаболического ацидоза.
15.7.5. Клиническая фармакология осмотических
диуретиков
К осмотическим диуретикам относят маннитол, мочевину.
Фармакокинетика. Осмотические диуретики плохо всасываются из ЖКТ, из-за чего их приходится вводить парентерально. При приеме внутрь маннитол вызывает осмотическую диарею. В организме не метаболизируется, выводится путем почечной фильтрации без последующей канальцевой реабсорбции.
Показания к применению. В качестве дегидратирующего средства осмотические диуретики назначают для быстрого снижения внутричерепного или внутриглазного давления при отеке мозга, внутричерепной гипертензии, эпилептическом статусе, остром приступе глаукомы. Осмотические диуретики применяют в рамках форсированного диуреза при отравлениях барбитуратами, салицилатами и другими веществами. Маннитол показан для профилактики и лечения ОПН при условии сохранения фильтрационной функции почек.
НЛР. Дегидратация, диспепсические расстройства, нарушения электролитного баланса, головная боль, галлюцинации.
Противопоказания. Осмотические диуретики не применяют у больных с тяжелыми нарушениями функции почек - в этом случае моча может не образовываться даже при осмотической нагрузке и тогда гипертонический раствор вызывает увеличение внутрисосу-дистого объема жидкости и развитие острой сердечной недостаточности и отека легких. Осмотические диуретики не назначают больным с декомпенсацией ХСН из-за повышения объема внеклеточной жидкости и увеличения нагрузки на сердце, при электролитных нарушениях - гипохлоремии, гипонатриемии, гипокалиемии.