Клиническая фармакология и фармакотерапия: учебник. - 3-е изд., перераб. и доп. / под ред. В. Г. Кукеса, А. К. Стародубцева. - 2012. - 840 с.: ил.
|
|
|
|
Глава 14. СЕРДЕЧНАЯ НЕДОСТАТОЧНОСТЬ
14.1 . ХРОНИЧЕСКАЯ СЕРДЕЧНАЯ НЕДОСТАТОЧНОСТЬ
ХСН - синдром, развивающийся в исходе различных заболеваний сердечно-сосудистой системы, приводящих к снижению насосной функции сердца и хронической гиперактивации нейрогормональ-ных систем. Основные проявления ХСН - одышка, сердцебиение, повышенная утомляемость, ограничение физической активности и избыточная задержка жидкости в организме. Выраженность симптомов может варьировать от минимальных, возникающих только при выполнении значительных нагрузок, до значительных отеков и тяжелой одышки в состоянии покоя. Для ХСН характерно прогрессирующее течение с постепенным (в течение 1-5 лет) нарастанием симптомов и снижением эффективности лечения.
Эпидемиология. В возрасте до 50 лет ХСН отмечается только у 1% населения, но у людей старше 65 лет распространенность ХСН может достигать 6-8%, а к 80 годам симптомы сердечной недостаточности отмечаются почти у 10%. В настоящее время ХСН - ведущая причина госпитализации больных в возрасте 65 лет и старше.
Этиология и патогенез. ХСН может развиться на фоне практически любого заболевания сердечно-сосудистой системы, но наиболее частыми ее причинами становятся ИБС и АГ. На долю этих заболеваний приходится более половины всех случаев ХСН, при этом СД, гипертрофия миокарда ЛЖ или злоупотребление алкоголем значительно увеличивают риск возникновения ХСН. Наиболее частые причины развития ХСН:
• ИБС;
• АГ;
• кардиомиопатии (общее название группы болезней с поражением миокарда неишемической природы):
- идиопатическая дилатационная кардиомиопатия;
- гипертрофическая кардиомиопатия;
- алкогольная кардиомиопатия;
- кардиомиопатия на фоне СД;
- кардиомиопатии вирусной природы (вирусы Коксаки В, эхови-русы);
- кардиомиопатии при амилоидозе1 и саркоидозе2;
- токсические кардиомиопатии;
- кардиомиопатии у больных гипотиреозом (см. главу 18);
- кардиомиопатии у пожилых;
• пороки сердца;
• заболевания перикарда3;
• длительно существующие тахиаритмии (см. главу 13).
У больных ИБС в результате хронической коронарной недостаточности клетки миокарда прогрессивно теряют жизнеспособность, что приводит к снижению его сократимости, дилатации (расширению) камер сердца и развитию ХСН. Если ИБС осложняется ИМ, в зоне поражения формируется рубец, снижается сократимость и происходит дилатация полости ЛЖ. Эти процессы способствуют прогрессирующему снижению насосной функции сердца в целом и развитию ХСН.
При АГ развивается гипертрофия миокарда, из-за которой сердце может долго сохранять нормальную насосную функцию даже при дополнительном сопротивлении сосудов, вызванном повышением АД (увеличение постнагрузки). Однако гипертрофия вызывает нарушение диастолического4 наполнения сердца кровью, что также может приводить к снижению сердечного выброса и развитию ХСН.
При пороках сердца нарушается нормальная работа клапанов, что приводит к перегрузке его камер повышенным объемом крови, с развитием их дилатации и снижением сердечного выброса. В остальных случаях причина развития ХСН заключается в диффузном поражении миокарда алкоголем, токсичными веществами или вирусами.
Уменьшение сердечного выброса у больного с начальными проявлениями ХСН сопровождается компенсаторной активацией симпатоа-
1 Амилоидоз - болезнь, при которой в миокарде, эндокарде и стенках сосудов откладываются продукты нарушения белкового обмена - амилоид.
2 Саркоидоз - болезнь, поражающая преимущественно легкие, этиология которой до конца не изучена.
3 Перикард - серозная оболочка, покрывающая сердце снаружи и состоящая из двух листков.
4 Диастола - период расслабления сердечной мышцы. В период диастолы (клапаны между предсердиями и желудочками сердца открыты) кровь заполняет полость желудочков, а в период систолы (клапаны между предсердиями и желудочками закрыты) происходит изгнание крови в аорту. Гипертрофия (утолщение стенок) желудочков сердца препятствует их адекватному заполнению в диастолу.
дреналовой системы (медиаторы норадреналин и адреналин), системы натрийуретических факторов и РААС (ангиотензин II и альдостерон). На начальных этапах ХСН удается компенсировать снижение насосной функции сердца путем увеличения ЧСС, повышения АД и силы сердечных сокращений, а также в результате задержки натрия и жидкости в организме. Однако высокие концентрации нейрогормонов со временем вызывают дополнительную гипертрофию миокарда, ишемию и энергетическое истощение кардиомиоцитов, а кроме того, оказывают прямое токсическое действие, вызывая некроз и гибель клеток. В результате замыкается порочный круг, вызывающий у больных с ХСН прогрессивное снижение насосной функции сердца и гибель клеток миокарда. Активизация натрийуретического пептида и РААС приводит к значительной задержке в организме натрия и жидкости (перегрузка объемом), при этом часть жидкости не удерживается в сосудистом русле и распределяется в тканях организма:
• в подкожной клетчатке - отеки;
• в плевральной полости1 - гидроторакс;
• в брюшной полости - асцит;
• в строме легких - отек легких.
Симптомокомплекс ХСН. На ранних этапах ХСН может протекать бессимптомно, ее первые признаки - утомляемость, сердцебиения и одышка при физической нагрузке, которую ранее больной переносил адекватно. Развернутая клиническая картина ХСН возникает только при задержке жидкости в организме и нарастании перегрузки объемом.
Симптомы и жалобы больных при перегрузке объемом сердечнососудистой системы:
• повышенная утомляемость при физической нагрузке;
• одышка при физической нагрузке;
• ортопноэ (появление/усиление одышки в положении лежа);
• никтурия (частое мочеиспускание ночью);
• анорексия.
Объективные признаки, выявляемые при обследовании больного:
• периферические отеки;
• расширение яремных вен (в переднебоковых отделах шеи);
• увеличение печени;
• выпот в плевральной и брюшной полости;
1 Плевральная полость - полость между листками висцеральной и париетальной плевры, которые покрывают легкие и внутреннюю поверхность грудной клетки соответственно.
• влажные хрипы при аускультации легких.
У больного с ХСН одышка в покое уменьшается в вертикальном положении (ортопноэ), так как при этом снижается венозный возврат к сердцу (часть крови депонируется в венах нижних конечностей) и уменьшается преднагрузка.
При объективном осмотре у больного можно обнаружить отеки (чаще всего на нижних конечностях), вздутие шейных вен, увеличение печени, скопление жидкости в брюшной (асцит) и плевральной (гидроторакс) полости. Жидкость может накапливаться в строме легких или поступать в альвеолы1. В последнем случае в нижних отделах легких выслушиваются характерные влажные хрипы.
Тяжесть и течение заболевания. ХСН - проградиентно протекающее заболевание, но применение современных лечебных методов может существенно затормозить прогрессирование и значительно улучшить состояние больных.
Для описания тяжести течения ХСН в 1964 г. Нью-Йоркской ассоциацией кардиологов была создана функциональная классификация (табл. 14-1), которая предполагает выделение четырех ФК по способности больных переносить физические нагрузки.
Таблица 14-1. Функциональная классификация ХСН Нью-Йоркской ассоциации кардиологов

1 Альвеолы - мельчайшие сферические образования на концах самых мелких бронхов; в альвеолах происходит газообмен.
Необходимо отметить, что ФК ХСН у больного может существенно изменяться за короткий промежуток времени. Так, при поступлении в стационар состояние больного с декомпенсацией ХСН соответствовало IV ФК (одышка в покое), а через 3 нед после лечения - II ФК (одышка при физической нагрузке).
Диагноз и методы обследования. Согласно рекомендациям Европейского кардиологического общества (2005), диагностика ХСН должна опираться на два обязательных критерия: симптомы сердечной недостаточности в покое или при физической нагрузке и объективные доказательства дисфункции сердца.
Если диагноз ХСН вызывает сомнения, можно использовать дополнительный критерий - эффективность лечебных мероприятий, которые обычно проводят при ХСН.
Инструментальное обследование больного:
• 1 этап - ЭКГ (выявление признаков ИБС или аритмии), рентгенография органов грудной клетки (увеличение размеров сердца, признаки застоя в малом круге кровообращения) и определение концентрации натрийуретического пептида (биохимический маркер ХСН) в крови. Если эти исследования не выявили отклонений от нормы - диагноз ХСН маловероятен.
• 2 этап - ЭхоКГ, радионуклидная вентрикулография или магнитно-резонансная томография для уточнения величины фракции выброса ЛЖ и выявления структурных нарушений клапанов сердца и миокарда.
Дальнейшее обследование зависит от этиологии ХСН. Например, при ИБС показано ангиографическое исследование, при АГ - исследование функций почек и т.д.
В клинической практике и при отсутствии специального оборудования для оценки физической толерантности и объективизации функционального статуса больных ХСН можно использовать тест ходьбы в течение 6 мин, соответствующий субмаксимальной нагрузке. Проведение нагрузочных тестов у пациентов с ХСН оправдано не для диагностики, а с целью оценки функционального статуса пациента и эффективности лечения, а также для определения степени риска. Тем не менее нормальный результат нагрузочного теста у пациента, не получающего специфического лечения, практически полностью исключает диагноз ХСН. Данные исследований свидетельствуют о высокой корреляционной связи теста с ФК ХСН и прогностической значимости: пройденная дистанция <300 м соответствует неблагоприятному прогнозу.
Клинико-фармакологические подходы к выбору лекарственных средств для лечения хронической сердечной недостаточности
Современный подход к лечению сердечной недостаточности предполагает его максимально раннее начало. Только до того, как сформировались тяжелые и необратимые изменения структуры сердечной мышцы, можно предотвратить прогрессирование процесса. Современные руководства по клинической практике [Европейского кардиологического общества (2005), Руководства Американского кардиологического колледжа и Американской ассоциации кардиологов] выделяют больных без ХСН, но с факторами риска ее развития: АГ, ИБС, СД, отягощенной наследственностью - кардиомиопатиями у близких родственников (табл. 14-2). Вторичную профилактику сердечной недостаточности нужно проводить у больных, имеющих снижение насосной функции сердца без клинических признаков заболевания (стадия В; см. табл. 14-2). Этим больным показаны ИАПФ и БАБ - препараты с доказанным профилактическим действием по отношению к сердечной недостаточности. Кроме того, все больные с сердечной недостаточностью должны получать адекватное лечение основного заболевания.
Лечение ХСН направлено на уменьшение госпитализации и смертности больных, числа и тяжести эпизодов декомпенсации сердечной недостаточности, выраженности симптомов заболевания (снижение ФК, замедление прогрессирования недостаточности кровообращения), а также на улучшение качества жизни и прогноза.
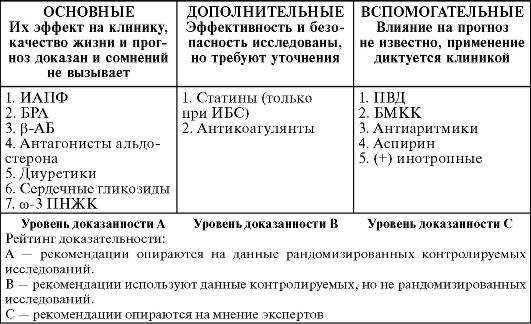
Существует группа ЛС, назначение которых позволяет вплотную приблизиться к этим целям и способны воздействовать на течение заболевания. Согласно современным национальным рекомендациям по лечению ХСН лекарственные препараты разделяют на три категории (основные, дополнительные и вспомогательные ЛС) соответственно их эффективности и степени доказанности (табл. 14-3).
Основные средства - это ЛС, эффект которых доказан, сомнений не вызывает и которые рекомендованы именно для лечения ХСН (степень доказанности А):
1. Ингибиторы АПФ, которые показаны всем больным ХСН вне зависимости от этиологии, стадии процесса и типа декомпенсации.
2. Блокаторы рецепторов ангиотензина II (БРА), которые применяются в основном в случаях непереносимости ИАПФ в качестве средства первой линии для блокады РААС у больных с клинически выраженной декомпенсацией, а также плюс к ИАПФ; у пациентов с ХСН, у которых эффективность одних ИАПФ недостаточна.
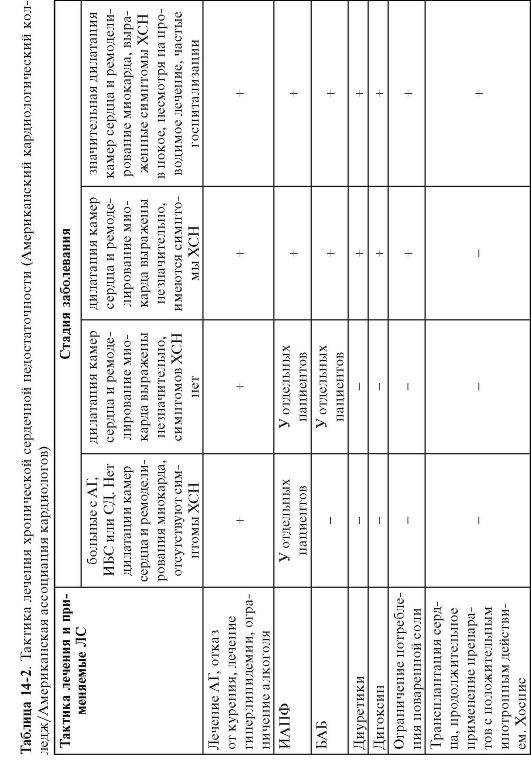
Таблица 14-3. Препараты, эффективность которых у больных с ХСН доказана в ходе клинических исследований
3. β-адреноблокаторы (β-АБ) - нейрогормональные модуляторы, применяемые «сверху» (дополнительно) к ИАПФ.
4. Антагонисты рецепторов к альдостерону, применяемые вместе с ИАПФ и β-АБ у больных с выраженной ХСН (III-IV ФК) и пациентов, перенесших в прошлом ОИМ.
5. Диуретики - показаны всем больным при клинических симптомах ХСН, связанных с избыточной задержкой натрия и воды в организме.
6. Сердечные гликозиды - в малых дозах. При мерцательной аритмии они остаются средством «первой линии», а при синусовом ритме и ишемической этиологии ХСН применение требует осторожности и контроля.
7. Этиловые эфиры полиненасыщенных жирных кислот (эйкоза-пентаеновой и декозагексаеновой).
Дополнительные средства, эффективность и (или) безопасность которых показана в отдельных крупных исследованиях, но требует уточнения (степень доказанности В):
• статины, рекомендуемые к применению у всех больных с ишеми-ческой этиологий ХСН; кроме того, обладающие способностью предотвращать развитие ХСН у больных с разными формами
ИБС;
• непрямые антикоагулянты, показанные к использованию у большинства больных ХСН, протекающей на фоне мерцательной аритмии, а также у пациентов с ХСН и синусовым ритмом.
Вспомогательные средства, эффект и влияние которых на прогноз больных ХСН не известны (не доказаны), что соответствует уровню доказательности С. В принципе этими препаратами не нужно (да и невозможно) лечить саму ХСН, и их применение диктуется определенными клиническими ситуациями, осложняющими течение собственно декомпенсации:
• периферические вазодилататоры (ПВД) - нитраты, применяемые только при сопутствующей стенокардии;
• блокаторы медленных кальциевых каналов (БМКК) - длитель-нодействующие дигидропиридины при упорной стенокардии и стойкой АГ, плохо корригируемой легочной гипертензии и выраженной клапанной регургитации;
• антиаритмические средства (кроме β-АБ, входящих в число основных препаратов, в основном III класса) при опасных для жизни желудочковых аритмиях;
• аспирин (и другие антиагреганты) для вторичной профилактики после перенесенного ИМ;
• негликозидные инотропные стимуляторы - при обострении ХСН, протекающей с низким сердечным выбросом и упорной гипотонией.
Объем лечения должен отвечать тяжести сердечной недостаточности и выраженности симптомов (табл. 14-4). При лечении ХСН следует отказаться от назначения малоэффективных ЛС (вазодилататоров, нитратов) и препаратов с отрицательным инотропным эффектом.
Таблица 14-4. Выбор ЛС в зависимости от ФК ХСН

Медикаментозная терапия занимает центральное место в лечении ХСН, но большое значение имеют и вспомогательные мероприятия, такие, как соблюдение диеты, оптимального режима физической активности, а также психологическая реабилитация пациентов и организация школ для больных ХСН.
Диета пациентов с ХСН должна иметь соответствующую энергетическую ценность, быть легкоусвояемой, с достаточным количеством витаминов, белка и содержать малое количество поваренной соли (до 1,5-3 г в день). Это намного эффективнее, чем ограничение приема жидкости. Больной должен получать не менее 1,5 л жидкости в сутки при любой стадии ХСН.
Физическая реабилитация пациентов подразумевает ходьбу или тредмил 5 раз в неделю по 20-30 мин.
Клинико-фармакологический подход к лечению ХСН включает в себя назначение высоких доз петлевых диуретиков, а также препаратов с положительным инотропным действием при сниженном АД (допамин). Подобное лечение проводят в условиях стационара, а при отеке легких и артериальной гипотензии - в условиях отделения интенсивной терапии.
Больным с декомпенсацией ХСН не следует принимать БАБ (если они не получали их раньше), назначение в этой ситуации ИАПФ также требует осторожности и предварительной отмены диуретиков для профилактики гипотонии.
Отек легких (встречается также у больных острой ишемией/ИМ, аритмией и у пациентов с ГК) развивается при резком снижении насосной функции сердца. Жидкость пропотевает в легочные альвеолы при повышении давления в малом круге кровообращения, что сопровождается развитием дыхательной недостаточности (снижение площади газообмена в альвеолах).
Лечение проводят в условиях отделения интенсивной терапии. Тактика включает в себя ингаляции кислорода, лечение основного заболевания, приведшего к отеку легких. Всем больным внутривенно вводят фуросемид, морфин и назначают нитроглицерин.
Оценка эффективности лечения ХСН заключается в регулярном обследовании больных с оценкой симптомов перегрузки объемом. Кроме того, критериями эффективности лечения считают:
• увеличение фракции выброса при эхокардиографии;
• переход ХСН в более низкий ФК;
• увеличение толерантности к физической нагрузке;
• стабильную массу тела;
• отсутствие НЛР.
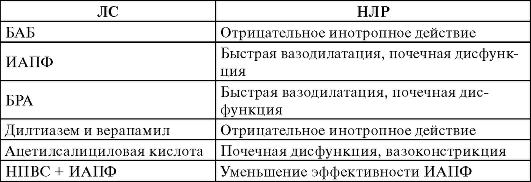
Оценка безопасности лечения ХСН. Некоторые ЛС, применяемые при этом синдроме, вызывают опасные НЛР (табл. 14-5). В первую очередь это падение АД, брадикардия и изменение в крови концентрации ионов калия. Безопасность лечения обеспечивается постепенным увеличением доз ЛС - так называемой титрацией. Титрация особенно важна при назначении БАБ и ИАПФ. Оценка безопасности лечения приведена в разделах, посвященных отдельным препаратам.
Таблица 14-5. ЛС, применение которых у больных с ХСН связано с риском
НЛР
14.2. ПРИМЕНЕНИЕ ИНГИБИТОРОВ АНГИОТЕНЗИНПРЕВРАЩАЮЩЕГО ФЕРМЕНТА В ЛЕЧЕНИИ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
Фармакодинамика (см. главу 10). В настоящее время ИАПФ считают важнейшей группой препаратов для лечения всех стадий сердечной недостаточности, так как активация РААС имеет основное значение в ее патофизиологии. Повышение концентрации ангиотензина II в крови и тканях определяет повышение периферического сопротивления сосудов (постнагрузка), задержку натрия и увеличение ОЦК (преднагрузка), развитие интерстициального миокардиального фиброза и в итоге прогрессирование сердечной недостаточности.
ИАПФ - смешанные вазодилататоры, снижающие давление наполнения и системное сопротивление. Они, с одной стороны, тормозят РААС и симпатическую нервную систему, а с другой - положительно модифицируют гемодинамические нарушения при сердечной недостаточности. Снижая концентрацию ангиотензина II, альдостерона, катехоламинов и реабсорбцию натрия в почках, ИАПФ уменьшают сосудистое сопротивление, улучшают систолическую и диастоли-
ческую функции желудочков, препятствуют развитию структурных изменений в миокарде, сосудах и в результате замедляют про-грессирование заболевания. ИАПФ препятствуют ремоделированию сердца, а в ряде случаев вызывают обратное развитие гипертрофии миокарда. Увеличивая концентрацию брадикинина, они приводят к увеличению почечного кровотока, диуреза и натрийуреза.
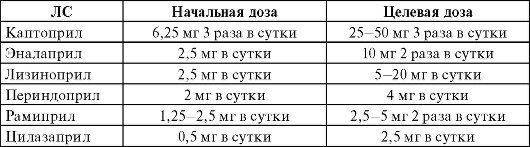
В настоящее время в медицинской практике в ходу более 10 ИАПФ: каптоприл, эналаприл, периндоприл, лизиноприл, рами-прил и т. д (табл. 14-6). Они повышают эффективность диуретиков, а их гемодинамические эффекты усиливаются сердечными глико-зидами. Препараты повышают качество жизни пациентов с ХСН, уменьшая одышку, мышечную усталость и увеличивая переносимость нагрузок. ИАПФ существенно снижают смертность больных с сердечной недостаточностью различной этиологии и тяжести. Наиболее изученный в этом плане препарат - эналаприл.
Таблица 14-6. Дозы ингибиторов АПФ при лечении ХСН
Относительно недавно для лечения ХСН стали применять БРА - лозартан, валсартан и кандесартан. Клинические эффекты этих препаратов схожи с эффектами ИАПФ.
Особенности применения у больных ХСН. Применение ИАПФ у больных ХСН имеет ряд особенностей:
• за 24 ч до назначения ИАПФ необходимо уменьшить дозу диуретиков или отменить их;
• желательно начать лечение вечером, когда больной лежит в постели, для минимизации влияния ИАПФ на АД и продолжения наблюдения за уровнем АД в течение нескольких часов;
• лечение ИАПФ следует начинать с низких доз, а затем ступенчато увеличивать дозу (титрация) (см. табл. 14.6);
• при появлении/прогрессировании признаков ухудшения функции почек (увеличение концентрации креатинина в крови) лечение ИАПФ следует прекратить. Необходимо контролировать
уровень АД, концентрацию креатинина, электролитов в плазме через 1-2 нед после каждого повышения дозы ИАПФ, затем каждые 3-6 мес;
• следует избегать одновременного назначения калийсберегающих диуретиков (кроме случаев гипокалиемии) и НПВС;
• назначению ИАПФ должна предшествовать консультация врача-кардиолога, если:
- причина развития ХСН неизвестна;
- уровень систолического АД ниже 100 мм рт. ст.;
- концентрация креатинина в сыворотке крови выше 150 мкмоль/л;
- концентрация натрия в сыворотке крови ниже 135 ммоль/л;
- высокий ФК ХСН;
- у больного имеется порок сердца.
Фармакокинетика и НЛР отдельных препаратов этой группы приведены в главу 10.
14.3. ПРИМЕНЕНИЕ β-АДРЕНОБЛОКАТОРОВ В ЛЕЧЕНИИ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
Фармакодинамика. БАБ - одни из самых эффективных средств для длительного лечения ХСН.
Их положительное влияние проявляется в значительном уменьшении риска смерти (на 30-35% по сравнению с плацебо) и потребности в госпитализации (на 25-30% по сравнению с плацебо). Кроме того, прием БАБ положительно влияет на величину сердечного выброса и некоторые симптомы ХСН.
Особенности назначения БАБ больным ХСН. Применение БАБ показано при любой тяжести сердечной недостаточности, даже сердечную недостаточность IV ФК не считают противопоказанием к назначению БАБ (при их переносимости). Препаратом выбора в этом случае является карведилол - единственный БАБ, эффективность которого при IV ФК доказана в ходе плацебоконтролируемых исследований. При ХСН II-III ФК бисопролол, карведилол и метопролол имеют примерно одинаковую эффективность.
Избежать нежелательных эффектов БАБ при их первом назначении можно путем постепенного титрования дозы (табл. 14-7). Кроме того, к моменту начала терапии у больного не должно быть признаков перегрузки объемом. Противопоказано применение БАБ у больных бронхиальной астмой и при брадикардии или выраженной гипотензии.
Таблица 14-7. Титрование дозы БАБ при лечении ХСН
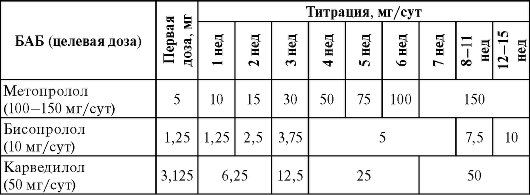
При ХСН II-IV ФК БАБ назначают в составе комплексной терапии с ИАПФ и диуретиками.
Не следует без особых показаний назначать при ХСН БАБ с внутренней симпатомиметической активностью, кардиоселективные препараты и соталол.
Метопролол. Выпускается в таблетках по 50 и 100 мг. Биодоступность 95%, только 8% препарата в крови находится в связи с белком. Подвергается интенсивному пресистемному метаболизму в печени. Период полувыведения составляет 3-4 ч, продолжительность эффекта - 10-20 ч. Хорошо проникает через гематоэнцефалический барьер, в высоких концентрациях обнаруживается в грудном молоке. При почечной недостаточности значимой кумуляции препарата в организме не наблюдается, у пациентов с циррозом печени биотрансформация замедлена.
Гипотензивный эффект наступает быстро: систолическое АД начинает снижаться уже через 15 мин.
Препарат назначают 1-3 раза в сут в зависимости от лекарственной формы.
Карведилол - блокатор α1-, β1-, Р2-адренорецепторов. Блокада β-адренорецепторов приводит к снижению частоты и силы сердечных сокращений без резкой брадикардии и проводимости. В результате блокады β-адренорецепторов расширяются периферические сосуды. Блокада β2-адренорецепторов вызывает некоторое повышение тонуса бронхов, сосудов микроциркуляторного русла, повышение тонуса и усиление перистальтики кишечника.
Препарат быстро всасывается при приеме внутрь, пища может замедлить адсорбцию, но не уменьшает ее. При одновременном приеме с пищей уменьшается риск развития ортостатической гипотен-
зии. Биодоступность карведилола составляет 25-35%. Для препарата характерен эффект первого прохождения через печень. На интенсивность метаболизма карведилола могут влиять ингибиторы CYP2D6. Период полувыведения 7-10 ч.
Наиболее серьезная НЛР при приеме карведилола - ортостатиче-ская гипотензия (1,8%), из-за этого после повышения дозы больной должен несколько часов сидеть или лежать под наблюдением медицинского работника. Развитие ортостатической гипотензии не требует отмены препарата, необходима лишь более медленная титрация. У 14,4% больных после приема карведилола возникает боль в грудной клетке, часто наблюдаются нарушение толерантности к глюкозе и сонливость, особенно в первые дни лечения.
Препарат назначают внутрь 2 раза в сутки.
Бисопролол - селективный блокатор β1-адренорецепторов.
Всасывание препарата быстрое и полное. В связи с белками плазмы находятся от 26 до 33% бисопролола. Характерен эффект первого прохождения через печень. Начало действия при приеме внутрь происходит через 1-2 ч, пиковая концентрация препарата в плазме достигается через 1,7-3 ч. Период полувыведения составляет 9-12 ч. От 3 до 10% препарата выводится почками. Возможны нежелательные взаимодействия с субстратами цитохрома 2D6.
НЛР - бессонница и снижение либидо. Крайне редко при приеме этого препарата возникают брадикардия, увеличение отеков, диарея.
Бисопролол назначают внутрь 1 раз в сутки.
14.4. ПРИМЕНЕНИЕ ДИУРЕТИКОВ В ЛЕЧЕНИИ
СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
Фармакодинамика. Диуретики - важный компонент комплексного лечения пациентов с ХСН. Эти препараты быстро устраняют одышку, снижают давление в легочных капиллярах и давление наполнения. Увеличивая экскрецию натрия, они уменьшают ОЦК и реактивность сосудистой стенки; усиливают действие вазодилата-торов и ИАПФ. У больных с резко выраженной дилатацией полостей сердца под влиянием диуретиков уменьшается объем камер сердца и относительная клапанная недостаточность, что приводит к увеличению сердечного выброса.
Особенности назначения больным ХСН. Для лечения сердечной недостаточности используют петлевые или тиазидные диуретики
(табл. 14-8), которые следует назначать только в качестве дополнения к ИАПФ. При скорости клубочковой фильтрации менее 30 мл/мин не следует назначать тиазидные диуретики, за исключением их сочетания с петлевыми (для обеспечения синергизма действия).
Таблица 14-8. Диуретики при лечении ХСН
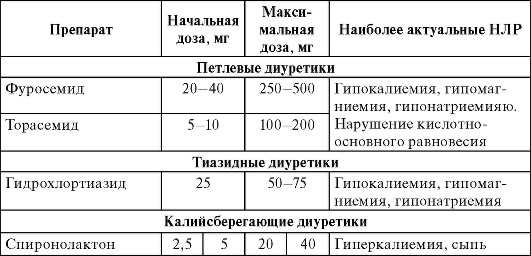
В 2006 г. в РФ зарегистрирован петлевой диуретик торасемид, блокирующий реабсорбцию натрия и воды в восходящей части петли Генле. По фармакокинетическим свойствам он превосходит фуросе-мид. Торасемид имеет лучшую и более предсказуемую всасываемость, по сравнению с фуросемидом, причем его биоусвояемость не зависит от приема пищи и почти вдвое выше, чем у фуросемида. Стартовая доза препарата составляет 5-10 мг, при необходимости возможно ее увеличение до 100-200 мг в сутки.
Калийсберегающие диуретики, обладающие свойствами антагонистов альдостерона, - спиронолактон, эплеренон®.
Эти препараты применяют не только, как калийсберегающие диуретики, но и как антагонисты нейрогормона альдостерона, блокируя его негативное действие. Блокируя рецепторы к альдостерону, калийсберегающие диуретики оказывают следующее действие:
• препятствуют ремоделированию ЛЖ и стенок сосудов;
• препятствуют нарушению всасывания в тонкой кишке;
• препятствуют дистрофии поперечно-полосатой мускулатуры;
• улучшают прогноз - уменьшение летальности на 25%. Спиронолактон обладает сродством к андрогеновым и проге-
стероновым рецепторам, и его назначение в 25% случаев вызывает болезненную гинекомастию.
Эплеренон - селективный антагонист рецепторов альдостеро-на. Примечательно, что препарат обладает более низким сродством к андрогеновым и прогестероновым рецепторам, и его применение позволяет снизить риск развития болезненной гинекомастии, наблюдаемой при приеме спироналактона.
Следует отметить, что при назначении спиронолактона и эпле-ренона® возможно повышение риска развития тяжелой гиперкалие-мии. Концентрация креатинина сыворотки крови более 221 ммоль/л и калия в плазме более 5 ммоль/л указывает на необходимость отмены этих препаратов.
В качестве монотерапии ХСН диуретики не используют, так как они не могут поддерживать стабильное состояние пациентов из-за активации РААС и развития гипокалиемии и гипомагниемии. У пациентов без симптомов перегрузки объемом их не применяют.
Диуретики особенно эффективны у больных с признаками задержки натрия и воды. Они уменьшают застойные явления, периферические отеки, одышку, приступы сердечной астмы, повышают переносимость физических нагрузок, улучшая качество жизни пациентов. Однако данных об их влиянии на продолжительность жизни больных ХСН нет.
НЛР. Одним из основных осложнений назначения больших доз диуретиков считают развитие гипокалиемии и гипомагниемии, что приводит к повышению риска внезапной смерти от аритмий. Этого можно избежать, комбинируя петлевые диуретики с калийсбе-регающими. При длительном лечении диуретиками может развиться синдром отмены (чаще у женщин), проявляющийся увеличением отеков в течение 10-15 сут, которые затем спонтанно уменьшаются. Происхождение отеков объясняется повышением активности РААС на фоне приема диуретиков.
Резистентность к диуретикам у больных ХСН. В ряде случаев у таких пациентов возникает резистентность к действию диуретиков. Механизм ее развития достаточно сложный и объясняется несколькими причинами:
• гипонатриемией разведения (возникает при увеличении общего содержания воды в организме);
• снижением объема почечного кровотока (например, при выраженной гипотензии);
• снижением экстрацеллюлярного объема жидкости, а также повышением активности РААС и развитием вторичного гиперальдо-стеронизма при назначении высоких доз диуретиков.
Преодолеть резистентность при недостаточном эффекте позволяют:
• увеличение дозы;
• использование сочетания петлевых и тиазидных диуретиков;
• назначение диуретиков 2 раза в сутки.
При неэффективности этих рекомендаций можно использовать метолазон*3 (при этом необходим контроль концентрации креатини-на и электролитов в крови).
Особый интерес для лечения сердечной недостаточности представляют антагонисты альдостерона (спиронолактон), поскольку, кроме умеренного натрийуретического действия, они улучшают функциональное состояние кардиомиоцитов, уменьшают прогрессирование кардиосклероза и повышают выживаемость больных. Тем не менее на фоне ХПН лечение калийсберегающими диуретиками может осложниться гиперкалиемией с последующей асистолией.
Спиронолактон назначают пациентам с ХСН III-IV ФК. Лечение должно проводиться под регулярным контролем уровня калия и кре-атинина сыворотки.
14.5. ПРИМЕНЕНИЕ СЕРДЕЧНЫХ ГЛИКОЗИДОВ В ЛЕЧЕНИИ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
Дигоксин - сердечный гликозид, который наиболее широко применяют у больных ХСН.
Фармакокинетика. Обладает высокой биодоступностью и коротким периодом полувыведения. Концентрацию дигоксина в крови определяют в основном скорость и полнота его абсорбции. Биологическая доступность зависит от индивидуальных особенностей больного, метода введения препарата, взаимоотношений с другими вводимыми препаратами, лекарственной формы и от наполнителя таблеток. С белками плазмы связывается только 20-25% препарата. Концентрация дигоксина в миокарде значительно выше, чем в плазме. Он способен проникать через плаценту, но его концентрация у плода ниже, чем у матери. 80% препарата выводится с мочой в неизмененном виде, причем выведение дигоксина пропорционально почечной фильтрации. Концентрацию дигоксина в крови необходимо проверить через 1 нед после начала приема (она не должна превышать 2 нг/мл), а затем достаточно регулярно (каждые 2-3 мес) контролировать этот показатель, особенно у пожилых, похудевших и принимающих диуретики пациентов. Новорожденные и дети младшего возраста лучше переносят боль-
шие дозы дигоксина в пересчете на единицу массы или поверхности тела, чем взрослые. Стабильная концентрация препарата при обычных методах дозирования достигается в течение 7 сут.
Особенности назначения больным ХСН. Исследование DIG (1997) доказало безопасность применения дигоксина при лечении пациентов с сердечной недостаточностью на фоне синусового ритма. Дигоксин хотя и не влиял на продолжительность жизни больных, в дозах 0,125-0,25 мг/сут повышал качество жизни и уменьшал число госпитализаций из-за обострения заболевания. Наоборот, отмена дигоксина у больных с умеренно выраженными симптомами ХСН и синусовым ритмом сопровождается усилением симптомов и увеличением частоты госпитализаций. Другие сердечные гликозиды также можно применять у данной категории больных, но достоверных данных об их влиянии на прогноз нет.
Профилактика тромбоэмболических осложнений
Поражение митрального клапана может быть одной из причин развития тромбов. Перегрузка и дилатация предсердия также часто сопровождаются развитием тромбов в полости левого предсердия. Эти факторы, особенно при МА, повышают вероятность тромбо-эмболических осложнений. По данным крупных популяционных исследований, частота инсультов у больных с МА составляет около 0,3-4,1%. При этом собственно МА повышает риск мозгового инсульта в 2,3-6,9 раза по сравнению с таковым у больных с синусовым ритмом. Из этого следует необходимость профилактического анти-тромботического лечения.
Возможны два пути профилактики: назначение дезагрегантов, в частности ацетилсалициловой кислоты, или непрямых антикоагулянтов (варфарина, аценокумарола, фениндион), непрямые антикоагулянты более эффективны. Во всем мире чаще всего назначают варфарин, относящийся к производным кумарина. В РФ из препаратов этого класса чаще используют аценокумарол. Применение непрямых антикоагулянтов обязательно у пациентов с недостаточностью митрального клапана, старше 65 лет, при МА, особенно при признаках тромбообразования в полостях сердца.
Этот вид лечения требует контроля из-за опасности геморрагических осложнений, причем кровотечения чаще возникают именно у пожилых больных, которым назначение антикоагулянтов наиболее показано. Оптимальным способом контроля за эффективностью лечения считают расчет МНО.
14.6 ПРИМЕНЕНИЕ БЛОКАТОРОВ РЕЦЕПТОРОВ АНГИОТЕНЗИНА II ПРИ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ
НЕДОСТАТОЧНОСТИ
Фармакодинамика (см. главу 10). По данным современных национальных и международных рекомендаций БРА являются одной из семи основных групп лекарственных препаратов, применяемых в медикаментозной терапии ХСН (степень доказанности А).
Полученные в последние годы результаты мультицентровых клинических исследований показали эффективность БРА в лечении и профилактике ХСН. Так, при приеме кандесартана снижение риска смерти составляло 33% после первого, 20% после второго и 12% после третьего года наблюдения, что очень близко к показателям, полученным с эналаприлом (23% через год, 23% через два и 16% через три года терапии, соответственно). Применение валсартана у больных ХСН, не получавших ингибиторы АПФ в связи с наличием противопоказаний, снижало риск общей смертности на 33,1%. Эти данные позволили рекомендовать валсартан больным, которые по разным причинам не могут получать терапию ингибиторами АПФ. Применение лозарта-на в дозе 150 мг/сут достоверно снижает риск смерти и госпитализаций больных ХСН. Лозартан в дозах 100 мг/сут может предупреждать развитие ХСН, в том числе у пациентов с диабетом и нефропатией, что обусловливает его применение для профилактики декомпенсации сердечной деятельности. Нужно отметить, что не все представители класса сартанов выглядят одинаково в качестве средств профилактики ХСН. Ирбесартан и телмисартан не показали достоверной способности к снижению риска ХСН у больных ИБС.
Таким образом, можно констатировать, что некоторые БРА - кан-десартан (степень доказанности А), валсартан и лозартан (степень доказанности В) не уступают ИАПФ и могут применяться для лечения ХСН наравне с ними (табл. 14-9).
Таблица 14-9. Рекомендуемые дозы блокаторов рецепторов ангиотензина II при лечении ХСН

Фармакокинетика и НЛР отдельных препаратов этой группы приведены в главу 10.