Детские болезни: учебник / Под ред. А.А. Баранова - 2-е изд., - 2009. - 1008 с.
|
|
|
|
ГЛАВА 14 АЛЛЕРГИЧЕСКИЕ БОЛЕЗНИ
БРОНХИАЛЬНАЯ АСТМА
Бронхиальная астма у детей - хроническое воспалительное заболевание дыхательных путей, тесно связанное с атопией, сопровождающееся повышением бронхиальной гиперреактивности с эпизодами обратимой бронхиальной обструкции в виде одышки, удушья, приступов кашля и свистящего дыхания. Ведущие механизмы развития бронхиальной астмы в детском возрасте - атопия и обусловленные сенсибилизацией организма IgE-опосредованные реакции.
Эпизоды бронхиальной обструкции, частично или полностью обратимые, сопровождаются приступообразным кашлем, свистящими хрипами и ощущением сдавления в груди.
Распространённость бронхиальной астмы среди детей в разных странах варьирует от 1,5 до 8-10%. Расхождения между данными официальной статистики по обращаемости и результатами эпидемиологических исследований связаны с гиподиагностикой бронхиальной астмы в различных возрастных группах. Болезнь может начаться в любом возрасте. У 50% больных детей симптомы развиваются к 2 годам, у 80% - к школьному возрасту.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Развитие бронхиальной астмы у детей обусловлено генетической предрасположенностью и факторами окружающей среды. Выделяют три основные группы факторов, способствующих развитию заболевания.
• Предрасполагающие (отягощённая аллергическими заболеваниями наследственность, атопия, бронхиальная гиперреактивность).
• Причинные, или сенсибилизирующие (аллергены, вирусные инфекции, лекарственные средства).
• Вызывающие обострение (так называемые триггеры), стимулирующие воспаление в бронхах и/или провоцирующие развитие острого бронхоспазма (аллергены, вирусные и бактериальные инфекции,
холодный воздух, табачный дым, эмоциональный стресс, физическая нагрузка, метеорологические факторы и др.). Сенсибилизацию дыхательных путей вызывают ингаляционные аллергены (бытовые, эпидермальные, грибковые, пыльцевые). Один из источников аллергенов - домашние животные (слюна, выделения, шерсть, роговые чешуйки, слущенный эпителий). Пыльцевую бронхиальную астму вызывают аллергены цветущих деревьев, кустарников, злаковых. У некоторых детей приступы удушья могут быть обусловлены различными лекарственными средствами (например, антибиотиками, особенно пенициллинового ряда, сульфаниламидами, витаминами, ацетилсалициловой кислотой). Несомненна роль сенсибилизации к промышленным аллергенам. Кроме прямого воздействия на органы дыхания, техногенное загрязнение атмосферного воздуха может усиливать иммуногенность пыльцы и других аллергенов. Нередко первым фактором, провоцирующим обструктивный синдром, становятся ОРЗ (парагрипп, РСВ- и риновирусная инфекции, грипп и др.). В последние годы отмечают роль хламидийной и микоплазменной инфекций.
У детей бронхиальная астма обусловлена проявлением атопии и наследственной предрасположенностью к излишней продукции IgE. Хронический воспалительный процесс и нарушение регуляции тонуса бронхов развиваются под влиянием различных медиаторов. Их высвобождение из тучных клеток, активированных IgE, приводит к развитию немедленного и отсроченного бронхоспазма. Ключевую роль в сенсибилизации организма играют CD4+ T-лимфоциты. Под воздействием аллергенных стимулов происходит активация и пролиферация Тп2-субпопуляции CD4+ T-лимфоцитов с последующим выделением ими цитокинов (ИЛ4, ИЛ6, ИЛ10, ИЛ13), индуцирующих гиперпродукцию общего и специфических IgE. Последние образуются под воздействием различных ингалируемых аллергенов внешней среды. Повторное поступление аллергена приводит к выделению клетками преформированных медиаторов и развитию аллергического ответа, проявляющегося нарушением бронхиальной проходимости и приступом астмы. Бронхиальная обструкция, возникающая во время приступа астмы, - результат кумуляции спазма гладкой мускулатуры мелких и крупных бронхов, отёка стенки бронхов, скопления слизи в просвете дыхательных путей, клеточной инфильтрации подслизистой оболочки и утолщения базальной мембраны. В связи с наличием гиперреактивности бронхов обострения астмы могут возникать под воздействием как аллергических, так и неаллергических факторов.
КЛИНИЧЕСКАЯ КАРТИНА
Основные симптомы приступа бронхиальной астмы: одышка, чувство нехватки воздуха, свистящее дыхание, приступообраз-
ный кашель с тягучей прозрачной мокротой (мокрота отходит тяжело), экспираторная одышка, вздутие грудной клетки, в более тяжёлых случаях - удушье. У детей раннего возраста эквивалентами приступа бронхиальной астмы могут быть эпизоды кашля ночью или в предутренние часы, от которых ребёнок просыпается, а также затяжной повторный обструктивный синдром при ОРЗ с положительным эффектом бронхолитиков. Бронхиальная астма у детей нередко сочетается с аллергическим ринитом (сезонным или круглогодичным) и атопическим дерматитом. Следует учитывать, что при обследовании больного аускультативных изменений может и не быть. Вне приступа, при спокойном дыхании хрипы выслушивают лишь у небольшой части больных.
Тяжёлый приступ сопровождается выраженной одышкой (ребёнок с трудом говорит, не может есть) с ЧДД более 50 в минуту (более 40 в минуту у детей старше 5 лет), ЧСС более 140 в минуту (более 120 в минуту после 5 лет), парадоксальным пульсом, участием вспомогательной мускулатуры в акте дыхания (у грудных детей эквивалент участия вспомогательной мускулатуры - раздувание крыльев носа во время вдоха). Положение ребёнка в момент астматического приступа вынужденное (ортопноэ, нежелание лежать). Отмечают набухание шейных вен. Кожные покровы бледные, возможны цианоз носогубного треугольника и акроцианоз. Аускультативно выявляют свистящие сухие хрипы по всем полям лёгких, у детей раннего возраста нередко бывают разнокалиберные влажные хрипы (так называемая «влажная астма»). Пиковая объёмная скорость выдоха (ПОС) составляет менее 50% возрастной нормы. К признакам, угрожающим жизни, относят цианоз, ослабление дыхания или «немое» лёгкое, ПОС менее 35%.
• Согласно классификации (табл. 14-1), тяжесть течения астмы (лёг- кая, среднетяжёлая, тяжёлая) оценивают исходя из клинических симптомов, частоты приступов удушья, потребности в бронхолитических препаратах и объективной оценки проходимости дыхательных путей. Лёгкая интермиттирующая бронхиальная астма характеризуется редкими, иногда сезонными эпизодами затруднённого дыхания при контакте с конкретным аллергеном, исчезающими спонтанно или при однократном использовании бронхолитика. При лёгкой персистирующей бронхиальной астме приступы затруднённого дыхания возникают 1-3 раза в месяц и купируются однократным при- ёмом бронхолитика. Ночные симптомы, как правило, отсутствуют или редки. При лёгкой бронхиальной астме (интермиттирующей и персистирующей) в периоде ремиссии общее состояние больного не страдает, функциональные показатели внешнего дыхания колеблются в пределах возрастной нормы. Наряду с приступами затруднённого дыхания возникают кратковременные симптомы болезни, такие
как кашель, свистящее дыхание. Необходимо подчеркнуть, что с появлением типичных, характерных приступов удушья бронхиальную астму следует расценивать (минимум) как средней тяжести.
• При среднетяжёлой бронхиальной астме приступы затруднённого дыхания повторяются чаще одного раза в неделю, но не ежедневно, наблюдаются ночные приступы. Приступы нередко купируются лишь повторным использованием бронхолитиков, а иногда и глюкокортикоидов (по показаниям). В периоде ремиссии обычно сохраняются изменения функции внешнего дыхания. Переносимость физической нагрузки может быть снижена.
• Тяжёлая бронхиальная астма характеризуется частыми (несколько раз в неделю или ежедневными, по несколько раз в день), в том числе частыми ночными приступами удушья. Они обычно тяжёлые, купируются сочетанным применением бронхолитиков (повторные ингаляции и/или парентеральное введение) и глюкокортикоидов. В фазе ремиссии сохраняются клинико-функциональные проявления бронхиальной обструкции.
Таблица 14-1. Клиническая классификация бронхиальной астмы*
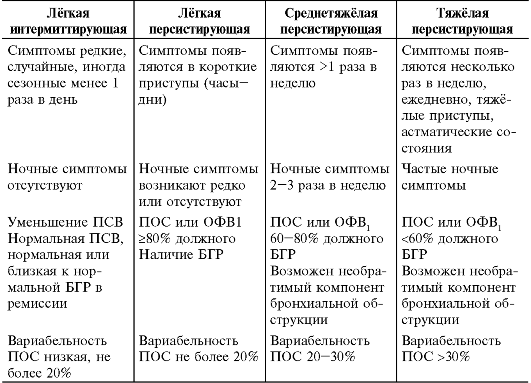
* Принята на XIII Национальном конгрессе по болезням органов дыхания, Москва, 2004.
Осложнения бронхиальной астмы: ателектаз лёгких, медиастинальная и подкожная эмфизема, спонтанный пневмоторакс, эмфизема лёгких, лёгочное сердце. В течении заболевания выделяют период обострения и период ремиссии.
ДИАГНОСТИКА
Основа предварительного диагноза бронхиальной астмы - целенаправленно собранный анамнез. Если на нижеприведённые вопросы больной ребёнок (или его мать) отвечает утвердительно, диагноз астмы достаточно вероятен.
Что из перечисленного происходило с ребёнком в течение последних 12 мес?
• Внезапные или рецидивирующие эпизоды кашля, свистящих дистанционных хрипов, одышки.
• Повторный или длительно сохраняющийся обструктивный синдром во время ОРЗ.
• Кашель, дистанционные свистящие хрипы и/или одышка, возникающие в определённое время года.
• Кашель, дистанционные свистящие хрипы или одышка при контакте с животными, табачным дымом, резкими запахами и др.
• Облегчение симптомов при использовании бронхолитических лекарственных средств.
• Кашель, дистанционные свистящие хрипы или одышка, вызывающие:
- пробуждение ночью;
- пробуждение в предутренние часы.
• Появление или нарастание указанных симптомов после бега, умеренной физической нагрузки, воздействия холодного воздуха. Учитывают также данные аллергологического и семейного анамнеза
и физикального обследования. Значимым является также выявление у больного ребёнка сопутствующих заболеваний аллергического генеза (атопический дерматит, крапивница, отёк Квинке и др.).
Инструментально-лабораторные методы включают спирометрию (для детей старше 5 лет) с проведением тестов с бронхолитическим препаратом, физической нагрузкой и метахолином; пикфлоуметрию, анализ периферической крови и мокроты, кожные аллергические пробы (скарификационные или уколочные), определение специфических АТ классов IgE и IgG4 в сыворотке крови, общего IgE, при необходимости рентгенографию органов грудной клетки.
• Наиболее доступны и воспроизводимы объём форсированного выдоха за 1 с (ОФВ1) и ПОС. Обычно при спирометрии выявляют сниженную или нормальную форсированную жизненную ёмкость лёгких (ФЖЕЛ), уменьшение ОФВ1, соотношения ОФВ1/ФЖЕЛ и ПОС.
• Весьма информативный метод диагностики - проба с бронхолитическим лекарственным средством. Пробу считают положительной при увеличении ОФВ1 более чем на 12% через 15-20 мин после применения бронхолитического средства.
• Степень гиперреактивности бронхов оценивают по снижению ОФВ1 на 20% с помощью теста с физической нагрузкой на велоэргометре и ингаляции постепенно возрастающих доз метахолина.
• Пикфлоуметрия - наблюдение за функцией внешнего дыхания, проводимое при помощи специального прибора. При пикфлоуметрии ПОС определяют в течение 2-3 нед минимум дважды в день (утром и вечером), а также после приёма больным бронхолитического средства, что позволяет оценить вариабельность бронхиальной проходимости и проследить тенденции в течении заболевания.
• В мокроте определяют большое количество эозинофилов, кристаллы Шарко-Лейдена (шестигранной или игловидной формы, содержащие высвобождаемую из эозинофилов лизофосфолипазу), спирали Куршманна (слепки слизи с просвета дыхательных путей) и тельца Креола (скопления эпителиальных клеток).
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Обструкция бронхов и свистящие хрипы характерны, но не патогномоничны для бронхиальной астмы. У детей первых месяцев жизни такие симптомы возможны при различных врождённых, приобретён- ных и наследственных заболеваниях: аспирации инородного тела (в том числе мекония), муковисцидозе, трахео- и бронхомаляции, бронхолёгочной дисплазии, стенозе, бронхогенных кистах, облитерирующем бронхиолите, аномалии сосудов, вызывающей компрессию дыхательных путей, интерстициальных лёгочных заболеваниях, сердечной недостаточности и т.п.
При этих заболеваниях обструктивный синдром длительно сохраняется или упорно повторяется, обструкция резистентна к терапии, носит необратимый характер. Чем меньше возраст ребёнка (до одного года), тем выше вероятность альтернативного диагноза.
• Рентгенография органов грудной клетки помогает выявить врож- дённые аномалии и аспирацию инородного тела. Кроме того, при этих состояниях большую помощь окажет целенаправленно собранный анамнез.
• Положительная потовая проба характерна для муковисцидоза.
• Контрастное исследование с бариевой взвесью проводят при подозрении на трахеоэзофагеальный свищ, сосудистые аномалии.
У детей первых 2 лет жизни (наиболее часто от 2 до 6 мес) диагностические трудности вызывает обструктивный синдром при бронхиолите. Обычно у этих детей в течение 3-5 дней острой респираторной
инфекции развиваются прогрессирующий кашель, свистящие хрипы, симптомы дыхательной недостаточности. Приблизительно у 50% та- ких детей в дальнейшем регистрируют рецидивы обструктивного синдрома при последующих ОРЗ.
Обструктивный бронхит диагностируют у детей и подростков с неотягощённым аллергологическим анамнезом, но частыми ОРЗ, вызы- вающими бронхиальную обструкцию. Появляясь в раннем возрасте, к 5-6 годам обструктивный синдром обычно исчезает. В пользу бронхиальной астмы свидетельствуют рецидивы (три эпизода и более, начиная с первого года жизни) выраженной бронхиальной обструкции, возникающие не только при ОРЗ, но и вследствие контакта с различными триггерами (холодным воздухом, табачным дымом, шерстью домашних животных). Характерны отчётливое уменьшение клиничес- ких проявлений под влиянием бронхолитической и противовоспалительной терапии, отягощённый аллергологический семейный анамнез и ранние проявления аллергии у больного ребёнка, например в виде атопического дерматита.
ЛЕЧЕНИЕ
Лечение бронхиальной астмы у детей направлено на:
• предотвращение развития угрожающих жизни состояний и летального исхода;
• ликвидацию или сведение к минимуму клинических проявлений;
• нормализацию или улучшение показателей функции внешнего дыхания;
• восстановление или поддержание жизненной активности, включая переносимость физических нагрузок;
• снижение потребности в бронхолитических препаратах;
• предотвращение побочных эффектов терапии;
• предупреждение инвалидизации.
Основные принципы лечения
Комплексная программа лечения бронхиальной астмы включает следующие компоненты.
• Обучение больных детей и их родителей: они должны знать цели лечения, возможные пути их достижения, методы самоконтроля, технику ингаляции, самопомощи при начинающемся приступе.
• Выявление и удаление (элиминация) факторов, провоцирующих обострение болезни.
• Рациональное применение препаратов, предотвращающих обострение (противовоспалительных) и облегчающих симптомы заболевания в период обострения (бронхолитиков).
• Специфическая иммунотерапия (специфическая аллерговакцинация).
• Восстановительное лечение с использованием немедикаментозных методов, в том числе санаторно-курортных.
• Регулярное врачебное наблюдение с коррекцией терапии.
Согласно современным представлениям элиминационные мероприятия должны быть индивидуальными для каждого боль- ного, гибкими и экономически эффективными.
Противовоспалительные противоастматические препараты (базисная терапия)
Основу современной медикаментозной терапии составляют противовоспалительные (базисные, контролирующие) препараты, кото- рые принимают регулярно, ежедневно, длительно, для контроля персистирующей астмы. К ним относятся ингаляционные и системные глюкокортикоиды, кромоглициевая кислота, недокромил, длительнодействующие ингаляционные и пероральные b2-адреномиметики, медленно высвобождаемые теофиллины, антагонисты лейкотриеновых рецепторов, антиаллергические средства.
Стабилизаторы мембран тучных клеток
Кромоглициевая кислота и недокромил действуют местно, предотвращая дегрануляцию тучных клеток и высвобождение из них гиста- мина; подавляют как немедленную, так и отсроченную бронхоспастическую реакцию на вдыхаемый аллерген, предупреждают развитие бронхоспазма при вдыхании холодного воздуха или при физической нагрузке. При длительном приёме они уменьшают гиперреактивность бронхов, снижают частоту и длительность приступов бронхоспазма, безопасны для детей. Кромоглициевую кислоту выпускают в виде порошка для ингаляций (в капсулах) и раствора для ингаляций (в ампулах, аэрозольных баллонах), назначают детям любого возраста. Недокромил (аэрозоль для ингаляций дозированный) применяют у детей с 2 лет.
Ингаляционные глюкокортикоиды
Ингаляционные глюкокортикоиды назначают при тяжёлой и среднетяжёлой бронхиальной астме или недостаточном действии стабилизаторов мембран тучных клеток. Ингаляционные глюкокортикоиды обладают высокой противовоспалительной активностью. Их доза зависит от тяжести заболевания. Системный эффект ингаляционных глюкокортикоидов проявляется редко, однако, учитывая их возможное влияние на рост детей при длительном применении, предпочтительнее назначать низкие и средние дозы препаратов. Используют различные препараты ингаляционных глюкокортикоидов: беклометазон, флутиказон, флунизолид, будесонид.
Ингаляционные глюкокортикоиды, в отличие от системных, оказывают преимущественно местное противовоспалительное действие и
практически не вызывают системных побочных эффектов. При недостаточной эффективности дозу ингаляционных глюкокортикоидов можно увеличить. Длительность терапии индивидуальна и определяется достижением стабильного состояния или ремиссии, при тяжёлой бронхиальной астме составляет не менее 6-12 мес.
Использование пероральных глюкокортикоидов (3-5-дневный курс) у детей с бронхиальной астмой ограничено более тяжёлыми или длительными обострениями, вызванными вирусными инфекциями или другими причинами. Существующие в настоящее время данные позволяют предполагать, что нет необходимости в постепенном снижении дозы перорального преднизолона. Для длительного лечения пероральные препараты предпочтительнее парентеральных. Лучше назначать такие пероральные глюкокортикоиды, как преднизолон или метилпреднизолон, обладающие минимальным минералокортикоидным эффектом, относительно коротким периодом полувыведения и нерезко выраженным действием на поперечнополосатую мускулатуру, в дозе 0,5-1 мг/кг/сут. При длительной терапии пероральные глюкокортикоиды следует назначать один раз в сутки, утром, ежедневно или через день.
При сочетании бронхиальной астмы и аллергического ринита эффективна комплексная терапия, включающая наряду с лечением астмы назальные спреи кромоглициевой кислоты или ингаляционных глюкокортикоидов и антигистаминные препараты, преимущественно II поколения.
b2-Адреномиметики длительного действия. Наряду с глюкокортикоидами в настоящее время в длительном лечении детей с тяжёлой бронхиальной астмой используются препараты, обладающие длительным бронхорасширяющим действием (салметерол и формотерол). Оба препарата оказывают выраженный бронхорасширяющий эффект, который сохраняется по крайней мере 12 ч, однако действие формотерола начинается быстрее, через 1-5 мин. b2-Адреномиметики длительного действия обеспечивают профилактику бронхоспазма перед физической нагрузкой, выходом на холодный воздух, контактом с известным аллергеном, поддерживают стойкий контроль бронхоспазма в течение дня и ночью при среднетяжёлой и тяжёлой бронхиальной астме.
Комбинированные препараты. В фармакотерапии бронхиальной астмы у детей используют комбинацию лекарственных средств или комбинированные лекарственные препараты.
• Флутиказон+салметерол («Серетид Мультидиск») оказывает противовоспалительное и бронхорасширяющее действие и предназначен для регулярного приёма. Препарат можно назначать детям с 4 лет с различной степенью тяжести бронхиальной астмы при сохранении симптомов заболевания, несмотря на проводимую терапию инга-
• ляционными глюкокортикоидами. Препарат хорошо переносим и высоко эффективен при лечении детей. Будесонид+формотерол («Симбикорт») используется у детей с 6 лет. Применяется гибкий подход с увеличением (удвоением) дозы при ухудшении состояния и возвращением к минимальной поддерживающей дозе при стабилизации. Комбинация ингаляционного глюкокортикоида с ингаляционным Р2-адреномиметиком длительного действия предпочтительна увеличению дозы ингаляционного глюкокортикоида.
Антагонисты лейкотриеновых рецепторов
Антагонисты лейкотриеновых рецепторов (зафирлукаст, монтелукаст) назначают в таблетках. Эти препараты эффективны при бронхоитазми в связи с физической нагрузкой аспириновой непереносимости (так называемой аспириновой триаде). Их можно использовать в комбинации с ингаляционными глюкокортикоидами, что позволяет усилить противовоспалительное действие без повышения дозы глюкокортикоидов. Возможно использование в качестве монотерапии при нетяжёлом течении бронхиальной астмы.
Теофиллины замедленного высвобождения можно назначать пациентам с более лёгкой формой заболевания и в ступенчатой терапии бронхиальной астмы как дополнительное лечение при среднетяжёлой и тяжёлой бронхиальной астме к малым и большим дозам ингаляционных глюкокортикоидов (менее эффективны, чем ингаляционные Р2-адреномиметики длительного действия). Наиболее ценно использование теофиллина при ночной бронхиальной астме, препарат может быть полезен также в предупреждении бронхоспзма на физическую нагрузку. Антигистаминные препараты. Эффективность антигистаминных лекарственных средств при бронхиальной астме у детей невелика, так как гистамин - лишь один из медиаторов, участвующих в патогенезе воспаления. В терапии бронхиальной астмы используют антигистаминные препараты второго поколения, обладающие большей специфичностью к Н1-гистаминовым рецепторам, более длительным действием, меньшим седативным и другими побочными эффектами по сравнению с так называемыми «ранними» или «старыми» антигистаминными средствами.
Специфическая иммунотерапия
Специфическую иммунотерапию относят к базисной терапии бронхиальной астмы, её проводит аллерголог во время ремиссии у больного. Специфическая иммунотерапия особенно эффективна при аллер- гическом рините и моновалентной сенсибилизации. Принцип лечения заключается во введении в организм (парентерально, сублингвально) в постепенно возрастающих дозах одного или нескольких причинно значимых аллергенов (домашней пыли, пыльцевых аллергенов и др.),
что приводит к гипосенсибилизации организма больного и уменьшению частоты обострений.
Бронхорасширяющие препараты
Бронхорасширяющие средства (облегчающие состояние) включают β2-адреномиметики быстрого действия, метилксантины короткого действия, ипратропия бромид.
β2 -Адреномиметики
β2-Адреномиметики - одни из основных средств лечения бронхиальной астмы. Их применяют для купирования приступов бронхоспазма (ингаляционные формы быстрого действия) и в качестве профилактического средства для предупреждения ночных приступов удушья и обострения самого заболевания. Однако даже при лёгкой бронхиальной астме с необходимостью частого (более 3 раз в неделю) назначения β2-адреномиметиков рекомендуют раннее проведение или коррекцию противовоспалительной терапии.
• β2-Адреномиметики короткого действия (сальбутамол, фенотерол) приводят к быстрому облегчению состояния детей при приступе бронхиальной астмы. Эффект после ингаляции наступает через 3- 5 мин и продолжается 4-6 ч.
• β2-Адреномиметики длительного действия с быстрым началом (формотерол) начинают действовать через 1-3 мин после приёма и продолжают в течение 12 ч.
При назначении ингаляционных β2-адреномиметиков следует уделить пристальное внимание технике проведения ингаляций. В зависимости от возраста используют различные ингаляционные способы: дозирующий аэрозольный ингалятор со спейсером или спейсером и маской, небулайзер для введения растворов, спинхалеры, дискхалеры, турбохалеры, аэролайзер, лёгкое дыхание для введения порошков. При ингаляции любого лекарства 10-15% попадает в лёгкие, а 75-80% - в ЖКТ. К современным эффективным способам доставки лекарственного средства в дыхательные пути, особенно у детей раннего возраста, относят небулайзер, в котором распыление препарата в форме влажного аэрозоля происходит с помощью сжатого воздуха, подаваемого компрессором. В таком растворе образуются частицы размером 2-5 мкм, оптимальные для поступления в дыхательные пути. Небулайзер можно использовать как в стационаре, так и в домашних условиях. Метилксантины
Метилксантины (аминофиллин) назначают в таблетках или внутривенно при недостаточном эффекте β2-адреномиметиков. Холиноблокаторы
Ипратропия бромид применяют в ингаляциях при нетяжёлых приступах, чаще добавляют к β2-адреномиметику для усиления бронхоли-
тического действия. Эффективна комбинация ипратропия бромида и фенотерола.
Схема лечения бронхиальной астмы
В настоящее время при лечении бронхиальной астмы применяют принцип ступенчатой терапии, т.е. использование медика- ментозных средств в чёткой зависимости от тяжести заболевания. Дозу и частоту приёма препаратов повышают по мере увеличения тяжести болезни или уменьшают при купировании симптомов (табл. 14-2). Нередко противовоспалительные препараты назначают в комбинации с бронхорасширяющими препаратами пролонгированного действия ф2-адреномиметиками или препаратами теофиллина).
Таблица 14-2. Ступенчатая терапия бронхиальной астмы у детей*
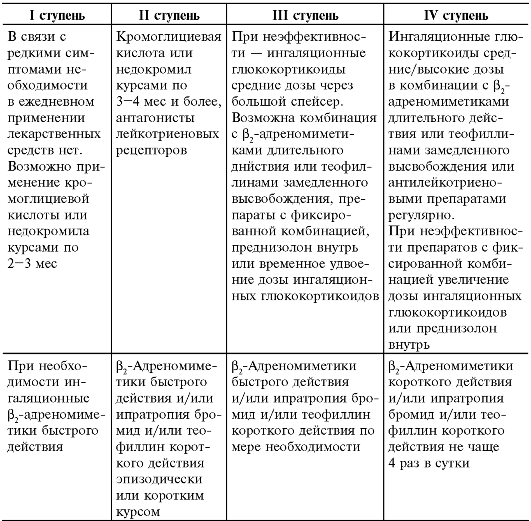
Рациональное и своевременное назначение базисной терапии бронхиальной астмы и аллергического ринита с использованием принципа ступенчатого подхода может обеспечить длительную ремиссию, предотвратить прогрессирование аллергического заболевания.
Неотложная терапия при приступе бронхиальной астмы
Алгоритм неотложной терапии при приступе бронхиальной астмы приведён в таблице 14-3.
Первичная помощь на амбулаторном этапе при лёгком приступе бронхиальной астмы включает ингаляции β2-адреномиметика быстрого действия из дозирующего аэрозольного ингалятора. При среднетяжелом и тяжёлом приступах используют β2-адреномиметик повторно с интервалом 20-30 мин в течение часа, затем каждые 4 ч (по необходимости). Предпочтение отдают небулайзерной терапии. Бронхорасширяющий эффект можно усилить добавлением ипратропия бромида. Если эффект недостаточен, назначают преднизолон внутрь [до 1 года 1-2 мг/кг/сут, в 1-5 лет 10-20 мг] или парентерально. Для лечения обострения бронхиальной астмы эффективна суспензия будесонида, её можно разбавлять физиологическим раствором, а также смешивать с растворами бронхолитиков (сальбутамол, ипратропия бромид). Доза у детей составляет 0,25-0,5 мг (до 1 мг) 2 раза в день.
У больных с тяжёлым обострением в клинической картине могут проявляться не все симптомы. Появление хотя бы одного - цианоз, «немое лёгкое», общая слабость, ПСВ менее 30% должно привлечь внимание врача для решения вопроса о госпитализации. При неэффективности терапии в течение часа необходимо экстренно направить больного в стационар.
ПРОФИЛАКТИКА
Современные подходы к профилактике бронхиальной астмы предусматривают три уровня мероприятий:
• первичную профилактику (предотвращение сенсибилизации);
• вторичную профилактику (предупреждение развития бронхиальной астмы у детей);
• третичную профилактику (предупреждение прогрессирования и неблагоприятного исхода болезни).
Важное место в организации профилактических программ всех уровней занимает определение групп риска.
Таблица 14-3. Алгоритм терапии обострения бронхиальной астмы у детей
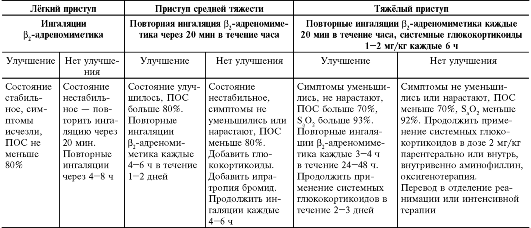
* Из: Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактики». 2-е изд. М., 2006.
Первичная профилактика. Сенсибилизация может развиваться уже внутриутробно, во II триместре беременности. Нарушение барьерных функций плаценты приводит к поступлению в амниотическую жидкость аллергенов, даже небольших концентраций которых достаточно для развития у плода реагинового иммунного ответа. Профилактика аллергии у плода в этом периоде заключается в предупреждении пато- логического течения беременности. Каких-либо иных мероприятий по пренатальной профилактике бронхиальной астмы в настоящее время не разработано. Эффективность диетических ограничений у матери в период беременности не доказана.
Первичная профилактика также включает создание благоприятной экологической обстановки, здоровый образ жизни, элиминацию из окружающей среды неспецифических раздражающих факторов (хими- ческих веществ, табачного дыма и т.п.). Имеют значение своевременное выявление атопии и причинно значимых аллергенов, в том числе пищевых, предупреждение развития вирусных инфекций, лечение атопического дерматита, аллергического ринита и т.д. Единственным доказанным мероприятием, направленным на развитие толерантности в постнатальном периоде, является сохранение естественного вскармливания ребёнка до 4-6-го месяца жизни.
Вторичная профилактика. Мероприятия по вторичной профилактике ориентированы на детей, у которых при наличии сенсибилизации симптомы бронхиальной астмы отсутствуют. К вторичной профилактике относят уменьшение экспозиции аллергенов, ведущее к снижению воспаления в бронхах и их гиперреактивности.
Третичная профилактика строится на основе устранения контакта с аллергенами и поллютантами в целях лучшего контроля бронхиальной астмы и уменьшения потребности в медикаментозной терапии. Ограничение экспозиции аллергенов, как и осуществление образовательных программ, направленных на достижение комплаентности, является непременной частью комплекса мероприятий по лечению бронхиальной астмы.
Большое значение в профилактике тяжёлых исходов придают регулярному диспансерному наблюдению и обучению родителей и детей методам самоконтроля. С этой целью используют пикфлоуметрию с системой цветовых зон (по аналогии с сигналами светофора).
• Зелёная зона: состояние ребёнка стабильное, симптомы отсутствуют или минимальны, ПОС более 80% возрастной нормы. Ребёнок может вести обычный образ жизни, не принимать лекарственных средств или продолжать без изменений терапию, назначенную врачом.
• Жёлтая зона: появляются умеренно выраженные симптомы астмы: эпизоды кашля и свистящего дыхания, нарушение самочувствия, ПОС менее 80% возрастной нормы. В этом случае необходимо
увеличить объём лечения, дополнительно принять лекарства, рекомендованные врачом. Если состояние не улучшается в течение 24 ч, необходима консультация врача.
• Красная зона: ПОС менее 50% возрастной нормы, самочувствие плохое, появляются приступы кашля, удушья, в том числе ночные приступы. Появление таких признаков - показание для срочной консультации врача. Если ранее больной принимал гормональные препараты, необходимо немедленно дать больному преднизолон внутрь в рекомендованной врачом дозе и срочно госпитализировать ребёнка.
ПРОГНОЗ
Сведения об исходах бронхиальной астмы у детей достаточно противоречивы. После полового созревания симптомы бронхиальной астмы могут уменьшиться до полного исчезновения, сохраниться или усилиться. Бронхиальная астма, начавшаяся в детстве, в 60-80% продолжается у взрослых. Исчезновение симптомов отмечено в основном у больных лёгкой формой бронхиальной астмы. В тяжёлых случаях возможны формирование гормональной зависимости, инвалидизация и даже летальный исход. Существенное значение для исхода бронхиальной астмы имеет раннее начало адекватного и систематического лечения.
АТОПИЧЕСКИЙ ДЕРМАТИТ
Атопический дерматит - хроническое рецидивирующее аллергическое заболевание кожи, развивающееся у лиц с генетической предрасположенностью к атопии. Характеризуется кожным зудом, экссудативными и/или лихеноидными высыпаниями, причём локализация и морфология очагов воспаления зависят от возраста больного.
Классификация
• Выделяют три стадии заболевания - младенческая (от рождения до 3 лет), детская (от 3 до 12 лет), подростковая (от 12 до 18 лет). Младенческая, как правило, соответствует острой фазе болезни, а детская и подростковая - хронической. В раннем детском возрасте атопический дерматит протекает в виде двух форм поражения кожи: экссудативной («мокнущей») и эритематозно-сквамозной («сухой»). В детской стадии практически всегда эритематозно-сквамозная форма атопического дерматита сочетается с первыми признаками лихенификации, что свидетельствует о хронизации процесса. В подростковой стадии преобладает лихноидный либо пруригоподобный варианты атопического дерматита.
• В зависимости от течения выделяют следующие стадии: начальную, выраженных изменений кожи, ремиссии и клинического выздоровления.
- Начальная стадия развивается, как правило, у детей раннего возраста. Наиболее частые проявления - гиперемия и отёчность кожи щёк с шелушением. Одновременно возможны гнейс (себорейные чешуйки вокруг большого родничка, бровей, за ушами) «молочный струп» (ограниченное покраснение кожи лица и появление на ней желтоватых корочек), преходящая эритема кожи щёк, ягодиц.
- Несвоевременное и/или неадекватное лечение кожных высыпаний приводит к переходу в стадию выраженных изменений кожи или период обострения (при повторных рецидивах атопического дерматита). О хронической фазе атопического дерматита свидетельствует появление лихенификации.
- В период ремиссии происходит исчезновение или значительное уменьшение симптомов заболевания. Ремиссия может быть различной продолжительности - от нескольких недель и месяцев до 5-7 лет и более.
- Клиническое выздоровление - стадия заболевания, при которой отсутствуют клинические симптомы атопического дерматита в течение 3-7 лет.
• По распространённости атопический дерматит может быть ограниченным, распространённым, диффузным.
- При ограниченном атопическом дерматите очаги ограничены по площади и локализуются в одной из следующих областей: в локтевых сгибах, на тыле кистей, на лучезапястных суставах, в подколенных сгибах, на передней поверхности шеи.
- При распространённом атопическом дерматите процесс не ограничивается локтевыми и/или подколенными сгибами, а распространяется на прилегающие участки конечностей, грудь и спину, что сопровождается интенсивным зудом.
- Диффузный атопический дерматит - наиболее тяжёлая форма заболевания, характеризующаяся поражением всей поверхности кожи (за исключением ладоней, носогубного треугольника). Зуд выраженный, может приводить к скальпированию кожи самим больным, особенно в области спины и конечностей.
• Выделяют 3 степени тяжести течения атопического дерматита: лёгкую, среднюю и тяжёлую (для оценки тяжести атопического дерматита широко используют полуколичественную шкалу SCORAD).
- Лёгкое течение атопического дерматита характеризуется высыпаниями, проявляющимися лёгкой гиперемией, экссудацией и
шелушением, единичными папуло-везикулёзными элементами, слабым зудом кожных покровов, увеличением лимфатических узлов до размеров горошины. Частота обострений - 1-2 раза в год, продолжительность ремиссий - 6-8 мес.
- При атопическом дерматите средней степени тяжести наблюдают множественные очаги поражения на коже с достаточно выраженной экссудацией или инфильтрацией и лихенификацией, экскориациями и геморрагическими корками. Зуд умеренный или сильный. Лимфатические узлы увеличены до размеров лесного ореха или фасоли. Частота обострений - 3-4 раза в год, продолжительность ремиссий - 2-3 мес.
- Для тяжёлого течения атопического дерматита характерны множественные и обширные очаги поражения с выраженной экссудацией, стойкой инфильтрацией и лихенификацией, глубокими линейными трещинами и эрозиями. Зуд сильный «пульсирующий» или постоянный. Наблюдают увеличение практически всех групп лимфатических узлов до размеров лесного или грецкого ореха. Частота обострений - 5 раз в год и более, ремиссии не- продолжительные - от 1 до 1,5 мес и, как правило, неполные.
• Клинико-этиологические варианты атопического дерматита выделяют в зависимости от характера сенсибилизации (с преобладанием пищевой, клещевой, грибковой, пыльцевой аллергии и др.).
Эпидемиология
Атопический дерматит - одно из наиболее частых кожных заболеваний у детей грудного возраста и первых лет жизни. У 45% больных атопический дерматит развивается в первые 6 мес жизни; в первые 5 лет заболевание начинается, по крайней мере, у 85% детей. Распространённость атопического дерматита в экономически развитых странах колеблется от 10 до 28%. В России распространённость атопического дерматита в разных регионах составляет от 5 до 15%.
Этиология
• Пищевые аллергены занимают ведущее место в развитии атопического дерматита, особенно у детей первого года жизни. Практически любой пищевой продукт может стать причиной развития атопического дерматита, но у детей первого года жизни наиболее часто развивается сенсибилизация к молочным продуктам, яйцу, пищевым злакам, сое, рыбе. Толерантность к пище развивается у 30% детей с доказанной IgE-опосредованной сенсибилизацией в течение 3 лет, у 40% - в течение 6 лет, у 53% - в течение 12 лет (при соблюдении элиминационной диеты).
• У детей старше 5-7 лет очень часто обострение заболевания связано с ингаляционными аллергенами (шерсть, пух, эпидермис и слюна животных, пыльца растений). Клещи домашней и библиотечной пыли вызывают обострение кожного процесса не только за счёт ингаляционного пути попадания в организм, но и при непосредственном контакте с кожей. У части больных атопическим дерматитом в сезон цветения возникает обострение кожного процесса, даже в отсутствие респираторного аллергического синдрома.
• Лекарственные аллергены нередко становятся причинными факторами развития и обострения атопического дерматита, особенно после их неадекватного назначения или бесконтрольного применения. В 90% случаев причинно значимыми аллергенами выступают антибиотики (наиболее часто - пенициллины), а также сульфаниламиды, местные анестетики, НПВС, витамины.
• Имеют значение и инфекционные факторы. Микробиоценоз кожи составляют грамположительные бактерии, дожжеподобные грибки. При повышенной колонизации происходит сенсибилизация к этим микроорганизмам, которые, обладая свойствами суперантигенов, поддерживают не только инфекционное, но и аллергическое воспаление. Важнейшее значение придают золотистому стафилококку, который продуцирует токсины. Нередко при атопическом дерматите выявляют паразитозы и протозойные инвазии (описторхоз, энтеробиоз, аскаридоз и др.).
Патогенез
В основе симптомов атопического дерматита лежит аллергическое воспаление кожи, связанное с формированием клеточного воспалительного инфильтрата. Эпидермис больных с атопическим дерматитом содержит увеличенное количество IgE-несущих клеток Лангерганса и воспалительных дендритных эпидермальных клеток, представляющих высокоаффинный рецептор для IgE. Высокоаффинные рецепторы (FceR1) для IgE участвуют в захвате и представлении Аг Т-клеткам в коже с активацией Т-лимфоцитов и усилением процесса дифференцировки Th0- в Th2- и активаций и секрецией провоспалительных цитокинов (ИЛ4, ИЛ5, ИЛ13). Клетки Лангерганса мигрируют в лимфатические узлы и стимулируют нулевые Т-клетки, таким образом вызывая увеличение пула Тh2-клеток. Тh2-клетки памяти мигрируют по сосудистому руслу к различным местам, включая слизистую оболочку носа и лёгких, костный мозг, что приводит к формированию «ато- пического марша» (под последним понимают процесс естественного развития атопических проявлений у ребёнка вследствие прогрессирования клинических признаков атопического заболевания от атопического дерматита до бронхиальной астмы и аллергического ринита).
В патогенезе атопического дерматита важное значение имеют психонейроиммунные взаимодействия, в частности, различные нейро- пептиды (субстанция Р, нейротензины А и В и др.) опосредуют вазодилатацию, проявляющуюся эритемой.
Клиническая картина
Младенческая форма. Излюбленная локализация поражений - область лица (за исключением носогубного треугольника), разгибательная (наружная) поверхность верхних и нижних конечностей, локтевые и подколенные ямки, запястья, туловище, ягодицы. Основной субъективный симптом - зуд кожи различной интенсивности, приводящий к формированию порочного круга: зуд ? расчесы ? сыпь ? зуд.
Кожа гиперемирована и отёчна, покрыта микровезикулами. Наблюдают экссудацию (мокнутие), корки, шелушение, трещины; красный или смешанный дермографизм. Типичным считают отсутствие поражений в области под подгузниками (у детей грудного возраста), этот эффект, вероятно, отражает комбинацию повышенной гидратации в зоне подгузников, защиту от триггеров и невозможность расчёсов и трения.
Детская форма. Характеризуется гиперемией (эритемой) и отёком кожи, появлением лихенификации, зудом. Наблюдают папулы, бляшки, эрозии, экскориации, геморрагические корочки. Трещины особенно болезненны на ладонях, пальцах и подошвах. Кожа сухая, покрыта большим количеством мелкопластинчатых и/или отрубевидных чешуек. Кожные высыпания возникают преимущественно на сгиба- тельных поверхностях конечностей, тыле кисти, передне-задне-боковой поверхности шеи, в локтевых и подколенных ямках. Возможна гиперпигментация век в результате расчёсывания глаз, появление характерной складки кожи под нижним веком (линия Денье-Моргана). Выявляют белый или смешанный дермографизм.
Подростковая форма. Крупные, слегка блестящие лихеноидные папулы с выраженной лихенификацией, а также множеством экскориаций и геморрагических корочек локализуются на лице (периорбикулярная, периоральная области), шее (в виде «декольте»), локтевых сгибах, вокруг запястий и на тыльной поверхности кистей. Отмечают сильный зуд, нарушение сна, невротические реакции. У большинства больных, как правило, выявляют стойкий белый дермографизм.
Лабораторные исследования
Для выявления аллергии у детей с атопическим дерматитом используют комплекс методов специфической диагностики, включающий:
• кожные тесты (скарификационные, прик-тест);
• провокационные пробы;
• лабораторные методы: клинический и биохимический анализ крови, определение концентрации IgE (общего и специфического), IgA, IgG и IgM в сыворотке крови (по показаниям), копроовоцистоскопия, бактериологическое исследование фекалий (по показаниям).
Диагностика
Главные диагностические критерии включают:
• кожный зуд;
• типичные морфология (основной первичный элемент - папуловезикула+вторичные элементы) и локализация поражений кожи в зависимости от возраста;
• хроническое рецидивирующее течение;
• атопия в анамнезе или наследственная предрасположенность к атопии.
Дополнительные диагностические критерии включают:
• ксероз;
• ихтиоз/усиление рисунка на ладонях;
• хейлит;
• реакции немедленного типа при кожном тестировании с аллергенами;
• повышенную концентрацию IgE в сыворотке крови;
• начало заболевания в раннем детском возрасте (до 2 лет);
• частые инфекционные поражения кожи, в основном стафилококковой и герпетической этиологии;
• локализацию кожного процесса на кистях и стопах;
• экзему сосков;
• рецидивирующие коньюнктивиты;
• дополнительные суборбитальные складки Денни-Моргана;
• периорбитальную гиперпигментацию, тёмные круги под глазами;
• катаракту, кератоконус;
• эритродемию;
• белый дермографизм.
Для постановки диагноза атопического дерматита необходимо наличие не менее 3 главных критериев, а также 3 и более дополнитель- ных, при минимальном сроке сохранения симптомов не менее 6 нед.
Дифференциальная диагностика
• Себорейный дерматит: отсутствует наследственная предрасположенность к атопии, характерно появление на волосистой части головы (на фоне гиперемии и инфильтрации) скоплений жирных, сальных чешуек, покрывающих голову в виде корок. При поражении естественных складок кожи туловища и конечностей наблюдается гиперемия с наличием пятнисто-папулёзных элементов, покрытых
чешуйками на периферии. Зуд умеренный или отсутствует. Связь с действием тех или иных аллергенов обычно отсутствует.
• Контактный дерматит обусловлен реакциями на химические агенты окружающей среды. Характеризуется эритемой, уртикарной сыпью, иногда усеянной пузырями и пузырьками; наблюдается выраженный отёк соединительной ткани. Высыпания локализуются на участке контакта с раздражающим веществом (например, пелёночный дерматит).
• Иммунодефицитные заболевания (синдром Вискотта-Олдрича, гипериммуноглобулинемия Е) проявляется у детей в возрасте от 1 мес до 3 лет и характеризуется триадой симптомов: дерматитом, клинически идентичным атопическому, тромбоцитопенией, рецидивирующими инфекциями желудочно-кишечного и респираторного трактов. В основе заболевания лежит первичная комбинированная иммунологическая недостаточность с преимущественным поражением гуморального звена иммунитета. Синдром гипериммуноглобулинемии Е (синдром Джоба) - симптомокомплекс, характеризующийся высокой концентрации общего IgE в сыворотке крови, атопическим дерматитом и рецидивирующими инфекционными процессами. Начинается заболевание в раннем возрасте. Сопутствующие симптомы - подкожные абсцессы, гнойные отиты, пневмонии.
• Чесотка - контагиозное заболевание из группы дерматозоонозов, вызываемое чесоточным клещом, с характерными кожными изменениями на тыле кистей рук, в межпальцевых складках, паховых складках, животе, ладонях и подошвах. Вследствие расчёсов появляются линейно расположенные высыпания в виде удлинённых, слегка выступающих беловато-розовых валиков, с пузырьками или корочками на одном конце.
Лечение
Гидратация и уход за кожей. У больных с атопическим дерматитом снижены эпидермальная гидратация, концентрация поверхностных липидов кожи и керамидов, что отражает нарушения состояния гидролипидной пленки кожи. Для предупреждения эффекта испарения, который повреждает кожный барьер, кожу больных необходимо обрабатывать лекарственными или косметическими средствами сразу после купания и увлажнения кожи. Рекомендуется поддерживать тем- пературный режим с умеренной влажностью.
Кожа больных атопическим дерматитом более чувствительна к воздействию факторов окружающей среды и различного рода раздражающих веществ, чем кожа здоровых людей. Поэтому важно определить и исключить раздражающие агенты, которые могут вызывать и подде-
рживать зуд. К ним относятся различные виды физических, химических и биологических раздражающих факторов, в том числе моющие средства, химические препараты, грубая одежда, крайние значения температуры и влажности. Полезны мягкие очищающие средства, особенно при частых инфекциях кожи, ежедневный душ водой комфортной температуры, ограничение использования мыла, наружных средств, содержащих компоненты, растворяющие жир, различных детергентов, ароматических добавок.
Диетотерапия. Дети первого года жизни должны находиться на ес- тественном вскармливании. Исключительно грудное вскармливание до 4-6 мес жизни снижает выраженность проявлений атопического дерматита.
• При доказанной пищевой аллергии следует исключить из питания причинно-значимые аллергены, продукты, вызывающие перекрёстные аллергические реакции, обладающие повышенной сенсибилизирующей и гистамин-либерирующей активностью, а также содержащие экстрактивные вещества, консерванты и красители.
• Необходима адекватная замена исключённых продуктов натуральными или лечебными продуктами, соответствующих возрасту ребёнка.
• Целесообразно «функциональное питание», т.е. использование продуктов, способствующих нормализации кишечного биоценоза, регулирующих иммунную систему.
Наружная терапия
• Местные ингибиторы кальциневрина (пимекролимус) разработаны специально для лечения воспалительных изменений кожи и используют у детей с первых месяцев жизни в форме 1% крема («Элидел»). Ингибиторы кальциневрина являются первой линией терапии, местные глюкокортикоиды назначают коротким курсом при тяжёлом обострении.
• При островоспалительных процессах с наличием отёка, эритемы, мокнутия назначают примочки и влажно-высыхающие повязки в виде водных растворов (1-2% танина, 0,25% нитрата серебра, жидкость Бурова и др.). При остром воспалении без мокнутия предпочтение отдают эмульсиям, пастам, кремам, в состав которых входит нафталан, глюкокортикоиды.
• В случае хронического течения процесса с выраженной инфильтрацией применяют пасты и мази, содержащие 5-20% ихтаммола («Ихтиола»). Возможность их применения в амбулаторной практике ограничивают неприятный запах и способность пачкать одежду.
• При инфицировании кожи стафилококками и/или стрептококками используют наружные антибактериальные препараты (эритромицин, линкомицин, анилиновые красители, фукорцин, водный
раствор бриллиантового зелёного, метиленового синего и т.д.). При наличии грибковой инфекции применяют наружные противогриб- ковые препараты: клотримазол, тербинафин, кетоконазол. При осложнённых формах, вызванных бактериальной и грибковой флорой применяют комбинированные препараты (например, мазь или крем гентамицин + бетаметазон + клотримазол - «Тридерм»). При распространённых формах пиодермии часто требуется назначение системных антибиотиков.
• Топические глюкокортикоиды эффективны как при остром, так и при хроническом заболевании. Механизм противовоспалительного действия этих препаратов заключается в блокаде фосфолипазы А2, вследствие чего происходит снижение продукции лейкотриенов, выраженный и длительный ангиоспазм, торможение синтеза глюкозамингликанов, коллагена и эластина, повышение связывания гистамина и других медиаторов, снижение выброса лизосомальных ферментов, уменьшение в эпидермисе количества клеток Лангерганса и тучных клеток. Глюкокортикоиды эффективно уменьшают воспаление и зуд и снижают бактериальную колонизацию, в том числе Staphylococcus aureus. В настоящее время топические глюкокортикоиды подразделяют на 4 группы по степени фармакотерапевтической активности (слабой, умеренной, высокой, очень высокой активности). По составу различают простые и комбинированные глюкокортикоиды. Среди простых глюкокортикоиды выделяют фторированные и нефторированные препараты. Комбинированные глюкокортикоиды имеют в своем составе антибактериальные и/или противогрибковые препараты.
• Применение антагонистов Н1-рецепторов гистамина в качестве базисных препаратов для лечения АД основывается на
важнейшей роли гистамина в механизме кожного зуда при атопическом дерматите. Антигистаминные препараты I поколения назна- чают в острый период атопического дерматита парентерально или перорально для уменьшения зуда. Для предотвращения рецидивов, особенно при длительном лечении, используют препараты II поколения.
• Нарушения со стороны пищеварительной системы не только поддерживают аллергический воспалительный процесс в коже, но и могут быть его причиной. Основные задачи терапии заключаются в улучшении процессов расщепления и всасывания пищевых продуктов (ферментные препараты), нормализации микробного пейзажа кишечника (селективное подавление условно-патогенных микроорганизмов, «заселение» кишечника нормальной флорой с помощью пробиотиков, стимуляция роста нормальной микрофлоры кишечника пребиотиками). Назначение пробиотиков в перинатальный
период уменьшает частоту атопического дерматита среди детей из группы высокого риска в первые 2 года жизни.
• Кратковременная терапия системными глюкокортикоидами показана при острых формах заболевания и неэффективности наружной терапии, а также у больных с тяжёлым диффузным атопическим дерматитом.
Профилактика
Факторы риска развития атопического дерматита:
• отягощённый собственный и семейный аллергологический анамнез;
• нарушение диеты матери во время беременности и кормления грудью;
• курение матери и другие отрицательные факторы во время беременности и лактации;
• раннее искусственное вскармливание и неправильный режим питания детей, позднее прикладывание к груди;
• нарушение режима дня и неправильный уход за кожей;
• нарушение правил проведения вакцинации;
• климатогеографические условия;
• неблагоприятные условия жизни, отрицательные социальные и экологические факторы;
• антибактериальная терапия во время беременности, лактации, а также антибактериальная терапия в младенческом возрасте;
• нарушения функций ЖКТ с рождения, энзимопатии, дисбактериоз кишечника и др.
В профилактике развития аллергических заболеваний важнейшую роль играет грудное вскармливание. При развитии атопического дерматита у ребёнка, находящегося на грудном вскармливании, необходимо в первую очередь внести соответствующие изменения в рацион кормящей матери. С этой целью для кормящих матерей разработаны специальные гипоаллергенные диеты, особенностями которых является элиминация продуктов, обладающих высокой сенсибилизирующей активностью, на весь период кормления ребёнка грудью.
При отсутствии эффекта, что обычно наблюдается при тяжёлом течении заболевания, выраженной сенсибилизации к белкам коровьего молока показано использование смесей на основе гидролизатов белка лечебного назначения.
У детей, находящихся на смешанном или искусственном вскармливании, необходимо провести строгий анализ рациона ребёнка с его последующей коррекцией. В качестве докорма возможно использовать адаптированные кисломолочные смесям («Агуша-1», «Агуша-2», «Нан кисломолочный») или гипоаллергенные смеси на основе гидролизатов белка лечебно-профилактического назначения.
В питании детей старше 7,5-8 мес допускается применение неадаптированных кисломолочных продуктов (кефир, биокефир, бифи- докефир, биолакт), а также напитков, полученных путём сквашивания сухого коровьего молока или молочных смесей специальными заквасками, содержащими бифидобактерии и ацидофильные палочки («Наринэ», «Ацидолакт») в объёме не более 1 кормления.
В настоящее время производят целый ряд продуктов для детей, страдающих пищевой аллергией. Врач имеет возможность выбрать необходимую смесь в соответствии с возрастом и нутритивным статусом ребёнка, периодом заболевания, степенью сенсибилизации к белкам коровьего молока. Вакцинацию проводят по индивидуальному календарю вне обострения атопического дерматита.
Прогноз
Прогноз атопического дерматита весьма вариабелен. Недавние исследования показывают полное исчезновение симптомов к пубертатному возрасту или сразу после пубертатного периода у 40-60% пациентов.
АЛЛЕРГИЧЕСКИЙ РИНИТ
Аллергический ринит - хроническое заболевание слизистой оболочки носа, в основе которого лежит IgE-опосредованное аллергическое воспаление, обусловленное воздействием различных аллергенов.
Классификация
Выделяется сезонный (интермиттирующий) и круглогодичный (персистирующий) аллергический ринит. По тяжести течения - лёг- кий, среднетяжёлый и тяжёлый.
Эпидемиология
В развитых странах аллергическим ринитом страдает 10-25% населения. В России по данным официальной статистики частота аллергического ринита составляет 0,3-0,6%. По результатам эпидеми- ологических исследований по программе ISAAC (International Study of Asthma and Allergic in Childhood) показана высокая распространён- ность аллергического ринита в России - 8-23%.
Аллергический ринит диагностируют в основном у детей после 6-7 лет, тогда как первые симптомы могут наблюдаться уже у 2-3-летних детей и даже на первом году жизни.
Этиология
Основные факторы вызывающие появление симптомов аллергического ринита - содержащиеся в воздухе аллергены: пыльцевые, быто-
вые аллергены жилищ (клещей домашней пыли, животных, насекомых, плесени, некоторых домашних растений), грибковые аллергены.
Пусковые факторы, которые способствуют развитию неспецифической назальной гиперреактивности, включают холодовое воздействие, эмоциональные нагрузки, стрессовые ситуации, острую пищу.
Патогенез
Аллергический ринит - классический пример IgE-опосредованной аллергической реакции I типа, которая состоит из двух фаз. В ранней фазе аллергического ответа тучные клетки, несущие специфические IgE, мигрируют в слизистую оболочку носа и распознают попавшие туда аллергены. Связывание тучной клетки с аллергеном немедленно вызывает её активацию и дегрануляцию с выделением медиаторов воспаления, ведущим из которых является гистамин. Медиаторы вызывают повышение проницаемости тканей и местный отёк слизистой оболочки, ринорею, расширение артериовенозных анастомозов с увеличением кровенаполнения кавернозной ткани и затруднением дыхания. Гистамин вызывает раздражение афферентных нервов с ощущением жжения, рефлекторными приступами чихания.
Через несколько часов возникает отсроченная или поздняя фаза аллергического ответа, обусловленная активацией ТЪ2-лимфоцитов. При взаимодействии их с антигенпрезентирующими клетками вырабатываются цитокины (ИЛ5), которые участвуют в увеличении количества эозинофилов и базофилов в слизистой оболочке полости носа с вторичным повышением содержания гистамина и других медиаторов воспаления.
Повторная провокация даже меньшей концентрацией аллергенов вызывает более выраженные клинические симптомы. При персистирующем (круглогодичном) рините имеет место длительное воздействие низких концентраций аллергена с развитием хронического воспаления и сохранением «минимального персистирующего воспаления» даже при отсутствии аллергенной стимуляции.
Клиническая картина
К основным клиническим симптомам аллергического ринита относятся затруднённое носовое дыхание, выделения из носа (ринорея), зуд (жжение) в полости носа, приступообразное чихание. Сопутствующие симптомы - снижение обоняния, головная боль, нарушение сна, общее недомогание. Дополнительные симптомы: приоткрытый рот, тём- ные круги под глазами, отёчность и гиперемия кожи крыльев носа и над верхней губой, носовые кровотечения, боль в горле, покашливание, боль в ушах. Нередко аллергический ринит сочетается с отитами, синуситами, бронхиальной астмой. До 3-летнего возраста превалиру-
ют заложенность носа с отёком слизистой оболочки и слизистыми выделениями, чихание, зуд и приступообразная ринорея менее характерны. У детей младшего возраста привычный жест потирания кончика носа, так называемый «аллергический салют», приводит к образованию красной поперечной полоски в области кончика носа.
Для пыльцевой аллергии характерно сочетание аллергического ринита и конъюнктивита, сезонность обострений, метеозависимость, перекрёстная сенсибилизация с пищевыми аллергенами.
При бытовой аллергии характерным является эффект элиминации при перемене места жительства, обострение в сырое время года, при уборке квартиры. При грибковой аллергии отмечается непереносимость продуктов, содержащих дрожжи (кисломолочные продукты, квас).
Лабораторные и инструментальные исследования
В общем анализе крови и при микроскопии мазка отделяемого из носа, окрашенного по методу Романовского, выявляют эозинофилию.
Важны для диагностики кожные аллергические пробы (скарификационные или прик-тест) с причинно значимыми аллергенами, внутриносовой провокационный тест с аллергенами, на которые получены положительные кожные реакции, определение концентрации общего и специфических IgE в случае невозможности проведения кожных проб или проблем с интерпретацией полученных результатов.
Инструментальные исследования
Передняя риноскопия и эндоскопическое исследование выявляют отёк носовых раковин, серый, цианотичный цвет и характерную пятнистость слизистой оболочки, а также значительное количество белого, иногда пенистого секрета в носовых ходах. При многолетнем течении могут быть также выявлены полипозные изменения слизистой оболочки.
Дифференциальная диагностика
• У детей раннего возраста с рецидивами респираторных вирусных инфекций необходимо исключить аллергический ринит. Дополнительный диагностический критерий в пользу аллергического ринита - положительный эффект от терапии антигистаминными препаратами.
• Инфекционный ринит - характерно острое начало, предшествующий контакт с больным ОРВИ, типичная последовательность появления и исчезновения симптомов. При упорном течении показано исследование клеточного состава мазка из полости носа, а также исследование на микрофлору и чувствительность к антибиотикам, исключение вовлечения в процесс придаточных пазух носа.
• Вазомоторный ринит характеризуется стойкими клиническими проявлениями в виде затруднения носового дыхания и водянистыми выделениями из носа. Слизистая гиперемированная, цианотичная, иногда бледная с кровоизлияниями. Отсутствует связь с аллергическими факторами.
• Аденоидные вегетации характеризуются стабильным или прогрессирующим затруднением носового дыхания, в том числе ночью, отсутствует связь с аллергическими факторами.
Лечение
Лечение аллергического ринита включает элиминацию аллергенов, специфическую иммунотерапию, фармакотерапию. Основные группы лекарственных средств: блокаторы Н1-рецепторов гистаминов, назальные спреи глюкокортикоидов, стабилизаторы мембран тучных клеток. В качестве симптоматических средств используют промывания полости носа тёплым 0,9% раствором хлорида натрия, орошение раствором морской соли, короткие курсы сосудосуживающих препаратов (ксилометазолин, оксиметазолин, фенилэфрин), М-холиноблокаторы (ипратропия бромид).
При лёгком аллергическом рините применяют курсы пероральных антигистаминных препаратов поколения II (дезлоратадин, лоратадин, фексофенадин, цетиризин, эбастин). Препараты для местного примене- ния (в виде назальных спреев) - азеластин, левокабастин. Применяют и стабилизаторы мембран тучных клеток: кетотифен перорально, кромоглициевую кислоту для местной терапии. Хороший стабильный эффект достигается проведением специфической иммунотерапии причинно-значимыми аллергенами.
При среднетяжёлом и тяжёлом аллергическом рините терапию также начинают с пероральных блокаторов Н1-рецепторов гистамина II поколения. При недостаточном эффекте к терапии добавляются назальные спреи глюкокортикоидов (беклометазона, будесонида, мометазона, флутиказона).
Профилактика
Необходимо контролировать контакт с аллергенами. Легче уменьшить экспозицию аллергенов в помещении, чем пыльцевых и других экологических воздействий. Перед предполагаемым контактом с аллергеном следует принять профилактические средства.
Прогноз
Своевременная диагностика, устранение сенсибилизирующих и провоцирующих факторов, специфическая иммунотерапия позволяют устранить все симптомы аллергического ринита и предотвратить раз- витие осложнений.
КРАПИВНИЦА И ОТЁК КВИНКЕ
Крапивница - гетерогенное заболевание, проявляющееся эритематозными зудящими элементами, возвышающимися над поверхностью кожи и, как правило, усиливающимися при расчёсах. Первичный эле- мент - волдырь, реже папула.
Отёк Квинке (гигантская крапивница, ангионевротический отёк) - наследственное или приобретённое заболевание, характеризующееся отёком кожи, подкожной клетчатки, а также слизистых оболочек различных органов и систем (дыхательных путей, кишечника, и др.)
Классификация
В зависимости от этиологических признаков и патофизиологических механизмов, лежащих в основе развития крапивницы, выделяют следующие её варианты.
• Иммунологически-обусловленная (анафилактический тип, цитотоксический тип, иммунокомплексный тип).
• Анафилактоидная (вызванная медиатор-высвобождающими агентами, аспиринзависимая).
• Физическая (механическая, холодовая, тепловая, холинергическая, солнечная, контактная, вибрационная).
• Другие виды (идиопатическая, папулёзная, пигментная, системный мастоцитоз, инфекционная крапивница, кожная форма васкулита и другие системные заболевания, обусловленная неопластическими процессами, эндокринная, психогенная).
• Наследственные формы (наследственный ангионевротический отёк, нарушение метаболизма протопорфирина 9, наследственная холодовая крапивница, дефицит СЗв).
В зависимости от течения крапивницу разделяют на острую (до 6 нед) и хроническую (более 6-8 нед).
Эпидемиология
Крапивница - широко распространённое заболевание. У 10-20% людей хоть раз в жизни была крапивница, которая нередко сочетается с отёками Квинке. Крапивница и отёк Квинке чаще развиваются у девочек. Возможен изолированный отёк Квинке.
Этиология
Наиболее частые причины крапивницы и отёка Квинке включают: пищевые продукты (рыба, рыбная икра, ракообразные, молоко, яйца, орехи, бобовые, картофель, сельдерей, цитрусовые, красные сорта яблок, клубника, сухие колбасы, сыр, шоколад), пищевые добавки (краситель жёлтого цвета - тартразин, содержащийся в кондитерских и
гастрономических изделиях, консерванты - салицилаты, бензоаты, сульфиты, нитриты), лекарственные препараты (антибиотики, особенно группы пенициллина, сульфаниламиды, витамины, особенно группы В, белковые препараты - кровь, плазма, иммуноглобулины, инсулин, рентгеноконтрастные средства, плазмозаменители, НПВС и др.), укусы насекомых (ос, пчёл, шершней и др.), паразиты (простейшие, гельминты) и инфекционные агенты (вирусы, в том числе гепатита В и С, бактерии, грибы). У детей с крапивницей часто выявляют очаги хронической инфекции в ЛОР-органах (синусит, тонзиллит, отит), ротовой полости, пищеварительной системе (хронический гас- трит, холецистит, дисбактериоз), урогенитальном тракте. Физические факторы: давление, холод, тепло, инсоляция, физическая нагрузка и др. могут вызывать крапивницу, так же как психогенные факторы (нервно-психический стресс, тревога). Крапивница и отёк Квинке могут возникнуть на фоне других заболеваний (пищеварительной системы, опухоли, лимфопролиферативные заболевания, диффузные болезни соединительной ткани и др.), что требует детального диагностического поиска. Нередко причина остаётся неизвестной (идиопатическая крапивница и отёк Квинке).
Патогенез
По механизмам развития различают аллергическую, неаллергическую и идиопатическую формы заболевания. Аллергическая крапивница и отёк Квинке обусловлены I, реже II и III типами реакций гиперчувствительности. Наиболее часто встречается IgE-зависимый тип, который характеризуется дегрануляцией тучных клеток и базофилов под влиянием взаимодействия аллергена и реагинов. Медиаторы этих клеток ответственны за появление основных симптомов заболевания. Кроме того, гистамин и ПгD2 активируют С-волокна, которые секретируют нейропептиды (субстанция Р, вазоактивный интестинальный пептид, нейрокинин), вызывающие дополнительную вазодилатацию и дегрануляцию тучных клеток. Накапливающиеся в коже под влиянием хемоаттрактантов лимфоциты, эозинофилы, нейтрофилы секретируют фактор, высвобождающий гистамин из мастоцитов. Эозинофилы являются источником эозинофильного катионного протеина, обладающего цитотоксичностью.
Цитотоксический тип реакций гиперчувствительности лежит в основе крапивницы, возникающей при гемотрансфузиях, иммунокомплексный - при сывороточной болезни.
У 40-50% пациентов с хронической идиопатической крапивницей в крови обнаруживаются аутоантитела (IgG и IgM) к высокоаффинным рецепторам реагинов и IgE. Их взаимодействие приводит к дегра- нуляции тучных клеток и базофилов.
Неаллергическая крапивница и отёк Квинке обусловлены неспецифической либерацией медиаторов (гистамин, лейкотриены и др.) из тучных клеток, активацией калликреин-кининовой системы и накоплением в коже эозинофилов и нейтрофилов.
Контактная крапивница и отёк Квинке у части больных обусловлены IgE-зависимой гиперчувствительностью, чаще у пациентов с атопическими заболеваниями или неспецифической либерацией медиаторов из тучных клеток при проникновении через кожу различных веществ (лекарства, металлы, парфюмерия и др.). У 75-80% пациентов этиологический фактор выявить не удается. Не исключается роль Helicobacter pylori в развитии хронической рецидивирующей крапивницы.
Этиология и механизмы развития холодовой крапивницы изучены недостаточно. По механизму развития приобретённая холодовая крапивница, вероятно, является инфекционно-аллергической или ау- тоаллергической, обусловлена IgE и, реже, другими АТ (IgM, IgG) криоглобулинами, криофибриногеном. Уртикарные элементы могут возникать под влиянием механических воздействий на кожу. В зависимости от их характера различают дермографическую, вибрационную крапивницу и крапивницу от давления. Предполагается, что заболевание обусловлено неспецифической дегрануляцией тучных клеток и, возможно, высвобождением гистамина из эндотелия сосудов. Оно часто имеет семейный характер с аутосомно-доминантным типом наследования. Ацетилхолин способен вызывать дегрануляцию тучных клеток и увеличение секреции их медиаторов (гистамина, эозинофильного и нейтрофильного хемотаксического фактора и др.). Аналогичные изменения лежат в основе тепловой и аквагенной кра- пивниц. Первая возникает под действием тепла (горячий душ, ванна, нагревание кожи при загаре и т.д.). Появление второй провоцируется водой независимо от её температуры.
Клиническая картина
Для крапивницы характерны кожный зуд и появление волдырей различного размера м формы, нередко сливающихся между собой, бледных в центре и гиперемированных по периферии, как правило, исчезающих бесследно через несколько дней или часов. Наблюдается повышение температуры тела, слабость, снижение АД. Отёки Квинке проявляются плотными безболезненными инфильтратами, обычно локализующимися на лице (губы, веки), в полости рта (мягкое нёбо, язык, миндалины). Поражение дыхательной системы (гортани, трахеи, бронхов) проявляется осиплостью голоса, лающим кашлем, приступами удушья и асфиксией. Симптомы при вовлечении пищеварительной
системы зависят от локализации: дисфагия при поражении пищевода, тошнота, рвота - при поражении желудка, боли, метеоризм, кишечная непроходимость - при поражении кишечника. Контактная крапивница и отёк Квинке наблюдаются в месте соприкосновения кожи и слизистых оболочек с пищевыми продуктами (рыба, яйца, орехи и др.), латексом, аллергенами животных, лекарствами, парфюмерией, металлами (браслеты, застёжки и др.). Крапивница и отёк Квинке могут быть предвестниками анафилактического шока.
Хроническая рецидивирующая крапивница наблюдается у пациентов с новообразованиями лёгких, желудка, кишечника, СКВ, аутоиммунными болезнями щитовидной железы (тиреоидит Хашимото, диффузный токсический зоб), лимфопролиферативными заболеваниями. Холодовая крапивница характеризуется появлением кожного зуда и уртикарных высыпаний на коже, подвергшейся действию низких температур (холодный воздух, вода). Заболевание может быть локализованным (лицо, шея, руки) или генерализованным (например, при купании в холодной воде), а также проявляться отёками Квинке губ, языка, мягкого нёба, глотки при употреблении холодной пищи (мороженое, напитки и др.). Крапивницу от давления характеризует появление волдырей при проведении по коже тупым предметом, растирании её полотенцем, в местах давления одежды (обычно развивается через 4-6 ч после воздействия). Световая крапивница возникает на открытых частях тела (лицо, шея, руки, и т.д.) под действием ультрафиолетового излучения, преимущественно весной и летом. Характеризуется появлением в течение 1-3 мин после экспозиции кожи зуда, уртикарных элементов и отёка. Изменения сохраняются в течение 1-3 ч.
Лабораторные и инструментальные исследования
В клиническом анализе крови у пациентов с крапивницей может быть эозинофилия. Для выявления причинно значимых аллергенов проводят кожные аллергические пробы и/или определение специфических IgE АТ. Провокационные тесты - холодовой, световой, тест с давлением, дозированной физической нагрузкой, с вибрацией и др. - проводят для подтверждения крапивницы от физического воздействия. При наследственном ангионевротическом отёке часто отмечается снижение С1-ингибитора одновременно с уменьшением второго и четвёртого компонентов комплемента в результате его избыточной активации.
При неаллергической крапивнице и отёках Квинке требуется углуб- лённое обследование больного для выявления патологии пищевари- тельной системы, коллагенозов, порфирии и др.
Диагностика
Для постановки диагноза аллергической крапивницы и отёка Квинке используют результаты аллергологического анамнеза, кожного тестирования, провокационных и лабораторных тестов.
Дифференциальная диагностика
• При уртикарном васкулите наблюдаются болезненные волдырные, папулёзные, иногда геморрагические высыпания, оставляющие после исчезновения шелушение и пигментацию. Характерны поражения сосудов других органов: артриты и артралгии, хронический гломерулонефрит, боли в животе, обструкция бронхов, конъюнктивит, увеит. Решающее исследование для постановки диагноза - биопсия кожи, выявляющая периваскулярные клеточные инфильтраты, состоящие из нейтрофилов, эозинофилов и лимфоцитов.
• При экссудативной эритеме наблюдают полиморфные высыпания, состоящие из пятен, пузырьков, пузырей и оставляющие после себя пигментацию и шелушение. Они поражают кожу и слизистые оболочки полости рта, губ и конъюнктивы глаз. Разновидностью этого заболевания является синдром Стивенса-Джонсона, возникающий при приёме некоторых лекарственных препаратов.
• При чесотке больных беспокоит мучительный кожный зуд, усиливающийся вечером и ночью. Характерны узелковые и везикулярные высыпания, корочки и ссадины от расчёсов, которые локализуются на кистях рук (межпальцевые промежутки), предплечьях (в области лучезапястных суставов), животе, мошонке, внутренней поверхности бёдер, реже - на туловище, подмышечных впадинах, молочных железах. Заболевают часто несколько членов семьи. Волдырей при чесотке не бывает. Диагноз подтверждается при микроскопии соскобов кожи, где обнаруживают чесоточных клещей и их яйца.
• Системный мастоцитоз (пигментная крапивница) - генетически детерминированное заболевание, при котором происходит накопление тучных клеток в коже и различных органах (печени, селезён- ке, лимфатических узлах, лёгких). У больных возникает уртикарная кожная сыпь, оставляющая после исчезновения пигментацию. Характерен симптом Унна - при механическом раздражении пигментных пятен возникают эритема и отёк.
Лечение
При лечении аллергической крапивницы и отёка Квинке используют элиминационную терапию, фармакотерапию и образовательные программы для пациентов. Элиминационная терапия предусматривает удаление из окружения больного этиологически значимых аллер-
генов. При пищевой аллергии необходима элиминационная диета, а также элиминация уже поступившего в организм аллергена с помощью очистительных клизм.
Лечение сопутствующих заболеваний пищеварительной системы (хронического холецистита, панкреатита, дисбактериоза и др.). При лекарственных крапивницах отменяют как препарат, вызвавший их развитие, так и комбинированные средства, в состав которых он входит.
Больному необходимо иметь при себе противошоковый набор (жгут, ампулы с эпинефрином, преднизолон, клемастин, хлоропирамин).
Используют лекарственные средства, тормозящие развитие различных фаз реакций гиперчувствительности. Применяют антигистамин- ные препараты I (парентерально) и II (перорально) поколений. Первые показаны при острой генерализованной крапивнице, вторые - при хроническом течении заболевания. При дермографической крапивнице эффективно комбинированное применение H1- и Н2-блокаторов. При холинергической крапивнице используют препараты, обладающие холинолитической активностью. При тяжёлом течении болезни показан короткий курс глюкокортикоидов (парентерально при острой крапивнице, перорально при хронической). Исключительно важное значение имеет лечение очаговой хронической инфекции.
Больным с
наследственным ангионевротическим отёком в период обострения необходимо
проведение заместительной терапии натив- ной плазмой в дозе не менее
250-300 мл одномоментно, а также введение раствора ε-аминокапроновой
кислоты внутривенно капельно в дозе 100-200 мл, затем - по 100 мл
капельно каждые 4 ч или
Прогноз
При обнаружении причинно значимого аллергена при аллергической крапивнице и отёке Квинке прогноз, как правило, хороший. Наследственный ангионевротический отёк, локализующийся в гортани, может быть причиной смерти больных.