Детские болезни: учебник / Под ред. А.А. Баранова - 2-е изд., - 2009. - 1008 с.
|
|
|
|
ГЛАВА 8 АНЕМИИ
Анемия - патологическое состояние, при котором происходит снижение содержания Hb в единице объёма крови. Это очень широкое понятие, включающее как ряд очерченных нозологических форм, так и синдромы при различных заболеваниях. Показатели красной крови значительно изменяются с возрастом ребёнка. По данным ВОЗ, 20% населения Земли, преимущественно дети и женщины фертильного возраста, страдают анемией, наиболее часто связанной с недостаточным питанием и/или дефицитом железа в пище.
Классификация
Анемии классифицируют по следующим параметрам.
• Средний размер эритроцитов (нормо-, макро- и микроцитарные).
• Цветовой показатель (нормо-, гипо- и гиперхромные).
• Регенераторная возможность красного костного мозга, т.е. по количеству ретикулоцитов (нормо-, гипо- и гиперрегенераторные).
• Этиология (нарушения образования, избыточное разрушение клеток крови, кровопотеря).
Ниже приведена патогенетическая классификация анемий.
I. Анемии, вызванные недостатком гемопоэтических факторов (преимущественно железодефицитная, преимущественно белководефицитная, преимущественно витаминодефицитная).
II. Анемии постгеморрагические (острые, хронические).
III. Анемии гипо- и апластические (наследственные, приобретённые).
IV. Анемии гемолитические.
• Связанные с внутренними аномалиями эритроцитов (мембранопатии, ферментопатии, гемоглобинопатии).
• Связанные с внешними воздействиями [аутоиммунные гемолитические; вследствие повреждения (турбулентность тока крови при стенозе устья аорты, искусственных клапанах и т.д.), инфекционные и паразитарные (например, при малярии); вследствие отравления (тяжёлыми металлами, змеиным ядом), связанные с дефицитом витамина Е].
V. Анемии при различных (хронических) заболеваниях.
ДЕФИЦИТНЫЕ АНЕМИИ
Практически до 90% анемий у детей и женщин относятся к дефицитным, причём значительную часть из них составляют железодефицитные. Дефицит железа в той или иной степени присутствует у 30-40% жителей планеты, причём сидеропения развивается в 2 раза чаще, чем анемия, и её выявляют у всех беременных в последнем триместре. В России железодефицитной анемией страдают до 40% детей первых 3 лет жизни, до 1/3 подростков и 44% женщин фертильного возраста. В группу высокого риска входят дети от матерей с неблагополучно протекавшей и/или многоплодной беременностью, недоношенные, дети в возрасте 6-12 мес, крупные и интенсивно растущие дети в любом возрасте, дети, получающие нерациональное и несбалансированное питание, страдающие дис- бактериозом, мальабсорбцией и хроническими воспалительными заболеваниями кишечника, а также девочки-подростки с гиперполименореей. Значение имеют не только возраст и пол, но и уровень жизни в стране.
Этиология и патогенез
Этиология дефицитных анемий отражена в их названии. Они обычно возникают в периоды бурного роста организма (первые годы жизни, пубертатный период), когда высокие потребности организма в веществах, необходимых для кроветворения (полноценный белок, витамины, микроэлементы, железо) не покрываются пищей. Кроме того, усвоение этих веществ может быть нарушено в силу незрелости ферментных и транспортных систем организма ребёнка.
Патогенез зависит от преобладания недостаточности того или иного фактора, необходимого для нормального кроветворения. При преимущественном дефиците белка снижаются продукция эритропоэтина почками, активность ферментов кишечника, всасывание железа и ви- таминов. Вследствие этого нарушается гемопоэз. При недостаточном поступлении витаминов в организм (в первую очередь витаминов В6 и В12) замедляется как включение железа в гем (витамин В6), так и нормальный процесс созревания клеток эритроидного ряда из-за дефекта синтеза ДНК (витамин В12). Однако белково- и витаминодефицитные анемии возникают довольно редко, обычно при грубом нарушении вскармливания. Гораздо чаще развивается дефицит железа, тяжело отражающийся на процессе кроветворения и состоянии всего организма. Это связано с особенностями метаболизма, распределения и усвоения железа, высокими потребностями растущего организма в этом элементе и низким его содержанием в пище.
0
Железодефицитная анемия
ОБМЕН ЖЕЛЕЗА В ОРГАНИЗМЕ РЕБЁНКА
Плод получает железо от матери через плаценту в течение всей беременности, наиболее интенсивно с 28-32-й недели. В организме доношенного ребёнка содержится около 300-400 мг железа, недоношен- ного - всего 100-200 мг. После рождения запасы железа, полученные от матери, пополняются за счёт утилизации Hb при распаде «лишних» эритроцитов, содержащих HbF. Неонатальное (материнское и эритроцитарное) железо расходуется на синтез Hb, миоглобина, железосодержащих ферментов, необходимых для поддержания нормального обмена веществ и гомеостаза, а также на компенсацию естественных потерь (с калом, мочой, потом), на регенерацию клеток кожи, слизистых оболочек и т.д. Кроме того, ребёнку необходимо создавать резервы железа, т.е. баланс железа должен быть положительным.
Потребности доношенного ребёнка до 3-4 мес удовлетворяются за счёт эндогенного железа и молока матери, содержащего железо в среднем в количестве 0,5 мг/л, причём до 50% его (0,25 мг) всасывается в кишечнике с помощью специального белка лактоферрина. Однако уже к 5-6 мес у доношенного и к 3-4 мес у недоношенного ребёнка потребность в железе, составляющая 1 мг/сут, удовлетворяется за счёт указанных источников только на 1/4. Искусственное вскармливание коровьим молоком, употребление сыра, яиц, чая, оксалатов, фосфатов замедляет всасывание железа. Способствуют всасыванию железа аскорбиновая, янтарная и другие органические кислоты, фруктоза, сорбит, животный белок.
Всосавшееся в тонкой кишке железо с помощью транспортного белка трансферрина переносится в красный костный мозг и тканевые депо. Различают гемовое (80% железа в организме) и негемовое железо (табл. 8-1).
К негемовому железу, кроме указанного в таблице, относят также трансферрин (основной транспортный белок), ферритин и гемосидерин (белки, служащие резервным источником железа в организме). Железо участвует во многих обменных процессах. Без него невозможны нормальные рост и развитие ребёнка.
Дефицит железа в организме (сидеропения) проходит три стадии.
1. Прелатентная - недостаточное содержание железа в тканях, концентрация Hb и сывороточного железа не изменены.
2. Латентная - концентрация Hb нормальная, но сывороточного железа снижена.
3. Железодефицитная анемия - изменены все показатели красной крови.
Таблица 8-1. Распределение и функции железа в организме

КЛИНИЧЕСКАЯ КАРТИНА ЖЕЛЕЗОДЕФИЦИТНЫХ СОСТОЯНИЙ Клиническая картина железодефицитных состояний (сидеропений) неспецифична и включает несколько синдромов.
• Астено-вегетативный синдром - следствие нарушения функций головного мозга. Маленькие дети с железодефицитной анемией отстают в психомоторном развитии. Они плаксивы, раздражительны, капризны, плохо контактируют со сверстниками. У детей старшего возраста страдает интеллектуальное развитие: снижены память, внимание, интерес к учёбе. Появляются признаки СВД. Возможны мышечные боли и гипотония (в частности - мочевого пузыря), энурез.
• Эпителиальный синдром включает дистрофию и атрофию барьерных тканей (слизистых оболочек, кожи и её производных - ногтей, волос). К трофическим нарушениям легко присоединяются воспалительные изменения. В результате снижается аппетит, возникают извращение вкуса и обоняния (pica chlorotica), дисфагия, диспептические расстройства, нарушения процессов всасывания в кишечнике, скрытые кишечные кровотечения. Бледность кожи и конъюнктивы выявляют только при значительном снижении концентрации Hb.
• Иммунодефицитный синдром проявляется частыми ОРВИ и ОКИ. Около 70% часто болеющих детей страдают сидеропенией. У них снижен как неспецифический (лизоцим, пропердин и т.д.), так и специфический иммунитет. Показано, что в отсутствие железа IgA теряет свою бактерицидную активность.
• Сердечно-сосудистый синдром наблюдают при тяжёлой железодефицитной анемии. У детей развиваются повышенная утомляемость, низкое АД, тахикардия, снижение тонуса сердечной мышцы, приглушение тонов, функциональный, довольно грубый систолический шум, хорошо выслушиваемый на сосудах («шум волчка») и связанный с гидремией. Возможны головокружения.
• Гепатолиенальный синдром возникает редко, обычно при тяжёлой анемии и сочетании рахита и анемии.
Лабораторные критерии сидеропений представлены в табл. 8-2. В последнее время стали обращать внимание на то, что дефицит железа увеличивает абсорбцию свинца в ЖКТ. Это особенно важно для детей, живущих в больших городах, вблизи магистральных дорог. К проявлениям сидеропении в таком случае может присоединиться (особенно у маленьких детей) свинцовая интоксикация, приводящая к тяжёлым психическим и неврологическим расстройствам, нарушениям функций почек и кроветворения. Анемия при этом становится рефрактерной к лечению препаратами железа.
Таблица 8-2. Лабораторные критерии железодефицитньгх состояний у детей*
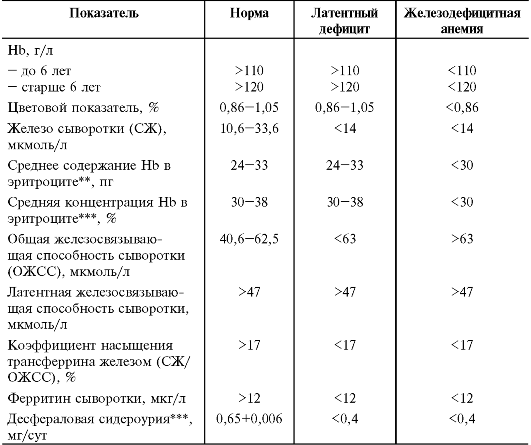
* По Коровиной Н.А. и соавт., 1999.
** Показатели, определяемые автоматически на современных анализаторах красной крови.
*** Определяют содержание в суточной моче железа после введения дефероксамина («Десферала») внутримышечно из расчёта 10 мг/кг.
ДИАГНОСТИКА ЖЕЛЕЗОДЕФИЦИТНЫХ СОСТОЯНИЙ Диагноз железодефицитной анемии и латентного дефицита железа основывают на изложенных выше лабораторных критериях. Основной показатель - содержание ферритина в сыворотке крови. При невозможности получить все указанные данные можно ориентироваться на следующие показатели, доступные в любом медицинском учрежде- нии.
• Концентрация Hb.
• Цветовой показатель рассчитывают следующим образом: цветовой показатель = [(концентрация Hb, г/л)х3]+(три первые цифры количества эритроцитов без запятой). В норме составляет 0,85-1,05.
• Морфология эритроцитов в мазке периферической крови.
• Результат от лечения препаратами железа при приёме внутрь: через 10-14 дней концентрация Hb повышается ежедневно на 1-4 г/л, содержание ретикулоцитов увеличивается до 3-4% (ретикулоцитарный криз).
КЛИНИЧЕСКИЕ ФОРМЫ ПРЕИМУЩЕСТВЕННО ЖЕЛЕЗОДЕФИЦИТНЫХ АНЕМИЙ
Ранняя анемия недоношенных
Ранняя анемия недоношенных имеет сложный патогенез и развивается на 1-2-м месяце жизни более чем у половины недоношенных и изредка у доношенных детей («физиологическая» доброкачественная анемия), особенно при неблагоприятном преморбидном фоне. При объективном обследовании отмечают только бледность (при снижении концентрации Hb до 80 г/л). При исследовании периферической крови обнаруживают нормоили гиперхромную норморегенераторную анемию, часто достигающую тяжёлой степени.
Основными причинами развития ранней анемии считают усиленный «физиологический» гемолиз эритроцитов, содержащих HbF, недостаточную функциональную и морфологическую зрелость красного костного мозга, снижение продукции тканевых эритропоэтинов вследствие гипероксии, имевшей место при рождении ребёнка. Большое значение имеет также дефицит многих необходимых для кроветворения веществ, откладывающихся в депо только в последние 2 мес беременности (белок, витамины C, E, группы B, медь, кобальт) и обеспечивающих всасывание, транспорт, обмен и фиксацию железа в молекуле гема, а также стабильность оболочек и мембран эритроцитов. Присутствует и дефицит железа в депо, временно компенсированный текущим гемолизом, но чётко выявляемый путём обнаружения микроцитоза и гипохромии части эритроцитов, снижения концентрации
сывороточного железа и количества сидероцитов в пунктате красного костного мозга. Как только неонатальные запасы железа истощаются, ранняя анемия переходит в позднюю анемию недоношенных.
Лечение ранней анемии вызывает затруднения. Ранее по жизненным показаниям переливали эритроцитарную массу, сейчас с успе- хом применяют эпоэтин бета (эритропоэтин человека рекомбинантный). Назначают 10 инъекций в дозе 200 ЕД/кг п/к 3 раза в неделю. Одновременно назначают препараты железа (2 мг элементарного железа в сутки), фолиевую кислоту (0,001 г/сут) и витамин E (25 мг/сут в течение 2-3 мес).
Поздняя анемия недоношенных
Поздняя анемия недоношенных (конституциональная) развивается на 3-4-м месяце жизни в результате истощения неонатальных запасов железа в депо. Клинические проявления обычно незначительны, лабораторные данные свидетельствуют о преимущественном дефиците железа.
Алиментарная и инфекционная анемии
Алиментарная и инфекционная анемии развиваются во втором полугодии жизни у доношенных детей. В происхождении алиментарной анемии играют роль нарушения вскармливания, одновременно вызы- вающие и дистрофию. Инфекционные заболевания, чаще всего ОРВИ и отиты, обычно способствуют более тяжёлому течению алиментарной анемии. Клинические и лабораторные проявления характерны для преобладания дефицита железа.
Хлороз
Хлороз - редкое заболевание девочек в период полового созревания. Развивается на фоне нарушения режима и эндокринной дисфункции. Проявляется слабостью, повышенной утомляемостью, анорексией, извращением вкуса, головокружениями, иногда обмороками, сердцебиением, болями в эпигастральной области, тошнотой, рвотой, запорами. Характерны «алебастровая», в некоторых случаях с зеленоватым оттенком, бледность кожи, нарушения менструального цикла (олигоили аменорея). Выздоровление обычно самопроизвольное, возможны рецидивы. Лабораторные исследования указывают на преимущественный дефицит железа.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА ДЕФИЦИТНЫХ АНЕМИЙ Дифференциальную диагностику железодефицитной анемии проводят с другими дефицитными анемиями, талассемией и сидеробластными анемиями - свинцовой и пиридоксинзависимой, при которых
эритропоэз нарушен в результате нарушения включения железа в гем. Гипохромия эритроцитов в последнем случае сочетается с повышением концентрации сывороточного железа.
• Клинические проявления приобретённой сидеробластной анемии, вызванной свинцовой интоксикацией, более манифестны, чем при железодефицитной анемии: схваткообразные боли в животе, выраженные диспептические проявления, бледность с землистым оттенком, психические и неврологические расстройства. В анализах крови - базофильная зернистость, гипохромия эритроцитов, повышение концентрации сывороточного железа. В анализах мочи определяют аминолевулиновую кислоту.
• При наследственной пиридоксинзависимой сидеробластной анемии синтез гема нарушается на последнем этапе. В гипохромных эритроцитах накапливается свободный протопорфирин, концентрация сывороточного железа повышена, в красном костном мозге много сидеробластов.
• Белководефицитная анемия сопровождается более выраженной бледностью и дисхромией кожи и волос, блефаритами, пастозностью тканей или отёками, анорексией, рвотой, диареей. Концентрация Hb снижена до 40-90 г/л, цветовой показатель в пределах нормальных значений, выражены анизо- и пойкилоцитоз.
• Витаминодефицитная анемия (дефицит витаминов В12, С) проявляется астенизацией, парестезиями, бледностью с лимонно-жёлтым оттенком, субиктеричностью склер, глосситом, афтозным стоматитом, умеренной гепатомегалией. Концентрация Hb снижена, как и содержание эритроцитов, нормо- и гиперхромных, цветовой показатель повышен (более 1,0). Появляются макро-, пойкило- и анизоцитоз, тельца Жолли, кольца Кэбота, мегалобласты, гигантские метамиелоциты. В пунктате красного костного мозга выявляют мегалобластный тип кроветворения.
ЛЕЧЕНИЕ
Лечение железодефицитной анемии проводят в три этапа (табл. 8-3).
Обязательная и наиболее важная составная часть каждого из этапов - приём препаратов железа. Препараты железа в подавляющем большинстве случаев принимают перорально. При лечении железоде- фицитной анемии и латентного дефицита железа, помимо препаратов железа, необходимо соблюдение режима и диеты, сбалансированной по основным ингредиентам; нормализация всасывания железа при его нарушении (например, сочетанное лечение ферментными препаратами при синдроме мальабсорбции), дозированная физическая активность.
Таблица 8-3. Этапы лечения железодефицитной анемии*
Этапы | Цель | Продолжительность | Средние суточные дозы элементарного железа |
Устранение анемии | Восстановление нормальной кон- центрации Hb | 1,5-2 мес | До 3 лет - 3-5 мг/кг/сут; от 3 до 7 лет - 100-120 мг/ сут; старше 7 лет - до 200 мг/сут |
Терапия насыщения | Восстановление запасов железа в ор- ганизме | 3-6 мес | До 3 лет - 1-2 мг/кг/сут; от 3 до 7 лет - 50-60 мг/сут; старше 7 лет - 50-100 мг/сут |
Поддерживающая терапия | Сохранение нормального уровня всех фондов железа | При кровотечениях из ЖКТ - 7- 10 дней каждый месяц, а у девочекподростков с гиперполименореей - 7-10 дней после каждой менструации | 40-60 мг/сут |
* По Аркадьевой Г.В., 1999.
Лечение пероральными препаратами железа
К наиболее часто применяемым соединениям железа относят железа [III] гидроксид полимальтозат и соли двухвалентного железа - сульфат, фумарат, хлорид и глюконат. Для улучшения всасывания соли двухвалентного железа комбинируют с органическими кислотами, аминокислотами и другими соединениями.
• Детям раннего возраста показаны жидкие лекарственные формы, позволяющие более точно дозировать железо (табл. 8-4).
Таблица 8-4. Препараты железа, применяемые у детей раннего возраста
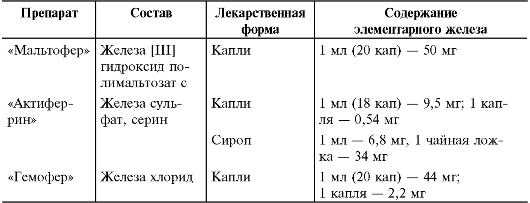
• Детям старшего возраста и подросткам назначают таблетки и капсулы, содержащие железо. В последнее время в основном с профилактической целью применяют комбинированные препараты, содержащие кроме железа витамины и другие микроэлементы (табл. 8-5). Препаратом выбора служит мальтофер, содержащий железо в неионной форме, не вызывающий побочных действий, обладающий приятным вкусом, принимаемый сразу после или во время еды. Его можно добавлять в любые соки и блюда. Остальные препараты принимают между при- ёмами пищи, запивают фруктовыми соками (лучше цитрусовыми). Одновременно принимают возрастную дозу аскорбиновой кислоты.
Таблица 8-5. Наиболее часто применяемые препараты железа*
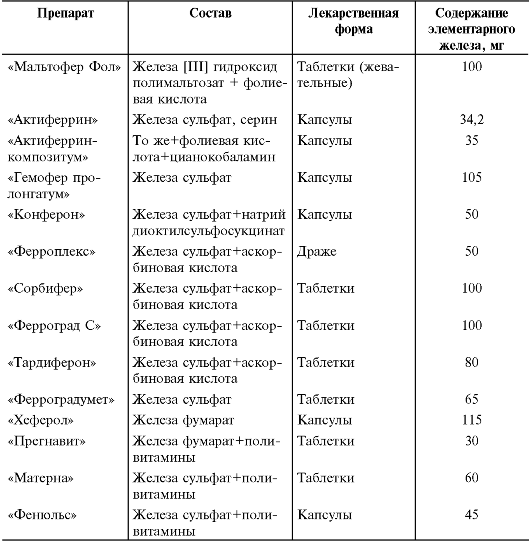
* По Аркадьевой Г.В., 1999.
Суточную дозу всех препаратов распределяют на три приёма. В начале лечения в течение нескольких дней препараты назначают в половинной дозе для уточнения их индивидуальной переносимости. При отсутствии диспептических явлений и других побочных эффектов переходят к возрастной дозе. Комбинированные препараты, назначаемые с профилактической целью, принимают 1 раз в сутки.
Препараты железа для парентерального введения
Парентерально препараты железа вводят только при наличии соответствующих показаний.
• Состояния после операций на ЖКТ.
• Синдром нарушенного всасывания в тонкой кишке.
• Хронический энтероколит и неспецифический язвенный колит.
• Непереносимость железа при приёме внутрь.
Основной препарат для парентерального введения - железа (III) гидроксид полиизомальтозат («Феррум лек»). Средние суточные дозы представлены в табл. 8-6.
Таблица 8-6. Средние суточные дозы препаратов железа для парентерального введения (расчёт по элементарному железу)*
Возраст детей | Суточная доза элементарного железа, мг/сут |
1-12 мес 1-3 года Старше 3 лет | до 25 25-40 40-50 |
* По Коровиной Н.А. и соавт., 1999.
Расчёт курсовой дозы элементарного железа для парентерального введения проводят по формуле:
Количество элементарного железа = М х (78 - 0,35 х Hb),
где М - масса тела пациента, кг; Hb - концентрация Hb, г/л.
Курсовую дозу препарата для парентерального введения вычисляют по формуле:
Количество препарата на курс = КДЖ/СЖП,
где КДЖ - курсовая доза железа, мг; СЖП - содержание железа в мг в 1 мл препарата.
При парентеральном введении препаратов железа нередко возникают побочные эффекты: диспептические расстройства, аллергические реакции (вплоть до развития анафилактического шока), гемосидероз. Переливание эритроцитарной массы проводят только при снижении концентрации Hb менее 60 г/л.
ПРОФИЛАКТИКА
Антенатальная профилактика. В течение всей беременности женщине следует принимать пролонгированные или комплексные препараты железа с поливитаминами («Тардиферон», «Ферроградумет», «Матерна» и др.). Приём этих препаратов необходимо продолжать и во время кормления ребёнка грудью. Кроме того, имеют значение предупреждение и лечение невынашивания и гестозов, полноценное питание, дозированная физическая нагрузка.
Постнатальная профилактика
• Естественное вскармливание со своевременным введением соков и мясных продуктов.
• Профилактика других заболеваний раннего возраста.
• Адекватный режим, хороший уход, достаточное пребывание на свежем воздухе.
• Ежемесячный анализ периферической крови.
• Проведение в группах риска превентивных курсов с назначением препаратов железа в половинной дозе (1-2 мг/кг/сут).
ПРОГНОЗ
Прогноз при железодефицитной анемии при своевременно начатом и последовательном лечении благоприятный.
ПОСТГЕМОРРАГИЧЕСКИЕ АНЕМИИ
Постгеморрагические анемии обусловлены острой или хронической потерей крови.
• Острые кровопотери развиваются у детей довольно часто и бывают обусловлены родовой травмой (кровоизлияния во внутренние органы и мозговые оболочки), фето-материнской и фето-фетальной трансфузиями, плацентарными кровотечениями, геморрагическими диатезами, травмами, язвенными процессами в ЖКТ, метроррагиями у девочек и др. Массивная потеря крови сопровождается развитием гиповолемического шока с признаками эксикоза, централизацией кровообращения, сердечно-сосудистой недостаточностью и быстрым истощением коры надпочечников. Анемизацию у новорождённых выявляют уже через 20-30 мин после кровопотери, у более старших детей - на следующий день, иногда позднее. В анализах крови в первые сутки выявляют лейкоцитоз со сдвигом лейкоцитарной формулы влево, гипертромбоцитоз. Из-за компенсаторного сосудистого спазма концентрация Hb, гематокрит, содержание эритроцитов могут сохраняться на нормальном уровне. На 2-3-и сутки эти показатели снижаются за счёт увеличения объёма
плазмы. Через 2-3 дня нарастает содержание ретикулоцитов, в мазке крови выявляют пойкилоцитоз, полихромазию, нормобластоз. Нормализация всех показателей происходит через 4-8 нед. Лечение направлено на остановку кровотечения и восстановление ОЦК (инфузионная терапия коллоидными растворами, при необходимости переливание эритроцитарной массы).
• Хроническая кровопотеря приводит к развитию типичной железодефицитной анемии (см. раздел «Железодефицитная анемия»). Лечение сводится к устранению причины кровопотери и коррекции железодефицитного состояния.
ГИПО- И АПЛАСТИЧЕСКИЕ АНЕМИИ
Апластические и гипопластические анемии - группа редких наследственных (анемия Фанкони, анемия Блекфэна-Дайемонда и др.) и приобретённых (лекарственные, постинфекционные, вирусные, вызванные химическими веществами) анемий. Они обусловлены дефектом стволовой клетки, приводящим к уменьшению или отсутствию гемопоэза.
• Клиническая картина анемии Фанкони обусловлена панцитопенией и включает анемический (резкая бледность кожи и слизистых оболочек, повышенная утомляемость, слабость, одышка, тахикардия), геморрагический (петехии, экхимозы, экстравазаты, длительные кровотечения различной локализации) синдромы и агранулоцитоз (в результате чего возникают инфекционно-воспалительные и гнойно-некротические процессы). Часто анемия Фанкони сочетается с множественными врождёнными аномалиями. В анализах крови выявляют панцитопению, нормоили макроцитарную анемию, часто повышена концентрация HbF, содержание ретикулоцитов резко снижено, или они вообще отсутствуют. В миелограмме обнаруживают замещение красного костного мозга жёлтым, отсутствие или резкое уменьшение количества клеток-предшественников всех ростков. Лечение - трансплантация красного костного мозга, назначение андрогенов. Если лечение андрогенами неэффективно и нет совместимых доноров красного костного мозга, показано пробное лечение гемопоэтическими ростовыми факторами.
• При парциальной красноклеточной аплазии с изолированным поражением эритроидного ростка (анемия Блекфэна-Дайемонда) у большинства детей при рождении или несколько позже отмечают бледность. Часто анемия сопровождается врождёнными аномалиями развития. В анализах крови - макроцитарная, реже нормоцитарная анемия, ретикулоцитопения, гипоплазия или аплазия
эритроидного ростка; содержание лейкоцитов в норме или слегка уменьшено, тромбоцитов - в норме или слегка увеличено. При анемии Блекфэна-Дайемонда проводят регулярные трансфузии эритроцитарной массы. Через 5-6 лет у этих детей нередко развивается вторичный гемохроматоз.
ГЕМОЛИТИЧЕСКИЕ АНЕМИИ
Гемолитические анемии возникают в результате усиленного разрушения клеток эритроидного ряда. Они могут быть наследственными или приобретёнными; с внутрисосудистым или внутриклеточным ти- пом гемолиза; связанными с внутренними аномалиями самих эритроцитов или внешними воздействиями.
Гемолитические анемии, связанные с внутренними аномалиями эритроцитов
МЕМБРАНОПАТИИ
Наиболее частый вариант мембранопатий в России - наследственный сфероцитоз, или болезнь Минковского-Шоффара. Распространённость наследственного сфероцитоза - около 1:5000 без учёта лёгких и бессимптомных форм болезни.
Этиология и патогенез. В 70% случаев болезнь МинковскогоШоффара - 9ΐ, в 30% - возникает в результате спонтанных мутаций или р. В основе заболевания лежит молекулярный дефект белков мембраны эритроцита, снижающий их осмотическую стойкость. Длительность жизни эритроцита уменьшается до 8-10 дней, дефектные клетки разрушаются в селезёнке.
Клиническая картина
Клиническая картина разнообразна - от бессимптомных форм до угрожающей жизни гемолитической анемии. Характерна триада симптомов: желтуха, спленомегалия, анемия. Часто возникают задержка физического развития, аномалии черепа и лицевого скелета. В анализах крови выявляют снижение концентрации Hb, ретикулоцитоз, микросфероцитоз, смещение кривой Прайс-Джонса влево. Снижена осмотическая стойкость эритроцитов. Течение среднетяжёлой и тяжё- лой форм болезни может сопровождаться гемолитическими и апластическими кризами.
• Гемолитический криз возникает спонтанно или на фоне инфекции: появляется или усиливается желтуха, нарастают размеры селезёнки, она становится болезненной. В крови снижаются концентрация Hb и содержание эритроцитов, нарастает ретикулоцитоз, повышается
• концентрация непрямого билирубина и ЛДГ. Первый гемолитический криз, протекающий атипично и редко диагностируемый, может развиться в период новорождённости. Апластический криз обычно провоцирует парвовирусная инфекция (парвовирус В19), оставляющая стойкий иммунитет, поэтому такой криз развивается у пациентов один раз в жизни. Быстро снижаются концентрация Hb и содержание эритроцитов, иногда - лейкоцитов и тромбоцитов. Содержание билирубина и количество ретикулоцитов не увеличиваются. Состояние больных часто тяжёлое из-за развивающихся гипоксемии и гипоксии.
Относительно часто у больных наследственным сфероцитозом развивается желчнокаменная болезнь.
Лечение. Вне криза при лёгкой и среднетяжёлой формах лечение не проводят. При гемолитическом кризе необходимы инфузионная терапия, переливание эритроцитарной массы при снижении концентрации Hb менее 70 г/л. Спленэктомия показана при тяжёлой или осложнённой среднетяжёлой форме. Перед операцией желательно провести вакцинацию детей поливалентной пневмококковой и ме- нингококковой вакцинами, а также вакциной гемофильной палочки, так как после спленэктомии пациенты подвержены риску более частых и тяжёлых вирусных и бактериальных инфекций. Детям до 6 лет предпочтительно проведение альтернативной операции - рентгенэндоваскулярной окклюзии сосудов селезёнки, сохраняющей функцию органа и уменьшающей гемолиз.
ЭНЗИМОПАТИИ
Наиболее распространённый вариант энзимопатий, приводящий к развитию гемолитической анемии - недостаточность глюкозо-6-фос- фат дегидрогеназы. Частный случай недостаточности глюкозо-6-фос- фат дегидрогеназы - фавизм. Гемолиз развивается при употреблении в пищу конских бобов, фасоли, гороха, вдыхании нафталиновой пыли.
Этиология и патогенез. Наследование недостаточности глюкозо-6- фосфат дегидрогеназы (К), в силу чего чаще болеют мужчины. В мире насчитывают около 400 млн носителей этого патологического гена. Заболевание развивается, как правило, после приёма определённых лекарственных средств (производные нитрофурана, хинин, изониазид, фтивазид, аминосалициловая кислота, налидиксовая кислота, сульфаниламиды и др.) или на фоне инфекции.
Клиническая картина. Заболевание проявляется бурным развитием гемолиза при употреблении перечисленных выше веществ или инфекциях (особенно при пневмониях, брюшном тифе, гепатите). Недостаточность глюкозо-6-фосфат дегидрогеназы может быть при-
чиной желтухи новорождённых. В анализе крови выявляют ретикулоцитоз, повышение уровня прямого и непрямого билирубина, ЛДГ, щелочной фосфатазы. Морфология эритроцитов и эритроцитарные индексы не изменены. Диагноз устанавливают на основании результатов определения активности фермента.
Лечение. Вне криза лечение не проводят. При лихорадке приме- няют физические методы охлаждения. При хроническом гемолизе назначают фолиевую кислоту 1 мг/сут по 3 нед каждые 3 мес. При кризе отменяют все лекарственные средства, проводят инфузионную терапию на фоне дегидратации.
ГЕМОГЛОБИНОПАТИИ
Гемоглобинопатии - группа наследственных болезней, обусловленных нарушениями синтеза или строения Hb. Они характеризуются неэффективным эритропоэзом из-за нарушения утилизации внутри- клеточного железа для синтеза Hb.
Талассемии
Талассемии - самая распространённая гетерогенная группа гемоглобинопатий, выявляемых преимущественно в странах Средиземноморья, на Востоке и Северном Кавказе.
Этиология и патогенез. В основе заболевания лежит генетический дефект (р). Избыток непарных глобиновых цепей индуцирует образование нерастворимых тетрамеров, абсорбирующихся на мембранах эритроцитов и повреждающих их.
Клиническая картина. У гетерозиготных носителей гена заболевание протекает легко или не проявляется совсем. У гомозиготных носителей гена и при комбинированных формах развивается тяжёлая форма талассемии (большая талассемия, анемия Кули). В последнем случае анемию выявляют в первые месяцы жизни. У больных обычно имеется много стигм дизэмбриогенеза (монголоидный разрез глазных щелей, гиперплазия бугров черепа, низкорослость), гиперпигмента- ция кожи; увеличены и уплотнены печень и селезёнка. Это связано с появлением очагов экстрамедуллярного кроветворения и прогрессирующим гемохроматозом. Часто развиваются перикардит, цирроз печени, гиперспленизм и снижение иммунитета. Без лечения больные погибают в раннем возрасте.
Лабораторные и инструментальные исследования. В анализах крови снижены концентрация Hb и содержание эритроцитов (мишеневидных, с базофильной зернистостью). Характерны эритробластоз и микроцитоз. Снижена концентрация HbА, повышена - HbF и HbА2. Повышены осмотическая стойкость эритроцитов и концентрация непрямого билирубина. Концентрация сывороточного железа нормаль-
ная или повышенная. Общая железосвязывающая способность сыворотки в пределах нормы. Коэффициент насыщения трансферрина железом значительно повышен. Обнаруживают десфераловую сидероурию. На рентгенограмме выявляют характерные изменения черепа в виде поперечной исчерченности («щётка») и остеопороза, а также патологические переломы трубчатых костей.
Лечение лёгких форм симптоматическое. Назначают фолиевую кислоту курсами по 3 нед каждые 3 мес, по 1-2 мг/сут. При среднетяжё- лых формах переливают отмытые эритроциты по мере необходимости, проводят курсы дефероксамина для выведения лишнего железа, спленэктомию. При выраженной талассемии единственный радикальный метод лечения - трансплантация красного костного мозга. Изучают эффективность при талассемии цитостатиков, эпоэтина бета.
Серповидноклеточная анемия
Серповидноклеточная анемия - часто регистрируемая наследственная гемоглобинопатия, характеризующаяся умеренно выраженной хронической гемолитической анемией, рецидивирующими острыми болевыми кризами и повышенной восприимчивостью к инфекционным заболеваниям (обусловленным главным образом Streptococcus pneumoniae). Заболевание диагностируют у 1% афроамериканцев, часто регистрируют в Азербайджане и Дагестане.
Этиология и патогенез. Заболевание связано с наличием патологического гена HbS (9ΐ). HbS полимеризуется с формированием длинных цепей, изменяющих форму эритроцитов (они становятся серповидными). Серповидные эритроциты вызывают увеличение вязкости крови, стаз, создают механическую преграду в мелких артериолах и капиллярах, приводя к тканевой ишемии (с чем связаны болевые кризы). Кроме того, серповидные эритроциты менее устойчивы к механичес- ким воздействиям, что приводит к их гемолизу.
Клиническая картина. Появляются умеренная желтуха, трофические язвы в области лодыжек, отставание в физическом развитии (особенно у мальчиков), предрасположенность к апластическим и гемолитическим кризам, болевые кризы, спленомегалия, холелитиаз, аваскулярные некрозы, остеонекроз с развитием остеомиелита.
Лабораторные исследования. При электрофорезе Hb обнаруживают полимеризованный HbS. В анализах крови выявляют снижение концентрации Hb, ретикулоцитоз (гиперрегенераторная анемия), лейкоцитоз, тромбоцитоз, уменьшение СОЭ. В мазке периферической крови эритроциты имеют форму серпа. Концентрация билирубина сыворотки крови слегка повышена. В красном костном мозге - эритроидная гиперплазия, увеличение количества многоядерных клеток-предшес- твенников.
Лечение. При острых болевых кризах средней степени тяжести в амбулаторных условиях применяют ненаркотические анальгетики (ибупрофен, парацетамол), при острых болевых кризах в стационарных условиях - наркотические анальгетики парентерально. При развитии инфекционных осложнений назначают антибиотики. Поддерживающая терапия - трансфузии отмытых или размороженных эритроцитов, а также антикоагулянтов. Анемия радикально неиз- лечима. Некоторые дети умирают от некротических осложнений или сепсиса.
Гемолитические анемии, связанные с внешними воздействиями
АУТОИММУННЫЕ ГЕМОЛИТИЧЕСКИЕ АНЕМИИ
Аутоиммунные гемолитические анемии - наиболее распространён- ный вариант этой группы анемий. Аутоиммунные гемолитические анемии развиваются в результате иммунного конфликта - образования АТ к изменённым поверхностным Аг собственных эритроцитов. Образовавшиеся комплексы «эритроцит-АТ» либо подвергаются агглютинации друг с другом при незначительном воздействии холода (внутрисосудистый гемолиз), либо поглощаются макрофагами селезёнки (внутриклеточный гемолиз).
Классификация
Классификация основана на различии аутоантител.
• Тепловые АТ (реагируют с эритроцитами при температуре тела не менее
• Холодовые АТ (реагируют с эритроцитами при температуре менее
•
Двухфазные гемолизины (фиксируются на эритроцитах при охлаждении
какого-либо участка тела и вызывают гемолиз при последующем повышении
температуры тела до
Распространённость аутоиммунной гемолитической анемии составляет 1:75 000-1:80 000, причём у 80% больных любого возраста она вызвана тепловыми АТ (агглютининами). У детей в 79% случаев они направлены против Rh-Аг. Реже наблюдают анемии с холодовыми АТ, чаще после вирусной инфекции у детей раннего возраста и пожилых людей. Аутоиммунная гемолитическая анемия может быть как идиопатической, так и симптоматической (при вирусных инфекциях, лимфопролиферативных заболеваниях, гистиоцитозах, приёме лекарственных препаратов).
Клиническая картина
Заболевание часто начинается с острого гемолитического криза при сочетании внутриклеточного и внутрисосудистого гемолиза. У больного внезапно повышается температура тела, появляются слабость, одышка, тахикардия, желтушность кожи и слизистых оболочек, ко- ричневое или бурое окрашивание мочи, увеличиваются печень и селезёнка. При постепенном начале заболевания возникают артралгии, боли в животе. В анализе крови выявляют нормоили гиперхромную анемию, анизоцитоз, небольшой ретикулоцитоз. Возможно развитие нормобластоза, сфероцитоза, тромбоцитопении, лейкоцитоза со сдвигом лейкоцитарной формулы влево. Увеличивается СОЭ. Проба Кумбса положительная (проба выявляет комплекс «эритроцит-АТ»).
Лечение
Основные принципы лечения: блокирование синтеза аутоантител (преднизолон, цитостатики, циклоспорин), ограничение доступа АТ к клеткам-мишеням (очищенный высокодозный Ig, преднизолон), сти- муляция регенерации клеток крови (фолиевая кислота). Применяют и оперативное лечение (спленэктомия). При необходимости проводят трансфузии отмытых эритроцитов.
МЕХАНИЧЕСКИЕ МИКРОАНГИОПАТИЧЕСКИЕ
ГЕМОЛИТИЧЕСКИЕ АНЕМИИ
Происхождение гемолитических анемий этих групп связано с травматической фрагментацией эритроцитов. Причинами механического разрушения могут быть следующие факторы.
• Стеноз или аневризма аорты.
• Сужения или обструкция мелких кровеносных сосудов (ДВС, гемолитико-уремический синдром, синдром Мошкович, системные васкулиты, заболевания почек и печени, стрептококковая пневмония).
• Повреждение клапанами сердца и крупных сосудов (протезы клапанов).
• Бег на большие дистанции, занятия контактными видами спорта и др. Основные причины фрагментации эритроцитов в мелких сосудах:
повреждение самих сосудов, образование тромбов и фибриновых нитей в кровотоке.
Клиническая картина
В клинической картине преобладают желтуха и геморрагический синдром. В анализе крови снижены концентрация Hb, содержание эритроцитов и тромбоцитов. Выражены анизоцитоз, пойкилоцитоз, микросфероцитоз, выявляют «шиповидные», «шлемовидные» клетки
и фрагменты эритроцитов. В биохимическом анализе крови - повышение ЛДГ, непрямого билирубина, возможно снижение сывороточного железа из-за потери его с мочой. В моче - гемосидеринурия, реже - гемоглобинурия. Прямая проба Кумбса отрицательна. Дифференциально-диагностический критерий - сочетание гемолитической анемии, фрагментации эритроцитов, лейкоцитоза и тромбоцитопении.
Лечение
Лечение механических гемолитических анемий включает лечение основного заболевания, а также плазмаферез, трансфузии больших доз свежезамороженной плазмы, в случае необходимости - эритроцитарной массы. Разрабатывают новые методы лечения с применением высоких доз внутривенно вводимого Ig (400 мг/кг/сут) и более] и ингибиторов апоптоза.
АНЕМИИ ПРИ ДРУГИХ ЗАБОЛЕВАНИЯХ
Анемии при других заболеваниях (хронических инфекционных, системных, онкологических и т.д.) - вторичные синдромы, рассмат- риваемые как приспособительные и характеризующиеся сниженной продукцией эритроцитов и нарушением реутилизации железа.
Клиническая картина связана с основным заболеванием; анемия не определяет самочувствие и состояние пациента. Обычно она появляется поздно, медленно развивается и не прогрессирует в даль- нейшем. В анализе крови умеренно снижена концентрация Hb, у 1/4 пациентов обнаруживают микроцитоз и гипохромию, особенно при тяжёлом течении основного заболевания. Другие изменения красной крови отсутствуют. Возможны лейкоцитоз и токсическая зернистость нейтрофилов. Снижены концентрация сывороточного железа и общая железосвязывающая способность сыворотки, умеренно повышена концентрация сывороточного ферритина. Концентрация эритропоэтина не соответствует степени анемии. Выявляют биохимические признаки активного воспалительного процесса (повышение С-реактивного белка, фибриногена, СОЭ). Анемия рефрактерна к лечению препаратами железа.
Основные принципы лечения: терапия основного заболевания; коррекция содержания эритропоэтина (назначают эпоэтин бета подкожно начиная с 20 ЕД/кг с постепенным увеличением дозы под контролем уровня гематокрита); восполнение (в случае крайней необходимости) Hb трансфузиями эритроцитарной массы.