Клиническая фармакология.: учебник для вузов / Под ред. В.Г. Кукеса.- 4-е издание., перераб. и доп., - 2009. - 1056 с.
|
|
|
|
ГЛАВА 27. ГОРМОНАЛЬНЫЕ ПРЕПАРАТЫ
27.1. САХАРОСНИЖАЮЩИЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА
Препараты инсулина
Большой выбор препаратов инсулина с различными фармакокинетическими характеристиками и пероральных сахароснижающих препаратов с разными механизмами действия позволяет проводить индивидуализированную коррекцию обменных процессов при любом типе сахарного диабета. При назначении препаратов учитывают степень компенсации углеводного и жирового обмена, наличие абсолютных и относительных противопоказаний к назначению отдельных групп сахароснижающих средств.
Молекула инсулина состоит из двух полипептидных цепей, включающих 51 аминокислотный остаток. А-цепь содержит 21 аминокислоту, В-цепь - 30 аминокислот. А и В цепи соединены двумя бисульфидными мостиками, третий бисульфидный мостик формирует третичную структуру цепи А. Инсулин - анаболический гормон, влияющий на ассимиляцию углеводов, белков.
Классификация
Различают четыре генерации инсулинов.
• К первой генерации относят препараты инсулина из свиной и говяжьей поджелудочной железы в произвольных соотношениях с содержанием неинсулиновых примесей до 20%.
• Вторую генерацию составляют препараты, содержащие примеси до 0,5% (монопиковые инсулины).
• К третьей генерации относят препараты, полностью очищенные от проинсулина, глюкагона, С-пептида, соматостатина, панкреатического полипептида (монокомпонентные инсулины).
• Инсулины четвёртой генерации получают при помощи генной инженерии.
Все инсулины подразделяют по длительности эффекта (табл. 27-1).
Таблица 27-1. Длительность действия препаратов инсулина
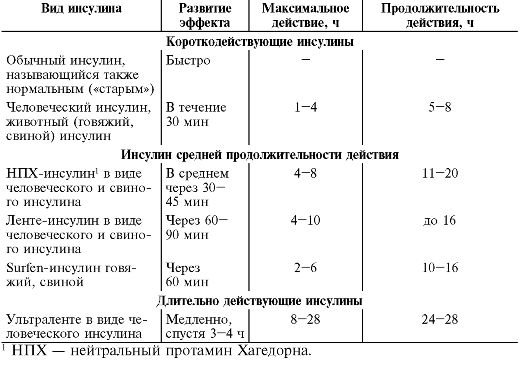 Механизм действия и основные фармакодинамические эффекты
Механизм действия и основные фармакодинамические эффекты
Инсулин стимулирует транспорт глюкозы через клеточные мембраны и активацию гексокиназы, благодаря чему глюкоза превращается в глюкозо-6-фосфат, активирует гликогенсинтетазу, в результате чего стимулируется синтез гликогена, подавляет действие гормонов гипофиза и активацию надпочечников. Под воздействием инсулина происходит также синтез белков и жирных кислот.
Инсулин метаболизируется почти во всех тканях организма, но большая его часть - в печени, почках, поджелудочной железе и плаценте. Наиболее важный фермент, разрушающий инсулин, - глютатион-инсулин-трансгидрогеназа. Период полураспада инсулина составляет около 5 мин.
Показания к применению
• Сахарный диабет 1-го типа (инсулинзависимый).
• Состояние прекомы или комы, осложнившее течение сахарного диабета (кетоацидотическая, лактатацидемическая, гиперосмолярная комы).
• Ювенильный сахарный диабет.
• Сахарный диабет 2-го типа (во время беременности и лактации, при неэффективности лечения пероральными сахароснижающими препаратами, интеркуррентных тяжёлых заболеваниях, операциях, наличии противопоказаний к приёму пероральных сахароснижающих препаратов).
Режим дозирования
Режим приёма препарата подбирают индивидуально с учётом суточного профиля гликемии и глюкозурии. Отимальную дозу и режим введения препаратов инсулина подбирают с целью не только компенсировать углеводный обмен, но и устранить другие нарушения метаболизма. Дозу инсулина необходимо корректировать при изменении режима питания и физической активности, инфекционных заболеваниях, хирургических операциях, выраженном нарушении функции почек, беременности и лактации.
Побочные эффекты
Анафилактический шок, гипогликемия, липодистрофии.
Гипогликемию необходимо немедленно купировать приёмом легко усвояемых углеводов. При развитии гипогликемической комы необходимо немедленно ввести 60-80 мл 40% раствора глюкозы. Для лечения липодистрофии в поражённую область вводят препараты свиного инсулина.
Взаимодействие
См. прил. 3 на компакт-диске.
Пероральные сахароснижающие препараты применяют для лечения инсулинонезависимого сахарного диабета, который не удаётся компенсировать диетическим питанием. Их подразделяют на несколько подгрупп:
• препараты сульфонилмочевины;
• бигуаниды;
• гликомодуляторы;
• препараты, уменьшающие резистентность тканей к инсулину;
• глиниды.
Препараты сульфонилмочевины
Механизм действия и основные фармакодинамические эффекты Препараты сульфонилмочевины:
• повышают чувствительность рецепторов тканей к инсулину;
• увеличивают инкрецию инсулина из β-клеток поджелудочной железы при повышении концентрации глюкозы крови;
• усиливают поглощение глюкозы клетками мышечной ткани и печени;
• тормозят липолиз в жировой ткани и глюконеогенез в печени;
• ингибируют инкрецию глюкагона.
Препараты сульфонилмочевины подразделяют на две генерации. К первой относят толбутамид , карбутамид*, толазамид*. Ко второй (препараты созданы после 1968 г.) - глибенкламид, гликвидон, хлорпропамид, глипизид, гликлазид. Препараты второй генерации обладают большей фармакодинамической активностью и меньшей токсичностью. Большинство из них обладают умеренным ангиопротективным действием (уменьшают агрегацию тромбоцитов и проницаемость сосудистой стенки) и снижают концентрацию холестерина в крови. Необходимо отметить, что развивающаяся у больных резистентность к препаратам первого и второго поколений перекрёстная.
Толбутамид, карбутамид и толазамид*9начинают действовать через 1-1,5 ч после приёма, а максимальный эффект развивается через 4-8 ч. Действуют эти препараты в течение 12 ч. Метаболизируются в печени на 80%, оставшиеся 20% в неизменённом виде экскретируются с мочой.
Хлорпропамид начинает действовать через 3 ч после приёма, а его эффект длится не менее 24 ч. Он обладает антидиуретическим действием. В связи с особенностями метаболизма и экскреции не следует назначать его больным ХПН.
Глипизид начинает снижать концентрацию глюкозы в крови через 10-15 мин, максимальный эффект развивается через 1,5-2 ч, что позволяет связать его приём с ритмом питания. Его назначают за 15- 20 мин до еды и имитируют тем самым физиологический ритм обратной связи (табл. 27-2).
Таблица 27-2. Характеристика сахароснижающих лекарственных средств - производных сульфонилмочевины
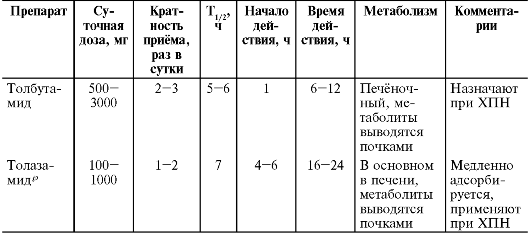 Окончание табл. 27-2
Окончание табл. 27-2
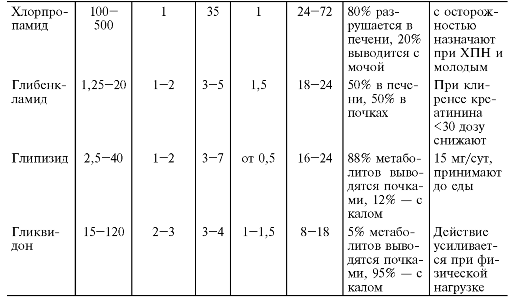 Фармакокинетика
Фармакокинетика
Препараты сульфонилмочевины хорошо абсорбируются из ЖКТ, основные различия фармакокинетических параметров определяются особенностями их элиминации. Толбутамид, карбутамид* и толазамид* полностью карбоксилируются в печени и выделяются с мочой в виде неактивных соединений. Хлорпропамид метаболизируется в печени на 80%, с мочой в неизменённом виде экскретируется 20% (табл. 27-3, 27-4).
Наиболее широко применяют глибенкламид, который обладает пролонгированным действием, в основном метаболизируется в печени и экскретируется с мочой в виде неактивных метаболитов. На его кумуляцию ХПН влияет незначительно.
До 95% метаболитов гликвидона (Т1/2 составляет 4-5 ч) выводится через ЖКТ и только 5% экскретируется почками. Это позволяет применять его у больных сахарным диабетом с почечной патологией и начальными стадиями нефро- и ангиопатии.
Таблица 27-3. Фармакокинетические параметры некоторых препаратов сульфонилмочевины
 Окончание табл. 27-3
Окончание табл. 27-3
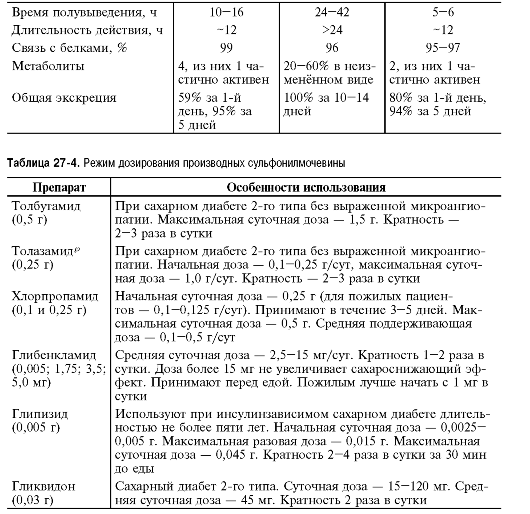 Показания к применению и режим дозировоания
Показания к применению и режим дозировоания
Препараты производных сульфонилмочевины назначают больным сахарным диабетом 2-го типа в том случае, если соблюдение строгой диеты не приводит к компенсации углеводного обмена. В ряде случаев эти препараты успешно применяют в комбинации с инсулином при обоих типах диабета. Учитывая длительность действия, производные сульфонилмочевины принимают от 1 до 3 раз в сутки за 30-60 мин до еды (см. табл. 27-4).
Больных, получавших инсулин, переводят на лечение препаратами производных сульфонилмочевины в тех случаях, когда инсулинопо-
требность не сильно превышает возможность β-клеток к его синтезу, а гликемии натощак менее 11 ммоль/л, а после еды не более 14 ммоль/л. Лечение начинают с максимальных доз, постепенно снижая их до поддерживающих состояние компенсации углеводного обмена. Устойчивого клинического эффекта достигают обычно к 5-7 дню, а иногда к 14 от начала приёма препаратов. Дозу начинают снижать с вечернего приёма.
Иногда развивается резистентность к производным сульфонилмочевины I и II поколения. Для профилактики резистентности необходимо периодически менять препараты либо на короткое время назначать инсулин. Считают, что временное назначение инсулина больным сахарным диабетом 2-го типа повышает специфичность связывания инсулина с тканевыми рецепторами, что приводит к усилению эффекта эндогенного инсулина. Это в свою очередь обусловливает восстановление чувствительности к производным сульфонилмочевины.
Режим дозирования и особенности применения производных сульфонилмочевины приведены в табл. 27-4.
Противопоказания к назначению
Абсолютные противопоказания к монотерапии производными сульфонилмочевины:
• сахарный диабет 1-го типа;
• тяжёлые формы сахарного диабета;
• состояние прекомы и комы;
• выраженные обменные нарушения со склонностью к кетоаци-
дозу;
• почечная и печёночная недостаточность;
• заболевания крови, сопровождающиеся лейкопенией, тромбоцитопенией;
• предоперационная подготовка;
• детский возраст;
• беременность.
Относительно противопоказаны производные сульфонилмочевины при интеркуррентных заболеваниях, поздних осложнениях сахарного диабета.
Побочные эффекты
• Гипогликемические состояния: при передозировке препарата, недостаточном содержании углеводов в пище, приёме алкоголя и лекарств, потенцирующих действие производных сульфонилмочевины (гипогликемическая кома при приёме препаратов производных сульфонилмочевины встречается крайне редко).
• Местные аллергические реакции: дерматит, крапивница, эксфолиативный дерматит (описаны единичные случаи).
• Диспептический синдром: анорексия, гиперсаливация, боли в животе, тошнота, рвота, диарея.
• Нарушение функции печени: холестатическая желтуха (после приёма толбутамида).
• Поражение костного мозга: агранулоцитоз (редко), лейкопении, нейтропении, тромбоцитопении.
• Нарушение синтеза гормонов и увеличение объёма щитовидной железы.
Во время лечения производными сульфонилмочевины необходимо ежемесячно исследовать кровь и мочу. Свойственный хлорпропамиду антидиуретический эффект может приводить к дилюционной гипонатриемии и водной интоксикации. При применении адекватных доз препаратов производных сульфонилмочевины побочные эффекты встречаются редко.
Взаимодействие
Усиливают сахароснижающий эффект производных сульфонилмочевины: салицилаты, фенилбутазон (бутадион*), противотуберкулёз- ные препараты, хлорамфеникол (левомицетин*), тетрациклиновые антибиотики, производные кумарина, циклофосфамид, ингибиторы МАО и β-адреноблокаторы. Ослабляют сахароснижающий эффект: пероральные контрацептивны, хлорпромазин (аминазин*), симпатомиметики, глюкокортикоиды, гормоны щитовидной железы, никотиновая кислота.
Сульфаниламиды увеличивают время циркуляции толбутамида в плазме крови, угнетая образование гидрокситолбутамида в печени. Доксициклин замедляет элиминацию метаболитов сульфонилмочевины. В свою очередь толбутамид может увеличивать содержание свободного билирубина крови и усиливать его миграцию из плазмы. Под действием препаратов производных сульфонилмочевины увеличивается концентрация свободной фракции антикоагулянтов, что при длительном неконтролируемом сочетанном приёме может привести к кровотечению. У некоторых больных, получающих препараты производных сульфонилмочевины, при приёме алкоголя может развиться антабус-алкогольная реакция.
Бигуаниды
Бигуаниды - производные гуанина. Их подразделяют на 2 подгруппы: диметилбигуаниды (метформин) и бутилбигуаниды (буформин* ).
Механизм действия и основные фармакодинамические эффекты
Бигуаниды усиливают поглощение глюкозы мышечными волокнами за счёт активации анаэробного гликолиза. Под влиянием бигуанидов возрастает продукция молочной и пировиноградной кислот и коэффициент лактат/пируват в крови. Эти метаболиты угнетают глюконеогенез, гликогенолиз в печени, замедляют всасывание глюкозы и других субстратов в тонком кишечнике. Бигуаниды подавляют липогенез, снижают концентрацию триглицеридов, ЛПНП, ЛПОНП в плазме крови, увеличивают содержание свободных жирных кислот и глицерина в крови, чем способствуют нормализации липидного обмена у больных диабетом. Умеренный анорексический эффект бигуанидов обусловливает снижение массы тела у больных с ожирением, а активация фибринолиза снижает риск тромбоэмболических осложнений у больных с диабетом. Бигуаниды эффективны только тогда, когда у больного синтезируется собственный инсулин.
Фармакокинетика
Фармакокинетические параметры бигуанидов представлены в табл.
27-5.
Таблица 27-5. Фармакокинетические параметры бигуанидов
 Показания к применению и режим дозирования
Показания к применению и режим дозирования
Монотерапию проводят только больным с лёгкой формой диабета. Больным сахарным диабетом 2-го типа, при среднетяжёлой форме его течения, или у больных с повышенной массой тела назначают комбинацию бигуанидов и препаратов сульфонилмочевины. В некоторых случаях при сахарном диабете 1-го типа бигуаниды применяют в комбинации с инсулином с целью уменьшения потребности в инсулине и предотвращения увеличения массы тела.
Широкое применение получили бигуаниды пролонгированного действия. Они эффективнее своих короткодействующих аналогов и реже вызывают развитие осложнений, среди них буформин-ретард* ,
силубин-ретард* , глюкофаж*-ретард (метформин) и его аналоги (производные буформина и метформина).
Следует помнить, что при сочетанном применении производных сульфонилмочевины и бигуанидов может повыситься содержание молочной и пировиноградной кислоты, аланина и кетоновых тел в крови, а также возрасти коэффициент лактат/пируват и концентрация β-оксимасляной кислоты, что будет способствовать развитию тяжёло- го нарушения обмена веществ. Недопустимо назначать эти препараты при нарушенной функции почек.
Бигуаниды принимают во время или после еды. Вследствие быстрого достижения максимальной концентрации в крови и достаточно короткого периода полувыведения средние суточные дозы препаратов целесообразно делить на 2-3 приёма. При подборе режима дозирования ориентируются на изменения гликемии и распределение углеводной нагрузки в течение суток.
Режим дозирования и особенности использования бигуанидов приведены в табл. 27-6.
Таблица 27-6. Режим дозирования и особенности использования бигуанидов
 Противопоказания к назначению
Противопоказания к назначению
• Повышенная чувствительность к препаратам.
• Гипоксия тканей.
• Нарушение функций печени и почек.
• Кахексия.
• Недостаточность кровообращения.
• Острые воспалительные заболевания.
• Диабетическая кома.
• Кетоацидоз и/или лактатацидоз.
• Беременность и лактация.
Нельзя назначать бигуаниды, если больной придерживается низкокалорийной (малоуглеводной) диеты. При включении в пищевой рацион фруктозы сильно возрастает вероятность развития лактатацидоза.
Пожилым пациентам назначать бигуаниды следует с осторожностью в дозе 50 мг/сут.
Препараты фенформина* запрещены к использованию в большинстве стран мира, в том числе и в России. При их использовании лактатацидотическая кома, в 50% случаев приводящая к смертельному исходу, развивается у 0,25-4 людей из 1000.
Побочные эффекты
• Лактатацидоз вследствие накопления молочной кислоты (активация анаэробного гликолиза).
• Диспептические расстройства: тошнота, рвота, анорексия, ощущение металлического вкуса во рту, диарея.
• Аллергические реакции: фотосенсибилизации (быстро проходит).
• Нарушения функций печени: повышение уровня щёлочной фосфатазы и холестаз, проходящие в течение 5-6 нед после отмены препаратов.
• Лейкопения, агранулоцитоз, тромбоцитопеническая пурпура (редко). Около 3% больных не переносят бигуаниды.
Взаимодействие
Особенности взаимодействия бигуанидов с другими препаратами представлено в прил. 3.
Гликомодуляторы
Ингибиторы α-гликозидазы, к которым относится акарбоза, замедляют переваривание и всасывание углеводов в кишечнике. Это ведёт к более равномерному поступлению углеводов в кровь после еды и уменьшению колебаний гликемии в течение дня, снижению показателей постпрандиальной гипергликемии.
Акарбоза практически не всасывается в ЖКТ, поэтому системные побочные эффекты встречаются редко. Могут быть дозозависимые диспептические расстройства (диарея, метеоризм).
Глиниды
К новому классу сахароснижающих препаратов относят глиниды - репаглинид, натеглинид, меглитинид*.
Механизм действия и основные фармакодинамические эффекты
Репаглинид - быстродействующий сахароснижающий препарат, стимулирующий высвобождение инсулина из β-клеток поджелудочной железы. Механизм действия заключается в активации специфических АТФ-зависимых калиевых каналов мембран β-клеток, что приводит к их деполяризации и открытию кальциевых каналов. Повышение концентрации ионов кальция в цитоплазму индуцирует секрецию инсулина β-клетками.
В исследованиях доказана эффективность репаглинида для снижения концентрации глюкозы в крови (натощак и после приёма пищи) и содержания гликозилированного HbA1c. Препарат эффективен как в качестве монотерапии, так и в комбинации со стандартной сахароснижающей терапией. В периоды между приёмами пищи концентрация инсулина не повышается.
Фармакокинетика
Препарат быстро всасывается из ЖКТ и инкреторный ответ развивается в течение 30 мин после приёма. В печени происходит биотрансформация, в результате которой образуются неактивные метаболиты, выводящиеся с мочой и жёлчью. Т1/2 около 1 ч.
Показания к применению
• Сахарный диабет 2-го типа.
Противопоказания к назначению
• Повышенная чувствительность к препарату.
• Сахарный диабет 1-го типа.
• Кетоацидоз.
• Выраженные нарушения функций печени, почек.
• Беременность и лактация.
Побочные эффекты
• Гипогликемия.
• Диспептические реакции: диарея, тошнота, рвота, запоры.
• Аллергические реакции.
Режим дозирования
Препарат начинают принимать по 0,5 мг перед едой, постепенно увеличивая дозу. Максимальная разовая доза - 4 мг, максимальная суточная доза - 16 мг.
Взаимодействие
Некоторые препараты способны усиливать или уменьшать сахароснижающий эффект репаглинида (см. табл. 27-6). Следует учитывать, что репаглинид метаболизируется в печени с участием цитохрома 3А4, поэтому препараты, ингибирующие (кетоконазол, эритромицин, флуконазол) или индуцирующие этот цитохром, могут влиять на концентрацию репаглинида в крови. Совместное применение этих препаратов нежелательно.
Глитазоны
Тиазолидиндионы (глитазоны) - новый класс препаратов, усиливающих действие инсулина в мышцах, печени и жировой ткани (уменьшают инсулинорезистентность тканей). К этому классу препаратов относят пиоглитазон , троглитазон*, розиглитазон*. Препараты этой группы использовали для снижения концентрации триглицеридов в крови, затем обнаружили, что они в большей степени снижают гликемию.
Механизм действия и основные фармакодинамические эффекты
Тиазолидиндионы связываются со специфическими рецепторами в ядре клетки, в результате чего активируется экспрессия некоторых генов, вовлечённых в липидный и углеводный метаболизм. Это приводит к уменьшению инсулинорезистентности тканей, повышению интенсивности захвата глюкозы клетками, снижению гликемии и концентрации циркулирующего инсулина. Известно, что при сахарном диабете 2-го типа осложнения, обусловленные развитием макроангиопатии, связаны не столько с концентрацией глюкозы в крови, сколько с инсулинорезистентностью тканей.
Внедрение этих препаратов в клиническую практику может улучшить отдаленной прогноз и снизить смертность пациентов с сахарным диабетом 2-го типа от характерных кардиоваскулярных осложнений. По результатам многоцентровых рандомизированных плацебоконтролируемых исследований (The Pioglitazone 001 Study Group), пиоглитазон эффективен как в качестве монотерапии, так и в комбинации со стандартными сахароснижающими препаратами сульфонилмочевины, метформином и инсулином. При добавлении пиоглитазона к схеме лечения пациентов с сахарным диабетом 2-го типа не только нормализуется гликемия, но и снижается концентрация гликозилированного HbA1c, а также и нормализуется липидный спектр крови.
Троглитазон*не применяют для лечения пациентов в связи с его гепатотоксичностью.
Побочные эффекты
Пиоглитазон характеризуется лучшей переносимостью и небольшим количеством побочных эффектов:
• изменение массы тела;
• отёки;
• снижение концентрации гемоглобина;
• повышение концентрации общего холестерина в крови.
Таким образом, глитазоны и глиниды могут стать альтернативными инсулину препаратами для пациентов, у которых применение метформина и препаратов производных сульфонилмочевины не поддерживает состояние компенсации углеводного обмена.
Обсуждают перспективы применения других химических соединений.
Мультифункциональный антиоксидант α-липоевая кислота в норме продуцируется в клетках организма в небольшом количестве и участвует в биохимических процессах как Ко-фермент. Её применяют при лечении диабетической нейропатии. Было показано, что при внутривенном введении (в отличие от перорального) уменьшается инсулинорезистентность тканей.
Проводят клинические испытания сульфата ванадия, также способного уменьшать инсулинорезистентность, снижать гликемию, гликозилированного гемоглобина, фруктозамина, общего холестерина и ЛПНП в плазме крови.
Исследуют влияние неорганического хрома на течение сахарного диабета. Препараты хрома в сочетании со стандартными ЛС улучшают показатели гликемии, снижают содержание фруктозамина и триглицеридов, что позволяет уменьшать дозу традиционных сахароснижающих препаратов.
Контроль эффективности и безопасности сахароснижающих лекарственных средств
Основные клинические показатели эффективности инсулинов: улучшение общего состояния больного, исчезновение или уменьшение жажды, сухости во рту, полиурии.
Обязательно проводят:
• исследования мочи - диурез, суточную глюкозурию, осадочные белковые пробы, определение клеточных тел мочи;
• исследования крови - гликемию натощак, рН, концентрацию остаточного азота и креатинина, протромбина, билирубина, холестерина, β-липопротеидов;
• гликемический и глюкозурический суточный профиль (6-8 исследований, в ходе которых каждые 3-4 ч определяют концентрацию глюкозы в крови и моче);
• электрокардиографию;
• исследование глазного дна;
• оценку неврологического статуса.
Дополнительные (факультативные) исследования проводят исходя из возможностей клинического учреждения. Их выполняют для расширенной оценки эффективности препарата. К ним относятся: определение концентрации кетоновых тел, неэтерифицированных жирных кислот, инсулина, глюкагона, соматотропного гормона, иммуноглобулинов, параметров агрегации тромбоцитов.
Для больных средней тяжести и тяжёлой формой заболевания критерием компенсации сахарного диабета считают уровень сахара в крови, не превышающий в течение суток 130-180 мг% (по Хагедорну-Йенсену) или 110-160 мг% (ортотолуидиновый метод) и снижение суточной глюкозурии, которая не должна превышать 5% сахарной ценности пищи.
Клиническую и параклиническую оценку эффективности пероральных сахароснижающих препаратов проводят аналогично препаратам инсулина.
Эффективность препаратов оценивают в течение 1-3 мес. При этом определяют максимально эффективные дозы препарата и поддерживающую дозировку, которая устанавливается после сохранения аглюкозурии и нормогликемии в течение двух недель.
Частота определения глюкозы крови у больных с диабетом 1-го типа не реже 3 раз в неделю в стационаре, не реже 1 раза в 2 нед в амбулаторных условиях. У больных с диабетом 2-го типа - не реже 1 раза в неделю в стационаре, не реже 1 раза в месяц в амбулаторных условиях.
Необходимо контролировать концентрацию калия, молочной и пировиноградной кислоты, соотношение лактат/пируват, кетоновых тел в крови и моче.
Один из наиболее надёжных тестов для определения степени компенсации углеводного обмена при сахарном диабете - определение концентрации HbA1c. Содержание HbA1c обратно пропорционально степени компенсации заболевания. Кроме того, о компенсации сахарного диабета можно судить по нарушению липидного обмена. Необходимо определить концентрацию холестерина, триглицеридов и липопротеидов низкой плотности. Нарушение этих показателей свидетельствует о недостаточной компенсации углеводного обмена при сахарном диабете.
Принципы выбора сахароснижающих препаратов
При сахарном диабете 1-го типа обязательно назначают препараты инсулина. Возможно присоединение к схеме лечения пероральных
сахароснижающих препаратов (чаще - производных сульфонилмочевины или бигуанидов) для снижения дозы инсулина, профилактики повышения массы тела.
При неадекватном контроле сахарном диабете 2-го типа с помощью диеты препаратами выбора считают производные сульфонилмочевины и бигуаниды. Их можно сочетать с репаглинидом, а также с инсулином.
Инсулин считают препаратом выбора в следующих случаях:
• состояние прекомы и комы;
• тяжёлые формы сахарного диабета;
• выраженные обменные нарушения со склонностью к кетоаци-
дозу;
• почечная и/или печёночная недостаточность;
• заболевания крови, сопровождающиеся лейкопенией, тромбоцитопенией;
• кахексия;
• недостаточность кровообращения;
• острые воспалительные заболевания;
• во время предоперационной подготовки;
• в период беременности и лактации;
• в детском возрасте.
27.2. ГЛЮКОКОРТИКОИДЫ
Глюкокортикоиды - группа препаратов структурных и функциональных аналогов гормонов, синтезируемых пучковой зоной коры надпочечников. В организме человека глюкокортикоиды синтезируются под контролем гипоталамо-гипофизарно-надпочечниковой системы. Выделение гипофизарного адренокортикотропного гормона происходит под влиянием стресса или при снижении концентрации циркулирующего в крови гидрокортизона1. Секреция глюкокортикоидов также подчиняется циркадным ритмам: её максимум приходится на утреннее время (6-8 ч) и снижается в вечернее и ночное.
Принято выделять природные глюкокортикоиды - кортизон2 и гидрокортизон (кортизол) и синтетические препараты - преднизолон, дексаметазон и др.
1 Гипоталамо-гипофизарно-надпочечниковая система также чувствительна к концентрации синтетических препаратов и может угнетаться при длительном сохранении высокой концентрации этих ЛС в крови.
2 Кортизон - пролекарство, а гидрокортизон - его активный метаболит.
27.2.1. Взаимосвязь между структурой и фармакодинамикой
Все глюкокортикоиды обладают сходной базовой структурой. Вместе с тем добавление к молекуле кортизола различных химических групп сопровождается существенным изменением свойств этих препаратов:
• преднизон (заменена гидроксильная группа на кетогруппу в 11' положении) - пролекарство (его активный метаболит образуется в процессе биотрансформации);
• преднизолон (введена двойная связь между атомами углерода в 1 ' и 2' положении) обладает в 4 раза большей глюкокортикоидной активностью по сравнению с кортизолом;
• метилпреднизолон (добавлена 6β-метильная группа) по своей глюкокортикоидной активности в 5 раз превосходит кортизол;
• флудрокортизон (добавлен атом фтора в 9α' положение) превосходит кортизол как по своей глюкокортикоидной активности (в 12 раз), так и по минералокортикоидной активности (в 125 раз). Этот препарат используется вместо альдостерона1 у пациентов с первичной надпочечниковой недостаточностью или гипоальдостеронизмом;
• дексаметазон (к молекуле 1δ-флудрокортизона добавлена метильная группа положение 16α'), в отличие от своего предшественника - 15-флудрокортизона, обладает незначительной минералокортикоидной активностью, но сохраняет высокую глюкокортикоидную активность;
• бетаметазон (структурно идентичен дексаметазону, за исключением метильной группы в положении 16β') используют для местного применения;
• триамцинолон (в молекуле дексаметазона заменена метильная группа на гидроксильную в положении 16α') по глюкокортикоидной активности аналогичен метилпреднизолону, но практически не вызывает задержки натрия в организме.
Механизм действия и основные фармакодинамические эффекты
Рецепторы к глюкокортикоидам присутствуют практически во всех видах клеток и располагаются внутриклеточно, где и происходит их активация. Активированный комплекс «гормон-рецептор» транслоцируется в ядро клетки и стимулирует образование информационной РНК, что обусловливает синтез целого ряда регуляторных белков. Не исключено, что специфические рецепторы к глюкокортикоидам могут располагаться на мембранах клеток (что было доказано для альдосте-
1 Получение альдостерон в качестве ЛС - технически очень сложная задача.
рона), однако важнейшие эффекты препаратов этой группы реализуются за счёт взаимодействия с ДНК.
Ряд медиаторов (катехоламины, медиаторы воспаления) способны инактивировать комплексы «гормон-рецептор», снижая тем самым активность глюкокортикоидов.
Основные эффекты глюкокортикоидов
• Иммунная система:
- противовоспалительное действие (преимущественно при аллергической и иммунной формах воспалительного процесса) опосредовано нарушением синтеза простагландинов, лейкотриенов и цитокинов, уменьшением проницаемости капилляров, снижением хемотаксиса иммунокомпетентных клеток и подавлением активности фибробластов;
- подавление клеточного иммунитета, реакции «хозяин против трансплантата», снижение активности Т-лимфоцитов, макрофагов, эозинофилов.
• Водно-электролитный обмен:
- задержка в организме натрия и воды (благодаря увеличению реабсорбции в дистальных отделах почечных канальцев), активное выведения калия (у препаратов с минералокортикоидной активностью);
- уменьшение всасывания кальция с пищей, уменьшение его содержания в костной ткани (остеопороз), усиление экскреции кальция с мочой.
• Обмен веществ:
- увеличение массы тела1;
- перераспределение жировой ткани (повышенное отложение жира в области лица, шеи, плечевого пояса; наряду с этим в конечностях преобладают процессы липолиза) - ожирение, типичное для синдрома Кушинга;
- стимуляция глюконеогенеза в печени, уменьшение проницаемости мембран для глюкозы, а у ряда больных - развитие стероидного диабета;
- угнетение анаболизма, стимуляция катоболических процессов в коже, костной ткани и мышцах (вплоть до развития мышечной дистрофии и поражений кожных покровов).
1 В отношении этого эффекта все ЛС можно расположить в следующем порядке: флудрокортизон > природные глюкокортикоиды > синтетические глюкокортикоиды > фторированные глюкокортикоиды.
• Сердечно-сосудистая система:
- повышение АД (стероидная гипертензия);
- задержка жидкости;
- увеличение числа и чувствительности адренергических рецепторов в сердце и сосудах, усиление прессорного эффекта ангио- тензина-II.
• Гипоталамо-гипофизарно-надпочечниковая система:
- угнетение гипоталамо-гипофизарно-надпочечниковой системы по механизму отрицательной обратной связи.
• Система крови:
- лимфоцитопения, моноцитопения и эозинопения;
- стимуляция пролиферации эритроцитов, увеличение числа нейтрофилов и тромбоцитов1.
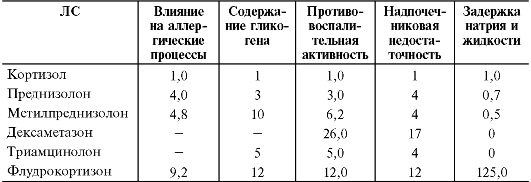
Таблица 27-7. Фармакодинамика различных глюкокортикоидов для системного применения
 Фармакокинетика
Фармакокинетика
Всасывание
Системные глюкокортикоиды плохо растворимы в воде (в крови циркулируют преимущественно в связанном с белками виде), хорошо растворимы в жирах и различных органических растворителях.
Инъекционные формы глюкокортикоидов представляют собой эфиры или соли этих препаратов - сукцинаты, гемисукцинаты и фосфаты. Это делает препарат растворимым в воде и обеспечивает быстрое начало действия при парентеральном применении. Существуют также мелкокристаллические суспензии глюкокортикоидов, действие которых начинается медленно, однако продолжительность действия может достигать 0,5-1,0 мес (депо-формы). Эти формы глюкокортикоидов применяют для внутрисуставных инъекций.
1 Изменения в клеточном составе крови проявляются уже спустя 6-12 ч после при- ёма глюкокортикоидов и сохраняются (при длительном применении этих препаратов) в течение нескольких недель.
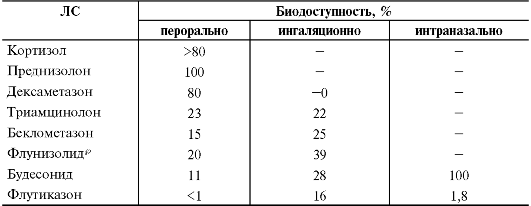
Глюкокортикоиды хорошо всасываются в ЖКТ. Максимальная концентрация в крови достигается через 0,5-1,5 ч после приёма препарата. На скорость всасывания может оказывать влияние одновременный приём пищи - при этом скорость всасывания уменьшается, но биодоступность не изменяется (табл. 27-8).
Таблица 27-8. Биодоступность глюкокортикоидов
 Распределение
Распределение
При концентрации кортизола в плазме крови 200 мкг/л практически 95% его связано с кортизолсвязывающим α-глобулином (КСГ, транскортин), в то время как активность свободного кортизола составляет всего 10 мкг/л. При увеличении концентрации кортизола >200 мкг/л происходит полное насыщение кортикостероидными гормонами. Все синтетические глюкокортикоиды по сравнению с гидрокортизоном меньше связываются с белками (60-70%) и практически полностью проникают в ткани, поэтому более эффективны в меньших дозах.
При снижении синтеза белка (цирроз печени) или большой его потере (нефротический синдром, спру, синдром мальабсорбции) развивается токсическое действие от обычных терапевтических доз глюкокортикоиды.
Метаболизм
Глюкокортикоиды метаболизируются в печени путём окисления, восстановления и конъюгации и выделяются с мочой в виде конъюгатов серной и глюкуроновой кислот. Кортизон и преднизон подвергаются пресистемному метаболизму с превращением их в активные формы - гидрокортизон и преднизолон, соответственно. Скорость и характер метаболизма глюкокортикоидов оценивают по экскреции нейтральных 17-глюкокортикоидов и 17-глюкокортикоидных гормонов. Синтетические глюкокортикоиды метаболизируются в печени так
же, как и гидрокортизон, однако это происходит медленнее. Фторированные глюкокортикоиды (триамцинолон, дексаметазон, бетаметазон) метаболизируются ещё медленнее.
Все системные ГК проникают через плаценту, где гидрокортизон и преднизолон превращаются в менее активные кортизон и преднизон. Дексаметазон и бетаметазон, проникнув через плаценту, создают высокие концентрации в крови плода и могут привести к подавлению у него функции гипоталамо-гипофизарно-надпочечниковой системы. В связи с этим беременным предпочтительнее назначать преднизолон, а не дексаметазон и бетаметазон.
Выведение
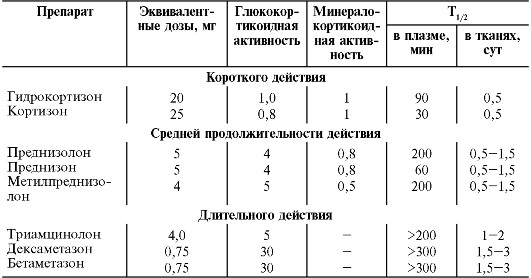
Глюкокортикоиды выделяются с мочой в виде конъюгатов серной и глюкуроновой кислот. Природные глюкокортикоиды имеют наиболее короткий Т1/2, фторированные препараты - наиболее длинный. Т1/2 в плазме крови варьирует от нескольких минут до 5 ч в отличие от длительности их Т1/2 глюкокортикоидной активности (ГКА). Системные ГК делят на короткодействующие, препараты средней длительности и длительного действия (табл. 27-9).
При почечной недостаточности величина Т1/2 не изменяется, а дозы ГК не требуют коррекции.
Таблица 27-9. Сравнительная активность глюкокортикоидов
 Побочные эффекты
Побочные эффекты
Частота побочных эффектов при приёме глюкокортикоидов возрастает с увеличением дозы и/или продолжительности лечения. Ис-
пользование альтернирующей терапии и местное (ингаляционное, накожное, внутрисуставное) введение позволяют уменьшить частоту развития нежелательных лекарственных реакций.
Наиболее часто встречающиеся побочные эффекты.
• Инфекционные осложнения (бактериальные, вирусные, грибковые, паразитарные).
• Туберкулёз1.
• Остеопороз - патологические переломы костей, компрессионные переломы позвонков, асептический некроз головки бедренной кости.
• Кровоизлияния, угри, атрофия кожи и подкожной клетчатки.
• Отёки.
• Артериальная гипертензия.
• Диабет.
• Задержка роста и полового созревания у детей.
• Неустойчивое настроение, психозы (при приёме высоких доз).
• Глаукома (с возможным экзофтальмом).
• Нарушения метаболизма - гипергликемия, гиперлипидемия, повышение аппетита, синдром Кушинга.
• Стероидные язвы желудка и кишечника, кровотечения из ЖКТ, эзофагит, панкреатит.
• Вторичная надпочечниковая недостаточность (при отмене ГК после их длительного применения2). Факторы риска развития осложнения:
- доза >2,5-5,0 мг/сут (в пересчёте на преднизолон);
- длительность лечения >10-14 дней;
- приём препарата в вечерние часы3;
- приём фторированных глюкокортикоидов.
Взаимодействие глюкокортикоидов
Эффективность ГК усиливается при одновременном назначении эритромицина (замедляет метаболизм глюкокортикоидов в печени), салицилатов (увеличивает не связанную с белками фракцию глюкокортикоидов), эстрогенов. Индукторы микросомальных ферментов печени (фенобарбитал, фенитоин, рифампицин) снижают эффективность этих ЛС.
1 Наличие у больного туберкулёза - одно из противопоказаний к лечению ГК.
2 Профилактика вторичной надпочечниковой недостаточности включает в себя при- мём препаратов только в утренние часы, использование альтернирующей терапии, постепенное снижение дозы при отмене ГК.
3 Опаснее назначать 5 мг преднизолона вечером, чем 20 мг утром.
Глюкокортикоиды ослабляют действие антикоагулянтов, сахароснижающих и антигипертензивных препаратов и усиливают действие теофиллина, симпатомиметиков, иммуносупрессантов, нестероидных противовоспалительных препаратов (прил. 3).
Показания к применению и режим дозирования
Показания к применению глюкокортикоидов:
• заместительная терапия при надпочечниковой недостаточности любой этиологии в физиологических дозах;
• супрессивная терапия при адреногенитальном синдроме;
• патогенетическая терапия, основанная на противовоспалительном, противоаллергическом, иммуносупрессивном и противошоковом действии этих препаратов.
Альтернирующая терапия заключается в назначении глюкокортикоидов через день в двойной суточной дозе, что обеспечивает снижения риска вторичной надпочечниковой недостаточности.
Интермиттирующая терапия - аналог альтернирующей, однако глюкокортикоиды в этом случае применяют короткими курсами в 3- 4 дня, с последующими 4-дневными интервалами между курсами. Эта схема имеет также преимущества перед непрерывным применением глюкокортикоидов.
Пульс-терапия - кратковременное назначение сверхвысоких доз глюкокортикоидов. Препарат выбора при проведении пульс-терапии - метилпреднизолон. Показаниями к проведению пульс-терапии служат тяжёлые и опасные для жизни заболевания - системные коллагенозы, васкулиты, тяжёлый ревматоидный артрит с висцеральными поражениями, рассеянный склероз.
При продолжительной терапии глюкокортикоидами возникает необходимость в снижении дозы до минимально эффективной, а при возможности - и в полной отмене глюкокортикоидов. Отмена глюкокортикоидов может потребоваться не только в результате положительной динамики патологического процесса, позволяющей обходиться без глюкокортикоидной терапии, но также при появлении тяжёлых побочных действий глюкокортикоидов, не позволяющих продолжать терапию.
Противопоказания к назначению
Относительные противопоказания:
• сахарный диабет (особенно опасны фторированные глюкокортикоиды);
• психические заболевания, эпилепсия;
• язвенная болезнь желудка и двенадцатиперстной кишки;
• выраженный остеопороз;
• тяжёлая артериальная гипертензия.
В неотложных ситуациях (например, при шоке) глюкокортикоиды вводят без учёта противопоказаний.
Местное применение глюкокортикоидов позволяет создать в патологическом очаге высокую концентрацию препарата и значительно снизить риск развития системных нежелательных реакций. Формы местного применения глюкокортикоидов:
• ингаляции;
• внутрисуставные и околосуставные инъекции;
• эпидуральное введение;
• внутриполостные инъекции (внутриперикардиально, внутриплеврально и др.);
• ректальные формы;
• формы для наружного применения (кожа, глаза, уши).
Глюкокортикоиды для интраназального применения
Механизм действия и основные фармакодинамические эффекты
Глюкокортикоиды для местного (интраназального) применения - наиболее активные противовоспалительные средства, применяемые при лечении аллергического ринита. Кроме противовоспалительного, они оказывают противоаллергическое и иммунодепрессивное действие. Увеличивают продукцию липомокортина (ингибитора фосфолипазы А), тормозят образование арахидоновой кислоты и последующий синтез продуктов её метаболизма - циклических эндоперекисей и простагландинов. Эти препараты уменьшают воспалительную экссудацию и продукцию лимфокинов, тормозят высвобождение из тучных клеток медиаторов воспаления, не проявляют минералокортикоидную активность.
Для этих препаратов свойственна высокая местная активность, которая у таких препаратов, как будесонид, флутиказон, мометазона в 100 и более раз превосходит дексаметазон (см. табл. 27-10). Глюкокортикоиды для интраназального применения эффективны в отношении всех симптомов ринита, кроме того, они снижают гиперреактивность слизистой носа, а у больных с полипами полости носа приводят к уменьшению размеров этих образований.
Фармакокинетика
При применении глюкокортикоидов в виде назальных спреев лишь очень незначительная часть препарата всасывается в системный кро-
воток (табл. 27-10). Таким образом, действие этих препаратов преимущественно местное.
Таблица 27-10. Сравнительная характеристика интраназальных спреев глюкокортикоидов
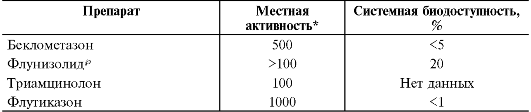 * За единицу принята местная активность дексаметазона.
* За единицу принята местная активность дексаметазона.
Побочные эффекты
Местные глюкокортикоиды способны вызывать повышенную сухость полости носа, реже при длительном приёме этих ЛС у больных может развиться кандидоз слизистых оболочек носоглотки. В качестве побочных эффектов были описаны кровотечения из носа. Благодаря низкой биодоступности этих препаратов риск воздействия на гипоталамо-гипофизарно-надпочечниковую систему при их применении минимален.
Для лечения аллергического ринита чаще всего применяют будесонид, флутиказон, флунизолид*, а также мометазон.
Местное применение глюкокортикоидов
Местные глюкокортикоиды лучше адсорбируются из воспалённых областей, чем со здоровых участков кожи. Кожа у детей лучше поглощает эти ЛС. Разные области кожи обладают различной способностью к адсорбции глюкокортикоидов: хуже всего эти препараты адсорбируются кожей подошв, ладоней и рук, а максимальная адсорбция наблюдается на коже лица и гениталий (табл. 27-11). Принятие ванны или использование других способов увлажнения кожи перед нанесением глюкокортикоидов значительно увеличивает их эффективность.
Таблица 27-11. Особенности всасывания глюкокортикоидов при их местном применении
 Механизм действия и основные фармакодинамические эффекты
Механизм действия и основные фармакодинамические эффекты
Противовоспалительная активность глюкокортикоидов для местного применения оценивается по степени сужения сосудов кожи (тест побледнения кожи). Местные глюкокортикоиды делят на 7 групп в зависимости от их эффективности (табл. 27-12).
Таблица 27-12. Относительная эффективность некоторых глюкокортикоидов для местного применения
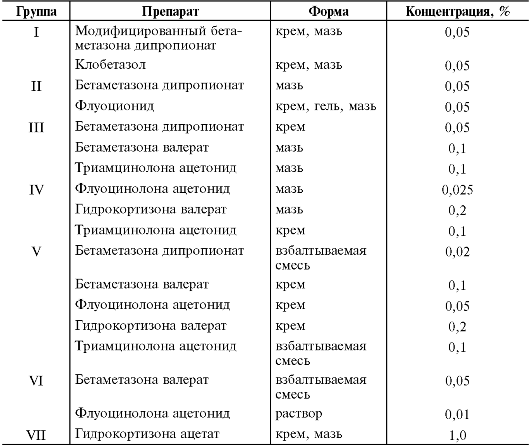 Наиболее
активные лекарственные препараты относятся к первой группе - они
приблизительно в 1000 раз более эффективны, чем 1% раствор
гидрокортизона. Препараты этой группы применяют только при тяжёлых
дерматозах - псориазе, атопическом дерматите, контактном дерматите (но
не области лица и гениталий, где их высокая адсорбция может вызвать
системные побочные эффекты и местные изменения в виде атрофии кожных
покровов). Они особенно эффективны при терапии заболеваний ладоней и
стоп, так как степень адсорбции глюкокортикоидов в этих областях низкая.
Наиболее
активные лекарственные препараты относятся к первой группе - они
приблизительно в 1000 раз более эффективны, чем 1% раствор
гидрокортизона. Препараты этой группы применяют только при тяжёлых
дерматозах - псориазе, атопическом дерматите, контактном дерматите (но
не области лица и гениталий, где их высокая адсорбция может вызвать
системные побочные эффекты и местные изменения в виде атрофии кожных
покровов). Они особенно эффективны при терапии заболеваний ладоней и
стоп, так как степень адсорбции глюкокортикоидов в этих областях низкая.
Препараты с высокой активностью (II-III группы) используют при умеренно выраженных дерматозах, но не в области лица и гениталий. Дерматозы в области век и половых органов требуют лечения глюкокортикоидами с промежуточной активностью (IV-V группы). При лечении больших областей кожи следует применять средства II-IV групп из-за риска системных побочных эффектов.
Продолжительность лечения препаратами I группы не должна превышать 3 нед, а препаратами с промежуточной активностью (IV- V группы) - не более 3 мес.
Побочные эффекты
Препараты с максимальной активностью (I группа) уже через 3 дня после начала применения могут вызвать атрофию кожи, а при их назначении в суточной дозе 2 г уже через 2 нед отмечается угнетение функции надпочечников. В целом для глюкокортикоидов при местном их применении характерно развитие инфекционных заболеваний кожи, угревой сыпи. Ряд препаратов могут вызывать аллергические реакции.
Тахифилаксия - прогрессивное уменьшение клинической эффективности местных глюкокортикоидов при их многократном назначении из-за развития толерантности клеток кожи к их фармакологическому действию. Особенно часто тахифилаксию отмечают при местном применении глюкокортикоидов. Поэтому при длительном назначении этих ЛС рекомендуют планировать перерывы или попеременно назначать альтернативные препараты с другим механизмом действия.