Клиническая фармакология.: учебник для вузов / Под ред. В.Г. Кукеса.- 4-е издание., перераб. и доп., - 2009. - 1056 с.
|
|
|
|
ГЛАВА 20. ЛЕКАРСТВЕННЫЕ СРЕДСТВА, ПРИМЕНЯЕМЫЕ ПРИ ЗАБОЛЕВАНИЯХ ОРГАНОВ ПИЩЕВАРЕНИЯ
20.1. СРЕДСТВА, СНИЖАЮЩИЕ АКТИВНОСТЬ КИСЛОТНО-ПЕПТИЧЕСКОГО ФАКТОРА
В развитии и рецидивировании заболеваний, связанных с повреждением слизистых оболочек желудка и двенадцатиперстной кишки, доказана роль факторов (кислотно-пептического, инфекционного (Helicobacter pylori), моторных нарушений), на которые можно влиять с помощью лекарственных препаратов. В 1910 году было сформулировано положение «без кислоты нет язвы», и это старое правило Шварца не потеряло актуальности по настоящее время. Однако агрессивность желудочного сока физиологична, и нормальная слизистая оболочка желудка и двенадцатиперстной кишки резистентна к его воздействию. Соляная кислота обеспечивает активацию пепсиногена, создает необходимый для функционирования желудочных протеаз уровень pH, способствует набуханию белковых коллоидов пищи, участвует в регуляции секреции и моторики желудка, жёлчного пузыря, обладает бактерицидными свойствами. Гиперсекрецию соляной кислоты рассматривают как основной патофизиологический механизм повреждения слизистой оболочки, а процесс обратной диффузии ионов водорода называют ключевым в снижении ее резистентности. К агрессивным факторам также относят пепсин, жёлчные кислоты, ускорение опорожнения желудка.
Элементом слизистой оболочки, ответственным за секрецию соляной кислоты, является париетальная (обкладочная) клетка. На её апикальной мембране находится фермент, способствующий обмену находящихся в цитоплазме протонов на ионы калия (K+) с выделением первых в окружающую среду. Этот так называемый протонный насос функционирует с участием цАМФ, ионов кальция (Ca2+) и при наличии ионов калия, локализующихся в просвете секреторных канальцев. Активация фермента начинается с реакции рецепторов (находящихся на базальной мембране) на специфические хемостимуляторы и трансмембранной передачи сигнала Н+/К+-АТФазе (протонному насосу). Доказано существование трех клинически значимых типов рецепторов: ацетилхолиновых, гистаминовых и гастриновых.
Париетальная клетка содержит Н2-гистаминовые рецепторы, м3- мускариновые рецепторы и гастриновые рецепторы. Рецептор для гастрина относят к типу В-рецепторов для холецистокинина. В результате активации париетальных клеток под действием как гастрина, так и ацетилхолина могут происходить увеличение внутриклеточной концентрации Ca2+ и фосфорилирование белков-мишеней под действием протеинкиназы С. Гистамин, связываясь с Н2-гистаминовым рецептором клетки через G-белки, активизирует аденилатциклазу, в результате чего повышается содержание внутриклеточного цАМФ. После этого происходит возрастание внутриклеточной концентрации Ca2+ (входят в клетку через плазматическую мембрану).
Сигнал с Н2-гистаминового рецептора передается через цАМФ-зависимые пути. Холинергические и гастринергические влияния осуществляются через Са2+-зависимые процессы (система фосфатидилинози- тол-инозитолтрифосфатдиацилглицерол). Конечное звено этих процессов - протонный насос, обладающий К+, Н+-АТФазной активностью и способствующий выведению ионов водорода в просвет желудка.
Благодаря клиническим исследованиям установлено, что между заживлением язвы и способностью лекарственных препаратов подавлять кислотность существует прямая зависимость. Именно поэтому при заболеваниях, в патогенезе которых повышение желудочной секреции соляной кислоты является пусковым механизмом повреждения слизистой оболочки, управление кислотопродукцией - важнейшая задача лекарственной терапии.
«Эволюция» лекарственных средств, уменьшающих влияние кислотно-пептического фактора, происходила от создания антацидных препаратов, блокаторов м-холино- и Н2-гистаминовых рецепторов к появлению ингибиторов протонного насоса, результатом чего стало повышение эффективности, селективности, а следовательно, и безопасности применяемой фармакотерапии.
Антацидные средства
Механизм действия и основные фармакодинамические эффекты
Антациды - лекарственные средства, уменьшающие содержание уже выделившейся соляной кислоты в желудке (anti - против, acidum - кислота). По выражению Б.Е. Вотчала, «щелочи подметают желудок».
Требования, предъявляемые к антацидам:
• максимально быстрое взаимодействие с находящейся в просвете желудка соляной кислотой для купирования боли, изжоги, дискомфорта, ликвидации спазма привратника, нормализации мото-
рики желудка и прекращения кислотного «выброса» в начальные отделы двенадцатиперстной кишки;
• способность нейтрализовать значительное количество соляной кислоты желудочного сока, т.е. иметь большую кислотную (буферную) ёмкость;
• способность поддерживать состояние среды желудка на уровне рН 4-5 (при этом концентрация Н+ снижается на 2-3 порядка, что достаточно для подавления протеолитической активности желудочного сока);
• безопасность;
• экономическая доступность;
• хорошие органолептические свойства.
Классификация
Антацидные препараты разделяют на:
• системные и несистемные (местного действия). Первые способны увеличивать щёлочность плазмы крови, вторые не влияют на кислотно-основное состояние;
• анионные (натрия гидрокарбонат, кальция карбонат) и катионные (гели гидроксидов алюминия и магния);
• нейтрализующие и нейтрализующе-обволакивающе-адсорбирующие [алюминия гидроксид*, трисиликат магния, альмагель*, алюминия фосфат (фосфалюгель*) и др.].
Системные антацидные средства (натрия гидрокарбонат, натрия цитрат), быстро вступая в реакцию с соляной кислотой желудка, нейтрализуют её и тем самым способствуют снижению пептической активности желудочного сока, устранению прямого раздражающего действия на слизистую оболочку желудка и двенадцатиперстной кишки.
Несистемные антацидные средства. К ним относятся: магния оксид, магния гидроксид, магния карбонат, трисиликат магния, алюминия гидроксид*, алюминия фосфат (фосфалюгель*), редко - кальция карбонат осаждённый*, кальция карбонат, кальция фосфат, висмута карбонат и др.
Препараты этой группы не растворимы в воде и мало адсорбируются. В процессе нейтрализации желудочного сока образуются хлористоводородные соли, которые, реагируя с карбонатом кишечного сока и сока поджелудочной железы, образуют гидроксид или карбонат исходной соли. Таким образом, организм не теряет ни катионов (Н+), ни анионов (НСО3-) и не происходит изменения кислотно-основного состояния.
Свойства Al-содержащих антацидов:
• антипептическая способность;
• вяжущие свойства, образуют защитное покрытие;
• усиливают синтез простагландинов;
• адсорбируют жёлчные кислоты, пепсин, лизолецитин, токсины, газы, бактерии;
• ослабляют моторику;
• повышают тонус нижнего пищеводного сфинктера. Свойства Mg-содержащих антацидов:
• антипептическая способность;
• вяжущие свойства, образуют защитное покрытие;
• предупреждают высвобождения пепсина;
• усиливают слизеобразование;
• усиливают моторику;
• усиливают резистентность слизистой оболочки желудка.
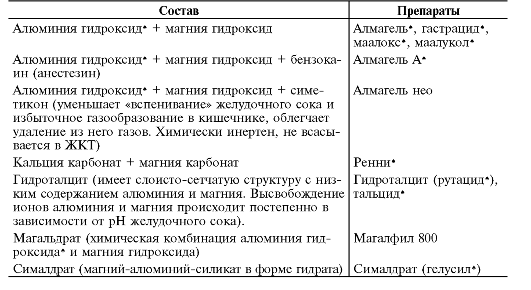
Некоторые препараты содержат и алюминия гидроксид (Al), и магния гидроксид (Mg). Гидроксид Mg и гидроксид Al способны образовывать на повреждённой ткани защитную пленку, усиливая защитные возможности слизистой оболочки гастродуоденальной зоны, способствуют качественному улучшению процессов рубцевания. Соли Al вызывают констипацию, а соли Mg обладают небольшим слабительным эффектом. Гидроксид Mg обеспечивает быстрое начало, а гидроксид Al - длительное действие. Гидроксид Mg предупреждает высвобождение пепсина, а гидроксид Al адсорбирует пепсин, жёлчные соли, изолецитин, оказывает цитопротекторное действие за счёт повышения секреции простгландинов (PgE2), увеличивает тонус нижнего эзофагеального сфинктера. Состав несистемных антацидов представлен в табл. 20-1.
Таблица 20-1. Несистемные антациды комбинированного состава
 Показания к применению и режим дозирования Показания к применению антацидов:
Показания к применению и режим дозирования Показания к применению антацидов:
• осенне-весенняя профилактика язвенной болезни желудка и двенадцатиперстной кишки;
• лечение больных с язвенной болезнью, гастроэзофагеальным рефлюксом, пептическими язвами пищевода, неязвенной диспепсией, гастритами с повышенной секрецией, дуоденитами, симптоматическими пептическими язвами желудка или двенадцатиперстной кишки;
• дискомфорт и боли в эпигастрии, изжога, кислая отрыжка после погрешностей в диете, избыточного употребления алкоголя, при- ёма лекарственных средств;
• профилактика желудочно-кишечных кровотечений при длительном лечении НПВС, глюкокортикоидами и некоторыми другими препаратами;
• устранение синдромов гипертонуса привратника при резком повышении объема желудочной секреции;
• профилактика «стрессовых» язв при интенсивной терапии;
• функциональная диарея. Режим дозирования
Эффективность антацидных препаратов оценивают по количеству миллиэквивалентов соляной кислоты, нейтрализуемых так называемой стандартной дозой. Обычно это 1 г твердой и 5 мл жидкой лекарственной формы - количество, способное поддерживать рН содержимого желудка на уровне 3,5-5,0 на протяжении 15-30 мин. Назначают антациды не менее шести раз в сутки. При лечении больных гастритами или язвенной болезнью антациды целесообразно назначать через 1-1,5 ч после приёма пищи. При гастроэзофагеальном рефлюксе, диафрагмальной грыже приём препаратов осуществляют сразу после еды и на ночь. Продолжительность применения антацидов не должна превышать 2 нед (см. ниже).
Побочное действие и противопоказания
Всасывающиеся антациды интенсивно связывают соляную кислоту, однако их действие непродолжительно, возможен феномен «кислотного рикошета». Они быстро всасываются из кишечника и при частом применении приводят к развитию некомпенсированного метаболического алкалоза. Изменение кислотно-основного состояния обусловливается также и особенностями взаимодействия с пищеварительными соками: при назначении натрия бикарбоната* нейтрализация соляной кислоты происходит с образованием натрия хлорида, избыток которого, поступая в системное кровообращение, способствует развитию
алкалоза. Особенно быстро алкалоз наступает при нарушении выделительной функции почек. Вследствие алкалоза возникает гипокалиемия. Экскреция натрия бикарбоната* приводит к ощелачиванию мочи, что может способствовать развитию фосфатного нефролитиаза. Натрийсодержащие препараты у больных со склонностью к сердечной или почечной недостаточности могут вызывать отёки. Избыточный приём антацидов и кальция, поступающего с пищей, может привести к состоянию, называемому «молочно-щелочным синдромом», что проявляется сочетанием гиперкальциемии и почечной недостаточности с признаками алкалоза. В острой форме этот синдром развивается уже через неделю после лечения растворимыми антацидными препаратами и проявляется ощущением слабости, тошнотой, рвотой, головной болью, психическими нарушениями, полиурией, увеличением содержания в сыворотке крови кальция, креатинина. В настоящее время натрия гидрокарбонат стал применяться реже, преимущественно для быстрого купирования изжоги и болей в животе.
Наиболее серьезные побочные эффекты алюминийсодержащих антацидов могут возникнуть при их длительном приёме или при применении высоких доз. Препараты этой группы образуют в тонкой кишке нерастворимый фосфат алюминия, таким образом, нарушается абсорбция фосфатов. Гипофосфатемия проявляется недомоганием, мышечной слабостью, при значительном дефиците фосфатов может возникать остеомаляция и остеопороз. Незначительное количество алюминия все-таки попадает в кровь, и при длительном применении алюминий поражает костную ткань, нарушая минерализацию, токсически действуя на остеобласты, нарушая функцию паращитовидных желёз. Также алюминий угнетает синтез активного метаболита витамина D3 - 1,25-дигидрооксихолекальциферола. Кроме того, может возникать целый ряд серьёзных, вплоть до летального исхода, побочных эффектов: поражение костной ткани и мозга, нефропатии.
Препараты кальция и алюминия способствуют задержке стула. Избыток препаратов магния может вызвать понос. При назначении кальция карбоната 10% его всасывается, что иногда приводит к гиперкальциемии. Это, в свою очередь, снижает продукцию паратгормона, задерживает экскрецию фосфора, и возникает угроза кальцинации тканей, нефролитиаза и почечной недостаточности.
Кремний в составе трисиликата магния может экскретироваться с мочой, что способствует образованию камней в почках.
Невсасывающиеся антациды противопоказаны при выраженном нарушении функции почек, а также при повышенной чувствительности к компонентам препарата, беременности, грудном вскармливании (можно применять фосфалюгель*), болезни Альцгеймера. С осторож-
ностью препараты нужно применять пожилым людям и детям (применение некоторых антацидов противопоказано детям до 10 лет).
Взаимодействие
Нейтрализуя соляную кислоту, антациды ускоряют эвакуацию желудочного содержимого вместе с другими ЛС. Скорость всасывания ЛС слабых оснований (аминазин*, анаприлин*, триметоприма) возрастает, так как увеличивается рН желудочного сока. В то же время адсорбция сульфаниламидов, барбитуратов (слабые кислоты) замедляется. При одновременном приёме снижается абсорбция из ЖКТ дигоксина, индометацина и других НПВС, салицилатов, хлорпромазина, фенитоина, блокаторов гистаминовых Н2-рецепторов, бета-адреноблокаторов, изониазида, антибиотиков тетрациклинового ряда, фторхинолонов, азитромицина, рифампицина, кетоконазола, пеницилламина, непрямых антикоагулянтов, барбитуратов, дипиридамола, жёлчных кислот (хенодезоксихолевой и урсодезоксихолевой), препаратов железа и лития, хинидина, мексилетина, препаратов, содержащих фосфор. При одновременном приёме с препаратами, имеющими кишечнорастворимую лекарственную форму, изменение pH желудочного сока (более щелочная реакция) может привести к ускоренному разрушению оболочки и вызвать раздражение слизистой оболочки желудка и двенадцатиперстной кишки. При совместном применении м-холиноблокаторы, замедляя опорожнение желудка, усиливают и удлиняют действие невсасывающихся антацидов. Ощелачивание мочи может приводить к изменению эффективности противомикробного действия антибиотиков в мочевом тракте.
М-холиноблокаторы
К м-холиноблокаторам, используемым при заболеваниях органов пищеварения, относят следующие группы препаратов:
• препараты красавки (белладонны): белладонны настойка, белладонны экстракт; действующие агенты - гиосциамин, скополамин и др.;
• комбинированные препараты красавки: бекарбон*, белластезин*, беллалгин*;
• препараты природных и синтетических соединений с холиноблокирующими свойствами: атропин, платифиллин, гиосциамин, гиосцина бутилбромид (бускопан*), метацин*, пирензепин (гастроцепин*).
Механизм действия и основные фармакодинамические эффекты
М-холиноблокаторы воздействуют на мускариновые рецепторы органов и тканей в области окончаний парасимпатических нервных волокон. Результаты блокады:
• снижение секреции пищеварительных и бронхиальных желёз;
• торможение моторной активности пищевода, желудка и кишечника;
• снижение тонуса бронхов, мочевого пузыря;
• улучшение атриовентрикулярной проводимости;
• тахикардия;
• расширение зрачков;
• спазм аккомодации.
На фоне приёма антихолинергических лекарственных средств снижается тонус и уменьшается сила сокращений гладкой мускулатуры всех полых органов. Они снижают базальную и ночную секрецию желудочного сока, в меньшей степени секрецию, стимулированную пищей. Снижая объем и общую кислотность желудочного сока, они уменьшают количество муцина, снижают возможность травматизации слизистой оболочки желудка и двенадцатиперстной кишки. Воздействие на моторику и уровень секреции желудка не всегда параллельно; последняя блокируется лишь в том случае, когда преобладает влияние холинергической реакции в регуляции секреции желудочного сока.
Передозировка м-холиноблокаторов характеризуется возбуждением, галлюцинациями, судорогами, параличом дыхания. Расширяется зрачок (мидриаз), за счёт пареза круговых мышц радужки и реснитчатого тела происходит паралич аккомодации, повышается внутриглазное давление. В токсических дозах они блокируют н-холинорецепторы в вегетативных ганглиях и скелетной мускулатуре. Из-за угнетения сосудодвигательного центра и симпатических ганглиев присоединяется гипотензия.
Атропин снижает секрецию слюнных желёз, уменьшает секрецию муцина и протеолитических ферментов железами желудка и тонкого кишечника. В меньшей степени тормозит продукцию соляной кислоты в желудке.
Платифиллин по своему действию близок к атропину, но его эффективность ниже.
Хлорозил* по своим фармакологическим свойствам также сходен с атропином, является периферическим холиноблокатором.
Метацин* считают четвертичным азотистым соединением. Почти не проникает через гематоэнцефалический и гематоофтальмический барьеры, обладает преимущественно периферическим действием. В меньшей степени, чем атропин, учащает сердцебиение.
Пирензепин преимущественно блокирует внутрижелудочную кислотопродукцию. Пирензепин - представитель подгруппы специфических блокаторов м1-холинорецепторов. Он избирательно угнетает секрецию соляной кислоты и пепсиногена и лишь незначительно блоки-
рует м-холинорецепторы слюнных желёз, сердца, гладких мышц глаза и других органов. По химической структуре пирензепин сходен с трициклическими антидепрессантами и в большей степени имеет сродство к м1-холинорецепторам, расположенным в нервных сплетениях желудка, а не на самих обкладочных клетках и в гладких мышцах. Именно поэтому эффект препарата преимущественно антисекреторный, но не спазмолитический. Пирензепин подавляет базальную и стимулированную выработку пепсина, но не влияет на секрецию гастрина и ряда других гастроинтестинальных пептидов (соматостатина, нейротензина, секретина). Доказано наличие у пирензепина цитопротекторных свойств. Пирензепин на 50% снижает базальную секрецию желудка при приёме внутрь и на 80-90% - при внутривенном введении.
Показания и режим дозирования
Атропиноподобные препараты для лечения язвенной болезни желудка и двенадцатиперстной кишки применяют редко из-за незначительного влияния на кислотопродукцию и большого количества системных эффектов. Их применяют, например, при выраженном болевом синдроме, при наличии пилороспазма.
Показания к применению пирензепина:
• лечение и профилактика язвенной болезни желудка и двенадцатиперстной кишки (в качестве вспомогательного средства);
• хронический гастрит с повышенной секреторной функцией желудка, эрозивный эзофагит, рефлюкс-эзофагит, синдром Золлин- гера-Эллисона;
• эрозивно-язвенные поражения ЖКТ, возникающие на фоне терапии противоревматическими и противовоспалительными средствами.
Пирензепин назначают взрослым внутрь в первые 2-3 дня - по 50 мг 3 раза в сутки за 30 мин до еды, затем по 50 мг 2 раза в сутки. Курс лечения - 4-6 нед. При необходимости - вводят в/м или в/в по 5-10 мг 2-3 раза в сутки. Возможно сочетанное применение внутрь и парентерально. Максимальная доза при приеме внутрь - 200 мг/сут.
Фармакокинетика
После приёма внутрь пирензепин плохо абсорбируется из ЖКТ. Биодоступность составляет 20-30%, при одновременном приёме с пищей - 10-20%. Максимальная концентрация 50 пг/мл достигается через 2 ч. T1/2 составляет 10-12 ч. Средний период полуэлиминации составляет 11 ч. Около 10% выводится в неизменённом виде с мочой, остальная часть - с калом. Очень небольшое количество пирензепина подвергается метаболизму. Связывание с белками плазмы - 10-12%.
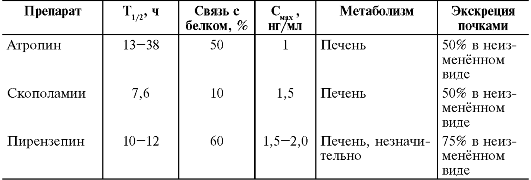
Плохо проникает через ГЭБ. Сравнительная фармакокинетика основных м-холиноблокаторов приведена в табл. 20-2.
Таблица 20-2. Фармакокинетика м-холиноблокаторов
 Побочные эффекты и противопоказания к назначению
Побочные эффекты и противопоказания к назначению
При применении м-холиноблокаторов отмечается ощущение сухости во рту, мидриаз, тахикардия, нарушение аккомодации, нарушение мочеотделения, атония желудка и кишечника. При назначении препаратов в субмаксимальных дозах возможно развитие двигательных и психических расстройств. Противопоказания к назначению м-холиноблокаторов: глаукома, доброкачественная гиперплазия предстательной железы. Переносимость пирензепина, как правило, хорошая, нежелательные реакции бывают слабовыраженными и не требуют отмены препарата. Препарат обычно не вызывает повышения внутриглазного давления, расстройств мочеиспускания и нежелательных явлений со стороны сердечно-сосудистой системы. Однако больным с глаукомой, нарушениями ритма, аденомой предстательной железы пирензепин назначают с осторожностью. Абсолютные противопоказанияе к применению м-холиноблокаторов - гиперплазия предстательной железы, паралитическая непроходимость кишечника, токсический мегаколон, неспецифический язвенный колит, стеноз привратника, I триместр беременности; повышенная чувствительность к пирензепину. Нежелательно применение атропиноподобных препаратов при недостаточности кардии, грыже пищеводного отверстия диафрагмы и рефлюксэзофагите, встречаемых в качестве сопутствующей патологии.
Взаимодействие
При одновременном применении с антихолинергическими средствами возможно усиление антихолинергических эффектов. При одновременном применении с опиоидными анальгетиками повышается риск возникновения тяжёлого запора или задержки мочи.
При одновременном применении возможно уменьшение действия метоклопрамида на двигательную активность ЖКТ.
Одновременное применение пирензепина и блокаторов Н2-гистаминовых рецепторов приводит к потенцированию их антисекреторных эффектов. Пирензепин уменьшает стимулирующее влияние алкоголя и кофеина на желудочную секрецию.
Блокаторы Н2-гистаминовых рецепторов (Н2-гистаминоблокаторы)
К блокаторам Н2-гистаминорецепторов относятся циметидин, ранитидин (зантак*, ацилок*, ранисан*), фамотидин (гастросидин*, ква- мател*, ульфамид*, фамосан*), низатидин, роксатидин.
Механизм действия и основные фармакологические эффекты
Общим в механизме действия этих препаратов является конкурентное ингибирование действия гистамина на Н2-гистаминовые рецепторы мембраны париетальной клетки.
Н2-гистаминоблокаторы - специфические антагонисты Н2-гистаминовых рецепторов. В соответствии с закономерностями конкурентного антагонизма Н2-гистаминоблокаторы угнетают секреторные реакции париетальных клеток в зависимости от дозы. При их приёме подавляется базальная кислотная продукция, ночная секреция, секреция соляной кислоты, стимулированная пентагастрином, агонистами Н2-гистаминовых рецепторов, кофеином, инсулином, ложным кормлением, растяжением дна желудка. В больших дозах Н2-гистаминоблокаторы подавляют секрецию практически полностью. При повторном приёме эффект, как правило, воспроизводится и выраженной толерантности не обнаруживается. В то же время выявлены категории больных язвенной болезнью с рефрактерностью к терапии Н2-гистаминоблокаторами.
Курсовое применение этих препаратов может приводить к повышенному образованию простагландина Е2 в слизистой оболочке желудка и двенадцатиперстной кишки, посредством которого реализуется цитопротективный эффект. При применении Н2-гистаминоблокаторов продукция пепсина понижается на 30-90%, но секреция бикарбоната и слизи мало изменяется. Эти препараты улучшают микроциркуляцию в слизистой облочке. Доказано, что Н2-гистаминоблокаторы тормозят дегрануляцию тучных клеток, снижают содержание гистамина в периульцерозной зоне и увеличивают количество ДНК-синтезирующих эпителиальных клеток, стимулируя тем самым репаративные процессы.
Классификация
• Среди Н2-гистаминоблокаторов различают препараты: I поколения - циметидин;
• II поколения - ранитидин;
• III поколения - фамотидин;
• IV поколения - низатидин;
• V поколения - роксатидин.
Общий принцип химического строения Н2-гистаминоблокаторов одинаков, однако конкретные соединения отличаются от гистамина «утяжелённой» ароматической частью или изменением алифатических радикалов. Циметидин содержит в качестве основы молекулы имидазольный гетероцикл. Другие вещества относятся к производным фурана (ранитидин), тиазола (фамотидин, низатидин) или более сложным циклическим комплексам (роксатидин).
Основные различия между Н2-блокаторами:
• по селективности действия, то есть по способности взаимодействовать с гистаминовыми рецепторами только 2-го типа и не влиять на рецепторы 1-го типа;
• по активности, то есть по степени ингибирования кислотной продукции;
• по липофильности, то есть по способности растворяться в жирах и проникать через клеточные мембраны в ткани. Это, в свою очередь, определяет системность действия и влияние препаратов на другие органы;
• по переносимости и частоте побочных эффектов;
• по взаимодействию с системой цитохрома Р-450, от чего зависит скорость метаболизма других лекарственных препаратов в печени;
• по наличию синдрома отмены.
Циметидин относится к I поколению блокаторов Н2-рецепторов гистамина париетальных клеток слизистой оболочки желудка. Подавляет продукцию соляной кислоты как базальную, так и стимулированную пищей, гистамином, гастрином, и в меньшей степени ацетилхолином. Снижает активность пепсина. Угнетает микросомальные ферменты печени. Продолжительность антисекреторного эффекта циметидина составляет 6-8 ч. Концентрация гастрина в сыворотке крови при этом существенно не меняется. Наряду с выраженной способностью тормозить желудочное кислотовыделение, циметидин вызывает угнетение моторной активности желудка, уменьшение ритмического компонента двигательной активности, снижение амплитуды сокращения антрального отдела, а также замедление пассажа желудочного содержимого. В организме циметидин связывается не только с Н2-гистаминовыми рецепторами желудка, так как имеет дополнительные места связывания с другими тканевыми рецепторами, причём у некоторых больных эти взаимодействия могут привести к клинически важным побочным
реакциям. При использовании в высоких дозах циметидин может оказывать влияние на Н1-рецепторы.
Ранитидин, благодаря уникальной структуре, селективно связывается с Н2-гистаминовыми рецепторами желудка. Ранитидин обладает более продолжительным антисекреторным эффектом: уменьшает как объем выделившегося желудочного сока, так и концентрацию в нем ионов водорода. Ранитидин в 4-10 раз активнее циметидина. У больных с пептической язвой ранитидин достоверно снижает суточную интрагастральную кислотность и, особенно, ночную секрецию кислоты, тем самым купирует боли и способствует быстрому заживлению язв. При прекращении приема ранитидина и циметидина возможно развитие синдрома отмены.
Фамотидин по сравнению с ранитидином обладает большей селективностью и продолжительностью действия, он в 40 раз активнее циметидина и в 8-10 раз активнее ранитидина, не вызывает синдрома отмены. Практически не взаимодействует с системой цитохрома Р-450, не влияет на метаболизм других лекарственных средств, не снижает активности алкогольдегидрогеназы в печени. Фамотидин не обладает антиандрогенным действием, не вызывает импотенцию; не повышает уровень пролактина, не вызывает гинекомастию. Частота побочных эффектов не более 0,8%.
Ранитидин, фамотидин и последующие поколения препаратов обладают большей селективностью. Различия эффективности Н2-гистаминоблокаторов определяются дозами препаратов, необходимыми для развития антисекреторного эффекта. Кроме того, сила связывания с рецепторами определяет длительность действия. Препарат, сильно связывающийся с рецептором, медленно диссоциирует, следовательно, оказывает более продолжительную блокаду кислотообразования. Исследования показали, что эффективное снижение базальной секреции поддерживается после приема циметидина в течение 2-5 ч, ранитидина - 7-8 ч, фамотидина - 10-12 ч. Все Н2-блокаторы относятся к гидрофильным лекарственным веществам. Циметидин наименее гидрофильный и умеренно липофильный препарат, поэтому он способен проникать в разные органы и ткани, воздействуя на локализованные в них Н2-гистаминовые рецепторы. Это определяет наличие максимального количества побочных эффектов среди препаратов данной фармакологической группы. Ранитидин и фамотидин высокогидрофильны, плохо проникают в ткани, оказывают преимущественное действие на Н2-гистаминовые рецепторы париетальных клеток.
Низатидин и роксатидин еще не нашли широкого применения в клинической практике, преимущества их применения по сравнению с предыдущими поколениями препаратов изучены недостаточно.
Фармакокинетика
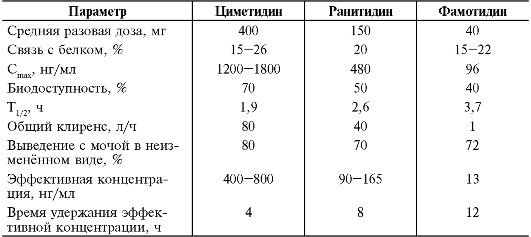
Основные фармакокинетические параметры блокаторов Н2-гистаминорецепторов представлены в табл. 20-3.
Таблица 20-3. Фармакокинетические параметры Н2-гистаминоблокаторов
 При приёме внутрь Н2-гистаминоблокаторы
обладают сравнительно высокой биодоступностью, величина которой у
некоторых из них достигает 90%. Наибольшая биодоступность отмечается у
циметидина, наименьшая - у фамотидина. Связь с белками крови данных ЛС
не превышает 26%. Необходимо отметить, что при курсовой монотерапии
остаточная концентрация циметидина утром, после вечернего приема
практически не определяется, а у ранитидина составляет 300 нг/мл.
При приёме внутрь Н2-гистаминоблокаторы
обладают сравнительно высокой биодоступностью, величина которой у
некоторых из них достигает 90%. Наибольшая биодоступность отмечается у
циметидина, наименьшая - у фамотидина. Связь с белками крови данных ЛС
не превышает 26%. Необходимо отметить, что при курсовой монотерапии
остаточная концентрация циметидина утром, после вечернего приема
практически не определяется, а у ранитидина составляет 300 нг/мл.
Н2-гистаминоблокаторы подвергаются частичной биотрансформации в печени. В значительном количестве (50-60%), особенно при внутривенном введении, выводятся в неизменённом виде почками. Период полувыведения колеблется от 1,9 до 3,7 ч. Прием циметидина после еды изменяет его фармакокинетику, приводя к формированию двугорбой кривой концентрация-время (изменение портального кровотока, заполнение рецепторов слизистой оболочки ингредиентами пищи, а также уклонение работы поглотительно-выделительных структур гепатоцита).
Таким образом, Н2-гистаминоблокаторы характеризуются смешанным (почечным и печёночным) клиренсом. У пациентов с почечной недостаточностью и при нарушении функции печени, а также у пожилых людей клиренс Н2-гистаминоблокаторов снижается. В первичную мочу препарат попадает не только с фильтратом, но и благодаря механизму активной канальцевой секреции. Н2-гистаминоблокаторы способны проникать через гематоэнцефалический барьер.
Необходимо учитывать, что при длительном назначении ЛС этой группы происходит постоянное поддержание высокой активности гистидиндекарбоксилазы, что приводит к накоплению гистамина в слизистой оболочке и усилению репаративных процессов в начале лечения. Это обусловливает трофические положительные эффекты гистамина. При накоплении чрезмерного количества гистамина начинают развиваться дистрофические процессы с образованием эрозий. В случае быстрой отмены Н2-гистаминоблокаторов нередко развивается синдром отмены («рикошета»).
У кормящих женщин Н2-гистаминоблокаторы могут обнаруживаться в грудном молоке в количествах, достаточных для фармакологического воздействия на ребенка.
Циметидин блокирует микросомальное окисление, подавляя активность изоферментов цитохрома Р-450 CYP1A2, CYP2C9, CYP2C19, CYP2D6, CYP3A4, что может привести к нарушению биотрансформации эндогенных и экзогенных веществ, метаболизирующихся путём микросомального окисления. Ранитидин и представители последующих поколений Н2-гистаминоблокаторов меньше влияют на изоферменты цитохрома Р-450, однако известно, что ранитидин является ингибитором CYP2D6, CYP3A4. Фамотидин и представители последующих поколений Н2-гистаминоблокаторов практически не влияют на систему цитохрома Р-450.
Показания к применению и режим дозирования
Н2-гистаминоблокаторы применяют при таких кислотозависимых заболеваниях как хронический гастрит, дуоденит, язвенная болезнь желудка и двенадцатиперстной кишки, синдром Золлингера-Эллисо- на, симптоматические язвы, развившиеся на фоне обширных ожогов, сочетанных травм, сепсиса, нарушения мозгового кровообращения, почечной недостаточности и т.д. Н2-Гистаминоблокаторы показаны при стероидных язвах желудка и двенадцатиперстной кишки, рефлюкс-эзофагите, анастомозитах.
При язвенной болезни все Н2-гистаминоблокаторы в соответствующих дозах терапевтически эквивалентны, они обеспечивают исчезновение боли у большинства больных в течение 1-10 сут, а эндоскопически подтверждаемое заживление наблюдается через 4 нед в 60-80% и через 6 нед в 80-92% случаев, что считается адекватным при данном заболевании. При крупных язвах на фоне применения аспирина или других нестероидных противовоспалительных средств, а также у курящих больных, лечебный процесс удлиняется. Профилактически Н2-гистаминоблокаторы применяются 1-2 раза в сутки в весеннеосенний период в среднетерапевтических дозах.
Н2-гистаминоблокаторы применяют для профилактики синдрома Мендельсона. Синдром Мендельсона (кислотно-аспирационный синдром) - гиперергическая реакция на аспирацию в дыхательные пути кислого желудочного содержимого вследствие рвоты или пассивного вытеснения содержимого желудка в ротоглотку при коматозном состоянии больного, наркозе, при угнетении гортанно-глоточных рефлексов любой этиологии.
Циметидин для лечения обострений язвенной болезни двенадцатиперстной кишки назначают по 200-400 мг 3 раза в течение дня (во время еды) и 400-800 мг на ночь. Возможно назначение в дозе 800 мг в 1 приём (перед сном), а также по 400 мг 2 раза в сутки. Максимальная суточная доза - 2,0 г. Продолжительность курса лечения - 4- 6 нед. Для профилактики обострений назначают по 400 мг на ночь. Средняя продолжительность курса лечения при язве, связанной с при- ёмом НПВС - 8 нед. Дозы те же. При рефлюкс-эзофагите назначают по 400 мг 4 раза в сутки во время еды и на ночь. Курс лечения - 4-8 нед. При синдроме Золлингера-Эллисона - по 400 мг 4 раза в сутки, при необходимости дозу можно увеличить. В целях профилактики кровотечений и при лечении эрозивно-язвенных повреждений верхних отделов ЖКТ, вызванных стрессом, циметидин назначают парентерально, при стабилизации состояния больного переходят на приём внутрь в суточной дозе до 2,4 г (по 200-400 мг каждые 4-6 ч). При подготовке к оперативному вмешательству назначается 400 мг за 90-120 мин до начала общей анестезии. При нарушении функции почек доза циметидина должна быть снижена. При клиренсе креатинина 30-50 мл/мин - до 800 мг/сут, 15-30 мл/мин - до 600 мг/сут, менее 15 мл/мин - до 400 мг/сут.
Рекомендованная доза ранитидина при обострении язвы двенадцатиперстной кишки или доброкачественной язвы желудка составляет 300 мг (делят на два приёма по 150 мг утром и вечером или принимают один раз в сутки). Лечение продолжают до рубцевания язвы или, если повторное обследование провести невозможно, в течение 4-8 нед. В большинстве случаев дуоденальные и желудочные язвы заживают через 4 нед. В отдельных случаях может потребоваться продолжать лечение до 8 нед. При лечении язвенной болезни не рекомендуют резкую отмену препарата (особенно до рубцевания язвы), обычно рекомендуют переход на поддерживающую дозу 150 мг на ночь. При лечении неязвенной диспепсии и гастритов возможен более короткий курс. Во многих странах ранитидин 75 мг продаётся в качестве препарата безрецептурного отпуска для применения при неязвенной диспепсии по 75 мг 4 раза в день. При рефлюкс-эзофагите рекомендованная доза составляет 150 мг 2 раза в сутки в течение 8 нед, при
необходимости до 150 мг 4 раза в сутки. Кроме того, улучшению состояния способствует приподнимание головного конца постели и лечение метоклопрамидом. Для профилактики рецидивов язвенной болезни рекомендуется принимать 150 мг один раз в сутки, перед отходом ко сну. При состояниях с патологической гиперсекрецией, например, синдроме Золлингера-Эллисона, рекомендованная доза ранитидина составляет 600-900 мг в сутки в несколько приемов. В тяжёлых случаях применялись дозы до 6 г в сутки, которые хорошо переносились больными. Рекомендуемые для Helicobacter pylori схемы с применением ранитидина - см. в разделе, посвящённом ингибиторам протонного насоса. Обычная доза для профилактики рецидивирующих желудочно-кишечных кровотечений у больных язвенной болезнью равна 150 мг два раза в сутки. Хирургическим больным с риском аспирации желудочного содержимого назначают 300 мг ранитидина внутрь вечером накануне операции.
Фамотидин при язвенной болезни желудка и двенадцатиперстной кишки в стадии обострения назначают по 20 мг 2 раза в сутки (утром и вечером) или 40 мг 1 раз в сутки на ночь. При необходимости суточная доза может быть увеличена до 80-160 мг. Курс лечения 4-8 нед. С целью профилактики рецидивов - по 20 мг 1 раз в сутки перед сном. При рефлюкс-эзофагите - 20-40 мг 2 раза в день в течение 6- 12 нед. При синдроме Золлингера-Эллисона дозу препарата и продолжительность курса лечения устанавливают индивидуально, начальная доза обычно составляет 20 мг каждые 6 ч. При общей анестезии для профилактики аспирации желудочного сока - внутрь по 40 мг вечером накануне операции и/или утром перед операцией в/в струйно или капельно (применяется при невозможности приёма внутрь). Обычная доза - по 20 мг 2 раза в сутки (каждые 12 ч). При наличии синдрома Золлингера-Эллисона начальная доза составляет 20 мг каждые 6 ч. В дальнейшем доза зависит от уровня секреции соляной кислоты и клинического состояния больного. При почечной недостаточности, если клиренс креатинина составляет <30 мл/мин или креатинин сыворотки крови >3 мг/100 мл, суточную дозу препарата необходимо уменьшить до 20 мг или увеличить интервал между приёмами до 36-48 ч.
Побочные эффекты и противопоказания
Соотношение токсической и терапевтической доз для всех Н2-гистаминоблокаторов очень высоко. Разные препараты этой группы вызывают побочные эффекты с разной частотой. При применении циметидина она составляет 3,2%, ранитидина - 2,7%, фамотидина - 1,3%. Могут отмечаться головная боль, чувство усталости, сонливости, тревога, тошнота, рвота, боль в животе, метеоризм, нарушения акта де-
фекации, миалгии, аллергические реакции. Острый панкреатит, гепатоцеллюлярные, холестатические или смешанные гепатиты с желтухой или без нее, гипоплазия костного мозга, серьёзные поражения ЦНС (результат проникновения препаратов через гематоэнцефалический барьер), включая спутанность сознания, обратимые нарушения остроты зрения, головокружение, возбуждение, галлюцинации, гиперкинезы, депрессия, отмечались, хотя и крайне редко, но при использовании всех антагонистов Н2-гистаминовых рецепторов.
Нейротропные неблагоприятные реакции чаще возникают у пожилых людей и при нарушениях функции печени и почек, а также при нарушении целостности гематоэнцефалического барьера. Описаны изменения со стороны крови (тромбоцитопения, лейкопения, нейтропения, апластическая и иммунная гемолитическая анемия) и умеренное обратимое повышение активности печёночных ферментов, уровня креатинина в сыворотке крови. Распространённость этих реакций невелика.
Н2-гистаминоблокаторы могут вызывать обратимые, связанные с идиосинкразией, гематологические побочные эффекты. Они возникают обычно в первые 30 дней лечения, носят обратимый характер и чаще всего проявляются тромбоцитопенией и гранулоцитопенией. Описаны случаи алопеции, повышения креатинина в крови, брадикардии и гипотонии, кишечной непроходимости, психических расстройств, поражений нервно-мышечного аппарата, парестезий. Подобные реакции на фоне применения ранитидина, фамотидина встречаются, в основном, при применении высоких доз препаратов, например, при синдроме Золлингера-Эллисона.
Нарушения деятельности эндокринной системы обусловлены способностью Н2-гистаминоблокаторов вытеснять из связи с рецепторами эндогенный тестостерон, а также лекарственные препараты, содержащие этот гормон, приводя к расстройствам половой сферы (импотенция, гинекомастия). Фамотидин вызывает эти эффекты реже, чем циметидин и ранитидин. Они (эффекты) дозозависимы, возникают на фоне длительного применения препаратов, обратимы (исчезают при отмене препарата или замене его на другой).
Фамотидин оказывает побочное действие преимущественно на желудочно-кишечный тракт: развиваются или диарея, или (реже) запор. Диарея - результат антисекреторного действия. Уменьшение продукции соляной кислоты повышает рН в желудке, что препятствует превращению пепсиногена в пепсин, участвующий в расщеплении белков пищи. Кроме того, уменьшение продукции желудочного сока, а также блокада Н2-гистаминовых рецепторов поджелудочной железы становятся причиной снижения выделения пищеварительных ферментов
поджелудочной железой и жёлчи. Все это приводит к нарушению процесса пищеварения и развитию диареи. Однако частота этих осложнений невелика (для фамотидина - 0,03-0,40%) и обычно не требует прекращения лечения. Подобные эффекты свойственны всем Н2-гистаминоблокаторам. Они дозозависимы и их можно ослабить, снизив дозы препарата.
Н2-блокаторы могут нарушать функцию сердечно-сосудистой системы, блокируя Н2-гистаминовые рецепторы миокарда, сосудистой стенки. У страдающих сердечно-сосудистыми заболеваниями и пожилых больных они способны вызывать аритмии, усиливать сердечную недостаточность, провоцировать коронароспазм. Гипотензия иногда наблюдается при внутривенном введении циметидина.
Гепатотоксичность Н2-гистаминоблокаторов, проявляемая гипертрансаминаземией, гепатитом, нарушением активности цитохрома Р-450, связана с метаболизмом этих препаратов в печени. Это наиболее характерно для циметидина. Н2-гистаминоблокаторы пациентам с нарушениями функции печени назначают с осторожностью и в уменьшенных дозах.
При применении фамотидина в связи с его незначительным метаболизмом частота подобных осложнений минимальна.
Н2-гистаминоблокаторы могут ухудшать течение бронхообструктивных заболеваний, приводя к бронхоспазму (действие на Н1-гистаминовые рецепторы). Побочный эффект, свойственный Н2-гистаминоблокаторам (в основном, циметидину и ранитидину), - развитие синдрома отмены. Именно поэтому рекомендуется дозы снижать постепенно.
Противопоказания к назначению Н2-гистаминоблокаторов: беременность, лактация, детский возраст (до 14 лет), выраженные нарушения функции печени и почек, нарушения сердечного ритма. Препараты следует с осторожностью принимать пожилым людям.
Взаимодействие
При назначении с другими ЛС необходимо учитывать, что циметидин и, значительно реже, ранитидин ингибируют активность изоферментов цитохрома Р-450 CYP1A2, CYP2C9, CYP2D6, CYP3A4, что может привести к повышению концентрации в плазме крови совместно применяемых ЛС-субстратов данных изоферментов, например, теофиллина, эритромицина, этмозина*, непрямых антикоагулянтов, фенитоина, карбамазепина, метронидазола. Циметидин также может подавлять метаболизм трициклических антидепрессантов, бензодиазепинов, β-блокаторов, блокаторов кальциевых каналов, амиодарона, лидокаина. При одновременном применении с хинидином концентра-
ция хинидина в плазме крови повышается, возникает риск усиления побочных эффектов; с хинином - возможно уменьшение выведения хинина и увеличение его T1/2, имеется риск усиления побочных эффектов.
Ранитидин тоже связывается с энзимами системы, но с более низкой аффинностью, поэтому его влияние на метаболизм лекарственных средств незначительно. Фамотидин, низатидин, роксатидин вообще не обладают способностью связываться с системой цитохрома и подавлять метаболизм других препаратов.
Благодаря возможному снижению скорости печёночного кровотока на 15-40%, особенно при внутривенном применении циметидина и ранитидина, может уменьшаться пресистемный метаболизм препаратов с высоким клиренсом. Фамотидин не изменяет скорости портального кровотока.
По аналогии с антацидами антагонисты Н2-гистаминовых рецепторов путем повышения рН в желудке могут влиять на биодоступность некоторых лекарственных средств. Установлено, что стандартные дозы циметидина и ранитидина повышают абсорбцию нифедипина, усиливая его антигипертензивное действие. Ранитидин также уменьшает всасывание итраконазола и кетоконазола.
При одновременном применении с дигоксином возможно как повышение, так и снижение концентрации дигоксина в плазме крови. При одновременном применении с карведилолом увеличивается AUC карведилола без изменения его Cmax в плазме крови. При одновременном применении с лоратадином повышается концентрация лоратадина в плазме крови, усиления побочных эффектов не отмечено. Курение снижает эффективность ранитидина.
Циметидин уменьшает инактивацию панкреатических ферментов в кишечнике. Напротив, одновременное применение Н2-гистаминоблокаторов снижает биодоступность итраконазола и кетоконазола.
Антациды, сукральфат замедляют абсорбцию ранитидина, фамотидина, в связи с чем при одновременном использовании перерыв между приёмом антацидов и ранитидина должен быть не менее 1-2 ч.
Лекарственные средства, угнетающие кроветворение в костном мозге, при одновременном с фамотидином применении увеличивают риск развития нейтропении.
Н2-гистаминоблокаторы - слабые основания, экскретируются активной секрецией в канальцах почек. Может происходить взаимодействие с другими лекарственными препаратами, экскреция которых осуществляется такими же механизмами. Так, циметидин и ранитидин снижают почечную экскрецию зидовудина, хинидина, новокаинами-
да*. Фамотидин не изменяет выведение этих препаратов, возможно, вследствие использования других транспортных систем. Кроме того, средние терапевтические дозы фамотидина обеспечивают низкие концентрации в плазме крови, которые не могут значимо конкурировать с другими препаратами на уровне канальцевой секреции.
Фармакодинамические взаимодействия Н2-гистаминоблокаторов с другими антисекреторными препаратами (например, холиноблокаторами) могут усиливать терапевтическую эффективность. Комбинация Н2-гистаминоблокаторов с препаратами, воздействующими на хеликобактер (препаратами висмута, метронидазолом, тетрациклином, амоксициллином, кларитромицином), ускоряет заживление пептических язв.
При одновременном применении с фентанилом возможно усиление эффектов фентанила; с флекаинидом - повышается концентрация флекаинида в плазме крови вследствие уменьшения его почечного клиренса и метаболизма в печени под влиянием циметидина.
Неблагоприятное фармакодинамическое взаимодействие наблюдается с препаратами, содержащими тестостерон. Циметидин вытесняет гормон из связи с рецепторами и на 20% увеличивает его концентрацию в плазме крови. Ранитидин и фамотидин не оказывают такого действия.
При приёме с флувастатином возможно повышение абсорбции флувастатина; с фторурацилом - повышается концентрация фторурацила в плазме крови на 75%, усиливаются побочные эффекты фторурацила; с хлорамфениколом - описаны случаи развития тяжёлой апластической анемии; с хлорпромазином - как уменьшение, так и повышение концентрации хлорпромазина в плазме крови. При одновременном применении с циклоспорином нельзя исключить повышение концентрации циклоспорина в плазме крови. При одновременном применении повышается концентрация в плазме крови пефлоксацина (при приёме внутрь).
При одновременном применении с пероральными гипогликемическими средствами, производными сульфонилмочевины в редких случаях наблюдалась гипогликемия.
Ингибиторы протонного насоса
Механизм действия и основные фармакодинамические эффекты
Ингибиторы Н+/К+-АТФазы - производные бензимидазола. Препараты в щелочной нейтральной среде фармакологически неактивны (пролекарства), представляют собой липофильные слабые основания, плохо растворимые в воде. В кислой среде они неустойчивы, поэто-
му коммерческие лекарственные формы представляют собой кишечнорастворимые таблетки или гранулы в желатиновых капсулах (чем выше рН среды, тем больше процент высвобождения вещества из гранул или таблеток). Препараты всасываются в тонкой кишке. Будучи слабыми основаниями, ингибиторы протонного насоса легко проникают из плазмы в кислую среду секреторного канальца, где образуют сульфеновую кислоту и катионный сульфенамид тетрациклической структуры, который ковалентно взаимодействует с SH-группами на внеклеточном, люминальном домене Н+/К+-АТФазы. При связывании двух молекул ингибитора с одной молекулой энзима образуется практически необратимый блок, так как катионный сульфенамид плохо диссоциирует от рецептора (табл. 20-4). Восстановление активности молекулярной помпы обусловлено, в основном, её синтезом de novo.
Таблица 20-4. Антисекреторный эффект ингибиторов протонного насоса после 5 дней лечения (по Scholtz H.E. и др., 1995)
Препарат | Средние значения интрагастрального рН | Время в течение суток с рН>4,0, % |
Омепразол, 20 мг/сут Лансопразол, 30 мг/сут Пантопразол, 40 мг/сут Рабепразол, 20 мг/сут Эзомепразол, 20 мг/сут Эзомепразол, 40 мг/сут | 2,75 3,70 3,20 6,5 6,3 7,2 | 35 46 41 53 53 71 |
Поскольку ингибиторы протонного насоса превращаются в фармакологически активное вещество только при низких значениях рН, встречаемых в секреторных канальцах париетальных клеток, считается, что это и обусловливает их высокую селективность и безопасность. Однако возможна активация препаратов в умеренно кислых тканях с ингибированием почечной Na+/К+-АТФазы и образованием активных форм кислорода нейтрофилами, угнетение Т-киллеров и хемотаксиса полиморфноядерных клеток.
Блокаторы Н+/К+-АТФазы потенцируют синтез слизи и бикарбонатов в антральном отделе желудка и в двенадцатиперстной кишке.
Классификация
Классификация ингибиторов протонного насоса весьма условна. С развитием новой группы препаратов - производных бензимидазола, ввиду общности механизма их действия, классификация основывалась на очередности их создания (поколения ингибиторов протонного насоса). Однако направление поиска новых высокоэффективных пре-
паратов данной фармакологической группы пошло по двум направлениям: с одной стороны, был создан рабепразол, отличающийся по химической структуре от представителей предыдущих поколений; с другой стороны, был создан эзомепразол, представляющий собой моноизомер (S-изомер) омепразола - представителя I поколения ингибиторов протонного насоса. В основу синтеза эзомепразола положено разделение рацемической смеси омепразола на право- и левовращающие (соответственно R- и S-) изомеры. Способ такого разделения был признан фундаментальным достижением, его разработчики были удостоены Нобелевской премии в области химии в 2001 г. R-форма омепразола менее эффективна, чем S-форма (эзомепразол) из-за их различий в биохимической доступности. Большая часть R-формы подвергается метаболизму в печени и не достигает париетальной клетки. Эти преимущества метаболизма эзомепразола приводят к увеличению AUC по сравнению с таковой для омепразола.
Рабепразол и эзомепразол продемонстрировали большую, по сравнению с предыдущими поколениями блокаторов Н+/К+-АТФазы, продолжительность основного фармакодинамического эффекта (блокады кислотопродукции), с другой стороны, два направления развития фармакологической группы вносят разногласие в принципы построения классификации по поколениям (рис. 20-1).
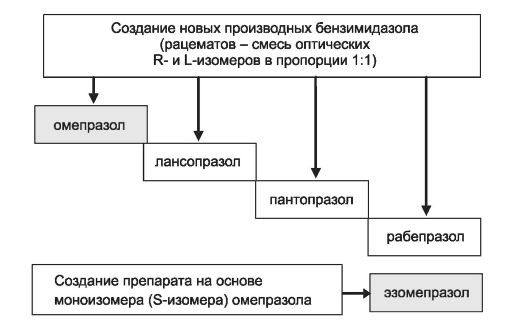 Рис. 20-1. Направления развития фармакологической группы препаратов - ингибиторов протонного насоса (схема).
Рис. 20-1. Направления развития фармакологической группы препаратов - ингибиторов протонного насоса (схема).
Фармакокинетика
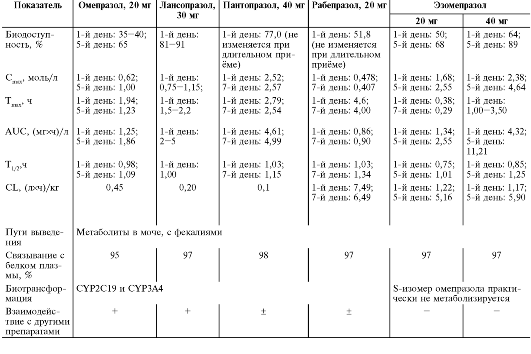
Фармакокинетика ингибиторов протонного насоса зависит от применяемой дозы. Это связано с их свойством, таким как высокая лабильность в кислой среде. Они способны блокировать внутрижелудочную кислотопродукцию, увеличивать собственную биодоступность (более характерно для омепразола, эзомепразола и лансопразола; биодоступность пантопразола и рабепразола при длительном применении практически не изменяется). Поскольку блокаторы протонного насоса неустойчивы в кислой среде, коммерческие лекарственные формы выпускают в виде кишечнорастворимых гранул, заключенных в желатиновые капсулы или кишечнорасторимые таблетки. Сравнительная фармакокинетика ингибиторов протонного насоса отражена в табл. 20-5.
Следует отметить, что биодоступность ингибиторов протонного насоса изменяется при наличии некоторых заболеваний печени, пищевода, желудка, кишечника (например, при рефлюкс-эзофагите, обострении язвенной болезни двенадцатиперстной кишки).
Для пациентов с заболеваниями почек или для пожилых уменьшение дозы ингибиторов протонного насоса не требуется. Несмотря на уменьшение клиренса ингибиторов протонного насоса в печени, нет необходимости регулировать дозу препарата для пациентов с нарушениями функции этого органа. Регуляция дозы не обязательна и для больных с различной степенью почечной недостаточности, а также для пациентов с циррозом печени, несмотря на уменьшение суммарного клиренса ингибитора.
Метаболиты омепразола, идентифицированные в образцах плазмы крови и в моче, - это омепразол сульфон, омепразол сульфид, гидроксиомепразол. Омепразол метаболизируется практически полностью до неактивного сульфона и в 100 раз менее активного гидроксипроизводного.
Интересен тот факт, что для ингибиторов протонного насоса характерен эффект функциональной кумуляции, то есть происходит накапливание антисекреторного эффекта, а не препарата. Таким образом, при достаточно низком периоде полувыведения, учитывая, что активная форма препарата навсегда блокирует функциональную активность Н+/К+-АТФазы и секреция соляной кислоты восстанавливается лишь при появлении новых молекул протонного насоса, продолжительность основного фармакодинамического эффекта намного превышает время нахождения препарата в крови.
Показания к применению и режим дозирования Показания к применению:
• неязвенная диспепсия;
• язвенная болезнь желудка и двенадцатиперстной кишки;
Таблица 20-5. Основные фармакокинетические параметры ингибиторов протонного насоса
•  пептическая язва;
пептическая язва;
• стрессовые язвы;
• эрозивно-язвенный эзофагит;
• рефлюкс-эзофагит;
• синдром Золлингера-Эллисона;
• полиэндокринный аденоматоз;
• системный мастоидоз;
• инфекция Helicobacter pylori.
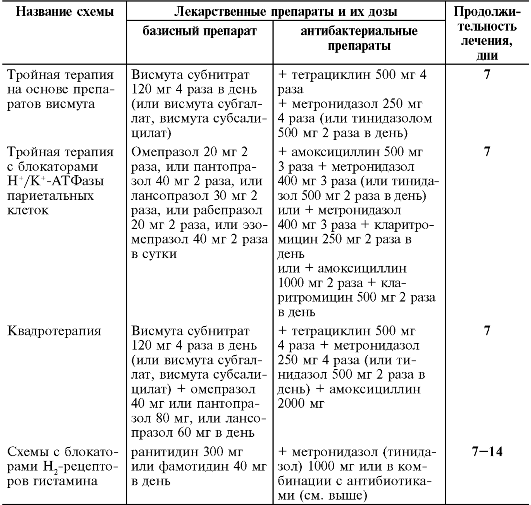
При язвенной болезни желудка, двенадцатиперстной кишки и рефлюкс-эзофагите омепразол назначают по 20 мг 1 раз в день, лансопразол по 30 мг 1 раз в день, пантопразол по 40 мг в сутки, рабепразол по 40 мг в сутки, эзомепразол по 40 мг в сутки. При необходимости (сохранение симптомов диспепсии или удлинение сроков заживления дефектов слизистой оболочки) увеличивают дозы или продолжительность лечения (при необходимости до 40 мг). При язве двенадцатиперстной кишки курс лечения 2-4 нед, при язве желудка и рефлюкс-эзофагите - 4-8 нед. Препараты используют для профилактики сезонных обострений или в режиме «по требованию» (on demand), когда пациент самостоятельно принимает препараты при появлении непродолжительных и незначительно выраженных явлений диспепсии. При синдроме Золлингера-Эллисона начальные дозы препаратов увеличивают (под контролем секреции желудка). При пептической язве, в патогенезе которой бактерия Helicobacter pylori играет одну из ведущих ролей, принимают удвоенные дозы ингибиторов протонного насоса в комбинациях с антибактериальными препаратами (табл. 20-6).
Побочные эффекты и противопоказания к назначению
Частые жалобы пациентов, длительно получающих ингибиторы протонного насоса, - головная боль, головокружение, сухость во рту, тошнота, диарея, запор, общая слабость, аллергические реакции, различные варианты кожной сыпи, редко - импотенция, гинекомастия. При длительном непрерывном применении ингибиторов протонного насоса возможно снижение продукции защитного гексозаминсодержащего муцина желудка.
Вследствие ахлоргидрии могут произойти заселение микроорганизмами прежде практически стерильной слизистой оболочки желудка и двенадцатиперстной кишки; гипергастринемия, гиперплазия ECL- клеток, возможно, увеличивается риск развития ECL-клеточной карциномы. Возможны активизация препарата в умеренно кислых тканях с ингибированием почечной Na+/К+-АТФазы и образованием активных форм кислорода нейтрофилами, угнетение Т-киллеров и хемо-
Таблица 20-6. Схемы эрадикационной терапии инфекции Helicobacter pylori
 таксиса
полиморфноядерных клеток, нейтропения, агранулоцитоз. При длительном
применении омепразола появляются гипонатриемия, дефицит витамина В12.
Редко встречаются кандидозы (как следствие иммунодефицита),
аутоиммунные нарушения. Описаны случаи гемолиза, острого гепатита,
острого интерстициального нефрита, острой почечной недостаточности.
Недостаточно изученной остается проблема возможного влияния препарата на
плод.
таксиса
полиморфноядерных клеток, нейтропения, агранулоцитоз. При длительном
применении омепразола появляются гипонатриемия, дефицит витамина В12.
Редко встречаются кандидозы (как следствие иммунодефицита),
аутоиммунные нарушения. Описаны случаи гемолиза, острого гепатита,
острого интерстициального нефрита, острой почечной недостаточности.
Недостаточно изученной остается проблема возможного влияния препарата на
плод.
Взаимодействие
Омепразол замедляет элиминацию лекарственных средств, метаболизирующихся в печени, путём микросомального окисления изоферментами цитохрома Р-450 CYP2C9, CYP3A4, диазепама, фенитоина,
непрямых антикоагулянтов. Омепразол снижает на 10% клиренс теофиллина. Ингибиторы протонового насоса изменяют рН-зависимую абсорбцию лекарственных средств, относящихся к группам слабых кислот (замедление) и оснований (ускорение). Сукральфат снижает биодоступность омепразола на 30%, в связи с чем необходимо соблюдать интервал между приемом этих препаратов в 30-40 мин. Антациды замедляют и снижают абсорбцию ингибиторов протонного насоса, поэтому их следует назначать за 1 ч до или через 1-2 ч после приема ланзопразола.
20.2. ГАСТРОПРОТЕКТОРЫ
К гастропротекторам относят ЛС, повышающие резистентность слизистой оболочки желудка и двенадцатиперстной кишки к воздействию агрессивных факторов. Подобная гастропротекция может быть осуществлена или путём активации естественных механизмов защиты слизистой оболочки, или за счет образования дополнительного защитного барьера в области эрозии или язвы.
Известны следующие фармакологические механизмы защиты слизистой оболочки:
• стимуляция устойчивости клеток гастродуоденальной зоны к неблагоприятным воздействиям (истинная цитопротекция);
• повышение секреции слизи и изменение ее качественных характеристик в сторону большей устойчивости к кислотно-пептической агрессии;
• стимуляция секреции клетками слизистой оболочки бикарбонатов;
• повышение устойчивости капиллярного русла к агрессии и нормализация микроциркуляции в слизистой оболочке желудка и двенадцатиперстной кишки;
• стимуляции регенерации клеток слизистой оболочки;
• механическая защита дефектов слизистой оболочки.
Механизм действия и основные фармакодинамические эффекты (См. подробно для каждой группы препаратов.)
Классификация
Выделяют пять групп гастропротекторов:
• пленкообразующие: сукральфат, препараты коллоидного висмута (висмута субнитрата и висмута субсалицитата): де-нол*, триби- мол*, вентрисол*;
• адсорбирующие и обволакивающие ЛС: сималдрат (гелусил*, гелусил лак*);
• цитопротективные: простагландины - синтетический аналог простагландина Е-мизопростол;
• стимуляторы регенерации (репаранты): метилурацил*, пентоксил*, этаден*, метандиенон (метандростенолон*), нандролон (ре- таболил*), калия оротат, препараты АТФ, биогенные стимуляторы (алоэ древовидного листья, каланхоэ сок*, апилак*, прополис), облепихи масло, шиповника масло, препараты корней девясила высокого, солкосерил*, гастрофарм* и др.;
• стимуляторы слизеобразования: препараты корня солодки голой, карбеноксолон, капусты сок сухой* и др.
Препараты коллоидного висмута. В кислой среде желудочного содержимого они образуют гликопротеин-висмутовый комплекс, концентрируемый в зоне эрозивных и язвенных поражений. При этом создается защитный барьер, препятствующий обратной диффузии ионов водорода, что ускоряет заживление эрозии или язвы. Препараты висмута слабо влияют на агрессивные факторы язвообразования, но способны предупреждать поражения слизистой оболочки желудка химическими раздражителями - этанолом, уксусной кислотой и др. Известно, что под влиянием препаратов коллоидного висмута на 50% усиливается локальный синтез простагландина Е2 в слизистой оболочке желудка или двенадцатиперстной кишки. Важен в противоязвенной терапии угнетающий эффект висмута в отношении Helicobacter pylori.
Сукральфат - комплексный сульфатированный дисахарид, содержащий алюминий. Препарат сходен с гепарином, однако лишен антикоагулянтных свойств и состоит из октасульфата сахарозы. В кислой среде желудка полимеризуется, при реакции с кислотой расходуется алюминия гидроксид. Образующийся полианион формирует прочные связи с положительно заряженными радикалами белков слизистой оболочки желудка и двенадцатиперстной кишки, особенно в зоне эрозий и язв, где концентрация препарата в 5-7 раз выше, чем в участках здоровой слизистой. Этот защитный слой относительно стабилен - в желудке сохраняется до 8 ч, в двенадцатиперстной кишке до 4 ч.
Сукральфат не обладает выраженными антацидными свойствами, но приблизительно на 30% тормозит пептическую активность желудочного сока. Он способен адсорбировать жёлчные кислоты, пепсин и повышать синтез простагландинов.
Простагландины представляют собой ненасыщенные карбоксикислоты эндогенного происхождения и содержат по 20 атомов углерода в виде циклопентанового кольца. Простагландины являются производным эссенциальных жирных кислот, входящих в состав клеточ-
ных мембран. Их предшественник - арахидоновая кислота, высвобождаемая из мембран под влиянием фосфолипазы А2. Многие простагландины (G, A, I2) ингибируют желудочную секрецию, уменьшая кислотность и пептическую активность желудочного сока; уменьшают сосудистую проницаемость, нормализуют микроциркуляцию, усиливают секрецию слизи и бикарбонатов. Гастропротективные свойства простагландинов связаны с их способностью предупреждать некроз слизистой оболочки при воздействии на нее НПВС, этанола, гипертонического солевого раствора и пр.
Эффект от воздействия простагландинов развивается очень быстро, в течение одной минуты при введении внутрь, и продолжается до двух часов. Синтетические аналоги простагландинов (мизопростол) более стабильны в организме. Мизопростол (синтетический аналог простагландина Е1) связывается с рецепторами простагландинов париетальных клеток, угнетая базальную, стимулированную и ночную секрецию. Действие препарата начинается через 30 мин после приёма внутрь и продолжается не менее 3 ч. Показано, что при дозе 50 мкг эффект короткий; при дозе 200 мкг - более выраженный и продолжительный.
Стимуляторы регенерации (репаранты). Метилурацил*- аналог пиримидиновых оснований, стимулирует белковый синтез при язвенной болезни, ускоряет регенерацию клеток, способствует заживлению язв, ожогов.
Метандиенон (метандростенолон*), нандролон (ретаболил*) - анаболические гормоны. Стимулируют азотистый баланс, уменьшают выделение мочевины, калия, серы, фосфора. У больных повышается аппетит, нарастает масса тела, облегчается период реконвалесценции после обострения ряда заболеваний, ускоряется заживление язв, ран, ожогов. Эти препараты показаны для лечения больных, истощённых язвенной болезнью.
Биогенный стимулятор солкосерил* - небелковый экстракт крови телят, ускоряет регенерацию тканей при язвенных поражениях, ожогах, отморожениях, пролежнях и др.
К биогенным стимуляторам также относятся вышеупомянутые алоэ древовидного листья, каланхоэ сок*, апилак*, прополис. Репаранты со сложным механизмом воздействия на заживление язв, ожогов, ран - облепихи масло, шиповника масло. Они содержат большие количества каротинов, каротиноидов, витаминов С, Е, фолиевой кислоты и др. Под действием масла облепихи в гомогенате слизистой оболочки желудка повышается содержание ацетилнейраминовой кислоты, снижается уровень перекисей. В корнях девясила высокого содержится эфирное масло, кристаллическая часть которого (геленин) состоит из
смеси лактонов алантолактона, его изо- и дигидроаналогов и алантоновой кислоты. Препарат корней девясила - алантон*, стимулирует процессы регенерации тканей, в том числе и язвенных поверхностей.
В связи с низкой эффективностью применение этих препаратов в настоящее время ограничено.
Стимуляторы слизеобразования. Корень солодки голой богат биологически активными веществами. К ним относятся ликуразид, глицирризиновая кислота (тритерпеновый гликозид*, обладающий противовоспалительными свойствами), флавоновые гликозиды, ликвиритон*, ликвиритозид (имеющий спазмолитический эффект), эфирное масло, слизистые и многие другие продукты метаболизма растения. В начале 60-х годов на основе глицирризиновой кислоты был синтезирован пентациклический тритерпен, который под названием карбеноксолон (биогастрон, дуогастрон) применялся при лечении больных с язвенной болезнью. Препарат при курсовом применении улучшал количество и качество слизистого слоя, что повышало устойчивость его к кислотноагрессивному воздействию.
Фармакокинетика
Ниже приводится фармакокинетика основных препаратов группы.
Препараты висмута обладают низкой биодоступностью. При курсовом лечении концентрация висмута в плазме крови достигает 50 мкг/л приблизительно через один месяц. При этом концентрация препарата в желудочном соке сохраняется на уровне 100 мг/л. Всосавшийся висмут концентрируется в почках и выделяется с мочой. Невсосавшаяся часть висмута выводится с калом в виде сульфида. Период полувыведения 4-5 сут. Изредка отмечают головные боли, головокружение, диарею. Описаны висмутовые энцефалопатии, когда концентрация в плазме препарата достигала 100 мкг/л.
Сукральфат обладает низкой всасываемостью из ЖКТ. Абсорбция составляет 3-5% от введенной дозы (до 5% дисахаридного компонента и менее 0,02% алюминия). Выводится через кишечник - 90% в неиз- менённом виде, незначительное количество сульфатного дисахарида, попавшего в кровоток, выводится почками. При приёме внутрь мизопаростол быстро и полно абсорбируется (пища задерживает абсорбцию). С max наступает через 12 мин; 90% препарата в плазме связывается с белками. Т1/2 составляет 20-40 мин. В стенках ЖКТ и печени метаболизируется до фармакологически активной мизопростоловой кислоты. 80% метаболитов выводится с мочой, 15% - с жёлчью. Css - через 2 сут. Не кумулируется при многократном приёме. Выводится почками (80%) и с жёлчью (15%). При нарушении функции почек почти в 2 раза повышаться Cmax, удлиняется T1/2.
Показания к применению и режимы дозирования
Описываемую группу лекарственных препаратов применяют при лечении и профилактике больных с эрозиями и язвами желудка и двенадцатиперстной кишки, при рефлюкс-эзофагите, гастрите. Препараты висмута входят в состав схем для эрадикации Helicobacter pylori. Сукральфат показан также при гиперфосфатемии у больных с уремией, находящихся на гемодиализе. Их терапевтическая значимость при язвенной болезни уменьшилась (в связи с широким применением антикислотных средств), однако у каждого из препаратов существует своя терапевтическая «ниша» и определённые показания к применению. Мизопростол, кроме того, применяют для профилактики и лечения нестероидной гастропатии, у пациентов с повышенным риском язвообразования.
Де-нол* применяют по 2 таблетки (каждая по 120 мг) в день за полчаса до завтрака и обеда в течение 4-8 нед. Препараты висмута чаще всего применяют в составе схем антигеликобатерной терапии (см. таблицу в разделе, посвящённом ингибиторам протонного насоса).
Сукральфат применяют внутрь по 1 г 4 раза в сутки или по 2 г 2 раза в сутки за 1 ч до еды и перед сном, максимальная суточная доза - 8 г. Средняя продолжительность курса лечения язвенной болезни 4-6 нед, при необходимости - до 12 нед. У пациентов с гиперфосфатемией при снижении концентрации фосфатов в плазме крови доза сукральфата может быть уменьшена.
Мизопростол назначают взрослым по 200 мкг 4 раза в сутки (во время или после еды и на ночь). Возможно применение по 400 мкг 2 раза в сутки (последний приём на ночь). У пациентов, принимающих НПВС, мизопростол применяют в течение всего периода лечения НПВС. Курс лечения при обострении язвенной болезни двенадцатиперстной кишки 4 нед. Если по данным эндоскопии не отмечено полного рубцевания язвы, лечение продолжают еще в течение 4 нед.
Противопоказания
Гастропротекторы противопоказаны при беременности, выраженных нарушениях функции почек, повышенной чувствительности к препаратам. Мизопростол, обладающий тератогенным действием, противопоказан при беременности, лактации, а также при нарушениях функции печени, повышенной чувствительности к простагландинам. Де-нол* не применяют при нарушении функции почек. Сукральфат не назначают детям до 4 лет, пациентам с выраженными нарушения функции почек, кровотечением из ЖКТ, повышенной чувствительностью к препарату, дисфагией или непроходимостью ЖКТ.
Побочные эффекты
При применении всех гастропротекторов возможно возникновение головной боли, тошноты, рвоты, нарушения акта дефекации. Изредка отмечают аллергические реакции в виде кожной сыпи и зуда. При применении мизопрастола часто наблюдают диарею, возможны меноррагии, метроррагии. Продолжительный приём больших доз препаратов висмута не рекомендуют, так как известны случаи возвратной энцефалопатии.
Побочные эффекты препаратов висмута (слабость, снижение аппетита, нефропатия, гингивиты, артралгии) наблюдают при концентрации висмута в плазме крови свыше 100 мкг/л.
Побочные эффекты сукральфата: запоры, диарея, тошнота, сухость во рту, гастралгия, сонливость, головокружение, головная боль, кожный зуд, сыпь, крапивница, боль в области поясницы. Появление сонливости и судорог обусловлено токсическим действием алюминия.
Побочные эффекты мизопростола: боль в животе, метеоризм, тошнота, рвота, диарея, запор, боли внизу живота (связанные с сокращениями миометрия), дисменорея, полименорея, меноррагия, метроррагия. Аллергические реакции: кожная сыпь, зуд, отёк Квинке. Могут наблюдаться: изменение массы тела, астения, повышенная утомляемость; крайне редко - судороги (у женщин в предили постклимактерическом периоде). С осторожностью мизопростол применяют у пациентов с артериальной гипотензией, поражениями артерий сердца и головного мозга, эпилепсией, повышенной чувствительностью к простагландинам или их аналогам.
Взаимодействие
Де-нол* может вызывать снижение абсорбции тетрациклинов, препаратов железа, кальция. Не следует за полчаса до приёма и полчаса спустя употреблять молоко. Не следует одновременно использовать другие препараты висмута или употреблять алкоголь. Субсалицилат висмута не рекомендуется назначать одновременно с антикоагулянтами, противоподагрическими средствами и антидиабетическими препаратами.
При одновременном применении сукральфата с непрямыми антикоагулянтами возможно уменьшение их антикоагулянтой активности. При одновременном применении уменьшается абсорбция производных фторхинолона, а также снижается абсорбция амитриптилина, что может привести к уменьшению его клинической эффективности. Полагают, что при одновременном применении сукральфата с амфотерицином B, тобрамицином возможно образование хелатных комплексов, что может привести к уменьшению их противомикробной активности.
При одновременном применении с дигоксином возможно уменьшение его абсорбции. Полагают, что при одновременном применении возможно небольшое уменьшение абсорбции кетоконазола и флуконазола. При одновременном применении с левотироксином заметно уменьшается эффективность левотироксина натрия. При одновременном применении с сукральфатом наблюдались небольшие изменения фармакокинетики теофиллина. Полагают также, что возможно значительное уменьшение абсорбции теофиллина из лекарственных форм с замедленным высвобождением. Полагают, что при одновременном применении возможно уменьшение абсорбции тетрациклина. При одновременном применении уменьшается абсорбция фенитоина, сульпирида. Описан случай уменьшения концентрации хинидина в плазме крови при одновременном применении с сукральфатом. При одновременном применении нельзя исключить некоторого уменьшения биодоступности циметидина, ранитидина, роксатидина.
При одновременном применении мизопростола с антацидами уменьшается концентрация мизопростола в плазме крови. При одновременном применении с магнийсодержащими антацидами возможно усиление диареи. При одновременном применении с аценокумаролом описан случай уменьшения антикоагулянтного действия аценокумарола.
20.3. ПРОТИВОРВОТНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА
Тошнота - неприятное, безболезненное, своеобразное ощущение, предшествующее рвоте. Рвота - это рефлекторный акт выталкивания содержимого желудка через рот, при этом диафрагма и наружные косые мышцы живота сокращаются, создавая положительное давление как в брюшной, так и в грудной полостях. Происходит расслабление верхнего пищеводного сфинктера, расширение брюшного отдела пищевода и сокращение привратника, что способствует более быстрому выходу пищи через рот. Рвота - защитная физиологическая реакция, способствующая освобождению желудка от токсических или неудобоваримых продуктов.
Различают три вида рвоты:
• собственно рефлекторная рвота, связанная с патологией органов пищеварения;
• токсическая - при накоплении в организме экзогенных ядов, или токсинов, или лекарственных препаратов;
• центральная - при заболеваниях или поражениях ЦНС.
В дорсальном отделе латеральной ретикулярной формации продолговатого мозга локализован так называемый рвотный центр. Кроме
того, существует и вторая область, участвующая в акте рвоты, - «хеморецепторная триггерная зона». Она расположена в дне четвёртого желудочка головного мозга. Афферентные сигналы к центру рвоты поступают из многочисленных периферических зон, включая глотку, сердце, брюшину, сосуды брыжейки и желчевыводящие пути. Стимуляция каждой из этих зон может вызывать рвоту. Независимо от причины, вызывающей рвотный рефлекс, в его реализации принимают участие нейромедиаторы: дофамин, гистамин, ацетилхолин, эндогенные опиаты, серотонин, ГАМК, субстанция Р. Фармакологическое воздействие на некоторые из этих веществ является основой создания многих противорвотных препаратов.
Механизм действия и основные фармакодинамические эффекты (См. подробно для каждой группы препаратов.)
Классификация
В группе противорвотных препаратов встречаются лекарственные средства различной химической природы. По фармакологическому эффекту их можно разделить на несколько подгрупп:
• препараты центрального действия, блокирующие серотониновые рецепторы: гранисетрон, ондансетрон, трописетрон;
• препараты центрального действия, блокирующие дофаминовые рецепторы: домперидон, метоклопрамид, сульпирид;
• препараты центрального действия, блокирующие дофаминовые и холинорецепторы: тиэтилперазин.
Препараты центрального действия, блокирующие серотониновые рецепторы. Ондансетрон селективно блокирует серотониновые 5-НТ3- рецепторы нейронов, устраняя тошноту и рвоту, обусловленную высвобождением серотонина. Применяют на фоне лечения цитостатическими препаратами, при лучевой терапии, в послеоперационном периоде.
Трописетрон так же, как и ондансетрон, является конкурентным антагонистом серотониновых 5-НТ3-рецепторов в периферических тканях и ЦНС. Блокирует рвотный рефлекс, вызываемый химеотерапевтическими противоопухолевыми препаратами, стимулирующими выброс серотонина из энтерохромаффиноподобных клеток слизистой оболочки желудка и кишечника. Гидроксилируется с последующей коньюгацией с глютатионом в печени; метаболиты этого процесса неактивны. Длительность действия препарата до 24 ч, из организма выводится медленно.
Гранисетрон считают антагонистом 5-НТ3-рецепторов с высокой степенью селективности.
Препараты центрального действия, блокирующие дофаминовые рецепторы. Эффект обусловлен центральным дофаминоблокирующим действием. Эти препараты влияют на триггерные зоны ствола головного мозга, оказывая регулирующее влияние на моторику желудка и кишечника, не влияя на желудочную секрецию, таким образом, оказывая противорвотное действие, успокаивая икоту и устраняя тошноту.
Метоклопрамид, домперидон и сульпирид при некоторых ситуациях снимают тошноту, рвоту, вызванную апоморфином, морфином, но малоэффективны при рвоте, вызванной цитостатиками. Эти препараты тормозят выработку гастрина в ответ на приём мясной пищи, оказывают сосудорасширяющее действие, улучшают кровоток в органах брюшной полости, усиливают репаративные процессы. Сульпирид оказывает также умеренное антисеротониновое действие.
Метоклопрамид и сульпирид в большей степени понижают двигательную активность пищевода, ускоряют опорожнение желудка, активизируют пищеводно-желудочный сфинктер, повышают активность пилорической части желудка, перистальтику двенадцатиперстной кишки. Метоклопрамид ускоряет продвижение пищи по тонкому кишечнику, не усиливая значительно перистальтику и не вызывая диарею. Холиномиметические эффекты метоклопрамида и сульпирида ограничены проксимальным отделом кишечника, устраняются холиноблокаторами и морфином.
Препараты центрального действия, блокирующие дофаминовые и холинорецепторы. Тиэтилперазин действует на хеморецепторную триггерную зону и на собственный центр рвоты, оказывая центральное противорвотное действие. Обладает адрено- и м-холиноблокирующим действием; связывает дофаминовые рецепторы в нигростриатных путях, но, в отличие от нейролептиков, не имеет антипсихотических и каталептогенных свойств.
Фармакокинетика
При введении внутрь биодоступность ондансетрона достигает 60%; Сmax - 1,5 ч; с белками плазмы связывается до 70-76% препарата. Т1/2 при парентеральном введении - 3 ч. Выделяется с мочой. Противопоказан больным с повышенной чувствительностью к препарату и в I триместре беременности.
После быстрого внутривенного введения 20 или 40 мкг/кг гранисетрона его средняя пиковая концентрация в плазме крови составляет соответственно 13,7 и 42,8 мкг/л. Связывание с белками плазмы составляет 65%. Препарат быстро метаболизируется путём деметилирования и окисления. Период полувыведения составляет 3,1-5,9 ч, у онкологических пациентов он повышается до 10-12 ч. Выводится с
мочой и калом, в основном в виде конъюгатов, 8-15% препарата обнаруживают в моче в неизменённом виде.
Трописетрон в течение 20 мин всасывается из кишечника (более 95%). Cmax достигается в течение 3 ч. С белками плазмы крови связывается до 70% препарата.
Метоклопрамид быстро всасывается из ЖКТ, биодоступность - 60-80%, Cmax достигается через 1-2 ч. Время достижения максимальной концентрации в плазме крови 30-120 мин. Выводится через почки в неизменённом виде (около 30%) и в виде конъюгатов. Период полувыведения от 3 до 5 ч, при нарушениях функции почек увеличивается до 14 ч. Проникает через ГЭБ, плацентарный барьер, в грудное молоко.
Домперидон быстро абсорбируется при приёме внутрь натощак. Cmax в плазме крови достигается примерно в течение 1 ч. Низкая абсолютная биодоступность домперидона при приёме внутрь (приблизительно 15%) обусловлена экстенсивным первичным метаболизмом в стенке кишечника и печени. Гипоацидность желудочного сока снижает абсорбцию домперидона. При приёме внутрь домперидон не кумулирует и не индуцирует собственный метаболизм. Cmax в плазме через 90 мин после приема, равная 21 нг/мл, после 2-недельного приёма по 30 мг/сут была почти такой же, как после приёма первой дозы (18 нг/мл). Домперидон на 91-93% связывается с белками плазмы. Препарат метаболизируется в печени путём гидроксилирования и N-дезалкилирования. При исследованиях метаболизма препарата in vitro с использованием диагностических ингибиторов было обнаружено, что CYP3A4 является основным изоферментом системы цитохрома Р-450, участвующим в процессе N-дезалкилирования домперидона, тогда как CYP3A4, CYP1A2 и CYP2E1 участвуют в процессе ароматического гидроксилирования домперидона. Выведение с мочой и калом составляет 31% и 66% от принятой внутрь дозы соответственно. Выводится в неизменённом виде с калом - 10% и с мочой приблизительно 1%. T1/2 из плазмы крови после приёма разовой дозы составляет 7-9 ч у здоровых людей. У пациентов с тяжёлой почечной недостаточностью T1/2 увеличивается до 20,8 ч.
Тиэтилперазин после приёма внутрь хорошо всасывается из ЖКТ. Максимальная концентрация в плазме - через 2-4 ч. Объём распределения 2,7 л/кг. Препарат метаболизируется в печени. Т1/2 около 12 ч. В неизменённом виде выводится примерно 3% дозы.
Показания к применению и режим дозирования. Противорвотные препараты показаны для симптоматического лечения тошноты и рвоты. Препараты центрального действия, блокирующие серотониновые рецепторы, учитывая их механизм действия, применяются при тош-
ноте и рвоте, развившейся во время проведения химиотерапии онкологических заболеваний, для профилактики и лечения рвоты после наркоза.
Препараты центрального действия, блокирующие дофаминовые рецепторы применяются:
• при тошноте, рвоте;
• при послеоперационой атонии кишечника;
• при гипокинетическом опорожнении желудка;
• при рефлюкс-эзофагите;
• в составе комплексной терапии язвенной болезни;
• при дискинезии жёлчных путей;
• при метеоризме, икоте;
• при рвоте, развившейся на фоне токсемии, лучевой терапии, нарушений диеты, приёма ЛС, при рентгенологических обследованиях, эндоскопиях.
Тиэтилперазин, метоклопрамид, сульпирид рекомендуют также при тошноте, рвоте центрального генеза на фоне вестибулярных нарушений, головокружений. Способы применения противорвотных средств отражены в табл. 20-7.
Таблица 20-7. Режим дозирования противорвотных лекарственных средств
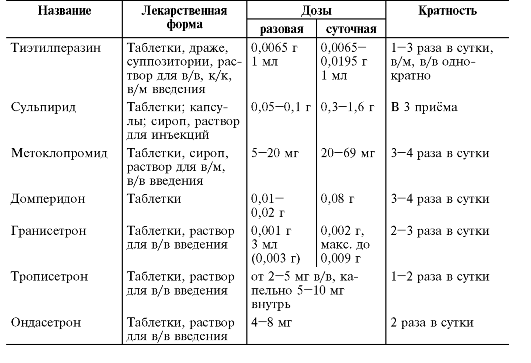 Побочное действие и противопоказания
Побочное действие и противопоказания
При применении ондансетрона и трописетрона возможно появление головной боли, головокружения, диареи, запоров. Эти препараты противопоказаны при беременности и кормлении грудью, ондансетрон противопоказан, а трописетрон не рекомендован для применения у детей.
При приёме ондансетрона возможны:
• боли в грудной клетке (в ряде случаев с депрессией сегмента ST);
• аритмии;
• артериальная гипотензия, брадикардия;
• икота, сухость во рту;
• транзиторное бессимптомное повышение активности трансаминаз в сыворотке крови;
• спонтанные двигательные расстройства, судороги;
• крапивница, бронхоспазм, ларингоспазм, ангионевротический отёк, анафилаксия;
• приливы крови к лицу, чувство жара;
• временное нарушение остроты зрения;
• гипокалиемия.
При приёме трописетрона у больных с артериальной гипертензией может повышаться артериальное давление; в редких случаях возможны зрительные галлюцинации. При применении гранисетрона возможны транзиторное повышение активности печёночных ферментов (трансаминаз) в крови, запоры, головная боль, кожная сыпь. Препарат противопоказан при повышенной чувствительности к нему.
При приеме метоклопрамида иногда возникают чувство усталости, головные боли, головокружение, беспокойство, депрессия, сонливость, шум в ушах, агранулоцитоз, у детей может развиться дискинетический синдром (непроизвольные тикообразные подёргивания мышц лица, шеи или плеч). Возможно появление экстрапирамидных расстройств. В единичных случаях развивается тяжёлый нейролептический синдром. При длительном лечении метоклопрамидом может развиться паркинсонизм. Со стороны сердечно-сосудистой системы: суправентрикулярная тахикардия, гипотензия, гипертензия. Со стороны желудочно-кишечного тракта: запор, диарея, сухость во рту. Со стороны эндокринной системы: гинекомастия, галакторея или нарушения менструального цикла. При развитии этих явлений метоклопрамид отменяют. Приём метоклопрамида противопоказан при повышенной чувствительности к препарату, феохромоцитоме, кишечной непроходимости, перфорации кишечника и желудочно-кишечном кровотечении, пролактинозависимой опухоли, эпилепсии и экстрапирамидных двигательных расстройствах, в I триместре беременности и
период лактации, детям до 2 лет. С осторожностью применяют при артериальной гипертензии, бронхиальной астме, нарушениях функций печени, повышенной чувствительности к прокаину и прокаинамиду, детям в возрасте от 2 до 14 лет. Во время II и III триместра беременности препарат назначают только по жизненным показаниям. Больным с пониженной функцией почек препарат назначают в уменьшенных дозах.
При приёме домперидона возможно развитие преходящих спазмов кишечника (полностью обратимы и исчезают после прекращения лечения). Редко развиваются экстрапирамидные симптомы у детей, в единичных случаях - обратимые экстрапирамидные симптомы у взрослых. При нарушении функций гематоэнцефалического барьера полностью исключают возможность появления неврологических побочных эффектов. Возможны гиперпролактинемия, галакторея, гинекомастия. Аллергические реакции: сыпь и крапивница. Домперидон противопоказан при желудочно-кишечных кровотечениях, механической непроходимости или перфорациях, при которых стимуляция двигательной функции желудка может быть опасна, при пролактинсекретирующей опухоли гипофиза (пролактинома), повышенной чувствительности к компонентам препарата. Применение домперидона в I триместре беременности не желательно. С осторожностью назначают препарат больным с печёночной недостаточностью, учитывая высокую степень метаболизма домперидона в печени.
При приёме тиэтилперазина могут возникнуть сухость во рту, головокружения, при длительном применении возможны экстрапирамидные расстройства, нарушение функций печени. Препарат противопоказан детям до 15 лет, при депрессии, коматозных состояниях, остром приступе глаукомы, тяжёлой печёночной и почечной недостаточности, гиперчувствительности к препаратам фенотиазинового ряда.
Взаимодействие
Следует учитывать, что ондансетрон метаболизируется ферментной системой цитохрома P-450 печени. Поэтому с осторожностью следует назначать ондансетрон-лэнс одновременно с индукторами цитохрома P-450 (CYP2D6 и CYP3A) - барбитуратами, карбамазепином, каризопродолом, аминоглутетимидом , гризеофульвином , азота закисью*, папаверином, фенилбутазоном, фенитоином (вероятно, и с другими гидантоинами), рифампицином, толбутамидом; с ингибиторами цитохрома P-450 (CYP2D6 и CYP3A) - аллопуринолом, антибиотиками группы макролидов (в том числе эритромицином), антидепрессантами (ингибиторами МАО), хлорамфениколом, циметидином, содержащими эстрогены пероральными контрацептивами, дилтиаземом, дисуль-
фирамом, вальпроевой кислотой, натрием вальпроатом, флуконазолом, фторхинолонами, изониазидом, кетоконазолом, ловастатином, метронидазолом, омепразолом, пропранололом, хинидином, хинином, верапамилом.
При одновременном приёме трописетрона с рифампицином, фенобарбиталом или другими препаратами, индуцирующими микросомальные ферменты печени, происходит снижение его концентрации в плазме и уменьшение противорвотного действия.
Никаких специфических лекарственных взаимодействий с гранисетроном не отмечено.
Метоклопрамид снижает действие антихолинэстеразных средств, усиливает всасывание антибиотиков (тетрациклина, ампициллина), парацетамола, леводопы, лития и алкоголя, уменьшает всасывание дигоксина и циметидина, усиливает действие лекарственных средств, угнетающих ЦНС. Не следует одновременно с метоклопрамидом назначать нейролептические препараты во избежание возможного усиления экстрапирамидных расстройств. Препарат может влиять на действие трициклических антидепрессантов, ингибиторов МАО и симпатомиметических средств, снижает эффективность терапии Н2-гистаминоблокаторами, увеличивает риск развития гепатотоксичности при комбинации с гепатотоксичными средствами, снижает эффективность перголида, леводопы, увеличивает биодоступность циклоспорина, что может потребовать контроля его концентрации, повышает концентрацию бромокриптина.
Антихолинергические препараты, циметидин, натрия бикарбонат* могут нейтрализовать действие домперидона. Не следует принимать антацидные и антисекреторные препараты одновременно с мотилиу- мом*, так как они снижают его биодоступность (после приёма внутрь). Основной путь метаболических превращений домперидона происходит при участии изофермента CYP3A4 системы цитохрома P-450. На основании исследований in vitro можно предположить, что при одновременном применении домперидона и лекарственных средств, значительно ингибирующих этот изофермент, возможно повышение уровня домперидона в плазме. Примерами ингибиторов изофермента CYP3A4 являются следующие лекарственные средства: противогрибковые препараты азолового ряда, антибиотики из группы макролидов, ингибиторы ВИЧ-протеазы, нефазодон. Теоретически, так как домперидон обладает гастрокинетическим действием, он мог бы влиять на абсорбцию препаратов при одновременном приёме внутрь, в частности препаратов с замедленным высвобождением активного вещества или препаратов, покрытых кишечно-растворимой оболочкой. Однако применение домперидона у больных на фоне приема парацетамола или
подобранной терапии дигоксином не влияло на уровень этих препаратов в крови. Мотилиум может также сочетаться с нейролептиками, действие которых он не усиливает; агонистами допаминергических рецепторов (бромокриптином, леводопой), нежелательные периферические эффекты которых, такие, как нарушения пищеварения, тошнота, рвота, он подавляет, не нейтрализуя их основные свойства.
Тиэтилперазин потенцирует действие алкоголя, бензодиазепинов, наркотических анальгетиков и других препаратов, угнетающих функции ЦНС.
20.4. ФЕРМЕНТНЫЕ ПРЕПАРАТЫ
Показанием для назначения ферментных препаратов больным с заболеваниями желудочно-кишечного тракта считают синдром мальдигестии и мальабсорбции различного происхождения при наличии внешнесекреторной недостаточности поджелудочной железы или без нее. Расстройства полостного пищеварения наблюдают при алиментарных погрешностях, дисфункции и заболеваниях желудка, тонкой кишки, поджелудочной железы, печени, желчевыводящих путей или при сочетанной патологии. Сначала возникают расстройства пристеночного пищеварения, а затем и всасывания (мальабсорбция). Клинические проявления нарушений пищеварения обусловлены симптомами диспепсии различной выраженности. Наиболее часто больных беспокоит метеоризм, несколько реже - неустойчивый стул. К клиническим признакам внешнесекреторной недостаточности поджелудочной железы относят боли в околопупочной области, снижение аппетита, метеоризм, неустойчивый стул, стеаторею, креаторею, тошноту, рецидивирующую рвоту, общую слабость, похудание, снижение физической активности, отставание в росте (при тяжёлых формах).
Ферментные препараты являются многокомпонентными лекарственными средствами, основу которых составляет комплекс энзимов животного, растительного или грибкового происхождения в чистом виде или в комбинации со вспомогательными компонентами (жёл- чными кислотами, аминокислотами, гемицеллюлазой, симетиконом, адсорбентами и др.).
Препараты, содержащие ферменты слизистой оболочки желудка.
Пепсин - препарат, содержащий протеолитический фермент. Получают его из слизистой оболочки желудка свиней. Таблетки ацидинпепсина* (аналоги: бетацид*, аципепсол*, пепсамин, пепсацид) содержат 1 часть пепсина и 4 части бетаина (ацидина*). При введении в желудок бетаина гидрохлорид гидролизуется и отделяет свободную
соляную кислоту. Пепсидил* - раствор в соляной кислоте продуктов ферментативного гидролиза слизистой оболочки желудка свиней, содержащей пепсин. Абомин* содержит сумму протеолитических ферментов. Его получают из слизистой оболочки желудка телят и ягнят молочного возраста.
Препараты, содержащие ферменты поджелудочной железы или аналогичные им. Ферментативные ЛС этой группы содержат в своем составе пищеварительные ферменты поджелудочной железы (табл. 20-8).
Таблица 20-8. Пищеварительные ферменты поджелудочной железы
 * Ферменты секретируются поджелудочной железой в неактивной форме (проферменты); они активируются в двенадцатиперстной кишке.
* Ферменты секретируются поджелудочной железой в неактивной форме (проферменты); они активируются в двенадцатиперстной кишке.
Ферментативные препараты, содержащие или аналогичные ферментам поджелудочной железы:
• панкреатин (трипсин, α-амилаза*, липаза);
• креон 10000, креон 25000* (панкреатин);
• ораза* (амилаза, мальтаза, протеаза, липаза);
• солизим* (липолитический фермент из культуры Penicillium solitum);
• сомилаза* (солизим*, α-мальтаза);
• нигедаза* (липолитический фермент из растительного сырья);
• панзинорм форте Н* (экстракт жёлчи, панкреатин, аминокислоты из желёз крупного рогатого скота);
• панкурмен* (амилаза, липаза, протеаза, экстракт кукурмы);
• фестал* (амилаза, липаза, протеаза, гемицеллюлоза, компоненты жёлчи);
• дигестал* (панкреатин, экстракт жёлчи, гемицеллюлоза);
• энзистал* (панкреатин, гемицеллюлоза, экстракт жёлчи);
• мезим форте* (панкреатин, амилаза, липаза, протеаза).
Все ферментные лекарственные средства различаются по активности ферментов, их составу и существуют в разных лекарственных формах. В одних случаях это однослойные таблетки, растворимые только в кишечнике, в других - двухслойные, например, панзинорм форте Н*. Наружный слой его растворяется в желудке, содержит экстракт слизистой оболочки желудка и аминокислоты, а вторая оболочка кислотоустойчивая, растворяется в кишечнике, содержит панкреатин и экстракт жёлчи крупного рогатого скота.
Наряду с ферментами поджелудочной железы и желудка в комбинированный ферментный препарат часто включают и гемицеллюлозу, способствующую расщеплению растительных оболочек, что снижает процессы брожения, уменьшает образование газов в кишечнике (фес- тал*) (табл. 20-9).
Таблица 20-9. Состав основных ферментных препаратов
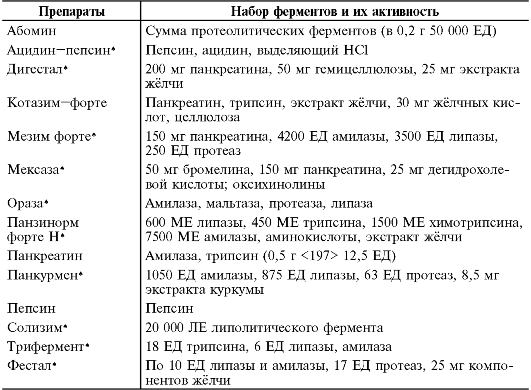 Препараты, содержащие ферменты растительного происхождения.
Препараты, содержащие ферменты растительного происхождения.
Ферментом растительного происхождения, используемым для коррекции мальдигестии, мальадсорбции и внешнесекреторной недостаточ-
ности поджелудочной железы, считают папаин (пепфиз*, юниэнзим*). Папаин - протеолитический фермент, присутствующий в латексе дынного дерева (Carica papaya L.). Он способен гидролизовать практически любые пептидные связи, за исключением тех, что образованы остатками пролина. Иногда в состав этой группы препаратов входит бромелаин.
Кроме того, в состав препаратов может входить грибковая диастаза (α-амилаза), расщепляющая полисахариды (крахмал, гликоген) на простые дисахариды (мальтозу и мальтотриозу), вещества, уменьшающие явления метеоризма (симетикон, активированный уголь). Симетикон способствует коалесценции (разрушению пены).
Иногда применяются комбинированные препараты, содержащие панкреатин в сочетании с растительными энзимами (вобэнзим*).
20.5. ЖЕЛЧЕГОННЫЕ, ГЕПАТОПРОТЕКТОРНЫЕ, ХОЛЕЛИТОЛИТИЧЕСКИЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА
К данной группе лекарственных средств относят препараты, которые могут воздействовать на образование жёлчи и ее эвакуацию, осуществлять защитные функции в отношении гепатоцита, препятствовать развитию холелитиаза. Для более полного понимания механизма их действия необходимо оценить физиологические особенности жёл- чевыделения, функции гепатоцита и жёлчного пузыря.
Гепатоциты - основные субъединицы печени, отделены от жёлчных капилляров так называемой базолатеральной мембраной, а от синусоидов - синусоидальной. Основной функцией базолатеральной мембраны считают выделение жёлчи в жёлчные капилляры, из которых она попадает в терминальные жёлчные протоки. Из них жёлчь поступает в более крупные протоки, затем в интралобулярные, откуда в общий жёлчный проток, в жёлчный пузырь и двенадцатиперстную кишку. На этой мембране расположены специфические ферменты: щелочная фосфатаза, лейцинаминопептидаза, γ-глютамилтранспептидаза.
Через синусоидальную мембрану осуществляются транспортные процессы: захват аминокислот, глюкозы, органических анионов (жёл- чные, жирные кислоты и билирубин) для последующих внутриклеточных реакций. На синусоидальной мембране гепатоцита располагаются специфические транспортеры, в частности Na+, К+-АТФаза, и происходят процессы выделения альбумина, липопротеинов и факторов свёртывания крови.
Жёлчь (так называемая первичная, или порция «С») представляет собой жидкость с осмотическим давлением, равным таковому
в плазме крови, и является продуктом экзокринной секреции печени. В нормально функционирующем органе она секретируется постоянно и суточный объем ее колеблется от 250 до 1000 мл. В составе жёлчи много компонентов, определяющих ее функциональную роль в пищеварении:
• неорганические вещества: бикарбонаты, хлориды и фосфаты натрия, калия, кальция, магния, железа и других металлов;
• органические соединения: жёлчные кислоты первичные (холевая, хенодезоксихолевая); жёлчные кислоты вторичные (дезоксихолевая, литохолевая); холестерин; фосфолипиды; жирные кислоты; белок; мочевина, мочевая кислота;
• витамины А, В, С;
• некоторые ферменты: амилаза, фосфатаза, протеазы, каталаза и др. Формирование жёлчи складывается из трёх этапов.
• 1-й этап. Захват из крови содержащихся в ней жёлчных кислот, билирубина, холестерина и др.
• 2-й этап. Метаболизм и синтез новых составляющих жёлчи.
• 3-й этап. Выделение всех компонентов через билиарную мембрану в жёлчные канальцы, затем в последующие протоки и двенадцатиперстную кишку.
В кишечнике жёлчь участвует в гидролизе жиров для подготовки их к всасыванию. Помимо этого, жёлчь активирует панкреатическую липазу, подавляет действие желудочных протеаз, регулирует перистальтику кишечника. Она обладает слабо выраженными бактерицидными свойствами, однако в ней длительно могут сохраняться сальмонеллы, большинство вирусов.
Жёлчный пузырь концентрирует и депонирует жёлчь между приё- мами пищи. Он также эвакуирует жёлчь за счёт сокращения гладкомышечных элементов стенки в ответ на стимуляцию холецистокинином и поддерживает гидростатическое давление в жёлчных протоках.
Желчегонные лекарственные средства
Лекарственные средства, воздействующие и нормализующие жёл- чевыделение (желчегонные ЛС), принято подразделять на три группы: холеретики, холекинетики и миотропные спазмолитики.
Холеретики. Механизм действия холеретиков связан с рефлекторными реакциями со слизистой оболочкой преимущественно тонкой кишки при воздействии жёлчных кислот или веществ, содержащих эфирные масла.
В эту группу входят:
• препараты, содержащие жёлчные кислоты;
• синтетические препараты;
• ЛС растительного происхождения;
• минеральные воды.
К холеретикам, содержащим жёлчные кислоты, относят аллохол*, лиобил*, холензим*, панзинорм форте-Н*, фестал*, дехолин, холагол*. Аллохол* содержит жёлчь сгущенную, экстракт чеснока густого, экстракт крапивы густой, уголь активированный. Действие препарата основано на стимуляции секреторной функции печени и этой же функции кишечника, усилении перистальтики желудка и кишечника, воздействии на аномальную микрофлору толстой кишки. Не показано применение препарата при острых заболеваниях печени, при желтухе или индивидуальной непереносимости. Лиобил* содержит 0,2 г лиофизированной бычьей жёлчи. Препараты жёлчи способствует усилению образования жёлчи, стимулируют ее отток, усиливают секрецию сока поджелудочной железы, стимулируют моторику кишечника. Холензим* содержит жёлчи сухой 0,1 г, поджелудочной железы высушенной 0,1 г, слизистых оболочек тонких кишок убойного скота высушенного 0,1 г. В связи с наличием в препарате ферментов - трипсина и амилазы, помимо жёлчегонного эффекта при его приёме, отмечают стимуляцию процесса пищеварения.
К синтетическим холеретикам относят гимекромон, осалмид, никодин*, цикловалон и др. Гимекромон возбуждает рецепторы слизистой оболочки кишечника и тем самым усиливает секрецию жёлчи. Препарат повышает осмотический градиент между жёлчью и кровью, что приводит к возрастанию фильтрации в жёлчные канальцы электролитов и воды, снижению содержания холатов и противодействию камнеобразования. Гимекромон, помимо этого, является миотропным спазмолитиком и действует на желчевыводящие пути и их сфинктеров, не стимулирует моторику жёлчного пузыря и протоков. Препарат также не действует на гладкие мышцы сосудов и кишечника. Всасывается быстро, с белками крови связывается плохо, подвергается метаболизму в печени, экскретируется преимущественно через кишечник. Препарат применяют при дискинезиях жёлчного пузыря и желчевыводящих путей, холециститах, при неосложнённой желчнокаменной болезни и гепатитах с холестазом. Использование его не показано больным с гиперчувствительностью к гимекромону, при обострении язвенной болезни желудка и двенадцатиперстной кишки, при нарушении свёртываемости крови. При лечении иногда возникают диарея, боли в животе, головная боль, нарушается свёртываемость крови.
К холеретикам растительного происхождения относят алоэ древовидное*, барбарис обыкновенный*, валериану лекарственную*, душицу обыкновенную*, зверобой продырявленный*, календулу*, кукурузы рыльца*, шиповника плоды и многие другие средства, а также флаку-
мин*, конвафлавин*, берберина бисульфат* и др. Фламин* - сухой концентрат бессмертника, содержащий сумму флавоноидов. Желчегонный эффект достаточно выраженный. Кукурузы рыльца* (столбики с рыльцами, собранные в период созревания початков кукурузы) содержат ситостерол, стигмастерол, жирные масла, эфирное масло, сапонины и другие активные вещества. Установлено, что при лечении препаратами кукурузы увеличивается секреция жёлчи, уменьшается её вязкость и относительная плотность, уменьшается содержание билирубина. Берберина бисульфат* - алкалоид берберин, находящийся в корнях и листьях барбариса обыкновенного, по химическому строению относится к производным изохинолина, относят к четвертичным аммониевым основаниям. Помимо гипотензивного, обладает выраженным жёлчегонным средством и применяется при хроническом гепатите, холецистите. Желчегонным эффектом обладает также и настойка из листьев барбариса амурского.
Минеральные воды, содержащие преимущественно гидрокарбонаты, сульфаты, хлор и магний (Ессентуки ? 4 и ? 17, Джермук, Славяновская, Смирновская, Нарзан кисловодский, Нафтуся, Миргородская, Московская, Сочинская, Ростовская, Смоленская и др.) также обладают холеретической активностью.
Холекинетики. Эффект холекинетиков связан с повышением тонуса жёлчного пузыря и понижением тонуса жёлчных путей и сфинктера Одди. Практически все холекинетики обладают определённой холесекреторной активностью и противовоспалительным эффектом. К ним относят холекинетики растительного происхождения и синтетические холекинетики
Холекинетики растительного происхождения: берберина бисульфат* и др.
Синтетические холекинетики: осалмид, гидроксиметилникотинамид (никодин*), фенипентол (фебихол*). Осалмид стимулирует образование и выделение жёлчи, уменьшает ее вязкость, действует спазмолитически в отношении гладких мышц жёлчных протоков, в том числе сфинктеров, обладает гипохолестеринемическими свойствами, нормализует содержание билирубина. Гидроксиметилникотинамид, помимо желчегонного, обладает антимикробным действием. Препарат усиливает образование и выделение жёлчи. Антимикробный эффект обусловлен отщеплением в кишечнике формальдегидной части молекулы. Другая часть, никотинамид, реализует витаминную РР-активность. Формальдегид связывается с электрофильными субстратами, в том числе с микробными клетками, коагулирует их, а никотинамид повторяет в организме путь витамина РР и стимулирует желчевыделение. Фенипентол преимущественно холеретический препарат. Он возбуждает рецепторы
слизистой оболочки кишечника и рефлекторно стимулирует печёноч- ную секрецию, увеличивая количество выделяемой жёлчи, содержание в ней холестерина и жёлчных кислот, тем самым оптимизируя осмотический градиент между жёлчью и кровью. Кроме того, препарат усиливает осмотическую фильтрацию воды и электролитов в жёлчные протоки, тормозит образование жёлчных и холестериновых камней, стимулирует моторику желудка и кишечника. Не показан при острых заболеваниях печени, жёлчного пузыря, при механической желтухе.
Миотропные спазмолитики, такие, как папаверин , дротаверин (ношпа*), бенциклан (галидор*), пинаверия бромид (дицетел*), отилония бромид, тримебутин (дебридат*), способны ингибировать фосфодиэстеразу и блокировать аденозиновые рецепторы. Эти процессы изменяют ионный баланс и уменьшают накопление кальция в гладкомышечных клетках. Указанные эффекты приводят к снижению двигательной активности гладкой мускулатуры. Бенциклан, помимо действия на гладкую мускулатуру внутренних органов, обладает умеренным сосудорасширяющим и седативным эффектами, местноанестезирующей активностью. При приёме внутрь быстро и полностью абсорбируется. Максимальная концентрация в плазме крови достигается после однократного приёма в течение первых трёх часов. Период полувыведения шесть часов, элиминирует преимущественно с мочой (97%) в виде неактивных метаболитов. Может вызывать головокружения, головную боль, возбуждение, сухость во рту, тошноту, анорексию, диарею, тахикардию. Пинаверия бромид понижает повышенный тонус гладкой мускулатуры кишечника и желчевыводящих путей. Иногда способствует появлению диспепсических явлений. Отилония бромид избирательно расслабляет гладкую мускулатуру желудочно-кишечного тракта. При приёме внутрь абсорбируется около 5% дозы, выводится в основном с жёлчью и выделяется с каловыми массами. С осторожностью назначают при глаукоме и во время беременности.
Для быстрого купирования боли при дискинезиях желчевыводящих путей применяют нитраты, однако они малопригодны для длительного курсового лечения из-за кардиоваскулярных эффектов и других побочных проявлений.
Гепатопротекторные средства
Гепатопротекторные средства - это ЛС, повышающие устойчивость гепатоцитов к патологическим воздействиям и усиливающие обезвреживающие функции печени. К ним относят:
• ингибиторы перикисного окисления липидов;
• эссенциальные фосфолипиды;
• препараты растительного происхождения.
Ингибиторы перекисного окисления липидов - тиоктовая кислота (α-липоевая кислота*, берлитион 300*, тиогамма*, тиоктацид 600Т*, эспа-липон*). Тиоктовая кислота является коферментом окислительного декарбоксилирования пировиноградной кислоты и α-кетокислот, нормализует энергетический, углеводный и липидный обмен, регулирует метаболизм холестерина. При курсовом лечении улучшает функции печени, снижает повреждающее действие токсических экзогенных и эндогенных агентов. Препарат быстро всасывается из кишечника; Cmax достигается через 50 мин. Биодоступность около 30%, в печени окисляется и коньюгирует. Экскретируется преимущественно почками в виде неактивных метаболитов (80-90%); Т1/2 равен 20-50 мин. Общий плазменный клиренс 10-15 мл/мин. Иногда препарат вызывает гипогликемию, аллергические реакции; несовместим с растворами Рингера и глюкозы. При передозировке возможно появление головной боли, тошноты, рвоты.
Эссенциальные фосфолипиды содержаться в препарате эссенциале (эссенциале Н*, эссенциале форте Н*). Одна капсула препарата содержит «эссенциальных» фосфолипидов 300 мг, тиамина мононитрата 6 мг, рибофлавина 6 мг, пиридоксина гидрохлорида* 6 мг, цианокобаламина 6 мкг, никотинамида 30 мг, токоферола ацетата* 6 мг. Фосфолипиды, содержащиеся в препарате, - это диглицериновые фосфолипиды холинофосфорной кислоты, линолевой, линоленовой и других ненасыщенных жирных кислот. Поскольку эти вещества считают основными элементами клеточной структуры гепатоцита, то вместе с входящими в препарат витаминами при курсовом лечении они нормализуют метаболизм печени, улучшают ее детоксикационную функцию, оптимизируют микроциркуляцию в печени, уменьшают желтуху, положительно влияют на липидный спектр плазмы крови.
К гепатопротекторам растительного происхождения относят, прежде всего, препараты, содержащие алколоиды расторопши пятнистой [ге- патофальк планта, силибинин (карсил*), легалон 70* (силимарин*)], один из которых - силибинин, обладает ярко выраженными гепатопротекторными и антитоксическими свойствами. Механизм цитопротекции связан с подавлением перекисного окисления липидов, повреждающих мембраны печёночных клеток. Если гепатоцит уже поврежден, силибинин стимулирует синтез белков и фосфолипидов, восстанавливающих состав и физико-химические свойства клеточных мембран. Силибинин препятствует развитию фиброза, препятствует проникновению в печёночную клетку некоторых гепатотоксических ядов.
Абсорбция силибинина низкая. Подвергается энтеропечёночной циркуляции. Метаболизируется в печени путем коньюгации, Т1/2 ра-
вен 6 ч, экскретируется преимущественно с жёлчью в форме глюкуронидов и сульфатов. Не кумулирует. Препарат не показан больным с гиперчувствительностью к его компонентам. Силибилин иногда может вызывать диарею. Легалон 70*; одно драже содержит силимарина* 70 мг с минимум 30 мг силибинина в 90 мг расторопши пятнистой плодов экстракта (Carduus marianus, син. Silybum marianum). Гепатофальк планта содержит в одной капсуле сухой экстракт расторопши пятнистой, экстракт чистотела большого и турмерика яванского.
Холелитолитические средства
Известно, что холестерин растворяется в жёлчи под действием жёл- чных кислот. В случаях, при которых содержание холестерина превышает содержание жёлчных кислот и лецитина, возможен процесс его кристаллизации и образование жёлчных камней, а одним из способов борьбы с камнеобразованием считают снижение его концентрации в жёлчи. Положительным холелитолитическим эффектом (способность растворять жёлчные камни) при достаточно длительном курсовом применении обладают хенодеоксихолевая кислота и урсодезоксихолевая кислота, имеющие модифицированную структуру жёлчных кислот.
Эти препараты увеличивают гидрофильность жёлчи. Они препятствуют кристаллизации и выпадению в осадок холестерина и способствуют растворению холестериновых камней. Поскольку воспалительные процессы в жёлчном пузыре способствуют кристаллизации холестерина и нарушению минерального состава жёлчи, применение антимикробных средств в этих случаях является профилактикой холелитиаза.
Хенодеоксихолевую и урсодеоксихолевую кислоты изготовляют полусинтетическим путём из животной жёлчи за счёт хенодезоксихолевой, кетолитохолевой и других жёлчных кислот. Препараты угнетают активность 3-гидрокси-3-метил-глутарил-коэнзим А-редуктазы, что уменьшает общий синтез холестерина вследствие субстратного блока его печёночного метаболизма, облегчает работу печени и способствует выведению холестерина из организма. При этом холестерин не только не выпадает в осадок в желчевыводящих путях, но и растворяется из уже сформировавшихся камней. В дозе 20 мг/кг в день (на три при- ёма, после еды) хенодезоксихолевая кислота способна растворять в жёлчном пузыре конкременты, содержащие холестерин, со скоростью 0,5-1,0 мм (по диаметру) в месяц.
Для проведения холелитолитической терапии необходимы следующие условия:
• камни в жёлчном пузыре должны быть только холестериновыми и диаметром не более 2 см;
• полноценность сократительной функции жёлчного пузыря при объёме жёлчных камней менее 30% объёма жёлчного пузыря;
• отсутствие противопоказаний для подобной терапии: активные гепатиты и циррозы печени, язвенная болезнь желудка и двенадцатиперстной кишки, поражение почек;
• длительность лечебного курса от 4 мес до 2 лет.
20.6. ИНГИБИТОРЫ ПРОТЕОЛИЗА
К препаратам, ингибирующим протеолитические ферменты в плазме и тканях, относятся апротинин (гордокс*, контрикал*, трасилол 500 000*). Этот препарат подавляет активность трипсина, плазмина и других протеаз, что приводит к снижению активности фактора Хагемана и блокированию перехода калликреиногена в калликреин. Вышеуказанные биологически активные вещества способствуют развитию тяжёлых некротических изменений поджелудочной железы при ее остром воспалении. Следствием действия антиферментов считают подавление образования кининов (брадикинина в плазме крови и калликреина в тканях), вызывающих нарушение микроциркуляции, вазодилатацию, повышающих проницаемость сосудов.
Апротинин - вещество полипептидной природы, панкреатический ингибитор трипсина. Его получают из лёгких крупного рогатого скота. Ингибирует протеолитические ферменты: трипсин, химотрипсин, калликреин, в том числе активирующий фибринолиз - плазмин. Применяют для лечения больных с острым панкреатитом, при гиперфибринолитических кровотечениях, для лечения и профилактики различных форм шока (эндотоксического, травматического, гемолитического).
После внутривенного введения препарат быстро распределяется во внеклеточном пространстве. Кратковременно накапливается в печени. Период полувыведения из плазмы крови около 150 мин. Распадается под действием лизосомальных ферментов почек и выводится с мочой.
20.7. ЛЕКАРСТВЕННЫЕ СРЕДСТВА, ПРИМЕНЯЕМЫЕ ПРИ ДИАРЕЕ
Диарея (понос) - частое или однократное опорожнение кишечника с выделением жидких каловых масс более 250 г/сут. Любая диарея - это клиническое проявление нарушения всасывания воды и электролитов в кишечнике. В патогенезе диареи участвуют четыре механизма: кишечная гиперсекреция, повышение осмотического дав-
ления в полости кишки, нарушение транзита кишечного содержимого и кишечная гиперэкссудация. Диарея считается острой, если ее продолжительность не превышает 2-3 нед, и хронической - если она длится 4-6 нед и более.
В связи с многообразием этиологии и патогенеза диареи в терапевтической практике используется весьма значительное количество лекарственных средств, разнообразных как по химической структуре, так и по механизму воздействия. Тактика их применения зависит от выраженности основного и сопутствующих заболеваний у данного больного. Ниже приведены характеристики основных групп ЛС, используемых при лечении больных с диареей.
Антибактериальные препараты, такие, как интетрикс*, нифуроксазид (эрсефурил*), дипендал-м, энтероседив*, применяют при диарее бактериальной этиологии. Интетрикс* содержит тилихинол н-додецил сульфат, тилброхинол; депендал-м - фуразолидон и метронидазол; энтероседив* - стрептомицин, менадиона натрия бисульфит и натрия цитрат.
Бактериальные препараты, такие, как бактисубтил*, энтерол*, хилак форте*, также обладают антидиарейной активностью. Бактисубтил* представляет собой культуру бактерий IP-5832 в виде спор, карбонат кальция, белую глину, окись титана и желатин; энтерол* содержит лиофилизированную культуру Saecharamyces doulardii; хилак форте* содержит стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочную кислоту, лактозу, аминокислоты, жирные кислоты.
Адсорбирующие средства. Смекта (смектит) содержит смектит диоктаэдрический, обладающий сильными адсорбирующими свойствами. Препарат стабилизирует слизистый барьер, восполняя его дефекты, образуя поливалентные связи с гликопротеинами слизи; защищает слизистую оболочку желудка и кишечника от отрицательного действия ионов водорода, соляной кислоты, жёлчных солей, вирусов, бактерий, других агрессивных факторов.
Аттапулгит (каопектат*) - природный очищенный алюминиево-магниевый силикат в коллоидной форме (природная смесь из группы палигорскитных минералов). Обладает противодиарейным, адсорбирующим, обволакивающим лечебными свойствами. После приёма внутрь не всасывается, образует на слизистой оболочке желудка и кишечника своеобразную плёнку. Адсорбирует жидкость, токсические вещества, бактерии, уменьшает воспалительную реакцию, нормализует кишечную флору. Не показан детям до 6 лет, лицам с гиперчувствительностью к этому препарату или больным с амебной дизентерией. При употреблении с другими лекарственными средствами может нарушать их всасывание.
Таннакомп* содержит альбуминат таннина, лактат этакридина. Оказывает вяжущее, противомикробное, противодиарейное и противовоспалительное действие. Особенно показан при лечении больных с неспецифической диареей (понос путешественника, изменение характера питания, внезапная смена климатических условий и пр.).
Регуляторы двигательной активности желудка и кишечника. Лоперамид (имодиум*) обладает противодиарейной активностью, взаимодействует с опиатными рецепторами продольных и кольцевых мышц стенки кишечника, ингибирует высвобождение ацетилхолина и простагландинов. Препарат замедляет перистальтику и движение кишечного содержимого. В кишечнике всасывается около 40% полученной больным дозы, с белками плазмы связывается до 95% препарата. Cmaxдостигается через 5 ч. Не проникает через гематоэнцефалический барьер, метаболизируется в печени, Т1/2 от 9 до 14 ч, выводится с калом и мочой. Не показан больным с гиперчувствительностью к препарату, при кишечной непроходимости, в I триместре беременности. Может вызывать головную боль, усталость, задержку стула.
Октреотид - синтетический октапептид, аналог соматостатина. Считают ингибитором синтеза активных секреторных агентов, в том числе пептидов и серотонина. Способствует снижению секреции и двигательной активности кишечника. После подкожного введения быстро всасывается, Cmaxдо 5,2 мг/мл при дозе 100 мкг достигается в течение 25- 30 мин, 65% введённой дозы связывается в плазме с липопротеинами и, в меньшей степени, с альбуминами. Т1/2 после инъекции составляет 100 мин, длительность действия около 12 ч. С мочой экскретируется 32% неизменённого препарата. Противопоказан при беременности.
Лекарственные растения: анис обыкновенный*, бессмертник песчаный*, девясил высокий*, душица обыкновенная*, зверобой продырявленный*, кориандра плоды, коровяк обыкновенный*, лапчатка прямостоячая*, мать-и-мачеха обыкновенная*, мелисса лекарственная*, ромашка аптечная*, солодка голая*, сушеница топяная*, тысячелистник обыкновенный*, черника*, черёмуха обыкновенная* и другие также обладают антидиарейной активностью.
20.8. СЛАБИТЕЛЬНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА
Под запором подразумевают замедленное, затруднённое, редкое или систематически неполное опорожнение кишечника с твёрдыми, как правило, каловыми массами. Наиболее частые причины -нару- шения процессов формирования каловых масс и их пассажа по толстой кишке:
• расстройство моторной функции (дискинезия) толстой кишки;
• ослабление естественных позывов на дефекацию;
• изменения анатомической структуры толстой кишки или окружающих ее тканей, препятствующие нормальному продвижению кала.
Запор подразделяют на первичный, вторичный, идиопатический. Причиной первичного запора являются аномалии, пороки развития толстой кишки и ее иннервации. Причиной вторичного запора служат заболевания и повреждения ободочной кишки, а также болезни других органов и систем, протекающие с метаболическими нарушениями. Идиопатический запор обусловлен нарушением двигательной активности прямой и ободочной кишки, причина которой неизвестна, например, инертная кишка, идиопатический мегаколон.
С патогенетических позиций запор может быть разделен на три основных типа: алиментарный, механический и дискинетический.
При лечении больных с запорами используют следующие группы
ЛС:
• осмотические слабительные;
• лекарственные средства, тормозящие абсорбцию воды из кишечника;
• синтетические слабительные;
• солевые слабительные;
• средства, вызывающие увеличение объёма каловых масс;
• средства, смягчающие каловые массы;
• лекарственные средства, стимулирующие кишечный транзит.
Осмотические слабительные, содержащие плохо всасывающиеся углеводы: лактулоза (нормазе*, дюфалак*) или высокомолекулярные полимеры, способствующие задержке воды - макрогол (форлакс*). Они повышают осмотическое давление химуса в тонкой кишке и способствуют секреции воды в ее просвет.
Лактулоза - синтетический полисахарид, снижает концентрацию ионов аммония в крови на 25-50% и уменьшает выраженность гепатогенной энцефалопатии; стимулирует размножение молочнокислых бактерий и перистальтику толстой кишки, действуя послабляюще. В кишке лактулоза гидролизируется до молочной и муравьиной кислот, причём увеличивается осмотическое давление, подкисляется содержимое кишки, улучшается ее опорожнение. Действие наступает через 24-48 ч после введения; в кровь всасывается незначительно, с мочой выводится около 3% введённой дозы препарата. Лактулоза противопоказана лицам с повышенной к этому препарату чувствительностью. В качестве побочных эффектов может отмечаться диарея, метеоризм, избыточная потеря электролитов.
Макрогол (форлакс*) образует водородные связи с молекулами воды в просвете кишечника, увеличивает осмотическое давление в кишечнике и объём содержащейся в нем жидкости, усиливает перистальтику и действует послабляюще. Не абсорбируется и не подвергается метаболизму; слабительный эффект наступает через 24-48 ч. Иногда возможно появление коликообразных болей в нижних отделах живота и диареи.
Лекарственные средства, тормозящие абсорбцию воды из кишечника
и стимулирующие секрецию путём раздражения хеморецепторов слизистой оболочки преимущественно толстой кишки (антрагликозиды). К ним относят препараты сенны листьев* (сеннозиды А и Б; бекунис*, регулакс*, тисасен*) и сабура, ревеня корень*, крушины слабительной плоды, крушины ольховидной кора, касторовое масло.
Препараты сенны содержат сумму антрагликозидов из листьев сенны остролистной и узколистной. Слабительный эффект обусловлен торможением абсорбции ионов натрия, воды и стимуляцией секреции натрия и воды в просвет кишечника за счёт увеличения концентрации простагландина Е2 в его стенке. Это приводит к увеличению объё- ма кишечного содержимого и усилению моторики кишечника. После приёма внутрь эффект развивается через 8-10 ч. Препараты не всасываются и резорбтивного действия не оказывают.
Ревеня дальневидного корни содержат антрагликозиды и таногликозиды, а также их свободные агликоны: реумэмодин, хризофанол, реин и другие; хризофановую кислоту, смолы, красящие вещества. Слабительное действие наступает через 8-10 ч после приёма внутрь и обусловлено главным образом эмодином, реином и хризофановой кислотой, которые, раздражая рецепторы слизистой оболочки толстого кишечника, вызывают усиление его перистальтики и более быстрое прохождение каловых масс.
Крушины слабительной плоды (жостера слабительного плоды*) содержат свободные и гликозидно связанные антрахиноны и антранолы: рамноэмодин, рамнокатартин; сахара, пектины; слизистые, красящие вещества; флавоноиды; горечи негликозидные. Рамноцитрин, ксанторамнетин, кемпферол обеспечивают, помимо слабительного, и противовоспалительное действие.
Крушины ольховидной кора содержит антрагликозиды: франгулин; кликофрангулин, франгулаэмодин; хризофановую кислоту, а также дубильные вещества, органические кислоты, эфирное масло, сахара, алкалоиды. Слабительное действие крушины обусловлено в первую очередь антрагликозидами и хризофановой кислотой.
Касторовое масло получают из семян клещевины. При приёме внутрь оно расщепляется липазой в тонком кишечнике с образова-
нием рицинолевой кислоты, вызывающей раздражение рецепторов кишечника, причём на всем его протяжении, и усиливающей перистальтику. Слабительный эффект наступает через 5-6 ч.
Синтетические слабительные. Бисакодил (дульколакс*) представляет собой синтетическое слабительное средство, обладающее также ветрогонным действием. Этот препарат раздражает рецепторы слизистой оболочки толстой кишки, тем самым повышая продукцию слизи, ускоряет и усиливает перистальтику. Противопоказан больным с острыми воспалительными заболеваниями брюшной полости.
Натрия пикосульфат (гутталакс*) гидролизируется в кишечнике под влиянием сульфатпроизводящих бактерий и образует свободный дифенол (активный метаболит), раздражающий рецепторы слизистой оболочки толстой кишки и стимулирующий перистальтику. Не всасывается, слабительный эффект наступает через 6-12 ч. Не рекомендуют назначать лицам с повышенной чувствительностью к препаратам сенны, при острых заболеваниях органов пищеварения. Может вызывать непродолжительные коликообразные боли в животе.
Солевые слабительные, такие, как натрия сульфат, магния сульфат, карловарская соль исскуственная*, медленно всасываясь из кишечника, изменяют в его полости осмотическое давление, что приводит к накоплению воды, разжижению каловых масс и усилению их пропульсии. Некоторую роль играет раздражение рецепторов слизистой оболочки кишечника. Солевые слабительные в отличие от антрагликозидов действуют на всем протяжении кишечника. Показаны они и при пищевых токсикоинфекциях, поскольку замедляют поступление токсинов в кровь.
Средства, вызывающие увеличение объёма каловых масс. К этим ЛС относят неабсорбируемые дисахариды (сорбитол), ламинарию* (ламинарид* ), метилцеллюлозу, псиллиум (фиберлак), поликарбофил кальция, отруби, льняное семя. Ламинария* (морская капуста) - бурая водоросль, встречаемая в виде зарослей вдоль Дальневосточного побережья, в Белом и Черном морях. Слабительное свойство обусловлено способностью водоросли интенсивно набухать в просвете кишечника, увеличиваясь в объёме, раздражать рецепторы слизистой оболочки и тем самым способствовать ускорению опорожнения кишечника. Препарат не показан лицам, имеющим повышенную чувствительность к йоду.
Средства, смягчающие каловые массы облегчают их продвижение по кишечнику. К ЛС из этой группы относят вазелиновое*, миндальное*, оливковое масла*, норгалакс*, натрия фосфат (энимакс эпима*).
Лекарственные средства, стимулирующие кишечный транзит. К этой группе ЛС относят пшеничные отруби, дивизит, мукофальк*. Му-
кофальк* - гранулы для приготовления пероральной суспензии с запахом яблока или апельсина. Это гидрофильные волокна из наружной оболочки семян подорожника. Гидрофильные волокна способны удерживать воду в количествах, значительно превышающих их массу. Препарат предотвращает сгущение кишечного содержимого и тем самым облегчает опорожнение кишечника. Практически не всасывается.
20.9. ПРОКИНЕТИКИ
Прокинетики - препараты, нормализующие двигательную активность пищевода, желудка и кишечника. К ним относят следующие ЛС: метоклопрамид, домперидон, цизаприд, тегасерод и прукалоприд, (сравнительная характеристика приведена в табл. 20-10).
Таблица 20-10. Сравнительная характеристика основных прокинетических препаратов
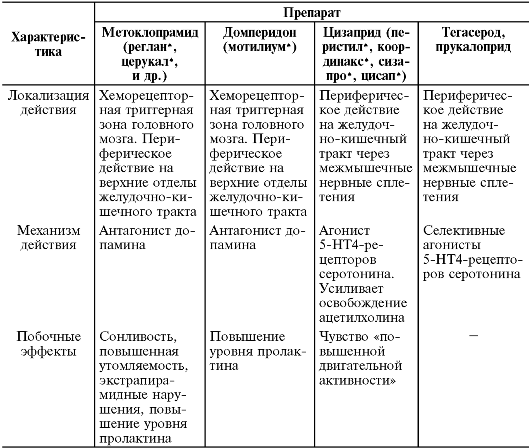 Наиболее широко эти препараты используются при следующих заболеваниях:
Наиболее широко эти препараты используются при следующих заболеваниях:
• дискинезии пищевода, рефлюкс-эзофагит;
• функциональные расстройства желудка, неязвенная (функциональная) диспепсия;
• синдром раздражённого кишечника;
• антиперистальтическая дискинезия желудка и двенадцатиперстной кишки, сопровождающаяся тошнотой и рвотой;
• послеоперационные расстройства моторной функции желудка и кишечника;
• органические заболевания органов пищеварительной системы, при которых вторичные расстройства моторики начинают доминировать в клинической картине болезни (гастриты, язвенная болезнь, энтериты, колиты, холециститы и пр.).
Метоклопрамид. Препарат является антагонистом дофамина, нормализует нарушенную двигательную активность гладкомышечного аппарата желудочно-кишечного тракта, повышает тонус нижнего пищеводного сфинктера, усиливает тонус и амплитуду перистальтических волн желудка, способствует движению кишечного содержимого по верхним отделам тонкого кишечника, действует антиспастически, способствует прекращению тошноты и рвоты (см. выше). Широко применяют при рефлюкс-эзофагите, функциональных моторных расстройствах желудка и кишечника.
Метоклопрамид быстро всасывается из кишечника, достигая максимума концентрации в плазме крови через 1-2 ч после приё- ма разовой дозы. До 30% препарата связывается с белками крови, после чего он быстро распределяется по тканям организма. Эффект сохраняется на протяжении 1-2 ч; период полувыведения около 5- 6 ч. До 85% метоклопрамида выводится с мочой.
Противопоказания: повышенная чувствительность пациента к препарату, глаукома, феохромоцитома, экстрапирамидные расстройства, беременность. При продолжительном приёме метоклопрамида могут возникать сухость во рту, диарея, повышенная сонливость, экстрапирамидные нарушения, иногда кожные высыпания.
Домперидон. Препарат блокирует центральные дофаминовые (D2) рецепторы, увеличивает продолжительность перистальтических сокращений антрального отдела желудка и двенадцатиперстной кишки, нормализует функцию нижнего пищеводного сфинктера, способствует движению желудочного и кишечного содержимого, уменьшает проявления тошноты и рвоты (см. выше). Применяют при нарушениях двигательной активности пищевода, желудка и начальных отделов кишечника. Было показано, что домперидон, в сравнении с другими про-
кинетиками, лучше нормализует моторику пищевода, гладких мышц желудка и начальных отделов кишечника. Он более эффективен при лечении больных с анорексией, тошнотой, рвотой, болями в животе, раннем насыщении, вздутии живота, особенно у лиц с диабетической гастропатией.
Общепризнано, что метоклопрамид и домпериодон остаются весьма эффективными и значимыми ЛС в лечении дискинезий желудка и кишечника в педиатрической практике. Метоклопрамид в подобной ситуации менее удобен, поскольку иногда вызывает сонливость, астению.
Домпериодон быстро всасывается из желудочно-кишечного тракта. Максимум концентрации в крови достигается через один час. С белками крови связывается до 90% препарата. Плохо проникает через гематоэнцефалический барьер. Период полувыведения составляет 7-9 ч. С мочой выделяется 31% метаболитов домперидона ; с каловыми массами - 66%. Не рекомендуют назначать препарат лицам с повышенной чувствительностью к нему, при желудочно-кишечных кровотечениях, непроходимости кишечника, беременности. Иногда у пациента во время приёма препарата могут возникать головная боль, головокружение, сухость во рту, задержка стула, крапивница.
Цизаприд. Препарат возбуждает серотониновые рецепторы и тем самым способствует более быстрому высвобождению ацетилхолина из холинергических нейронов мезентериального сплетения. Это ведет к повышению чувствительности к нему м-холинорецепторов гладкой мускулатуры органов ЖКТ, что, в свою очередь, стимулирует тонус и двигательную активность пищевода, желудка и кишечника, нормализует деятельность сфинктеров желудочно-кишечного тракта, способствует пропульсии пищи из желудка и химуса в кишечнике.
Цизаприд быстро всасывается из кишечника, достигая максимальной концентрации в плазме крови через 1,0-1,5 ч. Биодоступность 35-40%. С белками крови, преимущественно альбумином, связывается на 97-98%. В печени подвергается интенсивному N-деалкилирова- нию при участии изофермента 3А4 цитохрома P-450 и превращается в неактивный метаболит норцизаприд. В неизменённом виде с мочой и калом выводится около 10% препарата. Антихолинэстеразные препараты и м-холиномиметики усиливают эффект, циметидин ускоряет абсорбцию. Кетоконазол, эритромицин, кларитромицин увеличивают концентрацию цизаприда в крови, что повышает риск развития аритмии.
Наиболее широко применяют цизаприд при лечении больных с дискинезиями пищевода, желудка и кишечника, вызыванными многими причинами, встречаемыми как в качестве первичного заболевания,
так и вторичного, например, рефлюкс-эзофагит, неязвенная диспепсия, синдром раздражённого кишечника и др.
При применении цизаприда могут возникнуть такие побочные эффекты: как головокружение, экстрапирамидные расстройства, судорожные подергивания мышц, сонливость, головная боль, эпизодические нарушения сердечного ритма, тошнота, рвота и ряд других.
Противопоказанием к применению цизаприда считают следующие заболевания: гиперчувствительность к препарату; острые заболевания органов пищеварительной системы: желудочно-кишечное кровотечение; непроходимость кишечника; перфорация желудка или кишечника; беременность и период грудного вскармливания.
У цизаприда выявлена способность в редких случаях удлинять интервал Q-T на электрокардиограмме, на фоне чего могут возникнуть опасные для жизни нарушения ритма (желудочковая тахикардия «пируэт»). Полагают, что этот эффект цизаприда в подавляющем большинстве случаев обусловлен нерациональным его использованием: передозировка препарата, сочетание с ЛС, угнетающими активность изофермента цитохрома P-450 CYP3A4 (макролидные антибиотики). Отрицательные эффекты цизаприда могут возникать при низком содержании в крови кальция, калия, магния; при глубоких нарушениях функции печени; при врожденном Q-T-синдроме.
Необходима осторожность при назначении цизаприда недоношенным младенцам в течение трёх месяцев после рождения.
20.10. ЛЕКАРСТВЕННЫЕ СРЕДСТВА, ПРИМЕНЯЕМЫЕ ПРИ ДИСБАКТЕРИОЗЕ КИШЕЧНИКА
Дисбактериоз - состояние, характеризуемое нарушением подвижного равновесия кишечной микрофлоры с появлением значительных количеств микробов в тонком кишечнике и изменением микробного состава толстой кишки. Крайней степенью дисбактериоза кишечника считают появление бактерий желудочно-кишечного тракта в крови (бактериемия) или даже развитие сепсиса.
Сам по себе дисбактериоз не самостоятельное заболевание. Он возникает при нарушении кишечного пищеварения, дискинезии желудка и кишечника, изменениях местного иммунитета, при применении антибиотиков и других лекарственных препаратов, при ряде заболеваний желудка и кишечника, после оперативных вмешательств и др. Признаки дисбактериоза в различных сочетаниях обнаруживают практически у всех больных с хроническими заболеваниями кишечника, при опре- делённых изменениях в питании и воздействии некоторых факторов
окружающей среды. По своей сути дисбактериоз кишечника - это бактериологическое понятие, а не нозологическая форма.
При лечении больных дисбактериозом кишечника используются разнообразные лекарственные средства. К ним относятся следующие препараты.
• Противогрибковые препараты: тетрациклины, пенициллины, цефалоспорины, фторхинолоны, метронидазол, интетрикс*, эрсефурил*, фуразолидон; сульфаниламидные препараты (фталазол*, сульгин*).
• Антигрибковые препараты.
• Бактериальные препараты: бифидобактерии бифидум (бифидумбактерин*), бифиформ*, лактобактерии ацидофильные (лактобактерин*), бактисубтил*, линекс*, энтерол* и др.
• Продукты микробного метаболизма: хилак форте*.
• Регуляторы пищеварения и двигательной активности кишечника: ферментативные препараты и препараты, содержащие компоненты жёлчи (панзинорм форте-Н*, дигестал*, фестал*, энзистал* и др.); ветрогонные препараты; препараты, восстанавливающие нарушенную пропульсивную функцию кишечника (лоперамид, тримебутин).
• Иммуномодуляторы: тимуса экстракт (тактивин*, тималин*), тимоген*, иммунал* и др.
• Лекарственные растения и препараты природного происхождения.
• Слабительные средства.
• Антидиарейные средства.
Характеристика и клинико-фармакологические особенности данных лекарственных средств, в основном, описаны выше. Более подробно мы остановимся на бактериальных препаратах и препаратах микробного метаболизма, используемых для нормализации микрофлоры кишечника.
Бактисуптил*. Одна капсула содержит не менее 1 млрд чистой сухой культуры бактерии штамма IP 5832 с вегетативными спорами. При поступлении в кишечник способствует коррекции физиологического равновесия микрофлоры. Вегетативные формы бактерий, содержащихся в препарате, высвобождают энзимы, которые расщепляют углеводы, жиры, белки, и в создаваемой ими кислой среде препятствуют процессам гниения. Помимо этого, бактисуптил оптимизирует процессы синтеза витаминов группы В и Р в кишечнике.
Бифидумбактерин*. Выпускают в пакетиках из алюминиевой фольги. Один пакетик содержит 5х108 КОЕ лиофильно высушенных микробных клеток живых бифидобактерий антагонистически активного
штамма Bifidobacterium bifidum N 1, очищенного от среды культивирования, и 0,85 лактозы-бифидогенного фактора. Бифидумбактерин* в данном случае - антагонист большинства патогенных и условнопатогенных микроорганизмов толстой кишки. Помимо этого, препарат стимулирует процесс пищеварения, повышает неспецифическую резистентность организма. Он показан при терапии больных с дисбактериозом кишечника, который возник при применении антибиотиков, гормонов; при проведении лучевой и химиотерапии; у больных в послеоперационном периоде; при синдроме раздражённого кишечника и других заболеваниях толстой кишки. У взрослых применяется по 1-2 пакетика 3 раза в день; содержимое перемешивается с жидкой частью пищи комнатной температуры.
Бифиформ*. Капсулы препарата, которые растворяются в кишечнике, содержат не менее 107 бифидум бактерий, а также 107 энтерококков. Применяется препарат по 1-2 капсулы в день во время еды.
Хилак форте*. 100 мл капель для приёма внутрь содержат беззародышевый водный субстрат продуктов обмена веществ бактерий Escherichia coli DSM 4087, Streptococcus faecalis DSM 4086, Lactobacillus acidophilus DSM 4149, Lactobacillus helveticus DSM 4149 и другие необходимые компоненты. Препарат нормализует микрофлору кишечника, воздействует на синтез эпителиальных клеток слизистой оболочки, нормализует рН среды толстой кишки и водно-электролитный баланс. Применяется при дисбактериозе кишечнка, вызванном разнообразными причинами.
Линекс. Одна капсула препарата содержит 1,2х107 молочнокислых лиофилизированных бактерий. Молочнокислые бактерии, входящие в состав препарата, продуцируют молочную кислоту и, в меньшей степени, уксусную и пропиленовую. Они участвуют в резорбции моносахаридов, стабилизируют мембраны клеток кишечного эпителия, регулируют всасывание электролитов. Закисление просвета кишечника замедляет рост патогенных и условно-патогенных микроорганизмов. В целом, при курсовом лечении линексом нормализуется кишечная микрофлора. Доза для взрослых составляет 2 капсулы 3 раза в день.