Клиническая фармакология.: учебник для вузов / Под ред. В.Г. Кукеса.- 4-е издание., перераб. и доп., - 2009. - 1056 с.
|
|
|
|
ГЛАВА 14. ИНОТРОПНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА
Сократительная функция миокарда - одно из ключевых звеньев системы кровообращения. Сократимость обусловлена взаимодействием сократительных белков миокарда и ионов кальция цитозоля. Выделяют следующие основные патофизиологические подходы усиления сократимости.
• Увеличение внутриклеточного содержания ионов кальция.
• Повышение чувствительности сократительных белков к ионам кальция.
Первый подход можно реализовать с помощью следующих механизмов (рис. 14-1).
• Угнетение Na+, К+-зависимой АТФазы и замедление обмена ионов натрия и калия. К препаратам, действующим подобным образом, относят сердечные гликозиды.
• Повышение концентрации цАМФ при β-адренергической стимуляции (добутамин, допамин) или ингибировании фосфодиэстеразы (милринон* амринон*). цАМФ активирует протеинкиназы, фосфорилирующие белки потенциалзависимых кальциевых каналов, что увеличивает поступление ионов кальция внутрь клетки.
Повышение чувствительности сократительных белков кардиомиоцитов к ионам кальция отмечают при назначении новой группы инотропных препаратов - «сенситизаторов кальция» (левосимендан).
14.1. СЕРДЕЧНЫЕ ГЛИКОЗИДЫ
Благодаря отрицательному хронотропному, нейромодулирующему и положительному инотропному эффектам сердечные гликозиды часто применяют при сердечной недостаточности. За более чем 200-лет- ний период использования интерес к данной группе препаратов угасал и снова усиливался. Даже в настоящее время некоторые аспекты клинического использования сердечных гликозидов остаются неуточнён- ными, поэтому история изучения этих ЛС продолжается.
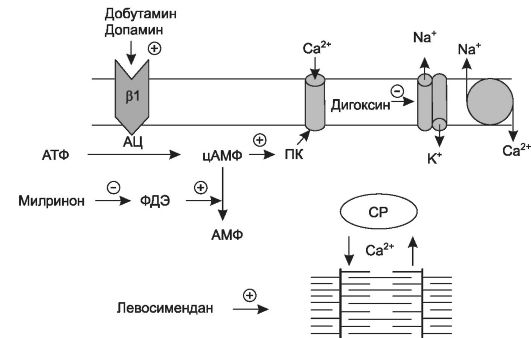 Рис. 14.1. Механизм
действия препаратов с положительным инотропным эффектом. АЦ -
аденилатциклаза, ПК - протеинкиназа, ФДЭ - фосфодиэстераза, СР -
саркоплазматический ретикулум.
Рис. 14.1. Механизм
действия препаратов с положительным инотропным эффектом. АЦ -
аденилатциклаза, ПК - протеинкиназа, ФДЭ - фосфодиэстераза, СР -
саркоплазматический ретикулум.
Классификация
Традиционно сердечные гликозиды подразделяют на полярные (гидрофильные) и неполярные (липофильные). Полярные (гидрофильные) сердечные гликозиды хорошо растворяются в воде, но плохо в липидах, недостаточно адсорбируются в ЖКТ, мало связываются с белками плазмы крови, почти не подвергаются биотрансформации и выделяются в основном почками. К этой группе сердечных гликозидов относят строфантин-К, ацетилстрофантин* и ландыша гликозид.
Более липофильные препараты лучше всасываются в ЖКТ, больше связываются с белками крови и метаболизируются в печени. По нарастанию липофильности сердечные гликозиды можно расположить следующим образом: ланатозид Ц , дигоксин , метилдигоксин , дигитоксин.
В клинической практике в настоящее время, как правило, назначают дигоксин, ланатозид Ц и строфантин-К. Дигитоксин редко используют из-за длительного периода полувыведения. Фармакодинамические эффекты ландыша гликозида среди препаратов сердечных гликозидов наименее выражены. Строфантин-К применяют в стационарных условиях. Таким образом, наиболее широко в клинической практике используют дигоксин. Метилдигоксин отличается от дигок-
сина более полной абсорбцией, однако это существенно не влияет на основные фармакодинамические параметры, поэтому метилдигоксин практически не применяют.
Механизм действия и основные фармакодинамические эффекты
Механизм действия сердечных гликозидов заключается в торможении Na+, К+-зависимой АТФазы, что приводит к увеличению внутриклеточного содержания ионов натрия, которые обмениваются на ионы кальция. В результате этих изменений повышается внутриклеточная концентрация ионов кальция в саркоплазматическом ретикулуме. При возникновении потенциала действия больше ионов кальция выходит в цитозоль кардиомиоцитов и взаимодействует с тропонином C. Конечным итогом действия сердечных гликозидов служит повышение количества активных участков актина, доступных для связи с другим сократительным белком - миозином, что сопровождается усилением сократимости кардиомиоцитов. В то же время из-за повышения содержания ионов кальция и снижения концентрации ионов калия в клетках миокарда в определённых ситуациях развивается электрическая нестабильность кардиомиоцитов, что проявляется различными аритмиями (положительный батмотропный эффект).
Положительный инотропный эффект сердечных гликозидов заключается в увеличении силы и скорости сокращения миокарда. В результате увеличения контрактильности миокарда увеличиваются ударный и минутный объёмы кровообращения. Из-за уменьшения конечно-систолического и конечно-диастолического объёмов сердца сокращаются его размеры и сокращается потребность данного органа в кислороде.
Отрицательный дромотропный эффект сердечных гликозидов проявляется в удлинении рефрактерного периода атриовентрикулярного узла, поэтому количество импульсов, проходящих через это соединение за единицу времени, снижается. Благодаря данному эффекту сердечные гликозиды назначают при мерцательной аритмии. При мерцании предсердий к атриовентрикулярному узлу поступает 400- 800 импульсов в минуту, однако в желудочки проходит только 130- 200 импульсов (в зависимости от возраста и функционального состояния атриовентрикулярного узла этот диапазон может быть шире и достигать 50-300 импульсов в минуту). Сердечные гликозиды увеличивают рефрактерный период и снижают «пропускную способность» атриовентрикулярного узла до 60-80 в минуту. При этом диастола удлиняется, в результате чего улучшается наполнение желудочков и, следовательно, увеличивается сердечный выброс.
У пациентов с атриовентрикулярной блокадой при назначении сердечных гликозидов возможно дальнейшее ухудшение атриовентри-
кулярной проводимости и появление приступов Морганьи-Адамса- Стокса. При мерцательной аритмии в сочетании с синдромом Воль- фа-Паркинсона-Уайта сердечные гликозиды, удлиняя время прохождения возбуждения через атриовентрикулярное соединение, уменьшают рефрактерный период добавочных путей проведения импульсов в обход атриовентрикулярного узла, что сопровождается возрастанием числа импульсов, проведённых на желудочки.
Отрицательный хронотропный эффект сердечных гликозидов характеризуется уменьшением ЧСС из-за снижения автоматизма синусового узла. Это происходит в результате повышения тонуса блуждающего нерва при стимуляции барорецепторов дуги аорты и каротидного синуса.
В последние годы большое значение придают нейромодулирующему действию сердечных гликозидов, развивающемуся при приёме препаратов даже в низких дозах. При этом отмечают угнетение активности симпатоадреналовой системы, что проявляется уменьшением содержания норадреналина в плазме крови. При ингибировании Na+, К+-зависимой АТФазы в клетках эпителия почечных канальцев снижается реабсорбция ионов натрия и повышается концентрация данных ионов в дистальных канальцах, что сопровождается уменьшением секреции ренина.
Фармакокинетика
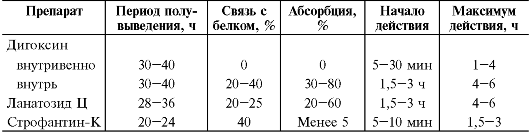
Абсорбция дигоксина во многом зависит от активности транспортного белка энтероцитов гликопротеина P, который «выбрасывает» препарат в просвет кишки. Метаболизм сердечных гликозидов в печени зависит от полярности ЛС (этот показатель выше у липофильных препаратов) (табл. 14-1). Вследствие этого биодоступность дигоксина составляет 50-80%, а ланатозида Ц - 15-45%.
Таблица 14-1. Основные фармакокинетические параметры сердечных гликозидов
 Попадая
в кровь, сердечные гликозиды связываются с белками плазмы крови в
различной степени. Наибольшее сродство к белкам плазмы крови отмечают у
низкополярных, а наименьшее - у полярных сердечных гликозидов.
Попадая
в кровь, сердечные гликозиды связываются с белками плазмы крови в
различной степени. Наибольшее сродство к белкам плазмы крови отмечают у
низкополярных, а наименьшее - у полярных сердечных гликозидов.
Сердечные гликозиды имеют большой объём распределения, т.е. накапливаются в основном в тканях. Например, объём распределения дигоксина составляет около 7 л/кг. Это связано с тем, что препараты этой группы связываются с Na+, К+-зависимой АТФазой скелетной мускулатуры, поэтому в организме сердечные гликозиды депонируются в основном в скелетных мышцах. В жировую ткань препараты данной группы проникают плохо, что имеет практическое значение: у больных с ожирением расчёт дозы следует проводить с учётом не реальной, а идеальной массы тела. С другой стороны, необходимо учитывать наличие кахексии при тяжёлой сердечной недостаточности.
Примерно у 10% пациентов отмечают «интестинальный» метаболизм, который заключается в переработке дигоксина в неактивный дигидродигоксин под влиянием кишечной микрофлоры. Это может быть причиной низкого содержания ЛС в плазме крови.
Показания к применению и режим дозирования
Показания к назначению сердечных гликозидов, в сущности, мало изменились за 200 лет использования данных препаратов в клинической практике: это сердечная недостаточность и мерцательная аритмия. Иногда сердечные гликозиды применяют для профилактики АВ-реципрокной тахикардии.
Благодаря развитию представлений о патогенезе сердечной недостаточности, созданию новых лекарственных препаратов, внедрению в клиническую практику принципов терапии, построенной на доказательной медицине, основательно изменилась фармакотерапия сердечными гликозидами.
Рассматривая показания к назначению сердечных гликозидов, в первую очередь следует выделить сердечную недостаточность с синусовым ритмом и мерцательной аритмией. На рубеже 80-90-х годов прошлого века после разработки ингибиторов АПФ изменились подходы к терапии сердечной недостаточности, благодаря чему в настоящее время удаётся эффективно лечить тяжёлых больных с данным заболеванием и синусовым ритмом без применения сердечных гликозидов. Необходимость осторожно относиться к назначению сердечных гликозидов была подтверждена результатами клинических испытаний препаратов с положительным инотропным действием: было обнаружено повышение смертности при приёме внутрь веснаринона*, ксамотерола*, милринона* и ряда других инотропных ЛС. При сердечной недостаточности с мерцательной аритмией сердечные гликозиды продолжали оставаться препаратами выбора, поскольку β-адреноблокаторы ещё не применяли широко в клинической практике, а блокаторы медленных кальциевых каналов недигидропиридинового ряда, с одной стороны,
не вызывают столь же существенного снижения ЧСС, как сердечные гликозиды, с другой - неблагоприятно влияют на прогноз заболевания. В 1997 г. были опубликованы результаты крупного плацебо-контролируемого исследования (7000 больных с сердечной недостаточностью с синусовым ритмом), в котором было доказано, что дигоксин не оказывает влияния на прогноз болезни; тем не менее, улучшая клиническую картину сердечной недостаточности, дигоксин сохраняет свое значение в терапии некоторых больных с данным заболеванием и синусовым ритмом, например, у пациентов с симптомами тяжёлой сердечной недостаточности, сохраняющимися, несмотря на назначение адекватных доз ингибиторов АПФ, диуретиков и β-адреноблокаторов.
В настоящее время β-адреноблокаторы начинают широко использовать у пациентов с мерцательной аритмией и сердечной недостаточностью, т.е. в ситуации, при которой традиционно использовали сердечные гликозиды. Становится обычным добавление к дигоксину небольших доз метопролола, карведилола или бисопролола с их последующим титрованием. По мере снижения ЧСС дозу дигоксина можно уменьшить (вплоть до полной отмены).
Высокий объём распределения считают признаком того, что необходимо время для накопления препарата в тканях до установления равновесной концентрации. Для ускорения данного процесса используют режим нагрузочной дозы (дигитализация) с переходом на поддерживающую дозу препарата. Согласно классическим принципам клинической фармакологии, дигитализация - обязательный этап лечения сердечной недостаточности. В настоящее время дигитализацию проводят редко, поскольку невозможно спрогнозировать индивидуальную чувствительность пациента к сердечным гликозидам. Кроме того, внедрение новых подходов к терапии сердечной недостаточности, таких, как использование вазодилататоров (нитраты), нейрогуморальных антагонистов (ингибиторы АПФ, антагонисты рецепторов ангиотензина II), инотропных ЛС (добутамин и допамин), позволяет добиться стабилизации состояния пациента дигитализации. Следует также учитывать наличие различных факторов риска гликозидной интоксикации у больных с сердечной недостаточностью (нарушения электролитного баланса и кислотно-щелочного состояния, приём препаратов, повышающих концентрацию сердечных гликозидов в крови). Дигитализацию иногда проводят при тахисистолической форме мерцательной аритмии в случае отсутствия выраженных признаков сердечной недостаточности. Нагрузочную дозу дигоксина можно рассчитать по следующей формуле.
Нагрузочная доза = (7 л/кг xидеальная масса тела x 1,5 мкг/л) 0,65, где 7 л/кг - объём распределения дигоксина, «идеальную массу тела» рассчи-
тывают по номограмме для больных с ожирением (при кахексии учитывают реальную массу тела), 1,5 мкг/л - терапевтическая концентрация препарата в плазме крови, 0,65 - биодоступность дигоксина.
Если насыщение проводят путём внутривенного введения дигоксина, используют ту же формулу, за исключением биодоступности. Дигитализацию с назначение нагрузочной дозы называют быстрой.
Режим дозирования для ланатозида Ц детально не разработан, так как препарат применяют значительно реже по сравнению с дигоксином. Расчёт данных параметров для строфантина-К делать нецелесообразно, поскольку ЛС используют кратковременно и лекарственной формы для приёма строфантина-К внутрь нет.
Поддерживающая доза дигоксина составляет 0,0625-0,5 мг/сут в зависимости от возраста больного, состояния функций почек, ЧСС, сопутствующей терапии и индивидуальной переносимости препарата. Благодаря основным фармакокинетическим принципам можно рассчитать поддерживающую дозу дигоксина. Сначала определяют клиренс дигоксина по следующей формуле:
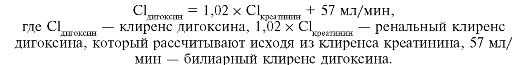 При сердечной недостаточности используют другую формулу (с учё- том сниженной перфузии почек и печени):
При сердечной недостаточности используют другую формулу (с учё- том сниженной перфузии почек и печени):
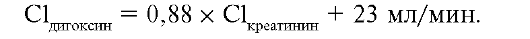 Указанная
формула была выведена при обработке фармакокинетических параметров,
полученных у большого числа больных с сердечной недостаточностью,
принимавших дигоксин. Значение, выраженное в мл/мин, переводят в л/сут.
Указанная
формула была выведена при обработке фармакокинетических параметров,
полученных у большого числа больных с сердечной недостаточностью,
принимавших дигоксин. Значение, выраженное в мл/мин, переводят в л/сут.
Клиренс креатинина можно определить по формуле Кокрофта- Голля.
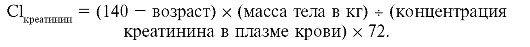 Для женщин результат умножают на 0,85.
Для женщин результат умножают на 0,85.
Таким образом, можно рассчитать поддерживающую дозу дигоксина.
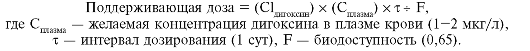 В
настоящее время терапию дигоксином сразу начинают с поддерживающей
дозы, при этом равновесную концентрацию препарата отмечают через 4-6
периодов полувыведения. Подобный темп насыщения называют медленной
дигитализацией.
В
настоящее время терапию дигоксином сразу начинают с поддерживающей
дозы, при этом равновесную концентрацию препарата отмечают через 4-6
периодов полувыведения. Подобный темп насыщения называют медленной
дигитализацией.
Терапевтический лекарственный мониторинг
Определение концентрации дигоксина в плазме крови - стандартный метод мониторинга эффективности и безопасности препарата. Терапевтический диапазон содержания дигоксина в крови составляет 1-2 нг/мл (0,5-1,5 мкг/л). Известно, что основные фармакодинамические эффекты препарата (положительный инотропный и отрицательный хронотропный) зависят от дозы, поэтому, согласно основополагающим принципам клинической фармакологии, обычной практикой ведения пациентов с сердечной недостаточностью было назначение максимально переносимых доз лекарственного препарата для получения наибольшего терапевтического эффекта. Однако на основании результатов нескольких крупных исследований данный подход был пересмотрен.
• Стало известно, что терапевтическая и токсическая концентрации дигоксина в плазме крови нередко «перекрываются».
• Показано, что при отмене дигоксина ухудшается течение сердечной недостаточности, однако это не связано с тем, какая концентрация препарата в плазме крови была до отмены (низкая или высокая).
• Доказано, что нейромодулирующее действие дигоксина (снижение активности ренина и концентрации норадреналина в крови) появляется уже при низком содержании дигоксина в плазме крови, причём при увеличении концентрации препарата этот эффект не нарастает.
• Наиболее высокую летальность среди больных с сердечной недостаточностью и синусовым ритмом отмечают в группе с содержанием дигоксина в плазме крови более 1,5 нг/мл.
Таким образом, в настоящее время основной тенденцией в клиническом применении сердечных гликозидов служит отказ от максимально переносимых доз.
Побочные эффекты
Частота гликозидной интоксикации составляет 10-20%. Это обусловлено малой широтой терапевтического действия сердечных гликозидов (токсические дозы препаратов превышают оптимальные терапевтические не более чем в 1,8-2 раза). Для сердечных гликозидов характерна выраженная способность к кумуляции, и индивидуальная толерантность к данным препаратам у больных варьирует в очень широких пределах. Наименьшую толерантность отмечают, как правило, у тяжёлых больных.
Факторы, способствующие развитию гликозидной интоксикации, представлены ниже.
• Пожилой возраст.
• Поздняя стадия ХСН.
• Выраженная дилатация отделов сердца.
• Острая стадия инфаркта миокарда.
• Выраженная ишемия миокарда.
• Воспалительные поражения миокарда.
• Гипоксия любой этиологии.
• Гипокалиемия и гипомагниемия.
• Гиперкальциемия.
• Нарушение функций щитовидной железы.
• Повышенная активность симпатической нервной системы.
• Дыхательная недостаточность.
• Почечная и печёночная недостаточность.
• Нарушения кислотно-основного состояния (алкалоз).
• Гипопротеинемия.
• Электроимпульсная терапия.
• Генетический полиморфизм гликопротеина P. Клинические проявления дигиталисной интоксикации перечислены ниже.
• Сердечно-сосудистая система: желудочковая экстрасистолия (часто бигеминия, политопная желудочковая экстрасистолия), узловая тахикардия, синусовая брадикардия, синоатриальная блокада, мерцательная аритмия, АВ-блокада.
• ЖКТ: анорексия, тошнота, рвота, диарея, боли в животе, некроз кишечника.
• Орган зрения: желто-зелёное окрашивание предметов, мелькание мушек перед глазами, снижение остроты зрения, восприятие предметов в уменьшенном или увеличенном виде.
• Нервная система: нарушения сна, головные боли, головокружения, невриты, парестезии.
• Гематологические нарушения: тромбоцитопеническая пурпура, носовые кровотечения, петехии.
Интоксикацию следует подозревать при появлении даже одного симптома со стороны любого органа или системы. Как правило, самым ранним симптомом интоксикации сердечными гликозидами бывает анорексия и/или тошнота.
Объём лечебных мероприятий при гликозидной интоксикации зависит в первую очередь от поражения ССС, т.е. аритмий. При подозрении на интоксикацию следует отменить сердечные гликозиды, провести ЭКГ, определить содержание калия и дигоксина в плазме крови. При наличии показаний к назначению антиаритмических препаратов в случае желудочковых аритмий вводят препараты IB класса (лидокаин или мексиле-
тин), так как эти ЛС не влияют на проводимость миокарда предсердий и АВ-узла. Антиаритмические препараты используют только внутривенно, поскольку в этом случае в зависимости от эффекта удаётся быстро корригировать дозу. Внутрь антиаритмические препараты не назначают.
При наличии показаний к терапии наджелудочковых нарушений ритма можно использовать β-адреноблокаторы или блокаторы медленных кальциевых каналов, однако только при условии контроля за АВ-проводимостью.
При выраженной брадикардии, синоатриальной или АВ-блокаде вводят м-холиноблокаторы. β-Адреномиметики применять опасно ввиду возможного усиления аритмогенного действия сердечных гликозидов. При неэффективности лекарственной терапии решают вопрос о временной электрокардиостимуляции.
При сопутствующей гипокалиемии внутривенно назначают препараты калия. ЛС, содержащие калий, также показаны при нормальном содержании данного элемента в крови, если у пациента отмечают аритмии. Однако следует помнить, что калий вызывает замедление АВ-проводимости, поэтому при нарушениях проведения по АВ-узлу (блокады I-II степени) в случае гликозидной интоксикации препараты калия следует вводить с осторожностью.
Наиболее эффективным, но дорогостоящим методом лечения служит введение антител к дигоксину. Положительный эффект (купирование аритмий) развивается в течение 30-60 мин. Традиционные антидоты (димеркаптопропансульфонат натрия, эдетовая кислота) при интоксикации сердечными гликозидами с позиций доказательной медицины не оценивали.
Противопоказания
Абсолютным противопоказанием к назначению сердечных гликозидов считают гликозидную интоксикацию. Относительными противопоказаниями служат синдром слабости синусового узла и АВ-блокада I-II степени (опасность усугубления дисфункции синусового узла и дальнейшего замедления проводимости по АВ-узлу), желудочковые нарушения ритма (опасность усиления аритмий), мерцательная аритмия в сочетании с синдромом Вольфа-Паркинсона-Уайта, синусовая брадикардия. Нецелесообразно использовать сердечные гликозиды в случаях сердечной недостаточности без нарушения систолической функции левого желудочка (гипертрофическая кардиомиопатия, аортальный стеноз, митральный стеноз с синусовым ритмом, констриктивный перикардит).
Оценка эффективности и безопасности Оценка эффективности
При оценке эффективности терапии сердечными гликозидами следует разделять стабильную и декомпенсированную сердечную недостаточность. При декомпенсации фармакотерапия предусматривает комплексный подход, заключающийся в изменении режима дозирования (или назначении) всех основных групп препаратов (диуретики, ингибиторы АПФ, антагонисты рецепторов ангиотензина II, нитраты). Сердечные гликозиды - составная часть такого подхода. Результаты лечения будут зависеть от рационального применения всех препаратов. Например, трудно добиться уменьшения ЧСС при мерцательной аритмии в условиях недостаточной эффективности диуретической терапии. С другой стороны, неверно считать, что усиление сократимости сердца вызвано только назначением сердечных гликозидов, поскольку пациент получает ЛС, влияющие на преднагрузку и постнагрузку и, по закону Фран- ка-Старлинга, изменяющие инотропную функцию сердца. По этим причинам оценка эффективности сердечных гликозидов при декомпенсации отражает влияние всего комплекса лечебных мероприятий (при условии, что содержание дигоксина в крови находится в пределах терапевтического диапазона). При стабильной сердечной недостаточности, в ситуации, когда врач добавляет сердечные гликозиды к проводимому лечению, динамика одышки, результатов 6-минутного теста с ходьбой, ЧСС отражают действие только сердечных гликозидов (если при этом сопутствующую терапию не изменяли).
Оценка безопасности
Оценка безопасности необходима для предупреждения и диагностики гликозидной интоксикации. «Интоксикация сердечными гликозидами» - исторически сложившийся термин, который отражает совокупность нежелательных клинико-инструментальных изменений, возникающих при приёме сердечных гликозидов. Следует отметить, что симптомы интоксикации могут появиться до развития клинического эффекта, при- чём раньше подобные случаи отличались от собственно интоксикации и назывались непереносимостью данной группы ЛС. В настоящее время термин «гликозидная интоксикация» включает понятие непереносимость. Основные меры предупреждения интоксикации приведены ниже.
• Опрос пациента для выявления симптомов интоксикации.
• Контроль пульса и ЧСС.
• Анализ ЭКГ.
• Контроль содержания калия в крови, функций почек (концентрация креатинина и мочевины в крови).
• Коррекция дозы сопутствующих препаратов, неблагоприятно взаимодействующих с сердечными гликозидами.
• Контроль содержания дигоксина в плазме крови.
Необходимо отметить, что изменения на электрокардиограмме, возникающие в процессе лечения сердечными гликозидами («корытообразная» депрессия сегмента ST, укорочение интервала Q-T, изменения зубца Т), не корелируют с концентрацией данных препаратов в плазме крови и изолированно их не расценивают в качестве показателей насыщения или интоксикации сердечными гликозидами.
Взаимодействие
Дигоксин взаимодействует с целым рядом ЛС (прил. 3, см. ). Фармакодинамическое взаимодействие необходимо учитывать при назначении дигоксина фактически со всеми антиаритмическими препаратами (за исключением класса IB), поскольку в этом случае возможно угнетение проведения по предсердиям и атриовентрикулярному узлу.
14.2. АГОНИСТЫ АДРЕНОРЕЦЕПТОРОВ
К ЛС этой подгруппы инотропных препаратов относят добутамин, допамин, эпинефрин и норэпинефрин . Положительный инотропный эффект агонистов адренорецепторов обусловлен стимуляцией β1-адренорецепторов сердца, активацией системы G-протеинов, которые взаимодействуют с аденилатциклазой, что приводит к увеличению продукции цАМФ, повышению содержания кальция в цитозоле и развитию положительного инотропного эффекта.
Агонисты адренорецепторов обладают также вазоконстрикторным действием, благодаря которому данные препараты используют при острой и хронической сердечной недостаточности, в том числе и рефрактерной к мочегонным ЛС, сердечным гликозидам и вазодилататорам. Положительное инотропное действие - следствие стимуляции β1-адренорецепторов, но в зависимости от дополнительных свойств и используемых доз препараты по-разному влияют на тонус периферических сосудов, почечный кровоток и АД (табл. 14-2).
Таблица 14-2. Эффекты агонистов адренорецепторов
 Окончание табл. 14-2
Окончание табл. 14-2
 Добутамин
Добутамин
Добутамин - синтетический адреномиметик, состоящий из двух изомеров. Стимуляция β-адренорецепторов связана с (+)-изомером, а α-адренорецепторов - с (-)-изомером. Однако α-адренергические эффекты препарата практически не выражены из-за способности (+)-изомера блокировать α-адренорецепторы. При внутривенном введении добутамина отмечают зависящее от дозы увеличение сердечного выброса вследствие повышения сократимости миокарда, снижения преднагрузки и постнагрузки. При назначении в средних дозах добутамин слабо влияет на АД (вероятно, периферическая вазоконстрикция, обусловленная блокадой α-адреноррецепторов, нивелируется вазодилатацией, опосредованной влиянием на β2-адренорецепторы). Сопротивление сосудов в малом круге кровообращения на фоне применения препарат снижается. В связи с коротким периодом полувыведения добутамин следует вводить непрерывно. Активность добутамина может уменьшиться, если больной принимает β-адреноблокаторы. В этом случае возможно проявление скрытого α-адренергического эффекта (сужение периферических сосудов и повышение АД). Наоборот, при блокаде α-адренорецепторов существует вероятность большей выраженности эффектов стимуляции β1 и β2-адренорецепторов (тахикардия и расширение периферических сосудов).
При длительной непрерывной терапии (более 72 ч) развивается привыкание к препарату.
Показания
Показаниями к назначению добутамина служат острая (отёк лёг- ких, кардиогенный шок) и тяжёлая ХСН, сердечная недостаточность в острой стадии инфаркта миокарда или кардиохирургического лечения, передозировка β-адреноблокаторов. Острый фармакологический тест с добутамином используют для диагностики ИБС (оценивают локальную сократимость левого желудочка с помощью эхокардиографии или радионуклидной вентрикулографии).
Побочные эффекты
Побочные эффекты добутамина - нарушение ритма сердца и стенокардия.
Противопоказания
Добутамин противопоказан при повышенной чувствительности к нему.
Меры предосторожности
Необходимо контролировать содержания калия в плазме крови. Следует помнить о несовместимости добутамина с щелочными растворами.
Фармакокинетика и режим дозирования
Период полувыведения препарата составляет 2-4 мин. Добутамин вводят внутривенно со скоростью 2,5-20 мкг/кг массы тела в минуту (по показаниям скорость введения можно увеличить до 40 мкг/кг массы тела в минуту). Устойчивую концентрацию препарата в плазме крови отмечают через 10-15 мин после корректировки дозы. Добутамин применяют под контролем АД, ЧСС и ЭКГ. По показаниям проводят катетеризацию лёгочной артерии с прямым измерением гемодинамических показателей.
Допамин
Допамин - эндогенный катехоламин, служащий предшественником норадреналина. Допамин действует опосредованно через высвобождение норадреналина из нервных окончаний. Фармакодинамические эффекты препарата связаны со ступенчатой активацией D1- и D2-рецепторов к дофамину (при дозе менее 2 мкг/кг массы тела в минуту) и β-адренорецепторов (при дозе 2-10 мкг/кг массы тела в минуту) и α-адренорецепторов (при дозе более 10 мкг/кг массы тела в минуту). В результате стимуляции дофаминовых рецепторов увеличивается не только почечный, но и мезентериальный и мозговой кровоток, а ОПСС при этом снижается. В дозах выше 15 мкг/кг массы тела в минуту препарат (у некоторых больных в дозе 5 мгк/кг массы тела в минуту) действует фактически как норэпинефрин. При продолжительном введении допамина даже с оптимальной скоростью происходит постепенное накопление норадреналина, что неизбежно приводит к возрастанию ЧСС и ОПСС.
Показания
Допамин назначают в случае артериальной гипотензии при кардиогенном и септическом шоке, сердечной недостаточности (инфаркт
миокарда, после хирургических операций), а также при острой почечной недостаточности.
Побочные эффекты
Побочные эффекты допамина - нарушение ритма сердца и стенокардия.
Противопоказания
Допамин противопоказан при феохромоцитоме, желудочковых нарушениях ритма.
Меры предосторожности
Необходимо контролировать содержание калия в плазме крови. Из-за снижения ОПСС, которое может возникать при назначении допамина в низких дозах, следует ограничить использование препарата у больных с обструкцией выносящего тракта левого желудочка (аортальный стеноз, гипертрофическая кардиомиопатия). Риск развития жизнеопасных аритмий зависит от дозы ЛС.
Фармакокинетика и режим дозирования
Период полувыведения допамина составляет 2 мин. Введение начинают с дозы 0,5-1 мгк/кг массы тела в минуту и повышают её до достижения необходимого АД. Дозу препарата титруют в зависимости от АД, ЧСС и диуреза. Если целью терапии служит увеличение диуреза, то максимальная доза препарата составляет 2-2,5 мгк/кг массы тела в минуту. Как правило, оптимальные гемодинамические показатели отмечают при скорости инфузии от 5 до 10 мкг/кг массы тела в минуту. Более высокие дозы препарата приводят к снижению почечного кровотока и периферической вазоконстрикции. В дозах выше 15 мкг/кг массы тела в минуту допамин действует фактически как норэпинефрин. При продолжительном введении допамина даже с оптимальной скоростью происходит постепенное накопление норадреналина, что неизбежно приводит к увеличению ЧСС и ОПСС. В практической деятельности следует стремиться к использованию минимально активных доз допамина, учитывая, что наибольшее увеличение почечного кровотока возникает при скорости инфузии 6-7 мкг/кг массы тела в минуту.
Эпинефрин
Эпинефрин - α-, β1- и β2-адреномиметик. Показания
Положительные хронотропный и инотропный эффекты препарата в клинической практике не используют. Основная цель назна-
чения эпинефрина - периферическая вазоконстрикция. С этой целью ЛС применяют при сердечно-лёгочной реанимации (остановка сердца) для увеличения тонуса коронарных и мозговых сосудов и при анафилактической реакции для повышения АД и уменьшения отёка слизистых оболочек. В ситуации анафилаксии эпинефрин бывает полезен при бронхоспазме. Передозировку β-адреноблокаторов не считают показанием к назначению эпинефрина, поскольку в этом случае преобладает α-стимулирующий эффект, приводящий к резкому повышению АД.
Побочные эффекты
К побочным эффектам эпинефрина относят тахикардию, аритмии, головную боль, возбуждение, боль в груди, отёк лёгких.
Противопоказания
Эпинефрин противопоказан при беременности.
Фармакокинетика и режим дозирования
Период полувыведения препарата составляет 2 мин. Эпинефрин назначают подкожно, внутримышечно, внутривенно и эндотрахеально в дозе 0,5-1 мг. При необходимости препарат вводят повторно каждые 3-5 мин под контролем ЧСС, АД и ЭКГ.
Норэпинефрин
Норэпинефрин в основном действует на α- и β1-адренорецепторы, и в меньшей степени - на β2-адренорецепторы. Норэпинефрин - активный вазоконстриктор, слабо влияющий на сердечный выброс. Поскольку препарат стимулирует преимущественно α-адренорецепторы, при его применении возможно снижение мезентериального и ренального кровотока, вплоть до острой почечной недостаточности. При назначении норэпинефрина также существует вероятность уменьшения ЧСС вследствие стимуляции каротидных барорецепторов.
Показания
Поскольку препарат вызывает значительное сужение сосудов, его используют при септическом шоке, а при кардиогенном шоке норэпинефрин назначают при сохраняющейся артериальной гипотензии на фоне введения других инотропных ЛС.
Побочные эффекты
Побочные эффекты норэпинефрина - тахикардия, аритмии, головная боль, возбуждение.
Противопоказания
Норэпинефрин противопоказан при беременности.
Фармакокинетика и режим дозирования
Период полувыведения норэпинефрина составляет 3 мин. Препарат назначают внутривенно в дозе 8-12 мкг/мин. Инфузию ЛС следует всегда осуществлять в центральные вены из-за опасности развития некрозов поверхностных тканей при длительном введении.
14.3. ИНГИБИТОРЫ ФОСФОДИЭСТЕРАЗЫ
Эта группа ЛС включает амринон*, милринон* и эноксимон* Препараты ингибируют фосфодиэстеразу, тормозят разрушение цАМФ и усиливают сократимость миокарда. Кроме того, эти ЛС оказывают сосудорасширяющее действие и умеренно снижают АД. Из-за комбинации положительного инотропного и вазодилатирующего эффектов данный класс препаратов также называют инодилататорами.
Показание
Ингибиторы фосфодиэстеразы показаны при отёке лёгких и декомпенсации ХСН. Считают, что при сердечной недостаточности в условиях пониженной чувствительности β-адренорецепторов к эндогенным катехоламинам и симпатомиметикам лучше назначать ингибиторы фосфодиэстеразы (при отсутствии артериальной гипотензии).
Противопоказания
Ингибиторы фосфодиэстеразы противопоказаны при аортальном стенозе и гипертрофической кардиомиопатии с обструкцией выносящего тракта.
Фармакокинетика и режим дозирования
Период полувыведения милринона составляет 3-5 ч. После болюсного введения препарата в дозе 50 мкг/кг массы тела осуществляют внутривенную инфузию милринона со скоростью 0,375-0,75 мкг/кг массы тела в течение до 48 ч. Препарат используют под контролем АД, ЧСС и ЭКГ. В связи с тем что при назначении амринона часто развивается тромбоцитопения, данный препарат применяют очень редко. Клиническую эффективность эноксимона продолжают изучать.
Побочные эффекты
Побочные эффекты ингибиторов фосфодиэстеразы - артериальная гипотензия и нарушения ритма сердца.
14.4. ПРЕПАРАТЫ, ПОВЫШАЮЩИЕ ЧУВСТВИТЕЛЬНОСТЬ СОКРАТИТЕЛЬНЫХ БЕЛКОВ К КАЛЬЦИЮ («КАЛЬЦИЕВЫЕ СЕНСИТИЗАТОРЫ»)
К данной группе ЛС относят левосимендан. Препарат связывается с тропонином C в присутствии ионов кальция, стабилизируя структуру тропонина C и удлиняя время взаимодействия актина и миозина. В результате этого образуются новые места для связи сократительных белков, и сократимость кардиомиоцитов повышается. Важно отметить, что трансмембранный градиент ионов кальция не изменяется, поэтому риск аритмий не увеличивается. Связь левосимендана и тропонина C зависит от исходной внутриклеточной концентрации ионов кальция, поэтому действие препарата проявляется только при повышенном содержании ионов кальция в клетке. В диастолу происходит обратный захват кальция саркоплазматическим ретикулумом, концентрация ионов кальция в цитоплазме снижается, связь препарата и тропонина C прекращается и процесс релаксации миокарда не нарушается.
В больших дозах левосимендан может угнетать фосфодиэстеразу. Кроме того, ЛС способствует активации АТФ-зависимых калиевых каналов периферических сосудов, что приводит к вазодилатации.
Левосимендан вводят внутривенно. Показаниями к его назначению служат декомпенсация ХСН и сердечная недостаточность при инфаркте миокарда.