Клиническая фармакология.: учебник для вузов / Под ред. В.Г. Кукеса.- 4-е издание., перераб. и доп., - 2009. - 1056 с.
|
|
|
|
ГЛАВА 19. АНТИГИСТАМИННЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА
Патофизилогия гистамина и Н1-рецепторов гистамина
Гистамин и его эффекты, опосредуемые через Н1-рецепторы
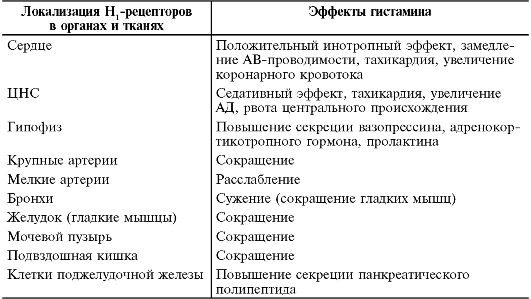
Стимуляция Н1-рецепторов у человека приводит к повышению тонуса гладкой мускулатуры, сосудистой проницаемости, появлению зуда, замедлению атриовентрикулярной проводимости, тахикардии, активации ветвей блуждающего нерва, иннервирующего дыхательные пути, повышению уровня цГМФ, повышению образования простагландинов и т.д. В табл. 19-1 показаны локализация Н1-рецепторов и эффекты гистамина, опосредуемые через них.
Таблица 19-1. Локализация Н1-рецепторов и эффекты гистамина, опосредуемые через них
 Роль гистамина в патогенезе аллергии
Роль гистамина в патогенезе аллергии
Гистамину отводится ведущая роль в развитии атопического синдрома. При аллергических реакциях, опосредуемых через IgE, из тучных клеток в ткани поступает большое количество гистамина, вызывающего возникновение нижеперечисленных эффектов посредством воздействия на Н1-рецепторы.
В гладких мышцах крупных сосудов, бронхов и кишечника активация Н1-рецепторов вызывает изменение конформации Gp-белка, что, в свою очередь, ведёт к активации фосфолипазы С, катализирующей гидролиз инозитолдифосфата до инозитолтрифосфата и диацилглицеролов. Увеличение концентрации инозитолтрифосфата приводит к открытию кальциевых каналов в ЭПР («депо кальция»), что вызывает выход кальция в цитоплазму и повышение его концентрации внутри клетки. Это приводит к активации кальций/кальмодулин-зависимой киназы лёг- ких цепей миозина и, соответственно, сокращению гладкомышечных клеток. В эксперименте гистамин вызывает двухфазное сокращение гладких мышц трахеи, состоящее из быстрого фазового сокращения и медленного тонического компонента. В экспериментах показано, что быстрая фаза сокращения этих гладких мышц зависит от внутриклеточного кальция, а медленная - от входа внеклеточного кальция через неблокируемые антагонистами кальция медленные кальциевые каналы. Действуя через Н1-рецепторы, гистамин вызывает сокращение гладкой мускулатуры дыхательных путей, в том числе бронхов. В верхних отделах дыхательных путей Н1-рецепторов гистамина больше, чем в нижних, что имеет существенное значение в степени выраженности бронхоспазма в бронхиолах при взаимодействии гистамина с этими рецепторами. Гистамин индуцирует обструкцию бронхов в результате прямого влияния на гладкие мышцы дыхательных путей, реагируя с Н1-рецепторами гистамина. Кроме того, через Н1-рецепторы гистамин увеличивает секрецию жидкости и электролитов в дыхательных путях и вызывает усиленную продукцию слизи и отёк дыхательных путей. Больные бронхиальной астмой в 100 раз более чувствительны к гистамину, чем здоровые лица при проведении гистаминового провокационного теста.
В эндотелии мелких сосудов (посткапиллярные венулы) через Н1-рецепторы опосредуется вазодилатирующий эффект гистамина при аллергических реакциях реагинового типа (через Н2-рецепторы гладкомышечных клеток венул, по аденилатциклазному пути). Активация Н1-рецепторов ведёт (по фосфолипазному пути) к увеличению внутриклеточного уровня кальция, который вместе с диацилглицеролом активирует фосфолипазу А2, вызывающую следующие эффекты.
• Местный выброс эндотелий-релаксирующего фактора. Он проникает в соседние гладкомышечные клетки и активирует гуанилатциклазу. В результате увеличивается концентрация цГМФ, активирущего цГМФ-зависимую протеинкиназу, что приводит к снижению внутриклеточного кальция. При одновременном снижении уровня кальция и повышении уровня цГМФ происходит расслабление гладкомышечных клеток посткапиллярных венул, что приводит к развитию отёка и эритемы.
• При активации фосфолипазы А2 увеличивается синтез простагландинов, преимущественно вазодилататора простациклина, что также способствует образованию отёка и эритемы.
Классификация антигистаминных лекарственных средств
Существует несколько классификаций антигистаминных препаратов (блокаторов Н1-рецепторов гистамина), хотя ни одну из них не считают общепринятой. Согласно одной из наиболее популярных классификаций, антигистаминные препараты по времени создания подразделяют на препараты I и II поколения. Препараты I поколения принято также называть седативными (по доминирующему побочному эффекту), в отличие от неседативных препаратов второй генерации. К антигистаминным препаратам I поколения относят: дифенгидрамин (димедрол*), прометазин (дипразин*, пипольфен*), клемастин, хлоропирамин (супрастин*), хифенадин (фенкарол*), секвифенадин (бикар- фен*). Антигистаминные препараты II поколения: терфенадин*, асте- мизол*, цетиризин , лоратадин , эбастин , ципрогептадин , оксатомид*9, азеластин, акривастин, мебгидролин, диметинден.
В настоящее время принято выделять и III поколение антигистаминных препаратов. К нему относят принципиально новые средства - активные метаболиты, для которых характерны помимо высокой антигистаминной активности, отсутствие седативного эффекта и свойственного для препаратов второго поколения кардиотоксического действия. К III поколению антигистаминных препаратов относят фексофенадин (телфаст*), дезлоратадин.
Кроме того, по химическому строению антигистаминные препараты подразделяют на несколько групп (этаноламины, этилендиамины, алкиламины, производные альфакарболина, хинуклидина, фенотиазина*, пиперазина* и пиперидина*).
Механизм действия и основные фармакодинамические эффекты антигистаминных лекарственных средств
Большинство используемых антигистаминных средств обладает специфическими фармакологическими свойствами, что характеризует их как отдельную группу. Сюда относят следующие эффекты: противозудный, противоотёчный, антиспастический, антихолинергический, антисеротониновый, седативный и местноанестезирующий, а также предупреждение гистамининдуцированного бронхоспазма.
Антигистаминные препараты - антагонисты Н1-рецепторов гистамина, причём их сродство к этим рецепторам значительно ниже, чем у гистамина (табл. 19-2). Именно поэтому данные ЛС не способны вытеснить гистамин, связанный с рецептором, они только блокируют незанятые или высвобождаемые рецепторы.
Таблица 19-2. Сравнительная эффективность антигистаминных лекарственных средств по степени блокадыН1-рецепторов гистамина
 Соответственно, блокаторы Н1-рецепторов
гистамина наиболее эффективны для предупреждения аллергических реакций
немедленного типа, а в случае развившейся реакции предупреждают выброс
новых порций гистамина. Связывание антигистаминных препаратов с
рецепторами носит обратимый характер, а количество блокируемых
рецепторов прямо пропорционально концентрации препарата в месте
нахождения рецептора.
Соответственно, блокаторы Н1-рецепторов
гистамина наиболее эффективны для предупреждения аллергических реакций
немедленного типа, а в случае развившейся реакции предупреждают выброс
новых порций гистамина. Связывание антигистаминных препаратов с
рецепторами носит обратимый характер, а количество блокируемых
рецепторов прямо пропорционально концентрации препарата в месте
нахождения рецептора.
Молекулярный механизм действия антигистаминных препаратов можно представить в виде схемы: блокада Н1-рецептора - блокада фосфоинозитидного пути в клетке - блокада эффектов гистамина. Связывание ЛС с Н1-рецептором гистамина приводит к «блокаде» рецептора, т.е. препятствует связыванию гистамина с рецептором и запуску каскада в клетке по фосфоинозитидному пути. Таким образом, связывание антигистаминного ЛС с рецептором вызывает замедление активации фосфолипазы С, что ведёт к уменьшению образования инозитолтрифосфата и диацилглицерола из фосфатидилинозитола, в итоге замедляется выход кальция из внутриклеточных депо. Уменьшение выхода кальция из внутриклеточных органелл в цитоплазму в различных типах клеток приводит к снижению доли активированных ферментов, опосредующих эффекты гистамина в этих клетках. В гладких мышцах бронхов (а также ЖКТ и крупных сосудов) замедляется активация кальций-кальмодулин-зависимой киназы лёгких цепей миозина. Это препятствует сокращению гладких мышц, вызванному гистамином, особенно у больных бронхиальной астмой. Однако при бронхиальной астме концентрация гистамина в лёгочной ткани настолько высока, что современные Н1-блокаторы не в состоянии заблокировать по такому механизму эффекты гистамина на бронхи. В эндотелиальных клетках всех посткапиллярных венул антигистаминные ЛС препятствуют вазодилатирущему эффекту гистамина (прямому и через простагландины) при местных и генерализованных аллергических реакциях (гистамин действует и через Н2-рецепторы гистамина гладкомышечных клеток
венул по аденилатциклазному пути). Блокада Н1-рецепторов гистамина в этих клетках препятствует увеличению внутриклеточного уровня кальция, в итоге замедляя активацию фосфолипазы А2, что приводит к развитию следующих эффектов:
• замедление местного выброса эндотелий-релаксирующего фактора, проникающего в соседние гладкомышечные клетки и активирующего гуанилатциклазу. Торможение активации гуанилатциклазы уменьшает концентрацию цГМФ, далее снижается фракция активированной цГМФ-зависимой протеинкиназы, что препятствует снижению уровня кальция. Одновременно нормализация уровня кальция и цГМФ препятствует расслаблению гладкомышечных клеток посткапиллярных венул, то есть препятствует развитию отёка и эритемы, вызываемых гистамином;
• снижение активированной фракции фосфолипазы А2 и уменьшение синтеза простагландинов (преимущественно простациклина), блокируется вазодилатация, что препятствует возникновению отёка и эритемы, вызываемых гистамином по второму его механизму действия на эти клетки.
Исходя из механизма действия антигистаминных ЛС, эти препараты следует назначать с целью профилактики аллергических реакций реагинового типа. Назначение данных препаратов при развившейся аллергической реакции менее эффективно, так как они не устраняют симптомов развившейся аллергии, а препятствуют их появлению. Блокаторы Н1-рецепторов гистамина предотвращают реакцию гладкой мускулатуры бронхов на гистамин, уменьшают зуд, предотвращают опосредованное гистамином расширение мелких сосудов и их проницаемость.
Фармакокинетика антигистаминных лекарственных средств
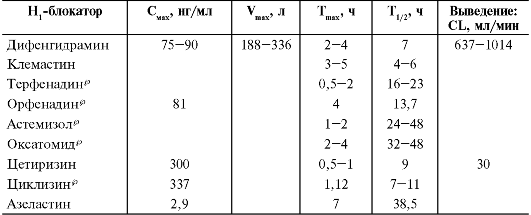
Фармакокинетика блокаторов Н1-рецепторов гистамина первого поколения принципиально отличается от фармакокинетики ЛС второго поколения (табл. 19-3).
Проникновение антигистаминных препаратов I поколения через ГЭБ приводит к появлению выраженного седативного эффекта, что считается существенным недостатком препаратов этой группы и значительно ограничивает их применение.
Антигистаминные препараты II поколения отличаются относительной гидрофильностью и в силу этого не проникают через ГЭБ и, следовательно, не вызывают седативного эффекта. Известно, что 80% астемизола* выделяется через 14 дней после последнего приёма, а тер- фенадина* - через 12 дней.
Выраженная ионизация дифенгидрамина при физиологических значениях рН и активное неспецифическое взаимодействие с сыво-
роточным альбумином обусловливает его влияние на Н1-рецепторы гистамина, расположенные в различных тканях, что приводит к достаточно выраженным побочным эффектам этого препарата. В плазме крови максимальная концентрация ЛС определяется через 4 ч после его приёма и равна 75-90 нг/л (при дозе препарата 50 мг). Период полувыведения - 7 ч.
Пик концентрации клемастина достигается через 3-5 ч после однократного приёма внутрь в дозе 2 мг. Период полувыведения равен 4-6 ч.
Терфенадин* быстро абсорбируется при приёме внутрь. Метаболизируется в печени. Максимальная концентрация в тканях определяется через 0,5-1-2 ч после приёма препарата, период полувыведения -
16-23 ч.
Максимальный уровень неизменённого астемизола* отмечают в течение 1-4 ч после приёма препарата. Пища понижает всасывание астемизола* на 60%. Пик концентрации ЛС в крови при однократном его приёме внутрь наступает через 1 ч. Период полувыведения препарата равен 104 ч. Гидроксиастемизол и норастемизол - его активные метаболиты. Астемизол* проникает через плаценту, в небольшом количестве - в грудное молоко.
Максимальная концентрация оксатомида* в крови определяется через 2-4 ч после приёма. Период полувыведения 32-48 ч. Основной путь метаболизма - ароматическое гидроксилирование и окислительное дезалкилирование на азоте. 76% всосавшегося препарата присоединяется к альбуминам плазмы, от 5 до 15% выделяется с грудным молоком.
Таблица 19-3. Фармакокинетические параметры некоторых антигистаминных лекарственных средств
 Максимальный
уровень цетиризина в крови (0,3 мкг/мл) определяют через 30-60 мин
после приёма этого препарата в дозе 10 мг. Почечный
Максимальный
уровень цетиризина в крови (0,3 мкг/мл) определяют через 30-60 мин
после приёма этого препарата в дозе 10 мг. Почечный
клиренс цетиризина равен 30 мг/мин, период полувыведения составляет около 9 ч. Препарат устойчиво связывается с белками крови.
Пик концентрации акривастина в плазме достигается через 1,4-2 ч после приёма. Период полувыведения равен 1,5-1,7 ч. Две трети препарата в неизменённом виде выделяется почками.
Лоратадин хорошо всасывается в ЖКТ и уже через 15 мин определяется в плазме крови. Пища не оказывает влияния на степень всасывания ЛС. Период полувыведения препарата составляет 24 ч.
Антигистаминные препараты I поколения
Для блокаторов Н1-рецепторов гистамина I поколения характерны некоторые особенности.
Седативное действие. Большинство антигистаминных ЛС I поколения, легко растворяясь в липидах, хорошо проникают через ГЭБ и связываются с Н1-рецепторами головного мозга. По-видимому, седативный эффект развивается при блокаде центральных серотониновых и м-холинорецепторов. Степень развития седативного эффекта варьирует от умеренной до выраженной и усиливается при сочетании с алкоголем и психотропными средствами. Некоторые ЛС этой группы используют как снотворные (доксиламин). Редко вместо седации возникает психомоторное возбуждение (чаще в среднетерапевтических дозах у детей и в высоких токсических у взрослых). В связи с седативным эффектом препаратов их нельзя использовать в период выполнения работ, требующих внимания. Все блокаторы Н1-рецепторов гистамина I поколения потенцируют действие седативных и снотворных ЛС, наркотических и ненаркотических анальгетиков, ингибиторов моноаминооксидазы и алкоголя.
Анксиолитическое действие, свойственное гидроксизину. Этот эффект, возможно, возникает за счёт подавления гидроксизином активности некоторых участков подкорковых образований головного мозга.
Атропиноподобное действие. Этот эффект связан с блокадой м-холинорецепторов, наиболее характерен для этаноламинов и этилендиаминов. Характерны сухость во рту, задержка мочи, запоры, тахикардия и нарушение зрения. При неаллергическом рините эффективность этих ЛС возрастает за счёт блокады м-холинорецепторов. Однако возможно усиление бронхообструкции за счёт увеличения вязкости мокроты, что опасно при бронхиальной астме. Блокаторы Н1-рецепторов гистамина I поколения могут обострять глаукому и вызывать острую задержку мочи при аденоме предстательной железы.
Противорвотное и противоукачивающее действие. Эти эффекты, возможно, тоже связаны с центральным м-холиноблокирующим действием этих препаратов. Дифенгидрамин, прометазин, циклизин* , мекли-
зин* уменьшают стимуляцию вестибулярных рецепторов и угнетают функции лабиринта, в связи с чем могут использоваться при болезни движения.
Некоторые блокаторы Н1-рецепторов гистамина уменьшают симптомы паркинсонизма, что обусловлено блокадой центральных м-холинорецепторов.
Противокашлевое действие. Наиболее характерно для дифенгидрамина, реализуется за счёт непосредственного действия на кашлевой центр в продолговатом мозге.
Антисеротониновое действие. В наибольшей степени им обладает ципрогептадин, поэтому его применяют при мигрени.
Эффект блокады а1-рецепторов адреналина с периферической вазодилатацией особенно характерен для препаратов фенотиазинового ряда. Это может приводить к транзиторному снижению АД.
Местноанестезирующее действие характерно для большинства ЛС этой группы. Эффект местной анестезии дифенгидрамина и прометазина сильнее, чем у новокаина*.
Тахифилаксия - снижение антигистаминного эффекта при длительном приёме, подтверждающее необходимость чередования ЛС каждые 2-3 нед.
Фармакодинамика блокаторов Н1-рецепторов гистамина I поколения
Все блокаторы Н1-рецепторов гистамина I поколения липофильны и, помимо Н1-рецепторов гистамина, блокируют также м-холинорецепторы и серотониновые рецепторы.
При назначении блокаторов рецепторов гистамина необходимо учитывать фазовое течение аллергического процесса. Блокаторы Н1-рецепторов гистамина следует применять в основном для профилактики патогенетических сдвигов при предполагаемой встрече больного с аллергеном.
Блокаторы Н1-рецепторов гистамина I поколения не влияют на синтез гистамина. В больших концентрациях эти ЛС способны вызывать дегрануляцию тучных клеток и выход из них гистамина. Блокаторы Н1-рецепторов гистамина более эффективны для предупреждения действия гистамина, чем для ликвидации последствий его влияния. Эти ЛС ингибируют реакцию гладкой мускулатуры бронхов на гистамин, уменьшают зуд, предотвращают усиление гистамином расширения сосудов и увеличение их проницаемости, уменьшают секрецию эндокринных желёз. Доказано, что блокаторы Н1-рецепторов гистамина I поколения обладают прямым бронхорасширяющим действием, а главное - предотвращают выход гистамина из тучных клеток и базофилов крови, что считается основанием для применения этих ЛС
в качестве профилактических средств. В терапевтических дозах они существенно не влияют на сердечно-сосудистую систему. При форсированном внутривенном введении могут вызвать снижение АД.
Блокаторы Н1-рецепторов гистамина I поколения эффективны в профилактике и лечении аллергических ринитов (эффективность около 80%), конъюнктивитов, зуда, дерматитов и крапивницы, ангионевротического отёка, некоторых типов экземы, анафилактического шока, при отёках, вызванных переохлаждением. Блокаторы Н1-рецепторов гистамина первого поколения применяют совместно с симпатомиметиками при аллергической ринорее. Производные пиперазина* и фенотиазина* применяют для предупреждения тошноты, рвоты и головокружения, вызванных резкими движениями, при болезни Меньера, при рвоте после наркоза, при лучевой болезни и утренней рвоте у беременных.
Местное применение этих ЛС учитывает их противозудное, анестезирующее и анальгезирующее действие. Применять их длительно не рекомендовано, так как многие из них способны вызывать гиперчувствительность и обладают фотосенсибилизирующим эффектом.
Фармакокинетика блокаторов Н-рецепторов гистамина I поколения
Блокаторы Н1-рецепторов гистамина I поколения отличаются от препаратов второго поколения кратковременностью действия при относительно быстром наступлении клинического эффекта. Эффект этих ЛС возникает, в среднем, через 30 мин после приёма препарата, достигая пика в пределах 1-2 ч. Длительность действия антигистаминных препаратов первого поколения равна 4-12 ч. Кратковременность клинического действия антигистаминных ЛС первого поколения связана, прежде всего, с быстрым метаболизмом и экскрецией почками.
Большинство из блокаторов Н1-рецепторов гистамина первого поколения хорошо всасывается в ЖКТ. Эти ЛС проникают через ГЭБ, плаценту, а также поступают в грудное молоко. Наибольшие концентрации этих ЛС находят в лёгких, печени, головном мозге, почках, селезёнке и мышцах.
Большинство блокаторов Н1-рецепторов гистамина I поколения метаболизируются в печени на 70-90%. Они индуцируют микросомальные ферменты, что при длительном применении может уменьшить их терапевтический эффект, а также действие других ЛС. Метаболиты многих антигистаминных препаратов выделяются в течение 24 ч с мочой и только небольшие количества - в неизменном виде.
Побочные эффекты и противопоказания к назначению
Побочные эффекты, вызываемые блокаторами Н1-рецепторов гистамина I поколения, представлены в табл. 19-4.
Таблица 19-4. Нежелательные лекарственные реакции антигистаминных лекарственных средств I поколения
 Большие дозы блокаторов Н1-рецепторов
гистамина могут вызвать возбуждение и судороги, особенно у детей. При
этих симптомах нельзя применять барбитураты, так как это вызовет
аддитивный эффект и значительное угнетение дыхательного центра.
Циклизин* и хлорциклизин* имеют тератогенное действие, поэтому их нельзя применять при рвоте у беременных.
Большие дозы блокаторов Н1-рецепторов
гистамина могут вызвать возбуждение и судороги, особенно у детей. При
этих симптомах нельзя применять барбитураты, так как это вызовет
аддитивный эффект и значительное угнетение дыхательного центра.
Циклизин* и хлорциклизин* имеют тератогенное действие, поэтому их нельзя применять при рвоте у беременных.
Взаимодействие лекарственных средств
Блокаторы Н1-рецепторов гистамина I поколения потенцируют эффекты наркотических анальгетиков, этанола, снотворных средств, транквилизаторов. Могут усиливать действие стимуляторов ЦНС у детей. При длительном применении эти ЛС снижают эффективность стероидов, антикоагулянтов, фенилбутазона (бутадиона*) и других ЛС, подвергающихся метаболизму в печени. Сочетанное применение их с антихолинергическими средствами может привести к чрезмерному усилению их эффектов. Ингибиторы МАО усиливают эффект антигистаминных ЛС. Некоторые препараты первого поколения потенцируют влияние адреналина и норадреналина на сердечно-сосудистую систему. Блокаторы Н1-рецепторов гистамина I поколения назначают для профилактики клинических симптомов аллергии, в частности, ринита, часто сопровождающего атопическую бронхиальную астму, для купирования анафилактического шока.
Антигистаминные лекарственные средства II и III поколений
К препаратам II поколения относят терфенадин* , астемизол* , цетиризин, меквипазин* , фексофенадин, лоратадин, эбастин, к III поколению блокаторов Н1-рецепторов гистамина - фексофенадин (телфаст*).
Можно выделить следующие особенности блокаторов Н1-рецепторов гистамина II и III поколений:
• высокая специфичность и высокое сродство к Н1-рецепторам гистамина при отсутствии влияния на серотониновые и м-холинорецепторы;
• быстрое наступление клинического эффекта и длительность действия, что обычно достигается путём высокой степени связи с белками, кумуляции ЛС или его метаболита в организме и замедленного выведения;
• минимальный седативный эффект при использовании препаратов в терапевтических дозах; у некоторых пациентов может наблюдаться умеренная сонливость, которая редко бывает причиной отмены препарата;
• отсутствие тахифилаксии при длительном применении;
• способность блокировать калиевые каналы клеток проводящей системы сердца, что ассоциируется с удлинением интервала Q-T и нарушением ритма сердца (желудочковая тахикардия по типу «пируэт»).
В табл. 19-5 представлена сравнительная характеристика некоторых блокаторов Н1-рецепторов гистамина II поколения.
Таблица 19-5. Сравнительная характеристика блокаторов Н1-рецепторов гистамина II поколения
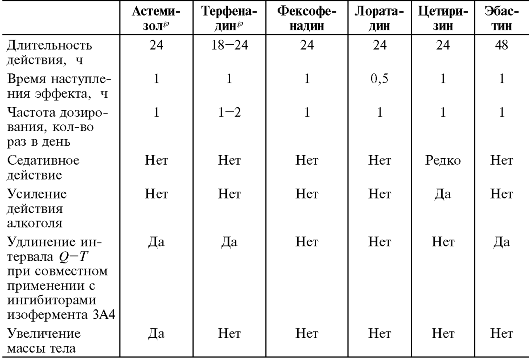 Окончание табл. 19-5
Окончание табл. 19-5
 Фармакодинамика блокаторов Н-рецепторов гистамина II поколения
Фармакодинамика блокаторов Н-рецепторов гистамина II поколения
Астемизол* и терфенадин* не обладают холин- и β-адреноблокирующей активностью. Астемизол* блокирует α-адрено- и серотониновые рецепторы только в больших дозах. Блокаторы Н1-рецепторов гистамина II поколения оказывают слабое терапевтическое действие при бронхиальной астме, так как на гладкую мускулатуру бронхов и бронхиальные железы влияют не только гистамин, но и лейкотриены, фактор активации тромбоцитов, цитокины и другие медиаторы, вызывающие развитие заболевания. Использование только блокаторов Н1-рецепторов гистамина не гарантирует полного купирования бронхоспазма аллергического генеза.
Особенности фармакокинетики блокаторов Н1-рецепторов гистамина II поколения Все блокаторы Н1-рецепторов гистамина II поколения действуют длительно (24-48 ч), а время развития эффекта невелико - 30-60 мин. Около 80% астемизола* выделяется через 14 дней после последнего приёма, а терфенадина* - через 12 дней. Кумулятивный эффект этих ЛС, протекающий без изменения функций ЦНС, позволяет широко использовать их в амбулаторной практике у больных поллинозами, крапивницей, ринитами, нейродермитами и т.д. Блокаторы Н1-рецепторов гистамина II поколения применяют при лечении больных бронхиальной астмой при индивидуальном подборе доз.
Для блокаторов Н1-рецепторов гистамина II поколения в разной степени характерен кардиотоксический эффект, обусловленный бло-
кадой калиевых каналов кардиомиоцитов и выражающийся удлинением интервала Q-T и аритмией на электрокардиограмме.
Риск возникновения данного побочного эффекта увеличивается при комбинации антигистаминных средств с ингибиторами изофермента цитохрома Р-450 3А4 (прил. 1.3): противогрибковыми ЛС (кетоконазол и интраконазол* ), макролидами (эритромицином, олеандомицином и кларитромицином), антидепрессантами (флуоксетином, сертралином и пароксетином), при употреблении грейпфрутового сока, а также у пациентов с выраженными нарушениями функций печени. Совместное применение вышеуказанных макролидов с астемизолом* и терфенадином* в 10% случаев приводит к кардиотоксическому эффекту, связанному с удлинением интервала Q-T. Азитромицин и диритромицин* - макролиды, не ингибирующие изофермент 3А4, а, значит, не вызывающие удлинения интервала Q-T при одновременном приёме с блокаторами Н1-рецепторов гистамина второго поколения.