Онкология : учебник / М. И. Давыдов, Ш. Х. Ганцев. 2010. - 920 с.
|
|
|
|
ГЛАВА 28 ОПУХОЛИ ПОЧЕЧНОЙ ЛОХАНКИ И МОЧЕТОЧНИКА
ЭПИДЕМИОЛОГИЯ
Опухоли почечной лоханки и мочеточника относительно редки. Опухоли лоханки составляют 10 % всех новообразований почки и 5 % всех уротелиальных опухолей. Опухоли мочеточника встречаются в 4 раза реже новообразований почечной лоханки. Заболеваемость опухолями верхних мочевыводящих путей в последнее время увеличивается, но пока неясно, является это истинным увеличением или обусловлено улучшением эндоскопической диагностики, онкологической настороженностью.
Как и опухоли мочевого пузыря, новообразования верхних отделов мочевыводящей системы наиболее часто встречаются в возрасте 60-70 лет. Заболеваемость увеличивается с возрастом, однако опухоли верхних мочевыводящих путей являются редкой находкой на аутопсии. Чаще всего данным заболеванием страдают мужчины (соотношение 3:1). Наиболее часто новообразования данной группы развиваются у европеоидов; соотношение с представителями негроидной расы 2:1. Отмечено повышение заболеваемости раком лоханки и мочеточника у лиц, страдающих балканской нефропатией, в 100- 200 раз. Балканская нефропатия - дегенеративный интерстициальный нефрит неясной этиологии, особенно часто встречающийся на Балканском полуострове. Опухоли верхних мочевых путей, ассоциированные с этим заболеванием, как правило, высокодифференцированные, множественные и двусторонние.
ЭТИОЛОГИЯ
Выявлен ряд факторов, повышающих риск возникновения опухолей верхних мочевыводящих путей. Табакокурение - фактор, повышающий риск развития переходно-клеточного рака верхних мочевых
путей в 3 раза. Около 70 % заболевших мужчин и 40 % женщин - курящие.
С увеличением вероятности развития заболевания сопряжено употребление более семи чашек кофе в сутки.
Анальгетики также повышают риск заболеваемости уротелиальным раком. Существует независимая синергичная взаимосвязь между опухолями верхних мочевых путей и папиллярным некрозом. Длительное употребление анальгетиков индуцирует нефропатию, которая связана с высокой частотой уротелиального рака, достигающей 70 %.
Отмечено повышение риска заболеваемости у лиц, контактировавших с продуктами нефтепереработки, пластиком и пластмассами.
Хроническая мочевая инфекция, травматизация и конкременты могут повысить предрасположенность к развитию переходно-клеточных опухолей и аденокарциномы верхних мочевых путей.
Циклофосфамид увеличивает вероятность развития уротелиального рака. Причиной этого считают негативное действие его метаболита - акролеина. Как правило, возникающие в этом случае опухоли имеют высокую степень дифференцировки.
Кроме того, на появление рака лоханки и мочеточника может оказать влияние наследственность. Существует взаимосвязь данного вида опухолей с синдромом Линча II, включающим раннее появление опухолей толстой кишки и внекишечных опухолей.
МОРФОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ
Наиболее распространенным гистологическим типом опухолей верхних мочевыводящих путей является переходно-клеточный рак, который выявляется у 90 % заболевших. Его развитие строго коррелирует с курением.
Плоскоклеточные опухоли составляют 1-7 % всех уротелиальных опухолей. Плоскоклеточный рак часто ассоциирован с инфицированными конкрементами. Данный гистологический вариант опухоли часто имеет умеренную и низкую степень дифференцировки, а также характеризуется ранним распространением опухолевого процесса.
Аденокарцинома составляет менее 1 % новообразований данной локализации. Нередко при этом гистологическом варианте опухоли у больных имеются конкременты, вызывавшие длительную обструкцию верхних мочевых путей.
Инвертированная папиллома - нечастое новообразование верхних мочевых путей, которое считается доброкачественным, однако возможна ее малигнизация.
В зависимости от степени дифференцировки опухоли выделяют высокодифференцированные (G1), умеренно диффренцированные (G2) и низкодифференцированные (G3) опухоли.
Рост и метастазирование
Переходно-клеточные опухоли верхних мочевых путей распространяются строго в каудальном направлении. Например, отмечается высокая частота рецидивов в культе мочеточника у пациентов, подвергнутых нефрэктомии, резекции мочеточника по поводу рака лоханки. Напротив, рецидивирование в зонах, расположенных проксимальнее поражения мочеточника, практически не встречается. У 30-75 % больных с уротелиальными опухолями верхних мочевых путей в процессе развития болезни развиваются опухоли мочевого пузыря.
Переходно-клеточным опухолям лоханки и мочеточника свойственна лимфогенная и гематогенная диссеминация опухолевого процесса. В зависимости от локализации первичной опухоли могут быть поражены парааортальные, паракавальные, общие подвздошные и тазовые лимфатические узлы со стороны новообразования.
Гематогенные метастазы чаще всего поражают легкие, печень и кости.
Частота переходно-клеточного рака разных отделов верхних мочевыводящих путей такова:
• почечная лоханка - 58 %;
• мочеточник - 35 % (73 % опухолей локализуется в дистальном отделе);
• почечная лоханка и мочеточник - 7 %;
• двустороннее поражение - 2-5 %.
КЛИНИЧЕСКАЯ КАРТИНА
Гематурия является самым распространенным симптомом опухолей верхних мочевыводящих путей (75 %). Боль в пояснице (18 %) бывает следствием нарушения оттока мочи из чашечно-лоханочной системы вследствие наличия опухоли или обструкции мочевых
путей кровяными сгустками. Жалобы на дизурию предъявляют 6 % пациентов. Снижение массы тела, анорексия, пальпируемая опухоль, боль в костях - симптомы распространенного опухолевого процесса и встречаются редко.
ДИАГНОСТИКА
При подозрении на опухоль верхних мочевыводящих путей необходимы лабораторные исследования: общий и биохимический анализы крови (включая определение креатинина, электролитов и щелочной фосфатазы сыворотки крови), коагулограмма, общий анализ мочи (подтверждение гематурии и исключение сопутствующей мочевой инфекции).
Цитологическое исследование мочи из мочевого пузыря - обязательный метод исследования при подозрении на опухоли верхних мочевых путей. Его чувствительность при высокодифференцированных опухолях невысока: частота ложноотрицательных ответов достигает 80 %. При низкодифференцированных опухолях чувствительность цитологического исследования выше (83 %). Диагностическая эффективность метода повышается при селективном получении мочи из обоих мочеточников.
Экскреторная урография позволяет в 50-75 % случаев выявить дефект заполнения верхних мочевых путей, обусловленный опухолью. У 30 % пациентов опухоль вызывает обструкцию мочевых путей, и экскреторная урография выявляет нефункционирующую почку.
Ретроградная урография позволяет лучше визуализировать контуры верхних мочевых путей, чем экскреторная урография; метод предпочтителен у больных с выраженной почечной недостаточностью. Диагностическая точность ретроградной урографии при опухолях лоханки и мочеточника достигает 75 %.
КТ (нативная и с внутривенным болюсным контрастированием) с 3-мерной реконструкцией изображения вытесняет экскреторную урографию из алгоритма диагностики, так как дает более полную информацию об анатомическом строении верхних мочевых путей и пассаже мочи по ним (рис. 28.1). Как правило, на КТ-граммах переходно-клеточные опухоли представлены образованием неправильной формы, обусловливающим дефект заполнения верхних мочевых путей, чаще - гиповаскулярным и слабо
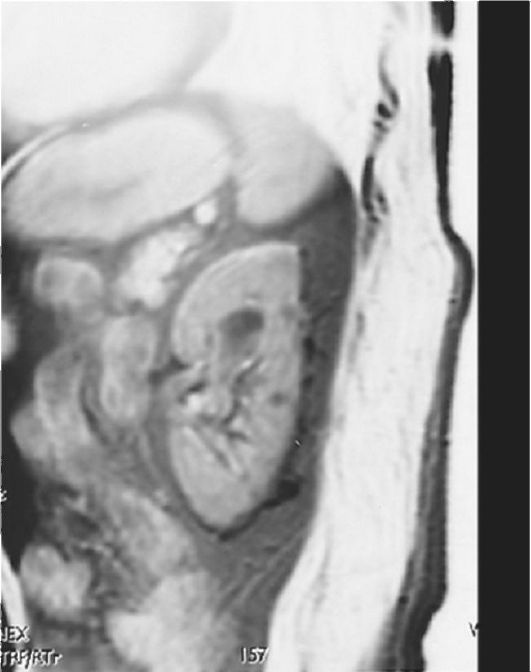 Рис. 28.1. Рак лоханки почки. Компьютерная томограмма
Рис. 28.1. Рак лоханки почки. Компьютерная томограмма
накапливающим контрастный препарат. КТ имеет ограниченную точность в дифференциации категорий Та, Т1 и Т2, однако высокоэффективна в оценке перипельвикальной/периурете- ральной инфильтрации.
МРТ также играет ограниченную роль в определении ранних стадий и характеризуется высокой точностью при оценке распространенных форм опухолей верхних мочевых путей.
Цистоскопия является обязательным методом обследования пациентов с опухолями верхних мочевых путей, направленным на обнаружение опухолей мочевого пузыря.
При наличии технической
возможности всем пациентам выполняют уретеропиелоскопию с биопсией опухоли и цитологическим исследованием промывных вод (рис. 28.2). Диагностическая точность метода при опухолях лоханки составляет 86 %, мочеточника - 90 %. Частота осложнений уретеропиелоскопии достигает 7 %. Тяжелыми осложнениями процедуры являются перфорация, отрыв и последующее развитие стриктуры мочеточника.
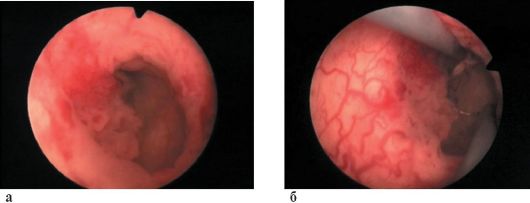 Рис. 28.2. Рак лоханки почки. Эндоскопическое исследование (а, б)
Рис. 28.2. Рак лоханки почки. Эндоскопическое исследование (а, б)
КЛАССИФИКАЦИЯ TNM (2002)
Правила классификации
Представленная ниже классификация применима только для рака. Случаи папилломы настоящей классификацией не описываются. В каждом случае необходимо гистологическое или цитологическое подтверждение диагноза.
Анатомические области
1. Почечная лоханка.
2. Мочеточник.
Регионарные лимфатические узлы
К регионарным относят лимфатические узлы ворот почки, а также парааортальные, преаортальные, интераортокавальные, ретрокавальные и ретроаортальные лимфатические узлы. Для мочеточника к регионарным также относят лимфатические узлы таза.
Наличие ипсилатеральных либо контралатеральных регионарных метастазов не влияет на показатель классификации N.
Клиническая классификация TNM
T - первичная опухоль
Тх - оценка первичной опухоли невозможна.
Т0 - первичная опухоль не обнаружена.
Та - папиллярный неинвазивный рак.
Tis - преинвазивная карцинома (carcinoma in situ).
Т1 - опухоль с поражением подслизистого слоя.
Т2 - опухоль с поражением мышечного слоя.
Т3 - опухоль с поражением жировой клетчатки в области ворот
почки или паренхимы почки (только для рака почечной
лоханки).
Т3 - опухоль с поражением жировой клетчатки таза вокруг мочеточника (только для рака мочеточника).
Т4 - опухоль с поражением соседних органов и околопочечной клетчатки.
N - регионарные лимфатические узлы
? - состояние регионарных лимфатических узлов оценить невозможно.
N0 - метастазов в регионарных лимфатических узлах нет.
N1 - метастаз в один регионарный лимфатический узел, размерами до 2 см в наибольшем измерении.
N2 - метастазы в один или несколько регионарных лимфатических узлов, размером 2,1-5 см в наибольшем измерении.
N3 - метастазы в один или несколько регионарных лимфатических узлов, размером более 5 см в наибольшем измерении.
М - отдаленные метастазы
Мх - наличие отдаленных метастазов оценить невозможно.
М0 - отдаленных метастазов нет.
М1 - наличие отдаленных метастазов.
Патоморфологическая классификация pTNM
Критерии выделения категорий рТ, pN и рМ соответствуют таковым для категорий Т, N и М.
ЛЕЧЕНИЕ
Хирургическое лечение
Локализованные и местно-распространенные опухоли верхних мочевыводящих путей служат показанием к хирургическому лечению. Стандартным подходом к данной категории новообразований является нефруретерэктомия. Открытая нефруретерэктомия выполняется трансперитонеальным доступом и включает удаление почки, мочеточника и части мочевого пузыря, окружающей устье. Регионарная лимфодиссекция при опухолях верхних мочевых путей позволяет адекватно оценить категорию N, а также обладает потенциальным лечебным эффектом у пациентов с метастазами в лимфатические узлы.
Альтернативой открытому хирургическому вмешательству может служить лапароскопическая нефруретерэктомия с резекцией мочевого пузыря. При выполнении лапароскопических вмешательств используются трансперитонеальный, ретроперитонеальный доступы, а также методика с ручным пособием. Техника операции не отличается от таковой при открытом доступе. Резекция мочевого пузыря может быть выполнена эндоскопически до лапароскопии или лапаротомным доступом до удаления эндоскопически мобилизованных почки и мочеточника. Лапароскопическая нефруретерэктомия
ассоциирована с уменьшением объема операционной кровопотери, потребности в обезболивании, укорочением периода госпитализации и реконвалесценции и хорошим косметическим эффектом. При коротких сроках наблюдения онкологические результаты лапароскопических операций соответствуют таковым при использовании открытого доступа.
В последние годы отмечается тенденция к увеличению доли органосохраняющих операций у пациентов с опухолями верхних мочевыводящих путей. Сохранение почки может быть рекомендовано при небольших высокодифференцированных поверхностных опухолях, а также больным с двусторонним поражением, единственной почкой и высоким риском терминальной почечной недостаточности после нефруретерэктомии.
Резекция мочеточника с уретероцистоанастомозом показана пациентам с опухолями дистального отдела мочеточника. Частота местных рецидивов после органосохраняющего лечения достигает 25 %.
Уретероскопическое вмешательство считается методом выбора при небольших высокодифференцированных поверхностных опухолях всех отделов верхних мочевых путей. Объем операции может заключаться в лазерной вапоризации (ниодимовый - Nd:YAG и гольмиевый - Ho:YAG лазеры), трансуретеральной резекции, коагуляции и аблации опухоли. Общими требованиями к уретероскопическим вмешательствам являются: обязательное получение ткани опухоли для гистологического исследования, бережное отношение к интактной слизистой оболочке мочевыводящих путей во избежание развития стриктур (предпочтительнее использование лазера, а не электрохирургического инструментария), дренирование мочевого пузыря и, по показаниям, верхних мочевых путей со стороны операции - для обеспечения адекватного оттока мочи.
Альтернативой нефруретерэктомии при опухолях почечной лоханки и проксимального отдела мочеточника могут служить перкутанные (чрескожные) нефроскопические хирургические вмешательства. Перкутанный доступ позволяет использовать эндоскопы значительного диаметра, что способствует улучшению визуализации. Это позволяет удалять опухоли большего размера, а также осуществлять более глубокую резекцию, чем при уретеропиелоскопии. Для осуществления перкутанного доступа выполняется пункция чашечно-лоханочной системы с последующей дилатацией хода. По сформированному свищу проводят нефроскоп, выполняют пиелоуретеро-
скопию, биопсию и (или) резекцию/аблацию опухоли под контролем зрения. Недостатком метода является риск опухолевого обсеменения нефроскопического хода и развития рецидива. Частота рецидивирования зависит от степени анаплазии опухоли и составляет 18 % при
G1, 33 % - при G2, 50 % - при G3.
Противопоказаниями к хирургическому лечению являются терминальная почечная недостаточность, тяжелые сопутствующие заболевания, а также диссеминация опухолевого процесса.
Консервативное лечение
Эффективность лекарственного лечения в неоадъювантном (дооперационном) и адъювантном (после полного удаления опухоли) режимах при локализованных и местно-распространенных опухолях верхних мочевых путей в отношении времени до прогрессирования и выживаемости не доказана. После эндоскопических операций при множественных, двусторонних и (или) низкодифференцированных поверхностных опухолях (Ta, T1) и carcinoma in situ верхних мочевых путей может проводиться адъювантная терапия, заключающаяся в местных инстилляциях цитостатиков (митомицин С, тиоТЭФ, доксирубицин) или вакцины БЦЖ. Возможно введение данных препаратов через нефростому, по мочеточниковому или уретральному катетеру (у больных с пузырно-мочеточниковым рефлюксом). Обычно инстилляции требуют госпитализации для контроля за объемом и темпами перфузии с целью предотвращения системной абсорбции препаратов.
При местно-распространенных опухолях верхних мочевых путей группы высокого риска (T3-T4, N+) может проводиться адъювантная химиотерапия в режиме (GC): гемцитабин (1000 мг/м2 в 1-й и 8-й дни), цисплатин (70 мг/м2 - 2-й день) или химиолучевая терапия (химиотерапия в режиме GC и облучение ложа удаленной опухоли).
В случае наличия массивных опухолей, вероятность радикального удаления которых низка, можно попытаться провести химиотерапию в том же режиме с последующим хирургическим вмешательством.
До недавнего времени стандартным методом лечения неоперабельных местно-распространенных и диссеминированных опухолей верхних мочевых путей была химиотерапия в режиме MVAC (метотрексат, винбластин, доксорубцин, цисплатин), дающая умеренное увеличение выживаемости в сочетании с высокой токсичностью. Комбинация GC обеспечивает аналогичные частоту объективных ответов, то же время до прогрессирования и выживаемость, но при
меньшей токсичности. В связи с этим GC в настоящее время является стандартом химиотерапии 1-й линии при распространенных уротелиальных опухолях верхних мочевых путей. Проводятся исследования, направленные на выявление в лечении данной категории больных роли сорафениба (таргетный, т.е. действующий на определенные молекулярные мишени, агент, мультикиназный ингибитор).
НАБЛЮДЕНИЕ
Частота наблюдения может варьировать в зависимости от стадии заболевания, степени анаплазии опухоли и вида проведенного лечения. Более тщательный контроль необходим при низкодифференцированных новообразованиях высоких стадий, а также после органосохраняющего лечения.
Стандартный режим наблюдения включает цистоскопию, цитологическое исследование мочи, экскреторную урографию, УЗИ брюшной полости и забрюшинного пространства, а также рентгенографию легких. В связи с низкой диагностической эффективностью цитологического исследования мочи при рецидивах опухолей верхних мочевых путей возможно использование новых маркеров уротелиального рака, таких, как FDP (продукты деградации фибриногена), BTA (мочепузырный опухолевый антиген). Чувствительность методов в отношении выявления рецидивов опухолей лоханки и мочеточника составляет соответственно 29; 100 и 50 %, специфичность - 59; 83 и 62 %.
Пациентам, перенесшим органосохраняющие вмешательства, также выполняют уретеропиелоскопию со стороны поражения. Если невозможно эндоскопическое исследование, проводят ретроградную уретеропиелографию. Чувствительность и специфичность методов в отношении выявления рецидивов составляют соответственно 93,4
и 71,7 %; 65,2 и 84,7 %.
Контрольное обследование проводят каждые 3 мес в течение 1-го года, каждые 6 мес в течение 2-5 лет, далее - ежегодно.
ПРОГНОЗ
5-летняя общая выживаемость больных раком верхних мочевыводящих путей Tis, Ta, T1 составляет 91 %, T2 - 43 %, T3/T4 и (или) N1/N2 - 23 %, N3/M1 - 0 %. При опухолях G1-2 вид хирургического
вмешательства не влияет на выживаемость. Однако результаты органосохраняющего лечения низкодифференцированного уротелиального рака уступают нефруретерэктомии.
Вопросы для самоконтроля
1. Перечислите факторы риска развития рака лоханки почки.
2. Какой гистологический тип опухоли наиболее часто развивается в верхних мочевыводящих путях?
3. Какие группы лимфатических узлов наиболее часто поражаются при опухолях лоханки?
4. Какие органы чаще всего поражаются при гематогенной диссеминации опухоли лоханки почки?
5. Чем обусловлено развитие болевого синдрома в поясничной области при опухоли лоханки?
6. Какой инструментальный метод обследования является обязательным при опухолях лоханки?
7. Какой лабораторный метод обследования является обязательным при опухолях лоханки?
8. Какой объем оперативного вмешательства включает в себя термин «нефруретерэктомия с резекцией мочевого пузыря» при опухолях лоханки почки?
9. Что является показанием для органосохраняющей операции при опухоли лоханки почки?
10. Что является противопоказанием для хирургического лечения опухолей лоханки?
11. Какие методы диагностики входят в стандартное обследование при динамическом контроле у больных, получавших лечение по поводу опухоли лоханки?
12. В какие сроки проводят контрольное обследование у больных, получавших лечение по поводу опухоли лоханки? Какие факторы могут влиять на частоту контрольных обследований?