Онкология : учебник / М. И. Давыдов, Ш. Х. Ганцев. 2010. - 920 с.
|
|
|
|
ГЛАВА 16 ПРЕДРАКОВЫЕ ЗАБОЛЕВАНИЯ И РАК МОЛОЧНОЙ ЖЕЛЕЗЫ
ЭПИДЕМИОЛОГИЯ
Рак молочной железы (РМЖ) - одно из наиболее распространенных злокачественных новообразований у женщин. Заболеваемость РМЖ неуклонно растет и является одной из главных причин смертности женщин среднего возраста в экономически развитых странах. В России РМЖ занимает 1-е место в структуре онкологической заболеваемости у женщин, причем отмечается увеличение заболеваемости и смертности в трудоспособном возрасте. Если в 1997 г. показатель заболеваемости был 52,0 на 100 тыс. женского населения, то в 2007 г. он достиг 67,9. В структуре смертности населения России в трудоспособном возрасте РМЖ занимает 1-е место и составляет 24 %. Высокая заболеваемость РМЖ зарегистрирована в Чеченской Республике (55,5 на 100 тыс. женщин), Калининградской области (50,4), Москве (51,0) и Санкт-Петербурге (49,6). Относительно низкая заболеваемость отмечена в Кировской области (27,5), Республике Тыва (28,1), Калмыкии (25,8) и Дагестане (22,4). В 2000 г. стандартизованный показатель смертности был 17,2 на 100 тыс. населения, в 2005 г. - 17,5. Летальность в течение 1-го года после установления диагноза РМЖ в РФ снизилась
с 12,4 % в 1997 г. до 10,1 % в 2007 г.
ФАКТОРЫ РИСКА
При выявлении групп повышенного риска по РМЖ учитывается ряд факторов, которые условно можно разделить на эндогенные (связанные с внутренней средой организма) и экзогенные.
Классификация факторов риска рака молочной железы (Семиглазов В.Ф. и др., 2001)
1. Факторы, характеризующие функционирование репродуктивной системы организма.
1.1. Менструальная, половая, детородная, лактационная функции.
1.2. Гиперпластические и воспалительные заболевания яичников и матки.
2.Эндокринно-метаболические факторы, обусловленные сопутствующими и предшествующими заболеваниями.
2.1. Ожирение.
2.2. Гипертоническая болезнь.
2.3. Сахарный диабет пожилых.
2.4. Атеросклероз.
2.5. Заболевания печени.
2.6. Заболевания щитовидной железы (гипотиреоз).
2.7. Дисгормональная гиперплазия молочных желез.
3.Генетические факторы (носители генов BRCA1 или BRCA2).
3.1. РМЖ у кровных родственников (наследственные и «семейные» случаи РМЖ).
3.2. Молочно-яичниковый синдром (РМЖ и рак яичников в семье).
3.3. Синдромы.
3.3.1. РМЖ + опухоль мозга.
3.3.2. РМЖ + саркома.
3.3.3. РМЖ + рак легкого + рак гортани + лейкоз.
3.3.4. SBLA-синдром + саркома + РМЖ + лейкоз + карцинома коры надпочечников.
3.4. Раковоассоциированные генодерматозы.
3.4.1. Болезнь Cowden - множественные трихолеммомы кожи + рак щитовидной железы, аденоматозный полипоз, рак толстой кишки + РМЖ.
3.4.2. Болезнь Bloom - аутосомальный наследственный генодерматоз + РМЖ.
4.Экзогенные факторы.
4.1. Ионизирующая радиация.
4.2. Курение.
4.3. Химические канцерогены, общие для всех локализаций опухолей.
4.4. Избыточное потребление животных жиров, высококалорийная диета.
Роль гормональных нарушений
Повышенный риск развития РМЖ связан с нарушением функции гормонпродуцирующих органов. Определяющее значение имеет нарушение гормональной функции яичников, надпочечников, щитовидной железы, гипофиза, гипоталамической системы. Отмечено увеличение риска развития РМЖ при раннем менархе и поздней менопаузе и снижение - у рожавших до 18 лет и с увеличением числа родов.
Другие факторы риска
В последние годы в развитии РМЖ большое внимание уделяется генетическим нарушениям. В литературе описаны 2 типа молекулярных нарушений, связанных с развитием рака: мутация генов и индукция клеточной пролиферации (Семиглазов В.Ф., 2001). Мутация происходит в ключевых генах, ответственных за регуляцию клеточного роста, дифференцировку и гибель клеток (Her 2/neu, c-myc, циклин D1, p53), в результате чего они активизируются или, наоборот, инактивируются. С помощью пролиферации осуществляется «опухольформирующий» эффект.
МАСТОПАТИЯ
Мастопатия - одно из самых распространенных заболеваний у женщин; ее частота в различных популяциях составляет от 40 до 90 %. По определению экспертов ВОЗ, мастопатия является фиброзно-кистозной болезнью, характеризующейся дисплазией - спектром пролиферативных и регрессивных изменений ткани молочной железы с нарушенным соотношением эпителиального и соединительнотканного компонентов. В основе лежит изменение гормонального статуса организма, поэтому мастопатии или дисплазии молочной железы относятся к дисгормональным гиперплазиям. Многие исследователи считают мастопатию, включающую большую группу заболеваний, предраковым состоянием.
Этиология и патогенез
Этиологию и патогенез мастопатии определяют гормональные нарушения гипоталамо-гипофизарно-яичниковой системы, обусловленные колебанием уровней факторов роста и гормонов (эстрогена, прогестерона, дегидроэпиандростерона, трийодтиронина, тироксина, лютеинизирующего гормона (ЛГ), β-хорионического человеческого гонадотропина (β-ХГ), а также изменениями концентрации и активности цитоплазматических рецепторов к ним.
Классификация
В клинической практике принята следующая классификация мастопатии.
1. Диффузная (мелко- и крупноочаговая).
2. Узловая.
3. Смешанная, когда на фоне диффузных изменений определяются узлы.
Д.В. Головин (1969) подразделяет диффузную мастопатию на 5 вариантов.
1. Мазоплазия (масталгия).
2. Фиброаденоматоз.
3. Фиброзирующий аденоз.
4. Цистоаденопапиллома.
5. Эктазия крупных протоков.
Различают 2 основных варианта фиброаденоматоза: непролиферирующий и пролиферирующий.
Клинически различаются 3 формы мастопатии: фиброзная, кистозная, фиброзно-кистозная.
Гистологическая классификация доброкачественных опухолей молочной железы (ВОЗ, 1978-1981):
1. Эпителиальные опухоли.
1.1. Интрадуктальная папиллома.
1.2. Аденома соска.
1.3. Аденома.
1.3.1. Тубулярная.
1.3.2. Лактирующая.
1.4. Прочие.
2. Смешанные соединительнотканные и эпителиальные опухоли. 2.1. Фиброаденома:
2.1.1. Периканаликулярная (околопротоковая) фиброаденома.
2.1.2. Интраканаликулярная (внутрипротоковая) фиброаденома.
2.1.2.1. Простой тип.
2.1.2.2. Клеточная внутрипротоковая фиброаденома. 2.2. Филлоидная опухоль (кистозная карцинома филлоидная).
3. Смешанные опухоли.
3.1. Опухоли мягких тканей.
3.2. Опухоли кожи.
4. Неклассифицируемые опухоли.
5. Дисплазия молочной железы (фиброзно-кистозное заболевание).
6. Опухолеподобные процессы.
6.1. Эктазия протока.
6.2. Воспалительные псевдоопухоли.
6.3. Гамартома.
6.4. Гинекомастия.
6.5. Прочие.
Клиническая картина
Первым симптомом мастопатии является боль в молочных железах, связанная или не связанная с менструальным циклом; при осмотре определяются уплотнения диффузного или локального характера. Участки уплотнений не имеют четких контуров, могут быть разными по консистенции и размеру. При мастопатии могут отмечаться сероватые или желтого цвета, водянистые или слизеподобные выделения из соска. Если на фоне диффузно-кистозной мастопатии выявляются отдельные узлы, то определяют узловую форму мастопатии. При узловых формах патологический процесс локализуется преимущественно на ограниченных участках в виде плотных конгломератов. Морфологически отмечается пролиферация всех элементов ткани молочной железы - протоков, долек и фиброзной соединительной ткани. Морфологически также отмечаются кистозные образования, узлы с выраженной пролиферацией и атипией эпителия.
Лечение диффузной мастопатии
Лечение мастопатии должно носить комплексный характер и может включать:
1) эндокринотерапию:
• препараты растительного происхождения, нормализующие баланс гонадотропных гормонов гипофиза (мастодинон, циклодинон и др.);
• антиэстрогены (кломифен, тамоксифен, торемифен);
• препараты, подавляющие гонадотропную функцию гипофиза и приводящие к ановуляции или даже прекращению менструальной функции (даназол);
• эстрогены в малых (физиологических) дозах;
• андрогены в малых дозах;
• эндокринотерапия, направленная на подавление секреции гипофизом пролактина (парлодел, леводофа);
• тиреотропные средства и гормоны щитовидной железы (тиреоидин);
• в возрасте 18-34 лет - последовательный прием эстрогенов и прогестинов, оральных контрацептивов, прогестинов; в 35-47 лет - прием эстрогенов и прогестинов; в 48-54 года - прием прогестинов и антиэстрогенов; в возрасте старше 55 лет - антиэстрогенов; у женщин в доклимактерическом периоде - антигонадотропинов (бусерелин, даноген). Но в активном детородном периоде назначать их рекомендуется лишь в ситуациях особого риска рака (III степень дисплазии или cancer in situ);
2) витамины;
3) седативные средства;
4) мочегонные и средства, улучшающие лимфодренаж;
5) терапию сопутствующих заболеваний (в основном заболеваний печени).
При локализованных формах мастопатий, не поддающихся консервативному лечению, необходимо хирургическое лечение: иссечение опухоли, секторальная резекция молочной железы.
Диспансеризация
Оптимальная частота обследования пациенток из группы риска при диффузных формах дисгормональных заболеваний - 6 мес; при узловых формах (в случае отказа от оперативного лечения) - 3 мес; при отсутствии клинических признаков заболевания с наличием факторов риска: до 40 лет - 24 мес, после 40 лет - 12 мес. Периодичность осмотров для здоровых женщин - 1 раз в год.
ПРОФИЛАКТИКА
Профилактика РМЖ подразделяется на первичную, вторичную и третичную.
Первичная профилактика - это предупреждение заболевания путем изучения этиологических факторов и факторов риска, охрана окружающей среды и уменьшение влияния канцерогенов на организм человека, нормализация семейной жизни, регулярная половая жизнь, своевременное осуществление детородной функции, грудное вскармливание младенца, исключение браков при обоюдной онкологической отягощенности.
Вторичная профилактика - раннее выявление и лечение предопухолевых заболеваний молочных желез - различных форм мастопатии, фиброаденом, других доброкачественных опухолей и заболеваний, а также нарушений эндокринной системы, заболеваний женских половых органов, нарушений функции печени (Демидов В.П., 2000).
Третичная профилактика - предупреждение, ранняя диагностика и лечение рецидивов, метастазов и метахронных новообразований.
Патолого-анатомическая характеристика
Патолого-анатомическую характеристику РМЖ отражают гистологические особенности опухоли. Они включают: размер опухоли, локализацию первичного очага в молочной железе, тип роста, морфологическое строение, степень дифференцировки и злокачественности, наличие регионарных метастазов.
Размер первичной опухоли является показателем биологической активности опухоли и важным прогностическим фактором при РМЖ. С увеличением массы опухоли нарастают ее агрессивность, интенсивность лимфогенного и гематогенного метастазирования. Локализация рака в молочной железе имеет прогностическое значение, что обусловлено путями лимфооттока из разных ее квадрантов. Метастазирование рака в подмышечные лимфатические узлы наиболее часто происходит из опухолей, расположенных в подареолярной зоне и на границе наружных и внутренних квадрантов железы, что объясняется наиболее выраженной в этих зонах отводящей лимфатической сетью. Опухоли, расположенные в медиальных и центральных отделах молочной железы, могут метастазировать в парастернальные лимфатические узлы.
Важное прогностическое значение имеет тип роста опухоли, что отражает степень ее злокачественности. С учетом типа развития выделяются 2 основные формы рака: узловая и диффузная
(диффузно-инфильтративная, отечно-инфильтративная, панцирная, инфламаторная - мастито- и рожеподобная). По темпу роста различают:
1) быстрый рост опухоли (время удвоения размеров опухоли - 1-3 мес);
2) средний (удвоение размеров опухоли - в сроки от 3 до 12 мес);
3) медленный (время удвоения размеров опухоли - более 12 мес). По анатомической форме роста РМЖ различают 3 разновидности
(Семиглазов В.Ф. и др., 1986):
• узловые формы (отграниченно растущие, местно-инфильтративно растущие);
• диффузные формы (отечные, диффузно-инфильтративные, лимфангитические);
• атипичные формы (рак Педжета, первично-метастатический (скрытый) рак).
Морфологическая структура РМЖ имеет определенное значение для прогноза заболевания. Гистологическое строение опухоли зависит от исходных клеток, из которых она развивается. Наиболее часто РМЖ представлен инвазивным протоковым и инвазивным дольковым раком, а также их комбинациями.
На основании степени тканевой и клеточной атипии (изучение тубулярных и протоковоподобных структур, числа митозов, клеточного полиморфизма) определяют 3 степени злокачественности опухоли - по сумме баллов (модифицированная схема P. Scarff, H. Bloom и W. Richardson):
• I (низкая степень атипии) - 3-5 баллов;
• II (умеренная) - 6-7 баллов;
• III (высокая) - 8-9 баллов.
На мембранах клеток имеются белки-рецепторы, которые, соединяясь c гормонами, могут определять скорость деления опухолевых клеток. Определение уровня рецепторов стероидных гормонов позволяет судить о чувствительности опухоли к гормональному лечению и определять тактику лечения.
Пути метастазирования
При РМЖ метастазирование происходит по молочным ходам железы, лимфатическим щелям, капиллярам и кровеносным сосудам. В зависимости от путей метастазы распространяются в разные ткани и органы (рис. 16.1, 16.2).
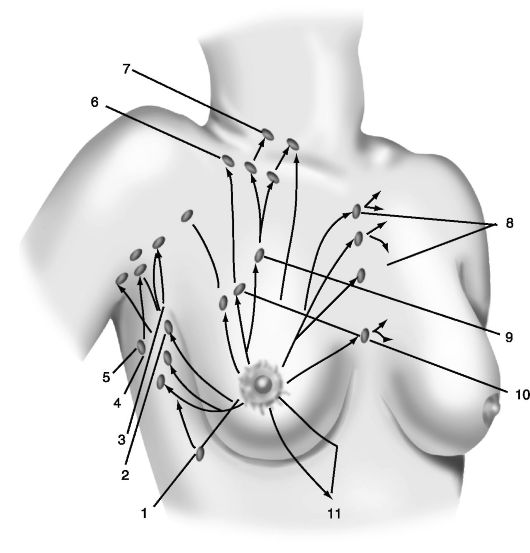 Рис. 16.1. Пути лимфооттока в регионарные лимфатические узлы молочной железы с учетом квадранта:
Рис. 16.1. Пути лимфооттока в регионарные лимфатические узлы молочной железы с учетом квадранта:
1 - околоареолярная сеть лимфатических сосудов (сплетение Саппея); 2 - узел Бартельса, узел Соргцуса; 3 - латеральные подмышечные лимфатические узлы; 4 - центральные подмышечные лимфатические узлы; 5 - подлопаточные лимфатические узлы; 6 - подключичные лимфатические узлы; 7 - надключичные лимфатические узлы; 8 - парастернальные лимфатические узлы; 9 - позадигрудинные лимфатические узлы; 10 - межгрудинные лимфатические узлы (узел Роттера); 11 - лимфатические сосуды, направляющиеся в эпигастральную область
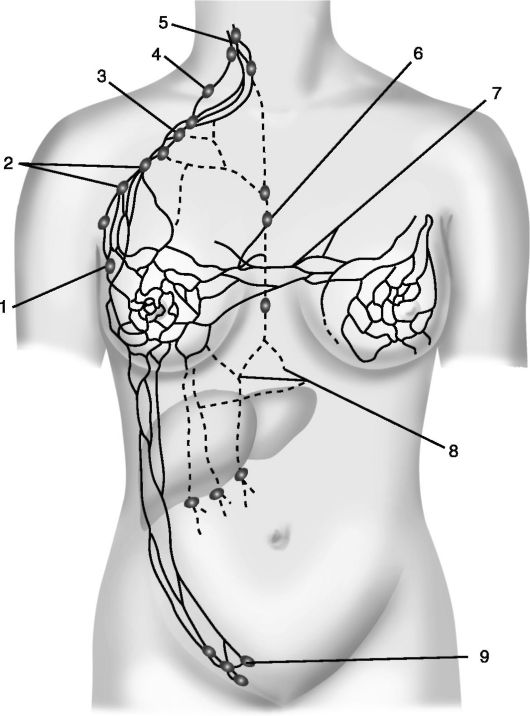 Рис. 16.2. Схема лимфооттока из молочной железы:
Рис. 16.2. Схема лимфооттока из молочной железы:
1 - парамаммарные лимфатические узлы; 2 - центральные подмышечные лимфатические узлы; 3 - подключичные лимфатические узлы; 4 - надключичные лимфатические узлы; 5 - глубокие шейные лимфатические узлы; 6 - парастернальные лимфатические узлы; 7 - перекрестные лимфатические пути, соединяющие лимфатические системы обеих молочных желез; 8 - лимфатические сосуды, идущие в брюшную полость; 9 - поверхностные паховые лимфатические узлы
Метастазирование при РМЖ.
1. Регионарное (лимфогенное) - в лимфатические узлы.
1.1. Подмышечные.
1.2. Подлопаточные.
1.3. Подключичные.
1.4. Надключичные.
1.5. Парастернальные.
2. Отдаленное (лимфогематогенное) - в следующие структуры.
2.1. Контралатеральные подмышечные лимфатические узлы.
2.2. Контралатеральные надключичные лимфатические узлы.
2.3. Мягкие ткани, кожу.
2.4. Печень.
2.5. Легкие.
2.6. Кости: тела позвонков, тазовые, бедренные и др.
2.7. Плевру.
2.8. Яичники.
2.9. Головной мозг и другие органы.
Лимфогенное метастазирование рака может происходить в разных направлениях. Существуют:
1) пекторальный путь (60-70 %) - к парамаммарным лимфатическим узлам и далее к подмышечным;
2) подключичный путь (20-30 %) - к подключичным лимфатическим узлам;
3) парастернальный путь (10 %) - к парастернальным узлам;
4) перекрестный путь (5 %) - в подмышечные лимфатические узлы противоположной стороны и в другую молочную железу;
5) позадигрудинный путь (2 %) - к медиастинальным лимфатическим узлам, минуя парастернальные;
6) транспекторальный путь (редко) - к центральным (верхним) подмышечным лимфатическим узлам;
7) лимфоотток по лимфатическим путям Герота (встречается редко) - к эпигастральным лимфатическим узлам и узлам брюшной полости;
8) внутрикожный путь (редко) - по брюшной стенке к паховым лимфатическим узлам.
Наиболее часто при РМЖ отдаленные метастазы гематогенным путем поражают кости, легкие, печень, кожу. Метастазы рака в легкие бывают в виде одиночных или множественных узлов. По данным В.П. Демидова (2000), метастатическое поражение костей при РМЖ
выявляется при первичном лечении больных в 1,3-6 % случаев, а на аутопсии обнаруживается в 44-70 % наблюдений; частота метастазов рака в печень, выявленных сканированием до радикального лечения, составляет около 1,5 %, а на аутопсии - от 35 до 67 %.
Деление на стадии
Классификация РМЖ по распространенности процесса способствует составлению индивидуального рационального плана лечения, выбору комплекса методов лечения и оценке отдаленных результатов.
Отечественная клинико-морфологическая классификация по стадиям (1985)
I стадия - опухоль диаметром до 2 см без прорастания в окружающую жировую клетчатку и кожу. Регионарные метастазы отсутствуют.
Па стадия - опухоль диаметром от 2 до 5 см, не прорастающая в окружающую ткань, или опухоль того же или меньшего размера, прорастающая в жировую клетчатку и спаянная с кожей (симптомы морщинистости, «площадки»). Регионарные метастазы отсутствуют.
Пб стадия - опухоль той же или меньшей степени местного распространения с одиночными (не более 2) метастазами на стороне поражения, смещаемыми подмышечными и (или) парастернальными.
Ша стадия - опухоль диаметром более 5 см, не прорастающая в окружающую ткань, или опухоль любого размера, инфильтрирующая подлежащие фасциально-мышечные слои или кожу (симптом умбиликации, «лимонной корки», ограниченный отек, возможно изъязвление кожи, втяжение соска). Регионарные метастазы отсутствуют.
Шб стадия - опухоль той же или меньшей степени местного распространения с одиночными (не более 2) ограниченно смещаемыми или множественными метастазами в подмышечных, подлопаточных, подключичных, парастернальных узлах на стороне поражения; опухоль той же или меньшей степени распространения с метастазами в надключичных лимфатических узлах на стороне поражения. Метастазы в надключичной области могут сочетаться с другими метастазами.
!Уа стадия - местно-распространенная опухоль с наличием диссеминации по коже (сателлиты) или обширным изъязвлением, или
фиксированная к грудной клетке, или с тотальным отеком молочной железы. Все острые формы рака молочной железы, рожеподобные, маститоподобные, панцирные. Регионарные метастазы не определяются.
IV6 стадия - опухоль той же степени местного распространения с любыми вариантами регионарного метастазирования или опухоль меньшей степени местного распространения с одиночными ограниченно смещаемыми или множественными смещаемыми надключичными (или несмещаемыми) регионарными метастазами. Опухоль любой степени местного распространения с клинически определяемыми отдаленными метастазами, в том числе лимфогенными контралатеральными.
МЕЖДУНАРОДНАЯ КЛАССИФИКАЦИЯ ПО СИСТЕМЕ TNM (2002)
Правила классификации
Представленная ниже классификация применима для РМЖ как у женщин, так и мужчин. В каждом случае необходимы гистологическое подтверждение диагноза и указание гистологического типа опухоли. Анатомическую локализацию опухоли следует указывать, несмотря на то что этот критерий не включен в классификацию.
В случае множественного ипсилатерального рака показатель Т зависит от размеров самого крупного очага. При одновременном билатеральном раке каждый очаг оценивают как отдельную опухоль в изолированном органе.
Анатомические области
1. Сосок и ареола.
2. Центральная часть железы.
3. Верхневнутренний квадрант железы.
4. Нижневнутренний квадрант железы.
5. Верхненаружный квадрант железы.
6. Нижненаружный квадрант железы.
7. Подмышечная задняя часть молочной железы.
8. Комбинированное поражение отдельных областей молочной железы.
Регионарные лимфатические узлы
1. Подмышечные (ипсилатеральные): межгрудные лимфатические узлы (Po^epa), а также узлы по ходу подмышечной вены и ее притоков. Последние могут быть разделены на 3 уровня:
А - I уровень (нижние подмышечные) - лимфатические узлы по
наружной границе малой грудной мышцы. В - II уровень (средние подмышечные) - лимфатические узлы в проекции малой грудной мышцы, а также межгрудные лимфатические узлы (Роттера). С - III уровень (нижние подмышечные) - лимфатические узлы, расположенные кнутри от медиальной границы малой грудной мышцы, включая узлы у ее вершины.
Обратите внимание!
Негрудинные лимфатические узлы относят к подмышечным.
2. Подключичные (ипсилатеральные).
3. Окологрудинные (ипсилатеральные): лимфатические узлы межреберных промежутков вдоль края грудины в толще внутригрудной фасции.
4. Надключичные: лимфатические узлы в надключичной ямке - треугольном пространстве, ограниченном снаружи и сверху брюшком и сухожилием лопаточно-подъязычной мышцы, изнутри - внутренней яремной веной, а снизу - ключицей и подключичной веной.
Поражение остальных групп лимфатических узлов, включая шейные или контралатеральные окологрудинные, относят к отдаленным метастазам (М1).
Клиническая классификация TNM
Т - первичная опухоль
Тх - оценка первичной опухоли невозможна. Т0 - первичная опухоль не обнаружена. Tis - рак in situ.
Tis (DCIS) - протоковый рак in situ.
Tis (LCIS) - дольковый рак in situ.
Tis (Paget>s) - рак Педжета соска молочной железы.
Обратите внимание!
Рак Педжета в сочетании с опухолью паренхимы железы оценивают в соответствии с размерами последней.
Т1 - опухоль не более 2 см в наибольшем измерении:
Т1гшс - микроинвазивный* рак размером до 0,1 см в наибольшем измерении; Т1а - опухоль более 0,1 см, но до 0,5 см в наибольшем измерении;
T1b - опухоль более 0,5 см, но до 1 см в наибольшем измерении;
Т1с - опухоль более 1 см, но до 2 см в наибольшем измерении.
Т2 - опухоль более 2 см, но до 5 см в наибольшем измерении.
Обратите внимание!
* Микроинвазия - это распространение опухолевых клеток за пределы базальной мембраны размером до 0,1 см в наибольшем измерении. В случае множественных очагов микроинвазии указывают самый крупный очаг (суммарные размеры очагов подсчитывать не нужно). Кроме того, аналогично случаю с множественным инвазивным РМЖ, необходимо указать точное число очагов.
Т3 - опухоль более 5 см в наибольшем измерении.
Т4 - опухоль любых размеров с непосредственным распространением на грудную стенку (а) или (b) с учетом описанных ниже принципов:
Т4а - опухоль поражает грудную стенку, но не распространяется на грудные мышцы*;
T4b - отек (включая симптом лимонной корки), изъязвление кожи или сателлитные метастазы в коже одноименной молочной железы;
Т4с - сочетание признаков Т4а и T4b;
T4d - воспалительная форма рака молочной железы**.
Обратите внимание!
* Грудная стенка включает ребра, межреберные мышцы и переднюю зубчатую мышцу. Грудные мышцы в состав грудной стенки не входят.
** Воспалительная форма рака характеризуется диффузным покраснением и отеком (включая симптом «лимонной корки») железы. Объемное образование при пальпации железы в большинстве случаев не выявляют. Воспалительную форму РМЖ относят к группе T4d; в первую очередь ее определяют по данным клинических методов исследования. При отсутствии характерных изменений по результатам биопсии
кожи показатель Т расценивают как рТХ. Втяжение кожи и соска, а также иные изменения на коже, за исключением описанных применительно к группам T4b и T4d, способны развиться на любой стадии опухоли (Т1, Т2, ТЗ) и не ведут к пересмотру категории классификации.
N - регионарные лимфатические узлы
? - состояние регионарных лимфатических узлов оценить невозможно (к примеру, они были ранее удалены).
N0 - регионарные лимфатические узлы не пальпируются.
N1 - пальпируются подвижные подмышечные лимфатические узлы на стороне поражения.
N2 - подмышечные лимфатические узлы на стороне поражения спаяны друг с другом и с окружающими тканями, либо имеются клинические признаки* метастазов в окологрудинных лимфоузлах при отсутствии таковых в подмышечных узлах: ?а - подмышечные лимфатические узлы на стороне поражения спаяны друг с другом и с окружающими тканями;
N2b - клинические признаки* метастазов в окологрудинных лимфатических узлах при отсутствии таковых в подмышечных узлах. N3 - пальпируются подключичные лимфатические узлы на стороне поражения вне зависимости от состояния подмышечных узлов, либо имеются клинические признаки* метастазов в окологрудинные лимфатические узлы на стороне поражения и подмышечные узлы, либо имеются метастазы в надключичные лимфатические узлы вне зависимости от состояния подмышечных или окологрудинных узлов: N3a - метастазы в подключичные лимфатические узлы на
стороне поражения; N3b - метастазы в окологрудинные и подмышечные лимфатические узлы на стороне поражения; N3c - метастазы в надключичные лимфатические узлы на стороне поражения.
Обратите внимание!
* Клинические признаки метастазов включают в себя данные клинических и лучевых методов исследования (за исключением лимфосцинтиграфии) или патоморфологического исследования при условии макроскопической опухоли.
М - отдаленные метастазы
Мх - наличие отдаленных метастазов оценить невозможно.
М0 - отдаленных метастазов нет.
М1 - наличие отдаленных метастазов.
Категории M1 могут быть дополнены в зависимости от локализации отдаленных метастазов: легкое - PUL, костный мозг - MAR, кости - OSS, плевра - PLE, печень - HEP, брюшина - PER, головной мозг - BRA, надпочечник - ADR, лимфатические узлы - LYM, кожа - SKI, другие - OTH.
Патоморфологическая классификация pTNM
рТ - первичная опухоль
Для оценки показателя рТ удаление первичной опухоли проводят таким образом, чтобы ее макроскопические признаки в краях резекции отсутствовали. В противном случае для оценки показателя рТ такой образец РМЖ не используют; чаще всего эти опухоли оценивают как рТх.
Обратите внимание!
С помощью патоморфологических методов измеряют только инвазивный компонент опухоли. К примеру, если внутрипротоковый компонент рака составляет 4 см, а инвазивный - 0,5 см, такую опухоль относят к группе T1a.
pN - регионарные лимфатические узлы
С целью оценки показателя pN проводят резекцию и микроскопическое исследование нижних подмышечных лимфатических узлов (1-го уровня). Объем резекции обычно составляет 6 лимфатических узлов или более.
В настоящее время принято, что отсутствие характерных изменений ткани при патоморфологическом исследовании биоптатов меньшего количества лимфатических узлов позволяет подтвердить стадию pN0.
Иногда для патоморфологического стадирования проводят исследование одного или нескольких сторожевых лимфатических узлов. Если стадия основана только на данных гистологического исследования сторожевого лимфатического узла, обозначение опухоли дополняют символами sn в скобках - например, pN1(sn).
pN - состояние регионарных лимфатических узлов оценить невозможно (к примеру, их невозможно удалить либо они были удалены ранее).
pN0 - по данным гистологического исследования метастазы в регионарных узлах отсутствуют, дополнительные исследования для выявления изолированных опухолевых клеток не предпринимали.
Обратите внимание!
Под изолированными опухолевыми клетками понимают одиночные клетки или их скопление размером до 0,2 мм в наибольшем измерении, которые выявляют с помощью иммуногистохимии, молекулярно-генетических методов, а также при микроскопии гистологических срезов, окрашенных гематоксилином и эозином. В большинстве случаев изолированные опухолевые клетки не проявляют признаков гистологической активности (пролиферации злокачественных клеток или лимфогистиоцитарной инфильтрации стромы).
p^ink; - микрометастазы размером более 0,2 мм, но до 2,0 мм.
pN1 - микроскопическое метастазы в 1-3 подмышечных и (или) окологрудинных узлах по данным гистологического исследования сторожевого лимфатического узла (клинические признаки метастазов отсутствуют)**:
pN1a - метастазы в 1-3 подмышечных лимфатических узлах;
pN1b - микроскопические метастазы в окологрудинные лимфатические узлы по данным гистологического исследования сторожевого узла (клинические признаки метастазов отсутствуют)**;
pN1c - микроскопические метастазы в 1-3 подмышечных и окологрудинных узлах по данным гистологического исследования сторожевого лимфатического узла (клинические признаки метастазов отсутствуют)**.
pN2 - метастазы в 4-9 подмышечных лимфатических узлах или наличие клинических признаков* поражения окологрудинных узлов при отсутствии метастазов в подмышечных лимфоузлах:
pN2a - метастазы в 4-9 подмышечных лимфоузлах (максимальные размеры хотя бы одного метастаза превышают 2,0 мм);
pN2b - клинические признаки* метастазов в окологрудинных лимфоузлах при отсутствии поражения подмышечных узлов.
pN3 - метастазы в десяти подмышечных лимфатических узлах и более либо в подключичных узлах. К этой же группе относят опухоли с клиническими признаками* метастазов в окологрудинных узлах на стороне поражения, а также с наличием одного пораженного подмышечного узла или более, либо опухоли с поражением четырех подмышечных узлов и более, а также с микроскопическими окологрудинными метастазами, не имеющими клинических проявлений. К этой же группе относят опухоли с метастазами в надключичных узлах на стороне поражения: pN3a - метастазы в десяти подмышечных лимфатических узлах и более (максимальные размеры хотя бы одного метастаза превышают 2,0 мм) или поражение подключичных узлов; - клинические признаки* метастазов в окологрудинных узлах на стороне поражения при наличии одного или нескольких метастазов в подмышечных узлах или поражение четырех подмышечных и более, а также микроскопическое поражение окологрудинных узлов по данным гистологического исследования сторожевого узла при отсутствии соответствующих клинических признаков**; р?с - метастазы в надключичные лимфоузлы на стороне поражения.
Обратите внимание!
* К клиническим признакам метастазов относят результаты физикального обследования, а также лучевых методов исследования (за исключением лимфосцинтиграфии).
** Отсутствие клинических признаков метастазов - отсутствие результатов лучевых методов исследования (за исключением лимфосцинтиграфии).
рМ - отдаленные метастазы
Критерии выделения категории рМ соответствуют таковым для категории М.
G - гистопатологическая дифференцировка
Ох - степень дифференцировки не может быть установлена. G1 - высокая степень дифференцировки. G2 - средняя степень дифференцировки. G3 - низкая степень дифференцировки. G4 - недифференцированные опухоли.
R-классификация
Наличие или отсутствие резидуальных опухолей после лечения обозначается символом R:
Rх - недостаточно данных для определения резидуальной опухоли.
R0 - резидуальная опухоль отсутствует.
R1 - резидуальная опухоль определяется микроскопически. R2 - резидуальная опухоль определяется макроскопически.
Группировка по стадиям
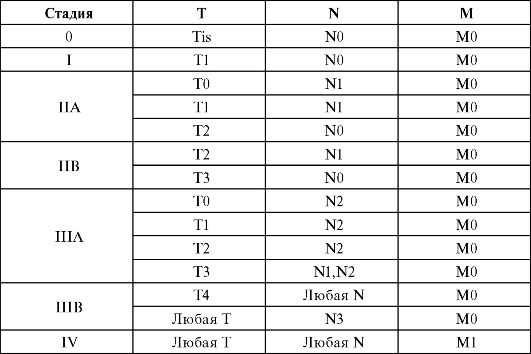 Прогноз больных с pN1a аналогичен прогнозу больных с pN0.
Прогноз больных с pN1a аналогичен прогнозу больных с pN0.
КЛИНИЧЕСКАЯ КАРТИНА
По клинической картине РМЖ подразделяется на 3 основные формы: узловую, диффузную и атипические, характеризующиеся различным течением и прогнозом.
Клиническая классификация
1. Узловая форма.
2. Диффузная форма:
2.1. Отечно-инфильтративная.
2.2. Маститоподобная.
2.3. Рожистоподобная.
2.4. Панцирная.
3. Атипические формы:
3.1. Рак Педжета.
3.2. Рак из придатков кожи.
3.3. Двусторонний рак.
3.4. Эктопированный рак.
3.5. Мультицентрический рак.
Узловая форма
При I-II стадии у больных может выявляться небольшой опухолевидный узел плотной консистенции, безболезненный; могут быть кожные симптомы - морщинистость, умбиликация; в подмышечной области нередко определяются единичные или несколько подвижных лимфатических узлов (рис. 16.3).
При раке молочной железы III-IV стадии обнаруживается большая опухоль, имеются кожные симптомы в виде морщинистости, «лимонной корки», гиперемии кожи, втяжения соска (рис. 16.4) и деформации молочной железы, изъязвления или прорастания кожи опухолью (рис. 16.5, 16.6), пакеты малоподвижных лимфатических узлов в регионарных зонах или отдаленные метастазы, возможен отек руки.
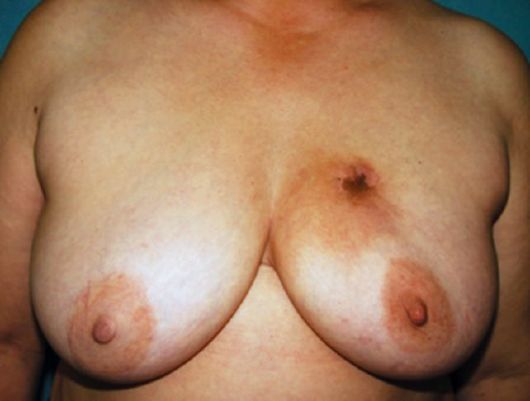 Рис. 16.3. Рак левой молочной железы
Рис. 16.3. Рак левой молочной железы
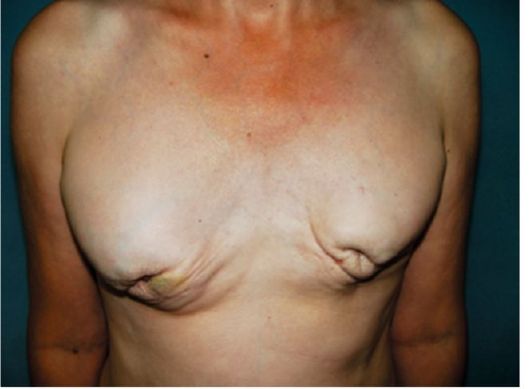 Рис. 16.4. Рак обеих молочных желез
Рис. 16.4. Рак обеих молочных желез
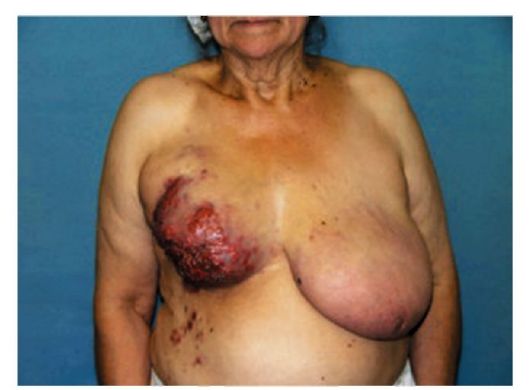 Рис. 16.5. Рак правой молочной железы с диссеменацией на переднюю брюшную стенку
Рис. 16.5. Рак правой молочной железы с диссеменацией на переднюю брюшную стенку
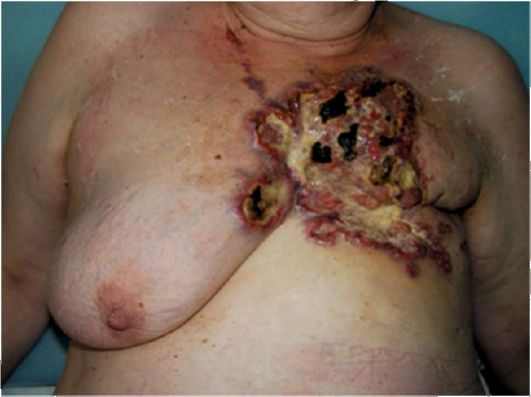 Рис. 16.6. Рак левой молочной железы с распадом
Рис. 16.6. Рак левой молочной железы с распадом
Особые формы
При отечно-инфильтративной форме определяется инфильтрат без четких контуров, занимающий большую часть молочной железы; железа увеличена в объеме, кожа мраморного цвета, отечна, выражены гиперемия и симптом «лимонной корки».
При маститоподобной форме молочная железа значительно увеличена, плотная при пальпа-
ции. Выражены гиперемия и гипертермия кожи за счет присоединившейся инфекции, которая обусловливает деструкцию ткани со всеми признаками мастита. Отмечается высокая температура тела.
При эризипелоидной (рожистоподобной) форме опухолевый процесс с переходом на кожные покровы сопровождается выраженной гиперемией кожи (внешне напоминает рожистое воспаление). Гиперемия может распространяться на грудную клетку. Кожа железы представлена красными плотными очагами иногда с изъязвлениями.
При панцирной форме наблюдается опухолевая инфильтрация всей молочной железы и кожи с переходом на грудную стенку. Появляется множество внутрикожных опухолевых узлов. Молочная
железа сморщивается, деформируется. Эта форма является IV стадией отечно-инфильтратив-
ного РМЖ.
Рак Педжета - своеобразная злокачественная опухоль, поражающая сосок и ареолу (рис. 16.7). По клинической картине различают экземоподобную (узелковые мокнущие изменения в области ареолы), псориазоподобную (с образованием чешуек и бляшек), язвенную (кратерообразная язва с плотными краями) и опухолевую (уплотнение в подареолярной зоне или в области соска) формы. Первым клиническим признаком является утолщение соска - симптом Краузе.
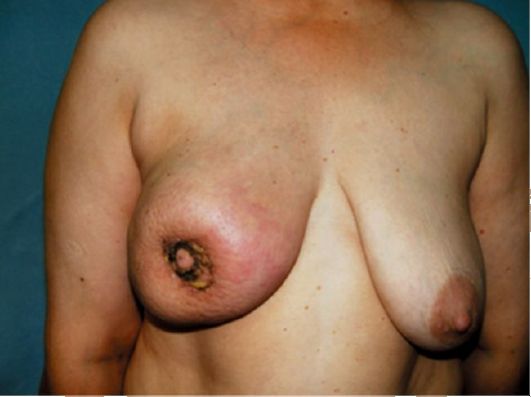 Рис. 16.7. Рак Педжета
Рис. 16.7. Рак Педжета
ДИАГНОСТИКА
При дифференциальной диагностике РМЖ и других заболеваний определяющее значение имеет цитологическое исследование пунктата из уплотнения и выделений из соска. РМЖ следует дифференцировать с доброкачественными новообразованиями молочной железы (различными узловыми формами мастопатии, фиброаденомами, липомами, лимфогранулемами, галактоцеле, ангиоматозными опухолями, саркомами). Необходимо осуществить комплексное обследование и на основе данных клиники, маммографии, УЗ-диагностики, цитологии проводить дифференциальную диагностику. Следует дифференцировать маститоподобные формы рака, отечно-инфильтративную форму РМЖ и острый мастит. Мастит характеризуется острым и коротким началом, сопровождается болями и поддается противовоспалительному лечению; чаще встречается у молодых женщин и бывает связан с лактацией.
Обследование больных
Важный метод диагностики РМЖ - объективное обследование. Диагностика должна быть комплексной, включающей несколько методов исследования.
При подозрении на рак основными методами являются:
1) клинический - осмотр, пальпация;
2) рентгенологический - бесконтрастная маммография, дуктография (галактография), чрезгрудинная флебография, пневмоцистография, КТ;
3) морфологический: цитологический и гистологический;
4) ультразвуковой.
Методика пальпации молочных желез и лимфатических узлов
Пальпация является доступным и наиболее простым методом диагностики РМЖ.
Пальпацию молочных желез необходимо проводить в вертикальном и горизонтальном положении больной, раздетой до пояса. Проводят поверхностную и глубокую пальпацию молочных желез, в направлении от соска к периферии по всем квадрантам железы. Пальпацией определяют локализацию опухоли, ее размеры, границы, отношение к окружающим тканям. Узловые формы рака пальпируются как плотные образования; твердость их уменьшается от центра к периферии. Опухоли нередко связаны с подкожной клетчаткой и кожей, реже - с подлежащей мышечной фасцией и грудной стенкой, поэтому плохо смещаются при пальпации. При осмотре можно заметить изменения со стороны кожи молочной железы в виде утолщения, отека, нарушения сосудистого рисунка, покраснения, гиперемии; эти признаки могут быть присущи отечным, диффузным формам РМЖ. Лимфатические узлы с метастазами при пальпации плотные, порой увеличены в размере; при прорастании опухолью капсулы узлы становятся малоподвижными, иногда сливаются в конгломерат.
Методы специального исследования
Маммография обладает высокой диагностической достоверностью при РМЖ (рис. 16.8), достигающей 83-95 % (Демидов В.П., 2000). Обычно производят исследование молочной железы в двух взаимно перпендикулярных, стандартных проекциях - прямой и боковой. Маммографию выполняют с помощью специальных рентгеновских аппаратов - маммографов.
В работах Л.Д. Линденбратена (1965; 1997), А.П. Баженовой (1985), В.П. Демидова (2000), Б.И. Долгушина (2005) описаны рентгенологические признаки РМЖ. При рентгенодиагностике опухолевой патологии молочной железы различают первичные и вторичные признаки
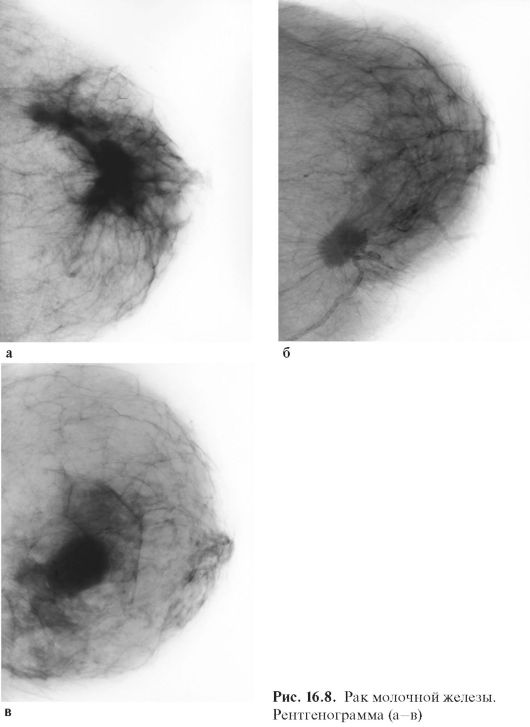 злокачественности.
Первичным признаком рака является наличие опухолевидной тени и
микрокальцинатов; тень опухоли может быть неправильной формы -
звездчатой или амебовидной, с неровными, нечеткими контурами,
характерной радиарной тяжистостью. Часто опухолевый узел сопровождается
«дорожкой» к соску и втяжением последнего, утолщением кожи железы,
иногда ее втяжением. Одним из наиболее достоверных и ранних
рентгенологических признаков РМЖ служит наличие микрообызвествлений,
отражающих отложения солей кальция в стенке протока. Симптомы со стороны
кожи, соска, окружающих опухоль тканей, усиленную васкуляризацию
относят к вторичным (косвенным) рентгенологическим признакам РМЖ.
злокачественности.
Первичным признаком рака является наличие опухолевидной тени и
микрокальцинатов; тень опухоли может быть неправильной формы -
звездчатой или амебовидной, с неровными, нечеткими контурами,
характерной радиарной тяжистостью. Часто опухолевый узел сопровождается
«дорожкой» к соску и втяжением последнего, утолщением кожи железы,
иногда ее втяжением. Одним из наиболее достоверных и ранних
рентгенологических признаков РМЖ служит наличие микрообызвествлений,
отражающих отложения солей кальция в стенке протока. Симптомы со стороны
кожи, соска, окружающих опухоль тканей, усиленную васкуляризацию
относят к вторичным (косвенным) рентгенологическим признакам РМЖ.
Дуктография осуществляется путем введения контрастного вещества в молочные протоки с последующим осуществлением маммографии. Дуктографию выполняют при секретирующей и кровоточащей молочной железе; она помогает проводить дифференциальную диагностику между доброкачественными новообразованиями и РМЖ.
Ультразвуковая (эхографическая) диагностика РМЖ показана у женщин молодого возраста (до 35-40 лет), у которых рентгенологическая диагностика затруднена из-за плотного однородного фона железы, наблюдаемого у 57 % больных (Демидов В.П., 2000). Метод неинвазивный, не требует больших материальных затрат, обладает большой пропускной способностью, не имеет противопоказаний, что позволяет использовать его в качестве скринингового. УЗИ чаще всего используется для дифференцирования солидных и кистозных образований, реже применяется для первичной диагностики РМЖ. По данным литературы, с помощью УЗИ удается выявить РМЖ в 65-92 % случаев.
При любом подозрении на злокачественный процесс в молочной железе необходимо проводить пункционную биопсию, брать мазки с последующим цитологическим исследованием пунктата или выделений из соска. Верификация рака - важнейший этап установления диагноза. Достоверность цитологического метода исследования при
РМЖ составляет 80-96 %.
Комплексная диагностика - сочетание клинического, маммографического, цитологического, УЗ-методов - дает наиболее высокий процент достоверных заключений. Суммарно по всем стадиям заболевания клиническое исследование обеспечивает 88 % правильных
заключений, рентгенологическое - 79 %, цитологическое - 90 %, а комплексное - 95 %. При неэффективности этих методов может быть произведена биопсия опухоли или секторальная резекция с экспресс-биопсией. Только морфологическое исследование позволяет определять тактику лечения.
Раннее выявление. Методика самообследования
Чрезвычайно важно раннее выявление РМЖ, так как это позволяет провести радикальное лечение, что значительно улучшает результаты и прогноз заболевания.
Самообследование - один из дополнительных методов выявления опухолей молочной железы. Самообследование молочных желез необходимо проводить 1 раз в месяц, на 6-12-й день от начала менструации. Неменструирующие женщины должны проводить самообследование в произвольно установленный ими самими определенный день каждого месяца. Самообследование состоит из осмотра и ощупывания молочных желез и подмышечных областей. Обследование необходимо проводить при вертикальном (стоя) и горизонтальном (лежа на спине) положении тела. Необходимо осмотреть соски: нет ли их втяжения, не изменились ли их цвет и форма, нет ли изъязвлений. Важно осмотреть кожу желез: нет ли изменений цвета, отека, втяжений, изъязвлений. Самообследование молочных желез должна проводить каждая женщина, это поможет раньше диагностировать РМЖ и получить более хорошие результаты при лечении.
Скрининг
Скрининг - массовое периодическое обследование здорового населения с целью выявления скрыто протекающего онкологического заболевания. Как показывает опыт, методика массовых профилактических осмотров врачами общей лечебной сети не оправдала себя из-за низкой эффективности. Поэтому широкое распространение получила концепция вторичной профилактики РМЖ, в частности скрининга. Подобные мероприятия приняты во многих странах в виде национальных программ - программ предупреждения РМЖ. По данным В.Ф. Семиглазова и соавт. (2001), скрининг предусматривает применение методики выявления скрытой патологии у большой группы практически здоровых лиц. При скрининге необходимы высокая чувствительность метода или теста (благодаря чему обнаруживается большинство злокачественных опухолей в обследуемой
группе при минимальном числе ложноотрицательных заключений); высокая специфичность метода (что позволяет исключить большинство здоровых женщин, у которых нет РМЖ, и свести к минимуму число ложноотрицательных заключений); а также приемлемая средняя стоимость одного выявленного случая рака; минимальный вред для здоровья обследуемой; простота эксплуатации и содержания оборудования.
Эффект массового скрининга может быть оценен тремя основными путями: оценкой воздействия на здоровье населения, определением показателей выявляемости РМЖ и характеристикой скринингового теста. Скрининг предусматривает применение таких инструментально-диагностических средств, которые обнаруживали бы проявления значительно более ранних форм опухолей, излечимых существующими методами (хирургическими, химиогормональными или лучевыми). Современный скрининг включает высокочувствительную маммографию, квалифицированное ежегодное физикальное обследование молочных желез и методически правильное ежемесячное самообследование.
Наиболее рациональна организация системы маммологической помощи с целью ранней диагностики РМЖ и оказания консультативной помощи при неопухолевых заболеваниях. Маммологическая служба состоит из следующих функционально взаимосвязанных звеньев: автоматизированный анамнестический скрининг на этапе доврачебного приема - смотровые (женские) кабинеты поликлиник - маммологические кабинеты общей лечебной сети - онкологи поликлиник - онкологические поликлиники и диспансеры.
ЛЕЧЕНИЕ
В настоящее время существует более 6000 вариантов лечения больных РМЖ. При этом все лечебные мероприятия разделяются на местно-регионарные (операция, лучевая терапия) и системные (химиотерапия, гормонотерапия, иммунотерапия) воздействия.
Лечебная тактика должна быть индивидуальной с учетом целого ряда факторов прогноза. Лечение может быть радикальным, паллиативным, симптоматическим.
Важно выработать план лечения больного. В предоперационном периоде, после проведения предоперационного лечения необходимо оценить степень резорбции опухоли и наметить объем оперативного
вмешательства. После выполнения операции, получения гистологического ответа и определения рецепторов опухоли нужно выработать план послеоперационного лечения с включением химио-, гормоноили лучевой терапии.
Типы радикальных операций
Хирургическое вмешательство занимает доминирующее положение в лечении РМЖ. При РМЖ могут быть выполнены:
1. Стандартная радикальная мастэктомия (Halsted W., 1889; Meyer W., 1894) - одноблочное удаление молочной железы вместе с большой и малой грудной мышцами и их фасциями, подключичной, подмышечной и подлопаточной клетчаткой с лимфатическими узлами в пределах анатомических футляров.
2. Расширенная подмышечно-грудинная радикальная мастэктомия (Margottini M., Bucalossi P., 1949; Urban J., 1951; Veroseni U., 1952; Холдин С.А., Дымарский Л.Ю., 1975) - одноблочное удаление молочной железы с грудными мышцами, подключично-подмышечной и подлопаточной клетчаткой, а также с участком грудной стенки с парастернальными лимфатическими узлами и внутренними грудными сосудами.
3. Сверхрадикальная расширенная мастэктомия (Wangensteen O., 1952) - удаление не только парастернального коллектора, но также лимфатических узлов, клетчатки надключичной области и переднего средостения.
4. Модифицированная радикальная мастэктомия отличается от мастэктомии Холстеда сохранением большой грудной мышцы (Patey D., Dyson W., 1948) или обеих грудных мышц (Auchincloss H., 1956; Madden J., 1965). В случае оставления мышц мастэктомия менее травматична и выполняется с меньшей кровопотерей; послеоперационная рана заживает лучше. Сохранение мышц приводит к лучшим косметическим результатам и функции верхней конечности, поэтому такие операции получили название функционально щадящих.
5. Мастэктомия с подмышечной лимфаденэктомией (Пирогов Н.И., 1847; Volkmann K., 1875; Winiwarter A., 1978) - удаление молочной железы и лимфатических узлов нижнего уровня подмышечной области (так называемой первой зоны Берга). Показанием к такой операции являются начальные (I-IIA) стадии заболевания при локализации опухоли в наружных квадрантах молочной железы
у пожилых и ослабленных больных, с тяжелыми сопутствующими заболеваниями.
6. Простая мастэктомия (ампутация) - удаление молочной железы с фасцией большой грудной мышцы. Показаниями к такой операции являются распадающаяся опухоль, преклонный возраст больных, тяжелые сопутствующие заболевания.
7. Радикальная секторальная резекция молочной железы является органосохраняющей операцией и предусматривает удаление сектора молочной железы вместе с опухолью, части подлежащей фасции большой и малой грудной мышцы, подключичной, подмышечной, подлопаточной клетчатки с лимфатическими узлами в одном блоке. При локализации опухоли в медиальных отделах молочной железы операция может быть выполнена из двух разрезов кожи - на молочной железе и в подмышечной области. Для выполнения подобных операций важно соблюдать критерии отбора больных. Риск местного рецидивирования при такой операции повышен, поэтому больным после органосохраняющей операции показана послеоперационная лучевая терапия на оставшуюся часть молочной железы.
8. Секторальная резекция предусматривает удаление сектора молочной железы до подлежащей фасции. Секторальная резекция как самостоятельный метод лечения при раке не имеет обоснования к выполнению. Ее следует применять только в диагностических целях. В лечебных целях секторальную резекцию применяют в исключительно редких случаях и дополняют лучевой терапией (например, при одиночных очагах неинвазивного cancer in situ).
Лучевая терапия
Использование операции как единственного метода лечения пациентов с регионарными метастазами приводит к частому рецидивированию и возникновению отдаленных метастазов. С целью улучшения непосредственных и отдаленных результатов оперативного лечения возникла идея использовать лучевую терапию. Она применяется с 1901 г., но до настоящего времени не прекращаются споры о ее месте и роли в лечении РМЖ.
Лучевую терапию применяют в пред- и послеоперационном периодах. В задачи предоперационной лучевой терапии входят: снижение степени злокачественности опухоли за счет девитализации наиболее анаплазированных клеток (которые наиболее ранимы), инактивации радиорезистентных опухолевых клеток; повреждение до полной
регрессии микродиссеминатов и микрометастазов в зонах возможного субклинического распространения. Для решения этих задач достаточной является СОД 40-45 Гр, за 4-5 нед. Предоперационную лучевую терапию чаще проводят укрупненными фракциями - ежедневно по 5 Гр на молочную железу с 2 тангенциальных полей; всего 5 фракций - 25 Гр, что по биологическому изоэффекту соответствует 40 Гр при классическом режиме фракционирования - по 2 Гр в день. На подключично-подмышечную область ежедневно проводят по 4 Гр с одного фигурного поля, всего 6 фракций, что соответствует 35 Гр при классическом режиме фракционирования дозы. Операция на молочной железе при таком методе облучения может быть осуществлена на 2-3-й день после его окончания. Надключичную и парастернальную зоны облучают через 10-14 дней после операции в классическом режиме - по 2 Гр ежедневно на каждую зону до суммарной дозы 44 Гр. При отечно-инфильтративных формах РМЖ применяют классический режим фракционирования дозы на молочную железу и все зоны регионарного лимфооттока в предоперационном периоде.
Химиотерапия
РМЖ относится к опухолям, для которых характерна высокая частота гематогенного и лимфогенного метастазирования. Использование адъювантной химиотерапии позволяет значительно сократить риск рецидива и смерти у больных операбельным РМЖ. Цели лекарственной терапии: излечение, продление жизни, уменьшение стадии опухолевого процесса, улучшение качества жизни и контроль симптомов болезни, повышение результатов хирургического и лучевого лечения, отказ от калечащих операций, уменьшение объема вмешательств. Каждый химиопрепарат действует только на те клетки, которые находятся в определенной фазе клеточного цикла. Поэтому монохимиотерапия менее эффективна, чем полихимиотерапия (ПХТ) - сочетание нескольких препаратов с различными фазовоспецифичностью и механизмом действия. Клинический опыт показал, что при РМЖ наиболее эффективны в качестве дополнения к операции (адъювантная терапия) химиопрепараты циклофофосфамид, тиотепа, фторурацил, метотрексат, доксорубицин и некоторые другие, противоопухолевое действие которых потенцируется при их сочетании.
Международная консенсусная группа экспертов на конференции в St. Gallen (2005) рекомендовала изменение традиционных критериев выбора адъювантной терапии раннего РМЖ. Это в первую очередь
определение гормональной зависимости опухоли с учетом ее рецепторного статуса, затем - определение степени риска (низкий, промежуточный, высокий) в зависимости от размеров опухоли, вовлечения в процесс лимфатических узлов, опухолевой инвазии сосудов, степени злокачественности опухоли. Обязательным признано определение HER 2/neu-статуса. Сохраняют свое значение возраст и состояние овариальной функции.
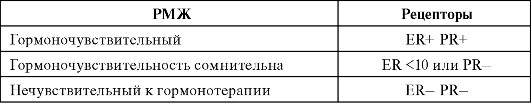
В таблице 16.1 представлены категории гормоночувствительности РМЖ. Системная адъювантная терапия показана преобладающему большинству больных РМЖ, за исключением небольшой, наиболее прогностически благоприятной группы больных старше 35 лет, с гормоночувствительной опухолью размером менее 1 см (Т1АВ1 N0M0), с I степенью злокачественности (G1) без метастазов в лимфатические узлы. Прогностически благоприятны опухоли с тубулярным, муцинозным, папиллярным строением.
Таблица 16.1. Категории гормоночувствительности РМЖ
 Схемы химиотерапии при РМЖ: I-я линия лечения
Схемы химиотерапии при РМЖ: I-я линия лечения
1. CMF:
циклофосфамид - по 100 мг/м2 внутрь ежедневно с 1-го по 14-й дни;
метотрексат - по 40 мг/м2 внутривенно в 1-й и 8-й дни; фторурацил - 600 мг/м2 внутривенно в 1-й и 8-й дни. Повторение курса каждые 4 нед (интервал - 2 нед).
2. CAF:
циклофосфамид - по 100мг/м2 внутрь или внутримышечно с 1-го по 14-й дни;
доксорубицин - по 30мг/м2 внутривенно в 1-й и 8-й дни; фторурацил - по 500 мг/м2 внутривенно в 1-й и 8-й дни. Повторение курса каждые 4 нед.
3. FAC:
фторурацил - 500 мг/м2 внутривенно в 1-й день;
доксорубицин - 50 мг/м2 внутривенно в 1-й день;
циклофосфамид - 500 мг/м2 внутривенно в 1-й день. Повторение курса каждые 3 нед. II линия лечения
1. DAC:
доксорубицин - 50 мг/м2 внутривенно в 1-й день; доцетаксел (таксотер) - 75 мг/м2 инфузия в течение 1 ч в 1-й день (на фоне соответствующей премедикации); циклофосфамид - 500 мг/м2 внутривенно в 1-й день. Перерыв 3 нед.
2. ED:
эпирубицин - 75-80 мг/м2 внутривенно в 1-й день; доцетаксел (таксотер) - 75 мг/м2 инфузия в течение 1 ч в 1-й день (на фоне премедикации). Перерыв 3 нед.
3. Доцетаксел (таксотер) - 75 мг/м2 внутривенно инфузия в течение 1 ч в 1-й день;
цисплатин - 75 мг/м2 внутривенно капельно в 1-й день. Повторение курса каждые 3 нед.
Лечение больных диссеминированным РМЖ должно быть своевременным, рациональным, последовательным, адекватным, перспективным, этапным, комплексным. При лечении необходимо учитывать: характер опухолевого процесса, спектр чувствительности опухоли к предлагаемому лечению, общее состояние больного, возраст, ожидаемую продолжительность жизни, сопутствующую патологию, функциональные показатели органов (печени, почек, сердца), эффективность и токсичность предшествующего противоопухолевого лечения. К вопросу о продолжительности химиотерапии предлагается 2 подхода:
1) химиотерапия по одной схеме проводится до прогрессирования опухоли (10-14 циклов и более);
2) проводится по одной схеме 4-8 циклов, но не менее двух циклов после достижения максимального эффекта с последующим наблюдением за больной.
Таргетная терапия
Гиперэкспрессия эпидермального фактора роста (EGF) HER2/neu обусловливает агрессивное течение заболевания. К моноклональным антителам против белковых трансмембранных рецепторов эпидермального фактора роста человека 2-го типа HER2/neu или c-erbB2
относят трастузумаб (герцептин), который обладает противоопухолевой активностью и увеличивает эффект применения комбинированной химиотерапии у больных с HER2/neu+-опухолями. Гиперэкспрессия HER2/neu является абсолютным показанием к назначению герцептина.
Высокая частота гиперэкспрессии HER2/neu на поверхности клеток РМЖ и большое прогностическое значение делают этот рецептор важной целью - мишенью таргетной (от англ. target - мишень) противоопухолевой терапии. Потенциальные механизмы действия трастузумаба весьма разнообразны: препарат влияет на экспрессию рецептора, передачу сигнала, ангиогенез, иммунный ответ. Трастузумаб обладает высоким аффинитетом к рецептору HER2/neu и, связываясь с ним, предотвращает пролиферацию в культуре клеток рака молочной железы SK-BR-3, гиперэкспрессирующих протеин HER2/neu рецептора, уменьшая фракцию клеток, находящихся в S-фазе клеточного цикла, и увеличивая процент клеток в фазах G0/G1. По данным М.Б. Стениной (2006), в настоящее время проводятся соответствующие клинические исследования. Опубликованы первые результаты работ по предоперационной терапии: комбинация трастузумаба с доцетакселом и цисплатином позволила получить объективный противоопухолевый эффект у 100 % больных, причем у 25 % из них получена полная морфологическая регрессия. Эффективность трастузумаба в сочетании с паклитакселом составила 73 %; полная морфологическая регрессия достигнута у 18 % больных.
Лапатиниб - новый ингибитор тирозинкиназ EGFR и HER2/neu, является пероральным обратимым ингибитором тирозинкиназ 2 представителей семейства рецепторов EGF (EGFR и HER2/neu). В рандомизированном исследовании III фазы сочетание лапатиниба и капецитабина по сравнению только с капецитабином у 399 больных после прогрессирования на фоне герцептинсодержащих комбинаций позволило добиться увеличения времени до прогрессирования - соответственно 27,1 и 18,6 мес (Sherrill B. et al., 2007).
Гиперэкспрессия стимуляторов ангиогенеза VEGF обнаруживается в 55-95 % случаев РМЖ и сопровождается сокращением безрецидивной и общей выживаемости (Harmey Y. еt al., 2002). Повышенный уровень VEGF может способствовать резистентности опухоли к химиогормонотерапии РМЖ. Бевацизумаб (авастин) - химерные человеческие рекомбинантные антитела против VEGF. В исследовании эффективности комбинации бевацизумаб и паклитаксела, а также
паклитаксела у больных метастатическим РМЖ в 1-й линии терапии медиана времени без прогрессирования была статистически выше в группе больных, получавших паклитаксел и авастин.
Гормонотерапия
Эстрогены являются ведущими факторами в канцерогенезе опухолей молочных желез в эксперименте и клинике. В настоящее время опухоль считают гормоночувствительной, если более 10 % опухолевых клеток содержат рецепторы к эстрогену или прогестерону. Рецепторположительными и чувствительными к гормонотерапии считают опухоли, содержание рецепторных белков в которых превышает 10 фентамоль на 1 мг белка. Чем выше содержание гормональных рецепторов, тем эффективнее гормонотерапия.
Гормонотерапия РМЖ претерпела значительные изменения: если на первых этапах это было хирургическое удаление яичников, то в последующие годы разрабатывались методы консервативного воздействия на органы, участвующие в синтезе эстрогенов. Хирургическая кастрация впервые была применена шотландским хирургом G. Beatson в Глазго в 1896 г. Лучевая кастрация известна с 1922 г. Однако описывались случаи, когда после лучевой кастрации восстанавливались менструации, что было обусловлено, видимо, неадекватностью суммарных доз.
Альтернативой хирургической или лучевой кастрации у менструирующих и находящихся в пременопаузе женщин является использование гонадотропин-рилизинггормона (ГтРГ) и агониста ГтРГ гозерелин или его отечественного аналога - бусерелина. Комбинация агониста ГтРГ и тамоксифена (метаанализ четырех рандомизированных исследований) превосходит по эффективности монотерапию агонистом ГтРГ у женщин в пременопаузальном периоде, больных распространенным РМЖ.
Все шире применяются физиологически неактивные антиэстрогенные препараты (нестероидные антигормоны), непосредственно воздействующие на опухолевую клетку и не затрагивающие центральные механизмы гормонообразования. Большую роль играет тамоксифен у больных в менопаузе при гормональнозависимых опухолях с метастазами в подмышечные лимфатические узлы.
Современные достижения в гормонотерапии РМЖ связаны с появлением новых препаратов, в том числе «чистых» антиэстрогенов, селективных модуляторов эстрогеновых рецепторов, включая
ралоксифен, а также новых ингибиторов ароматазы 3-го поколения, включающих нестероидные препараты анастрозол, летрозол, фулвестрант (фазлодекс) и стероидный ингибитор экземестан.
Для уточнения показаний к гормонотерапии, в частности овариэктомии, следует пользоваться определением гормональных рецепторов удаленной опухоли или ее кусочка, взятого при трепанобиопсии до начала лечения. После овариэктомии больным назначают тамоксифен (по 20 мг в день на срок 2 года) для блокады надпочечниковых эстрогенов.
Иммунотерапия
Показанием для иммунотерапии является нарушенная реактивность организма, обусловленная наличием самой опухоли и иммунодепрессивными методами химиолучевого и хирургического лечения. До начала и в процессе лечения необходимо определение иммунологического статуса, в частности показателей клеточного и гуморального иммунитета. По данным Н.И. Переводчиковой (2000), к иммуномодуляторам относятся: цитокины (интерлейкины, интерфероны, колониестимулирующие факторы), моноклональные антитела, дифференцирующие агенты, антиангиогенезные факторы.
Показания к комбинированному и комплексному лечению
Многообразие характеристик опухоли молочной железы, факторов прогноза, высокая частота метастазирования явились основанием для развития комплексных методов лечения, при которых хирургическое вмешательство дополняется лучевым, гормональным и лекарственным воздействиями.
При начальных формах РМЖ может быть применено только хирургическое лечение - модифицированная мастэктомия по Маддену или радикальная резекция (она должна быть дополнена послеоперационной лучевой терапией на оставшуюся часть молочной железы). При неблагоприятных факторах прогноза лечение может быть дополнено химиотерапией.
При IIB и IIIA стадиях РМЖ проводят комбинированное лечение: предоперационную лучевую терапию укрупненными фракциями, радикальную мастэктомию и послеоперационную дистанционную гамма-терапию на зоны регионарного лимфооттока. Лучевая терапия может быть заменена или дополнена химиотерапией.
Лечение больных РМЖ IIIB стадии представляет определенные трудности в связи с агрессивностью течения, запущенностью процесса.
Больные, успешно перенесшие радикальное лечение по поводу РМЖ и, по сути, излеченные от этого заболевания, в большинстве своем не могут считаться здоровыми. Функциональные нарушения верхней конечности, возникшие после радикального лечения, не позволяют им не только возобновить производственную деятельность, но даже осуществлять полноценное самообслуживание. Неуклонное прогрессирующее развитие и стойкое течение множества разнообразных и взаимосвязанных органических и функциональных нарушений и расстройств закономерно приводят к инвалидизации более 80 % больных, успешно перенесших радикальное лечение по поводу РМЖ, а более 40 % из них остаются инвалидами 1-й и 2-й групп. Важно отметить, что наряду с потерей у них работоспособности (т.е. с потерей биологической способности человека к выполнению того или иного труда) крайне неудовлетворительным остается и качество их жизни. Если учесть, что почти половина женщин, заболевших РМЖ, находятся в трудоспособном возрасте (от 40 до 60 лет), становится понятной высокая социальная значимость проблемы реабилитации пациенток этой категории. Лечение больных РМЖ не может и не должно ограничиваться решением сугубо специальных онкологических вопросов, а под термином «излечение» необходимо понимать не только клиническое, с точки зрения онколога, выздоровление, но и возвращение трудоспособности, а также прежнего бытового и социального статуса.
Хирургическое лечение, как и лучевая терапия, отличается выраженной агрессивностью и неизменно сопровождается весьма значительными повреждениями мягких тканей соответствующей половины грудной клетки и плечевого пояса. В процессе выполнения радикальной операции при пересечении множества лимфатических и кровеносных сосудов вынуждено происходит пересечение большого количества мелких нервов, обеспечивающих иннервацию конечности и тканей соответствующей половины грудной стенки.
Повреждающее действие ионизирующего излучения в процессе лучевой терапии вызывает соответствующие морфологические изменения мягких тканей, и прежде всего периферических нервов шейно-плечевого сплетения, что обусловливает развитие травматического шейно-плечевого плексита, сенсорных и моторных нарушений, нередко сопровождающихся выраженным болевым синдромом.
Клинические проявления операционных и лучевых повреждений нервов, а также лимфатических и кровеносных сосудов, как правило, носят ярко выраженный характер, однако внимание в большинстве наблюдений сконцентрировано на отеке верхней конечности на стороне проведенного радикального лечения. При этом следует отметить, что отек 0 степени в отличие от отека 1-4-й степеней не имеет каких-либо клинических проявлений и устанавливается лишь при капилляроскопии. 1-4-ю степень отека определяют по разнице длины окружности верхних конечностей на уровне средней трети плеча и средней трети предплечья. При разнице показателей до 2 см говорят об отеке 1-й степени, для 2-й степени характерна разница от 2 до 4 см, для 3-й - от 4 до 6 см и, наконец, при 4-й степени отека она превышает 6 см.
Несомненно, в основе постмастэктомического отека прежде всего лежит нарушение лимфооттока и кровообращения в конечности. Однако не следует забывать, что у больных вследствие операционных и лучевых повреждений развивается комплекс не только васкулярных, но и неврологических расстройств, совокупность которых обусловливает разнообразие функциональных и органических нарушений верхней конечности и других анатомических структур, находящихся в непосредственной близости от молочной железы, пораженной опухолью. При этом общность этиологии и патогенеза органических и функциональных нарушений, их комбинированный характер, взаимообусловленность и взаимозависимость приводят к необходимости рассматривать комплекс постмастэктомических нарушений как единый патологический процесс - «постмастэктомический синдром».
Обследование больных, перенесших радикальное лечение по поводу РМЖ, показывает что отек верхней конечности различной степени выраженности (от 0 до 4) выявляется у всех без исключения пациентов, независимо от времени, прошедшего после окончания радикального лечения. Помимо отека, у 63 % больных ограничена подвижность плечевого сустава на стороне перенесенной операции, у 50 % - определяются слабость мышц конечности и снижение их тонуса. Различные нарушения чувствительности кожи (гиперестезия, гипестезия или парастезия) беспокоят половину больных, а боль в конечности наблюдается почти у 40 %.
В течение 1-го года после перенесенного радикального лечения по поводу РМЖ на стороне проведенного лечения закономерно развивается скаленус-синдром. Скорость его формирования и интенсивность
клинических проявлений находятся в прямой зависимости от времени, прошедшего с момента радикальной операции, а также от лучевой терапии, которая проводится в комбинации с хирургическим методом лечения больных РМЖ в то же время объем радикальной операции влияет на формирование скаленус-синдрома в значительно меньшей степени.
Этот патологический комплекс оказывает влияние не только на состояние верхней конечности, соответствующую половину плечевого пояса и грудной клетки, но и на весь организм пациента и играет главную роль в формировании, упорном и прогрессирующем течении постмастэктомического синдрома.
Сдавление кровеносных сосудов, обусловленное напряжением передней лестничной мышцы, не только усиливает отек конечности, но и обусловливает весьма низкую эффективность противоотечной терапии, которая традиционно проводится больным РМЖ после радикального лечения и направлена в основном на улучшение микро- и макроциркуляции крови и лимфы в конечности.
У больных со скаленус-синдромом симптомы угнетения периферической нервной системы (гипестезия, гипотрофия мышц, парез, паралич) явно преобладают над симптомами раздражения (боль, гиперестезия, парестезия). Общемозговые, кохлеовестибулярные, стволовые и стволово-мозжечковые расстройства, свидетельствующие о нарушении мозгового кровообращения в каротидном и вертебрально-базилярном бассейнах, выявляют у каждого 3-го больного со скаленус-синдромом.
Классификация постмастэктомического синдрома
Стадия 1а - наличие на стороне операции постмастэктомического отека 0-1-й степени верхней конечности без проявлений синдрома напряжения передней лестничной мышцы.
Стадия Ib - наличие на стороне операции постмастэктомического отека 2-4-й степени верхней конечности без проявлений синдрома напряжения передней лестничной мышцы.
Стадия 11а - наличие на стороне операции постмастэктомического отека 0-1-й степени верхней конечности и клинических проявлений синдрома напряжения передней лестничной мышцы.
Стадия IIb - наличие на стороне операции постмастэктомического отека 2-4-й степени верхней конечности и клинических проявлений синдрома напряжения передней лестничной мышцы.
Стадия III - возникновение в результате прогрессирующего нарушения обменных процессов в мягких тканях конечности дегенеративных и некробиотических изменений (стадия фибрэдемы), которые при дальнейшем развитии приводят к разрастанию соединительной ткани и ее склерозу. Необратимость этих процессов делает данную фазу постмастэктомического синдрома не поддающейся лечению.
Выбор терапевтических методов, входящих в лечебно-восстановительный комплекс, во многом зависит от стадии развития постмастэктомического синдрома.
В основе комплексной терапии больных с постмастэктомическим синдромом лежит методика патогенетической профилактики и терапии последствий мастэктомии, выполненной больным по поводу РМЖ, в том числе в комбинации с одним из известных видов лучевой терапии. С целью профилактики разнообразных послеоперационных осложнений необходимы постоянная активная аспирация раневого секрета и лимфы и эластомерная повязка с надувным устройством для дозированной компрессии на рану. Плотное прижатие кожных лоскутов за счет дозированной компрессии на них и присасывающего эффекта, обеспечиваемого дренажной системой активной аспирации, способствуют хорошему гемостазу, уменьшению продолжительности лимфореи и создают более благоприятные условия для быстрого заживления раны.
С целью коррекции различных нарушений в верхней конечности на стороне операции необходимо применение комплекса лечебной физкультуры (ЛФК), включающего лечебную гимнастику, самостоятельные занятия по индивидуальным заданиям и лечебный массаж верхней конечности.
Для компенсации нарушений микроциркуляции в верхней конечности у больных с постмастэктомическим отеком 0-1-й степени наряду с ЛФК и лечебным массажем возможно применение дозированной компрессии на мягкие ткани верхней конечности.
У больных с постмастэктомическим отеком 2-4-й степени данный комплекс лечебно-восстановительных мероприятий дополняется медикаментозной терапией: дигидроэрготамин - по 20 капель 3 раза в день в течение 3-4 мес; фитин - по 0,5 г 3 раза в день в течение 3-4 мес; курантил - по 0,025 г 3 раза в день в течение 3-4 мес; фуросемид по 0,04 г ежедневно в течение 3 дней с 2-дневным перерывом; длительность курса лечения - 1,5 мес; панангин - по 1 драже 3 раза
в день на время приема фуросемида; гепарин - по 5000 ЕД 2 раза в день внутримышечно в течение 12 дней и венорутон - по 0,5 г в день в течение 2 нед с последующим применением рутина - по 0,02 г 3 раза в день.
К указанному лечебному комплексу могут быть добавлены лазерная и фототерапия. Курс лазеро- и фототерапии, состоящий из 10-12 сеансов, проводят через каждые 3-4 мес, а после 5-6 курсов - 1 раз в полгода.
Больным с постмастэктомическим синдромом 2-3-й стадии (при наличии синдрома передней лестничной мышцы) курс лазеро- и фототерапии целесообразно проводить в комбинации с одним из известных методов релаксации передней лестничной мышцы:
• аппликационным воздействием на переднюю лестничную мышцу смеси растворов димексида с новокаином;
• мануальной постизометрической релаксацией передней лестничной мышцы по Г.А. Иваничеву (1984);
• применением препаратов миорелаксирующего действия (толперизон, баклофен, тизанидин и др.).
Важно отметить, что лечение пациентов с постмастэктомическим синдромом необходимо проводить на протяжении всей последующей (после радикального лечения по поводу РМЖ) жизни.
ПРОГНОЗ. ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ
На основании данных о стадии опухолевого процесса и с учетом биологических характеристик опухоли необходимо оценить прогноз заболевания и выработать оптимальный план лечения конкретной пациентки. Различают большое количество прогностических факторов: размер опухоли, состояние регионарных лимфатических узлов, степень дифференцировки опухоли, рецепторы эстрогенов, НЕК2/пеи-статус. Предсказывающие факторы освещают связь между биологией опухоли и эффективностью лечения, коррелируют с частотой объективного ответа независимо от прогноза, разделяют больных по чувствительности к различным видам лечения. Таких факторов немного: рецепторы эстрогенов и оценка гормональной терапии, ИЕЯ2/пеи-статус и оценка ответа на трастузумаб и т.д.
Наиболее важными прогностическими признаками являются: распространенность процесса, количество метастазов в подмышечных
лимфатических узлах, отек молочной железы, наличие инвазивных свойств протоковой карциномы, степень злокачественности опухоли.
Отдаленные результаты лечения принято оценивать по 5-летней выживаемости. Выживаемость больных во многом зависит от стадии заболевания, при которой начато лечение. Современные методы лечения позволяют достичь 5-летней выживаемости при I стадии рака у 96 %, IIA - у 90 %, IIB - у 80 %, IIIA - у 87 %, IIIB - у 67 % больных (Демидов В.П., 2000).
СИСТЕМА ДИСПАНСЕРИЗАЦИИ, РЕАБИЛИТАЦИЯ И ЭКСПЕРТИЗА НЕТРУДОСПОСОБНОСТИ
При диспансеризации больных РМЖ контрольный осмотр осуществляется: в первые 2 года - 1 раз в 3 мес, до 5 лет - 1 раз в 6 мес, в последующие годы - 1 раз в год.
Проблема качества жизни больных РМЖ обусловлена, с одной стороны, достигнутыми высокими показателями лечения (одногодичная продолжительность жизни составляет 90 %), с другой - значительными психологическими и социальными аспектами мастэктомии. Различают 3 направления реабилитации (Баженова А.П. и
соавт., 1985):
1) восстановительная - без потери трудоспособности;
2) поддерживающая - с потерей трудоспособности, которую можно уменьшить соответствующим лечением;
3) паллиативная - при прогрессировании заболевания, когда предупреждают развитие некоторых осложнений.
Консервативные (компрессионный массаж, ЛФК, физиотерапия) и хирургические (восстановление молочной железы, наложение лимфовенозных анастомозов, иссечение рубцов) методы лечения, как показывает практика, явно недостаточны. В настоящее время применяются различные методики реконструктивно-пластических операций молочной железы. Очень важны вопросы психологической реабилитации больных РМЖ.
При экспертизе определяют степень утраты способности к труду; при этом оценивают клинический прогноз, который зависит от следующих факторов:
• клинико-морфологических (размер опухоли, ее локализация в органе, характер поражения регионарных лимфатических узлов,
наличие отдаленных метастазов, гистологическое строение, степень дифференцировки);
• общебиологических (возраст, клинические проявления заболевания, наличие сопутствующих заболеваний, иммунный статус больной);
• связанных с видом проведенного лечения, а также ближайшими и отдаленными его последствиями;
• социальных (характер и условия труда, образование, профессия, стаж работы пациентки).
Экспертиза трудоспособности позволяет оценить степень нарушения жизнедеятельности, социальной дезадаптации и при необходимости разработать программу реабилитации больных РМЖ.
Вопросы для самоконтроля
1. Охарактеризуйте состояние заболеваемости РМЖ в Российской Федерации.
2. Перечислите основные факторы риска развития РМЖ.
3. Определите место и роль гормональных нарушений в этиологии и патогенезе РМЖ.
4. Чем отличаются клинические проявления и тактика лечения при узловой и диффузной мастопатии?
5. Каковы основные принципы лечения мастопатий?
6. Какие существуют методы профилактики РМЖ?
7. Назовите пути метастазирования при РМЖ.
8. Назовите основные факторы, определяющие стадирование при
РМЖ.
9. Какие размеры опухоли соответствуют II стадии РМЖ?
10. Чем характеризуется отечно-инфильтративная форма РМЖ?
11. Приведите дифференциально-диагностические критерии мастита и маститоподобной формы РМЖ.
12. С какими заболеваниями необходимо дифференцировать рак Педжета?
13. В чем заключается понятие «скрининга» на РМЖ?
14. Какие методы обследования необходимы при подозрении на РМЖ?
15. В какой период менструального цикла необходимо проводить обследование молочных желез?
16. Опишите клинические признаки РМЖ.
17. Назовите виды операций при РМЖ и укажите, каким из них отдается предпочтение в последние годы.
18. Определите показания к комбинированному и комплексному лечению РМЖ.
19. Перечислите элементы комплексной терапии больных с постмастэктомическим синдромом.
20. Приведите классификацию постмастэктомического синдрома.
21. Какие факторы определяют прогноз при РМЖ?
22. Перечислите режимы лучевой терапии при РМЖ.
23. Какие схемы химиотерапии чаще используют при РМЖ?
24. Каковы отдаленные результаты лечения больных при ранних и запущенных стадиях РМЖ?
25. С какой частотой необходимо проводить диспансерное наблюдение больных РМЖ после радикального лечения?
26. В чем заключается реабилитация больных после радикального лечения?
27. Перечислите критерии определения нетрудоспособности при РМЖ.