Онкология : учебник / М. И. Давыдов, Ш. Х. Ганцев. 2010. - 920 с.
|
|
|
|
ГЛАВА 21 РАК ОБОДОЧНОЙ КИШКИ
ЭПИДЕМИОЛОГИЯ
Рак ободочной кишки (РОК) занимает 2-3 место в структуре злокачественных новообразований ЖКТ и составляет от 4до6 % всей онкологической заболеваемости. Преимущественный возраст заболевших - более 50 лет. В 2007 г. число больных с впервые в жизни установленным диагнозом РОК составило 30 814 человек: 12 709 мужчин и 18 105 - женщин. Заболеваемость в 2007 г. в целом по России была 21,7 на 100 тыс. населения. Наиболее высокие ее показатели в 2005 г. у мужчин были зарегистрированы в Магаданской области (35,9), у женщин - в Чукотском автономном округе (32,1), наименьшие - в Республике Тыва (у мужчин - 4,7, у женщин - 4,8). Смертность мужчин от РОК в России в 2005 г. была 10,1 на 100 тыс. населения, среди женщин - 7,7.
ЭТИОЛОГИЧЕСКИЕ И ПАТОГЕНЕТИЧЕСКИЕ ФАКТОРЫ
По мнению большинства исследователей, на рост заболеваемости РОК оказывают влияние следующие этиологические и патогенетические факторы:
1) характер питания населения: малошлаковая пища с преобладанием животных жиров, белков и рафинированных углеводов (сахар);
2) малоподвижный образ жизни - гипокинезия, ожирение, возраст старше 50 лет;
3) гипотония и атония кишечника в пожилом возрасте - хронический запор;
4) наличие в кишечном содержимом эндогенных канцерогенов (индола, скатола, гуанидина, метаболитов стероидных гормонов)
и их воздействие на слизистую оболочку кишки в условиях длительного застоя каловых масс; 5) хроническая травматизация калом слизистой оболочки толстой кишки в местах физиологических изгибов.
ПРЕДРАКОВЫЕ ЗАБОЛЕВАНИЯ
К предраковым заболеваниям относятся:
• хронический колит, в частности хронический неспецифический язвенный колит и гранулематозный колит (болезнь Крона), которые составляют основную группу факультативных предраковых заболеваний;
• дивертикулы (дивертикулез) ободочной кишки (дивертикулит). Малигнизируются редко;
• полипозное поражение ободочной кишки (облигатный предрак):
а) одиночные полипы (аденоматозный, ворсинчатый), которые малигнизируются в 45-50 % случаев, особенно полипы величиной >2 см; ворсинчатые полипы озлокачествляются чаще;
б) множественный полипоз ободочной кишки, который, в свою очередь, может иметь следующие формы:
генетически детерминированные:
- семейно-наследственный диффузный полипоз;
- синдром Пейтца-Егерса;
- синдром Тюрка; ненаследственные:
- спорадический полипоз;
- сочетанный полипоз;
- синдром Кронкхайта-Канада;
- семейно-наследственный полипоз (является облигатным предраком и почти в 100 % случаев приводит к раку).
Болезнь Крона - это хроническое неспецифическое воспаление подслизистого слоя с изъязвлением слизистой оболочки, гранулематозными изменениями (отсюда другое название - гранулематозный колит), свищами, инфильтратами, сопровождающимися сужением просвета, воспалением, утолщениями стенки кишки. Патология может локализоваться и в прямой кишке, но наиболее часто - в терминальном отделе подвздошной кишки. Болезнь
может напоминать саркоидоз, трещины, язвы прямой кишки. Рельеф кишечника напоминает «булыжную мостовую» с линейными язвами.
Полипы бывают гиперпластические (воспалительные) и аденоматозные (железистые).
Морфологически полипы представляют собой папиллярные и тубулярные разрастания железистой ткани со стромой, отличающейся от нормальной слизистой оболочки полиморфизмом клеточных элементов, высокой митотической активностью, полной или частичной утратой способности к дифференциации.
Полипы бывают гладкие и бархатистые (ворсинчатые). Целесообразно выделение двух групп полипоза толстой кишки - наследственный и ненаследственный, так как при генетически детерминированных формах необходимо обследовать родственников и всех членов семьи заболевшего, даже если отсутствуют жалобы на дисфункцию ЖКТ. В то же время внекишечные сопутствующие проявления синдромов Пейтца-Егерса, Гарднера, Тюрка могут быть ранними диагностическими паранеопластическими признаками полипоза толстой кишки.
Так, для синдрома Пейтца-Егерса характерно полипозное поражение ЖКТ с мелкопятнистой меланиновой гиперпигментацией слизистой оболочки щек и губ, а также других естественных анатомических отверстий тела человека. Для синдрома Гарднера характерно сочетание полипозного поражения толстой кишки с множественными доброкачественными опухолями (костные экзостозы, остеомы черепа и нижней челюсти, эпидермоидные кисты и опухоли кожи) и послеоперационными рубцовыми десмоидами. Для синдрома Тюрка типична комбинация полипоза толстой кишки с опухолями различных отделов нервной системы (глиомы и глиобластомы).
При сочетанном полипозе полипы обнаруживают не только в толстой кишке, но и в желудке, двенадцатиперстной и тонкой кишках. Относительно редкой его разновидностью считается синдром Кронкхайта-Канада - ненаследственный, генерализованный желудочно-кишечный полипоз в сочетании с тотальной алопецией и атрофией ногтей. Поэтому с учетом возможности одновременной локализации новообразований в других отделах ЖКТ, показано его комплексное рентгеноэндоскопическое обследование даже при обнаружении одиночного полипа в толстой кишке.
ПРОФИЛАКТИКА
1. Профилактические осмотры необходимы для выявления групп населения повышенного риска и ранних форм рака ободочной и прямой кишок. Современные автоматизированные скрининги предусматривают использование разработанных карт-анкет с последующей их обработкой на ЭВМ. Огромное значение при этом имеет использование гемокульт-теста для отбора групп повышенного риска с целью последующего эндоскопического исследования (ректороманоскопия, фиброколоноскопия с морфологическим исследованием биоптатов опухоли).
2. Диспансеризация, наблюдение и лечение больных с предопухолевыми заболеваниями и доброкачественными опухолями.
3. Формирование и пропаганда здорового образа жизни, рационального питания.
4. Оздоровление экологической обстановки.
5. У излеченных больных с учетом возможности рецидива или появления второй опухоли, при первично-множественных поражениях показана диспансеризация, включающая периодические активные осмотры с применением рентгенологических, эндоскопических, морфологических и лабораторных методов.
Патолого-анатомическая характеристика
РОК может локализоваться в любых анатомических отделах, но частота их поражения неодинакова. Преобладающей локализацией РОК является сигмовидная кишка - 50 %, на 2-м месте слепая кишка - 21-23 %. Остальные отделы поражаются гораздо реже. В 1-3 % случаев наблюдается первично-множественная локализация опухоли.
Согласно клиническому материалу РОНЦ (Кныш В.И. и соавт., 1996), в правой половине ободочной кишки опухоли локализовались у 34,3 % больных, в левой - у 59,3 %, т.е. значительно чаще.
Клинико-анатомические формы РОК:
1) экзофитная (полиповидная, ворсинчато-папиллярная, узловая);
2) эндофитная (инфильтрирующая, язвенно-инфильтративная, циркулярно-стриктурирующая);
3) переходная или смешанная.
Рак с преимущественно экзофитной формой роста чаще наблюдается в правой половине ободочной кишки, а с преимущественно инфильтрирующим характером роста - в левой.
Согласно отечественной гистологической классификации, различают следующие формы опухолей ободочной кишки: аденокарцинома, солидный рак, слизистый (перстневидно-клеточный) и скиррозный рак. Различают также 3 степени дифференцировки рака: высокодифференцированный, средней степени дифференцировки и низкодифференцированный.
Приводим Международную морфологическую классификацию
РОК.
1. Аденокарцинома:
а) высокодифференцированная;
б) умеренно дифференцированная;
в) малодифференцированная.
2. Слизистая аденокарцинома:
а) мукоидный рак;
б) слизистый рак;
в) коллоидный рак.
3. Перстневидно-клеточный рак - мукоцеллюлярный.
4. Недифференцированный рак (carcinoma simplex, медуллярный, трабекулярный).
5. Неклассифицируемый рак.
Закономерности метастазирования
Метастазирование РОК имеет свои особенности.
Лимфогенный путь. Различают 3 этапа метастазирования в регионарные лимфатические узлы:
• I этап - эпиколические или параколические лимфатические узлы;
• II этап - промежуточные или собственно брыжеечные лимфатические узлы;
• III этап - парааортальные, в область корня брыжейки ободочной кишки.
Далее лимфа собирается в лимфатическую цистерну, расположенную поперечно в области I-II поясничных позвонков. От цистерны лимфа по грудному лимфатическому протоку вливается в венозную систему в области левого венозного угла - места слияния подключичной вены с внутренней яремной. Там же обычно определяются надключичные метастазы.
Гематогенный путь метастазирования связан с прорастанием опухоли в венозную сеть с последующим распространением с током крови - прежде всего в печень, легкие, кости и другие органы.
Имплантационный путь метастазирования, или контактный, связан с прорастанием опухолью всех слоев стенки кишки, отрывом раковых клеток от основной массы опухоли и их имплантацией по брюшине. Эти раковые клетки дают начало мелкобугристому высыпанию, называемому карциноматозом брюшины. Последний обычно сопровождается раковым асцитом. Проявлением карциноматоза являются метастазы в пупок и по брюшине малого таза. Эти метастазы могут быть определены при первичном осмотре больного с применением пальцевого ректального и вагинального методов обследования. Их обнаружение свидетельствует о запущенном процессе.
Деление на стадии
Стадию рака ободочной кишки или степень распространенности опухолевого процесса определяют следующие 3 компонента:
• размер и глубина инвазии первичной опухоли;
• метастазирование в регионарные лимфатические узлы;
• метастазирование в отдаленные органы.
I стадия - опухоль до 1,5 см в наибольшем измерении, локализующаяся в пределах слизистой оболочки и подслизистого слоя кишечной стенки. Регионарных метастазов при этой стадии нет.
II стадия:
а) опухоль больших размеров, но занимающая не более полуокружности кишки и не прорастающая серозный покров; регионарных метастазов нет;
б) опухоль такого же или меньшего размера, но имеются одиночные метастазы в ближайших регионарных лимфатических узлах.
III стадия:
а) опухоль, занимающая более половины окружности кишки, прорастающая все слои ее стенки и серозный покров; метастазов нет;
б) опухоль любого размера, но при наличии множественных метастазов в регионарных лимфатических узлах.
IV стадия - обширная опухоль, прорастающая в соседние органы, наличие множественных лимфогенных метастазов или опухоль любых размеров с наличием отдаленных метастазов.
Необходимо отметить, что достоверно стадия заболевания должна быть установлена после всестороннего обследования больного - выяснения местного статуса, возможных метастазов, морфологического исследования операционного материала. Отсутствие соответствующей
информации часто ведет к необоснованному завышению стадии процесса, что, естественно, отражается на показателях запущенности.
Для унификации стадирования РОК используется Международная клиническая классификация по системе TNM (2002).
МЕЖДУНАРОДНАЯ КЛАССИФИКАЦИЯ ПО СИСТЕМЕ TNM (2002)
Правила классификации
Представленная ниже классификация применима только для рака. В каждом случае необходимо гистологическое подтверждение диагноза.
Анатомические области
Ободочная кишка
1. Червеобразный отросток.
2. Слепая кишка.
3. Восходящая ободочная кишка.
4. Печеночный изгиб ободочной кишки.
5. Поперечная ободочная кишка.
6. Селезеночный изгиб ободочной кишки.
7. Нисходящая ободочная кишка.
8. Сигмовидная кишка. Ректосигмоидное соединение
Регионарные лимфатические узлы
Ниже представлены основные группы лимфатических узлов для каждой анатомической области.
Червеобразный отросток: подвздошно-ободочные лимфати-
ческие узлы.
Слепая кишка: подвздошно-ободочные и правые
ободочные лимфатические узлы.
Восходящая ободочная кишка: подвздошно-ободочные, правые
ободочные, средние ободочные лимфатические узлы.
Печеночный изгиб: правые ободочные и средние обо-
дочные лимфатические узлы.
 Метастазы
в иные лимфатические узлы расценивают как отдаленные. Исключение
составляет первичная опухоль, которая распространяется на другие
сегменты ободочной и прямой кишки либо на тонкую кишку.
Метастазы
в иные лимфатические узлы расценивают как отдаленные. Исключение
составляет первичная опухоль, которая распространяется на другие
сегменты ободочной и прямой кишки либо на тонкую кишку.
Клиническая классификация TNM
Т - первичная опухоль
Тх - оценка первичной опухоли невозможна. Т0 - первичная опухоль не обнаружена.
Tis - рак in situ: раковые клетки обнаруживают в пределах базальной мембраны желез или в собственной пластинке слизистой оболочки*.
Т1 - опухоль поражает подслизистый слой.
Т2 - опухоль проникает в мышечный слой.
Обратите внимание!
* К раку in situ не относят опухоли, которые проникают в подслизистый слой или мышечную пластинку слизистой оболочки.
Т3 - опухоль проникает в субсерозный слой либо не покрытую брюшиной околоколитическую и параректальную клетчатку.
Т4 - опухоль поражает соседние органы и ткани*, ** и (или) проникает через висцеральную брюшину.
Обратите внимание!
* Поражение соседних органов и тканей включает распространение опухоли на другие отделы толстой кишки через серозную оболочку (например, распространение опухоли слепой кишки на сигмовидную кишку).
** Макроскопическое распространение опухоли на соседние органы расценивают как стадию Т4. Поражение органов, по данным микроскопического исследования, расценивают как стадию рТ3.
N - регионарные лимфатические узлы
? - состояние регионарных лимфатических узлов оценить невозможно.
N0 - метастазов в регионарных лимфатических узлах нет. N1 - поражено от 1 до 3 регионарных лимфатических узлов. N2 - поражено 4 регионарных лимфатических узла и более.
Обратите внимание!
Обнаружение пораженных лимфатических узлов обычной формы в околоколитической или параректальной жировой клетчатке при отсутствии резидуальных лимфатических узлов без гистологического подтверждения описывают по pN и расценивают как метастазы в регионарные лимфатические узлы. В свою очередь, обнаружение метастатических узлов неправильной формы определяется как рТ и свидетельствует о поражении сосудов. В случае микроскопического прорастания стенки вен опухоль описывают как V1, при макроскопическом прорастании - как V2.
М - отдаленные метастазы
Мх - недостаточно данных для определения отдаленных метастазов.
М0 - нет отдаленных метастазов. М1 - имеются отдаленные метастазы.
Патоморфологическая классификация pTNМ
Критерии выделения категорий рТ, pN и рМ соответствуют таковым для категорий Т, N и М.
С целью патоморфологической оценки показателя N проводят удаление 12 регионарных лимфатических узлов или более. В настоящее время принято, что отсутствие характерных изменений ткани
при патоморфологическом исследовании биоптатов меньшего количества лимфатических узлов позволяет подтвердить стадию pN0.
Группировка по стадиям
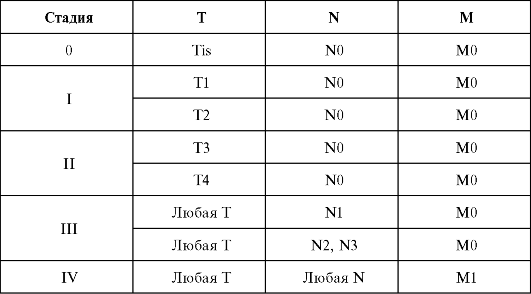 Осложнения
Осложнения
К осложнениям РОК относятся:
• обтурационная кишечная непроходимость;
• перфорация опухоли толстой кишки с развитием перитонита;
• перифокальные воспалительно-гнойные процессы (гнойный параколит, паранефрит, флегмона брюшной стенки, забрюшинного пространства);
• кровотечение из опухоли (редко профузное);
• прорастание опухоли в соседние органы и развитие межорганных свищей.
КЛИНИЧЕСКАЯ КАРТИНА
Симптомы рака правой и левой половины ободочной кишки
Клинические проявления РОК весьма многообразны и определяются локализацией опухоли, анатомическим типом роста новообразования, гистологической структурой рака, стадией и степенью распространенности опухолевого процесса, осложнениями и индивидуальной реактивностью организма.
Клиническая картина РОК характеризуется следующими группами симптомов.
1. Боли в животе. Как начальный признак в 2-3 раза чаще встречаются при расположении опухоли в правой половине ободочной кишки. По характеру болевые ощущения могут быть самыми разнообразными - от тупых, ноющих незначительных болей до сильных, приступообразных, вынуждающих госпитализировать больных в хирургические стационары в порядке экстренной помощи. Появление таких болей свидетельствует о нарушении пассажа кишечного содержимого, развитии кишечной непроходимости, наблюдающейся чаще всего при левосторонней локализации опухоли.
2. Кишечный дискомфорт (потеря аппетита, отрыжка, иногда рвота, ощущение тяжести в верхней половине живота). Эти симптомы чаще наблюдаются при поражении поперечной ободочной кишки, правой ее половины, реже - при левосторонней локализации опухоли.
3. Кишечные расстройства (запор, понос, чередование запора с поносом, урчание и вздутие живота). Эти симптомы расстройства кишечного пассажа чаще всего наблюдаются при левосторонней локализации опухоли, что объясняется, во-первых, преимущественно циркулярным ростом опухоли в левой половине ободочной кишки, во-вторых, плотной консистенцией уже сформировавшихся каловых масс. Конечным этапом нарушения кишечного пассажа является развитие частичной, а затем и полной обтурационной толстокишечной непроходимости.
4. Патологические выделения в виде крови, слизи, гноя во время акта дефекации - частое проявление рака дистальных отделов сигмовидной кишки.
5. Нарушение общего состояния больных выражается недомоганием, повышенной утомляемостью, слабостью, похудением, лихорадкой, бледностью кожных покровов и нарастающей гипохромной анемией. Все эти общие симптомы заболевания связаны с интоксикацией организма, обусловленной распадающейся раковой опухолью и инфицированным кишечным отделяемым, характерным для рака правой половины ободочной кишки. Он связан с функциональной особенностью (всасывательной способностью) слизистой оболочки этого отдела толстой кишки.
Наличие пальпируемой опухоли редко бывает первым симптомом заболевания, ему, как правило, предшествуют другие симптомы. Тем
не менее пальпаторное определение опухоли зачастую служит основанием для постановки правильного диагноза.
Основные клинические формы
В настоящее время, по мнению большинства исследователей, целесообразно выделять 6 форм клинического течения РОК.
1. Токсико-анемическая форма - чаще всего наблюдается при раке правой половины ободочной кишки, при котором на первый план выступают признаки нарушения общего состояния больных на фоне прогрессирующей гипохромной анемии и лихорадки. Такие больные значительное время обследуются в различных лечебных учреждениях по поводу анемии неясного генеза, пока не появятся кишечные расстройства. Этот контингент больных нуждается в тщательном специальном исследовании всей толстой кишки.
2. Энтероколитическая форма - клиническая картина заболевания начинается с кишечных расстройств. Таким больным очень часто ставят различные диагнозы: колит, энтерит, энтероколит, а при наличии крови в кале или при жидком кале - диагноз дизентерии. Поэтому при наличии перечисленных симптомов всегда требуется тщательное исследование всей толстой кишки.
3. Диспепсическая форма - характерно наличие признаков желудочно-кишечного дискомфорта. При этой форме течения РОК зачастую ставят диагноз: гастрит, язвенная болезнь, холецистит, и т.п., поэтому проводят обследование только верхних отделов ЖКТ. При дальнейшем прогрессировании заболевания присоединяются кишечные расстройства, и правильный диагноз устанавливают только после полного рентгеноэндоскопического исследования толстой кишки.
4. Обтурационная форма - чаще всего служит проявлением рака левой половины ободочной кишки с симптомами прогрессирующей кишечной непроходимости (частичная и полная обтурационная толстокишечная непроходимость).
5. Псевдовоспалительная форма - в клинической картине заболевания на 1-е место выступают признаки воспалительного процесса в брюшной полости (боли в животе, повышение температуры, появление признаков раздражения брюшины, в анализе крови - лейкоцитоз). Этот симптомокомплекс часто бывает проявлением течения РОК, осложненного гнойно-воспалительным процессом по типу параколита. Данная форма рака трудна для диагностики, так как в зависимости от локализации опухоли клиническая картина
может симулировать острый аппендицит, холецистит, аднексит, пиелонефрит и другие воспалительные заболевания органов брюшной полости и малого таза.
6. Опухолевая (атипичная) форма - при этой форме течения рака ободочной кишки заболевание начинается с того, что сам больной или врач при профилактическом осмотре на фоне полного благополучия пальпаторно находят в брюшной полости опухоль. Пальпаторное определение опухоли в животе - частое явление у больных РОК. Однако к опухолевой форме течения рака следует относить только те случаи, когда пальпаторное определение опухоли клинически доминирует, а другие признаки не выражены либо столь незначительны, что не фиксируют на себе внимание больного.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
С учетом тесного взаимоотношения ободочной кишки с органами брюшной полости, забрюшинного пространства, передней брюшной стенки РОК необходимо дифференцировать со многими заболеваниями как самой кишки, так и смежных с ней органов и тканей. Чаще всего это:
1) воспалительные заболевания ободочной кишки - хронический колит, хронический неспецифический язвенный колит, болезнь Крона, аппендикулярный инфильтрат и др.;
2) специфические воспалительные процессы - туберкулез, актиномикоз;
3) внекишечные заболевания органов брюшной полости и малого таза;
4) неэпителиальные доброкачественные (лейомиома, фибромиома) и злокачественные (саркома) опухоли ободочной кишки;
5) другие виды кишечной непроходимости - спаечная, странгуляционная, заворот, инвагинация, копростаз, динамическая кишечная непроходимость;
6) полипоз ободочной кишки;
7) дивертикулез (дивертикулиты) ободочной кишки;
8) опухоли и кисты почек, нефроптоз;
9) внеорганные забрюшинные опухоли;
10) опухоли и кисты яичников.
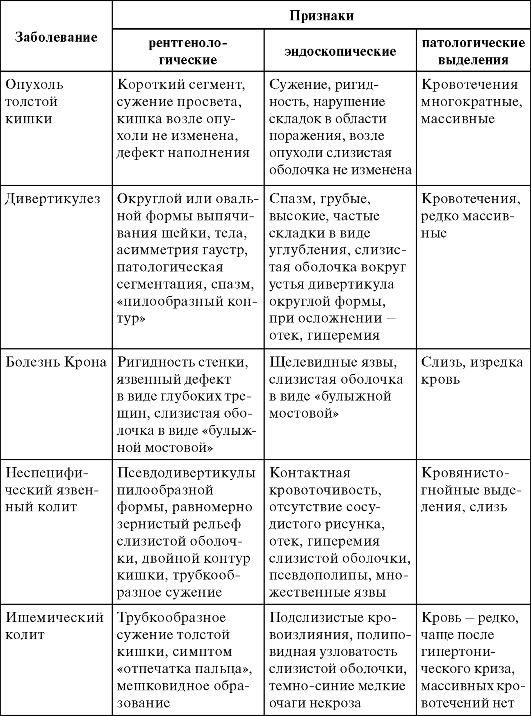
Схема дифференциальной диагностики заболеваний ободочной кишки представлена в табл. 21.1.
Таблица 21.1. Дифференциальная диагностика некоторых заболеваний толстой кишки
 Хронический
колит чаще бывает следствием перенесенного дизентерийного или амебного
колита. Возможны частые обострения, бактерионосительство.
Хронический
колит чаще бывает следствием перенесенного дизентерийного или амебного
колита. Возможны частые обострения, бактерионосительство.
Хронический неспецифический язвенный колит характеризуется аутоаллергией на собственную слизистую оболочку толстой кишки, которая отторгается, обнажая раневую поверхность; через нее выделяются эритроциты, плазма, белки плазмы и т.д. За сутки больные могут терять до 500 мл крови. Наблюдается частый, жидкий стул - несколько десятков раз в сутки. Вследствие хронического воспалительного процесса кишка становится короткой (до 60-80 см), просвет суживается; при эндоскопическом исследовании обнаруживаются язвы, которые подлежат биопсии и морфологическому исследованию.
Болезнь Крона - это терминальный илеит, но патологический процесс может локализоваться также в ободочной и прямой кишке. Этот неспецифический воспалительный инфильтрат может протекать как рак слепой кишки. Рентгенологически отмечается чередование суженных и расширенных участков. Кишка деформирована. Эндоскопическая картина напоминает «булыжную мостовую».
Периаппендикулярный инфильтрат является следствием острого аппендицита. Он включает в себя слепую кишку, червеобразный отросток, большой сальник, петлю тонкой кишки, переднюю брюшную стенку. Как правило, в его центре расплавленный червеобразный отросток, гнойник, который может при определенных условиях прорваться в свободную брюшную полость. Обычно инфильтрат появляется на 3-й и последующие дни после приступа острого аппендицита, который не был своевременно диагностирован. Инфильтрат, как правило, пальпируется в правой подвздошной области, вначале он болезненный. Такие больные подлежат консервативному лечению - им назначают местно холод, антибактериальную, противовоспалительную, детоксикационную терапию. При абсцедировании и прорыве гнойника в свободную брюшную полость показано экстренное оперативное вмешательство - лапаротомия, аппендэктомия и дренирование брюшной полости.
После консервативного лечения и рассасывания инфильтрата показана аппендэктомия через 4-6 мес.
Туберкулез толстой кишки чаще локализуется в слепой кишке, развивается у лиц молодого возраста и страдающих туберкулезом легких. У этих больных обнаруживается гладкая опухоль в проекции слепой кишки, которая характеризуется плотноэластической
консистенцией, болезненностью, малоподвижностью. У больных наблюдаются субфебрильная температура, лейкопения, лимфоцитоз. Возможно обнаружение в каловых массах туберкулезной палочки. Диагностике помогает колоноскопия с биопсией.
Актиномикоз наблюдается редко. При этом заболевании формируется инфильтрат деревянистой плотности, часто со свищами в области слепой кишки. Облегчает дифференциальную диагностику обнаружение в выделяемых из свища друз лучистого грибка - актиномицета.
Неэпителиальные опухоли ободочной кишки наблюдаются редко. Злокачественные их варианты отличаются инфильтрирующим ростом, распадом. Саркома может достигать больших размеров.
Опухоли сигмовидной кишки ввиду большой подвижности ее брыжейки часто приходится дифференцировать с опухолями и кистами яичников. Поэтому при патологии яичников необходимо обследование толстой кишки.
Большая группа опухолей забрюшинного пространства, рядом расположенных органов также требует проведения дифференциальной диагностики между ними и РОК - начиная от нефроптоза, кисты почки, первичного или вторичного рака печени, эхинококка печени, рака желудка, поджелудочной железы и т.д.
ДИАГНОСТИКА
Диагностика РОК должна быть комплексной, включать клиническое исследование, рентгенологические, эндоскопические лабораторные методы, а также специальные дополнительные методы, в т.ч. эксплоративную лапаротомию.
1. Клинические методы:
• жалобы больного. Симптомы, связанные с недостаточностью переваривания, всасывания, экссудативной энтеропатией, кишечным дискомфортом, патологическими выделениями;
• сбор анамнеза, при котором могут быть найдены указания на наличие семейного полипоза, колита и других предшествующих заболеваний;
• данные объективного исследования - применяются все методы объективного исследования: осмотр, пальпация, перкуссия брюшной полости с обязательным изменением положения больного;
• пальцевое исследование прямой кишки - также необходимо проводить в различных положениях больного.
2. Рентгенологическая диагностика - ирригоскопия, ирригография, обзорная рентгенография брюшной полости. Эти методы имеют свои разрешающие возможности и постоянно совершенствуются.
Исследование ободочной кишки проводится с применением контрастного вещества - раствора сернокислого бария, который вводят в толстую кишку с помощью клизмы. Тугое наполнение кишки раствором бария проводится не всегда, а по показаниям.
Чаще используют следующую методику: 300-400 мл раствора сернокислого бария вводят в кишечник в положении больного на спине или левом боку и делают 1-й рентгеновский снимок. В этом случае контрастируется прямая и сигмовидная кишка. Затем приподнимают ножной конец кушетки, на которой лежит больной; в таком положении заполняются селезеночный (левый) изгиб и дистальный сегмент поперечной ободочной кишки. Делают 2-й рентгеновский снимок. Затем больной поворачивается на правый бок; при этом заполняется правый изгиб. Больной встает в вертикальное положение - заполняются слепая кишка и восходящий отдел ободочной кишки. Для двойного контрастирования с помощью газоотводной трубки в просвет кишки вводят воздух.
Чаще всего при опухолях выявляют дефект наполнения толстой кишки, депо бария, отмечается отсутствие гаустраций, наблюдаются сужение просвета кишки, ригидность контура, нерасправление кишки, нарушение смещаемости и перистальтики, а также затекание контрастного вещества за пределы контура кишки при появлении свищевого хода.
Обзорная рентгенография брюшной полости позволяет определить симптом чаши Клойбера. Они свидетельствуют о нарушении пассажа по кишке, но могут быть как при обтурационной непроходимости, так и при паралитической.
О состоянии пассажа по ЖКТ можно судить с помощью приема 2-3 глотков густого бария, который в норме через 2 ч должен покинуть просвет желудка, через 6-8 ч - тонкую кишку, а через 15-20 ч достичь прямой кишки. Отклонения от указанных временных показателей свидетельствуют о нарушении пассажа, что может служить основанием к принятию решения об экстренной операции.
3. Эндоскопическая диагностика - ректороманоскопия, фиброколоноскопия, лапароскопия (с биопсией, взятием мазков для цитологического и гистологического исследования).
Фиброколоноскопия позволяет осмотреть просвет толстой кишки до купола слепой кишки. Исследование включает обязательное
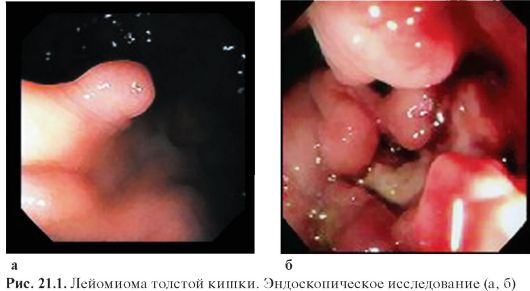 взятие материала на цитологическое и гистологическое исследование (рис. 21.1).
взятие материала на цитологическое и гистологическое исследование (рис. 21.1).
4. Лабораторная диагностика:
• общий анализ крови (для опухоли толстой кишки характерны гипохромная анемия, повышение СОЭ, лейкоцитоз);
• анализ кала на скрытую кровь (положительные реакция Грегерсена, криптогемтест);
• коагулограмма (наблюдаются признаки гиперкоагуляции);
• анализ крови на раково-эмбриональный антиген (РЭА) гликопротеид, который содержится в плазме, кишечнике, поджелудочной железе и печени эмбрионов и новорожденных. В небольших концентрациях РЭА обнаруживается как у здоровых людей, так и при некоторых формах злокачественных новообразований, в частности при РОК и раке прямой кишки.
5. Специальные дополнительные методы исследования для уточнения степени распространенности опухолевого процесса:
• сканирование печени - для диагностики гематогенных метастазов;
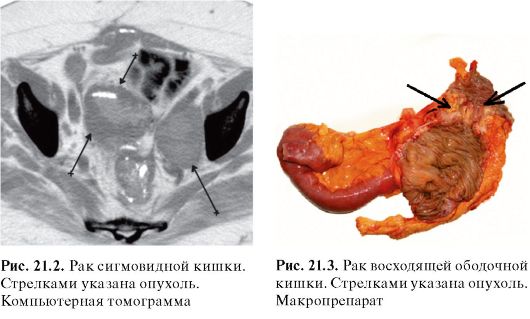
• УЗИ и КТ - для диагностики метастазов в печень и забрюшинные лимфатические узлы и коллекторы (рис. 21.2).
6. Эксплоративная (диагностическая) лапаротомия.
 ЛЕЧЕНИЕ
ЛЕЧЕНИЕ
Основной метод лечения РОК - хирургический, включающий 2 вида оперативных вмешательств.
1. Радикальные операции:
а) одномоментные: правосторонняя гемиколэктомия (рис. 21.3), резекция поперечной ободочной кишки, левосторонняя гемиколэктомия, внутрибрюшная резекция сигмовидной кишки, передняя резекция ректосигмоидного отдела толстой кишки с восстановлением кишечной непрерывности или резекция ректосигмы по Гартману;
б) 2- и 3-этапные операции: операция Цейдлера-Шлоффера (колостомия + резекция кишки + закрытие кишечной стомы), операция обструктивной резекции ободочной кишки по Микуличу или по Грекову и др.;
в) комбинированные операции с резекцией смежных органов и окружающих тканей при местно-распространенных формах РОК.
2. Паллиативные операции:
а) наложение обходного анастомоза;
б) наложение кишечной стомы - илеостома, цекостома, трансверзостома, сигмостома.
Оперативные вмешательства на ободочной кишке целесообразно заканчивать пальцевым растяжением (девульсией, редрессацией) ануса. По показаниям проводится интубация зондом или двупросветной трубкой приводящего отдела кишки.
Тактика при раке, осложненном острой кишечной непроходимостью
Обтурационная кишечная непроходимость является одним из частых осложнений в течении РОК. На ее развитие влияет ряд факторов; доминирующие из них: локализация, анатомическая форма и стадия опухолевого процесса. Непроходимость кишечника при раке сигмовидной или нисходящей ободочной кишки развивается в 2-3 раза чаще, чем при поражении правой половины ободочной кишки, по следующим причинам:
1) диаметр сигмовидной и нисходящей ободочной кишки почти вдвое меньше диаметра слепой и восходящей ободочной кишки;
2) в левой половине чаще развиваются эндофитные стенозирующие опухоли;
3) сформировавшийся плотный кал чаще обтурирует стенозированный участок, чем жидкое или кашицеобразное содержимое оральных отделов ободочной кишки.
В лечении больных с острой кишечной непроходимостью, обусловленной опухолью, весьма ответственным моментом является выбор тактики и характера оперативного вмешательства. Как правило, такие операции проводятся в неблагоприятных условиях у тяжелобольных, ослабленных основным и сопутствующим заболеванием, что, несомненно, отражается на исходе лечения.
Основной задачей хирургического вмешательства при обтурационной толстокишечной непроходимости на 1-м этапе является опорожнение кишечника от содержимого и устранение его непроходимости. Эта задача может быть решена 2 путями: наложением свища (колостомы) для отведения кишечного содержимого наружу или созданием обходного анастомоза для его отведения внутрь кишечника. Каждое из этих вмешательств может быть окончательным (обычно при раке IV стадии) или временным, производимым для подготовки больного к последующим этапам. Эти оперативные вмешательства носят паллиативный характер и направлены прежде всего на устранение непосредственной угрозы жизни больному, возникшей в результате непроходимости толстой кишки.
В отдельных случаях при осложненных формах рака толстой кишки могут быть проведены радикальные оперативные вмешательства по типу первичной обструктивной резекции, в том числе с наложением проксимальной колостомы. Последующие этапы выполняют через несколько месяцев, после дополнительной подготовки пациента. Однако первичные радикальные операции у больных с обтурационной кишечной непроходимостью опухолевого генеза показаны только при общем удовлетворительном их состоянии, отсутствии явлений перитонита и асцита. При этих же условиях, но при неудалимой опухоли может быть наложен обходной межкишечный анастомоз.
При острой кишечной непроходимости, обусловленной опухолью правой половины толстой, а также правой и средней третей поперечной ободочной кишки, могут быть выполнены следующие оперативные вмешательства:
1) правосторонняя гемиколэктомия с выведением концов подвздошной и поперечной ободочной кишки на переднюю брюшную стенку;
2) наложение обходного илеотрансверзоанастомоза, наложение обходного или илеотрансверзоанастомоза с односторонним выключением правой половины ободочной и выведением аборального конца подвздошной кишки на переднюю брюшную стенку, наложение двуствольной илеостомы и цекостомы.
Правосторонняя гемиколэктомия при острой обтурационной толстокишечной непроходимости, являющаяся радикальной операцией, осуществляется только при общем удовлетворительном состоянии пациента и отсутствии признаков перитонита или асцита.
В период острой кишечной непроходимости, обусловленной раком левой половины толстой кишки, в основном применяются 2 вида оперативных вмешательств: обструктивная резекция пораженного опухолью участка толстой кишки с наложением проксимальной колостомы или только колостомы. Первичная резекция осуществляется лишь при общем удовлетворительном состоянии больного и отсутствии признаков перитонита или асцита. Однако основным видом оперативных вмешательств при острой обтурационной непроходимости левой половины толстой кишки является наложение проксимального по отношению к опухоли свища на толстую кишку (трансверзостома, сигмостома).
При острой кишечной непроходимости, обусловленной раковой опухолью левой половины толстой кишки, широко применяется
3-этапная операция типа Цейдлера-Шлоффера. Эта операция выполняется в случаях, когда имеются явления перитонита. На 1-м ее этапе производится наложение разгрузочной колостомы проксимальнее опухоли (по типу цекостомы, трансверзостомы или сигмостомы); 2-й этап заключается в резекции пораженного опухолью участка левой половины толстой кишки и наложении межкишечного анастомоза для восстановления непрерывности кишечника; этот этап выполняется после полной ликвидации признаков кишечной непроходимости и улучшения общего состояния больного. На 3-м этапе, обычно через 2-3 нед после заживления анастомоза, выполненного на 2-м этапе, производится закрытие колостомы.
Одним из оперативных вмешательств, применяемых при острой толстокишечной непроходимости, обусловленной раком, является операция Гартмана, предложенная для лечения рака сигмовидной и ректосигмоидного отдела ободочной кишки, а также опухолевого поражения верхнеампулярного отдела прямой кишки. Суть операции заключается в резекции пораженного опухолью участка толстой кишки и наложении проксимальной одноствольной колостомы. Преимущество операции заключается в возможности последующего отсроченного восстановления непрерывности кишечного тракта.
Распространенный РОК остается во всем мире существенной причиной смертности, связанной с раком. У большинства больных выживаемость может повысить химиотерапия. Многие десятилетия с этой целью применяется 5-фторурацил. В качестве монохимиотерапии препарат используется в суммарной дозе 2600 мг/м2 в виде 24-ча- совой инфузии еженедельно до проявлений токсичности. Стандартом комбинированной химиотерапии РОК является сочетание 5-фтору- рацила с фолиевой кислотой - фторурацил в дозе 500 мг/м2 внутривенно в 1, 8, 15, 22, 29, 36-й дни и лейковорин (фолинат кальция) в дозе 500 мг/м2 внутривенно в виде 2-часовой инфузии за 1 ч до введения 5-фторурацила в те же дни.
В последние 10 лет произошла эволюция в лечении РОК с переходом от лечения 5FU/LV к ПХТ: флуоропиримидины с оксалиплатином (FOLFOX, XELOX) или иринотеканом (FOLFIRI, R-IFL) с интеграцией их в терапевтические стратегии, когда хирургическому лечению отводится все более важное место в терапии больных с метастазами. Оксалиплатин с 5FU/LV (FOLFOX) - первая комбинация, демонстрирующая превосходство перед 5FU/LV в адъювантном лечении колоректального рака. В корреляции с этим медиана
выживаемости больных с метастатическим раком ободочной кишки находится между 17 и 22 мес. Комбинация 5-фторурацил/фолие- вая кислота + капецитабин или оксалиплатин рассматривается как схема выбора в 1-й линии терапии метастатического колоректального рака. При добавлении высокодозной химиотерапии оксалиплатином к простому режиму (5-FU/LV 1 раз в 2 мес) как 2-й линии химиотерапии метастатического колоректального рака приводило к удлинению медианы выживаемости от 6,8 до 8,8 мес и увеличению выживаемости до 4,5 мес.
Современные тенденции лечения РОК связываются с использованием методов лечения, специфичных для каждого больного, чему способствуют выявление генетического и молекулярного профиля опухолей и увеличение числа таргетных агентов. Молекулярные факторы прогноза лучше всего изучены при колоректальном раке вследствие его большей распространенности и доступности для исследования и диагностики среди всех солидных опухолей - это опухолевые супрессоры онкогенеза р53, k-ras, DCC, биохимические детерминанты метаболизма 5-фторурацила и дефекты репарации ДНК. Улучшение результатов лечения при распространенных формах рака может быть продолжено в связи с разработкой мультимодальных подходов и внедрением новых таргетных агентов с инновационными комбинациями химиопрепаратов.
Две из наиболее перспективных мишеней в лечении колоректального рака - это эпителиальный рецептор фактора роста (EGFR) и сосудистый эндотелиальный фактор роста (VEGF). Ангиогенез - обязательное условие роста опухоли более 2 мм, так как при этом простая диффузия кислорода не может больше поддерживать быструю пролиферацию злокачественных клеток. Процесс ангиогенеза - это точный баланс между ингибирующими и стимулирующими факторами, знание которых помогает определить мишени для лечения колоректального рака. Ангиогенез в первичных опухолях последовательно запускает каскад молекулярных событий, приводящих к быстрому экспоненциальному росту опухоли. При первичных опухолях метастазы в печень могут развиваться без традиционных путей ангиогенеза, кооптируясь в имеющуюся печеночную сосудистую сеть. Исследование ангиогенеза позволило выявить множество различных мишеней, которые могут атаковаться агентами типа ингибиторов тирозинкиназы. В настоящее время предклиническую оценку проходит множество антиангиогенных агентов, из которых
несколько проходят I и II фазы клинических испытаний. Однако уже сейчас предварительные результаты позволяют заключить, что антиангиогенная терапия может быть важным дополнением к конвенциональной химиотерапии РОК.
Компоненты, которые инактивируют EGFR или связывают VEGF, продемонстрировали клиническую активность как самостоятельно, так и в комбинации с химиотерапией во II и III фазах клинических испытаний. Наиболее перспективные из этих компонентов - цетуксимаб, который блокирует связывание EGF и FCF-α с EGFR, и бевацизумаб, который связывает свободный VEGF. Цетуксимаб и иринотекан оценивали в двух клинических исследованиях в США. Изучали результаты применения цетуксимаба у пациентов, рефрактерных к иринотекану, с EGFR-позитивными колоректальными метастазами. В 10,5 % случаев отмечена частичная регрессия, у 22,5 % больных удалось добиться объективной регрессии при использовании цетуксимаба и иринотекана. Другой перспективный агент бевацизумаб - вариант анти-VEGF моноклональных антител. VEGF продуцируется здоровыми и опухолевыми клетками. Установлена его активность к двум рецепторам тирозинкиназы. VEGF-сигнализация - проявление физиологического и патологического ангиогенеза. Бевацизумаб изучался как антиангиогенный терапевтический фактор в качестве самостоятельного агента и в комбинации с химиотерапией у больных с III и IV стадиями РОК. В дополнение к прямому антиангиогенному эффекту бевацизумаб может способствовать более эффективной доставке химиопрепаратов, повреждая опухолевую сосудистую сеть и уменьшая повышенное тканевое давление в опухоли. Добавление бевацизумаба в дозе 5 мг/кг к химиотерапии (5FU/LV) привело к более высокой частоте объективного эффекта (40 вместо 17 %), увеличению времени до опухолевой прогрессии (9 против 5,2 мес) и удлинению медианы выживаемости (21,5 против 13,8 мес). Исследования, направленные на выявление маркерных генов, позволяют спрогнозировать реакцию опухоли на химиотерапию. Цель этих исследований - выявление пациентов, которым необходима химиотерапия, и проведение лечения в соответствии с молекулярным профилем опухоли и больного.
Лучевое лечение РОК в настоящее время применяется ограниченно (Важенин А.В. и соавт., 2003), что обусловлено такими факторами, как подвижность ободочной кишки, небольшая толщина стенки, опасность перфорации, а также радиорезистентность аденокарциномы толстой кишки.
ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ
Отдаленные результаты лечения больных с ранними стадиями рака ободочной кишки удовлетворительные. При опухолях, ограниченных слизистой оболочкой, 5-летняя выживаемость достигает 90-100 %. При II стадии этот показатель снижается до 70 %. При III стадии с метастазами в лимфатические узлы 5-летняя выживаемость составляет около 30 %.
Вопросы для самоконтроля
1. Назовите показатели заболеваемости при РОК.
2. Перечислите предраковые заболевания ободочной кишки.
3. Приведите патолого-анатомические характеристики РОК.
4. Опишите особенности метастазирования РОК.
5. Как осуществляется деление на стадии?
6. Перечислите основные клинические проявления РОК.
7. В чем особенности течения РОК в зависимости от локализации?
8. Перечислите основные клинические варианты РОК.
9. С какими заболеваниями проводится дифференциальная диагностика РОК?
10. Охарактеризуйте принципы и методы диагностики РОК.
11. Какое диагностическое значение имеют рентгенологические и эндоскопические методы исследования?
12. Осветите принципы лечения РОК.
13. Какие объемы операций выполняются в зависимости от локализации рака?
14. В чем суть паллиативных операций?
15. Перечислите показания к лекарственному и комбинированному лечению.