Онкология : учебник / М. И. Давыдов, Ш. Х. Ганцев. 2010. - 920 с.
|
|
|
|
ГЛАВА 10 МЕЛАНОМА
ЭПИДЕМИОЛОГИЯ
Меланома является злокачественной опухолью нейроэктодермального происхождения, развивающейся из меланоцитов, расположенных преимущественно в коже. Во всем мире отмечается неизменная тенденция к постоянному росту заболеваемости меланомой кожи.
По данным Американского противоракового общества с 1973 по 2005 г. заболевамость меланомой кожи удвоилась и к настоящему времени составляет около 40-50 случаев на 100 тыс. человек среди европейцев. По оценкам того же общества, ежегодно в США выявляется около 60 тыс. новых случаев заболевания и умирают от меланомы около 7800 человек. Заболеваемость в Австралии удвоилась с 1983 по 1998 г. (с 25 случаев на 100 тыс. населения - как для мужчин, так и для женщин, до 50 - для мужчин и примерно 35 - для женщин).
Аналогичные тенденции роста заболеваемости меланомой отмечаются и в Европе, где в целом показатели остаются в пределах 5-20 на 100 тыс. населения, при этом наибольшая заболеваемость отмечается в развитых странах Северной Европы (Великобритании, Норвегии, Финляндии, Исландии, Дании, Швеции, Швейцарии, Королевстве Нидерландов и Германии), где она составляет от 8 до 18 на 100 тыс. населения. Наименьшие показатели заболеваемости в Европе отмечаются в Португалии, на Кипре и в Болгарии - менее 5 на 100 тыс., средние показатели (5-10 на 100 тыс.) характерны для Литвы, Латвии, Словакии, Украины, Польши.
В России абсолютное число больных с впервые в жизни установленным диагнозом меланомы в 2007 г. составило 7732 человека. В структуре онкологической заболеваемости доля меланомы кожи у мужчин составила 1 %, у женщин - 1,6 %. Отмечается рост заболеваемости: показатель впервые в жизни установленного диагноза в 1997 г. составил 3,89, в 2007 г. - 5,4.
Следует отметить, что среди всех злокачественных опухолей кожи меланома занимает особое место. Так, составляя структурно не более 10 % всех форм рака кожи, она ответственна за 80 % смертей, приходящихся на группу злокачественных опухолей кожи. Причина этого феномена состоит в том, что в отличие от базально-клеточного и плоскоклеточного рака кожи меланома является более злокачественной опухолью, для которой характерны не только местный рецидив или появление регионарных лимфогенных метастазов, но в значительно большей степени гематогенное метастазирование с развитием отдаленных метастазов.
Общемировая тенденция роста заболеваемости меланомой кожи объясняется произошедшим за последние десятилетия увеличением суммарного времени воздействия УФ-части спектра солнечного света на человека, генетически к этому не подготовленного.
Несмотря на быстрый рост заболеваемости меланомой кожи в мире, статистика смертности от этого заболевания практически не изменилась. Например, при почти двукратном росте заболеваемости в Австралии в период с 1983 по 1998 г. смертность от меланомы кожи осталась на прежнем уровне, а в США при более чем двукратном росте заболеваемости с 1973 по 2005 г. выросла незначительно. В России смертность от меланомы кожи пока продолжает расти.
ФАКТОРЫ, СПОСОБСТВУЮЩИЕ МАЛИГНИЗАЦИИ ПИГМЕНТНЫХ НЕВУСОВ, МЕРЫ ПРОФИЛАКТИКИ ИХ ОЗЛОКАЧЕСТВЛЕНИЯ
Заболеваемость меланомой кожи выше среди европеоидов с 1-м и 2-м фототипами кожи - кельтским и скандинавским (табл. 10.1), составляющих большую часть населения Северной Европы. Среди людей с 3-м и 4-м фототипами заболеваемость меланомой кожи существенно ниже, а при 5-м и 6-м фототипах (афроамериканцы) меланома кожи - крайне редкое заболевание.
Таблица 10.1. Фототипы кожи по Д.Е. Фитцпатрику
Тип кожи Характеристика Популяции | ||
1-й | Чрезмерно белая кожа, рыжие или светлорусые волосы, голубые или зеленые глаза, кожа не подвержена загару, легко возникают солнечные ожоги (кельтский фототип) | Европеоиды |
Окончание табл. 10.1
 Значимыми
факторами риска развития меланомы кожи являются наличие 1-го и 2-го
фототипов кожи у лиц, периодически или регулярно подвергающихся
повышенной солнечной инсоляции в результате временного или постоянного
проживания в регионах с жарким климатом.
Значимыми
факторами риска развития меланомы кожи являются наличие 1-го и 2-го
фототипов кожи у лиц, периодически или регулярно подвергающихся
повышенной солнечной инсоляции в результате временного или постоянного
проживания в регионах с жарким климатом.
Другими факторами риска являются 3 эпизода солнечных ожогов и более в течение жизни, наличие на поверхности кожи веснушек и лентиго или трех атипичных меланоцитарных невусов и более.
Весьма важным обстоятельством является то, что у части больных меланома развивается на месте существующего пигментного невуса. Меланомоопасные невусы представляют собой в основном приобретенные меланоцитарные невусы, а не врожденные.
Все пигментные невусы на коже человека можно разделить на 3 клинико-гистологических типа: внутридермальные, пограничные и смешанные (сложные).
Внутридермальные невусы характеризуются глубоким залеганием в толще дермы. При этом они приподнимают эпидермис и клинически выглядят в виде горошины или узелка, чаще светло-коричневых
оттенков. Внутридермальные невусы могут быть действительно врожденными или появляются на теле в раннем детском возрасте.
Когда в процессе формирования внутридермального невуса его клетки достигают базальной мембраны, которая отделяет собственно дерму от эпидермиса, возникает смешанный, или сложный, невус. Клинически он имеет сходство с внутридермальным невусом, только иногда вокруг основания подобного узелкового образования может наблюдаться небольшая кайма пигментации, представляющая собой приграничный к дерме и эпидермису компонент. Смешанный невус, как и внутридермальный, может быть врожденным или сформироваться сразу после рождения.
По большому счету, ни внутридермальный, ни смешанный типы невусов не являются меланомоопасными, хотя часто привлекают к себе внимание из-за не совсем эстетической формы (иногда наблюдается рост редких волосков на их приподнятой поверхности). Но всегда эти «родинки» имеют один доминирующий оттенок цвета - от светлодо темно-коричневого. В последнем случае они ложно привлекают к себе внимание, хотя в действительности настораживать должна не интенсивность пигментации, а полихромия, т.е. разные ее оттенки.
Онкологическую настороженность следует проявлять в отношении пограничного невуса, который действительно является меланомоопасным. Подобный тип невуса формируется вдоль границы дермы и эпидермиса. Клинически он представляет собой совершенно плоское пигментное образование. Пограничные невусы почти всегда бывают приобретенными. Чаще они начинают проявляться на разных участках тела в возрасте 15-25 лет. Долгое время их размеры не превышают 2-3 мм; это создает иллюзию у их носителя, что они существуют с рождения, хотя это не так. Большинство пограничных невусов так и остаются без изменений годами, однако некоторые из них могут иметь тенденцию к росту. Обычно это длительный процесс: за год подобного рода образование может увеличиться всего на 1 мм и, таким образом, достигнуть размеров до 1 см за несколько лет. Следует помнить, что если плоская приобретенная «родинка» увеличивается и достигает размера 5-6 мм, обязательно следует проконсультироваться у онколога. В случае роста пограничного невуса из него может сформироваться реальный предшественник меланомы кожи - диспластический невус, который характеризуется появлением легкой или выраженной ассиметрии, точечных участков депигментации, размером более 5 мм, со склонностью к заметному
росту за последние 1-2 года. Нередко эту заметную склонность к росту можно связать с интенсивным воздействием солнечных УФ-лучей (вплоть до ожогов кожи).
Данный процесс может иметь системный характер, в этом случае речь идет о так называемом синдроме множественных диспластических невусов, ассоциированном с меланомой, - FAMMM (Familial atypical multiple mole melanoma syndrome). Этот синдром служит наиболее значимым известным фактором риска развития меланомы кожи; основное его клиническое проявление - наличие множества диспластических невусов на поверхности кожи.
Помимо описанных, встречаются редкие пигментные образования кожи, также являющиеся меланомоопасными, - к ним относятся меланоз Дюбрея, невус Ота, гиганский врожденный меланоцитарный невус, голубой невус.
ОСОБЕННОСТИ РОСТА И МЕТАСТАЗИРОВАНИЯ
Клинически меланома кожи представлена четырьмя основными формами с учетом как клинических симптомов, так и гистологических характеристик. Они включают:
- поверхностнораспространяющуюся меланому;
- акрально-лентигинозную меланому;
- меланому типа злокачественного лентиго;
- узловую меланому.
Первые 3 типа опухоли можно рассматривать вместе, поскольку в своем развитии они проходят 2 фазы роста. Опухолевый процесс начинается с распространения опухоли в горизонтальном направлении по поверхности кожи. Микроскопически он определяется как фаза радиального роста. Постепенно, в течение разного периода времени, в горизонтально распространяющейся опухоли начинают развиваться узловые компоненты: наступает 2-я, вертикальная фаза роста.
Поверхностнораспространяющаяся меланома - наиболее часто встречающаяся клиническая форма (70 %); возникает преимущественно на фоне существующего пигментного невуса; может находиться на любом участке кожи, у женщин чаще встречается на ногах, у мужчин - в области верхней половины спины; средний возраст начала заболевания - 30-50 лет (рис. 10.1). Эта форма характеризуется относительно благоприятным прогнозом, связанным с наличием 2 фаз развития - радиального и вертикального роста. В фазе радиального роста, которая может длиться несколько лет, опухоль обладает
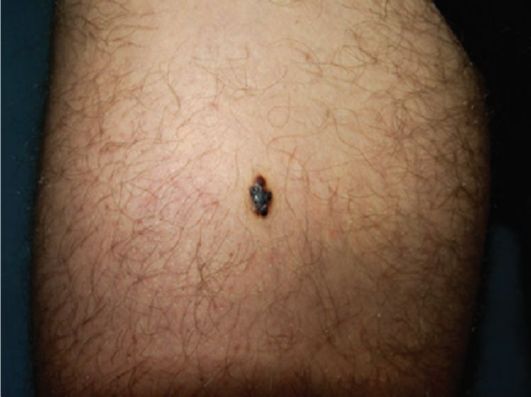 Рис. 10.1. Меланома кожи правой голени
Рис. 10.1. Меланома кожи правой голени
низким потенциалом для дальнейшего развития; в последующем эта фаза переходит в фазу вертикального роста, которая характеризуется проникновением опухолевых клеток в более глубокие слои кожи и подкожную жировую клетчатку, что способствует дальнейшему распространению болезни.
Акрально-лентигинозная меланома локализуется на коже ладоней, подошв и в области ногтевой пластины. Этот тип опухоли европеоидов встречается в 10 % случаев и более распространен среди представителей негроидной расы (до 70 %). По морфологическим и клиническим особенностям акрально-лентигинозная меланома в значительной степени схожа с поверхностнораспространяющейся формой, поскольку также характеризуется наличием двух фаз роста. Специфическая локализация опухоли затрудняет ее раннюю диагностику, что ухудшает прогноз заболевания.
Меланома типа злокачественного лентиго (лентиго-меланома) встречается довольно редко (5 % от всех форм меланомы) и выделена в особую группу вследствие некоторых клинических особенностей - позднего возраста начала заболевания (в среднем около 70 лет), анатомической локализации (преимущественно на коже лица), медленного роста и относительно благоприятного течения. Развивается на фоне предракового изменения кожи - злокачественного лентиго, которое характеризуется появлением различных по форме и окраске пигментных пятен, похожих на крупные веснушки, длительным хроническим течением и отсутствием способности к инвазии. Эта форма опухоли, как и поверхностнораспространяющаяся меланома, проходит 2 фазы роста, причем фаза радиального роста продолжается
до 10-20 лет, а фаза вертикального роста может длиться несколько лет, а не месяцев, как при меланоме поверхностнораспространяющегося типа. Такие особенности биологического развития объясняют отсутствие резких скачков в течении опухоли и относительно низкий риск развития метастазов. Прогноз при этой форме меланомы более благоприятный.
Узловая меланома - 2-я по частоте встречаемости форма (15 %); может возникать в любом возрасте, чаще развивается на неизмененной коже в области туловища, головы и шеи (рис. 10.2, 10.3). Характеризуется быстрым ростом (в течение нескольких месяцев) и менее благоприятным прогнозом в связи с отсутствием фазы радиального роста. Узловой тип меланомы, в отличие от первых трех типов, с самого начала развития опухолевого процесса не имеет
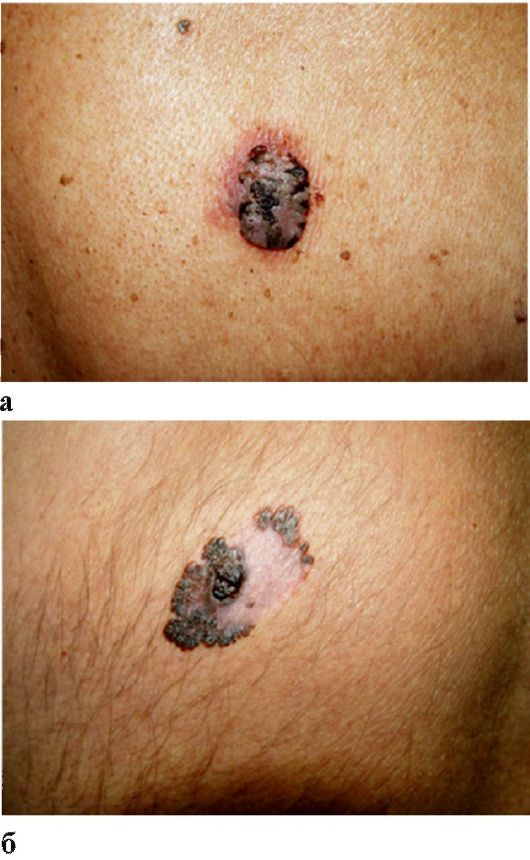 Рис. 10.2. Меланома кожи спины (а, б)
Рис. 10.2. Меланома кожи спины (а, б)
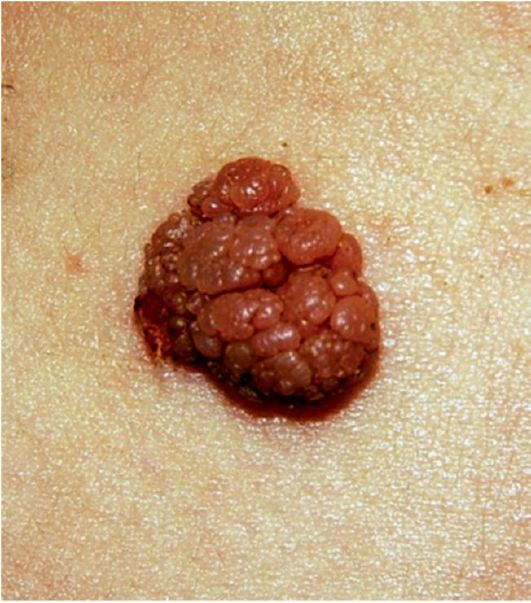 Рис. 10.3. Меланома кожи спины
Рис. 10.3. Меланома кожи спины
горизонтального компонента и сразу представляет собой инвазивный узел в фазе вертикального роста.
К редким типам опухоли относят амеланотическую (беспигментную) меланому, клетки которой лишены пигмента, а поэтому опухоль не имеет характерной темной окраски, и десмопластический или нейротропный вариант меланомы.
МЕЖДУНАРОДНАЯ КЛАССИФИКАЦИЯ ПО СИСТЕМЕ TNM (2002)
Правила классификации
В каждом случае необходимо гистологическое подтверждение
диагноза.
Регионарные лимфатические узлы
Локализация регионарных лимфатических узлов зависит от первичной опухоли.
Односторонние опухоли
Голова, шея: ипсилатеральные предушные, под-
нижнечелюстные шейные и надключичные лимфатические узлы.
Грудная клетка: ипсилатеральные подмышечные
лимфатические узлы.
Верхние конечности: ипсилатеральные локтевые и под-
мышечные лимфатические узлы.
Живот, ягодицы и пах: ипсилатеральные паховые лимфати-
ческие узлы.
Нижние конечности: ипсилатеральные подколенные и
паховые лимфатические узлы.
Перианальная область: ипсилатеральные паховые лимфати-
ческие узлы.
Опухоли пограничных зон
Лимфатические узлы, примыкающие с обеих сторон к пограничной зоне, рассматривают как регионарные. Пограничная зона распространяется на 4 см от указанных ниже ориентиров:
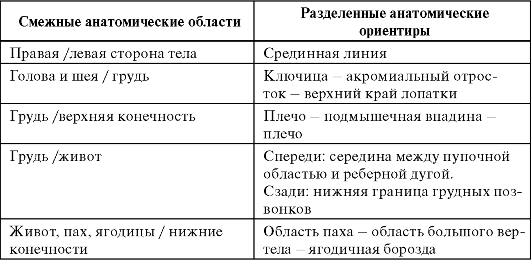 Любые метастазы в иные лимфатические узлы следует расценивать как М1.
Любые метастазы в иные лимфатические узлы следует расценивать как М1.
Клиническая классификация TNM
Т - первичная опухоль
Размеры опухоли оценивают после ее иссечения (см. рТ). N - регионарные лимфатические узлы
? - состояние регионарных лимфоузлов оценить невозможно. N0 - метастазов в регионарных лимфоузлах нет. N1 - метастазы в одном регионарном лимфоузле:
N1a - скрытые (микроскопические) метастазы.
N1b - макроскопические метастазы. N2 - метастазы в двух или трех регионарных лимфатических
узлах, а также сателлитные или транзитные метастазы:
N2a - скрытые (микроскопические) метастазы.
N2b - макроскопические метастазы.
N2c - сателлитные или транзитные метастазы без поражения регионарных лимфатических узлов. N3 - метастазы в четырех или более регионарных лимфатических узлах, сливающиеся метастазы, либо сателлитные (транзитные) метастазы с поражением регионарных лимфатических узлов.
Обратите внимание!
К внутрилимфатическим регионарным метастазам относят сателлитные метастазы (расположенные на расстоянии менее 2 см от первичного очага меланомы) и транзитные метастазы (расположенные на расстоянии более 2 см от первичного очага меланомы, но ближе, чем регионарные узлы 1-го порядка).
М - отдаленные метастазы
Мх - наличие отдаленных метастазов оценить невозможно.
М0 - отдаленных метастазов нет.
М1 - наличие отдаленных метастазов:
Мга - метастазы в коже, подкожной жировой клетчатке или отдаленных лимфатических узлах.
М1Ь - метастазы в легкие.
М1с - метастазы во внутренние органы либо отдаленные метастазы любой локализации с повышением уровня лактатдегидрогеназы сыворотки крови.
Патоморфологическая классификация pTNM
рТ - первичная опухоль
Патоморфологическая классификация pTNM основана на трех гистологических критериях:
1) толщина опухоли (метод Бреслоу [Breslow]) - наибольший вертикальный диаметр опухоли, в мм;
2) глубина инвазии опухоли (метод Кларка [Clark]);
3) наличие или отсутствие язвенного поражения первичной опухоли.
рТ - первичная опухоль
рТх - оценка первичной опухоли невозможна (тонкий срез выполнен скальпелем или имеет место регрессирующая меланома). рТ0 - первичная опухоль не обнаружена.
pTis - меланома in situ (1-й уровень инвазии по методу Кларка) - атипичная меланоцитарная гиперплазия, неинвазивная опухоль.
рТ1 - меланома толщиной до 1,0 мм с наличием или отсутствием изъязвления:
рТ1а - меланома толщиной до 1,0 мм с уровнем инвазии II или III и отсутствием изъязвления;
рТ1Ь - меланома толщиной до 1,0 мм с уровнем инвазии IV или V или с изъязвлением. рТ2 - меланома толщиной 1, 01-2 мм с наличием или отсутствием
изъязвления:
рТ2а - меланома толщиной 1,01-2 мм без изъязвления; рТ2Ь - меланома толщиной 1,01-2 мм с изъязвлением. рТ3 - меланома толщиной 2,01-4 мм с наличием или отсутствием изъязвления:
рТ3а - меланома толщиной 2,01-4 мм без изъязвления; рТ3Ь - меланома толщиной 2,01-4 мм с изъязвлением. рТ4 - меланома толщиной более 4 мм с наличием или отсутствием изъязвления:
рТ4а - меланома толщиной более 4 мм без изъязвления; рТ4Ь - меланома толщиной более 4 мм с изъязвлением.
pN - регионарные лимфатические узлы
Критерии выделения категории pN соответствуют таковым для категории N.
С целью патоморфологической оценки показателя N проводят удаление 6 регионарных лимфатических узлов или более. В настоящее время принято, что отсутствие характерных изменений ткани при патоморфологическом исследовании биоптатов меньшего количества лимфатических узлов позволяет подтвердить стадию pNO. Оценка показателя pN, по данным биопсии сторожевого лимфатического узла, сопровождается указанием дополнительных индексов sn (например, pN1sn).
рМ - отдаленные метастазы
Критерии выделения категории pМ соответствуют таковым для категории М.
По данным Европейского общества медицинской онкологии (ESMO), 10-летняя выживаемость больных, у которых иссечение меланомы кожи было осуществлено на стадии IA, составляет до 90 %, в то время как при стадии IIc - лишь 32,3 % (табл. 10.2). Обе эти стадии характеризуются наличием лишь первичной опухоли при отсутствии клинически определяемых регионарных или отдаленных метастазов, и такое различие в выживаемости обусловлено только стадией самой опухоли - рТ. Стадию первичной меланомы кожи устанавливают на основании данных морфологического исследования, в ходе которого измеряют толщину и уровень инвазии опухоли по Breslow и Clark, а также определяют такую характеристику опухоли, как изъязвление.
Таблица 10.2. Стадирование меланомы кожи по AJCC (6-я классификация) и 10-летний прогноз при различных стадиях заболевания (2002 г.)
 Окончание табл. 10.2
Окончание табл. 10.2
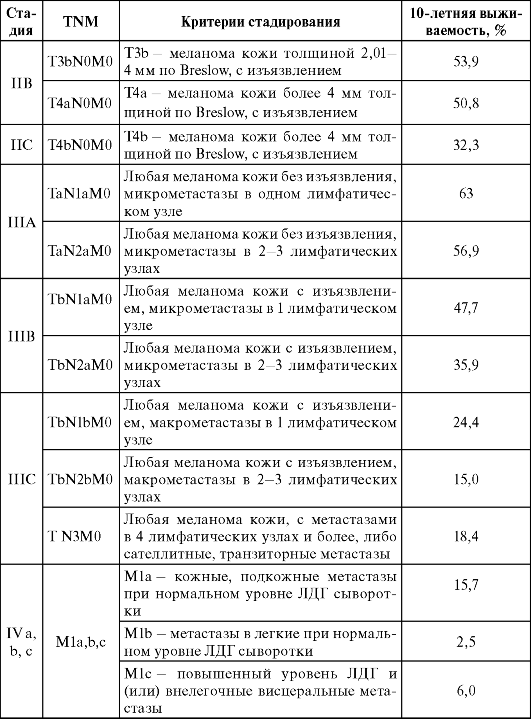 Видно,
что еще до развития клинически и инструментально определяемых
регионарных или отдаленных метастазов прогноз заболевания существенно
различается в зависимости от стадии развития первичной опухоли. Это
обусловлено биологическими особенностями меланомы кожи - агрессивным
течением и ранним лимфогенным и гематогенным метастазированием,
возможным наличием неопределяемых современными методами исследования
микрометастазов уже на ранних стадиях, при толщине меланомы >1 мм.
Видно,
что еще до развития клинически и инструментально определяемых
регионарных или отдаленных метастазов прогноз заболевания существенно
различается в зависимости от стадии развития первичной опухоли. Это
обусловлено биологическими особенностями меланомы кожи - агрессивным
течением и ранним лимфогенным и гематогенным метастазированием,
возможным наличием неопределяемых современными методами исследования
микрометастазов уже на ранних стадиях, при толщине меланомы >1 мм.
Метастазирование меланомы происходит лимфогенным путем в кожу, лимфатические узлы и гематогенным путем - в печень, легкие, головной мозг, кости, почки, надпочечники. Тенденции к метастазированию меланомы зависят от биологических особенностей опухоли. Встречаются формы, которые метастазируют в течение длительного времени только лимфогенно в регионарные лимфатические узлы. Существуют меланомы с высоким потенциалом злокачественности, со склонностью к раннему гематогенному метастазированию. Особо следует выделить такие формы кожных метастазов, как сателлитная, узловая, рожеподобная, тромбофлебитоподобная.
Сателлиты - это мелкие множественные высыпания около первичного очага или на некотором расстоянии от него в виде пятен, сохранивших окраску первичной опухоли. Узловая форма кожных метастазов проявляется множественными подкожными узлами различного размера, которые могут располагаться на любом расстоянии от первичной опухоли. Рожеподобная форма кожных метастазов выглядит как участок отечной кожи синевато-красного цвета, окружающей опухоль. Тромбофлебитоподобная форма кожных метастазов проявляется радиально распространяющимися болезненными уплотнениями, расширенными поверхностными венами и гиперемией кожи вокруг меланомы.
ДИАГНОСТИКА
Диагностика меланомы кожи первоначально основывается на визуальных признаках проявлений этой опухоли. Диагностический алгоритм визуальной оценки пигментного образования включает в себя оценку размеров, симметрии, краев, цвета и динамики эволюционных изменений образования. Традиционно данный алгоритм описывается правилом ABCDE:
A - asymmetry: оценивается симметричность образования; для меланомы кожи характерна асимметрия, выражающаяся
в геометрическом несоответствии одной половины образования другой.
B - boundary: край меланомы кожи обычно неровный, изъеденный.
С - color: для меланомы кожи характерны неоднородность окраски, вариабельность цветовой гаммы - от черного до белого и голубого.
D - dimension: для меланомы кожи характерен диаметр >6 мм,
однако данная харакетристика не является обязательной. E - evolution или elevation: какие-либо изменения пигментного образования в течение последних 6 мес - 1 года или образование, возвышающееся над поверхностью кожи (характеризует узловой компонент). Наличие подозрения на меланому кожи, основанного на данных клинических признаках, является показанием к проведению эксцизионной (тотальной) биопсии пигментного образования.
Единственным окончательным методом диагностики и стадирования меланомы кожи является морфологическое исследование образования, иссеченного в пределах здоровых тканей.
Стандартом ВОЗ, ESMO и NCCN (Национальной противораковой согласительной сети США) при выявлении кожного образования, подозрительного на меланому, является эксцизионная биопсия с отступом в пределе 2 мм - 1 см от края образования.
Методы специального обследования
Несмотря на кажущуюся простоту представленного выше диагностического алгоритма, первоначальная оценка пигментного образования может быть затруднительной. Это связано с широким распространением среди европеоидов других образований кожи, внешние характеристики которых могут напоминать меланому кожи: различных меланоцитарных, сложных и пограничных невусов, возрастного лентиго, гемангиом и других. Также следует заметить, что сложности в визуальной оценке образования возникают именно на ранних стадиях меланомы, в фазе горизонтального роста, когда узлового компонента еще нет.
Особую сложность в диагностике представляют пациенты с синдромом множественных диспластических невусов, у которых формально могут быть подозрительными на меланому кожи несколько десятков или сотен невусов. В этих условиях проведение эксцизионной биопсии всех подозрительных образований не представляется
возможным и в связи с этим требуется более точная предварительная диагностика с учетом того, что данный синдром является наиболее значимым фактором риска развития меланомы кожи.
В настоящее время ведется поиск более эффективных неинвазивных методов диагностики меланомы кожи, одним из которых является эпилюминесцентная дерматоскопия, позволяющая оценить как «классические» ABCDE-симптомы при 10-60-кратном увеличении, так и наличие в пигментном образовании специфических дерматоскопических симптомов меланомы. Сегодня в дерматоскопической диагностике меланомы кожи общеприняты 2 основных алгоритма, учитывающих эти симптомы: алгоритм Штольца, оценивающий образование по ABCDE-системе, и алгоритм Аргезиано, суммирующий баллы, полученные при оценке дерматоскопических характеристик.
Таким образом, при использовании эпилюминесцентной дерматоскопии в большинстве случаев удается отдифференцировать меланому кожи от доброкачественных образований, выделить образования, требующие эксцизионной биопсии и динамического наблюдения. У пациентов с FAMMM-синдромом динамический контроль с помощью данного метода исследования является адекватным способом оценки изменений в диспластическом невусе и диагностики меланомы на ранней стадии ее развития.
При выявлении меланомы кожи для исключения диссеминации процесса европейскими стандартами рекомендуется выполнять:
- общий анализ крови, определять уровень лактатдегидрогеназы (ЛДГ) и щелочной фосфатазы в сыворотке крови;
- рентгенографию органов грудной клетки;
- УЗИ органов брюшной полости, забрюшинного пространства, регионарных лимфатических узлов - при толщине опухоли > 1 мм или при подозрительных клинических находках.
Другие специальные исследования (КТ, ПЭТ, радиоизотопные исследования) проводятся по клиническим показаниям, при обоснованном подозрении на наличие метастазов в каком-либо конкретном органе или области.
ЛЕЧЕНИЕ
В лечении меланомы кожи применяются хирургические, лучевые, лекарственные методы лечения, а также их комбинации (комбинированный метод).
Хирургическое лечение
Необходимо иссечение первичной опухоли в пределах здоровых тканей с краями резекции от границы опухоли:
• 0,5 см для стадии IA;
• 1,0 см для стадии IB-IIA;
• 2,0 см при толщине опухоли >2 мм.
Увеличение границ отступа нецелесообразно, так как не предотвращает дальнейшего прогрессирования заболевания: биологической особенностью кожи является раннее метастазирование, а не локальный рецидив (рис. 10.4, 10.5).
Исключениями из этого правила служат десмопластический вариант меланомы кожи и меланома кожи особых локализаций.
Для десмопластического (или нейротропного) варианта меланомы кожи характерно развитие местных рецидивов, в связи с этим для данного типа опухоли считается целесообразным резекцию выполнять с отступом от края опухоли >3 см.
Особой локализацией меланомы кожи считается кожа пальцев, подногтевого ложа, стопы; при таком расположении соблюдение требуемого отступа не всегда возможно. С учетом биологических особенностей меланомы допускается уменьшение величины отступа при условии адекватного динамического наблюдения в последующем.
Выполнение профилактической регионарной лимфаденэктомии или проведение лучевой терапии на регионарные лимфатические
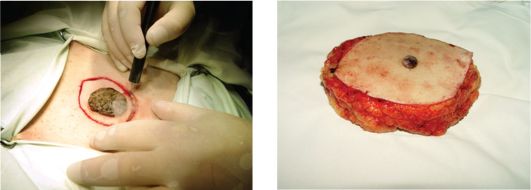 Рис. 10.4. Иссечение меланомы кожи Рис. 10.5. Макропрепарат меланомы живота кожи после иссечения
Рис. 10.4. Иссечение меланомы кожи Рис. 10.5. Макропрепарат меланомы живота кожи после иссечения
узлы не рекомендуется, так как эти манипуляции ни в какой мере не влияют на выживаемость больных.
В учреждениях онкологического профиля может быть рекомендована биопсия сторожевого лимфатического узла, позволяющая определить наличие микрометастазов непосредственно в лимфатическом узле, к которому идет лимфооток от области удаленного новообразования. Методика биопсии сторожевого лимфатического узла подразумевает введение в анатомическую область первичной опухоли радионуклида и определение его накопления в конкретных регионарных лимфатических узлах с последующей тотальной биопсией последних.
При наличии метастазов в регионарные лимфатические узлы, выявленные перед иссечением первичной опухоли или после ее иссечения (т.е. являющиеся дальнейшим развитием опухолевой болезни), всем больным, способным перенести хирургическое вмешательство, показана регионарная лимфаденэктомия. При этом должно проводиться иссечение всех групп поверхностных и глубоких лимфатических узлов данной области.
При отдаленных метастазах хирургическое лечение (метастазэктомия) показано в следующих случаях:
- наличие единичных резектабельных метастазов, так как установлено, что метастазэктомия в этих случаях может улучшить прогноз;
- наличие резектабельных метастазов, непосредственно угрожающих жизни больного или существенно ухудшающих прогноз вследствие своей локализации (например, метастазов в головной мозг);
- с целью уменьшения количества опухолевой массы перед предполагаемым лекарственным лечением (так называемые циторедуктивные операции);
- с целью получения опухолевого материала для приготовления вакцин в рамках клинических исследований либо с иными научными целями.
Меланома кожи не является радиочувствительной опухолью, в связи с чем возможности ее лучевого лечения ограничены. Лучевая терапия может использоваться при наличии множественных транзиторных метастазов конечности, при наличии неоперабельных метастазов в головном мозгу - как самостоятельный метод или в комбинации с лекарственным или хирургическим методами. Также
паллиативная лучевая терапия может быть целесообразна при метастатическом поражении костей, поскольку обладает, кроме прочего, выраженным противоболевым эффектом.
Меланома не относится к химиочувствительным опухолям, поэтому возможности химиотерапии при меланоме ограничены.
Иссечение первичной опухоли обеспечивает хороший прогноз для жизни больных только на стадиях IA-IB, при толщине опухоли до 1-2 мм. При большей толщине опухоли или при наличии изъязвления удаление первичной меланомы кожи не гарантирует выздоровления. У35 % больных в дальнейшем развиваются регионарные и отдаленные метастазы уже на стадии IIA, а при наличии на момент диагностики метастазов в регионарные лимфатические узлы прогноз еще хуже. Высокий риск метастазирования спустя некоторое время после иссечения первичной опухоли обусловлен биологической особенностью меланомы: способностью к раннему метастазированию с наличием клинически неопределяемых микрометастазов уже на относительно ранних стадиях болезни.
Эта особенность меланомы и связанное с ней ухудшение прогноза на ранних стадиях обусловливают необходимость поисков режимов адъювантной терапии для стадий IIA и выше, которые могли бы снизить риск дальнейшего прогрессирования заболевания.
Широкомасштабные исследования эффективности адъювантной химиотерапии не подтвердили ее эффективности, поэтому химиотерапия в адъювантном режиме не рекомендована в странах Европы и Северной Америки.
Поскольку меланома кожи традиционно считается иммуногенной опухолью, предпринимались попытки разработать режимы адъювантной иммунотерапии. Из исследованных в адъювантном режиме препаратов некоторую эффективность продемонстировали препараты рекомбинантных α-интерферонов. Эти исследования продемонстрировали, что α-интерфероны, применяемые в высоких дозах, способны уменьшить риск прогрессирования заболевания примерно на 15 %, что позволило FDA (Администрация по контролю за пищевыми продуктами и медикаментами США) рекомендовать высокодозную интерферонотерапию для адъювантного лечения меланомы кожи.
Следует отметить, что высокодозная адъювантная терапия α-интерферонами представляет собой лечение, сопровождающееся выраженной токсичностью, что обусловливает необходимость его
отмены примерно у половины больных. Соотношение риск-польза при применении такого лечения неоднозначно, в связи с чем на территории Европы и в России высокодозная адъювантная иммунотерапия не получила распространения. Здесь чаще применяются режимы интерферонотерапии с использованием среднемалых доз, однако эффективность этих режимов при их значительно меньшей токсичности до сих пор не подтверждена крупными клиническими исследованиями. В связи с этим ESMO до сих пор не признан какой-либо стандарт адъювантной терапии в лечении меланомы кожи.
Целесообразность проведения адъювантной иммунотерапии как в Европе, так и в США определяется общим состоянием, возрастом больного, переносимостью лечения. Альтернативой адъювантной иммунотерапии является наблюдение.
В связи с низкой чувствительностью метастазов меланомы кожи к химиотерапии эффективных методов лекарственного лечения не разработано. Тем не менее применение химиотерапии при метастатической болезни в ряде случаев способно принести пользу больному: в 10-20 % случаев отмечается определенный эффект от химиотерапии, выражающийся в клиническом ответе на лечение: удается добиться частичного уменьшения метастазов (частичный эффект) или стабилизации болезни. Редко (менее чем в 5 % случаев) отмечается полный эффект - исчезновение проявлений болезни (метастазов) на фоне лечения. При том, что статистически наличие клинических ответов не связано с увеличением выживаемости, химиотерапия метастатической меланомы может быть целесообразна в качестве паллиативного лечения, с целью уменьшения на какой-то период симптомов заболевания, с возможностью проведения циторедуктивных операций на фоне стабилизации, что может быть, в свою очередь, связано с увеличением продолжительности жизни конкретного больного, а также с улучшением качества жизни пациентов.
В связи с этим ESMO рекомендовано проведение химиотерапии при метастатической меланоме пациентам с исходно хорошим соматическим статусом.
«Классическим» препаратом в лечении метастатической меланомы кожи является дакарбазин (диметилтриазеноимидазолкарбоксамид - ДТИК). Это алкилирующее соединение: препарат нарушает синтез ДНК и РНК за счет образования комплексов с карбониевыми
ионами и останавливает митотический клеточный цикл. Частота клинических ответов при его применении в монорежиме составляет 10-20 %. Другим препаратом для лечения метастатической меланомы, активно использующимся в последнее десятилетие, является темозоламид. Попадая в кровь, он при физиологических значениях рН подвергается быстрому химическому превращению с образованием активного соединения - монометилтриазеноимидазолкарбоксамида (МТИК); последнее, являясь химическим аналогом ДТИК, обладает важным отличием от него - способностью проникать через гематоэнцефалический барьер, что обусловливает возможность применения препарата при метастазах меланомы в головной мозг. Он удобен в применении благодаря лекарственной форме - выпускается в виде капсул для приема внутрь.
Еще одним препаратом, применяющимся в монорежиме при метастатической меланоме, является фотемустин. Представляя собой производное нитрозомочевины и обладая иным механизмам действия, фотемустин также проникает через гематоэнцефалический барьер, что позволяет использовать его в качестве альтернативы темозоламиду.
Существующие режимы полихимиотерапии повышают частоту ответов на лечение до 30-40 %, но не ассоциированы с увеличением выживаемости больных. В связи с выраженной токсичностью режимы полихимиотерапии целесообразно применять при резистентности опухоли к препаратам, используемым в монорежимах.
В лечении метастатической меланомы помимо химиотерапевтических могут применяться режимы биохимиотерапии. Аналогично ситуации с химиотерапией, нет доказательств того, что биохимиотерапия с использованием рекомбинантных цитокинов способна привести к увеличению продолжительности жизни, однако сравнительно лучшая переносимость при аналогичной клинической эффективности обусловили ее достаточно широкое распространение. В биохимиотерапии могут применяться различные комбинации химиопрепаратов с рекомбинантными цитокинами - как α-интерферонами, так и интерлейкином-2.
Применение рекомбинантных цитокинов в монорежимах при метастатической меланоме редко сопровождается выраженным клиническим ответом, однако в отдельных случаях такие монорежимы могут применяться в качестве альтернативы химиотерапии.
НАБЛЮДЕНИЕ
С учетом высокого риска прогрессирования заболевания на стадиях IIB и выше, а также того, что и на ранних стадиях возможно появление регионарных и отдаленных метастазов после иссечения первичной опухоли, всем больным с подтвержденным диагнозом меланомы кожи показано наблюдение у онколога по определенному алгоритму.
1. В первые 2 года, когда риск прогрессирования заболевания наиболее высок, всех больных онколог должен осматривать 1 раз в 3 мес. С проведением:
• осмотра кожных покровов, включая область послеоперационного рубца и его пальпации;
• пальпации периферических лимфатических узлов, по возможности - УЗ-регионарных лимфатических узлов;
• по показаниям - исследования органов брюшной полости, грудной клетки (УЗИ, рентгенография, РКТ), головного мозга (МРТ или РКТ с контрастированием при появлении неврологической симптоматики).
2. В последующие 3 года, до достижения 5-летнего периода после операции, обследование проводится 1 раз в полгода; процедуры обследования аналогичны таковым в первые 2 года. По достижении 5-летнего срока больные с толщиной первичной опухоли <1,5 мм могут дальше не проходить регулярных обследований, однако должны быть должным способом информированы о возможном прогрессировании заболевания и необходимости самообследования кожных покровов и периферических лимфатических узлов, а также о необходимости обращения к онкологу при появлении каких-то новых симптомов.
3. Больным с опухолью толщиной 1,5 мм и больше после 5 лет показано наблюдение 1 раз в полгода в течение еще 5 лет, до достижения 10-летнего периода от момента операции.
Все пациенты с меланомой кожи, а также здоровые люди с синдромом множественных диспластических невусов должны быть информированы об опасности инсоляции, обучены методикам самообследования кожи и периферических лимфатических узлов.
Вопросы для самоконтроля
1. Назовите особенности эпидемиологии меланом.
2. Какие факторы, способствующие малигнизации пигментных невусов, вы знаете?
3. Назовите меры профилактики меланомы.
4. Охарактеризуйте особенности роста и метастазирования меланом.
5. Приведите классификацию меланомы по стадиям.
6. Охарактеризуйте клиническую картину меланомы.
7. Какие признаки малигнизации невусов вы знаете?
8. Каков стандартный объем диагностического исследования при выявлении кожного образования, подозрительного на меланому?
9. Какие методы специального обследования применяются при диагностике меланомы?
10. Как проводится лечение меланомы?
11. Укажите отдаленные результаты лечения меланомы.