Гистология, эмбриология, цитология : учебник / Ю. И. Афанасьев, Н. А. Юрина, Е. Ф. Котовский и др.. - 6-е изд., перераб. и доп. - 2012. - 800 с. : ил.
|
|
|
|
Глава 8. СОЕДИНИТЕЛЬНЫЕ ТКАНИ
Соединительные ткани - это большая группа тканей производных мезенхимы, как правило, полидифферонные и с преобладанием межклеточного вещества (волокнистых структур и аморфного компонента), участвующие в поддержании постоянства состава внутренней среды организма.
Соединительная ткань составляет более 50 % массы тела человека. Она участвует в формировании стромы органов, прослоек между другими тканями, дермы кожи, скелета. Полифункциональный характер соединительных тканей определяется сложностью их состава и организации.
Функции соединительных тканей. Соединительные ткани выполняют различные функции: трофическую, защитную, опорную (биомеханическую), пластическую, морфогенетическую. Трофическая функция в широком смысле этого слова связана с регуляцией питания различных тканевых структур, с участием в обмене веществ и поддержанием постоянства состава внутренней среды организма. В реализации этой функции главную роль играет основное вещество, через которое осуществляется транспорт воды, солей, молекул питательных веществ, - интегративно-буферная среда. Защитная функция заключается в предохранении организма от нефизиологических механических воздействий (повреждений) и обезвреживании чужеродных веществ, поступающих извне или образующихся внутри организма. Это обеспечивается физической защитой (костной тканью), а также фагоцитарной деятельностью макрофагов и иммунокомпе-тентными клетками, участвующими в реакциях клеточного и гуморального иммунитета. Опорная (биомеханическая) функция обеспечивается прежде всего коллагеновыми и эластическими волокнами, образующими волокнистые основы всех органов, составом и физико-химическими свойствами межклеточного вещества скелетных тканей (минерализацией). Чем плотнее межклеточное вещество, тем значительнее опорная, биомеханическая функция. Пластическая функция соединительной ткани выражается в адаптации к меняющимся условиям существования, регенерации, участии в замещении дефектов органов при их повреждении. Морфогенетическая
(структурообразовательная) функция проявляется формированием тканевых комплексов и обеспечением общей структурной организации органов (образование капсул, внутриорганных перегородок), регулирующим влиянием некоторых ее компонентов на пролиферацию и дифференцировку клеток различных тканей.
Классификация соединительных тканей. Разновидности соединительной ткани различаются по составу и соотношению клеточных дифферонов, волокон, а также по физико-химическим свойствам аморфного межклеточного вещества. Соединительные ткани подразделяются на собственно соединительную ткань (рыхлая соединительная ткань и соединительные ткани со специальными свойствами) и скелетные ткани. Последние, в свою очередь, подразделяются на три разновидности хрящевой ткани (гиалиновая, эластическая, волокнистая), две разновидности костной ткани (ретикулофиброзная и пластинчатая), а также цемент и дентин зуба (схема 8.1).
Гистогенез соединительных тканей. Источником развития соединительных тканей является мезенхима (от греч. mesos - средний, enchima - заполняющая масса). Это один из эмбриональных зачатков (по некоторым представлениям - эмбриональная ткань), представляющий собой разрыхленную честь среднего зародышевого листка. Клеточные элементы мезенхимы образуются в процессе дифференцировки дерматома, склеро-тома, висцерального и париетального листков спланхнотома. Кроме того, существует эктомезенхима (нейромезенхима), развивающаяся из нервного гребня (ганглиозной пластинки). По мере развития зародыша в мезенхиму мигрируют клетки иного происхождения из других эмбриональных
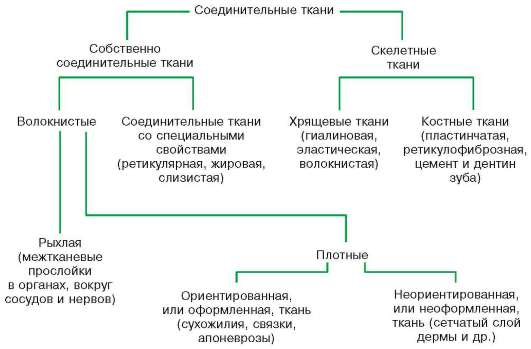
Схема 8.1. Классификация соединительных тканей
зачатков, например клетки нейробластического дифферона, миобласты из закладки скелетных мышц, пигментоциты и др.
Следовательно, с определенной стадии развития зародыша мезенхима представляет собой мозаику клеток, возникших из разных зародышевых листков и эмбриональных зачатков тканей. Однако морфологически все клетки мезенхимы мало чем отличаются друг от друга, и только очень чувствительные методы исследования (как правило, иммуноцитохимические, электронно-микроскопические) выявляют в составе мезенхимы клетки различной природы. Мезенхима существует только в эмбриональном периоде развития человека. После рождения в организме человека сохраняются лишь малодифференцированные (полипотентные) клетки в составе рыхлой волокнистой соединительной ткани (адвентициальные клетки), которые могут дивергентно дифференцироваться в различных направлениях, но в пределах определенной тканевой системы.
Различают эмбриональный и постэмбриональный гистогенез соединительных тканей. В процессе эмбрионального гистогенеза мезенхима приобретает черты тканевого строения раньше закладки других тканей. Этот процесс в различных органах и системах происходит неодинаково и зависит от их неодинаковой физиологической значимости на различных этапах эмбриогенеза. В дифференцировке мезенхимы отмечаются топографическая асин-хронность как в зародыше, так и во внезародышевых органах, высокие темпы размножения клеток и волокнообразования. Постэмбриональный гистогенез в нормальных физиологических условиях происходит медленнее и направлен на поддержание тканевого гомеостаза, пролиферацию малодифференциро-ванных клеток и замену ими отмирающих клеток. Существенную роль в этих процессах играют межклеточные внутритканевые взаимодействия, индуцирующие и ингибирующие факторы (интегрины, межклеточные адгезивные факторы, функциональные нагрузки, гормоны, оксигенация, наличие мало-дифференцированных клеток).
Общие принципы организации соединительных тканей. Главными компонентами соединительных тканей являются производные клеток - волокнистые структуры коллагенового и эластического типов, основное (аморфное) вещество, играющее роль интегративно-буферной метаболической среды, и клеточные элементы, создающие и поддерживающие количественное и качественное соотношение состава неклеточных компонентов.
Органная специфичность клеточных элементов соединительной ткани выражается в количестве, форме и соотношении различных видов клеток, их метаболизме и функциях, оптимально приспособленных к функции органа. Специфичность клеточных элементов проявляется также их взаимодействием между собой (индивидуально расположенные, клеточные ассоциации), особенностями их внутреннего строения (состав органелл, структура ядра, наличие ферментов и др.). Специфика соединительной ткани обнаруживается и в соотношении клеток различных дифферонов и неклеточных структур в различных участках тела. В рыхлой волокнистой соединительной ткани превалируют клетки различных дифферонов и аморфное вещество над волокнами, а в плотной соединительной ткани - наоборот, основную ее массу составляют волокна.
8.1. СОБСТВЕННО СОЕДИНИТЕЛЬНАЯ ТКАНЬ
8.1.1. Волокнистые соединительные ткани
Рыхлая соединительная ткань
Рыхлая соединительная ткань (textus connectivus laxus) обнаруживается во всех органах, так как она сопровождает кровеносные и лимфатические сосуды и образует строму многих органов. Несмотря на наличие органных особенностей, строение рыхлой соединительной ткани в различных органах имеет сходство. Она состоит из клеток различной гистогенетической детерминации и межклеточного вещества (рис. 8.1).
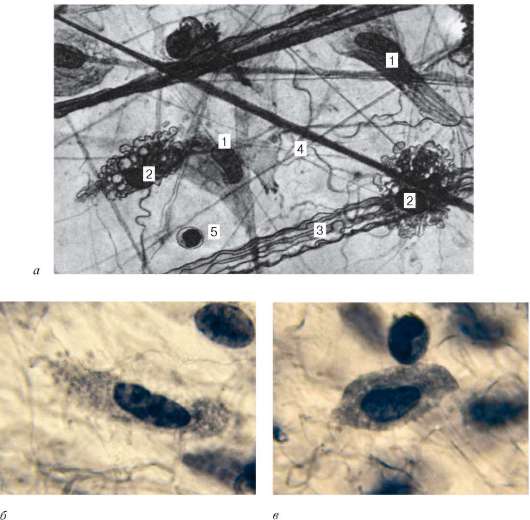
Рис. 8.1. Рыхлая соединительная ткань:
а - пленочный препарат: 1 - фибробласт; 2 - макрофаги; 3 - коллагеновые волокна; 4 - эластические волокна; 5 - лимфоцит; б - фибробласт; в - макрофаг
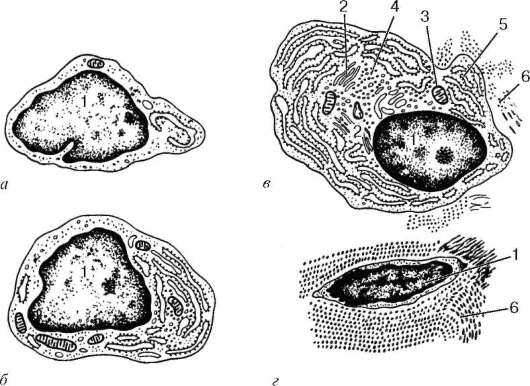
Рис. 8.2. Ультрамикроскопическое строение фибробласта на разных стадиях дифференцировки (по Н. А. Юриной и А. И. Радостиной, с изменениями): Фибробласты: а - малодифференцированный; б - молодой; в - зрелый; г - фиброцит. 1 - ядро; 2 - комплекс Гольджи; 3 - митохондрии; 4 - рибосомы и полирибосомы; 5 - гранулярная эндоплазматическая сеть; 6 - коллагеновые фибриллы
Клетки
Основными клетками соединительной ткани являются фибробласты (семейство фибриллообразующих клеток), макрофаги (семейство), тучные клетки, адвентициальные клетки, плазматические клетки, перициты, жировые клетки, а также лейкоциты, мигрирующие из крови; иногда пигментные
клетки.
Фибробласты (от лат. fibra - волокно, греч. blastos - росток, зачаток) - клетки, синтезирующие компоненты межклеточного вещества: белки (коллаген, эластин), протеогликаны, гликопротеины (см. рис. 8.1; рис. 8.2, 8.3).
Среди мезенхимных клеток имеются стволовые клетки, дающие начало дифферону фибробластов: стволовые клетки, полустволовые клетки-предшественники, малодифференцированные (малоспециализированные), дифференцированные фибробласты (зрелые, активно функционирующие), фиброциты (дефинитивные - конечные формы клеток), а также миофиб-робласты и фиброкласты. С главной функцией фибробластов связаны образование основного вещества и волокон, заживление ран, развитие грануляционной ткани, образование соединительнотканной капсулы вокруг инородного тела и др. Морфологически в этом диффероне можно идентифицировать только клетки, начиная с малодифференцированного фибробласта. Последние - малоотростчатые клетки с округлым или овальным ядром и небольшим ядрышком, базофильной цитоплазмой, богатой РНК. Размер клеток не превышает 20-25 мкм. В цитоплазме этих клеток обнаруживается
большое количество свободных рибосом (см. рис. 8.2). Эндоплазматическая сеть и митохондрии развиты слабо. Комплекс Гольджи представлен скоплениями коротких трубочек и пузырьков.
Авторадиографически показано, что на этой стадии цитогенеза фибробласты обладают очень низким уровнем синтеза и секреции белка. Эти фибробласты способны к размножению митотическим путем.
Дифференцированные зрелые фибробласты крупнее по размеру и в распластанном виде на пленочных препаратах могут достигать 40-50 мкм и более (см. рис. 8.1). Это активно функционирующие клетки. Ядра у них светлые, овальные, содержат 1-2 крупных ядрышка; цитоплазма базофильна, с хорошо развитой гранулярной эндоплазматической сетью, которая местами контактирует с плазмолеммой (см. рис. 8.2, рис. 8.3, а). Комплекс Гольджи распределен в виде цистерн и пузырьков по всей клетке. Митохондрии и лизосомы развиты умеренно.
В цитоплазме фибробластов, особенно в периферической части, располагаются микрофиламенты толщиной 5-6 нм, содержащие белки типа актина и миозина, что обусловливает способность этих клеток к движению. Движение фибробластов становится возможным только после их связывания с опорными фибриллярными структурами (фибрин, соединительнотканные волокна) с помощью фибронектина - гликопротеина, синтезированного фибробластами и другими клетками, обеспечивающего адгезию клеток и неклеточных структур. Во время движения фибробласт уплощается, а его поверхность может увеличиться в 10 раз.
Плазмолемма фибробластов является важной рецепторной зоной, которая опосредует воздействие различных регуляторных факторов. Активизация фибробластов обычно сопровождается накоплением гликогена и повышенной активностью гидролитических ферментов. Энергия, образуемая при метаболизме гликогена, используется для синтеза полипептидов и других компонентов, секретируемых клеткой.
Биосинтез белков коллагена и эластина, протеогликанов, необходимых для формирования основного вещества и волокон, в зрелых фибробластах осуществляется довольно интенсивно, особенно в условиях пониженной концентрации кислорода. Стимулирующими факторами биосинтеза коллагена являются ионы железа, меди, хрома, аскорбиновая кислота. Один из гидролитических ферментов - коллагена-за - расщепляет внутри клеток незрелый коллаген, что, по-видимому, регулирует на клеточном уровне интенсивность секреции коллагена.
По способности синтезировать фибриллярные белки к семейству фибробластов можно отнести ретикулярные клетки ретикулярной соединительной ткани кроветворных органов, хондробласты и остеобласты скелетных разновидностей соединительной ткани.
Фиброциты - дефинитивные формы развития фибробластов. Эти клетки веретенообразные с крыловидными отростками. Они содержат небольшое число органелл, вакуолей, липидов и гликогена. Синтез коллагена и других веществ в фиброцитах резко снижен.
Миофибробласты - клетки, морфологически сходные с фибробластами, сочетающие в себе способность к синтезу не только коллагена, но и сократи-
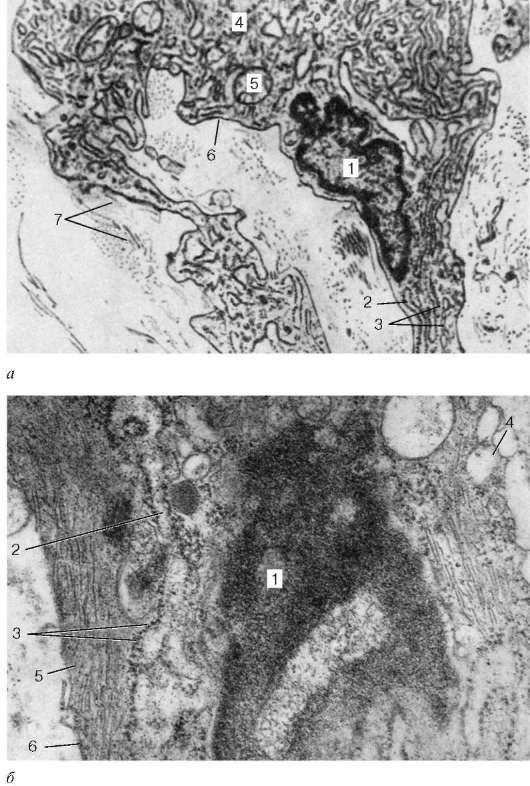
Рис. 8.3. Фибробласт, миофибробласт и фиброкласт:
а - фибробласт (препарат А. И. Радостиной): 1 - ядро; 2 - гранулярная эндоплаз-матическая сеть; 3 - рибосомы; 4 - комплекс Гольджи; 5 - митохондрии; 6 - плаз-молемма; 7 - коллагеновые фибриллы; б - миофибробласт (препарат А. Б. Шехтера): 1 - ядро; 2 - гранулярная эндоплазматическая сеть; 3 - рибосомы; 4 - комплекс Гольджи; 5 - сократительные филаменты; 6 - плазмолемма
тельных белков в значительном количестве (см. рис. 8.3, б). Установлено, что фибробласты могут развиваться в миофибробласты, функционально сходные с гладкими мышечными клетками, но в отличие от последних имеют хорошо развитую эндоплазматическую сеть. Такие клетки наблюдаются в
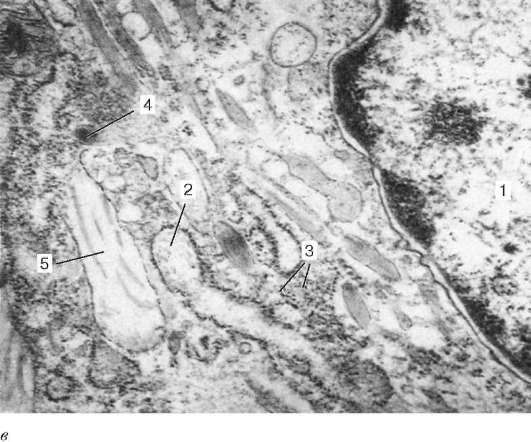
Рис. 8.3. Продолжение:
в - фиброкласт (препарат А. Б. Шехтера): 1 - ядро; 2 - гранулярная эндоплазмати-ческая сеть; 3 - рибосомы; 4 - лизосомы; 5 - фаголизосомы с фрагментами колла-геновых фибрилл. Электронные микрофотографии. Увеличение 20 000
грануляционной ткани в условиях регенерации раневого процесса и в матке при развитии беременности.
Фиброкласты - клетки с высокой фагоцитарной и гидролитической активностью, принимают участие в «рассасывании» межклеточного вещества (см. рис. 8.3, в) в период инволюции органов (например, матки после окончания беременности). Они сочетают в себе структурные признаки фибриллообразующих клеток (развитую гранулярную эндоплазматическую сеть, комплекс Гольджи, относительно крупные, но немногочисленные митохондрии), а также лизосомы с характерными для них гидролитическими ферментами. Выделяемый ими за пределы клетки комплекс ферментов расщепляет цементирующую субстанцию коллагеновых волокон, после чего происходят фагоцитоз и внутриклеточное переваривание коллагена кислыми протеазами лизосом.
Макрофаги (макрофагоциты) (от греч. makros - большой, длинный, fagos - пожирающий) - это гетерогенная специализированная клеточная популяция защитной системы организма. Различают две группы макрофагов - свободные и фиксированные. К свободным макрофагам относятся макрофаги рыхлой соединительной ткани, или гистиоциты; макрофаги серозных полостей; макрофаги воспалительных экссудатов; альвеолярные макрофаги легких. Макрофаги способны перемещаться в организме. Группу фиксированных (резидентных) макрофагов составляют макрофаги костного мозга, костной и хрящевой тканей (остеокласты, хондрокласты), селе-
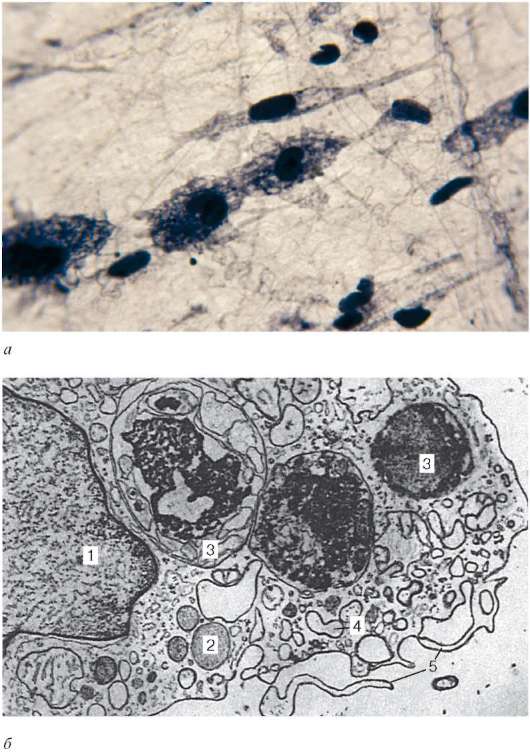
Рис. 8.4. Макрофаги:
а - макрофаги подкожной соединительной ткани крысы (микрофотография, окраска - железный гематоксилин); б - макрофаг (электронная микрофотография; препарат А. И. Радостиной, увеличение 18 000): 1 - ядро; 2 - первичные лизосомы; 3 - вторичные лизосомы; 4 - профили канальцев эндоплазматической сети; 5 - микровыросты периферического слоя цитоплазмы
зенки, лимфатических узлов (дендритные макрофаги), внутриэпидермаль-ные макрофаги (клетки Лангерганса), макрофаги ворсин плаценты (клетки Хофбауэра), макрофаги ЦНС (микроглия).
Размер и форма макрофагов варьируют в зависимости от их функционального состояния (рис. 8.4). Обычно макрофаги, за исключением некоторых их
видов (гигантские клетки инородных тел, хондро- и остеокласты), имеют одно ядро. Ядра макрофагов небольшого размера, округлые, бобовидные или неправильной формы. В них содержатся крупные глыбки хроматина. Цитоплазма базофильна, богата лизосомами, фагосомами (отличительные признаки) и пиноцитозными пузырьками, содержит умеренное количество митохондрий, гранулярную эндоплазматическую сеть, комплекс Гольджи, включения гликогена, липидов и другие (см. рис. 8.4, б). В цитоплазме макрофагов выделяют «клеточную периферию», обеспечивающую макрофагу способность передвигаться, втягивать микровыросты цитоплазмы, осуществлять эндо- и экзоци-тоз. Непосредственно под плазмолеммой находится сеть актиновых филамен-тов диаметром 5-6 нм. Через эту сеть проходят микротрубочки диаметром 20 нм, которые прикрепляются к плазмолемме. Микротрубочки направлены радиально от клеточного центра к периферии клетки и играют важную роль во внутриклеточных перемещениях лизосом, микропиноцитозных везикул и других структур. На поверхности плазмолеммы имеются рецепторы для опухолевых клеток и эритроцитов, Т- и В-лимфоцитов, антигенов, иммуноглобулинов, гормонов. Наличие рецепторов иммуноглобулинов обусловливает участие макрофагов в иммунных реакциях (см. главу 14).
Формы проявления защитной функции макрофагов: 1) поглощение и дальнейшее расщепление или изоляция чужеродного материала; 2) обезвреживание его при непосредственном контакте; 3) передача информации о чужеродном материале иммунокомпетентным клеткам, способным его нейтрализовать; 4) оказание стимулирующего воздействия на другую клеточную популяцию защитной системы организма. Макрофаги имеют орга-неллы, синтезирующие ферменты для внутриклеточного и внеклеточного расщепления чужеродного материала, антибактериальные и другие биологически активные вещества (протеазы, кислые гидролазы, пироген, интерферон, лизоцим и др.).
Количество макрофагов и их активность особенно возрастают при воспалительных процессах. Макрофаги вырабатывают хемотаксические факторы для лейкоцитов. Секретируемый макрофагами ИЛ-1 способен повышать адгезию лейкоцитов к эндотелию, секрецию лизосомных ферментов ней-трофилами и их цитотоксичность, активирует синтез ДНК в лимфоцитах. Макрофаги вырабатывают факторы, активирующие выработку иммуноглобулинов В-лимфоцитами, дифференцировку Т- и В-лимфоцитов; цитоли-тические противоопухолевые факторы, а также факторы роста, влияющие на размножение и дифференцировку клеток собственной популяции, стимулируют функцию фибробластов (см. главу 14).
Контакт макрофагов с антигенами резко усиливает расход глюкозы, липидный обмен и фагоцитарную активность.
Макрофаги образуются из СКК, а также из промоноцита и моноцита (см. рис. 7.15). Полное обновление макрофагов рыхлой волокнистой соединительной ткани у экспериментальных животных осуществляется примерно в 10 раз быстрее, чем фибробластов.
Одной из разновидностей макрофагов являются многоядерные гигантские клетки, которые раньше называли «гигантскими клетками инород-
ных тел», так как они могут формироваться, в частности, в присутствии инородного тела. Многоядерные гигантские клетки содержат 10-20 ядер и более, возникают либо путем слияния одноядерных макрофагов, либо путем эндомитоза без цитотомии. По данным электронной микроскопии, в многоядерных гигантских клетках присутствуют синтетический и секреторный аппарат и большое количество лизосом. Плазмолемма образует многочисленные складки.
Понятие о макрофагической системе. К этой системе относятся макрофаги (гистиоциты) рыхлой волокнистой соединительной ткани, звездчатые клетки синусоидных сосудов печени, свободные и фиксированные макрофаги кроветворных органов (костного мозга, селезенки, лимфатических узлов), макрофаги легкого, воспалительных экссудатов (перитонеальные макрофаги), остеокласты, гигантские клетки инородных тел и глиальные макрофаги нервной ткани (микроглия). Все они активные фагоциты. Фагоцитированный материал подвергается внутри клетки ферментативному расщеплению («завершенный фагоцитоз»), благодаря чему ликвидируются вредные для организма агенты, возникающие местно или проникающие извне. Клетки имеют на своей поверхности рецепторы иммуноглобулинов и возникают из промоноци-тов костного мозга и моноцитов крови. В отличие от таких «профессиональных» фагоцитов способностью к факультативному поглощению обладают фибробласты, ретикулярные клетки, эндотелиоциты, нейтро-фильные гранулоциты и др. Но эти клетки не входят в состав макро-фагической системы.
И. И. Мечников первым пришел к мысли о том, что фагоцитоз, возникающий в процессе эволюции как форма внутриклеточного пищеварения и закрепившийся за многими клетками, одновременно является важным защитным механизмом. Он обосновал целесообразность объединения их в одну систему и предложил назвать ее макрофагиче-ской. Макрофагическая система представляет собой мощный защитный аппарат, принимающий участие как в общих, так и в местных защитных реакциях организма. В целостном организме макрофагиче-ская система регулируется как местными механизмами, так и нервной и эндокринной системами.
В 1930-1940-х гг. эту защитную систему называли ретикулоэндоте-лиальной. В последнее время ее называют системой мононуклеарных фагоцитов, что, однако, неточно характеризует ее в связи с тем, что среди клеток, входящих в эту систему, есть и многоядерные (остеокласты).
Тучные клетки (мастоциты, тканевые базофилы, лаброциты). Этими терминами называют клетки, в цитоплазме которых находится специфическая зернистость, напоминающая гранулы базофильных гранулоцитов. Тучные клетки принимают участие в понижении свертывания крови, повышении проницаемости гематотканевого барьера, в процессе воспаления, иммуно-
генеза и др. У человека тучные клетки обнаруживаются всюду, где имеются прослойки рыхлой соединительной ткани. Особенно много тучных клеток в стенке органов пищеварительного тракта, матке, молочной железе, тимусе, миндалинах. Они часто располагаются группами по ходу кровеносных сосудов микроциркуляторного русла - капилляров, артериол, венул и мелких лимфатических сосудов (рис. 8.5, а).
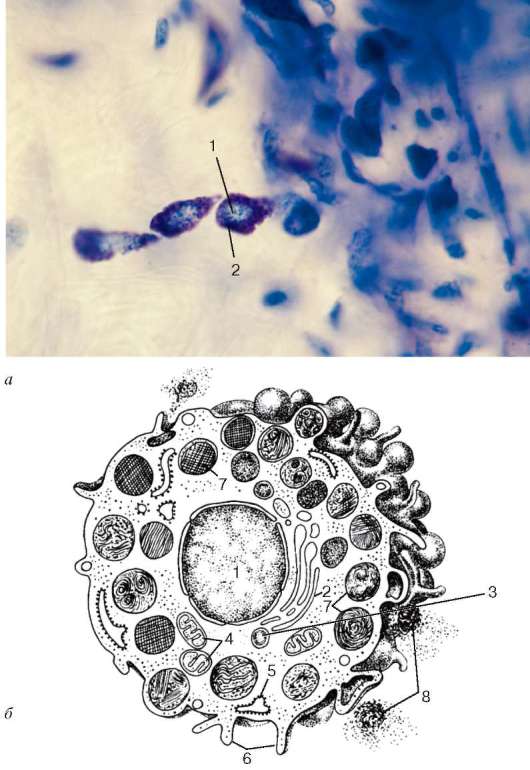
Рис. 8.5. Тучные клетки: а - в подкожной соединительной ткани (микрофотография): 1 - ядро; 2 - мета-хроматические гранулы в цитоплазме; б - схема ультрамикроскопического строения (по Ю. И. Афанасьеву): 1 - ядро; 2 - комплекс Гольджи; 3 - лизосома; 4 - митохондрии; 5 - эндоплазматическая сеть; 6 - микроворсинки; 7 - гетерогенные гранулы; 8 - секреторные гранулы в межклеточном веществе
Форма тучных клеток разнообразна. Клетки могут быть неправильной формы, овальными. Иногда эти клетки имеют короткие широкие отростки, что обусловлено способностью их к амебоидным движениям. У человека ширина таких клеток колеблется от 4 до 14 мкм, длина до 22 мкм. Ядра клеток сравнительно невелики, обычно круглой или овальной формы с плотно расположенным хроматином. В цитоплазме имеются многочисленные гранулы. Величина, состав и количество гранул варьируют. Их диаметр около 0,3-1 мкм (рис. 8.5, б). Меньшая часть гранул представляет собой ортохроматически окрашивающиеся азурофильные лизосомы. Большинство гранул отличаются метахромазией, содержат гепарин, хондроитинсерные кислоты типа А и С, гиалуроновую кислоту, гистамин, серотонин. Гранулы имеют сетчатое, пластинчатое, кристаллоидное и смешанное строение.
Органеллы тучных клеток (митохондрии, комплекс Гольджи, эндоплаз-матическая сеть) развиты слабо. В цитоплазме обнаружены различные ферменты: протеазы, липазы, кислая и щелочная фосфатазы, пероксидаза, цитохромоксидаза, АТФ-аза и др. Однако маркерным ферментом следует считать гистидиндекарбоксилазу, с помощью которой осуществляется синтез гистамина из гистидина.
Тучные клетки способны к секреции и выбросу своих гранул. Дегрануляция тучных клеток может происходить в ответ на любое изменение физиологических условий и действие патогенов. Однако выход биогенных аминов из тучной клетки может происходить и путем секреции растворимых компонентов (секреция гистамина). Гистамин немедленно вызывает расширение кровеносных капилляров и повышает их проницаемость, что проявляется локальными отеками. Он обладает также гипотензивным свойством и является важным медиатором воспаления.
Гистамин выступает как антагонист гепарина, который снижает проницаемость межклеточного вещества и свертываемость крови, оказывает противовоспалительное влияние.
Количество тучных клеток изменяется в зависимости от физиологических состояний организма: возрастает в матке, молочных железах в период беременности, а в желудке, кишечнике, печени - на высоте пищеварения.
Предшественники тучных клеток происходят из стволовых кроветворных клеток красного костного мозга. Процессы митотического деления тучных клеток наблюдаются крайне редко.
Плазматические клетки (плазмоциты). Эти клетки обеспечивают выработку антител - гамма-глобулинов (белки) при появлении в организме антигена. Они образуются в лимфоидных органах из В-лимфоцитов (см. главу 14), обычно встречаются в рыхлой соединительной ткани собственной пластинки слизистых оболочек полых органов, сальнике, интерстициальной соединительной ткани различных желез (молочных, слюнных и др.), лимфатических узлах, селезенке, костном мозге и др.
Величина плазмоцитов колеблется от 7 до 10 мкм. Форма клеток круглая или овальная. Ядра относительно небольшие, круглой или овальной формы, расположены эксцентрично. Цитоплазма резко базофильна, содержит хорошо развитую концентрически расположенную гранулярную эндоплазма-
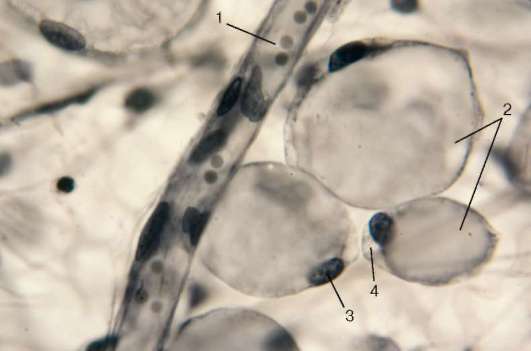
Рис. 8.6. Адипоциты:
1 - капилляр; 2 - липидные включения; 3 - ядро; 4 - цитоплазма (микрофотография). Окраска - железный гематоксилин
тическую сеть, в которой синтезируются белки (антитела). Базофилия отсутствует только в небольшой светлой зоне цитоплазмы около ядра, образующей так называемую сферу или дворик. Здесь располагаются центриоли и комплекс Гольджи. Иногда обнаруживаются скопления иммуноглобулинов в виде оксифильных телец Русселя.
Для плазматических клеток характерна высокая скорость синтеза и секреции антител, что отличает их от своих предшественников. Хорошо развитый секреторный аппарат позволяет синтезировать и секретировать несколько тысяч молекул иммуноглобулинов в секунду. Количество плаз-моцитов увеличивается при различных инфекционно-аллергических и воспалительных заболеваниях.
Адипоциты (жировые клетки). Так называют клетки, которые обладают способностью накапливать в больших количествах резервный жир, принимающий участие в трофике, энергообразовании и метаболизме воды. Адипоциты располагаются группами, реже поодиночке и, как правило, около кровеносных сосудов. Накапливаясь в больших количествах, эти клетки образуют жировую ткань (белую или бурую) (см. ниже).
Форма одиночно расположенных жировых клеток шаровидная. Зрелая жировая клетка обычно содержит одну большую каплю нейтрального жира (триглицеридов), занимающую всю центральную часть клетки и окруженную тонким цитоплазматическим ободком, в утолщенной части которого лежит ядро (рис. 8.6). Кроме того, в цитоплазме адипоцитов имеется небольшое количество других липидов: холестерина, фосфолипидов, свободных жирных кислот и др. Липиды хорошо окрашиваются суданом III в оранжевый цвет или осмиевой кислотой в черный цвет. В прилежащей к ядру цитоплазме, а иногда и в более тонкой противоположной ее части
Рис. 8.7. Пигментоциты в коже (микрофотография). Препарат не окрашен
выявляются палочковидные и нитевидные митохондрии с плотно расположенными кристами. На периферии клетки встречаются многочисленные пиноцитозные пузырьки.
Адипоциты бурой жировой ткани отличаются мелкими липидными включениями и митохондриями, расположенными вокруг ядра. Адипоциты обладают большой способностью к метаболизму. Как количество жировых включений в адипоцитах, так и число самих жировых клеток в рыхлой соединительной ткани подвержено значительным колебаниям.
Функции адипоцитов - трофическая, связанная с обеспечением энергии и резерва воды в организме, а также участие в процессе терморегуляции.
Новые жировые клетки в соединительной ткани взрослого организма могут развиваться при усиленном питании из адвентициальных (камбиальных) клеток, прилегающих к кровеносным капиллярам. При этом в цитоплазме клеток появляются сначала мелкие капельки жира, которые, увеличиваясь в размере, постепенно сливаются в более крупные капли. По мере увеличения жировой капли эндоплазматическая сеть и комплекс Гольджи редуцируются, а ядро сдавливается, уплощается и оттесняется на периферию клетки.
Скопления жировых клеток, встречающихся во многих органах, называют жировой тканью.
Адвентициальные клетки. Это малодифференцированные (камбиальные) клетки, сопровождающие мелкие кровеносные сосуды. Они имеют уплощенную или веретенообразную форму со слабобазофильной цитоплазмой, овальным ядром и небольшим числом органелл. Эти клетки путем дивергентной дифференцировки дают начало различным клеточным дифферонам (фибробластическому, миофибробластическому, адипоцитарному и др.).
Перициты - клетки, окружающие кровеносные капилляры и входящие в состав их стенки (см. главу 13).
Пигментоциты (пигментные клетки, меланоциты). Эти клетки содержат в своей цитоплазме пигмент меланин. Их много в родимых пятнах, а также в соединительной ткани людей черной и желтой рас. Пигментоциты имеют короткие, непостоянной формы отростки (рис. 8.7), большое количество меланосом (гранул меланина) размером 15-25 нм и рибосом. Часть мелано-сом из меланоцитов мигрируют в кератиноциты шиповатого и базального слоев эпидермиса.
В цитоплазме меланоцитов содержатся также биологически активные амины, которые могут принимать участие вместе с тучными клетками в регуляции тонуса стенок сосудов (см. главу 14).
Меланоциты только формально относятся к соединительной ткани, так как располагаются в ней. Что касается их происхождения, то доказано образование этих клеток из стволовых клеток в составе нервных гребней, а не из мезенхимы. Клетки соединительной ткани функционально связаны в единую систему благодаря многочисленным факторам взаимодействия, особенно в процессах воспаления и посттравматической регенерации, при нарушении водно-солевого режима организма и др.
Межклеточное вещество
Межклеточное вещество, или матрикс (substantia intercellularis), соединительной ткани состоит из коллагеновых и эластических волокон, а также из основного (аморфного) вещества. Межклеточное вещество как у зародышей, так и у взрослых образуется, с одной стороны, путем секреции, осуществляемой соединительнотканными клетками, а с другой - из плазмы крови, поступающей в межклеточные пространства.
У зародышей человека образование межклеточного вещества происходит, начиная с 1-2-го мес внутриутробного развития. В течение жизни межклеточное вещество постоянно обновляется.
Коллагеновые структуры, входящие в состав соединительных тканей организмов человека и животных, являются наиболее представительными ее компонентами, образующими сложную организационную иерархию. Основу всей группы коллагеновых структур составляет волок-нис тый белок - коллаген, который определяет свойства коллагеновых структур.
Коллагеновые волокна (fibrae collagenae) в составе разных видов соединительной ткани определяют их прочность. В рыхлой неоформленной соединительной ткани они располагаются в различных направлениях в виде волнообразно изогнутых, спиралевидно скрученных, округлых или уплощенных в сечении тяжей толщиной 1-3 мкм и более. Длина их различна. Внутренняя структура коллагенового волокна определяется фибриллярным белком - коллагеном, который синтезируется на рибосомах гранулярной эндоплазматической сети фибробластов.
Различают около 20 типов коллагена, отличающихся молекулярной организацией, органной и тканевой принадлежностью.
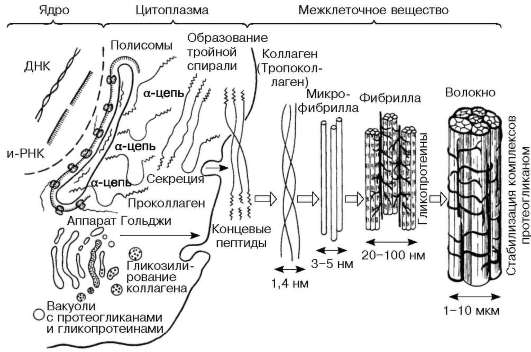
Рис. 8.8. Биосинтез коллагена и фибриллогенез
В организме человека наиболее распространены следующие: коллаген I типа встречается главным образом в соединительной ткани кожи, сухожилиях, кости, роговице глаза, склере, стенке артерий; коллаген II типа входит в состав гиалиновых и фиброзных хрящей, стекловидного тела, роговицы; коллаген III типа находится в дерме кожи плода, в стенках крупных кровеносных сосудов, в ретикулярных волокнах органов кроветворения; IV типа - в базальных мембранах, капсуле хрусталика; V тип коллагена присутствует в хорионе, амнионе, эндомизии, пери-мизии, коже, вокруг клеток (фибробластов, эндотелиальных, гладкомышечных), синтезирующих коллаген.
Молекулы коллагена имеют длину около 280 нм и ширину 1,4 нм. Они построены из триплетов - трех полипептидных цепочек (α-цепочки) предшественника коллагена - проколлагена, свивающихся еще в клетке в единую спираль. Это первый, молекулярный, уровень организации коллагеново-го волокна. Проколлаген секретируется в межклеточное вещество (рис. 8.8).
Второй, надмолекулярный, уровень - внеклеточной организации колла-генового волокна - представляют собой агрегированные в длину и поперечно связанные с помощью водородных связей молекулы тропоколлаге-на, образующиеся путем отщепления концевых пептидов проколлагена. Сначала образуются протофибриллы, а 5-6 протофибрилл, скрепленных между собой боковыми связями, составляют микрофибриллы толщиной около 5 нм.
При участии гликозаминогликанов, также секретируемых фибробласта-ми, формируется третий, фибриллярный, уровень организации коллагенового волокна. Коллагеновые фибриллы представляют собой поперечно исчерчен-

Рис. 8.9. Коллагеновая фибрилла (препарат Н. П. Омельяненко). П - период. Электронная микрофотография. Увеличение 200 000
ные структуры толщиной в среднем 20-100 нм. Период повторяемости темных и светлых участков 64-67 нм (рис. 8.9, 8.10). Каждая молекула коллагена в параллельных рядах, как полагают, смещена относительно соседней цепи на четверть длины, что служит причиной чередования темных и светлых полос. В темных полосах под электронным микроскопом видны вторичные тонкие поперечные линии, обусловленные расположением полярных аминокислот в молекулах коллагена.
Четвертый, волоконный, уровень организации. Коллагеновое волокно, образующееся путем агрегации фибрилл, имеет толщину 1-10 мкм (в зависимости от топографии). В него входит различное количество фибрилл - от единичных до нескольких десятков. Волокна могут складываться в пучки толщиной до 150 мкм.
Коллагеновые волокна отличаются малой растяжимостью и большой прочностью на разрыв. В воде толщина сухожилия в результате набухания увеличивается на 50 %, а в разбавленных кислотах и щелочах - в 10 раз, но при этом волокно укорачивается на 30 %. Способность к набуханию больше выражена у молодых волокон. При термической обработке в воде коллаге-новые волокна образуют клейкое вещество (греч. kolla - клей), что и дало название этим волокнам.
Разновидностью коллагеновых волокон являются ретикулярные и прекол-лагеновые волокна. Последние представляют собой начальную форму образования коллагеновых волокон в эмбриогенезе и при регенерации. В их состав входят коллаген III типа и повышенное количество углеводов, которые синтезируются ретикулярными клетками органов кроветворения. Они образуют трехмерную сеть - ретикулум, что и обусловило их название.
Эластические волокна. Наличие эластических волокон (fibra elasticae) в соединительной ткани определяет ее эластичность и растяжимость. По прочности эластические волокна уступают коллагеновым. Форма поперечного разреза волокон округлая и уплощенная. В рыхлой соединительной ткани они широко анастомозируют друг с другом. Толщина эластических волокон обычно меньше коллагеновых (0,2-1 мкм), но может достигать нескольких микрометров (например, в выйной связке). В составе эластических волокон различают микрофибриллярный и аморфный компоненты.
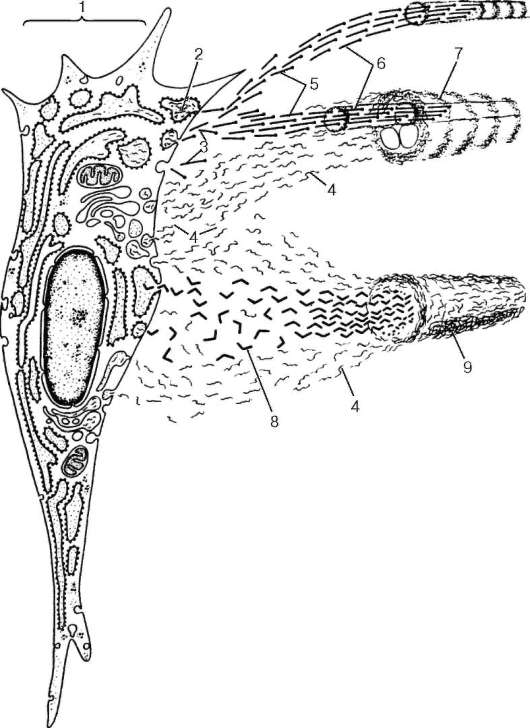
Рис. 8.10. Образование межклеточного вещества (по Р. Крстичу, с изменениями):
1 - фибробласт; 2 - полипептидные цепочки; 3 - молекулы тропоколлагена; 4 - гликозаминогликаны; 5 - полимеризация молекул тропоколлагена; 6 - протофибрилла; 7 - пучок протофибрилл (коллагеновая фибрилла); 8 - молекула эластина; 9 - эластическая фибрилла
Основой эластических волокон является глобулярный гликопротеин - эластин, синтезируемый фибробластами и гладкими мышечными клетками (первый, молекулярный, уровень организации). Для эластина характерны большое содержание пролина и глицина и наличие двух производных аминокислот - десмозина и изодесмозина, которые участвуют в стабилизации молекулярной структуры эластина и придании ему способности к растяжению, эластичности. Молекулы эластина, имеющие глобулы диаметром 2,8 нм, вне клетки соединяются в цепочки - эластиновые протофибрил-лы толщиной 3-3,5 нм (второй, надмолекулярный, уровень организации). Эластиновые протофибриллы в сочетании с гликопротеином (фибрил-лином) образуют микрофибриллы (рис. 8.11) толщиной 8-19 нм (третий, фибриллярный, уровень организации). Четвертый уровень организации -
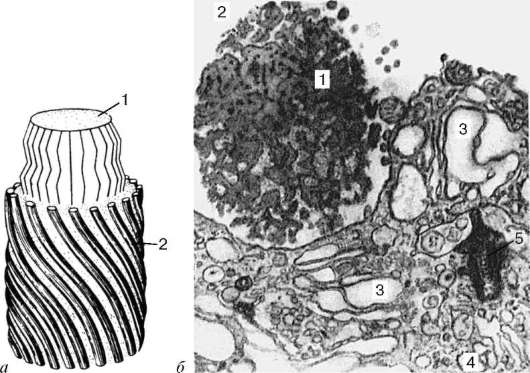
Рис. 8.11. Ультрамикроскопическое строение эластического волокна: а - схема: 1 - центральная гомогенная часть; 2 - микрофибриллы (по Ю. И. Афанасьеву); б - электронная микрофотография, увеличение 45 000 (препарат В. П. Слюсарчука): 1 - центральная гомогенная часть; 2 - микрофибриллы на периферии волокна; 3 - комплекс Гольджи фибробласта; 4 - эндоплазматическая сеть; 5 - центриоль
волоконный. Наиболее зрелые эластические волокна содержат около 90 % аморфного компонента эластического белка (эластина) в центре, а по периферии - микрофибриллы. В эластических волокнах в отличие от коллаге-новых нет структур с поперечной исчерченностью на их протяжении.
Кроме зрелых эластических волокон, различают элауниновые и окситалановые волокна. В элауниновых волокнах соотношение микрофибрилл и аморфного компонента примерно равное, а окситалановые волокна состоят только из микрофибрилл.
Аморфный компонент межклеточного вещества. Клетки и волокна соединительной ткани заключены в аморфный компонент, или основное вещество (substantia fundamentalis). Эта гелеобразная субстанция представляет собой метаболическую, интегративно-буферную многокомпонентную среду, которая окружает клеточные и волокнистые структуры соединительной ткани, нервы и сосуды. В состав компонентов основного вещества входят белки плазмы крови, вода, неорганические ионы, продукты метаболизма клеток, растворимые предшественники коллагена и эластина, протео-гликаны, гликопротеины и комплексы, образованные ими. Все эти вещества находятся в постоянном движении и обновлении (рис. 8.12).
Протеогликаны (ПГ) - белково-углеводные соединения, содержащие 90-95 % углеводов.
Гликозаминогликаны (ГАГ) - полисахаридные соединения, содержащие обычно гексуроновую кислоту с аминосахарами (N-ацетилгликозамин, N-ацетилгалак-
Протеогликан
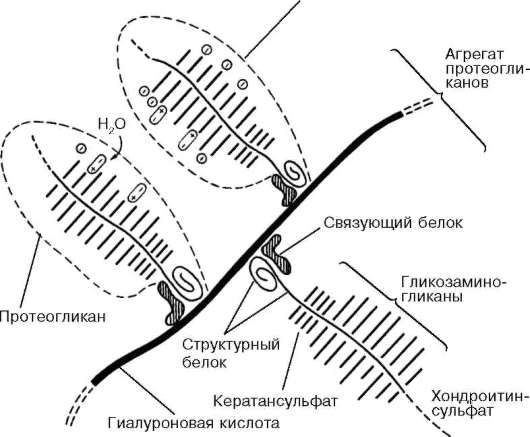
Рис. 8.12. Молекулярная организация аморфного вещества соединительной ткани
тозамин). Молекулы ГАГ содержат много гидроксильных, карбоксильных и сульфатных групп, имеющих отрицательный заряд, легко присоединяют молекулы воды и ионы, в частности Na+, и поэтому определяют гидрофильные свойства ткани. ГАГ проницаемы для кислорода и СО2, но предохраняют органы от проникновения чужеродных тел и белков. ГАГ участвуют в формировании волокнистых структур соединительной ткани и их механических свойствах, репаративных процессах соединительной ткани, в регуляции роста и дифференцировке клеток. Среди этих соединений наиболее распространена в разновидностях соединительной ткани гиа-луроновая кислота, а также сульфатированные ГАГ: хондроитинсульфаты (в хряще, коже, роговице), дерматансульфат (в коже, сухожилиях, в стенке кровеносных сосудов и др.), кератансульфат, гепаринсульфат (в составе многих базальных мембран).
Гепарин - ГАГ, состоящий из глюкуроновой кислоты и гликозамина. В организме человека и животных он вырабатывается тучными клетками, является естественным противосвертывающим фактором крови.
Гликопротеины (ГП) - класс соединений белков с олигосахаридами (гексоза-мины, гексозы, фукозы, сиаловые кислоты), входящими в состав как волокон, так и аморфного вещества. К ним относятся растворимые ГП, связанные с протеогли-канами; ГП кальцинированных тканей; ГП, связанные с коллагеном. ГП играют большую роль в формировании структуры межклеточного вещества соединительной ткани и определяют его функциональные особенности (фибронектин, хондро-нектин, фибриллин, ламинин и др.).
Фибронектин - главный поверхностный ГП фибробласта. В межклеточном пространстве он связан главным образом с интерстициальным коллагеном. Полагают, что фибронектин обусловливает липкость, подвижность, рост и специализацию клеток и др.
Фибриллин формирует микрофибриллы, усиливает связь между внеклеточными компонентами.
Ламинин - компонент базальной мембраны, состоящий из трех полипептидных цепочек, связанных между собой дисульфидными соединениями, а также с коллагеном V типа и поверхностными рецепторами клеток.
Плотные соединительные ткани
Плотные соединительные ткани (textus connectivus compactus) характеризуются относительно большим количеством плотно расположенных волокон и незначительным количеством клеточных элементов и основного аморфного вещества между ними. В зависимости от характера расположения волокнистых структур различают неориентированный (неоформленный), ориентированный (оформленный) и смешанный типы плотной соединительной ткани.
Неориентированный тип ткани характеризуется неупорядоченным расположением волокон (например, дерма кожи). В ориентированном типе ткани расположение волокон строго упорядочено и в каждом случае соответствует тем условиям, в каких функционирует данный орган (сухожилия, связки, фиброзные мембраны). Смешанный тип, как правило, имеет слоистое строение (роговица, склера) с чередованием направлений волокнистых элементов плотной соединительной ткани.
Сухожилие (tendo). Оно состоит из толстых, плотно лежащих параллельных пучков коллагеновых волокон, организованных параллельно. Между этими пучками располагаются фиброциты, называемые сухожильными клетками (tendinocyti), и небольшое количество фибробластов и основного аморфного вещества. Тонкие пластинчатые отростки фиброцитов входят в промежутки между пучками волокон и тесно соприкасаются с ними. Каждый пучок коллагеновых волокон, отделенный от соседнего слоем фиброцитов, называется пучком первого порядка. Несколько пучков первого порядка, окруженных тонкими прослойками рыхлой соединительной ткани, составляют пучки второго порядка. Прослойки рыхлой соединительной ткани, разделяющие пучки второго порядка, называются эндотенонием. Из пучков второго порядка слагаются пучки третьего порядка, разделенные более толстыми прослойками рыхлой соединительной ткани - перитенонием. Иногда пучком третьего порядка является само сухожилие. В крупных сухожилиях могут быть и пучки четвертого порядка.
В перитенонии и эндотенонии проходят кровеносные сосуды, питающие сухожилие, нервы и находятся проприоцептивные нервные окончания, посылающие ЦНС сигналы о состоянии натяжения ткани сухожилий.
К оформленному типу плотной соединительной ткани относится и вый-ная связка, только она образуется из толстых эластических волокон.
Некоторые сухожилия в местах прикрепления к костям заключены во влагалища, построенные из двух волокнистых соединительнотканных оболочек (vagina), между которыми находится жидкость (смазка), богатая гиа-луроновой кислотой.
Фиброзные мембраны. К этим структурам, построенным из плотной соединительной ткани, относят фасции, апоневрозы, сухожильные центры диафрагмы, капсулы некоторых органов, твердую мозговую оболочку, склеру, надхрящницу, надкостницу, а также белочную оболочку яичника и яичка и др. Фиброзные мембраны этой разновидности ткани трудно растяжимы вследствие того, что пучки коллагеновых волокон и лежащие между ними фибробласты и фиброциты располагаются в определенном порядке в несколько слоев друг над другом. В каждом слое волнообразно изогнутые пучки коллагеновых волокон идут параллельно друг другу в одном направлении, не совпадающем с направлением в соседних слоях (соединительная ткань, организованная параллельно в разных направлениях). Отдельные пучки волокон переходят из одного слоя в другой, связывая их между собой. Кроме пучков коллагеновых волокон, в фиброзных мембранах есть эластические волокна. Такие фиброзные структуры, как надкостница, склера, белочная оболочка яичка, капсулы суставов и другие, характеризуются менее правильным расположением пучков коллагеновых волокон и большим количеством эластических волокон по сравнению с апоневрозами.
8.1.2. Соединительные ткани со специальными свойствами
К таким тканям относят ретикулярную, жировую и слизистую. Они характеризуются преобладанием однородных клеток, с которыми обычно связано само название этих разновидностей соединительной ткани.
Ретикулярная ткань
Ретикулярная ткань (textus reticularis) является разновидностью соединительной ткани, имеет сетевидное строение и состоит из отростчатых ретикулярных клеток и ретикулярных (аргирофильных) волокон (рис. 8.13). Большинство ретикулярных клеток связаны с ретикулярными волокнами и стыкуются друг с другом отростками, образуя трехмерную сеть. Ретикулярная ткань образует строму кроветворных органов и микроокружение для развивающихся в них клеток крови.
Ретикулярные волокна (диаметр 0,5-2 мкм) - продукт синтеза ретикулярных клеток. Они обнаруживаются при импрегнации солями серебра, поэтому называются еще аргирофильными (от греч. argentum - серебро). Эти волокна устойчивы к действию слабых кислот и щелочей и не перевариваются трипсином.
В группе аргирофильных волокон различают собственно ретикулярные и преколлагеновые волокна. Собственно ретикулярные волокна - дефинитивные, окончательные образования, содержащие коллаген III типа. Ретикулярные волокна по сравнению с коллагеновыми содержат в высокой концентрации серу, липиды и углеводы. В электронный микроскоп фибриллы ретикулярных волокон имеют не всегда отчетливо выраженную исчерченность с периодом 64-67 нм. По растяжимости эти волокна занима-
ют промежуточное положение между коллагеновыми и эластическими. Преколлагеновые волокна представляют собой начальную форму образования коллагеновых волокон в эмбриогенезе и при регенерации.
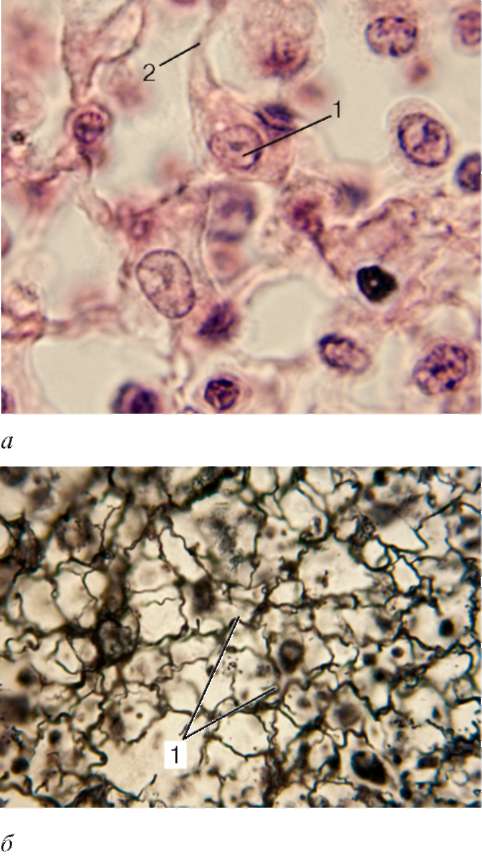
Рис. 8.13. Ретикулярная ткань: а - микрофотография ретикулярных клеток: 1 - ядро ретикулярной клетки; 2 - отростки цитоплазмы; б - микрофотография ретикулярных волокон лимфатического узла: 1 - ретикулярные волокна. Импрегнация нитратом серебра
Жировая ткань
Жировая ткань (textus adiposus) - это скопления жировых клеток, встречающихся во многих органах (см. Адипоциты). Различают две разновидности жировой ткани - белую и бурую. Эти термины условны и отражают особенности окраски клеток. Белая жировая ткань широко распространена в организме человека, а бурая встречается главным образом у новорожденных и у некоторых животных (грызунов и зимоспящих) в течение всей жизни.
Белая жировая ткань у человека располагается под кожей, особенно в нижней части брюшной стенки, на ягодицах и бедрах, где она образует подкожный жировой слой, в сальнике, брыжейке и ретроперитонеальной области. Жировая ткань более или менее отчетливо делится прослойками рыхлой волокнистой соединительной ткани на дольки различных размеров и формы. Жировые клетки внутри долек довольно близко прилегают друг к другу (рис. 8.14). В узких пространствах между ними располагаются фибробласты, лимфоидные элементы, тучные клетки. Между жировыми клетками во всех направлениях ориентированы тонкие колла-геновые волокна. Кровеносные и лимфатические капилляры, располагаясь в прослойках рыхлой волокнистой соединительной ткани, тесно охватывают своими петлями группы жировых клеток или дольки жировой ткани. В жировой ткани происходят активные процессы обмена жирных кислот, углеводов и образование жира из углеводов.
При распаде жиров высвобождается большое количество воды и выделяется энергия, поэтому жировая ткань играет не только роль депо субстратов для синтеза макроэргических соединений, но косвенно и роль депо воды.
Во время голодания подкожная и околопочечная жировая ткань, жировая ткань сальника и брыжейки быстро теряют запасы жира. Капельки липи-
дов внутри клеток измельчаются, и жировые клетки приобретают звездчатую или веретеновидную форму. В области орбиты глаз, в коже ладоней и подошв жировая ткань теряет лишь небольшое количество липидов даже во время продолжительного голодания. Здесь жировая ткань играет преимущественно механическую, а не обменную роль. В этих местах она разделена на мелкие дольки, окруженные соединительнотканными волокнами.
Бурая жировая ткань встречается у новорожденных детей и у некоторых животных на шее, около лопаток, за грудиной, вдоль позвоночника, под кожей и между мышцами. Она состоит из жировых клеток, густо оплетенных гемокапиллярами. Эти клетки принимают участие в процессах теплопродукции. Адипоциты бурой жировой ткани имеют множество мелких жировых включений в цитоплазме (рис. 8.15). По сравнению с клетками белой жировой ткани в них значительно больше митохондрий. Бурый цвет жировым клеткам придают железосодержащие пигменты - цитохромы митохондрий.
Окислительная способность бурых жировых клеток примерно в 20 раз выше белых и почти в 2 раза превышает окислительную способность мышцы сердца. При понижении температуры окружающей среды повышается активность окислительных процессов в бурой жировой ткани. При
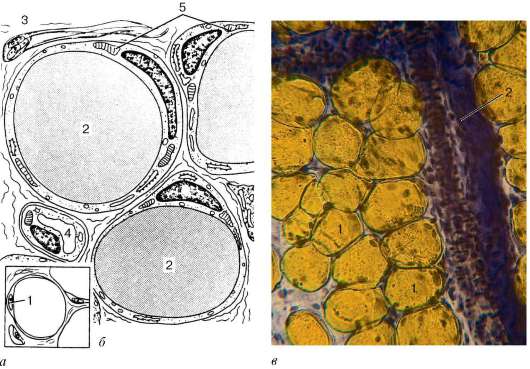
Рис. 8.14. Строение белой жировой ткани (по Ю. И. Афанасьеву): а - адипоциты с удаленным жиром в световом оптическом микроскопе; б - ультрамикроскопическое строение адипоцитов: 1 - ядро адипоцита; 2 - крупные капли липидов; 3 - нервные волокна; 4 - гемокапилляры; 5 - митохондрии адипоцита; в - жировая ткань: 1 - адипоциты; 2 - кровеносный сосуд. Микрофотография (окраска суданом III)
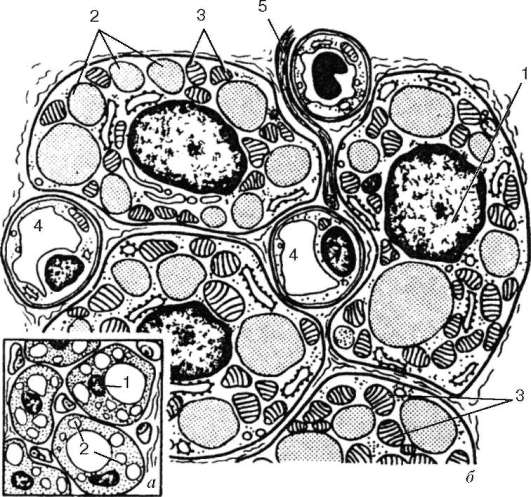
Рис. 8.15. Строение бурой жировой ткани (по Ю. И. Афанасьеву): а - адипоциты с удаленным жиром в световом оптическом микроскопе; б - ультрамикроскопическое строение адипоцитов: 1 - ядро адипоцита; 2 - мелко раздробленные липиды; 3 - многочисленные митохондрии; 4 - гемокапилляры; 5 - нервное волокно
этом выделяется тепловая энергия, обогревающая кровь в кровеносных капиллярах. В регуляции теплообмена определенную роль играют симпатическая нервная система и гормоны мозгового вещества надпочечников - адреналин и норадреналин, которые стимулируют активность тканевой липазы, расщепляющей триглицериды на глицерин и жирные кислоты. Это приводит к высвобождению тепловой энергии, обогревающей кровь, протекающую в многочисленных капиллярах между адипоцитами. При голодании бурая жировая ткань изменяется меньше, чем белая.
Слизистая ткань
Слизистая ткань (textus mucosus) в норме встречается только у зародыша. Классическим объектом для ее изучения является пупочный канатик человеческого плода (рис. 8.16). Клеточные элементы здесь представлены гетерогенной группой клеток, дивергентно дифференцирующихся из мезен-химных клеток на протяжении внутриутробного периода. Среди них различают крупные звездчатой формы фибробласты, миофибробласты, гладкие мышечные клетки. Они отличаются способностью к синтезу виментина, десмина, актина, миозина. Фибробласты слизистой ткани пупочного кана-
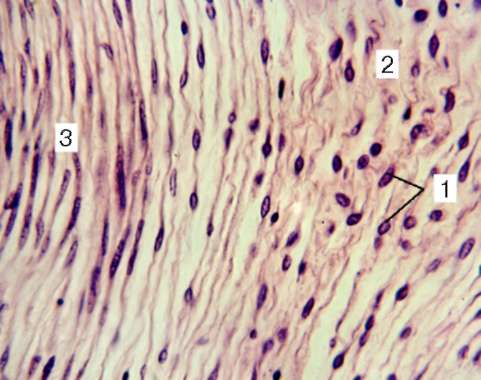
Рис. 8.16. Слизистая соединительная ткань из пупочного канатика: 1 - мукоциты; 2 - межклеточное вещество; 3 - стенка кровеносного сосуда
тика («вартонов студень») синтезируют коллаген IV типа, характерный для базальных мембран, ламинин, гепаринсульфат.
Между клетками этой ткани в первой половине беременности в большом количестве обнаруживается гиа-луроновая кислота, что обусловливает желеобразную консистенцию основного вещества. Фибробласты студенистой соединительной ткани слабо синтезируют фибриллярные белки. Лишь на поздних стадиях развития зародыша в студенистом веществе появляются рыхло расположенные коллагеновые фибриллы.
8.2. СКЕЛЕТНЫЕ ТКАНИ
Скелетные ткани (textus skeletales) - это разновидности соединительной ткани со значительно выраженной опорной, механической функцией, обусловленной наличием плотного межклеточного вещества: хрящевые, костные ткани, дентин и цемент зуба. Помимо главной функции, эти ткани принимают участие в водно-солевом обмене веществ.
8.2.1. Хрящевые ткани
Хрящевые ткани (textus cartilaginei) входят в состав органов дыхательной системы, суставов, межпозвонковых дисков и другого, состоят из клеток - хондроцитов и хондробластов и большого количества межклеточного гидрофильного вещества, отличающегося упругостью. Именно с этим связана опорная функция хрящевых тканей. В свежей хрящевой ткани содержится около 70-80 % воды, 10-15 % органических веществ и 4-7 % солей. От 50 до 70 % сухого вещества хрящевой ткани составляет коллаген. Собственно хрящевая ткань не имеет кровеносных сосудов, а питательные вещества диффундируют из окружающей ее надхрящницы.
Классификация. Различают три вида хрящевой ткани: гиалиновую, эластическую, волокнистую. Такое подразделение хрящевых тканей основано на структурно-функциональных особенностях строения их межклеточного вещества, степени содержания и соотношения коллагеновых и эластических волокон.
Развитие хрящевой ткани (хондрогистогенез)
Источником развития хрящевых тканей является мезенхима. Вначале в некоторых участках тела зародыша, где образуется хрящ, клетки мезенхи-
мы теряют свои отростки, усиленно размножаются и, плотно прилегая друг к другу, создают определенное напряжение - тургор. Такие участки называют хондрогенными зачатками, или хондрогенными островками (рис. 8.17). В их составе находятся стволовые клетки, которые дифференцируются в полустволовые хон-дрогенные клетки. Стволовые клетки характеризуются округлой формой, высоким значением ядерно-цитоплазматических отношений, диффузным расположением хроматина и небольшим ядрышком. Органеллы в этих клетках развиты слабо. В полустволовых клетках (прехондробластах) увеличивается количество свободных рибосом, появляются мембраны эндоплазма-тической сети гранулярного типа, удлиняется форма клеток, уменьшаются ядерно-цитоплазматические отношения. В дальнейшем малодиф-ференцированные предшественники дифференцируются в морфологически идентифицируемые хондробла-сты (см. рис. 8.17).
Хондробласты (от греч. chondros - хрящ, blastos - зачаток) - это молодые уплощенные клетки, способные к пролиферации и синтезу межклеточного вещества хряща (протеогли-канов). Цитоплазма хондробластов имеет хорошо развитую гранулярную и агранулярную эндоплазма-тическую сеть, комплекс Гольджи. При окрашивании цитоплазма хон-дробластов оказывается базофиль-ной в связи с богатым содержанием
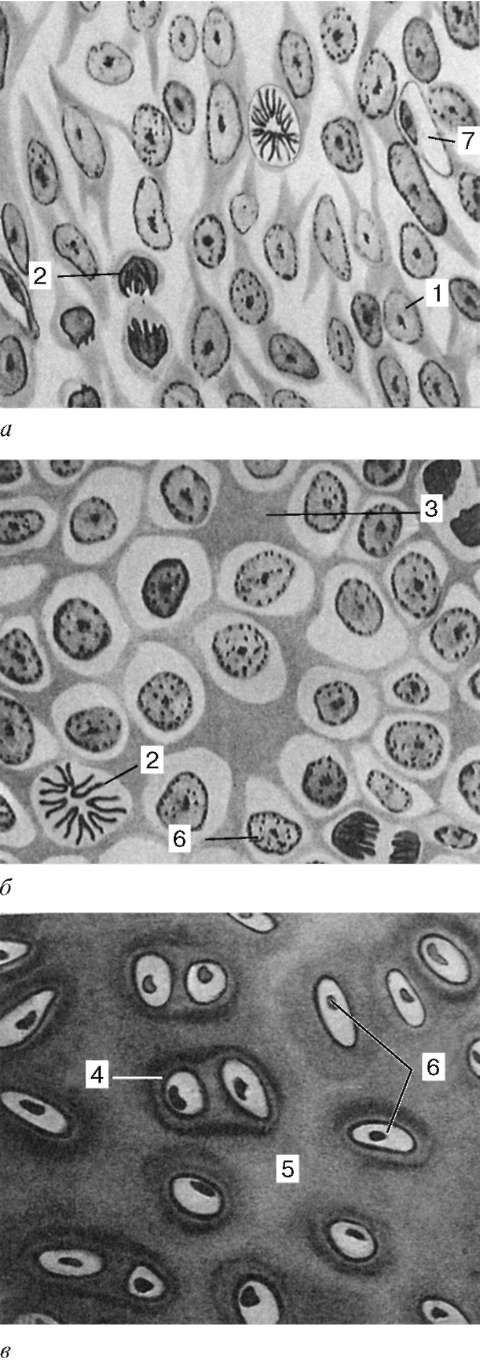
Рис. 8.17. Развитие гиалиновой хрящевой ткани (схема по Ю. И. Афанасьеву): а - хондрогенный островок; б - первичная хрящевая ткань; в - стадии дифференцировки хондроцитов. 1 - мезенхимные клетки; 2 - митотически делящиеся клетки; 3 - межклеточное вещество; 4 - оксифильное межклеточное вещество; 5 - базофильное межклеточное вещество; 6 - молодые хондроциты; 7 - гемокапилляр
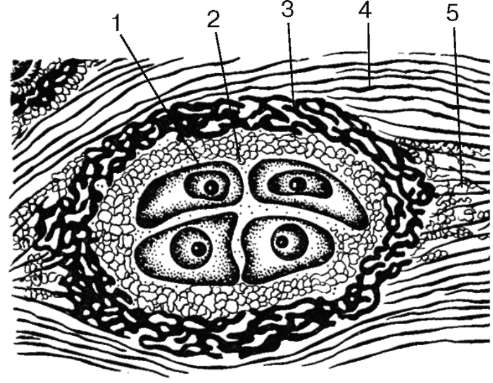
Рис. 8.18. Изогенные группы хрящевых клеток:
1 - хондроцит; 2 - матрикс клеточной территории, состоящий из петлистой сети неколлагеновых белков и протео-гликанов; 3 - коллагеновые волокна, образующие стенку лакуны; 4 - межтерриториальный участок хряща; 5 - проте-огликаны в межтерриториальном матрик-се (по В. Н. Павловой, с изменениями)
РНК. Хондробласты синтезируют и секретируют фибриллярные белки (коллаген), возникает межклеточное вещество, которое окрашивается оксифильно. Так образуется первичная хрящевая ткань. При участии хондробластов происходит периферический (аппозиционный) рост хряща. При дальнейшей дифференцировке хрящевой ткани хондробласты развиваются в хондроциты.
Хондроциты - основной вид клеток хрящевой ткани. Они бывают овальными, круглыми или полигональной формы - в зависимости от степени дифференцировки. Расположены в особых полостях (лакунах) в межклеточном веществе поодиночке или группами. Группы клеток, лежащие в общей полости, называются изогенными (от греч. isos - равный, genesis - развитие). Они образуются путем деления одной клетки (рис. 8.18). В изогенных группах различают три типа хондроцитов.
Первый тип хондроцитов характеризуется высоким ядерно-цитоплазматическим отношением, развитием вакуолярных элементов комплекса Гольджи, наличием митохондрий и свободных рибосом в цитоплазме. В этих клетках нередко наблюдаются фигуры митотического деления, что позволяет рассматривать их как источник возникновения изогенных групп клеток (рис. 8.19). Хондроциты I типа преобладают в молодом, развивающемся хряще. Хондроциты II типа отличаются снижением ядерно-цитоплазматического отношения, ослаблением синтеза ДНК, сохранением высокого уровня РНК, интенсивным развитием гранулярной эндоплазматической сети и всех компонентов комплекса Гольджи, которые обеспечивают образование и секрецию гликозаминогликанов и протеогликанов в межклеточное вещество. Хондроциты III типа отличаются самым низким ядерно-цитоплазматическим отношением, сильным развитием и упорядоченным расположением гранулярной эндо-плазматической сети. Эти клетки сохраняют способность к образованию и секреции белка, но в них снижается синтез гликозаминогликанов.
По мере развития хрящевой закладки на периферии на границе с мезенхимой формируется надхрящница - оболочка, покрывающая развивающийся хрящ снаружи и состоящая из наружного волокнистого и внутреннего хон-дрогенного (камбиального) слоев. В хондрогенной зоне клетки интенсивно делятся, дифференцируются в хондробласты, которые сохраняют способность к синтезу ДНК, размножению, а также к синтезу компонентов межклеточного вещества (коллагена I и III типов). В процессе секреции продуктов синтеза и наслаивания на уже имеющийся хрящ по его периферии сами
клетки «замуровываются» в продукты своей деятельности. Так происходит рост хряща способом наложения, или аппозиционный рост.
Хрящевые клетки, лежащие в центре молодого развивающегося хряща, сохраняют способность в течение некоторого времени делиться митотически, оставаясь в одной лакуне (изогенные группы клеток), и вырабатывать коллаген II типа. За счет увеличения количества этих клеток и выработки ими межклеточного вещества происходит увеличение массы хряща изнутри, что называется интерстициальным ростом. Интерстициальный рост наблюдается в эмбриогенезе, а также при регенерации хрящевой ткани.
При росте и развитии хряща его центральные участки все более отдаляются от близлежащих сосудов и начинают испытывать затруднения в питании, осуществляемом диф-фузно со стороны сосудов надхрящницы. Вследствие этого хондроциты теряют способность размножаться, некоторые из них подвергаются разрушению, а протеогликаны превращаются в более простой оксифиль-ный белок - альбумоид.
Таким образом, хондробласти-ческий дифферон в эмбриональном гистогенезе представлен всеми формами созревающих клеток. Однако в последующем он включает только средние и конечные звенья (хондробласты и хондроциты) и является единственным в хрящевых тканях.
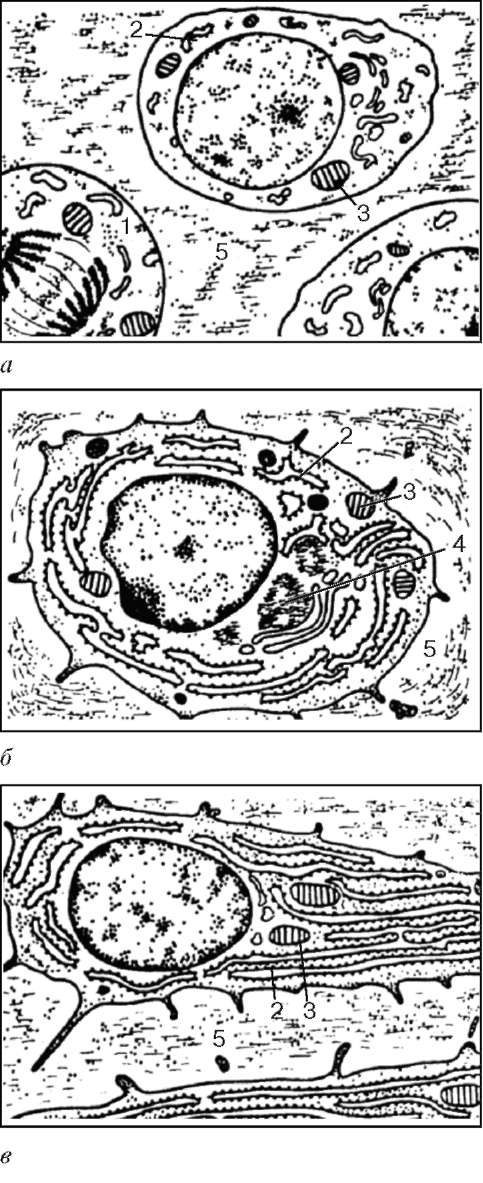
Рис. 8.19. Три типа хондроцитов (по Ю. И. Афанасьеву):
а - I тип; б - II тип; в - III тип. 1 - митотически делящаяся клетка; 2 - эндоплаз-матическая сеть; 3 - митохондрии; 4 - гликоген; 5 - межклеточное вещество
Гиалиновая хрящевая ткань
Гиалиновая хрящевая ткань (textus cartilagineus hyalinus), называемая еще стекловидной (от греч. hyalos - стекло) - в связи с ее прозрачностью и голубовато-белым цветом, является наиболее распространенной разновид-
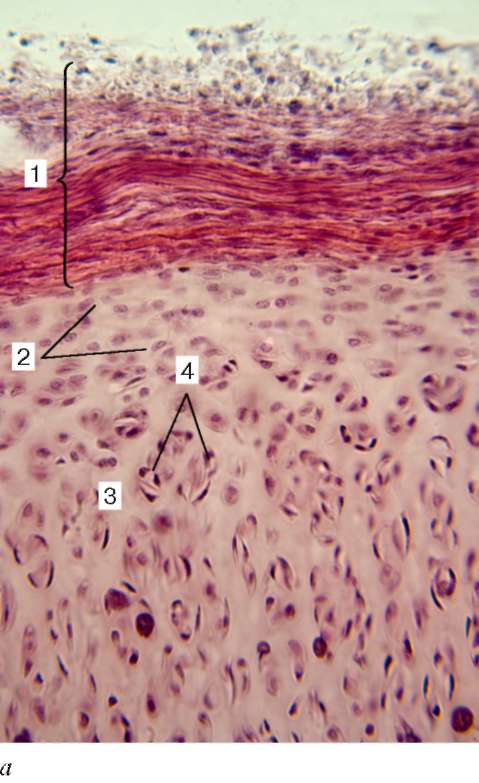
Рис. 8.20. Гиалиновый хрящ: а - микрофотография гиалинового хряща трахеи: 1 - надхрящница; 2 - молодые хондроциты; 3 - основное вещество с расположенными внутри него изогенными группами хондроцитов (4)
ностью хрящевой ткани. Во взрослом организме гиалиновая ткань встречается в местах соединения ребер с грудиной, в гортани, воздухоносных путях, на суставных поверхностях костей.
Гиалиновая хрящевая ткань различных органов имеет много общего, но в то же время различается по органоспецифичности - расположению клеток, строению межклеточного вещества. Большая часть встречающейся в организме человека гиалиновой хрящевой ткани покрыта надхрящницей (perichondrium) и представляет собой анатомические образования - хрящи.
В надхрящнице выделяют два слоя: наружный, состоящий из волокнистой соединительной ткани с кровеносными сосудами; внутренний, преимущественно клеточный, содержащий хондробласты и их предшественники - прехон-дробласты. Под надхрящницей в поверхностном слое располагаются молодые хондроциты веретенообразной формы, длинная ось которых направлена вдоль поверхности хряща (рис. 8.20). В более глубоких слоях хрящевые клетки приобретают овальную или круглую форму. В связи с тем, что синтетические и секреторные процессы у этих клеток ослабляются, они после деления далеко не расходятся, а лежат компактно, образуя так называемые изогенные группы из 2-4 хондроцитов.
Более дифференцированные хрящевые клетки и изогенные группы, кроме оксифильного перицеллюлярного слоя межклеточного вещества, имеют расположенную кнаружи базофильную зону. Эти свойства объясняются неравномерным распределением химических компонентов межклеточного вещества - белков и гликозаминогликанов.
В гиалиновом хряще любой локализации принято различать территориальные участки межклеточного вещества, или матрикса (см. рис. 8.18). К территориальному участку относится матрикс, непосредственно окружающий хрящевые клетки или их группы. В этих участках коллагеновые волокна II типа и фибриллы, извиваясь, окружают изогенные группы хрящевых клеток, предохраняя их от механического давления. В межтерриториаль-
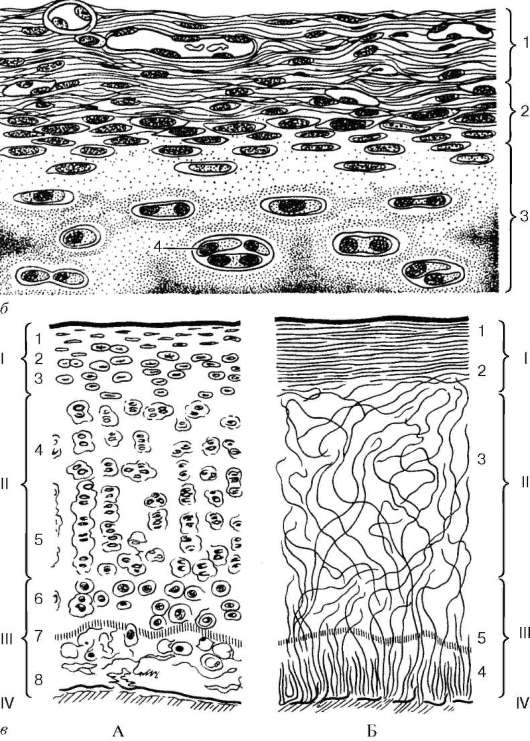
Рис. 8.20. Продолжение
б - схема строения хряща и надхрящницы (рис. Ю. И. Афанасьева): 1 - наружный волокнистый слой; 2 - внутренний клеточный слой; 3 - хрящевая ткань; в - клеточные и волокнистые компоненты суставного хряща (по В. П. Модяеву, В. Н. Павловой, с изменениями). I - поверхностная зона; II - промежуточная зона; III - базальная (глубокая) зона; IV - субхондральная кость; А - клеточные компоненты суставного хряща: 1 - бесклеточная пластинка; 2 - хондроциты тангенциального слоя; 3 - хон-дроциты переходного участка; 4 - изогенные группы; 5 - «колонки» хондроцитов; 6 - гипертрофированные хондроциты; 7 - базофильная (пограничная) линия между кальцинированным и некальцинированным хрящом; 8 - кальцифицирующийся хрящ; Б - фибриллярная система суставного хряща: 1 - бесклеточная пластинка; 2 - тангенциальные волокна поверхностной зоны; 3 - основные направления кол-лагеновых волокон в промежуточной зоне; 4 - радиальные волокна базального слоя; 5 - базофильная (пограничная) линия
ном матриксе коллагеновые волокна ориентированы в направлении вектора действия сил основных нагрузок. Пространство между коллагеновыми структурами заполнено протеогликанами.
В структурной организации межклеточного вещества хряща большую роль играет хондронектин. Этот гликопротеин соединяет клетки между собой и с различными субстратами (коллагеном, гликозаминогликанами). Опорная биомеханическая функция хрящевых тканей при сжатии, растяжении обеспечивается не только строением ее волокнистого каркаса, но и наличием гидрофильных протеогликанов с высоким уровнем гидратации (65-85 %). Высокая гидрофильность межклеточного вещества способствует диффузии питательных веществ, солей. Газы и многие метаболиты также свободно диффундируют через него. Однако крупные белковые молекулы, обладающие антигенными свойствами, не проходят. Этим объясняется успешная трансплантация в клинике (пересадка от одного человека к другому) участков хряща. Метаболизм хон-дроцитов преимущественно анаэробный, гликолитический.
Однако не все хрящи построены одинаково. Структурной особенностью гиалинового хряща суставной поверхности является отсутствие надхрящницы на поверхности, обращенной в полость сустава. Суставной хрящ состоит из трех нечетко разграниченных зон: поверхностной, промежуточной и базальной (см. рис. 8.20, в).
В поверхностной зоне суставного хряща располагаются мелкие уплощенные малоспециализированные хондроциты, напоминающие по строению фиброциты.
В промежуточной зоне клетки более крупные, округлой формы, метаболически очень активные: с крупными митохондриями, хорошо развитой гранулярной эндо-плазматической сетью, комплексом Гольджи с многочисленными пузырьками.
Глубокая (базальная) зона делится базофильной линией на некальцинирую-щийся и кальцинирующийся слои. В последний из подлежащей субхондральной кости проникают кровеносные сосуды. Особенностью межклеточного вещества глубокой зоны суставного хряща является содержание в нем плотных матриксных пузырьков - мембранных структур диаметром от 30 нм до 1 мкм, которые являются локусами инициальной минерализации скелетных тканей (помимо хряща, они обнаруживаются в костной ткани и предентине). Мембранные структуры образуются путем выбухания участка плазмолеммы хондроцита (соответственно остеобласта в костной ткани и одонтобласта в предентине) с последующим отпочковыванием от поверхности клетки и локализованным распределением в зонах минерализации. Они также могут являться продуктом полной дезинтеграции клеток. Питание суставного хряща лишь частично осуществляется из сосудов глубокой зоны, а в основном за счет синовиальной жидкости полости сустава.
Эластическая хрящевая ткань
Эластическая хрящевая ткань (textus cartilagineus elasticus) встречается в тех органах, где хрящевая основа подвергается изгибам (в ушной раковине, рожковидных и клиновидных хрящах гортани и др.). В свежем, нефиксированном состоянии эластическая хрящевая ткань бывает желтоватого цвета и не такая прозрачная, как гиалиновая. По общему плану строения эластический хрящ сходен с гиалиновым. Снаружи он покрыт надхрящницей. Хрящевые клетки (молодые и специализированные хондроциты) располагаются в капсулах поодиночке или образуют изогенные группы. Одним из главных отли-
чительных признаков эластического хряща является наличие в его межклеточном веществе наряду с колла-геновыми волокнами эластических волокон, пронизывающих межклеточное вещество во всех направлениях (рис. 8.21).
Из слоя, прилежащего к надхрящнице, эластические волокна без перерыва переходят в эластические волокна надхрящницы. Липидов, гликогена и хондроитинсульфатов в эластическом хряще меньше, чем в гиалиновом.
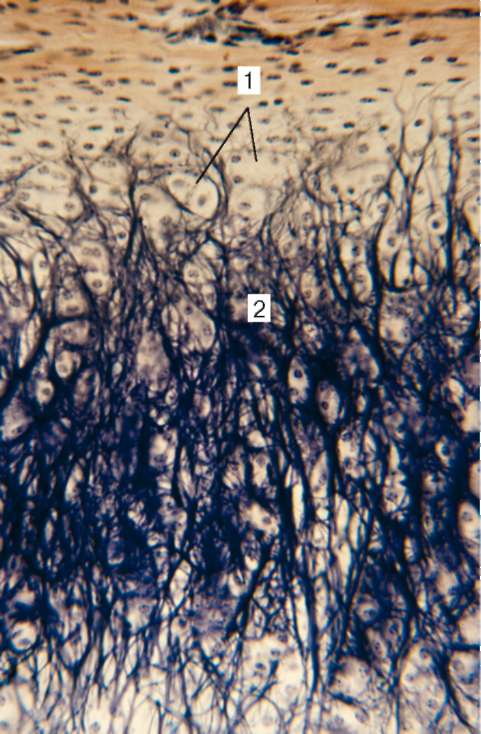
Рис. 8.21. Эластическая хрящевая ткань. Микрофотография, окраска - орсеин: 1 - изогенные группы хондроцитов; 2 - эластические волокна
Волокнистая хрящевая ткань
Волокнистая хрящевая ткань (textus cartilagineus fibrosa) находится в межпозвонковых дисках, полуподвижных сочленениях, в местах перехода волокнистой соединительной ткани (сухожилия, связки) в гиалиновый хрящ, где ограниченные движения сопровождаются сильными натяжениями. Межклеточное вещество содержит параллельно направленные коллагеновые пучки,
постепенно разрыхляющиеся и переходящие в гиалиновый хрящ. В хряще имеются полости, в которые заключены хрящевые клетки. Последние располагаются поодиночке или образуют небольшие изогенные группы. Цитоплазма клеток часто бывает вакуолизированной. По направлению от гиалинового хряща к сухожилию волокнистый хрящ становится все более похожим на сухожилие. На границе хряща и сухожилия между коллагено-выми пучками лежат столбиками сдавленные хрящевые клетки, которые без какой-либо границы переходят в сухожильные клетки, расположенные в плотной соединительной ткани (рис. 8.22).
Возрастные изменения. По мере старения организма в хрящевой ткани уменьшаются концентрация протеогликанов и связанная с ними гидро-фильность. Ослабляются процессы размножения хондробластов и молодых хондроцитов. В цитоплазме этих клеток уменьшается объем комплекса Гольджи, гранулярной эндоплазматической сети, митохондрий и снижается активность ферментов.
В резорбции дистрофически измененных клеток и межклеточного вещества участвуют хондрокласты, морфологически идентичные остеокластам. Часть лакун после гибели хондроцитов заполняются аморфным веществом и коллагеновыми фибриллами. Местами в межклеточном
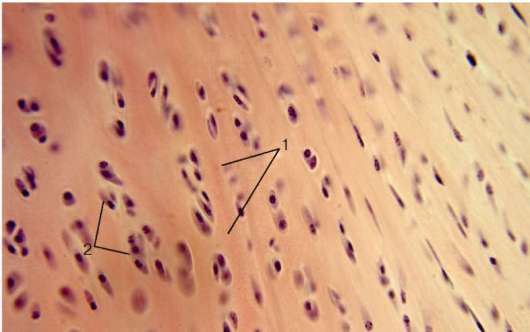
Рис. 8.22. Волокнистая хрящевая ткань. Срез межпозвонкового диска: 1 - коллагеновые волокна; 2 - хондроциты
веществе обнаруживаются отложения солей кальция («омеление хряща»), вследствие чего хрящ становится мутным, твердым и ломким. В результате появляющееся нарушение трофики центральных участков хряща может привести к врастанию в них кровеносных сосудов с последующим костеобразованием.
Регенерация. Физиологическая регенерация хрящевой ткани осуществляется за счет малодифференцированных клеток надхрящницы и хряща, путем размножения и дифференцировки прехондробластов и хондробла-стов. Однако этот процесс идет очень медленно. Посттравматическая регенерация хрящевой ткани внесуставной локализации осуществляется за счет надхрящницы (рис. 8.23).
В суставном хряще в зависимости от глубины травмы регенерация происходит как за счет размножения только клеток в изогенных группах (при неглубоком повреждении), так и за счет второго источника регенерации - камбиальных клеток субхондральной костной ткани (при глубоком повреждении хряща), которые образуют органический матрикс кости - остеоид.
В любом случае непосредственно в области травмы хрящевой ткани отмечаются дистрофические (некротические) процессы, а центробежнее располагаются про-лиферирующие хондробласты. В ране формируется волокнистая соединительная ткань, которая в последующем замещается хрящевой. В целом регенерация завершается через 3-6 мес после травмы.
Факторы регуляции метаболизма хрящевых тканей. Регуляция метаболизма хрящевой ткани происходит под действием механической нагрузки, нервных и гормональных факторов. Периодическое давление на хрящевую ткань и ослабление нагрузки являются постоянно действующими факторами диффузии растворенных в воде питательных веществ, продуктов метаболизма и гормонально-гуморальных регуляторов из капилляров надхрящницы, имеющей рецепторы и эффекторы, или синовиальной жидкости суставов. Кроме того, хондроциты имеют циторецепторы ряда гормонов, циркулирующих в крови. Так, гормоны гипофиза - соматотропин
и пролактин - стимулируют рост хрящевых тканей, но не влияют на их созревание. Гормоны щитовидной железы - тироксин и трийодтиронин - ускоряют цитодифференцировку хондроцитов, но ингибируют ростовые процессы в хрящах. Гормоны щитовидной и околощитовидной желез - кальцитонин и паратгормон - оказывают сходное действие на метаболизм хрящей, способствуют стимуляции ростовых процессов, но в меньшей степени их созреванию. Гормон эндокринных островков поджелудочной железы - инсулин - усиливает цитодифференцировку клеток скелетогенной мезенхимы, а на этапах постнатального онтогенеза оказывает ростовое и митогенное действие. Гормоны коры надпочечников - глюкокортикои-ды и женский половой гормон эстроген - ингибируют в хондроцитах биосинтез коллагена и гликозаминогликанов, а в раннем постнатальном периоде их высокие концентрации способствуют старению хрящевой ткани и деструктивным изменениям в ней. Мужской половой гормон - тестостерон - стимулирует биосинтез несульфатированных гликозаминогликанов, что приводит к снижению процессов созревания хрящевой ткани. В целом необходимо отметить, что гормоны регулируют специфические метаболические процессы в хондроцитах, но способность хондроцитов давать реакцию на их действие зависит как от состояния эндокринного статуса организма (норма, дефицит или избыток гормонов), так и структурно-функционального состояния самих хондроцитов.
8.2.2. Костные ткани
Костные ткани (textus ossei) - это специализированный полидифферон-ный вид соединительной ткани с высокой минерализацией межклеточного
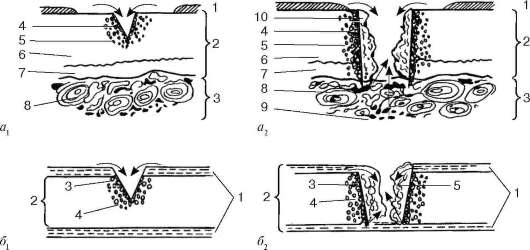
Рис. 8.23. Посттравматическая регенерация гиалинового хряща при неглубоком (а1 и
б1 и глубоком (а2 и б2) повреждениях: а\ 2 - регенерация суставного хряща: 1 - синовиальная оболочка; 2 - хрящ; 3 - кость; 4 - зона некроза; 5 - зона пролиферации; 6 - некальцифицированный хрящ; 7 - каль-цифицированный хрящ; 8 - остеоны с сосудами; 9 - костный мозг; 10 - грануляционная ткань; б - регенерация реберного хряща: 1 - перихондр; 2 - хрящ; 3 - зона некроза; 4 - зона пролиферации; 5 - грануляционная ткань (по В. Н. Павловой). Стрелки - направления перемещений клеток и тканей в раневом процессе
органического вещества, содержащего около 70 % неорганических соединений, главным образом фосфатов кальция. В костной ткани обнаружено более 30 микроэлементов (медь, стронций, цинк, барий, магний и др.), играющих важнейшую роль в метаболических процессах в организме.
Органическое вещество - матрикс костной ткани - представлено в основном белками коллагенового типа и липидами. По сравнению с матрик-сом хрящевой ткани в нем содержится относительно небольшое количество воды, хондроитинсерной кислоты, но много лимонной и других кислот, образующих комплексы с кальцием, импрегнирующим органическую матрицу кости. Органические и неорганические компоненты в сочетании друг с другом определяют механические свойства - способность сопротивляться растяжению, сжатию и др. Из всех разновидностей соединительных тканей в костной ткани наиболее выражены опорная, механическая и защитная функции. Для внутренних органов она также является депо солей кальция, фосфора и др.
Несмотря на высокую степень минерализации, в костных тканях происходят постоянное обновление входящих в их состав веществ, постоянное разрушение и созидание, адаптация в связи с изменяющимися условиями функционирования. Морфофункциональные свойства костной ткани меняются в зависимости от возраста, мышечной деятельности, условий питания, а также под влиянием деятельности желез внутренней секреции, иннервации и др.
Классификация. Существуют два основных типа костных тканей: грубо-волокнистая (сетчато-волокнистая) и пластинчатая. Эти разновидности костной ткани различаются по структурным и физическим свойствам, которые обусловлены главным образом строением межклеточного вещества. К костным тканям относятся также дентин и цемент зуба, имеющие сходство с костной тканью по высокой степени минерализации межклеточного вещества (см. главу 16) и опорной, механической функцией.
Грубоволокнистая костная ткань
Грубоволокнистая костная ткань (textus osseus reticulofibrosus) встречается главным образом у зародышей. У взрослых ее можно обнаружить на месте заросших черепных швов, в местах прикрепления сухожилий к костям. Беспорядочно расположенные коллагеновые волокна образуют в ней толстые пучки, хорошо заметные даже при сравнительно небольших увеличениях микроскопа (рис. 8.24).
В основном веществе грубоволокнистой костной ткани находятся удлиненно-овальной формы костные полости, или лакуны, с длинными ана-стомозирующими канальцами, в которых лежат костные клетки - остеоци-ты с их отростками. С поверхности кость покрыта надкостницей.
Пластинчатая костная ткань
Пластинчатая костная ткань (textus osseus lamellaris) - наиболее распространенная разновидность костной ткани во взрослом организме. Она состоит из костных пластинок (lamellae ossea). Толщина и длина последних
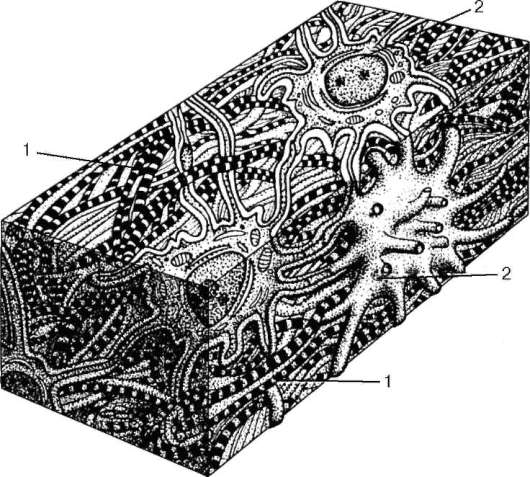
Рис. 8.24. Строение грубоволокнистой костной ткани (по Ю. И. Афанасьеву): 1 - пучки переплетающихся коллагеновых волокон; 2 - остеоциты
колеблется от нескольких десятков до сотен микрометров соответственно. Они не монолитны, а содержат параллельно направленные коллагеновые (оссеиновые) фибриллы, ориентированные в различных плоскостях. В центральной части пластин фибриллы имеют преимущественно продольное направление, по периферии - прибавляется тангенциальное и поперечное направления. Пластинки могут расслаиваться, а фибриллы одной пластинки могут продолжаться в соседние, создавая единую волокнистую основу кости. Кроме того, костные пластинки пронизаны отдельными фибриллами и волокнами, ориентированными перпендикулярно костным пластинкам, вплетающимися в промежуточные слои между ними, благодаря чему достигается большая прочность пластинчатой костной ткани (рис. 8.25). Из этой ткани построены компактное и губчатое вещество в большинстве плоских и трубчатых костей скелета.
Развитие костных тканей (остеогистогенез)
Развитие костной ткани у эмбриона осуществляется двумя способами: 1) непосредственно из мезенхимы (прямой остеогенез); 2) из мезенхимы на месте ранее развившейся хрящевой модели кости (непрямой остеогенез). Постэмбриональное развитие костной ткани происходит при физиологической и репаративной регенерации.
Костная ткань включает остеобластический и остеокластический дифферо-ны. Первый (основной) состоит из ряда дифференцирующихся клеток: стволовые, полустволовые клетки (преостеобласты), остеобласты (разновидность
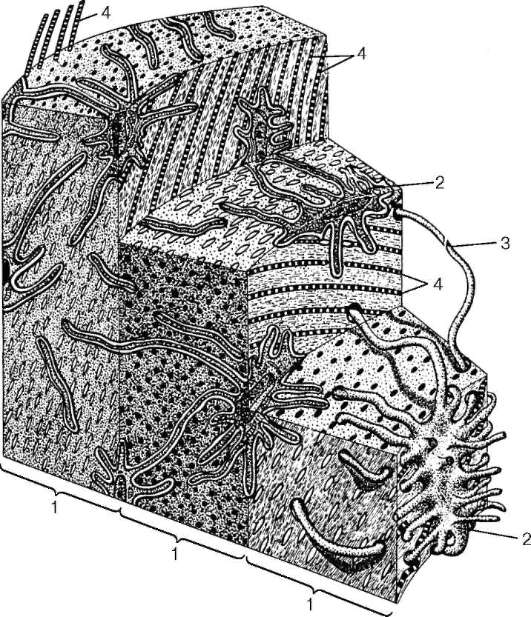
Рис. 8.25. Строение пластинчатой костной ткани (по Ю. И. Афанасьеву):
1 - костные пластинки; 2 - остеоциты; 3 - контакты отростков остеоцитов; 4 -
коллагеновые волокна, ориентированные в пределах каждой костной пластинки
параллельно
фибробластов), остеоциты. На процессы остеогенной дифференцировки клеток влияют остеогенные факторы (костный морфогенетический белок), парциальное давление кислорода в ткани, наличие щелочной фосфатазы и др. Второй (сопутствующий) дифферон включает остеокласты (разновидность макрофагов), развивающиеся из стволовых клеток крови.
Стволовые и полустволовые остеогенные клетки морфологически не идентифицируются.
Остеобласты (от греч. osteon - кость, blastos - зачаток) - это молодые клетки, создающие костную ткань. В сформировавшейся кости они встречаются только в глубоких слоях надкостницы и в местах регенерации костной ткани после ее травмы. Они способны к пролиферации, в образующейся кости покрывают почти непрерывным слоем всю поверхность развивающейся костной балки (рис. 8.26). Форма остеобластов бывает различной: кубической, пирамидальной или угловатой. Размер их тела около 15-20 мкм. Ядро округлой или овальной формы, часто располагается эксцентрично, содержит одно или несколько ядрышек.
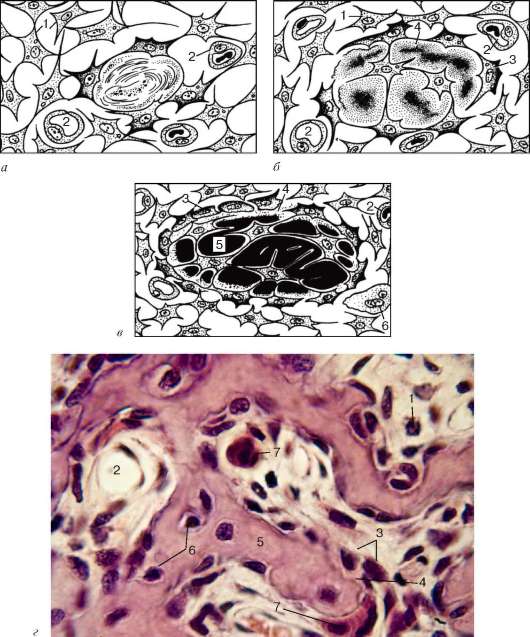
Рис. 8.26. «Прямой» остеогенез:
а - остеогенный островок (схема); б - остеоидная стадия (схема); в - оссификация межклеточного вещества (схема); г - «прямой» остеогенез в плоской кости (микрофотография). 1 - мезенхимные клетки; 2 - кровеносные капилляры; 3 - остеобласты; 4 - остеоид; 5 - минерализованное межклеточное вещество; 6 - остеоцит; 7 - остеокласт
В цитоплазме остеобластов хорошо развиты гранулярная эндоплазматическая сеть, митохондрии и комплекс Гольджи (рис. 8.27). В ней выявляются в значительных количествах РНК и высокая активность щелочной фосфа-тазы. Остеобласты выделяют матриксные пузырьки, содержащие липиды,
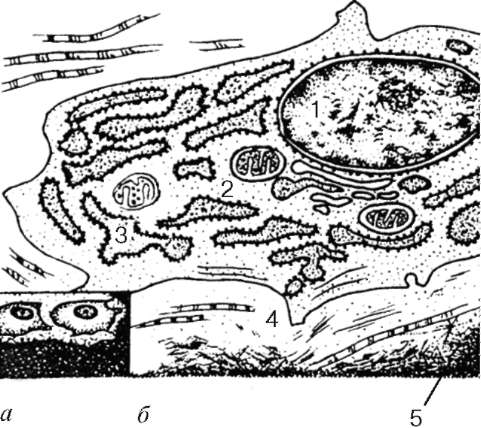
Рис. 8.27. Строение остеобласта (по Ю. И. Афанасьеву):
а - на светооптическом уровне; б - на ультрамикроскопическом уровне. 1 - ядро; 2 - цитоплазма; 3 - гранулярная эндоплазматическая сеть; 4 - остеоид; 5 - минерализованное вещество костной ткани
Са2+, щелочную фосфатазу, что приводит к кальцификации органического матрикса ткани.
Остеоциты (от греч. osteon - кость, cytus - клетка) - это преобладающие по количеству дефинитивные клетки костной ткани, утратившие способность к делению. Они имеют отрост-чатую форму, компактное, относительно крупное ядро и слабобазофильную цитоплазму (рис. 8.28). Органеллы развиты слабо. Наличие центриолей в остеоцитах не установлено.
Костные клетки лежат в костных полостях, или лакунах, которые повторяют контуры остеоцита. Длина полостей колеблется от 22 до 55 мкм, ширина - от 6 до 14 мкм. Канальцы костных полостей заполнены тканевой жидкостью, анасто-мозируют между собой и с перива-
скулярными пространствами сосудов, заходящих внутрь кости. Обмен веществ между остеоцитами и кровью осуществляется через тканевую жидкость.
Остеокласты (от греч. osteon - кость и clastos - раздробленный). Эти клетки гематогенной природы способны разрушать обызвествленный хрящ и кость. Диаметр их достигает 150-180 мкм, они содержат от 3 до нескольких десятков ядер (рис. 8.29). Цитоплазма слабобазофильна, иногда оксифильна. Остеокласты располагаются обычно на поверхности костных перекладин. На той стороне остеокласта, которая прилежит к разрушаемой поверхности, имеется микроскладчатая (гофрированная) кайма; она является областью синтеза и секреции гидролитических ферментов. По периферии остеокласта находится зона плотного прилегания клетки к костной поверхности, которая как бы герметизирует область действия ферментов. Эта зона цитоплазмы светлая, содержит мало органелл, за исключением микрофиламен-тов, состоящих из актина.
Периферический слой цитоплазмы над гофрированным краем содержит многочисленные мелкие пузырьки и более крупные - вакуоли. Полагают, что остеокласты выделяют СО2 в окружающую среду, а фермент - карбоан-гидраза, обнаруживаемый здесь, способствует образованию кислоты (Н2СО3) и растворению кальциевых соединений. Остеокласт богат митохондриями и лизосомами, ферменты которых (коллагеназа и другие протеазы) расщепляют коллаген и протеогликаны матрикса костной ткани. В том месте, где остеокласт соприкасается с костным веществом, в последнем образуется резорбционная лакуна. Один остеокласт может разрушить столько кости, сколько создают 100 остеобластов за это же время. Функции остеобла-
стов и остеокластов взаимосвязаны и коррелируют с участием гормонов, простагландинов, функциональной нагрузкой, витаминами и др.
Межклеточное вещество (substantia intercellularis) состоит из основного аморфного вещества, импрегниро-ванного неорганическими солями, в котором располагаются коллаге-новые волокна, образующие небольшие пучки. Они содержат (до 90 %) белок - коллаген I типа. Волокна могут иметь беспорядочное (в гру-боволокнистой костной ткани) или строго ориентированное (в пластинчатой костной ткани) направление.
В основном веществе костной ткани по сравнению с хрящевой содержится относительно небольшое количество хондроитинсерной кислоты, но много лимонной и других кислот, образующих комплексы с кальцием, импрегни-рующих органический матрикс кости. Кроме коллагенового белка, в основном веществе костной ткани обнаруживают неколлагеновые белки (остеокальцин, сиалопротеин, остеонектин, остеопон-тин и др., принимающие участие в процессах минерализации), а также гли-козаминогликаны. Основное вещество кости содержит кристаллы гидроксиа-патита, упорядоченно расположенные по отношению к фибриллам органической матрицы кости, а также аморфный фосфат кальция. В костной ткани обнаружено более 30 микроэлементов (медь, стронций, цинк, барий, магний и др.), играющих важнейшую роль в метаболических процессах в организме. Систематическое увеличение физической нагрузки приводит к нарастанию костной массы от 10 до 50 % вследствие высокой минерализации.
Прямой остеогистогенез. Такой способ остеогенеза характерен для развития грубоволокнистой костной ткани при образовании плоских
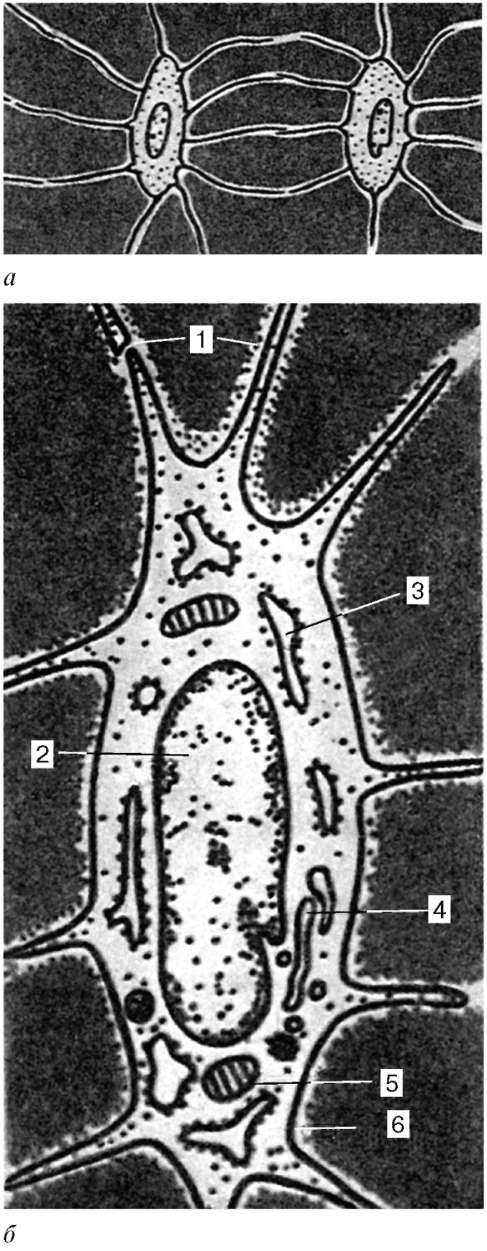
Рис. 8.28. Строение остеоцита (по Ю. И. Афанасьеву):
а - на светооптическом уровне; б - на ультрамикроскопическом уровне. 1 - отростки остеоцитов; 2 - ядро; 3 - эндоплазматическая сеть; 4 - комплекс Гольджи; 5 - митохондрии; 6 - остеоидное (необызвест-вленное) вещество кости по краю лакуны, в которой расположены остеоциты
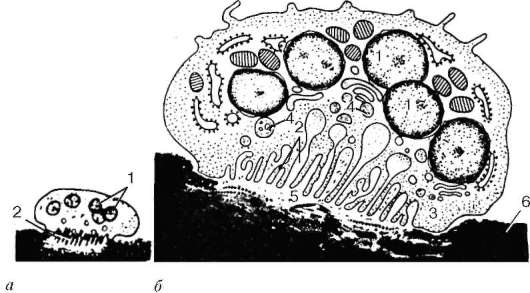
Рис. 8.29. Строение остеокласта (по Ю. И. Афанасьеву):
а - на светооптическом уровне; б - на ультрамикроскопическом уровне. 1 - ядро; 2 - гофрированный край остеокласта; 3 - светлая зона; 4 - лизосомы; 5 - зона резорбции межклеточного вещества; 6 - минерализованное вещество
костей, например покровных костей черепа. Этот процесс наблюдается в основном в течение 1-го мес внутриутробного развития и характеризуется образованием сначала первичной «перепончатой», остеоидной костной ткани с последующей импрегнацией (отложением) солей кальция, фосфора и других в межклеточном веществе. На первой стадии - образование ске-летогенного островка - в местах развития будущей кости происходят очаговое размножение мезенхимных клеток и васкуляризация скелетогенного островка. Клетки мезенхимы ориентируются согласно векторам нагрузки и дифференцируются в остеогенные предшественники - преостеобласты. На второй стадии происходит дифференцировка клеток островков в остеобласты, в которых начинается биосинтез белков коллагена и его секреция, в результате чего появляется оксифильное межклеточное вещество с колла-геновыми фибриллами - органический матрикс костной ткани (остеоид-ная стадия). Разрастающиеся волокна раздвигают клетки, которые с помощью формирующихся отростков остаются связанными друг с другом. Так остеобласты приобретают отростчатую форму и становятся остеоцитами, включенными в толщу волокнистой массы, и теряют способность к размножению. В основном веществе появляются мукопротеиды (оссеомукоид), цементирующие волокна в одну прочную массу. В то же время из окружающей мезенхимы образуются новые генерации остеобластов, которые наращивают кость снаружи (аппозиционный рост).
Третья стадия - кальцификация (импрегнация солями) межклеточного вещества. При этом остеобласты выделяют фермент щелочную фосфатазу, расщепляющую содержащиеся в периферической крови глицерофосфаты на углеводные соединения (сахара) и фосфорную кислоту. Последняя вступает в реакцию с солями кальция, который осаждается в основном веществе и волокнах сначала в виде соединений кальция, формирующих аморфные
отложения [Са3(РО4)2], в дальнейшем из него образуются кристаллы гидро-ксиапатита [Са10(РО4)6(ОН)2].
Одним из посредников кальцификации служит остеонектин - гликопро-теин, избирательно связывающий соли кальция и фосфора с коллагеном. В результате кальцификации образуются костные перекладины, или балки. Затем от этих перекладин ответвляются выросты, соединяющиеся между собой и образующие широкую сеть. Пространства между перекладинами оказываются занятыми рыхлой волокнистой соединительной тканью с проходящими в ней кровеносными сосудами.
К моменту завершения гистогенеза по периферии зачатка кости в эмбриональной соединительной ткани появляется большое количество волокон и остеогенных клеток. Часть этой волокнистой соединительной ткани, прилегающей непосредственно к костным перекладинам, развивается в периост (periosteum), который обеспечивает трофику и регенерацию кости. Такая кость, появляющаяся на стадиях эмбрионального развития и состоящая из перекладин грубоволокнистой костной ткани, называется первичной губчатой костью. На более поздних стадиях развития она заменяется вторичной губчатой костью взрослых, которая отличается от первой тем, что построена из пластинчатой костной ткани (четвертая стадия остеогене-за). Развитие пластинчатой костной ткани тесно связано с процессом разрушения отдельных участков кости и врастанием кровеносных сосудов в толщу грубоволокнистой кости. В этом процессе как в период эмбрионального остеогенеза, так и после рождения принимают участие остеокласты (см. рис. 8.29). Вокруг кровеносных сосудов образуется слой остеобластов и в дальнейшем возникают новые концентрические пластинки остеона. Коллагеновые волокна в каждой пластинке расположены параллельно, но ориентированы под углом к волокнам предыдущей пластинки. Таким образом, вокруг сосуда формируются как бы костные цилиндры, вставленные один в другой (первичные остеоны). С момента появления остеонов грубо-волокнистая костная ткань перестает развиваться и заменяется пластинчатой костной тканью. Со стороны надкостницы формируются наружные опоясывающие (общие, генеральные) пластинки, охватывающие всю кость снаружи. Так развиваются плоские кости. В дальнейшем образовавшаяся в эмбриональном периоде кость подвергается перестройке: разрушаются первичные остеоны и развиваются новые генерации остеонов. Такая перестройка кости практически продолжается всю жизнь.
В отличие от хрящевой ткани кость всегда растет способом наложения новой ткани на уже имеющуюся, т. е. путем аппозиции, и для дифференцировки клеток скелетогенного островка необходимо оптимальное кровоснабжение.
Непрямой остеогистогенез. На 2-м мес эмбрионального развития в местах будущих трубчатых костей закладывается из мезенхимы хрящевой зачаток, который очень быстро принимает форму будущей кости (хрящевая модель). Зачаток состоит из эмбрионального гиалинового хряща, покрытого надхрящницей (рис. 8.30). Некоторое время он растет как за счет клеток, образующихся со стороны надхрящницы, так и за счет размножения клеток во внутренних участках.
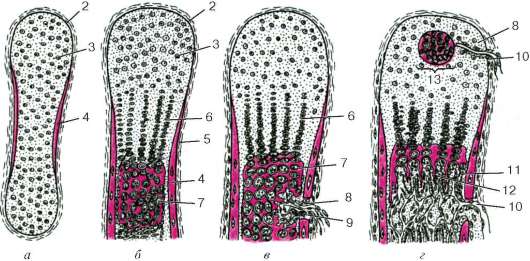
Рис. 8.30. Непрямой (хрящевой) остеогенез. Образование хрящевой модели кости и перихондральной костной манжетки (по Ю. И. Афанасьеву):
а-г - стадии остеогенеза. 1 - первичная хрящевая модель трубчатой кости; 2 - надхрящница; 3 - хрящевая ткань; 4 - перихондральная костная манжетка; 5 - надкостница; 6 - колонки хрящевых клеток; 7 - зона пузырчатых клеток; 8 - врастающая в хрящ мезенхима с дифференцирующимися остеокластами (9) и кровеносными капиллярами (10); 11 - остеобласты; 12 - эндохондрально образованная костная ткань; 13 - точка окостенения в эпифизе
Развитие кости на месте хряща, т. е. непрямой остеогенез, начинается в области диафиза (перихондральное окостенение). Образованию перихондрально-го костного кольца (манжетки) предшествует разрастание кровеносных сосудов с дифференцировкой в надхрящнице, прилежащей к средней части диафиза, остеобластов, образующих в виде манжетки сначала грубоволокнистую костную ткань (первичный центр окостенения), затем заменяющуюся пластинчатой.
Образование костной манжетки нарушает питание хряща. Вследствие этого в центре диафизарной части хрящевого зачатка возникают дистрофические изменения. Хондроциты вакуолизируются, их ядра пикнотизируют-ся, образуются так называемые пузырчатые хондроциты. Рост хряща в этом месте прекращается. Расширение перихондрального костного кольца сопровождается увеличением зоны деструкции хряща и появлением остеокластов, которые очищают пути для врастающих в модель трубчатой кости кровеносных сосудов и остеобластов (см. рис. 8.30). Это приводит к появлению очагов эндохондрального окостенения (вторичные центры окостенения). В связи с продолжающимся ростом соседних неизмененных дистальных отделов диафиза хондроциты на границе эпифиза и диафиза собираются в колонки, направление которых совпадает с длинной осью будущей кости. Таким образом, в колонке хондроцитов имеются два противоположно направленных процесса - размножение и рост в дистальных отделах диафиза и дистрофические процессы в его проксимальном отделе. Одновременно между набухшими клетками происходит отложение минеральных солей, обусловливающее появление резкой базофилии и хрупкости хряща.
С момента разрастания сосудистой сети и появления остеобластов надхрящница перестраивается, превращаясь в надкостницу. В дальнейшем кровеносные сосуды с окружающей их мезенхимой, остеогенными клетками и остеокластами врастают через отверстия костной манжетки и входят в соприкосновение с обызвествленным хрящом (см. рис. 8.30). Под влиянием ферментов, выделяемых остеокластами, происходит растворение (хондро-лиз) обызвествленного межклеточного вещества. Диафизарный хрящ разрушается, в нем возникают удлиненные пространства, в которых «поселяются» остеобласты, образующие на поверхности оставшихся участков обызвествленного межклеточного вещества хряща костную ткань.
Первичный, или диафизарный, центр окостенения. Процесс образования кости внутри хрящевого зачатка получил название эндохондрального окостенения (греч. endon - внутри).
Одновременно с процессом развития эндохондральной кости появляются и признаки ее разрушения остеокластами. Вследствие разрушения эндохон-дральной костной ткани образуются еще большие полости и пространства (полости резорбции) и, наконец, возникает костномозговая полость. Из проникшей сюда мезенхимы образуется строма костного мозга, в которой поселяются стволовые клетки крови и соединительной ткани. В это же время по периферии диафиза со стороны надкостницы возникают все новые и новые перекладины костной ткани. Костная ткань, разрастаясь в длину по направлению к эпифизам и увеличиваясь в толщину, образует плотный слой кости.
Организация периостальной кости протекает иначе, чем организация эндохондральной костной ткани. На месте разрушающейся грубоволокни-стой кости вокруг проникших сюда сосудов, которые идут вдоль длинной оси зачатка кости, начинают образовываться концентрические пластинки, состоящие из параллельно ориентированных тонких коллагеновых волокон и цементирующего межклеточного вещества. Так возникают первичные осте-оны. Просвет их широк, границы пластинок нерезко контурированы. Вслед за появлением первой генерации остеонов со стороны периоста начинается развитие наружных опоясывающих (генеральных) пластинок, окружающих кость в области диафиза. Вслед за диафизом центры окостенения появляются в эпифизах. Этому предшествуют сначала дифференцировка хондроцитов, их гипертрофия, сменяемая ухудшением питания, дистрофией и кальцинацией межклеточного вещества. В дальнейшем отмечается процесс окостенения, подобный описанному выше. Оссификация сопровождается врастанием в эпифизы сосудов.
В промежуточной области между диафизом и эпифизами сохраняется хрящевая ткань - метафизарный хрящ, являющийся зоной роста костей в длину.
Гистологическое строение трубчатой кости как органа
Трубчатая кость как орган в основном построена из пластинчатой костной ткани, кроме бугорков. Снаружи кость покрыта надкостницей, за исключением суставных поверхностей эпифизов, покрытых разновидностью гиалинового хряща.
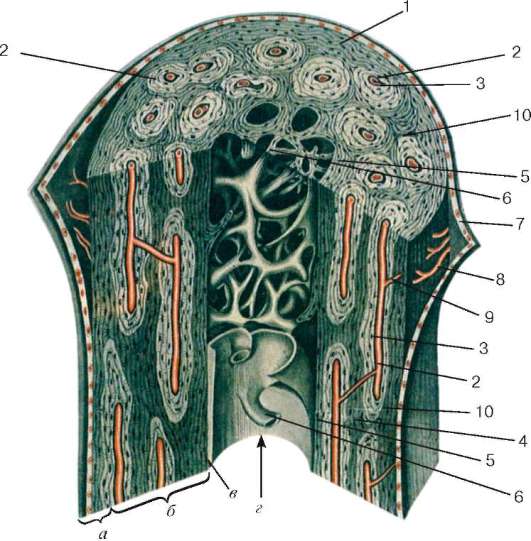
Рис. 8.31. Строение трубчатой кости (по В. Г. Елисееву, Ю. И. Афанасьеву, Е. Ф. Котовскому):
а - надкостница; б - компактное вещество кости; в - эндост; г - костномозговая полость. 1 - слой наружных общих пластинок; 2 - остеон; 3 - канал остеона; 4 - вставочные пластинки; 5 - слой внутренних общих пластинок; 6 - костная тра-бекула губчатого вещества; 7 - волокнистый слой надкостницы; 8 - кровеносные сосуды надкостницы; 9 - прободающий канал; 10 - остеоциты
Надкостница, или периост (periosteum). В надкостнице различают два слоя: наружный (волокнистый) и внутренний (клеточный). Наружный слой образован в основном волокнистой соединительной тканью (рис. 8.31, 8.32). Внутренний слой содержит большое количество клеток: камбиальные клетки, преостеобласты и остеобласты различной степени дифференцировки. Камбиальные клетки веретеновидной формы имеют небольшой объем цитоплазмы и умеренно развитый синтетический аппарат. Преостеобласты - энергично пролиферирующие клетки овальной формы, способные синтезировать гликозаминогликаны. Остеобласты характеризуются хорошо развитым белок-синтезирующим (коллаген) аппаратом. Через надкостницу проходят питающие кость сосуды и нервы.
Надкостница связывает кость с окружающими тканями и принимает участие в ее трофике, развитии, росте и регенерации.
Строение диафиза. Компактное вещество, образующее диафиз кости, состоит из костных пластинок, толщина которых колеблется от 4 до 12-15 мкм. Костные пластинки располагаются в определенном порядке,

Рис. 8.32. Надкостница (по Ю. И. Афанасьеву):
1 - наружный (волокнистый) слой; 2 - внутренний (клеточный) слой; 3 - остеоген-ные клетки; 4 - костная ткань
образуя сложные системы. В диафизе различают три слоя: наружный слой опоясывающих (общих, генеральных) пластинок, средний, образованный концентрически напластованными вокруг сосудов костными пластинками - остеонами и называемый остеонным слоем (рис. 8.33), и внутренний слой опоясывающих (общих) пластинок.
Наружные пластинки не образуют полных колец вокруг диафиза кости, перекрываются на поверхности следующими слоями пластинок. Внутренние пластинки хорошо развиты только там, где компактное вещество кости непосредственно граничит с костномозговой полостью. В тех же местах, где компактное вещество переходит в губчатое, его внутренние общие пластинки продолжаются в пластинки перекладин губчатого вещества.
Наружные пластинки пронизаны прободающими (фолькмановыми) каналами, по которым из надкостницы внутрь кости входят сосуды. Со стороны надкостницы в кость под разными углами проникают коллагеновые волокна. Эти волокна получили название прободающих (шарпеевых) волокон. Чаще всего они разветвляются только в наружном слое общих пластинок, но могут проникать и в средний остеонный слой, однако они никогда не входят в пластинки остеонов.
В среднем слое костные концентрические (остеонные) пластинки формируют остеоны. Между остеонами располагаются промежуточные (вставочные) пластинки. Толщина и длина костных пластинок колеблются от нескольких десятков до сотен микрометров. Остеоны (гаверсовы системы) являются структурными единицами компактного вещества трубчатой кости (см. рис. 8.31, рис. 8.33). Они представляют собой цилиндрические образования, состоящие из концентрических костных пластинок, как бы вставленных друг в друга. В костных пластинках и между ними располагаются тела костных клеток и их отростки, замурованные в костном межклеточном веществе. Каждый остеон отграничен от соседних остеонов цементирующей (спайной) линией, образованной основным веществом. В центральном
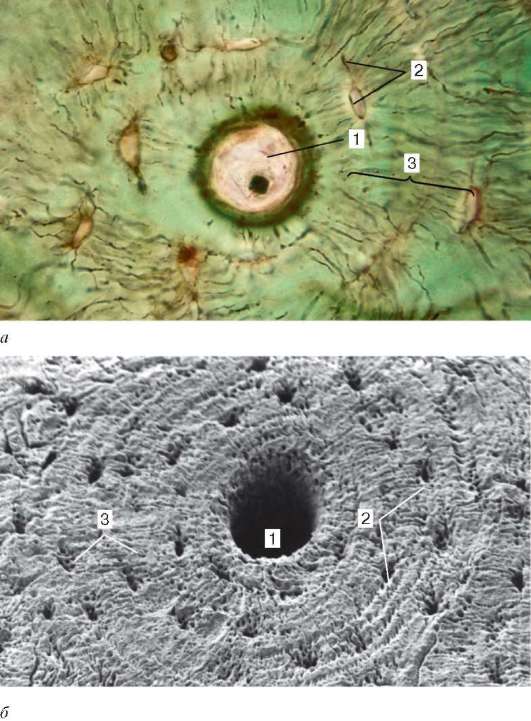
Рис. 8.33. Остеон:
а - микрофотография (окраска по методу Шморля); б - сканирующая электронная микроскопия фрагмента кости (препарат О. В. Слесарева). 1 - канал остеона; 2 - остеоциты (лакуны - б); 3 - костные пластинки
канале остеона проходят кровеносные сосуды с сопровождающей их соединительной тканью и остеогенными клетками.
В диафизе длинной кости остеоны расположены преимущественно параллельно длинной оси. Каналы остеонов анастомозируют друг с другом, в местах анастомозов прилежащие к ним пластинки изменяют свое направление (см. рис. 8.31). Такие каналы называют прободающими, или питающими. Сосуды, расположенные в каналах остеонов, сообщаются друг с другом и с сосудами костного мозга и надкостницы. Большую часть диафиза составляет компактное вещество трубчатых костей. На внутренней поверхности диа-
физа, граничащей с костномозговой полостью, пластинчатая костная ткань образует костные перекладины губчатого вещества кости. Полость диафиза трубчатых костей заполнена костным мозгом.
Эндост (endosteum) - оболочка, покрывающая кость со стороны костномозговой полости. В эндосте сформированной поверхности кости различают осмиофильную линию на наружном крае минерализованного вещества кости; остеоидный слой, состоящий из аморфного вещества, коллагеновых фибрилл и остеобластов, кровеносных капилляров и нервных окончаний, слоя клеток, нечетко отделяющих эндост от элементов костного мозга. Толщина эндоста превышает 1-2 мкм, но меньше, чем у периоста.
В областях активного формирования кости толщина эндоста возрастает в 10-20 раз за счет остеоидного слоя вследствие повышения синтетической активности остеобластов и их предшественников. При ремоделировании кости в составе эндоста обнаруживаются остеокласты. В эндосте стареющей кости уменьшается популяция остеобластов и клеток-предшественников, но возрастает активность остеокластов, что ведет к истончению компактного слоя и перестройке губчатого вещества кости.
Между эндостом и периостом существует определенная микроциркуляция жидкости и минеральных веществ благодаря лакунарно-канальцевой системе костной ткани.
Васкуляризация костной ткани. Кровеносные сосуды образуют во внутреннем слое надкостницы густую сеть. Отсюда берут начало тонкие артериальные веточки, которые через питательные отверстия кровоснабжают остеоны, а потом проникают в костный мозг и принимают участие в образовании питающей его сети капилляров. Лимфатические сосуды располагаются главным образом в наружном слое надкостницы.
Иннервация костной ткани. В надкостнице миелиновые и безмиелино-вые нервные волокна образуют сплетение. Часть волокон сопровождают кровеносные сосуды и проникают с ними через питательные отверстия в одноименные каналы, а затем в каналы остеонов и далее достигают костного мозга. Другая часть волокон заканчиваются в надкостнице свободными нервными разветвлениями, а также участвуют в образовании инкапсулированных телец.
Рост трубчатых костей. Рост костей - процесс очень длительный. Он начинается у человека с ранних эмбриональных стадий и завершается в среднем к 20-летнему возрасту. В течение всего периода роста кость увеличивается как в длину, так и в ширину. Рост трубчатой кости в длину обеспечивается наличием метаэпифизарной хрящевой пластинки роста, в которой проявляются два противоположных гистогенетических процесса.
Один - это разрушение эпифизарной пластинки, а другой, противоположный ему, - непрестанное пополнение хрящевой ткани путем новообразования клеток. Однако со временем процессы разрушения клеток начинают преобладать над процессами новообразования, вследствие чего хрящевая пластинка истончается и исчезает. Рост кости в длину прекращается.
В метаэпифизарном хряще различают пограничную зону, зону столбчатых клеток и зону пузырчатых клеток. Пограничная зона, расположенная вблизи
эпифиза, состоит из округлых и овальных клеток и единичных изогенных групп, которые обеспечивают связь хрящевой пластинки с костью эпифиза. В полостях между костью и хрящом находятся кровеносные капилляры, обеспечивающие питанием клетки глубжележащих зон хрящевой пластинки. Зона столбчатых клеток содержит активно размножающиеся клетки, которые формируют колонки, расположенные вдоль продольной оси кости, и обеспечивают ее рост и длину. Проксимальные концы колонок состоят из созревающих, дифференцирующихся хрящевых клеток. Они богаты гликогеном и щелочной фосфатазой. Обе эти зоны наиболее реактивны при действии гормонов и других факторов, оказывающих влияние на процессы окостенения и роста костей. Зона пузырчатых клеток характеризуется гидратацией и разрушением хондроцитов с последующим эндохондральным окостенением. Дистальный отдел этой зоны граничит с диафизом, откуда в нее проникают кровеносные капилляры и остеогенные клетки. Продольно ориентированные колонки эндохондральной кости являются по существу костными трубочками, на месте которых формируются остеоны.
Впоследствии центры окостенения в диафизе и эпифизе сливаются, и рост кости в длину заканчивается.
Рост трубчатой кости в ширину осуществляется за счет периоста. Со стороны периоста очень рано начинают образовываться концентрические слои пластинчатой костной ткани. Этот аппозиционный рост продолжается до окончания формирования кости. Количество остеонов непосредственно после рождения невелико, но уже к 25 годам в длинных костях конечностей количество их значительно увеличивается.
Регенерация. Физиологическая регенерация костных тканей происходит медленно за счет остеогенных клеток надкостницы - эндоста и остеоген-ных клеток в канале остеона. Посттравматическая регенерация костной ткани протекает лучше в тех случаях, когда концы сломанной кости не смещены относительно друг друга. Процессу остеогенеза предшествует формирование соединительнотканной мозоли, в толще которой могут образовываться хрящевые островки (рис. 8.34). Оссификация в этом случае идет по типу вторичного (непрямого) остеогенеза. В условиях оптимальной окси-генации тканей, хорошей репозиции и фиксации концов сломанной кости регенерация происходит без образования мозоли. Однако прежде чем остеобласты начнут строить кость, остеокласты образуют небольшую щель между сопоставленными концами кости. На этой биологической закономерности основано применение травматологами аппаратов постепенного растягивания сращиваемых костей в течение всего периода регенерации.
Перестройка кости и факторы, влияющие на ее структуру
В костной ткани в течение всей жизни человека происходят взаимосвязанные процессы разрушения и созидания, обусловленные функциональными нагрузками и другими факторами внешней и внутренней среды. Перестройка остеонов всегда связана с разрушением первичных остеонов и одновременным образованием новых остеонов как на месте разрушения, так и со стороны периоста. Под влиянием остеокластов, активизированных
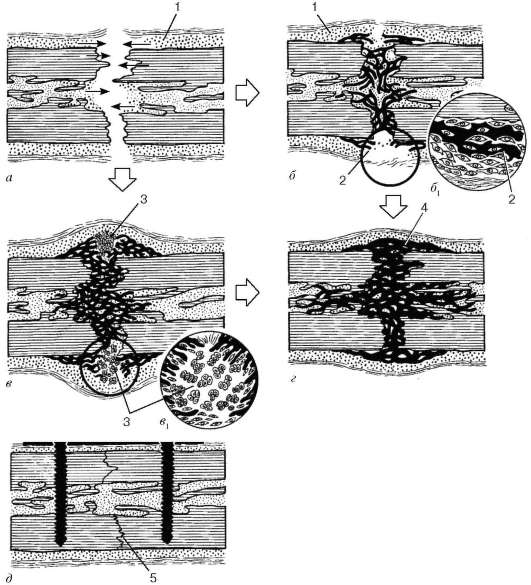
Рис. 8.34. Посттравматическая регенерация трубчатой кости: а - локализация травмы; б-г - последовательные стадии регенерации без жесткой фиксации репонированных костей (б1, в1 - фрагменты); д - регенерация после фиксации отломков. 1 - надкостница; 2 - перекладины из грубоволокни-стой костной ткани; 3 - соединительнотканный регенерат с островками хрящевой ткани; 4 - костный регенерат из грубово-локнистой костной ткани; 5 - линия сращения (по Р. В. Крстичу, с изменениями)
различными факторами, костные пластинки остеона разрушаются, и на его месте образуется полость. Этот процесс называется резорбцией (от лат. resorptia - рассасывание) костной ткани. В образовавшейся полости вокруг оставшегося сосуда появляются остеобласты и начинается построение новых пластинок, концентрически наслаивающихся друг на друга. Так возникают вторичные генерации остеонов. Между остеонами располагаются остатки разрушенных остеонов прежних генераций. Процесс перестройки остеонов не приостанавливается и после окончания роста кости.
Среди факторов, влияющих на перестройку костной ткани, существенную роль играет ее так называемый пьезоэлектрический эффект. Оказалось, что в костной пластинке при изгибах появляется определенная разность потенциалов между вогнутой и выпуклой стороной. Первая заряжается отрицательно,
а вторая - положительно. На отрицательно заряженной поверхности всегда отмечаются активация остеобластов и процесс аппозиционного новообразования костной ткани, а на положительно заряженной, напротив, наблюдается ее резорбция с помощью остеокластов. Искусственное создание разности потенциалов приводит к такому же результату (рис. 8.35). Нулевой потенциал, отсутствие физической нагрузки на костную ткань (продолжительная иммобилизация, пребывание в состоянии невесомости и др.) обусловливают повышение функций остеокластов и выведение солей.
На структуру костной ткани и костей оказывают влияние витамины (С, A, D), гормоны щитовидной, околощитовидной и других эндокринных желез.
В частности, при недостаточном количестве витамина С в организме (например, при цинге) подавляется образование коллагеновых волокон, ослабляется деятельность остеобластов, уменьшается их фосфатазная активность, что практически приводит к остановке роста кости вследствие торможения образования органической основы костных тканей. При дефиците витамина D (рахит) не происходит полной кальцификации органической матрицы кости, что обусловливает размягчение костей (остеомаляция). Витамин А поддерживает рост костей, но избыток этого витамина способствует усилению разрушения остеокластами метаэпифизарных хрящей - зоны роста костей и замедлению их удлинения.
При избытке гормона околощитовидной железы - паратирина - наблюдаются повышение активности остеокластов и резорбция кости. Тирокальцитонин, вырабатываемый С-клетками щитовидной железы, действует диаметрально противоположно, понижая функцию остеокластов, имеющих рецепторы этого гормона. При гипофункции щитовидной железы замедляется рост длинных трубчатых костей в результате подавления активности остеобластов и торможения процесса оссифи-кации. Регенерация кости в этом случае происходит слабо и неполноценно. В случае тестикулярной недоразвитости или препубертатной кастрации задерживается окостенение метаэпифизарной пластинки, вследствие чего руки и ноги у такого индивидуума становятся непропорционально длинными. При недостатке эстрогенов после наступления климактерического периода у женщин иногда развивается остеопороз. При раннем половом созревании намечается остановка роста из-за преждевременного диафизо-эпифизарного сращения костей. Определенную позитивную роль в росте костей играет соматотропный гормон аденогипофиза, который стимулирует пропорциональное развитие скелета в молодом (юношеском) возрасте и непропорциональное (акромегалия) у взрослых.
Возрастные изменения. Соединительные ткани с возрастом претерпевают изменения в строении, количестве и химическом составе. С возрастом увеличиваются общая масса соединительнотканных образований, рост костного скелета. Во многих разновидностях соединительнотканных структур изменяется соотношение типов коллагена, гликозаминогликанов; в частности, в них становится больше сульфатированных соединений.
Соединения костей
Две кости могут иметь соединения непрерывные (синдесмозы, синхондрозы и синостозы) и прерывистые (суставы).
Непрерывные соединения - соединения с помощью плотной волокнистой соединительной ткани, пучки которой в виде прободающих волокон внедряются в кост-
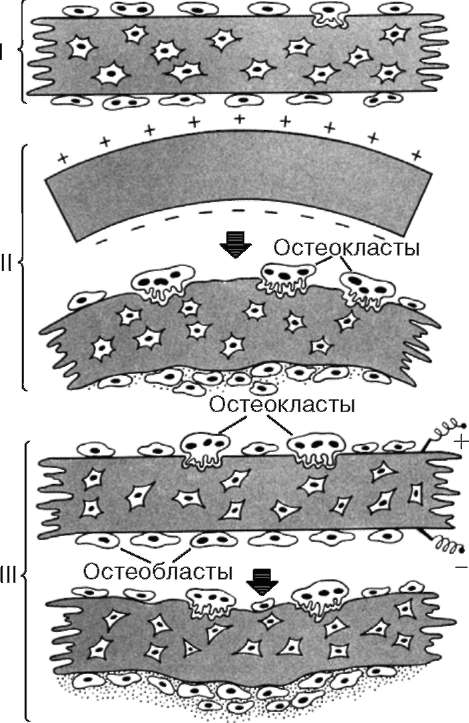
Рис. 8.35. Пьезоэлектрический эффект (пояснения в тексте): I - схема структурной организации костной трабекулы; II - активация остеокластов и остеобластов при изменении формы костной трабекулы; III - искусственное создание разности потенциалов (по Ю. И. Афанасьеву)
ную ткань. Примером таких соединений являются швы теменных костей черепа, соединительнотканная мембрана между лучевой и локтевой костями.
Синхондрозы (симфизы) - соединения при помощи хряща, например межпозвоночные диски. Они состоят из наружного фиброзного кольца и внутренней части, называемой пульпозным ядром. Обе эти части нерезко отделены и незаметно переходят друг в друга. Пульпозное ядро располагается во внутренней зоне межпозвоночного диска. В разные возрастные периоды оно имеет различное строение. В возрасте до 2 лет оно представляет собой полость с гомогенным содержимым, в котором находятся только отдельные клетки. В последующие годы жизни эта полость разделяется на отдельные камеры. С 6-8-летнего возраста в пуль-позном ядре отмечается появление, а затем и нарастание количества коллагено-вых волокон и хрящевых клеток. С 15 лет нарастание волокон и хрящевых клеток еще больше усиливается, и в возрасте 20-23 лет пульпозное ядро приобретает характерный вид волокнистого хряща. Примером другого, более плотного соединения может быть лобковый симфиз. К синхондрозам относятся также соединения эпифиза и диафиза с помощью метаэпифизарного хряща.
Синостозы - плотные соединения костей без волокнистой соединительной ткани, например тазовые кости.
Прерывистые соединения, или суставы (диартрозы), состоят из сочлененных поверхностей, покрытых хрящом, а в некоторых случаях из хрящевого промежуточного мениска и суставной сумки. Суставная капсула состоит из наружного фиброзного и внутреннего синовиального слоев. Под последним понимают пласт специфически дифференцированной соединительной ткани, содержащей кровеносные и лимфатические сосуды, нервные волокна и окончания. Пограничное положение этой соединительной ткани, несвойственное другим производным мезенхимы, постоянное растяжение, смещение и давление в связи с участием локомоторной функции сочленения определяют рост и ее структурные особенности.
В синовиальной оболочке млекопитающих и человека различают два волокнистых коллагеново-эластических слоя (поверхностный и глубокий) и выстилающий полость покровный слой (см. рис. 8.20). Резкой границы между слоями не существует. В крупных сочленениях отмечается богатый жировой тканью подсиновиальный слой, граничащий с фиброзной капсулой. Коллагеновые и эластические волокна поверхностного слоя ориентированы в направлении длинной оси сочленения. В глубоком слое они расположены под углом к волокнам поверхностного слоя.
Покровный слой синовиальной оболочки состоит из клеток - синовиоцитов. Различают макрофагальные синовиоциты и синовиальные фибробласты, которые обладают способностью к выработке и секреции гиалуроновой кислоты - специфического компонента синовиальной жидкости.
Кровеносные сосуды проникают в синовиальную оболочку со стороны подлежащих тканей и распределяются в ее толще, включая и покровный слой, где они располагаются непосредственно под синовиоцитами. Таким образом, синовиальная полость отделена от кровеносного русла только клетками, основным веществом соединительной ткани и эндотелием самих капилляров. Для эндотелия гемокапил-ляров синовиальных оболочек характерны фенестры и способность к фагоцитозу. Лимфатические капилляры располагаются всегда глубже кровеносных в пределах поверхностного волокнистого слоя.
Синовиальная оболочка богато иннервирована волокнами афферентной и эфферентной (симпатической) природы.
Контрольные вопросы
1. Мезенхима как источник развития соединительных тканей: понятие о дивергентной дифференцировке мезенхимы, морфологические признаки мезенхимы.
2. Соединительные ткани со специальными свойствами: классификация, топография в организме, строение, функции.
3. Клеточные диффероны рыхлой соединительной ткани: источники развития, строение, функции, участие в физиологической и репара-тивной регенерации.
4. Хрящевые ткани: классификация, топография, строение, функции, регенерация.
5. Костные ткани: прямой и непрямой остеогенез, строение, клеточно-дифферонный состав, регенерация.