Гистология, эмбриология, цитология : учебник / Ю. И. Афанасьев, Н. А. Юрина, Е. Ф. Котовский и др.. - 6-е изд., перераб. и доп. - 2012. - 800 с. : ил.
|
|
|
|
Глава 7. КРОВЬ И ЛИМФА. КРОВЕТВОРЕНИЕ
7.1. ПОНЯТИЕ О СИСТЕМЕ КРОВИ
Система крови включает кровь, органы кроветворения - красный костный мозг, вилочковую железу (тимус), селезенку, лимфатические узлы, лим-фоидную ткань некроветворных органов, а также клетки крови в составе соединительной и эпителиальной тканей.
Элементы системы крови связаны генетически и функционально, подчиняются общим законам нейрогуморальной регуляции, объединены тесным взаимодействием всех звеньев. Так, постоянный состав периферической крови поддерживается сбалансированными процессами новообразования (гемопоэза) и разрушения клеток крови. Поэтому понимание вопросов развития, строения и функции отдельных элементов системы возможно лишь с позиций изучения закономерностей, характеризующих систему в целом.
Система крови тесно связана с лимфатической и иммунной системами. Образование иммуноцитов происходит в органах кроветворения, а их циркуляция и рециркуляция - в периферической крови и лимфе.
Кровь и лимфа - ткани мезенхимного происхождения. Они образуют внутреннюю среду организма (вместе с рыхлой соединительной тканью), состоят из плазмы (жидкого межклеточного вещества) и взвешенных в ней форменных элементов. Обе ткани тесно взаимосвязаны, в них происходит постоянный обмен форменными элементами, а также веществами, находящимися в плазме. Установлен факт рециркуляции лимфоцитов из крови в лимфу и из лимфы в кровь. Все клетки крови развиваются из общей полипотентной стволовой клетки крови в эмбриогенезе (эмбриональный гемопоэз) и после рождения (постэмбриональный гемопоэз). Сущность и этапы гемопоэза рассмотрены ниже.
7.2. КРОВЬ
Кровь (sanguis, haema) - это циркулирующая по кровеносным сосудам жидкая ткань, состоящая из двух основных компонентов - плазмы и взве-
шенных в ней форменных элементов: эритроцитов, лейкоцитов и кровяных пластинок. Плазма составляет 55-60 % объема крови, а форменные элементы - 40-45 %. Кровь в организме человека составляет 5-9 % массы тела. В среднем в теле человека с массой тела 70 кг содержится около 5-5,5 л крови.
Функции крови. Основные функции крови: дыхательная (перенос кислорода из легких во все органы и углекислоты из органов в легкие); трофическая (доставка органам питательных веществ); защитная (обеспечение гуморального и клеточного иммунитета, свертывание крови при травмах); выделительная (удаление и транспортировка в почки продуктов обмена веществ); гомеостатическая (поддержание постоянства внутренней среды организма, в том числе иммунного статуса организма). Через кровь (и лимфу) транспортируются также гормоны и другие биологически активные вещества. Все это определяет важнейшую роль крови в организме. Потеря более 30 % крови приводит к смерти. Анализ крови в клинической практике является одним из основных в постановке диагноза.
7.2.1. Плазма крови
Плазма крови представляет собой межклеточное вещество жидкой консистенции. Это сложная смесь белков, аминокислот, углеводов, жиров, солей, гормонов, ферментов, растворенных газов. Плазма содержит 90-93 % воды и 7-10 % сухого вещества, в котором около 6,6-8,5 % белков и 1,5- 3,5 % других органических и минеральных соединений. К основным белкам плазмы крови относятся альбумины, глобулины и фибриноген. Плазма крови имеет рН около 7,36. Подробное описание химического состава плазмы крови дается в учебниках биохимии и физиологии.
7.2.2. Форменные элементы крови
К форменным элементам крови относятся лейкоциты и постклеточные структуры - эритроциты и кровяные пластинки (тромбоциты) (рис. 7.1). Популяция клеток крови обновляющаяся, с коротким циклом развития, где большинство зрелых форм являются конечными (погибающими) клетками.
Эритроциты
Эритроциты, или красные кровяные тельца, человека и большинства млекопитающих - это самые многочисленные форменные элементы крови, утратившие в фило- и онтогенезе ядро и часть органелл (постклеточные структуры). Эритроциты являются высокодифференцированными структурами, не способными к делению. Основная функция эритроцитов - дыхательная - транспортировка кислорода и углекислоты. Эта функция обеспечивается дыхательным пигментом - гемоглобином - сложным белком, имеющим в своем составе железо. Кроме того, эритроциты участвуют в
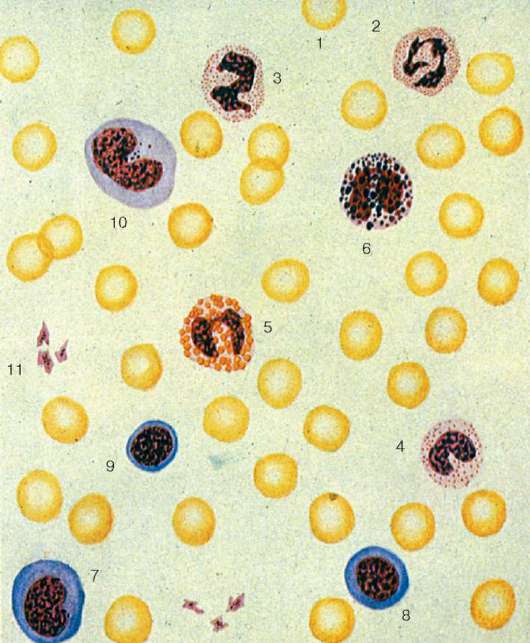
Рис. 7.1. Форменные элементы крови человека:
1 - эритроцит; 2 - сегментоядерный нейтрофильный гранулоцит; 3 - палочкоя-дерный нейтрофильный гранулоцит; 4 - юный нейтрофильный гранулоцит; 5 - эозинофильный (ацидофильный) гранулоцит; 6 - базофильный гранулоцит; 7 - большой лимфоцит; 8 - средний лимфоцит; 9 - малый лимфоцит; 10 - моноцит;
11 - тромбоциты (кровяные пластинки). Мазок, окраска по Романовскому-Гимзе
транспорте аминокислот, антител, токсинов и ряда лекарственных веществ, адсорбируя их на поверхности плазмолеммы.
Количество эритроцитов у взрослого мужчины составляет 3,9-5,5*1012/л, а у женщин - 3,7-4,9*1012/л крови. Однако число эритроцитов у здоровых людей может варьировать в зависимости от возраста, эмоциональной и физической нагрузки, действия экологических факторов и др.
Форма и строение. Популяция эритроцитов неоднородна по их форме и размерам. В нормальной крови человека основную массу (80-90 %) составляют эритроциты двояковогнутой формы - дискоциты. Кроме того, имеются планоциты (с плоской поверхностью) и стареющие формы эритроци-
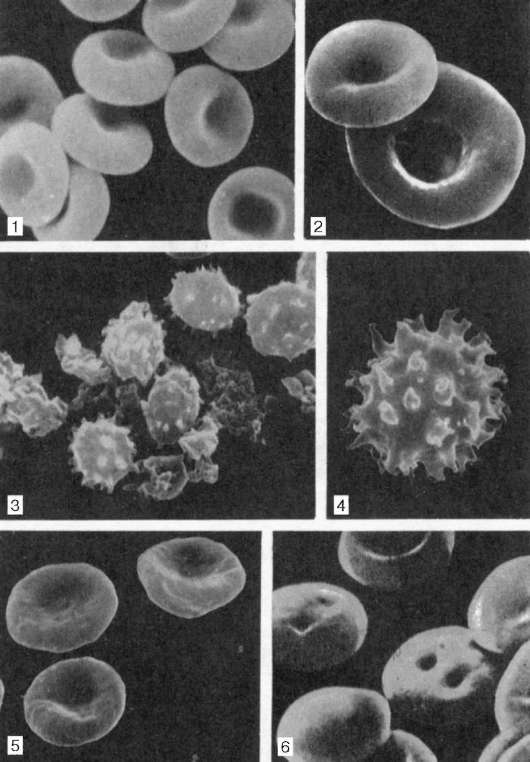
Рис. 7.2. Эритроциты различной формы в сканирующем электронном микроскопе, ув. 8000 (по Г. Н. Никитиной):
1 - дискоциты-нормоциты; 2 - дискоцит-макроцит; 3, 4 - эхиноциты; 5 - стома-тоциты; 6 - сфероцит
тов - шиповидные эритроциты, или эхиноциты (~6 %), куполообразные, или стоматоциты (~1-3 %), и шаровидные, или сфероциты (~1 %) (рис. 7.2). Процесс старения эритроцитов идет двумя путями - кренированием (образование зубцов на плазмолемме) или путем инвагинации участков плазмо-леммы (рис. 7.3).
Одним из проявлений процесса старения эритроцитов служит их гемолиз, сопровождающийся выходом гемоглобина; при этом в крови обна-
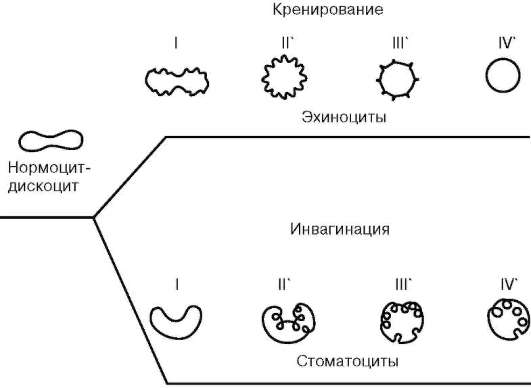
Рис. 7.3. Изменение формы эритроцитов в процессе старения (схема):
I, II, III, IV - стадии развития эхиноцитов и стоматоцитов (по Т. Фуджии)
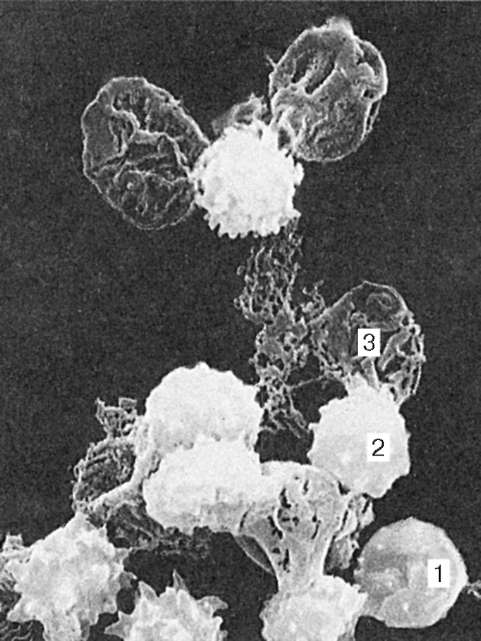
Рис. 7.4. Электронная микрофотография гемолиза эритроцитов и образование их «теней» (по Г. Н. Никитиной): 1 - дискоцит; 2 - эхиноцит; 3 - «тени» эритроцитов. Увеличение 8000
руживаются «тени» (оболочки) эритроцитов (рис. 7.4). Обязательной составной частью популяции эритроцитов являются их молодые формы (1-5 %), называемые ретикулоцитами. В них сохраняются рибосомы и эндо-плазматическая сеть, формирующие зернистые и сетчатые структуры (substantia granulofilamentosa), которые выявляются при специальной супра-витальной окраске (рис. 7.5). При обычной гематологической окраске азуром II-эозином они в отличие от основной массы эритроцитов, окрашивающихся в оранжево-розовый цвет (оксифилия), проявляют полих-роматофилию и окрашиваются в серо-голубой цвет.
При заболеваниях могут появляться аномальные формы эритроцитов, что чаще всего обусловлено изменением структуры гемоглобина (Нb). Замена даже одной аминокислоты в молекуле НЬ может быть причиной изменения формы эри-
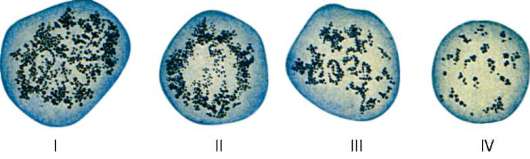
Рис. 7.5. Ретикулоциты (по Г. А. Алексееву и И. А. Кассирскому): зернисто-сетчатая субстанция имеет вид клубка (I), отдельных нитей, розетки (II, III), зернышек (IV)
троцитов. В качестве примера можно привести появление эритроцитов серповидной формы при серповидно-клеточной анемии, когда у больного имеет место генетическое повреждение в β-цепи гемоглобина. Нарушение формы эритроцитов при заболеваниях получило название пойкилоцитоз.
Размеры эритроцитов в нормальной крови также варьируют. Большинство эритроцитов (~75 %) имеют диаметр около 7,5 мкм и называются нормоци-тами. Остальная часть эритроцитов представлена микроцитами (~12,5 %) и макроцитами (~12,5 %). Микроциты имеют диаметр менее 7,5 мкм, а макро-циты - 9-12 мкм. Изменение размеров эритроцитов встречается при заболеваниях крови и называется анизоцитозом.
Плазмолемма. Плазмолемма эритроцита - белково-липидная клеточная мембрана. Она имеет хорошо развитый гликокаликс, образованный олиго-сахарами, входящими в состав гликолипидов, гликосфинголипидов и гли-копротеинов мембраны. Распространены мембранные гликопротеины - гликофорины. С ними связывают антигенные различия между группами крови человека. Гликофорины обнаружены только в эритроцитах. В состав гликофорина входят остатки сиаловой кислоты, придающие отрицательный заряд поверхности эритроцита.
Олигосахариды гликолипидов и гликопротеинов определяют антигенный состав эритроцитов, т. е. наличие в них агглютиногенов. На поверхности эритроцитов выявлены агглютиногены АиВ, в состав которых входят полисахариды, содержащие аминосахара и глюкуроновую кислоту. Они обеспечивают агглютинацию (склеивание) эритроцитов под влиянием соответствующих белков плазмы крови - α-и β-агглютининов, находящихся в составе фракции γ-глобулинов.
По содержанию агглютиногенов и агглютининов различают 4 группы крови: в крови 0(1) группы отсутствуют агглютиногены А и В, но имеются а- и β-агглютини-ны; в крови А(П) группы имеются агглютиноген А и α-агглютинин; в крови В(Ш) группы содержатся В-агглютиноген и α-агглютинин; в крови AB(IV) группы имеются агглютиногены А и В и нет агглютининов. При переливании крови для предотвращения гемолиза (разрушение эритроцитов) нельзя допускать вливания реципиентам эритроцитов с агглютиногенами А или В, имеющим а- и β-агглютинины.
На поверхности эритроцитов имеется также антиген - резус-фактор (Rh-фактор) - агглютиноген. Он присутствует у 86 % людей; у 14 % отсут-
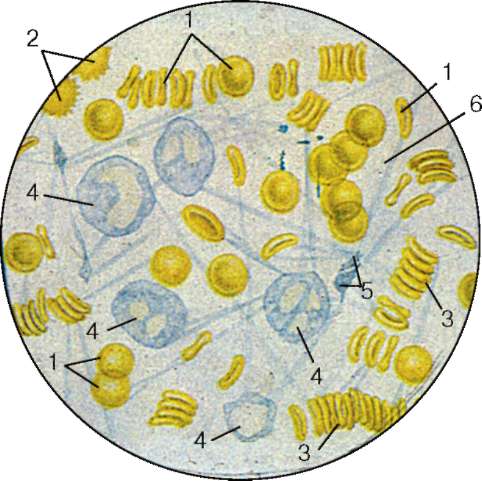
Рис. 7.6. Свежая кровь: 1 - эритроциты (дискоциты); 2 - эритроциты с выростами цитоплазмы (эхи-ноциты); 3 - «монетные столбики» эритроцитов (агглютинированные эритроциты); 4 - лейкоциты; 5 - тромбоциты (кровяные пластинки); 6 - нити фибрина
ствует (резус-отрицательные). Переливание резус-положительной крови резус-отрицательному пациенту вызывает образование резус-антител и гемолиз эритроцитов. Агглютинация эритроцитов свойственна нормальной свежей крови, при этом образуются так называемые «монетные столбики» (рис. 7.6). Это явление связано с потерей заряда плаз-молеммой эритроцитов.
С внутренней стороны плазмо-леммы эритроцита расположена группа белков цитоскелета.
Среди них белок спектрин формирует в примембранном пространстве сеть, которая прикрепляется к плаз-молемме с помощью белков анки-рина и белка полосы 3. Все это обеспечивает плазмолемме упругость и эластичность, а эритроциту - двояковогнутую форму (рис. 7.7, а, б). Скорость оседания (агглютинации) эритроцитов (СОЭ) в 1 ч у здоровых мужчин составляет 4-8 мм и 7-10 мм у женщин. СОЭ может значительно изменяться при заболеваниях, например при воспалительных процессах, и поэтому служит важным диагностическим признаком. В движущейся крови эритроциты отталкиваются из-за наличия на их плазмолемме одноименных отрицательных зарядов. Поверхность плазмолеммы одного эритроцита составляет около 130 мкм2.
Цитоплазма эритроцита состоит из воды (60 %) и сухого остатка (40 %), содержащего около 95 % гемоглобина и 5 % других веществ.
Наличие гемоглобина обусловливает желтую окраску отдельных эритроцитов свежей крови, а совокупность эритроцитов - красный цвет крови. При окрашивании мазка крови азуром II-эозином по Романовскому-Гимзе большинство эритроцитов приобретают оранжево-розовый цвет (оксифиль-ны), что связано с высоким содержанием в них гемоглобина.
В небольшой части эритроцитов (1-5 %), являющихся более молодыми формами, сохраняются остатки органелл (рибосомы, гранулярная эндоплазматическая сеть), которые проявляют базофилию. Такие эритроциты окрашиваются как кислыми красителями (эозин), так и основными (азур II) и называются полихроматофиль-ными. При специальной суправитальной окраске (бриллиант-крезилфиолетовым) в них выявляются сетевидные структуры, поэтому их называют ретикулоцитами. Эритроциты различаются по степени насыщенности гемоглобином. Среди них выделяются нормохромные, гипохромные и гиперхромные, соотношение между которыми значительно изменяется при заболеваниях. Количество гемоглобина в одном эритроците называют цветным показателем. Электронно-микроскопически
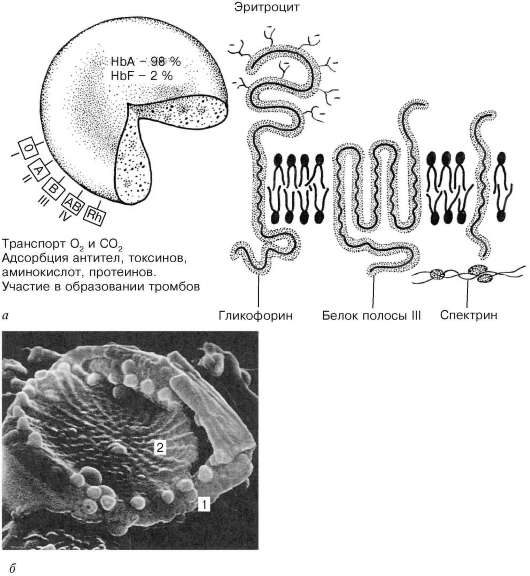
Рис. 7.7. Строение плазмолеммы и цитоскелета эритроцита: а - схема строения эритроцита и расположение белков в плазмолемме; А, В, АВ, Rh - антигены групповой совместимости крови; HbA - гемоглобин взрослого человека; HbF - гемоглобин плода (фетальный); б - плазмолемма и цито-скелет эритроцита в сканирующем электронном микроскопе. 1 - плазмолемма; 2 - сеть спектрина
гемоглобин выявляется в гиалоплазме эритроцита в виде многочисленных плотных гранул диаметром 4-5 нм.
Гемоглобин - это сложный белок (68 килодальтон), состоящий из 4 полипептидных цепей глобина и гема (железосодержащий порфирин), обладающий высокой способностью связывать кислород. В норме у человека содержится два типа гемоглобина - НbА и HbF. Эти гемоглобины различаются составом аминокислот в глобиновой (белковой) части.
У взрослых людей в эритроцитах преобладает НbА (от англ. adult - взрослый), составляя 98 %. HbF, или фетальный гемоглобин (от англ. foetus - плод), составляет у взрослых около 2 % и преобладает у плодов. К моменту рождения ребенка HbF составляет около 80 %, а НЬА только 20 %. Эти гемоглобины различаются составом аминокислот в глобино-
вой (белковой) части. В связи с этим сродство к кислороду у фетального гемоглобина выше, чем у гемоглобина взрослых. В результате кислород из крови матери легко переходит к фетальному гемоглобину плода.
Железо (Fe2+) в геме может присоединять О2 в легких (в таких случаях образуется оксигемоглобин - НЬ02) и отдавать его в тканях путем диссоциации НЬО, на кислород (О2) и НЬ; валентность Fe2+ не изменяется.
При ряде заболеваний (гемоглобинозы, гемоглобинопатии) в эритроцитах появляются другие виды гемоглобинов, которые характеризуются изменением аминокислотного состава в белковой части гемоглобина.
В настоящее время выявлено более 150 видов аномальных гемоглобинов. Например, при серповидно-клеточной анемии имеет место генетически обусловленное повреждение в β-цепи гемоглобина - глутаминовая кислота заменена на аминокислоту валин. Такой гемоглобин обозначается как HbS (от англ. sickle - серп). Эритроциты в условиях понижения парциального давления О2 приобретают форму серпов, полулуний. В ряде стран тропического пояса определенный контингент людей являются гетерозиготными для серповидных генов, а дети двух гетерозиготных родителей по законам наследственности имеют либо нормальный тип (25 %), либо бывают гетерозиготными носителями, и 25 % страдают серповидно-клеточной анемией.
Гемоглобин способен связывать О2 в легких, при этом образуется оксигемоглобин, который транспортируется ко всем органам и тканям и там отдает О2. В тканях выделяемая СО2 поступает в эритроциты и соединяется с НЬ, образуя карбоксигемоглобин. При разрушении эритроцитов (старых или при воздействии различных факторов - токсины, радиация и др.) гемоглобин выходит из клеток, и это явление называется гемолизом. Старые эритроциты разрушаются макрофагами главным образом в селезенке, а также в печени и костном мозге, при этом НЬ распадается, а высвобождающееся из железосодержащего гема железо используется для образования новых эритроцитов.
В макрофагах гемоглобин распадается на пигмент билирубин и гемосидерин - аморфные агрегаты, содержащие железо. Железо гемосидерина связывается с транс-феррином - негеминовым белком плазмы, содержащим железо, и захватывается специальными макрофагами костного мозга. В процессе образования эритроцитов (эритропоэз) эти макрофаги передают трансферрин в формирующиеся эритроциты. В цитоплазме эритроцитов содержатся ферменты анаэробного гликолиза, с помощью которых синтезируются АТФ и NADН, обеспечивающие энергией главные процессы, связанные с переносом О2 и СО2, а также поддержание осмотического давления и перенос ионов через плазмолемму эритроцита. Энергия гликолиза обеспечивает активный транспорт катионов через плазмолемму, поддержание оптимального соотношения концентрации К+ и Na+ в эритроцитах и плазме крови, сохранение формы и целостности мембраны эритроцита. NАDН участвует в метаболизме НЬ, предотвращая его окисление в метгемоглобин.
Эритроциты участвуют в транспорте аминокислот и полипептидов, регулируют их концентрацию в плазме крови, т. е. играют роль буферной системы. Постоянство концентрации аминокислот и полипептидов в плазме крови
поддерживается с помощью эритроцитов, которые адсорбируют их избыток из плазмы, а затем отдают различным тканям и органам. Таким образом, эритроциты являются подвижным депо аминокислот и полипептидов.
Сорбционная способность эритроцитов связана с состоянием газового режима (парциальное давление О2 и СО2 - Ро2, Рсо2): в частности при действии О2 наблюдаются выход аминокислот из эритроцитов и увеличение их содержания в плазме.
Продолжительность жизни и старение эритроцитов. Средняя продолжительность жизни эритроцитов составляет от 70 до 120 сут. В организме ежедневно разрушается около 200 млн эритроцитов. При их старении происходят изменения в плазмолемме эритроцита: в частности в гликокаликсе снижается содержание сиаловых кислот, определяющих отрицательный заряд плазмолеммы. Отмечаются изменения цитоскелетного белка спектрина, что приводит к преобразованию дисковидной формы эритроцита в сферическую. В плазмолем-ме появляются специфические рецепторы аутологичных антител (IgGl, IgG2), которые при взаимодействии с этими антителами образуют комплексы, обеспечивающие «узнавание» их макрофагами и последующий фагоцитоз. В стареющих эритроцитах снижаются интенсивность гликолиза и соответственно содержание АТФ. Вследствие нарушения проницаемости плазмолеммы снижается осмотическая резистентность, наблюдаются выход из эритроцитов ионов К+ в плазму и увеличение в них содержания Na+. При старении эритроцитов отмечается нарушение их газообменной функции.
Лейкоциты
Общая характеристика и классификация. Лейкоциты (leucocytus), или белые кровяные клетки, в свежей крови бесцветны, что отличает их от окрашенных эритроцитов. Число их составляет в среднем 4-9409/л, т. е. в 1000 раз меньше, чем эритроцитов. Лейкоциты в кровяном русле и лимфе способны к активным движениям, могут проходить через стенку сосудов в соединительную ткань органов, где они выполняют основные защитные функции. По морфологическим признакам и биологической роли лейкоциты подразделяют на две группы: зернистые лейкоциты, или гранулоциты (granulocytus), и незернистые лейкоциты, или агранулоциты (agranulocytus).
У зернистых лейкоцитов при окраске крови по Романовскому-Гимзе смесью кислого (эозин) и основного (азур II) красителей в цитоплазме выявляются специфическая зернистость (эозинофильная, базофильная или нейтрофильная) и сегментированные ядра. В соответствии с окраской специфической зернистости различают нейтрофильные, эозинофильные и базофиль-ные гранулоциты (см. рис. 7.1). Группа незернистых лейкоцитов - лимфоциты и моноциты - характеризуется отсутствием специфической зернистости и несегментированными ядрами. Процентное соотношение основных видов лейкоцитов называется лейкоцитарной формулой. Общее число лейкоцитов и их процентное соотношение у человека могут изменяться в норме в зависимости от употребляемой пищи, физического и умственного напряжения и при различных заболеваниях. Именно поэтому исследование показателей крови необходимо для установления диагноза и назначения лечения.
Все лейкоциты способны к активному перемещению путем образования псевдоподий, при этом у них изменяется форма тела и ядра. Они способны проходить между клетками эндотелия сосудов и клетками эпителия, через базальные мембраны и перемещаться по основному веществу (матриксу) соединительной ткани. Скорость движения лейкоцитов зависит от следующих условий: температуры, химического состава, рН, консистенции среды и др. Направление движения лейкоцитов определяется хемотаксисом под влиянием химических раздражителей - продуктов распада тканей, бактерий и др. Лейкоциты выполняют защитные функции, обеспечивая фагоцитоз микробов (гранулоциты, макрофаги), инородных веществ, продуктов распада клеток (моноциты - макрофаги), участвуя в иммунных реакциях (лимфоциты, макрофаги).
Гранулоциты (зернистые лейкоциты)
К гранулоцитам относятся нейтрофильные, эозинофильные и базофиль-ные лейкоциты. Они образуются в красном костном мозге, содержат специфическую зернистость в цитоплазме и имеют сегментированные ядра.
Нейтрофильные гранулоциты (нейтрофильные лейкоциты, или нейтро-филы) - самая многочисленная группа лейкоцитов, составляющая 2,0- 5,5-109/л крови (48-78 % общего числа лейкоцитов). Их диаметр в мазке крови 10-12 мкм, а в капле свежей крови 7-9 мкм. В зрелом сегментоядер-ном нейтрофиле ядро имеет 3-5 сегментов, соединенных тонкими перемычками. В ядре гетерохроматин занимает широкую зону по периферии ядра, а эухроматин расположен в центре. Для женщин характерно наличие в ряде нейтрофилов полового хроматина (Х-хромосома) в виде барабанной палочки - тельце Барра (corpusculum chromatini sexualis), которое имеет форму висячей капли и соединено с ядром тонкой перемычкой. В популяции ней-трофилов крови могут находиться клетки различной степени зрелости - юные, палочкоядерные и сегментоядерные. Первые два вида - молодые клетки. Доля юных клеток в норме не превышает 0,5 % или они вообще отсутствуют. Эти клетки характеризуются бобовидным ядром. Палочкоядерные составляют 1-6 %, имеют несегментированное ядро в форме буквы S, изогнутой палочки или подковы. Увеличение содержания в крови юных и палочкоя-дерных нейтрофилов свидетельствует о наличии кровопотери или воспалительного процесса, сопровождающихся усилением гемопоэза в костном мозге и выходом молодых форм. Цитоплазма нейтрофилов при окраске по Романовскому-Гимзе окрашивается слабооксифильно, в ней видна очень мелкая зернистость розово-фиолетового цвета (окрашивается кислыми и основными красками), поэтому называется нейтрофильной, или гетерофильной. В поверхностном слое цитоплазмы зернистость и органеллы отсутствуют. Здесь расположены гранулы гликогена, актиновые филаменты и микротрубочки, обеспечивающие образование псевдоподий для движения клетки. Сокращение актиновых филаментов обеспечивает передвижение клетки по соединительной ткани.
Во внутренней части цитоплазмы расположены органеллы (комплекс Гольджи, гранулярная эндоплазматическая сеть, единичные митохондрии),
видна зернистость. Число зерен в каждом нейтрофиле варьирует и составляет 50-200.
В нейтрофилах можно различить два типа гранул: специфические и азуро-фильные, окруженные одинарной мембраной (рис. 7.8, а). Специфические гранулы, более светлые, мелкие и многочисленные, составляют 80-90 % всех гранул. Их размер около 0,2 мкм, они электронно-прозрачны, но могут содержать кристаллоид. В них обнаружены щелочная фос-фатаза, бактерицидные ферменты (лизоцим, лактоферрин), белок, связывающий витамин В12, коллагеназа. Азурофильные гранулы (лизосомо-подобные) более крупные (~0,4 мкм), окрашиваются в фиолетово-красный цвет, имеют электронно-плотную сердцевину; их количество составляет 10-20 % всей популяции гранул. В них содержатся миелопероксидаза, набор разнообразных гидролитических ферментов, катионные белки, лизоцим, гликозаминогликаны. Азу-рофильные гранулы в процессе диф-ференцировки нейтрофилов в костном мозге появляются раньше, поэтому называются первичными в отличие от вторичных - специфических. Основная функция нейтрофи-лов - фагоцитоз микроорганизмов, поэтому их называют микрофагами. В процессе фагоцитоза бактерий сначала (в течение 0,5-1 мин) с образующейся фагосомой (захваченная
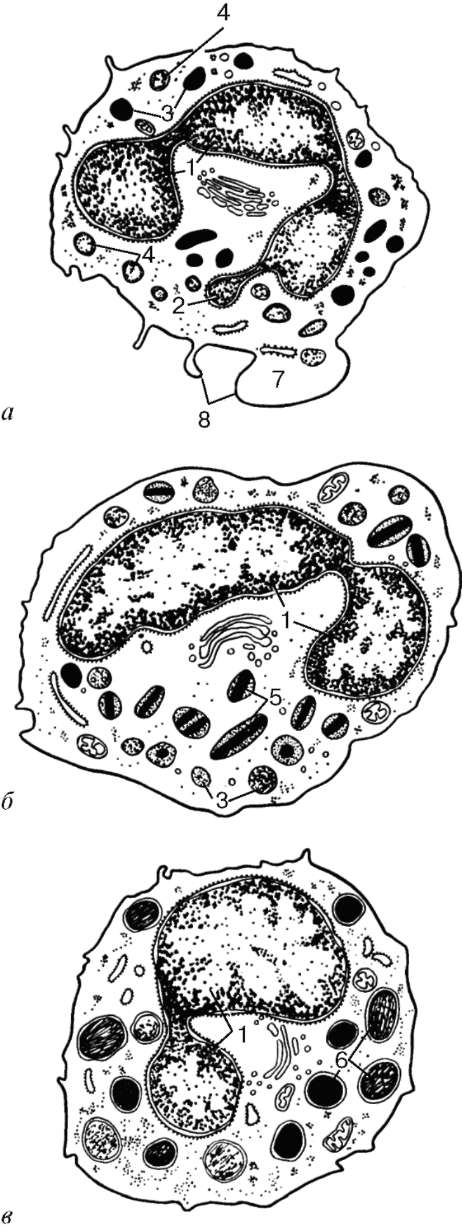
Рис. 7.8. Ультрамикроскопическое строение гранулоцитов (по Н. А. Юриной и Л. С. Румянцевой):
а - сегментоядерный нейтрофильный гранулоцит; б - эозинофильный (ацидофильный) гранулоцит; в - базофильный гранулоцит. 1 - сегменты ядра; 2 - тельце полового хроматина; 3 - первичные (азурофильные) гранулы; 4 - вторичные (специфические) гранулы; 5 - зрелые специфические гранулы эозинофила, содержащие кристаллоиды; 6 - гранулы базофила различной величины и плотности; 7 - периферическая зона цитоплазмы, не содержащая органелл; 8 - микроворсинки и псевдоподии
бактерия) сливаются специфические гранулы, ферменты которой убивают бактерию, при этом образуется комплекс, состоящий из фагосомы и специфической гранулы. Позднее с этим комплексом сливается лизосома, гидролитические ферменты которой переваривают микроорганизмы. При распаде нейтрофилов и бактериальных токсинов выделяются вещества, которые названы пирогенами. Последние с током крови попадают к центрам регуляции температуры тела, вызывают ее повышение. Кроме того, стимулируют образование нейтрофилов в костном мозге.
В популяции нейтрофилов у здоровых людей в возрасте 18-45 лет фагоцитирующие клетки составляют 69-99 %. Этот показатель называют фагоцитарной активностью. Фагоцитарный индекс - другой показатель, которым оценивается число частиц, поглощенных одной клеткой. Для нейтрофилов он равен 12-23. Нейтрофилы циркулируют в крови 8-12 ч, в тканях находятся 5-7 сут.
Эозинофильные (ацидофильные) гранулоциты (эозинофилы). Количество эозинофилов в крови составляет 0,02- 0,3*109/л, или 0,5-5 % общего числа лейкоцитов. Их диаметр в мазке крови равен 12-14 мкм, в капле свежей крови - 9-10. Ядро эозинофилов имеет, как правило, 2 сегмента, соединенных перемычкой. В цитоплазме расположены органеллы - комплекс Гольджи (около ядра), немногочисленные митохондрии, актиновые фила-менты в цитоплазме под плазмолеммой и гранулы числом до 200. Среди гранул различают азурофильные (первичные) и эозинофильные (вторичные), являющиеся модифицированными лизосомами. Они электронно-плотные, содержат гидролитические ферменты (см. рис. 7.8, б). Специфические эозинофильные гранулы заполняют почти всю цитоплазму, имеют размер 0,6-1 мкм. Характерно наличие в центре гранулы кристаллоида, который содержит главный основной белок, богатый аргинином (что обусловливает оксифилию гранул), лизосомные гидролитические ферменты, пероксидазу и другие белки - эозинофильный катионный белок, гистаминазу (рис. 7.9).
Электронно-микроскопически в экваториальной плоскости эозино-фильных гранул выявляются единичные или множественные кристаллоид-ные структуры, имеющие пластинчатое строение, погруженные в тонкозернистый матрикс гранулы. Кристаллоиды эозинофильных гранул содержат главный основной белок (major basic protein), который участвует в обеспечении антипаразитарной функции эозинофилов.
Плазмолемма имеет рецепторы: Fc-рецептор иммуноглобулина Е (IgE) (участвует в аллергических реакциях), IgG и IgM, а также С3- и С4-рецепторы. Эозинофилы являются подвижными клетками и способны к фагоцитозу, однако их фагоцитарная активность ниже, чем у нейтрофилов.
Эозинофилы обладают положительным хемотаксисом к гистамину, выделяемому тучными клетками (особенно при воспалении и аллергических реакциях), к лимфокинам, выделяемым стимулированными Т-лимфоцитами, и иммунным комплексам, состоящим из антигенов и антител (см. главу 14).
Выявлена роль эозинофилов в реакциях на чужеродный белок, в аллергических и анафилактических реакциях, где они участвуют в метаболизме гистамина, вырабатываемого тучными клетками. Гистамин повышает проницаемость сосудов,
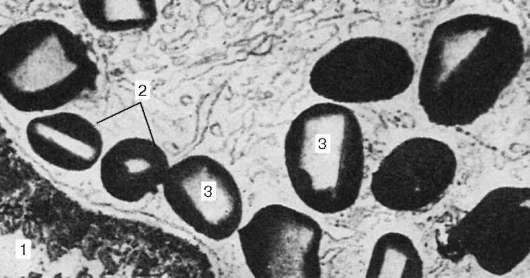
Рис. 7.9. Гранулы эозинофильных гранулоцитов (по Д. Байнтону и М. Фарквару): 1 - ядро; 2 - пероксидаза в зрелых гранулоцитах; 3 - кристаллический центр зрелых гранул с отрицательной реакцией на пероксидазу. Реакция на пероксидазу. Электронная микрофотография. Увеличение 12 000
вызывает развитие отека тканей; в больших концентрациях может вызвать шок со смертельным исходом.
Эозинофилы способствуют снижению содержания гистамина в тканях различными путями. Они разрушают гистамин с помощью фермента гистаминазы, фагоцитируют гистаминсодержащие гранулы тучных клеток, адсорбируют гистамин на плазмолемме, связывая его с помощью рецепторов, и, наконец, вырабатывают фактор, тормозящий дегрануляцию и освобождение гистамина из тучных клеток.
Специфической функцией эозинофилов является антипаразитарная. При паразитарных заболеваниях (гельминтозы, шистосомоз и др.) наблюдается значительное увеличение числа эозинофилов - до 90 % общего числа лейкоцитов. Эозинофилы убивают личинки паразитов, поступившие в кровь или органы (например, в слизистую оболочку кишки).
Они привлекаются в очаги воспаления хемотаксическими факторами и прилипают к паразитам благодаря наличию на них обволакивающих компонентов комплемента крови. При этом происходят дегрануляция эозинофилов и выделение белка, разрушающего кутикулу паразитов.
Эозинофилы находятся в периферической крови менее 12 ч и потом переходят в ткани. Их мишенями являются такие органы, как кожа, легкие и пищеварительный тракт, где они выполняют свои функции в течение 8-12 сут. Изменение содержания эозинофилов может наблюдаться под действием медиаторов и гормонов: например, при стресс-реакции отмечается снижение числа эозинофилов в крови, обусловленное увеличением содержания гормонов надпочечников.
Базофильные гранулоциты (базофилы). Количество базофилов в крови составляет 0-0,06×109/л, или 0-1 % общего числа лейкоцитов. Их диаметр в мазке крови составляет 11-12 мкм, в капле свежей крови - около 9 мкм.
Ядра базофилов сегментированы, имеют 2-3 дольки; в цитоплазме выявляются все виды органелл - эндоплазматическая сеть, рибосомы, комплекс Гольджи, митохондрии, актиновые филаменты (см. рис. 7.8, в). Характерно наличие специфических крупных метахроматических гранул числом около 400, часто закрывающих ядро, размеры которых варьируют от 0,5 до 1,2 мкм. Метахромазия (азур II окрашивает гранулы в фиолетовый цвет) обусловлена наличием гепарина - гликозаминогликана. Специфические гранулы содержат пероксидазу, гистамин, гепарин, АТФ, факторы хемотаксиса нейтрофилов и эозинофилов и др. Часть гранул представляют собой модифицированные лизосомы. При электронно-микроскопическом исследовании видны окружающая гранулы мембрана и кристаллическая область. Гранулы неоднородны по электронной плотности. Помимо специфических гранул, в базофилах содержатся и азурофильные гранулы (лизосомы). Базофилы, как и тучные клетки соединительной ткани, выделяя гепарин и гистамин, участвуют в регуляции процессов свертывания крови и проницаемости стенки сосудов. Базофилы участвуют в иммунологических реакциях организма. Дегрануляция базофилов происходит при реакциях гиперчувствительности немедленного типа (например, при астме, анафилаксии, сыпи, которая может ассоциироваться с покраснением кожи).
Базофилы образуются в костном мозге. Они циркулируют в крови до 1 сут, затем мигрируют в ткани, где в течение 1-2 сут выполняют свои функции и затем погибают.
Агранулоциты (незернистые лейкоциты)
К этой группе лейкоцитов относятся лимфоциты и моноциты. В отличие от гранулоцитов они не содержат в цитоплазме специфической зернистости, а их ядра не сегментированы.
Лимфоциты (lymphocytus). В крови взрослых людей они составляют 20-35 % общего числа лейкоцитов (1,0-4,0×109/л). Величина лимфоцитов в мазке крови значительно варьирует - от 4,5 до 10 мкм. Среди них различают малые лимфоциты (диаметром 4,5-6 мкм), средние (диаметром 7-10 мкм) и большие (диаметром 10 мкм и более) (см. рис. 7.1). Большие лимфоциты встречаются в крови новорожденных и детей, у взрослых они отсутствуют. Для всех видов лимфоцитов характерно наличие интенсивно окрашенного ядра округлой или бобовидной формы, содержащего компактный гетеро-хроматин, и относительно узкого ободка базофильной цитоплазмы. В цитоплазме некоторых лимфоцитов содержится небольшое количество азуро-фильных гранул (лизосомы). Малые лимфоциты составляют большую часть (85-90 %) всех лимфоцитов крови человека. При электронной микроскопии в их ядрах выявляются небольшие впячивания; гетерохроматин расположен преимущественно по периферии ядра (рис. 7.10). В цитоплазме обнаруживаются пузырьки, лизосомы, свободные рибосомы, полисомы, митохондрии, комплекс Гольджи, центриоли, небольшое количество элементов гранулярной эндоплазматической сети. Среди малых лимфоцитов различают светлые и темные. Малые темные лимфоциты меньше светлых, имеют более плотное ядро, более узкий ободок базофильной цитоплазмы, обладающей
высокой электронной плотностью. В цитоплазме расположено большое количество рибосом.
Средние лимфоциты составляют около 10-12 % лимфоцитов крови человека. Ядра этих клеток округлые, иногда бобовидные с пальцевидным впячиванием ядерной оболочки. Хроматин более рыхлый, ядрышко хорошо выражено. В цитоплазме расположены удлиненные канальцы гранулярной эндоплазматической сети, элементы агранулярной сети, свободные рибосомы и полисомы, лизосо-мы. Центросома и комплекс Гольджи расположены рядом с областью инвагинации ядерной оболочки.
Кроме типичных лимфоцитов, в крови человека в небольшом коли-
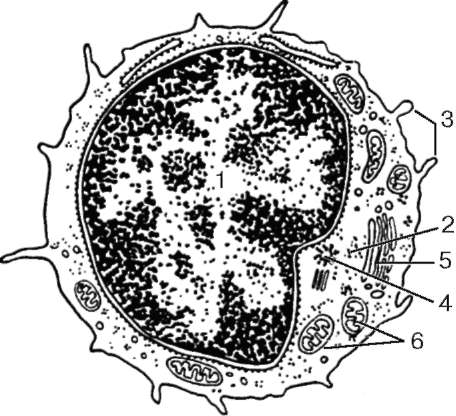
Рис. 7.10. Ультрамикроскопическое строение лимфоцита (по Н. А. Юриной, Л. С. Румянцевой):
1 - ядро; 2 - рибосомы; 3 - микроворсинки; 4 - центриоль; 5 - комплекс Гольджи; 6 - митохондрии
честве могут встречаться лимфоплазмоциты (около 1-2 %), которые отличаются концентрическим расположением вокруг ядра канальцев гранулярной эндоплазматической сети.
Основной функцией лимфоцитов является участие в иммунных реакциях. Однако популяция лимфоцитов разнообразна по характеристике поверхностных рецепторов и роли в реакциях иммунитета.
Среди лимфоцитов различают три основных функциональных класса: В-лимфоциты, Т-лимфоциты и нулевые лимфоциты.
В-лимфоциты впервые были обнаружены в фабрициевой сумке птиц (bursa Fabricius), поэтому и получили соответствующее название. Они образуются у эмбриона человека из стволовых клеток - в печени и костном мозге, а у взрослого - в костном мозге.
В-лимфоциты составляют около 30 % циркулирующих лимфоцитов. Их главная функция - участие в выработке антител, т. е. обеспечение гуморального иммунитета. Плазмолемма В-лимфоцитов содержит множество рецепторов иммуноглобулина. При действии антигенов В-лимфоциты способны к пролиферации и дифференцировке в плазмоциты - клетки, способные синтезировать и секретировать защитные белки - иммуноглобулины (Ig), которые поступают в кровь, обеспечивая гуморальный иммунитет.
Т-лимфоциты, или тимусзависимые лимфоциты, образуются из стволовых клеток костного мозга, а созревают в тимусе, что и обусловило их название. Они преобладают в популяции лимфоцитов, составляя около 70 % циркулирующих лимфоцитов. Для Т-клеток, в отличие от В-лимфоцитов, характерен низкий уровень рецепторов иммуноглобулина в плазмолемме. Однако Т-клетки имеют специфические рецепторы, способные распознавать и связывать антигены, участвовать в иммунных реакциях. Основными функциями Т-лимфоцитов являются обеспечение реакций клеточного иммунитета
и регуляция гуморального иммунитета (стимуляция или подавление диф-ференцировки В-лимфоцитов). Т-лимфоциты способны к выработке лим-фокинов, которые регулируют деятельность В-лимфоцитов и других клеток в иммунных реакциях. Среди Т-лимфоцитов выявлено несколько функциональных групп: Т-хелперы, Т-супрессоры, Т-киллеры. Подробную характеристику В-лимфоцитов и различных групп Т-лимфоцитов, их участие в реакциях иммунитета - см. в главе 14.
В настоящее время оценка иммунного статуса организма в клинике проводится с помощью иммунологических и иммуноморфологических методов выявления различных видов лимфоцитов.
Продолжительность жизни лимфоцитов варьирует от нескольких недель до нескольких лет. Т-лимфоциты являются «долгоживущими» (месяцы и годы) клетками, а В-лимфоциты относятся к «короткоживущим» (недели и месяцы).
Для Т-лимфоцитов характерно явление рециркуляции, т. е. выход из крови в ткани и возвращение по лимфатическим путям снова в кровь. Таким образом, они осуществляют иммунологический надзор за состоянием всех органов, быстро реагируя на внедрение чужеродных агентов.
Среди клеток, имеющих строение, характерное для малых лимфоцитов, следует назвать циркулирующие стволовые клетки крови (СКК), которые поступают в кровь из костного мозга. Впервые эти клетки были описаны А. А. Максимовым и обозначены как «подвижный мезенхимный резерв». Из СКК, поступающих в кроветворные органы, дифференцируются различные клетки крови, а из СКК, поступающих в соединительную ткань, - тучные клетки, фибробласты и др. СКК составляют 0,1 % общего числа клеток крови. Диаметр клетки 8-10 мкм, ядро содержит 1-2 ядрышка. Цитоплазма без включений, в которой обнаруживаются рибосомы и небольшое количество митохондрий.
Моноциты (monocytus). В капле свежей крови эти клетки лишь немного крупнее других лейкоцитов (9-12 мкм), в мазке крови они сильно распластываются по стеклу, и размер их достигает 18-20 мкм. В крови человека количество моноцитов колеблется в пределах 6-8 % общего числа лейкоцитов.
Ядра моноцитов разнообразной и изменчивой конфигурации: встречаются бобовидные, подковообразные, редко - дольчатые ядра с многочисленными выступами и углублениями. Гетерохроматин рассеян мелкими зернами по всему ядру, но обычно в больших количествах он располагается под ядерной оболочкой. В ядре моноцита содержится одно или несколько маленьких ядрышек (см. рис. 7.1; рис. 7.11).
Цитоплазма моноцитов менее базофильна, чем цитоплазма лимфоцитов. При окраске по Романовскому-Гимзе она имеет бледно-голубой цвет, но по периферии окрашивается несколько темнее, чем около ядра; в ней содержится различное количество очень мелких азурофильных зерен (лизосом).
Характерно наличие пальцеобразных выростов цитоплазмы и образование фагоцитарных вакуолей. В цитоплазме расположено множество пино-цитозных пузырьков. Имеются короткие канальцы гранулярной эндоплаз-
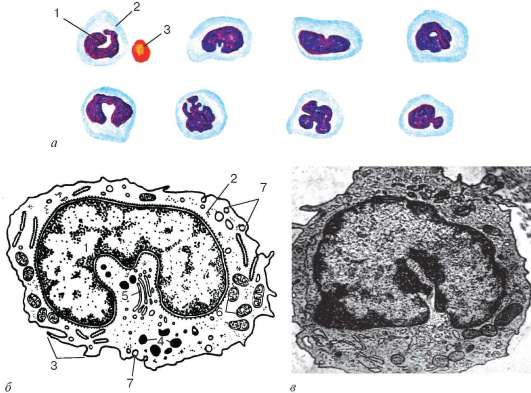
Рис. 7.11. Строение моноцитов:
а - разновидности моноцитов по размерам и форме в мазке крови человека. Окраска по Романовскому-Гимзе (по Ю. И. Афанасьеву): 1 - ядро; 2 - цитоплазма; 3 - эритроцит; б - схема ультрамикроскопического строения моноцитов (по Н. А. Юриной, Л. С. Румянцевой): 1 - ядро; 2 - рибосомы; 3 - микроворсинки; 4 - лизосомы; 5 - комплекс Гольджи; 6 - митохондрии; 7 - пиноцитозные пузырьки; в - электронная микрофотография (по Н. А. Юриной, А. И. Радостиной). Увеличение 15 000
матической сети, а также небольшие митохондрии. Моноциты относятся к макрофагической системе организма, или к так называемой мононуклеарной фагоцитарной системе (МФС), объединяющей моноциты крови и макрофаги различных органов (макрофаги альвеол легкого, костного мозга, лимфатических узлов, селезенки, гистиоциты соединительной ткани, остеокласты, глиальные макрофаги ЦНС и др.). Клетки этой системы характеризуются происхождением из промоноцитов костного мозга, способностью прикрепляться к поверхности стекла, активностью пиноцитоза и иммунного фагоцитоза, наличием на плазмолемме рецепторов иммуноглобулинов и комплемента. Моноциты циркулирующей крови представляют собой подвижный пул относительно незрелых клеток, находящихся на пути из костного мозга в ткани. В кровотоке моноциты циркулируют 12-32 ч, затем выселяются в ткани. Продолжительность жизни в ткани - в пределах 1 мес. При этом они увеличиваются в размерах, появляется большое число лизосом, возникают рецепторы иммуноглобулинов (антител), повышается фагоцитарная активность, клетки могут сливаться друг с другом с обра-
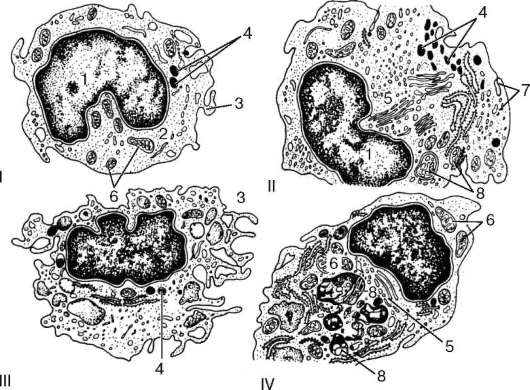
Рис. 7.12. Дифференцировка моноцита в макрофаг (по А. И. Радостиной): I - моноцит; II - дифференцирующийся макрофаг; III, IV - зрелые макрофаги. 1 - ядро; 2 - рибосомы; 3 - микроворсинки и складки; 4 - лизосомы; 5 - комплекс Гольджи; 6 - митохондрии; 7 - пиноцитозные пузырьки; 8 - фаголизосомы
зованием гигантских форм. Клетки способны синтезировать и выделять множество веществ, влияющих на кроветворение, активность лейкоцитов, развитие воспалительной реакции и др. (рис. 7.12).
Кровяные пластинки
Кровяные пластинки, тромбоциты (thrombocytus), в свежей крови человека имеют вид мелких бесцветных телец округлой, овальной или веретено-видной формы размером 2-4 мкм. Они могут объединяться (агглютинироваться) в маленькие или большие группы. Количество их в крови человека колеблется от 2,0×109/л до 4,0×109/л. Кровяные пластинки представляют собой безъядерные фрагменты цитоплазмы, отделившиеся от мегакариоцитов - гигантских клеток костного мозга.
Тромбоциты в кровотоке имеют форму двояковыпуклого диска. При окраске мазков крови азуром II-эозином в кровяных пластинках выявляются более светлая периферическая часть - гиаломер и более темная, зернистая часть - грануломер, структура и окраска которых могут варьировать в зависимости от стадии развития кровяных пластинок. В популяции тромбоцитов находятся как более молодые, так и более дифференцированные и стареющие формы. Гиаломер в молодых пластинках окрашивается в голубой цвет (базофильный), а в зрелых - в розовый (оксифильный).
В популяции тромбоцитов различают пять основных форм: 1) юные - с голубым (базофильным) гиаломером и единичными азурофильными гранулами в гра-нуломере красновато-фиолетового цвета (1-5 %); 2) зрелые - со слабо-розовым
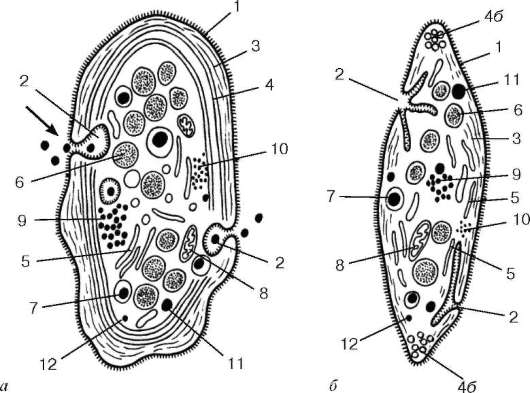
Рис. 7.13. Ультрамикроскопическое строение тромбоцита (кровяной пластинки) (по Н. А. Юриной):
а - горизонтальный срез; б - поперечный срез. 1 - плазмолемма с гликокаликсом; 2 - открытая система канальцев, связанная с инвагинациями плазмолеммы; 3 - актиновые филаменты; 4 - циркулярные пучки микротрубочек; 4б - микротрубочки в поперечном разрезе; 5 - плотная тубулярная система; 6 - альфа-гранулы; 7 - бета-гранулы; 8 - митохондрии; 9 - гранулы гликогена; 10 - гранулы ферритина; 11 - лизосомы; 12 - пероксисомы
(оксифильным) гиаломером и хорошо развитой азурофильной зернистостью в гра-нуломере (88 %); 3) старые - с более темным гиаломером и грануломером (4 %); 4) дегенеративные - с серовато-синим гиаломером и плотным темно-фиолетовым грануломером (до 2 %); 5) гигантские формы раздражения - с розовато-сиреневым гиаломером и фиолетовым грануломером, размерами 4-6 мкм (2 %). Молодые формы тромбоцитов крупнее старых.
При заболеваниях соотношение различных форм тромбоцитов может изменяться, что учитывается при постановке диагноза. Повышенное количество юных форм наблюдается у новорожденных. При онкологических заболеваниях увеличивается число старых тромбоцитов.
Плазмолемма имеет толстый слой гликокаликса (15-20 нм), образует инвагинации с отходящими канальцами, также покрытыми гликокаликсом. В плазмолемме содержатся гликопротеины, которые выполняют функцию поверхностных рецепторов, участвующих в процессах адгезии и агрегации кровяных пластинок (рис. 7.13).
Цитоскелет в тромбоцитах хорошо развит и представлен актиновыми микрофиламентами и пучками (по 10-15) микротрубочек, расположенными циркулярно в гиаломере и примыкающими к внутренней части плазмо-леммы. Элементы цитоскелета обеспечивают поддержание формы кровяных пластинок, участвуют в образовании их отростков. Актиновые филамен-
ты участвуют в сокращении объема (ретракции) образующихся кровяных тромбов.
В кровяных пластинках имеются две системы канальцев и трубочек, хорошо видных в гиаломере при электронной микроскопии. Первая - это открытая система каналов, связанная, как уже отмечалось, с инвагинациями плазмолеммы. Через эту систему выделяется в плазму содержимое гранул кровяных пластинок и происходит поглощение веществ. Вторая - это так называемая плотная тубулярная система, которая представлена группами трубочек с электронно-плотным аморфным материалом. Она имеет сходство с гладкой эндоплазматической сетью, образуется в комплексе Гольджи.
В грануломере выявлены органеллы, включения и специальные гранулы. Органеллы представлены рибосомами (в молодых пластинках), элементами эндоплазматической сети, комплексом Гольджи, митохондриями, лизосо-мами, пероксисомами. Имеются включения гликогена и ферритина в виде мелких гранул.
Специальные гранулы в количестве 60-120 составляют основную часть грануломера и представлены двумя главными типами. Первый тип: а-грану-лы (альфа-гранулы) - это самые крупные (300-500 нм) гранулы, имеющие мелкозернистую центральную часть, отделенную от окружающей мембраны небольшим светлым пространством. В них обнаружены различные белки и гликопротеины, принимающие участие в процессах свертывания крови, факторы роста, литические ферменты.
Второй тип гранул - δ-гранулы (дельта-гранулы) - представлен плотными тельцами размером 250-300 нм, в которых имеется эксцентрично расположенная плотная сердцевина. Главными компонентами гранул являются серотонин, накапливаемый из плазмы, и другие биогенные амины (гистамин, адреналин), Са2+, АДФ, АТФ в высоких концентрациях и до десяти факторов свертывания крови.
Кроме того, имеется третий тип мелких гранул (200-250 нм), представленный лизосомами (иногда называемыми λ-гранулами), содержащими лизосомные ферменты, а также микропероксисомами, содержащими фермент пероксидазу.
Содержимое гранул при активации пластинок выделяется по открытой системе каналов, связанных с плазмолеммой.
Основная функция кровяных пластинок - участие в процессе свертывания крови - защитной реакции организма на повреждение и предотвращение потери крови. Разрушение стенки кровеносного сосуда сопровождается выделением из поврежденных тканей веществ (факторов свертывания крови), что вызывает прилипание (адгезию) тромбоцитов к базальной мембране эндотелия и коллагеновым волокнам сосудистой стенки. При этом через систему трубочек из тромбоцитов выходят плотные гранулы, содержимое которых приводит к образованию сгустка - тромба.
При ретракции сгустка сокращается его объем до 10 % первоначального, изменяется форма пластинок (дисковидная становится шаровидной), наблюдаются разрушение пограничного пучка микротрубочек, полимеризация актина, появление
многочисленных миозиновых филаментов, формирование актомиозиновых комплексов, обеспечивающих сокращение сгустка. Отростки активированных пластинок вступают в контакт с нитями фибрина и втягивают их в центр тромба. Затем в сгусток, состоящий из тромбоцитов и фибрина, проникают фибробласты и капилляры, и происходит замещение сгустка соединительной тканью. В организме существуют и противосвертывающие системы. Известно, что мощным антикоагулянтом является гепарин, вырабатываемый тучными клетками.
Изменения показателя свертывания крови отмечаются при ряде заболеваний. Например, усиление свертывания крови обусловливает образование тромбов в кровеносных сосудах, например при атеросклерозе, когда изменены рельеф и целостность эндотелия. Уменьшение числа тромбоцитов (тромбоцитопения) приводит к снижению свертываемости крови и кровотечениям. При наследственном заболевании гемофилии имеют место дефицит и нарушение образования фибрина из фибриногена.
Одной из функций тромбоцитов является их участие в метаболизме серото-нина. Тромбоциты - это практически единственные элементы крови, в которых, поступая из плазмы, накапливаются резервы серотонина. Связывание тромбоцитами серотонина происходит с помощью высокомолекулярных факторов плазмы крови и двухвалентных катионов с участием АТФ.
В процессе свертывания крови из разрушающихся тромбоцитов высвобождается серотонин, который действует на проницаемость сосудов и сокращение гладких миоцитов их стенки. Серотонин и продукты его метаболизма оказывают противоопухолевое и радиозащитное действие. Торможение связывания серотонина тромбоцитами обнаружено при ряде заболеваний крови - злокачественном малокровии, тромбоцитопенической пурпуре, миелозах и др.
При иммунных реакциях тромбоциты активизируются и секретируют факторы роста и свертывания крови, вазоактивные амины и липиды, нейтральные и кислые гидролазы, принимающие участие в воспалении.
Продолжительность жизни тромбоцитов в среднем 9-10 сут. Стареющие тромбоциты фагоцитируются макрофагами селезенки. Усиление разрушающей функции селезенки может быть причиной значительного снижения числа тромбоцитов в крови (тромбоцитопения). Для устранения этого требуется операция - удаление селезенки (спленэктомия).
При снижении числа кровяных пластинок, например при кровопотере, в крови накапливается тромбопоэтин - гликопротеид, стимулирующий образование пластинок из мегакариоцитов костного мозга.
Гемограмма. Лейкоцитарная формула
В медицинской практике анализ крови играет большую роль. При клинических анализах исследуют химический состав крови, определяют количество эритроцитов, лейкоцитов, гемоглобина, резистентность эритроцитов, быстроту их оседания - скорость оседания эритроцитов (СОЭ) и др. У здорового человека форменные элементы крови находятся в определенных количественных соотношениях, которые принято называть гемограммой, или формулой крови. Большое значение для характеристики состояния организма имеет так называемый дифференциальный подсчет лейкоцитов.
Определенные процентные соотношения лейкоцитов называют лейкоцитарной формулой.
Возрастные изменения крови
Число эритроцитов в момент рождения и в первые часы жизни выше, чем у взрослого человека, и достигает 6,0-7,0×1012/л. К 10-14-м сут оно равно тем же цифрам, что и во взрослом организме. В последующие сроки происходит снижение числа эритроцитов с минимальными показателями на 3-6-м мес жизни (физиологическая анемия). Число эритроцитов становится таким же, как и во взрослом организме, в период полового созревания. Для новорожденных характерны наличие анизоцитоза (разнообразие размеров эритроцитов) с преобладанием макроцитов, увеличенное содержание рети-кулоцитов, а также присутствие незначительного числа ядросодержащих предшественников эритроцитов.
Число лейкоцитов у новорожденных увеличено и достигает 10,0-30,0×109/л. В течение 2 нед после рождения число их снижается до 9,0-15,0×109/л. Количество лейкоцитов достигает к 14-15 годам уровня, свойственного взрослым. Соотношение числа нейтрофилов и лимфоцитов у новорожденных такое же, как и у взрослых. В последующем содержание лимфоцитов возрастает, а нейтрофилов - снижается; таким образом, к 4-м сут количество этих видов лейкоцитов уравнивается (первый физиологический перекрест лейкоцитов). Дальнейшее возрастание числа лимфоцитов и снижение числа нейтрофилов приводят к тому, что на 1-2-м году жизни лимфоциты составляют 65 %, а нейтрофилы - 25 %. Новое снижение числа лимфоцитов и повышение числа нейтрофилов приводят к выравниванию обоих показателей у 4-летних детей (второй физиологический перекрест). Постепенное снижение содержания лимфоцитов и повышение числа нейтрофилов продолжаются до полового созревания, когда количество этих видов лейкоцитов достигает нормы взрослого.
7.3. ЛИМФА
Лимфа (лат. lympha - влага) представляет собой слегка желтоватую жидкость белковой природы, протекающую в лимфатических капиллярах и сосудах. Она состоит из лимфоплазмы (plasma lymphae) и форменных элементов. По химическому составу лимфоплазма близка к плазме крови, но содержит меньше белков. Среди фракций белка альбумины преобладают над глобулинами. Часть белка составляют ферменты - диастаза, липаза и глико-литические ферменты. Лимфоплазма содержит также нейтральные жиры, простые сахара, NaCl, Na2CO3 и другие, а также различные соединения, в состав которых входят кальций, магний, железо.
Форменные элементы лимфы представлены главным образом лимфоцитами (98 %), а также моноцитами и другими видами лейкоцитов, иногда в ней обнаруживаются эритроциты. Лимфа накапливается в лимфатических
капиллярах тканей и органов, куда под влиянием различных факторов, в частности осмотического и гидростатического давления, из тканей постоянно поступают различные компоненты лимфоплазмы. Из капилляров лимфа перемещается в периферические лимфатические сосуды, по ним - в лимфатические узлы, затем в крупные лимфатические сосуды и вливается в кровь. Состав лимфы постоянно меняется. Различают лимфу периферическую (до лимфатических узлов), промежуточную (после прохождения через лимфатические узлы) и центральную (лимфа грудного и правого лимфатического протоков). Процесс лимфообразования тесно связан с поступлением воды и других веществ из крови в межклеточные пространства и образованием тканевой жидкости.
7.4. КРОВЕТВОРЕНИЕ (ГЕМОПОЭЗ)
Гемопоэзом (haemopoesis) называют развитие крови. Различают эмбриональный гемопоэз, который происходит в эмбриональный период и приводит к развитию крови как ткани, и постэмбриональный гемопоэз, который представляет собой процесс физиологической регенерации крови.
Развитие эритроцитов называют эритропоэзом, развитие гранулоцитов - гранутоцитопоэзом, тромбоцитов - тромбоцитопоэзом, развитие моноцитов - моноцитопоэзом, развитие лимфоцитов и иммуноцитов - лимфоцито-и иммуноцитопоэзом.
7.4.1. Эмбриональный гемопоэз
В развитии крови как ткани в эмбриональный период можно выделить три основных этапа, последовательно сменяющих друг друга: 1) мезобластический, когда начинается развитие клеток крови во внезаро-дышевых органах - мезенхиме стенки желточного мешка и хориона (с 3-й по 9-ю нед развития зародыша человека) и появляется первая генерация стволовых клеток крови; 2) печеночный, который начинается в печени с 5-6-й нед развития зародыша, когда печень становится основным органом гемопоэза, в ней образуется вторая генерация СКК. Кроветворение в печени достигает максимума через 5 мес и завершается перед рождением. СКК печени заселяют вилочковую железу (здесь, начиная с 7-8-й нед, развиваются Т-лимфоциты), селезенку (гемопоэз начинается с 12-й нед) и лимфатические узлы (гемопоэз отмечается с 10-й нед); 3) медуллярный (костномозговой) - появление третьей генерации СКК в костном мозге, где гемопоэз начинается с 10-й нед и постепенно нарастает к рождению, а после рождения костный мозг становится центральным органом гемопоэза.
Кроветворение в стенке желточного мешка. У человека оно начинается в конце 2-й - начале 3-й нед эмбрионального развития. В мезенхиме стенки желточного мешка обособляются зачатки сосудистой крови, или
кровяные островки. В них мезенхимные клетки теряют отростки, округляются и преобразуются в стволовые клетки крови. Клетки, ограничивающие кровяные островки, уплощаются, соединяются между собой и образуют эндотелиальную выстилку будущего сосуда. Часть СКК дифференцируются в первичные клетки крови (бласты), крупные клетки с базофиль-ной цитоплазмой и ядром, в котором хорошо заметны крупные ядрышки (рис. 7.14). Большинство первичных кровяных клеток митотически делятся и превращаются в первичные эритробласты, характеризующиеся крупным размером (мегалобласты). Это превращение совершается в связи с накоплением эмбрионального гемоглобина в цитоплазме бластов, при этом сначала образуются полихроматофильные эритробласты, а затем ацидофильные эри-тробласты с большим содержанием гемоглобина. В некоторых первичных эритробластах ядра подвергаются кариорексису и удаляются из клеток, в других клетках ядра сохраняются. В результате образуются безъядерные и ядросодержащие первичные эритроциты, отличающиеся большим размером от ацидофильных эритробластов и поэтому получившие название мегало-цитов. Такой тип кроветворения называется мегалобластическим. Он характерен для эмбрионального периода, но может появляться в постнатальном периоде при некоторых заболеваниях (злокачественное малокровие).
Наряду с мегалобластическим в стенке желточного мешка начинается нормобластическое кроветворение, при котором из бластов образуются вторичные эритробласты; сначала по мере накопления в их цитоплазме гемоглобина они превращаются в полихроматофильные эритробласты, далее в нормобласты, из которых образуются вторичные эритроциты (нормоци-ты); размеры последних соответствуют эритроцитам (нормоцитам) взрослого человека (см. рис. 7.14, а). Развитие эритроцитов в стенке желточного мешка происходит внутри первичных кровеносных сосудов, т. е. интраваску-лярно. Одновременно экстраваскулярно из бластов, расположенных вокруг сосудов, дифференцируется небольшое количество гранулоцитов - ней-трофилов и эозинофилов. Часть СКК остается в недифференцированном состоянии и разносится током крови по различным органам зародыша, где происходит их дальнейшая дифференцировка в клетки крови или соединительной ткани. После редукции желточного мешка основным кроветворным органом временно становится печень.
Кроветворение в печени. Печень закладывается примерно на 3-4-й нед эмбрионального развития, а с 5-й нед она становится центром кроветворения. Кроветворение в печени происходит экстраваскулярно, по ходу капилляров, врастающих вместе с мезенхимой внутрь печеночных долек. Источником кроветворения в печени служат стволовые клетки крови, из которых образуются бласты, дифференцирующиеся во вторичные эритроциты. Процесс их образования повторяет описанные выше этапы образования вторичных эритроцитов. Одновременно с развитием эритроцитов в печени образуются зернистые лейкоциты, главным образом нейтрофильные и ацидофильные. В цитоплазме бласта, становящейся более светлой и менее базофильной, появляется специфическая зернистость, после чего ядро приобретает неправильную форму. Кроме гранулоцитов, в печени формируют-
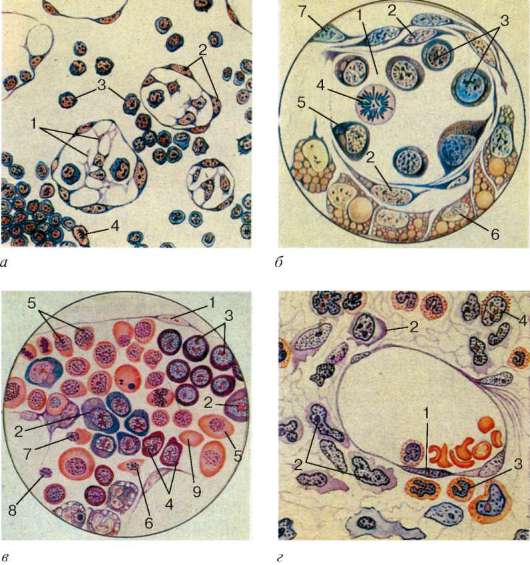
Рис. 7.14. Эмбриональный гемопоэз (по А. А. Максимову):
а - кроветворение в стенке желточного мешка зародыша морской свинки: 1 - мезенхимальные клетки; 2 - эндотелий стенки сосудов; 3 - первичные кровяные клетки-бласты; 4 - митотически делящиеся бласты; б - поперечный срез кровяного островка зародыша кролика 8,5 сут: 1 - полость сосуда; 2 - эндотелий; 3 - интра-васкулярные кровяные клетки; 4 - делящаяся кровяная клетка; 5 - формирование первичной кровяной клетки; 6 - энтодерма; 7 - висцеральный листок мезодермы; в - развитие вторичных эритробластов в сосуде зародыша кролика 13,5 сут: 1 - эндотелий; 2 - проэритробласты; 3 - базофильные эритробласты; 4 - поли-хроматофильные эритробласты; 5 - оксифильные (ацидофильные) эритробласты (нормобласты); 6 - оксифильный (ацидофильный) эритробласт с пикнотическим ядром; 7 - обособление ядра от оксифильного (ацидофильного) эритробласта (нор-мобласта); 8 - вытолкнутое ядро нормобласта; 9 - вторичный эритроцит; г - кроветворение в костном мозге зародыша человека с копчиково-теменной длиной тела 77 мм. Экстраваскулярное развитие клеток крови: 1 - эндотелий сосуда; 2 - бласты; 3 - нейтрофильные гранулоциты; 4 - эозинофильный миелоцит
ся гигантские клетки - мегакариоциты. К концу внутриутробного периода кроветворение в печени прекращается.
Кроветворение в тимусе. Вилочковая железа закладывается в конце 1-го мес внутриутробного развития, и на 7-8-й нед ее эпителий начинает заселяться стволовыми клетками крови, которые дифференцируются в лимфоциты тиму-
са. Увеличивающееся число лимфоцитов тимуса дает начало Т-лимфоцитам, заселяющим Т-зоны периферических органов иммунопоэза.
Кроветворение в селезенке. Закладка селезенки происходит в конце 1-го мес внутриутробного развития. Из вселяющихся в нее стволовых клеток происходит экстраваскулярное образование всех видов форменных элементов крови, т. е. селезенка в эмбриональном периоде представляет собой универсальный кроветворный орган. Образование эритроцитов и гранулоци-тов в селезенке достигает максимума на 5-м мес внутриутробного развития. После этого в ней начинает преобладать лимфоцитопоэз.
Кроветворение в лимфатических узлах. Первые закладки лимфатических узлов у человека появляются на 7-8-й нед эмбрионального развития. Большинство лимфатических узлов развиваются на 9-10-й нед. В этот же период начинается проникновение в лимфатические узлы стволовых клеток крови, из которых дифференцируются эритроциты, гранулоциты и мегака-риоциты. Однако формирование этих элементов быстро подавляется образованием лимфоцитов, составляющих основную часть клеток лимфатических узлов. Появление единичных лимфоцитов происходит уже на 8-15-й нед развития, однако массовое «заселение» лимфатических узлов предшественниками Т- и В-лимфоцитов начинается с 16-й нед, когда формируются посткапиллярные венулы, через стенку которых осуществляется процесс миграции клеток. Из клеток-предшественников дифференцируются лим-фобласты (большие лимфоциты), а далее средние и малые лимфоциты. Дифференцировка Т- и В-лимфоцитов происходит в Т- и В-зависимых зонах лимфатических узлов.
Кроветворение в костном мозге. Закладка костного мозга осуществляется на 2-м мес внутриутробного развития. Первые гемопоэтические элементы появляются на 12-й нед развития; в это время основную их массу составляют эритробласты и предшественники гранулоцитов. Из СКК в костном мозге формируются все форменные элементы крови, развитие которых происходит экстраваскулярно (см. рис. 7.14, г). Часть СКК сохраняются в костном мозге в недифференцированном состоянии, они могут расселяться по другим органам и тканям и являться источником развития клеток крови и соединительной ткани. Таким образом, костный мозг становится центральным органом, осуществляющим универсальный гемопоэз, и остается им в течение постнатальной жизни. Он обеспечивает стволовыми кроветворными клетками тимус и другие органы гемопоэза.
7.4.2. Постэмбриональный гемопоэз
Постэмбриональный гемопоэз представляет собой процесс физиологической регенерации крови (клеточное обновление), который компенсирует физиологическое разрушение дифференцированных клеток. Миелопоэз происходит в миелоидной ткани (textus myeloideus), расположенной в эпифизах трубчатых и полостях многих губчатых костей (см. главу 14). Здесь развиваются форменные элементы крови: эритроциты, гранулоциты, моноциты, кровяные пластинки, предшественники лимфоцитов. В миелоид-
ной ткани находятся стволовые клетки крови и соединительной ткани. Предшественники лимфоцитов постепенно мигрируют и заселяют такие органы, как тимус, селезенка, лимфатические узлы и др.
Лимфопоэз происходит в лимфоидной ткани (textus lymphoideus), которая имеет несколько разновидностей, представленных в тимусе, селезенке, лимфатических узлах. Она выполняет основные функции: образование Т- и В-лимфоцитов и иммуноцитов (плазмоцитов и др.).
СКК являются плюрипотентными (полипотентными) предшественниками всех клеток крови и относятся к самоподдерживающейся популяции клеток. Они редко делятся. Впервые представление о родоначальных клетках крови сформулировал в начале XX в. А. А. Максимов, который считал, что по своему строению они сходны с лимфоцитами. В настоящее время это представление нашло подтверждение и дальнейшее развитие в новейших экспериментальных исследованиях, проводимых главным образом на мышах. Выявление СКК стало возможным при применении метода коло-ниеобразования.
Экспериментально (на мышах) показано, что при введении смертельно облученным животным (утратившим собственные кроветворные клетки) взвеси клеток красного костного мозга или фракции, обогащенной СКК, в селезенке появляются колонии клеток - потомков одной СКК. Пролиферативную активность СКК модулируют колониестимулирующие факторы (КСФ), интерлейкины (ИЛ-3 и др.). Каждая СКК в селезенке образует одну колонию и называется селезеночной колониеобразующей единицей (КОЕ-С). Подсчет колоний позволяет судить о количестве стволовых клеток, находящихся во введенной взвеси клеток. Таким образом, было установлено, что у мышей на 105 клеток костного мозга приходится около 50 стволовых клеток. Исследование очищенной фракции стволовых клеток с помощью электронного микроскопа позволяет сделать вывод, что по ультраструктуре они очень близки к малым темным лимфоцитам.
Исследование клеточного состава колоний выявляет две линии их диф-ференцировки. Одна линия дает начало мультипотентной клетке - родоначальнику гранулоцитарного, эритроцитарного, моноцитарного и мега-кариоцитарного дифферонов гемопоэза (КОЕ-ГЭММ). Вторая линия дает начало мультипотентной клетке - родоначальнику лимфопоэза (КОЕ-Л) (рис. 7.15). Из мультипотентных клеток дифференцируются олигопотент-ные (КОЕ-ГМ) и унипотентные родоначальные (прогениторные) клетки. Методом колониеобразования определены родоначальные унипотентные клетки для моноцитов (КОЕ-М), нейтрофилов (КОЕ-Гн), эозинофилов (КОЕ-Эо), базофилов (КОЕ-Б), эритроцитов (БОЕ-Э и КОЕ-Э), мегака-риоцитов (КОЕ-МГЦ), из которых образуются клетки-предшественники (прекурсорные). В лимфопоэтическом ряду выделяют унипотентные клетки - предшественники В-лимфоцитов и соответственно Т-лимфоцитов. Полипотентные (плюрипотентные и мультипотентные), олигопотентные и унипотентные клетки морфологически не различаются.
Все приведенные выше стадии развития клеток составляют четыре основных компартмента: I - стволовые клетки крови (плюрипотентные, полипо-
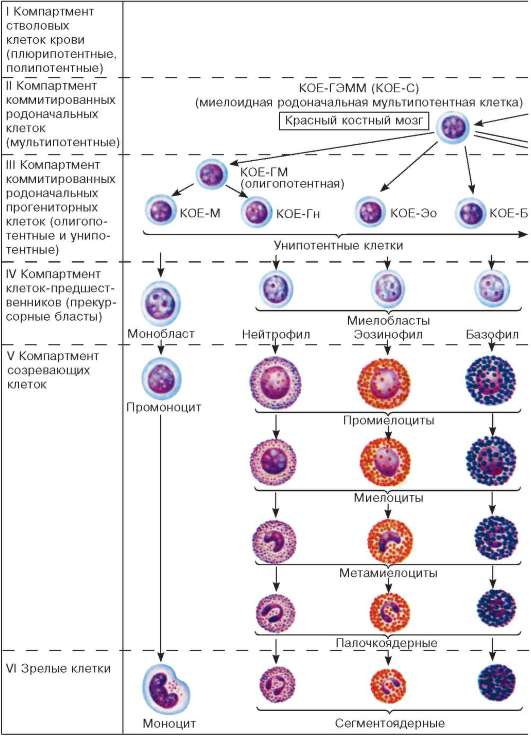
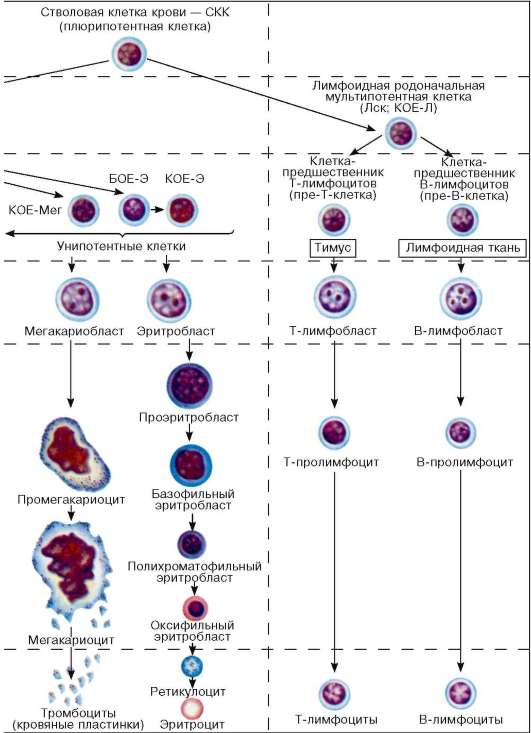
Рис. 7.15. Постэмбриональный гемопоэз, окраска азуром II-эозином (по Н. А. Юриной).
Стадии дифференцировки крови: I-IV - морфологически неидентифицируе-мые клетки; V, VI - морфологически идентифицируемые клетки. Б - базофил;
БОЕ - бурстобразующая единица; Г - гранулоциты; Гн - гранулоцит нейтрофильный; КОЕ - колониеобразующие единицы; КОЕ-С - селезеночная колониеобразующая единица; Л - лимфоцит; Лск - лимфоидная стволовая клетка; М - моноцит; Мег - мегакариоцит; Эо - эозинофил; Э - эритроцит. Ретикулоцит окрашен суправитально
тентные); II - коммитированные родоначальные клетки (мультипотентные); III - коммитированные родоначальные (прогенторные) олигопотентные и унипотентные клетки; IV - клетки-предшественники (прекурсорные).
Дифференцировка полипотентных клеток в унипотентные определяется действием ряда специфических факторов - эритропоэтинов (для эритро-бластов), гранулопоэтинов (для миелобластов), лимфопоэтинов (для лим-фобластов), тромбопоэтинов (для мегакариобластов) и др.
Из каждой клетки-предшественника образуется конкретный вид клеток. Клетки каждого вида при созревании проходят ряд стадий и в совокупности образуют компартмент созревающих клеток (V). Зрелые клетки представляют последний компартмент (VI). Все клетки V и VI компартментов морфологически можно идентифицировать (рис. 7.15).
Эритроцитопоэз
Родоначальником эритроидных клеток человека, как и других клеток крови, является полипотентная стволовая клетка крови, способная формировать в культуре костного мозга колонии. Полипотентная СКК в результате дивергентной дифференцировки дает два типа мультипотентных частично коммитированных кроветворных клеток: 1) коммитированные к лимфо-идному типу дифференцировки (Лск, КОЕ-Л); 2) КОЕ-ГЭММ - единицы, образующие смешанные колонии, состоящие из гранулоцитов, эритроцитов, моноцитов и мегакариоцитов (аналог КОЕ-С in vitro). Из второго типа мультипотентных кроветворных клеток дифференцируются унипотентные единицы: бурстобразующая (БОЕ-Э) и колониеобразующая (КОЕ-Э) эри-троидные клетки, которые являются коммитированными родоначальными клетками эритропоэза.
БОЕ-Э - взрывообразующая, или бурстобразующая, единица (burst - взрыв) по сравнению с КОЕ-Э является менее дифференцированной. БОЕ-Э может при интенсивном размножении быстро образовать крупную колонию клеток. БОЕ-Э в течение 10 сут осуществляет 12 делений и образует колонию из 5000 эритроцитарных клеток с незрелым фетальным гемоглобином (HbF). БОЕ-Э малочувствительна к эритропоэтину и вступает в фазу размножения под влиянием интерлейкина-3 (бурстпромоторная активность), вырабатываемого моноцитами - макрофагами и Т-лимфоцитами. Интерлейкин-3 (ИЛ-3) является гликопротеином с молекулярной массой 20-30 килодальтон. Он активирует ранние полипотентные СКК, обеспечивая их самоподдержание, а также запускает дифференцировку полипотент-ных клеток в коммитированные клетки. ИЛ-3 способствует образованию клеток (КОЕ-Э), чувствительных к эритропоэтину.
КОЕ-Э по сравнению с БОЕ-Э - более зрелая клетка. Она чувствительна к эритропоэтину, под влиянием которого размножается (в течение 3 сут делает 6 делений), формирует более мелкие колонии, состоящие примерно из 60 эри-троцитарных элементов. Количество эритроидных клеток, образуемых в сутки из КОЕ-Э, в 5 раз меньше аналогичных клеток, образуемых из БОЕ-Э.
Таким образом, БОЕ-Э содержат клетки-предшественники эритроцитов, которые способны генерировать тысячи эритроидных прекурсоров
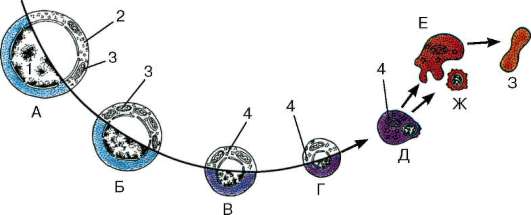
Рис. 7.16. Последовательные стадии дифференцировки проэритробласта в эритроцит: А - проэритробласт; Б - базофильный эритробласт; В - полихроматофильный эритробласт; Г - ацидофильный эритробласт (нормобласт); Д - выталкивание ядра из ацидофильного эритробласта; Е - ретикулоцит; Ж - пикнотичное ядро; З - эритроцит. 1 - ядро; 2 - рибосомы и полирибосомы; 3 - митохондрии; 4 - гранулы гемоглобина
(предшественников). Они содержатся в малом количестве в костном мозге и крови благодаря частичному самоподдержанию и миграции из компарт-мента мультипотентных кроветворных клеток. КОЕ-Э является более зрелой клеткой, образующейся из пролиферирующей БОЕ-Э.
Эритропоэтин - гликопротеиновый гормон, образующийся в юкста-гломерулярном аппарате (ЮГА) почки (90 %) и печени (10 %) в ответ на снижение парциального давления кислорода в крови (гипоксия) и запускающий эритропоэз из КОЕ-Э. Под его влиянием КОЕ-Э дифференцируются в проэритробласты, из которых образуются эритробласты (базофиль-ные, полихроматофильные, ацидофильные), ретикулоциты и эритроциты. Образующиеся из КОЕ-Э эритроидные клетки морфологически идентифицируются (рис. 7.16). Сначала образуется проэритробласт.
Проэритробласт - клетка диаметром 14-18 мкм, имеющая большое круглое ядро с мелкозернистым хроматином, одно-два ядрышка, слабобазо-фильную цитоплазму, в которой содержатся свободные рибосомы и полисомы, слаборазвитые комплекс Гольджи и гранулярная эндоплазматическая сеть. Базофильный эритробласт - клетка меньшего размера (13-16 мкм). Его ядро содержит больше гетерохроматина. Цитоплазма клетки обладает хорошо выраженной базофильностью в связи с накоплением в ней рибосом, в которых начинается синтез Нb. Полихроматофильный эритробласт - клетка размером 10-12 мкм. Ее ядро содержит много гетерохроматина. В цитоплазме клетки накапливается синтезируемый на рибосомах НЬ, окрашивающийся эозином, благодаря чему она приобретает серовато-фиолетовый цвет. Проэритробласты, базофильные и полихроматофильные эритробла-сты способны размножаться путем митоза, поэтому в них часто видны фигуры деления.
Следующая стадия дифференцировки - образование ацидофильного (оксифилия) эритробласта (нормобласта). Это клетка небольшого размера (8-10 мкм), имеющая маленькое пикнотичное ядро. В цитоплазме эритро-
бласта содержится много НЬ, обеспечивающего ее ацидофилию (оксифи-лию) - окрашивание эозином в ярко-розовый цвет. Пикнотическое ядро выталкивается из клетки, в цитоплазме сохраняются лишь единичные органеллы (рибосомы, митохондрии). Клетка утрачивает способность к делению.
Ретикулоцит - постклеточная структура (безъядерная клетка) с небольшим содержанием рибосом, обусловливающих наличие участков базофи-лии, и преобладанием НЬ, что в целом дает многоцветную (полихромную) окраску (поэтому эта клетка получила название «полихроматофильный эритроцит»). При выходе в кровь ретикулоцит созревает в эритроцит в течение 1-2 сут. Эритроцит - это клетка, образующаяся на конечной стадии дифференцировки клеток эритроидного ряда. Период образования эритроцита, начиная со стадии проэритробласта, занимает 7 сут.
Таким образом, в процессе эритропоэза происходят уменьшение размера клетки в 2 раза (см. рис. 7.16); уменьшение размера и уплотнение ядра и его выход из клетки; уменьшение содержания РНК, накопление НЬ, сопровождаемые изменением окраски цитоплазмы - от базофильной до полихро-матофильной и ацидофильной; потеря способности к делению клетки. Из одной СКК в течение 7-10 сут в результате 12 делений образуется около 2000 зрелых эритроцитов.
Эритропоэз у млекопитающих и человека протекает в костном мозге в особых морфофункциональных ассоциациях, получивших название эри-тробластических островков, впервые описанных французским гематологом М. Бесси (1958). Эритробластический островок состоит из макрофага, окруженного одним или несколькими слоями эритроидных клеток, развивающихся из унипотентной КОЕ-Э, вступившей в контакт с макрофагом КОЕ-Э. Образующиеся из нее клетки (от проэритробласта до ретикулоцита) удерживаются в контакте с макрофагом его рецепторами (сиалоадгезинами и др.) (рис. 7.17, 7.18).
У взрослого организма потребность в эритроцитах обычно обеспечивается за счет усиленного размножения полихроматофильных эритробластов (гомопластический гемопоэз). Однако, когда потребность организма в эритроцитах возрастает (например, при потере крови), эритробласты начинают развиваться из предшественников, а последние - из стволовых клеток (гетеропластический эритропоэз).
В норме из костного мозга в кровь поступают только эритроциты и рети-кулоциты.
Гранулоцитопоэз
Источниками гранулоцитопоэза являются также СКК и мультипотент-ные КОЕ-ГЭММ (см. рис. 7.15). В результате дивергентной дифференци-ровки через ряд промежуточных стадий в трех различных направлениях образуются гранулоциты трех видов: нейтрофилы, эозинофилы и базофилы. Клеточные диффероны для гранулоцитов представлены следующими формами: СКК → КОЕ-ГЭММ → КОЕ-ГМ → унипотентные предшественники (КОЕ-Б, КОЕ-Эо, КОЕ-Гн) → миелобласт → промиелоцит → миелоцит →
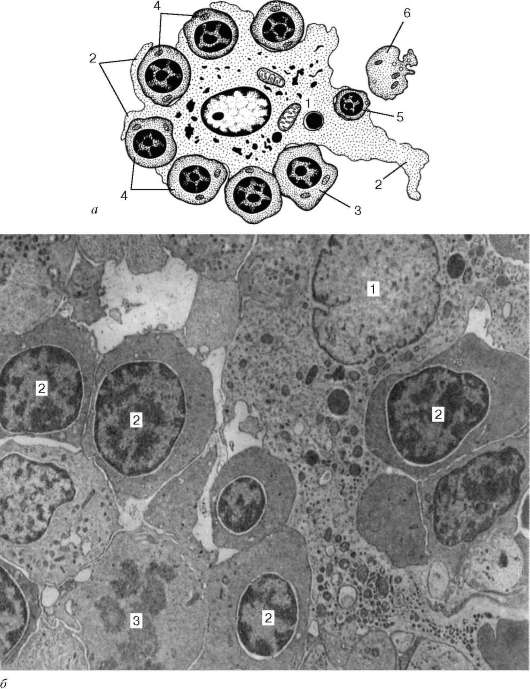
Рис. 7.17. Динамика развития эритробластического островка (по М. Бесси и соавт., с изменениями):
а - схема: 1 - цитоплазма макрофага; 2 - отростки макрофага; 3 - базофильные эритробласты; 4 - полихроматофильные эритробласты; 5 - ацидофильный эритро-бласт; 6 - ретикулоцит; б - срез эритроидного островка: 1 - макрофаг; 2 - эритроциты; 3 - митотически делящийся эритробласт. Электронная микрофотография по Ю. М. Захарову. Увеличение 8000
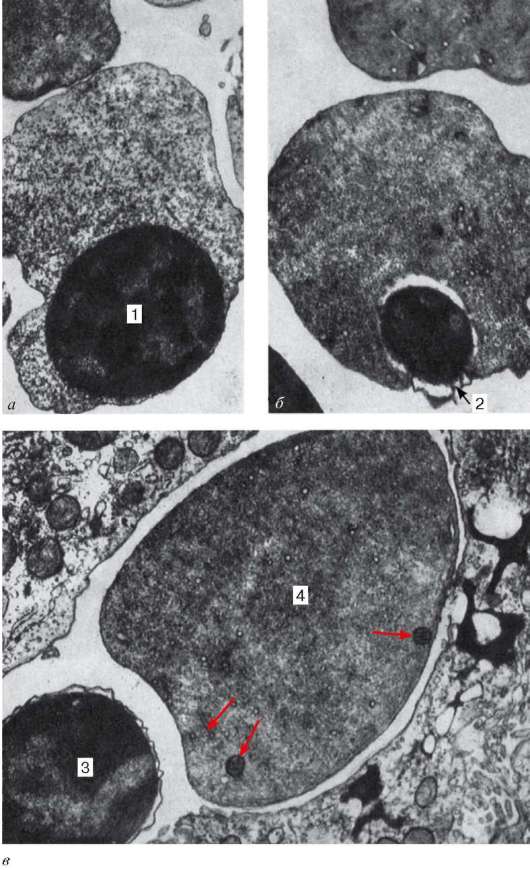
Рис. 7.18. Развитие эритроцитов в печени плода человека:
а, б - 15-недельный плод (увеличение 6000); в - 20-недельный плод (увеличение 15 000). 1 - эксцентрично расположенное ядро эритробласта; 2 - обособление пикнотического ядра ацидофильного эритробласта; 3 - отделение пикнотического ядра с узким ободком цитоплазмы от ацидофильного эритробласта; 4 - ретикулоцит с единичными органеллами (указано стрелками). Электронная микрофотография (по Замбони)
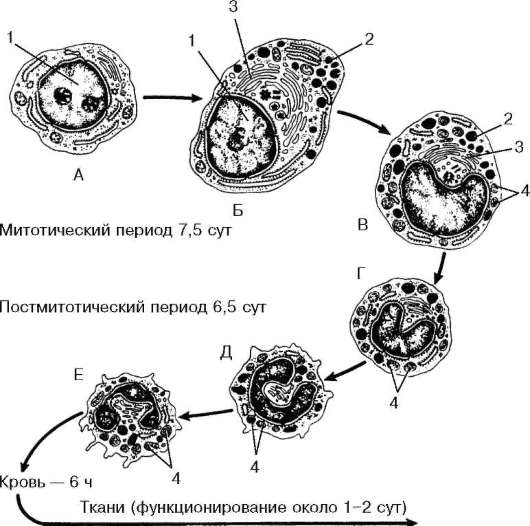
Рис. 7.19. Дифференцировка нейтрофильного гранулоцита в костном мозге (по Д. Байнтону, М. Фарквару, Дж. Элиоту, с изменениями):
А - миелобласт; Б - промиелоцит; В - миелоцит; Г - метамиелоцит; Д - палоч-коядерный нейтрофильный гранулоцит (нейтрофил); Е - сегментоядерный нейтрофильный гранулоцит. 1 - ядро; 2 - первичные (азурофильные) гранулы; 3 - комплекс Гольджи; 4 - вторичные - специфические гранулы
метамиелоцит → палочкоядерный гранулоцит → сегментоядерный гранулоцит.
По мере созревания гранулоцитов клетки уменьшаются в размерах, изменяется форма их ядер от округлой до сегментированной, в цитоплазме накапливается специфическая зернистость (рис. 7.19).
Миелобласты (myeloblastus), дифференцируясь в направлении того или иного гранулоцита, дают начало промиелоцитам (promyelocytus) (см. рис. 7.15). Это крупные клетки, содержащие овальное или круглое светлое ядро, в котором имеется несколько ядрышек. Около ядра располагается ясно выраженная центросома, хорошо развиты комплекс Гольджи, лизосомы. Цитоплазма слегка базофильна. В ней накапливаются первичные (азуро-фильные) гранулы, которые характеризуются высокой активностью мие-лопероксидазы, а также кислой фосфатазы, т. е. относятся к лизосомам. Промиелоциты делятся митотически. Специфическая зернистость отсутствует.
Нейтрофильные миелоциты (myelocytus neutrophilicus) имеют размер от 12 до 18 мкм. Эти клетки размножаются митозом. Цитоплазма их становится диффузно ацидофильной, в ней появляются наряду с первичными вторичные (специфические) гранулы, характеризующиеся меньшей электронной плотностью. В миелоцитах обнаруживаются все органеллы. Количество митохондрий невелико. Эндоплазматическая сеть состоит из пузырьков. Рибосомы располагаются на поверхности мембранных пузырьков, а также диффузно в цитоплазме. По мере размножения нейтрофильных миелоцитов круглое или овальное ядро становится бобовидным, начинает окрашиваться темнее, хроматиновые глыбки становятся грубыми, ядрышки исчезают.
Такие клетки уже не делятся. Это метамиелоциты (metamyelocytus) (см. рис. 7.19). В цитоплазме увеличивается число специфических гранул. Если метамиелоциты встречаются в периферической крови, то их называют юными формами. При дальнейшем созревании их ядро приобретает вид изогнутой палочки. Подобные формы получили название палочкоядерных гранулоцитов. Затем ядро сегментируется, и клетка становится сегментоядер-ным нейтрофильным гранулоцитом. Полный период развития нейтрофильного гранулоцита составляет около 14 сут, при этом период пролиферации продолжается около 7,5 сут, а постмитотический период дифференцировки - около 6,5 сут.
Эозинофильные (ацидофильные) миелоциты (см. рис. 7.15) представляют собой клетки округлой формы диаметром (на мазке) около 14-16 мкм. По характеру строения ядра они мало отличаются от нейтрофильных миелоци-тов. Цитоплазма их заполнена характерной эозинофильной зернистостью. В процессе созревания миелоциты митотически делятся, а ядро приобретает подковообразную форму. Такие клетки называются ацидофильными мета-миелоцитами. Постепенно в средней части ядро истончается и становится двудольчатым, в цитоплазме увеличивается количество специфических гранул. Клетка утрачивает способность к делению.
Среди зрелых форм различают палочкоядерные и сегментоядерные эозино-фильные гранулоциты с двудольчатым ядром.
Базофильные миелоциты (см. рис. 7.15) встречаются в меньшем количестве, чем нейтрофильные или эозинофильные миелоциты. Размеры их примерно такие же, как и эозинофильных миелоцитов; ядро округлой формы, без ядрышек, с рыхлым расположением хроматина. Цитоплазма базофильных миелоцитов содержит в широко варьирующих количествах специфические базофильные зерна неодинаковых размеров, которые проявляют мета-хромазию при окрашивании азуром и легко растворяются в воде. По мере созревания базофильный миелоцит превращается в базофильный метамиелоцит, а затем в зрелый базофильный гранулоцит.
Все миелоциты, особенно нейтрофильные, обладают способностью фагоцитировать, а начиная с метамиелоцита, приобретают подвижность.
У взрослого организма потребность в лейкоцитах обеспечивается за счет размножения миелоцитов. При кровопотерях, например, миелоциты начинают развиваться из миелобластов, а последние из унипотентных и поли-потентных СКК.
Мегакариоцитопоэз. Тромбоцитопоэз
Кровяные пластинки образуются в костном мозге из мегакариоцитов - гигантских по величине клеток, которые дифференцируются из СКК, проходя ряд стадий. Последовательные стадии развития можно представить следующим клеточным диффероном: СКК → КОЕ-ГЭММ → КОЕ-МГЦ → мегакариобласт → промегакариоцит → мегакариоцит → тромбоциты (кровяные пластинки). Весь период образования пластинок составляет около 10 сут (см. рис. 7.15).
Мегакариобласт (megacaryoblastus) - клетка диаметром 15-25 мкм, имеет ядро с инвагинациями и относительно небольшой ободок базофильной цитоплазмы. Клетка способна к делению митозом, иногда содержит два ядра. При дальнейшей дифференцировке утрачивает способность к митозу и делится путем эндомитоза, при этом увеличиваются плоидность и размер ядра.
Промегакариоцит (promegacaryocytus) - клетка диаметром 30-40 мкм, содержит полиплоидные ядра - тетраплоидные, октаплоидные (4 n, 8 n), несколько пар центриолей. Объем цитоплазмы возрастает, в ней начинают накапливаться азурофильные гранулы. Клетка также способна к эндоми-тозу и дальнейшему увеличению плоидности ядер.
Мегакариоцит (megacaryocytus) - дифференцированная форма. Среди мегакариоцитов различают резервные клетки, не образующие пластинок, и зрелые активированные клетки, образующие кровяные пластинки. Резервные мегакариоциты диаметром 50-70 мкм, имеют очень большое, дольчатое ядро с набором хромосом 16-32 n; в их цитоплазме имеются две зоны - околоядерная, содержащая органеллы и мелкие азурофильные гранулы, и наружная (эктоплазма) - слабобазофильная, в которой хорошо развиты элементы цитоскелета. Зрелый, активированный мегакариоцит - крупная клетка диаметром 50-70 мкм (иногда даже до 100 мкм). Содержит очень крупное, сильно дольчатое полиплоидное ядро (до 64 n). В ее цитоплазме накапливается много азурофильных гранул, которые объединяются в группы. Прозрачная зона эктоплазмы также заполняется гранулами и вместе с плазмолеммой формирует псевдоподии в виде тонких отростков, направленных к стенкам сосудов. В цитоплазме мегакариоцита наблюдается скопление линейно расположенных пузырьков, которые разделяют зоны цитоплазмы с гранулами. Из пузырьков формируются демаркационные мембраны, разделяющие цитоплазму мегакариоцита на участки диаметром 1-3 мкм, содержащие по 1-3 гранулы (будущие кровяные пластинки). В цитоплазме можно выделить три зоны - перинуклеарную, промежуточную и наружную. В наружной зоне цитоплазмы наиболее активно идут процессы демаркации, формирования протромбоцитарных псевдоподий, проникающих через стенку синусов в их просвет, где и происходит отделение кровяных пластинок (рис. 7.20). После отделения пластинок остается клетка, содержащая дольчатое ядро, окруженное узким ободком цитоплазмы, - резидуальный мегакариоцит, который затем подвергается разрушению. При уменьшении числа кровяных пластинок в крови (тромбоцитопения), например после кровопотери, отмечается усиление мегакариоцитопоэза, приво-
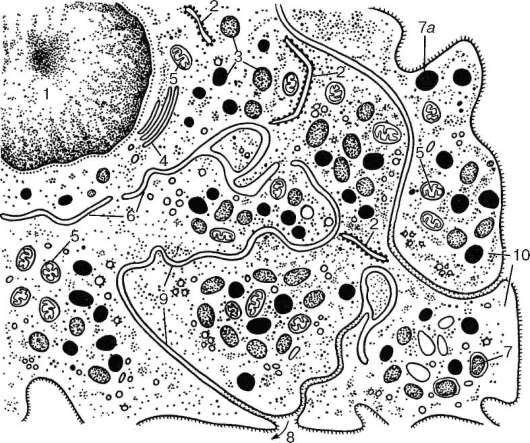
Рис. 7.20. Ультрамикроскопическое строение мегакариоцита (по Н. А. Юриной, Л. С. Румянцевой):
1 - ядро; 2 - гранулярная эндоплазматическая сеть; 3 - гранулы; 4 - комплекс Гольджи; 5 - митохондрии; 6 - гладкая эндоплазматическая сеть; 7 - альфа-гранулы; 7а - лизосомы; 8 - инвагинация плазмолеммы; 9 - демаркационные мембраны; 10 - формирующиеся кровяные пластинки
дящее к увеличению количества мегакариоцитов в 3-4 раза с последующей нормализацией числа тромбоцитов в крови.
Моноцитопоэз
Образование моноцитов происходит из стволовых клеток костного мозга по схеме: СКК → КОЕ-ГЭММ → КОЕ-ГМ → унипотентный предшественник моноцита (КОЕ-М) → монобласт (monoblastus) → промоноцит → моноцит (monocytus). Моноциты из крови поступают в ткани, где являются источником развития различных видов макрофагов.
Лимфоцитопоэз и иммуноцитопоэз
Лимфоцитопоэз проходит следующие стадии: СКК → КОЕ-Л (лимфоидная родоначальная мультипотентная клетка) → унипотентные предшественники лимфоцитов (пре-Т-клетки и пре-В-клетки)→ лимфобласт (lymphoblastus) → пролимфоцит → лимфоцит. Особенность лимфоцитопоэ-за - способность дифференцированных клеток (лимфоцитов) дедифферен-цироваться в бластные формы.
Процесс дифференцировки Т-лимфоцитов в тимусе приводит к образованию из унипотентных предшественников Т-бластов, из которых формируются эффекторные лимфоциты - киллеры, хелперы, супрессоры.
Дифференцировка унипотентных предшественников В-лимфоцитов в лимфоидной ткани ведет к образованию плазмобластов (plasmoblastus), затем проплазмоцитов, плазмоцитов (plasmocytus). Более подробно процессы образования иммунокомпетентных клеток описаны в главе 14.
Регуляция гемопоэза
Кроветворение регулируется факторами роста, обеспечивающими пролиферацию и дифференцировку СКК и последующих стадий их развития, факторами транскрипции, влияющими на экспрессию генов, определяющих направление дифференцировки гемопоэтических клеток, а также витаминами, гормонами.
Факторы роста включают колониестимулирующие факторы , интерлей-кины и ингибирующие факторы. Они являются гликопротеинами с молекулярной массой около 20 килодальтон. Гликопротеины действуют и как циркулирующие гормоны, и как местные медиаторы, регулирующие гемопоэз и развитие клеточных дифферонов. Они почти все действуют на СКК, КОЕ, коммитированные и зрелые клетки. Однако отмечаются индивидуальные особенности действия этих факторов на клетки-мишени.
Например, фактор роста стволовых клеток влияет на пролиферацию и миграцию СКК в эмбриогенезе. В постнатальном периоде на гемопоэз оказывают влияние несколько КСФ, среди которых наиболее изучены факторы, стимулирующие развитие гранулоцитов и макрофагов (ГМ-КСФ, Г-КСФ, М-КСФ), а также интерлейкины.
Как видно из табл. 7.1, мульти-КСФ и интерлейкин-3 действуют на поли-потентную стволовую клетку и большинство КОЕ. Некоторые КСФ могут действовать на одну или более стадий гемопоэза, стимулируя деление, диф-ференцировку клеток или их функцию. Большинство указанных факторов выделено и применяется для лечения различных болезней. Для получения их используются биотехнологические методы.
Большая часть эритропоэтина образуется в почках (интерстициальные клетки), меньшая - в печени. Его образование регулируется содержанием в крови О2, которое зависит от количества циркулирующих в крови эритроцитов. Снижение числа эритроцитов и соответственно парциального давления кислорода (Ро2) является сигналом для увеличения продукции эритропоэтина. Эритропоэтин действует на чувствительные к нему КОЕ-Э, стимулируя их пролиферацию и дифференцировку, что в конечном итоге приводит к повышению содержания в крови эритроцитов. К факторам роста для эритроидных клеток, кроме эритропоэтина, относится фактор бурст-промоторной активности (БПА), который влияет на БОЕ-Э. БПА образуется клетками ретикулоэндотелиальной системы. В настоящее время считают, что он является интерлейкином-3.
Тромбопоэтин синтезируется в печени, стимулирует пролиферацию КОЕ-МГЦ, их дифференцировку и образование тромбоцитов.
Ингибирующие факторы дают противоположный эффект, т. е. тормозят гемопоэз. К ним относятся липопротеины, блокирующие действие КСФ (лактофер-рин, простагландины, интерферон, кейлоны). Гормоны также влияют на гемопоэз. Например, гормон роста стимулирует эритропоэз, глюкокортикоиды, напротив, подавляют развитие клеток-предшественников.
Таблица 7.1. Гемопоэтические факторы роста (стимуляторы)
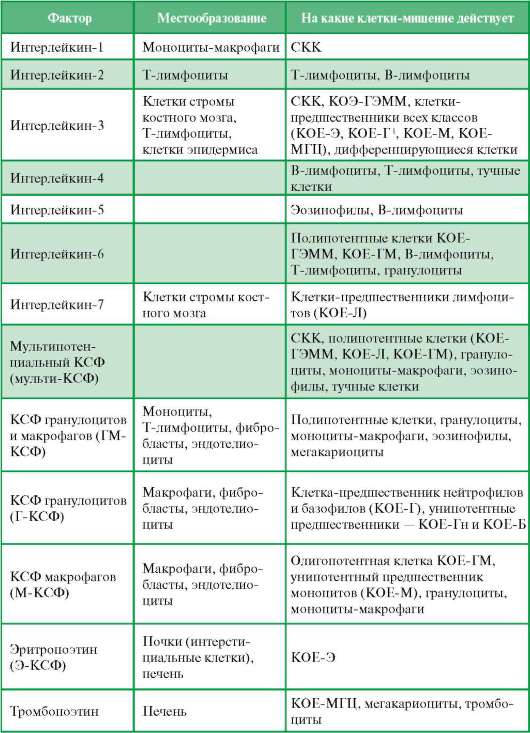
1 Нейтрофилы, эозинофилы, базофилы.
Витамины необходимы для стимуляции пролиферации и дифференцировки гемо-поэтических клеток. Витамин В12 потребляется с пищей и поступает с кровью в костный мозг, где влияет на гемопоэз. Нарушение процесса всасывания при различных заболеваниях может служить причиной дефицита витамина В12 и нарушений в гемопоэ-зе. Фолиевая кислота участвует в синтезе пуриновых и пиримидиновых оснований.
Таким образом, развитие кроветворных клеточных дифферонов протекает в неразрывной связи с микроокружением. Миелоидная и лимфоидная ткани являются разновидностями соединительной ткани, т. е. относятся к тканям внутренней среды. Ретикулоцитарный, адипоцитарный, тучнокле-точный и остеобластический диффероны вместе с межклеточным веществом (матриксом) формируют микроокружение для гемопоэтических диф-феронов. Гистологические элементы микроокружения и гемопоэтические клетки функционируют в неразрывной связи. Микроокружение оказывает воздействие на дифференцировку клеток крови (при контакте с их рецепторами или путем выделения специфических факторов). В миелоидной и лимфоидной тканях стромальные ретикулярные и гемопоэтические элементы образуют единое функциональное целое. В тимусе имеется сложная строма, представленная как соединительнотканными, так и ретикулоэпи-телиальными клетками. Эпителиальные клетки секретируют особые вещества - тимозины, оказывающие влияние на дифференцировку из СКК Т-лимфоцитов. В лимфатических узлах и селезенке специализированные ретикулярные клетки создают микроокружение, необходимое для пролиферации и дифференцировки в специальных Т- и В-зонах Т- и В-лимфоцитов и плазмоцитов.
Контрольные вопросы
1. Гемограмма, лейкоцитарная формула: определение, количественные и качественные характеристики у здорового человека.
2. Основные положения унитарной теории кроветворения А. А. Максимова. Перечислить свойства стволовой кроветворной клетки.
3. Эритропоэз, стадии, роль клеточного микроокружения в дифферен-цировке клеток эритробластического дифферона.
4. Агранулоциты: морфологические и функциональные характеристики.