Клиническая генетика. Геномика и протеомика наследственной патологии : учеб. пособие. - 3-е изд., перераб. и доп. - Мутовин Г.Р. 2010. - 832 с. : ил
|
|
|
|
ГЛАВА 22. МУЛЬТИФАКТОРИАЛЬНЫЕ ПРИЗНАКИ И ЗАБОЛЕВАНИЯ
ОБЩАЯ ХАРАКТЕРИСТИКА
Наследование нормальных и патологических признаков организма, генетическая изменчивость которых очевидна, нельзя объяснить с помощью только моногенного варианта, но даже при моногенном наследовании невозможно с уверенностью сказать, что анализируемый ген будет единственной причиной признака или фенотипа, поскольку один и тот же признак (фенотип) может быть обусловлен мутациями в разных генах или генокопированием (см. главы 4, 5 и 21).
К таким труднообъяснимым вариантам наследования генов и признаков относятся не только редкие качественные отклонения от нормы, но и широко распространенные заболевания неинфекционной природы, а также ряд ВПР.
Среди них: необычные рост, масса и пропорции тела, черты и выражение лица, цвет (окраска) кожных покровов, давление крови, неспецифическая УО или ее противоположность - высокоразвитый интеллект (или даже гениальность), относительно большая по сравнению с обычной продолжительность жизни и так называемое практическое здоровье человека.
В середине XX в. было показано, что такие признаки обусловлены суммарным (аддитивным) действием генетических средовых факторов, и по этой причине их стали называть мультифакториальными. Были выделены три группы мультифакториальных признаков.
• Признаки, характеризующиеся постоянными различиями. Сюда относятся экстремальные варианты распределения признаков, т.е. выходящие за пределы границ нормы, характеризующие эти показатели (пределы гауссова распределения). При этом учитываются отклонения от средних значений более чем на две стандартные ошибки (ниже нижней или выше верхней границы нормы). Если большинство различий в количественных признаках (например, рост или масса тела) имеют нормальное распределение (гауссова кривая с одной вершиной или модой), и это
относится к 94% всех различий, то меньшая доля различий (6%) относится к признакам, характеризующимся постоянными количественными отклонениями, выходящими за переделы нижней и верхней границ нормы или находящимся на грани крайних нормальных значений.
• ВПР. Сюда относятся пороки развития, сопровождающиеся грубыми морфофункциональными изменениями: аномалад Пьера- Робена (расщелина нёба, микрогнатия, глоссоптоз, лучелоктевой синостоз), атрезия пищевода, болезнь Гиршпрунга, «заячья губа» и «волчья пасть», врожденный пилоростеноз, врожденный вывих бедра, врожденные косолапость и плоскостопие, пороки невральной трубки (spina bifida, анэнцефалия), пороки сердца и магистральных сосудов, пороки развития почек, гипоспадия, эписпадия, неклассифицированные комплексы МВПР, синдром Клиппеля-Фейла (аномалии развития шейных позвонков) и др.
• Хронические широко распространенные заболевания неинфекционной природы или собственно МФЗ. Сюда относятся: артериальная (эссенциальная) гипертензия, БА, ишемическая болезнь сердца, многие формы рака, псориаз, ревматизм, сахарный диабет I типа, шизофрения и маниакально-депрессивный психоз, ЯБЖиДК и др. На их долю приходится 94-96% всей хронической неинфекционной патологии.
Таким образом, в основе любого мультифакториального признака и заболевания лежат несколько причин. При этом индивидуальный вклад каждой причины в проявление болезни может быть незначительным, и только их суммарный вклад ведет к развитию заболевания.
При многих МФЗ патогенетический механизм может быть запущен несколькими способами: либо одной причиной, либо комбинацией из нескольких причин, которые могут быть чисто генетическими (например, один или несколько главных генов или весь полигенный комплекс), другие - чисто средовыми (например, химические аллергены), третьи - поведенческими (например, пристрастие к определенной пище), четвертые - социальными и/или психологическими (например, влияние родителей, школы, сослуживцев на работе).
Характеризуя генетические причины, необходимо иметь в виду, что значительное число структурных генов человека включают множественные аллели, расположенные в полиморфных генных локусах (их не менее 6 тыс.), ответственных за производство полиморфных
белковых продуктов (см. главу 5). Следовательно, поскольку число белков человеческого организма весьма велико (их 350-400 тыс., а объем их модификаций - 6 млн) должны существовать организмы с разным сочетанием белков, формирующих мультифакториальные признаки и фенотипы. Их развитие обусловлено совместным действием генетических (наследственных) и негенетических (ненаследственных) причин, на основе которых формируется наследственная предрасположенность. Поэтому МФЗ часто называют болезнями с наследственной предрасположенностью (БНП).
Наследственная предрасположенность
Наследственная предрасположенность (подверженность) - это преобладающий генетический компонент, от вклада которого зависит результат суммарного эффекта генетических и средовых факторов, обусловливающих для индивида большую или меньшую вероятность иметь (или не иметь) мультифакториальный признак, заболеть (или не заболеть) МФЗ.
Наследственная подверженность включает в себя индивидуальные и семейные составляющие части на основе неповторимой уникальности индивида (его генетической конституции), с одной стороны, и наличия у него общих генов с близкими и дальними родственниками - с другой (см. главы 4 и 18).
Порог подверженности
При превышении определенных значений предрасположенности - так называемого порога подверженности - запускается механизм развития мультифакториального заболевания.
За порогом подверженности располагаются больные лица (рис. 67). Однако физически это понятие вряд ли существует, это некая условная шкала индивидуальной восприимчивости к заболеванию, внутри которой от действия средовых факторов будет зависеть, заболеет индивид или нет.
С математической точки зрения, распределение подверженности (как гауссова кривая) имеет одну вершину (моду) и обусловлено большим количеством аддитивно (суммарно) действующих генов и факторов среды, где каждый фактор вносит свой вклад.
Из сказанного следует, что индивид с высокой подверженностью (большим генетическим компонентом) (по Фогелю Ф., Мотульски А., 1989) может не заболеть даже при благоприятных
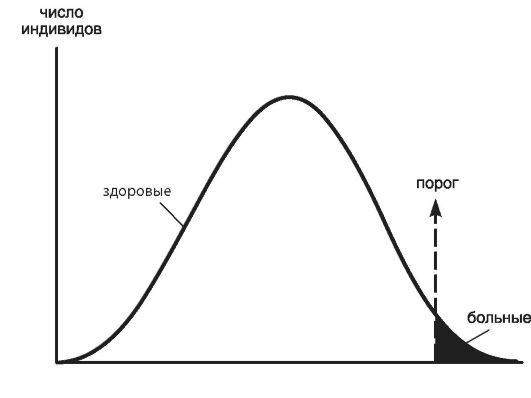
Рис. 67. Распределение подверженности к мультифакториальному признаку и заболеванию (по Фогелю Ф., Мотульски А., 2006).
для проявления болезни условиях среды. Вместе с тем, возможна обратная ситуация.
Таким образом, отличительной особенностью мультифакториального признака и заболевания является то, что один генный локус не может быть ответственным за его развитие - это всегда результат аддитивного (суммарного) действия множества генных локусов и большого числа внешних факторов. Относительная роль каждого генетического фактора и фактора среды различна в каждом конкретном случае.
НАСЛЕДУЕМОСТЬ
Понятие «наследуемость» введено для оценки роли генетических причин и механизмов, т.е. вклада генетических факторов в этиологию и патогенез болезни. Наследуемость - это степень, с которой предрасположенность определяется генетическими факторами в сравнении с факторами среды. Вместе с тем, оценка наследуемости может быть состоятельна лишь при условии, когда
предрасположенность определяется большим числом наследуемых генов.
Для расчетов наследуемости болезни предложен коэффициент, значение которого определяется по формуле h2 = Vg/Vp, где h2 или Кн - это коэффициент наследуемости, Vg и Vp - соответственно генетическая и фенотипическая компоненты дисперсии. Этот коэффициент выражается в абсолютных числах (от 0 до 1) или процентах и наглядно отражает аддитивный вклад в фенотип только генетических факторов. Низкое значение коэффициента наследуемости подразумевает малый вклад в признак аддитивно действующих генов, высокое значение - большой вклад.
Итак, наследуемость - это популяционно-статистический параметр. Наследуемость большинства БНП превышает 60% (см. главу 4). Теперь рассмотрим основные модели наследования БНП.
Основные модели наследования
Моделей наследования мультифакториальных признаков и фенотипов много. Рассмотрим основные из них.
Во-первых, это простая (аддитивная) модель. Она предполагает совместное действие нескольких генов, определяющих подверженность. Модель упрощена и абстрактна, ибо вклад каждого из генов, действующих в мультифакториальной системе, различается в количественном и качественном отношениях, и какие-то гены оказываются более важными по значению.
Во-вторых, это модель наследуемости количественных признаков. Она предполагает наличие некой переменной величины, которая отражает предрасположение. С одной стороны, эта величина зависит от влияния сходно действующих генов всего генного (полигенного) компонента, а с другой стороны, - от влияния факторов среды.
Каждый из генов и факторов среды влияет на признак, но заболевание возникает лишь в том случае, когда предрасположение достигнет порогового уровня, т.е. речь идет о модели полигенного компонента с пороговым эффектом. В случае предрасположенности к заболеванию кривая распределения болезни в семье больного будет сдвинута в область более высокого предрасположения, и поэтому среди родственников будет больше больных, ибо у них имеется некоторое количество общих генов, определяющих предрасположение к болезни.
И хотя эта модель не позволяет конкретизировать роль факторов среды, она удовлетворительно объясняет распространение в семьях
таких заболеваний, как рак, сахарный диабет, врожденные аномалии развития нервной системы, семейная гиперхолестеринемия и др.
В-третьих, имеется смешанная модель; ее авторы (Мортон Н. и Мак-Лин К., 1974 г.) анализируют зависимость предрасположения от действия главного гена и/или полигенного комплекса и факторов среды. В этом случае считается, что главный ген и/или полигенный комплекс наследуются по моногенному варианту. При этом лица с генотипом «аа» будут здоровы; у лиц с генотипом «АА» вероятность заболеть будет больше, чем у лиц с генотипом «Аа», и болезнь возникнет в результате влияния генов полигенного комплекса и факторов внешней среды. Причем передача от родителей к детям главного гена и полигенного комплекса происходит с учетом двух условий: влияния факторов среды, общих для родителей и детей, и влияния части признаков (обусловленных полигенным комплексом), различающихся у родителей и детей.
В-четвертых, это более сложные модели, согласно которым возникновение признака (фенотипа) зависит от главного локуса, полигенного комплекса и факторов среды. При этом факторы среды могут быть как случайными, так и общими для родственников одной семейной родословной, например пристрастие к сладкой, соленой или острой пище, что является фактором риска развития соответственно сахарного диабета, гипертонической болезни или болезней желудочнокишечного тракта.
Следует подчеркнуть важность учета семейных негенетических факторов, ибо нередко только одним их действием можно объяснить семейный характер наследования некоторых МФЗ.
В-пятых, это концептуальная модель предрасположенности, предложенная Ф. Фогелем и А. Мотульски (1989). В ней подчеркивается важность предрасположенности за счет главных генов и генов всего полигенного комплекса, определяющих основной вклад в развитие болезни (рис. 68). При этом главные гены не действуют в «вакууме», они экспрессируются на фоне всей совокупности генов, модифицирующих их работу. Вместе с тем, предположение об участии главного гена в формировании наследственной предрасположенности к заболеванию может быть высказано только в случае обнаружения в этом гене мутаций, не встречающихся у здоровых людей.
В большинстве случаев патологический белковый продукт, производимый одним или даже несколькими главными генами, играет ключевую роль в развитии симптомов болезни. Например, установлен
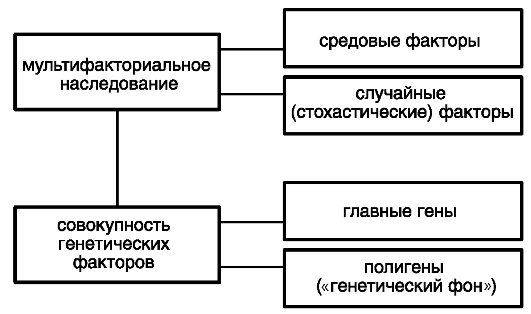 Рис. 68. Концептуальная модель предрасположенности к МФЗ (по Фогелю Ф. и Мотульски А., 1989)
Рис. 68. Концептуальная модель предрасположенности к МФЗ (по Фогелю Ф. и Мотульски А., 1989)
значительный вклад главных генов (DRCA1 и DRCA2) в предрасположенность к семейным формам рака грудной железы, а в последние годы показано участие в предрасположенности к этому заболеванию еще и третьего главного гена - DRCA3.
Кроме того, с помощью модели Ф. Фогеля и А. Мотульски в разных группах больных с БНП удалось выделить редкие формы заболеваний, характеризующиеся сочетанным мультифакториальным и моногенным вариантами наследования.
• В группе гиперлипидемий, обусловливающих ишемическую болезнь сердца (ИБС), были выделены две такие формы - семейная гиперхолестеринемия (ген LDRL локализован на хромосоме 19р13.2-р13.1) и семейный дефект Аро-В-100 (ген аро-В локализован на хромосоме 2р23-р24).
• В группе ЭГ были выделены:
- гипертензия, купируемая небольшими дозами глюкокортикоидов (причина - неравный кроссинговер между генами альдостерон-синтазы и 11-бета-гидроксилазы; оба гена локализованы в сегменте 8q21, являющемся областью гена цитохрома
Р450);
- синдром Лиддла или псевдоальдостеронизм (причина - два гена эпителиального натриевого канала SCNN2 и SCNN3; оба локализованы в сегментах 16р13-р12);
• - синдром Гордона или псевдоальдостеронизм второго типа, а также синдром избытка минералокортикоидов (ген почечной 11-бета- гидроксистероид-дегидрогеназы, локализован в 16р13-р12). В группе сахарного диабета I типа были выделены ряд MODY- форм, обусловленных мутациями единичных генов, в том числе 6 форм, связанных с мутациями в структурных и регуляторных генах: HNF4A (форма 1), GCK - ген глюкокиназы (2), ядерного фактора гепатоцитов (3), фактора-1 промотора инсулина (4), почечного фактора транскрипции 2 (5), NEURODY (6). Следует отметить, что роль генетических факторов оказалась весьма значительной при таких БНП, как ЯБЖиДК, ВПР (дефекты невральной трубки, расщелины верхней губы и нёба, врожденная косолапость). При этом семейное наследование отличалось от классического моногенного варианта. В развитии этих БНП и ВПР участвовали неспецифические гены, действующие совместно с факторами окружающей среды. И хотя действие всех факторов было аддитивным, первичный молекулярный эффект неспецифических генов не был определен (рассматривается как «черный ящик»).
При ВПР была дополнительно показана роль случайных факторов, которые нельзя отнести ни к генетическим, ни средовым, ибо они действовали стохастически.
Таким образом, несмотря на наличие множества моделей наследования мультифакториальных признаков и фенотипов и основанного на них сегрегационного анализа, рассмотренная проблема пока не решена.
Ассоциации и сцепление БНП с полиморфными маркерами
Поиск генетических причин предрасположенности к МФЗ подразумевает определение ассоциации болезни с полиморфными маркерами (генами и антигенами) и сцепления болезни с ДНК-маркерами (см. главу 19).
Ассоциация - это более высокая частота определенного полиморфного гена-маркера при конкретном заболевании. Например, имеют место ассоциации антигенов системы HLA с рядом МФЗ, среди которых анкилозирующий и псориатический спондилит и синдром Рейтера (сцеплены с антигеном В27), болезнь Адисона и сахарный диабет I типа (DR3), гемохроматоз (А3), гнездная алопеция (DQW7), псориаз (CW6), ревматоидный артрит и сахарный диабет I типа (антиген DR4), рассеянный склероз (DRВ1).
В конце XX в. была описана ассоциация полиморфизма альфа- 1-антитрипсина с хронической эмфиземой легких у взрослых, патогенез которой был связан с множественными аллелями локуса Р1 (всего 23 разных фенотипа), обусловливающими механизмы разрушения легочной ткани при хронической эмфиземе легких в результате инфицирования.
При этом было показано, что ассоциация не подразумевает, что ген болезни и маркерный ген расположены в одной хромосоме. Например, с HLA-локусами, расположенными на хромосоме 6, могут быть сцеплены гены разных моногенных заболеваний, находящиеся на измеримом расстоянии от НLA-комплекса (АГС, гемохроматоз, спиноцеребеллярная атаксия).
Вместе с тем, сегодня нет оснований считать, что БНП и HLA- комплекс как-то связаны между собой физиологически. Например, к таким заболеваниям относятся аутоиммунные или иммуноассоциированные болезни: болезнь Аддисона, детская спру, миастения гравис, множественный склероз, ревматоидный артрит, сахарный диабет I типа, тиреотоксикоз, хронический гепатит.
Семейный анализ выявил сегрегацию случаев этих заболеваний среди родственников больных пробандов, хотя моногенное наследование отсутствовало.
Следовательно, будучи ассоциированными, D/DR-гены HLA- комплекса и гены аутоиммунных заболеваний не являются сцепленными между собой, т.е. ассоциацию и сцепление следует строго разграничить.
Сцепление относится к двум генам, расположенным в одной хромосоме на определенном расстоянии друг от друга. Для анализа сцепления БНП с полиморфными маркерами в настоящее время используется от 300 до 500 ДНК-маркеров, распределенных по всему геному. На их применении основан метод полного геномного скрининга.
ОТДЕЛЬНЫЕ НОЗОЛОГИИ БОЛЕЗНЕЙ
С НАСЛЕДСТВЕННОЙ ПРЕДРАСПОЛОЖЕННОСТЬЮ
В последние годы БНП приобрели большое значение в МГК пациентов, имеющих такие заболевания. В целом на долю подобных пациентов приходится не менее 10% от общего контингента больных, а доля самих БНП (как наиболее распространенной наследственной
патологии во взрослой жизни) достигает 60% в общей структуре заболеваемости населения.
Артериальная гипертензия
Артериальная гипертензия (АГ) и выделяемая за рубежом ее разновидность - эссенциальная гипертензия (ЭГ) имеют сходную клиническую симптоматику. И для первой, и для второй характерны семейное накопление, солезависимость и низкий уровень ренина.
В рамках ЭГ выделены три синдрома: синдром Лиддла или псевдоальдостеронизм с АГ (16р13-р12), синдром АМЕ или ложной минералокортикоидной избыточности (16q22), и семейный гиперальдостеронизм, поддающийся лечению небольшими дозами глюкокортикоидов
(8q21).
Установлено: аллельные формы генов этих синдромов одновременно служат генетическими маркерами предрасположенности как к ЭГ, так и к АГ, что является подтверждением правильности объединения этих форм гипертензии на основе клинического сходства.
Итак, АГ - это гетерогенная группа болезней со следующими основными клиническими проявлениями: повышением уровня артериального давления и связанными с ним осложнениями (инфаркты, инсульты, почечная недостаточность).
В настоящее время выделены свыше 100 генов-кандидатов АГ, продукты которых прямо или косвенно участвуют в механизмах ее развития. К числу генов-кандидатов АГ относятся гены:
• SCNN IB и SCNN IG или соответственно 1-бета и 1-гамма - субъединицы эпителиального Na+-канала; оба гена локализованы на хромосоме 16 (16р13-р12);
• APNH или ген Na+ / Н+-антипорта (локализован там же);
• REN или ген ренина (1р36.1-р35);
• AGT или ген ангиотензина I (1q42-q43);
• AGE или ген ангиотензина I, конвертирующего фермент (17q22-
q24);
• PLA2 или ген панкреатической фосфолипазы А2 (12q23-q24.1);
• SAH или ген гипертензии, обусловленной геном, экспрессирующимся в почке (16р13.11);
• NOS3 или ген эндотелиальной синтазы окиси азота (7q35-q36);
• F13B или ген фактора свертывания крови XIII;
• PON или ген параоксаназы.
Следует отметить, что в последние годы особый интерес был связан с геном NOS: выделены три изоформы (индуцибельная, невральная и эндотелиальная), определяющие уровень окиси азота в стенках кровеносных сосудов. Этот уровень регулируется с помощью кальмодулинзависимого механизма.
Показано, что именно ген NOS3 отвечает за предрасположенность к развитию ИБС (см. ниже) и способствует тяге к курению.
К продуктам экспрессии указанных генов относятся:
• компоненты ренин-ангиотензиновой и калликреин-кининовой систем;
• компоненты, поддерживающие сосудистый тонус: компоненты кальциевых каналов, синтазы закиси азота;
• компоненты структуры сосудов: коллагенсвязывающий белок, фибриллин, эластин;
• продукты метаболизма стероидных гормонов: 11-бета- гидроксилазы, 17-альфа-гидроксилазы;
• продукты водно-солевого гомеостаза: аквапорины, ионные каналы, рецепторы вазопрессинов;
• рецепторы адренергической системы, например дофаминовые рецепторы.
Следует, однако, отметить, что при изучении полиморфизма генов, контролирующих производство перечисленных выше компонентов, их продуктов и рецепторов, не выявлено значимых ассоциаций с тремя специфическими синдромами, характеризующими ЭГ.
Вместе с тем было показано, что ряд генов, формирующих предрасположенность к АГ, вносят существенный вклад в этиологию другого широко распространенного заболевания с наследственной предрасположенностью - атеросклероза.
Опытные врачи-клиницисты давно отметили, что атеросклероз «ходит» за АГ как тень за человеком, и нередко обе эти формы сочетаются у одного и того же больного индивида, страдающего ожирением и сахарным диабетом (см. ниже).
Атеросклероз и связанные с ним синтропические конгломераты болезней
В конце XX в. заболеваемость атеросклерозом среди взрослого населения разных стран мира стали называть «эпидемией века». Была разработана концепция атерогенеза, объясняющая, что в осно-
ве механизмов развития атеросклероза лежит накопление липидов и липопротеинов низкой плотности в сосудистой стенке.
В настоящее время большое значение приобрела диагностика предрасположенности к атеросклерозу с учетом следующих молекулярногенетических критериев.
Во-первых, повышенный уровень липидов в плазме крови, нарушение процессов свертывания крови и целостности сосудистой стенки.
Во-вторых, общность генов, обусловливающих развитие двух сходных по симптоматике заболеваний: АГ (см. выше) и атеросклероза, что объясняется нарушениями функционирования ренинангиотензиновой и калликреин-кининовой систем. В качестве основных генов-кандидатов атеросклероза рассматриваются гены, продукты которых обеспечивают липидный обмен.
В-третьих, достоверно значимое сцепление атеросклероза с локусом СЕРТ на хромосоме 16 или генным локусом, контролирующим транспортный белок эфиров холестерина, а также с кластером генов аро-А1/ароС3/ароА4 на хромосоме 11.
В-четвертых, атерогенная совокупность липопротеинов (APL), которая рассматривается как отдельно наследуемый признак, объединяющий три параметра:
• преобладание частиц липопротеинов низкой плотности (ЛПНП) или LDL (подкласс В);
• высокий уровень липопротеинов, содержащих повышенное количество триглицеридов (ЛПНОП);
• сниженный уровень липопротеинов высокой плотности (ЛПВП). Выявление у больных атеросклерозом сразу всех трех параметров
нарушения липидного обмена увеличивает риск развития инфаркта миокарда в три раза.
В-пятых, тесное сцепление между APL и локусом рецептора LDL
(Р-ЛПНП).
Выдвинута гипотеза, что ген, отвечающий за предрасположенность к атеросклерозу, отождествляется с геном Р-ЛПНП. Показано, что потенциальный ген развития атеросклероза располагается дистальнее D19S7: в районе гена (19р13.2-р13.12).
Сцепление атеросклероза с локусом Р-ЛПНП подтверждено с помощью метода сибсов в 1996 г. у больных сибсов и пар родственников в семьях, имеющих коронарный атеросклероз.
В-шестых, доказательство принадлежности к генам-кандидатам атеросклероза гена недостаточности гепаринового фактора II (HCF2),
который локализован на хромосоме 22 (22q11) и совместно с другими факторами определяет антикоагуляционное действие гепарина.
В-седьмых, доказательство важной роли ангиотензин-I- конвертирующего фермента (AGE) в регуляции артериального давления и электролитного баланса крови. Этот фермент активизирует ангиотензин I в ангиотензин II и инактивирует брадикинин, а также является сильным вазопрессором и регулятором синтеза альдостеронстимулирующего белка.
Ген AGE I локализован на хромосоме 17 (17q22-q24) и также относится к генам-кандидатам атеросклероза.
Завершая рассмотрение столь важных для диагностики предрасположенности к атеросклерозу молекулярно-генетических критериев, следует отметить, что все они являются общими кретериями диагностики многих МФЗ.
Как отмечают В.П. Пузырев и соавт. (2005), такая общность - совсем не случайный факт, а тенденция к полипатии, множественности болезней у одних и тех же пациентов. Около 40% терапевтических больных в возрасте 15-75 лет имеют одновременно две соседствующие болезни, а у каждого пятого терапевтического больного одновременно проявляются четыре болезни - это синтропический конгломерат.
Такие сочетания могут быть чисто случайными, но могут быть результатом общности этиологии и патогенеза, составляя отдельные семейства болезней, изучение которых, безусловно, отвечает целям и задачам протеомики.
Одним из таких синтропических конгломератов болезней является сочетание АГ, атеросклероза, стеноза коронарных сосудов сердца и сахарного диабета II типа - это конгломерат NIDDM.
Генами-кандидатами предрасположенности и факторами ассоциации с двумя последними заболеваниями этого конгломерата являются: АСЕ, аллель D при NIDDM, а также связь с уровнем липидов, артериальным давлением, гипертрофией левого желудочка сердца (ГЛЖС) по ЭКГ-критериям и DD-генотипом АСЕ.
Связь ГЛЖС с DD-генотипом АСЕ сильнее выражена у мужчин, чем у женщин, и более четко проявляется у лиц с нормальным артериальным давлением (Schunkert H. et al., 1994). В частности, указанными авторами был сделан вывод, что DD-генотип является генетическим маркером повышенного риска развития гипертрофии ГЛЖС у мужчин среднего возраста.
Бронхолегочные болезни
Количество генов, контролирующих развитие и функционирование бронхолегочной системы человека, достигает 2000. Связанные с этими генами бронхолегочные болезни выявляются у 60% пациентов пульмонологических стационаров. На долю моногенных болезней бронхов и легких приходится от 5 до 35% контингента больных с неспецифическими болезнями легких. Их суммарная частота составляет 4:1000.
Как отмечено выше, МФЗ часто сочетаются с МБ. Не является исключением и бронхолегочная патология, которая сочетается с синдромами Марфана, Рандю-Ослера, Эллерса-Данлоса, МВ, МПС и др.
Вместе с тем, гетерозиготные носители генов этих МБ являются, как правило, практически здоровыми людьми, но при воздействии на них и их потомство неблагоприятных экологических и социальных факторов у них наблюдается повышенный риск развития бронхолегочной патологии. Одной из частых причин развития такой патологии служит недостаточность альфа-1-антитрипсина, которая может проявиться как самостоятельное моногенное заболевание или стать ведущим клиническим симптомом при таких МФЗ, как БА, хроническая эмфизема легких и хронические бронхиты.
Недостаточность альфа-1-антитрипсина
Недостаточность альфа-1-антитрипсина в сыворотке крови больных выявляется как в случае выделения ее в отдельную моногенную патологию, так и при ее определении в качестве ведущего симптома при МФЗ. Она проявляется не только хроническими неспецифическими болезнями и эмфиземой легких, но и поражением печени и сосудов.
Ген болезни (ген Pi) картирован на хромосоме 14 (14q32). Выделены 75 аллельных вариантов этого гена, наиболее частым из которых является аллель PiZ или замена глутаминовой кислоты (кодон GAG) на лизин (кодон AAG). Этот аллель обычно встречается у европеоидов и почти не встречается у негров и монголоидов.
На рис. 69 показана зависимость риска бронхолегочной патологии от наличия разных аллельных вариантов и концентрации альфа-1- антитрипсина в сыворотке крови больных.
Факторами риска развития бронхолегочной патологии являются: курение (основной фактор), пассивное курение, гиперактивность дыхательных путей, нарушающая легочную функцию (например, у больных БА), частые ОРЗ (особенно в детстве), про-
фессиональные вредности (кадмиевая и угольная пыль, неспецифические поллютанты), загрязнение окружающей среды, старческий возраст.
Развитию такой патологии чаще подвержены мужчины, чем женщины. Актуальной проблемой пульмонологии в развитых странах стала проблема организации эффективного селективного скрининга взрослых людей, страдающих эмфиземой легких, и селективного скрининга детей, часто болеющих ОРЗ, включая ОРВИ, на определение недостаточности альфа-1-антитрипсина. Серьезным аргументом в пользу такого скрининга, в ходе которого выявляются мутации гена Pi, стала возможность заместительной терапии препаратами, стимулирующими у больных синтез и секрецию альфа-1- антитрипсина гепатоцитами (демазол и тамоксифен).
Кроме того, для лечения такой патологии широко применяется трансплантация легких.
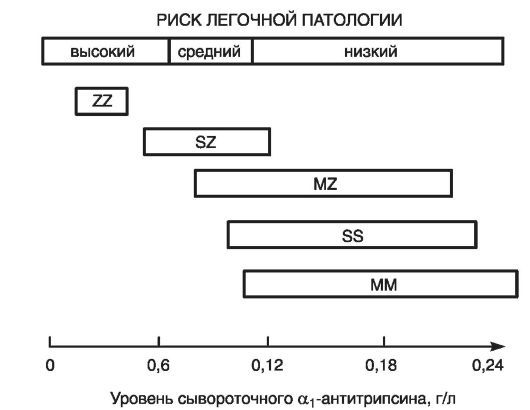 Рис. 69. Риск легочной патологии при разных аллельных вариантах и концентрациях OL-антитрипсина в сыворотке крови (по Баранову В.С. и соавт., 2005)
Рис. 69. Риск легочной патологии при разных аллельных вариантах и концентрациях OL-антитрипсина в сыворотке крови (по Баранову В.С. и соавт., 2005)
Бронхиальная астма
БА - это хроническое воспалительное заболевание верхних дыхательных путей с периодическими приступами удушья. В большинстве случаев БА является атопическим заболеванием с участием аллергенов внешней среды (см. главу 15) и сопровождается IgE-зависимым иммунным ответом, т.е. это экзогенная форма БА.
Патогенетический механизм БА связан со сложным взаимодействием дендритных клеток (см. главу 20), находящихся в слизистой бронхов, с иммунокомпетентными клетками, медиаторами, развитием отека бронхиальной стенки, гиперсекрецией слизи и деструктивными изменениями в бронхах. Результатом этих реакций является повторная экспрессия доминирующего эпитопа внешнего аллергена, вступившего в комплекс с молекулами антигенов HLA II типа на поверхности дендритных клеток. Образовавшийся комплекс связывается с рецепторами СD4 Т-клеток, что стимулирует дифференцировку Т1г0-лимфоцитов в Т1г2-лимфоциты, которые приобретают способность к секреции цитокинов; функционирование связано с гуморальным иммунным ответом и образованием ряда интерлейки-
нов (ИЛ 3-ИЛ5, ИЛ-9, ИЛ13).
В случае действия антигенов микобактерий и некоторых вирусов D4 Т-клетки превращаются в ТЫ-лимфоциты, секретирующие ИЛ-2, гамма-интерферон и ФНО, что вызывает активацию макрофагов и последующую илиминацию микроорганизмов.
Эндогенной или криптогенной формой БА является форма, этиология которой либо неизвестна, либо не связана с аллергическим механизмом высвобождения медиаторов воспаления.
Кроме того, выделена аспириновая форма БА вследствие дефекта метаболизма соединений арахидоновой кислоты. В ответ на прием аспирина происходит выброс медиаторов воспаления без участия иммунных реакций, связанных с образованием антител
(Суздальцева Т.В., 1999).
Точное число генов-кандидатов предрасположенности к БА не определено, но, по некоторым оценкам, оно уже достигло 1900. Среди наиболее важных генов-кандидатов БА выделены несколько групп, в том числе:
• 32 гена для идентификации антигенов и факторов гуморального иммунного ответа, включая гены цитокинов (интерлейкины, интерфероны, ФНО и др.), гены рецепторов Т- и В- клеток, а также гены HLA;
• 32 гена рецепторов цитокинов и факторов гуморального иммунитета, белковые продукты которых фиксируют на клеткахмишенях молекулы внешних лигандов;
• 26 генов медиаторов воспаления и сопутствующих им факторов, гены ферментов метаболизма этих соединений, а также гены хемокинов и молекул межклеточной адгезии;
• гены внутриклеточных сигнальных молекул или гены нескольких семейств белков, обеспечивающих и контролирующих трансдукцию сигналов молекул лигандов на «чувствительные» генные локусы; по-видимому, к данной группе относятся еще 11 генов транскрипционных факторов, которые активируются при участии этих посредников;
• другие гены, имеющие функциональные отношения со всеми перечисленными группами генов БА, например гены биотрансформации ксенобиотиков (NAT2, CYP1A, GSTT1 и GSTM1).
В настоящее время проведены исследования генов-кандидатов предрасположенности к БА, выполненные на основе методов позиционного клонирования. Основные результаты: а) среди идентифицированных локусов большое значение имеют локусы: 5q31.1-33, 6p12-21.2, 11q12-13, 12q14-24.1, 13q12.22, 14q11-12, 16p12.12-11.2; б) подтверждено сцепление БА с локусами 5q23-33, 6p23-21, 11q13,12q15- 24.1, 13q12-22; в) дополнительно определено 15 участков хромосом, сцепленных с БА; г) получено подтверждение молекулярных различий между основной формой БА (per se) и атопической формой БА (BHR) по сцеплению с уровнем IgE и наличию специфической сенсибилизации при кожном тестировании; д) показана достоверная зависимость количества генов-кандидатов БА, эффектов генов-модификаторов и факторов окружающей среды от межпопуляционной вариабельности частоты заболеваемости астмой или этнического фона.
Завершая краткий анализ основных форм бронхолегочной патологии, следует заключить, что БА относится к одной из наиболее трудных проблем молекулярной медицины. Это обусловлено широкой генетической и клинической гетерогенностью БА, невыясненным характером наследования генов предрасположенности, отсутствием четких критериев диагностики БА и другими причинами. По-видимому, выход из создавшегося положения необходимо искать в определении вклада неблагоприятных сочетаний генетических причин в этиологию и патогенез БА или вклада неблагоприятных
«ансамблей» из сотен и тысяч генов («генных сетей») и средовых факторов.
Безусловно, ускорению таких исследований будет способствовать тщательный анализ общности патогенетических механизмов БА и недостаточности альфа-1-антитрипсина, а также организация эффективной диагностики этих двух сочетающихся заболеваний (синтропического конгломерата) на основе организации селективного скрининга взрослых, страдающих эмфиземой легких, и детей, часто болеющих ОРЗ и ОРВИ, на недостаточность альфа-1-антитрипсина, а также на наличие мутаций генов-кандидатов предрасположенности
к БА.
Сахарный диабет I типа
Сахарный диабет I типа (СД I типа), или инсулинзависимый СД, относят к тяжелым МФЗ. Клиника СД хорошо изучена. Еще со студенческих лет известна симптоматическая аббревиатура СД I типа - это 3 «п» (полифагия, полидипсия и полиурия) и 2 «г» (гипергликемия и гликозурия).
Мультифакториальная модель наследования СД I типа предполагает, что манифестация болезни определяется суммарным действием генетических и средовых факторов. В случае генетических факторов речь идет о вкладе ряда аллелей полиморфных генов, вовлеченных в развитие заболевания, которые получили название генетических маркеров СД I типа. В случае средовых факторов речь идет о дополнительном вкладе неблагоприятных факторов среды. Это подтверждается близнецовыми исследованиями, свидетельствующими, что заболеваемость СД I типа у монозиготных близнецов составляет 40-50% в разных популяционных группах.
Более того, генетическая предрасположенность к СД I типа связана с наследованием группы аллелей «здоровых» генов, которые сцеплены с заболеванием и поэтому называются «этиологическими мутациями» или вариантами мутаций (в отличие от истинных мутаций).
Считается, что только наличие определенных комбинаций аллельных вариантов в генах предрасположенности может привести к развитию СД I типа. Однако сочетание аллельных вариантов с характером и спектром действия факторов среды пока мало изучено.
Современным подходом в изучении предрасположенности к СД I типа является также анализ ассоциации этого заболевания с полиморфными ДНК-маркерами.
Геном-кандидатом СД I типа называется ген, продукт экспрессии которого (фермент, гормон, рецептор, структурный или транспортный белок) может прямо или косвенно участвовать в развитии этой болезни. Известен ряд следующих полиморфных ДНК-маркеров.
• Однонуклеотидные полиморфизмы в экзонах. Им иногда соответствуют аминокислотные полиморфизмы, а также однонуклеотидные полиморфизмы в интронах, промоторных или регуляторных областях и в 5'- и 3'-нетранслируемых областях генов.
• Последовательности ДНК, содержащие вставки или делеции одного или нескольких нуклеотидов.
• Полиморфные миниили микросателлиты, представляющие собой тандемные повторы с изменяющимся числом повторяющихся единиц. Такого рода повторы могут располагаться как внутри гена (например, в интроне), так и рядом с геном в ближайших к нему районах. Вместе с тем, в большинстве случаев полиморфные ДНК-маркеры не являются этиологическими вариантами, которые определяют предрасположенность к СД I типа, но они достаточно часто могут быть сцеплены с этими вариантами.
В случае исследования СД I типа с применением подхода «генкандидат» в геноме удалось идентифицировать только два локуса, связанных с предрасположенностью к этому заболеванию: локус МНС (главный комплекс гистосовместимости), расположенный на хромосоме 6 (6р21.3), и полиморфный тандемный повтор (VNTR) в 5'-нетранслируемой области гена инсулина (INS), локализованный на хромосоме 11 (11р15.5). Эти два локуса получили специфическое обозначение: соответственно IDDM1 и IDDM2, и именно они определяют 42% случаев семейного наследования СД I типа.
При исследовании СД I типа с применением другого подхода, основанного на анализе полиморфных маркеров в ядерных семьях с двумя больными сибсами (семьи с конкордантными сибсами), а также дополнительного подхода с использованием полных семей с дискордантными сибсами удалось подтвердить сцепление с этим заболеванием 5'-нетранслируемой области гена инсулина.
Кроме того, были изучены предрасполагающие к СД I типа высокополиморфные микросателлитные маркеры, равномерно расположенные на всех хромосомах. Так, было идентифицировано 23 локуса, сцепленных с СД I типа. Анализ полученных данных позволяет заключить, что СД I типа ассоциирован с:
• аллелями гена HLA DQA1, которые кодируют аргинин в положении 52 (Arg 52+);
• аллелями HLA DQB1, которые не кодируют аспарагиновую кислоту в положении 57 (Asp57-).
Обе группы этих аллелей обозначаются как аллели, предрасполагающие к развитию СД I типа или аллели S.
В противоположность этим аллелям были выделены аллели, кодирующие Arg 52- и Asp 57+, которые обозначаются как аллели, предохраняющие от развития СД I типа, или аллели Р.
Вместе с тем, наиболее высокие оценки риска развития СД I типа могут быть получены при рассмотрении не самих аллелей, а их комбинаций, получаемых из сочетания всех четырех аллелей двух хромосом. Например, риск при сочетании SS/SS составил 52% против 4% в контрольной группе.
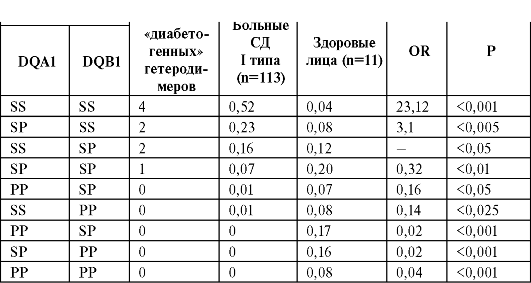
В табл. 12 приведено распределение комбинаций предрасполагающих (S) и предохраняющих (Р) аллелей генов HLA DQB1 в группах больных СД I типа и здоровых лиц на примере московской популяции.
Таблица 12. Распределение комбинаций предрасполагающих (S) и предохраняющих (Р) аллелей генов HLA-DQA1 и DQB1 в группах больных СД I типа и здоровых лиц в московской популяции (по Носикову В.В., 2005 г.)
 Как
видно из данных этой таблицы, среди больных резко снижена частота
комбинаций из двух предрасполагающих и двух предохраняющих аллелей.
Совсем нет лиц с одним предрасполагающим и
Как
видно из данных этой таблицы, среди больных резко снижена частота
комбинаций из двух предрасполагающих и двух предохраняющих аллелей.
Совсем нет лиц с одним предрасполагающим и
тремя предохраняющими аллелями. Нет лиц с четырьмя предохраняющими аллелями, в то же время в контрольной группе частота таких комбинаций 56%. Следует отметить, что кроме генов HLA DQ, в предрасположенность к СД I вовлечены и другие гены HLA, наиболее важными из которых считаются два полиморфных гена DRB1 и DPB1, относящихся к классу II.
Таким образом, основная часть генов предрасположенности к СД I определяется локусом IDDM1 и аллельными вариантами генов: HLA-DRB1, DQA1, DQB1 и DPB1. Предрасположенность к СД I связана с локусами многих других хромосом (всего 20 локусов IDDM). Эти локусы определены на 8 хромосомах: 2 (2q31-q33; 2q33 и 2q31-q34); 3 (3q21-q25); 10 (10p11; 10q11 и 10q25); 11 (11р15.5; 11q13 и 11q22.2-23.3); 12 (12р12-ptеr); 14 (14q12-q21; 14q24.3-q31 и 14q32.3); 15(15q26), а также Х-хромосома, где предполагается 4 сцепленных с этим заболеванием маркера, в том числе у одного маркера выделена область сцепления, соответствующая локусам
Хр11.4-р21.1.
Также обнаружено сцепление 5 маркеров СД I с геном глюкокиназы (GCK), а на экспериментальных моделях животных (крысы и мыши) показана роль гена индуцируемой NO-синтетазы (NOS2), которая разрушает бета-клетки островков Лангерганса. Кроме того, в последние годы обнаружен ряд дополнительных локусов, сцепленных с СД I, которые пока не получили обозначения в номенклатуре IDDM и поэтому не имеют номеров. Описаны также маркерные локусы хромосом 1(1q41-q43 - 6 маркеров; 1р41-р34 и 1q12-q24); 5 (5р15 и 5q34-gter) и 16 (16q22-q24).
Завершая рассмотрение данных об этиологии и механизмах патогенеза СД I, необходимо отметить, что сегодня нельзя однозначно признать наличие сцепления с этим заболеванием многочисленных генов-кандидатов предрасположенности к нему. Вместе с тем, при применении метода «ген-кандидат» удалось надежно идентифицировать два локуса: IDDM1 и IDDM2 (VNTR). Главный из них - это первый локус, определяющий 32% случаев семейной ассоциации с ним СД I типа. Причем район его максимального сцепления (MLS=45) находится на расстоянии 85 тыс. н.п. от гена
HLA-DQB1.
Второй локус определяет только 5-15% случаев семейной ассоциации с СД I типа. Обнаружена большая гетерогенность этого локуса в популяции, по-видимому, связанная в одних случаях с материн-
ским типом импринтинга, а в других случаях - с отцовским типом импринтинга (см. главу 4). Вклад других генов второго локуса хотя и значителен, но он меньше вклада генов первого локуса.
Кроме того, аллели локуса VNTR гена инсулина отнесены к «доминантно-предохраняющим» аллелям, а аллели первого локуса - к «рецессивно-предрасполагающим» аллелям. По-видимому, можно считать окончательно доказанным сцепление СД I типа еще с семью локусами (кроме двух вышеперечисленных). В их числе локусы: IDDV4-IDDM6, IDDM10, IDDM12, IDDM13 и маркер DXS1068, расположенный на Х-хромосоме; итого - 9 локусов, в которых расположены предрасположенности к СД I.
Язвенная болезнь желудка и двенадцатиперстной кишки
ЯБЖиДК - это системное МФЗ с полигенным вариантом наследования (см. главу 4). Прежде чем рассмотреть причины и механизмы ЯБЖиДК, необходимо отметить, что устойчивость слизистых оболочек желудка и двенадцатиперстной кишки к действию повреждающих факторов обеспечивается активностью тесно связанных между собой клеточных, тканевых и органных ферментных защитных систем, действие которых направлено на:
• достаточную (по количеству и содержанию) продукцию слизи в желудке; снижение общей продукции слизи и изменение содержания отдельных ее компонентов (например, мукополисахаридов, гликопротеинов, сиаловых кислот) ведет к потере способности слизи обволакивать слизистую оболочку;
• активную секрецию бикарбонатов; снижение секреции бикарбонатов нарушает процесс нейтрализации соляной кислоты в гастродуоденальной зоне;
• активную регенерацию покровных эпителиальных клеток в гастродуоденальной зоне; угнетение этой регенерации снижает прочность барьера слизистой желудка, что связано с дефицитом коллагенов I и III типов, необходимых для формирования рубца;
• оптимальное кровоснабжение слизистых оболочек; нарушения регионального кровотока и микроциркуляции в гастродуоденальной зоне сочетаются с нарушениями свертывающей и противосвертывающей системы крови, проницаемостью сосудов и обменом биогенных аминов, что ведет к очаговой ишемии либо в малой кривизне желудка, либо в луковице двенадцатиперстной кишки, которые бедны сосудами;
• сохранение барьерной функции апикальной мембраны клеток поверхностного эпителия - эпителиоцитов, состоящей из трехслойного липопротеинового комплекса; разрушение этой мембраны лежит в основе патогенеза длительно не рубцующихся язв;
• угнетение желудочной кислотной продукции; показано, что аполипопротеин А-IV и трефоил-пептиды снижают кислотную продукцию и ускоряют восстановление поврежденной гастроинтестинальной слизистой оболочки; также показано, что интерлейкин-1-бета и трансформирующий альфа-фактор роста гепатоцитов влияют на белки цитоскелета эпителиоцитов и способствуют их миграции к язвенному дефекту;
• снижение уровня ПОЛ клеточных мембран эпителиоцитов слизистой оболочки; интенсификация уровня ПОЛ ведет к снижению концентрации фосфолипидов в мембранах эпителиоцитов слизистой оболочки, деструкции клеточных структур, нарушению их физиологической и репаративной регенерации.
Кроме того, показано значение иммунных механизмов в развитии язвенной болезни, наиболее выраженных при медиогастральной локализации труднорубцующихся язв. В этом случае нарушается неспецифическая защита, снижается гуморальный иммунитет, изменяется содержание цитокинов, уменьшается количество Т-лимфоцитов и соотношение Т-хелперов и Т-супрессоров.
Также эффективно изучается роль нарушений защитной системы глутатиона при ЯБЖиДК. Установлено, что основным этиологическим фактором в 75-95% случаев язвенной болезни двенадцатиперстной кишки (ЯБДК) и 65-80% случаев язвенной болезни желудка (ЯБЖ) служит Helicobacter pylori (HP). Этот условно-патогенный микроорганизм сосуществует с человеком, но при нарушении равновесия в микроэкологической системе желудка и двенадцатиперстной кишки начинает проявлять свое отрицательное воздействие. В России данной бактерией инфицировано 73-91% взрослого и 44-50% детского населения.
Окончательно доказан семейный характер пилорического хелиобактериоза. Например, в Ирландии семейный характер отмечен при инфицировании одного из родителей больного ребенка в 94% заболеваний и при инфицировании сразу двух родителей в 61,5%.
Механизмом патогенетического действия НР является цепь последовательных событий, начинающихся с адгезии НР к желудочному эпителию посредством АЕL-феномена: повреждение НР конкретной
области слизистой оболочки - повышение внутриклеточной концентрации Са2+ - фосфорилирование и перестройка белков цитоскелета эпителиоцитов и эритроцитов. В пользу этого механизма свидетельствует следующее.
• Ассоциация ЯБЖ с первой группой крови; в частности, у лиц с этой группой крови на слизистой оболочке желудка были экспрессированы адгезивные рецепторы к НР в достоверно большей степени, чем у лиц с другими группами крови.
• НР-опосредованный ульцерогенез (образование язвы) или формирование цитотоксических и нецитотоксических реакций замедленного типа, ведущих к иммуноцитолизу участка гастродуоденальной зоны слизистой оболочки. При этом формирование цитотоксической реакции связано с тремя последовательными событиями. Первое событие - продукция вакуолизирующего цитотоксина vacA, уменьшающая скорость реэпителизации язв, пролиферацию эпителия и полимеризацию актина в эпителиоцитах, что нарушает целостность их цитоскелета. Второе событие - продукция цитоксинассоциированного белка cagA. Третье событие - продукция уреазы, служащей индуктором апоптоза эпителиоцитов.
• НР-стимулированное ПОЛ, поддерживающее активный воспалительный процесс в пилородуоденальной зоне.
• Дополнительное воздействие других эндогенных и экзогенных факторов, участвующих в патогенезе заболевания и определяющих патогенность НР.
Вместе с тем, теория развития ЯБЖиДК на основе НР не объясняет множества особенностей патогенеза данного заболевания. Не выяснены механизмы образования одиночных язвенных дефектов слизистой оболочки, сезонности смены обострений и ремиссий, а также причины половых различий в проявлении заболевания (редкость поражения лиц женского пола и высокая частота поражения лиц мужского пола). Поэтому НР-инфицированию отводится роль важного, но только пускового локального фактора.
Вместе с тем, главное внимание уделяется наследованию предрасположенности к ЯБЖиДК. В пользу этого свидетельствуют многочисленные данные (Хорошая И.В., 2006). В частности, показано, что наследование предрасположенности к ЯБЖиДК выявляется у 40-50% больных и реализуется независимо от наследственных фак-
торов, предрасполагающих к колонизации НР гастродуоденальной зоны. При этом частота конкордантности монозиготных близнецов по манифестации ЯБЖиДК в 2-5 раз выше, чем дизиготных близнецов. У больных с наследственной отягощенностью, подтвержденной наличием генетических маркеров, заболевание протекало менее благоприятно (тяжелее, с манифестацией в раннем возрасте и в сочетании с пилоростенозом, кровотечениями и перфорациями слизистой); выявлялась генетическая общность между ЯБЖ и хроническим гастритом.
Кроме того, показаны ассоциативные связи между язвенной болезнью и:
• менделирующими признаками (первая группа крови для ЯБДК, вторая группа крови для язвенной болезни кардиальной части желудка); в первом случае риск развития заболевания был на 35% выше, а количество клеток, секретирующих пепсиноген, было на 15% выше, чем во втором случае;
• снижением активности ацетилхолинэстеразы, щелочной фосфатазы (отсутствие кишечного компонента при желудочной локализации и снижение индекса В) и холинэстеразы (отсутствие фракции 3-1 и связь с С5-компонентом локуса Е2);
• способностью ощущать горький вкус фенилтиокарбомида;
• астеническим телосложением и дактилоскопическим рисунком. Показана гетерогенность болезни по скорости Na+-Li+-
противотранспорта.
Среди факторов, предрасполагающих к развитию болезни и повышающих ее риск в 1,5-3 раза, отмечено снижение активности альфа- 1-антитрипсина и альфа-2-макроглобулина.
Для русской популяции определены иммуногенетические маркеры предрасположенности к дуоденальной язве (HLA-B15) и ее осложненному течению (HLA-A1, HLA-A2).
Показано, что HLA-фенотипы В35, А2/А3, А2/А0 являются прогностически значимыми для оценки риска кровотечения из дуоденальной язвы, а антигены HLA B8 и A3 могут служить прогностическими критериями, свидетельствующими, что болезнь, вероятно, не разовьется. В случае ульцерогенеза предрасположенность может проявиться увеличением массы обкладочных клеток, гиперплазией гастриновых клеток, секреторной гиперактивностью желудка. В последнем случае гиперактивность рассматривается в роли субклинического маркера семейного накопления случаев ЯБДК. В таких
семьях повышение уровня пепсиногена обнаруживается как у больных пробандов, так и их родителей. Также показана связь между аллельным полиморфизмом локуса гена пепсиногена С и язвой тела желудка, а гиперпепсиногенемия и гипергастринемия участвуют в патогенезе ювенильных дуоденальных язв.
Таким образом, в исследованиях по этиологии и механизмам патогенеза ЯБЖ и ДК накоплено много фактов, свидетельствующих о значительном вкладе условно-патогенного микроорганизма Heliobacter pylori - основного пускового локального фактора, проявляющего свое действие на фоне экспрессии генов предрасположенности к этому заболеванию.