Клиническая генетика. Геномика и протеомика наследственной патологии : учеб. пособие. - 3-е изд., перераб. и доп. - Мутовин Г.Р. 2010. - 832 с. : ил
|
|
|
|
ГЛАВА 18 МЕТОДЫ ПЕРВОГО ЭТАПА ДИАГНОСТИКИ НАСЛЕДСТВЕННОЙ ПАТОЛОГИИ
Методика обследования больных с наследственной патологией включает: первый (клинический) и второй (параклинический) этапы.
На клиническом этапе применяются: основные и дополнительные клинические, а также основные клинико-инструментальные и клинико-лабораторные методы. Кроме того, на завершающей стадии этого этапа применяется метод постановки предварительного диагноза на основе компьютерных баз данных. В случае обследования организма беременной, зародыша, эмбриона и плода дополнительно применяются специальные клинико-инструментальные и клинико-лабораторные методы преимплантационной и пренатальной диагностики.
На параклиническом этапе применяются специальные лабораторные методы, цитогенетические, молекулярно-генетические и биохимические методы, а в определенных ситуациях еще и популяционностатистический метод (см. главу 19).
МЕТОДЫ ПЕРВОГО ЭТАПА ДИАГНОСТИКИ НАСЛЕДСТВЕННОЙ ПАТОЛОГИИ
Основные клинические методы
К основным клиническим методам относятся: первичный прием у врача, клинико-генеалогический метод, объективный врачебный осмотр и синдромологический метод.
Первичный прием у врача
Первичный прием у врача предусматривает работу с пробандом (консультируемое лицо) и его ближайшими родственниками. Во время первичного приема проводятся сбор данных анамнеза жизни и анамнеза заболевания и их анализ.
Собираемые врачом данные чрезвычайно важны для постановки точного диагноза, ибо они нередко содержат опорные пункты, на основе которых диагноз можно предположить сразу.
В числе таких данных должны быть собраны сведения о:
• сибсах (братья и сестры), родителях и других родственниках пробанда, как минимум I и II степеней родства;
• предыдущих беременностях и родах, периодах новорожденности, вскармливания и раннего развития пробанда;
• отягощенном характере течения данной беременности (прием лекарств, воздействие мутагенных и тератогенных факторов на эмбрион и плод, наличие у супругов вредных привычек и профессиональных вредностей);
• отягощенном акушерском анамнезе (наличие токсикозов, угрозы выкидыша, многоили маловодия, преждевременных родов, случаев предшествующего мертворождения или рождения детей с ЗВУР, ВПР, ХБ, МБ и МФЗ;
• отягощенном гинекологическом анамнезе (инфекции, передаваемые половым путем, хронические соматические заболевания неинфекционной природы).
Кроме данных о пробанде, врач собирает и анализирует данные о его близких родственниках, имеющих подобное заболевание или частично сходную симптоматику. Если такие родственники выявляются, то они приглашаются для объективного обследования.
Клинико-генеалогический метод
Клинико-генеалогический (генеалогический) метод основан на данных, полученных у пробанда или его родственников в ходе первичного приема у врача. Этот метод является обязательной составной частью первичного приема.
Генеалогический метод относится к наиболее старым методам медицины, но по-прежнему остается и будет оставаться одним из самых востребованных.
Данный метод относительно прост и доступен. Его сущность заключается в сборе врачом генеалогических данных, необходимых для последующего составления и анализа семейной родословной пробанда.
Сбор таких данных нацелен на выявление и изучение симптомов наследственного и врожденного заболевания, проявившихся у пробанда, а также у его больных и здоровых родственников.
Порядок сбора генеалогических данных и характер вопросов, задаваемых пробанду и его близким родственникам, приведены ниже. В ходе сбора данных желательно использование семейных фотоальбомов, медицинских архивов и другой документации.
При составлении родословной врач применяет стандартные приемы и символы.
Индивид, с которого начинается генеалогическое исследование, - это пробанд. Братья и сестры пробанда - это сибсы пробанда (родные, двоюродные, троюродные).
Каждый человек, включенный в семейную родословную, получает свой символ (квадрат обозначает мужчину, кружок - женщину) и шифр, состоящий из двух цифр (римская обозначает номер поколения в родословной, арабская - номер индивида в родословной; нумерация членов одного поколения осуществляется последовательно слева направо).
Имеются и другие условные обозначения (символы): аборт, гетерозиготный носитель мутантного гена, моно- и дизиготные близнецы, выкидыш (самопроизвольный аборт), мертворожденный, умерший индивид и т.д. (рис. 60). Под семейной родословной помещается ее легенда, расшифровка условно принятых обозначений. Схематическое изображение такой родословной начинается с пробанда (помечен стрелкой), который обычно располагается в последнем (изучаемом) поколении родственников. Семейная родословная должна охватывать не менее двух-трех поколений родственников. Ограничений в количестве анализируемых поколений нет, и чем больше будет их исследовано, тем достовернее будут выводы.
Далее собираются и обозначаются данные о детях пробанда (если это взрослый человек) и его сибсах (с учетом последовательности беременностей и их исхода).
Затем собираются сведения о родственниках по линии матери: сначала все о матери пробанда, ее сибсах и их детях, затем все о бабушке по линии матери, ее сибсах и их детях и внуках. Если возможно, то собираются сведения о прабабушке пробанда. В такой же последовательности собираются сведения о родственниках по линии отца.
Следующий этап - это анализ причин имеющегося заболевания (признака). Тут принципиальное значение имеют: величина выборки, на основе которой составлена родословная (2-3 поколения родственников), полнота регистрации носителей признака и другие показатели. Необходимо помнить о фенокопиях заболевания (см. главу 3).
Современное значение клинико-генеалогического метода трудно переоценить. Собранные врачом генеалогические данные позволяют определить у пробанда наследственный или ненаследственный харак-
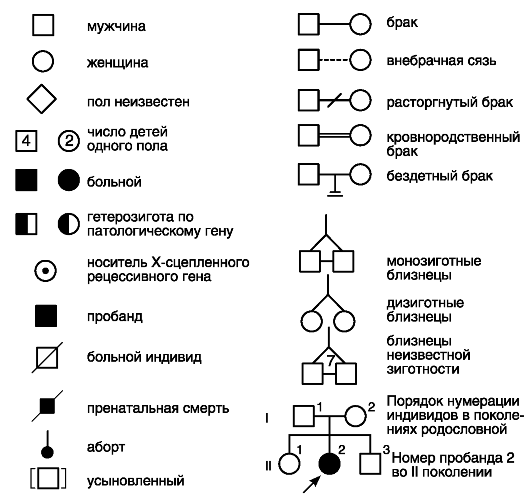 Рис. 60. Символы, используемые при составлении родословной
Рис. 60. Символы, используемые при составлении родословной
тер заболевания (отдельного симптома), вариант его наследования (традиционные моногенный или полигенный либо нетрадиционный варианты), установить в случае моногенного варианта локализацию патологического гена на аутосоме или гоносоме (т.е. картировать ген), а также определить частоту его распространения в популяции.
Клинико-генеалогический метод успешно применяется для анализа сцепления гена заболевания с его маркером (маркерным локусом). Такой анализ широко используется в диагностике гетерозиготных состояний, пренатальной диагностике, ранней диагностике заболевания в доклинической фазе, диагностике стертых форм и
при позднем проявлении болезни. Например, с помощью анализа сцепления генов (см. главу 19) диагностируются гемофилия АиВ, миодистрофия Дюшенна-Беккера, миотоническая дистрофия, синдром недоразвития ногтей и отсутствия коленной чашечки и многие другие заболевания.
После сбора генеалогических данных врач приступает к объективному осмотру пробанда и его родственников.
Объективный врачебный осмотр
Объективный врачебный осмотр начинается с изучения внешнего вида пробанда. Методической основой такого осмотра является семиотика - наука о знаках (символах) патологического процесса в организме, правильном их обозначении, морфологических и функциональных изменениях органов и частей тела, динамике клинических проявлений, т.е. идентификация символов наследственной патологии - это обязательное условие для ее успешного выявления у пробанда.
С этой целью широко используются разные предметно-образные знаки для обозначения разнообразных признаков, например: «барабанные палочки», «веслообразные ребра», «капельное сердце» и т.п.
Характерные предметно-образные знаки используются и в клинической генетике. С их помощью обозначают главные симптомы наследственного или врожденного заболевания.
Известно, что во многих случаях у больного с наследственной патологией наблюдается характерный внешний вид или знаки генетического заболевания, например: «лицо эльфа» (синдром Вильямса), «птицеголовая карликовость» (синдром Секкеля), гаргоилический дисморфизм (мукополисахаридозы и муколипидозы), «кошачий крик» (синдром делеции короткого плеча хромосомы 5), «кошачий глаз» (синдром Шмида-Фраккаро), «глаза лани» (синдром частичной моносомии по длинному плечу хромосомы 22) и т.д.
Неудивительно, что характерный внешний вид делает разных больных из разных контингентов и семей более похожими друг на друга, чем даже на близких родственников.
При внешнем осмотре пробанда внимание врача должно быть направлено также на выявление соответствующих предметнообразных знаков у близких родственников.
После внешнего осмотра врач выявляет у пробанда другие характерные особенности заболевания: время манифестации или возраст больного, на который приходится появление первых признаков, прогредиентный характер течения, множественность (полисистемность)
поражения, сегрегацию заболевания и/или его симптомов в родословной, резистентность к терапии (см. главу 17).
Следует отметить, что метод объективного врачебного осмотра должен параллельно сопровождаться синдромологическим методом (подходом), являющимся его составной частью.
Синдромологический метод
Синдромологический метод - это вторая (после семиотики) методическая основа для успешной диагностики наследственной патологии. Обязательным условием применения данного метода является знание врачом основных понятий и положений клинической генетики (см. главы 2-5).
Выявление знаков (символов), характерных для наследственной патологии, предусматривает «поэтажное» (сверху вниз) обследование организма пробанда: лицо, голова, шея, плечевой пояс и верхние конечности, грудная клетка и область живота, позвоночник, тазовый пояс и нижние конечности, наружные половые органы. При этом врач последовательно оценивает:
• весо-ростовые (антропометрические) отклонения от нормы;
• своевременность закрытия родничков, зон роста длинных трубчатых костей, так называемый костный возраст;
• тип телосложения и наличие асимметрии, пропорциональность строения скелета, головы, туловища и конечностей;
• состояние кожи, подкожной жировой клетчатки и слизистых оболочек, наличие нарушений пигментации кожи и слизистых, состояние оволосения, рост волос и ногтей;
• размеры, форму и наличие аномалий развития черепа, глаз, ушных раковин, лица, носа, рта, губ, верхней и нижней челюсти, нёба и зубов;
• размеры и форму шеи;
• размеры и форму грудной клетки: состояние грудины, ключиц, лопаток и ребер;
• наличие грыж белой линии живота, паховых и пупочных грыж;
• состояние мышц передней брюшной стенки;
• форму, длину и другие особенности строения верхних и нижних конечностей;
• степень подвижности суставов;
• состояние мышечного тонуса;
• состояние внутренних органов, эндокринных желез и репродуктивных органов;
• состояние и тип задержки развития организма, включая физическое, психомоторное (на первом году жизни), умственное (психическое), речевое и половое развитие;
• наличие и степень выраженности неврологической симптоматики, офтальмологических изменений, нарушений вкуса, обоняния, осязания, слуха, болевой и тактильной чувствительности;
• цвет и запах мочи и/или запах тела.
Из выявленных при «поэтажном» обследовании пробанда признаков врач выделяет главные признаки болезни. В их числе: патогномоничные признаки, например низкий рост при наследственных формах карликовости; ведущие признаки, например атаксия (нарушение координации и походки) и телеангиэктазии (сосудистые звездочки на коже, склерах и слизистых оболочках) при синдроме Луи-Бар; типичные признаки, например сколиоз при наследственных заболеваниях соединительной ткани и скелета.
Кроме главных признаков, врач выделяет неспецифические признаки, например клинодактилию мизинца (может встречаться в норме и при синдроме Сильвера-Рассела).
Следует отметить, что все выделенные врачом признаки должны оцениваться не сами по себе, а как показатели (символы) определенного патологического процесса.
Любой признак может быть знаком наследственного заболевания, но может и не иметь символического значения, наблюдаясь у совершенно здорового человека.
Важно помнить, что диагностика и особенно дифференциальная диагностика наследственного и врожденного заболевания всегда начинается с определения патогномоничных, ведущих и типичных признаков, которые вовсе не должны подсчитываться, а скорее должны «взвешиваться» (по своему значению). Это прежде всего относится к признакам МАР, при которых количество не имеет определяющего значения без оценки каждого признака в отдельности.
Особенности врачебного осмотра при врожденных аномалиях развития
Врачебный осмотр пробанда при врожденных аномалиях развития нацелен на их полное выявление и регистрацию. Наиболее эффективно он проводится с помощью карты фенотипа пробанда (см. приложение 1). Эта карта позволяет выявить практически весь спектр больших и малых аномалий развития при «поэтажном» осмотре больного. Причем на каждом «этаже» можно обнаружить значительное число типов МАР, включая таковые черепа - 17 типов
(аномалии формы, окружности, особенности волосистой части головы); лица - 75 типов (аномалии лба, надбровных дуг, бровей, ресниц, орбит, носа, ушных раковин, ротовой области и полости рта); шеи - 6 типов; грудной клетки - 10 типов; живота - 6 типов; позвоночника и спины - 9 типов; половых органов - 10 типов; туловища в целом - 10 типов; конечностей и суставов - 18 типов; кожи и ее придатков - 14 типов.
После выявления аномалий развития подсчитывается их количество: сначала отдельно БАР и МАР, затем их общая сумма, а также число дополнительных аномалий, регистрация которых не была предусмотрена картой фенотипа.
После всех подсчетов врач определяет степень и вариант ЗВУР (гипопластический, гипотрофический или диспластический) и оценивает у пробанда: отставание массы тела от нормы при данном гестационном возрасте и росте, трофические нарушения и снижение тургора кожи, нарушения гомеостаза, иммунологической реактивности и изменения функционального состояния ЦНС.
Затем врач ставит предварительный диагноз врожденного заболевания, по возможности выделяя: моногенные пороки, наследственные синдромы, множественные ВПР, пороки мультифакториальной природы, пороки при хромосомных нарушениях и пороки неустановленного генеза. Большую помощь в постановке диагноза наследственного и врожденного заболевания врачу может оказать метод предварительного диагноза с помощью компьютерных баз данных (см. ниже).
Дополнительные клинические методы
Близнецовый метод
Близнецовый метод - это незаслуженно забытый практиками дополнительный клинический метод. Теперь он чаще применяется специалистами по медицинской психологии, став для них одним из основных методов исследования.
Вероятно, такая «забывчивость» врачей объясняется общим снижением в России показателя рождаемости детей, а на этом фоне - еще большей редкостью случаев рождения близнецов. Вместе с тем, общая частота рождения двоен в мире - 1-2% новорожденных, тогда как тройни рождаются с частотой 1 случай на 10-15 тыс. родов.
Важным аргументом в пользу применения близнецового метода является разработка на его основе таких информативных методов, как метод экспериментального изучения близнецов (см. ниже).
Сущность же близнецового метода состоит в выяснении у близнецовой пары, тройни или четверни наследственной обусловленности нормальных и патологических признаков или гено-фенотипических корреляций.
Главный принцип близнецового метода заключается в сравнении монозиготных и дизиготных близнецов. При этом вычисляются показатели соответствия (конкордантность) или несоответствия (дискордантность) и определяется частота возникновения одного и того же заболевания (признака) у близнецов в каждой паре, тройне или четверне. С одной стороны, известно, что генетическая характеристика монозиготных близнецов - это 100% общность их генов (генотипов), а особенность дизиготных близнецов - 50% общность их генов (генотипов). С другой стороны, факторы среды, как правило, одинаково воздействуют на тех и других близнецов не только на внутриутробном, но и на внеутробном этапе их развития.
Вместе с тем, иногда постнатальные условия для каждого из близнецов одной пары могут оказаться разными, и тогда фенотипические различия у дизиготных близнецов будут объясняться их генотипическими различиями. Наоборот, у монозиготных близнецов генотипы одинаковые, и возникающие у них фенотипические различия объясняются разным влиянием внешней среды на экспрессию генов в их генотипах. Иными словами, речь идет о специфических проявлениях генетического полиморфизма у близнецов двоен и троен, т.е. проявлениях небольших повторяющихся последовательностей ДНК (мини- и микросателлитных повторов).
Не исключено, что генетический полиморфизм оказывает существенное влияние на функции многих генов, включая поведенческие гены. В связи с этим не должно удивлять различие (хотя и наблюдающееся крайне редко) в характерах монозиготных близнецов, что позволяет оценивать роль генотипа и факторов среды в каждом конкретном случае как уникальную особенность организма.
Например, конкордантность по УО составляет у монозиготных близнецов 97%, у дизиготных близнецов - 37%; по шизофрении - 69% и 10%, эпилепсии - 67% и 30% соответственно, т.е. роль генотипа в данных случаях ярко выражена.
В настоящее время при применении близнецового метода выделяют: диагностику зиготности близнецов, статистическое исследование близнецовой выборки и экспериментальное изучение близнецов. В основе диагностики зиготности лежит изучение сходства и различий
у партнеров одной близнецовой пары (тройни, четверни) по совокупности ряда признаков, изменяющихся под влиянием факторов окружающей среды. С этой целью разработан метод полисистемного сходства (подобия) по внешним признакам (цвет и форма волос, разрез и цвет глаз, форма ушных раковин, бровей, носа, губ, подбородка и т.д.).
Разработан метод контроля по партнеру, используемый только у монозиготных близнецов. Он позволяет точно оценить то или иное внешнее воздействие, если один партнер по монозиготной паре подвергся такому воздействию, а другой нет (например, прием лекарственного препарата).
Следует отметить, что подобные близнецовые исследования выгодны в экономическом плане, ибо позволяют ограничивать выборку двумя-тремя десятками пар близнецов.
К статистическому исследованию близнецовой выборки относится анкетирование близнецов, которое целесообразно проводить в популяционных исследованиях с большими выборками. Перспективно также применение близнецового метода в сочетании с другими методами (цитогенетические, биохимические и др.).
К методам экспериментального изучения близнецов относятся:
• иммуногенетический метод: сравнение по антигенам, белкам сыворотки крови, гаплотипам HLA, т.е. менделирующим признакам, которые не изменяются в течение всей жизни индивида, несмотря на воздействие факторов среды;
• исследование дерматоглифики (в настоящее время почти не применяется);
• изучение наследуемых способностей (например, чувства вкуса фенилтиокарбамида);
• изучение данных ЭКГ и ЭГ;
• трансплантация кожного лоскута.
Метод дерматоглифики
Метод дерматоглифики также забыт врачами (но уже безнадежно) и применяется лишь в судебной медицине. Сущность метода состоит в анализе врачом полученных от пробанда кожных узоров (рисунков) его ладоней и стоп. Метод наиболее информативен при хромосомных болезнях, когда, например, выявляются: дистальный осевой трирадиус, избыток дуг на пальцах, отсутствие дистальной межфаланговой складки, радиальные петли на I, IV и V пальцах, четырехпальцевая (обезьянья) складка.
В дальнейшем необходимость применения метода дерматоглифики, по-видимому, вообще отпадет из-за эффективного внедрения в медицину «ДНК-дактилоскопии».
Вместе с тем, метод дерматоглифики останется в истории медицины как метод начала эпохи развития клинической генетики.
Основные клинико-инструментальные и клинико-лабораторные методы
После применения основных и дополнительных клинических методов обследования врач в случае необходимости использует основные клинико-инструментальные и клинико-лабораторные методы.
К первым относятся: методы функциональной диагностики (антропометрия, аудиометрия, велоэргометрия, исследование объема легких и функции внешнего дыхания, исследование остроты зрения, ультразвуковое исследование, электро(эхо)кардиография, электромиография, электроэнцефалография и др., эндоскопические методы исследования внутренних органов (бронхоскопия, гастродуоденоскопия, колоноскопия, цистоскопия), а также рентгеноскопия и рентгенография, томография и метод ядерно-магнитного резонанса.
Ко вторым относятся: биопсия и микроскопия кожи, копрология, общий анализ мочи, общий и биохимический анализы крови, определение гормонального и метаболического профилей, уровня иммуноглобулинов сыворотки крови, группы крови и резус-фактора.
Метод предварительного диагноза на основе компьютерных баз данных
Заключительной частью первого этапа обследования является проведение метода постановки предварительного диагноза на основе компьютерных баз данных. Его использование существенно повышает эффективность работы врача, позволяет ему во многих случаях предотвратить рождение в семье больного ребенка с наследственным и врожденным заболеванием и осуществить своевременное патогенетическое лечение такого заболевания.
Базы данных
В настоящее время создан и размещен в Интернете ряд удобных и эффективных для пользователя баз данных и экспертных диагностирующих систем, применяемых для предварительной диагностики МБ (4,5 тыс. нозологий), ХБ (100 нозологий) и хромосомных нарушений (900 типов), а также БАР (23 обязательных для учета ВПР).
В число наиболее известных баз данных входят:
• каталог менделирующих признаков человека В. Мак-Кьюсика (OMIM);
• Лондонская (Оксфордская) медицинская база данных (LMD);
• ряд отечественных систем.
Все эти диагностические системы позволяют врачу любой специальности при его обычном умении пользоваться компьютером быстро и надежно диагностировать по минимальному набору признаков наследственные и врожденные заболевания.
Ниже приводится краткое описание используемых с этой целью основных баз компьютерных данных.
Каталог менделирующих признаков человека В. Мак-Кьюсика (OMIM)
OMIM разработан в конце 90-х годов XX в., применяется для получения данных через сеть Интернет и расположен на сайте NCBI Национального центра биотехнологии и информации. База данных содержит текстовую информацию и множество ссылок на дополнительные ресурсы в NCBI и других источниках. Поиск необходимой информации можно осуществлять, вводя одно или несколько ключевых слов в текстовом блоке.
Расширенные опции поиска доступны через закладки Limits, Preview/Index, History и Clipboard в серой области под текстовым блоком. OMIM содержит дополнительную информацию, примеры пользования основной и расширенной поисковой системами. Специальные ссылки обеспечивают быстрый доступ к подробной технической информации, информации по опциям поиска, часто задаваемым вопросам (FAQ) и информации о «родственных» ресурсах.
OMIM предназначен для использования врачами и другими специалистами, имеющими непосредственное отношение к генетическим нарушениям, учеными-генетиками и студентами-медиками, биологами. OMIM также открыта для общего пользования, поэтому любые пользователи, ищущие информацию в базе данных, имеют возможность обращаться к ней для постановки диагноза и получения ответов на персональные вопросы. Ниже приведен логотип этой базы данных.
 Лондонская (Оксфордская) медицинская база данных
Лондонская (Оксфордская) медицинская база данных
Лондонская (Оксфордская) медицинская база данных (Oxford Medical Databases или LMD) наиболее широко применяется в клинической практике для оказания помощи врачам в постановке диагноза заболевания, а также как источник клинической и генетической информации, позволяющий целенаправленно обследовать каждого больного.
Используя интерфейс Windows, врач с помощью этой программы получает данные в самых разных вариантах. Быстрые и гибкие средства поиска применяются для запроса необходимых сведений, которые обычно поставляются пользователю на подписной (коммерческой) основе.
Обновление базы данных ведется непрерывно с середины 80-х годов XX в. В базе содержится клиническая и генетическая информация из сотен журналов и ресурсов online. К основному перечню синдромов постоянно добавляются новые синдромы. В свою очередь, информация о синдромах, ранее включенная в базу данных, дополняется новыми сообщениями и самыми последними клиническими и генетическими сведениями.
В базе LMD имеется подробное описание каждого синдрома:
• название синдрома и наиболее часто используемые его синонимы;
• локализация гена, обусловливающего синдром, на хромосоме (если известно);
• номер по каталогу В. МакКьюсика (OMIM); в этом случае предусмотрена связь непосредственно с OMIM;
• тип наследования синдрома;
• компактный информативный обзор данных о синдроме и список литературы, посвященный ему и известный в настоящий момент;
• список признаков и симптомов синдрома;
• фотографии больных из данных литературы и/или собственных коллекций авторов.
Фотобиблиотека, интегрированная в базу данных, содержит свыше 12 500 образцов.
Используя программное обеспечение LMD, можно:
• просматривать названия синдромов в алфавитном порядке;
• отображать отдельные записи синдромов, содержащие краткое описание; характеристики, ссылки и фотографии (если доступ-
но), локализацию генов на хромосоме, тип наследования и номер по каталогу OMIM;
• осуществлять поиск синдромов, используя определенную подборку клинических характеристик и/или любого из указанных выше типов данных;
• искать синдром по названию или используя информацию об авторе, журнале и дате публикации;
• вставлять в программу собственные фотографии пациентов;
• создавать коллекции фотографий, используя образцы из библиотеки или собственные;
• создавать списки синдромов или ссылок для дальнейшего анализа синдромов;
• распечатывать информацию и сохранять ее в отдельных файлах. Ниже приведен логотип LMD.
 Отечественные информационно-поисковые диагностические системы
Отечественные информационно-поисковые диагностические системы
Мультимедийная информационно-справочная система «Врожденные пороки развития»
Мультимедийная информационно-справочная система (МИСС) «Врожденные пороки развития» сформирована в виде электронного учебника, который позволяет врачу получать необходимую клиническую и генетическую информацию для диагностики и профилактики 23 обязательных для учета ВПР.
Доступ пользователя к различным разделам программы производится на основе предметного указателя (указателя гиперссылок).
Программа выполняет следующие функции.
• 1. Предоставление информации об общей характеристике и классификации ВПР, этиологии и патогенезу, зависимости ВПР от времени возникновения в ходе внутриутробного онтогенеза, локализации в организме, частоте в популяции, тяжести ВПР и его влиянии на здоровье ребенка, систематизации по анатомофизиологическому принципу.
• 2. Предоставление информации с учетом полного перечня нозологических форм ВПР, подлежащих обязательной регистрации при их мониторинге, который проводится в регионах РФ с 1999 г.
Информация о ВПР содержит сведения об определении, популяционной частоте, этиологии и патогенезе, клинической характеристике, пренатальной диагностике, лечении, профилактике, регистрационном коде по международной классификации болезней.
МИСС ВПР предусматривает возможность распечатки визуальных (экранных) форм, содержащих текстовую информацию, таблицы, рисунки, схемы, фотографии.
Обеспечение информационного доступа осуществляется в интерактивном режиме с использованием алфавитного указателя (словаря), гиперссылок, перечня нозологических форм ВПР, подлежащих обязательной регистрации при мониторинге.
Ниже приведен логотип МИСС ВПР.
 Система диагностики наследственных нервно-мышечных заболеваний
Система диагностики наследственных нервно-мышечных заболеваний
Информационно-поисковая система диагностики (ИПСД) наследственных нервно-мышечных заболеваний (ННМЗ) создана в ГУ «Медико-генетический научный центр РАМН» коллективом авторов (Угаров И.В., Дадали Е.Л., Евдокименков В.Н. и др.).
Информационное наполнение ИПСД ННМЗ осуществлено за счет обобщения многочисленных клинических и генетических данных, отечественных и зарубежных источников литературы, ресурсов online.
При создании каталога признаков ННМЗ за основу взята структура клинических признаков ННМЗ из Лондонской базы данных (см. выше).
Базу иллюстративного клинического материала авторы ИПСД дополнили фотографиями больных из собственных коллекций, результатами изучения биоптатов мышечных и нервных волокон, электрофорограммами и электронейромиограммами больных с ННМЗ, предоставленными сотрудниками кафедры общей и меди-
цинской генетики медико-биологического факультета ГОУ ВПО РГМУ. Эта ИПДС рассчитана на диагностику 114 форм ННМЗ.
Вспомогательные модули поддержки принятия решения, включающие «виртуального советника» и справочные разделы, оптимизируют процедуру диагностического поиска и принятие решения в сложных диагностических ситуациях.
Ниже приведен логотип ИПСД ННМЗ.
 После
постановки предварительного диагноза с помощью компьютерных баз данных
врач переходит ко второму этапу диагностики наследственной патологии с
применением параклинических методов (см. главу 19).
После
постановки предварительного диагноза с помощью компьютерных баз данных
врач переходит ко второму этапу диагностики наследственной патологии с
применением параклинических методов (см. главу 19).
Если на первом этапе диагностики возникает необходимость обследования организма беременной, зародыша, эмбриона и плода, врач применяет специальные клинико-инструментальные и клиниколабораторные методы.
Специальные клинико-инструментальные и клиниколабораторные методы
К специальным клинико-инструментальным и клиниколабораторным методам относятся методы преимплантационной и пренатальной диагностики наследственных и врожденных болезней. Среди этих методов выделяют: неинвазивные (без проникновения в организм) и инвазивные (с проникновением в организм).
Методы преимплантационной диагностики
Преимплантационная диагностика - это исследование молекулы ДНК в клетках зародыша на ранней стадии развития зиготы - ста-
дии бластоциста (6-8 клеток, полученных при оплодотворении in vitro - неинвазивный метод) или при помощи маточного лаважа в период 90-130 ч после оплодотворения (инвазивный метод).
Суть этих методов заключается в том, что с помощью микрохирургического вмешательства от зародыша отделяются одна или две клетки для последующего генетического анализа.
Остальные зародышевые клетки замораживаются до окончания анализа. Если в анализируемых клетках исключается наследственная патология, то оставшиеся клетки размораживаются и для них создаются условия, оптимальные для нормального развития, после чего они имплантируются в матку в соответствующий период менструального цикла.
Преимущество этих методов - возможность прервать беременность при обнаружении у зародыша наследственной патологии.
Недостаток этих методов - низкий процент успешных имплантаций (всего 10-20%), а также возможные осложнения в ходе беременности после успешной имплантации зародыша.
С помощью данного метода, например, осуществима диагностика синдрома Марфана, основанная на ПЦР с обратной транскрипцией, позволяющей идентифицировать мутации в гене фибриллина.
Методы пренатальной диагностики
Неинвазивные методы
Неинвазивные методы ПД следующие:
• УЗИ - наиболее эффективный метод. Проводится в различные сроки беременности, в том числе на 18-22 нед - первое УЗИ, 25-29 нед - второе УЗИ, 32-36 нед - третье УЗИ. С помощью УЗИ выявляются: врожденные пороки сердца, дефекты невральной трубки, поликистоз почек, скелетные дисплазии, расщелина верхней губы, мягкого и/или твердого нёба, клеточная гигрома, менингоцеле, микроцефалия, полидактилия, пороки лица и наружных половых органов. УЗИ может проводиться в ранние сроки беременности (12-14 нед) с целью выявления дефектов невральной трубки.
• Электро(эхо)кардиография плода. Применяется в III триместре беременности для диагностики врожденных пороков сердца.
• Фетоскопия и фетоамниография. Применяются во II триместре беременности для биопсии клеток плаценты и клеток кожи плода (буллезный эпидермолиз).
Инвазивные методы
Инвазивные методы ПД основаны на двух подходах, с помощью которых осуществляются заборы клеток эмбриона и плода (под контролем УЗИ).
Первый подход - трансцервикальный (через влагалище и шейку матки).
Второй подход - трансабдоминальный (через переднюю брюшную стенку).
В ранние сроки беременности (8-12 нед) для лабораторного анализа используются клетки, выделенные из материала ворсин хориона (хорион-биопсия) или плаценты (плацентобиопсия). В поздние сроки беременности для лабораторного анализа используются клетки, полученные из амниотической (околоплодной) жидкости плода, или клетки, выделенные из пуповинной крови плода (см. «кордоцентез»).
Кратко рассмотрим основные инвазивные методы.
• Амниоцентез. Проводится на сроках беременности до 12 нед, а также на 16-18 нед. Позволяет анализировать в культуре клеток эмбриона или плода состояние кариотипа и молекулы ДНК; в амниотической жидкости плода определяется уровень альфафетопротеина (АФП), а сыворотке крови плода - уровень 17-оксипрогестерона.
• Биопсия хориона. Проводится на сроках 8-12 нед беременности. Анализируются нативные клетки и клетки в культурах тканей хориона. Исследуется все то же, что и при амниоцентезе, кроме
АФП.
• Кордоцентез. Проводится на 20-22 нед беременности путем анализа пуповинной крови плода, взятой из сосудов пуповины под контролем УЗИ.
И амниоцентез, и биопсия хориона применяются в развитых странах мира примерно при 10% всех беременностей. Эти методы связаны с наименьшим риском для эмбриона и плода. С их помощью диагностируются: синдромы Дауна, Патау и Эдвардса, трипло-Х, нарушения Y-хромосомы, а также более 100 МБ (болезнь Тея-Сакса, гипофосфатемия, лейциноз, метилмалоновая ацидемия, недостаточность аденозиндезаминазы, цитруллинемия и др.).
Окончательный диагноз наследственного и врожденного заболевания врач ставит при полном завершении клинического и параклинического этапов обследования пробанда.