Патофизиология: учебник / Литвицкий П.Ф. - 4-е изд., - 2009. - 496 с.
|
|
|
|
ГЛАВА 9. НАРУШЕНИЯ ОБМЕНА БЕЛКОВ И НУКЛЕИНОВЫХ КИСЛОТ
Белки и их комплексы выполняют в организме такие важные функции как информационная, рецепторная, каталитическая, структурная и некоторые другие. Нарушения обмена аминокислот и белка приводят к существенным расстройствам функций органов, их систем и организма в целом.
БАЛАНС АЗОТА
Азотистый баланс - суточная разница между поступающим и выделяемым азотом.
Виды азотистого баланса.
• Нулевой (количество поступающего и выводящегося азота совпадает).
• Положительный (количество поступающего в организм азота больше, чем выводящегося). Наблюдается как в норме (например, при регенерации тканей или беременности), так и в условиях патологии (например, при гиперпродукции СТГ или полицитемии).
• Отрицательный (количество поступающего в организм азота меньше, чем выводящегося). Наблюдается, например, при голодании, стрессе, тяжёлом течении СД, гиперкортицизме.
ОСТАТОЧНЫЙ АЗОТ
Интегративный параметр обмена белков и нуклеиновых кислот в организме - содержание небелкового (остаточного) азота крови (табл. 9-1). Аммиак обладает наиболее выраженными патогенными (цитотоксическими) свойствами из всех компонентов остаточного азота. Он беспрепятственно проникает через мембраны клеток, оказывая повреждающее действие на ферменты, компоненты цитозоля и мембран. В норме аммиак инактивируется внутриклеточно, вовлекаясь в реакции аминирования кетокислот с образованием нетоксических веществ. Мочевина сама по себе не обладает токсическим действием. Большая часть мочевины образуется в печени (в орнитиновом цикле, или цик-
Таблица 9-1. Содержание небелкового (остаточного) азота в крови (в ммоль/л)
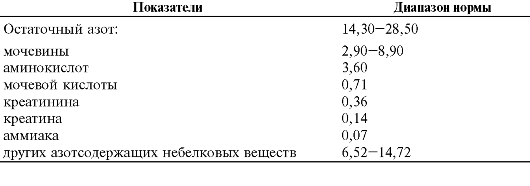 ле
мочевины) и выводится почками и потовыми железами. При почечной
недостаточности большое количество мочевины удаляется из организма через
кишечник, где она подвергается катаболизму кишечной флорой с
образованием внеклеточного аммиака. Креатин и креатинин. Уровни
креатина и креатинина в крови и моче, как правило, существенно меняются
при почечной недостаточности, гипотрофии мышц, миозитах и миастении,
длительном голодании, СД.
ле
мочевины) и выводится почками и потовыми железами. При почечной
недостаточности большое количество мочевины удаляется из организма через
кишечник, где она подвергается катаболизму кишечной флорой с
образованием внеклеточного аммиака. Креатин и креатинин. Уровни
креатина и креатинина в крови и моче, как правило, существенно меняются
при почечной недостаточности, гипотрофии мышц, миозитах и миастении,
длительном голодании, СД.
Мочевая кислота является финальным метаболитом обмена пуринов и образуется, главным образом, в гепатоцитах и энтероцитах с участием ксантиноксидазы, а разрушается в кишечнике при участии бактерий с образованием глиоксалевой кислоты и аммиака.
ТИПОВЫЕ НАРУШЕНИЯ БЕЛКОВОГО ОБМЕНА
К типовым нарушениям белкового обмена относят: несоответствие потребностям организма количества и аминокислотного состава поступающего белка, нарушение расщепления белка в ЖКТ, расстройства трансмембранного переноса аминокислот, дефекты метаболизма аминокислот, нарушения содержания белков в плазме крови, нарушения конечных этапов катаболизма белков, диспротеинозы.
Несоответствие потребностям организма количества и аминокислотного состава поступающего белка
Выделяют несколько видов несоответствия количества и состава белка потребностям организма: недостаток или избыток поступления белка в организм и нарушение аминокислотного состава потребляемого белка.
НЕДОСТАТОЧНОЕ ПОСТУПЛЕНИЕ БЕЛКА
Оптимальное количество белка, которое должно поступать в организм, колеблется в диапазоне 1,5-2,5 г на кг массы тела в сутки. Основная причина недостаточного поступления белка в организм - голодание. Выделяют несколько видов голодания.
• Абсолютное (прекращение поступления в организм пищи и воды).
• Полное (прекращение поступления в организм пищи, но не воды).
• Неполное (недостаточное количество принимаемой пищи, в том числе белка).
• Частичное (недостаток в пище отдельных её компонентов - белков, липидов, углеводов, химических элементов, витаминов).
Проявления белкового голодания
При белковом голодании могут развиваться такие заболевания, как квашиоркор и алиментарная дистрофия.
Квашиоркор - несбалансированная алиментарная белково-энергетическая недостаточность.
Вызывается рационом с недостаточным содержанием белка и незаменимых аминокислот, а также избытком калорийных небелковых продуктов (крахмала, сахара).
Алиментарная дистрофия (алиментарный маразм) - сбалансированная белково-калорическая недостаточность.
Полное или частичное белковое голодание приводит к мобилизации белка костей, мышц, кожи, в значительно меньшей мере - белка внутренних органов.
ИЗБЫТОЧНОЕ ПОСТУПЛЕНИЕ БЕЛКА
• Причины:
♦ Переедание.
♦ Несбалансированная диета (длительный приём пищи с высоким содержанием белка).
♦ Активация протеосинтеза (например, при гиперпродукции
СТГ).
• Проявления:
♦ Положительный азотистый баланс.
♦ Повышенное содержание белка в крови.
♦ Диспептические расстройства (поносы, запоры).
♦ Дисбактериоз кишечника с аутоинтоксикацией.
♦ Отвращение к пище, особенно богатой белком.
НАРУШЕНИЯ АМИНОКИСЛОТНОГО СОСТАВА ПОТРЕБЛЯЕМОГО БЕЛКА
В состав белков входят 22 аминокислоты, в том числе 8 незаменимых (валин, изолейцин, лейцин, лизин, метионин, треонин, триптофан, фенилаланин). Незаменимые аминокислоты не могут быть синтезированы в необходимом объёме в организме человека и должны поступать с пищей.
Дефицит незаменимых аминокислот
• Общие проявления характерны для недостатка любой незаменимой аминокислоты:
♦ Отрицательный азотистый баланс.
♦ Замедление роста и нарушения развития у детей.
♦ Снижение регенераторной активности тканей и органов.
♦ Уменьшение массы тела.
♦ Снижение аппетита и усвоения белка пищи.
• Специфические проявления характерны для дефицита конкретной незаменимой аминокислоты.
Избыток отдельных аминокислот
• Общие проявления. Избыточное поступление и образование аминокислот в организме приводит к нарушению вкуса, снижению аппетита, уменьшению массы тела, расстройствам обмена других аминокислот, нарушениям функций органов и тканей.
• Специфические проявления характерны для избытка конкретной аминокислоты.
Расстройства переваривания белка в желудке и кишечнике
Расстройства пищеварения в желудке и в тонком кишечнике приводят к нарушению обмена белка.
Нарушения расщепления белка в желудке
• Причины: гипоацидные состояния, снижение содержания или активности пепсина, резекция части желудка.
• Последствия и проявления: недостаточное расщепление белков, замедление эвакуации пищи в двенадцатиперстную кишку.
Нарушения переваривания белка в тонком кишечнике
• Причины: расстройство полостного и пристеночного расщепления белка в кишечнике, а также нарушение всасывания (синдромы мальабсорбции).
• Проявления:
♦ Креаторея.
♦ Целиакия глютеновая - синдром, характеризующийся нарушением полостного и мембранного переваривания белков, а также торможением всасывания аминокислот.
♦ Диспептические расстройства.
Нарушения трансмембранного переноса аминокислот
Нарушения трансмембранного переноса аминокислот обусловлены мембранопатиями различного генеза, которые приводят к расстройствам транспорта аминокислот на нескольких этапах: из кишечника в кровь, из крови в гепатоциты, из первичной мочи в кровь, из крови в клетки органов и тканей.
Примеры: синдром Фанкони, цистинурия, цистиноз нефропатический, отравления солями тяжёлых металлов (например, меди, кадмия, свинца, ртути), эндотоксинемии (например, при избытке соединений меди).
Расстройства метаболизма аминокислот
Различают первичные (наследственные, врождённые) и вторичные (приобретённые, симптоматические) расстройства метаболизма аминокислот.
Примеры первичных расстройств: фенилкетонурия, тирозинопатии (альбинизм, тирозинемии, тирозинозы), алкаптонурия, ацидемия изовалериановая, лейциноз, гомоцистеинурия.
Нарушение содержания белков в плазме крови
Уровень протеинемии является результатом соотношения процессов протеосинтеза и протеолиза в различных тканях и органах. В норме содержание белков в плазме крови составляет около 7% её массы. Белок крови представлен альбуминами (около 56%) и глобулинами (примерно 44%).
Диспротеинемии - типовые формы нарушения содержания белков в плазме крови.
Выделяют гиперпротеинемии, гипопротеинемии и парапротеинемии.
Гиперпротеинемии
Различают две разновидности увеличения общего содержания белков в плазме крови:
• Гиперсинтетическую (истинную, протеосинтетическую). Наблюдается гиперпродукция либо нормального белка (например, Ig),
либо парапротеинов (например, при плазмоцитомах, миеломной болезни);
• Гемоконцентрационную (ложную). Гипопротеинемия развивается в результате гемоконцентрации без усиления протеосинтеза (например, при ожоговой болезни, диарее, повторной рвоте, длительном усиленном потоотделении).
Гипопротеинемии
Известны два варианта уменьшения общей концентрации белков в плазме крови:
• Гипосинтетический (истинный). Этот вариант гипопротеинемии может быть двух видов.
♦ Первичной (наследственной или врождённой; например, гипопротеинемия при болезни Брутона).
♦ Вторичной (приобретённой, симптоматической; например, при печёночной недостаточности, белковом голодании, почечной недостаточности, ожоговой болезни).
• Гемодилюционный. Эта гипопротеинемия обусловлена гиперволемией (например, при гиперальдостеронизме или почечной недостаточности).
Парапротеинемии
Парапротеинемии наблюдают при:
♦ миеломной болезни: опухолевые плазмоциты продуцируют аномальные лёгкие или тяжёлые цепи молекул Ig;
♦ лимфомах (лимфоцитарных или плазмоцитарных). Лимфомы синтезируют аномальные IgM, обладающие повышенной агрегируемостью.
Расстройства финальных этапов катаболизма белка
Расстройства конечных стадий катаболизма белка характеризуются нарушением образования и дальнейших изменений мочевины, аммиака, креатинина, индикана, а также их выведения из организма.
Диспротеинозы
Диспротеинозы - патологические состояния, характеризующиеся изменением физико-химических свойств белков и расстройством их функций.
По преимущественной локализации патологического процесса различают клеточные и внеклеточные (амилоидоз, гиалиноз, мукоидное
и фибриноидное набухание) диспротеинозы. Подробно о диспротеинозах смотрите в разделе «Дистрофии» главы 4.
НАРУШЕНИЯ ОБМЕНА НУКЛЕИНОВЫХ КИСЛОТ
Нарушения обмена нуклеиновых кислот характеризуются расстройствами синтеза и деструкции пиримидиновых и пуриновых оснований.
• Пиримидиновые основания: урацил, тимин, цитозин, метил- и оксиметилцитозин.
• Пуриновые основания: аденин, гуанин, метиладенин, метилгуанин. Они являются составной частью макроэргических соединений - аденинди- и трифосфата, гуанинди- и трифосфата. Финальный метаболит обмена пуринов - мочевая кислота.
Расстройства метаболизма пиримидиновых оснований
К расстройствам, сопровождающимся нарушением метаболизма пиримидиновых оснований, относятся оротацидурия, гемолитическая анемия и аминоизобутиратурия вследствие недостаточности 3-гидрок- сиизобутират дегидрогеназы.
Нарушения обмена пуриновых оснований
К основным проявлениям, вызванным нарушениями обмена пуриновых оснований, относят подагру, гиперурикемию, синдром ЛешаНайена и гипоурикемию.
ГИПЕРУРИКЕМИЯ
Гиперурикемия - состояние, проявляющееся повышенной концентрацией мочевой кислоты в крови и, как следствие - в моче.
ПОДАГРА
Подагра - заболевание, характеризующееся хронической гиперурикемией, отложением уратов в органах и тканях, уратной нефропатией и уролитиазом.
Этиология
• Причины:
♦ Первичные. Представляют собой генетический дефект ферментов обмена мочевой кислоты.
♦ Вторичные. Наиболее часто это сахарный диабет, гиполипопротеинемии, артериальная гипертензия, ожирение.
• Факторы риска:
♦ Повышенное поступление в организм пуриновых оснований (например, при употреблении большого количества мяса, молока, икры, рыбы, кофе, какао, шоколада).
♦ Увеличение катаболизма пуриновых нуклеотидов (например, при противоопухолевой терапии; массивном апоптозе у пациентов с аутоиммунными болезнями).
♦ Торможение выведения мочевой кислоты с мочой (например, при почечной недостаточности).
♦ Повышенный синтез мочевой кислоты при одновременном снижении выведения её из организма (например, при злоупотреблении алкоголем, шоковых состояниях, гликогенозе с недостаточностью глюкозо-6-фосфатазы).
Патогенез подагры
Наиболее важными звеньями патогенеза подагры являются:
♦ активация системы комплемента с образованием факторов хемотаксиса C5a и C3a под влиянием избытка уратов в плазме крови и межклеточной жидкости;
♦ накопление лейкоцитов в местах отложения кристаллов мочевой кислоты: в коже, почках, хрящах, в околосуставных тканях под влиянием хемотаксических веществ;
♦ фагоцитоз кристаллов мочевой кислоты, который сопровождается высвобождением БАВ, инициирующих асептическое воспаление;
♦ повреждение клеток и неклеточных элементов медиаторами воспаления и непосредственно уратами, сопровождающееся образованием антигенных структур, что активирует реакции иммунной аутоагрессии;
♦ развитие (в зоне отложения уратов) хронического пролиферативного воспаления, образования подагрических гранулём и подагрических «шишек» - tophi urici, обычно вокруг составов.
Проявления подагры
• Постоянно повышенная концентрация мочевой кислоты в плазме крови и в моче.
• Воспаление суставов по типу моноартритов, что сопровождается сильной болью и лихорадкой.
• Уролитиаз и рецидивирующие пиелонефриты, завершающиеся нефросклерозом и почечной недостаточностью.
ГИПОУРИКЕМИЯ
Гипоурикемия - состояние, характеризующееся снижением концентрации мочевой кислоты в крови ниже нормы.
• Возможная причина: недостаточность ксантиноксидазы или сульфитоксидазы.
• Проявления
♦ Образование кристаллов ксантина в ткани почек, вокруг суставов и в мышцах.
♦ Мышечные судороги и нистагм (обусловлены миозитами, поражением центральных и периферических нейронов).