Патофизиология: учебник / Литвицкий П.Ф. - 4-е изд., - 2009. - 496 с.
|
|
|
|
ГЛАВА 17. ОПУХОЛЕВЫЙ РОСТ
Ежегодно на земном шаре новообразования выявляются примерно у 6 000 000 человек. Средние показатели заболеваемости в различных странах колеблются в диапазоне 190-300 случаев на 100 000 населения. Злокачественные опухоли зачастую становятся причинами смерти людей.
Опухолевый рост - типовая форма нарушения тканевого роста, возникающая под действием канцерогена. Характерезуется атипизмом роста, обмена веществ, структуры и функции.
Опухолевый рост проявляется патологическим разрастанием ткани с атипичными свойствами.
Согласно цитологической и гистологической структуре опухолевых клеток и тканей выделяют доброкачественные и злокачественные опухоли. Доброкачественные опухоли. Клетки их морфологически похожи на нормальные и формируют характерные для данной ткани, высокодифференцированные структуры. Такие опухоли растут медленно и, как правило, не метастазируют.
Злокачественные опухоли. Клетки их морфологически отличаются от нормальных и образуют низкодифференцированные тканевые структуры. Эти опухоли растут быстро, инвазируют в соседние ткани, формируют метастазы. Выделяют следующие разновидности злокачественных опухолей:
♦ Карциномы - злокачественные опухоли, происходящие из эпителия.
♦ Саркомы - злокачественные опухоли, возникающие из тканей мезенхимального происхождения (соединительных, костной, хрящевой).
Этиология
Инициальным звеном опухолевого роста является образование опухолевых клеток под воздействием канцерогенов.
Опухолевая трансформация - процесс превращения нормальных клеток в опухолевые вследствие трансформации нормальной генетической программы в программу формирования опухолевого атипизма.
ПРИЧИНЫ
Факторы химической, физической и биологической природы, способные вызвать опухолевую трансформацию, называют канцерогенами.
• Химические канцерогены. Более 75% случаев злокачественных опухолей человека вызвано воздействием химических факторов внешней среды. К возникновению опухолей приводят преимущественно продукты сгорания табака, некоторые компоненты пищи и промышленные соединения. Известно более 1500 химических соединений, обладающих канцерогенным эффектом. Из них не менее 20 опре- делённо являются причиной опухолей у человека. Например, к ним отнесены 2-нафтиламин, бензидин, 2-аминотиофенил, вызывающие рак мочевого пузыря у работников анилинокрасочной и резиновой промышленности; бис-(хлорметил)-эфир, приводящий к возникновению рака бронхов и лёгких.
• Физические канцерогены: ионизирующее излучение (α-, β- и γ-излучение), рентгеновские и ультрафиолетовые лучи, поток нейтронов. Так, врачи-рентгенологи заболевают лейкозами в 8-9 раз чаще, чем врачи других специальностей.
• Онкогенные вирусы.
♦ ДНК-вирусы, вызывающие опухолевую трансформацию, называют онковирусами. Гены ДНК-онковирусов способны непосредственно внедряться в геном клетки-мишени. Участок ДНК-вируса (собственно онкоген), интегрированный с клеточным геномом, может осуществить опухолевую трансформацию клетки. Не исключают также, что один из генов онковируса может играть роль промотора клеточного протоонкогена. К ДНК-содержащим онковирусам относят некоторые аденовирусы, паповавирусы и герпесвирусы (так, вирус Эпстайна-Барр вызывает развитие лимфом, а вирус гепатита B способен инициировать рак печени).
♦ РНК-содержащие вирусы, относящиеся к ретровирусам. Интеграция РНК-генов ретровирусов в клеточный геном происходит не непосредственно, а после образования их ДНК-копий.
УСЛОВИЯ, СПОСОБСТВУЮЩИЕ ВОЗНИКНОВЕНИЮ ОПУХОЛЕЙ (ФАКТОРЫ РИСКА)
Наследственные факторы. Существует не менее 300 так называемых семейных форм злокачественных опухолевых заболеваний. В ряде
случаев генетическая природа предрасположенности к возникновению опухолей определена. К числу наиболее значимых относятся следующие:
• Аномалии генов, контролирующих процесс репарации ДНК. Это определяет повышенную чувствительность к канцерогенным воздействиям.
• Аномалии генов-супрессоров опухолевого роста. Выявлены при новообразованиях толстой кишки и поджелудочной железы (делеция 18q21.1), множественном канцероматозе (потеря гетерозиготности в 10q23).
• Аномалии генов синтеза молекул межклеточного взаимодействия, например, E-кадгерина (расположенного в 16q22.1). Уменьшение экспрессии E-кадгерина - один из молекулярных механизмов, способствующих инвазии и метастазированию опухоли.
• Другие генные и хромосомные дефекты: мутации гена рецептора андрогенов (расположенного в хромосоме X) вызывают рак молочной железы у мужчин; различные хромосомные дефекты зарегистрированы при лейкозах; аномалии хромосом 8 и 9 выявляются при наследственных формах меланом кожи.
Низкая активность механизмов противоопухолевой защиты организма (см. ниже).
Патогенез
Клетка под воздействием канцерогена претерпевает ряд последовательных изменений, которые приводят к опухолевому росту. Механизм развития опухолевого роста называют канцерогенезом.
ОБЩИЕ ЭТАПЫ КАНЦЕРОГЕНЕЗА
Вне зависимости от конкретной причины опухолевой трансформации клетки, гистологической структуры и локализации новообразования, в процессе канцерогенеза можно выделить несколько общих этапов
(рис. 17-1).
• На первом этапе происходит взаимодействие канцерогенов химической, физической или биологической природы с протоонкогенами и антионкогенами (онкосупрессорами) генома нормальной клетки.
• На втором этапе канцерогенеза (в результате воздействия канцерогена на геном) подавляется активность антионкогенов и происходит трансформация протоонкогенов в онкогены. Последующая экспрессия онкогена - необходимое и достаточное условие для опухолевой трансформации.
• На третьем этапе канцерогенеза, в связи с экспрессией онкогенов, синтезируются и реализуют свои эффекты (непосредственно или
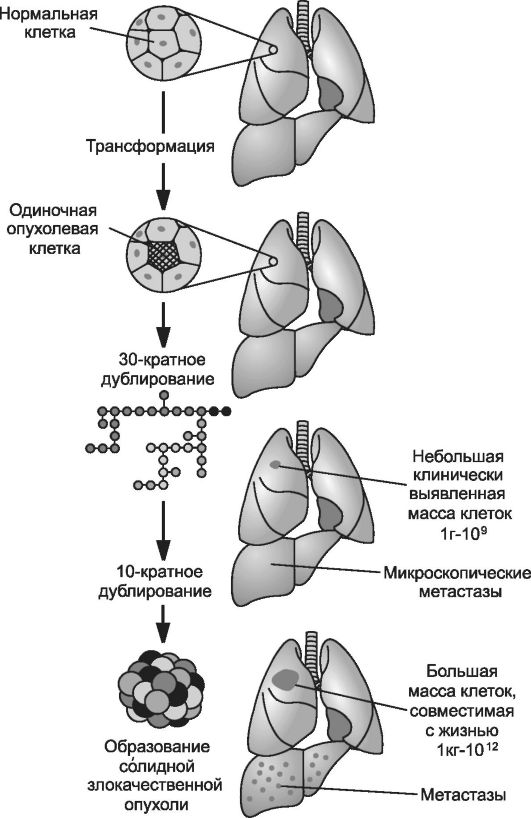 Рис. 17-1. Этапы опухолевого роста. [по 4].
Рис. 17-1. Этапы опухолевого роста. [по 4].
с участием клеточных факторов роста и рецепторов к ним) онкобелки. С этого момента генотипически изменённая клетка приобретает опухолевый фенотип.
• Четвёртый этап канцерогенеза характеризуется пролиферацией и увеличением числа опухолевых клеток, что ведёт к формированию новообразования (опухолевого узла).
ОСОБЕННОСТИ ЭТАПОВ ХИМИЧЕСКОГО,
ФИЗИЧЕСКОГО И ВИРУСНОГО КАНЦЕРОГЕНЕЗА Этапы химического канцерогенеза
Сами по себе потенциально канцерогенные вещества не вызывают опухолевого роста. В связи с этим их называют проканцерогенами, или преканцерогенами. В организме они подвергаются физико-химическим превращениям, в результате которых становятся истинными, конечными канцерогенами. Считают, что конечными канцерогенами являются алкилирующие соединения, эпоксиды, диолэпоксиды, свободнорадикальные формы ряда веществ.
Выделяют два взаимосвязанных этапа химического канцерогенеза: инициации и промоции.
• На этапе инициации конечный канцероген взаимодействует с генами, контролирующими деление и созревание клетки (протоонкогенами). При этом происходит либо мутация протоонкогена (геномный механизм изменения генетической программы), либо его регуляторная дерепрессия (эпигеномный механизм). Протоонкоген превращается в онкоген. Это и обеспечивает опухолевую трансформацию клетки. И хотя такая клетка ещё не имеет опухолевого фенотипа (её называют «латентной» опухолевой клеткой), процесс инициации уже необратим. Инициированная клетка становится иммортализованной (бессмертной, от англ. immortality - вечность, бессмертие). Она лишается так называемого лимита Хайфлика: строго ограниченного числа делений (в культуре клеток млекопитающих обычно около 50).
• На этапе промоции осуществляется экспрессия онкогена, происходит неограниченная пролиферация клетки, ставшей генотипически и фенотипически опухолевой, формируется новообразование.
Этапы физического канцерогенеза
Мишенью канцерогенных агентов физической природы также является ДНК. Допускается либо их прямое действие на геном, либо через посредники - медиаторы канцерогенеза. К последним относят свободные радикалы кислорода, липидов и других органических и неорганических веществ.
• Этап инициации заключается в прямом или опосредованном воздействии агентов физической природы на ДНК. Это вызывает либо повреждение её структуры (генные мутации, хромосомные аберрации), либо эпигеномные изменения. Как первое, так и второе может привести к активации протоонкогенов и последующей опухолевой трансформации клетки.
• На этапе промоции канцерогенеза осуществляется экспрессия онкогена и формирование фенотипа опухолевой клетки. В результате последовательных циклов пролиферации формируется опухоль.
Этапы вирусного канцерогенеза включают пять последовательных событий: проникновение онкогенного вируса в клетку, включение вирусного онкогена в геном клетки, экспрессию онкогена, превращение клетки в опухолевую, образование опухолевого узла.
АТИПИЗМ ОПУХОЛЕВЫХ КЛЕТОК
Опухолевый атипизм - качественное и количественное отличие свойств опухоли от нормальной (аутологичной) ткани (из которой произошло новообразование), а также от других патологически измененных тканей (например, гипертрофированных, атрофированных, рубцовой).
Опухолевый атипизм проявляется большим числом аномальных признаков, характеризующих рост, метаболизм, структуру и функции новообразованных клеток и опухолевой ткани в целом.
Атипизм роста
Атипизм клеточного роста характеризуется несколькими признаками.
• Атипизм деления. В опухоли значительно увеличено количество делящихся клеток. Если в большинстве обновляющихся нормальных тканей число пролиферирующих клеток не превышает 5%, то во многих новообразованиях оно составляет 40-60%, а в некоторых - до 100%. Увеличение числа делящихся клеток ведёт к быстрому нарастанию массы опухоли.
• Атипизм созревания. Заключается в частичном или полном подавлении процесса созревания (дифференцировки) опухолевых клеток.
• Инвазивный рост. Характеризуется проникновением клеток опухоли в окружающие нормальные ткани, что сопровождается деструкцией этой ткани. Причины инвазивного роста:
♦ уменьшение (в 3-6 раз по сравнению с нормальной тканью) сил сцепления (адгезии) между клетками опухоли, и отделение в связи с этим клеток от опухолевого узла;
♦ увеличение отрицательного заряда внешней поверхности опухолевых клеток в связи с фиксацией на ней отрицательно заряженных радикалов и уменьшением содержания катионов (Ca2+, Na+ и др.); это способствует электростатическому отталкиванию их друг от друга и отдалению от опухолевого узла;
♦ появление у опухолевых клеток способности к амебоидному движению;
♦ синтез клетками опухоли большого количества рецепторов к лигандам молекул адгезии, в том числе - к межклеточному фибронектину, ламинину базальных мембран и внеклеточного матрикса, коллагену, витронектину. Это способствует прикреплению клеток новообразования к неклеточным структурам и перемещению по их поверхности.
Указанные выше процессы обеспечивают как инвазивный рост опухоли, так и метастазирование её клеток (см. ниже).
Метаболический атипизм
Атипизм обмена веществ (метаболический, или биохимический атипизм) заключается в существенном изменении всех видов обмена: нуклеиновых кислот, белков, углеводов, липидов, ионов, жидкости, витаминов. В связи с этим закономерно изменяются и физико-химические параметры опухолевых клеток и новообразования в целом.
• Атипизм обмена нуклеиновых кислот проявляется увеличением синтеза ДНК и РНК в клетках опухоли. Причина: экспрессия онкогенов, а также некоторых других генов опухолевой клетки.
• Атипизм белкового обмена проявляется усилением включения аминокислот в реакции протеосинтеза (феномен «опухоль - ловушка азота»), интенсификацией синтеза различных классов белков (структурных, ферментов, онкобелков и других) при одновременном уменьшении или прекращении синтеза ряда иных белков (например, гистонов), изменением антигенного профиля опухолей. Изменения метаболизма нуклеиновых кислот и белка в новообразованиях обеспечивают, с одной стороны, реализацию большинства других проявлений их атипизма, а с другой - способствуют активации механизмов антибластомной защиты организма, обусловленной появлением у клеток опухоли Аг, не свойственных нормальным аутологичным клеткам.
• Атипизм обмена углеводов проявляется активацией реакций транспорта и утилизации опухолевыми клетками глюкозы - феномен «опухоль - ловушка углеводов», уменьшением относительной доли тканевого дыхания при ресинтезе АТФ, интенсификацией процесса прямого окисления углеводов в пентозофосфатном цикле.
♦ Причины: увеличение содержания или активности ферментов гликолиза в цитозоле, повышение эффективности механизмов транспорта глюкозы в клетки.
♦ Последствия: обеспечение энергией значительно интенсифицированных пластических процессов, существенное повышение устойчивости клеток новообразования к гипоксии и гипогликемии, а, следовательно, - увеличение их выживаемости.
• Атипизм обмена липидов проявляется значительным усилением утилизации ВЖК и холестерина (опухоль как «ловушка липидов»), активацией синтеза липидных структур клеток, интенсификацией процессов липопероксидации.
♦ Причины: повышение в опухолевых клетках активности или содержания ферментов метаболизма липидов, подавление или истощение в опухолях факторов антиоксидантной защиты.
♦ Значение: энергетическое и пластическое обеспечение усиленных анаболических процессов, реакций синтеза структур интенсивно делящихся опухолевых клеток.
• Атипизм обмена ионов и жидкости проявляется накоплением воды и ряда ионов, а также изменением соотношения отдельных ионов как в цитозоле опухолевых клеток, так и в межклеточной жидкости. В большинстве опухолей увеличивается [K+] и [Cu2+]. Наряду с этим отмечается уменьшение уровня кальция, а в некоторых бластомах - натрия, магния, цинка и других.
♦ Причины: дефекты клеточных мембран, изменение активности или содержания ферментов транспорта ионов (например, снижение активности Na+,К+-АТФазы, Са2+-АТФазы и др.), повышение осмотического давления в опухолевых клетках, разрушение клеток.
♦ Значение: изменения обмена ионов и воды в новообразованиях способствуют реализации других видов атипизма: роста, функции и структуры.
• Атипизм обмена витаминов проявляется интенсивным захватом опухолевыми клетками различных витаминов. Показано, что различные опухоли являются «ловушкой» витамина E, обладающего антиоксидантной активностью. По-видимому, это является одним из механизмов повышения устойчивости опухолевых клеток к цитотоксическим воздействиям свободных радикалов.
Для новообразований характерны общие проявления атипизма обмена веществ.
♦ Активное включение в метаболизм опухолей аминокислот, липидов, углеводов, ионов и других веществ (опухоль как «метаболическая ловушка»).
♦ Преобладание в новообразовании анаболических реакций над катаболическими.
♦ Утрата специализации клеток новообразования по сравнению с нормальными - дифференцированными. Это связано с пре-
кращением (или нарушением) синтеза в опухолевых клетках ряда важных для нормального метаболизма ферментов (например, глицерофосфатдегидрогеназы, что ведёт к доминированию гликолитического ресинтеза АТФ).
♦ Снижение эффективности местной регуляции обмена веществ на основе механизма обратной связи.
♦ «Ускользание» метаболизма новообразований от системных (нейрогенных и гормональных) регуляторных влияний. Это вызвано существенными изменениями рецепторного и пострецепторного аппарата регуляции обмена в опухолевых клетках.
♦ Переход опухолевых клеток на более простые варианты регуляции: аутокринный (внутриклеточное управление метаболическими реакциями с помощью веществ, образуемых самой клеткой) и паракринный (управление с помощью веществ - цитокинов, образуемых соседними клетками) механизмов.
В целом указанные и другие проявления атипизма обмена веществ в опухоли создают условия для существенного повышения её «конкурентоспособности» и выживаемости в организме.
Атипизм функций
Обычно функции клеток новообразования снижены или качественно изменены, реже - повышены.
• Гипофункция. Как правило, отдельные опухолевые клетки и новообразование в целом характеризуются пониженным функционированием.
• Гиперфункция. Нередко наблюдают признаки гиперфункции как отдельных раковых клеток, так и опухоли в целом. Обычно речь идет о неадекватной потребностям организма продукции каких-либо веществ. Так, некоторые гормональноактивные новообразования желёз внутренней секреции в избытке синтезируют гормоны (например, феохромоцитомы, инсулома и др.).
• Дисфункция. В некоторых опухолях выявляются признаки, не свойственные для нормальных аутологичных тканей. Например, низкодифференцированные клетки карциномы желудка иногда начинают продуцировать коллаген, рака лёгкого - гормоны аденогипофиза или биогенные амины. Причина этого феномена: экспрессия в опухолевых клетках соответствующих генов, которые неактивны в исходных клетках аутологичных тканей.
В целом, атипизм функции опухолей обусловливает нарушение деятельности тканей и органов, которые они поражают, а также - расстройство жизнедеятельности организма-опухоленосителя.
МЕТАСТАЗИРОВАНИЕ
Метастазирование - перенос клеток бластомы на расстояние от основного (материнского) узла, и развитие опухоли того же гистологического строения в другой ткани или органе.
Это одно из фатальных проявлений атипизма опухолевого роста.
Пути метастазирования
♦ Лимфогенный (с током лимфы по лимфатическим сосудам) - наиболее частый путь метастазирования опухолей, особенно карцином.
♦ Гематогенный (с током крови по кровеносным сосудам) путь наиболее характерен для сарком.
♦ Тканевой или имплантационный. Метастазирование осуществляется при соприкосновении опухолевой клетки с поверхностью нормальной ткани или органа (например, при контакте опухоли желудка с поверхностью брюшины или рака лёгкого с плеврой); при имплантации бластомных клеток, находящихся в жидкостях организма, например, брюшной, плевральной полости, в ликворе, на поверхность органов, соответственно брюшной и грудной полости, спинного и головного мозга.
Нередко опухоли метастазируют по нескольким путям одновременно или последовательно.
Этапы метастазирования
Основными этапами метастазирования являются:
• Отделение злокачественной клетки от опухоли и её инвазия в стенку лимфатического или кровеносного сосуда (интравазация/
• Эмболия - циркуляция в лимфатических и кровеносных сосудах опухолевой клетки с последующей её имплантацией на внутренней поверхности эндотелия стенки сосуда.
• Инвазия клетки бластомы в стенку сосуда и далее - в окружающую их ткань (экстравазация). В последующем клетки пролиферируют и формируют ещё один опухолевый узел - метастаз.
Метастазы нередко характеризуются органной избирательностью (тропностью). Так, клетки рака лёгкого чаще метастазируют в кости, печень, головной мозг; рака желудка - в яичники, ткани дна таза; рака молочной железы - в кости, лёгкие, печень. В основном, тропность метастазирования определяют: специфика обмена веществ в органе, особенности лимфо- и кровообращения, низкая эффективность механизмов антибластомной резистентности, положительный хемотаксис.
РЕЦИДИВИРОВАНИЕ
Рецидивирование - повторное развитие новообразования того же гистологического строения на прежнем месте после его удаления или деструкции.
Причины: опухолевые клетки, оставшиеся в ткани при неполном удалении новообразования (как правило, в связи с предшествующей удалению опухоли инвазией отдельных клеток бластомы в окружающую ткань). Допускается также возможность внедрения в геном нормальной клетки участка ДНК из разрушившихся при хирургическом удалении или хемо- и лучевой терапии опухолевых клеток. Повторное развитие опухоли нередко характеризуется ускоренным её ростом. Это является результатом, с одной стороны, повреждения местных тканей в ходе хирургического или иного вмешательства, а с другой - снижения эффективности факторов системы ИБН.
ОПУХОЛЕВАЯ ПРОГРЕССИЯ
Изменения в геноме, приводящие к трансформации нормальной клетки в опухолевую - лишь первый этап на пути дальнейшей модификации генома. В генетической программе клетки, ставшей опухолевой, постоянно происходят изменения, в основе которых лежат мутации.
• Фенотипически это проявляется изменением биохимических, морфологических, электрофизиологических и функциональных признаков опухоли.
• Изменения различных свойств опухолевых клеток происходят независимо друг от друга, поскольку мутации каждого отдельного гена автономны.
• Сроки изменений свойств разных опухолевых клеток сильно варьируют. В связи с этим признаки их появляются и изменяются без какой-либо закономерной хронологии.
• При опухолевой прогрессии формируются клоны клеток с самой различной комбинацией признаков (феномен клональной селекции бластомы). В связи с этим разные субклоны клеток одного новообразования могут весьма существенно отличаться друг от друга.
• Модификации в геноме опухолевой клетки наследуются, т.е. передаются дочерним клеткам.
Указанные выше отклонения генотипа и фенотипа клеток больше характерны для бластом. Они были описаны американским патологом Л. Фулдсом (1969 г.) и названы им феноменом опухолевой прогрессии.
Опухолевая прогрессия - генетически закреплённое, наследуемое опухолевой клеткой и необратимое изменение одного или нескольких её свойств.
Высокая и постоянная изменчивость разных свойств опухолей, с одной стороны, делает их гетерогенными, а с другой - способствует их адаптации к меняющимся условиям: недостатку кислорода, субстратов обмена веществ, а в ряде случаев - к ЛС.
Стадии опухолевого роста
Определение стадии новообразования базируется на оценке его размера и наличии либо отсутствии метастазов. Значение определения стадии опухолевого роста
• Оценка прогноза. Стадия опухоли имеет важное значение при оценке прогноза. Все классификации опухолей указывают на благоприятный прогноз в 1-й стадии заболевания. В последующих стадиях прогноз прогрессирующе ухудшается.
• Выбор оптимального лечения. Определение стадии болезни играет решающую роль в последовательности местного, регионарного и системного подходов к лечению, а также при составлении плана комбинированной терапии.
• Классификация. Существует несколько классификаций опухолей.
Классификация TNM
Классификация TNM используется наиболее широко и включает такие классифицирующие критерии:
♦ T (Tumor - опухоль) отражает размер и величину новообразования;
♦ N (Node - узел лимфатический) описывает степень вовлечения в опухолевый процесс лимфатических узлов;
♦ M (Metastasis - метастазы) указывает на наличие и размер от- далённых метастазов.
Взаимодействие опухоли и организма
Результат взаимодействия опухоли и организма может быть различным.
• Гибель бластомных клеток. В организме среди большого числа постоянно образующихся различных клеток-мутантов имеются и опухолевые. Однако они, как правило, сразу же обнаруживаются и уничтожаются при участии факторов системы ИБН.
• Латентное, «дремлющее» состояние опухолевых клеток. Как правило, при этом не наблюдается признаков инвазии клеток бластомы в окружающую нормальную ткань. Такую форму опухолевого роста обозначают как неинвазивную, или «рак на месте» - cancer in situ. Подобное состояние может наблюдаться в течение ряда лет. Оно
может завершиться либо гибелью клеток бластомы (при активации факторов системы ИБН), либо интенсификацией её роста - приобретением способности к инвазии в окружающие ткани, метастазированию и других (при снижении эффективности факторов системы ИБН).
• Прогрессирующее формирование новообразования с нарастанием степени его атипизма. При этом можно выделить местное и общее воздействие опухоли на организм.
❖ Местные эффекты новообразования характеризуются:
❖ нарушением функции поражённых опухолью тканей и органов;
❖ сдавлением окружающих тканей и органов, инвазивным ростом в них и их деструкцией;
❖ расстройством микрогемо- и лимфоциркуляции;
❖ образованием и выделением в межклеточную жидкость метаболитов, в том числе обладающих свойствами БАВ (гормонов, факторов роста, ферментов, иммунодепрессантов и др.), способных вызвать дисфункцию органов;
❖ подавлением активности местных факторов системы ИБН - фагоцитирующих клеток, лимфоцитов, лизоцима, ИФН и других, что способствует прогрессии опухолевого роста.
❖ Системное влияние новообразований проявляется развитием ряда общих неспецифических синдромов. Их называют паранеопластическими.
ПАРАНЕОПЛАСТИЧЕСКИЕ СИНДРОМЫ
К наиболее клинически значимым паранеопластическим синдромам относятся иммунопатологические состояния и кахексия. Также у больных могут выявляться психоневрологические, эндокринопатические и тромбогеморрагические синдромы, анемии и другие. Подробное описание этих паранеопластических синдромов приводится в соответствующих разделах учебника.
Кахексия у онкологических больных обусловлена совокупностью следующих факторов:
❖ поглощением клетками новообразований субстратов метаболизма;
❖ интоксикацией организма продуктами распада опухоли и окружающих её тканей;
❖ избыточным образованием макрофагами и моноцитами организма ФНОа (кахектина);
❖ снижением аппетита, что связывают с опухолевой интоксикацией и развитием у пациентов депрессии;
❖ болевым синдромом (при распаде опухоли, сдавлении ею окружающих тканей или прорастании в них);
♦ кровотечением из распадающейся ткани новообразования или аррозированных стенок сосудов при инфильтрации их опухолью.
Иммунопатологические состояния. У онкологических больных часто наблюдаются различные инфекции вследствие развития у них при- обретённого иммунодефицита. Описаны и другие иммунопатологические состояния, сопровождающие опухолевый рост: аллергические реакции, болезни иммунной аутоагрессии, патологическая толерантность. Причины:
♦ Антигенная перегрузка иммунной системы различными белками, образующимися при распаде опухолей.
♦ Иммуносупрессивное действие избытка глюкокортикоидов, обнаруженного при росте опухолей (что связывают с развитием стрессорного состояния).
♦ Повышение активности T-супрессоров при росте некоторых опухолей (например, гепатом).
♦ Дефицит субстратов, необходимых для пролиферации и дифференцировки иммуноцитов.
Противоопухолевая защита организма
Антибластомная резистентность - свойство организма препятствовать проникновению канцерогенных агентов в клетку, её ядро, а также их действию на геном; обнаруживать и устранять онкогены или подавлять их экспрессию; обнаруживать и разрушать опухолевые клетки, тормозить их рост.
Выделяют антиканцерогенные, антимутационные и антицеллюлярные механизмы противоопухолевой защиты.
АНТИКАНЦЕРОГЕННЫЕ МЕХАНИЗМЫ
Антиканцерогенные механизмы обеспечивают торможение или блокаду проникновения канцерогенов в клетку, её ядро, действие их на геном, а также инактивацию или элиминацию бластомогенных агентов из клетки и организма.
• Механизмы, препятствующие действию химических канцерогенных факторов:
♦ Физико-химическая фиксация (например, глюкуронизация, сульфатирование и удаление из организма с мочой, экскрементами, слюной, жёлчью, потом).
♦ Фагоцитоз канцерогенов, сочетающийся с их инактивацией и разрушением.
♦ Инактивация бластомогенных агентов при помощи АТ и Т-лимфоцитов.
♦ Конкурентная блокада неканцерогенными метаболитами клеточных рецепторов, с которыми способны взаимодействовать истинные бластомогенные вещества.
♦ Разрушение или инактивация канцерогенов в клетках и биологических жидкостях в процессе их метаболизма.
♦ Ингибирование свободных радикалов и гидроперекисей органических и неорганических соединений факторами антиоксидантной защиты.
• Механизмы, препятствующие действию онкогенных вирусов:
♦ Инактивация вирусов или разрушение вируссодержащих клеток иммуноглобулинами.
♦ Ингибирование ИФН - белками, тормозящими или блокирующими процесс внутриклеточной репликации вирусов.
♦ Обнаружение и разрушение вируссодержащих клеток организма естественными киллерами, цитотоксическими Т-лимфоцитами, мононуклеарными фагоцитами.
• Механизмы, препятствующие действию канцерогенов физической природы:
♦ Улавливание и инактивация свободных радикалов кислорода, липидов, других органических и неорганических веществ.
АНТИМУТАЦИОННЫЕ МЕХАНИЗМЫ
Антимутационные механизмы обеспечивают обнаружение, устранение или подавление активности онкогенов. Реализуются антимутационные механизмы при участии онкосупрессоров и систем репарации
ДНК.
АНТИЦЕЛЛЮЛЯРНЫЕ МЕХАНИЗМЫ
Антицеллюлярные механизмы обеспечивают обнаружение и разрушение генотипически и фенотипически чужеродных для организма опухолевых клеток или блокаду их роста.
Различают неиммунные (неспецифические) и иммунные (специфические) антицеллюлярные механизмы.
Неиммунные механизмы
Эти механизмы осуществляют надзор за сохранением индивидуального однородного клеточного состава организма. Реализуют эти механизмы киллерные клетки и гуморальные факторы.
• Киллерные клетки: фагоциты, естественные киллеры, цитотоксические Т-лимфоциты.
• Гуморальные факторы:
♦ ФНОа увеличивает образование активных форм кислорода и цитокинов с канцеролитическим эффектом (например, ИЛ и ИФН)
фагоцитами в ткани новообразования, активирует программы апоптоза, стимулирует тромбообразование в микрососудах опухоли и развитие ишемии в ней.
♦ Вещества со свойствами аллогенного торможения и деструкции генетически чужеродных клеток: специфические для каждого типа клеток метаболиты, а также некоторые цитокины.
♦ Факторы контактного торможения, подавляющие перемещение и пролиферацию опухолевых клеток (например, а-ЛП плазмы крови и других биологических жидкостей).
Иммунные механизмы
Иммунные механизмы реализуются через клеточные и гуморальные реакции иммунитета.
• Цитотоксические T-лимфоциты, стимулированные опухолевыми Аг, оказывают цитолитический эффект двояко:
♦ при непосредственном контакте с опухолевой клеткой;
♦ опосредованно (дистантно), путём выделения в биологические жидкости организма различных цитотоксических агентов.
• Специфические АТ, вырабатываемые плазмоцитами, действуют, в основном, на отдельные бластомные клетки (например, лейкозные). Клетки, находящиеся в составе опухолевого узла, мало доступны для Ig.
Принципы профилактики и терапии опухолей ПРОФИЛАКТИКА
Цель профилактики новообразований: предупредить или снизить действие на клеточный геном канцерогенов, и предотвратить тем самым возникновение опухолевой клетки.
Для достижения этой цели проводят различные мероприятия:
♦ Снижают содержание или устраняют в окружающей человека среде канцерогенные агенты.
♦ Обеспечивают индивидуальную защиту организма (например, с помощью специальной одежды).
♦ Повышают общую и противоопухолевую устойчивость организма путём реализации здорового образа жизни.
♦ Своевременно обнаруживают и ликвидируют так называемые предопухолевые состояния (например, очаги избыточной клеточной пролиферации).
ПРИНЦИПЫ ЛЕЧЕНИЯ ОПУХОЛЕЙ
• Дифференцированность. Лечение опухолей может быть радикальным и паллиативным.
♦ Радикальное лечение направлено на ликвидацию опухоли и предполагает возможность полного выздоровления либо длительной ремиссии.
♦ Паллиативное лечение применяют при невозможности проведения радикальной терапии (например, на поздних стадиях развития опухоли).
• Комплексность. Врачебные мероприятия должны включать хирургический, лучевой, химиотерапевтический методы терапии и, в некоторых случаях - использование модификаторов биологического ответа (например, иммуномодуляторов).
• Индивидуальность. Лечение планируют с учётом специфики этиологии и патогенеза опухолевого процесса у конкретного больного. Выбор метода лечения зависит от характера заболевания, стадии, гистологического типа опухоли, возраста больного, наличия сопутствующих заболеваний и цели лечения (радикальное или паллиативное вмешательство).