Неврология и нейрохирургия / под ред. А.Н. Коновало- ва, А.В. Коз лова ; Е.И. Гусев, А.Н. Коновалов, В.И. Скворцова : учебник : в 2 т. - т. 2. 2009. - 420 с.
|
|
|
|
ГЛАВА 7. ИНФЕКЦИОННЫЕ ЗАБОЛЕВАНИЯ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ
Инфекционные заболевания ЦНС в основном являются предметом неврологии, поскольку чаще не требуют хирургического вмешательства. Исключение составляют раневые (включая ятрогенные) инфекции, остеомиелит костей черепа или позвоночника и внутричерепные и спинальные абсцессы.
Посттравматический менингит
Посттравматический менингит развивается примерно у 10% пострадавших с проникающей ЧМТ, чаще всего (в 75% случаев) - при переломах основания черепа. Следует иметь в виду, что примерно в 15% случаев перелом основания черепа, приведший к менингиту, не сопровождается явной назальной или ушной ликвореей. При огнестрельных и минно-взрывных ранениях частота внутричерепных инфекционных осложнений превышает 20%, причем менингит часто сочетается с энцефалитом и абсцессами мозга.
Менингит развивается обычно в течение первых 2 нед после ЧМТ. Клинические проявления типичны для любого инфекционного менингита (головная боль, светобоязнь, симптомы Брудзинского и Кернига, лихорадка). Оптимальньгй метод диагностики - люмбальная пункция с определением числа и характера клеточных элементов в ликворе. Напомним, что нормальным является содержание 4 клеточных элементов в 1 мкл люмбального ликвора, или 12 в 3 мкл (обозначается как 12/3). При травматическом менингите содержание клеточных элементов - «цитоз» - в люмбальном ликворе может достигать сотен и тысяч в 1 мкл, и практически 100% этих клеточных элементов являются нейтрофильными лейкоцитами. Если при тяжелой ЧМТ люмбальная пункция времен-
но противопоказана (поскольку при наличии отека мозга может усугубить его дислокацию), диагноз подтверждается косвенными методами (лейкоцитоз со сдвигом формулы влево в периферической крови, повышение уровня С-реактивного белка и т.д.); при сохраняющихся сомнениях производят вентрикулярную пункцию. Наиболее типичными возбудителями являются:
• при проникающих повреждениях свода черепа - кожная флора, чаще - стафилококки;
• при переломах основания черепа - микрофлора полости носа: грамположительные (пневмококки, стафилококки - Staphylococcus epidermidis, S. haemolyticus, и Streptococcus pneumoniae) и грамотрицательные микроорганизмы (Escherichia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa, Acinetobacter spp.);
• при минно-взрывных ранениях возможно сочетание с анаэробами.
Лечение. Основным в лечении посттравматического менингита является закрытие «входных ворот» инфекции, без чего терапия не может быть эффективной. С этой целью выполняют различные хирургические вмешательства, направленные на восстановление герметичности краниоспинального пространства (герметичное ушивание раны с восстановлением целостности ТМО, закрытие ликворной фистулы на основании черепа прямым или эндоназальным эндоскопическим методом либо, при небольших фистулах, - за счет снижения внутричерепного давления путем повторных люмбальных пункций или установки наружного люмбального дренажа).
Антибактериальная терапия проводится эмпирически до выделения возбудителя и определения его антибиотикочувствительности; после получения результатов бактериологического анализа схема лечения меняется в соответствии с данными антибиотикограммы выделенного патогена.
При менингите, развившемся после проникающего повреждения свода черепа, в качестве эмпирической терапии обычно назначают цефалоспорины 3-4-го поколений (цефтриаксон, цефтазидим, цефепим). Если менингит развился вследствие перелома основания черепа, назначают цефалоспорины 3-го поколения (цефтриаксон, цефотаксим).
В случае непереносимости пенициллинов и цефалоспоринов альтернативой является хлорамфеникол (левомицетин) - 12,5 мг на 1 кг массы тела 2 раза в сутки внутривенно.
При менингите, развившемся после огнестрельных и минновзрывных ранений, целесообразно сразу назначать «препарат резерва» - меропенем (взрослым - 2,0 г внутривенно 3 раза в сутки) в сочетании с ванкомицином (взрослым - по 1,0 г внутривенно очень медленно 2-3 раза в сутки).
Антибактериальная терапия должна продолжаться не менее 10 сут (лучше - 14-21 сут) после полного регресса менингеального синдрома (при условии закрытия «входных ворот» инфекции).
У пострадавших с иммунодефицитом (в первую очередь - с синдромом приобретенного иммунодефицита [СПИД]) наиболее вероятным возбудителем менингита является Cryptococcus neoformans, поэтому в комплексном лечении (либо, при убежденности в криптококковой природе менингита, в режиме монотерапии) используют внутривенно амфотерицин B по 1 мг на 1 кг массы тела в сутки до регресса менингеального синдрома, после чего амфотерицин заменяют флуконазолом по 800 мг внутривенно или внутрь однократно, затем - по 400 мг/сут внутрь до 10 нед.
Остеомиелит костей черепа
Заболевание сегодня встречается редко, поскольку череп в связи с интенсивным кровоснабжением высокорезистентен к инфекции. Основная причина остеомиелита черепа - инфекционные очаги в околоносовых придаточных пазухах либо возникающие вследствие открытой ЧМТ, а также ятрогенные факторы - инфицирование при трепанации черепа, наложении скелетного вытяжения за теменные бугры и т.д. Основными возбудителями являются стафилококки, чаще - S. aureus или S. epidermidis.
Клинически остеомиелит костей черепа проявляется локальной болезненностью, отечностью, гиперемией кожи, вскоре обычно формируются незаживающие гнойные свищи. Пальпаторно и на рентгенограммах может определяться дефект кости с неровными, узурированными краями. Иногда остеомиелит черепа приводит к формированию эпидурального абсцесса (см. ниже), но практически никогда воспалительный процесс не проникает глубже ТМО, вследствие чего не представляет значительной опасности для жизни больного.
Лечение. Местная и системная антибактериальная терапия, в том числе с учетом антибиотикорезистентности выделенного воз-
будителя, чаще всего бывает неэффективной. Методом выбора является хирургическое вмешательство - удаление всей остеомиелитически измененной кости до макроскопически здоровых тканей. Пластическое закрытие образовавшегося костного дефекта при этом не производится. Мягкие ткани либо зашиваются наглухо, либо на 3 дня оставляют приточно-отточную дренажную систему. Антибактериальная терапия проводится с учетом чувствительности выделенного на дооперационном этапе патогена в течение не менее 6 нед (оптимально - до 12 нед). Костный дефект закрывают синтетическими материалами (полиметилметакрилат, титан и др.) при отсутствии признаков воспаления в ходе повторного хирургического вмешательства, не ранее чем через 6 мес после первой операции.
Абсцесс головного или спинного мозга
Абсцесс головного или спинного мозга - ограниченное скопление гноя либо в веществе мозга (такие абсцессы называются внутримозговыми), либо - реже - над или под ТМО, такие абсцессы называются эпидуральными или субдуральными. Встречаются с частотой 0,7 на 100 тыс. населения в год, в развивающихся странах - в несколько раз чаще.
Этиология и патогенез. В развитых странах основным путем формирования абсцессов мозга является гематогенный. Чаще всего источником бактериальных эмболов являются воспалительные процессы в легких (абсцесс легкого, бронхоэктатическая болезнь, эмпиема плевры, хроническая пневмония). Бактериальный эмбол (обычно - фрагмент инфицированного тромба из сосуда на периферии воспалительного очага) попадает в большой круг кровообращения и останавливается в сосуде меньшего диаметра (артериоле, прекапилляре или капилляре). При достаточной вирулентности патогена и неадекватности иммунитета развивается местный воспалительный процесс.
Причиной абсцесса мозга у детей часто являются «синие» пороки сердца, в первую очередь - тетрада Фалло, а также легочные артериовенозные шунты (50% из которых ассоциированы с синдромом Рендю-Ослера - множественными наследственными телеангиоэктазиями). Риск развития абсцесса мозга у таких больных - около 6%; патогенез неясен - возможно, имеют значение
повышение гематокрита и снижение РО2; источник инфекции, вероятно, является одонтогенным. Меньшее значение в патогенезе абсцессов мозга имеет острый бактериальный эндокардит, еще меньшее - хронический бактериальный эндокардит, сепсис и инфекции желудочно-кишечного тракта.
Помимо гематогенного пути формирования, абсцессы мозга могут возникать вблизи очагов воспалительных процессов в придаточных пазухах носа; крайне редко абсцессы имеют одонтогенное происхождение.
В прошлом основной причиной абсцессов мозга являлся расположенный вблизи (в первую очередь - в околоносовых придаточных пазухах) воспалительный процесс. И сегодня эта причина абсцессов мозга остается лидирующей в развивающихся странах, где больные с воспалительными процессами в околоносовых придаточных пазухах не получают адекватного лечения. Формирование абсцесса мозга в этом случае может быть обусловлено прямым проникновением инфекции через ТМО (при этом вначале формируется отграниченный воспалительный процесс в мозговых оболочках и затем - в прилежащем отделе мозга), но чаще воспалительный процесс распространяется ретроградно по синусам ТМО и мозговым венам.
Абсцессы мозга могут развиваться и вследствие прямого попадания инфекции при проникающей ЧМТ. В мирное время доля таких абсцессов не превышает 15%, но существенно возрастает при огнестрельных и минно-взрывных ранениях.
Наконец, в 25% случаев установить причину не представляется возможным. Частота абсцессов мозга существенно увеличивается у больных с иммунодефицитом различного генеза, но общая структура патогенеза остается той же.
Возбудители. Содержимое абсцессов мозга оказывается стерильным в 25% случаев. Среди выделенных возбудителей гематогенных абсцессов преобладают стрептококки (аэробные и анаэробные), часто - в ассоциации с бактероидами (Bacteroides spp.). В случае контактных абсцессов при хроническом среднем отите, а также при гематогенных абсцессах вследствие абсцесса легкого часто встречаются микроорганизмы семейства Enterobacteriaceae.
При проникающих ЧМТ в патогенезе абсцессов мозга лидируют стафилококки (в первую очередь - S. aureus), могут встречаться возбудители семейства Enterobacteriаceae.
У больных с иммунодефицитом (после трансплантации органов или ВИЧ-инфицированных) среди патогенов лидируют Aspergillus spp.
Патоморфология. Формирование абсцесса мозга проходит ряд стадий. Вначале при внедрении инфекции развивается ограниченное воспаление мозговой ткани - энцефалит (или, в современной американской литературе, - «ранний церебрит»). Длительность этой стадии - до 3 сут. В этот период воспалительный процесс обратим и может либо спонтанно, либо на фоне антибактериальной терапии завершиться рубцеванием. При недостаточности защитных механизмов и в случае неадекватного лечения воспалительный процесс прогрессирует, и к 4-9-м суткам в его центре возникает полость, заполненная гноем. Эта полость может увеличиваться, но к 10-13-м суткам вокруг гнойного очага начинает формироваться защитная соединительнотканная капсула, препятствующая дальнейшему распространению гнойного процесса. С 14-х суток эта капсула становится более плотной, вокруг нее формируется зона глиоза. Дальнейшее течение абсцесса мозга определяется вирулентностью флоры, реактивностью организма и адекватностью лечебно-диагностических мероприятий. Иногда абсцесс подвергается обратному развитию, но чаще происходит как увеличение его внутреннего объема, так и формирование новых воспалительных очагов по периферии капсулы, что в конечном счете при отсутствии адекватного лечения приводит к смерти больного.
Реже абсцесс локализуется не в мозгу, а в надили подоболочечном пространстве. Такие абсцессы обычно развиваются вследствие местного распространения инфекции из прилежащих гнойных очагов в околоносовых придаточных пазухах, при открытой ЧМТ и остеомиелите костей черепа. Неинкапсулированное скопление гноя в подили надоболочечном пространстве в соответствии с общехирургическими принципами называется соответственно субили эпидуральной эмпиемой. Прогноз в этом случае ухудшается, но тактика лечения принципиально не меняется.
Диагностика. Для постановки диагноза большое значение имеют тщательный сбор анамнеза и правильная его трактовка, поскольку патогномоничных симптомов абсцесса мозга не существует. Однако появление и прогрессирование в течение дней или недель у больного с диагностированным воспалительным процессом (в легких, после ЧМТ, в околоносовых придаточных пазухах и т.д.)
общемозговых (головная боль, тошнота, рвота, снижение уровня сознания) и очаговых (нарушение движений, чувствительности, речи) симптомов, эпилептических припадков, нарушений психики и т.д. заставляют заподозрить абсцесс мозга и назначить нейровизуализационное исследование. В ходе нейровизуализационного исследования необходимо изучить состояние околоносовых придаточных пазух. Если больной не был ранее обследован, следует провести и общее объективное исследование (минимум - рентгенографию органов грудной клетки, эхокардиографию и ЛОРосмотр).
КТ. Инкапсулированные абсцессы мозга с очень высокой, практически 100% точностью («чувствительностью») выявляются при КТ (рис. 7.1). Однако на ранних стадиях диагностировать абсцесс мозга с помощью КТ сложнее.
На стадии раннего энцефалита или «церебрита» (1-3-и сутки) при КТ без контрастного усиления выявляется зона сниженной плотности, часто - неправильной формы. При введении контрастного вещества его накопление происходит неравномерно, преимущественно - в периферических отделах очага, но иногда - и в его центре.
На стадии позднего энцефалита (4-9-е сутки) характерно накопление контрастного вещества большой ширины по периферии очага, контуры которого становятся более ровными и округлыми. По периферии очага может выявляться зона отека мозга. Рентгеновская плотность центральной зоны очага при введении контрастного вещества не изменяется, но через 30-40 мин при повторении КТ возможны диффузия контрастного вещества в центр очага, а также сохранение его в периферической зоне (последнее нехарактерно для опухолей).
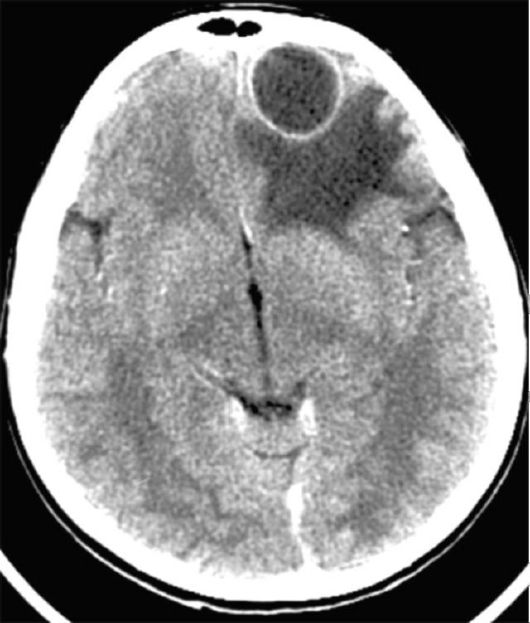 Рис. 7.1. Абсцесс правой лобной доли: КТ без контрастного усиления
Рис. 7.1. Абсцесс правой лобной доли: КТ без контрастного усиления
При анализе КТ следует иметь в виду, что глюкокортикоиды, часто используемые в лечении, значительно снижают накопление контрастного вещества в энцефалитическом очаге.
При иммунодефицитных состояниях перифокальный отек не выражен или отсутствует.
На стадии инкапсулированного абсцесса при нативной КТ (см. рис. 7.1) характерно наличие округлой зоны пониженной плотности в центре абсцесса (гной), зоны отека по периферии и тонкой зоны повышенной плотности между ними (фиброзная капсула).
При введении контрастного вещества его накопление носит кольцевидный характер, соответствующий фиброзной капсуле с небольшой прилежащей зоной глиоза, где нарушен гематоэнцефалический барьер. При повторении КТ через 30-40 мин капсула перестает контрастироваться.
МРТ. Еще более точным методом диагностики абсцесса мозга является МРТ. Энцефалитический очаг выглядит гипоинтенсивным на Т1- и гиперинтенсивным - на Т2-взвешенных изображениях. Инкапсулированный абсцесс (рис. 7.2) на Т1-взвешенных изображениях выглядит как зоны пониженного сигнала в центре и на периферии, в зоне отека, с кольцевидной зоной умеренно гиперинтенсивного сигнала между ними, соответствующей капсуле абсцесса (см. рис. 7.2, а). При введении контрастного вещества (см. рис. 7.2, б) четко контрастируется капсула. На Т2-взвешенных
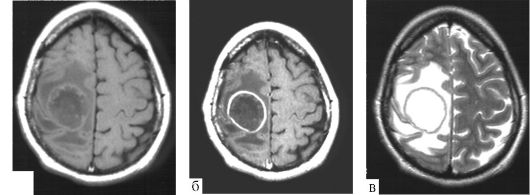
Рис. 7.2. Абсцесс правой заднелобно-теменной области: МРТ; а -Т1- взвешенное изображение; б - то же с контрастным усилением; в - Т2- взвешенное изображение
изображениях центральная зона абсцесса является изоили гипоинтенсивной, периферическая зона отека - гиперинтенсивная; между этими зонами прослеживается четко очерченная капсула (см. рис. 7.2, в).
Для абсцессов, обусловленных Nocardia spp., характерно многокамерное строение (рис. 7.3).
При сомнении в диагнозе и необходимости дифференцировки абсцесса с опухолевым поражением мозга исключительную роль играет МР-спектроскопия (дифференциальная диагностика
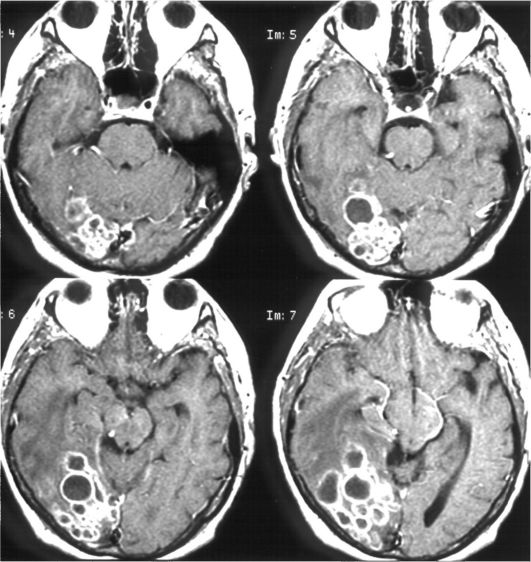 Рис. 7.3. Нокардиозный многокамерный абсцесс правой теменнозатылочной области; МРТ, Т1-взвешенное изображение с контрастным усилением
Рис. 7.3. Нокардиозный многокамерный абсцесс правой теменнозатылочной области; МРТ, Т1-взвешенное изображение с контрастным усилением
основывается на различном содержании лактата и аминокислот в абсцессах и опухолях) (рис. 7.4). При МР-спектроскопии могут также быть выявлены метаболиты, характерные для грибков.
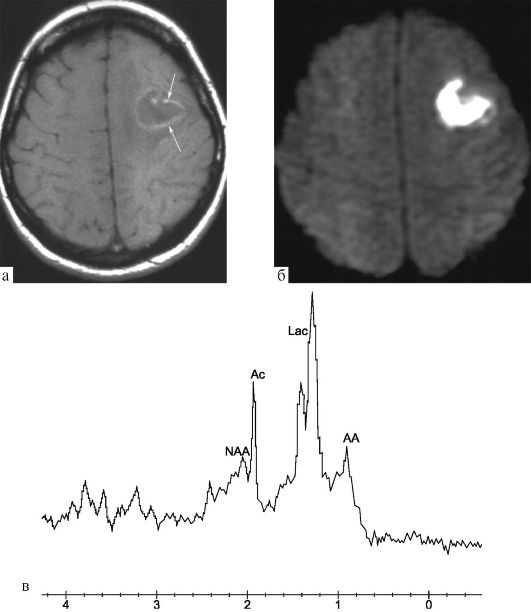 Рис. 7.4. Абсцесс левой лобной доли, неправильная форма затрудняет дифференциацию с опухолью: МРТ; а - T1-взвешенное
изображение; б - режим диффузии, выявляется характерный для абсцесса
высокий МР-сигнал; в -протонная МР-спектроскопия выявляет характерные
для абсцесса пики метаболитов - ацетата (Ас), лактата (Lac) и
аминокислот (АА)
Рис. 7.4. Абсцесс левой лобной доли, неправильная форма затрудняет дифференциацию с опухолью: МРТ; а - T1-взвешенное
изображение; б - режим диффузии, выявляется характерный для абсцесса
высокий МР-сигнал; в -протонная МР-спектроскопия выявляет характерные
для абсцесса пики метаболитов - ацетата (Ас), лактата (Lac) и
аминокислот (АА)
Наконец, если после проведения всего комплекса исследований остаются сомнения, проводят стереотаксическую биопсию капсулы: и аспирацию содержимого абсцесса.
Другие способы диагностики абсцесса мозга малоинформативны. Так, лихорадка, повышение СОЭ и содержания лейкоцитов в крови (у 70% больных с абсцессами мозга - не выше 10 000 в 1 мкл) могут наблюдаться при любых воспалительных процессах, не обязательно внутричерепных. Это же относится и к повышению содержания С-реактивного белка. Посевы крови обычно бывают стерильными. Люмбальная пункция в диагностике внутричерепных абсцессов сегодня не применяется в связи с низкой информативностью (в большинстве случаев воспалительный процесс в мозгу бывает отграниченным и не сопровождается менингитом) и опасностью дислокации мозга.
Лечение. Способ лечения абсцесса мозга зависит в первую очередь от его стадии и размера. Лечение больных с длительностью анамнеза заболевания до 2 нед, т.е. с энцефалитическим очагом, консервативное. Хотя некоторые авторы считают целесообразным проведение стереотаксической биопсии с целью верификации гистологического диагноза и выделения возбудителя, обычно тактикой является эмпирическая антибактериальная терапия.
Консервативное лечение в основном проводят также больным с небольшими (менее 3 см в диаметре, в том числе - множественными) абсцессами и при сопутствующем гнойном менингите или вентрикулите.
Прямое хирургическое вмешательство противопоказано при абсцессах, расположенных в жизненно важных (стволовых, подкорковых) структурах, но в этих ситуациях может быть использован стереотаксический метод - пункция абсцесса, часто - с установкой в его полость на несколько суток специального катетера для промывания полости абсцесса и введения антибактериальных препаратов. Следует учесть, что тяжелые соматические заболевания не являются абсолютным противопоказанием к хирургии абсцесса, ибо упомянутое минимально инвазивное стереотаксическое вмешательство может быть выполнено под местной анестезией.
Наконец, любое хирургическое вмешательство противопоказано у больных в крайне тяжелом состоянии (в терминальной коме).
Абсолютными показаниями к хирургическому вмешательству являются абсцессы, вызывающие повышение внутричерепного
давления и дислокацию мозга и расположенные вблизи желудочковой системы (поскольку прорыв гноя в желудочковую систему часто является фатальным). При травматических абсцессах в окружности инородного тела хирургическое вмешательство также является методом выбора, поскольку такой воспалительный процесс не может быть вылечен консервативно. Показанием к операции считаются и грибковые абсцессы, хотя прогноз в этой ситуации независимо от метода лечения крайне неблагоприятен.
Принципы консервативного лечения абсцесса мозга. Эмпирическая (по получении результата посева) антибактериальная терапия должна быть такой, чтобы воздействовать на максимально возможный спектр возбудителей. Поэтому используют следующий алгоритм.
• При бактериальном абсцессе головного мозга неясной этиологии назначают (одновременно):
о ванкомицин (взрослым - 1,0 г 2-3 раза в сутки внутривенно медленно капельно или через перфузор, детям - 15 мг на 1 кг массы тела 3 раза в сутки);
о цефалоспорин 3-4-го поколения (цефотаксим - 8-12 г/сут в 4-6 введений; цефтриаксон - 4 г/сут в 2 введения; цефтазидим и цефепим - по 6 г/сут в 3 введения);
о метронидазол (взрослым - 1,5 г 3 раза в сутки внутривенно, детям - 10 мг на 1 кг массы тела 3 раза в сутки).
• При посттравматических абсцессах назначают те же препараты, что и при посттравматическом менингите (см. выше) в максимальных дозах.
• У иммунодефицитных больных (кроме больных СПИД) наиболее вероятным возбудителем абсцесса мозга являются Cryptococcus neoformans, реже - Aspergillus spp. или Candida spp. В этом случае назначают амфотерицин B по 0,5-1 мг на 1 кг массы тела внутривенно в сутки, при исчезновении абсцесса по данным нейровизуализационных исследований - флуконазол по 800 мг внутривенно или внутрь однократно, затем - по 400 мг/сут внутрь до 10 нед.
• У больных СПИД наиболее вероятным возбудителем абсцесса мозга является Toxoplasma gondii, в эмпирическом лечении таких больных применяют сульфадиазин с пириметамином.
При получении культуры возбудителя лечение изменяют с учетом антибиотикограммы. При стерильном посеве продолжают эмпирическую антибактериальную терапию.
Продолжительность интенсивной антибактериальной терапии - не менее 6 нед.
Применение глюкокортикоидов приводит к уменьшению выраженности и более быстрому обратному развитию фиброзной капсулы абсцесса, что хорошо при адекватной антибактериальной терапии, но в противном случае может вести к распространению воспалительного процесса за пределы первичного очага. Поэтому назначение глюкокортикоидов оправдано лишь при нарастающем отеке и дислокации мозга, в остальных случаях является дискутабельным.
Хирургическое лечение абсцессов мозга. Первые предложенные операции предусматривали тотальное удаление абсцесса вместе с капсулой без вскрытия последней. Соответственно рекомендовалась выжидательная тактика, поскольку со временем капсула абсцесса обычно становится более выраженной.
Сегодня однозначно доказано, что удаление капсулы абсцесса в большинстве случаев смысла не имеет, поскольку влечет за собой дополнительную травматизацию мозга, тогда как капсула при адекватном лечении рассасывается в течение нескольких месяцев.
Исключениями являются грибковые и нокардиозные (вызванные Nocardia asteroides и реже - Nocardia brasiliensis) абсцессы, развивающиеся у иммунодефицитных больных. Радикальное удаление абсцессов в таких ситуациях несколько улучшает выживаемость.
Основной метод лечения большинства абсцессов мозга сегодня - простое или приточно-отточное дренирование. Сутью метода является установление в полость абсцесса катетера, через который эвакуируют гной и вводят антибактериальные препараты. При возможности в полость на несколько суток устанавливают второй катетер меньшего диаметра, через который осуществляют инфузию промывного раствора (обычно - 0,9% натрия хлорида, эффективность добавления к нему антибактериальных препаратов не доказана). Дренирование абсцесса подразумевает обязательную антибактериальную терапию (вначале - эмпирическую, затем - с учетом антибиотикочувствительности выделенного патогена).
Альтернативный метод - стереотаксическая аспирация содержимого абсцесса без установки дренажа. Достоинством метода являются снижение риска суперинфекции и меньшие требования к квалификации медицинского персонала (контроль за функционированием приточно-отточной системы требует специальных зна-
ний и пристального внимания), недостатком - частая, не менее чем в 70% случаев необходимость повторных аспираций.
При множественных абсцессах в первую очередь дренируют очаг, наиболее значимый для клинической картины или наиболее опасный в плане развития осложнений (дислокация мозга, прорыв гноя в желудочковую систему и т.д.).
Прогноз зависит от патогена, реактивности организма, числа абсцессов и своевременности и адекватности лечебных мероприятий. Летальность при абсцессах мозга - около 10%, инвалидизация - около 50%. Почти у 1/3 выживших больных развивается эпилептический синдром.
Субдуральные эмпиемы
Это - прогностически менее благоприятный вид патологии, чем абсцессы мозга, поскольку отсутствие границ гнойного очага указывает либо на высокую вирулентность патогена, либо на неадекватность иммунных реакций, либо и на то, и на другое. Для эмпием характерна большая выраженность менингеальных симптомов. Принципы диагностики субдуральных эмпием сходны с таковыми при абсцессах мозга.
Лечение предусматривает в первую очередь дренирование эмпиемы, иногда в полость эмпиемы устанавливают микроирригатор.
Летальность при субдуральных эмпиемах составляет около 50%, а при грибковых эмпиемах у иммунодефицитных больных - приближается к 100%. Инвалидизированными остаются большинство выживших.
Эпидуральные эмпиемы
Эпидуральные эмпиемы встречаются редко и в основном ассоциированы с остеомиелитом костей черепа. Лечение не отличается от такового при остеомиелите, прогноз обычно благоприятный - инфекция практически никогда не проникает через неповрежденную ТМО, и санация остеомиелитического очага приводит к ликвидации эпидуральной эмпиемы.
Специфические инфекционные поражения центральной нервной системы, требующие хирургического лечения
Сифилитические гуммы и туберкуломы в последние десятилетия стали казуистикой. Самым распространенным специфическим инфекционным процессом, при котором может потребоваться помощь нейрохирурга, сегодня является туберкулезный менингит (рис. 7.5). Поскольку при этом возможно существенное повышение
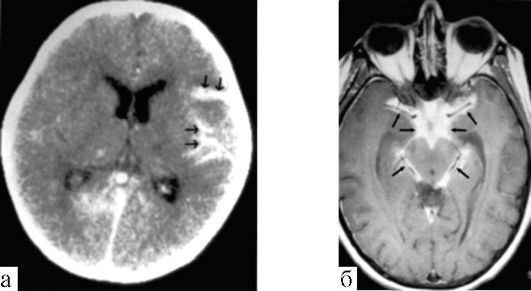 Рис. 7.5. Туберкулезный менингит: а - КТ с контрастным усилением; б - МРТ, Т1-взвешенное
изображение с контрастным усилением; стрелками обозначено накопление
контрастного вещества в левой лобно-теменной области (а) и цистернах
основания мозга (б)
Рис. 7.5. Туберкулезный менингит: а - КТ с контрастным усилением; б - МРТ, Т1-взвешенное
изображение с контрастным усилением; стрелками обозначено накопление
контрастного вещества в левой лобно-теменной области (а) и цистернах
основания мозга (б)
внутричерепного давления, нейрохирургу следует обеспечить его контроль. В острой стадии туберкулезного менингита можно применить наружное дренирование бокового желудочка (что позволяет также вводить противотуберкулезные средства непосредственно в ликворные пространства). В хронической стадии туберкулезного менингита часто развивается открытая (арезорбтивная) гидроцефалия, и тогда внутричерепное давление может быть нормализовано имплантацией вентрикулоперитонеального шунта. Подробно эти вмешательства описаны в предыдущей главе.