Фармакология / Под ред. проф. Р.Н. Аляутдина. - 4-е изд., перераб. и доп. - 2008. - 832 с. : ил.
|
|
|
|
ГЛАВА 8 СРЕДСТВА, ДЕЙСТВУЮЩИЕ НА ХОЛИНЕРГИЧЕСКИЕ СИНАПСЫ
Холинергические синапсы локализованы во внутренних органах, получающих постганглионарные парасимпатические волокна, в
вегетативных ганглиях, мозговом слое надпочечников, каротидных клубочках, скелетных мышцах. Передача возбуждения в холинергических синапсах происходит с помощью ацетилхолина.
Ацетилхолин синтезируется в цитоплазме окончаний холинергических нервов из ацетил-КоА и холина при участии фермента холинацетилтрансферазы (холинацетилазы) и депонируется в синаптических пузырьках (везикулах). Под влиянием нервных импульсов ацетилхолин высвобождается из везикул в синаптическую щель. Происходит это следующим образом. Распространяющийся по аксону импульс, вызывает деполяризацию пресинаптической мембраны окончания холинергического нерва, в результате чего открываются потенциалозависимые кальциевые каналы, через которые ионы кальция проникают в нервное окончание. Концентрация Са2+ в цитоплазме нервного окончания повышается, что способствует слиянию мембраны везикул с пресинаптической мембраной (слияние происходит вследствие взаимодействия белков везикулярной и пресинаптической мембран) и выделению содержимого везикул в синаптическую щель (рис. 8-1). Этот процесс носит название экзоцитоза. Слиянию везикулярной и пресинаптической мембран, и, следовательно, высвобождению ацетилхолина в синаптическую щель препятствует ботулинический токсин. Высвобождение ацетилхолина блокируют также вещества, которые снижают поступление Са2+ в цитоплазму нервных окончаний, например аминогликозидные антибиотики или ионы магния.
После высвобождения в синаптическую щель ацетилхолин стимулирует холинорецепторы, локализованные как на постсинаптической, так и на пресинаптической мембране холинергических синапсов.
В синаптической щели ацетилхолин очень быстро гидролизуется ферментом ацетилхолинэстеразой с образованием холина и уксусной кислоты. Холин захватывается нервными окончаниями (подвергается обратному нейрональному захвату) и вновь включается в синтез ацетилхолина. В плазме крови, печени и других органах присутствует фермент бутирилхолинэстераза (псевдохолинэстера- за, ложная холинэстераза), которая также может инактивировать ацетилхолин.
На передачу возбуждения в холинергических синапсах могут воздействовать вещества, которые оказывают влияние на следующие процессы:
• синтез ацетилхолина и его депонирование в везикулах;
• высвобождение ацетилхолина;
• взаимодействие ацетилхолина с холинорецепторами;
• гидролиз ацетилхолина в синаптической щели;
• обратный нейрональный захват холина.
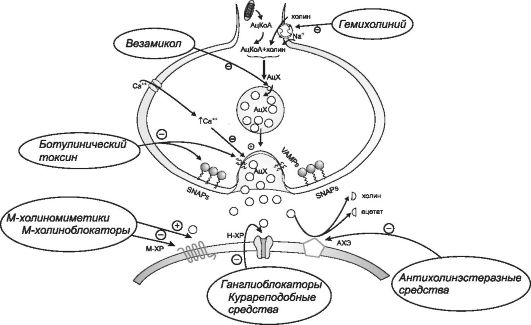
Рис. 8-1. Схема холинергического синапса. Локализация действия веществ, влияющих на холинергическую иннервацию: АцХ - ацетилхолин; АцКоА - ацетилкоэнзим А; Н-ХР - никотиновый холинорецептор; М-ХР - мускариновый холинорецептор; АХЭ -ацетилхолинэстераза; SNAPs - synaptosome-associated proteins; VAMPs- vesicle-associated membrane proteins
Депонирование ацетилхолина в везикулах уменьшает везами- кол**, который блокирует транспорт ацетилхолина из цитоплазмы в везикулы. Высвобождение ацетилхолина в синаптическую щель стимулирует аминопиридин (пимадин*). Блокирует высвобождение ацетилхолина ботулинический токсин. Обратный нейрональный захват холина ингибирует гемихолиний**, который блокирует транспортные белки пресинаптической мембраны нервного окончания. Однако эти вещества (за исключением препаратов ботулинического токсина) не нашли применение в качестве ЛС.
В медицинской практике в основном используют вещества, которые непосредственно взаимодействуют с холинорецепторами: холи- номиметики (вещества, стимулирующие холинорецепторы), и холиноблокаторы (вещества, которые блокируют холинорецепторы и таким образом препятствуют действию на них ацетилхолина). Применяют также вещества, которые ингибируют гидролиз ацетилхолина, - ингибиторы ацетилхолинэстеразы (антихолинэстеразные средства).
8.1. СРЕДСТВА, СТИМУЛИРУЮЩИЕ ХОЛИНЕРГИЧЕСКИЕ СИНАПСЫ
В этой группе выделяют холиномиметики - вещества, которые подобно ацетилхолину непосредственно стимулируют холинорецепторы, и а н т и х о л и н э с т е р а з н ы е с р е д с т в а , которые, ингибируя ацетилхолинэстеразу, повышают концентрацию ацетилхолина в синаптической щели и таким образом усиливают и пролонгируют действие ацетилхолина.
8.1.1. Холиномиметики
Холинорецепторы разных холинергических синапсов одинаково чувствительны к ацетилхолину, но проявляют неодинаковую чувствительность к другим веществам. Холинорецепторы, локализованные в постсинаптической мембране клеток эффекторных органов у окончаний постганглионарных парасимпатических волокон, проявляют высокую чувствительность к мускарину (алкалоиду, выделенному из некоторых видов мухоморов). Такие рецепторы называют мускариночувствительными, или М-холинорецепторами.
Холинорецепторы, расположенные в постсинаптической мембране нейронов симпатических и парасимпатических ганглиев, хромаффинных клеток мозгового вещества надпочечников, в каротидных клубочках (которые находятся в месте деления общих сонных артерий) и на концевой пластинке скелетных мышц (в нервно-мышечных синапсах), наиболее чувствительны к никотину и поэтому называются никотиночувствительными рецепторами или Н-холинорецепторами. Эти рецепторы подразделяются на Н-холинорецепторы ней- ронального типа (Нн) и Н-холинорецепторы мышечного типа (Нм),
различающиеся по локализации (табл. 8-1) и по чувствительности к фармакологическим веществам.
Вещества, которые избирательно блокируют Нн-холинорецепторы ганглиев, мозгового вещества надпочечников и каротидных клубочков, называются ганглиоблокаторами, а вещества, преимущественно блокирующие Нм-холинорецепторы скелетных мышц, - курареподобными средствами.
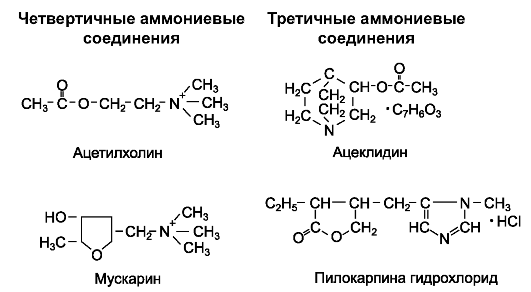
Среди холиномиметиков выделяют вещества, которые преимущественно стимулируют М-холинорецепторы (М-холиномиметики), Н-холинорецепторы (Н-холиномиметики) или оба подтипа холинорецепторов одновременно (М-, Н-холиномиметики). Классификация холиномиметико в М-холиномиметики: мускарин**, пилокарпин, ацеклидин Н-холиномиметики: никотин, цитизин (цититон*), лобелин. М-, Н-холиномиметики: ацетилхолин, карбахол (карбахолин*).
М-холиномиметики
М-холиномиметики стимулируют М-холинорецепторы, расположенные в мембране клеток эффекторных органов и тканей, получающих парасимпатическую иннервацию. М-холинорецепторы подразделяют на несколько подтипов, которые проявляют неодинаковую чувствительность к разным фармакологическим веществам. Обнаружено 5 подтипов М-холинорецепторов (М1, М2, М3, М4, М5). Наиболее под- робно изучены М1-, М2- и М3-холинорецепторы (см. табл. 8-1). Все М-холинорецепторы относятся к мембранным рецепторам, взаимодействующим с G-белками, а через них с определенными ферментами или ионными каналами.
Так, М2-холинорецепторы мембран кардиомиоцитов взаимодействуют с Gi-белками, угнетающими аденилатциклазу. При их стимуляции в клетках снижается синтез цАМФ и, как следствие, активность цАМФ-зависимых протеинкиназ, фосфорилирующих белки. В кардиомиоцитах нарушается фосфорилирование кальциевых каналов, в результате меньше Са2+ поступает в клетку во время деполяризации мембраны. Это приводит к снижению автоматизма синоатриального узла и, следовательно, к уменьшению частоты сердечных сокращений. Уменьшаются также и другие показатели работы сердца (см. табл. 8-1). Кроме того, при стимуляции М2-холинорецепторов активируются калиевые каналы и усиливается выход калия из клетки, что приводит
к гиперполяризации мембраны и развитию тормозных эффектов. М2-холинорецепторы локализованы также на пресинаптической мембране окончаний постганглионарных парасимпатических волокон. При их возбуждении уменьшается выделение ацетилхолина в синап- тическую щель.
М3-холинорецепторы гладкомышечных клеток и клеток экзокринных желез взаимодействуют с Gq-белками, которые активируют фосфолипазу С. При участии этого фермента из фосфолипидов клеточных мембран образуется инозитол-1,4,5-трифосфат, который способствует высвобождению Са2+ из саркоплазматического/эндоплазматического ретикулума (внутриклеточного депо кальция). В результате при стимуляции М3-холинорецепторов концентрация Са2+ в цитоплазме клеток увеличивается, что вызывает повышение тонуса гладких мышц внутренних органов и увеличение секреции экзокринных желез. Кроме того, в мембране эндотелиальных клеток сосудов располагаются неиннервируемые (внесинаптические) М3-холинорецепторы. При их стимуляции увеличивается высвобождение из эндотелиальных клеток эндотелиального релаксирующего фактора (NO), который вызывает расслабление гладкомышечных клеток сосудов. Это приводит к снижению тонуса сосудов и уменьшению АД.
М1-холинорецепторы также сопряжены с Gq-белками. Стимуляция М1-холинорецепторов энтерохромаффиноподобных клеток желудка приводит к повышению концентрации цитоплазматического Са2+ и увеличению секреции этими клетками гистамина. Гистамин в свою очередь, действуя на париетальные клетки желудка, стимулирует секрецию хлористоводородной кислоты. Подтипы М-холинорецепторов и эффекты, вызываемые их стимуляцией, представлены в табл. 8-1.
Прототип М-холиномиметиков - алкалоид мускарин, содержащийся в ядовитых грибах (мухоморах). Мускарин вызывает эффекты, связанные со стимуляцией всех подтипов М-холинорецепторов, при- веденных в табл. 8-1. Через ГЭБ мускарин не проникает и поэтому не оказывает существенного влияния на ЦНС. Мускарин не используют в качестве лекарственного средства. При отравлении мухоморами, содержащими мускарин, проявляется его токсическое действие, связанное с возбуждением М-холинорецепторов. При этом отмечают сужение зрачков, спазм аккомодации, обильное слюнотечение и пото- отделение, повышение тонуса бронхов и секреции бронхиальных желез (что проявляется ощущением удушья), брадикардию и снижение АД,
Таблица 8-1
Подтипы холинорецепторов и эффекты, вызываемые их стимуляцией
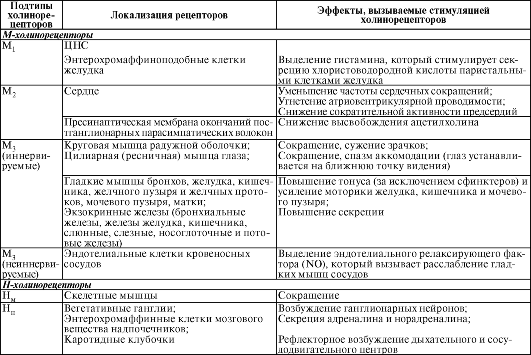
спастические боли в животе, диарею, тошноту и рвоту. Центральные эффекты при отравлении мухоморами вызваны содержащимися в них галлюциногенами. При отравлении мухоморами проводят промывание желудка и дают солевые слабительные. Для устранения действия мускарина применяют М-холиноблокатор атропин.
П и л о к а р п и н - алкалоид листьев кустарника Pilocarpus pinnatifolius Jaborandi, произрастающего в Южной Америке. Пилокарпин, применяемый в медицинской практике, получают синтетическим путем. Пилокарпин оказывает прямое стимулирующее действие на М- холинорецепторы и вызывает все эффекты, характерные для препаратов этой группы (см. табл. 8-1). Особенно сильно пилокарпин повышает секрецию желез, поэтому его иногда в небольших дозах (5-10 мг) назначают внутрь при ксеростомии (сухость слизистой оболочки полости рта). В ряде стран выпускают препарат пилокарпина для введения внутрь (салаген**). Но поскольку пилокарпин обладает довольно высокой токсичностью, его в основном применяют местно в виде глазных лекарственных форм для снижения внутриглазного давления.
Величина внутриглазного давления в основном зависит от двух процессов: образования и оттока внутриглазной жидкости (водянистой влаги глаза). Внутриглазная жидкость продуцируется ресничным телом, а оттекает главным образом через дренажную систему угла передней камеры глаза (между радужкой и роговицей). Эта дренажная система включает трабекулярную сеть (гребешковую связку) и веноз-
ный синус склеры (шлеммов канал). Через щелевидные пространства между трабекулами (фонтановы пространства) трабекулярной сети жидкость фильтруется в шлеммов канал, а оттуда по коллекторным сосудам оттекает в поверхностные вены склеры (рис. 8-2).
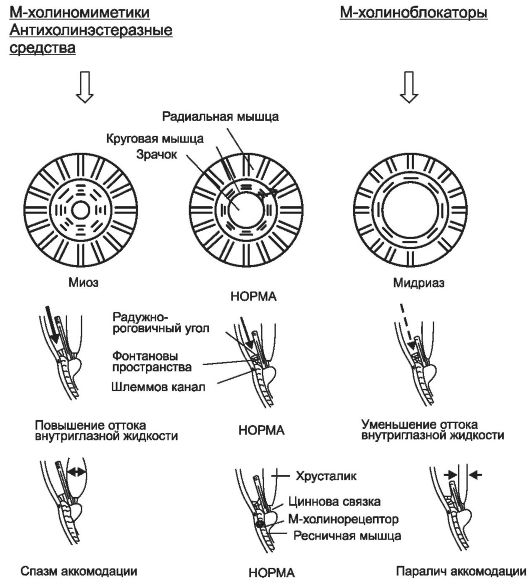
Рис. 8-2. Действие на глаз веществ, влияющих на холинергическую иннервацию (толщиной стрелки показана интенсивность оттока внутриглазной жидкости)
Снизить внутриглазное давление можно, уменьшив продукцию внутриглазной жидкости и/или увеличив ее отток. Отток внутриглазной жидкости во многом зависит от размера зрачка, величина которо-
го регулируется двумя мышцами радужной оболочки: круговой мышцей (m. sphincter pupillae) и радиальной мышцей (m. dilatator pupillae). Круговая мышца иннервируется парасимпатическими волокнами (n. oculomotorius), а радиальная - симпатическими (n. sympaticus). При сокращении круговой мышцы зрачок сужается, а при сокращении радиальной мышцы расширяется.
Способность пилокарпина снижать внутриглазное давление используют при лечении глаукомы - заболевания, которое характеризуется постоянным или периодическим повышением внутриглазного давле- ния, что может привести к атрофии зрительного нерва и потере зрения. Глаукома бывает закрытоугольной и открытоугольной. Закрытоугольная форма развивается при нарушении доступа к углу передней камеры глаза чаще всего при его частичном или полном закрытии корнем радужки. Внутриглазное давление при этом может повыситься до 60-80 мм рт.ст. (в норме внутриглазное давление составляет 16-26 мм рт.ст.). Открытоугольная форма глаукомы связана с нарушением дренажной системы угла передней камеры глаза, через которую осуществляется отток внутриглазной жидкости; сам угол при этом открыт.
Пилокарпин, как все М-холиномиметики, вызывает сокращение круговой мышцы радужной оболочки и сужение зрачков (миоз). Также он вызывает сокращение цилиарной (ресничной) мышцы.
В связи со способностью сужать зрачки (миотическое действие) пилокарпин обладает высокой эффективностью при лечении закрытоугольной глаукомы и в этом случае его используют в первую очередь (препарат выбора). При сужении зрачков радужная оболочка становится тоньше, что способствует раскрытию угла передней камеры глаза (между радужкой и роговицей) и оттоку внутриглазной жидкости через фонтановы пространства в шлеммов канал. Это приводит к снижению внутриглазного давления.
Назначают пилокарпин и при открытоугольной глаукоме. При этой форме глаукомы имеет значение действие пилокарпина на цилиарную мышцу. Сокращение цилиарной мыщцы вызывает натяжение трабекул гребешковой связки, вследствие чего фонтановы пространства увеличиваются в размерах и улучшается отток внутриглазной жидкости.
Пилокарпин применяют в виде 1-2% водных растворов (продолжительность действия - 4-8 ч), растворов с добавлением полимерных соединений, оказывающих пролонгированное действие (8-12 ч), мазей и специальных глазных пленок из полимерного материала (глазные пленки с пилокарпином закладывают за нижнее веко 1-2 раза в сутки).
Вызываемое пилокарпином сокращение ресничной мышцы приводит к расслаблению цинновой связки, расстягивающей хрусталик. Кривизна хрусталика увеличивается, он приобретает более выпуклую форму. При увеличении кривизны хрусталика повышается его преломляющая способность - глаз устанавливается на ближнюю точку видения (лучше видны предметы, находящиеся вблизи). Это явление, которое называют спазмом аккомодации, относится к побочным эффектам пилокарпина.
При закапывании в конъюнктивальный мешок пилокарпин практически не всасывается в кровь и не оказывает заметного резорбтивного действия.
Ацеклидин - синтетическое соединение с прямым стимулирующим действием на М-холинорецепторы, вызывает все эффекты, связанные с возбуждением этих рецепторов (см. табл. 8-1).
Ацеклидин можно применять местно (инстиллировать в конъюнктивальный мешок) для понижения внутриглазного давления при глаукоме. После однократной инстилляции снижение уровня внутриглазного давления продолжается до 6 ч. Однако растворы ацеклидина обладают местнораздражающим действием и могут вызвать раздражение конъюнктивы.
В связи с меньшей по сравнению с пилокарпином токсичностью ацеклидин можно применять для резорбтивного действия при атонии кишечника и мочевого пузыря. Назначают внутрь и парентерально.
Побочные эффекты: слюнотечение, диарея, спазмы гладкомышечных органов. Вследствие того, что ацеклидин повышает тонус гладких мышц бронхов, он противопоказан при бронхиальной астме.
Бетанехол** - также синтетический М-холиномиметик, применяемый при атонии кишечника и мочевого пузыря. Назначают внутрь и парентерально.
При передозировке М-холиномиметиков используют их антагонисты - М-холиноблокаторы (атропин и атропиноподобные средства).
Н-холиномиметики
К этой группе относят алкалоиды никотин, лобелин, цитизин, которые действуют преимущественно на Н-холинорецепторы нейронального типа, локализованные на нейронах симпатических и парасимпатических ганглиев, хромаффинных клетках мозгового вещества надпочечников, в каротидных клубочках и в ЦНС. На Н-холинорецепторы скелетных мышц эти вещества действуют в значительно больших дозах.
Н-холинорецепторы относят к мембранным рецепторам, непосредственно связанным с ионными каналами. По структуре это - гликопротеины, состоящие из нескольких субъединиц. Так, Н-холинорецептор нервно-мышечных синапсов включает 5 белковых субъединиц (α, α, β, γ, δ), которые окружают ионный (натриевый) канал. При связывании двух молекул ацетилхолина с α-субъединицами происходит открытие Na+-канала. Ионы Na+ входят в клетку, что приводит к деполяризации постсинаптической мембраны концевой пластинки скелетных мышц и мышечному сокращению.
Н и к о т и н - алкалоид, который содержится в листьях табака (Nicotiana tabacum, Nicotiana rustica). В основном никотин попадает в организм человека во время курения табака, примерно 3 мг за время курения одной сигареты (смертельная доза никотина - 60 мг). Он быстро всасывается со слизистых оболочек дыхательных путей (также хорошо проникает через неповрежденную кожу).
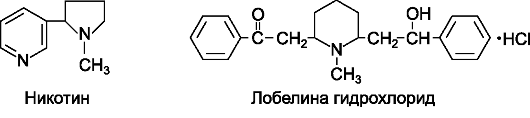
Никотин стимулирует Н-холинорецепторы симпатических и парасимпатических ганглиев, хромаффинных клеток мозгового вещества надпочечников (повышает выделение адреналина и норадреналина) и каротидных клубочков (стимулирует дыхательный и сосудодвигательный центры). Стимуляция симпатических ганглиев, мозгового вещества надпочечников и каротидных клубочков приводит к наиболее характерным для никотина эффектам со стороны сердечно-сосудистой системы: увеличению частоты сердечных сокращений, сужению сосудов и повышению АД. Стимуляция парасимпатических ганглиев вызывает повышение тонуса и моторики кишечника и повышение секреции экзокринных желез (большие дозы никотина оказывают на эти процессы угнетающее влияние). Стимуляция Н-холинорецепторов парасимпатических ганглиев также является причиной брадикардии, которую можно наблюдать в начале действия никотина.
Так как никотин обладает высокой липофильностью (третичный амин), он быстро проникает через ГЭБ в ткани мозга. В ЦНС никотин вызывает высвобождение дофамина, некоторых других биогенных аминов и возбуждающих аминокислот, с чем связывают субъектив-
ные приятные ощущения, возникающие у курильщиков. В небольших дозах никотин стимулирует дыхательный центр, а в больших дозах вызывает его угнетение вплоть до остановки дыхания (паралич дыхательного центра). В больших дозах никотин вызывает тремор и судороги. Действуя на триггерную зону рвотного центра, никотин может вызвать тошноту и рвоту.
Никотин в основном метаболизируется в печени и выводится почками в неизмененном виде и в виде метаболитов. Таким образом, он быстро элиминируется из организма (t1/2 - 1,5-2 ч). К действию никотина быстро развивается толерантность (привыкание).
Острое отравление никотином может произойти при попадании растворов никотина на кожу или слизистые оболочки. При этом отмечают гиперсаливацию, тошноту, рвоту, диарею, брадикардию, а затем тахикардию, повышение АД, сначала одышку, а затем угнетение дыхания, возможны судороги. Смерть наступает от паралича дыхательного центра. Основная мера помощи - искусственное дыхание.
При курении табака возможно хроническое отравление никотином, а также другими токсичными веществами, которые содержатся в табачном дыме и могут оказывать раздражающее и канцерогенное действие. Для большинства курильщиков типичны воспалительные заболевания дыхательных путей, например хронический бронхит; чаще отмечают рак легких. Повышен риск сердечно-сосудистых заболеваний.
К никотину развивается психическая зависимость, при прекращении курения у курильщиков возникает синдром отмены, который связан с возникновением тягостных ощущений, снижением работос- пособности. Для уменьшения синдрома отмены рекомендуют в период отвыкания от курения использовать жевательную резинку, содержащую никотин (2 или 4 мг), или трансдермальную терапевтическую систему (специальный накожный пластырь, который в течение 24 ч равномерно выделяет небольшие количества никотина).
В медицинской практике иногда используют Н-холиномиметики лобелин и цитизин.
Лобелин - алкалоид растения Lobelia inflata, третичный амин. Стимулируя Н-холинорецепторы каротидных клубочков, лобелин рефлекторно возбуждает дыхательный и сосудодвигательный центры.
Цитизин - алкалоид, который содержится в растениях ракитник (Cytisus laburnum) и термопсис (Thermopsis lanceolata), вторичный амин. По действию сходен с лобелином, но несколько сильнее возбуждает дыхательный центр.
Цитизин и лобелин входят в состав таблеток «Табекс»* и «Лобесил»*, которые применяют для облегчения отвыкания от курения. Препарат цититон* (0,15% раствор цитизина) и раствор лобелина иногда вводят внутривенно для рефлекторной стимуляции дыхания. Однако эти препараты эффективны только при сохранении рефлекторной возбудимости дыхательного центра. Поэтому их не применяют при отравлении веществами, которые снижают возбудимость дыхательного центра (снотворные средства, наркотические анальгетики).
М-, Н-холиномиметики
Ацетилхолин - медиатор, который передает возбуждение во всех холинергических синапсах, стимулирует как М-, так и Н-холи- норецепторы. Ацетилхолин выпускают в виде лиофилизированного препарата ацетилхолин-хлорида*. При введении ацетилхолина в организм преобладают его эффекты, связанные со стимуляцией М-холинорецепторов: брадикардия, расширение сосудов и понижение АД, повышение тонуса и усиление перистальтики ЖКТ, повышение тонуса гладких мышц бронхов, желчного и мочевого пузыря, матки, усиление секреции бронхиальных и пищеварительных желез. Стимулирующее влияние ацетилхолина на периферические Н-холинорецепторы (нико- тиноподобное действие) проявляется при блокаде М-холинорецепторов (например, атропином). В результате на фоне атропина ацетилхолин вызывает тахикардию, сужение сосудов и, как следствие, повышение АД. Происходит это вследствие возбуждения симпатических ганглиев, повышения выделения адреналина хромаффинными клетками мозгового вещества надпочечников и стимуляции каротидных клубочков.
В очень больших дозах ацетилхолин может вызвать стойкую деполяризацию постсинаптической мембраны и блокаду передачи возбуждения в холинергических синапсах.
По химической структуре ацетилхолин - четвертичное аммониевое соединение и поэтому плохо проникает через ГЭБ и не оказывает существенного влияния на ЦНС. В организме ацетилхолин быстро разрушается холинэстеразой плазмы крови и ацетилхолинэстеразой и поэтому оказывает кратковременное действие, которое продолжается всего несколько минут.
Ацетилхолин применяют только местно для сужения зрачка при глазных хирургических операциях. Для этих целей используют отечественный препарат ацетилхолин-хлорид*.
Карбахол (карбахолин*) - аналог ацетилхолина, но в отличие от него практически не разрушается ацетилхолинэстеразой и поэтому действует более продолжительно (в течение 1-1,5 ч). Вызывает такие же фармакологические эффекты. Раствор карбахола в виде глазных капель можно использовать при глаукоме.
8.1.2. Антихолинэстеразные средства
Антихолинэстеразные средства ингибируют ацетилхолинэстеразу, фермент, который гидролизует ацетилхолин в синаптической щели, и холинэстеразу плазмы крови (бутирилхолинэстераза, псевдохолинэс- тераза, ложная холинэстераза). Ингибирование ацетилхолинэстеразы в холинергических синапсах приводит к повышению концентрации ацетилхолина в синаптической щели, вследствие чего значительно усиливается и удлиняется действие ацетилхолина. Таким образом, все эффекты антихолинэстеразных средств вызваны эндогенным ацетилхолином.
При введении антихолинэстеразных средств стимулирующее действие ацетилхолина на М-холинорецепторы приводит к сужению зрачков, спазму аккомодации, брадикардии (и снижению сердечного выброса), повышению тонуса гладких мышц бронхов, тонуса и моторики ЖКТ, мочевого пузыря, увеличению секреции экзокринных желез. Антихолинэстеразные средства практически не влияют на тонус сосудов. Связано это с тем, что в сосудах находятся в основном неиннервируемые (внесинаптические) М-холинорецепторы. Артериальное давление снижается гораздо в меньшей степени, чем при введении М-холиномиметиков (в основном за счет снижения сердечного выброса).
При введении антихолинэстеразных средств из Н-холиномиметических эффектов ацетилхолина наиболее отчетливо проявляется его стимулирующее влияние на нервно-мышечную передачу, в результате чего повышается тонус скелетных мышц.
Стимулирующее влияние ацетилхолина на вегетативные ганглии проявляется в меньшей степени. Однако при введении больших доз антихолинэстеразных средств стимуляция Н-холинорецепторов симпатических ганглиев, хромаффинных клеток мозгового вещества надпочечников и каротидных клубочков может привести к возникновению тахикардии и повышению АД.
Антихолинэстеразные средства, проникающие через ГЭБ, оказывают возбуждающее действие на ЦНС.
По характеру взаимодействия с ацетилхолинэстеразой различают антихолинэстеразные вещества обратимого и необратимого действия.
Антихолинэстеразные средства обратимого действия
Физостигмин (эзерин**), неостигмина метил- сульфат (прозерин*), пиридостигмина бромид (калимин*), ривастигмина гидротартрат (экселон*), галантамина гидробромид* (реминил*, нивалин*), донепезил (арисепт*), эдрофоний** (тензилон**).
Ацетилхолинэстераза имеет два активных центра: анионный и эстеразный. Положительно заряженный четвертичный атом азота в молекуле ацетилхолина связывается с анионным центром, а углерод карбонильной группы - с эстеразным центром. В результате происходит гидролиз ацетилхолина с образованием холина и ацетилированного фермента (ковалентно связанного с ацетильной группой). Отщепление ацетильной группы и, как следствие, восстановление активности ацетилхолинэстеразы происходит очень быстро. Весь процесс гидролиза ацетилхолина занимает порядка 100-150 мксек.
Многие антихолинэстеразные вещества (физостигмин, неостигмин, пиридостигмин, ривастигмин и некоторые другие) являются эфирами карбаминовой кислоты (карбаматы). Эти вещества подобно ацетилхолину связываются как с анионным, так и с эстеразным центрами ацетилхолинэстеразы и подвергаются гидролизу, при этом ацетилхолинэстераза оказывается ковалентно связанной с карбамоильной группой. Гидролиз этой более прочной связи происходит медленнее - от 30 мин до нескольких часов. В основном препараты этой группы ингибируют ацетилхолинэстеразу в течение 3-6 ч. Другие обратимые ингибиторы ацетилхолинэстеразы (эдрофоний**, галантамин, донепезил) связываются посредством нековалентных связей только с одним центром фермента и препятствуют его взаимодействию с ацетилхолином. Эдрофоний** связывается с анионным центром ацетилхолинэстеразы при участии непрочных электростатических и водородных связей. Этот комплекс существует 5-10 мин, поэтому эдрофоний** оказывает кратковременное антихолинэстеразное действие. Кроме того, эдрофоний** - полярное гидрофильное соединение (четвертичный амин), быстро выводится из организма. Донепезил и галантамин обладают большим сродством к ферменту и действуют намного продолжительнее. Эти вещества, в отличие от
эдрофония**, являются третичными аминами и проникают через гематоэнцефалический барьер в ткани мозга.
Неостигмин - синтетическое соединение, содержащее четвертичный атом азота, плохо проникает через гематоэнцефалический барьер. Обладает выраженной антихолинэстеразной активностью, усиливая и удлиняя действие ацетилхолина преимущественно в пери- ферических холинергических синапсах. При применении неостигмина преобладают эффекты, связанные с возбуждением парасимпати-
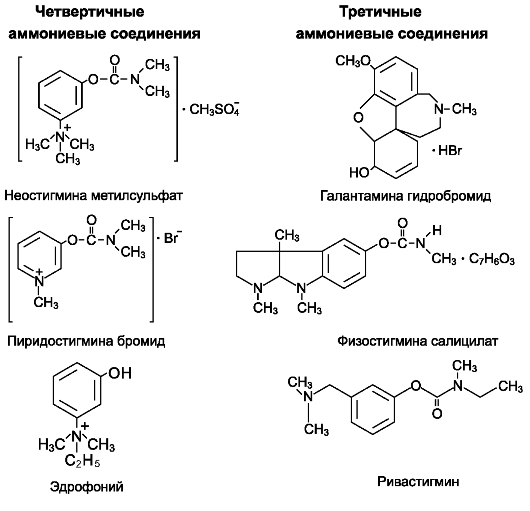
ческой иннервации. Неостигмин вызывает сужение зрачков (вследствие сокращения круговой мышцы радужки), что приводит к понижению внутриглазного давления (открывается угол передней камеры глаза и облегчается отток внутриглазной жидкости через фонтановы пространства в шлеммов канал). Одновремннно развивается спазм
аккомодации (вследствие сокращения цилиарной мышцы расслабляется циннова связка - хрусталик становится более выпуклым и глаз устанавливается на ближнюю точку видения). Неостигмин вызывает брадикардию и замедление атриовентрикулярной проводимости, повышает тонус бронхов, тонус и моторику ЖКТ, тонус и сократительную активность мочевого пузыря, матки, секрецию экзокринных желез. Из эффектов, связанных со стимуляцией Н-холинорецепторов, отмечают облегчение нервно-мышечной передачи.
В клинической практике в основном используют стимулирующее действие неостигмина на тонус скелетных мышц и тонус гладких мышц ЖКТ и мочевого пузыря.
Основные показания к применению неостигмина:
• миастения (аутоиммунное заболевание, при котором образуются антитела к Н-холинорецепторам скелетных мышц, вследствие чего уменьшается их количество; проявляется мышечной слабостью и повышенной утомляемостью скелетных мышц, в тяжелых случаях возможно нарушение дыхания из-за ослабления сократимости дыхательных мышц), препарат назначают внутрь, под кожу и внутримышечно, при миастеническом кризе - внутривенно;
• послеоперационная атония кишечника и мочевого пузыря, препарат вводят внутрь, под кожу или внутримышечно;
• в качестве антагониста курареподобных средств антидеполяризующего конкурентного типа действия для снятия остаточного нервно-мышечного блока, вводят внутривенно.
Неостигмин, будучи полярным гидрофильным соединением, после приема внутрь плохо всасывается из ЖКТ (дозы для приема внутрь в 30 раз превышают дозы для парентерального введения), действует непро- должительно (2-3 ч). Побочные эффекты неостигмина в основном связаны со стимуляцией М-холинорецепторов: тошнота, рвота, диарея, гиперсаливация, брадикардия, снижение АД, повышение тонуса бронхов. Стимуляция Н-холинорецепторов вызывает подергивание скелетных мышц. При передозировке препарата наряду с усилением симптомов, связанных со стимуляцией парасимпатической системы, возможно уси- ление симптомов миастении вследствие нарушения нервно-мышечной передачи (холинергический криз). Препарат противопоказан при эпилепсии, болезни Паркинсона, стенокардии, нарушениях проводящей системы сердца, бронхиальной астме, язвенной болезни желудка и двенадцатиперстной кишки и других заболеваниях, при которых усиление парасимпатических влияний на органы и ткани нежелательно.
Пиридостигмин - также четвертичное аммониевое соединение, не проникает через ГЭБ, действует подобно неостигмину, но более продолжительно (около 6 ч). В основном его применяют при лечении миастении, а также при атонии кишечника и мочевого пузыря, назначают внутрь и парентерально. По сравнению с неостигмином обладает менее выраженным мускариноподобным действием. Побочные эффекты и противопоказания аналогичны таковым для неостигмина. При передозировке пиридостигмина возможен холинергический криз.
Другой длительно действующий препарат, применяемый при миастении, - амбенония хлорид (оксазил*), оказывает эффект продолжительностью до 10 ч, принимают внутрь. Амбеноний является четвертичным аммониевым соединением, не проникает через ГЭБ.
Эдрофоний** - короткодействующий препарат (продолжительность действия 5-15 мин), являясь четвертичным амином, оказывает в основном периферическое действие. Применяют для диагностики миастении, вводят внутривенно (эффект наступает через 30-60 сек). Повышение тонуса скелетных мышц после введения препарата является признаком заболевания.
Эдрофоний** также используют для диагностики холинергического криза, вызываемого передозировкой антихолинэстеразных средств при лечении миастении. При передозировке антихолинэстеразных средств (неостигмина, пиридостигмина) вместо ожидаемого улучшения состояния отмечают мышечную слабость, связанную с чрезмерной деполяризацией постсинаптической мембраны, что препятствует передаче возбуждения в нервно-мышечных синапсах (деполяриза- ционный блок). В такой ситуации введение эдрофония** не вызывает повышения тонуса скелетных мышц и может даже усилить мышечную слабость (благодаря небольшой продолжительности действия препарата этот эффект исчезает быстро).
Эдрофоний** применяют также в качестве антагониста курареподобных средств антидеполяризующего типа действия.
Физостигмин - алкалоид калабарских бобов, произрастающих в Западной Африке, был первым антихолинэстеразным веществом, который стали применять в медицинской практике. Поскольку физостигмин по структуре является третичным амином и поэтому хорошо проникает через ГЭБ, его можно использовать как антидот при отравлении холиноблокаторами, проникающими в ЦНС (например, атропином). Растворы физостигмина иногда используют в глазной практике при глаукоме как миотическое средство, облегчающее отток внутриглазной жидкости.
Кроме того, физостигмин послужил прототипом для создания средств, используемых при лечении болезни Альцгеймера. Это заболе- вание характеризуется прогрессирующей потерей памяти и развитием слабоумия, что связывают с атрофией нейронов коры и подкорковых структур мозга, в том числе подкорковых холинергических нейронов. При этом отмечают снижение концентрации ацетилхолина в тканях мозга, что явилось основанием для использования антихолинэстеразных средств.
Сам физостигмин в настоящее время при болезни Альцгеймера не применяют по причине непродолжительного действия и выраженных побочных эффектов, связанных со стимуляцией периферических холинорецепторов. Препарат т а к р и н ** (когнекс**), ранее рекомендован- ный к применению при болезни Альцгеймера, в настоящее время имеет ограниченное использование, так как обладает многими побочными эффектами, наиболее серьезное из которых - нарушение функции печени.
Галантамин (реминил*), ривастигмин и донепе- з и л , применяемые при болезни Альцгеймера, имеют определенные преимущества. Эти вещества, в особенности ривастигмин, в меньшей степени ингибируют ацетилхолинэстеразу периферических тканей (скелетных мышц, внутренних органов), чем ацетилхолинэстеразу мозга, и поэтому вызывают менее выраженные побочные эффекты, связанные со стимуляцией периферических холинорецепторов. Кроме того, они не обладают характерной для такрина* гепатотоксичностью. Препараты оказывают продолжительное антихолинэстеразное действие (донепезил назначают 1 раз, а галантамин и ривастигмин - 2 раза в сутки). Курсовое применение этих препаратов способствует улучшению памяти (когнитивных функций) и частично снижает другие проявления болезни Альцгеймера. Среди побочных эффектов отмечают тошноту, рвоту, диарею, бессонницу.
Галантамин (нивалин*), кроме того, назначают при параличах скелетных мышц, связанных с нарушениями ЦНС, например при остаточных явлениях после перенесенного полиомиелита, при спастических формах церебрального паралича. Кроме того, препарат используют при атонии кишечника и мочевого пузыря, при миастении, вводят подкожно. Препарат также применяют как антагонист курареподобных средств антидеполяризующего конкурентного типа действия, вводят внутривенно.
При передозировке антихолинэстеразных средств обратимого действия применяют М-холиноблокаторы (например, атропин).
Антихолинэстеразные средства необратимого действия
К этой группе относятся фосфорорганические соединения (ФОС), которые ингибируют ацетилхолинэстеразу за счет образования ковалентных связей с эстеразным центром фермента. Эти связи очень прочные и гидролизуются очень медленно (в течение сотен часов). Поэтому ФОС ингибируют ацетилхолинэстеразу практически необратимо.
В медицинской практике ФОС применяют только местно, что связано с их высокой токсичностью. Препараты армин* и экотиоп а т ** могут быть использованы в качестве миотических средств для снижения внутриглазного давления при глаукоме. Экотиопат** - гидрофильное полярное соединение, плохо проникает через конъюнктиву и поэтому при его применении меньше опасность возникновения системных побочных эффектов. Продолжительность действия - около 4 сут. В отличие от других ФОС - устойчив в водном растворе.
В основном ФОС используют с немедицинскими целями: для уничтожения насекомых в качестве инсектицидов (карбофос, тиофос) и в сельском хозяйстве в качестве фунгицидов, гербицидов, дефолиантов. Некоторые ФОС используются как боевые отравляющие вещества (зоман). Поскольку ФОС обладают высокой липофильностью, они легко всасываются через неповрежденную кожу и слизистые оболочки, с поверхности легких и поэтому нередко бывают причиной отравлений.
При острых отравлениях ФОС наблюдают миоз (сужение зрачков), потливость, повышенную саливацию, спазм бронхов и повышение секреции бронхиальных желез, что проявляется ощущением удушья, брадикардию, сменяющуюся тахикардией, снижение АД (затем может быть повышение), рвоту, спастические боли в животе, диарею, психомоторное возбуждение. В более тяжелых случаях - подергивания мышц и судороги, резкое падение АД, коматозное состояние. Смерть наступает от паралича дыхательного центра.
При попадании ФОС на кожу и слизистые оболочки следует быстро вытереть кожу сухим ватным тампоном, и затем промыть 5-6% раствором натрия гидрокарбоната и теплой водой с мылом, а при введении внутрь - промыть желудок и дать адсорбирующие и слабительные средства. Если вещество всосалось в кровь, для ускорения его выведения применяют форсированный диурез. Используют также гемодиализ, гемосорбцию, перитонеальный диализ.
Поскольку основные симптомы острого отравления ФОС вызваны стимуляцией М-холинорецепторов, для их устранения применяют М-холиноблокаторы, чаще всего атропин, который вводят внутривенно в больших дозах (2-4 мл 0,1% раствора). Применяют также реактиваторы холинэстеразы - вещества, восстанавливающие активность фермента.
Реактиваторы холинэстеразы содержат в молекуле оксимную группу (-NOH), которая обладает высоким сродством к атому фосфора. Они взаимодействуют с остатками ФОС, связанными с ацетилхолинэстеразой, дефосфорилируют фермент и таким образом восстанавливают его активность. Реактиваторы холинэстеразы эффективны только в течение нескольких часов после отравления. Это связано с изменением химических связей между ацетилхолинэстеразой и остатками ФОС («старением» комплекса), в результате чего этот комплекс становится более устойчивым к действию реактиваторов.
В качестве реактиваторов холинэстеразы применяют т р и м е - доксим бромид (дипироксим*), аллоксим* и и з о - нитрозин*. Тримедоксим и аллоксим* относятся к четвертичным аммониевым соединениям, которые плохо проникают через ГЭБ. Изонитрозин* - третичный амин, хорошо проникает в ЦНС и устраняет не только периферические, но и центральные эффекты ФОС. Препараты используют в неотложной помощи в условиях стационара, вводят парентерально. Реактиваторы холинэстеразы не применяют при отравлениях антихолинэстеразными средствами обратимого действия.
8.2. СРЕДСТВА, БЛОКИРУЮЩИЕ ХОЛИНЕРГИЧЕСКИЕ СИНАПСЫ
К препаратам этой группы относят вещества, блокирующие М-холинорецепторы (М-холиноблокаторы), Н-холинорецепторы веге- тативных ганглиев (ганглиоблокаторы) и вещества, блокирующие Н-холинорецепторы скелетных мышц (курареподобные средства).
8.2.1. М-холиноблокаторы
М-холиноблокаторы блокируют М-холинорецепторы, локализованные на мембране клеток эффекторных органов, и таким образом препятствуют их взаимодействию с ацетилхолином. Поскольку М-холинорецепторы располагаются главным образом в органах и тканях, получающих парасимпатическую иннервацию, М-холиноблока-
торы, устраняя ее влияние, вызывают эффекты, противоположные эффектам возбуждения парасимпатической нервной системы. М-холиноблокаторы вызывают:
• расширение зрачков (мидриаз);
• паралич аккомодации (глаз устанавливается на дальнюю точку видения);
• повышение частоты сокращений сердца (тахикардия);
• повышение атриовентрикулярной проводимости;
• снижение тонуса гладких мышц бронхов;
• снижение тонуса и моторики ЖКТ и мочевого пузыря;
• уменьшение секреции бронхиальных и пищеварительных желез. Кроме того, М-холиноблокаторы устраняют влияние симпатической
системы на секрецию потовых желез, получающих симпатическую холинергическую иннервацию, и таким образом уменьшают их секрецию.
Среди М-холиноблокаторов выделяют вещества растительного происхождения и синтетические соединения.
К веществам растительного происхождения относятся алкалоиды тропанового ряда, полученные из растений семейства пасле- новых (Solanaceae): красавки (Atropa belladonna), белены (Hyosciamus niger), дурмана (Datura stramonium) и скополии (Scopolia carniolica). Главный алкалоид этих растений - L-гиосциамин, который при выделении превращается в рацемическую смесь L- и D-гиосциами- на - а т р о п и н . Атропин по химической структуре сложный эфир тропина и D-, L-троповой кислоты, относится к третичным аминам (липофильным неполярным соединениям), получен синтетическим путем. В тех же растениях содержится другой алкалоид с М-холиноблокирующей активностью - сложный эфир скопина и троповой кислоты скополамин (l-гиосцин). Из крестовника широколистного (Senecio platyphyllus) выделен алкалоид п л а т и ф и л л и н (производное метилпирролизидина).
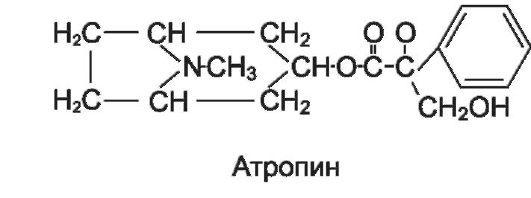
Атропин - наиболее известный М-холиноблокатор, поэтому другие препараты этой группы часто называют атропиноподобными средствами.
Атропин блокирует М1-, М2- и М3-подтипы холинорецепторов и устраняет влияние парасимпатической иннервации на многие органы и ткани. Поэтому он обладает широким спектром фармакологического действия.
Блокируя М3-холинорецепторы круговой мышцы радужной оболочки, атропин вызывает ее расслабление, вследствие чего происходит расширение зрачков (мидриаз). Он также вызывает расслабление ресничной (цилиарной) мышцы. Это приводит к натяжению цинновой связки, вследствие чего происходит уменьшение кривизны хрусталика (снижается его преломляющая способность) - глаз устанавливается на дальнюю точку видения. Такое состояние называют параличом аккомодации. При расширении зрачков и расслаблении цилиарной мышцы нарушается отток внутриглазной жидкости и у больных глаукомой может повыситься внутриглазное давление. Поэтому атропин и другие М-холиноблокаторы противопоказаны при глаукоме.
Атропин блокирует М2-холинорецепторы сердца и, устраняя тормозное влияние блуждающего нерва (вагуса) на синоатриальный узел, повышает его автоматизм, - возникает тахикардия. Так как атропин стимулирует центры блуждающего нерва в ЦНС, тахикардии может предшествовать кратковременная брадикардия (брадикардия возникает в основном при применении низких доз атропина). Уменьшение тормозного влияния вагуса на атриовентрикулярный узел приводит к повышению атриовентрикулярной проводимости.
Блокируя М3-холинорецепторы гладкомышечных клеток, атропин устраняет стимулирующее влияние парасимпатической иннервации на гладкие мышцы бронхов, желудка, кишечника, мочевого пузыря, желчевыводящих протоков и снижает их тонус и моторику ЖКТ. Атропин блокирует М3-холинорецепторы экзокринных желез (желез внешней секреции) и уменьшает секрецию бронхиальных, слюнных желез, желез желудка и поджелудочной железы, слезных, носоглоточных и потовых желез.
Атропин блокирует М1-холинорецепторы энтерохромаффиноподобных клеток желудка и таким образом уменьшает выделение гистамина, который стимулирует секрецию хлористоводородной кислоты париетальными клетками желудка. В результате секреция хлористоводородной кислоты снижается.
Атропин блокирует неиннервируемые М3-холинорецепторы эндотелия сосудов, но при этом не вызывает изменения тонуса сосудов.
Однако он препятствует взаимодействию рецепторов с М-холиномиметическими веществами и устраняет их сосудорасширяющее действие.
Многие из этих эффектов атропина (и других М-холиноблокаторов) используют в медицинской практике.
Способность атропина вызывать расширение зрачков используют в офтальмологии для исследования глазного дна, а также для лечения воспалительных заболеваний (ириты, иридоциклиты) и травм глаза, так как при расширении зрачка снижается опасность образования спаек между радужкой и капсулой хрусталика. Вызываемый атропином паралич аккомодации (циклоплегия) позволяет использовать его для определения истинной рефракции глаза (определение преломляющей способности хрусталика). После инсталляции в глаз 0,5-1% раствора атропина максимальное расширение зрачка наблюдают через 30-40 мин, паралич аккомодации - через 1-3 ч. Действие атропина на величину зрачков и аккомодацию сохраняется в течение 10-14 дней. Продолжительное расширение зрачков - преимущество атропина при лечении воспалительных заболеваний глаза. При длительном применении возможны местное раздражение, гиперемия и развитие конъюнктивита. Системные реакции при закапывании атропина в глаз (гипертермия, сухость во рту) чаще возникают у маленьких детей и лиц преклонного возраста.
В связи со способностью повышать атриовентрикулярную проводимость, атропин применяют при атриовентрикулярном блоке вагусного происхождения. Используют его также при синусовой брадикардии.
Так как атропин понижает тонус бронхов и уменьшает секрецию бронхиальных желез, его можно применять как бронхолитическое средство для купирования и предупреждения бронхоспазма. Однако в настоящее время с этой целью в основном используют другие М-холиноблокаторы: ипратропий, тиотропий и тровентол, которые вводят ингаляционно. Эти вещества - четвертичные аммониевые соединения. В отличие от атропина они плохо всасываются в кровь с поверхности легких (а также из кишечника при проглатывании) вследствие чего практически не вызывают системных побочных эффектов.
Эффект уменьшения секреции хлористоводородной кислоты париетальными клетками желудка позволяет использовать атропин и некоторые другие М-холиноблокаторы при язвенной болезни желудка и двенадцатиперстной кишки. Это действие атропина связано с блокадой нескольких подтипов М-холинорецепторов, в том числе М3-холинорецепторов париетальных клеток, секретирующих хлористоводородную кислоту, и М1-холинорецепторов
энтерохромаффиноподобных клеток желудка, которые выделяют гистамин (гистамин стимулирует секрецию хлористоводородной кислоты париетальными клетками). В настоящее время из препаратов этой группы при язвенной болезни желудка и двенадцатиперстной кишки в основном используют избирательный блокатор М1-холинорецепторов - п и р е н з е п и н . Пирензепин снижает секрецию хлористоводородной кислоты в меньшей степени, чем атропин, но в отличие от атропина практически не вызывает побочных эффектов, связанных с блокадой М2- и М3-холинорецепторов.
Атропин снижает тонус гладких мышц и обладает сильным спазмолитическим действием, поэтому он применяется при болезненных спазмах гладкомышечных органов (коликах): спазмах кишечника (кишечная колика), желчных протоков (печеночная колика); в меньшей степени атропин эффективен при почечной колике.
Атропин применяют в анестезиологии для премедикации перед хирургическими операциями, при этом атропин, блокируя М2-холинорецепторы сердца, предупреждает рефлекторную брадикардию и возможность рефлекторной остановки сердца. Полезной также является способность атропина уменьшать секрецию слюнных и бронхиальных желез.
Атропин используют как специфический антидот при отравлении М-холиномиметиками и антихолинэстеразными средствами.
Кроме того, атропин, проникая через ГЭБ, блокирует М-холинорецепторы экстрапирамидной системы и может уменьшать проявления болезни Паркинсона: тремор, ригидность, гипокинезию. В настоящее время в качестве противопаркинсонических средств используют центральные М-холиноблокаторы: тригексифенидил (циклодол*), бипериден (акинетон*), которые преимущественно блокируют М-холинорецепторы ЦНС и в отличие от атропина оказывают менее выраженные периферические побочные эффекты.
Применяют атропин в виде а т р о п и н а с у л ь ф а т а * внутрь, парентерально и местно в виде глазных лекарственных форм. Внутрь назначают за 30-40 мин до еды. Атропин хорошо всасывается из кишечника и быстро проникает в ЦНС (в течение 30-60 мин). Метаболизируется в печени путем гидролиза с образованием тропина и троповой кислоты.
составляет 2 ч. Выводится почками (около 30-50% в неизмененном виде). Продолжительность при введении внутрь составляет 4-6 ч. При применении атропина возникают следующие побочные эффекты, свя- занные с блокадой М-холинорецепторов в различных органах и тканях:
• сухость во рту вследствие снижения секреции слюнных желез;
• нарушение ближнего видения вследствие паралича аккомодации;
• повышение частоты сердечных сокращений (тахикардия);
• обстипация вследствие снижения тонуса и перистальтики ЖКТ и повышения тонуса сфинктеров;
• нарушение мочеиспускания вследствие снижения тонуса и моторики стенки мочевого пузыря и повышения тонуса сфинктера.
У больных глаукомой атропин вызывает повышение внутриглазного давления, поэтому он противопоказан при глаукоме. Вследствие задержки мочеиспускания атропин противопоказан при доброкачес- твенной гиперплазии предстательной железы.
В больших дозах атропин вызывает эффекты, связанные со стимулирующим действием на ЦНС: двигательное и психическое возбуждение, сильное беспокойство, нарушение памяти, координации. Эти эффекты возникают в основном при отравлении атропином. Кроме того, для отравления атропином характерны: расширение зрачков и ухудшение зрения, фотофобия (светобоязнь), сухость слизистых оболочек полости рта, носоглотки, что может привести к нарушению глотания и речи, сухость и покраснение кожи и повышение температуры тела (вследствие нарушения потоотделения и теплоотдачи, в основном бывает у детей), тахикардия, головная боль, головокружение, задержка мочеиспускания. В тяжелых случаях возникают зрительные и слуховые галлюцинации, бред, возможны судороги, которые сменяются состоянием угнетения и комой. Смерть наступает от паралича дыхательного центра. Частой причиной отравления, в особенности у детей, бывает употребление растений, содержащих атропин (красавка, дурман, белена). Для устранения эффектов атропина парентерально вводят антихолинэстеразные средства, проникающие в ЦНС (физос- тигмин). Другие меры при отравлении атропином состоят в промывании желудка и назначении солевых слабительных, энтеросорбентов (активированный уголь), танина* (можно крепкий чай); для удаления вещества из крови используют гемосорбцию, форсированный диурез. При сильном возбуждении применяют диазепам или барбитураты короткого действия. При необходимости - искусственное дыхание.
Препараты красавки (белладонны) содержат атропин. Применяют в виде настойки и экстрактов (сухой и густой) главным образом в качестве спазмолитических средств при болезненных спазмах гладких мышц ЖКТ, желчевыводящих протоков и других гладкомышечных органов.
Препараты красавки входят в состав таблеток «Бекарбон»*, «Бесалол»*, «Бепасал»*, «Беллалгин»*; свечей «Бетиол»*, «Анузол»*; «Капель Зеленина»* и др.
Скополамин (l-гиосцин) - алкалоид, который содержится в тех же растениях, что и атропин, по химической структуре близок к атропину (сложный эфир скопина и троповой кислоты). Скополамин вызывает эффекты, связанные с блокадой М-холинорецепторов как в периферических органах и тканях, так и в ЦНС (проникает через ГЭБ). Периферические эффекты скополамина сходны с эффектами атропина. В то же время центральные эффекты существенно различаются. Скополамин в отличие от атропина в терапевтических дозах оказывает выраженное угнетающее действие на ЦНС. Обычно это проявляется в виде общего успокоения, сонливости, возможна амнезия (ухудшение памяти). В токсических дозах скополамин подобно атропину может вызвать возбуждение ЦНС и коматозное состояние.
Применение скополамина в клинической практике во многом связано с особенностями его действия на ЦНС. Используют его способность угнетать вестибулярные центры при вестибулярных расстройствах, проявляющихся в виде головокружений, тошноты, рвоты, нарушения равновесия, а также для профилактики морской и воздушной болезни. Скополамин входит в состав таблеток «Аэрон»*, которые принимают перед полетом или морским путешествием, действие их продолжается 6 ч. Для обеспечения более длительного действия скополамина используют специальные трансдермальные терапевтические системы доставки, которые представляют собой накожные пластыри (приклеивают на здоровую кожу за ухом), выделяющие скополамин в течение 48-72 ч.
Скополамин (как и атропин) применяют для премедикации перед хирургическими операциями, чтобы предотвратить возникновение рефлекторной брадикардии и уменьшить секрецию слюнных и бронхиальных желез. При этом полезным также оказывается успокаивающее действие скополамина. Скополамин также, как и атропин, можно применять как спазмолитик при болезненных спазмах гладкомышечных органов (коликах). Выпускают в виде скополамина гидробромида. Как спазмолитическое средство при спазмах желудка, кишечника, желчевыводящих и мочевыводящих путей, а также в комплексной терапии синдрома раздраженного кишечника используют г и о с ц и - на бутилбромид (бускопан*). Кроме того, препарат применяют
в комплексной терапии язвы желудка и двенадцатиперстной кишки. В отличие от атропина и скополамина гиосцина бутилбромид - четвертичное аммониевое производное и поэтому плохо проникает через ГЭБ.
П л а т и ф и л л и н - алкалоид крестовника широколистного (Senecio platyphyllus), третичное аммониевое основание, хорошо всасывается в кишечнике и проникает через ГЭБ. По М-холиноблоки- рующему действию менее активен, чем атропин. Обладает прямым миотропным спазмолитическим действием (расслабляющее действие оказывает непосредственно на гладкие мышцы внутренних органов и кровеносных сосудов), вследствие чего расширяет сосуды и несколько снижает АД. Применяют платифиллин в виде платифиллина гидротартрата* при спазмах гладкомышечных органов (в частности, при почечной колике), язвенной болезни желудка и двенадцатиперстной кишки, спазмах сосудов головного мозга и периферических сосудов.
П и р е н з е п и н (гастроцепин) блокирует преимущественно М1-холинорецепторы, в связи с чем угнетает выделение гистамина энтерохромаффиноподобными клетками желудка. При этом снижается вызываемая гистамином секреция хлористоводородной кислоты париетальными клетками. Препарат применяют в качестве антисекреторного средства при лечении язвенной болезни желудка и двенадцатиперстной кишки (см. главу «Средства, влияющие на функции органов пищеварения»). Поскольку в средних терапевтических дозах пирензепин не блокирует М2- и М3-холинорецепторы, он практически не оказывает влияния на частоту сердечных сокращений, вели- чину зрачка и аккомодацию, тонус гладких мышц и перистальтику кишечника. При применении пирензепина несколько уменьшается секреция слюнных желез, в связи с чем возникает сухость во рту.
Толтеродин (детрузитол) блокирует М3-холинорецепторы и оказывает преимущественное спазмолитическое действие на гладкие мышцы мочевого пузыря, расслабляет детрузор и уменьшает его спонтанные сокращения. Преимущественное действие на мочевой пузырь (М-холиноблокирующее и прямое миотропное действие) оказывает также оксибутинин (дриптан). Оба препарата применяют при учащенном мочеиспускании, связанном с гиперреактивностью моче- вого пузыря.
И п р а т р о п и я б р о м и д (атровент) неизбирательно блокирует разные подтипы М-холинорецепторов (М1, М2, М3). Блокируя М3-холинорецепторы гладких мышц бронхов и бронхиальных желез, препарат оказывает выраженное бронхорасширяющее действие и снижает секрецию
желез. Последний эффект нежелателен, так как приводит к уменьшению объема и повышению вязкости мокроты, что затрудняет ее отделение. В связи с блокадой М2-холинорецепторов, расположенных на пресинаптической мембране холинергических нервных окончаний, усиливается выделение ацетилхолина, который конкурентно вытесняет ипратропий из связи с М3-холинорецептором бронхов. Это уменьшает как продолжительность действия препарата, так и выраженность его эффекта.
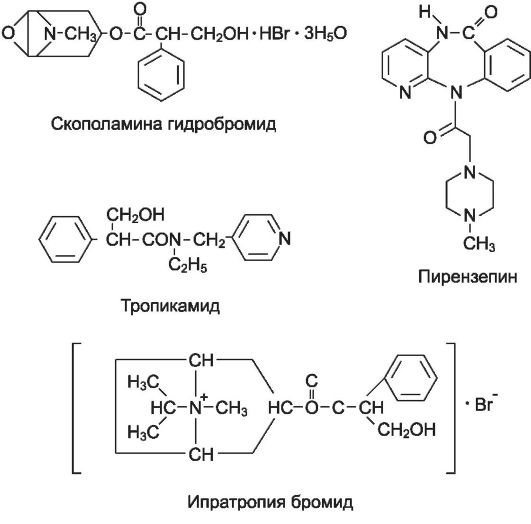
Применяют ипратропия бромид ингаляционно при обструктивных заболеваниях дыхательных путей (в том числе при бронхиальной астме). Максимальный эффект развивается через 30 мин после ингаляционного введения препарата и сохраняется и течение 5-6 ч. Ипратропий относится к четвертичным аммониевым соединениям и, будучи гидрофильным веществом, при ингаляционном введении плохо всасывается со слизистой оболочки дыхательных путей в кровь, а также из кишечника в случае проглатывания препарата, поэтому практически не оказывает системных побочных (атропиноподобных)
эффектов. В связи с уменьшением секреции слюнных и бронхиальных желез отмечается сухость во рту и повышение вязкости мокроты.
Тиотропия бромид (спирива) преимущественно блокирует М3-холинорецепторы дыхательных путей, а также M1-холино- рецепторы. Поскольку препарат не блокирует М2-холи норецепторы, локализованные на пресинаптической мембране нервных окончаний, он не повышает выделение ацетилхолина в синаптическую щель. Это благоприятно сказывается на активности препарата и продолжительности его действия (действует около 12 ч). Тиотропия бромид назначают ингаляционно 1 раз в сутки при хронической обструктивной болезни легких для предупреждения обострения заболевания. Эффект развивается медленнее, чем при применении ипратропия бромида. Тиотропия бромид - полярное гидрофильное соединение, плохо проникающее через мембраны клеток, поэтому при его применении системные побочные (атропиноподобные) эффекты выражены незначительно.
В офтальмологической практике применяют гоматропин, циклопентолат и тропикамид, которые оказывают менее продолжительное действие на глаз, чем атропин.
Тропикамид (мидриацил), блокируя М-холинорецепторы круговой мышцы радужки и цилиарной мышцы, вызывает мидриаз и паралич аккомодации (циклоплегия). Расширение зрачков наступает быстро: через 5-10 мин и продолжается до 6 ч. Паралич аккомодации отмечается через 20-40 мин и длится 1-2 ч. Применяют для исследования глазного дна. Непродолжительная циклоплегия в этом случае является преимуществом препарата. Тропикамид хорошо всасывается со слизистой оболочки слезного канала в кровь и может оказывать нежелательные системные эффекты: головную боль, тахикардию, фотофобию, сухость во рту, гипертермию (в особенности у детей).
Циклопентолат (цикломед) вызывает мидриаз и паралич аккомодации продолжительностью 20-24 ч. Его применяют для исследования рефракции у маленьких детей и непродолжительных диагностических исследований.
Гоматропин - синтетическое атропиноподобное вещество, сложный эфир тропина и миндальной кислоты, относится к третичным аминам. По фармакологическим свойствам близок к атропину, но отличается меньшей активностью и меньшей продолжительностью действия (15-20 ч). Его применяют в офтальмологической практике для расширения зрачков в виде гоматропина метилбромида.
Все М-холиноблокаторы противопоказаны при глаукоме.
8.2.2. Ганглиоблокаторы
Ганглиоблокаторы блокируют Н-холинорецепторы нейронов симпатических и парасимпатических ганглиев и таким образом нарушают передачу возбуждения с преганглионарных на постганглионарные волокна. В результате уменьшается или устраняется влияние как симпатической, так и парасимпатической иннервации на эффекторные органы и ткани. Кроме того, ганглиоблокаторы блокируют Н-холинорецепторы хромаффинных клеток мозгового вещества надпочечников, уменьшая выделение адреналина и норадреналина, а также Н-холинорецепторы каротидных клубочков, что препятствует рефлекторному возбуждению дыхательного и сосудодвигательного центров.
Блокада ганглиев симпатической системы приводит к уменьшению стимулирующего влияния симпатической системы на сердце и тонус сосудов (артерий и вен), при этом снижается ударный объем, расширяются артерии и вены - в результате снижается артериальное и венозное давление. Уменьшение выделения адреналина и норадреналина надпочечниками под влиянием ганглиоблокаторов также способствует снижению артериального и венозного давления.
Блокада ганглиев парасимпатической системы приводит к нарушению аккомодации (паралич аккомодации), учащению сокращений сердца (тахикардия), понижению тонуса гладких мышц ЖКТ и мочевого пузыря, угнетению секреции слюнных, бронхиальных желез, желез желудка и кишечника. В отличие от М-холиноблокаторов ганглиоблокаторы в меньшей степени расширяют зрачки и не оказывают существенного влияния на тонус бронхов.
В настоящее время в медицинской практике используют в основном гипотензивное действие ганглиоблокаторов. Препараты этой группы применяют для купирования гипертензивных кризов (быстрого снижения артериального давления), при отеке легких на фоне повышенного артериального давления, при спазме периферических артерий. Ганглиоблокаторы короткого действия можно использовать для управляемой гипотензии при хирургических операциях. Вещества вводят внутривенно капельно, при этом снижение артериального давления способствует уменьшению кровотечения из сосудов операционного поля, а при нейрохирургических операциях препятствует развитию отека мозга. Кроме того, таким образом можно уменьшить нежелательные рефлекторные реакции на сердце и сосуды, которые возникают во время операции.
Побочные эффекты ганглиоблокаторов в основном связаны с блокадой симпатических и парасимпатических ганглиев. Так, рас- ширение венозных сосудов, связанное с блокадой симпатических ганглиев, может быть причиной ортостатической гипотензии (резкого снижения давления крови при перемене положения тела из горизонтального в вертикальное). В результате может возникнуть обморок. Для предупреждения этого побочного эффекта после введения ганглиоблокатора больным рекомендуется лежать не менее 1,5-2 ч. К побочным эффектам ганглиоблокаторов, связанным с блокадой парасимпатических ганглиев, относятся мидриаз, паралич аккомодации, сухость во рту, тахикардия, снижение моторики кишечника и тонуса мочевого пузыря. Снижение моторики кишечника приводит к обстипации и даже может быть причиной паралитического илеуса (непроходимости кишечника), а снижение тонуса мочевого пузыря приводит к задержке мочеиспускания. При таких осложнениях вводят М-холиномиметические (ацеклидин) или антихолинэстеразные (неостигмин) средства. В связи с выраженными побочными эффектами ганглиоблокаторы не используют длительно.
При передозировке ганглиоблокаторов развивается гипотензия, для устранения которой применяют α-адреномиметики, повышающие артериальное давление. Показано применение аналептических средств, восстанавливающих дыхание.
Ганглиоблокаторы противопоказаны при выраженной гипотензии, гиповолемии и шоке, остром инфаркте миокарда, гиперплазии предстательной железы, почечной и печеночной недостаточности. Ганглиоблокаторы нельзя применять у больных с закрытоугольной глаукомой, так как в связи с расширением зрачков происходит ухудшение оттока жидкости из передней камеры глаза, что может привести к повышению внутриглазного давления. В связи с замедлением тока крови ганглиоблокаторы противопоказаны при повышенной склонности к тромбообразованию.
По химической структуре ганглиоблокаторы подразделяют на:
Бис-четвертичные аммониевые соединения: гексаметония бензосульфонат (бензогексоний*), азаметония бромид (пентамин*), трепирия йодид (гигроний*).
Сульфониевое соединение: триметафана камсилат (арфонад*).
Третичные амины: пемпидина тозилат (пирилен*), в настоящее время не используется.
Бис-четвертичные аммониевые соединения и сульфониевое соединение - гидрофильные полярные вещества, поэтому плохо вса- сываются из ЖКТ и не проникают через ГЭБ. Они различаются по длительности действия. Гексаметония бензосульфонат и азаметония бромид при внутримышечном и подкожном введении действуют 2-3 ч и в основном применяются для купирования гипертензивных кризов. Триметафан и гигроний* вызывают кратковременный эффект продолжительностью 10-20 мин. Поэтому эти препараты вводят внутривенно капельно для управляемой гипотензии. В настоящее время в связи с появлением более эффективных и безопасных гипотензивных средств ганглиоблокаторы используют редко.
Мекамиламин** - неполярное липофильное соединение (вторичный амин), легко проникает в ЦНС. Препарат может быть использован для облегчения отвыкания от курения (мекамиламин** устраняет вызываемую никотином эйфорию, вытесняя его из связи с Н-холинорецепторами мозга).
8.2.3. Средства, блокирующие нервно-мышечные синапсы
Средства, блокирующие нервно-мышечные синапсы, вызывают расслабление скелетных мышц (миорелаксацию) вследствие блокады передачи нервных импульсов с двигательных нервов на мышцы. Препараты этой группы называют также миорелаксантами периферического действия, в отличие от веществ, которые расслабляют скелетные мышцы, действуя на ЦНС (миорелаксанты центрального действия, см. бензодиазепины).
В зависимости от механизма нервно-мышечного блока выделяют миорелаксанты антидеполяризующего (недеполяризующего) дей- ствия и миорелаксанты деполяризующего действия.
Миорелаксанты антидеполяризующего действия
Вещества этой группы блокируют Н-холинорецепторы, локализованные на концевой пластинке скелетных мышц, и препятствуют их взаимодействию с ацетилхолином, в результате чего ацетилхолин не вызывает деполяризацию мембраны мышечных волокон - мышцы не сокращаются. Такое состояние называется нервно-мышечным блоком. Однако при повышении концентрации ацетилхолина в
синаптической щели (например, при применении антихолинэстеразных средств) ацетилхолин конкурентно вытесняет миорелаксант из связи с Н-холинорецептором и вызывает деполяризацию постсинаптической мембраны - происходит восстановление нервномышечной передачи. Вещества, действующие подобным образом, называются миорелаксантами антидеполяризующего конкурентного действия.
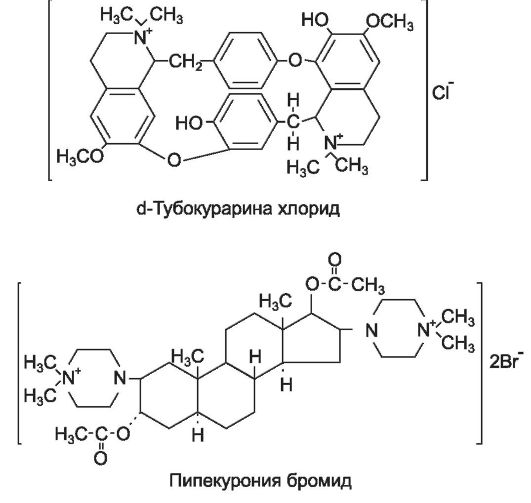
Первым препаратом этой группы был алкалоид тубокурари н * - основное действующее вещество стрельного яда кураре. В состав этого яда входят экстракты южноамериканских растений вида Strychnos и Chondodendron. Индейцы Южной Америки использовали кураре во время охоты на животных, смазывая им наконечники стрел. Кураре, попав в организм животного, вызывало паралич скелетных мышц, и животное теряло способность двигаться, но его мясо было пригодно к употреблению в пищу. Впоследствии было установлено, что по химической структуре тубокурарин* - четвертичное аммониевое соединение и не всасывается из ЖКТ.
Вещества, близкие тубокурарину* по действию, стали называть курареподобными средствами. Большинство курареподобных средств, так же как тубокурарин, относят к четвертичным аммониевым соединениям. В молекуле большинства веществ есть два положительно заряженных атома азота (катионные центры), которые и взаимодействуют с анионными структурами Н-холинорецепторов скелетных мышц, вызывая нервно-мышечный блок.
Антидеполяризующие миорелаксанты в основном относят к двум химическим группам:
• бензилизохинолины (тубокурарин*, атракурий**, цисатракурий**; мивакурий);
• аминостероиды (панкуроний**, пипекуроний, векуроний**, рокуроний **).
В зависимости от продолжительности вызываемого ими нервномышечного блока выделяют препараты: длительного действия (30-60 мин и более) - тубокурарин*, панкуроний**, пипекуроний (действует около 2 ч); средней продолжительности действия (20- 40 мин) - атракурий**, векуроний**, рокуроний**; короткого действия (10-15 мин) - мивакурий. Антидеполяризующие миорелаксанты действуют медленнее, чем деполяризующие; исключение составляет рокуроний**, который вызывает наиболее быстрый миопаралитический эффект (через 60-90 сек).
Продолжительность действия курареподобных средств в основном определяется характером их элиминации. Наиболее продолжительно действуют вещества, которые главным образом выделяются почками (пипекуроний). Вещества средней продолжительности действия в большей степени выделяются с желчью в неизмененном виде и в виде метаболитов (векуроний**, рокуроний**), или подвергаются спонтанному неферментативному гидролизу (элиминация Хоффмана) в плазме крови (атракурий**). Короткое действие мивакурия связано с тем, что он быстро разрушается холинэстеразой плазмы крови (псевдохолинэстераза). В связи с особым характером элиминации продолжительность действия атракурия не зависит от функционального состояния печени и почек (препарат может быть использован у больных с почечной и печеночной недостаточностью).
Курареподобные средства используются для расслабления скелетных мышц при хирургических операциях. Под действием курареподобных средств мышцы расслабляются в следующей последовательности: сначала мышцы лица, гортани, шеи, затем мышцы конечностей,
туловища и в последнюю очередь дыхательные мышцы - наступает остановка дыхания. При выключении дыхания больного переводят на искусственную вентиляцию легких.
Кроме того, курареподобные средства применяют для устранения тонических судорог при столбняке и при отравлении стрихнином. При этом расслабление скелетных мышц способствует устранению судорог.
Побочные эффекты большинства курареподобных средств из группы бензилизохинолинов (тубокурарин*, атракурий**, мивакурий) связаны главным образом с их способностью высвобождать гистамин. Это может быть причиной гипотензии, бронхоспазма, покраснения кожи, а также других анафилактоидных реакций. В большей степени высвобождению гистамина способствует тубокурарин*. Способность высвобождать гистамин практически отсутствует у цисатракурия и препаратов из группы аминостероидов, но некоторые из них (панку- роний**, рокуроний**) оказывают умеренное М-холиноблокирующее действие и поэтому могут вызвать тахикардию.
Поскольку тубокурарин* обладает выраженным гистаминогенным действием и, кроме того, в определенной степени блокирует Н-холинорецепторы симпатических ганглиев (вследствие чего при его применении возможно существенное снижение АД и существует опасность анафилактоидных реакций), в настоящее время его применяют редко.
Антагонистами миорелаксантов антидеполяризующего действия являются антихолинэстеразные средства. Угнетая активность ацетилхолинэстеразы, они предотвращают гидролиз ацетилхолина и таким образом увеличивают его концентрацию в синаптической щели. Ацетилхолин вытесняет препарат из связи с Н-холинорецепторами, что приводит к восстановлению нервно-мышечной передачи. Антихолинэстеразные средства (в частности, неостигмин) применяют для прерывания нервно-мышечного блока или устранения остаточных явлений после введения антидеполяризующих мышечных релаксантов. Для предотвращения эффектов неостигмина, вызываемых стимуляцией М-холинорецепторов, за 10 мин до неостигмина вводят атропин.
Миорелаксанты деполяризующего действия
С у к с а м е т о н и я х л о р и д (листенон*), с у к с а м е т о н и я й о д и д (дитилин*), суксаметония бромид.
По химической структуре суксаметоний представляет собой удвоенную молекулу ацетилхолина.
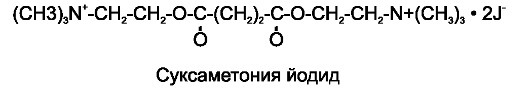
Суксаметоний взаимодействует с Н-холинорецепторами, локализованными на концевой пластинке скелетных мышц и подобно ацетилхолину вызывает деполяризацию постсинаптической мембраны. При этом мышечные волокна сокращаются, что проявляется в виде отдельных подергиваний скелетных мышц - фасцикуляций. Однако в отличие от ацетилхолина суксаметоний обладает устойчивостью к ацетилхолинэстеразе (он гидролизуется только холинэстеразой плазмы крови) и поэтому практически не разрушается в синаптической щели. В результате суксаметоний вызывает стойкую деполяризацию постсинаптической мембраны концевой пластинки скелетных мышц (деполяризационный блок). Это приводит к нарушению нервномышечной передачи и расслаблению скелетных мышц. При этом выделяющийся в синаптическую щель ацетилхолин лишь усиливает деполяризацию мембраны и углубляет нервно-мышечный блок.
По этой причине антихолинэстеразные средства не устраняют действие суксаметония. Более того, подавляя активность ацетилхо- линэстеразы, антихолинэстеразные средства повышают концентрацию ацетилхолина в синаптической щели, что поддерживает стойкую деполяризацию постсинаптической мембраны. Кроме того, ингибируя холинэстеразу плазмы крови, они препятствуют разрушению суксаметония, вследствие чего также усиливают и удлиняют его действие.
Суксаметоний применяют при интубации трахеи, эндоскопических процедурах (бронхо-, эзофаго-, цистоскопии), кратковременных операциях (наложение швов на брюшную стенку, вправление вывихов, репозиция костных отломков), для устранения тонических судорог при столбняке.
После внутривенного введения суксаметония его миопаралитическое действие начинается через 30-60 сек, и продолжается до 10 мин. Такое кратковременное действие препарата связано с его быстрым разрушением псевдохолинэстеразой (бутирилхолинэстеразой) плазмы крови (образуются холин и янтарная кислота). При генетической недостаточности этого фермента действие суксаметония может продолжаться до 2-6 ч. Миорелаксирующее действие препарата можно прекратить переливанием свежей цитратной крови, которая содержит активную псевдохолинэстеразу.
При частых повторных введениях суксаметония возможно развитие десенситизации Н-холинорецепторов концевой пластинки скелетных мышц, вследствие чего в ответ на введение препарата уже не возника- ет деполяризация мембраны и деполяризационный блок сменяется на антидеполяризационный. При таком характере нервно-мышечного блока антихолинэстеразные средства могут ослабить миопаралитическое действие суксаметония.
Побочные эффекты: послеоперационные мышечные боли (что объясняют микротравмами мышц во время их фасцикуляций), угнетение дыхания (апноэ), гиперкалиемия (выход ионов калия из скелетных мышц при стойкой деполяризации постсинаптической мембраны) и связанные с этим аритмии сердца, гипертензия (в связи со стимуляцией Н-холинорецепторов симпатических ганглиев при повторных введениях препарата), брадикардия и повышение секреции слюнных желез (М-холиномиметическое действие), повышение внутриглазного давления (тоническое сокращение под действием суксаметония экстраокулярных мышц затрудняет отток внутриглазной жидкости). Кроме того, возможны тяжелые осложнения: рабдомиолиз и миоглобинемия, а также злокачественная гипертермия, которая проявляется быстрым повышением температуры тела (до 41-42 градусов) и тоническим сокращением скелетных мышц, что связывают с повышенным выбросом ионов кальция из саркоплазматического ретикулума (для устранения этого эффекта вводят дантролен). Развитию злокачественной гипертермии при введении суксаметония способствует одновременное применение таких средств для наркоза, как галотан или изофлуран.
Суксаметоний противопоказан при глаукоме, нарушении функции печени, анемии, беременности, в грудном возрасте.
Сравнительные характеристики миорелаксантов антидеполяризующего и деполяризующего действия приведены в таблице 8-2.
Таблица 8-2
Сравнительные характеристики миорелаксантов антидеполяризующего и деполяризующего действия
Показатели | Антидеполяризующие миорелаксанты | Деполяризующие миорелаксанты |
Механизм развития нервно- мышечного блока | Блокада Н-холинорецепторов концевой пластинки скелетных мышц, устранение вызываемой ацетилхолином деполяризации постсинаптической мембраны | Стимуляция Н-холинорецепторов концевой пластинки скелетных мышц, стойкая деполяризация постсинаптической мембраны |
Окончание таблицы 8-2
Показатели | Антидеполяризующие миорелаксанты | Деполяризующие миорелаксанты |
Фазы действия | Фаза миорелаксации | Фаза мышечной фасцикуляции; Фаза миорелаксации |
Влияние антихолинэстераз- ных средств | Устранение нервно-мышечного блока | Усиление и удлинение нервно-мышечного блока |
8.2.4. Средства, уменьшающие выделение ацетилхолина
Ботулинический токсин А препятствует выделению ацетилхолина из окончаний холинергических нервных волокон.
Ботулинический токсин состоит из двух пептидных цепей (тяжелой и легкой, различающихся молекулярной массой), объединенных дисульфидным мостиком. Тяжелая цепь ботулинического токсина обладает способностью связываться со специфическими рецепторами мембран нервных клеток. После связывания с пресинаптической мембраной нервного окончания ботулинический токсин путем эндоцитоза проникает внутрь нейрона. По некоторым данным, легкая цепь токсина обладает протеазной активностью, вызывая протеолиз белков пресинаптической мембраны (SNAP-25, синтаксин) и везику- лярной мембраны (синаптобревин). При взаимодействии этих белков происходит процесс слияния мембран. В результате энзиматического расщепления белков слияние мембраны везикул с пресинаптической мембраной нарушается и не происходит высвобождения ацетилхолина в синаптическую щель (см. рис. 8-1).
Вследствие уменьшения выделения ацетилхолина в нервномышечных синапсах, развивается паралич скелетных мышц. Кроме того, нарушается передача нервных импульсов в других холинергических синапсах, в том числе с симпатических холинергических волокон, иннервирующих потовые железы.
Ботулинический токсин типа А выпускается в виде комплекса с гемагглютинином в форме лиофилизированного порошка для инъек- ций (препараты ботокс*, диспорт*). Препараты применяют в офтальмологии при блефароспазме, для лечения косоглазия, а также для лечения других спастических состояний, включая локальный мышечный спазм у взрослых и детей старше 2 лет. Вводят внутримышечно.
Действие продолжается 4-6 мес. Длительное действие препаратов объясняется тем, что мышечные сокращения восстанавливаются только вследствие процесса реиннервации (появления боковых отростков нервных окончаний).
Вследствие того, что ботулинический токсин* препятствует выделению ацетилхолина окончаниями симпатических холинергических волокон, иннервирующих потовые железы, препараты применяют при гипергидрозе для уменьшения секреции апокринных потовых желез (подмышечные впадины, ладони, стопы). Вводят внутрикожно, эффект продолжается 6-8 мес.
Ботулинический токсин концентрируется в месте инъекции в течение некоторого времени, а затем попадает в системный кровоток, не проникает через ГЭБ и быстро метаболизируется.
В качестве побочных эффектов отмечаются боль и микрогематомы в месте инъекции, незначительная общая слабость в течение 1 нед (при применении больших доз), в зависимости от места введения возможны птоз, слезотечение или дисфагия. У некоторых пациентов при применении препаратов появляются антитела к комплексу гемагглютинин - ботулинический токсин. Этому способствует введение препаратов в высоких дозах. Препараты ботулинического токсина*противопоказаны при миастении, беремен- ности, лактации.