Нормальная физиология: учебник / Орлов Р.С., Ноздрачев А.Д. - 2-е изд., исправл. и доп. 2010. - 832 с.
|
|
|
|
ГЛАВА 26. ФИЗИОЛОГИЯ ПОЧЕК И МОЧЕВЫДЕЛИТЕЛЬНОЙ СИСТЕМЫ
Почки (рис. 26-1) выполняют три основные группы функций: мочеобразовательную, гомеостатическую и эндокринную.
• Мочеобразовательная функция. Почки
экскретируют из организма конечные продукты обмена, посторонние
вещества и избыточные соединения. Оттекающие ежесуточно от почек
Почки выполняют много важных функций
• Регулируют осмотическое давление (осмоляльность) жидкостей организма.
• Регулируют концентрацию большого количества ионов в плазме крови, включая Na+, K+, Mg2+, Ca2+, Cl-, бикарбонаты, фосфаты и сульфаты.
• Играют исключительную роль в кислотно-щелочном равновесии, экскретируя H+, когда имеется избыток кислот, или HCO3, когда много оснований.
• Регулируют объём экстраклеточной жидкости, контролируя экскрецию воды и натрия.
• Помогают регулировать артериальное кровяное давление, подстраивая экскрецию Na+ и выделяя различные вещества (например, ренин), которые могут влиять на АД.
• Удаляют конечные продукты метаболизма, включая мочевину, мочевую кислоту и креатинин.
• Удаляют многие вещества (например, пенициллин), а также чужеродные или токсичные соединения.
• Являются местом выработки ряда гормонов, включая эритропоэтин и 1,25-дигидрооксивитамин D3.
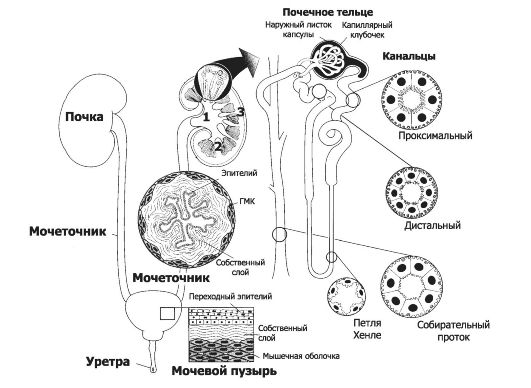
Рис. 26-1. Мочевыделительная система. Слева: почки, мочеточники, мочевой пузырь, мочеиспускательный канал (уретра). В составе правой почки: 1 - почечная лоханка, 2 - мозговое вещество почки, 3 - корковое вещество почки. Справа: в составе почечного тельца - капиллярный клубочек (кровь в клубочек вливается из приносящей артериолы, оттекает по вы- носящей артериоле), наружный листок эпителиальной капсулы Боумена- Шумлянского [внутренний листок эпителиальной капсулы представлен подоцитами (не изображены, см. рис. 26-9 и 26-10); кровь из просвета капилляров фильтруется в полость эпителиальной капсулы, фильтрат - первичная моча], канальцы нефрона и собирательные трубочки - почечные канальцы, по которым от почечного тельца оттекает первичная моча. В канальцах происходят реабсорбция и секреция, в результате образуется окончательная (вторичная) моча, поступающая в почечную лоханку [16].
Расщепляют некоторые полипептидные гормоны, включая инсулин, глюкагон и паратиреоидный гормон. Синтезируют аммиак, участвующий в КЩР. Синтезируют вещества, воздействующие на почечный кровоток и экскрецию Na+, включая дериваты арахидоновой кисло-
ты (простагландины, тромбоксан A2) и калликреин (протеолитический фермент, участвующий в синтезе кининов).
Фильтрация, реабсорбция, секреция и внутрипочечный метаболизм
Мочевыделительная и гомеостатическая функции почек - результат четырёх сопряжённых и последовательных процессов: фильтрации, канальцевого транспорта (реабсорбция и секреция), а также внутрипочечного метаболизма. Эти базовые процессы раз- вёртываются между кровеносными капиллярами почек и просветом почечных канальцев.
• Клубочковая фильтрация (ультрафильтрация,
рис. 26-2) происходит в почечных тельцах из просвета капилляров
клубочка (первичная капиллярная сеть) в просвет эпителиальной капсулы и
обусловливает образование первичной мочи. Каждые сутки обе почки
взрослого человека образуют около
• Канальцевая реабсорбция (рис.
26-2, 26-4) происходит из просвета почечных канальцев в интерстиций и
далее в просвет кровеносных капилляров вторичной капиллярной сети
(перитубулярные капилляры). Суточный объём реабсорбции равен примерно
• Канальцевая секреция. Эпителиальные клетки почечных канальцев выделяют в ультрафильтрат ряд химических соединений, поступающих из внеклеточного вещества и перитубулярных капилляров или образующихся в самих эпителиальных клетках канальцев.
Почечный кровоток
• Ток крови. Через
почечные артерии при каждом сокращении сердца почки получают не менее
20% сердечного выброса, т.е. около 1200 мл крови в минуту (350 мл/мин на
• Почечный ток плазмы крови (именно плазма крови после клубочковой фильтрации образует первичную мочу) составляет примерно 600-700 мл/мин (при значении Ht - гематокрита - 0,4):
Почечный ток плазмы крови = (1 - Ht) х (почечный кровоток) 600-700 мл/мин = 0,4 х1000 мл/мин.
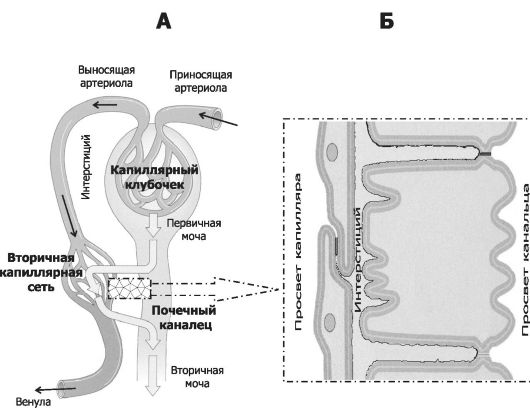
Рис. 26-2. Пути фильтрации, реабсорбции и секреции. А - капиллярный клубочек почечного тельца (первичная капиллярная сеть) перфузируется артериальной кровью из приносящих артериол. После фильтрации кровь оттекает от почечного тельца по выносящей артериоле. В интерстиции (между канальцами) выносящая артериола образует вторичную капиллярную сеть (перитубулярные капилляры), питающую паренхиму органа. В перитубулярные капилляры из просвета канальцев осуществляется реабсорбция, а из просвета капилляров в просвет канальцев - секреция. В результате из ультрафильтрата (первичная моча) образуется дефини- тивная моча. Выделенный прямоугольником участок схематически представлен на рис. Б.
• Первичная капиллярная сеть. От междольковых артерий параллельно поверхности органа ответвляются короткие приносящие (внутридольковые) артериолы; они распадаются на капилляры, формирующие клубочек в составе почечного тельца, - первичная капиллярная сеть (рис. 26-2, А). Клубочки первичной капиллярной сети входят в состав почечных телец, в которых происходят фильтрация плазмы и образование клубочкового фильтрата (ультрафильтрата, первичной мочи). Выносящая артериола собирает кровь из капилляров клубочка.
Φ Оттекающая от почечных телец кровь - артериальная: в выносящей артериоле содержание кислорода лишь примерно на 7% ниже, чем в приносящей артериоле.
Φ В просвете капилляров первичной капиллярной сети гидростатическое давление составляет примерно
Φ Фильтрация в почечных тельцах (см. рис. 26-2) происходит из просвета капилляров первичной капиллярной сети в полость капсулы Боумена-Шумлянского, движущая сила - Эффективное фильтрационное давление:
(Гидростатическое давление) - (Онкотическое давление) - (Давление в полости эпителиальной капсулы) = (
• Вторичная капиллярная сеть. В капилляры вторичной сети кровь поступает из первичной капиллярной сети через выносящие артериолы. Эти артериолы переходят в прямые артериальные сосуды, спускающиеся в мозговое вещество, образующие вторичную капиллярную сеть (перитубулярные капилляры) и направляющиеся в виде прямых венозных сосудов к корковому веществу. Эти сосуды (и артериальные, и венозные) проходят параллельно канальцам нефронов (канальцы петли Генле) и собирательным трубочкам, отчего и получили название vasa rectae. Капилляры перитубулярной сети располагаются в непосредственной близости от канальцев нефронов; в эти капилляры реабсорбируются вещества из просвета канальцев (см. рис. 26-2, 26-4). Из вторичной капиллярной сети также питаются ткани почки. Капилляры мозгового вещества переходят в прямые венулы, впадающие в дуговые вены. Φ Значительное содержание кислорода в капиллярах вторичной капиллярной сети эффективно обеспечивает активную реабсорбцию (см. рис. 26-2, 26-4) из просвета канальцев в просвет кровеносных капилляров. Кислород необходим главным образом для того, чтобы обеспечить работу Na+-, К+-АТФазы, вмонтированной в плазматическую мембрану эпителиальных клеток почечных канальцев. Φ Реабсорбцию поддерживает возросшее в результате фильтрации (по сравнению с капиллярами первичной капилляр-
ной сети) онкотическое давление в капиллярах вторичной капиллярной сети.
Итак, первичная капиллярная сеть, расположенная между артериолами, характеризуется высоким гидростатическим внутрикапиллярным давлением и теряет в результате фильтрации не менее 10% объёма крови и до 20% объёма плазмы. Вторичная капиллярная сеть имеет низкое гидростатическое внутрикапиллярное давление, способствующее эффективной реабсорбции из почечных канальцев (см. подробнее на рис. 26-4, Б). Таким образом, вся поступающая в почку артериальная кровь сначала перфузирует капилляры первичной капиллярной сети и лишь затем артериальная кровь поступает в капилляры вторичной капиллярной сети.
Кровоток в корковом веществе почки выше, чем в мозговом. В коре почки кровоток в среднем составляет 4-5 мл/мин на
Паренхима почки
• Паренхима каждой почки, подразделяемая на корковое и мозговое вещество, состоит из 0,8-1,2 млн функциональных структурных единиц - нефронов, а также из множества собирательных трубочек коркового и собирательных протоков мозгового вещества. В совокупности все трубочки почки (канальцы нефрона, собирательные трубочки и протоки) именуются почечными канальцами. Нефрон - эпителиальная трубка, начинающаяся от почечного тельца и впадающая в собирательную трубку. Стенка нефрона построена из однослойного эпителия, клетки которого (в зависимости от выполняемой функции) различны в разных отделах нефрона (рис. 26-5, А). По длине нефрона (рис. 26-3) различают проксимальный каналец (извитой и прямой) - тонкий каналец петли Генле - восходящую (толстая) часть петли Генле (эту часть называют также прямым дистальным канальцем) - извитой дистальный каналец. Дистальный прямой каналец (толстая часть петли Генле) возвращается к собственному почечному тельцу и контактирует с ним. Извитой дистальный каналец через связующий отдел впадает в собирательную трубочку, которая, в свою очередь, поступает в
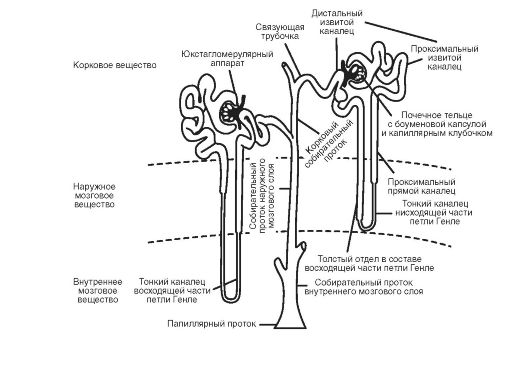
Рис. 26-3. Компоненты нефрона и системы собирательных протоков.
собирательные протоки. Разные отделы нефрона расположены либо в корковом, либо в мозговом веществе. Типы нефронов. Различают два основных типа нефронов (см. рис. 26-3) - кортикальные (все отделы нефрона расположены в корковом веществе, 85% всех нефронов - кортикальные) и юкстамедуллярные (петля Генле этих нефронов глубоко проникает в мозговое вещество почки).
Отделы почечных канальцев. В нефроне различают несколько отделов (см. рис. 26-3): капсулу почечного тельца, окружающую капиллярный клубочек; проксимальный извитой и проксимальный прямой канальцы, тонкий каналец (в составе нисходящей и восходящей частей петли Генле); толстый отдел в составе восходящей части петли Генле (дистальный прямой каналец), дистальный извитой каналец, а также связующий отдел (соединяет дистальный отдел нефрона с собирательной
трубочкой). Собирательные трубки, сливаясь, образуют собирательные протоки. Характерная особенность всех почечных канальцев состоит в том, что между соседними клетками всегда существуют диффузионные барьеры в виде полосок плотных контактов, окружающих верхушечные части клеток. Количество таких полосок плотных контактов увеличивается по мере продвижения по почечным канальцам, соответственно увеличивается электрическое сопротивление пласта эпителия, но уменьшается его проницаемость.
Ф Проксимальный каналец подразделяют на извитой и прямой отделы. Именно в проксимальном отделе нефрона происходит основной объём реабсорбции (рис. 26-4). В связи с этим обстоятельством клетки канальца имеют ряд особенностей, значительно увеличивающих площадь реабсорбции. Интенсивность реабсорбции постепенно уменьшается по мере продвижения первичной мочи по канальцу, соответственно уменьшается количество приспособлений, увеличивающих поверхность клеток, а также митохондрий, необ- ходимых для обеспечения транспортных процессов. По этой причине с функциональной точки зрения (интенсивность реабсорбции) проксимальный каналец подразделяют на последовательные сегменты - S1, S2 и S3. Между соседними клетками встречаются щелевые контакты. Основная функция проксимального канальца - осмос воды, реабсорбция NaCl, NaHCO3, глюкозы, аминокислот, Ca2+, HPO42-, SO42-, HCO3-, а также секреция NH4+ и некоторых органических катионов и анионов.
Ф Тонкий каналец петли Генле состоит из плоских эпителиальных клеток, что существенно уменьшает диффузионный путь для воды. Длина тонкого канальца невелика в кортикальных, но значительна в юкстамедуллярных нефронах. Эти последние (точнее, их петля Генле), составляя всего 15% от общего количества нефронов, крайне важны для концентрирования или разведения мочи. Клетки петли Генле перекачивают NaCl из просвета канальцев в интерстиций, который в результате становится гипертоничным, формируя в мозговом веществе осмотический градиент между корой и почечными сосочками, что имеет решающее значение для осмотической диффузии воды между почечными канальцами и интерстицием.
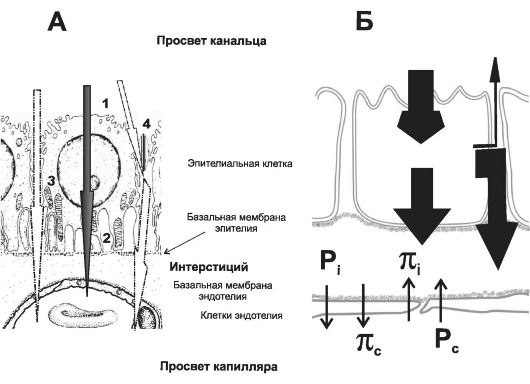
Рис. 26-4. Реабсорбция в проксимальном канальце. Сверху вниз просвет канальца, кубические клетки стенки канальца, интерстиций, перитубулярный капилляр. Стрелки указывают направление и пути перемещения ионов и молекул. А: сплошная - трансклеточный перенос, прерывистая - парацеллюлярный перенос, прерывистые стрелки - комбинированный вариант переноса (подробнее см. в разделе «Трансклеточная проницаемость» гл. 4, в том числе рис. 4-9). 1 - микроворсинки на поверхности эпителиальной клетки, 2 - глубокие впячивания в базальной части эпителиальных клеток, а также переплетающиеся между собой отростки боковых поверхностей соседних клеток значительно увеличивают поверхность реабсорбции, 3 - митохондрии в базальной и латеральной части эпителиальных клеток необходимы, чтобы обеспечить энергопотребности при реабсорбции, 4 - плотные контакты между клетками каналь- ца перекрывают неспецифические пути диффузии. В верхушечной части клеток в значительном числе находятся содержащие белок эндоцитозные пузырьки, а также лизосомы; Б - в верхней части (эпителиальная клетка) сплошными стрелками показаны трансклеточный, парацеллюлярный и комбинированный пути переноса. Обратите внимание на направленную кверху (в просвет канальца) тонкую стрелку («утечка» ионов из межклеточного пространства в просвет канальца). В нижней половине рисунка представлены движущие силы транспорта через стенку перитубулярного кровеносного капилляра (параметры: P - гидростатическое давление, π - онкотическое давление; индексы: i - интерстиций, c - капилляр).
Ф Толстый отдел петли Генле. Эпителиальные клетки имеют кубическую форму, сильные впячивания плазмолеммы по базальной и латеральной поверхности клеток, что значительно увеличивает поверхность обмена. Это обстоятельство в сочетании с встроенными в плазмолемму клеток ха- рактерными трансмембранными переносчиками (см. ниже) весьма важно для формирования гиперосмотической среды. Стенка канальца непроницаема для мочевины и воды.
Ф Дистальный каналец начинается от плотного пятна (здесь происходит регистрация параметров канальцевой жидкости, подробнее см. ниже) и по своей структуре напоминает клетки толстого отдела петли Генле.
Ф Связующий отдел и собирательные трубочки. Их стенка состоит из главных и вставочных клеток. Клетки связующего отдела синтезируют и секретируют калликреин.
♦ Главные клетки несут на свободной поверхности ресничку. Их основная функция - реабсорбция Na+ и Cl- и секреция K+.
♦ Вставочные клетки подразделяются на подтипы A (α) и B (β). Эти клетки реабсорбируют K+. Кроме того, α-клетки секретируют H+, а β-клетки - HCO3-.
Ф Собирательные протоки. По мере увеличения калибра протоков эпителий становится высоким цилиндрическим, а количество вставочных клеток уменьшается. Собирательные протоки (как и собирательные трубочки) принимают участие в транспорте электролитов, а также под влиянием альдостерона и АДГ - в транспорте воды и мочевины.
Оценка экскреторной функции почек
Для клинической оценки экскреторной функции почек, складывающейся из клубочковой фильтрации, канальцевой реабсорбции и канальцевой секреции, применяют методы визуализации и измерение почечного клиренса (от англ. clearance - очищение).
Клиренс
Клиренс вещества X (CX) - параметр, характеризующий выведение почками (экскрецию) из организма вещества X. Клиренс выражают в объёмных единицах за единицу времени (например, в мл/мин). Другими словами, клиренс вещества X - скорость его
экскреции, отнесённая к виртуальному объёму крови, полностью очищенной от вещества X.
• Для разных веществ значение клиренса (CX) различно. Так, для глюкозы, в норме не экскретируемой, CX равно 0. В то же время для парааминогиппурата, полностью удаляемого из крови, значение CX составляет 700 мл/мин, т.е. равно току плазмы крови через почку.
• Клиренс инулина. Некоторые вещества (например, инулин - полимер фруктозы, Mr 5000), как и парааминогиппурат, свободно фильтруются, но не реабсорбируются и не секретируются в канальцах. Такие вещества являются хорошим маркёром важного параметра мочевыделительной функции почек - скорости клубочковой фильтрации.
Скорость клубочковой фильтрации (СКФ), - объём плазмы крови, фильтруемой в единицу времени из крови в полость капсулы Боумена-Шумлянского (PX хСКФ).
• Для оценки почечного клиренса и СКФ применяют инулин, креатинин, маннитол, 1251-йоталамат, 57Co- или 58Co- цианокобаламин, 51Cr-этилендиаминтетрауксусную кислоту. Все эти маркёры экзогенны и требуют (в отличие от креатинина) их введения в сосудистое русло обследуемого.
Экскреция
Экскреторную функцию почки по отношению к веществу X (UXxV - скорость экскреции вещества X с мочой) определяют три фактора: скорости клубочковой фильтрации (СКФ), канальцевых реабсорбции и секреции. Эти процессы в общем виде можно записать следующим образом:
Экскреция = Фильтрация - Реабсорбция + Секреция.
• Экскретируемая фракция вещества X - полезный показатель, помогающий оценить функциональное состояние почек: отношение скорости экскреции вещества X (UXxV ) к объёму клубочковой фильтрации (PX х СКФ).
ФИЛЬТРАЦИЯ
Через фильтрационный барьер почечного тельца (рис. 26-
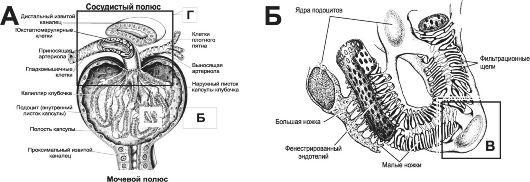
Рис. 26-5. Почечное тельце, фильтрационный барьер и околоклубочный комплекс [11]. А - почечное тельце состоит из капиллярного клубочка (примерно 50 капиллярных петель) и эпителиальной капсулы. Область, где в тельце входит приносящая и выходит выносящая артериола, называют сосудистым полюсом; область отхождения проксимального извитого канальца нефрона - мочевой полюс тельца. Эпителиальная капсула состоит из двух листков: наружного (париетальный) и внутреннего (висцеральный). Между листками имеется полость, куда из просвета кровеносных капилляров поступает клубочковый фильтрат. Полость капсулы открывается в проксимальный извитый каналец. Наружный листок капсулы, состоящий из однослойного плоского эпителия, ограничивает капсулярное пространство снаружи. Клетки внутреннего листка капсулы (подоциты) прикреплены к наружной поверхности капилляров клубочка и вместе с эндотелием и базальной мембраной, общей для капилляра и подоцитов, участвуют в процессе фильтрации. К сосудистому полюсу подходит дистальный извитый каналец того же самого нефрона, что начинается на мочевом полюсе почечного тельца. Видоизменённые клетки этого отдела нефрона (плотное пятно) вместе с видоизменёнными клетками приносящей артериолы (юкстагломерулярные клетки) образуют так называемый околоклубочковый комплекс. В состав почечного тельца и околоклубочкового комплекса также входят мезангиалъные клетки, расположенные между капиллярными петлями клубочка; Б - подоциты - видоизменённые эпителиальные клетки внутреннего листка капсулы. Они образуют большие ножки, от которых отходят многочисленные нитевидные малые ножки. Эндотелиальные клетки капилляров клубочка имеют многочисленные фенестры. Между внутренним листком капсулы и эндотелием капилляров формируется общая (трёхслойная) базальная мембрана.
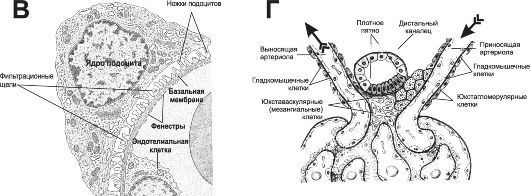
Рис. 26-5. Окончание. В - фильтрационные щели. Малые ножки подоцитов прикрепляются к базальной мембране. Между ножками подоцитов имеются узкие (30-40 нм) фильтрационные щели. Фильтрация плазмы осуществляется через волокнистую основу базальной мембраны и фильтрационные щели; Г - околоклубочковый комплекс образован тремя типами клеток, расположенных у корня клубочка. Первый тип - юкстагломерулярные (зернистые) клетки - видоизменённые ГМК средней оболочки приносящей артериолы, содержащие гранулы ренина. Второй тип - юкставаскулярные клетки (мезангиальные), расположенные между приносящей и выносящей артериолами. Третий тип - эпителиальные клетки дистального канальца в месте его контакта с корнем клубочка (клетки плотного пятна).
Фильтрационный барьер
Фильтрационньгй барьер (рис. 26-5, Б, В) состоит из эндотелия капилляров, базальной мембраны и фильтрационных щелей между ножками подоцитов.
• Эндотелиальные клетки капилляров максимально уплощены, за исключением области, содержащей ядро. Уплощённая часть клетки содержит не затянутые диафрагмой фенестры (овальные окна) полигональной формы диаметром 70 нм, суммарно занимающие примерно 30% всей поверхности эндотелия. В результате плазма крови непосредственно контактирует с базальной мембраной. Таким образом, эндотелиальная часть фильтра задерживает только клеточные элементы, но не плазму крови.
• Базальная мембрана толщиной до 300 нм формируется за счёт синтетической активности подоцитов и мезангиальных клеток. Основу базальной мембраны составляет мелкоячеистая сеть, образованная молекулами коллагена типа IV, ламинина и связывающего их сульфатированного гликопротеина энтактина. Отрицательно заряженные цепи гепарансульфата, входящие в состав протеогликанов базальной мембраны, препятствуют прохождению сквозь неё анионов, в том числе и анионных белков плазмы. Вещества с Mr <1 кД проходят через базальную мембрану свободно, <10 кД - в ограниченном количестве, а >50 кД - в ничтожных количествах.
• Фильтрационные щели образованы лабиринтом щелевидных пространств между малыми ножками подоцитов. Фильтрационные щели имеют ширину около 25 нм и затянуты щелевыми диафрагмами (сеть с ячейками размерами 4-14 нм). Щелевые диафрагмы содержат отрицательно заряженные гликопротеины, белок нефрин, а в участках соединения диафрагм с плазмолеммой ножек подоцитов содержится белок плотных контактов. Ножки подоцитов (за счёт актиновых микрофиламентов) в широких пределах изменяют свою толщину, что неизбежно сказывается на ширине фильтрационных щелей.
Параметры фильтрации
Клубочковую фильтрацию характеризуют различные параметры: объём фильтрата, скорость клубочковой фильтрации (СКФ), эффективное фильтрационное давление, показатель фильтруемо-
сти, разности осмотического давления между просветом капилляра и полостью эпителиальной капсулы, характер фильтруемых ионов и молекул.
• Объём первичной
мочи (отфильтрованной плазмы крови) составляет 10% объёма крови (20%
объёма плазмы), протекающей по капиллярам клубочка (для взрослого
человека 10% от
• СКФ определяют из уравнения:
СКФ = Kf xPUF
где Kf - коэффициент фильтрации, а PUF - эффективное фильтрационное давление.
Φ Коэффициент фильтрации (Kf) зависит от гидравлической проводимости клубочковых капилляров и площади филь- трации. При СКФ 125 мл/мин и PUF
♦ Увеличение значения Kf повышает СКФ.
♦ Уменьшение значения Kf понижает СКФ. Φ Эффективное фильтрационное давление (PUF, силы Старлин-
га, или движущая сила фильтрации):

Показатель фильтруемости (UFX/ Px) - отношение концентра- ции вещества X в ультрафильтрате к концентрации вещества X в плазме крови - зависит от молекулярной массы и эффективного молекулярного радиуса вещества X.
Φ UFX/PX <1. Вещества с малой молекулярной массой (<5,5 кД) и небольшим эффективным молекулярным радиусом (вода, мочевина, глюкоза, инулин), как правило, имеют в фильтрате ту же концентрацию, что и в плазме крови.
Φ UFX/PX <1. С увеличением молекулярной массы веществ их концентрация в фильтрате прогрессивно уменьшается (например, в ультрафильтрате обнаруживаются лишь сле- ды сывороточного альбумина). Тем не менее показатель фильтруемости для лизоцима, миоглобина, лактоглобулина и массы других белков с молекулярной массой менее 30 кД достаточен для появления в фильтрате ощутимых их коли- честв.
• Электрический заряд. Поскольку ячейки сети в базальной мембране и фильтрационные щели несут отрицательный заряд, это обстоятельство ограничивает фильтрацию анионов и способствует фильтрации катионов. Однако при этом существенное значение имеют величины молекулярной массы и радиуса заряженных веществ. Состав клубочкового фильтрата. В результате фильтрации состав первичной мочи оказывается близким к составу плазмы, но в ультрафильтрате нет клеточных элементов крови и относительно мало белка. В частности, в первичной моче отсутствуют макромолекулы, эффективный радиус которых превышает 4 нм.
Регуляция почечного кровотока и фильтрации
Имеющие чрезвычайно важное значение для адекватного выполнения функций почек параметры почечного кровотока и филь- трации находятся под жёстким контролем. Известно несколько механизмов, контролирующих кровоток и фильтрацию: авторегуляция в виде канальцево-клубочковой обратной связи и эффекты (сосудосуживающие и сосудорасширяющие) множества сосудистоактивных веществ.
Авторегуляция
Под авторегуляцией понимают не зависящее от нервных и гормональных влияний свойство кровеносной системы почек стабильно удерживать параметры почечного кровотока (следовательно, и СКФ) при значительных колебаниях системного АД (СКФ практически стабильна при систолическом АД 85-150 мм рт.ст.). Авторегуляцию обеспечивают два сопряжённых механизма - миоген-
ный ответ ГМК приносящих артериол и канальцево-клубочковая обратная связь.
• Миогенный ответ заключается в сокращении или расслаблении ГМК, циркулярно ориентированных по отношению к просвету приносящей артериолы, что приводит к вазоконстрикции или вазодилатации кровеносного сосуда соответственно. Повышение системного АД увеличивает просвет приносящих артериол. Это активирует (открывает) чувствительные к растяжению катионные каналы ГМК. Происходит деполяризация плазмолеммы ГМК, Ca2+ поступает в цитозоль, и сокращается ГМК. Просвет сосудов уменьшается, увеличивая сопротивление приносящей артериолы. В результате уменьшается СКФ.
• Канальцево-клубочковая обратная связь поддерживается структурами околоклубочкового комплекса.
Φ Околоклубочковый комплекс (рис. 26-
♦ Клетки плотного пятна реагируют на изменение концентрации [Na+] и [Cl-] в канальцевой жидкости. Na+-/K+-/ Cl--переносчик, расположенный в плазмолемме верхушечной поверхности клеток плотного пятна, при увеличении в просвете канальца [Na+] и [Cl-] способствует повышению содержания этих ионов и в цитозоле эпителиальных клеток. В результате открытия катионных каналов плазмолеммы Ca2+ поступает в цитозоль. Прирост [Ca2+] в цитозоле стимулирует секрецию из клеток плотного пятна паракринных и аутокринных агентов (см. раз-
дел «Контактная и дистантная регуляция функций» в гл. 4) в виде аденозина, тромбоксана и некоторых других.
♦ Гладкомышечные клетки, выстилающие стенки приносящей артериолы, имеют рецепторы к аденозину, их взаимодействие с выделяющимся из клеток плотного пятна аденозином обусловливает поступление Ca2+ в цитозоль, сокращение ГМК, вазоконстрикцию, увеличение сопротивления приносящей артериолы и уменьшение СКФ.
♦ Зернистые клетки, содержащиеся в стенках приносящей артериолы, также получают сигналы от клеток плотного пятна. Основная функция этих клеток - синтез фермента ренина, поступающего в общий кровоток. Субстрат ренина - ангиотензиноген (см. рис. 27-2), дальнейшие превращения которого вызывают появление в крови ангиотензина II - мощного вазоконстриктора, оказывающего и иное воздействие, в том числе и на механизм канальцево-клубочковой обратной связи (см. ниже).
♦ Мезангиальные клетки имеют рецепторы ангиотензина II, атриопептина и вазопрессина. Вазопрессин и ангиотензин II стимулируют сокращение мезангиальных клеток. Поскольку в цитоплазме клеток в большом количестве содержатся микрофиламенты, клетки обладают сократительной активностью и способны уменьшать площадь наружной поверхности стенки капилляров, через которую происходит фильтрация, снижая, таким образом, её уровень.
Сосудисто-активные регуляторы
В регуляции почечного кровотока и СКФ принимает участие множество гормонов и нейромедиаторов: ангиотензин II, норадреналин, адреналин, дофамин, АДГ, атриопептин, эндотелины, Пг, лейкотриены и оксид азота.
ТРАНСПОРТ В ПОЧЕЧНЫХ КАНАЛЬЦАХ
Транспорт через эпителиальные трубочки в общем виде рассмотрен в разделе «Трансклеточная проницаемость» главы 4 и проиллюстрирован на рис. 4-9 и 26-4. В этом разделе разобрано канальцевое (трансэпителиальное) перемещение конкретных веществ, т.е. их реабсорбция (из просвета канальцев в интерстиций и далее в околоканальцевые кровеносные капилляры) и секреция (из просвета капилляров в интерстиций и далее в просвет канальцев).
Натрий
Из поступающих в организм при сбалансированной диете 120 ммоль Na+ лишь 15% удаляется через потовые железы и ЖКТ, а 85% экскретируется с мочой. Каждые сутки почки отфильтровывают 25 500 ммоль и реабсорбируют 25 400 ммоль Na+, что примерно эквивалентно полутора килограммам поваренной соли. Поскольку вода пассивно перемещается между компартментами вслед за Na+ (и сопутствующим Cl-), ясно, сколь большое значение имеют почки для поддержания объёма жидкостей организма и их осмоляльности.
• Градиент реабсорбции (рис. 26-6, А). Реабсорбция Na+ (также CI-) максимальна в проксимальном извитом канальце, постепенно уменьшается в проксимально-дистальном направлении и минимальна в собирательных протоках.
• Пути и направление транспорта. Через стенку почечного канальца транспорт Na+ и Cl- (как и транспорт других ионов и воды) происходит как трансклеточно (сквозь клетку), так и по околоклеточному (парацеллюлярному) пути (рис. 26-6, Б, В; см. рис. 26-4).
• Механизмы канальцевого переноса Na+ через
верхушечную и базолатеральную плазмолемму различны в силу того
обстоятельства, что существенно различается внеклеточная
(внутриканальцевая и интерстициальная) и внутриклеточная [Na+]. При
реабсорбции Na+ пассивно входит в цитозоль через верхушечную плазмолемму, так как внутриклеточная [Na+] значительно ниже внутриканальцевой (
• Регуляция канальцевого транспорта Na+ осуществляется по следующим направлениям: автоматическая коррекция реабсорбции в проксимальных и дистальных канальцах вследствие изменений почечного кровотока (следовательно, фильтрации) и влияние на реабсорбцию в дистальном и отчасти в проксимальном отделе нефрона, а также в петле Генле и особенно в собирательных трубках и протоках гуморальных и нервных
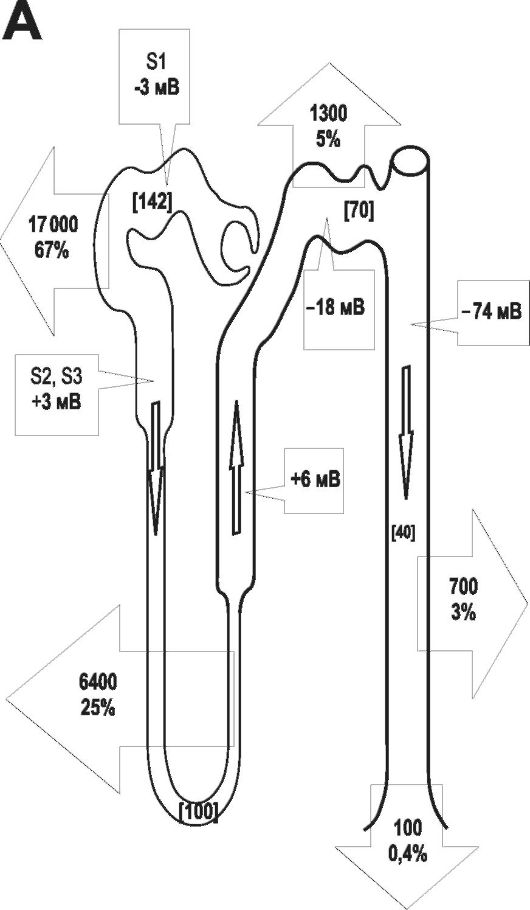
Рис. 26-6. Реабсорбция натрия [2]. А - реабсорбция Na+ в разных отделах почечных канальцев. Стрелки в просвете канальцев - направление движения фильтрата. Концентрация Na+ в просвете проксимального извитого канальца, петли Генле, дистального извитого канальца нефрона и в собирательных трубочках и протоках приведена в миллимолях (мМ, в прямых скобках). Количество реабсорбируемого Na+ в сутки (миллимоль/сут и % от отфильтрованного Na+) указано внутри стрелок, направленных из просвета канальца. Обозначена также трансэпителиальная разность электрохимического потенциала (∆μ?, мВ).
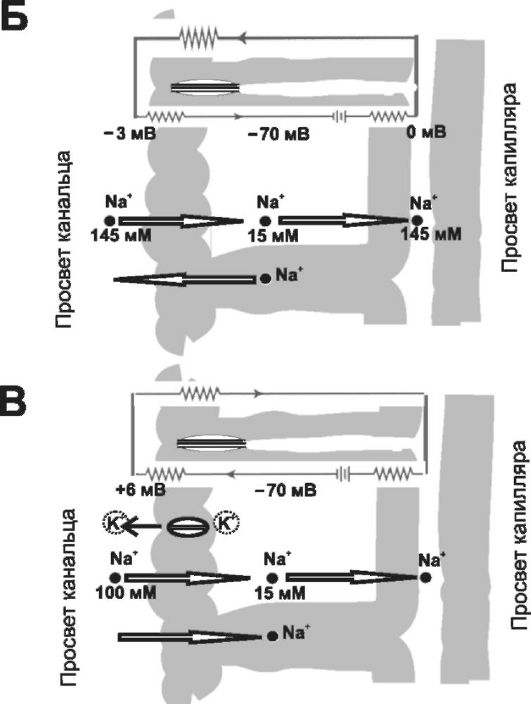
Рис. 26-6. Окончание. Б - механизм транспорта Na+ в проксимальном извитом канальце (сегмент S1). Реабсорбция Na+ из просвета канальца в интерстиций показана стрелками, направленными слева направо (трансклеточный путь). Na+ входит в клетку по его концентрационному градиенту (приведены значения концентрация Na+ в миллимолях), но выходит из клетки в интерстиций против градиента концентрации. В нижней части рисунка показано обратное движение Na+ по парацеллюлярному пути, частично замкнутому плотными контактами (в верхней части рисунка). В верхней части рисунка дана электрическая схема зарядов в разных частях канальца, из которой следует неизбежность движения катионов в просвет канальца по парацеллюляр- ному пути; В - механизм реабсорбции Na+ в толстом отделе петли Генле. Реабсорбция Na+ из просвета канальца в интерстиций обозначена стрелками, направленными слева направо (трансклеточный путь). Na+ входит в клетку по его концентрационному градиенту, но выходит из клетки в интерстиций против градиента концентрации. В нижней части рисунка показана реабсорбция Na+ по парацеллюлярному пути, частично замкнутому плотными контактами (изображены в верхней части рисунка). В верхней части рисунка помещена электрическая схема трансэпителиальной стенки (ср. с рис. 26-9, Б), из которой следует неизбежность движения катионов из просвета канальца по парацеллюлярному пути. Положительный заряд на канальцевой поверхности эпителия зависит от работы множества калиевых каналов, по которым из цитозоля в просвет канальца поступает K+.
факторов, увеличивающих или уменьшающих канальцевый транспорт Na+.
Φ Факторы, увеличивающие реабсорбцию Na+, т.е. обусловливающие задержку Na+ и воды в организме: альдостерон, АДГ и влияния симпатического отдела нервной системы.
Φ Факторы уменьшающие реабсорбцию Na+, т.е. вызывающие усиление диуреза и потенциально способные привести к потере Na+ и обезвоживанию организма: атриопептин, Пг, брадикинин, дофамин и эндогенный ингибитор Na+-, К+- АТФазы.
Хлор. Реабсорбция Cl- происходит по трансклеточному и око- локлеточному пути. Объёмы реабсорбции Cl- в разных отделах почечных канальцев практически такие же, как и для Na+ (см. рис. 26-6, Б). Cl- поступает в цитозоль против концентрационного градиента путём обмена внеклеточного Cl- на внутриклеточные анионы. Выход Cl- в интерстиций по всему протяжению почечных канальцев обеспечивают Cl--каналы, а в проксимальном отделе нефрона дополнительно К+-/Cl--котранспортёр.
Вода
Реабсорбция воды по всему протяжению почечных канальцев происходит только пассивно. Из
Калий
Почки ежесуточно отфильтровывают
Мочевина
Мочевина - конечный продукт катаболизма аминокислот - образуется в печени из NH4+,
её концентрация в крови (азот мочевины) - 2,5-8,32 ммоль/л. 100%
мочевины фильтруется в почках, экскретируется с мочой около 40%
отфильтрованной мочевины (ежесуточно 20-
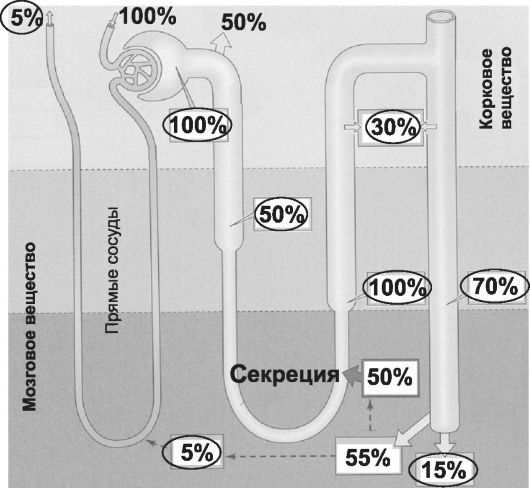
Рис. 26-7. Транспорт мочевины между канальцами, интерстицием и кровеносными сосудами [2]. Значения в овалах - содержание (в %) от отфиль- трованного (100%).
Глюкоза
Концентрация глюкозы в плазме крови натощак составляет 4-
Аминокислоты. Концентрация L-аминокислот в крови около
Олигопептиды и белки
• Фильтрация. Считают, что макромолекулы с молекулярной массой выше 40 000 не отфильтровываются. Однако этот ориентировочный порог не абсолютен. Например, концентрация альбуминов в фильтрате очень низка (от 4 до 20 мг/л, т.е. 0,01-0,05% концентрации альбумина в плазме крови); тем не менее при СКФ 180 л/сут, количество отфильтрованного альбумина составляет 0,7-3,6 г/сут. В то же время экскреция альбумина с мочой - около 30 мг/сут. Таким образом, реабсорбируется до 99% отфильтрованного альбумина.
• Реабсорбция. Перенос олигопептидов через щёточную каём- ку осуществляют Независимые котранспортёры, тогда как белки поступают в клетки путём опосредованного рецепторами эндоцитоза. Эндоцитозные пузырьки сливаются с лизосомами, где происходит гидролиз белков до аминокислот и олигопептидов. Олигопептиды расщепляются пептидазами до аминокислот и в щёточной каёмке, и в цитоплазме эпителиальных клеток. Аминокислоты поступают в интерстиций по механизму облегчённой диффузии.
Карбоновые кислоты. Монокарбоксилаты (лактат, пируват, ацетоацетат, β-гидроксибутират), соли ди- и трикарбоновых кислот (α-кетоглутарат, малат, сукцинат и цитрат) реабсорбируются трансклеточно практически полностью в проксимальных извитых канальцах. Экскреция карбоновых кислот - кетоновых тел (ацетоацетат и β-гидроксибутират) - происходит при голодании и сахарном диабете.
Органические анионы. Различные
органические анионы (метаболиты эндогенно катаболизируемых соединений и
экзогенно поступивших ЛС, а также парааминогиппуровая кислота) не
только фильтруются, но и секретируются. Секреция этих анионов (в том
числе оксалатов, солей жёлчных кислот, пенициллина) происходит в
проксимальных и дистальных отделах нефрона при помощи анионообменников
(в обмен на Cl-, ураты и ОН- просвета канальцев). Φ Ураты - моновалентные анионы - конечный продукт ка- таболизма пуринов. Их концентрация в плазме крови составляет 3-7 мг% (0,2-
Фосфаты. Концентрация фосфатов в плазме крови составляет 4,2 мг%, 50% находится в ионизированной форме (HPO42- - че- тыре пятых, H2PO4- - одна пятая), 40% - в электролитных комплексах, 10% связано с белками. В почках фильтруются фосфаты в ионизированной и комплексной форме. Ежесуточно фильтруется примерно на порядок больше фосфатов, чем содержится в межклеточной жидкости, и почти столько же реабсорбируется в проксимальном отделе нефрона при помощи котранспортёра натрия и фосфатов. Гормон паращитовидной железы ингибирует активность этого транспортёра. Некоторое количество фосфатов секретируется в просвет канальцев.
Кальций. Концентрация элементного кальция в плазме крови - 2,2-
Магний. Концентрация магния в плазме крови составляет 0,8-
КОНЦЕНТРИРОВАНИЕ И РАЗВЕДЕНИЕ МОЧИ
Почки могут выделять мочу в широком диапазоне осмоляльности: от разведённой (до 30 мОсм, 1/10 осмоляльности плазмы крови) до концентрированной (до 1200 мОсм, в 4 раза больше осмоляльности плазмы). Концентрирование и разведение мочи в значительной степени зависит от баланса воды в организме, от транспорта воды, натрия и мочевины в паренхиме почек и специфической организации прямых трубочек (прямые сосуды и петля Генле) в мозговой части почек в сочетании с избирательной проницаемостью разных отделов петли Генле и дистальных почечных канальцев.
• Баланс воды. В норме поступление воды в организм и потери воды организмом должны быть одинаковы. Поступление воды складывается из выпиваемой жидкости, содержащейся в пище воды и воды, образующейся в митохондриях при аэробном обмене. Потери воды происходят преимущественно через почки, и именно почки - главный регулятор водного обмена.
• Постоянство экскреции электролитов. Почки регулируют количество экскретируемой воды в зависимости от экскретируемых электролитов, главным образом хлористого натрия. Константа и стандарт экскреции электролитов - 600 мОсм в сутки. Нормально
эти 600 мОсм выделяются с обычными 1500 мл мочи. Для выделения большего
или меньшего количества воды почки должны продуцировать мочу иной
осмоляльности, но при условии, что количество экскретируемых
электролитов (600 мОсм) сохраняется. Например, для суточной секреции 600
мОсм в 1500 мл осмоляльность мочи (изоосмотическая моча) должна составлять 400 мОсм; для выделения избытка воды осмоляльность мочи (разведённая моча) может уменьшиться до 30 мОсм (тогда диурез составит
• Осмоляльность фильтрата в почечных канальцах (рис. 26-8).
Φ Концентрированная моча образуется при осмотическом перемещении воды из просвета канальцев через водопроницаемые сегменты канальцев в гиперосмотический интерстиций.
Φ Разведённая моча образуется при транспорте электролитов из просвета канальцев через непроницаемые для воды сегменты.
Φ Осмотичность фильтрата. В проксимальных отделах нефрона жидкость в просвете канальцев изоосмотична (300 мОсм), после прохождения по петле Генле - гипоосмотична (120 мОсм) и (в зависимости от баланса воды в организме) в конце собирательных протоков либо гипоосмотична (60 мОсм, рис. 26-8, Б), либо гиперосмотична (1200 мОсм,
рис. 26-8, А).
• Гиперосмотичность интерстиция мозгового вещества. Из рис. 26-8 видно, что при образовании и гипоосмотичной и гиперосмотичной мочи осмоляльность в интерстиции мозгового вещества почки всегда выше осмоляльности коркового вещества. Более того, существует градиент увеличения осмотичности интерстиция в направлении от коркового к мозговому веществу.
• Петля Генле играет ключевую роль в разведении и концентрировании мочи. Одна из функций петли Генле состоит в пере-
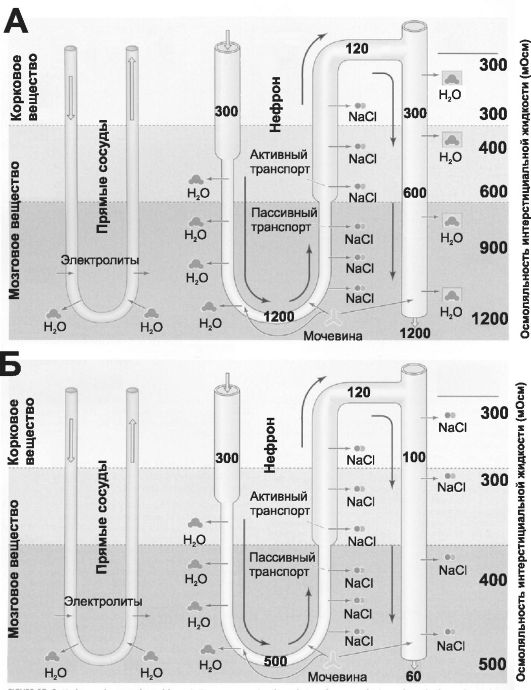
Рис. 26-8. Осмоляльность интерстициальной жидкости вокруг разных отделов почечных канальцев [2]. А - при ограничении питья; Б - обильное питьё. Пояснения в тексте.
мещении NaCl из канальцев в интерстиций. В то же время толстый отдел петли не реабсорбирует воду. Тем самым этот сегмент нефрона прямо участвует в образовании разведённой мочи. В то же время возникающая гиперосмотичность интерстиция мозговой части почки косвенно способствует образованию концентрированной мочи (ср. А и Б на рис. 26-8). Такое перемещение NaCl в интерстиций при одновременной непроницаемости для воды толстого отдела петли Генле в любой её точке создаёт поперечный градиент осмоляльности между канальцем и интерстицием, равный 200 мОсм. Этого градиента явно мало, чтобы создалась реально возникающая в месте перегиба петли осмоляльность от 500 (см. рис. 26-8, Б) до 1200 мОсм (см. рис. 26-8, А). Но эта задача решается повторяющимися циклами создания поперечного градиента между просветом канальца и интерстицием (противоточный умножитель).
• Противоточный умножитель петли Генле. Эффект создания поперечного градиента осмоляльности может умножиться в ситуации, когда существует противоположное движение жидкости в нисходящем и восходящем колене петли Генле. Так, осмоляльность 1200 мОсм в просвете канальца в месте перегиба петли может быть достигнута, если цикл повторится более 30 раз. Соответственно нарастает и вертикальный (от коркового к мозговому веществу) градиент осмоляльности (см. рис. 26-8, А). Таким образом, чем длиннее петля Генле, тем больше вертикальный градиент осмоляльности. Помимо транспорта NaCl в интерстиций из канальцев, существенное значение для гиперосмотичности интерстиция имеют и особенности распределения мочевины в разных отделах почечных канальцев (см. рис. 26-7).
• Роль прямых сосудов. Прямые сосуды мозгового вещества, расположенные параллельно канальцам петли Генле и организованные, как и петля Генле, по типу шпильки (нисходящий прямой сосуд спускается в мозговое вещество, а восходящий прямой сосуд поднимается после перегиба к корковому веществу), также необходимы, чтобы сформировался вертикальный градиент гиперосмоляльности мозгового вещества. На рис. 26-9 приведены модели противоточного обмена водой и NaCl между просветом сосудов и интерстицием: схема на
рис. 26-9, А отражает ситуацию только для одного сосуда, а на рис. 26-9, Б - для реальной шпильки из нисходящего и восходящего сосудов. Значение прямых сосудов в концентрировании и разведении мочи, как и петли Генле, состоит в том, что они поддерживают возрастающий от коры к почечным сосочкам вертикальный градиент гиперосмоляльности интерстиция. Здесь имеют значение два момента: во-первых, наличие противоточного обмена (ср. с противоточным умножителем градиента в петле Генле), во-вторых, относительно
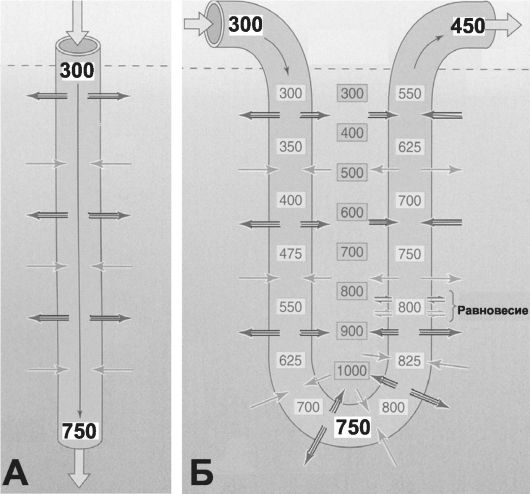
Рис. 26-9. Модель противоточного обмена [2]. А - вертикальная прямая трубка; Б - вертикальная шпилька (петля). Числовые значения - осмоляльное давление (мОсм), толстые стрелки - движение воды, тонкие стрелки - движение электролитов.
низкий кровоток в мозговом веществе по сравнению с корковым - не более 10% от объёма кровотока почки. Понятно, что чем ниже кровоток, тем меньше электролитов будет удалено из интерстиция и тем стабильнее будет гиперосмоляльный градиент в мозговом веществе.
• Собирательные протоки мозгового вещества также важны для формирования гиперосмотичной или гипоосмотичной мочи (см. рис. 26-8), так как их проницаемость имеет регулируемый характер. Так, без стимулирующего влияния АДГ стенка протоков относительно непроницаема для воды, АДГ увеличивает проницаемость (т.е. реабсорбцию) стенки протоков для воды. И наконец, АДГ увеличивает проницаемость (т.е. реабсорбцию) стенки протоков для мочевины. Комбинации этих эффектов результируют осмоляльность вторичной (дефинитивной) мочи.
ПОЧКИ И КИСЛОТНО-ЩЕЛОЧНОЕ РАВНОВЕСИЕ
Лёгкие и почки имеют первостепенное значение в поддержании кислотно-щелочного равновесия крови, которое осуществляют, контролируя компоненты её буферных систем - CO2 и HCO3-. Кислотно-щелочное равновесие рассматривается в главе 27, контроль [CO2] - в главе 25; в этом разделе рассмотрена роль почек в контроле [HCO3-] плазмы крови и в экскреции нелетучих кислот.
• Нелетучие кислоты. В организме образуются нелетучие кислоты (например, серная, фосфорная и различные органические) в суммарном количестве (за вычетом нейтрализованных основаниями) около 70 ммоль/сут (1 ммоль/кг массы тела). В перерасчёте на угольную кислоту (H2CO3) почка ежесуточно экскретирует около 70 ммоль H+ в мочу и одновременно переносит в кровь 70 ммоль вновь образованного HCO3-. В крови HCO3- нейтрализует 70 ммоль нелетучих кислот.
• Титрование отфильтрованного HCO3-. Ежесуточно обе почки отфильтровыгвают 4320 ммоль HCO3-. Этот огромный пул анионов практически не экскретируется и не реабсорбируется, а титруется секретируемым в просвет канальцев H+ до CO2 и H2O (H+ + HCO3- → H2CO3, H2CO3 → H2O + CO2). Однако реакция протекает слишком медленно для того, чтобы осуще-
ствилось быстрое и полное превращение HCO3 в H2O и CO2. Поэтому в процесс нейтрализации включается карбоангидраза эпителия почечных канальцев (фермент расщепляет HCO3- на CO2 и OH-, а секретируемый H+ нейтрализует OH-, в итоге образуются те же H2O и CO2).
• «Новый» HCO3-. Поверхностная мембрана эпителия хорошо проницаема для CO2 и воды, поэтому CO2 и H2O диффундируют в клетку, где карбоангидраза катализирует обратную реакцию - образование H+ и HCO3- из CO2 и H2O. Клетка экспортирует H+ в просвет канальцев, а HCO3- - в кровь через интерстиций. Таким образом, взамен оттитрованного в просвете канальцев и на поверхности эпителия HCO3- появляется «новый» HCO3-, секретируемый в кровь.
• Титрование отфильтрованного и секретированного аммиака. Секретируемый H+ также титрует NH3. Небольшая часть NH3 отфильтровывается, значительная часть диффундирует через эпителиальные клетки и поступает в просвет при помощи Na-H-обменника. В проксимальных канальцах превращение глутамина в α-кетоглутарат приводит к появлению двух ионов NH4+, образующих 2 NH3 два иона H+. При метаболизировании α-кетоглутарата образуется два иона OH-, которые карбоангидраза превращает в ион HCO3-. Этот «новый» HCO3- затем поступает в кровь.
• Титрование других отфильтрованных анионов. Помимо аммиака и HCO3-, секретированный H+ титрует также отфильтрованные HPO4-, креатинин и ураты.
Таким образом, в просвете канальцев H+ титрует HCO3-, HPO42-, NH3 и некоторые другие анионы. Из 4390 ммолей H+ 4320 ммолей (98%) идёт на титрование HCO3-. В итоге образуется «новый» HCO3-, поступающий в кровь. Эти процессы происходят преимущественно в проксимальном отделе нефрона (80%).
МОЧЕВЫДЕЛИТЕЛЬНАЯ СИСТЕМА
Мочевыделительная система (см. рис. 26-1) складывается из парных мочеточников, впадающих в мочевой пузырь, и отходящего от пузыря мочеиспускательного канала (уретра). Мочеиспускание - периодически возникающее и произвольное опорожнение мочевого пузыря.
Мочеточники
• Моча из собирательных трубок почки поступает в почечные чашечки, растягивает их стенки и вызывает перистальтические сокращения, распространяющиеся к почечным лоханкам. Отсюда перистальтика распространяется вдоль мочеточников, продвигая мочу в направлении мочевого пузыря. ГМК мочеточников по всей их длине иннервируют симпатические и парасимпатические волокна. Перистальтические сокращения мочеточников усиливаются парасимпатической стимуляцией и тормозятся симпатической стимуляцией. Мочеточники обильно снабжены болевыми нервными окончаниями. Закупорка мочеточника камнем сопровождается сильным болевым рефлекторным сокращением.
• Мочеточники входят в мочевой пузырь под небольшим косым углом через мышечную оболочку пузыря. Нормальный тонус мышечной оболочки пузыря (детрузорная мышца) сдавливает устья мочеточников, предотвращая тем самым обратное движение мочи, когда давление в мочевом пузыре возрастает в момент мочеиспускания или при сдавлении мочевого пузыря. Каждая перистальтическая волна, идущая вдоль мочеточника, увеличивает давление внутри мочеточника, сдавленный в мышечной стенке пузыря мочеточник открывается, и моча поступает в мочевой пузырь.
Наполнение мочевого пузыря
•
В отсутствие мочи в пузыре внутрипузырное давление приближается к
0. Поступление 30-50 мл мочи повышает давление до 5-6 см вод.ст.
Дополнительное поступление 200-300 мл мочи лишь ненамного повышает
давление. Этот постоянный уровень давления регулируется собственным
тонусом стенки мочевого пузыря. Накопление более 300-400 мл мочи в
пузыре вызывает быстрое повышение давления. Суммируясь с тоническим
давлением, давление, возникающее во время наполнения пузыря, создаёт
острый подъём давления, длящийся от нескольких секунд до минуты и более.
Пик давления может составлять более
Φ Эффективный объём мочевого пузыря - количество мочи в миллилитрах, выделенной за одно мочеиспускание.
• Φ Остаточная моча - моча, остающаяся в мочевом пузыре после мочеиспускания. У взрослых количество остаточной мочи в норме не должно превышать 30 мл (у детей - до 10% от возрастного объёма мочевого пузыря). ГМК детрузорной мышцы мочевого пузыря располагаются в виде спиральных, продольных и циркулярных пучков. Сокращение этой мышцы определяет опорожнение мочевого пузыря во время мочеиспускания. Пучки ГМК проходят также по стенке заднего отдела мочеиспускательного канала, эти мышечные волокна составляют внутренний сфинктер мочеиспускательного канала. Тонус внутреннего сфинктера удерживает шейку мочевого пузыря и задний отдел мочеиспускательного канала свободными от мочи. Внутренний сфинктер предохраняет опорожнение мочевого пузыря, пока давление не превысит критический уровень. Мочеиспускательный канал (уретра) проходит через мочеполовую диафрагму, содержащую пласты скелетной мышцы (наружный сфинктер мочеиспускательного канала, см. рис. 26-10). Наружный сфинктер контролируется нервной системой и может сдерживать мочеиспускание, когда снимается тонус внутреннего сфинктера.
Иннервация мочевого пузыря
Нервная регуляция функции мочевого пузыря обеспечивает чередование длительных периодов наполнения и коротких периодов опорожнения.
Парасимпатические (возбуждающие) волокна из крестцового отдела спинного мозга (см. рис. 26-10) в составе тазовых нервов направляются к мышце, выталкивающей мочу (m. detrusor vesicae). Возбуждение нервов вызывает сокращение детрузора и расслабление внутреннего сфинктера пузыря.
Симпатические (задерживающие) волокна из боковых ядер нижнего отдела спинного мозга направляются в нижний брыжеечный узел. Отсюда возбуждение передаётся по подчревным нервам к мускулатуре пузыря. Раздражение нервов вызывает сокращение внутреннего сфинктера и расслабление детрузора, т. е. опосредованно задерживает выделение мочи.
Чувствительные волокна. В составе тазовых нервов проходят также чувствительные нервные волокна, передающие информацию о том, в какой степени растянуты стенки мочевого пузыря. Наиболее сильные сигналы о растяжении поступают из заднего от-
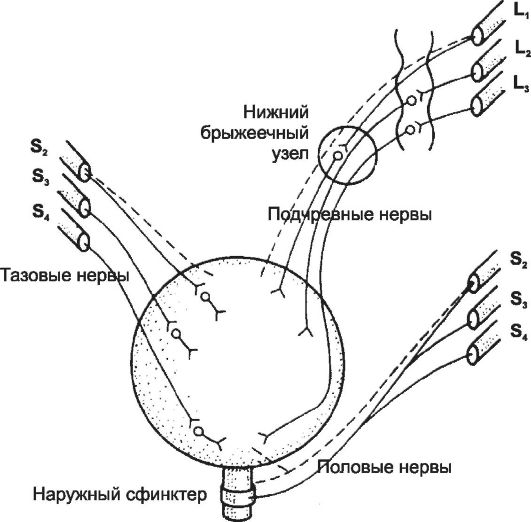
Рис. 26-10. Иннервация мочевого пузыря.
дела мочеиспускательного канала; именно они вызывают рефлекс опорожнения мочевого пузыря.
Соматические моторные волокна. В составе половых нервов проходят соматические моторные волокна, иннервирующие скелетную мускулатуру наружного сфинктера.
Мочеиспускательный рефлекс
Давление в мочевом пузыре, достигшее надпорогового уровня, вызывает раздражение рецепторов растяжения в стенке пузыря, особенно рецепторов в заднем отделе мочеиспускательного канала. Импульсы от рецепторов растяжения проводятся в крестцовые сегменты спинного мозга через тазовые нервы и рефлекторно возвращаются обратно к мочевому пузырю через парасимпатические
нервные волокна тех же тазовых нервов. Если мочевой пузырь заполнен частично, мочеиспускательные сокращения сменяются расслаблением, давление возвращается к исходному уровню. Если мочевой пузырь продолжает заполняться мочой, мочеиспускательные рефлексы учащаются и вызывают прогрессивно возрастающие сокращения детрузорной мышцы. Первое сокращение мочевого пузыря активирует рецепторы растяжения, которые посылают ещё больше импульсов, и сокращение усиливается. Этот цикл повторяется снова и снова, пока не будет достигнута сильная степень сокращения. Несколько секунд спустя мочевой пузырь расслабляется. Таким образом, цикл мочеиспускательного рефлекса включает быстрое нарастание давления, период удержания давления, возврат давления к исходному значению.
Произвольное
мочеиспускание начинается следующим образом. Индивидуум произвольно
сокращает мышцы живота, которые увеличивают давление в мочевом пузыре, и
затем дополнительные порции мочи входят в шейку мочевого пузыря и
наружный отдел мочевыводящего канала, растягивая их стенку. Это
стимулирует рецепторы растяжения, которые возбуждают мочеиспускательный
рефлекс и одновременно тормозят наружный сфинктер мочеиспускательного
канала. Мышцы промежности и наружный сфинктер могут сокращаться
произвольно, прекращая движение мочи в мочеиспускательный канал или
прерывая уже начавшееся мочеиспускание. Хорошо известно, что взрослые
способны удерживать наружный сфинктер в сокращённом состоянии, и они,
соответственно, способны задерживать мочеиспускание, вызванное
необходимыми обстоятельствами. После мочеиспускания моче-
испускательный канал женщин опустошается гравитацией. У мужчин
оставшаяся в мочеиспускательном канале моча выталкивается несколькими
сокращениями луковично-губчатых мышц. Первое ощущение наполненного
мочевого пузыря возникает у взрослых при объёме 100-150 мл, а первое
желание начать опорожнение пузыря - когда в нём содержится около
150-250 мл мочи. Человек испытывает дискомфорт, ощущая, что пузырь
наполнен при объёме 350-400 мл. При этом объёме гидростатическое
давление внутри мочевого пузыря приблизительно равно
Рефлекторный контроль. Рецепторы растяжения в стенке мочевого пузыря не имеют специальной регуляторной двигательной
иннервации. Однако порог мочеиспускательного рефлекса, подобно рефлексам растяжения скелетных мышц, управляется благодаря активности облегчающих и тормозящих центров ствола мозга. Облегчающие области находятся в зоне моста и заднего гипоталамуса, тормозящие - в зоне среднего мозга и верхней лобной извилины.
Мочеиспускание у детей
У новорождённых и детей грудного возраста мочеиспускание осуществляется рефлекторно. Дуги рефлексов замыкаются на уровне спинного и среднего мозга. Период наполнения сменяется неконтролируемым опорожнением. Когда процесс мочеиспускания становится полностью управляемым (контролируемым) ре- бёнком, говорят о зрелом типе мочеиспускания. Этот контроль представляет собой умение активно сокращать и расслаблять наружный сфинктер мочеиспускательного канала и мышцы тазового дна, а также подавлять детрузорную активность и тем самым регулировать позыв и задерживать (при необходимости) опорожнение мочевого пузыря. Этот процесс завершается обычно к 3-4 годам жизни.
Критерии зрелого типа мочеиспускания:
• соответствие объёма мочевого пузыря возрасту ребёнка; адекватное диурезу и объёму мочевого пузыря количество мочеиспусканий в сутки;
• полное удержание мочи днём и ночью;
• умение задерживать и прерывать при необходимости акт мочеиспускания, умение опорожнять мочевой пузырь без предшествующего позыва на мочеиспускание.
Нормативы мочеиспускания
• В норме у детей 3-14 лет, находящихся на обычном питьевом режиме, диурез (суточное количество мочи) составляет 500-1500 мл, 2/3 которых выделяется в течение первых 12 ч - с 6.00 до 18.00. Мочеиспускание, как правило, по позыву, не более 5-8 раз за время бодрствования. Количество одномоментно выделенной мочи колеблется от 50 до 350 мл. Процесс опорожнения мочевого пузыря всегда непрерывный, без напряжения мышц передней брюшной стенки; струя мочи широкая, с определённым напором.
• У взрослых число мочеиспусканий в среднем 4-6, активный объём каждого из них колеблется в широком диапазоне величин - от 100 до 400 (в среднем 200-300) мл.
обобщение главы
Почки занимают первостепенное место в контроле экскреции Na+. Только небольшой процент отфильтрованного Na+ обычно экскретируется в мочу, но это количество является критически важным в общем балансе натрия в организме.
Множество факторов влияет на экскрецию Na+, включая скорость клубочковой фильтрации, ангиотензин II и альдостерон, внутрипочечное давление, натрийуретические гормоны и такие факторы, как предсердный натрийуретический пептид и симпатические нервы.
Изменения в этих факторах могут объяснять нарушения экскреции Na+ в ответ на избыток или недостаток Na+. Эстрогены, глюкокортикоиды!, осмотические диуретики и диуретические ЛС также воздействуют на экскрецию Na+ почками.
Почки играют решающую роль в контроле баланса K+. K+ реабсорбируется в проксимальных извитых канальцах и петле Генле и секретируется клетками собирательных протоков коркового слоя. Неадекватная секреция K+ вызывает гиперкалиемию, а избыточная экскреция приводит к гипокалиемии.
Содержание кальция регулируется на входе и выходе из организма. Абсорбция Ca2+ из тонкой кишки контролируется 1,25- дигидрооксивитамином D3, а экскреция Ca2+ почками - паратиреоидным гормоном.
Магний в организме находится, главным образом, в костях, но он является необходимым внутриклеточным ионом. Почки регулируют содержание Mg2+ в плазме крови.
Количество фильтруемых фосфатов обычно превышает максимальную реабсорбционную ёмкость почечных канальцев для фосфатов, и приблизительно 5-20% профильтрованных фосфатов экскретируется. Фосфаты реабсорбируются в проксимальных канальцах, и этот процесс тормозится паратиреоидным гормоном. Фосфаты являются важным буфером pH в моче.
Мочевой пузырь накапливает мочу до тех пор, пока не сможет легко освободиться. Выделение мочи является комплексным процес- сом, вовлекающим как соматические, так и вегетативные нервы.