Нормальная физиология: учебник / Орлов Р.С., Ноздрачев А.Д. - 2-е изд., исправл. и доп. 2010. - 832 с.
|
|
|
|
ГЛАВА 24. КРОВЬ
Кровь относится к жидкостям внутренней среды организма, точнее - к внеклеточной жидкости, ещё точнее - к циркулирующей в сосудистой системе плазме крови и взвешенным (суспендированным) в плазме клеткам. Свернувшаяся (коагулировавшая) кровь состоит из сгустка (тромб), включающего клеточные элементы и некоторые белки плазмы, и прозрачной жидкости, сходной с плазмой, но лишённой фибриногена (сыворотка). Система крови включает органы кроветворения (гемопоэз) и периферическую кровь, как её циркулирующую, так и депонированную (зарезервированную) в органах и тканях фракцию. Кровь - одна из интегрирующих систем организма. Различные отклонения в состоянии организма и отдельных органов приводят к изменениям в системе крови, и наоборот. Именно поэтому, оценивая состояние здоровья или нездоровья человека, тщательно исследуют параметры, характеризующие кровь (гематологические показатели).
Функции крови
Многочисленные функции крови определяются не только присущими самой крови (плазме и клеточным элементам) свойствами, но и теми обстоятельствами, что кровь циркулирует в сосудистой системе, пронизывающей все ткани и органы, и находится в постоянном обмене с интерстициальной жидкостью, омывающей все клетки организма. В самом общем виде к функциям крови относятся транспортная, гомеостатическая, защитная и гемокоагуляционная. Как часть внутренней среды организма, кровь явля- ется интегральной частью практически любой функциональной активности (например, участие крови в дыхании, питании и метаболизме, экскреции, регуляция гормональная и температурная, регуляция кислотно-щёлочного равновесия и объёма жидкостей, осуществление иммунных реакций).
Объёмы крови
Общий объём крови принято рассчитывать исходя из массы тела (без учёта жира), что составляет примерно 7% (6-8%, для ново- рождённых - 8,5%). Так, у взрослого мужчины массой
Гематокрит (Ht, или гематокритное число) - отношение объё- ма клеточных элементов крови (99% приходится на эритроциты) к объёму плазмы - в норме равен у мужчин 0,41-0,50, у женщин 0,36-0,44. Определение объёма крови осуществляют прямо (за счёт мечения эритроцитов 51Cr) или косвенно (за счёт мечения альбумина плазмы 131I или определения гематокрита).
Реологические свойства
Реологические (в том числе вязкие) свойства крови важны, когда необходимо оценить движение крови в сосудах и суспензион- ную стабильность эритроцитов.
Вязкость - свойство жидкости, влияющее на скорость её дви- жения. Вязкость крови на 99% определяют эритроциты. Сопротивление потоку крови (по закону Пуазейля) прямо пропорционально вязкости, а вязкость прямо пропорциональна гематокриту. Таким образом, увеличение гематокрита означает увеличение нагрузки на сердце (т.е. происходит увеличение объёмов наполнения и выброса сердцем).
Суспензионная стабильность эритроцитов. Эритроциты в крови отталкиваются друг от друга, так как имеют на поверхности отрицательный заряд. Уменьшение поверхностного отрицательного заряда эритроцитов обусловливает их агрегацию; такие агрегаты менее устойчивы в гравитационном поле, так как увеличена их эффективная плотность. Скорость оседания эритроцитов (СОЭ) является мерой оценки суспензионной устойчивости эритроцитов. Величину СОЭ измеряют градуированными капиллярными пипетками, а чтобы предотвратить свёртывание крови, к ней добавляют трёхзамещённый цитрат натрия (так называемая цитратная кровь).
В течение часа в верхней части капиллярной трубки появляется светлый столбик плазмы, высота которого в миллиметрах и явля- ется величиной СОЭ (у здоровых лиц 2-15 мм/ч). Наиболее типичная причина повышения СОЭ - воспаление различного генеза (бактериальное, аутоиммунное), беременность, опухолевые заболевания, что приводит к изменениям белкового состава плазмы крови (особенно «ускоряет» СОЭ увеличение содержания фибри- ногена и отчасти γ-глобулинов).
ПЛАЗМА
Надосадочная жидкость, образующаяся после центрифугирования свернувшейся крови, - кровяная сыворотка. Надосадочная
жидкость после центрифугирования цельной крови с добавленными к ней
антикоагулянтами (цитратная кровь, гепаринизированная кровь) - плазма крови.
В отличие от плазмы в сыворотке нет ряда плазменных факторов
свёртывания крови (I - фибриноген, II - протромбин, V - проакцелерин и
VIII - антигемофиличе- ский фактор). Плазма - жидкость бледно-янтарного
цвета, содержащая белки, углеводы, липиды, липопротеины, электролиты,
гормоны и другие химические соединения. Объём плазмы - около 5% массы
тела (при массе
Белки
В плазме содержится несколько сотен различных белков, поступающих в основном из печени, но, кроме того, и из цирку- лирующих в крови клеточных элементов и из множества внесосудистых источников. Функции плазменных белков крайне разнообразны.
Классификации. Плазменные белки классифицируют по физико-химическим признакам (точнее, по их подвижности в электрическом поле), а также в зависимости от выполняемых функций.
Электрофоретическая подвижность. Выделены пять электрофоретических фракций плазменных белков: альбумины и глобулины (α1- и α2-, β- и γ-).
Φ Альбумины (40 г/л, Mr ~ 60-65 кД) в значительной степени определяют онкотическое (коллоидно-осмотическое) давление (
Φ Глобулины (30 г/л), в том числе (примеры):
♦ а^глобулины: а1-антитрипсин, а1-липопротеины (высокой плотности), протромбин;
♦ а2-глобулины: а2-макроглобулин, а2-антитромбин III, а2-гаптоглобулин, плазминоген;
♦ β-глобулины: β-липопротеины (низкой плотности), апоферритин, гемопексин, фибриноген, C-реактивный белок;
♦ γ-глобулины: иммуноглобулины (IgA, IgD, IgE, IgG, IgM). Функциональная классификация. Выделяют три главные группы: 1) белки системы свёртывания крови; 2) белки, участвую- щие в иммунных реакциях; 3) транспортные белки.
Φ 1. Белки системы свёртывания крови (см. подробнее ниже). Различают коагулянты и антикоагулянты. Обе группы белков обеспечивают равновесие между процессами формирования и разрушения тромба.
♦ Коагулянты (в первую очередь это плазменные факторы свёртывания) участвуют в формировании тромба, например фибриноген (синтезируется в печени и при гемокоагуляции превращается в фибрин).
♦ Антикоагулянты - компоненты фибринолитической системы (препятствуют свёртыванию).
Φ 2. Белки, участвующие в иммунных реакциях. К этой группе относят Ig (подробнее см. гл. 29) и белки системы комплемента.
Φ 3. Транспортные белки - альбумины (жирные кислоты), аполипопротеины (холестерин), трансферрин (железо), гаптоглобин (Hb), церулоплазмин (медь), транскортин (кортизол), транскобаламины (витамин B12) и множество других
Липопротеины
В плазме крови холестерин и триглицериды формируют комплексы с белками. Такие различные по величине и другим при- знакам комплексы называются липопротеинами (ЛП). Транспорт холестерина осуществляют липопротеины низкой плотности (ЛПНП), ЛП очень низкой плотности (ЛПОНП), ЛП промежуточной плотности (ЛППП), ЛП высокой плотности (ЛПВП), а также хиломикроны. С клинической точки зрения (вероятность развития артериосклеротического поражения - атеросклероза) существенное значение имеет содержание в крови холестерина и способность ЛП фиксироваться в стенке артерий (атерогенность).
• ЛПВП - наименьшие по размеру (5-12 нм) ЛП - легко проникают в стенку артерий и также легко её покидают, т.е. ЛПВП не атерогенны.
• ЛПНП (18-25 нм), ЛППП промежуточной плотности (25- 35 нм) и немногочисленные ЛПОНП (размер около 50 нм) слишком малы для того, чтобы проникнуть в стенку артерий. После окисления эти ЛП легко задерживаются в стенке артерий. Именно эти категории ЛП атерогенны.
• Крупные по размеру ЛП - хиломикроны (75-1200 нм) и ЛПОНП значительных размеров (80 нм) - слишком велики для того, чтобы проникнуть в артерии, и не расцениваются как атерогенные.
Осмотическое и онкотическое давление
Содержащиеся в плазме осмолиты (осмотически активные вещества), т.е. электролиты низкомолекулярных (неорганические соли, ионы) и высокомолекулярных веществ (коллоидные соединения, преимущественно белки) определяют важнейшие свойства крови - осмотическое и онкотическое давление. В медицинской практике эти параметры важны не только по отношению к крови per se (например, представление об изотоничности растворов), но и для реальной ситуации in vivo (например, для понимания механизмов перехода воды через капиллярную стенку между кровью и межклеточной жидкостью, в частности механизмов развития отё- ков, разделёнными эквивалентом полупроницаемой мембраны - стенкой капилляра). В этом контексте для клинической практики существенны и такие параметры, как эффективное гидростатическое и центральное венозное давление.
Φ Осмотическое давление (π,
см. подробнее в гл. 3, в том числе на рис. 2-9) - избыточное
гидростатическое давление на раствор, отделённый от растворителя (воды)
полупроницаемой мембраной, при котором прекращается диффузия
растворителя через мембрану (в условиях in vivo ею является
сосудистая стенка). Осмотическое давление крови можно определить по
точке замерзания (т.е. криоскопически); в норме оно составляет 7,5 атм (
Φ Онкотическое давление (коллоидно-осмотическое
давление - КОД) - давление, которое возникает за счёт удержания воды в
сосудистом русле белками плазмы крови. При нормальном содержании белка
в плазме (70 г/л) КОД плазмы -
Φ Эффективное гидростатическое давление - разница между гидростатическим давлением межклеточной жидкости (
Φ Центральное венозное давление - давление крови внутри венозной системы (в верхней и нижней полых венах), в норме составляющее 4-10 см вод.ст. Центральное венозное давление снижается при уменьшении ОЦК и повышается при сердечной недостаточности и застое в системе кровообращения. Инфузионные растворы
Солевые инфузионные растворы для внутривенного введения должны иметь то же осмотическое давление, что и плазма, т.е. быть изоосмотическими (изотоническими, например так называемый физиологический раствор - 0,85% раствор хлорида натрия).
Кислотно-щелочное равновесие, включая буферные системы крови, рассмотрено в главе 28.
КЛЕТОЧНЫЕ ЭЛЕМЕНТЫ КРОВИ
К клеткам крови (устаревшее название - форменные элементы) относятся эритроциты, лейкоциты и тромбоциты, или кровя- ные пластинки (рис. 24-1). Клетки крови изучают микроскопически
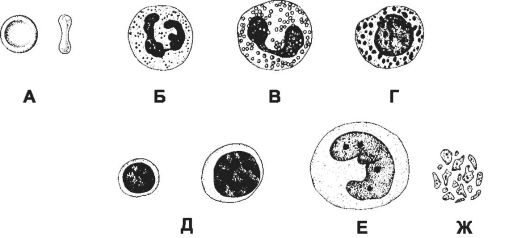
Рис. 24-1. Клетки крови [11]. Кровь содержит три разновидности клеток: эритроциты (безъядерные клетки, имеющие форму двояковогнутого диска), лейкоциты (ядерные клетки шаровидной формы, содержащие различного типа гранулы) и тромбоциты (фрагменты цитоплазмы расположенных в костном мозге гигантских клеток - мегакариоцитов). А - эритроцит; Б - нейтрофил; В - эозинофил; Г - базофил; Д - лимфоциты (малый и большой); Е - моноцит; Ж - тромбоциты.
на мазках, окрашенных по Романовскому-Гимзе, Райту и др. Содержание в периферической крови взрослого человека эритроцитов у мужчин - 4,5-5,7х1012/л (у женщин - 3,9-5х1012/л), лейкоцитов - 3,8-9,8х109/л (лимфоциты - 1,2-3,3х109/л, моноциты - 0,2-0,7х109/л, зернистые лейкоциты - 1,8-6,6х109/л), тромбоцитов - 190-405х109/л. В периферической крови циркулируют дефинитивные формы клеток, образование которых (кроветворение, или гемопоэз) происходит в красном костном мозге и органах лимфоидной системы (тимус, селезёнка, лимфатические узлы и лимфоидные фолликулы). Из стволовой кроветворной клетки в красном костном мозге формируются эритроидные клетки (в кровь поступают эритроциты и ретикулоциты), миелоидные клетки (зернистые лейкоциты, в кровь поступают палочко- и сегментоядерные нейтрофильные лейкоциты, зрелые базофильные и эозинофильные лейкоциты), моноциты, кровяные пластинки и часть лимфоцитов, в органах лимфоидной системы - T- и В-лимфоциты.
Гемопоэз
Кроветворение - образование из стволовой кроветворной клетки клеток-предшественниц конкретных гемопоэзов, их про-
лиферация и дифференцировка, а также созревание клеточных элементов крови в условиях специфического микроокружения и под влиянием факторов гемопоэза. В пренатальном периоде гемопоэз происходит в нескольких развивающихся органах (см. гл. 20). Кроветворение после рождения, у детей, подростков и взрослого человека осуществляется в костном мозге плоских костей (череп, рёбра, грудина, позвонки, кости таза) и эпифизов трубчатых ко- стей, а кроветворными органами для лимфоцитов являются се- лезёнка, тимус, лимфатические узлы, лимфоидные фолликулы в составе разных органов.
Зрелые клетки периферической крови развиваются из предшественников, созревающих в красном костном мозге. Унитарная теория кроветворения (рис. 24-2) предусматривает, что родона- чальница всех клеточных элементов крови - стволовая кроветворная клетка. Её потомки - полипотентные клетки-предшественницы лимфоцитопоэза (CFU-Ly) и миелопоэза (CFU-GEMM). В результате деления CFU-Ly и CFU-GEMM их потомки остаются
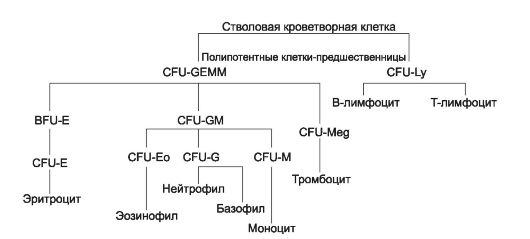
Рис. 24-2. Схема гемопоэза. CFU-GEMM - полипотентная клеткапредшественница миелопоэза; CFU-Ly - полипотентная клетка-предшественница лимфоцитопоэза; CFU-GM - полипотентная клеткапредшественница гранулоцитов и моноцитов; CFU-G - полипотентная клетка-предшественница нейтрофилов и базофилов. BFU-E и CFU-E - унипотентные предшественники эритроцитов; CFU-Eo - эозинофилов; CFU-M - моноцитов; CFU-Meg - мегакариоцитов. CFU (Colony Forming Unit) - колониеобразующая единица (КОЕ), BFU - Burst Forming Unit - взрывообразующая единица.
полипотентными или превращаются в коммитированные (пред- определённые судьбой) унипотентные клетки-предшественницы, также способные делиться, но дифференцирующиеся (развивающиеся) только в одном направлении. Пролиферацию унипотентных клеток-предшественниц стимулируют колониестимулирующие факторы и интерлейкины (особенно интерлейкин-3).
• Эритропоэз. Начало эритроидного ряда - стволовая клетка эритропоэза, или взрывообразующая единица (BFU-E), из которой формируется унипотентный предшественник эритроцитов (CFU-E). Последний даёт начало проэритробласту. В результате дальнейшей дифференцировки увеличивается содержание Hb и потеря ядра. Из проэритробласта путём пролиферации и дифференцировки последовательно развиваются эритробласты: базофильный - полихроматофильный - оксифильный (нормобласт) и далее неделящиеся формы - ретикулоцит и эритроцит. От BFU-E до нормобласта - 12 клеточных поколений, а от CFU-E до позднего нормобласта - 6 или меньше клеточных делений. Длительность эритропоэза (от его стволовой клетки BFU-E до эритроцита) - 2 нед. Интенсивность эритропоэза контролируется эритропоэтином. Основной стимул для выработки эритропоэтина - уменьшение содержания кислорода в крови (рО2) - гипоксия (рис. 24-3).
• Гранулоцитопоэз (рис. 24-4). Гранулоциты образуются в костном мозге. Нейтрофилы и базофилы происходят из полипотентной клетки-предшественницы нейтрофилов и базофилов (CFU-G), а эозинофилы - из унипотентного предшественника эозинофилов (CFU-Eo). CFU-G и CFU-Eo - потомки полипотентной клетки-предшественницы гранулоцитов и моноцитов (CFU-GM). При развитии гранулоцитов можно выделить такие стадии: миелобласты - промиелоциты - миелоциты - метамиелоциты - палочкоядерные и сегментоядерные гранулоциты. Специфические гранулы появляются на стадии миелоцитов; с этого момента клетки называются в соответствии с типом образующихся из них зрелых гранулоцитов. Клеточное деление прекращается на стадии метамиелоцита. Пролиферацию и дифференцировку клеток-предшественниц контролируют колониестимулирующие факторы (гранулоцитов и макрофагов - GM-CSF, гранулоцитов - G-CSF), ИЛ-3 и ИЛ-5 (предшественники эозинофилов).
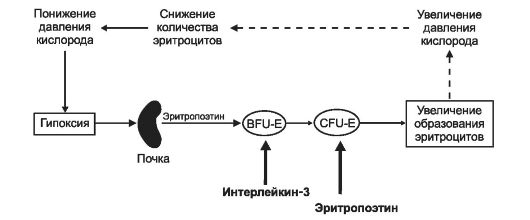
Рис. 24-3. Регуляция эритропоэза [11]. Пролиферацию взрывообразующей единицы эритропоэза (BFU-E) стимулирует интерлейкин-3. Унипотентный предшественник эритроцитов CFU-E чувствителен к эритропоэтину. Важнейший стимул для образования эритроцитов - гипоксия, запускающая синтез эритропоэтина в почке, а у плода - и в печени. Эритропоэтин выходит в кровь и поступает в костный мозг, где он стимулирует размножение и дифференцировку унипотентного предшественника эритроцитов (CFU-E) и дифференцировку последующих клеток эритроидного ряда. В результате количество эритроцитов в крови увеличивается. Соответственно возрастает количество кислорода, поступающего в почку, что тормозит образование эритропоэтина.
• Моноцитопоэз. Моноциты и гранулоциты имеют общую клетку-предшественницу - колониеобразующую единицу гранулоцитов и моноцитов (CFU-GM), образующуюся из полипотентной клетки-предшественницы миелопоэза (CFUGEMM). В развитии моноцитов выделяют две стадии - монобласт и промоноцит.
• Тромбоцитопоэз. Из мегакариобластов развиваются самые крупные (30-100 мкм) клетки костного мозга - мегакариоциты. При дифференцировке мегакариоцит увеличивается в размерах, его ядро становится дольчатым. Образуется развитая система демаркационных мембран, по которым происходит отделение («отшнуровка») тромбоцитов (рис. 24-5). Пролиферацию предшественников мегакариоцитов - мегакариобластов - стимулирует синтезируемый в печени тромбопоэтин.
• Лимфопоэз. Из стволовой кроветворной клетки (CFU-blast) происходит полипотентная клетка-предшественница лимфо-

Рис. 24-4. Гранулоцитопоэз [11]. В ходе дифференцировки предшественников гранулоцитов выделяют миелобласт, промиелоцит, миелоцит, метамиелоцит, палочкоядерный и сегментоядерный гранулоциты.
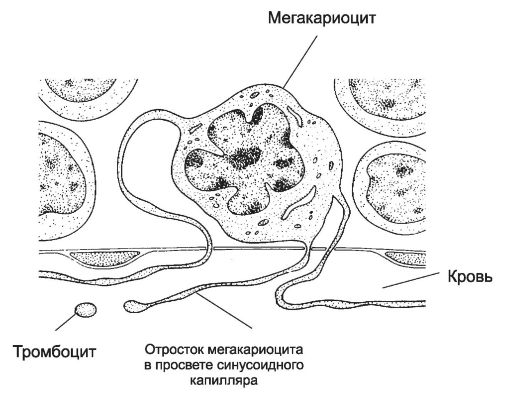
Рис. 24-5. Образование тромбоцитов [11]. Находящийся в костном мозге мегакариоцит образует протромбоцитарную псевдоподию. Последняя проникает сквозь стенку капилляра в его просвет. От псевдоподии отделяются тромбоциты и поступают в кровоток.
поэза (CFU-Ly), которая впоследствии даёт начало клеткампредшественницам B-лимфопоэза, T-лимфопоэза и (частично) предшественницам NK-клеток. Ранние предшественники В-лимфоцитов образуются в костном мозге, а Т-лимфоцитов - в тимусе. Дальнейшая дифференцировка включает в себя уровни про-B(T)-клеток, пре-B(T)-клеток, незрелых B(T)-клеток, зрелых («наивных») B(T)-клеток и (после контакта с Аг) - зрелых B(T)-клеток окончательных стадий дифференцировки. Продуцируемый клетками стромы костного мозга ИЛ-7 способствует образованию Т- и В-лимфоцитов, воздействуя на их клетки-предшественницы. В отличие от других клеток крови, лимфоциты могут пролиферировать и за пределами костного мозга. Это происходит в тканях иммунной системы в ответ на стимуляцию.
Эритроциты
Из красного костного мозга в кровь поступают преимущественно незрелые эритроциты - ретикулоциты. Они (в отличие от зрелых эритроцитов) содержат рибосомы, митохондрии и комплекс Гольджи. Окончательная дифференцировка в эритроциты происходит в течение 24-48 ч после выхода ретикулоцитов в кровоток. Количество поступающих в кровоток ретикулоцитов в норме равно количеству удаляемых эритроцитов. Ретикулоциты составляют около 1% всех циркулирующих красных клеток крови. Эритроциты (см. рис. 24-1, А) - безъядерные клетки диаметром 7-8 мкм (нормоциты). Количество эритроцитов у женщин составляет 3,9- 4,9х1012/л, у мужчин - 4,0-5,2х1012/л. Более высокое содержание эритроцитов у мужчин обусловлено стимулирующим эритропоэз влиянием андрогенов. Продолжительность жизни (время циркуляции в крови) 100-120 дней.
Форма и размеры. Эритроцит в крови имеет форму двояковогнутого диска диаметром 7-8 мкм. Считают, что именно такая конфигурация создаёт наибольшую площадь поверхности по отношению к объёму, что обеспечивает максимальный газообмен между плазмой крови и эритроцитом. При любой другой форме эритроцитов говорят о пойкилоцитозе. Разброс размеров эритроцитов - анизоцитоз, клетки диаметром более 9 мкм - макроциты, менее 6 мкм - микроциты. При ряде заболеваний крови изменяются размеры и форма эритроцитов, а также снижается их осмотическая резистентность, что приводит к разрушению (гемолизу) эритроцитов.
Возрастные изменения эритроцитов. При рождении и в первые часы жизни количество эритроцитов в крови повышено и составляет 6,0-7,0х1012/л.
У новорождённых наблюдают анизоцитоз с преобладанием макроцитов, а
также повышенное содержание ретикулоцитов. В течение первых суток
постнатального периода количество эритроцитов уменьшается, к 10-14-м
суткам достигает уровня взрослого и продолжает уменьшаться. Минимальный
показатель наблюдается на 3-6-м месяце жизни (физиологическая анемия),
когда снижен уровень эритропоэтина. Это связано с уменьшением синтеза
эритропоэтина в печени и началом его выработки в почке. На 3-4-м году
жизни количество эритроцитов снижено (ниже, чем у взрослого), т.е. в
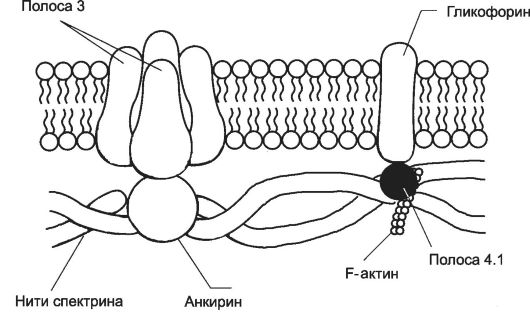
Рис. 24-6. Примембранный цитоскелет эритроцита [11]. Белок полосы 3 - главный трансмембранный белок. Спектрин-актиновый комплекс формирует сетеподобную структуру примембранного цитоскелета. С комплексом спектрин-актин, стабилизируя его, связан белок полосы 4.1. Анкирин через белок полосы 3 соединяет спектрин-актиновый комплекс с клеточной мембраной. Наименования полос белков характеризуют их электрофоретическую подвижность.
Содержание эритроцитов достигает нормы взрослого в период полового созревания.
Плазмолемма и примембранный цитоскелет. Клеточная мембрана эритроцита довольно пластична, что позволяет клетке деформироваться и легко проходить по узким капиллярам (их диаметр 3-4 мкм). Главные трансмембранные белки эритроцита - белок полосы 3 и гликофорины. Белок полосы 3 (рис. 24-6) вместе с белками примем- бранного цитоскелета (спектрин, анкирин, фибриллярный актин, белок полосы 4.1) обеспечивает поддержание формы эритроцита в виде двояковогнутого диска. Гликофорины - мембранные гликопротеины, их полисахаридные цепи содержат Аг-детерминанты (например, агглютиногены А и В системы групп крови AB0).
Гемоглобин
Практически весь объём эритроцита заполнен дыхательным белком - гемоглобином (Hb). Молекула Hb - тетрамер, состоя-
щий из четырёх субъединиц - полипептидных цепей глобина (две цепи α и две цепи β, γ, δ, ε, θ, ζ в разных комбинациях), каждая из которых ковалентно связана с одной молекулой гема. Гем построен из четырёх молекул пиррола, образующих порфириновое кольцо, в центре которого находится атом железа (Fe2+). Основная функция Hb - перенос O2. Существует несколько типов Hb, образующихся на разных сроках развития организма, различающихся строением глобиновых цепей и сродством к кислороду. Эмбриональные Hb (ζ- и ε-цепи) появляются у 19-дневного эмбриона, содержатся в эритроидных клетках в первые 3-6 мес беременности. Фетальный Hb (HbF - α2γ2) появляется на 8-36-й неделе беременности и составляет 90-95% всего Hb плода. После рождения его количество постепенно снижается и к 8 мес составляет 1%. Дефинитивные Hb - основные Hb эритроцитов взрослого человека (96-98% - HbA (A1,) - α2β2, 1,5-3% - HbA2 - α2δ2). Известно более 1000 мутаций разных глобинов, значительно изменяющих свойства Hb, в первую очередь способность транспортировать O2.
Формы гемоглобина. В эритроцитах Hb находится в восстановленной (HbH) и/или окисленной (HbO2) формах, а также в виде гликозилированного Hb. В ряде случае возможно наличие карбоксигемоглобина и метгемоглобина.
Ф Оксигемоглобин. В лёгких при повышенном pO2 Hb связывает (ассоциирует) O2, образуя оксигемоглобин (HbO2). В этой форме HbO2 переносит O2 от лёгких к тканям, где O2 легко освобождается (диссоциирует), а HbO2 становится дезоксигенированным Hb (обозначают как HbH). Для ассоциации и диссоциации O2 необходимо, чтобы атом железа гема был в восстановленном состоянии (Fe2+). При включении в гем трёхвалентного железа (Fe3+) образуется метгемоглобин - очень плохой переносчик O2. Ф Метгемоглобин (MetHb) - Hb, содержащий Fe гема в трёх- валентной форме (Fe3+), не переносит О2; прочно связывает O2, так что диссоциация последнего затруднена. Это приводит к метгемоглобинемии и неизбежным нарушениям газообмена. Образование MetHb может быть наследственным или приобретённым. В последнем случае это результат воздействия на эритроциты сильных окислителей. К ним относят нитраты и неорганические нитриты, сульфаниламиды и местные анестетики (например, лидокаин).
Φ Карбоксигемоглобин - плохой переносчик кислорода. Hb легче (примерно в 200 раз), чем с O2, связывается с монооксидом углерода СО (угарный газ), образуя карбоксигемо- глобин (O2 замещён CO).
Φ Гликозилированный Hb (HbA1C) - HbA (А1:), модифицированный ковалентным присоединением к нему глюкозы (норма HbA1C 5,8-6,2%). К одним из первых признаков са- харного диабета относят увеличение в 2-3 раза количества HbA1C. Этот Hb имеет худшее сродство к кислороду, чем обычный Hb.
Транспорт кислорода. Кровь ежедневно переносит из лёгких в ткани около
• Физически растворённый в крови газ. Согласно закону Генри, количество растворённого в крови O2 (любого газа) пропорционально Po2 (парциальному давлению любого газа) и коэффициенту растворимости конкретного газа. Физическая растворимость O2 в крови примерно в 20 раз меньше, чем растворимость СО2, но для обоих газов незначительна. В то же время физически растворённый в крови газ - необходимый этап транспорта любого газа (например, при перемещении O2 в эритроцит из полости альвеол).
• Кислородная ёмкость крови - максимально возможное количество связанного с HbО2 - теоретически составляет 0,062 ммоль О2 (1,39 мл О2) на
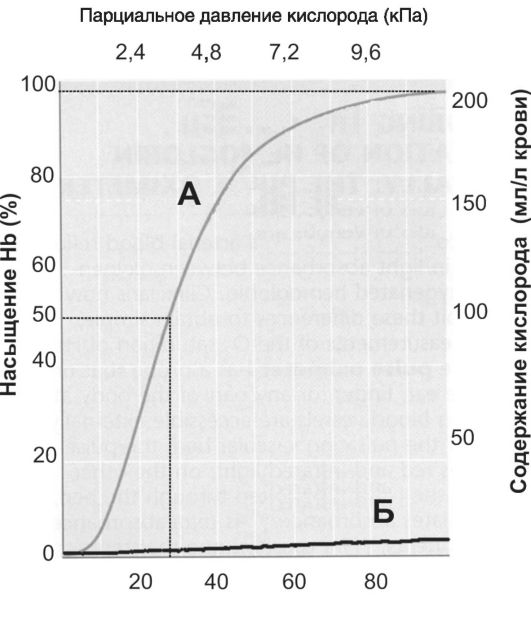
• Насыщение (сатурация, S) Hb()2 (So2) зависит от парциального давления кислорода (Po2) и фактически отражает содержание оксигенированного Hb (HbО2, см. кривую А на рис. 24-7). So2 может принимать значения от 0 (Hb()2 нет) до 1 (нет HbH). При половинном насыщении (S05) Po2 равно 3,6 кПа (
Парциальное давление кислорода (мм рт.ст.)
Рис. 24-7. Содержание кислорода в крови [23]. А - ассовдированный с HbO2. Б - физически растворённый в крови O2. Обратите внимание, что кривая А (в отличие от кривой Б) не имеет линейного характера, - это так называемая S-образная (сигмовидная) кривая; такая форма кривой отражает то обстоятельство, что четыре субъединицы Hb связываются с O2 кооперативно. Это обстоятельство имеет важное физиологическое значение: при конкретных и разных (!) значениях Po2 в артериальной и смешанной (венозной) крови создаются наиболее благоприятные условия для ассоциации Hb и O2 в капиллярах лёгкого и для диссоциации Hb и O2 в тканевых капиллярах. В то же время в плазме крови физически растворена только небольшая часть О2 (максимально 6%); физическую растворимость О2 описывает закон Генри: с увеличением Po2 содержание О2 линейно возрастает.
ми (см. кривую А на рис. 24-7), зависимость между So2 и Po2 не является линейной (характерная S-образная кривая), что благоприятствует не только связыванию О2 в лёгких (артериальная кровь) и транспорту О2, но и освобождению О2 в кровеносных капиллярах органов и тканей, так как насыщение артериальной крови кислородом (Sao2) составляет примерно 97,5%, а насыщение венозной крови (Svo2) - 75%. Аффинитет Hb к О2, т.е. насыщение Hb()2 при конкретном
Po2 изменяет ряд факторов (температура, pH и Pco2, 2,3-бифос-
фоглицерат; рис. 24-8).
• pH, Рсо2 и эффект Бора. Особенно существенно влияние pH: уменьшение водородного показателя (сдвиг в кислую сторо-
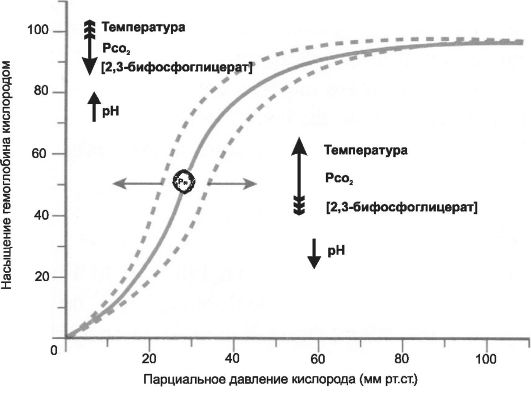
Рис. 24-8. Диссоциация оксигемоглобина в крови в зависимости от Po2 [4]. В зависимости от изменений (указаны стрелками) температуры, pH, Pco2 крови и концентрации 2,3-бифосфоглицерата в эритроцитах кривая насыщения гемоглобина O2 сдвигается вправо (что означает меньшее насыщение кислородом) или влево (что означает большее насыщение кислородом). На кривой кружочком отмечена позиция, соответствующая половинному насыщению (S05).
ну - в зону ацидоза) сдвигает кривую диссоциации Hb вправо (что способствует диссоциации О2), тогда как увеличение pH (сдвиг в щелочную сторону - в зону алкалоза) сдвигает кривую диссоциации Hb влево (что увеличивает аффинитет О2). Воздействие же Рсо2 на кривую диссоциации оксигемоглобина осуществляется преимущественно через изменение значений водородного показателя: при поступлении Co2 в кровь происходит уменьшение pH, что способствует диссоциации О2 и его диффузии из крови в ткани. Напротив, в лёгких CO2 диффундирует из крови в альвеолы, что вызывает увеличение pH, т.е. способствует связыванию О2 с Hb. Этот влияние CO2 и H+ на аффинитет О2 к Hb известно как эффект Кристиана Бора (отец великого физика Нильса Бора). Таким образом, эффект Бора обусловлен преимущественно изменением pH при увеличении содержания Co2 и лишь частично - связыванием Co2 с Hb (см. далее). Физиологическое следствие эффекта Бора - облегчение диффузии o2 из крови в ткани и связывание o2 артериальной кровью в лёгких.
• Температура. Влияние температуры на аффинитет Hb к О2 у гомойотермных животных теоретически не имеет значения, но может оказаться важным в ряде ситуаций. Так, при интенсивной мышечной нагрузке температура тела повышается, вследствие чего кривая диссоциации сдвигается вправо (возрастает поступление О2 в ткани). При снижении температуры (особенно пальцев, губ, ушной раковины) кривая диссоциации сдвигается влево, т.е. увеличивается аффинитет О2; следовательно, поступление О2 в ткани не увеличивается.
• 2,3-Бифосфоглицерат (БФГ) - промежуточный продукт гликолиза - содержится в эритроцитах примерно в той же молярной концентрации, что и Hb. БФГ связывается с Hb (в основном за счёт взаимодействия с β-субъединицей, т.е. с дефинитивными Hb, но не с фетальным Hb, в составе которого нет β-субъединицы). Связывание БФГ с Hb сдвигает кривую диссоциации Hb вправо (см. рис. 24-8), что способствует диссоциации О2 при умеренных значениях Ро2 (например, в тканевых капиллярах), но практически не влияет на кривую диссоциации при высоких значениях Ро2 (в капиллярах лёгкого). Существенно, что при усилении гликолиза (анаэробное окисление) концентрация БФГ в эритроцитах повышается, играя
роль
механизма, приспосабливающего организм к гипоксии, которая наблюдается
при заболеваниях лёгких, анемиях, подъёме на высоту. Так, в период
адаптации к высокогорью (более
Примерно 2/3 СО2 (68%, в том числе 63% в эритроцитах) транспортируется кровью в виде бикарбоната (НСО3-). Пятую часть СО2 (22%, в том числе в виде карбогемоглобина - 21%) переносят карбаматы (СО2 обратимо присоединён к неионизированным концевым α-аминогруппам белков, образуя группировку R-NH-СОО-). 10% СО2 находится в растворённом состоянии (поровну в плазме и в эритроцитах). Крайне существенно то обстоятельство, что в реакциях химического связывания СО2 образуются ионы Н+:
СО2 + Н2О ↔ Н2СО3↔ Н+ + НСО3-, R-NH2 + СО2 ↔ R-NH-СОО- + Н+.
Φ Из обеих равновесных реакций следует, что химическое связывание СО2 идёт с образованием ионов Н+. Таким образом, для химического связывания СО2 необходимо нейтрализовать Н+. Эту задачу решает гемоглобиновая буферная система.
Гемоглобиновая буферная система (связывание ионов Н+) важна для транспорта CO2 кровью.
• В капиллярах большого круга кровообращения HbO2 отдаёт кислород, а в кровь поступает CO2. В эритроцитах под влиянием карбоангидразы CO2 взаимодействует с H2O, образуется угольная кислота (H2CO3), диссоциирующая на HCO3- и H+. Ион H+ связывается с Hb (образуется восстановленный Hb - HHb), а HCO3- из эритроцитов выходит в плазму крови; взамен в эритроциты поступает эквивалентное количество
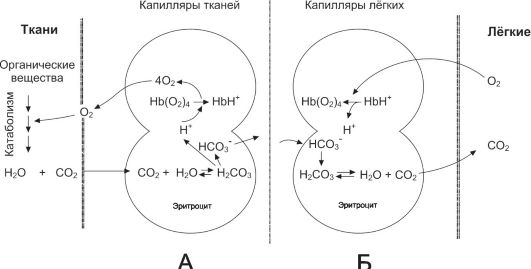
Рис. 24-9. Перенос О2 и СО2 с кровью [9]. А - влияние СО2 и Н+ на высвобождение О2 из комплекса с гемоглобином в тканях (эффект Бора); Б - оксигенирование дезоксигемоглобина в лёгких, образование и выделение СО2.
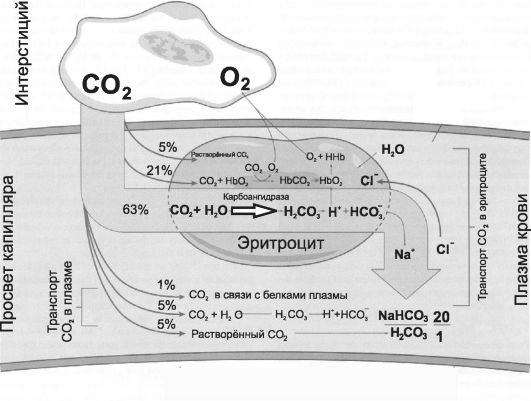
Рис. 24-10. Механизмы транспорта СО2 с кровью [4].
• Cl-. Одновременно часть CO2 связывается с Hb (образуется карбогемоглобин). В капиллярах лёгких (т.е. в условиях низкого рCO2 и высокого рO2) Hb присоединяет O2 и образуется оксигемоглобин (HbO2). В то же время в результате разрыва карбаминовых связей высвобождается CO2. При этом HCO3- из плазмы крови поступает в эритроциты (в обмен на ионы Cl-) и взаимодействует с H+, отщепившимся от Hb в момент его оксигенации. Образующаяся угольная кислота (H2CO3) под влиянием карбоангидразы расщепляется на CO2 и H2O. CO2 диффундирует в альвеолы и выводится из организма. Кривая диссоциации CO2 показывает связь между содержанием в крови CO2 и рCO2. В отличие от кривой диссоциации Hb и О2 (см. рис. 24-7), кривая диссоциации CO2 при физиологических значениях рОД2 (кровь артериальная -
МЕТАБОЛИЗМ ГЕМОГЛОБИНА
Удаление эритроцитов из кровотока происходит трояко: 1) путём фагоцитоза, 2) в результате гемолиза и 3) при тромбообразовании.
Распад гемоглобина. При любом варианте разрушения эритроцитов Hb распадается на гем и глобины (рис. 24-11). Глобины, как и другие белки, расщепляются до аминокислот, а при разрушении гема освобождаются ионы железа, оксид углерода (СО) и протопорфирин (вердоглобин, из которого образуется биливердин, восстанавливающийся в билирубин). Билирубин в комплексе с альбумином транспортируется в печень, откуда в составе желчи поступает в кишечник, где происходит его превращение в уроби-
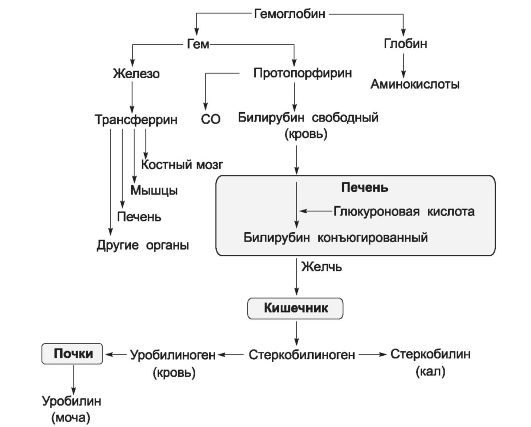
Рис. 24-11. Обмен гемоглобина и билирубина [16].
линогены. Превращение гема в билирубин можно наблюдать в гематоме: обусловленный гемом пурпурный цвет медленно переходит через зелёные цвета вердоглобина в жёлтый цвет билирубина.
Гематины. При некоторых условиях гидролиз Hb обусловливает образование гематинов (гемомеланин, или малярийный пигмент, и солянокислый гематин).
МЕТАБОЛИЗМ ЖЕЛЕЗА
Железо участвует в функционировании всех систем организма. Суточная потребность в железе составляет для мужчин 10 мг, для женщин 18 мг (в период беременности и лактации - 38 и 33 мг соответственно). Общее количество железа (преимущественно в со-
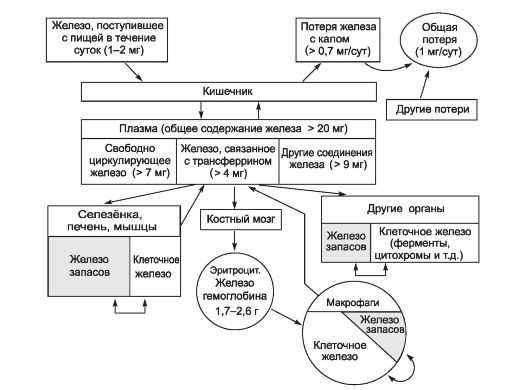
Рис. 24-12. Схема обмена железа (Fe) в организме здорового мужчины с массой тела
ставе гема Hb) в организме - около
Основная масса железа организма входит в состав гема (Hb, миоглобин, цитохромы). Часть железа запасается в виде феррити- на (в гепатоцитах, макрофагах костного мозга и селезёнки) и гемосидерина (в клетках фон Купфера печени и макрофагах костного мозга). Некоторое количество находится в лабильном состоянии в связи с трансферрином. Железо, необходимое для синтеза гема, извлекается преимущественно из разрушенных эритроцитов. Ис- точники железа - поступление с пищей и разрушенные эритроциты.
• Железо, поступающее с пищей, всасывается в кишечнике в двенадцатиперстной кишке и начальном отделе тощей кишки. Железо всасывается преимущественно в двухвалентной форме (Fe2+). Всасывание Fe2+ в ЖКТ ограничено и контролируется его концентрацией в плазме крови (соотношение белков - апоферритина, свободного от железа, и ферритина). Усиливают всасывание аскорбиновая, янтарная, пировиноградная кислота, сорбит, алкоголь; подавляют - оксалаты, препараты кальция и содержащие кальций продукты (например, творог, молоко и т.д.). В среднем в сутки всасывается 10 мг железа. В ЖКТ железо накапливается в эпителиальных клетках слизистой оболочки тонкого кишечника. Отсюда трансферрин переносит железо в красный костный мозг (для эритропоэза, это всего 5% всосавшегося Fe2+), в печень, селезёнку, мышцы и другие органы (для запасания).
• Железо погибших эритроцитов при помощи трансферрина поступает в эритробласты красного костного мозга (около 90%), часть этого железа (10%) запасается в составе ферритина и гемосидерина.
• Физиологическая потеря железа происходит с калом. Незначительная часть железа теряется с потом и клетками эпидермиса. Общая потеря железа - 1 мг/сут. Физиологическими считают также потери железа с менструальной кровью и грудным молоком.
• Дефицит железа наступает, когда его потери превышают 2 мг/сут. При дефиците железа развивается самая распространённая анемия - железодефицитная, т.е. анемия вследствие абсолютного снижения ресурсов железа в организме.
Эритроцитарные антигены и группы крови
В составе гликопротеинов и гликолипидов на поверхности эритроцитов существуют сотни антигенных детерминант, или антигенов (Аг), многие из которых определяют групповую принадлежность крови (группы крови). Эти Аг потенциально могут взаимодействовать с соответствующими им антителами (АТ), если бы такие АТ содержались в сыворотке крови. Однако тако- го взаимодействия в крови конкретного человека не происходит, так как иммунная система уже удалила клоны секретирующих эти АТ плазматических клеток (см. подробнее в гл. 29). Однако, если
соответствующие АТ попадают в кровь (например, при переливании чужой крови или её компонентов), развивается реакция взаи- модействия между эритроцитарными Аг и сывороточными АТ с зачастую катастрофическими последствиями (несовместимость по группам крови). В частности, при этом происходит агглютинация (склеивание) эритроцитов и их последующий гемолиз. Именно по этим причинам столь важно определять групповую принадлежность переливаемой крови (донорская кровь) и крови человека, которому переливают кровь (реципиент), а также неукоснительное выполнение всех правил и процедур при переливании крови или её компонентов (в РФ порядок переливания крови регламентирован приказом МЗ РФ и приложенной к приказу инструкцией по применению компонентов крови).
Из сотен
эритроцитарных Аг Международное общество переливания крови (The
International Society of Blood Transfusion - ISBT) к системам групп
крови по состоянию на
АБ0-СИСТЕМА
Эритроцитарные Аг системы AB0: A, B и 0 - относятся к классу гликофоринов. Их полисахаридные цепи содержат Аг-детерминанты - агглютиногены А и В. Формирование агглютиногенов А и В происходит под влиянием гликозилтрансфераз, кодируемых аллелями гена АВ0. Этот ген кодирует три полипептида (А, В, 0), два из них (гликозилтрансферазы А и В) модифицируют полисахаридные цепи гликофоринов, полипептид 0 функционально не активен. В результате поверхность эритроцитов разных лиц может содержать либо агглютиноген А, либо агглютиноген В, либо оба агглютиногена (А и В), либо не содержать ни агглютиногена А, ни агглютиногена В. В соответствии с типом экспрессии на поверхности эритроцитов агглютиногенов А и В
в системе AB0
выделены четыре группы крови, обозначаемые римскими цифрами I, II, III и
IV. Эритроциты группы крови I не содержат ни агглютиногена А, ни
агглютиногена В, её со- кращённое наименование - 0(I). Эритроциты IV
группы крови содержат оба агглютиногена - AB(IV), группы II - A(II),
группы III - B(III). Первые три группы крови обнаружил в
Агглютинины. В плазме крови к агглютиногенам А и В могут иметься АТ (соответственно α- и β-агглютинины). Плазма крови группы 0(I) содержит α- и β-агглютинины; группы A(II) - β-агглютинины, B(III) - α-агглютинины, плазма крови группы AB(IV) агглютининов не содержит.
Таблица 24-1. Содержание в крови разных групп (система AB0) агглюти- ногенов (Аг) и агглютининов (АТ)
Антигены | Антитела | |
0(I) | Нет | α, β |
A(II) | A | β |
B(III) | B | α |
AB(IV) | A, B | Нет |
Таким образом, в крови конкретного человека АТ к эритроцитарным Аг системы AB0 одновременно не присутствуют (табл. 24-1), но при переливании крови от донора с одной группой к реципиенту с другой группой может возникнуть ситуация, когда в крови реципиента одновременно будут находиться и Аг, и АТ именно к этому Аг, т.е. возникнет ситуация несовместимо- сти. Кроме того, такая несовместимость может возникнуть и по другим системам групп крови. Именно поэтому стало правилом, что переливать можно только одногруппную кровь. Если точнее, то переливают не цельную кровь, а компоненты, так как «показаний к переливанию цельной консервированной донорской крови нет, за исключением случаев острых массивных кровопотерь, когда от- сутствуют кровезаменители или свежезамороженная плазма, эритроцитная масса или их взвесь» (из приказа МЗ РФ). И именно поэтому теоретическое представление об «универсальном доноре» с кровью группы 0(I) на практике оставлено.
Rh-СИСТЕМА
Каждый человек может быть Rh-положительным либо Rh- отрицательным, что определяется его генотипом и экспрессируемыми Аг Rh-системы.
Φ Антигены. Шесть аллелей трёх генов системы Rh кодируют Аг: c, C, d, D, e, E. С учётом крайне редко встречающихся Аг системы Rh возможно 47 фенотипов этой системы. Φ Антитела системы Rh относятся к классу IgG (не обнаружены АТ только к Аг d). Rh-положительные и Rh-отрицательные лица. Если генотип конкретного человека кодирует хотя бы один из Аг C, D и E, такие лица резус-положительны (на практике резус-положительными считают лиц, имеющих на поверхности эритроцитов Аг D - сильный иммуноген). Таким образом, АТ образуются не только против «сильного» Аг D, но могут образоваться и против «слабых» Аг c, C, e и E. Резус-отрицательны только лица фенотипа cde/cde (rr).
Φ Резус-конфликт (несовместимость) возникает при переливании Rh-положительной крови донора Rh-отрицательному реципиенту либо у плода при повторной беременности Rh- отрицательной матери Rh-положительным плодом (первая беременность и/или роды Rh-положительным плодом). В этом случае развивается гемолитическая болезнь ново- рождённого.
Лейкоциты
Лейкоциты - ядерные клетки шаровидной формы (см. рис. 24-1). В цитоплазме лейкоцитов находятся гранулы. В зависимости от типа гранул лейкоциты подразделяют на гранулоциты (зернистые) и агранулоциты (незернистые).
Φ Гранулоциты (нейтрофилы, эозинофилы, базофилы) содержат специфические (вторичные) и азурофильные (лизосомы) гранулы.
Φ Агранулоциты (моноциты, лимфоциты) содержат только
азурофильные гранулы. Φ Ядро. Гранулоциты имеют дольчатое ядро разнообразной
формы, отсюда их общее название - полиморфно-ядерные
лейкоциты. Лимфоциты и моноциты имеют недольчатое
ядро, это мононуклеарные лейкоциты.
Φ Подвижность. Лейкоциты
используют кровоток как средство пассивного транспорта. Лейкоциты
имеют сократительные белки (актин, миозин) и способны к активному
перемещению, что позволяет им выходить из кровеносных сосудов, проникая
между эндотелиальными клетками (диапедез) и разрушая
секретируемыми ими ферментами базальную мембрану эндотелия.
Направленную миграцию лейкоцитов (хемокинез, хемотаксис) контролируют
различные вещества (в том числе хемоаттрактанты). Φ Функции. Лейкоциты
участвуют в заигитных реакциях, уничтожая микроорганизмы, захватывая
инородные частицы и продукты распада тканей, осуществляя реакции
гуморального и клеточного иммунитета. Число лейкоцитов в крови. В
• Физиологический лейкоцитоз - состояние, характеризующееся увеличением числа лейкоцитов в единице объёма крови выше нормы (>9х109/л). Среди физиологических лейкоцитозов выделяют функциональные и защитно-приспособительные.
Φ Функциональный лейкоцитоз обусловлен тем, что организм выполняет определённые функции (например, лейкоцитоз во время беременности, увеличение числа лейкоцитов в крови после приёма пищи или после длительной физической работы).
Φ Защитно-приспособительный лейкоцитоз развивается при воспалительных процессах, повреждении клеток и тканей (например, после инфарктов или инсультов, травмы мягких тканей), стресс-реакции.
• Лейкопения - состояние, при котором количество лейкоцитов в единице объёма крови уменьшается ниже нормы (<4х109/л). Различают первичные (врождённые или наследственные) и
вторичные (приобретённые, вследствие радиационного поражения, отравлений, применений ЛС) лейкопении. Лейкоцитарная формула - процентное содержание в периферической крови отдельных форм лейкоцитов. Подсчёт лейкоцитарной формулы крайне важен для клинической практики, посколь- ку именно лейкоциты раньше и быстрее других элементов крови реагируют на внешние и внутренние изменения (в частности, на воспаление).
Относительные и абсолютные изменения в лейкоцитарной формуле. При изменениях относительного (процентного) содержания того или иного вида лейкоцитов в лейкоцитарной формуле говорят либо об относительной нейтропении, эозинопении, лимфопении, моноцитопении (при уменьшении процентного содержания лейкоцитов соответствующего вида), либо об относительной нейтро- филии, эозонофилии, относительном моноцитозе, лимфоцитозе (при увеличении их относительного содержания).
Изменения абсолютного содержания лейкоцитов в единице объё- ма крови обозначают как абсолютную нейтропению, эозинопению, лимфопению, моноцитопению (если уменьшается их абсолютное число в единице объёма крови) или абсолютную нейтрофилию, эозинофилию, абсолютный моноцитоз или лимфоцитоз (если количество соответствующих разновидностей лейкоцитов возрастает).
Характеризуя изменения в составе лейкоцитов, необходимо оценивать как относительное, так и абсолютное (обязательно!) их содержание. Это определяется тем, что именно абсолютные величины отражают истинное содержание тех или иных видов лейкоцитов в крови, а относительные характеризуют только соотношение различных клеток между собой в единице объёма крови.
• Во многих случаях направленность относительных и абсолютных изменений совпадает. Часто встречается, например, относительная и абсолютная нейтрофилия или нейтропения.
• Отклонение относительного (процентного) содержания клеток в единице объёма крови не всегда отражает изменение их истинного, абсолютного количества. Так, относительная нейтрофилия может сочетаться с абсолютной нейтропенией (подобная ситуация возникает, если относительная нейтрофилия наблюдается в условиях значительной лейкопении: например, содержание нейтрофилов равно 80%, а общее число лейкоцитов составляет лишь 1,0х109/л).
• Чтобы определить абсолютное количество того или иного вида лейкоцитов в крови, необходимо рассчитать эту величину исходя из общего числа лейкоцитов и процентного содержания соответствующих клеток (в приведённом примере 80% от 1,0х109/л составит 0,8х109/л. Это более чем в два раза меньше 2,0х109/л - нижней границы нормального абсолютного содержания нейтрофилов).
Возрастные изменения клеток крови
• Эритроциты. При рождении и в первые часы жизни количество эритроцитов в крови повышено и составляет 6,0-7,0х1012/л.
У новорождённых наблюдают анизоцитоз с преобладанием макроцитов, а
также повышенное содержание ретикулоцитов. В течение первых суток
постнатального периода количество эритроцитов уменьшается, к 10-14-м
суткам достигает уровня взрослого и продолжает сокращаться. Минимальный
показатель наблюдается на 3-6-м месяце жизни (физиологическая анемия),
когда снижен уровень эритропоэтина. Это связано с уменьшением синтеза
эритропоэтина в печени и началом его выработки в почке. На 3-4-м году
жизни количество эритроцитов уменьшено (ниже, чем у взрослого), т.е. в
• Лейкоциты. Количество лейкоцитов у новорождённых повышено и равно 10-30х109/л. Число нейтрофилов составляет 60,5%, эозинофилов - 2%, базофилов - 0,2%, моноцитов - 1,8%, лимфоцитов - 24%. В течение первых 2 нед количество лейкоцитов сокращается до 9-15х109/л, к 4 годам уменьшается до 7-13х109/л, а к 14 годам достигает уровня, характерного для взрослого. Соотношение нейтрофилов и лимфоцитов меняется, что обусловливает возникновение так называемых физиологических перекрёстов.
Φ Первый перекрест. У новорождённого соотношение содержания этих клеток такое же, как у взрослого. В последующем содержание нейтрофилов падает, а лимфоцитов возрастает, так что на 3-4-е сутки их количество уравнивается. В дальнейшем количество нейтрофилов продолжает снижаться и к 1-2 годам достигает 25%. В этом же возрасте количество лимфоцитов составляет 65%.
Φ Второй перекрест. В течение следующих лет число нейтрофилов постепенно повышается, а лимфоцитов - снижа- ется, так что у четырёхлетних детей эти показатели снова уравниваются и составляют по 35% от общего количества лейкоцитов. Количество нейтрофилов продолжает увеличиваться, а количество лимфоцитов - уменьшаться, и к 14 го- дам эти показатели соответствуют таковым у взрослого.
Продолжительность жизни лейкоцитов
• Гранулоциты живут в циркулирующей крови 4-5 ч, а в тканях - 4-5 дней. В случаях серьёзной тканевой инфекции продолжительность жизни гранулоцитов укорачивается до нескольких часов, поскольку они очень быстро поступают в очаг инфекции, выполняют свои функции и разрушаются.
• Моноциты через 10-12 ч пребывания в кровотоке поступают в ткани. Попав в ткани, они увеличиваются в размерах и становятся тканевыми макрофагами. В этом виде они могут жить месяцами, до тех пор, пока не разрушатся, выполняя функцию фагоцитоза.
• Лимфоциты поступают в систему кровообращения постоянно в процессе дренирования лимфы из лимфатических узлов. Несколько часов спустя они поступают обратно в ткани посредством диапедеза и затем снова и снова возвращаются с лимфой в кровь. Таким образом осуществляется постоянная циркуляция лимфоцитов через ткань. Продолжительность жизни лимфоцитов составляет месяцы и даже годы в зависимости от потребностей организма в этих клетках.
Микрофаги и макрофаги. Основная функция нейтрофилов и моноцитов заключается в фагоцитозе и последующем внутриклеточном разрушении бактерий, вирусов, повреждённых и закончивших жизненный цикл клеток, чужеродных агентов. Нейтрофилы (и в некоторой степени эозинофилы) - зрелые клетки, фагоцитирующие различный материал (другое название фагоцитирующих нейтрофилов - микрофаги). Моноциты крови - незрелые клетки. Только после попадания в ткани моноциты созревают в тканевые макрофаги и приобретают способность бороться с болезнетворными агентами. Нейтрофилы и макрофаги перемещаются в тканях посредством амёбоидных движений, стимулируемых веществами, которые образуются в воспалённой области. Это притяжение нейтрофилов и макрофагов к области воспаления называется хемотаксисом.
Нейтрофилы
Нейтрофилы - наиболее многочисленный тип лейкоцитов. Они составляют 40-75% общего количества лейкоцитов. Размеры нейтрофила в мазке крови - 12 мкм; диаметр нейтрофила, мигрирующего в тканях, увеличивается почти до 20 мкм. Нейтрофилы образуются в костном мозге в течение 7 сут, через 4 сут выходят в кровоток и находятся в нём 8-12 ч. Продолжительность жизни - около 8 сут. Старые клетки фагоцитируются макрофагами.
• Пулы нейтрофилов. Выделяют три пула нейтрофилов: циркулирующий, пограничный и резервный.
Φ Циркулирующий - пассивно переносимые кровью клетки. При бактериальном инфицировании организма их количество возрастает в течение 24-48 ч в несколько (до 10) раз за счёт пограничного пула, а также за счёт ускоренного выхода резервных клеток из костного мозга.
Φ Пограничный пул состоит из нейтрофилов, связанных с эндотелиальными клетками мелких сосудов многих органов, особенно лёгких и селезёнки. Циркулирующий и пограничный пулы находятся в динамическом равновесии.
Φ Резервный пул - зрелые нейтрофилы костного мозга.
• Ядро. В зависимости от степени дифференцировки различают палочкоядерные и сегментоядерные (см. рис. 24-1, Б) нейтрофилы. В нейтрофилах у женщин один из сегментов ядра содержит вырост в форме барабанной палочки - тельце Барра, или половой хроматин (эта инактивированная Х-хромосома заметна у 3% нейтрофилов в мазке крови женщин).
♦ Палочкоядерные нейтрофилы - незрелые формы клеток с подковообразным ядром. В норме их количество состав- ляет 3-6% общего количества лейкоцитов.
♦ Сегментоядерные нейтрофилы - зрелые клетки с ядром, которое состоит из 3-5 сегментов, соединённых тонкими перемычками.
Φ Ядерные сдвиги лейкоцитарной формулы. Поскольку при микроскопии мазка крови основным критерием, позволяющим идентифицировать разные формы зрелости зернистых лейкоцитов, является характер ядра (форма, размер, интенсивность окраски), сдвиги лейкоцитарной формулы обозначаются как «ядерные».
Φ Сдвиг влево характеризуется тем, что увеличивается количество молодых и незрелых форм нейтрофилов (см. рис. 24-4). При острых гнойно-воспалительных заболеваниях, помимо лейкоцитоза, возрастает содержание молодых форм нейтрофилов, обычно палочкоядерных, реже - юных нейтрофилов (метамиелоцитов и миелоцитов), что указывает на серьёзный воспалительный процесс.
Φ Сдвиг вправо проявляется повышенным числом сегментированных ядерных форм нейтрофилов.
Φ Индекс ядерного сдвига отражает отношение процентного содержания суммы всех молодых форм нейтрофилов (па- лочкоядерных, метамиелоцитов, миелоцитов, промиелоцитов, см. рис. 24-4) к их зрелым формам. У здоровых взрослых людей индекс ядерного сдвига колеблется в диапазоне от 0,05 до 0,10. Увеличение его свидетельствует о ядерном сдвиге нейтрофилов влево, уменьшение - о сдвиге вправо.
• Гранулы нейтрофилов
Φ Азурофильные гранулы нейтрофилов содержат различные белки, разрушающие компоненты внеклеточного матрикса и обладающие антибактериальной активностью. В гранулах содержатся катепсины, эластаза, протеиназа-3 (миелобластин), азуроцидин, дефензины, катионные белки, лизоцим, арилсульфатаза. Главный фермент азурофильных гранул - миелопероксидаза. Этот белок составляет 2-4% массы нейтрофила, катализирует образование хлорноватистой кислоты и других токсичных агентов, значительно усиливающих бактерицидную активность нейтрофила.
Φ Специфические гранулы значительно мельче, но вдвое многочисленнее азурофильных. Гранулы содержат белки, обла- дающие бактериостатическими свойствами: лактоферрин, витамин В12-связывающие белки. Кроме того, в гранулах содержатся лизоцим, коллагеназа, щелочная фосфатаза, катионные белки.
• Рецепторы. В плазмолемму нейтрофилов встроены рецепторы молекул адгезии, цитокинов, колониестимулирующих факторов, опсонинов, хемоаттрактантов, медиаторов воспаления. Связывание с этими рецепторами их лигандов приводит к активации нейтрофилов (выход из сосудистого русла, миграция
в очаг воспаления, дегрануляция нейтрофилов, образование супероксидов).
• Функция нейтрофилов. В крови нейтрофилы находятся всего несколько часов (транзитом из костного мозга в ткани), а свойственные им функции выполняют за пределами сосудистого русла (выход из сосудистого русла происходит в результате хемотаксиса) и только после активации нейтрофилов. Главная функция - фагоцитоз тканевых обломков и уничтожение опсонизированных микроорганизмов. Фагоцитоз и последующее переваривание материала происходят параллельно с образованием метаболитов арахидоновой кислоты и респираторным взрывом. Фагоцитоз осуществляется в несколько этапов. После предварительного специфического распознавания подлежащего фагоцитозу материала происходит инвагинация мембраны нейтрофила вокруг частицы и образование фагосомы. Далее в результате слияния фагосомы с лизосомами образуется фаголизосома, после чего происходит уничтожение бактерии и разрушение захваченного материала. Для этого в фаголизосому поступают лизоцим, катепсин, эластаза, лактоферрин, дефензины, катионные белки; миелопероксидаза; супероксид О2- и гидроксильный радикал ОН-, образующиеся (наряду с Н2О2) при респираторном взрыве. После единственной вспышки активности нейтрофил погибает. Такие нейтрофилы составляют основной компонент гноя («гнойные» клетки).
Φ Активация. Биологически активные соединения различного происхождения: например, содержимое гранул тромбоцитов, метаболиты арахидоновой кислоты (липидные медиаторы), - воздействуя на нейтрофилы, стимулируют их активность (многие из этих веществ в то же время - хемоаттрактанты, по градиенту концентрации которых происходит миграция нейтрофилов).
Φ Липидные медиаторы продуцируют активированные нейтрофилы, а также базофилы и тучные клетки, эозинофилы, моноциты и макрофаги, тромбоциты. В активированной клетке из мембранных фосфолипидов освобождается арахидоновая кислота, из которой образуются простагландины, тромбоксаны, лейкотриены и ряд других биологически активных веществ.
Φ Респираторный взрыв. Нейтрофилы в течение первых секунд после стимуляции резко увеличивают поглощение кислоро- да и быстро расходуют значительное его количество. Это явление известно как респираторный (кислородный) взрыв. При этом образуются токсичные для микроорганизмов H2O2, супероксид O2- и гидроксильный радикал ОН-.
Φ Хемотаксис. Нейтрофилы мигрируют в очаг инфекции по градиенту концентрации многих химических факторов. Важное значение среди них имеют N-формилметионилпептиды (например, хемоаттрактант f-Met-Leu-Phe), образующиеся при расщеплении бактериальных белков или белков митохондрий при повреждении клеток.
Φ Адгезия. Активированный нейтрофил прикрепляется к эндотелию сосуда. Адгезию к эндотелию стимулируют многие агенты: анафилатоксины, ИЛ-I, тромбин, фактор активации тромбоцитов PAF, лейкотриены LTC4 и LTВ4, фактор некроза опухоли α и др.
Φ Миграция. После прикрепления к эндотелию и выхода из сосуда нейтрофилы увеличиваются в размерах, удлиняются и становятся поляризованными, образуя широкий головной конец (ламеллоподия) и суженную заднюю часть. Нейтрофил, продвигая вперёд ламеллоподию, мигрирует к источнику хемоаттрактанта. При этом гранулы перемещаются к головному концу, их мембраны сливаются с плазмолеммой, и происходит выброс содержимого гранул (в том числе протеаз) из клетки - дегрануляция.
Эозинофилы
Эозинофил - зернистый лейкоцит, участвующий в аллергических, воспалительных и антипаразитарных реакциях. Эозинофилы составляют 1-5% лейкоцитов, циркулирующих в крови. Их количество изменяется в течение суток и максимально утром. Эозинофилы в течение нескольких дней после образования остаются в костном мозге, затем циркулируют в крови 3-8 ч, большинство из них выходит из кровотока. Эозинофилы мигрируют в ткани, контактирующие с внешней средой (слизистые оболочки дыхательных и мочеполовых путей, кишечника). Размер эозинофила в крови >12 мкм, он увеличивается после выхода в соединительную ткань до 20 мкм. Продолжительность жизни - предположитель-
но 8-14 дней. Эозинофилы на поверхности имеют мембранные рецепторы Fc-фрагментов IgG, IgM и IgE, компонентов комплемента C1s, C3a, C3b, C4 и C5a, хемокина эотаксина, интерлейкинов. Миграцию эозинофилов в тканях стимулируют эотаксин, гистамин, фактор хемотаксиса эозинофилов ECF, интерлейкин-5 и др. После выполнения своих функций (после дегрануляции) или в отсутствие факторов активации (например, ИЛ-5) эозинофилы погибают.
• Специфические гранулы. В цитоплазме эозинофила содержатся крупные и мелкие специфические гранулы (красно-оранжевые). Крупные гранулы размером 0,5-1,5 мкм имеют овоидную форму и содержат удлинённый кристаллоид. Кристаллоид имеет структуру кубической решётки и состоит в основном из антипаразитарного агента - главного щелочного белка (MBP). В крупных гранулах также имеются нейротоксин (белок Х), пероксидаза эозинофила EPO, гистаминаза, фосфолипаза D, гидролитические ферменты, кислая фосфатаза, коллагеназа, цинк, катепсин. Мелкие гранулы содержат арилсульфатазу, кислую фосфатазу, пероксидазу, катионный белок эозинофилов ECP. При аллергических и воспалительных реакциях содержимое гранул секретируется (дегрануляция).
• Метаболическая активность. Как и нейтрофилы, эозинофилы синтезируют метаболиты арахидоновой кислоты (липидные медиаторы), включая лейкотриен LTC4 и фактор активации тромбоцитов PAF.
• Активация. Эозинофилы активируются множеством факторов из самых различных клеток: интерлейкинами (ИЛ-2, ИЛ-3, ИЛ-5), колониестимулирующими факторами GM-CSF и G-CSF, фактором активации тромбоцитов PAF, фактором некроза опухолей, интерферонами и факторами их паразитов.
• Хемотаксис. Активированные эозинофилы перемещаются по градиенту факторов хемотаксиса - бактериальных продуктов и элементов комплемента. Особенно эффективны в качестве хемоаттрактантов вещества, выделяемые базофилами и тучными клетками, - гистамин и фактор хемотаксиса эозинофилов ECF.
• Функции. Уничтожение паразитов, участие в аллергических и воспалительных реакциях. Эозинофилы способны к фагоцитозу, но менее выраженному, чем у нейтрофилов.
Φ Уничтожение паразитов. Эозинофилия возникает при многих паразитарных болезнях. Эозинофилы особенно активно уничтожают паразитов в местах их внедрения в организм, но менее эффективны в отношении паразитов, достигших области окончательной локализации. После активации АТ и компонентами комплемента эозинофилы выделяют содержимое гранул и липидные медиаторы, что оказывает повреждающее действие на паразитов. Секреция содержимого гранул запускается в течение нескольких минут и может продолжаться несколько часов.
Φ Участие в аллергических реакциях. Содержимое гранул эозинофилов инактивирует гистамин и лейкотриен LTC4. Эозинофилы вырабатывают ингибитор, блокирующий дегрануляцию тучных клеток. Медленно реагирующий фактор анафилаксии (SRS-A), выделяемый базофилами и тучными клетками, также ингибируется активированными эозинофилами.
Φ Участие в воспалительных реакциях. Эозинофилы отвечают хемотаксисом на многие сигналы, исходящие из эндотелия, макрофагов, паразитов и повреждённых тканей.
Φ Побочные эффекты эозинофилов. Секретируемые эозинофилом вещества могут повреждать нормальные ткани. Так, при постоянном высоком содержании эозинофилов в крови хроническая секреция содержимого гранул эозинофилов вызывает тромбоэмболические повреждения, некроз тканей (особенно эндокарда) и образование фиброзной ткани. IgE-стимуляция эозинофилов может вызывать обратимые изменения проницаемости сосудов. Продукты секреции эо- зинофилов повреждают бронхиальный эпителий, активируют комплемент и систему свёртывания крови.
Базофилы
Базофилы составляют 0-1% общего числа лейкоцитов циркулирующей крови. В крови базофилы диаметром 10-12 мкм находятся 1-2 сут. Как и другие зернистые лейкоциты, при стимуляции могут покидать кровоток, но их способность к амёбоидному движению ограничена. Продолжительность жизни и судьба в тканях не известны.
• Специфические гранулы довольно крупные (0,5-1,2 мкм), окрашиваются метахроматически (в иной цвет, чем краситель, от
красновато-фиолетового до интенсивно-фиолетового). В гранулах содержатся различные ферменты и медиаторы. К наиболее значимым из них можно отнести гепаринсульфат (гепа- рин), гистамин, медиаторы воспаления (например, медленно реагирующий фактор анафилаксии SRS-A, фактор хемотаксиса эозинофилов ECF).
• Метаболическая активность. При активации базофилы вырабатывают медиаторы липидной природы. В отличие от тучных клеток, не обладают активностью PGD2-синтетазы и окисляют арахидоновую кислоту преимущественно до лейкотриена
LTC4.
• Функция. Активированные базофилы покидают кровоток и в тканях участвуют в аллергических реакциях. Базофилы имеют высокоаффинные поверхностные рецепторы к Fc-фрагментам IgE, а IgE синтезируют плазматические клетки при попадании в организм Аг (аллергена). Дегрануляция базофилов опосредована молекулами IgE. При этом происходит перекрёстное связывание двух и более молекул IgE. Выделение гистамина и других вазоактивных факторов при дегрануляции и окисление арахидоновой кислоты вызывают развитие аллергической реакции немедленного типа (такие реакции характерны для аллергического ринита, некоторых форм бронхиальной астмы, анафилактического шока).
Моноциты
Моноциты (см. рис. 24-1, Е) - самые крупные лейкоциты (диаметр в мазке крови около 15 мкм), их количество составляет 2-9% от всех лейкоцитов циркулирующей крови. Образуются в костном мозге, выходят в кровоток и циркулируют около 2-4 сут. Моноциты крови - фактически незрелые клетки, находящиеся на пути из костного мозга в ткани. В тканях моноциты дифференцируются в макрофаги; совокупность моноцитов и макрофагов - система мононуклеарных фагоцитов.
• Активация моноцитов. Различные вещества, образующиеся в очагах воспаления и разрушения ткани, - агенты хемотаксиса и активации моноцитов. В результате активации увеличивается размер клетки, усиливается обмен веществ, моноциты выделяют биологически активные вещества (ИЛ-1, колониестимулирующие факторы M-CSF и GM-CSF, Пг, интерфероны, факторы хемотаксиса нейтрофилов и др.).
• Функция. Главная функция моноцитов и образующихся из них макрофагов - фагоцитоз. В переваривании фагоцитированного материала участвуют лизосомные ферменты, а также формируемые внутриклеточно H2O2, OH-, O2-. Активированные моноциты/макрофаги продуцируют также эндогенные пирогены.
Φ Пирогены. Моноциты/макрофаги продуцируют эндогенные пирогены (ИЛ-1, ИЛ-6, ИЛ-8, фактор некроза опухоли TNF-α, α-интерферон) - полипептиды, запускающие метаболические изменения в центре терморегуляции (гипоталамус), что приводит к повышению температуры тела. Критическую роль играет образование простагландина PGE2. Образование эндогенных пирогенов моноцитами/ макрофагами (а также рядом других клеток) вызывают экзогенные пирогены - белки микроорганизмов, бактериальные токсины. Наиболее распространённые экзогенные пирогены - эндотоксины (липополисахариды грамотрицательных бактерий).
Макрофаг - дифференцированная форма моноцитов - крупная (около 20 мкм), подвижная клетка системы мононуклеарных фагоцитов. Макрофаги - профессиональные фагоциты, они найдены во всех тканях и органах; это мобильная популяция клеток. Продолжительность жизни макрофагов - месяцы. Макрофаги подразделяются на резидентные и подвижные. Резидентные макрофаги содержатся в тканях в норме в отсутствие воспаления. Среди них различают свободные, имеющие округлую форму, и фиксированные макрофаги - звёздообразной формы клетки, прикрепляющиеся своими отростками к внеклеточному матриксу или к другим клеткам.
• Свойства макрофага зависят от их активности и локализации. В лизосомах макрофагов содержатся бактерицидные агенты: миелопероксидаза, лизоцим, протеиназы, кислые гидролазы, катионные белки, лактоферрин, супероксиддисмутаза - фермент, способствующий образованию H2O2, OH-, O2-. Под плазмолеммой в большом количестве имеются актиновые микрофиламенты, микротрубочки, промежуточные филаменты, необходимые для миграции и фагоцитоза. Макрофаги мигрируют по градиенту концентрации многих веществ, поступающих из различных источников. Активированные макрофаги
• образуют цитоплазматические псевдоподии неправильной формы, участвующие в амебоидном движении и фагоцитозе. Функции. Макрофаги захватывают из крови денатурированные белки, состарившиеся эритроциты (фиксированные макрофаги печени, селезёнки, костного мозга). Макрофаги фагоцитируют обломки клеток и тканевого матрикса. Неспецифический фагоцитоз характерен для альвеолярных макрофагов, захватывающих пылевые частицы различной природы, сажу и т.п. Специфический фагоцитоз происходит при взаимодействии макрофагов с опсонизированной бактерией. Активированный макрофаг секретирует более 60 факторов. Макрофаги проявляют антибактериальную активность, выделяя лизоцим, кислые гидролазы, катионные белки, лактоферрин, H2O2, OH-, O2-. Противоопухолевая активность заключается в прямом цитотоксическом действии H2O2, аргиназы, цитолитической протеиназы, фактора некроза опухоли из макрофагов. Макрофаг - антигенпредставляющая клетка: он процессирует Аг и представляет его лимфоцитам, что приводит к стимуляции лимфоцитов и запуску иммунных реакций (см. подробнее в главе 29). Интерлейкин-1 из макрофагов активирует Т-лимфоцигы и в меньшей степени - В-лимфоциты. Макрофаги продуцируют липидные медиаторы: ПгE2 и лейкотриены, фактор активации тромбоцитов PAF. Клетка также выделяет α-интерферон, блокирующий репликацию вирусов. Активированный макрофаг секретирует ферменты, разрушающие внеклеточный матрикс (эластазу, гиалуронидазу, коллагеназу). С другой стороны, факторы роста, синтезируемые макрофагом, эффективно стимулируют пролиферацию эпителиальных клеток (трансформирующий фактор роста TGFα, bFGF), пролиферацию и активацию фибробластов (фактор роста из тромбоцитов PDGF), синтез коллагена фибробластами (трансформирующий фактор роста TGFp), формирование новых кровеносных сосудов - ангиогенез (фактор роста фибробластов bFGF). Таким образом, основные процессы, лежащие в основе заживления раны (реэпителизация, образование внеклеточного матрикса, восстановление повреж- дённых сосудов), опосредованы факторами роста, производимыми макрофагами. Вырабатывая ряд колониестимулирующих факторов (макрофагов - M-CSF, гранулоцитов - G-CSF), макрофаги влияют на дифференцировку клеток крови.
Лимфоциты
Лимфоциты (см. рис. 24-1, Д) составляют 20-45% общего числа лейкоцитов крови. Кровь - среда, в которой лимфоциты цирку- лируют между органами лимфоидной системы и другими тканями. Лимфоциты могут выходить из сосудов в соединительную ткань, а также мигрировать через базальную мембрану и внедряться в эпителий (например, в слизистой оболочке кишечника). Продолжительность жизни лимфоцитов от нескольких месяцев до нескольких лет. Лимфоциты - иммунокомпетентные клетки, имеющие огромное значение для иммунных защитных реакций организма (см. подробнее в гл. 29). С функциональной точки зрения различают В-, Т-лимфоциты и NK-клетки.
• B-лимфоциты (произносят как «бэ») образуются в костном мозге и составляют менее 10% лимфоцитов крови. Часть В-лимфоцитов в тканях дифференцируется в клоны плазматических клеток. Каждый клон синтезирует и секретирует АТ только против одного Аг. Другими словами, плазматические клетки и синтезируемые ими АТ обеспечивают гуморальный иммунитет.
• T-лимфоциты. Клетка-предшественница T-лимфоцитов поступает в тимус из костного мозга. Дифференцировка T-лимфоцитов происходит в тимусе. Зрелые Т-лимфоциты покидают тимус, их обнаруживают в периферической крови (80% и более всех лимфоцитов) и лимфоидных органах. Т-лимфоциты, как и В-лимфоциты, реагируют (т.е. узнают, размножаются и дифференцируются) на конкретные Аг, но в отличие от В-лимфоцитов участие Т-лимфоцитов в иммунных реакциях сопряжено с необходимостью узнавать в мембране других клеток белки главного комплекса гистосовместимости MHC. Основные функции Т-лимфоцитов - участие в клеточном и гуморальном иммунитете (так, Т-лимфоциты уничтожают аномальные клетки своего организма, участвуют в аллергических реакциях и в отторжении чужеродного трансплантата). Среди Т-лимфоцитов различают CD4+- и CD8+-лимфоциты. CD4+-лимфоцитьI (Т-хелперы) поддерживают пролиферацию и дифференцировку В-лимфоцитов и стимулируют образование цитотоксических Т-лимфоцитов, а также способствуют пролиферации и дифференцировке супрессорных Т-лимфоцитов.
• NK-клетки - лимфоциты, лишённые характерных для Т- и В-клеток поверхностно-клеточных детерминант. Эти клетки составляют около 5-10% всех циркулирующих лимфоцитов, содержат цитолитические гранулы с перфорином, уничтожают трансформированные (опухолевые) и инфицированные вирусами, а также чужеродные клетки.
Кровяные пластинки
Тромбоциты, или кровяные пластинки (рис. 24-13), - фрагменты расположенных в красном костном мозге мегакариоцитов. Размеры кровяных пластинок в мазке крови составляют 3-5 мкм. Количество тромбоцитов в циркулирующей крови - 190-405х109/л. Две трети кровяных пластинок находится в крови, остальные депонированы в селезёнке. Продолжительность жизни тромбоцитов - 8 дней. Старые тромбоциты фагоцитируются в селезёнке, печени и костном мозге. Циркулирующие в крови тромбоциты могут при ряде обстоятельств активироваться, активированные тромбоциты участвуют в свёртывании крови и восстановлении целостности стенки сосуда. Одно из важнейших свойств активированных кровяных пластинок - их способность ко взаимной адгезии и агрегации, а также адгезии к стенке кровеносных сосудов.
• Гликокаликс. Выступающие наружу части молекул, составляющих интегральные белки плазматической мембраны, богатые полисахаридными боковыми цепями (гликопротеины), создают внешнее покрытие липидного бислоя - гликокаликс. Здесь же адсорбированы факторы коагуляции и иммуноглобулины. На наружных частях гликопротеиновых молекул находятся рецепторные места. После их соединения с агонистами индуцируется сигнал активации, передающийся к внутренним частям периферической зоны тромбоцитов.
• Плазматическая мембрана содержит гликопротеины, выполняющие роль рецепторов при адгезии и агрегации тромбоцитов. Так, гликопротеин Ib (GP Ib, Ib-IX) важен для адгезии тромбоцитов, он связывается с фактором фон Виллебранда и подэндотелиальной соединительной тканью. Гликопротеин IV (GP IIIb) - рецептор тромбоспондина. Гликопротеин IIb-IIIa (GP IIb-IIIa) - рецептор фибриногена, фибронектина, тромбоспондина, витронектина, фактора фон Виллебранда; эти факторы способствуют адгезии и агрегации тромбо-
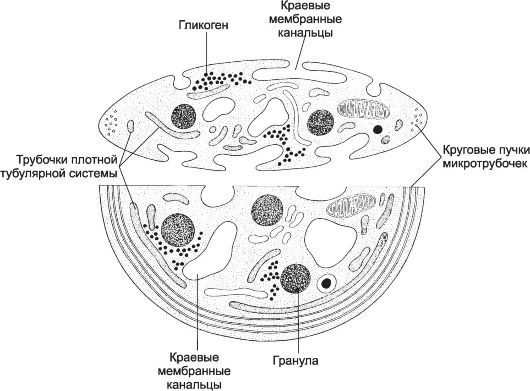
Рис. 24-13. Тромбоцит имеет форму овального или округлого диска. В цитоплазме видны мелкие скопления гликогена и крупные гранулы нескольких типов. Периферическая часть содержит циркулярные пучки микротрубочек (необходимы для сохранения овальной формы тромбоцита), а также актин, миозин, гельзолин и другие сократительные белки, нужные для изменения формы тромбоцитов, их взаимной адгезии и агрегации, а также для ретракции сгустка крови, образовавшегося при агрегации тромбоцитов. По периферии тромбоцита расположены также анастомозирующие мембранные канальцы, открывающиеся во внеклеточную среду и необходимые для секреции содержимого α-гранул. В цитоплазме рас- сеяны узкие, неправильной формы мембранные трубочки, составляющие плотную тубулярную систему. Трубочки содержат циклооксигеназу (необходима для окисления арахидоновой кислоты и образования тромбоксана TXA2. Ацетилсалициловая кислота (аспирин) необратимо ацетилирует циклооксигеназу, локализованную в трубочках плотной тубулярной системы, что блокирует образование тромбоксана, необходимого для агрегации тромбоцитов; в результате функция тромбоцитов нарушается и время кровотечения удлиняется) [11].
цитов, опосредуя формирование между ними «мостиков» из фибриногена.
• Гранулы. Тромбоциты содержат три типа гранул (α-, δ-, λ-) и микропероксисомы.
Φ α-Гранулы содержат различные гликопротеины (фибронектин, фибриноген, фактор фон Виллебранда), связывающие гепарин белки (например, фактор 4 тромбоцитов), тромбоцитарный фактор роста PDGF и трансформирующий фактор роста β, плазменные факторы свёртывания VIII и V, а также тромбоспондин (способствует адгезии и агрегации тромбоцитов) и рецептор клеточной адгезии GMP-140. Φ Другие гранулы. δ-Гранулы накапливают неорганический фосфат P., АДФ, АТФ, Ca2+, серотонин и гистамин (серотонин и гистамин синтезируются не в тромбоцитах, а поступают из плазмы). λ-Гранулы содержат лизосомные ферменты и могут участвовать в растворении тромба. Микропероксисомы обладают пероксидазной активностью. Функции тромбоцитов. В физиологических условиях тромбоциты находятся в неактивном состоянии, т.е. свободно циркулируют в крови, не адгезируют друг с другом и не прикрепляются к эндотелию сосуда (частично это связано с тем, что эндотелиальные клетки вырабатывают простациклин PGI2, препятствующий адгезии тромбоцитов к стенке сосуда). Однако при повреждении кровеносного сосуда тромбоциты вместе с плазменными факторами свёртывания крови образуют сгусток крови - тромб, предотвращающий кровотечение.
• Остановка кровотечения происходит в три этапа. 1. Сначала происходит сокращение просвета кровеносного сосуда. 2. Далее в повреждённом участке сосуда тромбоциты прикрепляются к стенке сосуда и, наслаиваясь друг на друга, образуют тромбоцитарную гемостатическую пробку (белый тромб). Эти процессы (изменение формы кровяных пластинок, их адгезия и агрегация) обратимы, так что слабо агрегированные тромбоциты могут отделяться от гемостатических тромбоцитарных пробок и возвращаться в кровоток. 3. Наконец растворимый фибриноген превращается в нерастворимый фибрин, который формирует прочную трёхмерную сеть, в петлях которой расположены клетки крови, в том числе и эритроциты. Это фибриновый, или красный, тромб.
Φ Образованию фибринового тромба предшествует каскад протеолитических реакций, приводящий к активации фермента тромбина, который и превращает фибриноген в фибрин. Таким образом, на одном из этапов тромбообразования происходит свёртывание крови (гемокоагуляция) - часть системы гемостаза, самое непосредственное отношение к которой имеют тромбоциты.
Гемостаз
В прикладном смысле термин «гемостаз» (от гр. haima - кровь, stasis - остановка) применяют, обозначая собственно процесс остановки кровотечения. Система гемостаза включает факторы и механизмы трёх категорий: свёртывающую, противосвёртываю- щую и фибринолитическую.
Φ Свёртывающая система, а именно плазменные факторы свёртывания (прокоагулянты), формируя сложный гемокоагуляционный каскад, обеспечивает коагуляцию фибриногена и тромбообразование (рис. 24-14). Каскад реакций, при- водящий к образованию тромбина, может осуществляться двумя путями - внешним (на рисунке слева и сверху) и внутренним (на рисунке справа и сверху). Для инициации реакций внешнего пути необходимо появление тканевого фактора на внешней поверхности плазматической мембраны тромбоцитов, моноцитов и эндотелия. Внутренний путь начинается с активации фактора XII при его контакте с по- вреждённой поверхностью эндотелия. Понятие о внутреннем и внешнем путях свёртывания весьма условно, так как каскад реакций свёртывания крови идёт преимущественно внешним путём, а не по двум относительно независимым путям.
Φ Противосвёртывающая система физиологических антикоагулянтов обусловливает торможение или блокаду свёртыва- ния крови.
Φ Фибринолитическая система осуществляет лизис фибринового тромба.
• Плазменные факторы свёртывания - различные компоненты плазмы, осуществляющие образование сгустка крови. Факторы свёртывания обозначают римскими цифрами (к номеру активированной формы фактора добавляют строчную букву «а»).
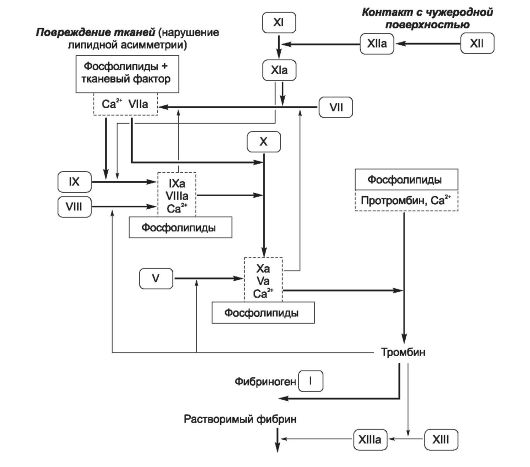
Рис. 24-14. Гемокоагуляционный каскад [8]. Активация фактора XII запускает внутренний (контактный) механизм, высвобождение тканевого фактора, а активация фактора VII - внешний механизм свёртывания. Оба пути приводят к активации фактора Х. В прямоугольниках с закруглён- ными углами - номера плазменных факторов свёртывания. Ферментные комплексы - рядом расположенные прямоугольники сплошного и прерывистого начертания границ.
♦ I - растворимый фибриноген, превращающийся в нерас- творимый фибрин под влиянием тромбина (фактор На).
♦ II - протромбин (профермент), превращающийся в протеазу тромбин (фактор IIa) под влиянием комплекса фактора Xa, фосфолипидов мембран тромбоцитов и других клеток, Са2+ и фактора Va.
♦ III - тканевый фактор. Комплекс тканевого фактора, фосфолипидов, фактора VIIa и Са2+ запускает внешний механизм свёртывания.
♦ IV - Ca2+.
♦ V - проакцелерин - предшественник акцелерина (Va) - белка-активатора мембранного комплекса Xa-Va-Ca2+.
♦ VII - проконвертин (профермент), VIIa - протеаза, ак- тивирующая факторы X и IX.
♦ VIII - неактивный антигемофильный глобулин А - пред- шественник фактора VIIIa (активного антигемофильного глобулина) - белка-активатора мембранного комплекса IXa-VIIIa-Ca2+. Недостаточность фактора VIII обусловливает развитие классической гемофилии А, наблюдающейся только у мужчин.
♦ IX - неактивный антигемофильный глобулин В (профермент, неактивный фактор Кристмаса) - предшественник активного антигемофильного фактора В (активный фактор Кристмаса) - протеазы, активирующей фактор X. Недостаточность фактора IX приводит к развитию гемофилии В (болезнь Кристмаса).
♦ X - неактивный фактор Стюарта-Прауэр (активная форма - фактор Xa - протеаза, активирующая фактор II), недостаточность фактора Стюарта приводит к дефектам свёртывания.
♦ XI - профермент контактного пути свёртывания крови - неактивный плазменный предшественник тромбопластина (активная форма - фактор XIa - сериновая протеаза, превращающая фактор IX в фактор IXa). Недостаточность фактора XI является причиной кровоточивости.
♦ XII - неактивный фактор Хагемана - профермент кон- тактного пути свёртывания крови, активная форма - фактор XIIa (активный фактор Хагемана) - активирует фактор XI, прекалликреин (профермент контактного пути свёртывания крови), плазминоген.
♦ XIII - фибринстабилизирующий фактор (фактор Лаки- Лорана) - активированный тромбином фактор XIII (фактор XIIIa), образует нерастворимый фибрин, катализируя образование амидных связей между молекулами фибрина-мономера, фибрином и фибронектином.
• Внешний путь занимает центральное место в свёртывании крови. Ферментные мембранные комплексы (см. ниже) образуются только при наличии на внешней поверхности плазматической мембраны тромбоцитов, эндотелиальных клеток тканевого фактора и отрицательно заряженных фосфолипидов, т.е. при формировании отрицательно заряженных (тромбогенных) участков и экспозиции апопротеина тканевого фактора. При этом тканевый фактор и поверхность клеточной мембраны становятся доступными для плазменных факторов. Ф Активация ферментов. В циркулирующей крови содержатся проферменты (факторы II, VII, IX, X). Белки-кофакторы (факторы Vа, VIIIa, а также тканевый фактор - фактор III) способствуют превращению проферментов в ферменты (сериновые протеазы). Ф Ферментные мембранные комплексы. При включении каскадного механизма активации ферментов последовательно образуются три ферментных комплекса, связанных с фосфолипидами клеточной мембраны. Каждый комплекс состоит из протеолитического фермента, белка-кофактора и ионов Са2+: VIIa-тканевый фактор-фосфолипид-Са2+, Ка-VIIIа-фосфолипид-Са2+ (теназный комплекс, активатор фактора Х); Xa-Va-фосфолипид-Ca2+ (протромбиназный комплекс, активатор протромбина). Каскад ферментативных реакций завершается образованием мономеров фибрина и последующим формированием тромба. Ф Ионы Ca2+. Взаимодействие ферментных комплексов с клеточными мембранами происходит с участием ионов Са2+. Остатки γ-карбоксиглутаминовой кислоты в факторах \VIIIа, Ка, Xа и протромбине обеспечивают взаимодействие этих факторов посредством Са2+ с отрицательно заряженными фосфолипидами клеточных мембран. Без ионов Са2+ кровь не свёртывается. Именно поэтому, чтобы предотвратить свёртывание крови, снижают концентрацию Ca2+ деионизацией кальция цитратом (цитратная кровь) либо осаждением кальция в виде оксалатов (оксалатная кровь). Ф Витамин К. Карбоксилирование остатков глутаминовой кислоты в проферментах прокоагулянтного пути катализирует карбоксилаза, коферментом которой является восстановленная форма витамина К (нафтохинон). Поэтому
недостаточность витамина К тормозит свёртывание крови и сопровождается кровоточивостью, подкожными и внутренними кровоизлияниями, а структурные аналоги витамина К (например, варфарин) применяются в клинической практике для предупреждения тромбозов.
• Контактный путь свёртывания крови начинается со взаимодействия профермента (фактор XII) с повреждённой эндотелиальной поверхностью сосудистой стенки. Такое взаимодействие приводит к активации фактора XII и инициирует образование мембранных ферментных комплексов контактной фазы свёр- тывания. Эти комплексы содержат ферменты калликреин, факторы XIa (плазменный предшественник тромбопластина) и XIIa (фактор Хагемана), а также белок-кофактор - высокомолекулярный кининоген.
• Противосвёртывающая система крови. Физиологические ингибиторы играют важную роль в поддержании крови в жидком состоянии и препятствуют распространению тромба за пределы повреждённого участка сосуда. Тромбин, образующийся в результате реакций свёртывания крови и обеспечивающий формирование тромба, вымывается током крови из тромба; в дальнейшем тромбин инактивируется при взаимодействии с ингибиторами ферментов свёртывания крови и в то же время активирует антикоагулянтную фазу, тормозящую образование тромба.
Ф Антикоагулянтная фаза. Эту фазу запускает тромбин (фактор II), вызывая образование ферментных комплексов антикоагулянтной фазы на неповреждённом эндотелии сосудов. В реакциях антикоагулянтной фазы, помимо тромбина, участвуют тромбомодулин эндотелиальных клеток, витамин К-зависимая сериновая протеаза - протеин С, активирующий протеин S и плазменные факторы свёртывания Va и
VIIIa.
Ф Физиологические ингибиторы ферментов свёртывания крови (антитромбин III, гепарин, а2-макроглобулин, антиконвертин, aj-антитрипсин) ограничивают распространение тромба местом повреждения сосуда.
• Фибринолитическая система. Тромб может раствориться в течение нескольких дней после образования. При фибринолизе - ферментативном расщеплении волокон фибрина - об-
разуются растворимые пептиды. Фибринолиз происходит под действием сериновой протеазы плазмина, точнее - при взаимодействии фибрина, плазминогена и тканевого активатора плазминогена.
• Лабораторные показатели системы гемостаза. Кровь здорового человека in vitro свёртывается за 5-10 мин. При этом образование протромбиназного комплекса занимает 5-8 мин, активация протромбина - 2-5 с и превращение фибриногена в фибрин - 2-5 с. В клинической практике для оценки гемостаза оценивают содержание разных компонентов системы свёртывания, антикоагулянтов и фибринолиза. К простейшим лабораторным методам относят определение времени кровотечения, тромбинового и протромбинового времени, активированного частичного тромбопластинового времени и протромбинового индекса.
Обобщение главы
Кровь - циркулирующая в сосудистой системе жидкая соединительная ткань, обладающая важнейшими функциями: транспортной, иммунной, свёртывания крови и поддержания гомеостаза организма.
В среднем у взрослого человека содержится приблизительно
Плазма содержит белки (альбумины, глобулины, фибриноген, ферменты, гормоны и др.), липиды (холестерин, триглицериды) и углеводы (глюкоза).
Эритроциты - безъядерные дископодобные клетки, которые доставляют кислород всем клеткам организма за счёт гемоглобина.
Изменения количества эритроцитов, их формы, размеров, цвета и зрелости являются ценным индикатором для диагностики раз- личных заболеваний.
В конце 4-го месяца жизни старые эритроциты поглощаются макрофагами. Их гемоглобин, включая железо, перерабатывается в дигностически важное вещество - билирубин.
Лейкоциты морфологически подразделяются на гранулоциты (эозинофилы, базофилы и нейтрофилы) и агранулоциты (моноциты и лимфоциты). Лимфоциты функционально подразделяются на T- и B-клетки с различными подгруппами.
Лейкоциты защищают организм от инфекции, используя фагоцитоз и различные антимикробные средства, выделяя медиаторы, контролирующие воспаление, и тем самым способствуя излечению.
Гемопоэз представляет собой развитие клеток крови из нейтральных мультипотентных стволовых клеток костного мозга. Не- зрелые клетки дифференцируются в зрелые клетки под влиянием гемопоэтинов и других цитокинов.
Тромбоциты (кровяные пластинки) - небольшие неправильной формы безъядерные структуры, которые вместе с белками плазмы контролируют свёртывание крови.
При переливании крови донор и реципиент должны избегать агглютинации между ассоциированными с эритроцитами антигенами A, B и Rh и анти-А-, анти-B- и анти-Rh-антителами, находящимися в плазме.