Руководство по кардиологии : Учебное пособие в 3 т. / Под ред. Г.И. Сторожакова, А.А. Горбаченкова. - Т. 2. - 512 с. : ил.
|
|
|
|
ГЛАВА 7 ЛЕГОЧНОЕ СЕРДЦЕ
Легочное сердце (ЛС) - это гипертрофия и/или дилятация правого желудочка (ПЖ), возникшая вследствие легочной артериальной гипертензии, обусловленной заболеваниями, поражающими функцию и/или структуру легких, и не связанными с первичной патологией левых отделов сердца или врожденными пороками сердца. ЛС формируется вследствие заболеваний бронхов и легких, торакодиафрагмальных поражений или патологии легочных сосудов. Развитие хронического легочного сердца (ХЛС) чаще всего обусловлено хронической легочной недостаточностью (ХЛН), а основной причиной формирования ХЛС является альвеолярная гипоксия, вызывающая спазм легочных артериол.
Диагностический поиск направлен на выявление основного заболевания, приведшего к развитию ХЛС, а также оценку ХЛН, легочной гипертензии и состояния ПЖ.
Лечение ХЛС - это терапия основного заболевания, являющегося причиной ХЛС (хронический обструктивный бронхит, бронхиальная астма и др.), устранение альвеолярной гипоксии и гипоксемии со снижением легочной артериальной гипертензии (тренировка дыхательной мускулатуры, электростимуляция диафрагмы, нормализация кислородтранспортной функции крови (гепарин, эритроцитаферез, гемосорбция), длительная кислородотерапия (ДКТ), альмитрин), а также коррекция правожелудочковой сердечной недостаточности (ингибиторы АПФ, диуретики, блокаторы альдостерона, антагонисты рецепторов ангиотезина II). ДКТ - самый эффективный метод лечения ХЛН и ХЛС, способный увеличить продолжительность жизни больных.
Ключевые слова: легочное сердце, легочная гипертензия, хроническая легочная недостаточность, хроническое легочное сердце, правожелудочковая сердечная недостаточность.
ОПРЕДЕЛЕНИЕ
Легочное сердце - это гипертрофия и/или дилатация правого желудочка, возникшая вследствие легочной артериальной гипертензии, обусловленной заболеваниями, поражающими функцию и/или структуру легких и не связанными с первичной патологией левых отделов сердца или врожденными пороками сердца.
Легочное сердце (ЛС) формируется на основе патологических изменений самого легкого, нарушений внелегочных механизмов дыхания, обеспечивающих вентиляцию легкого (повреждение дыхательной мускулатуры, нарушение центральной регуляции дыхания, эластичности костно-хрящевых образований грудной клетки или проведения нервного импульса по n. diaphragmicus, ожирение), а также поражения легочных сосудов.
КЛАССИФИКАЦИЯ
В нашей стране наибольшее распространение получила классификация легочного сердца, предложенная Б.Е. Вотчалом в 1964 году (табл. 7.1).
Острое ЛС связано с резким повышением легочного артериального давления (ЛАД) с развитием правожелудочковой недостаточности и обусловлено чаще всего тромбоэмболией основного ствола или крупных ветвей легочной артерии (ТЭЛА). Однако врач иногда сталкивается с подобным состоянием и при выключении из кровообращения больших участков легочной ткани (двусторонняя обширная пневмония, астматический статус, вентильный пневмоторакс).
Подострое легочное сердце (ПЛС) чаще всего является следствием рецидивирующей тромбоэмболии мелких ветвей легочной артерии. Ведущим клиническим симптомом является нарастающая одышка с быстро развивающейся (в течение месяцев) правожелудочковой недостаточностью. К другим причинам ПЛС следует отнести нервно-мышечные заболевания (миастения, полиомиелит, повреждение диафрагмального нерва), выключение из акта дыхания значительной части респираторного отдела легкого (тяжелое течение бронхиальной астмы, милиарный туберкулез легкого). Частой причиной ПЛС являются онкологические заболевания легких, желудочно-кишечного тракта, молочной железы и другой локализации, вследствие карциноматоза легких, а также сдавления сосудов легких прорастающей опухолью с последующим тромбозом.
Хроническое легочное сердце (ХЛС) в 80% случаев возникает при поражении бронхолегочного аппарата (чаще всего при ХОБЛ) и связано с медленным и постепенным повышением давления в легочной артерии в течение многих лет.
Развитие ХЛС прямо взаимосвязано с хронической легочной недостаточностью (ХЛН). В клинической практике используют классификацию ХЛН, основанную на наличии одышки. Выделяют 3 степени ХЛН: появление одышки при доступных ранее усилиях - I степень, одышка при обычных нагрузках - II степень, одышка в покое - III степень. Приведенную классификацию иногда уместно дополнить данными о газовом составе крови и патофизиологическими механизмами развития легочной недостаточности (табл. 7.2), что позволяет выбрать патогенетически обоснованные терапевтические мероприятия.
Классификация легочного сердца (по Вотчалу Б.Е., 1964)
Таблица 7.1.
Характер течения | Состояние компенсации | Преимущественный патогенез | Особенности клинической картины |
Острое легочное сердце: развитие в течение нескольких часов, дней | Декомпенсированное | Васкулярный | Массивная тромбоэмболия легочной артерии |
Бронхолегочный | Клапанный пневмоторакс, пневмомедиастинум. Бронхиальная астма, затяжной приступ. Пневмония с большой площадью поражения. Экссудативный плеврит с массивным выпотом | ||
Подострое легочное сердце: развитие в течение нескольких недель, месяцев | Компенсированное. Декомпенсированное | Васкулярный | Повторные мелкие тромбоэмболии в системе легочной артерии - тромбы, эмболы, яйца паразитов, обломки эритроцитов при серповидно-клеточной анемии и др. |
Бронхолегочный | Повторные затяжные приступы бронхиальной астмы. Раковый лимфангит легких | ||
Торакодиафрагмальный | Хроническая гиповентиляция центрального и периферического происхождения при ботулизме, полиомиелите, миастении и др. |
Окончание табл. 7.1.
Хроническое легочное сердце: развитие в течение ряда лет | Компенсированное. Декомпенсированное по правожелудочковому типу | Васкулярный | Первичная легочная гипертензия. Артерииты. Повторные ТЭЛА. Резекция легкого |
Бронхолегочный | Обструктивные процессы в бронхах и легких (хронический бронхит, бронхиальная астма, эмфизема легких, диффузный пневмосклероз с эмфиземой). Рестриктивные процессы - фиброзы и гранулематозы. Поликистоз легких | ||
Торакодиафрагмальный | Поражение позвоночника и грудной клетки с деформацией ее. Плевральные спайки. Ожирение (синдром Пиквика) |
Примечание. Диагноз легочного сердца ставится после диагноза основного заболевания: при формулировке диагноза используются только первые две графы классификации. Графы 3 и 4 способствуют углубленному пониманию сущности процесса и выбору терапевтической тактики
Таблица 7.2.
Клинико-патофизиологическая классификация хронической легочной недостаточности
(Александров О.В., 1986)
Стадия хронической легочной недостаточности | Наличие клинических признаков | Данные инструментальной диагностики | Лечебные мероприятия |
I. Вентиляционные нарушения (скрытая) | Клинические проявления отсутствуют или минимально выражены | Отсутствие или наличие только вентиляционных нарушений (обструктивный тип, рестриктивный тип, смешанный тип) при оценке ФВД | Базисная терапия хронического заболевания - антибиотики, бронхолитики, стимуляция дренажной функции легкого. ЛФК, электростимуляция диафрагмы, аэроионотерапия |
П. Вентиляционногемодинамические и вентиляционно-гемические нарушения | Клинические проявления: одышка, цианоз | К нарушениям ФВД присоединяются ЭКГ, эхокардиографические и рентгенографические признаки перегрузки и гипертрофии правых отделов сердца, изменения газового состава крови, а также эритроцитоз, повышение вязкости крови, морфологические изменения эритроцитов | Дополняются длительной оксигенотерапией (если раО2<60мм рт.ст.), альмитрином, ЛФК, кардиологическими средствами |
III. Метаболические нарушения | Клинические проявления резко выражены | Усиление описанных выше нарушений. Метаболический ацидоз. Гипоксемия, гиперкапния | Дополняются экстракорпоральными методами лечения (эритроцитаферез, гемосорбция, плазмаферез, экстракорпоральная мембранная оксигенация) |
В представленной классификации ХЛН диагноз ХЛС с большой вероятностью может быть поставлен на II и III стадии процесса. При I стадии ХЛН (латентной) обнаруживаются подъемы ЛАД обычно в ответ на физическую нагрузку и при обострении заболевания при отсутствии признаков гипертрофии ПЖ. Это обстоятельство позволило высказать мнение (Н.Р. Палеев), что для диагностики начальных проявлений ХЛС необходимо использовать не наличие или отсутствие гипертрофии миокарда ПЖ, а повышение ЛАД. Однако в клинической практике прямое измерение ЛАД у этой группы больных недостаточно обоснованно.
С течением времени возможно развитие декомпенсации ХЛС. При отсутствии специальной классификации недостаточности ПЖ используют известную классификацию сердечной недостаточности (СН) по В.Х. Василенко и Н.Д. Стражеско, которая как правило применяется при СН, развившейся вследствие поражения левого желудочка (ЛЖ) или обоих желудочков. Наличие у больных ХЛС левожелудочковой СН чаще всего обусловлено двумя причинами: 1) ХЛС у лиц старше 50 лет часто сочетается с ИБС, 2) системная артериальная гипоксемия у больных ХЛС ведет к дистрофическим процессам в миокарде ЛЖ, к его умеренной гипертрофии и сократительной недостаточности.
Главной причиной развития хронического легочного сердца являются хронические обструктивные заболевания легких.
ПАТОГЕНЕЗ
В основе развития хронического ЛС лежит постепенное формирование легочной артериальной гипертензии, обусловленной несколькими патогенетическими механизмами. Основной причиной ЛГ у больных с бронхо-легочной и торакодиафрагмальной формами ХЛС является альвеолярная гипоксия, роль которой в развитии легочной вазоконстрикции впервые была показана в 1946 г. U. Von Euler и G. Lijestrand. Развитие рефлекса Эйлера-Лильестранда объясняют несколькими механизмами: эффект гипоксии связывают с развитием деполяризации гладкомышечных клеток сосудов и их сокращением вследствие изменения функции калиевых каналов клеточных мемб-
ран, воздействием на стенку сосудов эндогенных вазоконстрикторных медиаторов, таких как лейкотриены, гистамин, серотонин, ангиотензин II и катехоламины, продукция которых в условиях гипоксии значительно возрастает.
Гиперкапния также способствует развитию легочной гипертензии. Однако высокая концентрация СО2, по-видимому, действует не прямо на тонус легочных сосудов, а опосредованно - преимущественно через обусловленный ею ацидоз. Кроме того, задержка СО2 способствует снижению чувствительности дыхательного центра к СО2, что еще больше уменьшает вентиляцию легких и способствует легочной вазоконстрикции.
Особое значение в генезе ЛГ придается дисфункции эндотелия, проявляющейся снижением синтеза вазодилатирующих антипролиферативных медиаторов (NO, простациклин, простагландин Е2) и повышением уровня вазоконстрикторов (ангиотензин, эндотелин-1). Дисфункция эндотелия легочных сосудов у больных ХОБЛ связана с гипоксемией, воспалением, а также воздействием сигаретного дыма.
У больных ХЛС происходят структурные изменения сосудистого русла - ремоделирование легочных сосудов, характеризующееся утолщением интимы за счет пролиферации гладкомышечных клеток, отложением эластических и коллагеновых волокон, гипертрофией мышечного слоя артерий с уменьшением внутреннего диаметра сосудов. У больных ХОБЛ вследствие эмфиземы происходит редукция капиллярного русла, компрессия легочных сосудов.
Кроме хронической гипоксии, наряду со структурными изменениями сосудов легких, на повышение легочного давления влияет и целый ряд других факторов: полицитемия с изменением реологических свойств крови, нарушение метаболизма вазоактивных веществ в легких, увеличение минутного объема крови, что обусловлено тахикардией и гиперволемией. Одной из возможных причин гиперволемии являются гиперкапния и гипоксемия, способствующие увеличению концентрации альдостерона в крови и, соответственно, задержке Na+ и воды.
У пациентов с тяжелой степенью ожирения развивается синдром Пиквика (названный по произведению Чарльза Диккенса), который проявляется гиповентиляцией с гиперкапнией, что связано с понижением чувствительности дыхательного центра к СО2, а также нарушением вентиляции из-за механического ограничения жировой тканью с дисфункцией (утомлением) дыхательной мускулатуры.
Повышенное АД в легочной артерии вначале может способствовать увеличению объема перфузии легочных капилляров, однако с течением времени развивается гипертрофия миокарда ПЖ с последующей его сократительной недостаточностью. Показатели давления в малом круге кровообращения представлены в табл. 7.3.
Таблица 7.3
Показатели легочной гемодинамики
Локализация | Артериальное давление (мм рт.ст.) | ||
систолическое | диастолическое | среднее | |
Правое предсердие | 5-7 | 0-2 | 2,8-3,5 |
Правый желудочек | 20-30 | 4-7 | 9-15 |
Легочная артерия | 20-30 | 8-15 | 12-18 |
Критерием легочной гипертензии является уровень среднего давления в легочной артерии в покое, превышающий 20 мм рт.ст.
КЛИНИКА
Клиническая картина складывается из проявлений основного заболевания, приводящего к развитию ХЛС и поражения ПЖ. В клинической практике чаще всего среди причинных легочных заболеваний обнаруживаются хроническая обструктивная болезнь легких (ХОБЛ), т.е. бронхиальная астма или хронический обструктивный бронхит и эмфизема легких. Клиника ХЛС неразрывно связана с проявлением собственно ХЛН.
Характерной жалобой больных является одышка. Вначале при физической нагрузке (I стадия ХЛН), а затем и в покое (III стадия ХЛН). Она имеет экспираторный или смешанный характер. Длительное течение (годы) ХОБЛ притупляет внимание больного и заставляет обратиться к врачу тогда, когда одышка появляется при легкой физической нагрузке или в покое, то есть уже при ХЛН II-III стадии, когда наличие ХЛС бесспорно.
В отличие от одышки, связанной с левожелудочковой недостаточностью и венозным застоем крови в легких, одышка при легочной АГ не усиливается в горизонтальном положении больного и не
уменьшается в положении сидя. Больные могут даже предпочитать горизонтальное положение тела, при котором диафрагма принимает большее участие во внутригрудной гемодинамике, чем облегчается процесс дыхания.
Тахикардия является частой жалобой больных ХЛС и появляется еще на этапе развития ХЛН в ответ на артериальную гипоксемию. Расстройство сердечного ритма встречается нечасто. Наличие мерцательной аритмии, особенно у лиц старше 50 лет, как правило, связано с сопутствующей ИБС.
У половины больных ХЛС возникают боли в области сердца, чаще неопределенного характера, без иррадиации как правило не связанные с физической нагрузкой и не купирующиеся нитроглицерином. Наиболее распространенным взглядом на механизм болей является относительная коронарная недостаточность, обусловленная значительным увеличением мышечной массы ПЖ, а также уменьшение наполнения коронарных артерий при увеличении конечно-диастолического давления в полости ПЖ, гипоксия миокарда на фоне общей артериальной гипоксемии («синяя стенокардия») и рефлекторное сужение правой коронарной артерии (пульмокоронарный рефлекс). Возможной причиной кардиалгии может быть растяжение легочной артерии при резком повышении в ней давления.
При декомпенсации легочного сердца могут появляться отеки на ногах, которые впервые возникают чаще всего при обострении бронхолегочного заболевания и сначала локализуются в области стоп и лодыжек. По мере прогрессирования правожелудочковой недостаточности отеки распространяются на область голеней и бедер, а редко, в тяжелых случаях правожелудочковой недостаточности, отмечается увеличение живота в объеме за счет формирующегося асцита.
Менее специфичным симптомом легочного сердца является потеря голоса, что связывают с компрессией возвратного нерва дилатированным стволом легочной артерии.
У больных ХЛН и ХЛС может развиваться энцефалопатия вследствие хронической гиперкапнии и гипоксии головного мозга, а также нарушения сосудистой проницаемости. При выраженной энцефалопатии у части пациентов наблюдается повышенная возбудимость, агрессивность, эйфория и даже психозы, а у других больных - вялость, подавленность, сонливость днем и бессонница ночью, головные боли. Редко возникают обмороки при физической нагрузке в результате выраженной гипоксии.
Частым симптомом ХЛН является диффузный «серовато-синий», теплый цианоз. При возникновении правожелудочковой недостаточности у больных ХЛС цианоз нередко приобретает смешанный характер: на фоне диффузного синюшного окрашивания кожи появляется цианоз губ, кончика носа, подбородка, ушей, кончиков пальцев рук и ног, причем конечности в большинстве случаев остаются теплыми, возможно в связи с периферической вазодилатацией, обусловленной гиперкапнией. Характерным является набухание шейных вен (в том числе и на вдохе - симптом Куссмауля). У некоторых больных может появляться болезненный румянец на щеках и увеличение количества сосудов на коже и конъюнктивах («кроличьи или лягушачьи глаза» вследствие гиперкапнии), симптом Плеша (набухание шейных вен при надавливании ладонью на увеличенную печень), лицо Корвизара, сердечная кахексия, признаки основного заболевания (эмфизематозная грудная клетка, кифосколиоз грудного отдела позвоночника и др.).
При пальпации области сердца может выявляться выраженный разлитой сердечный толчок, эпигастральная пульсация (за счет гипертрофии и дилатации ПЖ), а при перкуссии - расширение правой границы сердца вправо. Однако эти симптомы теряют свое диагностическое значение из-за часто развивающейся эмфиземы легких, при которой перкуторные размеры сердца могут быть даже уменьшены («капельное сердце»). Наиболее частым аускультативным симптомом при ХЛС являются акцент второго тона над легочной артерией, который может сочетаться с расщеплением второго тона, правожелудочковым IV тоном сердца, диастолическим шумом недостаточности легочного клапана (шум Грэхема-Стилла) и систолическим шумом трикуспидальной недостаточности, причем интенсивность обоих шумов усиливается на высоте вдоха (симптом Риверо-Корвальо).
Артериальное давление у больных с компенсированным ХЛС чаще повышено, а при декомпенсированном - снижено.
Гепатомегалия выявляется практически у всех больных декомпенсированным ЛС. Печень увеличена в размерах, при пальпации уплотнена, болезненна, край печени закруглен. При тяжелой сердечной недостаточности появляется асцит. Вообще подобные тяжелые проявления правожелудочковой сердечной недостаточности при ХЛС встречаются редко, ибо само наличие тяжелой ХЛН или присоединение инфекционного процесса в легком приводит к трагическому финалу больного раньше, чем это наступает вследствие сердечной недостаточности.
Клиника хронического легочного сердца определяется выраженностью легочной патологии, а также легочной и правожелудочковой сердечной недостаточностью.
ИНСТРУМЕНТАЛЬНАЯ ДИАГНОСТИКА
Рентгенологическая картина ХЛС зависит от стадии ХЛН. На фоне рентгенологических проявлений легочного заболевания (пневмосклероз, эмфизема, усиление сосудистого рисунка и т.д.), вначале отмечается лишь некоторое уменьшение тени сердца, затем появляется умеренное выбухание конуса легочной артерии в прямой и правой косой проекции. В норме в прямой проекции правый контур сердца образуется правым предсердием, а при ХЛС с увеличением ПЖ он становится краеобразующим, причем при значительной гипертрофии ПЖ может образовывать как правый, так и левый край сердца, оттесняя левый желудочек назад. В заключительной декомпенсированной стадии ХЛС правый край сердца может образовываться значительно расширенным правым предсердием. И тем не менее эта «эволюция» происходит на фоне относительно небольшой тени сердца («капельное» или «висячее»).
Электрокардиографическая диагностика ХЛС сводится к выявлению гипертрофии ПЖ. К основным («прямым») ЭКГ-критериям гипертрофии ПЖ относятся: 1) R в V1>7мм; 2) S в V5-6 > 7 мм; 3) RV1 + SV5 или RV1 + SV6 > 10,5 мм; 4) RaVR > 4 мм; 5) SV1,V2 =s2 мм; 6) RV5,V6<5 мм; 7) отношение R/SV1 >1; 8) полная блокада правой ножки пучка Гиса при RV1>15 мм; 9) неполная блокада правой ножки пучка Гиса при RV1>10 мм; 10) отрицательный TVl и снижение STVl,V2 при RVl>5 мм и отсутствии коронарной недостаточности. При наличии 2 и более «прямых» ЭКГ-признаков диагноз гипертрофии ПЖ считается достоверным.
Косвенные ЭКГ-признаки гипертрофии ПЖ позволяют предполагать гипертрофию ПЖ: 1) поворот сердца вокруг продольной оси по часовой стрелке (смещение переходной зоны влево, к отведениям V5-V6 и появление в отведениях V5, V6 комплекса QRS типа RS; SV5-6 глубокий, а RV1-2 - нормальной амплитуды); 2) SV5-6 > RV5-6; 3) RaVR > Q(S)aVR; 4) отклонение электрической оси сердца вправо, особенно если α>110; 5) электрическая ось сердца типа
SI-SII-SIII; 6) полная или неполная блокада правой ножки пучка Гиса; 7) электрокардиографические признаки гипертрофии правого предсердия (P-pulmonale в отведениях II, III, aVF); 8) увеличение времени активации правого желудочка в V1 более 0,03 с. Существует три типа ЭКГ-изменений при ХЛС:
1. rSR'-тип ЭКГ характеризуется наличием в отведении V1 расщепленного комплекса QRS типа rSR' и выявляется обычно при выраженной гипертрофии ПЖ;
2. R-тип ЭКГ характеризуется наличием в отведении V1 комплекса QRS типа Rs или qR и выявляется обычно при выраженной гипертрофии ПЖ (рис. 7.1).
3. S-тип ЭКГ часто выявляют у больных ХОБЛ с эмфиземой легких. Его связывают со смещением гипертрофированного сердца кзади, что обусловлено эмфиземой легких. ЭКГ имеет вид rS, RS или Rs с выраженным зубцом S и в правых, и в левых грудных отведениях
с V1 по V6.
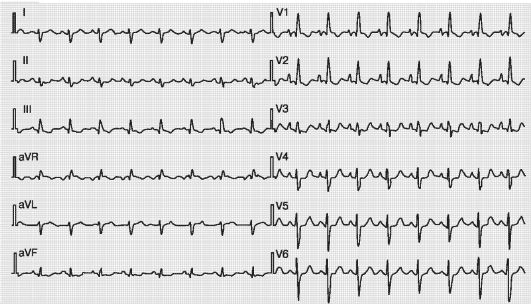 Рис. 7.1. ЭКГ
больного ХОБЛ и ХЛС. Синусовая тахикардия. Выраженная гипертрофия
правого желудочка (RV1 = 10 мм, SV1 отсутствует, SV5-6 = 12 мм, резкое
отклонение ЭОС вправо (α = +155°), отрицательный TV1-2 и снижение
сегмента STV1-2). Гипертрофия правого предсердия (P-pulmonale в V2-4)
Рис. 7.1. ЭКГ
больного ХОБЛ и ХЛС. Синусовая тахикардия. Выраженная гипертрофия
правого желудочка (RV1 = 10 мм, SV1 отсутствует, SV5-6 = 12 мм, резкое
отклонение ЭОС вправо (α = +155°), отрицательный TV1-2 и снижение
сегмента STV1-2). Гипертрофия правого предсердия (P-pulmonale в V2-4)
Электрокардиографические критерии гипертрофии ПЖ не достаточно специфичны. Они менее четкие, чем при гипертрофии ЛЖ, и могут приводить к ложноположительным и ложноотрицательным диагнозам. Нормальная ЭКГ не исключает наличие ХЛС, особенно у больных ХОБЛ, поэтому изменения ЭКГ надо сопоставлять с клинической картиной заболевания и данными ЭхоКГ.
Эхокардиография (ЭхоКГ) является ведущим неинвазивным методом для оценки легочной гемодинамики и диагностики ЛС. Ультразвуковая диагностика ЛС основана на выявлении признаков поражения миокарда ПЖ, которые приводятся ниже.
1. Изменение размера правого желудочка, который оценивается в двух позициях: в парастернальной позиции по длинной оси (в норме менее 30 мм) и в апикальной четырехкамерной позиции. Для выявления дилатации ПЖ чаще используется измерение его диаметра (в норме менее 36 мм) и площади в конце диастолы по длинной оси в апикальной четырехкамерной позиции. С целью более точной оценки выраженности дилатации ПЖ рекомендуется использовать отношение конечно-диастолической площади ПЖ к конечно-диастолической площади ЛЖ, тем самым, исключая индивидуальные различия в размерах сердца. Увеличение этого показателя более 0,6 свидетельствует о значительной дилатации ПЖ, а если он становится равным или больше 1,0, тогда делают заключение о резко выраженной дилатации ПЖ. При дилатации ПЖ в апикальной четырехкамерной позиции форма ПЖ меняется с серповидной на овальную, а верхушка сердца может быть занята не ЛЖ, как в норме, а ПЖ. Дилатация ПЖ может сопровождаться дилатацией ствола (более 30 мм) и ветвей легочной артерии. При массивном тромбозе легочной артерии может определяться ее значительная дилатация (до 50-80 мм), а просвет артерии становится овальным.
2. При гипертрофии ПЖ толщина его передней стенки, измеренная в диастолу в субкостальной четырехкамерной позиции в В- или М-режиме, превышает 5 мм. У больных ХЛС как правило гипертрофируется не только передняя стенка ПЖ, но и межжелудочковая перегородка.
3. Трикуспидальная регургитация различной степени, что в свою очередь вызывает дилатацию правого предсердия и нижней полой вены, снижение инспираторного коллапса которой указывает на повышенное давление в правом предсердии.
4. Оценка диастолической функции ПЖ производится по транстрикуспидальному диастолическому потоку в режиме импульсно-
волнового допплера и цветового М-модального допплера. У больных ХЛС находят снижение диастолической функции ПЖ, что проявляется уменьшением соотношения пиков Е и А.
5. Снижение сократительной способности ПЖ у больных ЛС проявляется гипокинезией ПЖ с уменьшением его фракции выброса. При эхокардиографическом исследовании определяют такие показатели функции ПЖ, как конечно-диастолический и конечно-систолический объемы, фракция выброса, которая в норме составляет не менее 50%.
Указанные изменения имеют различную выраженность в зависимости от остроты развития ЛС. Так, при остром ЛС будет выявляться дилатация ПЖ, а при хроническом ЛС к ней добавятся признаки гипертрофии, диастолической и систолической дисфункции ПЖ.
Другая группа признаков связана с развитием легочной гипертензии при ЛС. Степень их выраженности наиболее значительна при остром и подостром ЛС, а также у больных с первичной легочной гипертензией. Для ХЛС характерно умеренное повышение систолического давления в легочной артерии, которое редко достигает 50 мм рт.ст. Оценка легочного ствола и потока в выходном тракте ПЖ проводится из левого парастернального и субкостального доступа по короткой оси. У больных с легочной патологией вследствие ограничения ультразвукового окна субкостальная позиция может оказаться единственно возможным доступом для визуализации выходного тракта ПЖ. При помощи импульсно-волнового допплера можно измерить среднее давление в легочной артерии (Рра), для чего обычно используется формула, предложенная A. Kitabatake и соавт. (1983): Log10(Pра) = - 2,8 (AT/ET) + 2,4, где AT - время ускорения потока в выносящем тракте ПЖ, ET - время выброса (или время изгнания крови из ПЖ). Величина Рра, полученная при помощи данного метода, у больных ХОБЛ хорошо коррелирует с данными инвазивного обследования, а возможность получения надежного сигнала с клапана легочной артерии превышает 90%.
Наибольшее значение для выявления легочной гипертензии имеет выраженность трикуспидальной регургитации. Использование струи трикуспидальной регургитации лежит в основе наиболее точного неинвазивного метода определения систолического давления в легочной артерии. Измерения проводят в режиме непрерывно-волнового допплера в апикальной четырехкамерной или субкостальной позиции желательно с одновременным использованием цветового допплеровс-
кого картирования. Для расчета давления в легочной артерии необходимо к градиенту давления на трикуспидальном клапане прибавить давление в правом предсердии. Измерение транстрикуспидального градиента можно выполнить более чем у 75% больных ХОБЛ. Имеются качественные признаки легочной гипертензии:
1. При ЛГ изменяется характер движения задней створки клапана легочной артерии, что определяется в М-режиме: характерным показателем ЛГ является наличие среднесистолического зубца вследствие частичного перекрытия клапана, что формирует W-образное движение клапана в систоле.
2. У больных с легочной гипертензией за счет повышения давления в правом желудочке межжелудочковая перегородка (МЖП) уплощается, и левый желудочек напоминает по короткой оси букву D (D-образный левый желудочек). При высокой степени ЛГ МЖП становится как бы стенкой ПЖ и движется в диастолу парадоксально в сторону левого желудочка. Когда давление в легочной артерии и правом желудочке становится больше 80 мм рт.ст., левый желудочек уменьшается в объеме, сдавливается дилатированным правым желудочком и приобретает форму полумесяца.
3. Возможна регургитация на легочном клапане (в норме возможна регургитация первой степени у молодых людей). При постоянно-волновом допплеровском исследовании возможно измерение скорости легочной регургитации с дальнейшим расчетом величины конечно-диастолического градиента давления ЛА-ПЖ.
4. Изменение формы потока крови в выносящем тракте ПЖ и в устье клапана ЛА. При нормальном давлении в ЛА поток имеет равнобедренную форму, пик потока расположен в середине систолы; при легочной гипертензии пик потока смещается в первую половину систолы.
Однако у пациентов с ХОБЛ имеющаяся у них эмфизема легких часто затрудняет четкую визуализацию структур сердца и суживает «окно» ЭхоКГ, делая исследование информативным не более чем у 60-80% больных. В последние годы появился более точный и информативный метод ультразвукового исследования сердца - чреспищеводная эхокардиография (ЧПЭ). ЧПЭ у больных ХОБЛ является более предпочтительным методом для точных измерений и непосредственной визуальной оценки структур ПЖ, что обусловлено более высокой разрешающей способностью чреспищеводного датчика и стабильностью ультразвукового окна, и имеет особое значение при эмфиземе легких и пневмосклерозе.
Катетеризация правых отделов сердца и легочной артерии
Катетеризация правых отделов сердца и легочной артерии является методом «золотого стандарта» при постановке диагноза ЛГ. Эта процедура позволяет напрямую измерить давление в правом предсердии и ПЖ, давление в легочной артерии, рассчитать сердечный выброс и легочное сосудистое сопротивление, определить уровень оксигенации смешанной венозной крови. Катетеризация правых отделов сердца в связи с ее инвазивностью не может быть рекомендована для широкого применения в диагностике ХЛС. Показаниями являются: тяжелая легочная гипертензия, частые эпизоды декомпенсации правожелудочковой недостаточности, а также отбор кандидатов для трасплантации легких.
Радионуклидная вентрикулография (РВГ)
РВГ позволяет измерить фракцию выброса правого желудочка (ФВПЖ). ФВПЖ считается ненормальной при значении ниже 40- 45%, однако сам показатель ФВПЖ не является хорошим индикатором для оценки функции правого желудочка. Он позволяет оценить систолическую функцию правого желудочка, которая сильно зависит от постнагрузки, снижаясь при повышении последней. Поэтому снижение ФВПЖ регистрируется у многих больных ХОБЛ, не являясь показателем истинной дисфункции правого желудочка.
Магнитно-резонансная томография (МРТ)
МРТ - многообещающий метод, позволяющий оценивать легочную гипертензию и изменения структуры и функции правого желудочка. Диаметр правой легочной артерии, измеренный при МРТ, более 28 мм является высокоспецифичным признаком ЛГ. Однако метод МРТ довольно дорог и доступен лишь в специализированных центрах.
Наличие хронического легочного заболевания (как причины ХЛС) требует специального исследования функции внешнего дыхания. Перед врачом ставится задача уточнить тип вентиляционной недостаточности: обструктивный (нарушение прохождения воздуха по бронхам) или рестриктивный (уменьшение площади газообмена). В первом случае в качестве примера можно привести хронический обструктивный бронхит, бронхиальную астму, а во втором - пневмосклероз, резекцию легкого и т.д.
ЛЕЧЕНИЕ
ХЛС возникает чаще всего вслед за появлением ХЛН. Тера-певтические мероприятия носят комплексный характер и направлены главным образом на коррекцию этих двух синдромов, что можно представить в следующем виде:
1) лечение и профилактика основного заболевания - чаще всего обострений хронической легочной патологии (базисная терапия);
2) лечение ХЛН и ЛГ;
3) лечение правожелудочковой сердечной недостаточности. Базисные лечебно-профилактические мероприятия включают
профилактику острых вирусных заболеваний дыхательных путей (вакцинация) и исключение курения. При развитии хронической легочной патологии воспалительного характера необходимо лечение обострений с помощью антибиотиков, мукорегулирующих препаратов и иммунокорректоров.
Главное в терапии хронического легочного сердца - это улучшение функции внешнего дыхания (устранение воспаления, бронхообструктивного синдрома, улучшение состояния дыхательной мускулатуры).
Наиболее частой причиной ХЛН является бронхообструктивный синдром, причина которого в сокращении гладкой мускулатуры бронхов, накоплении вязкого воспалительного секрета, отека слизистой бронхов. Эти изменения требуют применения бета-2-аго- нистов (фенотерол, формотерол, сальбутамол), М-холинолитиков (ипратропия бромид, тиотропия бромид), а в ряде случаев и ингаляционных глюкокортикостероидных препаратов в виде ингаляций с помощью небулайзера или индивидуального ингалятора. Возможно применение метилксантинов (эуфиллин и пролонгированные теофиллины (теолонг, теотард и др.)). Терапия отхаркивающими средствами очень индивидуальна и требует различных сочетаний и подбора средств растительного происхождения (мать-и-мачеха, багульник, чабрец и т.д.), и химического производства (ацетилцистеин, амброксол и др.).
При необходимости назначают ЛФК и постуральный дренаж легких. Показано дыхание с положительным давлением на выдохе (не более 20 см водного столба) с помощью как простых приспособлений
в виде «свистков» с подвижной диафрагмой, так и сложных приборов, контролирующих давление на выдохе и вдохе. Данный метод снижает скорость потока воздуха внутри бронха (что оказывает бронхолитический эффект) и увеличивает давление внутри бронхов по отношению к окружающей легочной ткани.
К внелегочным механизмам развития ХЛН относится снижение сократительной функции дыхательной мускулатуры и диафрагмы. Возможности коррекции этих нарушений пока ограниченны: ЛФК или электростимуляция диафрагмы при II ст. ХЛН.
При ХЛН эритроциты претерпевают значительную функциональную и морфологическую перестройку (эхиноцитоз, стоматоцитоз и т.д.), что заметно снижает их кислородотранспортную функцию. В этой ситуации желательно вывести из кровотока эритроциты с утраченной функцией и стимулировать выброс молодых (функционально более способных). С этой целью возможно применение эритроцитафереза, экстракорпоральной оксигенации крови, гемосорбции.
Из-за повышения агрегационных свойств эритроцитов увеличивается вязкость крови, что требует назначения антиагрегантов (курантил, реополиглюкин) и гепарина (предпочтительно применение низкомолекулярных гепаринов - фраксипарин и др.).
У больных с гиповентиляцией, связанной со сниженной активностью дыхательного центра, в качестве вспомогательных методов терапии могут быть использованы лекарственные препараты, повышающие центральную инспираторную активность - стимуляторы дыхания. Их следует применять при умеренно выраженном угнетении дыхания, не требующем использования О2 или механической вентиляции легких (синдром апноэ во сне, синдром ожирения-гиповентиляции), либо при невозможности проведения кислородотерапии. К числу немногих препаратов, повышающих оксигенацию артериальной крови, относятся никетамид, ацетозаламид, доксапрам и медроксипрогестерон, однако все эти лекарственные средства при длительном использовании обладают большим количеством побочных эффектов и потому могут применяться только в течение короткого времени, например во время обострения заболевания.
В настоящее время к препаратам, способным в течение длительного времени корригировать гипоксемию у больных ХОБЛ, относится альмитрина бисмесилат. Альмитрин является специфическим аго-
нистом периферических хеморецепторов каротидного узла, стимуляция которых ведет к усилению гипоксической вазоконстрикции в плохо вентилируемых регионах легких с улучшением вентиляционно-перфузионных соотношений. Доказана способность альмитрина в дозе 100 мг/сут. у пациентов с ХОБЛ приводить к значимому повышению ра02 (на 5-12 мм рт.ст.) и снижению раС02 (на 3-7 мм рт.ст.) с улучшением клинической симптоматики и уменьшением частоты обострений заболевания, что способно на несколько лет отсрочить назначение длительной 02-терапии. К сожалению 20-30% больных ХОБЛ не отвечают на терапию, а широкое использование ограничено возможностью развития периферической нейропатии и других побочных эффектов. В настоящее время основным показанием к назначению альмитрина является умеренная гипоксемия у больных ХОБЛ (ра02 56-70 мм рт.ст. или Sа02 89-93%), а также его использование в комплексе к ДКТ, особенно на фоне гиперкапнии.
Вазодилататоры
С целью уменьшения степени ЛАГ в комплексную терапию больных легочным сердцем включают периферические вазодилататоры. Наиболее часто применяют антагонисты кальциевых каналов и нитраты. К числу рекомендованных в настоящее время антагонистов кальция относятся два препарата - нифедипин и дилтиазем. Выбор в пользу одного из них зависит от исходной частоты сердечных сокращений. Пациентам с относительной брадикардией следует рекомендовать нифедипин, при относительной тахикардии - дилтиазем. Суточные дозы этих препаратов, доказавших эффективность, достаточно высокие: для нифедипина 120-240 мг, для дилтиазема 240-720 мг. Были показаны благоприятные клинические и прогностические эффекты антагонистов кальция, применяемых в высоких дозах у больных с первичной ЛГ (особенно с предшествующей положительной острой пробой). Антагонисты кальция дигидропиридинового ряда III поколения - амлодипин, фелодипин и др. - также эффективны у этой группы больных ЛС.
Однако при легочной гипертензии, обусловленной ХОБЛ, антагонисты кальциевых каналов не рекомендуется к использованию, несмотря на их способность снижать Рра и повышать сердечный выброс у этой группы больных. Это связано с усугублением артериальной гипоксемии, вызванной дилатацией легочных сосудов в
плохо вентилируемых зонах легких с ухудшением вентиляционноперфузионных соотношений. Кроме того, при длительной терапии антагонистами кальция (более 6 мес.) благоприятное действие на параметры легочной гемодинамики нивелируется.
Аналогичная ситуация у больных ХОБЛ имеет место и при назначении нитратов: острые пробы демонстрируют ухудшение газообмена, а длительные исследования - отсутствие положительного эффекта препаратов на легочную гемодинамику.
Синтетический простациклин и его аналоги. Простациклин - мощный эндогенный вазодилататор, обладающий антиагрегационным, антипролиферативным и цитопротективным эффектами, которые направлены на предотвращение ремоделирования легочных сосудов (уменьшение повреждения эндотелиальных клеток и гиперкоагуляции). Механизм действия простациклина связан с релаксацией гладкомышечных клеток, ингибированием агрегации тромбоцитов, улучшением эндотелиальной функции, угнетением пролиферации сосудистых клеток, а также прямым инотропным эффектом, позитивными изменениями гемодинамики, увеличением утилизации кислорода в скелетной мускулатуре. Клиническое использование простациклина у больных ЛГ связано с синтезом его стабильных аналогов. К настоящему времени наибольший опыт в мире накоплен для эпопростенола.
Эпопростенол - это форма внутривенного простациклина (простагландин I2). Благоприятные результаты были получены у больных васкулярной формой ЛС - с первичной ЛГ при системных заболеваниях соединительной ткани. Препарат увеличивает сердечный выброс и уменьшает легочное сосудистое сопротивление, а при длительном применении улучшает качество жизни больных ЛС, увеличивая толерантность к физическим нагрузкам. Оптимальная для большинства пациентов доза составляет 20-40 нг/кг/мин. Применяется также аналог эпопростенола - трепростинил.
В настоящее время разработаны пероральные формы аналога простациклина (берапрост, илопрост) и проводятся клинические испытания в лечении больных с васкулярной формой ЛС, развившейся вследствие ТЭЛА, первичной легочной гипертензии, системных заболеваний соединительной ткани.
В России из группы простаноидов для лечения больных ЛС в настоящее время доступным является только простагландин Е1 (вазапростан), который назначают внутривенно капельно со ско-
ростью 5-30 нг/кг/мин. Курсовое лечение препаратом проводят в суточной дозе 60-80 мкг в течение 2-3 недель на фоне длительной терапии антагонистами кальция.
Антагонисты рецепторов к эндотелину
Активация системы эндотелина у больных ЛГ послужила обоснованием для использования антагонистов рецепторов к эндотелину. Доказана эффективность двух препаратов этого класса (бозентана и ситакзентана) в лечении больных ХЛС, развившимся на фоне первичной ЛГ или на фоне системных заболеваний соединительной ткани.
Ингибиторы фосфодиэстеразы типа 5
Силденафил - мощный селективный ингибитор цГМФ-зависимой фосфодиэстеразы (тип 5), предотвращая деградацию цГМФ, вызывает снижение легочного сосудистого сопротивления и перегрузки правого желудочка. К настоящему времени имеются данные об эффективности силденафила у больных ЛС различной этиологии. При применении силденафила в дозах 25-100 мг 2-3 раза в день он вызывал улучшение гемодинамики и толерантности к физическим нагрузкам у больных ЛС. Рекомендуется его применение при неэффективности другой медикаментозной терапии.
Длительная кислородотерапия
У больных с бронхолегочной и торакодиафрагмальной формой ХЛС главная роль в развитии и прогрессировании заболевания принадлежит альвеолярной гипоксии, поэтому кислородотерапия является наиболее патогенетически обоснованным методом лечения этих пациентов. Использование кислорода у больных с хронической гипоксемией является решающим и должно быть постоянным, длительным, и как правило проводиться в домашних условиях, поэтому такая форма терапии называется длительной кислородотерапией (ДКТ). Задачей ДКТ является коррекция гипоксемии с достижением значений раО2 >60 мм рт.ст. и Sa02 >90%. Считается оптимальным поддержание раО2 в пределах 60-65 мм рт.ст., а превышение этих значений приводит лишь к незначительному увеличению Sa02 и содержания кислорода в артериальной крови, однако может сопровождаться задержкой СО2, особенно во время сна, что имеет негативные
последствия для функции сердца, головного мозга и дыхательных мышц. Поэтому ДКТ не показана больным с умеренной гипоксемией. Показания к ДКТ: раО2 <55 мм рт.ст. или Sa02 < 88% в покое, а также раО2 56-59 мм рт.ст. или Sa02 89% при наличии легочного сердца или полицитемии (гематокрит >55%). Большинству больных ХОБЛ достаточно потока О2 1-2 л/мин., а у наиболее тяжелых больных поток может быть увеличен до 4-5 л/мин. Концентрация кислорода должна быть 28-34% об. Рекомендуется проведение ДКТ не менее 15 ч в сутки (15-19 ч/сут.). Максимальные перерывы между сеансами кислородотерапии не должны превышать 2 ч подряд, т.к. перерывы более 2-3 ч значительно усиливают легочную гипертензию. Для проведения ДКТ могут использоваться концентраторы кислорода, резервуары с жидким кислородом и баллоны со сжатым газом. Чаще всего применяются концентраторы (пермеаторы), выделяющие кислород из воздуха за счет удаления азота. ДКТ увеличивает продолжительность жизни больных с ХЛН и ХЛС в среднем на 5 лет.
Таким образом, несмотря на наличие большого арсенала современных фармакологических средств, ДКТ - самый эффективный метод лечения большинства форм ХЛС, поэтому терапия больных ХЛС является прежде всего задачей врача-пульмонолога.
Длительная оксигенотерапия - самый эффективный метод лечения ХЛН и ХЛС, увеличивающий продолжительность жизни больных в среднем на 5 лет.
Длительная домашняя вентиляция легких
В терминальных стадиях легочных заболеваний вследствие снижения вентиляционного резерва может развиться гиперкапния, требующая респираторной поддержки, которая должна проводиться длительно, на постоянной основе в домашних условиях.
Ингаляционная терапия NO
Ингаляционная терапия N0, действие которой аналогично эндотелий-релаксирующему фактору, оказывает положительный эффект у больных ХЛС. Его вазодилатирующее действие основано на активации гуанилатциклазы в гладкомышечных клетках легочных сосудов, которое приводит к повышению уровня цикло-ГМФ и снижению внутриклеточного содержания кальция. Ингаляционный N0 обла-
дает селективным действием на сосуды легких, причем он вызывает вазодилатацию в основном в хорошо вентилируемых регионах легких, улучшая газообмен. При курсовом применении N0 у больных ХЛС наблюдается снижение давления в легочной артерии, повышение парциального давления кислорода в крови. В дополнение к своим гемодинамическим эффектам N0 способствует предотвращению и обратному развитию ремоделирования легочных сосудов и ПЖ. Оптимальными дозами ингаляционного N0 являются концентрации 2-10 ppm, а высокие концентрации N0 (более 20 ppm) способны вызвать чрезмерную вазодилатацию легочных сосудов и привести к ухудшению вентиляционно-перфузионного баланса с усилением гипоксемии. Добавление ингаляций N0 к ДКТ у больных ХОБЛ усиливают положительный эффект на газообмен, снижая уровень легочной гипертензии и увеличивая сердечный выброс.
CPAP-терапия
Метод терапии постоянным положительным давлением в дыхательных путях (continuous positive airway pressure - CPAP) находит применение в качестве метода лечения при ХЛН и ХЛС у больных с синдромом обструктивного ночного апноэ, препятствуя развитию коллапса дыхательных путей. Доказанными эффектами СРАР являются предотвращение и расправление ателектазов, повышение легочных объемов, уменьшение вентиляционно-перфузионного дисбаланса, повышение оксигенации, комплаенса легких, перераспределение жидкости в ткани легких.
Сердечные гликозиды
Сердечные гликозиды у больных ХОБЛ и легочным сердцем эффективны только при наличии левожелудочковой сердечной недостаточности, а также могут быть полезны при развитии мерцательной аритмии. Более того, показано, что сердечные гликозиды могут индуцировать легочную вазоконстрикцию, а наличие гиперкапнии и ацидоза увеличивает вероятность гликозидной интоксикации.
Диуретики
В лечении больных декомпенсированным ХЛС с отечным синдромом используют терапию диуретиками, в том числе антагонистами
альдостерона (альдактон). Диуретики следует назначать осторожно, с небольших доз, так как при развитии ПЖ-недостаточности сердечный выброс больше зависит от преднагрузки, и, следовательно, чрезмерное сокращение внутрисосудистого объема жидкости может привести к уменьшению объема наполнения ПЖ и снижению сердечного выброса, а также к повышению вязкости крови и резкому снижению давления в легочной артерии, тем самым ухудшив диффузию газов. Другим серьезным побочным эффектом мочегонной терапии является метаболический алкалоз, который у больных ХОБЛ с дыхательной недостаточностью может приводить к угнетению активности дыхательного центра и ухудшению показателей газообмена.
Ингибиторы ангиотензинпревращающего фермента
В лечении больных с декомпенсированным легочным сердцем в последние годы на первое место вышли ингибиторы ангиотензинпревращающего фермента (ИАПФ). Терапия ИАПФ у больных ХЛС ведет к снижению легочной гипертензии и повышению сердечного выброса. С целью подбора эффективной терапии ХЛС у больных ХОБЛ рекомендуется определение полиморфизма гена АПФ, т.к. только у пациентов с субтипами гена АПФ II и ID наблюдается выраженное положительное гемодинамическое действие ИАПФ. Рекомендуется применение ИАПФ в минимальных терапевтических дозах. Помимо гемодинамического эффекта, отмечается положительное влияние ИАПФ на размеры камер сердца, процессы ремоделирования, толерантность к физическим нагрузкам и повышение продолжительности жизни больных сердечной недостаточностью.
Антагонисты рецепторов ангиотензина II
В последние годы получены данные об успешном применении этой группы препаратов в лечении ХЛС у больных ХОБЛ, что проявлялось улучшением гемодинамики и газообмена. Наиболее показано назначение этих препаратов у больных ХЛС при непереносимости ИАПФ (из-за сухого кашля).
Предсердная септостомия
В последнее время в лечении больных с правожелудочковой сердечной недостаточностью, развившейся на фоне первичной ЛГ, стали
использовать предсердную септостомию, т.е. создание небольшой перфорации в межпредсердной перегородке. Создание шунта справа-налево позволяет снизить среднее давление в правом предсердии, разгрузить правый желудочек, увеличить преднагрузку левого желудочка и сердечный выброс. Предсердная септостомия показана при неэффективности всех видов медикаментозного лечения правожелудочковой сердечной недостаточности, особенно в сочетании с частыми синкопе, или как подготовительный этап перед трансплантацией легких. В результате вмешательства наблюдаются уменьшение синкопе, повышение толерантности к нагрузке, однако повышается риск развития жизнеопасной артериальной гипоксемии. Смертность больных при проведении предсердной септостомии 5-15%.
Трансплантация легких или комплекса сердце-легкие
С конца 80-х гг. XX века после начала применения иммуносупрессивного препарата циклоспорина А при лечении терминальных стадий легочной недостаточности стала успешно применяться трансплантация легких. У больных ХЛН и ЛС проводят операции трансплантации одного или обоих легких, комплекса сердце-легкие. Было показано, что 3 и 5-летняя выживаемость после проведенных трансплантаций одного или обоих легких, комплекса сердце-легкие у больных ЛС составила 55 и 45% соответственно. В большинстве центров предпочитают выполнять билатеральную трансплантацию легких в связи с меньшим числом послеоперационных осложнений.