Руководство по кардиологии : Учебное пособие в 3 т. / Под ред. Г.И. Сторожакова, А.А. Горбаченкова. - Т. 2. - 512 с. : ил.
|
|
|
|
ГЛАВА 1 ДИЛАТАЦИОННЫЕ КАРДИОМИОПАТИИ
Дилатационные кардиомиопатии (ДКМП) - группа заболеваний миокарда с нарушением насосной функции сердца и его расширением, с хронической сердечной недостаточностью (ХСН) и плохим прогнозом. Фракция выброса левого желудочка (ФВ ЛЖ) снижена (менее 40%), как и сердечный выброс. ДКМП делятся на первичные, причинами которых являются врожденные установленные или не установленные генетические аномалии, и вторичные, связанные с известными сердечными или системными заболеваниями (специфические). Причины специфических ДКМП многообразны: КБС, АГ, инфекции, эндокринные заболевания, алкоголь, токсины, приобретенные генетические аномалии, тахиаритмии.
Естественное течение ДКМП неблагоприятное, хотя иногда возможно спонтанное (или под влиянием лечения) улучшение функции миокарда, состояния больного и прогноза.
Нарушение функции ЛЖ (снижение ФВ, расширение сердца) может существовать задолго (месяцы, годы) до появления жалоб. Больные погибают внезапно (аритмии) или от прогрессирования ХСН.
Жалобы больных (одышка, утомляемость, отеки, сердцебиение) обусловлены сердечной недостаточностью. Поэтому лечение ДКМП проводится по принципам терапии ХСН (диуретики, ингибиторы АПФ, бета-адреноблокаторы). В случаях вторичных ДКМП возможны специфические вмешательства (лечение алкоголизма, тиреотоксикоза, тахиаритмии, реваскуляризация миокарда при КБС и т.д.).
Трансплантация сердца устраняет ХСН, улучшает прогноз.
Ключевые слова: заболевания миокарда, дисфункция миокарда, дилатационная кардиомиопатия, хроническая сердечная недостаточность.
ВВЕДЕНИЕ
ДКМП являются следствием миокардиальной недостаточности, которая составляет главную причину развития ХСН с характерной клинической картиной. В специализированных центрах ДКМП представляют наиболее частый фенотип (90%) среди всех случаев КМП и характеризуются желудочковой дилатацией, снижением ФВ ЛЖ, плохим прогнозом (от 15 до 50% больных погибают в течение 5 лет после установления диагноза от сердечной недостаточности или внезапно). Применение ингибиторов АПФ, бета-адреноблокаторов и диуретиков улучшает прогноз у больных ДКМП, задерживает прогрессирование сердечной недостаточности. Пересадка сердца существенно повышает качество жизни и ее продолжительность.
ОБЩИЕ СВЕДЕНИЯ О КМП
Определение и классификация
Специфические заболевания миокарда традиционно отделялись от заболеваний неизвестной причины, которые называли «кардиомиопатиями». Для обозначения специфических поражений использовались разные названия: миокардит, если обнаруживалась связь с инфекцией, воспалением; миокардиодистрофия, если предполагали метаболические изменения без морфологических (климакс, тиреотоксикоз, анемия); миокардоз - по аналогии с нефрозом, гепатозом (например, при системной красной волчанке) или просто давали описательное название (алкогольное поражение сердца, спортивное сердце, тиреотоксическое сердце, гипертоническое сердце).
Сравнительно недавно (1996 г.) специализированная группа ВОЗ и Международного общества и федерации кардиологии рекомендовала использовать термин «кардиомиопатия» для всех случаев заболевания миокарда с «сердечной дисфункцией» с выделением 6 групп:
• дилатационные;
• гипертрофические;
• рестриктивные;
• аритмогенная дисплазия правого желудочка;
• специфические;
• неклассифицированные.
В последней редакции классификация КМП представлена в табл. 1.1.
В основу классификации при определении индивидуальной категории КМП положены два принципа. Первый принцип учитывает анатомо-физиологические особенности, и при этом выделяются две отличающиеся по анатомии и функции ЛЖ, прогнозу и подходам к лечению группы - дилатационные и рестриктивные КМП. Второй принцип строится на генетическом подходе: индивидуальные генетические мутации создают уникальный фенотип с поражением сердца без экстракардиальных проявлений - гипертрофическая КМП и аритмогенная дисплазия правого желудочка.
В классификации предусмотрено также подразделение КМП на первичные и вторичные.
Вторичные КМП - это КМП этиологически связанные с установленными болезнями сердца или другими заболеваниями (специфические КМП), и наиболее частыми из них являются ишемические,
Таблица 1.1
Классификация КМП (Всемирная организация здравоохранения/ Международное общество и федерация кардиологии)
Категории. Определяющие особенности
I. ДКМП. Увеличение конечных систолического (КСО) и диастолического (КДО) объемов, снижение ФВ
1. Первичные
2. Вторичные
II. Рестриктивные КМП. Уменьшение КДО, увеличение давления наполнения ЛЖ
1. Первичные
2. Вторичные
III. Гипертрофические КМП. Значительное утолщение МЖП, утолщение задней стенки ЛЖ, дезорганизация миофибрилл.
Мутация саркомерного белка, аутосомная доминантная наследственность.
IV. Аритмогенная дисплазия. Фиброзно-жировое замещение миокарда правого желудочка. Аутосомная доминантная (основная) и рецессивная наследственность.
V. Неклассифицированные. Нет критериев предыдущих категорий, черты нескольких категорий.
гипертензивные и клапанные. Первичные КМП обусловлены генетическими аномалиями в миокарде.
Существуют кардиологические школы, которые считают, что термин «кардиомиопатия» может использоваться только для обозначения первичных поражений миокарда, а вторичные, специфические КМП не могут называться «кардиомиопатиями».
Кратко остановимся на характеристике каждой из групп КМП.
1. ДКМП определяется дилатацией и систолической дисфункцией ЛЖ и может быть разной по происхождению. Большинство ДКМП являются вторичными. Рабочая классификация ДКМП приведена в табл. 1.2.
Во многих случаях ДКМП прогрессирует, но при некоторых ДКМП процесс можно остановить и добиться восстановления функции миокарда (ишемическая, воспалительная, алкогольная, тиреотоксическая). У небольшой части больных наступает спонтанное улучшение функции миокарда.
Предпринимаются попытки выделения «больших» гемодинамических критериев ДКМП:
Таблица 1.2
Рабочая классификация ДКМП
1. Этиология
Ишемическая Гипертензивная Клапанная Дисметаболическая
- сахарный диабет
- тиреотоксикоз
- гипотиреоз
- гемохроматоз Алиментарно-токсическая
- алкогольная
- химические и терапевтические агенты
- бери-бери
Воспалительная (инфекционная)
Семейно-генетическая
При системных заболеваниях
Тахиаритмическая
Перипартальная
Идиопатическая
2. Сердечная недостаточность Функциональные классы I-IV, стадии I-III
3. Coстояние компенсации* Компенсация Субкомпенсация Декомпенсация
Примечание. * Компенсация - присутствуют гемодинамические нарушения (ФВ, выброс, объем сердца), жалоб нет. Субкомпенсация - гемодинамические изменения и жалобы. Декомпенсация - присоединяются застойные явления (отеки, гидроторакс, гидроперикард, асцит).
• ФВ ЛЖ менее 45% и/или фракционное укорочение менее 25% по данным эхокардиографии, радионуклидной вентрикулографии или ангиографии;
• конечный диастолический размер ЛЖ более 2,7 см/м2 поверхности тела.
Распространенность отдельных видов ДКМП в разных странах может отличаться по ряду причин, например из-за специфических инфекций (трипаносомоз в Южной Америке).
В США наиболее частыми ДКМП являются ишемические, гипертензивные и клапанные.
Термин «идиопатическая» в приведенной выше рабочей классификации ДКМП используется в тех случаях, когда этиология ДКМП не установлена.
С развитием дилатации сердца и сердечной недостаточности лечение ДКМП проводится согласно принципам лечения ХСН, т.е. направлено на гемодинамическую разгрузку миокарда (бета-адреноблокаторы, ингибиторы АПФ, диуретики), а этиологическая принадлежность ДКМП частично утрачивает смысл. Но если этиология ДКМП установлена, то возможно дополнительное проведение специфических вмешательств, которые могут существенно улучшить результаты лечения и прогноз: реваскуляризация миокарда при КБС, устранение тахиаритмий, противовоспалительная и иммуномодулирующая терапия, лечение тиреотоксикоза и т.д.
2. Гипертрофическая КМП, упомянутая в табл. 1.1, является семейно-генетической КМП и обусловлена генетической мутацией с нарушением синтеза белков в миокарде . Она характеризуется выраженной гипертрофией только левого или/и правого желудочков (см. Главу 2 в данном томе). Иногда сопровождается развитием субаортального стеноза (идиопатический гипертрофический субаортальный стеноз).
Перечень гипертрофических КМП может быть расширен за счет включения КМП, развивающихся при АГ и аортальном стенозе. Все перечисленные выше три вида гипертрофических КМП - семейногенетическая, при АГ и при аортальном стенозе - характеризуются важным признаком: гипертрофией ЛЖ. Вследствие этого они имеют общие черты, определяющие клинику, прогноз и лечение: нарушение диастолической функции ЛЖ и развитие обусловленной этим сердечной недостаточности, склонность к желудочковым аритмиям, развитие в дальнейшем систолической дисфункции и дилатации ЛЖ, ишемия миокарда, регресс гипертрофии ЛЖ и улучшение функции ЛЖ при устранении причины гипертрофии.
3. Рестриктивные КМП - редкие в Европе заболевания. Характеризуются нормальным или уменьшенным объемом одного или обоих желудочков, увеличением их жесткости, нарушением диастолической функции и повышением давления наполнения желудочков. Могут быть первичными, идиопатическими (эндомиокардиальный фиброз), или вторичными, например инфильтративными
(амилоидоз, саркоидоз) или связанными с врожденными заболеваниями (болезнь Фабри, Гоше).
4. Аритмогенная дисплазия правого желудочка обусловлена генетическими мутациями и характеризуется фиброзно-жировым замещением сначала правого, а затем и частично левого желудочка с развитием аритмий.
5. Неклассифицированные КМП включают заболевания миокарда с особыми характеристиками либо с чертами разных КМП (при системной склеродермии, амилоидозе, некомпактный ЛЖ, первичные нарушения ритма и проводимости).
Практические врачи могут пользоваться как прежней, так и новой терминологией болезней миокарда.
ДКМП характеризуется нарушением сократительной способности миокарда, расширением сердца, снижением сердечного выброса и ФВ, клиникой сердечной недостаточности.
Морфологическая и общая клиническая характеристика ДКМП
При ДКМП миокард всегда изменен: кардиомиоциты гипертрофированы, присутствует экстрацеллюлярный фиброз. Во многих кардиомиоцитах видны вакуоли, миофибриллы не прослеживаются. Ориентация структурных сократительных компонентов в кардиомиоцитах нарушена, как и строение ионных каналов и распределение функционально важных белковых структур на поверхности кардиомиоцитов (адгезивные молекулы, коннексоны). Функция изолированного кардиомиоцита страдает: сокращение удлиняется, сила его уменьшается, расслабление замедляется. Наиболее важным и ранним нарушением является потеря способности саркоплазматического ретикулума захватывать кальций.
Оба желудочка сердца расширены, его форма приближается к сферической, в то время как здоровое сердце по форме эллипсоидное или грушеобразное.
В большинстве случаев начало заболевания скрытое. В других оно начинается после перенесенной вирусной инфекции или миокардита.
Нарушение функции миокарда (снижение ФВ, расширение сердца) может отмечаться задолго до появления симптомов заболевания (сердечная недостаточность, нарушения ритма сердца).
В развернутой стадии клиника ДКМП определяется ХСН разной степени выраженности. Часто возникают нарушения ритма и
проводимости, а при мерцательной аритмии и застойных явлениях - тромбоэмболии.
Хроническая сердечная недостаточность (ХСН) характеризуется гемодинамическими и регуляторными (нейрогуморальными) изменениями, которые первоначально имеют компенсаторный смысл: тахикардия, повышение сосудистого сопротивления, задержка натрия и воды, ионотропное воздействие на миокард (табл. 1.3).
Таблица 1.3
Гемодинамические и регуляторные изменения при ХСН
Снижение сердечного выброса | |
нарушение перфузии тканей | утомляемость |
активация САС | нарушение функции и структуры органов |
Активация САС | |
повышенное освобождение катехоламинов | тахикардия, инотропизм, повышение сосудистого сопротивления |
Активация РААС | |
повышенное образование ангиотензина II, альдостерона | жажда, задержка натрия и воды, вазопрессин, повышение сосудистого сопротивления, стимуляция САС, гипертрофия миокарда |
Активация стресс-лимитирующих систем | |
образование натрий-уретических пептидов (предсердного, головного мозга) | увеличение выделения натрия и воды |
простогландины | уменьшение сосудистого сопротивления |
Такие «компенсаторные» сдвиги увеличивают нагрузку на миокард, «истощают» его, и в развернутой стадии ХСН не способствуют выживанию больных.
Клиника ХСН определяется выраженностью нарушений гемодинамики, изменениями в органах, степенью активации РААС, САС и других стресс-реализующих систем, активностью стресс-лимитирующих систем (натрий-уретические пептиды и др.). Наиболее важный симптом ХСН - быстрая утомляемость - соотносится с нарушением
кровоснабжения скелетных мышц и развитием миопатии с нарастающей потерей мышечной массы, что само по себе снижает способность больных к выполнению физической нагрузки.
Одышка в значительной степени объясняется повышением давления в легочных венах вследствие высокого диастолического давления в ЛЖ. При увеличении притока крови это давление в ЛЖ и в легочных венах повышается и наоборот. Поэтому больные испытывают одышку и дискомфорт в положении лежа на спине, когда увеличивается венозный приток. Все мероприятия, уменьшающие венозный приток, уменьшают одышку и застойные явления в малом кругу (положение стоя, нитраты, салуретики, жгуты на ноги).
Жажда обусловлена активацией центра жажды ангиотензином II. Задержка натрия и воды из-за гиперпродукции ангиотензина II и альдостерона приводит к увеличению объема циркулирующей крови и диастолического наполнения сердца, появлению отеков и застойных явлений в органах (легкие, печень, почки, желудочно-кишечный тракт), увеличивается одышка, но сердцу удается поддерживать сердечный выброс.
По мере прогрессирования ХСН и сократительной дисфункции сердца сердечный выброс и АД снижаются, происходит централизация кровообращения за счет регионального повышения сосудистого сопротивления с дальнейшим ограничением кровотока в скелетных мышцах, коже, органах желудочно-кишечного тракта, печени, почках. Поэтому руки и ноги становятся холодными, кожа дистрофична.
Прогноз при ДКМП зависит от степени дилатации и дисфункции сердца.
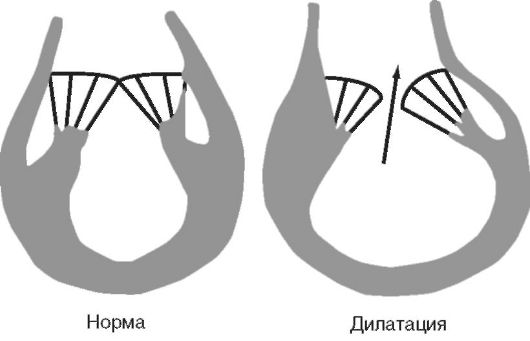 Рис. 1.1. Механизм развития атриовентрикулярной регургитации при ДКМП
Рис. 1.1. Механизм развития атриовентрикулярной регургитации при ДКМП
Вследствие нарушения перфузии органов и тканей в них развивается дистрофия, пневмофиброз, застойные пневмонии, фиброз печени с гипоальбуминемией, гиперферментемией, гипопротромбинемией, желтухой; «застойный гастрит», пептические эрозии и язвы желудка, нарушение моторики и функции желудочно-кишечного тракта, «застойная» почка с выделением белка, атрофия мышц с мышечной слабостью, энцефалопатия, анемия. В дилатированном сердце образуются тромбы, которые могут стать источником эмболий.
Ослабление сократительной функции миокарда при ДКМП сопровождается уменьшением ФВ и сердечного выброса. ФВ обычно ниже 40% (в норме 65-70%). Описан больной с ДКМП и ФВ 7% (!). Сердце расширяется и приобретает шарообразный вид (то же самое может быть при экссудативном перикардите).
Расширение сердца приводит к митрально-трикуспидальной регургитации даже при нормальной структуре клапанного аппарата, так как нарушается позиция папиллярных мышц (рис. которые, отдаляясь от центра желудочков, втягивают за собой створки клапанов в полости желудочков. В результате клапаны не закрывают отверстия между предсердиями и желудочками во время систолы, возникает регургитация, из-за которой выброс в сосуды еще больше снижается.
На ЭКГ обычно выявляется тахикардия. Могут присутствовать все известные нарушения ритма и проводимости. У половины боль-
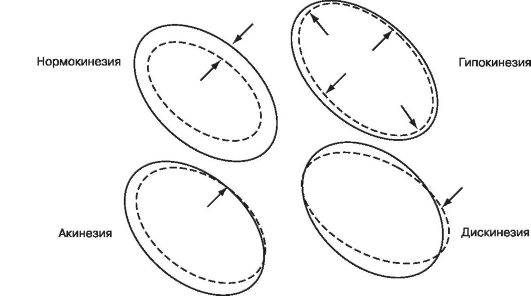 Рис. 1.2. Виды асинергии миокарда
Рис. 1.2. Виды асинергии миокарда
ных при суточном мониторировании ЭКГ видны периоды желудочковой тахикардии.
При выраженном миокардиофиброзе на ЭКГ может регистрироваться патологический зубец Q. Зубец Ти сегмент STвсегда изменены.
Мерцательная аритмия создает предпосылки для системных эмболий, а желудочковые нарушения ритма составляют угрозу внезапной аритмической смерти.
Принципы диагностики ДКМП и сердечной недостаточности
Увеличение сердца обычно обнаруживается при рентгенологическом или ультразвуковом исследовании сердца. Эхокардиографическое исследование позволяет оценить размеры полостей сердца, подвижность стенок (рис. 1.2) систолическую и диастолическую функцию ЛЖ, состояние клапанов, выявить аномальные сбросы и регургитации, жидкость в перикарде.
При ДКМП в полости перикарда может присутствовать небольшое количество жидкости, однако значительное количество жидкости при нерасширенных полостях сердца указывает на экссудативный перикардит.
По показаниям применяется коронароангиография, эндомиокардиальная биопсия (для диагностики воспалительных и инфильтративных болезней миокарда).
Дифференциальный диагноз при расширении сердца проводится между ДКМП, экссудативным перикардитом и пороками сердца.
Определение признаков сердечной недостаточности является важным и непростым, и врачи общей практики часто ставят неправильный диагноз. Согласно исследованию, проведенному в 1999 г. в Великобритании, диагноз сердечной недостаточности был подтвержден в клинике менее чем у 30% больных, направленных врачами общей практики с этим диагнозом.
Фрамингамские критерии сердечной недостаточности удовлетворяются при наличии 2 больших критериев или 1 большого и 2 малых (табл. 1.3).
Более простыми являются критерии сердечной недостаточности, рекомендованные рабочей группой по сердечной недостаточнос-
ти Европейского общества кардиологов (1995 г.): жалобы (одышка, усталость, задержка жидкости или их сочетание и признаки задержки жидкости в легких, подкожной клетчатке) в присутствии структурной или функциональной патологии сердца. В случае сомнения быстрый ответ на терапию сердечной недостаточности (обильный диурез с последующим ослаблением одышки) подтверждает ее диагноз.
Классификация ХСН
Признанной международной классификацией ХСН является классификация Нью-Йоркской ассоциации сердца (NYHA), которая разделяет больных по функциональным классам в зависимости от выраженности одышки и переносимости физической нагрузки (табл. 1.4).
Таблица 1.4
Классы сердечной недостаточности (классификация Нью-Йоркской ассоциации сердца)
ФК. Определение | Название |
I. Физическая активность не ограничена. Обычная физическая активность не вызывает необычной усталости, сердцебиения, одышки, стенокардии. | Бессимптомная дисфункция ЛЖ |
II. Легкое ограничение физической активности. В покое жалоб нет, но обычная физическая нагрузка сопровождается усталостью, одышкой, сердцебиением, стенокардией. | Легкая |
III. Заметное ограничение физической активности. В покое жалоб нет, но нагрузка меньше обычного уровня сопровождается усталостью, одышкой, сердцебиением. | Средней тяжести |
IV. Дискомфорт присутствует даже в покое, и физическая нагрузка любого уровня его усиливает. Одышка, сердцебиение усталость присутствуют даже в покое. | Тяжелая |
Данная классификация применима для заболеваний сердца, которые сопровождаются дисфункцией ЛЖ, что происходит параллельно
со снижением ФВ ЛЖ и появлением объективных признаков сердечной недостаточности. У лиц с «функциональными» сердечно-сосудистыми заболеваниями (кардионеврозы, нейроциркуляторная астения или дистония) с жалобами на слабость, сердцебиение и одышку - нет дисфункции сердца, сердечной недостаточности, и к ним эта классификация не применима.
В России имеет хождение клинико-морфологическая классификация сердечной недостаточности по стадиям, предложенная Г.Ф. Лангом в 1934 г., которая с тех пор многократно добавлялась и уточнялась (табл. 1.5.), или ее модификации (Н.Д. Стражеско - В.Х. Василенко). В описании стадий сохранена прежняя терминология Г.Ф. Ланга.
Таблица 1.5
Сердечная недостаточность по классификации Г.Ф. Ланга
Стадия | Определение |
I | Латентная. Симптомы нарушения кровообращения (одышка, утомляемость сердцебиение) появляются во время или после физической нагрузки. |
II а | Одышка и тахикардия становятся почти постоянными или появляются при очень легкой нагрузке. Обнаруживаются симптомы миогенной дилатации сердца и застойные явления в малом кругу при левожелудочковой недостаточности и в печени - при недостаточности правого сердца. |
III б | Застойные явления в малом и большом кругах кровообращения. Застой в печени, в почках, отеки выражены резко при недостаточности правого сердца. |
III | Характеризуется выраженными необратимыми симптомами, функции всех органов нарушены, в них развиваются резкие изменения обмена (дистрофическая стадия). |
Глава 3 данного Руководства специально посвящена ХСН.
ОТДЕЛЬНЫЕ ВИДЫ ДКМП
Ишемическая ДКМП
При КБС развитие ДКМП является следствием обратимой дисфункции миокарда в результате длительной ишемии (ишемия, гибернация, оглушение миокарда) либо необратимой потери кардиомиоцитов при гибернации (апоптоз) или в результате ИМ. После ИМ может формироваться аневризма сердца со своими гемодинамическими особенностями.
Таблица 1.6
Ишемические состояния миокарда
Состояние | Причина и сущность |
Некроз | Длительная окклюзия. Некроз с исходом в рубец и фиброз. Сократительная функция полностью отсутствует. |
Острая ишемия | Временное ограничение коронарного кровотока. Сократительная функция нормальная или частично нарушена, при продолжении ишемии возможно развитие ИМ. С восстановлением кровообращения функция нормализуется. |
Оглушение | Преходящее значительное уменьшение, но затем восстановление коронарного кровотока. Сократительная функция после восстановления кровотока остается нарушенной (оглушение), но в дальнейшем восстанавливается. |
Гибернация | Постоянное или преходящее ограничение коронарного кровотока, усугубляемое любым стрессовым воздействием. Сократительная функция нарушена. Прогрессирующая гибель кардиомиоцитов. Сократительная функция полностью или частично восстанавливается после реваскуляризации. |
Ишемическая подготовка | Повторные короткие эпизоды ограничения коронарного кровотока. Сократительная фунция не нарушена, в зоне ишемии создается временная защита от повторных ишемических повреждений. Если при продолжении ишемии развивается ИМ, то меньших размеров. |
Вследствие ишемии в миокарде развиваются необратимые (некроз) и многообразные обратимые состояния (табл. 1.6).
В то время как ИМ ведет к необратимым нарушениям функции миокарда вследствие окончательной потери массы кардиомиоцитов (рубец, ремоделирование), при оглушении или гибернации функция миокарда полностью или частично восстанавливается при нормализации кровообращения.
Повторные болевые или безболевые эпизоды ишемии миокарда оказывают пагубное воздействие на сократительность миокарда, вызывая появление участков оглушения и гибернации.
Оглушение характеризует процесс постишемической преходящей дисфункции миокарда, когда ишемия недостаточно длительная, чтобы вызвать некроз (менее 20-25 мин.). Оглушение имеет место после транслюминальной коронарной ангиопластики в участках по соседству со свежим ИМ после тяжелого приступа стенокардии. Оглушение может сохраняться от нескольких часов до нескольких суток.
Гибернация или «спящий миокард», по определению S. Rahimtola, есть хроническое состояние миокарда с нарушенной функцией вследствие уменьшения коронарного кровотока и недостаточного поступления кислорода. Эта функция может быть полностью или частично восстановлена либо путем увеличения доставки кислорода, либо путем уменьшения потребности. Гибернация рассматривается как приспособление ишемизированного миокарда, вследствие чего сохраняется жизнь клетки в обмен на ослабление функции. Повторные, особенно частые, приступы болевой или безболевой ишемии миокарда могут вызывать состояние гибернации в участках миокарда, подвергавшихся ишемии. Такие же участки обнаруживаются в периинфарктных зонах. По одному из определений гибернация может рассматриваться как накопленное оглушение.
Следствием гибернации является не только дисфункция миокарда, но и прогрессирующая гибель кардиомиоцитов пострадавших от ишемии (апоптоз), что ведет к дальнейшей потере сократительной способности сердца («диффузный атеросклеротический кардиосклероз»). Поэтому гибернация должна своевременно диагностироваться и устраняться.
У больного с КБС в миокарде, видимо, присутствуют в разное время все перечисленные состояния в разных комбинациях и разной выраженности.
Нарушение сократительной функции миокарда объективно проявляется появлением в миокарде участков асинергии в виде гипо-
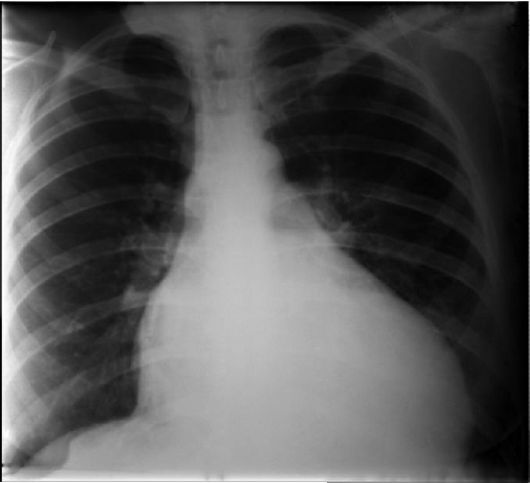 Рис. 1.3. Рентгенограмма грудной клетки больного с ДКМП. Значительное расширение сердца
Рис. 1.3. Рентгенограмма грудной клетки больного с ДКМП. Значительное расширение сердца
кинезии, акинезии или дискинезии (рис. 1.3). Если размеры таких участков значительны, то это приводит к нарушению насосной функции сердца со снижением ФВ ЛЖ и сердечного выброса. При КБС зоны асинергии могут быть локальными либо диффузными соответственно участкам гибернации, оглушения или миокарда с преобладанием рубцовой ткани.
Вследствие гибернации ХСН при КБС может развиваться не только у больных с болевыми формами (ИМ, стенокардия), но и при безболевых формах (безболевая ишемия миокарда), как бы исподволь, без предшествующих ИМ или стенокардии, и перед врачом предстает больной с «идиопатической» ДКМП.
Диагноз ишемической ДКМП строится на основании ряда критериев (табл. 1.7).
Таблица 1.7
Критерии ишемической ДКМП
 Некоторая нечеткость критериев объясняется следующим. Зубец Q на ЭКГ может быть не вследствие ИМ или ИМ может быть без зубца Q, наконец, ИМ может быть не следствием КБС. Ангиография может обнаружить стенотическое поражение артерий, однако следу-
Некоторая нечеткость критериев объясняется следующим. Зубец Q на ЭКГ может быть не вследствие ИМ или ИМ может быть без зубца Q, наконец, ИМ может быть не следствием КБС. Ангиография может обнаружить стенотическое поражение артерий, однако следу-
ет еще доказать, что это поражение является причиной миокардиальной дисфункции. Блокада ЛНПГ и другие изменения ЭКГ (например, синдром WPW) маскируют ИМ.
В настоящее время есть возможность обнаружения жизнеспособных, но плохо функционирующих участков миокарда (гибернация, оглушение).
Выявление гибернации требует специальных методик, часто недоступных в общей практике. Наиболее точной является позитрон-эмиссионная томография с использованием фтор-18 флуородеоксиглюкозы (ФДГ), которая «отмечает» области с повышенным использованием экзогенной глюкозы относительно сниженной перфузии (несоответствие ФДГ и перфузии). Таким образом, выявляются зоны жизнеспособного миокарда со сниженным кровотоком.
Другие методики обнаружения гибернизирующего миокарда - это сцинтиграфия миокарда с таллием-201 и технецием-99, которые обнаруживают перфузируемые и метаболически активные участки. Полученные характеристики распределения этих трейсеров в миокарде сравниваются с локализацией участков асинергии, обнаруженных при эхокардиографии или вентрикулографии.
Стресс-эхокардиография с добутамином помогает обнаружить участки жизнеспособного, но асинергичного миокарда. Добутамин в небольших дозах стимулирует жизнеспособный ишемизированный миокард, улучшая его сократительность, в то время как последующие большие дозы нарушают ее. Изменения толщины и подвижности стенок миокарда отслеживаются очень точно.
Если в основе ДКМП лежит гибернация миокарда, то операция реваскуляризации миокарда может привести к восстановлению или улучшению функции миокарда и уменьшению выраженности симптомов ХСН.
Нарушение сократительной способности миокарда при ишемической ДКМП связано с гибернацией или потерей кардиомиоцитов (инфаркт, апоптоз).
Успешная реваскуляризация миокарда (АКШ, ЧТКА) может привести к восстановлению функции миокарда при гибернации.
Гипертензивная ДКМП
Вклад АГ в развитие ДКМП оценить нелегко, так как АГ часто является сопутствующим заболеванием. У половины больных с ишемичес-
кой ДКМП присутствовала АГ; АГ отмечалась (в прошлом или настоящем) среди 44% всех больных ДКМП (Kasper E.K. и соавт., 1994).
По данным эпидемиологических исследований, АГ вторая после КБС причина развития ХСН. Провоцирующая роль АГ подчеркивается тем обстоятельством, что при правильном лечении АГ частота развития ХСН снижается наполовину по сравнению с группой нелеченых больных с АГ.
Табл. 1.8 дает схематическое представление о развитии поражения миокарда и ХСН при АГ.
Таблица 1.8
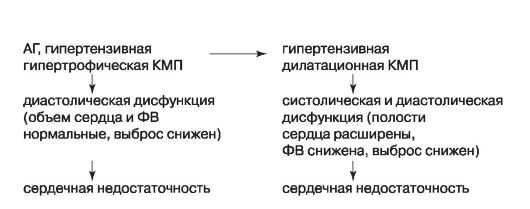 При
АГ развивается распространенная микроангиопатия (ремоделирование,
сужение артериол с гипертрофией мышечного слоя, потеря
микроциркуляторного русла), гипертрофия ЛЖ, его диастолическая и
систолическая дисфункция, более ранний и распространенный атеросклероз.
При
АГ развивается распространенная микроангиопатия (ремоделирование,
сужение артериол с гипертрофией мышечного слоя, потеря
микроциркуляторного русла), гипертрофия ЛЖ, его диастолическая и
систолическая дисфункция, более ранний и распространенный атеросклероз.
Из-за диастолической дисфункции нарушается наполнение ЛЖ, что отчетливо определяется при оценке трансмитрального потока (допплерография). Давление наполнения ЛЖ повышается, а ударный объем снижается. Формируется «диастолическая» сердечная недостаточность (при нормальном объеме и ФВ ЛЖ). Переносимость физической нагрузки ухудшается, появляются другие симптомы сердечной недостаточности.
Левое предсердие быстро дилатируется, наполняя неподатливый ЛЖ. Устанавливается мерцательная аритмия, что ведет к дальнейшему уменьшению наполнения ЛЖ.
На стадии гипертрофии ЛЖ без дилатации возможно частичное обратное развитие процесса при адекватной гипотензивной терапии,
которая может приводить к регрессии гипертрофии ЛЖ и улучшению диастолической функции.
Если АД не контролируется, ЛЖ дилатируется, развивается систолическая дисфункция ЛЖ, ФВ начинает снижаться. Гипертензивная гипертрофическая КМП (гипертоническое сердце) переходит в гипертензивную ДКМП.
Для диагноза гипертензивной ДКМП необходимо наличие АГ (АД более 160/100 мм рт.ст. при повторных измерениях) и/или признаков поражения органов мишеней. Мягкая АГ, которая очень распространена, не может объяснить значительную дисфункцию ЛЖ! С другой стороны, при развитии гипертензивной ДКМП АД у больных может снижаться и становиться нормальным («обезглавленная», «выгоревшая» АГ). В этом случае анамнез и поражения других органов-мишеней (глазное дно, почки) позволяют поставить диагноз. На ЭКГ, как правило, отмечаются признаки гипертрофии и перегрузки ЛЖ.
Гипертензивная ДКМП развивается при длительной и выраженной АГ, обычно поражены и другие органы-мишени (глазное дно, почки, головной мозг).
У больных с гипертензивной ДКМП при ультразвуковом исследовании сердца может выявляться фиброз створок клапанов (износ, дегенеративные изменения), что при дилатированном сердце и систолическом шуме в предсердной и подмышечной областях (в связи с дилатацией сердца) склоняет к диагнозу порока сердца.
Клапанная ДКМП
Термин «клапанная ДКМП» в соответствии с рекомендациями рабочей группы ВОЗ (1996 г.) можно применять в случаях, когда степень желудочковой дисфункции и дилатации у больных пороками сердца не пропорциональна выраженности ненормальных условий нагрузки. Такая расплывчатость определения предполагает, что при постановке диагноза существенное значение имеет клинический подход.
Например, специфические особенности рентгенологической конфигурации сердца свойственные тому или иному пороку (например, расширение сердца вправо и выбухание дуги легочной артерии при митральном стенозе) теряются, сердце расширяется во все стороны.
Из-за малого сердечного выброса патологические шумы могут не выслушиваться.
Дисметаболическая ДКМП
Сахарный диабет
Датский терапевт K. Lundback в 1954 г. предположил, что высокая распространенность ХСН при сахарном диабете обусловлена развитием специфической диабетической ДКМП.
К настоящему времени сложилось представление, что так называемая «диабетическая КМП» является следствием частого сочетания сахарного диабета, КБС и АГ.
При морфологическом исследовании в сердце больных с диабетической КМП не обнаружено специфических признаков.
Дисфункция эндотелия - один из «участников» развития диабетической КМП, сопровождается нарушением эндотелий-зависимой вазодилатации и при сахарном диабете, видимо, является следствием гипергликемии.
Избыточное окисление жирных кислот в миокарде требует повышенного количества кислорода и ведет к накоплению промежуточных продуктов обмена, которые оказывают нежелательные воздействия на миокард: нарушения ритма и проводимости, перегрузка кальцием.
Нейропатия, свойственная сахарному диабету, затрагивает и миокардиальную иннервацию. Следствием этого является парасимпатическая дисфункция с тахикардией, которая увеличивает миокардиальную потребность в кислороде, и уменьшение вариабельности сердечного ритма, что соотносится с увеличением риска внезапной смерти. Наконец, больные с сахарным диабетом имеют пониженную чувствительность к ишемической боли (нейропатия), и у них часто обнаруживаются безболевые формы КБС.
Среди особенностей лечения декомпенсированной диабетической КМП следует отметить использование петлевых диуретиков (фуросемид), которые не нарушают углеводный обмен, селективных бета-адреноблокаторов для устранения тахикардии и лечение самого сахарного диабета.
Тиреотоксикоз
Поражения сердечно-сосудистой системы почти всегда имеются при тиреотоксикозе и часто являются ведущими в клинической картине. ТЗ-активная форма тиреоидного гормона вызывает большинс-
тво биологических эффектов: изменения экспрессии различных клеточных белков, стимуляция термогенеза, воздействие на сердце и гладко-мышечные клетки сосудов. Большая часть ТЗ образуется путем конверсии из Т4, которая происходит в основном в печени, меньшая часть ТЗ (около 15%) образуется непосредственно в щитовидной железе.
Благодаря избытку ТЗ при тиреотоксикозе увеличивается сердечный выброс и сократительность миокарда, возникает тахикардия. Из-за снижения сосудистого сопротивления артериол большого круга кровообращения снижается среднее АД, что приводит к стимуляции РААС и задержке натрия. Увеличение объема плазмы наряду с увеличением продукции эритропоэтина приводит к увеличению объема циркулирующей крови и преднагрузки на сердце.
У части больных с тиреотоксикозом появляется одышка при нагрузке, ортапное, периферические отеки, расширение вен на шее и ритм галопа. Возникают признаки тиреотоксической КМП. На первых этапах развития тиреотоксического сердца сохраняется большой сердечный выброс, превышающий нормальный в 2-3 раза, а сердце не расширено. В этот период плохая переносимость нагрузки больными объясняется не сердечной недостаточностью, а слабостью периферических и дыхательных мышц.
Хотя сопротивление артериол большого круга кровообращения при тиреотоксикозе снижается, легочное сосудистое сопротивление не снижается. Это приводит к тому, что на фоне большого сердечного выброса и объема циркулирующей крови давление в легочной артерии становится высоким, развивается недостаточность правого желудочка с повышением венозного давления, набуханием шейных вен, увеличением печени, появлением периферических отеков.
При длительно существующей тахикардии и мерцательной тахиаритмии сократительность миокарда, сердечный выброс и фракция выброса ЛЖ становятся низкими, сердце дилатируется, возникает легочный застой, формируется застойная сердечная недостаточность. Полагают, что такая ДКМП возникает главным образом из-за тахикардии. Поэтому устранение тахиаритмии приводит к быстрому клиническому улучшению даже при отсутствии антитиреоидной терапии.
Тиреотоксикоз возникающий на фоне ишемической болезни сердца усугубляет все ее клинические проявления.
Ведущими при тиреотоксикозе являются такие симптомы, как нервозность, возбуждение, сердцебиение, тремор, диарея, потеря
веса, слабость, потливость. Вследствие периферической вазодилатации (из-за повышения основного обмена) руки влажные и теплые (у больных с нейроциркуляторной астенией - влажные и холодные), АД и пульсовое давление повышено, движения больных быстрые, что не свойственно больному с сердечной недостаточностью. У основания сердца выслушивается «функциональный» систолический шум (высокий сердечный выброс).
Приблизительно у 1/4 больных имеется постоянная или пароксизмальная форма мерцательной аритмии. Поэтому в случаях необъяснимой мерцательной аритмии после исключения митрального стеноза, КБС, дефекта межжелудочковой перегородки, миксомы левого предсердия, инфекционного эндокардита следует исключить и тиреотоксикоз. Если главной клинической чертой является сердечная недостаточность, то следует искать и другие ее причины, которые могут быть скрытыми: порок сердца, дефект межпредсердной перегородки, «обезглавленная» АГ, КБС, мерцательная аритмия с большой ЧСС.
Специальные методы диагностики включают: определение в крови тироксина (Т4), три-йод-тиронина (Т3), тиреотропного гормона.
Лечение гипертиреоидизма требует тиреостатических препаратов, применения радиоактивного йода или хирургической операции. Быстрое устранение сердечно-сосудистых симптомов дают бетаадреноблокаторы. Применение дигоксина неэффективно!
Если при достижении эутиреоидного состояния мерцательная аритмия сохраняется, показана кардиоверсия.
Гипотиреоидизм
Гипотиреоидизм обычно развивается вследствие аутоиммунного тиреоидита, после лечения радиоактивным йодом или тиреоидэктомии. Зябкость, слабость, сухая кожа, нарушение памяти встречаются часто. Кожа имеет желтоватый оттенок вследствие накопления каротина (нарушение его превращения в витамин А). Лицо одутловатое, плотные отеки голеней. Голос грубый. Активность креатинкиназы (мышечная форма) в крови значительно повышена. Уровень тиреотропного гормона низкий. Отмечается диастолическая гипертензия, обусловленная повышением периферического сосудистого сопротивления из-за нарушения продукции эндотелием релаксирующих факторов, главным образом оксида азота.
Рентгенологически сердце увеличено в размерах вследствие скопления экссудата в полости перикарда, дилатации сердца или сочетания того и другого. Жидкость может быть также в плевральной и брюшной полостях. Накопление жидкости связывают с замедлением лимфатического дренажа тканей.
При микседеме отмечается брадикардия, слабый пульс. Тоны сердца глухие. Вольтаж зубов ЭКГ низкий из-за перикардиального экссудата. Зубцы Р могут быть не видны, что создает впечатление узлового ритма. Интервал QT может быть удлинен, что приводит к появлению желудочковой тахикардии типа «пируэт». Содержание ХС и ЛПНП в крови значительно повышено. Кристаллы ХС могут присутствовать в перикардиальном экссудате. При ультразвуковом исследовании сердца функция ЛЖ обычно нормальная, а в более прогрессивных стадиях гипотиреоза ФВ снижена, а полость ЛЖ дилатирована. Эти нарушения связывают с повышением после нагрузки, дефицитом энергии в миокарде и ишемией миокарда. Сцинтиграфия миокарда с таллием обнаруживает признаки ишемии миокарда...
Гипотиреоидизм часто не диагностируется, так как симптомы развиваются медленно.
Вследствие гиперхолестеринемии, диастолической гипертензии, повышения уровня гомоцистеина больные с гипотиреозом имеют высокий риск развития атеросклеротических сосудистых заболеваний.
Заместительная терапия тиреоидными гормонами дает быстрый результат, однако у больных с сопутствующей КБС она должна начинаться осторожно из-за возможной провокации тахикардии, стенокардии, ИМ или застойной сердечной недостаточности.
Перикардиальная жидкость исчезает на фоне заместительной терапии.
Гемохроматоз
Развивается из-за избыточного накопления железа в тканях вследствие повышенного всасывания железа в кишечнике (идиопатический, генетический гемосидероз) или многократных гемотрансфузий (вторичный посттрасфузионный гемосидероз). Избыток железа откладывается в виде ферритина (первичный) или гемосидерина (при вторичном гемосидерозе) во внутренних органах (в печени, сердце, поджелудочной железе, селезенке и др.), вызывая развитие фиброза (сидероз).
Болезнь проявляется «бронзовым» диабетом в сочетании с циррозом печени, поражением сердца (с чертами ДКМП или рестриктивной КМП), артропатией с хондрокальцинозом. Примером вторичного сидероза миокарда с развитием прогрессирующей ДКМП является сидероз вследствие частых гемотрансфузий при большой бета-талассемии.
Диагноз гемохроматоза может быть установлен при сочетании ДКМП, цирроза печени или диабета и необычной бронзовой или серой окраски кожи. Бронзовая окраска связана с накоплением меланина, вызванного отложением железа. Уровень сывороточного железа и ферритина высокий. Диагноз подтверждается обнаружением избытков депонированного железа в костном мозге или в коже.
При первичном гемохроматозе лечение состоит из заборов крови путем венопункции в течение многих месяцев и применения дефроксамина. Дефроксамин связывает железо, которое находится в свободном виде, либо в составе ферритина и гемосидерина. Образующееся соединение выводится с мочой, вследствие чего уменьшаются отложения железа в тканях. Таким образом, возможно устранение симптомов ДКМП. При вторичном сидерозе применяются препараты, связывающие железо и способствующие его выведению из организма (деферипрон, десферриоксамин).
Алкогольная ДКМП
Данная патология имеет, видимо, значительное распространение. Согласно P. Pinney и M. Mancini (2005, США), до 45% от всех случаев ДКМП может быть связано с избыточным употреблением спиртных напитков. Алкогольная ДКМП или алкогольное поражение сердца является следствием действия продуктов метаболизма этанола на миокард. В Канаде описана эпидемия болезни сердца, вызванной кобальтом, который добавлялся в пиво для улучшения качества пены.
Алкоголь метаболизируется главным образом в желудке и печени с помощью нескольких ферментных систем-алкогольной дегидрогеназы, альдегиддегидрогеназы и этаноловой окислительной микросомальной системы. Большая часть алкоголя окисляется до ацетальдегида при участии алкогольной дегидрогеназы. Ацетальдегид является токсичным веществом и оказывает большую часть повреждающих эффектов на клетку вплоть до развития некроза. В даль-
нейшем ацетальдегид превращается в ацетил-КоА и ацетат. Ацетат окисляется до углекислого газа и воды либо превращается в жирные кислоты.
Калорийность алкоголя высокая, почти как у жиров - окисление 100 г этанола дает 700 ккал. Поэтому у алкоголиков энергетические потребности могут удовлетворяться за счет спирта.
Алкогольная ДКМП имеет все клинические и гемодинамические атрибуты ДКМП. Иногда в клинической картине преобладают пароксизмальные или постоянные нарушения ритма, особенно мерцательная аритмия. На фоне хронического поражения миокарда у больных могут возникать обострения: острая алкогольная дистрофия миокарда с новыми или нарастающими, но часто преходящими изменениями ЭКГ (зубца Т и сегмента ST), пароксизмальными нарушениями ритма, обычно в виде мерцательной тахиаритмии или желудочковых нарушений ритма. Последние могут являться причиной внезапной смерти или быстрого развития сердечной недостаточности, спровоцированной алкогольной перегрузкой или тахиаритмией. Такие поражения сердца часто вызываются острым алкогольным отравлением («праздничное сердце»).
Нарушения ритма могут быть единственными проявлениями алкогольного поражения сердца.
В соответствии с диагностическими критериями ВОЗ (1996 г.) у больных с алкогольной ДКМП должна быть: история длительного, более 5 лет, чрезмерного употребления алкоголя (более 40 г этанола в день у женщин и более 80 г у мужчин), в случае абстиненции через 6 мес. должна наступить ремиссия ДКМП. Малые дозы алкоголя не имеют повреждающего воздействия на миокард, и 10-30 г этанола, соответственно, для женщин и мужчин, считаются даже «кардиопрофилактической» дозой (1-3 станд. ед. алкоголя; 1 станд. ед. алкоголя равна 10 мл этанола) с антиатерогенным эффектом.
Опасной дозой этанола считается доза более 80 г в сутки. Риск поражения внутренних органов при систематическом употреблении алкоголя возрастает с увеличением дозы. При суточной дозе 160 г он считается высоким, при дозе 80 г - средним и при дозе 40 г низким. Для женщин соответствующие дозы в два раза меньше.
Алкоголь в количестве 8 мл нейтрализуется в организме в течение 1 часа. Долговременные эффекты алкоголя в виде развития
алкогольной висцеропатии не зависят от вида алкогольного напитка, но кратковременные (синдром похмелья) зависят от содержания в этих напитках других спиртов, прежде всего изоамилового, которые относятся к сивушным маслам (congeners).Эти спирты присутствуют в дешевых сортах крепких напитков.
При диагнозе алкогольной ДКМП следует учитывать более молодой возраст больных по сравнению с больными ишемической ДКМП, признаки полиорганного поражения, свойственного алкоголизму: цирроз печени, нефрит, полинейропатия, гастроэнтероколит, атрофия яичек и др. Однако поражения печени (стеатоз, гепатит, цирроз) или других органов не обязательно указывают на вовлеченность сердца.
Различные стигматы или знаки алкоголизма (гиперемия лица и конъюнктивы, паротит, конрактура Дюпюитрена) также не всегда соотносятся с поражением сердца.
Исследование печеночных ферментов (АЛТ, АСТ-гамма-глютамил транспептидаза) лишь подтверждает повреждение печени, но для диагноза алкогольной ДКМП, особенно в присутствии ХСН, лишено смысла, так как активность этих ферментов может быть повышена при ХСН любого происхождения. Увеличение объема эритроцитов (более 100 fl) характерно для алкогольной ДКМП, но также прямо не свидетельствует о поражении сердца. В крови алкоголиков может обнаруживаться в повышенном количестве асиалированный транферрин.
Диагноз алкогольного поражения сердца затрудняется тем, что многие больные скрывают факт злоупотребления алкоголем. В Москве, как показало одно из исследований, у большинства больных с алкогольной ДКМП устанавливался диагноз КБС.
При алкогольной ДКМП часто имеются и другие признаки алкогольной висцеропатии.
При раннем диагнозе алкогольной ДКМП воздержание от алкоголя имеет решающее значение для излечения. Если диагноз ставится поздно, то органные изменения и клиника необратимы. Смерть часто наступает внезапно.
К обычно проводимой терапии по поводу ДКМП следует добавить тиамин 50 мг в/в или перорально.
При развитии у алкоголиков тиаминовой недостаточности, обусловленной углеводной диетой, потреблением «алкогольных» калорий или инфекцией, выявляются признаки высокого сердечного выброса
(теплые конечности, скачущий пульс). Без тиаминовой недостаточности при алкогольной ДКМП имеются признаки малого сердечного выброса (холодные конечности, ФВ снижена). Большие дозы тиамина неэффективны при алкогольной ДКМП без тиаминовой недостаточности в противоположность «алкогольной» бери-бери.
При бери-бери вызванной углеводной диетой с недостатком тиамина, которые встречаются очень редко, имеются признаки сердечной недостаточности с высоким сердечным выбросом, и от тиамина наступает быстрое выздоровление.
Иммуновирусная или инфекционно-воспалительная ДКМП и острый миокардит
Вирусные миокардиты являются одной из важных причин развития ДКМП. Впечатляющими в этом отношении являются результаты исследования миокардиальных биоптатов, в которых у 20-25% больных с ДКМП обнаруживались кардиотропные вирусы-коксаки В и цитомегаловирусы.
Среди инфекционных агентов (табл. 1.9) вирусы наиболее часто вызывают миокардиты, особенно вирус коксаки В, что случается приблизительно у 5% заболевших этой инфекцией, однако клинические признаки вовлечения сердца обнаруживаются еще реже.
Таблица 1.9
Возбудители инфекционных миокардитов
Вирусы | Коксаки В, энтеровирусы, инфлюэнца, цитомегаловирусы, ВИЧ, вирусы краснухи, паротита, оспы, ветрянки, герпеса, адено |
Бактерии | Дифтерийная палочка, пневмококк, стрептококк |
Риккетсии | Возвратного тифа, гемморагической лихорадки |
Грибы | Гистоплазма, токсоплазма, кандида, аспергиллюс |
Паразиты | Трипаносома, шистозома |
Похожие на миокардит поражения миокарда развиваются при системных заболеваниях (системная красная волчанка, полиомиозит), при воздействии лекарств (цитостатики, гидролазин, дизопирамид, фенотиазин, кортикостероиды и др.), при отторжении сердечного трансплантата.
Миокардит может протекать бессимптомно или с характерной клиникой. Исходы могут быть различными: выздоровление, выздоровление с рецидивами, хронический миокардит, летальный исход.
Миокардит может быть диффузным с вовлечением перикарда или локальным, очаговым. Вирусный миокардит почти всегда сопровождается перикардитом с образованием выпота, «миоперикардит».
Гистологически миокардит характеризуется воспалительной инфильтрацией миокарда с некрозом и дегенеративными изменениями кардиомиоцитов. Выделяют три фазы в течении миокардита: активный, заживающий, заживший. Клинически и гистологически выделяют также злокачественные формы, заканчивающиеся либо ранней смертью, либо полным выздоровлением.
После периода забвения в клиническую практику вновь вводится термин «хронический миокардит», при котором в миокарде нет миоцитолиза, но имеются инфильтраты рядом с миофибриллами, либо в интерстиции, и выраженный в разной степени фиброз.
Остаточные изменения в миокарде могут проявляться нарушениями ритма и проводимости, изменениями конечной части желудочкового комплекса ЭКГ, признаками ДКМП, что послужило основанием для введения терминов «постмиокардитная болезнь», «миокардитический кардиосклероз». По клиническим признакам часто невозможно отличить острый миокардит или заживший от ДКМП, не прибегая к инвазивным исследованиям.
Несмотря на накопление доказательств связи ДКМП с вирусными поражениями сердца, пока нет четких диагностических критериев этого поражения, в качестве которых фигурируют: обнаружение вируса в миокарде (электронная микроскопия) либо вирусной РНК или ДНК (методы молекулярной биологии - полимеразная цепная реакция, гибридизация и др.). Четырехкратное увеличение титра противовирусных антител, положительный тест на ELISA после очевидного вирусного заболевания с поражением сердца увеличивает вероятность вирусной этиологии заболевания.
Термин «иммунное заболевание сердца» также обретает доказательства в случаях обнаружения признаков активации иммунной системы. В крови больных с ДКМП или в эндомиокардиальных биоптатах обнаруживаются многочисленные антитела и аутоантитела: против мембран сарколеммы или миолеммы (АMLA-antimyolemmal antibodies), антинуклеотидные транслокаторные антитела (anti-ANT antibodies), антифибрилляторные антитела (AFA), места связывания
иммуноглобулинов в биоптатах, экспрессия комплекса гистосовместимости классов I и II на кардиомиоцитах и др.
Клиника миокардита бывает яркой или стертой, когда только преходящие изменения ЭКГ указывают на вовлечение миокарда. У части больных может быть предшествующее инфекционное заболевание или «простуда» с повышением температуры, недомоганием, болями в мышцах. Больные жалуются на одышку, сердцебиение, перебои в работе сердца, боли в груди (вследствие перимиокардита, инфарктов легких). При поражении перикарда боли обычно длительные, загрудинной локализации, усиливаются при наклоне вперед и глубоком вдохе. Боли при остром миокардите могут возникать остро и по клинике и ЭКГ напоминать ИМ, особенно у молодых.
При тяжелом миокардите развивается гипотензия, олигурия, тоны сердца глухие, ритм галопа (трехчленный ритм из-за появления III тона), митральная и трикуспидальная регургитация из-за расширения сердца, шум трения перикарда при перикардите. Если болезнь прогрессирует, появляются периферические отеки, жидкость в плевральной и брюшной полостях, эмболии. Смерть может наступить внезапно.
Периферическая кровь при остром миокардите не имеет особенностей, хотя у 1/4 больных может быть лимфоцитоз.
У всех больных изменена ЭКГ. Это обычно подъем сегмента ST и инверсия зубца Т, нарушения ритма и проводимости. По мере стихания перикардита сегмент ST опускается. Патологический зубец Q появляется редко. При очаговых миокардитах даже при ненарушенной функции миокарда могут наступать опасные нарушения проводимости из-за локального поражения проводящей системы.
Описанные изменения ЭКГ при остром миокардите носят преходящий характер, в то время как при ДКМП они постоянные. Плохое прогностическое значение при миокардите имеет развитие полной атриовентрикулярной блокады.
Преходящие изменения ЭКГ (зубец Т, сегмент ST) или нарушения ритма, например пароксизмальная желудочковая тахикардия, могут быть единственными проявлениями миокардита.
При рентгенологическом исследовании отмечается расширение сердца за счет его камер, перикардиального выпота или сочетания того и другого. При полном выздоровлении размеры сердца быстро становятся нормальными.
При тяжелом миокардите во время эхокардиографии обнаруживается расширение всех камер сердца, распространенная гипокинезия,
редко дискинезия с развитием аневризмы, снижение ФВ, внутрисердечные тромбы. При очаговых миокардитах сердце нормальных размеров, но с участками асинергии, что требует проведения дифференциального диагноза с КБС, при которой также присутствуют локальные асинергии.
Обнаружение перикардиального выпота при эхокардиографии позволяет заподозрить воспалительный процесс. Иногда выявляется уплотнение перикарда.
Эхокардиография у больных миокардитом имеет большое значение в оценке сократительной функции миокарда.
Радионуклидные методики с использованием галия-67 и индия-111 (моноклональные антимиозиновые антитела) используются для обнаружения участков воспаления в миокарде. Пока нет ясности в том, каково соответствие между накоплением этих радионуклидов в миокарде и гистологической картиной в выявленных участках «воспаления».
Обычные лабораторные исследования также используются для доказательства воспалительного процесса (СОЭ, С-реактивный белок, белковые фракции).
Для выявления инфекционного начала разрабатываются вирусологические, иммунологические исследования, методы молекулярной биологии. Важное значение придается изоляции вируса из миокарда, а также многократному увеличению титра нейтрализующих противовирусных антител в острой фазе миокардита по сравнению с периодом выздоровления. Первый подход пока себя не оправдал, при втором возможны случайные «доказательные» находки. В научных целях используется ряд методик обнаружения вирусной РНК в миокарде (гибридизация, полимеразная цепная реакция).
Эндомиокардиальная биопсия левого или правого желудочка с доступом через феморальную артерию или вену позволяет увидеть гистологическую картину текущего, заживающего или зажившего миокардита. При исследовании большой группы больных ДКМП гистологические признаки миокардита в эндомиокардиальных биоптатах были выявлены у 4,5% больных. Однако в случаях «острой» ДКМП, развившейся в течение последних 9 месяцев, признаки миокардита были найдены у 19% больных (Cowie M.R. et al., 1999).
При очаговом миокардите, эндомиокардиальный биоптат может не показать признаков воспаления, если взят из здорового участка.
Коронароангиография позволяет уточнить диагноз ДКМП, в частности определить безболевые формы КБС с ДКМП.
Таблица 1.10
Диагноз вирусного миокардита
1. Клинические и инструментальные исследования | - Недавнее вирусоподобное заболевание; - боли в груди, шум трения перикарда; - изменения ЭКГ; - рентгенологическое исследование: расширение сердца; - эхокардиография: перикардиальный выпот, асинергия миокарда |
2. Лабораторные, вирусологические, иммунологические исследования | - Лимфоцитоз (у 1/4 больных); - признаки воспаления (СОЭ, С-реактивный белок, белковые фракции); - признаки миокардиального повреждения: МВ-КФК, тропонин-Т; - увеличение титра противовирусных нейтрализующих антител; - Ig M ELISA |
3. Радионуклидные исследования | - Галлий -67; - индий-111 (моноклональные антимиозиновые антитела) |
4. Инвазивные исследования | - Эндомиокардиальная биопсия; - коронароангиография |
Основные данные по диагнозу вирусного миокардита суммированы в табл. 1.10.
Клинические наблюдения устанавливают связь между острым вирусным миокардитом и развитием в дальнейшем ДКМП.
В 1971 г. японец C. Kawai обнаружил высокие титры антител к вирусу коксаки В и простого герпеса у больных ДКМП по сравнению со здоровыми и выдвинул инфекционно-иммунную теорию развития
ДКМП.
Оказалось, что в 1/3 сердец больных с ДКМП удаленных при трансплантации обнаруживается энтеровирусная РНК и другие маркеры вируса, который может существовать в миокарде в мутированной форме при отсутствии гистологических признаков воспаления.
Клинически имунно-вирусная или инфекционно-воспалительная ДКМП может быть неотличима от миокардита.
Факторами неблагоприятного прогноза при миокардите и иммуно-вирусной ДКМП являются: длительность заболевания, тяжелый
(III-IV) функциональный класс сердечной недостаточности, кардиомегалия, высокое диастолическое давление в ЛЖ, нарушения ритма и проводимости, присутствие вируса в миокарде.
Лечение тяжелых миокардитов и иммуно-вирусной ДКМП - это прежде всего лечение сердечной недостаточности, которое не имеет специфических особенностей по сравнению с лечением других ДКМП. При критическом состоянии больных могут использоваться инотропы (левосимендан) или вспомогательные насосные устройства.
Пока нет стандартизованного специфического лечения для миокардитов и воспалительной ДКМП. Исключение могут составлять инфекционные миокардиты с известным возбудителем (антибиотики, интерферон). Обобщенные сведения о специфических подходах к лечению приведены в табл. 1.11.
Таблица 1.11
Иммуномодулирующая терапия при воспалительных ДКМП (по Felix S., Staudt A., Baumann G., 2002)
Терапия | Комментарии |
Антицитокиновая | Без эффекта |
Иммуносупрессия | Не должна использоваться рутинно Специальные показания |
Противовирусная | Изучается эффективность интерферонов |
Иммуноглобулины | Без эффекта |
Иммуноадсорбция | Есть эффект |
Цитокины (интерлейкин-1, опухолевый некротический фактор и др.) играют определенную роль в развитии воспаления и повреждении миокарда при миокардитах и ДКМП. Однако блокада рецепторов некротического фактора альфа (ФНО-α) с помощью препаратов этанерцепт, инфликсимаб не дало эффекта при ДКМП.
Применение иммуноглобулинов у больных с недавно диагностированной ДКМП с предположением ее воспалительного происхождения не дало положительных результатов.
Иммуноадсорбция сопровождалась улучшением клинической симптоматики и гемодинамики у больных с предполагаемой воспалительной ДКМП и ХСН. Она проводилась по одному сеансу в день в течение 3 дней подряд на протяжении 3 месяцев. После процедуры
Таблица 1.12
Показания к иммуносупрессивной терапии (по Frustaci A., Pieroni M., Chimenty С. с изм., 2002)
Тип миокардита | Ассоциированные заболевания и замечания |
При заболеваниях соединительной ткани | Системная красная волчанка Ревматоидный артрит |
При гиперэозинофильных синдромах | Болезнь Леффлера Эндомиокардиальный фиброз |
Гигантоклеточный миокардит | Встречается редко: при системных заболеваниях, лекарственной аллергии, туберкулезе |
Реакция отторжения трансплантированного сердца | |
Вирусный или идиопатический миокардит | При отсутствии признаков вируса в миокарде |
больным вводили иммуноглобулин G для профилактики инфекции (Felix S. et al., 2002). При введении адсорбированных антител в культуру изолированных кардиомиоцитов крыс было отмечено, что они угнетали транспорт кальция в кардиомиоцитах и их сократительную способность. Авторы сделали вывод, что циркулирующие аутоантитела, направленные против миокарда, обладают отрицательным инотропным эффектом, а их удаление при иммуноадсорбции приводит к улучшению гемодинамики. Кроме того, иммуногистологическое исследование эндомиокардиальных биоптатов больных показало, что иммуноадсорбция сопровождается уменьшением выраженности воспалительного процесса в миокарде.
Иммуносупрессивная терапия при воспалительных заболеваниях миокарда должна применяться по строгим показаниям, которые представлены в табл. 1.12.
Для иммуносупрессивной терапии используются глюкокортикоиды в сочетании с азатиоприном и циклоспорином А. Преднизолон (или метилпреднизолон) дается в дозе 1 мг на 1 кг веса тела в течение 1 мес., затем в дозе 0,33 мг на 1 кг веса в течение 5 мес. Азатиоприн дается из расчета 2 мг на 1 кг веса тела в день на 6 мес.
При обнаружении вирусного генома в эндомиокардиальных биоптатах проводится противовирусная терапия бета-интерфероном в
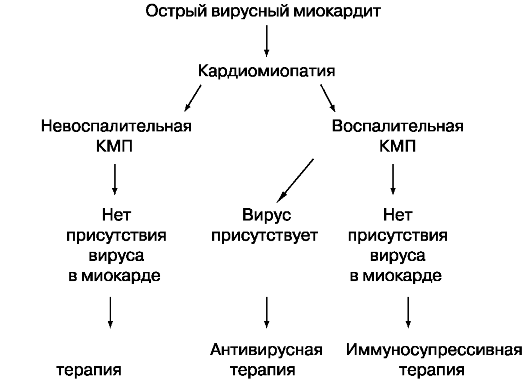
Схема 1.1. Лечение воспалительных КМП на основании исследований эндомиокардиальных биоптатов
течение 6 мес. Это приводит к значительному клиническому улучшению и устранению вирусного генома из миокарда. Направления терапии у больных с подозрением на воспалительную КМП приведены в схеме 1.1, составленной Kuhl U. и соавт. (2002).
Семейно-генетические КМП могут быть первичными, вследствие генетических мутаций в миокарде или вторичными на фоне существующих семейно-генетических заболеваний.
Доказана возможность генетической передачи ДКМП и этот механизм может присутствовать у 1/4 больных ДКМП. Однако, по данным клиники Mayo (1981), семейная ДКМП была диагностирована только у 2% больных ДКМП.
Описано несколько путей наследования ДКМП с локализованными хромосомными аномалиями. На основе клинических и молекулярно-генетических исследований выделены формы семейной ДКМП: аутосомно-доминантная с предшествующими нарушениями проводимости, аутосомно-доминантная, связанная с миопатией, аутосомно-рецессивная, Х-связанная, ДКМП вследствие мутации гена дистрофина, митохондриальная, ДКМП правого желудочка.
За исключением семейного анамнеза нет каких-либо клинических или гистопатологических характеристик, которые могли бы отличить семейную ДКМП от несемейной.
Основанием для подозрения семейной ДКМП являются:
• наличие не менее 2 случаев ДКМП в одной семье;
• случаи документированной внезапной смерти в возрасте до 35 лет среди родственников первой линии у больных ДКМП (Mestroni L. et al., 1999).
Обнаружение орган-специфических антител у больных и здоровых членов семьи с ДКМП показывает, что в патогенезе семейной ДКМП могут иметь значение аутоиммунные механизмы. Возможно, имеется семейная предрасположенность к вирусно-бактериальным инфекциям, вследствие которой включается аутоиммунный механизм, а антигенами являются белки митохондрий, сарколеммы, цитозоли кардиомиоцитов.
Диагноз семейной ДКМП ставится при наличии признаков ДКМП - расширение сердца, сниженная ФВ ЛЖ (см. в разделе «Определение и классификация»), которые являются главными критериями, и малых критериев (Mestroni):
• необъяснимые суправентрикулярные (фибрилляция предсердий или другие устойчивые аритмии) или желудочковые аритмии (экстрасистолия более 1000 в сутки или групповые 3 и более) в возрасте до 50 лет;
• расширение левого желудочка;
• необъяснимые нарушения проводимости: предсердно-желудочковая блокада 2-3 степени, полная блокада ЛНПГ, синоатриальная блокада;
• необъяснимая внезапная смерть или инсульт в возрасте до 50 лет;
• сегментарные асинергии ЛЖ при отсутствии нарушений внутрижелудочковой проводимости или КБС.
При клиническом обследовании больных с подозрением на семейную ДКМП особое внимание уделяется нейромышечной системе, поэтому стандартные лабораторные исследования включают определения КФК в крови. Рекомендуется консультация специалиста по нейромышечным заболеваниям.
Патологию нейромышечного аппарата следует заподозрить в следующих случаях:
• повышенный уровень КФК в крови;
• семейный анамнез мышечных заболеваний;
• патологическая электромиография;
• гипертрофия голеней, мышечные судороги, ригидность;
• мышечная слабость.
При обнаружении нейромышечной патологии проводятся специальные исследования:
• чрескожная биопсия скелетных мышц;
• электронная микроскопия мышц, определение содержания карнитина в мышцах и активности карнитин-пальмитил трансферазы (при нейромышечных метаболических расстройствах);
• при подозрении дистрофинопатии (высокий уровень ММ-КФК в крови) проведение специальных генетических исследований.
Поражение сердца может быть первым клиническим проявлением нейромышечных заболеваний (мышечные дистрофии Duchenne и Becker, митохондриальная миопатия, атаксия Freidreich, тяжелая миастения).
Клинико-лабораторные и инструментальные исследования следует выполнить и у членов семьи больного с подозрением на семейную ДКМП в поисках у них признаков ДКМП и возможной ее причины. Особое внимание при обследовании родственников также уделяется состоянию нейромышечной системы. Следует построить генеалогическую схему (родословную). Особенно трудно диагностировать ранние стадии семейной ДКМП, при которых начинающуюся патологию трудно отличить от нормы.
ДКМП при системных заболеваниях
Описано развитие ДКМП при саркоидозе, полиомиозите, системной склеродермии, красной волчанке.
При системной красной волчанке у 10-20% больных отмечается поражение сердца в виде миоперикардита с дилатацией сердца, часто на фоне АГ, связанной с поражением почек.
При тяжелой системной склеродермии в сердце развивается выраженный фиброз с клиникой рестриктивной КМП или ДКМП и сердечная недостаточность с нарушениями ритма и проводимости.
При саркоидозе сердечная недостаточность с ДКМП встречается редко. На аутопсии поражения сердца с формированием гранулем обнаруживаются у 1/4 больных. Может развиваться легочное сердце вследствие фиброза легких и поражения легочных сосудов.
Тахиаритмическая ДКМП
Тахиаритмической ДКМП, или тахикардиомиопатией обозначают нарушения сократительной функции миокарда с его дилатацией вследствие длительной тахикардии (суправентрикулярная, мерцательная тахиаритмия, длительные периоды желудочковой тахикардии, частая групповая экстраситолия). Такие тахиаритмии могут являться причинами развития сердечной недостаточности у больных с компенсированными до того заболеваниями сердца. Эффективное медикаментозное или хирургическое лечение нарушений ритма, как правило, приводит к восстановлению функции миокарда и устраняет симптомы сердечной недостаточности.
Перипартальная ДКМП
Заболевание неизвестного происхождения с признаками ДКМП, которое развивается в течение последних месяцев беременности, во время родов или спустя несколько месяцев после них. В благоприятных случаях заболевание продолжается 3-6 мес. с выздоровлением без клинических последствий, однако при повторной беременности симптомы сердечной недостаточности могут вновь появиться. У половины больных ДКМП быстро прогрессирует. Нередко наступает летальный исход.
Высказываются сомнения в существовании перипартальной ДКМП как самостоятельной формы заболевания, поскольку трудно доказать, что у заболевших не было скрыто протекавшей до беременности КМП.
Идиопатическая ДКМП
В половине случаев ДКМП причина заболевания остается нераспознанной. Предполагают, что под маской идиопатической ДКМП скрываются трудно выявляемые воспалительные или семейно-генетические ДКМП.
Диагноз идиопатической ДКМП устанавливается, если отвергаются другие возможные причины ДКМП с использованием следующих исключающих этот диагноз критериев:
• артериальная гипертензия: АД более 160/100 мм рт.ст. при повторных измерениях и/или признаки поражения органов-мишеней;
• КБС: обструкция более 50% одной из главных коронарных артерий и др. (см. «Ишемическая ДКМП»);
• типичный алкогольный анамнез (см. «Алкогольная ДКМП»);
• клинически выраженные устойчивые и с большой частотой тахикардии (см. «Тахиаритмичеакая ДКМП»);
• системные заболевания;
• пороки сердца;
• легочное сердце;
• болезни перикарда.
Если причина дилатации сердца и сердечной недостаточности не установлена, правомерен диагноз: идиопатическая ДКМП.
ЛЕЧЕНИЕ ДКМП
Как правило, больные с ДКМП обращаются к врачу при появлении симптомов сердечной недостаточности (одышка, слабость, утомляемость, отеки, сердцебиение). Лечение направлено на уменьшение
Таблица 1.13
Лечение ХСН при ДКМП
Мероприятия общего характера | • Сохранение оптимального веса, • ограничение поваренной соли и жидкости, • нутритивная поддержка, • воздержание от курения и чрезмерного, употребления алкоголя, • физические тренировки |
Фармакотерапия | • Ингибиторы АПФ, • диуретики, • бета-адреноблокаторы, • блокаторы рецепторов ангиотензина II, • антагонисты альдостерона, • сердечные гликозиды, • инотропы (спец. показания), • антикоагулянты (спец.показания), • антиаритмики (спец. показания) |
Хирургическое лечение | • Пересадка сердца, • вспомогательное сердце, • ресинхронизация |
выраженности этих симптомов с использованием мер общего характера, фармакотерапии и хирургии (табл. 1.13). В случаях вторичных ДКМП возможно и специфическое лечение, определяемое этиологией ДКМП (см. соответствующие разделы данной главы).
Фармакотерапия у больных с ДКМП и ХСН, как правило, включает диуретики, ингибиторы АПФ и бета-адреноблокаторы. В случае плохой переносимости ингибиторы АПФ могут быть заменены на блокаторы рецепторов ангиотензина II. При недостатоном диуретическом эффекте добавляются антагонисты альдостерона.
Терапия ХСН подробно представлена в главе 3 этого тома.