Нормальная физиология : Учебник. - Р.С. Орлов, А.Д. Ноздрачёв, 2009. - 688 с
|
|
|
|
ГЛАВА 3. ФИЗИОЛОГИЯ КЛЕТКИ
Функции организма выполняют органы и системы органов, состоящие из тканевых элементов. Главный тканевый элемент - клетка. Другими словами, выполнение функций организма определяется функциями клеток. Любую функцию клетки реализуют при помощи конкретных белков, информация о химической структуре которых записана в эндогенной клеточной программе - генах (сумма генов - клеточный геном). В этой главе изложены функции отдельных органоидов клетки, а также функции клеток, осуществляемые при помощи сочетанной работы разных органелл, а именно - реализация генетической информации (от гена до белка) и её регуляция, внутриклеточная подвижность (молекулярные моторы, или хемомеханические преобразователи), деградация внутриклеточного и поглощённого клеткой материала (внутриклеточное пищеварение), клеточный цикл и его регуляция.
Органеллы
Клетка состоит из трёх основных компартментов: плазматической мембраны (её функции рассмотрены в главе 2), ядра (включая ядерный геном) и цитоплазмы (цитозоль с находящимися в нём структурированными субклеточными единицами - органеллами, а также элементами цитоскелета и включениями). Органелла (органоид) - специализированный для выполнения конкретной функции элемент цитоплазмы (рис. 3-1). К органеллам относят свободные рибосомы, гранулярную эндоплазматическую сеть (шероховатый эндоплазматический ретикулум), гладкую эндоплазматическую сеть (гладкий эндоплазматический ретикулум), митохондрии, комплекс Гольджи, центриоли, окаймлённые пузырьки, лизосомы и пероксисомы.
Ядро
23 пары хромосом (диплоидньгй набор: 22x2 + XY у мужчин и 22x2 + 2X у женщин) ядра соматической клетки содержат ядерный
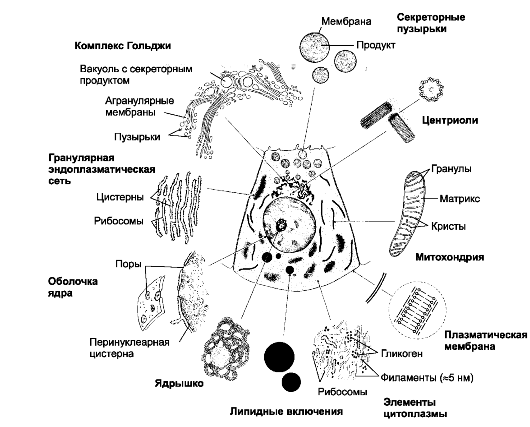 Рис. 3-1. Органеллы и включения [11]
Рис. 3-1. Органеллы и включения [11]
геном. Реализация генетической информации (транскрипция и процессинг, рис. 3-2) и другие функции ядра происходят при участии ДНК и разных видов РНК.
• Хроматин. Термином «хроматин» обозначают комплекс ядерной ДНК с белками (гистоны, негистоновые белки).
• ДНК. Молекула ДНК построена из двух полинуклеотидных цепей, образованных из нуклеотидов.
• Ген - участок молекулы ДНК, кодирующий последовательность аминокислот в полипептидной цепи. Экспрессия гена (рис. 3-2) протекает по схеме: транскрипция (синтез первичного транскрипта на матрице ДНК) - процессинг (образование мРНК) - трансляция (считывание информации с мРНК) - сборка полипептидной цепи (включение аминокислот в полипептидную цепь на рибосомах) - посттрансляционная модификация (добавление к полипептиду разных химических группировок, например, фос-
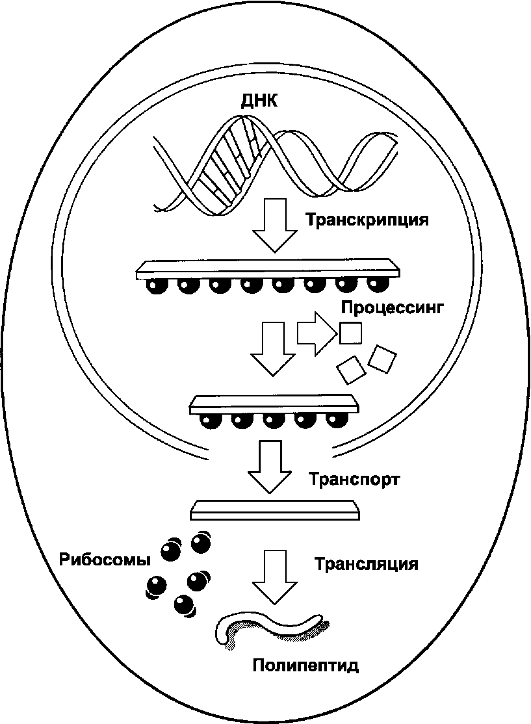 Рис. 3-2. Этапы реализации генетической информации [11].
В ходе транскрипции на ДНК-матрице синтезируется комплементарная ДНК -
длинная молекула РНК (первичный транскрипт), содержащая
последовательности экзонов и интронов. По завершении синтеза
РНК-транскрипта последовательности интронов удаляются (процессинг), что
делает молекулу РНК значительно короче. Эта мРНК выходит из ядра в
цитоплазму и соединяется с рибосомами. мРНК продвигается сквозь
рибосому, и её нуклеотидная последовательность транслируется в
соответствующую последовательность аминокислот создаваемой полипептидной
цепи
Рис. 3-2. Этапы реализации генетической информации [11].
В ходе транскрипции на ДНК-матрице синтезируется комплементарная ДНК -
длинная молекула РНК (первичный транскрипт), содержащая
последовательности экзонов и интронов. По завершении синтеза
РНК-транскрипта последовательности интронов удаляются (процессинг), что
делает молекулу РНК значительно короче. Эта мРНК выходит из ядра в
цитоплазму и соединяется с рибосомами. мРНК продвигается сквозь
рибосому, и её нуклеотидная последовательность транслируется в
соответствующую последовательность аминокислот создаваемой полипептидной
цепи
фатных (фосфорилирование), карбоксильных (карбоксилирование) и т.д.).
• РНК - полинуклеотид, сходный по химическому составу с ДНК, но содержащий в нуклеотидах рибозу вместо дезоксирибозы и азотистое основание урацил (U) вместо тимина (T). Различают РНК матричную (мРНК), транспортную (тРНК) и рибосомную (рРНК). Синтез полимеров рРНК, мРНК и тРНК на матрице ДНК катализируют соответственно РНК-полимераза I, II и III.
• Геном. Различают ядерный и митохондриальный геномы. Ядерный геном - полный комплект генов (примерно 50 тыс. на ядро диплоидной клетки, в гаплоидном наборе - около 24 тыс. генов) в хромосомах. Кариотип описывает количество и структуру хромосом. Гаплоидный набор - 23 хромосомы (3,5x109 пар нуклеотидов) - характерен для гамет (зрелых половых клеток), а диплоидный набор - стандарт хромосом (23x2) - для соматических клеток. Ядерный геном содержит гены, кодирующие полипептиды (примерно 2% генома), РНК (около 20% генома) и повторяющиеся последовательности (более 50% генома) неясного назначения.
• Ядрышко - компактная структура в ядре интерфазных клеток. Основные функции ядрышка - синтез рРНК (транскрипция и процессинг рРНК) и образование СЕ рибосом. Транскрипция рРНК происходит в хромосомах 13, 14, 15, 21 и 22.
• Нуклеоплазма содержит рибонуклеопротеины, ядерные рецепторы, ферменты (в том числе АТФазы, ГТФазы, ДНК- и РНКполимеразы) и множество других молекул (онкогенов, факторов транскрипции, белков теплового шока, вирусных ДНК, влияющих на транскрипцию и процессинг РНК).
Рибосомы. Рибосома состоит из большой и малой СЕ, содержащих различные типы рРНК и белки. Функция рибосом - трансляция (считывание кода мРНК и сборка полипептидов).
Гранулярная эндоплазматическая сеть (шероховатый эндоплазматический ретикулум) - система плоских мембранных цистерн с находящимися на их наружной поверхности рибосомами. Рибосомы связываются с мембранами сети при помощи рибофоринов. В шероховатой эндоплазматической сети происходит синтез белков для плазматической мембраны, лизосом, пероксисом, а также синтез белков на экспорт, т.е. предназначенных для экзоцитоза.
Гладкая эндоплазматическая сеть - система анастомозирующих мембранных каналов, пузырьков и трубочек - не содержит рибофоринов и по этой причине не связана с рибосомами. Функции гладкой эндоплазматической сети многообразны: синтез стероидных гормонов, детоксикация (например, фенобарбитала при помощи оксидаз в гепатоцитах), депонирование ионов кальция.
Митохондрии чаще имеют форму цилиндра диаметром 0,2-1 мкм и длиной до 7 мкм (в среднем около 2 мкм). У митохондрий две мембраны - наружная и внутренняя; последняя образует кристы. Между наружной и внутренней мембранами находится межмембранное пространство. Внемембранный объём митохондрии - матрикс. Митохондрии выполняют в клетке множество функций: окисление в цикле Кребса, транспорт электронов, хемиосмотическое
сопряжение, фосфорилирование АДФ, сопряжение окисления и фосфорилирования, функцию контроля внутриклеточной концентрации кальция, синтез белков, образование тепла.
Комплекс Гольджи образован стопкой из 3-10 уплощённых и слегка изогнутых цистерн с расширенными концами. Цистерны комплекса Гольджи образуют три основных компартмента: цис-сторона, транс-сторона, промежуточный компартмент. Функции комплекса Гольджи: модификация секреторного продукта, сортировка белков, концентрирование и упаковка секреторных продуктов.
Лизосомы - окружённые мембраной округлые пузырьки - образуются из эндосом путём включения в них лизосомных гидролаз и лизосомных мембранных белков после их синтеза в гранулярной эндоплазматической сети и процессинга в комплексе Гольджи. Известно более 50 лизосомных ферментов: рибонуклеазы, дезоксирибонуклеазы, катепсины, сульфатазы, β-глюкуронидазы, фосфолипазы, гликозидазы, липазы и другие. Лизосомные ферменты наиболее активны в кислой среде (pH-5,0), для поддержания которой в мембрану лизосомы встроен протонный насос (Н+,К+-АТФаза). Лизосомы участвуют во внутриклеточном пищеварении - в переваривании материала внутриклеточных компонентов (аутофагия) или частиц, различными путями попавших в клетку (гетерофагия). При нарушении функции лизосом развиваются т.н. лизосомные болезни накопления.
Пероксисомы - мембранные пузырьки размером 0,1-1,5 мкм с электроноплотной сердцевиной. Они особенно многочисленны в клетках печени и почки. В составе мембраны органеллы находятся специфичные для пероксисом белки - пероксины, а в матриксе - матричные белки, в т.ч. более 40 ферментов (например, каталаза и пероксидаза), катализирующие анаболические (биосинтез жёлчных кислот) и катаболические (β-окисление длинных цепей жирных кислот, Н2О2-зависимое дыхание, деградация ксенобиотиков) процессы. Все компоненты пероксисом поступают из цитозоля. Продолжительность жизни пероксисом - 5-6 сут. Новые органеллы возникают из предсуществующих путём их деления. Пероксисомы увеличиваются в размерах по мере поступления в них белков из цитозоля, и от них отделяются новые пероксисомы.
Цитозоль. Жидкая часть цитоплазмы (цитозоль) составляет около половины объёма клетки. Помимо воды, в цитозоле присутствуют ионы, множество химических соединений разной природы, макромолекулы. К макромолекулярным комплексам относятся апоптосомы - активаторы каспаз при регулируемой гибели клеток, а также протеосомы - комплексы нелизосомных протеаз, осуществляющие вместе с убиквитинами деградацию короткоживущих белков.
Включения. К разнородной группе включений относят находящиеся в цитозоле единичные или группы гранул и капель: гликогена, липидов, пигментов, липофусцина. Так, липиды содержатся в цитоплазме как капли самых различных размеров и плотности, они не связаны с клеточными мембранами, содержат триглицериды как источник энергии и холестерол, используемый для синтеза стероидов. В каком-то смысле включением, фактически занимающим весь объём эритроцита, можно назвать гемоглобин.
Цитоскелет
Трёхмерная цитоплазматическая сеть волокнистых и трубчатых структур различного типа формирует цитоскелет. К элементам цитоскелета относят микротрубочки, промежуточные филаменты, микрофиламенты (тонкие, или актиновые нити, а также толстые, или миозиновые нити). Цитоскелет придаёт клетке определённую форму и выполняет множество других функций (например, подвижность клетки, внутриклеточный транспорт).
Микротрубочки
Микротрубочки состоят из 13 тубулиновых протофиламентов (нитей), идущих по спирали; нити имеют диаметр 24 нм и длину несколько микрометров. Каждая нить собрана из субъединиц (СЕ) - чередующихся димеров α- и β-тубулина. Микротрубочки участвуют в поддержании формы клетки, в транспорте макромолекул и органелл, обеспечивают расхождения хромосом при делении клеток, подвижность жгутиков и ресничек, движение сперматозоидов (см. ниже раздел «Молекулярные моторы»). Для микротрубочек характерна полярность, т.е. микротрубочки - динамичные структуры, постоянно растущие с одного конца (полимеризация) и деполимеризующиеся с другого конца. Микротрубочки входят в состав базального тельца, центриоли и аксонемы.
• Органеллы, содержащие микротрубочки: базальное тельце, центриоли, аксонема.
❖ Базальное тельце (рис. 3-3,I) состоит из 9 триплетов микротрубочек, расположенных в основании реснички или жгутика; служит матрицей при организации аксонемы.
❖ Центриоли имеют цилиндрическую форму, диаметр 150 нм и длину до 500 нм; их стенка состоит из 9 триплетов микротрубочек. Центриоль - центр организации митотического веретена - участвует в делении клетки.
❖ Аксонема (рис. 3-3,I) состоит из 9 периферических пар микротрубочек и двух расположенных центрально одиночных мик-
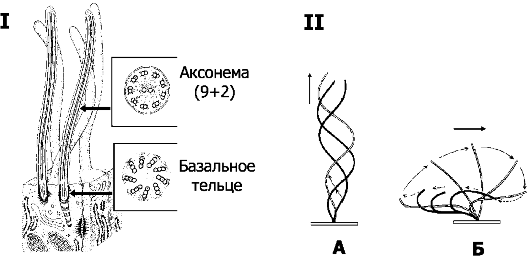 Рис. 3-3. I. Ресничка - тонкий вырост на поверхности клетки [11].
Стержень реснички образован аксонемой - системой микротрубочек 9+2. В
основании реснички расположено базальное тельце, служащее матрицей для
формирования аксонемы. II. Характер движения жгутика (А) и реснички (Б). Несмотря
на то, что молекулярная основа подвижности у жгутиков и ресничек
одинакова, характер их движения различен. Жгутики обычно длиннее
ресничек, и для них характерно синусоидальное движение, в отличие от
циклических волнообразных изгибов ресничек
Рис. 3-3. I. Ресничка - тонкий вырост на поверхности клетки [11].
Стержень реснички образован аксонемой - системой микротрубочек 9+2. В
основании реснички расположено базальное тельце, служащее матрицей для
формирования аксонемы. II. Характер движения жгутика (А) и реснички (Б). Несмотря
на то, что молекулярная основа подвижности у жгутиков и ресничек
одинакова, характер их движения различен. Жгутики обычно длиннее
ресничек, и для них характерно синусоидальное движение, в отличие от
циклических волнообразных изгибов ресничек
ротрубочек. В состав ручек периферических пар входит белок динеин, содержащий 2-3 глобулярные головки, соединённые с гибкой фибриллярной частью молекулы. Аксонема - основной структурный элемент реснички и жгутика.
• Ресничка - вырост клетки длиной 5-10 мкм и шириной 0,2 мкм, содержащий аксонему (рис. 3-3,1). Реснички присутствуют в эпителиальных клетках воздухопроводящих и половых путей, перемещают слизь с инородными частицами и остатками отмерших клеток и создают ток жидкости около клеточной поверхности.
• Жгутик в сперматозоиде имеет длину 50-55 мкм и толщину 0,2- 0,5 мкм и содержит аксонему.
Промежуточные нити (филаменты) состоят из белков, специфичных для определённых клеточных типов; имеют диаметр 8-11 нм. Различают цитокератины эпителия, десмины мышц, виментины мезенхимы, ламины ядерной оболочки, а также нейрофиламенты, глиофиламенты и чётковидные волокна хрусталика. Промежуточные нити создают внутриклеточный каркас, обеспечивают упругость клетки, поддерживают упорядоченность расположения компонентов цитоплазмы. Иммуноцитохимические реакции с АТ конкретных типов промежуточных нитей нашли применение в цитодиагностике генеза опухолей.
Микрофиламенты
Две переплетённые нити фибриллярного актина (F-актин, см. рис. 3-4А), составленные из глобулярного актина (G-актин), формируют микрофиламенты (тонкие нити) диаметром 6 нм. Актиновые микрофиламенты образуют скопления по периферии клетки и связаны с плазмолеммой посредством ряда белков. Тонкие нити могут взаимодействовать с миозином толстых нитей, образуя актомиозиновый хемомеханический преобразователь (см. ниже раздел «Молекулярные моторы»).
• Полярность микрофиламентов. Как и микротрубочки, микрофиламенты полярны; присоединение (полимеризация) СЕ G-актина происходит на (+)-конце. Известны токсины, связывающиеся с актином и блокирующие его полимеризацию, нарушая тем самым подвижность клеток, фагоцитоз и цитокинез. К таким токсинам относятся цитохалазины и фаллоидин.
• Функции микрофиламентов
❖ Изменение консистенции цитозоля, переход золя в гель и обратно (например, для изменения вязкости примембранной цитоплазмы при образовании псевдоподии).
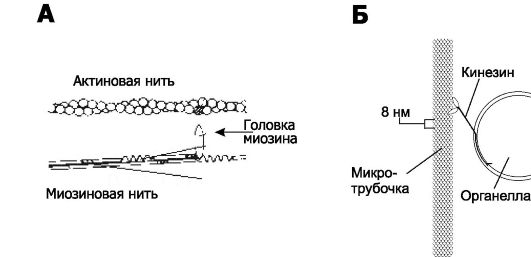 Рис. 3-4. Хемомеханические преобразователи [11]. А. В
актомиозиновом молекулярном моторе происходит расщепление АТФ при
взаимодействии актина тонких нитей (тонкие филаменты) с головкой
миозина, отходящей от миозиновой (толстой) нити. Освобождённая энергия
используется для взаимного перемещения относительно друг друга актиновых
и миозиновых нитей. Б. Кинезин обеспечивает транспорт органелл
из одной части клетки в другую вдоль микротрубочек. Шаг перемещения
кинезина по поверхности микротрубочки составляет 8 нм
Рис. 3-4. Хемомеханические преобразователи [11]. А. В
актомиозиновом молекулярном моторе происходит расщепление АТФ при
взаимодействии актина тонких нитей (тонкие филаменты) с головкой
миозина, отходящей от миозиновой (толстой) нити. Освобождённая энергия
используется для взаимного перемещения относительно друг друга актиновых
и миозиновых нитей. Б. Кинезин обеспечивает транспорт органелл
из одной части клетки в другую вдоль микротрубочек. Шаг перемещения
кинезина по поверхности микротрубочки составляет 8 нм
❖ Подвижность немышечных клеток (например, нейтрофилов и макрофагов) связана с изменением формы клеточной поверхности вследствие регулируемой полимеризации актина.
❖ Стабилизация локальных выпячиваний плазматической мембраны
связана с пучками поперечно сшитых актиновых филаментов (например, в микроворсинках эпителиальных клеток кишки, где пучок параллельных микрофиламентов образует их сердцевину).
Молекулярные моторы
Многие внутриклеточные процессы связаны с перемещением различных объектов (например, органелл, макромолекул). Реализацию таких процессов осуществляют так называемые молекулярные моторы, или хемомеханические преобразователи. При работе молекулярных моторов энергия, накопленная в макроэргических связях АТФ или ГТФ, расходуется для выполнения механической работы. В хемомеханических преобразователях, использующих энергию расщепления АТФ, происходит взаимодействие, как минимум, 2 белков; один из таких белков - АТФаза. К таким АТФазам относятся миозин, динеин и кинезин. Входящий в состав клатриновых пузырьков динамин расщепляет ГТФ.
• Актомиозиновый хемомеханический преобразователь расщепляет АТФ при взаимодействии актина и миозина (рис. 3-4А). Актомиозиновый мотор осуществляет мышечное сокращение, а также различные перемещения в немышечных клетках.
• Тубулин-кинезиновый молекулярный мотор. Кинезины и тубулины микротрубочек образуют молекулярный мотор (рис. 3-4Б), который обеспечивает внутриклеточный транспорт органелл и перемещение хромосом вдоль микротрубочек в ходе клеточного деления. Перемещение органелл вдоль микротрубочек с участием кинезинов осуществляется в направлении (+)-конца микротрубочек с шагом 3 нм при развиваемой силе 0,15 пН.
• Тубулин-динеиновый мотор входит в состав аксонемы ресничек, жгутиков и других органоидов (см. рис. 3-3) и функционирует за счёт расщепления АТФ динеином. При расщеплении АТФ глобулярная головка динеина скользит по поверхности микротрубочки по направлению к её (-)-концу. Этот механизм аналогичен скольжению элементов актомиозинового хемомеханического преобразователя в мышце.
• Динамин. Присоединение к динамину ГТФ инициирует формирование механохимической молекулярной пружины из плотно упакованных колец динамина с шагом в 11 нм вокруг шейки эндоцитозного пузырька (см. рис. 2-11). При гидролизе ГТФ расстояние между смежными кольцами увеличивается до 22 нм. Таким обра-
зом, ГТФаза динамина катализирует расщепление ГТФ и тем самым растяжение пружины с последующим отрывом окружённого клатрином эндоцитозного пузырька от плазмолеммы.
Депо кальция
Цистерны гладкой эндоплазматической сети многих клеток специализированы для накопления в них Ca2+ путём постоянного откачивания Ca2+ из цитозоля, где нормально содержание Ca2+ находится на уровне 10-7 М. Подобные депо кальция функционируют в любой клетке (гладкая эндоплазматическая сеть). Особенно велика роль кальциевых депо в скелетной и сердечной мышцах, нейронах, хромаффинных клетках, яйцеклетке, эндокринных клетках и т.д. Различные сигналы (например, гормоны, нейромедиаторы, факторы роста) влияют на функции клеток и их пролиферацию путём изменения концентрации в цитозоле внутриклеточного посредника - Ca2+. Например, условием сокращения мышечных элементов является резкое повышение концентрации Ca2+ в цитозоле. Для этого необходимо постоянно откачивать ионы кальция из цитозоля и накапливать их в специальных депо, образованных Ca2+-запасающими цистернами гладкой эндоплазматической сети (в мышечных элементах их называют саркоплазматический ретикулум - СР). Внутри цистерн находятся Са2+-связывающие белки (кальсеквестрин, кальретикулин и др.) В мембрану цистерн-депо Ca2+ встроены Са2+-насосы (Ca^-АТФаза), постоянно закачивающие Ca2+ внутрь цистерн, и Са2+-каналы, через которые происходит выброс Ca2+ из депо при поступлении сигнала (см. подробнее в главе 7 и на рис. 7-4).
Клеточный цикл
Клеточный цикл (рис. 3-5) состоит из митоза (М-фаза) и интерфазы. В интерфазе последовательно различают фазы G1, S и G2.
Пролиферация клеток, происходящая путём митоза, жёстко регулируется множеством молекулярных сигналов. Регуляторы клеточного цикла и митоза подразделяют на внутриклеточные и межклеточные.
• Внутриклеточные молекулярные сигналы многочисленны, среди них в первую очередь следует назвать собственно регуляторы клеточного цикла (циклины, циклин-зависимые протеинкиназы, их активаторы и ингибиторы) и онкосупрессоры.
• Межклеточные сигналы. Регуляция клеточного цикла и пролиферация (или блок пролиферации) клеток регулируются внеклеточными сигналами в виде гормонов (например, гормон роста, эстрогены, ФСГ), цитокинов (например, интерлейкины и интерфероны), факторов роста (например, фактор роста эпидерми-
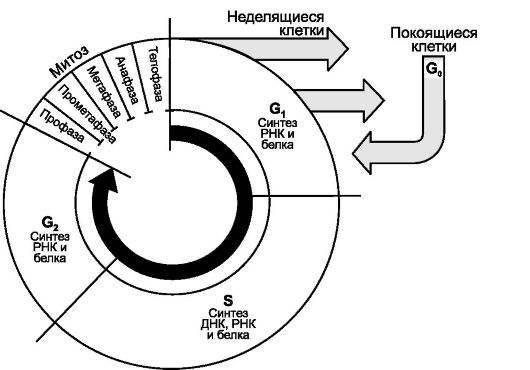 Рис. 3-5. Стадии клеточного цикла [11].
В клеточном цикле различают митоз - сравнительно короткую фазу M и
более длительный период - интерфазу. Фаза M состоит из профазы,
прометафазы, метафазы, анафазы и телофазы; интерфаза складывается из фаз
G1, S и G2. Клетки, выходящие из цикла, более не делятся и обычно специализируются. Клетки в фазе G0 обычно не возвращаются в цикл
Рис. 3-5. Стадии клеточного цикла [11].
В клеточном цикле различают митоз - сравнительно короткую фазу M и
более длительный период - интерфазу. Фаза M состоит из профазы,
прометафазы, метафазы, анафазы и телофазы; интерфаза складывается из фаз
G1, S и G2. Клетки, выходящие из цикла, более не делятся и обычно специализируются. Клетки в фазе G0 обычно не возвращаются в цикл
са). Некоторые из таких молекулярных сигналов расцениваются как стимулирующие митогенную активность факторы (митогены). Существенное влияние на пролиферативную активность клеток имеют и контакты с элементами межклеточного матрикса (например, с ламинином и фибронектином). После взаимодействия с соответствующими рецепторами такие митогенные сигналы (в значительном числе случаев при помощи связанных с G-белками протеинкиназ) передаются на соответствующие участки генома, активируя транскрипцию контролирующих фазы клеточного цикла генов (например, циклин-зависимых протеинкиназ). Взаимодействие лигандов с рецепторами и дальнейший внутриклеточный перенос информационного сигнала рассмотрены в главе 4 («Межклеточные взаимодействия»).
Экспрессия генов
Экспрессия генов происходит в несколько этапов: транскрипция - процессинг - трансляция - посттрансляционная модифи-
кация. На каждом из этих этапов на макромолекулы в виде гена, первичного транскрипта, мРНК, полипептида и белка воздействуют различные регуляторные факторы.
Транскрипция - первый этап реализации генетической информации - приводит к появлению на матрице ДНК первичного транскрипта (РНК), состоящего из линейной последовательности транскрибированных интронов и экзонов. ДНК служит только матрицей для синтеза РНК и в ходе транскрипции не изменяется. В основе механизма транскрипции (полимеразная реакция, катализируемая РНК-полимераза- ми) находится принцип комплементарного спаривания оснований. Синтез РНК начинается в определённых последовательностях (сайтах) ДНК - промоторах и завершается в сайтах терминации.
Процессинг. Первичные транскрипты подвергаются ряду ковалентных модификаций (модификации концов пре-мРНК и сплайсинг), в результате осуществления которых формируется способная к трансляции зрелая мРНК.
Трансляция. Для синтеза полипептидной цепи необходимы следующие основные компоненты: аминокислоты, тРНК (около 50 разных тРНК), мРНК, рибосомы, источники энергии (АТФ и ГТФ), белковые факторы инициации, элонгации и терминации трансляции.
Посттрансляционные изменения. Полипептидные цепи могут подвергаться структурным модификациям в виде удаления части цепи (частичный протеолиз), присоединения одного или нескольких низкомолекулярных лигандов (ковалентные модификации), приобретения белком естественной для него (нативной) конформации (фолдинг полипептида, формирование белка из отдельных полипептидов - СЕ белка).
Ингибиторы матричного биосинтеза
Большая группа веществ ингибирует матричный синтез ДНК (репликацию), РНК (транскрипцию), полипептида (трансляцию). К таким веществам относятся антибиотики, токсины, интерфероны, а также вирусы
• Антибиотики применяют в качестве противоопухолевых (курсы хемотерапии) и антибактериальных ЛС.
• Вирусы. Генетический материал вирусов - ДНК или РНК. После заражения клеток синтез вирусных ДНК, РНК и белков происходит за счёт ферментов, субстратов и источников энергии клет- ки-хозяина, но прекращаются собственные синтезы.
• Токсины (α-аманитин, рицин, бактериальные).
• Интерфероны секретируются некоторыми клетками в ответ на заражение вирусами и препятствуют распространению вирусной
инфекции путём стимулирования синтеза ферментов, способных разрушать мРНК вирусов и прекращения синтеза белков на рибосомах инфицированных вирусов, препятствуя тем самым экспрессии вирусных генов в заражённых клетках.
Регуляция экспрессии генов
• In vivo не более 1% ядерных генов доступно для транскрипции. Все потенциально доступные для экспрессии гены (следовательно, синтезируемые полипептиды) подразделяют на конститутивные (транскрибируются постоянно и во всех клетках, например гены ферментов гликолиза, разных РНК, альбумина и некоторых других белков) и клеточноспецифические (например, гены α- и β-цепей глобина транскрибируются в эритроидных клет- ках-предшественницах). Эти последние, а также некоторые другие гены подвергаются адаптивной регуляции и являются объектами индуцибельных воздействий (положительного контроля) или репрессии (негативного контроля). Другими словами, транскрибируемые гены и экспрессируемые полипептиды подразделяют на конститутивные, индуцируемые и репрессируемые. Все остальные структурные гены in vivo репрессированы необратимо.
❖ Конститутивные синтезы происходят в любой клетке всегда и в относительно постоянных количествах, вне зависимости от влияний на клетку.
❖ Регулируемые синтезы (индуцируемые и репрессируемые) контролируются влияниями на клетку и её ядерный геном.
• In vitro в принципе может транскрибироваться весь геном, что доказано клонированием организмов из соматических клеток.
• Регуляция экспрессии конкретных генов в конкретных клетках определяется множеством внутриклеточных и межклеточных факторов, оперирующих на уровне межклеточных взаимодействий, отдельных клеток, их хромосом и генов, а также на разных этапах экспрессии гена.
Генетическая изменчивость
Отдельные гены, хромосомы и геном в целом (как под влиянием внешних факторов, так и в результате сбоев различных механизмов) постоянно претерпевает разнообразные изменения. Хотя существуют механизмы репарации (восстановления) ДНК, часть повреждений или ошибок сохраняется. Изменения в последовательности и числе нуклеотидов в ДНК, не исправленные ферментами репарации, - «мутации». Различают мутации в соматических клетках (фенотипически проявляются только в мутировавшей клетке или её потомстве) и мута-
ции в половых клетках. Только последние потенциально могут быть переданы по наследству и могут проявляться в фенотипе потомства, в том числе и в виде наследственных заболеваний.
• Мутагены. Причинами мутаций могут быть различные факторы. Мутагены (равно и вызываемые ими мутации) классифицируют по происхождению (источнику) на эндогенные и экзогенные, а по природе на физические, химические и биологические.
• Частота мутаций. Средняя частота возникновения мутаций в структурных локусах оценена в пределах от 10-5 до 10-6 на одну гамету за каждое поколение. Весь геном содержит 3х109 пар оснований. Другими словами, каждое последующее поколение приобретает несколько десятков мутаций. В широко известном научному и медицинскому сообществу и ежедневно пополняемом Каталоге наследственных заболеваний человека (OMIM, Online Mendelian Inheritance in Man <http://www.ncbi.nlm.nih.gov/Omim/>) по состоянию на август 2004 г. перечислено не менее (и только!) 4600 моногенных болезней, вызываемых мутациями конкретного гена. Для значительного числа поражённых генов идентифицированы разные аллели, количество которых для некоторых моногенных болезней достигает десятков и сотен.
• Типы генных мутаций
❖ По характеру изменений в составе гена различают делеции, дупликации, инверсии, вставки, транзиции, миссенс- и нонсенс-мутации.
❖ По последствиям генных мутаций их классифицируют на нейтральные, регуляторные и динамические, а также на миссенс- и нонсенс-мутации.
• Хромосомные мутации (аберрации) характеризуются изменением структуры отдельных хромосом. При них последовательность нуклеотидов в генах обычно не меняется, но изменение числа или положения генов при аберрациях может привести к генетическому дисбалансу, что пагубно сказывается на нормальном развитии организма. Различают внутрихромосомные, межхромосомные и изохромосомные аберрации.
• Изменения генома. Геномные мутации характеризуются изменением числа хромосом. У человека известны полиплоидия (в том числе тетраплоидия и триплоидия) и анеуплоидия.
• Типы наследования. Для любого моногенного заболевания существенной характеристикой является тип наследования: аутосом- но-доминантный, аутосомно-рецессивный, сцепленный с хромосомой X (доминантный и рецессивный), голандрический (сцепленный с хромосомой Y) и митохондриальный.