Общая химия : учебник / А. В. Жолнин ; под ред. В. А. Попкова, А. В. Жолнина. - 2012. - 400 с.: ил.
|
|
|
|
Глава 6. ПРОТОЛИТИЧЕСКИЕ БУФЕРНЫЕ СИСТЕМЫ
Изменение любого фактора, могущего влиять на состояние химического равновесия системы веществ, вызывает в ней реакцию, стремящуюся противодействовать производимому изменению.
А. Ле Шателье
6.1. БУФЕРНЫЕ СИСТЕМЫ. ОПРЕДЕЛЕНИЕ И ОБЩИЕ ПОЛОЖЕНИЯ ТЕОРИИ БУФЕРНЫХ СИСТЕМ. КЛАССИФИКАЦИЯ БУФЕРНЫХ СИСТЕМ
Системы, поддерживающие протолитический гомеостаз, включают в себя не только физиологические механизмы (легочная и почечная компенсация), но и физико-химическое буферное действие, ионный обмен, диффузию. Поддержание на заданном уровне кислотно-основного равновесия обеспечивается на молекулярном уровне действием буферных систем.
Протолитическими буферными системами называются растворы, сохраняющие постоянное значение pH как при добавлении кислот и щелочей, так и при разведении.
Способность некоторых растворов сохранять неизменной концентрацию ионов водорода получила название буферного действия, которое является основным механизмом протолитического гомеостаза. Буферные растворы - это смеси слабого основания или слабой кислоты и их соли. В буферных растворах главными «действующими» компонентами являются донор и акцептор протонов, согласно теории Брёнстеда, или донор и акцептор электронной пары, согласно теории Льюиса, представляющие собой кислотно-основную пару.
По принадлежности слабого электролита буферной системы к классу кислот или оснований и по типу заряженной частицы они делятся на три типа: кислотный, основной и амфолитный. Раствор, содержащий одну или несколько буферных систем, называется буферным раствором. Буферные растворы можно приготовить двумя способами:
• частичной нейтрализацией слабого электролита сильным электролитом:
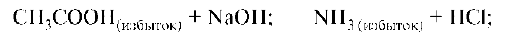
• смешиванием растворов слабых электролитов с их солями (или двух солей): CH3COOH и CH3COONa; NH3 и NH4Cl; NaH2PO4
и Na2HPO4.
Причина возникновения в растворах нового качества - буферного действия - заключается в совмещении нескольких протолитических равновесий:
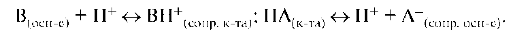
Сопряженные кислотно-основные пары B/BH+ и A-/HA называют буферными системами.
В соответствии с принципом Ле Шателье добавление в раствор слабой кислоты HB + H2O ↔ H3O+ + B- сильной кислоты или соли, содержащей анионы B-, происходит процесс ионизации, смещающий равновесие влево (эффект общего иона) B- + H2O ↔ HB + OH-, а добавление щелочи (OH-) - вправо, так как вследствие реакции нейтрализации уменьшится концентрация ионов гидроксония.
При совмещении двух изолированных равновесий (ионизации кислоты и гидролиза по аниону) оказывается, что процессы, которые в них будут протекать при воздействии одних и тех же внешних факторов (добавлении ионов гидроксония и гидроксид-ионов), разнонаправле-ны. Кроме того, концентрация одного из продуктов каждой из совмещенных реакций влияет на положение равновесия другой реакции.
Протолитическая буферная система представляет собой совмещенное равновесие процессов ионизации и гидролиза.
Уравнение буферной системы выражает зависимость pH буферного раствора от состава буферной системы:
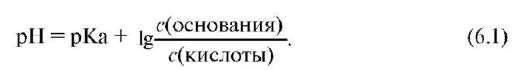
Анализ уравнения показывает, что величина pH буферного раствора зависит от природы веществ, образующих буферную систему, соотношения концентрации компонентов и температуры (так как от нее зависит величина pKa).
Согласно протолитической теории, кислоты, основания и амфоли-ты являются протолитами.
6.2. ТИПЫ БУФЕРНЫХ СИСТЕМ
Буферные системы кислотного типа
Кислотные буферные системы представляют собой смесь слабой кислоты HB (донор протона) и ее соли B- (акцептор протона). Они, как правило, имеют кислую среду (pH <7).
Гидрокарбонатная буферная система (зона буферного действия pH 5,4-7,4) - смесь слабой угольной кислоты H2CO3 (донор протона) и ее соли HCO3- (акцептор протона).
Гидрофосфатная буферная система (зона буферного действия pH 6,2-8,2) - смесь слабой кислоты H2PO4- (донор протона) и ее соли HPO42- (акцептор протона).
Гемоглобиновая буферная система представлена двумя слабыми кислотами (доноры протонов) - гемоглобином HHb и оксигемоглоби-ном HHbO2 и сопряженными им слабыми основаниями (акцепторами протонов) - соответственно гемоглобинат - Hb- и оксигемоглобинат-анионами HbO2-.
Буферные системы основного типа
Основные буферные системы представляют собой смесь слабого основания (акцептор протона) и его соли (донор протона). Они, как правило, имеют щелочную среду (pH >7).
Аммиачная буферная система: смесь слабого основания NH3•H2O (акцептор протона) и его соли - сильного электролита NH4+ (донор протона). Зона буферного действия при pH 8,2-10,2.
Буферные системы амфолитного типа
Амфолитные буферные системы состоят из смеси двух солей или из соли слабой кислоты и слабого основания, например CH3COONH4, в котором CH3COO- проявляет слабые основные свойства - акцептор протона, а NH4+ - слабая кислота - донор протона. Биологически значимой буферной системой амфолитного типа является белковая буферная система - (NH3+)m-Prot-(CH3COO-)n.
Буферные системы можно рассматривать как смесь слабого и силъ-ного электролитов, имеющих одноименные ионы (эффект общего иона). Например, в ацетатном буферном растворе - ацетат-ионы, а в гидрокарбонатном - карбонат-ионы.
6.3. МЕХАНИЗМ ДЕЙСТВИЯ БУФЕРНЫХ РАСТВОРОВ И ОПРЕДЕЛЕНИЕ PH В ЭТИХ РАСТВОРАХ. УРАВНЕНИЕ ГЕНДЕРСОНА-ХАССЕЛЬБАХА
Механизм действия буферных растворов кислотного типа рассмотрим на примере ацетатной буферной системы CH3COO-/CH3COOH, в основе действия которой лежит кислотно-основное равновесие CH3COOH ↔ H+ + CH3COO- (KИ = 1,75•10-5). Главный источник ацетат-ионов - сильный электролит CH3COONa. При добавлении сильной кислоты сопряженное основание CH3COO- связывает добавленные катионы водорода, превращаясь в слабую кислоту: CH3COO- + + H+ ↔ CH3COOH (кислотно-основное равновесие смещается влево). Уменьшение концентрации CH3COO- уравновешивается повышением концентрации слабой кислоты и указывает на процесс гидролиза. Согласно закону разведения Оствальда, увеличение концентрации кислоты несколько понижает ее степень электролитической диссоциации и кислота практически не ионизирует. Следовательно, в системе: Ск увеличивается, Сс и α уменьшается, [H+] - const, Ск/Сс увеличивается, где Cк - концентрация кислоты, Сс - концентрация соли, α - степень электролитической диссоциации.
При добавлении щелочи катионы водорода уксусной кислоты высвобождаются и нейтрализуются добавленными ионами OH-, связываясь в молекулы воды: CH3COOH + OH- → CH3COO- + H2O
(кислотно-основное равновесие смещается вправо). Следовательно, Ск увеличивается, Сс и α уменьшается, [H+] - const, Ск/Сс уменьшается.
Механизм действия буферных систем основного и амфолитного типов аналогичен. Буферное действие раствора обусловлено смещением кислотно-основного равновесия за счет связывания добавляемых Н+ и ОН- ионов компонентами буфера и образования малодиссоции-рующих веществ.
Механизм действия белкового буферного раствора при добавлении кислоты: (NH3+)m-Prot-(COO-)n + nH+ ↔ (NH3+)m-Prot-(COOH)n, при добавлении щелочи - (NH3+)m-Prot-(COO-)n + mOH- ↔ (NH2) m- Prot-(COO-)n + mH2O.
При больших концентрациях Н+ и ОН- (больше 0,1 моль/л) значительно изменяется соотношение компонентов буферной смеси - Ск/Сс увеличивается или уменьшается и pH может измениться. Подтверждением этого является уравнение Гендерсона-Хассельбаха, которое устанавливает зависимость [Н+], КИ, α и Ск/Сс. Уравнение
выводим на примере буферной системы кислотного типа - смеси уксусной кислоты и ее соли СН3СОONа. Концентрация ионов водорода в буферном растворе определяется константой ионизации уксусной кислоты:
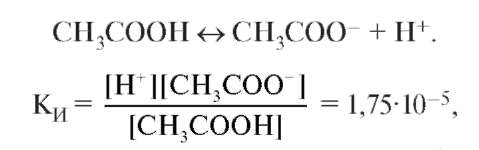
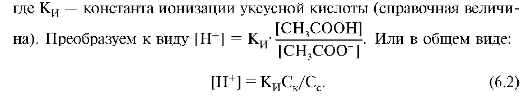
Уравнение показывает, что концентрация ионов водорода находится в прямой зависимости от КИ, α, концентрации кислоты Ск и в обратной зависимости от Сс и соотношения Ск/Сс. Логарифмируя обе части уравнения и взяв логарифм со знаком минус, получим уравнение в логарифмической форме:
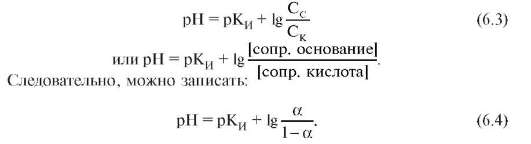
Уравнение Гендерсона-Хассельбаха для буферных систем основного и амфолитного типов выводится на примере вывода уравнения для буферных систем кислотного типа.
Для буферной системы основного типа, например аммиачной, концентрацию катионов водорода в растворе можно рассчитать, исходя из константы кислотно-основного равновесия сопряженной кислоты
NH4+:
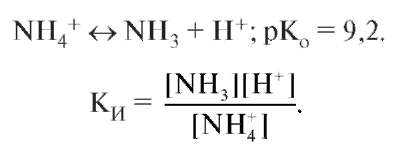
Уравнение Гендерсона-Хассельбаха для буферных систем основного типа:

Данное уравнение можно представить в виде:
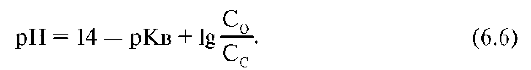
Для фосфатной буферной системы HPO42-/H2PO4- pH можно рассчитать по уравнению:
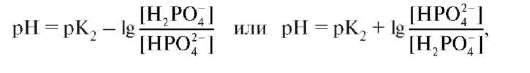
где pK2 - константа диссоциации ортофосфорной кислоты по второй ступени.
6.4. ЕМКОСТЬ БУФЕРНЫХ РАСТВОРОВ И ОПРЕДЕЛЯЮЩИЕ ЕЕ ФАКТОРЫ
Способность растворов поддерживать постоянное значение pH небезгранична. Буферные смеси можно различить по силе оказываемого ими сопротивления по отношению к действию кислот и оснований, вводимых в буферный раствор.
Количество кислоты или щелочи, которое нужно добавить к 1 л буферного раствора, чтобы значение его pH изменилось на единицу, называют буферной емкостью.
Таким образом, буферная емкость является количественной мерой буферного действия раствора. Буферный раствор имеет максимальную буферную емкость при pH = pK кислоты или основания, образующей смесь при соотношении ее компонентов, равном единице. Чем выше исходная концентрация буферной смеси, тем выше ее буферная емкость. Буферная емкость зависит от состава буферного раствора, концентрации и соотношения компонентов.
Нужно уметь правильно выбрать буферную систему. Выбор определяется необходимым интервалом pH. Зона буферного действия определяется силовым показателем кислоты (основания) ±1 ед.
При выборе буферной смеси необходимо учитывать химическую природу ее компонентов, так как вещества раствора, к которым добав-
ляется буферная система, могут образовывать нерастворимые соединения, взаимодействовать с компонентами буферной системы.
6.5. БУФЕРНЫЕ СИСТЕМЫ КРОВИ
Кровь содержит 4 основные буферные системы.
1. Гидрокарбонатная. На ее долю приходится 50% емкости. Она работает главным образом в плазме и играет центральную роль в транспорте СО2.
2. Белковая. На ее долю приходится 7% емкости.
3. Гемоглобиновая, на нее приходится 35% емкости. Она представлена гемоглобином и оксигемоглобином.
4. Гидрофосфатная буферная система - 5% емкости. Гидрокарбонатная и гемоглобиновая буферные системы выполняют
центральную и чрезвычайно важную роль в транспорте СО2 и установлении pH. В плазме крови pH 7,4. СО2 - продукт клеточного метаболизма, выделяющийся в кровь. Диффундирует через мембрану в эритроциты, где реагирует с водой с образованием Н2СО3. Соотношение устанавливается равным 7, и pH будет 7,25. Кислотность повышается, при этом имеют место реакции:
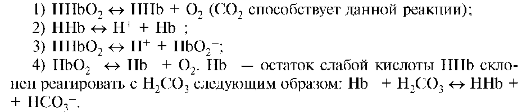
Образующийся НСО3- выходит через мембрану и уносится током крови. В плазме крови при этом pH 7,4. Когда венозная кровь вновь попадает в легкие, гемоглобин реагирует с кислородом с образованием оксигемоглобина, который является более сильной кислотой: ННb + + O2 ↔ НHbО2. pH понижается, так как образуется более сильная кислота, происходит реакция: НHbО2 + НСО3- ↔ HbO2- + Н2СO3. Затем СО2 выделяется в атмосферу. Таков один из механизмов транспорта СО2 и О2.
Гидратация и дегидратация СО2 катализируется ферментом карбо-ангидразой, которая имеется в эритроцитах.
Основания также связываются буферным раствором крови и выделяются с мочой, главным образом в виде одно- и двузамещенных фосфатов.
В клиниках всегда определяют резервную щелочность крови.
6.6. ВОПРОСЫ И УПРАЖНЕНИЯ ДЛЯ САМОПРОВЕРКИ ПОДГОТОВЛЕННОСТИ К ЗАНЯТИЯМ И ЭКЗАМЕНАМ
1. При совмещении каких протолитических равновесий растворы будут обладать буферными свойствами?
2. Дать понятие о буферных системах и буферном действии. Каков химизм буферного действия?
3. Основные типы буферных растворов. Механизм их буферного действия и уравнение Гендерсона-Хассельбаха, определяющее pH в буферных системах.
4. Основные буферные системы организма и их взаимосвязь. От чего зависит pH буферных систем?
5. Что называют буферной емкостью буферной системы? Какая из буферных систем крови обладает наибольшей емкостью?
6. Способы получения буферных растворов.
7. Выбор буферных растворов для медико-биологических исследований.
8. Определить, ацидоз или алкалоз наблюдается у больного, если концентрация ионов водорода в крови равна 1,2.10-7 моль/л?
6.7. ТЕСТОВЫЕ ЗАДАНИЯ
1. Какая из предложенных систем является буферной?
а) HCl и NaCl;
б) H2SO4 и NaHSO4;
в) H2CO3 и NaHCO3;
г) HNO3 и NaNO3;
д) HClO4 и NaClO4.
2. Для какой из предложенных буферных систем соответствует расчетная формула pH = рК?
а) 0,1 М р-р NaH2PO4 и 0,1 М р-р Na2HPO4;
б) 0,2 М р-р H2CO3 и 0,3 М р-р NaHCO3;
в) 0,4 М р-р NH4OH и 0,3 М р-р NH4Cl;
г) 0,5 М р-р СН3СООН и 0,8 М р-р CH3COONa;
д) 0,4 М р-р NaHCO3 и 0,2 М р-р Н2CO3.
3. Какая из предложенных буферных систем является бикарбонатной буферной системой?
а) NH4OH и NH4Cl;
б) Н2СО3 и КНСО3;
в) NaH2PO4 и Na2HPO4;
г) СН3СOOН и СН3СООК;
д) K2HPO4 и КН2РО4.
4. При каких условиях pH буферной системы равна рКк?
а) когда равны концентрация кислоты и ее соли;
б) когда не равны концентрация кислоты и ее соли;
в) когда соотношение объемов кислоты и ее соли равно 0,5;
г) когда соотношение объемов кислоты и ее соли при одинаковых концентрациях не равно;
д) когда концентрация кислоты больше концентрации соли в 2 раза.
5. Какая из предложенных формул подойдет для расчета [Н+], для системы СН3СООН и СН3СOOК?
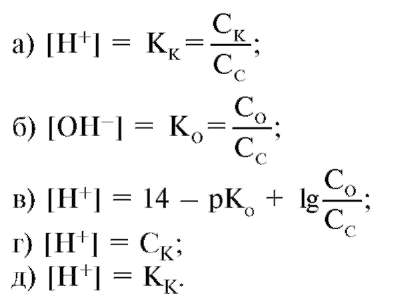
6. Какая из ниже перечисленных смесей входит в состав буферной системы организма?
а) HCl и NaCl;
б) H2S и NaHS;
в) NH4OH и NH4Cl;
г) H2CO3 и NaНСО3;
д) Ba(OH)2 и BaOHCl.
7. К какому типу кислотно-основных буферных систем относится белковый буфер?
а) слабая кислота и ее анион;
б) анионы кислой и средней соли;
в) анионы 2 кислых солей;
г) слабое основание и его катион;
д) ионы и молекулы амфолитов.
8. К какому типу кислотно-основных буферных систем относится аммиачный буфер?
а) слабая кислота и ее анион;
б) анионы кислой и средней соли;
в) анионы 2 кислых солей;
г) слабое основание и его катион;
д) ионы и молекулы амфолитов.
9. К какому типу кислотно-основных буферных систем относится фосфатный буфер?
а) слабая кислота и ее анион;
б) анионы кислой и средней соли;
в) анионы 2 кислых солей;
г) слабое основание и его катион;
д) ионы и молекулы амфолитов.
10. Когда белковая буферная система не является буфером?
а) в изоэлектрической точке;
б) при добавлении щелочи;
в) при добавлении кислоты;
г) в нейтральной среде.
11. Какая из предложенных формул подойдет для расчета [ОН-] системы: NH4OH и NH4Cl?