Биохимия: учебник для вузов/ под ред. Е.С.Северина - 5-е изд., - 2009. - 768 с.
|
|
|
|
РАЗДЕЛ 16 ОНКОГЕНЕЗ
Опухоли представляют собой группу генных болезней, характеризующихся неконтролируемой клеточной пролиферацией. По способности к распространению в организме их делят на 2 группы:
доброкачественные, или локальные, не обладающие способностью прорастать в соседние ткани;
злокачественные, способные к разрастанию (инвазии) в определённых тканях и перемещению в другие части тела, давая начало вторичным опухолям (метастазам). Описано более 100 различных видов рака, хотя 5 из них дают более 50% от всех диагностируемых случаев заболевания. Это - рак лёгкого, молочной железы, толстой и прямой кишки, простаты, матки и яичников (рис. 16-1).
Опухоли классифицируют также в зависимости от тканей и типов клеток, из которых они возникли:
карциномы - опухоли из клеток экто- и эн-
додермального происхождения; саркомы - из клеток мезодермального происхождения; гемобластозы (лейкозы и лимфомы) - из камбиальной клетки кроветворной и лимфатической ткани. После заболеваний ССС рак как причина смертности населения занимает второе место. У человека наиболее изученными причинами рака являются радиация, химические канцерогены и вирусы.
Исследования вирусов как возможной причины онкологических болезней привели к созданию онкогенной теории, которая позволила дать объяснение механизму, с помощью которого различные агенты вызывают превращение нормальной клетки в опухолевую.
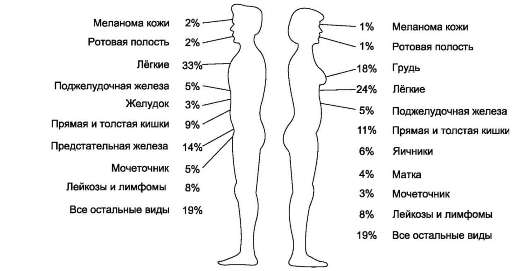
Рис. 16-1. Смертность от разных видов рака среди мужчин и женщин.
i. физические, химические и биологические агенты, вызывающие возникновение опухолей
Около 80% случаев рака у людей - результат воздействия факторов окружающей среды, под которыми понимают стиль жизни, пищевые продукты, заболевания, увеличивающие риск развития опухолей, и наследственные изменения в геноме.
Агенты, стимулирующие возникновение опухолей (канцерогены), можно разделить на три большие группы: излучения, химические соединения и вирусы.
А. ИЗЛУЧЕНИЯ
• Установлено, что УФО, х- и γ-лучи оказывают мутагенное и канцерогенное действие. Они повреждают ДНК несколькими способами. Под воздействием излучений из полинуклеотидных цепей могут удаляться азотистые основания и образовываться апуринизированные или апири-мидинизированные участки, могут появляться одно- и двухцепочечные разрывы или сшивки. УФО вызывает образование тиминовых димеров (см. раздел 4). Наряду с прямым воздействием х-и γ-излучения индуцируют образование в тканях свободных радикалов (О2 -, ОН-, ОН•, О2 и др.), воздействие которых на ДНК и другие макромолекулы повреждает генетический аппарат и нарушает матричные синтезы в клетке.
Так, в Австралии и Новой Зеландии, где высока интенсивность УФО солнечных лучей, у населения часто возникают карциномы и мелано-мы. Отмечено увеличение случаев заболевания лейкозами у жителей Японии после взрыва на их территории атомных бомб. Учащение случаев рака лёгких наблюдают у шахтёров, работающих с радиоактивными рудами.
Б. ХИМИЧЕСКИЙ КАНЦЕРОГЕНЕЗ
Канцерогенным действием обладает огромное количество различных по химическому строению веществ, основные группы которых представлены в табл. 16-1.
В печени большинство из этих веществ прокан-церогены - соединения, не взаимодействующие с генетическим аппаратом клеток, после дополнительной метаболической модификации превращаются в канцерогены, способные реагировать с молекулами нуклеиновых кислот и белков, нарушать работу регуляторных механизмов клеток и вызывать рост опухолей. Трансформация клеток под действием канцерогенов получила название химического канцерогенеза.
Установлено, что ферменты детоксикации, участвующие в метаболизме проканцерогенов, обнаруживают поразительный полиморфизм. Отдельные изоформы этих белков имеют низкую активность. У индивидуумов с такими вариантами ферментов проканцерогены медленнее подвергаются метаболическим превращениям и выводятся из организма, не успевая превратиться в активные канцерогены. С этим явлением связаны разная чувствительность людей к канцерогенам табачного дыма и предрасположенность курильщиков к раку лёгкого.
В покоящихся клетках ДНК двухспиральна, и азотистые основания защищены от воздействия повреждающих агентов. Однако в ходе репликации полинуклеотидные цепи очень чувствительны к канцерогенам, и клетки, получившие повреждения, могут иметь разную судьбу (рис.
16-2).
Полициклические ароматические углеводороды (ПАУ) входят в состав продуктов неполного сгорания каменного угля и нефти, продуктов пиролиза масел и веществ, найденных в жжёном мясе, а также образуются при курении табака. Они могут связываться с пуриновыми
Таблица 16-1. Основные химические канцерогены
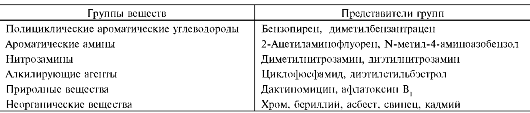
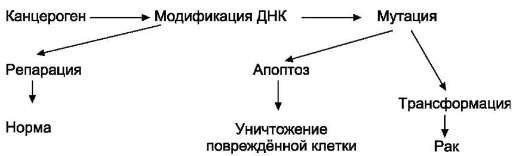
Рис. 16-2. Последствия повреждения ДНК клетки канцерогенами.
основаниями (особенно гуанином) только после ферментативной активации монооксигеназами (см. раздел 12), работающими при участии различных изоформ цитохрома Р450. Эти ферменты катализируют образование эпоксидов, которые превращаются в диолы с помощью эпоксидгид-
ролазы. Первичные или вторичные эпоксиды, обладая высокой реакционной способностью, могут взаимодействовать с нуклеофильными группами в молекуле ДНК (рис. 16-3).
ПАУ стали первыми соединениями, кан-церогенность которых была доказана экс-
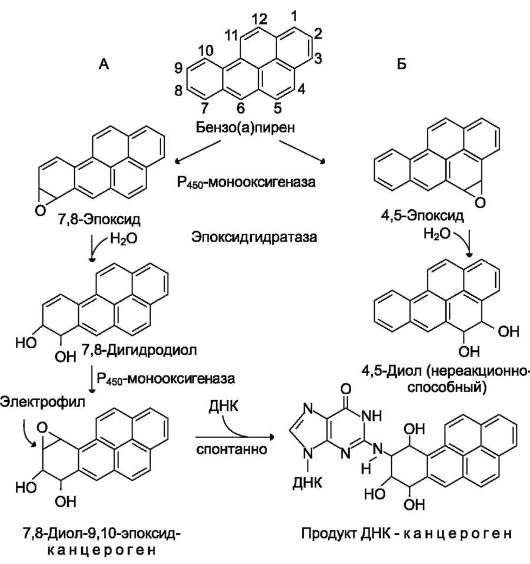
Рис. 16-3. Образование канцерогенов из ПАУ под действием ферментов детоксикации ксенобиотиков.
А и Б - два разных метаболических пути, по которым может превращаться бензо(а)пирен. Путь Б приводит к образованию нереакционноспособного продукта, а путь А превращает бензо(а)пирен в канцероген, способный связываться с остатками гуанина и аденина в молекуле ДНК.
периментально в
начале XX века, когда из каменноугольной смолы были выделены
бен-зантрацен, бензо(а)пирен, 7,12-диметилбен-зантрацен и другие
соединения, содержащие конденсированные ароматические кольца.
Наблюдения, связывающие контакты людей с определёнными веществами и
развитие рака, были описаны значительно раньше. Так, ещё в
Ароматические амины. К ароматическим аминам относят вещества, использующиеся в производстве анилиновых красителей и резиновой промышленности. Контакт с ними приводит к развитию у рабочих, занятых в указанных производствах, рака мочевого пузыря. Одним из представителей этой группы является 2-нафтиламин, химическая модификация которого происходит главным образом в печени (рис. 16-4).
Канцероген 2-амино-1-нафтол образуется в ходе гидроксилирования 2-нафтиламина. Однако в печени он быстро взаимодействует с ФАФС, превращаясь в нейтральный продукт, который выводится с мочой. В мочевом пузыре часть конъюгатов расщепляется гидролазами, присутствующими в незначительных количествах в моче. Вновь образуется 2-амино-1-нафтол - канцероген, который при повторяющихся контактах человека с нафтиламином вызывает развитие рака мочевого пузыря.
Нитрозамины появляются в организме в результате взаимодействия вторичных алифатических аминов с нитритами. Вторичные амины и нитриты являются постоянными компонентами пищи, поэтому нитрозамины синтезируются при запекании мяса, рыбы. Одно время нитриты широко применялись как консерванты мяса и рыбы, образуются они также в зелёных растениях.
Метаболизм нитрозаминов микросомальной системой окисления приводит к образованию иона метилдиазония, который способен метилировать ДНК клеток, индуцируя возникновение злокачественных опухолей лёгких, желудка, пищевода, печени и почек (рис. 16-5).
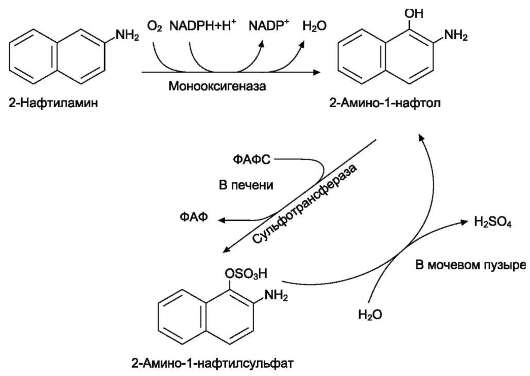
Рис. 16-4. Метаболизм 2-нафтиламина.
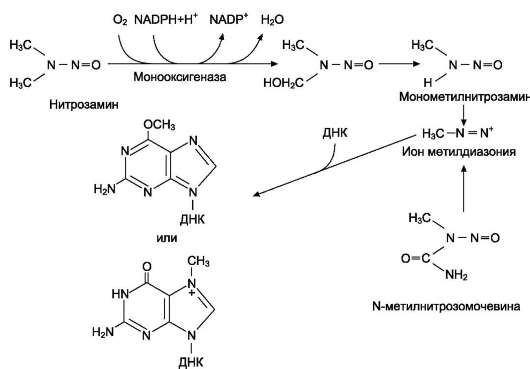
Рис. 16-5. Метилирование ДНК продуктами метаболизма нитрозаминов: диметилнитрозамина и N-метил-нитрозомочевины.
Основным продуктом взаимодействия нитрозаминов с ДНК клетки является N7-метилгу-анин-ДНК, но наибольшей канцерогенностью обладает минорный продукт этого взаимодействия - О6-метилированный гуанин-ДНК.
Алкилирующие и ацилирующие агенты, взаимодействуя с нуклеофильными амино- и гидрок-сильными группами ДНК, могут повреждать структуру генов и индуцировать образование опухолей. Такие соединения, как винилхло-рид, используемый в производстве пластмасс и упаковочных материалов, некоторые лекарства, применяемые в лечении опухолей или как им-муносупрессоры (циклофосфамид, бисульфан, диэтилстильбэстрол), можно рассматривать как факторы риска. Лекарственные препараты этой группы соединений способны вызывать вторичные опухоли у небольшого процента больных.
В. ДНК- И РНК-СОДЕРЖАЩИЕ ВИРУСЫ
Данные о роли вирусов в развитии опухолей были получены в начале XX столетия. Так, в
а в
ДНК-содержащие вирусы частично, а иногда полностью встраиваются в клеточный геном человека, экспрессируют вирусные гены, в результате чего образующиеся в ядре белки нарушают регуляцию клеточного цикла. К ДНК-содержащим онковирусам, помимо упомянутых выше, относят вирус герпеса, аденовирус, папова-вирус, вирус ветряной оспы. Как правило, эти вирусы вызывают инфекционные болезни и лишь в одном из миллиона случаев -
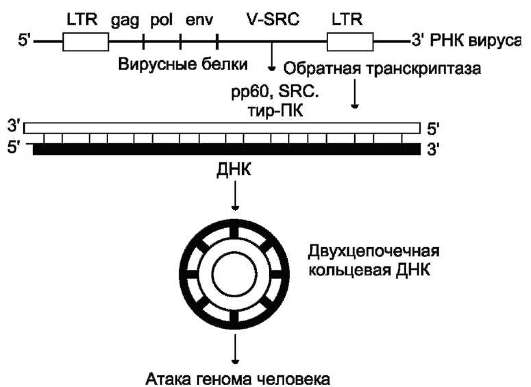
Рис. 16-6. Структура генома вируса саркомы Рауса. LTR - длинные концевые повторы (от англ. long terminal гереаts),содержащие промоторы, к которым присоединяется РНК-полимераза; gag,pol, env - гены, кодирующие вирусные белки; src - ген, кодирующий тирозиновую протеинкиназу (тир-ПК) с молекулярной массой 60 кД (рр60), которая вызывает нарушение контактного торможения (прекращения деления клеток при возникновении физического контакта между ними) и трансформацию клеток. Обратная транскриптаза - фермент, который синтезирует ДНК на матрице РНК. Благодаря активности этого фермента генетический материал вируса в клетках хозяина превращается в двухцепочечную кольцевую ДНК и может включаться в геном человека.
злокачественную трансформацию. С другой стороны, ДНК-содержащий вирус гепатита В является причиной рака печени, от которого в мире умирает ежегодно около 500 000 человек. При этом инфицирование пациентов происходит, как правило, за 20-25 лет до возникновения опухоли.
РНК-содержащие вирусы, попадая в клетки человека, синтезируют ДНК с помощью обратной транскриптазы и частично или полностью включают её в геном эукариотов в виде провируса (латентного вируса).
В
Г. НАСЛЕДСТВЕННАЯ ПРЕДРАСПОЛОЖЕННОСТЬ
Наследственные изменения в геноме играют важную роль в канцерогенезе. Так, у детей предрасположенность к ретинобластоме (злокачественная опухоль сетчатки глаза) наследуется как аутосомно-доминантный признак, и примерно 40% случаев заболевания имеют семейнsй характер. Также наследуется предрасположенность к множественному полипозу толстой кишки, и практически во всех случаях в зрелом возрасте у пациентов образуются аденокарциномы.
Нестабильность хромосомной ДНК может быть связана с дефектом ферментов репарации. Это нарушение встречается у пациентов с пигментной ксеродермой, которая часто сопровождается развитием карциномы кожи на участках, подверженных действию УФО.
ii. характеристика опухолевых клеток
Дифференцированные клетки соблюдают границы ткани и не вторгаются в сопредельные
территории, подчиняясь правилу контактного торможения. При трансформации это свойство утрачивается.
Клетки опухолей, как правило, имеют округлую или звёздчатую форму и крупнее, чем нормальные. В них изменено ядерно-цитоплаз-матическое соотношение, имеет место полиплоидия (состояние, при котором ядро содержит 3 и большее число гаплоидных наборов хромосом) или анэуплоидия, когда число хромосом изменяется и становится не кратным гаплоидному набору. Они могут расти, не прикрепляясь к поверхности из-за сниженной способности к адгезии, и образовывать мультислои.
А. ОСОБЕННОСТИ МЕТАБОЛИЗМА
В метаболизме опухолевых клеток обнаруживается ряд характерных особенностей, которые сообщают им существенные преимущества по сравнению с нормальными клетками. Так, в раковых клетках:
• возрастает активность рибонуклеотидредукта-зы и снижается катаболизм пиримидинов и пуринов, увеличивается синтез ДНК и РНК;
• повышается скорость гликолиза (как аэробного, так и анаэробного) и увеличивается продукция лактата. Характерная для многих опухолей повышенная секреция лак-тата получила название «эффект Варбурга». Преимущественный анаэробный гликолиз является, по-видимому, не внутренне присущим опухолевым клеткам свойством, а скорее следствием быстрого роста при слабой обеспеченности сетью кровеносных сосудов. Поскольку установлено, что чем менее дифференцирована опухоль и чем выше скорость её роста, тем интенсивнее протекает в ней анаэробный гликолиз и слабее окислительное фосфорилирование;
• в изоферментном спектре различных белков и ферментов возрастает содержание феталь-ных форм. Так, в углеводном обмене это фосфофруктокиназа, не ингибирующаяся АТФ и цитратом, изофермент гексокиназы, характеризующийся чрезвычайно высоким сродством к глюкозе, и очень активная лак-татдегидрогеназа.
Такие изменения обеспечивают раковую клетку чрезвычайно высоким сродством к глюкозе и способностью ассимилировать её даже при очень
низких концентрациях в крови. Аналогичные сдвиги в спектре изоферментов наблюдаются и в других обменах. Это позволяет опухолевым клеткам успешно конкурировать с окружающими тканями за жизненно важные метаболиты.
Б. ПОЯВЛЕНИЕ ЭМБРИОНАЛЬНЫХ БЕЛКОВ И ФЕРМЕНТОВ
Клетки синтезируют, а иногда и секретируют в кровь эмбриональные белки и антигены, такие как α-фетопротеин, карциноэмбриональный антиген и многие другие. В них появляется характерный для эмбриональных тканей высокоактивный фермент теломераза. Как уже указывалось ранее (см. раздел 4), у животных и человека на концах линейных хромосом расположены тысячи высоко консервативных повторов гексадезоксинуклеотидов -TTAGGG, называемых теломерами, которые позволяют концам хромосом прикрепляться к ядерной оболочке и предотвращают их разрушение и рекомбинации. При каждой репликации длина теломер укорачивается примерно на 120 пар оснований. Для делящихся соматических клеток укорочение теломер служит репликометром. После достижения теломерными последовательностями критического размера клетки теряют способность к делению, стареют и подвергаются апоптозу (запрограммированной гибели).
В опухолевых и эмбриональных тканях тело-мераза достраивает теломеры на З'-концах ДНК хромосом и после репликации восстанавливает их исходную длину. За счёт работы этого фермента прекращается старение клеток, и они становятся бессмертными.
В. ИЗМЕНЕНИЯ В СТРУКТУРЕ ПЛАЗМАТИЧЕСКИХ МЕМБРАН И СЕКРЕЦИИ
Трансформация клеток приводит к изменению состава и структуры олигосахаридных цепей гликопротеинов и гликосфинголипидов плазматической мембраны, а как следствие - её проницаемости и заряда. В частности, снижается интенсивность синтеза и изменяется структура адгезивных молекул и интегриновых рецепторов (см. раздел 5), входящих в состав мембран опухолевых клеток.
Наблюдается секреция некоторых протеаз, коллагеназ и гликозидаз, которые разрушают коллаген, белки, гликозаминогликаны меж-
клеточного матрикса и способствуют инвазии опухоли в соседние ткани и сосуды. Усиливается синтез факторов ангиогенеза, стимулирующих развитие сосудов, которые должны снабжать раковые клетки питательными веществами.
Г. РОЛЬ ГОРМОНОВ И ФАКТОРОВ РОСТА В РАЗВИТИИ ОПУХОЛЕЙ
Рост и развитие клетки в нормальных и опухолевых линиях начинаются с воздействия на
клетку факторов роста (ФР). Взаимодействуя с рецепторами, расположенными на поверхности клеток, или с внутриклеточными рецепторами, они стимулируют в клетке каскад событий, приводящих к активации генов, ответственных за синтез белков, обеспечивающих рост и деление клеток (рис. 16-7).
Очевидно, что если гены, кодирующие рецепторы, трансдукторы сигналов и транскрипционные факторы, изменены вследствие мутаций таким образом, что экспрессируются постоянно,
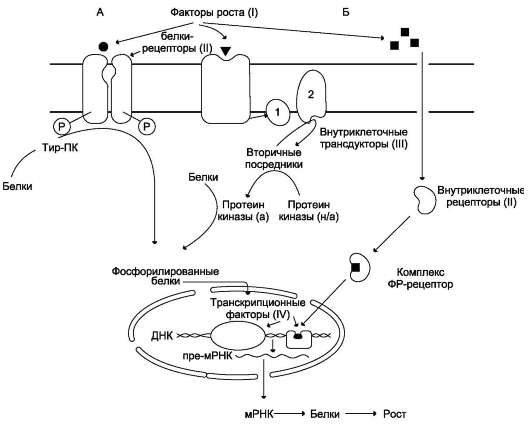
Рис. 16-7. Действие факторов роста на клетку. ФР связываются с рецепторами либо на поверхности мембраны, либо внутри клетки. А - ФР вызывают фосфорилирование белков либо непосредственно при взаимодействии с рецептором, являющимся тир-ПК-азой (ИФР-1, ИФР-2, инсулин), либо за счёт включения аденилатциклазного или фосфатидилинозитольного каскадов и активации протеинкиназ. Фосфорилированные белки активируют транскрипционные факторы, вызывающие синтез новых мРНК и белков. Б - ФР входит в клетку, в комплексе с внутриклеточным рецептором поступает в ядро, активируя транскрипцию генов, стимулирующих рост клетки. Гены, которые кодируют ФР (I), белки-рецепторы (II), трансдукторы сигналов (III) и транскрипционные факторы (IV), называют протоонкогенами. При изменении структуры I, II, III, IV протоонкогены становятся онкогенами и вызывают аномальный рост: 1 - G-белок; 2 - ферменты, синтезирующие вторичные посредники: аденилат-циклаза, фосфолипаза С, гуанилатциклаза.
то контролируемый рост заменяется неограниченной пролиферацией.
В опухолевых клетках возрастает скорость синтеза и секреции некоторых гормонов и факторов роста. Опухоли приобретают способность к автономному росту за счёт перехода на парак-ринный или аутокринный механизмы регуляции клеточного роста.
При аутокринном механизме регуляции опухоли синтезируют факторы роста и рецепторы к ним (рФР) или онкобелки, являющиеся аналогами ФР или рФР, которые, взаимодействуя между собой, вызывают аутостимуляцию роста и деления клеток.
Паракринная регуляция предполагает взаимодействие ФР, вырабатываемых одними клетками, с рФР, расположенными на соседних клетках. Так, например, при раке лёгкого клетки стромы вырабатывают инсулиноподобный фактор II, который взаимодействует с рецепторами раковых клеток лёгкого и стимулирует их рост и деление.
iii. онкогены, протоонкогены и гены-супрессоры опухолей
В
течение многих лет было неясно, почему и откуда у вирусов появились
гены, вызывающие рост опухолей. Сначала предполагали, что они
изначально принадлежат вирусному геному. Однако в
Чтобы отличать нормальные хозяйские гены от вирусных онкогенов, для первых было введено название протоонкогены. В группу протоонко-генов вошли гены, кодирующие белки, которые играют центральную роль в регуляции процессов роста и развития организма, такие как факторы
роста (ФР), рецепторы ФР, транскрипционные факторы и белки, вовлечённые в трансдукцию сигналов.
А. НОМЕНКЛАТУРА
Онкогены записывают трёхзначным кодом из строчных латинских букв, который обычно указывает объект, из которого данный онкоген был выделен впервые. Так, название онкогена ras указывает на ген, впервые идентифицированный в саркоме крысы (от англ. ratsarcomes). Иногда за трёхбуквенным кодом следует буква или цифра. Это становится необходимым, когда из одного и того же объекта выделяют онкогены, имеющие разные активности. В вирусе эритробластоза идентифицированы гены: erb A, являющийся вирусным гомологом рецептора тиреоидного гормона, и erb B - гомолог рецептора ЭФР.
Проставление числа за обозначением гена часто отражает тот факт, что гены являются членами близко родственных семейств, а номер указывает место гена в данном семействе: bcl 1, bcl 2 и т.д.
Для обозначения вирусных онкогенов перед трёхбуквенным названием онкогена вводят строчную букву v (от англ. virus - вирус) - v-onc, а для обозначения клеточных онкогенов, образующихся в трансформированных клетках при мутациях, букву с (от англ. cell - клетка) - c-onc.
Гены-супрессоры опухолей, кодирующие белки, которые ингибируют рост и деление клеток, имеют ещё более разнообразную номенклатуру. Наряду с двух- и трёхбуквенным кодом (ген rb) в некоторых случаях указывают размер белкового продукта. Ген p53 так называют потому, что он кодирует синтез белка с молекулярной массой
53 кД.
Белковые продукты генов часто обозначают так же, как гены, но с заглавной буквы. Так, ген ras кодирует белок Ras, ген р53 - белок Р53.
Б. ТИП НАСЛЕДОВАНИЯ ОНКОГЕНОВ
И ГЕНОВ-СУПРЕССОРОВ ОПУХОЛЕЙ
Большинство опухолей возникает из соматических клеток, а так как соматические клетки диплоидны, то они несут два аллеля каждого гена. Если мутация в одном из аллелей ведёт к нарушению функции клеток, то говорят о доминантном типе наследования. Именно такой тип наследования характерен для онкогенов и гена р53.
Если мутация в одном аллеле не проявляется функционально, то говорят о рецессивном типе наследования. В этом случае биологический эффект достигается только при повреждении обоих аллелей. По рецессивному механизму проявляются мутации в генах-супрессорах опухолей (за исключением р53). Когда вслед за первым аллелем в молекуле ДНК второй аллель также изменяется, то клетка переходит от гетерозиготного к гомозиготному наследованию информации о данном белке, т.е. наблюдается потеря гетерозиготности - LOH (от англ. loss of heterozygosity). Результатом повреждений генома такого типа является синтез изменённого и функционально неактивного белка.
В. ФУНКЦИИ ОНКОГЕНОВ
Изучение вирусных онкогенов показало, что более 50% из них кодируют тирозиновые про-теинкиназы (тир-ПК), а остальные содержат информацию о различных функционально активных белках: укороченном ФР тромбоцитов, укороченном эпидермальном факторе роста (ЭФР) и рецепторе ЭФР (рЭФР), ДНК-связы-вающих, ГТФ-связывающих и некоторых других регуляторных белках.
Рассмотрим основные группы белков, которые кодируются онкогенами.
Тирозиновые протеинкиназы (тир-ПК)
К группе тир-ПК относят: онкоген erb-B вируса эритробластоза птиц, кодирующий белок, идентичный β-субъединице ЭФР, гомологи факторов роста тромбоцитов и рецепторов инсулиноподобных факторов I и II. Src-ген, выделенный из вируса саркомы Рауса, кодирует белок РР60, который обладает активностью тир-ПК. Он фосфорилирует некоторые ферменты гликолиза и ускоряет использование глюкозы в опухолевых клетках, нарушает контактное торможение клеток и стимулирует трансформацию клеток.
В группу тир-ПК помимо онкогенов входят некоторые протоонкогены (рецептор инсулина, рЭФР, рФР тромбоцитов). Следует отметить, что хотя некоторые белки организма и обладают активностью тир-ПК, но количество фосфоти-розина в нормальных клетках очень низко (не более 1% от всех фосфорилированных аминокислот). При опухолевом перерождении ткани
активность тир-ПК сильно возрастает, и количество фосфотирозина в фонде аминокислот, входящих в белки, увеличивается.
Ras-онкогены
Другую группу онкобелков кодирует семейство генов ras. Протоонкогены ras содержат информацию о семействе Ras-белков, представляющих собой небольшие G-белки. Подобно G-белкам основных сигнальных систем, эти белки присоединяют ГТФ и обнаруживают ГТФ-азную активность, однако, в отличие от G-белков, имеющих олигомерную αβγ-структуру, Ras-белки мономерны. Они участвуют в трансдукции сигналов, полученных мембранными рецепторами клетки, и, будучи локализованы на внутренней поверхности мембран, тесно контактируют с фосфоли-пидами и мембранными белками. Установлено участие Ras-белков в изменении структуры цитоскелета, регуляции экзо- и эндоцитоза, реализации митогенных сигналов и активации белков, участвующих в транскрипции генов.
Ras-онкобелки, образующиеся в результате единичных миссенс-мутаций в ГТФ-связываю-щем домене, обладают очень низкой ГТФ-азной активностью. В результате аденилатциклаза или фосфолипаза С остаются в активированном состоянии дольше, чем обычно, и, таким образом, обеспечивают проведение более длительного сигнала.
Ras-онкобелки обнаружены в 25% всех опухолей человека, причём при некоторых формах опухолей значительно чаще: в 90% карцином поджелудочной железы и более чем в 50% карцином прямой кишки.
Ядерные онкобелки
В семейство ядерных онкогенов входят гены jun, fos, myc, myb и erb A. Онкобелки, образующиеся при экспрессии этих генов, связываются со специфическими последовательностями на ДНК и функционируют как транскрипционные факторы.
Например, онкобелки Jun и Fos образуют димер, который присоединяется к ДНК, Erb A является изменённой формой рецептора тире-оидного гормона, который тоже связывается со специфическими последовательностями на молекуле ДНК.
Аминокислотная последовательность онко-белка, закодированного геном v-jun, на 80% гомологична ядерному транскрипционному фактору АР1. Когда белки Jun и Fos объединяются, они образуют структуру лейциновой молнии - хорошо известного активатора транскрипции (см. раздел 1).
Г. РОЛЬ СУПРЕССОРОВ ОПУХОЛЕЙ
В МЕТАБОЛИЗМЕ КЛЕТОК
При слиянии нормальных клеток с опухолевыми возникают гибридные клетки, которые, как правило, не обладают злокачественностью. Из этого был сделан вывод о том, что в нормальных клетках присутствуют гены, белковые продукты которых сдерживают репликативный потенциал клеток и предотвращают развитие опухолей. Эти гены получили название ге-нов-супрессоров опухолей, или антионкогенов. Установлено, что в ходе злокачественной трансформации функции этих генов часто утрачиваются, что влечёт за собой нарушение контроля клеточной пролиферации.
В настоящее время описано более 10 генов-супрессоров опухолей (rb1, p53, p21, p16, p15, wt1 и др.), которые кодируют регуляторные белки,
ингибирующие аномальный рост и трансформацию клеток.
Ген rb1. Продуктом гена rb1 является ядерный белок с молекулярной массой 105 кД, участвующий в регуляции вступления клетки из фазы покоя G0 в фазу подготовки к синтезу ДНК G1 и прохождения проверочной точки G1/S. Белок Rb1, подобно циклинзависимым киназам (см. раздел 4), подвергается модификациям путём фосфорилирования и дефосфорилирования. В дефосфорилированной форме он может связываться и инактивировать транскрипционный фактор E2F, который, в свою очередь, усиливает экспрессию рост-стимулирующих белков и ферментов: ДНК-полимеразы α, MYC, CDC2 и некоторых других (рис. 16-8).
В норме, когда клетка вступает в S-фазу и начинает удваивать ДНК, белок Rb1 сильно фосфорилируется и перестает тормозить продвижение клетки по клеточному циклу.
Ген р53 - другой наиболее изученный пример гена-супрессора опухолей. Этот ген кодирует ядерный фосфопротеин с молекулярной массой 53 кД, который препятствует вхождению клеток в S-фазу, амплификации и мутациям ДНК. Полагают, что физиологическая функция
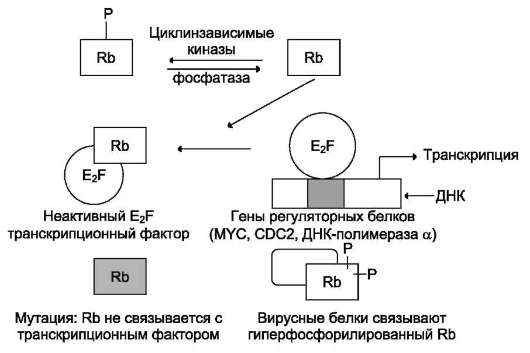
Рис. 16-8. Механизм действия белка Rb1. E2F - транскрипционный фактор, усиливающий транскрипцию ряда белков и ферментов, которые регулируют рост и деление клетки. Присоединяясь к E2F, белок-супрессор Rb1 ингибирует подготовку клеток к митозу. Гиперфосфорилированные и мутантные формы белка Rb1 не имеют сродства к E2F и перестают тормозить рост клеток.
белка Р53 состоит в том, чтобы задерживать в G1- и G2-фазах клетки, имеющие повреждения в структуре ДНК до тех пор, пока эти повреждения не будут устранены. В том случае, если репарирующие системы не способны устранить дефекты в структуре ДНК, то этот белок обеспечивает включение механизма апоптоза, уничтожающего повреждённую клетку.
Белок Р53 у человека содержит 393 аминокислоты и состоит из 3 доменов: N-концевого, обогащённого дикарбоновыми аминокислотами, который регулирует транскрипцию; центрального, обеспечивающего связывание с ДНК; С-концевого, ответственного за образование олигомерной структуры этого белка.
Р53 функционирует в форме тетрамера и связывается с регуляторными участками ДНК. Довольно много генов клетки имеют последовательности, способные присоединять Р53 и изменять экспрессию соответствующих генов
(рис. 16-9).
К генам-мишеням относят ген, кодирующий белок Р21 - ингибитор большинства циклин-зависимых киназ. Р53 усиливает транскрипцию гена р21, в результате продвижение по клеточному циклу, рост и деление клетки тормозятся.
Р53 усиливает транскрипцию гена gadd45, белковый продукт которого стимулирует репа-ративные процессы. Показано, что экспрессия
этого гена значительно возрастает в клетках, подвергнутых облучению.
К Р53 чувствительны 2 гена bcl 2 и bax, кодирующие белки, которые участвуют в регуляции апоптоза. Апоптоз активируется в том случае, когда Р53 присоединяется к регуляторным участкам генов bcl 2 и bax, при этом экспрессия антиапоптотического гена bcl 2 снижается, а проапоптотического гена bax увеличивается.
Активируя ключевые гены, реализующие программированную гибель клетки, Р53 ускоряет разрушение потенциально опасных клеток, которые повреждены и способны трансформироваться.
Р53 увеличивает экспрессию гена, который кодирует белок тромбоспондин, препятствующий росту сосудов в опухоли (ангиогенез) и, следовательно, препятствующего образованию метастазов (см. раздел 14).
Таким образом, Р53 функционирует в тканях как «хранитель» здоровья клеток, или «молекулярный полицейский».
iv. механизмы неопластической трансформации
В настоящее время установлено, что в регуляции роста и дифференцировки клеток принимает участие более 100 различных ге-
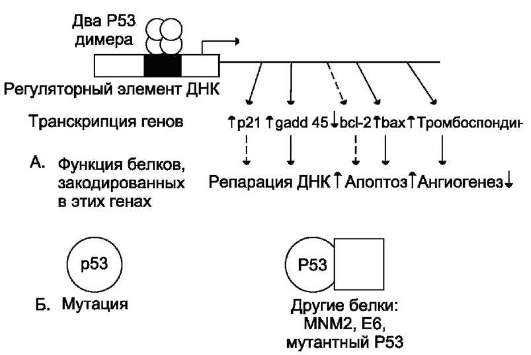
Рис. 16-9. Влияние белка Р53 на транскрипцию ряда генов. А - основные гены-мишени, экспрессию которых регулирует белок Р53; Б - инактивация Р53 в результате мутаций в гене или связывания с белками-ингибиторами делает его неспособным ингибировать транскрипцию указанных генов мишеней.
нов и около 10 генов-супрессоров опухолей. Злокачественная трансформация не является результатом единичного события. Прежде чем возникает малигнизированная клетка, проходит 5-7 стадий, вызывающих изменения в генетическом аппарате клетки (гипотеза многоступенчатого канцерогенеза).
А. ПРЕВРАЩЕНИЕ ПРОТООНКОГЕНОВ
В ОНКОГЕНЫ
В настоящее время выявлено пять основных механизмов превращения протоонкогенов в онкогены либо в результате повреждения структуры генов, либо за счёт изменения уровня экспрессии.
Включение в геномную ДНК новых промоторов
Ранее уже указывалось, что геном ДНК- и РНК-содержащих вирусов интегрирует с ДНК клетки хозяина в форме провирусов. Известно, что ДНК провирусов имеет с обоих концов длинные повторы - LTR, которые играют роль промоторов транскрипции (рис. 16-10). Так, после инфицирования В-лимфоцитов цыплёнка некоторыми вирусами лейкоза птиц провирусы иногда включаются около гена с-myc. В результате ген myc активируется, возрастает его транскрипция
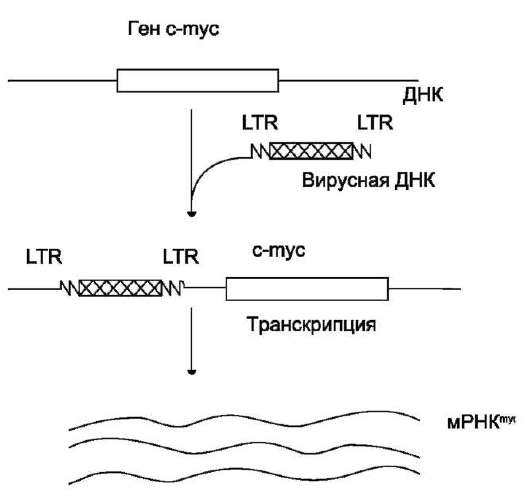
Рис. 16-10. Появление новых промоторов в геноме человека при включении генетического материала вируса в молекулу ДНК.
с образованием значительных количеств myc-мРНК и последующая трансляция.
Появление новых энхансерных последовательностей
В ряде случаев провирус встраивается в молекулу ДНК перед геном с-myc или после него, либо может быть ориентирован в противоположном направлении, и тем не менее ген с-myc активируется. Этот эффект свидетельствует о том, что в провирусе присутствуют энхансер-ные последовательности, которые увеличивают экспрессию гена (рис. 16-11).
Амплификация генов
Это явление обнаружено у ряда опухолей. Показано, что амплификация с-ras онкогенов играет существенную роль в прогрессии клеток в направлении большей злокачественности. А введение противоопухолевого препарата метот-рексата (ингибитора дигидрофолатредуктазы) вызывает в ходе лечения амплификацию гена дигидрофолатредуктазы более чем в 400 раз, снижая чувствительность опухолевых клеток к лекарству. В ходе цитологического исследования амплифицированные гены можно обнаружить в виде гомологично окрашенных областей на хромосомах, лишённых центромеров.
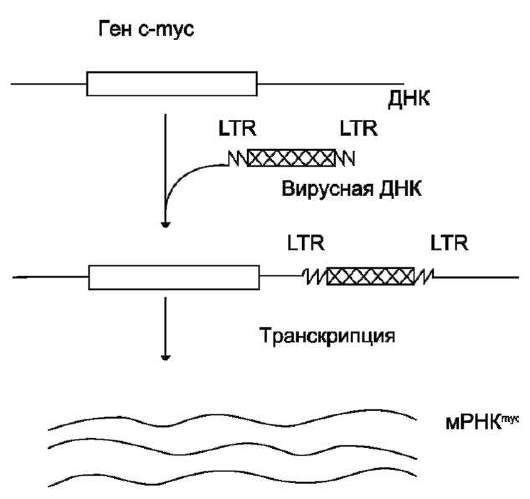
Рис. 16-11. Включение в геном человека провируса, содержащего энхансерную последовательность.
Точечные мутации
Онкоген с-ras, первоначально обнаруженный в некоторых ретровирусах, кодирует белок с молекулярной массой 21 кД, который назван белком Р21. Анализ ДНК-последовательностей с-ras протоонкогена из нормальных клеток и с-ras онкогена из опухоли жёлчного пузыря человека показал, что эти гены различаются по одному азотистому основанию, соответствующие им белки имеют разные аминокислоты в двенадцатом положении Р21. Аналогичные результаты были получены при исследовании структуры с-ras онкогена из других опухолей человека. Результат во всех случаях был одним и тем же: в структуре онкогена обнаруживалась одна миссенс-мутация, хотя положение мутации в гене могло быть разным. Тем не менее эта мутация изменяла конформацию кодируемого белка и снижала его ГТФ-азную активность. Мутантный белок вызывал длительную стимуляцию аденилатциклазы, повышение в клетке концентрации цАМФ и активацию цАМФ-за-висимых протеинкиназ.
Обнаружены мутации, вызывающие постоянную активацию цитозольной тир-ПК онкогена src и Сер-Тре-ПК онкогенов mos и ret. В результате ферменты фосфорилируют одну из изоформ фосфолипазы С, включают инозитолфосфатный путь передачи сигнала, активируют транскрипционные факторы, которые стимулируют клетки к пролиферации и делению.
В карциномах молочной железы и яичников часто обнаруживают онкоген erb В2 или neu, являющийся гомологом рецептора эпидермального фактора роста. Молекула рецептора содержит 3 домена: внеклеточный, или рецепторный домен, домен, пронизывающий мембрану, и внутриклеточный домен, обладающий активностью
Тир-ПК.
В ходе трансформации этот ген рецептора амплифицируется и утрачивает фрагмент, ответственный за связывание фактора роста. В результате в клетках образуется белок с нерегулируемой активностью Тир-ПК («эффект нажатой кнопки»), который стимулирует мито-тические процессы в клетке.
Хромосомные транслокации
В опухолевых клетках часто обнаруживаются хромосомные транслокации, когда фрагмент
одной хромосомы отделяется и включается в другую хромосому. Если участок второй хромосомы отдаёт на первую соответствующий фрагмент, то такую транслокацию называют реципрокной транслокацией. Изменение положения гена в ряде случаев увеличивает его экспрессию и стимулирует малигнизацию. Так, в геноме пациентов с хроническим миелолейкозом имеет место реципрокная транслокация, в ходе которой протоонкоген abl перемещается из хромосомы 9 в хромосому 22 (t 9:22) с образованием укороченной филадельфийской хромосомы (рис. 16-12, А), которая легко обнаруживается при рассмотрении хромосом под микроскопом. В результате в филадельфийской хромосоме появляется гибридный ген с-abl-bcr, кодирующий белок с высокой активностью тир-ПК. Этот фермент вызывает последовательность событий, стимулирующих злокачественную трансформацию кроветворных клеток.
При лимфоме Бёркитта протоонкоген с-myc переносится из хромосомы 8 в хромосому 14 (t 8:14). Транслокация такого типа обнаружена у 90% больных, а в 10% случаев имеет место t 8:2 или t 8:22. Установлено, что во всех случаях ген с-myc перемещается в область сильного промотора генов, кодирующих H-цепи иммуноглобулинов. В результате в клетках происходит гиперпродукция нормального белка C-MYC, который представляет собой транскрипционный фактор, участвующий в ранних стадиях пролиферации (рис. 16-12, Б).
Б. МУТАЦИИ В ГЕНАХ-СУПРЕССОРАХ
ОПУХОЛЕЙ
При ретинобластоме (редком детском онкологическом заболевании сетчатки глаза, 1:20 000 детей) наблюдают делецию в локусе rb1 хромосомы 13. На основании эпидемиологических исследований и статистического анализа было установлено, что ретинобластома развивается в случае мутации в гене обоих аллелей ретинобласта (рис. 16-13). Анализ ДНК из участков нормальной ткани и опухоли, полученных от больных в ходе операции, показал, что в образцах нормальной ткани ДНК гена rb1 гетерозиготна, т.е. содержит один неизменённый и другой изменённый аллели, тогда как в опухолевой ткани оба аллеля изменены, т.е. произошла потеря гетерозиготности. Мутация
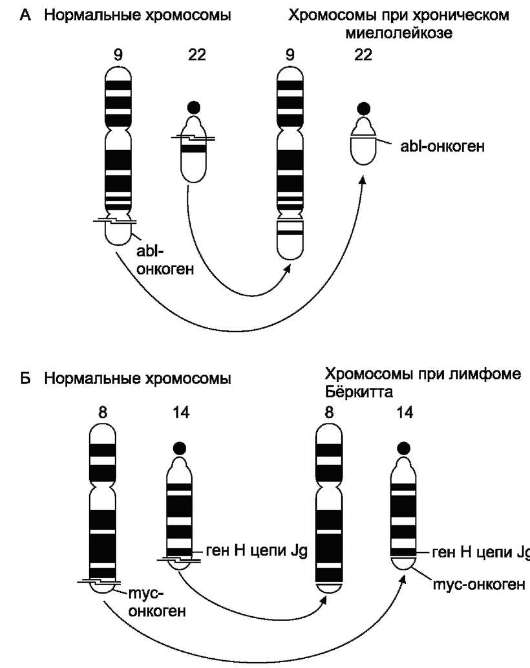
Рис. 16-12. Хромосомные транслокации и активация протоонкогенов. А - хронический миелолейкоз; Б - лимфома Бёркитта.
инактивирует белок, и он перестаёт оказывать ингибирующее действие на пролиферативные процессы, инактивация наблюдается и в том случае, если rbl связывается с вирусными белками-ингибиторами.
При наследственной ретинобластоме (~40% случаев) часто встречаются множественные опухоли. Они вызваны тем, что мутации в единственном неповреждённом аллеле могут возникать в нескольких ретинобластах. При ненаследственной спорадической форме болезни (~60% случаев) множественные опухоли редки, так как инактивация гена в обоих аллелях одной клетки происходит крайне редко.
Мутации в гене р53 встречаются более чем у половины онкологических больных. Статистика показывает, что функционально неактивный Р53
обнаруживается у 70% больных раком толстой кишки, в 50% случаев рака лёгких и 40% - рака груди.
Около 80% мутаций в гене р53 - миссенс-му-тации, затрагивающие наиболее консервативные области гена в участках CG динуклеотидных последовательностей, которые имеют как наследственный, так и ненаследственный характер.
Другой отличительной особенностью гена р53 является то, что мутации в нём проявляются по доминантному типу в результате нарушения структуры в одной из копий генов диплоидной клетки, тогда как для остальных генов-супрес-соров опухолей мутации проявляются по рецессивному механизму.
В нормальных тканях концентрация белка Р53 очень низка. Мутации удлиняют полупери-
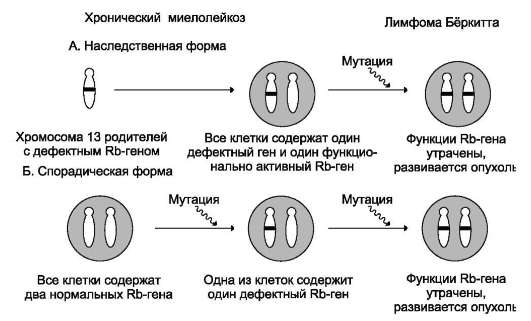
Рис. 16-13. Развитие наследственной (А) и спорадической (Б) форм ретинобластомы.
од жизни этого белка от нескольких минут до нескольких часов, в результате в ядрах клеток повышается концентрация мутантной формы Р53. Это нашло практическое применение в им-муногистохимическом исследовании опухолей на содержание мутантного белка.
Инактивация белка Р53 происходит не только в результате повреждений в структуре гена, но и при образовании неактивных белок-белковых комплексов с вирусными белками (например, SV40 большим Т-антигеном) или при разрушении белка, которое стимулируют онкобелки, образующиеся при заражении вирусом папилломы человека.
v. теория многоступенчатого канцерогенеза на модели рака прямой кишки
К числу наиболее распространённых типов злокачественных опухолей относят рак прямой кишки. Большинство заболеваний этой этиологии начинается с возникновения доброкачественных опухолей, называемых аденомами. На основании сравнения характерных хромосомных кариотипов, онкогенов, генов-супрессоров опухолей и уровня метилирования ДНК в образцах неизменённой ткани прямой кишки, аденом разного размера, карцином и метастазов рака
прямой кишки была предложена модель, устанавливающая последовательность событий в ходе образования карцином прямой кишки.
Как видно из рис. 16-14, развитию рака предшествуют 5-7 мутаций в онкогенах и ге-нах-супрессорах опухолей, гипометилирование ДНК и нарушения в работе ДНК-репарирующих систем. К ранним событиям этого процесса относят мутации в гене-супрессоре опухолей, локализованном в хромосоме 5. Они обнаружены у пациентов с семейным аденоматозным полипозом FAP (от англ. familial adenomatous polyposis), в результате чего заболевание дало соответствующее название гену fap-ген).
На ранних стадиях процесса происходит снижение уровня метилирования ДНК и активация ras-онкогена на хромосоме 12, которые способствуют росту аденом. Дефекты в работе репарирующих систем, утрата или инактивация генов-супрессоров опухолей вызывают появление генетической нестабильности и озлокачест-вление опухоли. При этом последовательность изменений несущественна, важнее общее накопление изменений в геноме. Дедифференци-ровка и продолжающееся накопление мутаций сообщают опухолевым клеткам способность к инвазии и метастазированию.
Нарушения в работе ДНК-репарирующей системы, участвующей в исправлении ошибок
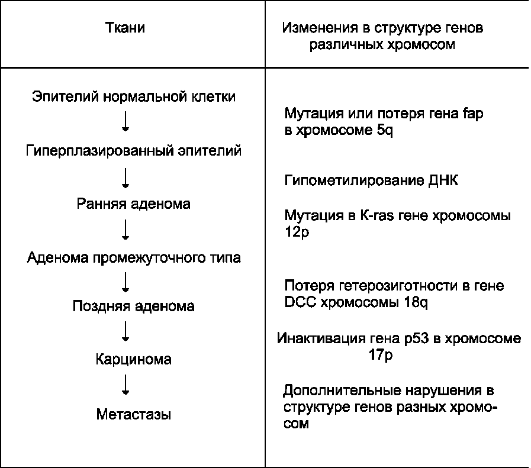
Рис. 16-14. Генетическая модель развития рака прямой кишки. Ранняя аденома имеет диаметр менее
репликации, отмечены при наследственной форме неполипозного рака прямой кишки и опухолях некоторых других тканей. В этих случаях имела место микросателлитная нестабильность. Микросателлитные последовательности - короткие некодирующие последовательности ДНК, которые повторяются в геноме много раз. В опухолях, в отличие от нормальной ткани, микросателлитные последовательности варьируют по длине, указывая на то, что опухолевые клетки либо теряют, либо приобретают лишние нуклеотиды. Это явление может наблюдаться в том случае, если в ходе репликации две нити ДНК скользят друг относительно друга. В зависимости от направления скольжения новая нить ДНК будет короче или длиннее родительской. В результате во вновь синтезированной двухцепочечной ДНК появятся небольшие петли неспаренной ДНК, которые в нормальных тканях устраняются репарирующей системой. В опухолях эта система работает плохо: так,
практически во всех случаях рака прямой кишки обнаружена мутация в генах, кодирующих белки репарирующего комплекса.
vi. инвазия и метастазирование
Доброкачественные опухоли иногда могут расти быстро и достигать больших размеров, но они не метастазируют. Только для злокачественных опухолей обнаруживается способность прорастать в другие ткани, как соседние, так и отдалённые, где они образуют вторичные опухоли.
Первоначально опухолевые клетки образуют клон генетически идентичных (моноклональ-ных) клеток, которые делятся чаще, чем соседние, нормальные клетки. Они не запрограммированы к движению. Однако состав и поведение таких клеток не статичны, и потомки одной клетки начинают «расходиться» как генетически, так и фенотипически. Каждое последующее
поколение клеток обнаруживает увеличение отклонений от нормы.
Когда клеточная масса опухоли достигает диаметра около
А. ИЗМЕНЕНИЕ СОСТАВА МЕМБРАННЫХ БЕЛКОВ
В метастазирующих клетках происходит существенное изменение состава мембранных белков. В эпителиальных клетках основным белком, отвечающим за адгезивные свойства, служит Е-кадгерин (см. раздел 5), внеклеточный домен которого участвует в образовании межклеточных связей с молекулами Е-кадгерина соседних клеток. Другой класс белков - катенины - отвечает за связывание Е-кадгерина с цитоскелетом.
В опухолевых клетках содержание Е-кад-герина снижено, а молекулы катенинов либо функционально неактивны, либо отсутствуют. Мутации в гене Е-кадгерина редки, но если они возникают, то у таких пациентов наблюдают низкодифференцированные формы рака. Контактное торможение и связь клеток друг с другом нарушаются, внутриклеточная архитектоника мало напоминает структуру нормальных клеток.
Было доказано, что β-катенин участвует также во внутриклеточной системе передачи сигналов и стимулирует пролиферацию клеток. Однако, будучи в комплексе с АРС-белком (от англ. adenomatous poliposis coli), он ингибирует деление и участвует в уничтожении дефектных клеток через апоптоз. Если в результате мутаций один из этих белков будет изменён, то комплекс не образуется, и β-катенин, не сдерживаемый АРС-белком, взаимодействует с ДНК и стимулирует
вступление клеток в клеточный цикл. Появление мутаций в АРС коррелирует с ростом полипов (небольших доброкачественных опухолей) в прямой кишке, а у людей с наследственной формой мутантного АРС повышается риск перерождения полипов в опухоль.
В связывании клеток с коллагеном участвуют белки-интегрины, а с другими компонентами межклеточного матрикса и базальными мембранами - фибронектин и ламинины (см. раздел 15). При трансформации клеток количественное и качественное содержание этих белков меняется. В большинстве опухолей снижено количество фибронектина и синтезируются модифицированные интегрины, которые помогают инвазив-ным клеткам мигрировать через соединительную ткань и стенку капилляров.
Б. ФЕРМЕНТЫ, ПРИСПОСАБЛИВАЮЩИЕ ОПУХОЛЕВЫЕ КЛЕТКИ К ДВИЖЕНИЮ
Инвазия - активный процесс, включающий стадии, в которых опухолевая клетка:
• проходит через межклеточный матрикс, достигая кровеносного или лимфатического сосуда;
• преодолевает стенку сосуда и поступает в кровеносное русло или лимфу;
• циркулирует с током крови в виде надмолекулярных комплексов с белками и клетками крови;
• прикрепляется к стенке сосуда и повторяет процесс в обратном направлении, продвигаясь на 2-3 клеточных диаметра в инвази-руемую ткань;
• закрепляется и начинает формировать новую опухоль.
Выполнение этих функций требует синтеза специфических ферментов, рецепторов и энергии. Метастазирующие клетки и окружающие опухолевую ткань фибробласты секретируют целый набор ферментов, обеспечивающих разрушение межклеточного матрикса и базальных мембран: коллагеназы, расщепляющие коллаген межклеточного матрикса; гепаразу, катализирующую гидролиз гепа-рансульфата - преобладающего протеогли-кана базальной мембраны; катепсин В - мощную протеазу, которая в нормальных клетках локализована в лизо-сомах, а у метастазирующих клеток встроена
в плазматическую мембрану и помогает им покинуть родительскую ткань. Этот фермент активирует проколлагеназу, которая специфически расщепляет коллаген IV типа (см. раздел 15);
плазмин, который расщепляет некоторые белки межклеточного матрикса неколлаге-нового происхождения;
семейство металлопротеаз, участвующее в разрушении различных компонентов межклеточного матрикса. Они секретируются в виде проферментов и активируются либо катеп-сином В, либо урокиназой типа активатора плазминогена.
В. циркуляция
МЕТАСТАЗИРУЮЩИХ КЛЕТОК
После успешного прохождения через соединительную ткань органа опухолевые клетки продвигаются к ближайшему кровеносному сосуду, проталкиваются между эндотелиальными клетками, выстилающими сосудистую стенку, и выходят в кровоток (рис. 16-15).
Кровеносные сосуды являются каналами, по которым опухолевые клетки доставляются к местам новой локализации. Они транспортируются по крови в виде комплексов с тромбоцитами, миграционными факторами и фрагментами межклеточного матрикса, которые маскируют их от иммунологического надзора и обеспечивают прикрепление к базальной мембране в органах-мишенях.
Г. ФОРМИРОВАНИЕ ВТОРИЧНЫХ ОПУХОЛЕЙ
Углеводы, выступающие на поверхность опухолевых клеток, связываются с селектином - углеводным компонентом рецепторов эндо-телиальных клеток. Каждый тип опухолевых клеток имеет на плазматической мембране характерную для них углеводную часть, которая может взаимодействовать лишь с определёнными олиго- и полисахаридами клеток эндотелия. Однако эти взаимодействия между углеводами слабы, и клетка окончательно прикрепляется к стенке сосуда с помощью интег-ринов (рис. 16-16).
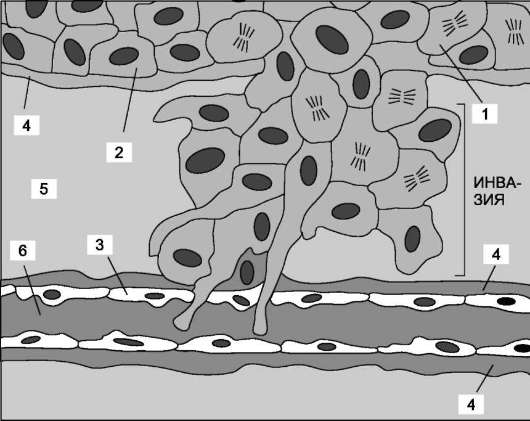
Рис. 16-15. Миграция опухолевых клеток в кровеносный или лимфатический сосуд. 1 - делящаяся опухолевая клетка; 2 - неделящаяся опухолевая клетка; 3 - эндотелиальная клетка; 4 - базальная мембрана; 5 - строма; 6 - просвет кровеносного сосуда.
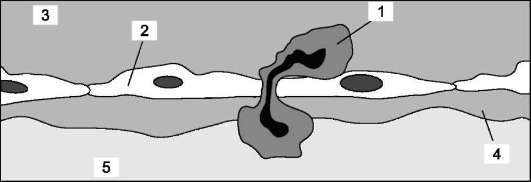
Рис. 16-16. Начало формирования вторичной опухоли. 1 - опухолевая клетка; 2 - эндотелиальная клетка; 3 - просвет кровеносного сосуда; 4 - базальная мембрана; 5 - строма.
Эти особенности закрепления опухолевой клетки в другом органе лежат в основе тропности процесса: метастазы появляются не в любых, а в «излюбленных» данной формой опухоли местах. Так, рак простаты, как правило, даёт метастазы в кости, рак молочной железы и лёгкого - в мозг, а рак прямой кишки - в печень.
vii. основные принципы диагностики опухолей и лечения рака
Несмотря на серьёзные и разносторонние исследования последних лет, в области онкологии остаётся много проблем, которые в первую очередь связаны с ранней диагностикой и лечением отдельных нозологических форм заболевания. Одним из направлений диагностики опухолей являются поиск и разработка методов выявления индикаторов опухолевого процесса - опухолевых маркёров.
А. ОПУХОЛЕВЫЕ МАРКЕРЫ
Опухолевыми маркёрами (ОМ) называют соединения (белки, биологически активные пептиды, гормоны, ферменты и метаболиты), которые синтезируются раковыми клетками, либо клетками нормальных тканей в ответ на развитие рака. Они должны синтезироваться в организме опухоленосителя и отсутствовать в нормальных клетках, так как являются продуктами аномальной экспрессии генома раковой клетки. ОМ, как правило, обнаруживают в крови или других биологических жидкостях организма и используют для скрининга населения на носи-тельство опухоли, как прогностический фактор,
для оценки состояния пациента в клинической стадии и мониторинга в ходе лечения, а также в целях обнаружения рецидивов болезни.
Согласно современной классификации ОМ делят на три основные группы:
• первичные опухолево-ассоциированные;
• вторичные, продуцируемые опухолью (специфические и неспецифические);
• вторичные, индуцируемые опухолевым процессом.
Эта классификация не лишена недостатков, так как одно и то же соединение может синтезироваться клетками опухоли и вырабатываться нормальными клетками органа в ответ на опухолевую инвазию.
Большинство известных в настоящее время ОМ не лишены недостатков. Почти во всех случаях при ряде патологических состояний, таких как воспалительные заболевания печени, поджелудочной железы и лёгких, отмечается неспецифическое, часто незначительное повышение уровня маркёра; иногда ОМ не определяется на ранней стадии болезни.
Онкофетальные белки
В клинической практике наиболее часто используют определение белков, которые обнаруживаются в эмбриональных тканях человека и крови в период внутриутробного развития. Они исчезают полностью либо остаются в следовых количествах после рождения. В ходе опухолевой прогрессии они начинают синтезироваться снова и секретируются в кровь.
Карциноэмбриональный антиген (КЭА) - одно-цепочечный белок, гликопротеин с молекулярной массой от 150 до 300 кД, углеводная компонента которого составляет от 45 до 57%
молекулярной массы. В углеводную часть молекулы в значительных количествах входят: фруктоза, манноза, галактоза, N-ацетил-глю-козамин. Определение этого ОМ наиболее часто проводят для диагностики рака прямой кишки и в слежении за состоянием больного в постоперационном периоде. После полного и удачного удаления опухоли концентрация КЭА снижается. Последующее повышение значений этого показателя у оперированных больных указывает на рецидив болезни и высокую вероятность метастазов.
α-Фетопротеин (α-ФП) - гликопротеин с молекулярной массой 61-70 кД, близкий по строению к альбумину. Углеводная часть составляет ~5% от общей массы белка. Он является нормальным сывороточным белком зародыша, синтезируется в печени, желточном мешке и ЖКТ и выделяется в кровь. Наиболее высокая концентрация этого белка наблюдается в ходе эмбриогенеза и внутриутробного развития плода. После рождения и в ходе первого года жизни ребёнка синтез и секреция α-ФП резко снижаются, и у взрослого человека его концентрация составляет лишь 20 нг/мл. Концентрация α-ФП повышается в крови при развитии рака печени, поэтому его определение используют для диагностики и в дальнейшем для оценки эффективности лечения.
В качестве опухолевых маркёров часто используют хорионический гонадотропин, плацентарную щелочную фосфатазу и некоторые другие плацентарные белки. β-Хорионический гонадотропин (β-ХГТ) - плацентарный гормон гликопротеиновой природы с молекулярной массой 45 кД, состоящий из α- и β-субъеди-ниц. В норме он не обнаруживается вовсе или содержится в ничтожных концентрациях. При беременности гормон начинает синтезироваться и секретироваться в кровь, достигая максимальных значений к 12 нед (тест на беременность). Затем его содержание медленно снижается и остаётся на очень низком уровне до и после родов.
При опухолях яичников и семенников концентрация гормона, а в некоторых случаях только его β-субъединицы, повышается. Поскольку С-концевой участок β-субъединицы ХГТ иммунореактивен, то иммуногистохимическое обнаружение гормона служит хорошим онко-маркёром в диагностике и слежении за ходом
лечения наследственных и спорадических опухолей. Измерение уровня β-ХГТ в спинномозговой жидкости помогает диагностировать метастазы в мозг и в ЦНС.
В качестве ОМ используют также дифферен-цировочные антигены, которые представляют собой органоили опухолеспецифические гликопротеины лимфоцитов (тканевый полипептидный антиген, тканевый полипептидный специфический антиген и другие), определяющиеся в крови с помощью моноклональных антител.
Для рака предстательной железы в качестве ОМ наиболее чувствителен простатоспеци-фический антиген PSA (от англ. prostate specific antigen). Он практически не определяется у женщин, у мужчин в норме ниже 2 нг/мг, но существенно возрастает в злокачественных и доброкачественных опухолях предстательной железы.
Гормоны и их рецепторы (эстрогены и андроге-ны, паратгормон, кальцитонин, гормон роста, инсулин, глюкагон, АКТГ, катехоламины, се-ротонин) являются ОМ гормонпродуцирующих органов. Их определение широко используют в клинической практике (табл. 16-2).
Определение рецепторов гормонов в качестве опухолевых маркёров оказалось важным тестом в выявлении пациентов, у которых после хирургического вмешательства велика вероятность рецидивов заболевания и которым необходима химиотерапия.
Так, для больных раком молочной железы важнейшим фактором прогноза дальнейшего течения болезни является определение рецепторов эстрогенов и прогестерона. Присутствие рецепторов позволяет в большом проценте случаев
Таблица 16-2. Гормоны как опухолевые маркёры некоторых видов опухолей

(50-75%) получить положительные результаты при лечении антиэстрогеном тамоксифеном и увеличивает выживаемость.
Некоторые ферменты и белки используют для диагностики и контроля за эффективностью терапии. Так, при различных морфологических вариантах рака лёгкого наиболее перспективным является определение нейронспецифической енолазы и растворимого фрагмента цитокера-тина - структурного компонента цитоскелета эпителия бронхов.
Высокая активность в биопсийном материале катепсина D свидетельствует о высоком метастатическом потенциале опухоли и коррелирует с низкой выживаемостью онкологических больных. Другим ОМ, свидетельствующим о неблагоприятном течении болезни, является высокая активность сериновой протеазы - активатора плазминогена урокиназного типа. Этот фермент катализирует образование плазмина, который участвует в активации металлопротеаз и способствует развитию инвазивных процессов и метастазирования.
К ОМ, появляющимся в организме больного в ответ на развитие опухолевого процесса, относят белки острой фазы воспаления: ферритин, церулоплазмин, гаптоглобин, С-ре-активный белок, изоформы ЛДГ и креатинки-назы.
Б. ЛЕЧЕНИЕ ОНКОЛОГИЧЕСКИХ БОЛЬНЫХ
К лечебным мероприятиям прибегают при обнаружении опухоли или на более поздних стадиях, используя химио-, радиотерапию и симптоматическое лечение. Важное условие успешного лечения - радикальное хирургическое удаление опухоли. Тактика лечения должна удовлетворять двум основным требованиям: оказывать цитоста-тический (предотвращающий пролиферацию) и цитотоксический (уничтожающий опухолевые клетки) эффекты. Однако химиотерапия прекращает синтез ДНК и клеточное деление по механизмам, общим для всех клеток, отсюда её токсичность и многочисленные побочные эффекты на здоровые, быстро пролиферирующие клетки: фолликулы волос, клетки кроветворной системы и кишечника. Успешность лечения связана с большей чувствительностью неопластических клеток к лекарствам по сравнению с нормальными, неизменёнными клетками и
отражает компромисс между эффективностью в отношении опухоли и токсичностью для здоровых тканей. Лекарственные препараты, используемые в химиотерапии, включают ал-килирующие агенты, повреждающие ДНК, антиметаболиты, которые ингибируют синтез нуклеиновых кислот, антибиотики, гормоны и природные соединения, оказывающие разнообразные эффекты.
Алкилирующие агенты
Алкилирующие агенты образуют связи с основаниями в молекуле ДНК и нарушают репликацию. Большинство алкилирующих агентов (циклофосфан, цисплатин, карбопла-тин и др.) имеют две функциональные группы, каждая из которых может взаимодействовать с основаниями ДНК, образуя внутриклеточные и межцепочечные поперечные сшивки в двойной спирали ДНК. Эти связи могут формироваться на любой стадии клеточного цикла, благодаря чему действие алкилирующих агентов неспецифично в отношении фаз клеточного цикла (рис. 16-17).
Антиметаболиты
Среди антиметаболитов в клинической практике наиболее часто используют метотрек-сат, 5-фторурацил и цитозинарабинозид (см. разд. 10).
Метотрексат - производное фолиевой кислоты, по конкурентному механизму инги-бирующий дигидрофолатредуктазу, активность которой поддерживает необходимую скорость синтеза пуриновых и тимидиновых нуклеотидов в клетках, а в конечном счёте - РНК и ДНК.
5-фторурацил (5-FU) может превращаться в нуклеозидтрифосфат и включаться в РНК. Модифицированная таким образом РНК становится функционально неактивной. Кроме того, из 5-FU может синтезироваться 5-FdУМФ, который образует неактивный тройной комплекс с N5, N10-метилен-Н4-фолатом и тимидилатсинтазой и, нарушая обеспечение клетки тимидиловыми нуклео-тидами, ингибирует синтез ДНК.
Цитозин арабинозид (Ara-C) может фосфори-лироваться до Ara-ЦТФ, который, с одной стороны, служит ингибитором ДНК полиме-
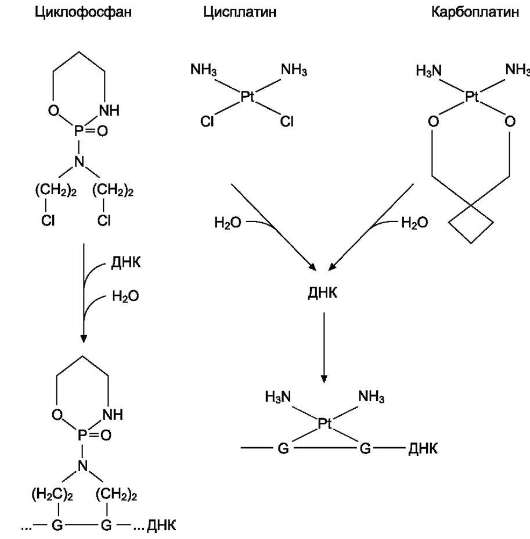
Рис. 16-17. Образование сшивок алкилирующих агентов с остатками гуанина в молекуле ДНК.
разы α, а с другой - частично включается в ДНК. Оба эффекта Ara-C блокируют синтез ДНК в S-фазе клеточного цикла. Антибиотики антрациклинового ряда: доксоруби-цин, карминомицин и рубомицин (см. разд. 4) широко используют в лечении лейкозов и солидных опухолей, таких как рак молочной железы, лёгких и яичников. Эти полициклические соединения оказывают многоплановое действие на структуру и синтез ДНК: «интеркалируют» в молекулы, инициируют и вызывают частичное расщепление двойной спирали; способствуют образованию одно- и двухцепочечных разрывов; связываются с топоизомеразой II, участвующей в образовании репликативной вилки на матрице ДНК. Кроме того, они генерируют свободные радикалы, которые увеличивают число разрывов в молекуле ДНК.
Алкалоиды Vinca - винкристин и винбластин. Растительные алкалоиды, которые связываются с белком микротрубочек тубулином и препят-
ствуют его полимеризации. Их рассматривают как митотические яды, препятствующие продвижению клеток по циклу на стадии метафазы. Алкалоиды Vinca нарушают все виды подвижности клеток и её органелл, связанные с сокращением или релаксацией микротрубочек. Винбластин и винкристин используют в клинической практике при лечении острого лимфобластного лейкоза, рака молочной железы, нейробластомы, сарком мягких тканей, меланомы, опухолей яичника.
Гормональная терапия
Хотя в процессе злокачественной трансформации нарушаются некоторые механизмы, контролирующие рост и дифференцировку тканей, но ряд опухолей всё же не ускользает полностью из-под регуляторного влияния организма, сохраняя рецепторы гормонов и нейромедиато-ров на поверхности или внутри клеток. К ним прежде всего относят опухоли, происходящие
из гормонзависимых тканей: молочной железы, матки, яичников, гипофиза, щитовидной железы, надпочечников, предстательной железы и некоторых других.
Поскольку синтез большинства стероидных гормонов регулируется гипоталамо-гипофи-зарной системой, то блокирование митоген-ного эффекта половых и кортикостероидных гормонов возможно на нескольких стадиях
(рис. 16-18), например: на стадии действия гонадотропин-рилизинг гормона на переднюю долю гипофиза; ингибируя синтез стероидных гормонов на стадии превращения тестостерона в эстрадиол под действием фермента ароматазы; за счёт присоединения антагонистов к рецепторам стероидных гормонов.
Наиболее широко используют тамоксифен (рис. 16-19). Вместе с другими классами стеро-
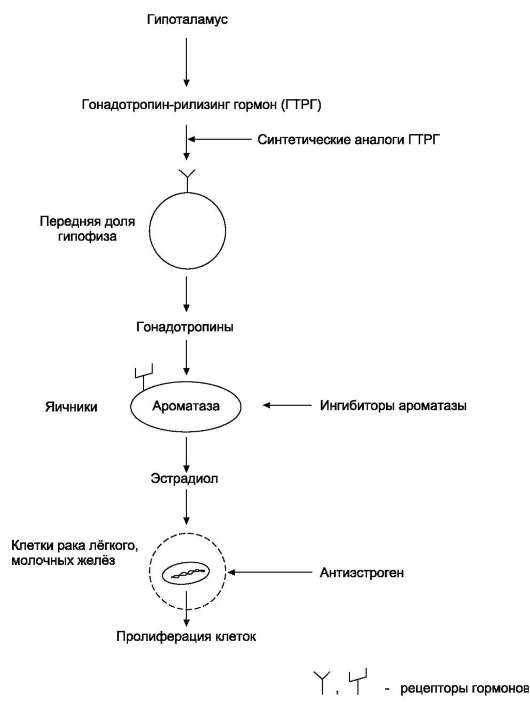
Рис. 16-18. Терапия гормонально-зависимого рака.
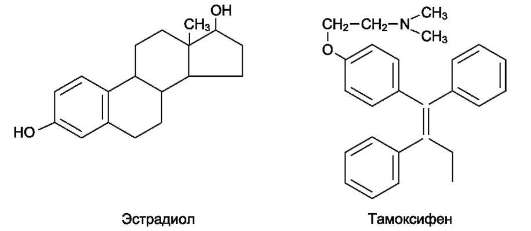
Рис. 16-19. Строение эстрадиола и тамоксифена.
идных гормонов (прогестогенами, глюкокорти-коидами, андрогенами) он очень эффективен в лечении рака молочной железы.
Более половины опухолей молочной железы, яичников и эндометрия содержат рецепторы эстрогенов и прогестерона и поддаются гормонотерапии эстрогенами, антиэстрогенами и прогестинами, а также комбинациями гормонов с цитостатиками. Опухоли, не содержащие рецепторов, малочувствительны к гормонотерапии, поэтому определение уровня рецепторов эстрогенов и прогестинов широко используют для прогнозирования эффективности гормонтера-пии при опухолях молочной железы, яичников и матки.
В. ЛЕКАРСТВЕННАЯ УСТОЙЧИВОСТЬ ОПУХОЛЕВЫХ КЛЕТОК
Несмотря на существенные успехи в области новых препаратов и подходов к лечению опухолей, химиотерапия во многих случаях остаётся малоэффективной. Главным фактором, ограничивающим успешность применения противоопухолевых средств, является лекарственная устойчивость, которая может быть:
• первичной и, следовательно, свойственной злокачественным клеткам до начала лечения определёнными препаратами;
• вторичной, которая развивается в ответ на введение лекарства.
В последнем случае в начале лечения наблюдается положительная динамика, но через некоторое время она исчезает. Высокая изменчивость опухолевых клеток и постоянно действующий отбор на большую злокачественность приводят к тому,
что первоначально с помощью препаратов удаётся уменьшить размер опухоли. Позже оставшаяся субпопуляция клеток становится резистентной сразу к целой группе лекарств, развивается так называемая множественная лекарственная устойчивость (МЛУ), сопровождающаяся рецидивами болезни и метастазами. Так, при лечении, например, винкристином, может возникнуть устойчивость опухолевых клеток не только к самому винкристину, но и к другим препаратам, которые не сходны по структуре и функциям с использованным лекарством, таким как доксо-рубицин и этопозид. Существуют разные механизмы возникновения МЛУ (табл. 16-3).
Некоторые биохимические механизмы лекарственной устойчивости, обнаруженные в опухолевых клетках, вызваны:
• снижением накопления препарата в клетках;
• появлением альтернативных путей метаболизма лекарства;
• изменением структуры клеток-мишеней для данного препарата;
• ослаблением апоптоза - процесса запрограммированной гибели клеток, с помощью которого из организма удаляются изменённые клетки.
Мембранный транспорт и Р-гликопротеины
В ряде случаев причиной МЛУ является почти 1000-кратное увеличение синтеза в опухолевых клетках мембранного белка Р-гликопротеи-на (см. раздел 12). Этот белок действует как энергозависимая помпа, которая осуществляет АТФ-зависимую «откачку» лекарств из клеток и препятствует их внутриклеточному накоплению
Таблица 16-3. Механизмы возникновения множественной лекарственной устойчивости
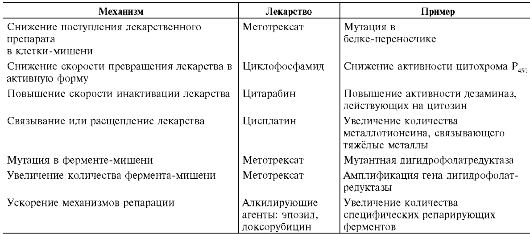
в цитотоксических концентрациях. Возникновение МЛУ вызвано амплификацией и/или точечными мутациями в mdr-генах. Появление МЛУ коррелирует с плохим прогнозом заболевания.
Поиски ингибиторов Р-гликопротеина показали, что блокаторы Са2+-каналов верапамил и циклоспорин могут конкурировать с винкристи-ном за активные центры этого белка и снижать устойчивость клеток к лекарству.
В этой связи практика показала, что лечение с помощью одного лекарства за редким исключением не способно привести к исцелению. Как правило, химиотерапию сочетают с радиотерапией, вызывающей в облучённой ткани индуцированные свободными радикалами разрывы нитей ДНК и апоптоз.
Г. НОВЫЕ НАПРАВЛЕНИЯ В ЛЕЧЕНИИ ОПУХОЛЕЙ
Фотодинамическая терапия стала перспективным направлением лечения опухолей. Принцип терапии состоит в разрушении опухоли в результате введённых в неё веществ, которые переходят в активированное состояние при воздействии на них лазера. При облучении в присутствии молекулярного кислорода генерируются свободные радикалы. Цитотоксический эффект наблюдают главным образом в результате разрушения мембран клеток, а не повреж-
дения ДНК, так как фотодинамическая терапия не вызывает мутаций.
Направленная доставка лекарств в клетки-мишени
основана на разной экспрессии мембранных антигенов (рецепторов ФР, карциноэмбрио-нального антигена и антител) на поверхности опухолевых и нормальных клеток. Количество таких белков на плазматической мембране раковых клеток сильно увеличено по сравнению с нормальными клетками.
Лиганды к этим белкам используют для доставки либо фермента, катализирующего превращение пролекарства на поверхности опухолевой клетки в активное лекарство, либо цитотоксического препарата, который благодаря этим белкам поступает
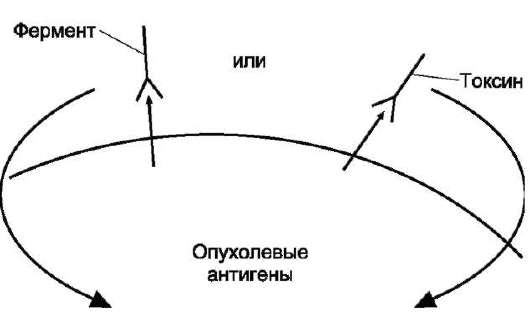
Рис. 16-20. Использование моноклональных антител для доставки лекарств или токсинов в опухолевые клетки.
в клетку-мишень по механизму эндоцитоза, не вызывая эффекта МЛУ (рис. 16-20).
Подавление ангиогенеза или образования новых кровеносных сосудов приводит к нарушению роста опухоли. Пролиферацию эндотелиальных клеток капилляров можно ингибировать, воздействуя недавно открытыми ингибиторами ангиогенеза: ангиостатином или тромбоспондином.
Перспективными лекарствами могут оказаться синтетические пептиды, являющиеся ингибиторами металлопротеаз. С помощью таких соединений в опытах на животных удавалось ингибировать рост и метастазирование рака прямой кишки.
Генная терапия представляет собой направление по использованию генов для лечения наследственных и опухолевых заболеваний (см. раздел 4). Такой способ лечения становится всё более реальным благодаря достижениям генной инженерии, которые позволяют получать реком-бинантные ДНК, содержащие «лечебный» ген. Основная трудность состоит в разработке метода
транспорта импортируемых генов в организм больного.
Клинические испытания проходит лечение больных с меланомой и раком прямой кишки, в ходе которого у пациента извлекают опухоль или клетки костного мозга и облучают. В облучённые клетки вводят «лечебный» ген (например, ген интерлейкина-2 или фактора некроза опухолей) и реимплантируют их больному. Продукты «лечебных» генов увеличивают иммуногенность опухоли и способствуют уничтожению как самой опухоли, так и метастазов.
Применяют также введение в организм вирусов в качестве векторов «лечебных» генов. Чаще всего используют аденовирусные и ретровирус-ные конструкции, которые легко включаются в ДНК трансформированных клеток. Вирусы лишают генетического материала, существенного для репродукции вирусов и инактивации Р53, и на его место вводят «лечебный» ген.
Всё вышесказанное даёт надежду на то, что в ближайшие годы человечество сможет эффективно бороться с онкологическими заболеваниями за жизнь и здоровье больных.