Биохимия: учебник для вузов/ под ред. Е.С.Северина - 5-е изд., - 2009. - 768 с.
|
|
|
|
РАЗДЕЛ 13 МЕТАБОЛИЗМ ГЕМА И ОБМЕН ЖЕЛЕЗА
Гем является простетической группой многих белков: гемоглобина, миоглобина, цитохромов митохондриальной ЦПЭ, цитохрома Р450, участвующего в микросомальном окислении. Ферменты каталаза, пероксидаза, цитохромоксидаза содержат гем в качестве кофермента.
Все клетки организма имеют гемсодержащие белки, поэтому синтез гема идёт во всех клетках, за исключением эритроцитов, не имеющих, как известно, белоксинтезирующей системы.
При распаде гема в клетках РЭС образуется жёлчный пигмент билирубин. Дальнейший катаболизм билирубина в печени, кишечнике и почках приводит к образованию конечных продуктов распада гема стеркобилина и уробилина, содержащихся, соответственно, в кале и моче. Железо, освобождающееся при распаде гема, снова используется для синтеза железосодержащих белков.
I. СТРОЕНИЕ И БИОСИНТЕЗ ГЕМА а. строение гема
Гем состоит из иона двухвалентного железа и порфирина (рис. 13-1). В основе структуры пор-фиринов находится порфин. Порфин представляет собой четыре пиррольных кольца, связанных между собой метеновыми мостиками (рис. 13-1). В зависимости от структуры заместителей в кольцах пирролов различают несколько типов порфиринов: протопорфирины, этиопорфи-рины, мезопорфирины и копропорфирины. Протопорфирины - предшественники всех других типов порфиринов.
Гемы разных белков могут содержать разные типы порфиринов (см. раздел 6). В геме гемоглобина находится протопорфирин IX, который имеет 4 метильных, 2 винильных радикала и 2 остатка пропионовой кислоты. Железо в геме находится в восстановленном состоянии (Fе+2) и связано двумя ковалентными и двумя координационными связями с атомами азота пиррольных колец. При окислении железа гем превращается
в гематин (Fe3+). Hаибольшее количество гема содержат эритроциты, заполненные гемоглобином, мышечные клетки, имеющие миоглобин, и клетки печени из-за высокого содержания в них цитохрома Р450.
б. биосинтез гема
Гем синтезируется во всех тканях, но с наибольшей скоростью в костном мозге и печени (рис. 13-2). В костном мозге гем необходим для синтеза гемоглобина в ретикулоцитах, в гепато-цитах - для образования цитохрома Р450.
Первая реакция синтеза гема - образование 5-аминолевулиновой кислоты из глицина и сукцинил-КоА (рис. 13-3) идёт в матриксе митохондрий, где в ЦТК образуется один из субстратов этой реакции - сукцинил-КоА. Эту реакцию катализирует пиридоксальзависимый фермент 5-аминолевулинатсинтаза.
Из митохондрий 5-аминолевулиновая кислота поступает в цитоплазму. В цитоплазме проходят промежуточные этапы синтеза гема: соединение 2 молекул 5-аминолевулиновой кислоты в молекулу порфобилиногена (рис. 13-4), дезаминирование порфобилиногена с образованием гидроксиметилбилана, ферментативное превращение гидроксиметилбилана в молекулу уропорфобилиногена III, декар-боксилирование последнего с образованием копропорфириногена III. Гидроксиметилбилан может также неферментативно превращаться в уропорфириноген I, который декарбоксилиру-ется в копропорфириноген I. Из цитоплазмы копропорфириноген III опять поступает в митохондрии, где проходят заключительные реакции синтеза гема. В результате двух последовательных окислительных реакций коп-ропорфириноген III превращается в протопор-фириноген IX, а протопорфириноген IX - в протопорфирин IX. Фермент феррохелатаза, присоединяя к протопорфирину IX двухвалентное железо, превращает его в гем (рис. 13-2). Источником железа для синтеза гема служит депонирующий железо белок ферритин. Син-
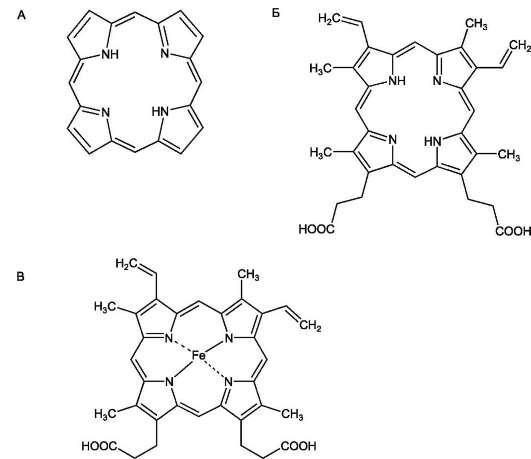
Рис. 13-1. Строение порфина (А), протопорфирина IX (Б) и гема гемоглобина (В). Порфин - циклическая структура, состоящая из четырёх пиррольных колец, связанных между собой метеновыми мостиками. Прото-порфирин IX имеет четыре метильных, два винильных радикала и два остатка пропионовой кислоты. В геме гемоглобина Fe2+ образует две ковалентные и две координационные связи с атомами азота пиррольных колец протопорфирина IX.
тезированный гем, соединяясь с α- и β-по-липепептидными цепями глобина, образует гемоглобин. Гем регулирует синтез глобина: при снижении скорости синтеза гема синтез глобина в ретикулоцитах тормозится.
В. РЕГУЛЯЦИЯ БИОСИНТЕЗА ГЕМА
Регуляторную реакцию синтеза гема катализирует пиридоксальзависимый фермент 5-аминолевулинатсинтаза. Скорость реакции регулируется аллостерически и на уровне трансляции фермента.
Аллостерическим ингибитором и корепрессо-ром синтеза 5-аминолевулинатсинтазы является гем (рис. 13-5).
В ретикулоцитах синтез этого фермента на этапе трансляции регулирует железо. На участке инициации мРHК, кодирующей фермент, имеется последовательность нуклеотидов, образующая шпилечную петлю, которая называется железочувствительным элементом (от англ. iron-responsive element, IRE) (рис. 13-6).
При высоких концентрациях железа в клетках оно образует комплекс с остатками цисте-ина регуляторного железосвязывающего белка. Взаимодействие железа с регуляторным желе-зосвязывающим белком вызывает снижение сродства этого белка к IRE-элементу мРHК, кодирующей 5-аминолевулинатсинтазу, и продолжение трансляции (рис. 13-6, А). При низких концентрациях железа железосвязывающий
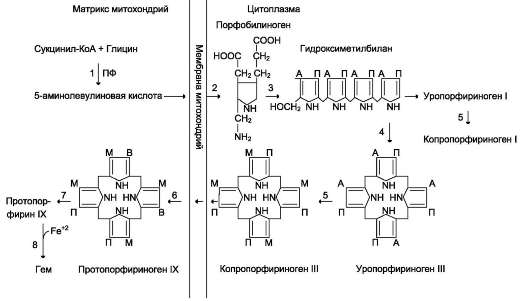
Рис. 13-2. Синтез гема. Цифрами на схеме указаны ферменты: 1 - 5-аминолевулинатсинтаза; 2 - 5-аминоле-вулинатдегидратаза; 3 - порфобилиногендезаминаза; 4 - уропорфириноген III косинтаза; 5 - уропорфирино-гендекарбоксилаза; 6 - копропорфириноген III оксидаза; 7 - протопорфириногеноксидаза; 8 - феррохелатаза. Буквами обозначены заместители в пиррольных кольцах: М - метил, В - винил, П - остатки пропионовой кислоты, А - ацетил, ПФ - пиридоксальфосфат. Донором железа служит депонирующий железо в клетках белок ферритин.
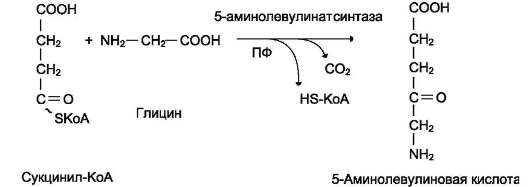
Рис. 13-3. Реакция образования 5-аминолевулиновой кислоты.
белок присоединяется к железочувствительному элементу, находящемуся на 5'-нетранслируемом конце мРНК, и трансляция 5-аминолевулинат-синтазы тормозится (рис. 13-6, Б).
5-Аминолевулинатдегидратаза также аллостери-чески ингибируется гемом, но так как активность этого фермента почти в 80 раз превышает активность 5-аминолевулинатсинтазы, то это не имеет большого физиологического значения.
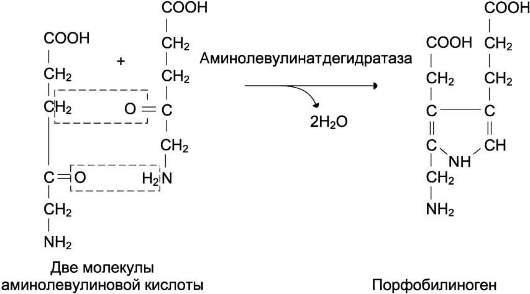
Рис. 13-4. Реакция образования порфобилиногена.
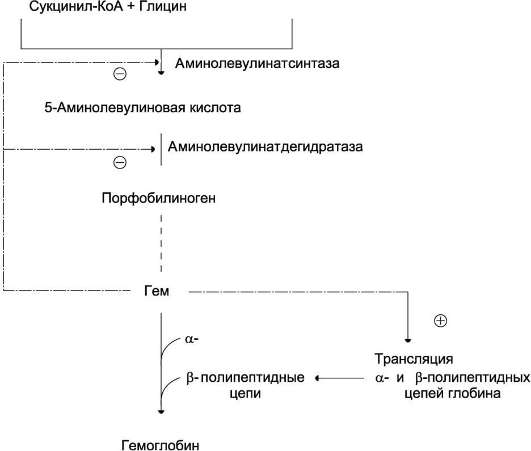
Рис. 13-5. Регуляция синтеза гема и гемоглобина. Гем по принципу отрицательной обратной связи ингибирует 5-аминолевулинатсинтазу и 5-аминолевулинатдегидратазу и является индуктором трансляции α- и β-цепей гемо глобина.
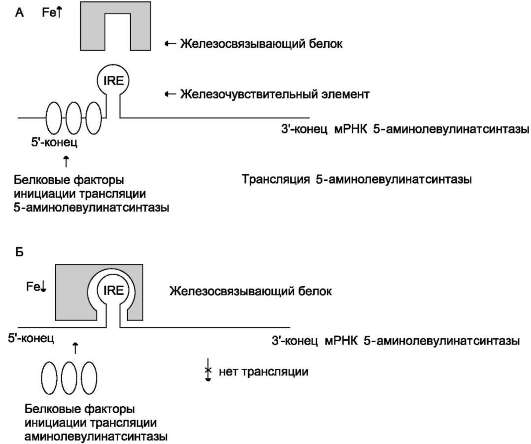
Рис. 13-6. Регуляция синтеза аминолевулинатсинтазы. А - при высокой концентрации железа в ретикулоцитах оно присоединяется к железосвязывающему белку и снижает сродство этого белка к железочувствительному элементу (IRE) матричной РНК, кодирующей 5-аминолевулинатсинтазу. Белковые факторы инициации трансляции связываются с мРНК и инициируют трансляцию 5-аминолевулинатсинтазы. Б - при низком содержании железа в ретикулоцитах железосвязывающий белок обладает высоким сродством к IRE и взаимодействует с ним. Белковые факторы инициации трансляции не могут присоединиться к мРНК, и трансляция прекращается.
Дефицит пиридоксальфосфата и лекарственные препараты, которые являются его структурными аналогами, снижают активность 5-амино-левулинатсинтазы.
Г. НАРУШЕНИЯ БИОСИНТЕЗА ГЕМА. ПОРФИРИИ
Hаследственные и приобретённые нарушения синтеза гема, сопровождающиеся повышением содержания порфириногенов, а также продуктов их окисления в тканях и крови и появлением их в моче, называют порфириями («порфирин» в переводе с греч. означает пурпурный). Моча больных имеет красный цвет.
Hаследственные порфирии обусловлены генетическими дефектами ферментов, участвующих
в синтезе гема, за исключением 5-аминолевули-натсинтазы. При этих заболеваниях отмечают снижение образования гема. Поскольку гем - ал-лостерический ингибитор 5-аминолевулинатсин-тазы, то активность этого фермента повышается, и это приводит к накоплению промежуточных продуктов синтеза гема - 5-аминолевулиновой кислоты и порфириногенов.
В зависимости от основной локализации патологического процесса различают печёночные и эритропоэтические наследственные порфирии. Эритропоэтические порфирии сопровождаются накоплением порфиринов в нормобластах и эритроцитах, а печёночные - в гепатоцитах.
При тяжёлых формах порфирий наблюдают нейропсихические расстройства, нарушения функций РЭС, повреждения кожи. Порфири-ногены не окрашены и не флуоресцируют, но на свету они легко превращаются в порфирины. Последние проявляют интенсивную красную флуоресценцию в ультрафиолетовых лучах. В коже на солнце в результате взаимодействия с порфиринами кислород переходит в синглетное состояние. Синглетный кислород вызывает ускорение ПОЛ клеточных мембран и разрушение клеток, поэтому порфирии часто сопровождаются фотосенсибилизацией и изъязвлением открытых участков кожи. Нейропсихические расстройства при порфириях связаны с тем, что 5-аминолевулинат и порфириногены являются нейротоксинами.
Иногда при лёгких формах наследственных порфирий заболевание может протекать бессимптомно, но приём лекарств, являющихся индукторами синтеза 5-аминолевулинатсинтазы, может вызвать обострение болезни. Индукторами синтеза 5-аминолевулинатсинтазы являются такие известные лекарства, как сульфанил-ами-ды, барбитураты, диклофенак, вольтарен, стероиды, гестагены. В некоторых случаях симптомы болезни не проявляются до периода полового созревания, когда повышение образования β-стероидов вызывает индукцию синтеза 5-ами-нолевулинатсинтазы. Порфирии наблюдают и при отравлениях солями свинца, так как свинец ингибирует 5-аминолевулинатдегидратазу и феррохелатазу. Некоторые галогенсодержащие гербициды и инсектициды являются индукторами синтеза 5-аминолевулинатсинтазы, поэтому попадание их в организм сопровождается симптомами порфирии.
II. ОБМЕН ЖЕЛЕЗА
В гемсодержащих белках железо находится в составе гема. В негемовых железосодержащих белках железо непосредственно связывается с белком. К таким белкам относят трансфер-рин, ферритин, окислительные ферменты рибонуклеотидредуктазу и ксантиноксидазу, железофлавопротеины NADH-дегидрогеназу и сукцинатдегидрогеназу.
В организме взрослого человека содержится 3-4 г железа, из которых только около 3,5 мг
находится в плазме крови. Гемоглобин имеет примерно 68% железа всего организма, ферри-тин - 27%, миоглобин - 4%, трансферрин - 0,1%, На долю всех содержащих железо ферментов приходится всего 0,6% железа, имеющегося в организме. Источниками железа при биосинтезе железосодержащих белков служат железо пищи и железо, освобождающееся при постоянном распаде эритроцитов в клетках печени и селезёнки.
В нейтральной или щелочной среде железо находится в окисленном состоянии - Fe3+, образуя крупные, легко агрегирующие комплексы с ОН-, другими анионами и водой. При низких значениях рН железо восстанавливается и легко диссоциирует. Процесс восстановления и окисления железа обеспечивает его перераспределение между макромолекулами в организме. Ионы железа обладают высоким сродством ко многим соединениям и образуют с ними хелатные комплексы, изменяя свойства и функции этих соединений, поэтому транспорт и депонирование железа в организме осуществляют особые белки. В клетках железо депонирует белок ферритин, в крови его транспортирует белок трансферрин.
а. всасывание железа в кишечнике
В пище железо в основном находится в окисленном состоянии (Fe3+) и входит в состав белков или солей органических кислот. Освобождению железа из солей органических кислот способствует кислая среда желудочного сока. Наибольшее количество железа всасывается в двенадцатиперстной кишке. Аскорбиновая кислота, содержащаяся в пище, восстанавливает железо и улучшает его всасывание, так как в клетки слизистой оболочки кишечника поступает только Fe2+. В суточном количестве пищи обычно содержится 15-20 мг железа, а всасывается только около 10% этого количества. Организм взрослого человека теряет около 1 мг железа в сутки.
Количество железа, которое всасывается в клетки слизистой оболочки кишечника, как правило, превышает потребности организма. Поступление железа из энтероцитов в кровь зависит от скорости синтеза в них белка апоферритина. Апоферритин «улавливает» железо в энтероцитах и превращается в ферритин, который остаётся в энтероцитах. Таким способом снижается поступ-
ление железа в капилляры крови из клеток кишечника. Когда потребность в железе невелика, скорость синтеза апоферритина повышается (см. ниже «Регуляция поступления железа в клетки»). Постоянное слущивание клеток слизистой оболочки в просвет кишечника освобождает организм от излишков железа. При недостатке железа в организме апоферритин в энтероцитах почти не синтезируется. Железо, поступающее из энтероцитов в кровь, транспортирует белок плазмы крови трансферрин (рис. 13-7).
Б. ТРАНСПОРТ ЖЕЛЕЗА В ПЛАЗМЕ КРОВИ И ЕГО ПОСТУПЛЕНИЕ В КЛЕТКИ
В плазме крови железо транспортирует белок трансферрин. Трансферрин - гликопротеин, который синтезируется в печени и связывает только окисленное железо (Fe3+). Поступающее в кровь железо окисляет фермент ферроксидаза, известный как медьсодержащий белок плазмы крови церулоплазмин. Одна молекула трансфер-рина может связать один или два иона Fe3+ , но одновременно с анионом СО32- с образованием комплекса трансферрин-2 (Fе3+-СО32-). В норме трансферрин крови насыщен железом приблизительно на 33%.
Трансферрин взаимодействует со специфическими мембранными рецепторами клеток.
В результате этого взаимодействия в цитозоле клетки образуется комплекс Са2+-кальмодулин-ПКС, который фосфорилирует рецептор транс-феррина и вызывает образование эндосомы. АТФ-зависимый протонный насос, находящийся в мембране эндосомы, создаёт кислую среду внутри эндосомы. В кислой среде эндосомы железо освобождается из трансферрина. После этого комплекс рецептор-апотрансферрин возвращается на поверхность плазматической мембраны клетки. При нейтральном значении рН внеклеточной жидкости апотрансферрин изменяет свою конформацию, отделяется от рецептора, выходит в плазму крови и становится способным вновь связывать ионы железа и включаться в новый цикл его транспорта в клетку. Железо в клетке используется для синтеза железосодержащих белков или депонируется в белке ферритине.
Ферритин - олигомерный белок с молекулярной массой 500 кД. Он состоит из тяжёлых (21 кД) и лёгких (19 кД) полипептидных цепей, составляющих 24 протомера. Разный набор протомеров в олигомере ферритина определяет образование нескольких изоформ этого белка в разных тканях. Ферритин представляет собой полую сферу, внутри которой может содержаться до 4500 ионов трёхвалентного железа, но обычно содержится менее 3000. Тяжёлые цепи
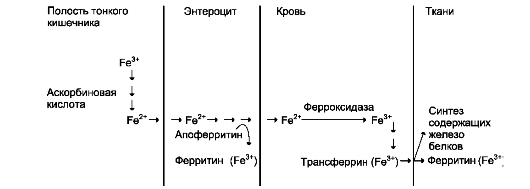
Рис. 13-7. Поступление экзогенного железа в ткани. В полости кишечника железо освобождается из белков и солей органических кислот пищи. Усвоению железа способствует аскорбиновая кислота, восстанавливающая железо. В клетках слизистой оболочки кишечника избыток поступившего железа соединяется с белком апофер-ритином с образованием ферритина, при этом ферритин окисляет Fe2+ в Fe3+. Поступление железа из клеток слизистой оболочки кишечника в кровь сопровождается окислением железа ферментом сыворотки крови фер-роксидазой. В крови Fe3+ транспортирует белок сыворотки крови трансферрин. В тканях Fe2+ используется для синтеза железосодержащих белков или депонируется в ферритине.
ферритина окисляют Fe2+ в Fe3+. Железо в виде гидроксидфосфата находится в центре сферы, оболочка которой образована белковой частью молекулы. Оно поступает внутрь и освобождается наружу через каналы, пронизывающие белковую оболочку апоферритина, но железо может откладываться и в белковой части молекулы ферритина. Ферритин содержится почти во всех тканях, но в наибольшем количестве в печени, селезёнке и костном мозге. Незначительная часть ферритина экскретируется из тканей в плазму крови. Поскольку поступление ферри-тина в кровь пропорционально его содержанию в тканях, то концентрация ферритина в крови - важный диагностический показатель запасов железа в организме при железодефицитной анемии. Метаболизм железа в организме представлен на рис. 13-8.
В. РЕГУЛЯЦИЯ ПОСТУПЛЕНИЯ ЖЕЛЕЗА В КЛЕТКИ
Содержание железа в клетках определяется соотношением скоростей его поступления, использования и депонирования и контролируется двумя молекулярными механизмами. Скорость поступления железа в неэритроидные клетки зависит от количества белков-рецепторов трансферрина в их мембране. Избыток железа в клетках депонирует ферритин. Синтез апофер-ритина и рецепторов трансферрина регулируется на уровне трансляции этих белков и зависит от содержания железа в клетке.
На нетранслируемом 3'-конце мРНК рецептора трансферрина и на нетранслируемом 5'-конце мРНК апоферритина имеются шпилечные петли - железочувствительные элементы IRE (рис. 13-9 и 13-10). Причём мРНК рецептора трансфер-
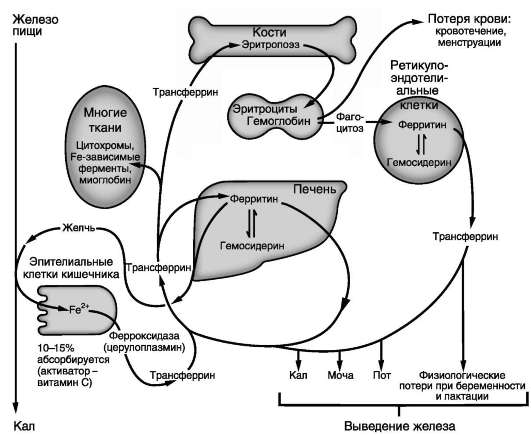
Рис. 13-8. Метаболизм железа в организме.
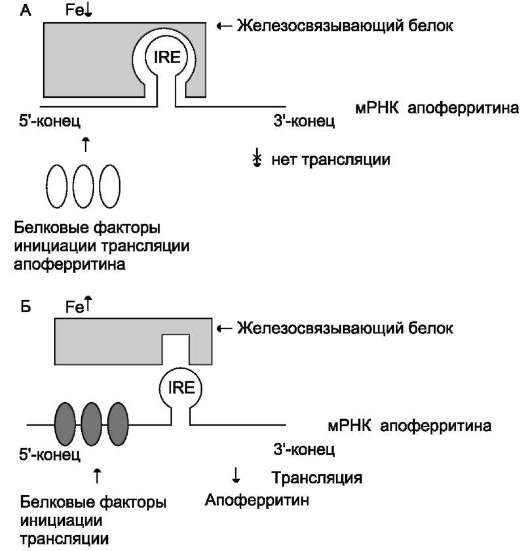
Рис. 13-9. Регуляция синтеза апоферритина. А - при снижении содержания железа в клетке железосвязывающий белок обладает высоким сродством к IRE и взаимодействует с ним. Это препятствует присоединению белковых факторов инициации трансляции к мРНК, кодирующей апоферритин, и синтез апоферритина прекращается; Б - при повышении содержания железа в клетке оно взаимодействует с железосвязывающим белком, в результате чего снижается сродство этого белка к IRE. Белковые факторы инициации трансляции присоединяются к мРНК, кодирующей апоферритин, и инициируют трансляцию апоферритина.
рина имеет 5 петель, а мРНК апоферритина - только 1.
Эти участки мРНК могут взаимодействовать с регуляторным IRE-связывающим белком. При низких концентрациях железа в клетке IRE-связывающий белок соединяется с IRE мРНК апоферритина и препятствует присоединению белковых факторов инициации трансляции (рис. 13-9, А). В результате этого снижаются скорость трансляции апоферри-тина и его содержание в клетке. Вместе с тем при низких концентрациях железа в клетке IRE-связывающий белок связывается с желе-зочувствительным элементом мРНК рецептора трансферрина и предотвращает её разрушение ферментом РНК-азой (рис. 13-10, А). Это вызывает увеличение количества рецепторов
трансферрина и ускорение поступления железа в клетки.
При повышении содержания железа в клетке в результате его взаимодействия с IRE-связывающим белком происходит окисление SH-групп активного центра этого белка и снижение сродства к железочувствительным элементам мРНК. Это приводит к двум последствиям:
• во-первых, ускоряется трансляция апоферритина (рис. 13-9, Б);
• во-вторых, IRE-связывающий белок освобождает шпилечные петли мРНК рецептора трансферрина, и она разрушается ферментом РНК-азой, в результате снижается скорость синтеза рецепторов трансферрина (рис. 1310, Б). Ускорение синтеза апоферритина и торможение синтеза рецепторов транс-
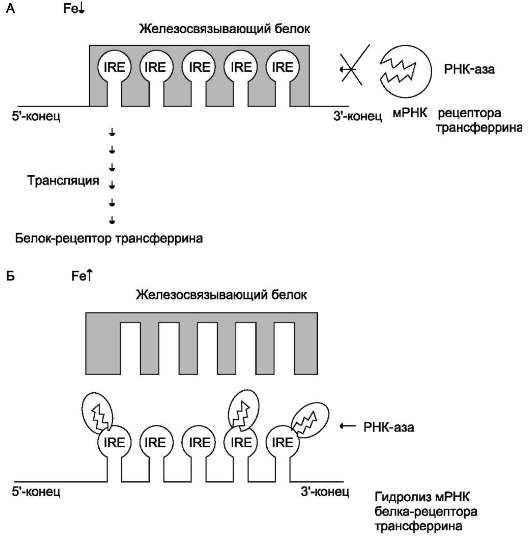
Рис. 13-10. Регуляция синтеза рецептора трансферрина. А - при низком содержании железа в клетке железочувствительный белок обладает высоким сродством к IRE мРНК, кодирующей белок-рецептор транс-феррина. Присоединение железосвязывающего белка к IRE мРНК предотвращает её разрушение РНК-азой и синтез белка-рецептора трансферрина продолжается; Б - При высоком содержании железа в клетке сродство железосвязывающего белка к IRE снижается, и мРНК становится доступной для действия РНК-азы, которая её гидролизует. Разрушение мРНК ведёт к снижению синтеза белка-рецептора трансферрина.
феррина вызывают снижение содержания
железа в клетке. В целом эти механизмы регулируют содержание железа в клетках и его использование для синтеза железосодержащих белков.
Г. НАРУШЕНИЯ МЕТАБОЛИЗМА ЖЕЛЕЗА
Железодефицитная анемия может наблюдаться при повторяющихся кровотечениях, беременности, частых родах, язвах и опухолях
ЖКТ, после операций на ЖКТ. При желе-зодефицитной анемии уменьшается размер эритроцитов и их пигментация (гипохромные эритроциты малых размеров). В эритроцитах уменьшается содержание гемоглобина, понижается насыщение железом трансферрина, а в тканях снижается концентрация ферритина. Причина этих изменений - недостаток железа в организме, вследствие чего снижается синтез гема и ферритина в неэритроидных тканях и гемоглобина в эритроидных клетках.
Гемохроматоз. Когда
количество железа в клетках превышает объём ферритинового депо, железо
откладывается в белковой части молекулы ферритина. В результате
образования таких аморфных отложений избыточного железа ферритин
превращается в гемосидерин . Гемо-сидерин плохо растворим в воде и
содержит до 37% железа. Накопление гранул гемосидерина в печени,
поджелудочной железе, селезёнке приводит к повреждению этих органов -
гемохроматозу. Гемохроматоз может быть обусловлен наследственным
увеличением всасывания железа в кишечнике, при этом содержание железа в
организме больных может достигать
III. КАТАБОЛИЗМ ГЕМОГЛОБИНА
Эритроциты имеют короткое время жизни (примерно 120 дней). При физиологических условиях в организме взрослого человека разрушается около 1-2х10и эритроцитов в сутки. Их катаболизм происходит главным образом в ретикулоэндотелиальных клетках селезёнки, лимфатических узлов, костного мозга и печени. При старении эритроцитов снижается содержание сиаловых кислот в составе гликопротеинов плазматической мембраны. Изменённые углеводные компоненты гликопротеинов мембран эритроцитов связываются рецепторами клеток РЭС, и эритроциты «погружаются» в них эн-доцитозом. Распад эритроцитов в этих клетках начинается с распада гемоглобина на гем и глобин и последующего гидролиза ферментами лизосом белковой части гемоглобина.
А. КАТАБОЛИЗМ ГЕМА
Первая реакция катаболизма гема происходит при участии NADРН-зависимого ферментативного комплекса гемоксигеназы. Ферментная система локализована в мембране ЭР, в области электронтранспортных цепей микросомального окисления. Фермент катализирует расщепление связи между двумя пиррольными кольцами, содержащих винильные остатки, - таким образом, раскрывается структура кольца (рис. 13-11). В ходе реакции образуются линейный тетрапир-рол - биливердин (пигмент жёлтого цвета) и монооксид углерода (СО), который получается из углерода метениловой группы. Гем индуцирует транскрипцию гена гемоксигеназы, абсолютно специфичной по отношению к гему.
Ионы
железа, освободившиеся при распаде гема, могут быть использованы для
синтеза новых молекул гемоглобина или для синтеза других
железосодержащих белков. Биливердин восстанавливается до билирубина
NADРН-зависимым ферментом биливердинредуктазой. Билирубин
образуется не только при распаде гемоглобина, но также при катаболизме
других гемсодержащих белков, таких как цитохромы и миоглобин. При
распаде
Б. МЕТАБОЛИЗМ БИЛИРУБИНА
Билирубин, образованный в клетках РЭС (селезёнки и костного мозга), плохо растворим в воде, по крови транспортируется в комплексе с белком плазмы крови альбумином. Эту форму билирубина называют неконъюгированным билирубином. Каждая молекула альбумина связывает 2 (или даже 3) молекулы билирубина, одна из которых связана с белком более прочно (более высокое сродство), чем другие. При сдвиге рН крови в кислую сторону (повышение концентрации кетоновых тел, лактата) изменяются заряд, конформация альбумина, снижается сродство к билирубину. Поэтому билирубин, связанный с альбумином непрочно, может вытесняться из центров связывания и образовывать комплексы с коллагеном межклеточного матрикса и липидами мембран. Ряд лекарственных соединений конкурирует с билирубином за
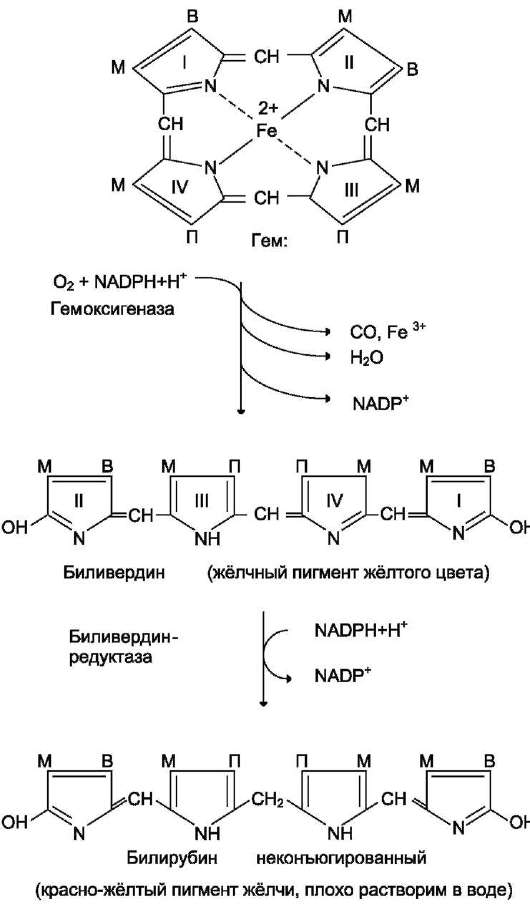
Рис. 13-11. Распад гема. М - (-СН3) - метильная группа; В - (-СН=СН2) - винильная группа; П - (-СН2-СН2-СООН) - остаток пропионовой кислоты. В ходе реакции одна метильная группа превращается в окись углерода и, таким образом, раскрывается структура кольца. Образованный биливердин под действием биливердинредуктазы превращается в билирубин.
высокоаффинный, имеющий высокое сродство центр альбумина.
Поглощение билирубина паренхиматозными клетками печени
Комплекс «альбумин-билирубин», доставляемый с током крови в печень, на поверх-
ности плазматической мембраны гепатоцита диссоциирует. Высвобожденный билирубин образует временный комплекс с липидами плазматической мембраны. Облегчённая диффузия билирубина в гепатоциты осуществляется двумя типами белков-переносчиков: лигандина (он транспортирует основное количество били-
рубина) и протеина Z. Активность поглощения билирубина гепатоцитом зависит от скорости его метаболизма в клетке.
Лигандин и протеин Z обнаружены также в клетках почек и кишечника, поэтому при недостаточности функции печени они способны компенсировать ослабление процессов детокси-кации в этом органе.
Конъюгация билирубина в гладком ЭР
В гладком ЭР гепатоцитов к билирубину присоединяются остатки глюкуроновой кислоты - реакции конъюгации. Билирубин имеет 2 карбоксильные группы, поэтому может соединяться с 2 молекулами глюкуроновой кислоты, образуя хорошо растворимый в воде конъюгат - ди-глюкуронид билирубина (конъюгированный, или прямой, билирубин) (рис. 13-12).
Донором глюкуроновой кислоты служит УДФ-глюкуронат. Специфические ферменты, УДФ-глюкуронилтрансферазы (уридиндифосфоглю-куронилтрансферазы) катализируют образование моно- и диглюкуронидов билирубина (рис. 13-13). Индукторами синтеза УДФ-глюкуронилтрансфераз служат некоторые лекарственные препараты, например, фенобарбитал (см. раздел 12).
Секреция билирубина в жёлчь
Секреция конъюгированного билирубина в жёлчь идёт по механизму активного транспорта, т.е. против градиента концентрации. Активный транспорт является, вероятно, скорость-лими-тирующей стадией всего процесса метаболизма билирубина в печени. В норме диглюкуронид
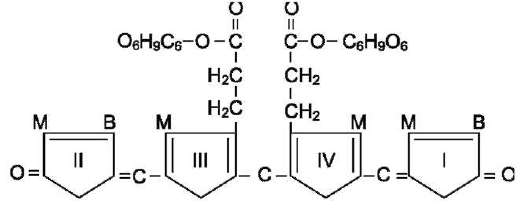
Рис. 13-12. Структура билирубиндиглюкуронида (конъюгированный, «прямой» билирубин). Глюку-роновая кислота присоединяется эфирной связью к двум остаткам пропионовой кислоты с образованием ацилглюкуронида.
билирубина - главная форма экскреции билирубина в жёлчь, однако не исключается присутствие небольшого количества моно-глюкуронида. Транспорт конъюгированного билирубина из печени в жёлчь активируется теми же лекарствами, которые способны индуцировать конъюгацию билирубина. Таким образом, можно сказать, что скорость конъюгации билирубина и активный транспорт билирубинглюкуронида из гепатоцитов в жёлчь строго взаимосвязаны (рис. 13-14).
В. КАТАБОЛИЗМ БИЛИРУБИНДИГЛЮКУРОНИДА
В кишечнике поступившие билирубинглюку-рониды гидролизуются специфическими бактериальными ферментами β-глюкуронидазами, которые гидролизуют связь между билирубином и остатком глюкуроновой кислоты. Освобо-
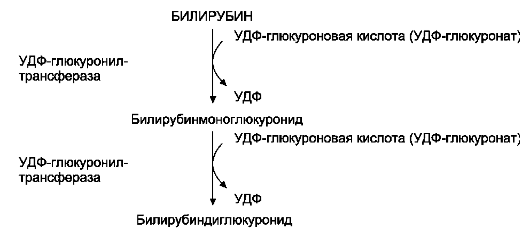
Рис. 13-13. Образование билирубиндиглюкуронида.
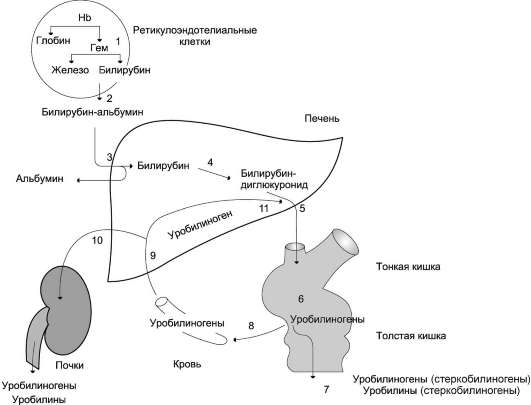
Рис. 13-14. Билирубин-уробилиногеновый цикл в печени. 1 - катаболизм Hb в ретикулоэндотелиальных клетках костного мозга, селезёнки, лимфатических узлов; 2 - образование транспортной формы комплекса билирубин-альбумин; 3 - поступление билирубина в печень; 4 - образование билирубинглюкуронидов;
5 - секреция билирубина в составе жёлчи в кишечник;
6 - катаболизм билирубина под действием кишечных бактерий; 7 - удаление уробилиногенов с калом; 8 - всасывание уробилиногенов в кровь; 9 - усвоение уробилиногенов печенью; 10 - поступление части уробилиногенов в кровь и выделение почками с мочой; 11 - небольшая часть уробилиногенов секретируется в жёлчь.
дившийся в ходе этой реакции билирубин под действием кишечной микрофлоры восстанавливается с образованием группы бесцветных тетрапиррольных соединений - уробилиногенов (рис. 13-15).
В подвздошной и толстой кишках небольшая часть уробилиногенов снова всасывается, попадает с кровью воротной вены в печень. Основная часть уробилиногена из печени в составе жёлчи выводится в кишечник и выделяется с
калом из организма, часть уробилиногена из печени поступает в кровь и удаляется с мочой в форме уробилина (рис. 13-14). В норме большая часть бесцветных уробилиногенов, образующихся в толстой кишке, под действием кишечной микрофлоры окисляется в прямой кишке до пигмента коричневого цвета уробилина и удаляется с калом. Цвет кала обусловлен присутствием уробилина.
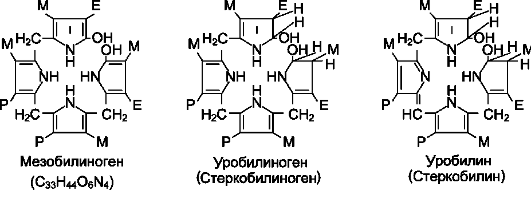
Рис. 13-15. Структура некоторых жёлчных пигментов. Мезобилиноген - промежуточный продукт катаболизма билирубина в кишечнике.
iv. диагностическое значение
определения концентрации билирубина в биологических жидкостях человека
В настоящее время для определения содержания билирубина в сыворотке (плазме) крови используют предложенный в
В нормальном состоянии концентрация общего билирубина в плазме составляет 0,3-1 мг/дл (1,7-17 мкмоль/л), 75% от общего количества билирубина находится в неконъюгированной форме (непрямой билирубин). В клинике ко-нъюгированный билирубин называют прямым, потому что он водорастворим и может быстро взаимодействовать с диазореагентом, образуя соединение розового цвета, - это и есть прямая реакция Ван дер Берга. Неконъюгированньш билирубин гидрофобен, поэтому в плазме крови содержится в комплексе с альбумином и не реагирует с диазореактивом до тех пор, пока не добавлен органический растворитель, например этанол, который осаждает альбумин. Неконъ-югированный билирубин, взаимодействующий с азокрасителем только после осаждения белка, называют непрямым билирубином.
Когда содержание билирубина в крови превышает норму, говорят о гипербилирубинемии. В зависимости от того, концентрация какого типа билирубина повышена в плазме - не-конъюгированного или конъюгированного, - гипербилирубинемию классифицируют как не-конъюгированную и конъюгированную.
У больных с печёночно-клеточной патологией, сопровождающейся длительным повышением
концентрации конъюгированного билирубина, в крови обнаруживают третью форму плазменного билирубина, при котором билирубин ковалентно связан с альбумином, и поэтому его невозможно отделить обычным способом. В некоторых случаях до 90% общего содержания билирубина крови может находиться в этой форме.
А. ЖЕЛТУХИ
Причинами гипербилирубинемии могут быть увеличение образования билирубина, превышающее способность печени экскретировать его, или повреждение печени, приводящее к нарушению секреции билирубина в жёлчь в нормальных количествах. Гипербилирубинемию отмечают также при закупорке желчевыводящих протоков печени.
Во всех случаях содержание общего билирубина в крови повышается. При достижении определённой концентрации он диффундирует в ткани, окрашивая их в жёлтый цвет. Пожелтение тканей из-за отложения в них билирубина называют желтухой. Клинически желтуха может не проявляться до тех пор, пока концентрация билирубина в плазме крови не превысит верхний предел нормы более чем в 2,5 раза, т.е. не станет выше 50 мкмоль/л.
1. Гемолитическая (надпечёночная) желтуха
Известно, что способность печени образовывать глюкурониды и выделять их в жёлчь в 3- 4 раза превышает их образование в физиологических условиях. Гемолитическая (надпечёноч-ная) желтуха - результат интенсивного гемолиза эритроцитов. Она обусловлена чрезмерным образованием билирубина, превышающим
способность печени к
его выведению. Гемолитическая желтуха развивается при исчерпании
резервных возможностей печени. Основная причина надпечёночной желтухи -
наследственные или приобретённые гемолитические анемии. При
гемолитических анемиях, вызванных сепсисом, лучевой болезнью, дефицитом
глюкозо-6-фосфатдегидрогеназы эритроцитов, талассемией, переливанием
несовместимых групп крови, отравлением сульфаниламидами, количество
освобождающегося из эритроцитов гемоглобина за сутки может доходить до
(при норме
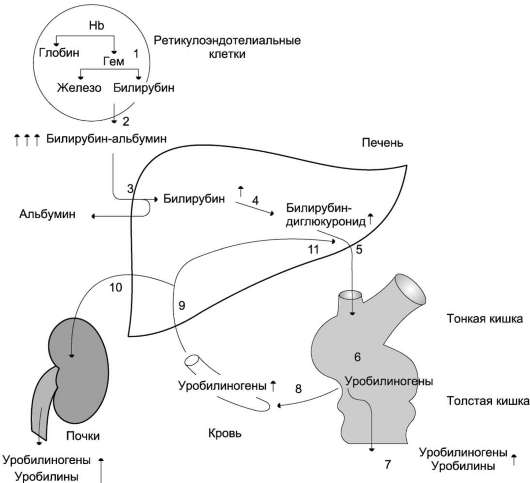
Рис. 13-16. Билирубин-уробилиногеновый цикл при гемолитической желтухе. 1 - катаболизм Hb идёт с повышенной скоростью; 2 - в крови примерно в 10 раз повышена концентрация непрямого билирубина; 3 - альбумин высвобождается из комплекса билирубин-альбумин; 4 - активность реакции глюкуронирования возрастает, но она ниже, чем скорость образования билирубина; 5 - секреция билирубина в жёлчь повышена; 6, 7,10 - повышенное содержание уробилиногенов в кале и моче придаёт им более интенсивную окраску; уро-билиноген всасывается из кишечника в кровь (8) и попадает в печень по воротной вене (9).
Один из главных признаков гемолитической желтухи - повышение содержания в крови неконъюгированного (непрямого) билирубина. Это позволяет легко отличить её от механической (подпечёночной) и печёночно-клеточной (печёночной) желтух.
Неконъюгированный билирубин токсичен. Гидрофобный, липофильный неконъюгирован-ный билирубин, легко растворяясь в липидах мембраны и проникая вследствие этого в митохондрии, разобщает в них дыхание и окислительное фосфорилирование, нарушает синтез белка, поток ионов калия через мембрану клетки и органелл. Это отрицательно сказывается на состоянии ЦНС, вызывая у больных ряд характерных неврологических симптомов.
Желтуха новорождённых
Частная разновидность гемолитической желтухи новорождённых - «физиологическая желтуха», наблюдающаяся в первые дни жизни ребёнка. Причиной повышения концентрации непрямого билирубина в крови служит ускоренный гемолиз и недостаточность функции белков и ферментов печени, ответственных за поглощение, конъюгацию и секрецию прямого билирубина. У новорождённых не только снижена активность УДФ-глюкуронилтрансферазы, но и, по-видимому, недостаточно активно происходит синтез второго субстрата реакции конъюгации УДФ-глюкуроната.
Известно, что УДФ-глюкуронилтрансфера-за - индуцируемый фермент (см. раздел 12). Новорождённым с физиологической желтухой вводят лекарственный препарат фенобарбитал, индуцирующее действие которого было описано в разделе 12.
Одно из неприятных осложнений «физиологической желтухи» - билирубиновая энцефалопатия. Когда концентрация неконъюгирован-ного билирубина превышает 340 мкмоль/л, он проходит через гематоэнцефалический барьер головного мозга и вызывает его поражение.
2. Печёночно-клеточная (печёночная) желтуха
Печёночно-клеточная (печёночная) желтуха обусловлена повреждением гепатоцитов и жёлчных капилляров, например, при острых вирусных инфекциях, хроническом и токсических гепатитах.
Причина повышения концентрации билирубина в крови - поражение и некроз части печёночных клеток. Происходит задержка билирубина в печени, чему способствует резкое ослабление метаболических процессов в поражённых гепатоцитах, которые теряют способность нормально выполнять различные биохимические и физиологические функции, в частности переводить конъюгированный (прямой) билирубин из клеток в жёлчь против градиента концентрации. Для печёночно-клеточной желтухи характерно то, что вместо преобладающих в норме диглюкуронидов билирубина в поражённой печёночной клетке образуются главным образом моноглюкурониды
(рис. 13-17).
В результате деструкции печёночной паренхимы образующийся прямой билирубин частично попадает в большой круг кровообращения, что ведёт к желтухе. Экскреция жёлчи также нарушена. Билирубина в кишечник попадает меньше, чем в норме.
При печёночно-клеточной желтухе повышается концентрация в крови как общего билирубина, так и обеих его фракций - неконъюги-рованного (непрямого) и конъюгированного (прямого).
Так как в кишечник поступает меньше били-рубинглюкуронида, то и количество образующегося уробилиногена также снижено. Поэтому кал гипохоличньгй, т.е. менее окрашенньгй. Моча, наоборот, имеет более интенсивную окраску за счёт присутствия там не только уробилинов, но и конъюгированного билирубина, который хорошо растворим в воде и экскретируется с мочой.
3. Механическая, или обтурационная (подпечё-ночная) желтуха
Механическая, или обтурационная (подпечё-ночная), желтуха развивается при нарушении желчеотделения в двенадцатиперстную кишку. Это может быть вызвано закупоркой жёлчных протоков, например при желчнокаменной болезни, опухолью поджелудочной железы, жёлчного пузыря, печени, двенадцатиперстной кишки, хроническим воспалением поджелудочной железы или послеоперационным сужением общего жёлчного протока (рис. 13-18).
При полной закупорке общего жёлчного протока конъюгированный билирубин в составе
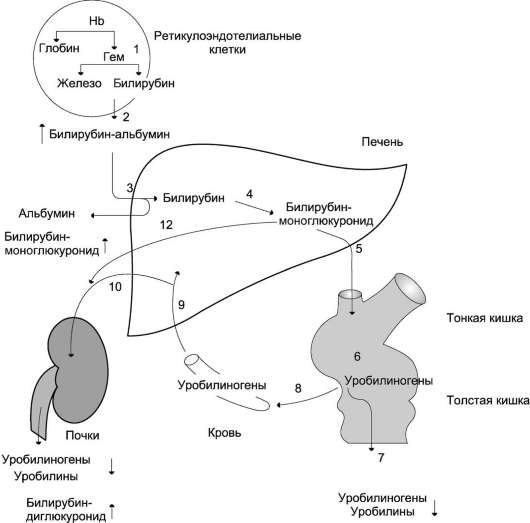
Рис. 13-17. Нарушение билирубин-уробилиногенового цикла при печёночно-клеточной желтухе. В печени снижена скорость реакции глюкуронирования билирубина (4), поэтому в крови повышается концентрация непрямого билирубина; вследствие нарушения паренхимы печени часть образованного в печени билирубинглюкуронида попадает в кровь (12) и далее с мочой (10) удаляется из организма. В моче больных присутствуют уробилины и билирубинглюкурониды. Остальные цифры соответствуют этапам метаболизма билирубина на рис. 13-16.
жёлчи не поступает в кишечник, хотя гепато-циты продолжают его вырабатывать. Поскольку билирубин в кишечник не попадает, продуктов его катаболизма уробилиногенов в моче и кале нет. Кал обесцвечен. Так как нормальные пути экскреции билирубина заблокированы, происходит его утечка в кровь, поэтому в крови больных повышена концентрация конъюгиро-ванного билирубина. Растворимый билирубин экскретируется с мочой, придавая ей насыщенный оранжево-коричневый цвет.
Б. ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА ЖЕЛТУХ
При диагностике желтух надо иметь в виду, что на практике редко отмечают желтуху какого-либо одного типа в «чистом» виде. Чаще встречается сочетание того или иного типа. Так, при выраженной гемолитической желтухе, сопровождающейся повышением концентрации непрямого билирубина, неизбежно страдают различные органы, в том числе и печень, что может вносить элементы
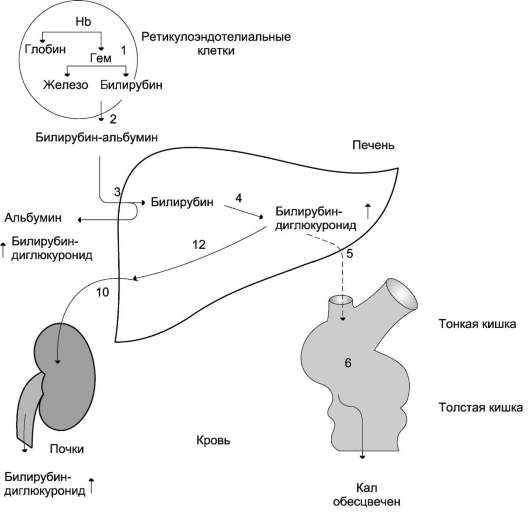
Рис. 13-18. Нарушение билирубин-уробилиногенового цикла при обтурационной желтухе. Вследствие закупорки жёлчного пузыря билирубинглюкуронид не секретируется в жёлчь (5); отсутствие билирубина в кишечнике приводит к обесцвечиванию кала (6); растворимый билирубинглюкуронид выделяется почками с мочой (10). Уробилинов в моче нет; образующийся в печени билирубинглюкуронид поступает в кровь (12), вследствие этого возрастает содержание прямого билирубина. Остальные цифры соответствуют этапам метаболизма билирубина на рис. 13-16.
паренхиматозной желтухи, т.е. повышение в крови и моче прямого билирубина. В свою очередь, паренхиматозная желтуха, как правило, включает в себя элементы механической. При подпечё-ночной (механической) желтухе, например, при раке головки поджелудочной железы, неизбежен повышенный гемолиз как результат раковой интоксикации и, как следствие, повышение в крови прямого и непрямого билирубина.
Итак, гипербилирубинемия может быть следствием избытка как связанного, так и свободного
билирубина. Измерение их концентраций по отдельности необходимо при постановке диагноза желтухи. Если концентрация билирубина в плазме <100 мкмоль/л и другие тесты функции печени дают нормальные результаты, возможно предположить, что повышение обусловлено за счёт непрямого билирубина. Чтобы подтвердить это, можно сделать анализ мочи, поскольку при повышении концентрации непрямого билирубина в плазме прямой билирубин в моче отсутствует.
При дифференциальной диагностике желтух необходимо учитывать содержание уробилиноге-нов в моче. В норме за сутки из организма выделяется в составе мочи около 4 мг уробилиногенов. Если с мочой выделяется повышенное количество уробилиногенов, то это - свидетельство недостаточности функции печени, например при печёночной или гемолитической желтухе. Присутствие в моче не только уробилиногенов, но и прямого билирубина указывает на поражение печени и нарушение поступления жёлчи в кишечник.
В. НАСЛЕДСТВЕННЫЕ НАРУШЕНИЯ МЕТАБОЛИЗМА БИЛИРУБИНА
Известно несколько заболеваний, при которых желтуха вызвана наследственными нарушениями метаболизма билирубина.
Примерно у 5% населения диагностируют наследственную желтуху, вызванную генетическими нарушениями в структуре белков и ферментов, ответственных за транспорт (захват) непрямого билирубина в печень и его конъюгацию с глюку-роновой кислотой. Эта патология наследуется по аутосомно-доминантному типу. В крови больных повышена концентрация непрямого билирубина.
Известно 2 типа наследственных желтух, обусловленных нарушением реакции глюкуро-нирования в печени - образования прямого билирубина.
Для первого типа характерно полное отсутствие УДФ-глюкуронилтрансферазы. Заболева-
ние наследуется по аутосомно-рецессивному типу. Введение фенобарбитала, индуктора УДФ-глюкуронилтрансферазы, не приводит к снижению уровня билирубина. Дети умирают в раннем возрасте из-за развития билирубиновой энцефалопатии.
Для второго типа характерно снижение активности (недостаточности) УДФ-глюкуронил-трансферазы, гипербилирубинемия возникает за счёт непрямого билирубина. Желтуха хорошо поддаётся лечению фенобарбиталом.
Нарушение активного транспорта образованных в клетках печени билирубинглюкуронидов в жёлчь характерно для желтухи, наследуемой по аутосомно-доминантному типу. Проявляется гипербилирубинемией за счёт прямого билирубина и билирубинурией (в моче определяется прямой билирубин).
Семейная гипербилирубинемия новорождённых связана с наличием конкурентных ингибиторов конъюгации билирубина (эстрогенов, свободных жирных кислот) в материнском молоке. При грудном вскармливании ингибиторы конъюгации билирубина обнаруживают в сыворотке крови ребёнка. Такая гиперби-лирубинемия была названа транзиторной. Ги-пербилирубинемия исчезает при переводе ребёнка на искусственное вскармливание. Не поддающаяся лечению гипербилирубинемия приводит к развитию билирубиновой энцефалопатии и ранней смерти.