Гистология, эмбриология, цитология: учебник для вузов / Под ред. Э.Г.Улумбекова, Ю.А.Челышева - 3-е изд., - 2009. - 480 с.
|
|
|
|
ГЛАВА 6 ТКАНИ ВНУТРЕННЕЙ СРЕДЫ
Система тканей внутренней среды включает кровь, соединительные ткани и скелетные ткани (хрящевую и костную). Несмотря на разнообразие тканей и клеточных типов, в системе тканей внутренней среды имеются общие черты: мезенхимный генез, большое количество межклеточного вещества, множество разных обновляющихся клеточных типов.
КРОВЬ
Кровь - одна из тканей внутренней среды. Жидкое межклеточное вещество (плазма) и взвешенные в нём клетки - два основных компонента крови. У взрослого человека общий объём крови около 5 л; около 1 л находится в депо крови, преимущественно в селезёнке. Кровь циркулирует в замкнутой системе сосудов и переносит газы, питательные вещества, гормоны, белки, ионы, продукты метаболизма. Кровь поддерживает постоянство внутренней среды организма, регулирует температуру тела, осмотическое равновесие и кислотно-щелочной баланс. Клетки крови участвуют в уничтожении микроорганизмов, в воспалительных и иммунных реакциях. Кровь содержит тромбоциты и плазменные факторы свёртывания.
• Плазма состоит из воды (90%), органических (9%) и неорганических (1%) веществ. Белки составляют 6% всех веществ плазмы. Среди сотен различных белков плазмы выделяют белки системы свёртывания крови, участвующие в иммунных реакциях белки, транспортные белки.
• Свернувшаяся кровь состоит из тромба (сгустка), включающего клетки крови и некоторые белки плазмы, и сыворотки - прозрачной жидкости, сходной с плазмой, но лишённой фибриногена.
• Клетки крови (форменные элементы) - эритроциты, лейкоциты и тромбоциты.
Эритроциты
Зрелый эритроцит (нормоцит) - безъядерная клетка диаметром 7- 8 мкм. Количество эритроцитов: у женщин - 3,9-4,9х1012/л, у муж-
чин - 4,0-5,2х1012/л. Более высокое содержание эритроцитов у мужчин обусловлено стимулирующим эритропоэз влиянием андрогенов. Продолжительность жизни (время циркуляции в крови) - 100-120 дней. Форма эритроцита - двояковогнутый диск. Такая конфигурация создаёт наибольшую площадь поверхности по отношению к объ- ёму, что обеспечивает максимальный газообмен.
Гематокрит - процентное отношение объёма эритроцитов к объёму крови. В норме гематокрит равен у мужчин 40-50%, у женщин - 35-45%, у детей до 10 лет - 45-65%.
Плазмолемма эритроцита довольно пластична, что позволяет клетке деформироваться и легко проходить по узким капиллярам диаметром 3-4 мкм. Главные трансмембранные белки эритроцита - белок полосы 3, гликофорины, транспортёр глюкозы GLUT1. Белок полосы 3 совместно с белками примембранного цитоскелета обеспечивают поддержание формы эритроцита в виде двояковогнутого диска.
Гемоглобин
Практически весь объём эритроцита заполнен гемоглобином (Hb). Молекула Hb - тетрамер, состоящий из четырёх полипептидных цепей глобина, каждая из которых ковалентно связана с одной молекулой гема. Основная функция Hb - перенос O2.
• Типы гемоглобина. Существует несколько типов гемоглобина, образующихся на разных сроках развития и различающихся строением цепей глобина. К этим типам относятся эмбриональные, фетальный и дефинитивные гемоглобины.
• Формы гемоглобина. Различают следующие формы гемоглобина: оксигемоглобин, метгемоглобин, карбоксигемоглобин и гликозилированный гемоглобин.
Гибель эритроцитов
Разрушение эритроцитов, закончивших жизненный цикл, происходит в основном в селезёнке, а также в печени и костном мозге. Поскольку синтез ферментов в эритроците невозможен, со временем в нём снижается обмен веществ, нарушается форма, происходит деградация белков, появляются новые антигены. Такие стареющие клетки распознаются макрофагами и фагоцитируются. В эритроцитах так называемый «антиген старения» представлен в виде деградированного белка полосы 3. В сутки из кровотока удаляется 0,5-1,5% общей массы эритроцитов (40 000-50 000 клеток/мкл).
Группы крови
В мембране эритроцита присутствует множество антигенных детерминант, взятых за основу для определения групповой принадлежности крови. Известно не менее 30 разных систем групповой принадлежности крови, но при гемотрансфузии совместимость крови донора и
реципиента в первую очередь определяют по антигенам системы AB0 (4 группы) и системы Rh (2 группы).
Лейкоциты
В1 л крови взрослого здорового человека содержится 3,8-9,8х109 лейкоцитов - клеток шаровидной формы. В цитоплазме лейкоцитов находятся гранулы - специфические (вторичные) и азурофильные (лизосомы). В зависимости от типа гранул лейкоциты делят на гранулоциты (зернистые) и агранулоциты (незернистые). Гранулоциты (нейтрофилы, эозинофилы, базофилы) содержат специфические и азурофильные гранулы. В цитоплазме агранулоцитов (моноцитов, лимфоцитов) присутствуют только азурофильные гранулы. Для гранулоцитов характерно дольчатое сегментированное ядро разнообразной формы, в связи с чем их называют полиморфноядерными лейкоцитами. Лимфоциты и моноциты имеют несегментированное ядро, их называют мононуклеарными лейкоцитами. Лейкоциты участвуют в защитных реакциях: уничтожают микроорганизмы, захватывают инородные частицы и продукты распада тканей, осуществляют реакции гуморального и клеточного иммунитета.
НЕЙТРОФИЛЫ
Нейтрофилы (рис. 6-3) - наиболее многочисленные из лейкоцитов. Они составляют 40-75% общего количества лейкоцитов. Размеры нейтрофила: в мазке крови - 12 мкм; диаметр нейтрофила, мигрирующего в тканях, увеличивается почти до 20 мкм. Нейтрофилы образуются в костном мозге, выходят в кровоток и циркулируют в крови 8-12 часов. Старые клетки фагоцитируются макрофагами.
Морфология нейтрофильных лейкоцитов
Ядро зрелой клетки - сегментоядерного нейтрофила - состоит из 3-5 сегментов, соединённых тонкими перемычками, хроматин сильно конденсирован. В нейтрофилах у женщин один из сегментов ядра содержит вырост в форме барабанной палочки - тельце Барра. Этот половой хроматин заметен у 3% нейтрофилов в мазке крови женщин. В крови также содержатся палочкоядерные нейтрофилы - незрелые формы клеток с подковообразным ядром. В норме их количество составляет 3-6%. Нейтрофил содержит большое количество гликогена. Азурофильные гранулы (красновато-пурпурного цвета на окрашенном мазке) - специализированные лизосомы. Помимо лизосомных гидролаз, азурофильные гранулы содержат также различные белки, разрушающие компоненты внеклеточного матрикса и обладающие
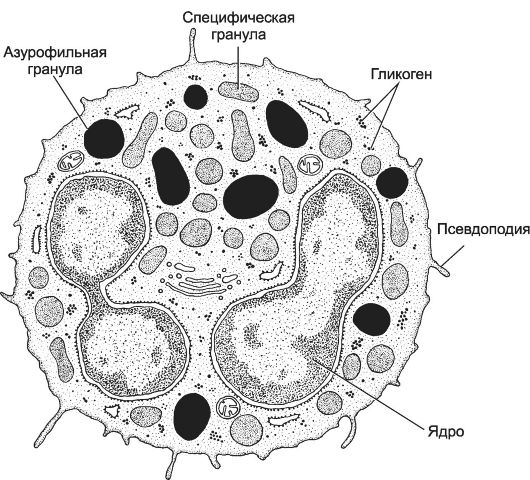 Рис. 6-3. Нейтрофил. Ядро
состоит из 3-5 сегментов, соединённых тонкими перемычками. В цитоплазме
- минимальное количество органелл, но много гранул гликогена. Нейтрофил
содержит небольшое количество азурофильных гранул и многочисленные
мелкие специфические гранулы. [17]
Рис. 6-3. Нейтрофил. Ядро
состоит из 3-5 сегментов, соединённых тонкими перемычками. В цитоплазме
- минимальное количество органелл, но много гранул гликогена. Нейтрофил
содержит небольшое количество азурофильных гранул и многочисленные
мелкие специфические гранулы. [17]
антибактериальной активностью: миелопероксидазу, протеиназу 3 (миелобластин), азуроцидин, эластазу, катепсины, дефензины, катионные белки, лизоцим, арилсульфатазу.
Специфические гранулы (окрашиваемые в оранжево-розовый цвет) значительно мельче азурофильных, но вдвое многочисленнее. Эти гранулы содержат белки, обладающие бактериостатическими свойствами и разрушающие внеклеточный матрикс: лактоферрин, лизоцим, металлопротеиназы (желатиназу и коллагеназу), щелочную фосфатазу, катионные белки (кателицидин).
Рецепторы. В плазмолемму нейтрофилов встроены рецепторы молекул адгезии, цитокинов, колониестимулирующих факторов (CSF), опсонинов (Fc-фрагментов IgG и белков комплемента), медиаторов воспаления.
Функции нейтрофильных лейкоцитов
Нейтрофилы обладают выраженной фагоцитарной активностью и участвуют в острой воспалительной реакции. Главная функция - фагоцитоз опсонизированных микроорганизмов. Фагоцитоз и последующее переваривание материала происходят параллельно с образованием метаболитов арахидоновой кислоты и респираторным взрывом.
• Респираторный взрыв. Нейтрофилы в течение первых секунд после стимуляции резко увеличивают поглощение кислорода и быстро расходуют значительное его количество. Это явление известно как респираторный (кислородный) взрыв. При этом образуются токсичные для микроорганизмов H2O2, супероксид O2- и гидроксильный радикал OH-.
• Фагоцитоз осуществляется в несколько этапов. После предварительного специфического распознавания подлежащего фагоцитозу материала происходит инвагинация мембраны нейтрофила вокруг частицы и образование фагосомы. Далее в результате слияния фагосомы с лизосомами образуется фаголизосома, после чего происходит уничтожение бактерии и разрушение захваченного материала. Для этого в фаголизосому поступают: лизоцим, катепсин, эластаза, лактоферрин, дефензины, катионные белки; миелопероксидаза; супероксид О2- и гидроксильный радикал ОН-, образующиеся (наряду с Н2О2) при респираторном взрыве. После единственной вспышки активности нейтрофил погибает. Такие нейтрофилы составляют основной компонент гноя (гнойные клетки).
ЭОЗИНОФИЛЫ
Эозинофилы (рис. 6-5) составляют 1-5% лейкоцитов, циркулирующих в крови. Их количество изменяется в течение суток и максимально утром. Эозинофилы в течение нескольких дней после образования остаются в костном мозге, затем циркулируют в крови 3-8 часов, большинство из них выходит из кровотока и мигрируют в ткани, контактирующие с внешней средой (слизистые оболочки дыхательных и мочеполовых путей, кишечника). Размер эозинофила в крови >12 мкм, увеличивается после выхода в соединительную ткань до 20 мкм. Продолжительность жизни - предположительно 8-14 дней.
Морфология эозинофильных лейкоцитов
Ядро эозинофила состоит из двух крупных сегментов, соединённых тонкой перемычкой (сегментоядерный эозинофил). Цитоплазма содержит хорошо развитую гранулярную эндоплазматическую сеть, небольшое количество цистерн гладкой эндоплазматической сети, скопления рибосом, отдельные митохондрии и много гликогена. Специфические гранулы. В цитоплазме эозинофила присутствуют крупные и мелкие специфические гранулы с выраженной ацидофилией (красно-оранжевые). Крупные гранулы размером 0,5-1,5 мкм имеют овоидную форму и содержат удлинённый кристаллоид. Кристаллоид имеет структуру кубической решётки и состоит в основном из анти-
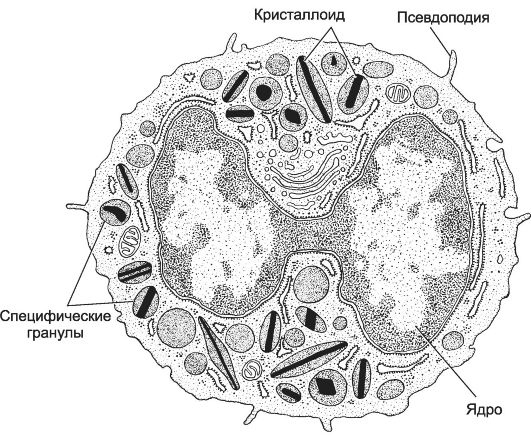 Рис. 6-5. Эозинофил. Ядро
эозинофила обычно образует два крупных сегмента, соединённых тонкой
перемычкой. Содержит умеренное количество типичных органелл, гликоген.
Крупные гранулы овоидной формы содержат электронно-плотный материал -
кристаллоид. Клетка образует цитоплазматические выросты, при помощи
которых мигрирует в тканях. [17]
Рис. 6-5. Эозинофил. Ядро
эозинофила обычно образует два крупных сегмента, соединённых тонкой
перемычкой. Содержит умеренное количество типичных органелл, гликоген.
Крупные гранулы овоидной формы содержат электронно-плотный материал -
кристаллоид. Клетка образует цитоплазматические выросты, при помощи
которых мигрирует в тканях. [17]
паразитарного агента - главного щелочного белка (MBP). В гранулах также присутствуют нейротоксин (белок X), пероксидаза эозинофила EPO, гистаминаза, фосфолипаза D, гидролитические ферменты, кислая фосфатаза, коллагеназа, цинк, катепсин. Мелкие гранулы содержат арилсульфатазу, кислую фосфатазу, пероксидазу, катионный белок эозинофилов ECP.
Рецепторы. Эозинофилы имеют мембранные рецепторы Fc-фрагмен- тов IgG, IgM и IgE, компонентов комплемента C1s, C3a, C3b, C4 и C5a, а также эотаксина и ИЛ5.
Функции эозинофильных лейкоцитов
Эозинофил участвует в уничтожении паразитов, в аллергических и воспалительных реакциях; при этом секретируется содержимое гранул
и одновременно происходит респираторный взрыв. После дегрануляции эозинофилы подвергаются апоптозу.
БАЗОФИЛЫ
Базофилы (рис. 6-6) составляют 0-1% общего числа лейкоцитов циркулирующей крови. В крови базофилы находятся 1-2 суток. Как и другие гранулоциты, при стимуляции и активации базофилы могут покидать кровоток, но их способность к амебоидному движению ог-
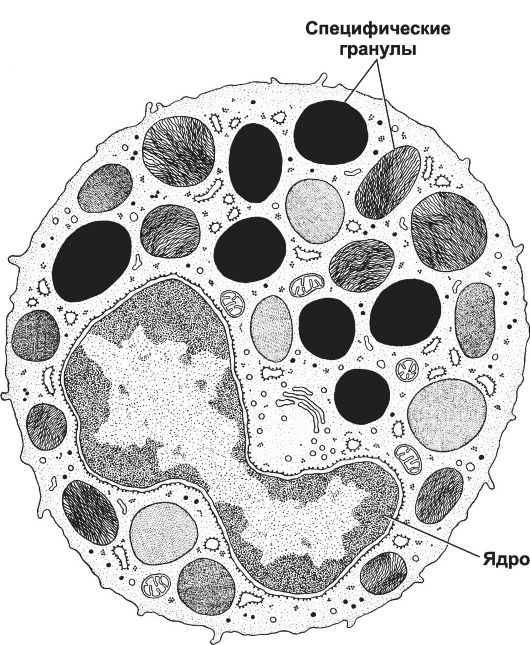 Рис. 6-6. Базофил. Слабодольчатое
ядро изогнуто в форме буквы S. В цитоплазме присутствуют все виды
органелл, свободные рибосомы, гликоген. Специфические гранулы
разнообразны по размерам и по форме. Содержимое гранул чаще неоднородно
по плотности. [17]
Рис. 6-6. Базофил. Слабодольчатое
ядро изогнуто в форме буквы S. В цитоплазме присутствуют все виды
органелл, свободные рибосомы, гликоген. Специфические гранулы
разнообразны по размерам и по форме. Содержимое гранул чаще неоднородно
по плотности. [17]
раничена. Размер - 10-12 мкм. Продолжительность жизни и судьба в тканях неизвестна. Уплотнённое ядро состоит из нечётко выраженных трёх долек, изогнуто в виде буквы S. В цитоплазме имеются все виды органелл, свободные рибосомы и гликоген.
Специфические гранулы довольно крупные (0,5-1,2 мкм), окрашиваются метахроматически (от красновато-фиолетовых до интенсивнофиолетовых). Имеют разнообразную, чаще овальную или округлую форму с плотным содержимым. В гранулах содержатся различные ферменты и медиаторы. К наиболее значимым из них можно отнести гепаринсульфат (гепарин), гистамин, серотонин, нейтральные протеазы триптазу и химазу, медиаторы воспаления.
Рецепторы. Базофилы имеют высокоаффинные поверхностные рецепторы к Fc-фрагментам IgE.
Функции. Активированные базофилы, покидая кровоток, мигрируют в очаги воспаления и участвуют в аллергических реакциях. Активация и дегрануляция базофилов происходит при попадании в организм аллергена и опосредована IgE. Молекулы IgE присоединяются к базофилу (формируется комплекс «IgE-базофил»). При повторном попадании антигена (аллергена) он связывается двумя и более молекулами IgE на поверхности базофила, что приводит к дегрануляции последнего - быстрому экзоцитозу содержимого гранул. Параллельно образуются метаболиты арахидоновой кислоты.
МОНОЦИТЫ
Моноциты (рис. 6-7) - самые крупные лейкоциты (диаметр в мазке крови приблизительно 15 мкм), количество их составляет 2-9% от всех лейкоцитов циркулирующей крови. Крупное, эксцентрично расположенное подковообразное ядро имеет пятнистый вид из-за неравномерно конденсированного хроматина. Бледная голубовато-серая (на окрашенном мазке) цитоплазма включает многочисленные лизосомы, содержащие кислые гидролазы, арилсульфатазу, катепсин C, кислую фосфатазу, пероксидазу, разные вакуоли, большое количество рибосом и полирибосом, комплекс Гольджи, мелкие удлинённые митохондрии. Моноциты крови - фактически незрелые клетки, находящиеся на пути из костного мозга в ткани. Образуются в костном мозге, выходят в кровоток и циркулируют в крови около 2-4 суток. Рецепторы. В мембрану моноцита встроены рецепторы Fc-фрагмента Ig, белков комплемента, цитокинов, медиаторов воспаления, бактериальных продуктов, холинорецепторы, адренорецепторы. Активация моноцитов. Различные вещества, образующиеся в очагах воспаления и разрушения ткани, - агенты хемотаксиса и активации моноцитов. В результате активации увеличивается размер клетки,
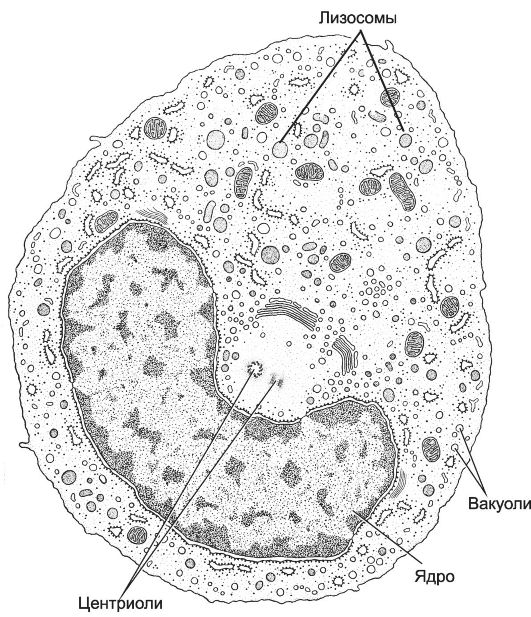 Рис. 6-7. Моноцит. Крупное
бобовидное или подковообразное ядро расположено эксцентрично. Хроматин
слабо конденсирован. В цитоплазме присутствуют типичные органеллы, много
рибосом и полирибосом, пиноцитозные пузырьки, фагоцитарные вакуоли,
многочисленные лизосомы. [17]
Рис. 6-7. Моноцит. Крупное
бобовидное или подковообразное ядро расположено эксцентрично. Хроматин
слабо конденсирован. В цитоплазме присутствуют типичные органеллы, много
рибосом и полирибосом, пиноцитозные пузырьки, фагоцитарные вакуоли,
многочисленные лизосомы. [17]
усиливается метаболизм, моноциты выделяют биологически активные вещества (ИЛ1, ИЛ6, фактор некроза опухоли α - TNFα, колониестимулирующие факторы M-CSF, GM-CSF, простагландины, интерфероны, факторы хемотаксиса нейтрофилов).
Функция. Главная функция моноцитов и образующихся из них макрофагов - фагоцитоз. Моноциты фагоцитируют опсонизированные частицы. В их переваривании участвуют лизосомные ферменты моно-
цитов, а также формируемые внутриклеточно H2O2, OH , O2 . Активированные моноциты/макрофаги продуцируют эндогенные пирогены.
ЛИМФОЦИТЫ
Лимфоциты (рис. 6-8) составляют 20-45% общего числа лейкоцитов, циркулирующих в крови. Они играют центральную роль во всех
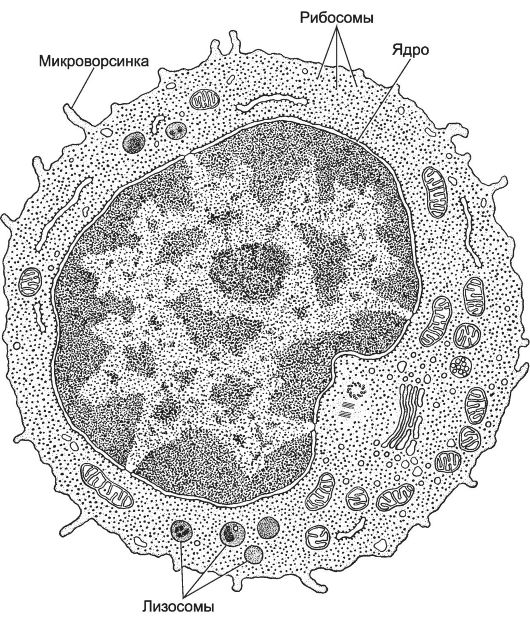 Рис. 6-8. Лимфоцит. Ядро
округлое с небольшими выемками или бобовидное. Хроматин сильно
конденсирован. Клетка имеет небольшой объём цитоплазмы, образующей узкий
ободок вокруг ядра. В цитоплазме присутствует минимальное количество
обычных органелл. Лимфоцит образует короткие цитоплазматические
отростки. [17]
Рис. 6-8. Лимфоцит. Ядро
округлое с небольшими выемками или бобовидное. Хроматин сильно
конденсирован. Клетка имеет небольшой объём цитоплазмы, образующей узкий
ободок вокруг ядра. В цитоплазме присутствует минимальное количество
обычных органелл. Лимфоцит образует короткие цитоплазматические
отростки. [17]
иммунологических реакциях. Кровь - среда, в которой лимфоциты циркулируют между органами лимфоидной системы и другими тканями. Лимфоциты выходят из сосудов в соединительную ткань в ответ на соответствующие сигналы. Лимфоциты могут мигрировать через базальную мембрану и внедряться в эпителий (например, в слизистой оболочке кишечника). Продолжительность жизни лимфоцитов достаточно велика: от нескольких месяцев до нескольких лет.
Классификация лимфоцитов
Применяют два критерия подразделения лимфоцитов: морфологический и функциональный.
• Функциональная классификация выделяет B-лимфоциты, T-лимфоци- ты и NK-клетки.
• Морфологическая классификация. Принято выделять малые (4,5- 6 мкм), средние (7-10 мкм) и большие лимфоциты (10-18 мкм).
B-лимфоциты составляют менее 15% лимфоцитов крови. Эти клетки (точнее, дифференцирующиеся из активированных В-лимфоцитов плазматические клетки) вырабатывают против конкретных антигенов соответствующие АТ.
T-лимфоциты составляют большинство лимфоцитов крови (80% и более). Они, как и B-лимфоциты, реагируют на конкретные антигены. Главная функция T-лимфоцитов - участие в клеточном и гуморальном иммунитете. T-лимфоциты уничтожают аномальные клетки своего организма, участвуют в аллергических реакциях, отторжении чужеродного трансплантата.
NK-клетки - лимфоциты, лишённые характерных для Т- и В-клеток поверхностных детерминант. Эти клетки составляют около 5-10% всех циркулирующих лимфоцитов, содержат цитолитические гранулы с перфорином, уничтожают трансформированные, инфицированные вирусами и чужеродные клетки.
Более подробно В-лимфоциты, T-лимфоциты и NK-клетки рассмотрены в главе 11.
Тромбоциты
Тромбоциты (кровяные пластинки, рис. 6-9) - фрагменты цитоплазмы находящихся в красном костном мозге мегакариоцитов. Количество тромбоцитов в циркулирующей крови - 190-405х109/л. Размер - 3-5 мкм. Две трети кровяных пластинок циркулирует в крови, остальные депонируются в селезёнке. Продолжительность жизни - 8 дней. Старые и дефектные тромбоциты фагоцитируются в селезён- ке, печени и костном мозге.
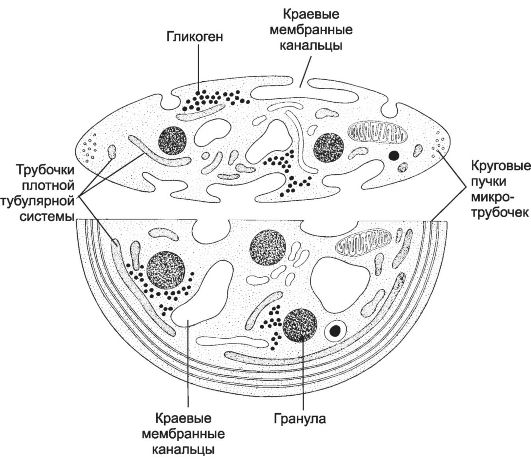 Рис. 6-9. Тромбоцит имеет
форму овального или округлого диска. В цитоплазме присутствуют
митохондрии, комплекс Гольджи, рибосомы, гликоген. В центральной части
тромбоцита сосредоточены различные гранулы. Периферическая часть
содержит циркулярные пучки микротрубочек, сократительные белки. Здесь же
имеются связанные между собой мембранные каналы, открывающиеся во
внеклеточную среду. В цитоплазме рассеяны мембранные трубочки плотной
тубулярной системы. [17]
Рис. 6-9. Тромбоцит имеет
форму овального или округлого диска. В цитоплазме присутствуют
митохондрии, комплекс Гольджи, рибосомы, гликоген. В центральной части
тромбоцита сосредоточены различные гранулы. Периферическая часть
содержит циркулярные пучки микротрубочек, сократительные белки. Здесь же
имеются связанные между собой мембранные каналы, открывающиеся во
внеклеточную среду. В цитоплазме рассеяны мембранные трубочки плотной
тубулярной системы. [17]
Морфология
Гликокаликс. Тромбоцит окружён толстым слоем гликокаликса, богатым кислыми гликозаминогликанами. Гликокаликс образует фибриллярные мостики между мембранами соседних тромбоцитов при их агрегации.
Плазматическая мембрана содержит гликопротеины, выполняющие роль рецепторов адгезии и агрегации.
Цитоплазма на окрашенном мазке - пурпурная и зернистая. Тромбоциты содержат в большом количестве митохондрии, элементы комп-
лекса Гольджи и рибосомы, а также гранулы гликогена и ферменты для аэробного и анаэробного дыхания. Периферическая часть цитоплазмы содержит актин, миозин, гельзолин и другие контрактильные белки, участвующие в округлении тромбоцита и ретракции тромба. Имеются также пучки микротрубочек, циркулярно расположенные под плазмолеммой. Эти микротрубочки необходимы для сохранения овальной формы тромбоцита. По периферии тромбоцита расположены анастомозирующие краевые мембранные канальцы, открывающиеся во внеклеточную среду; их мембраны связаны с элементами цитоскелета. Система этих канальцев участвует в секреции содержимого α-гранул. Кроме α-гранул, тромбоциты содержат ещё 3 типа гранул - δ-, λ-гранулы и микропероксисомы.
• α-Гранулы (300-500 нм) наиболее значимы для осуществления функций тромбоцита и содержат разнообразные вещества, в том числе фактор роста из тромбоцитов (PDGF), трансформирующий фактор роста β (TGFb), тромбоспондин, фактор V свёртывания крови и Р-селектин.
• δ-Гранулы (250-300 нм) имеют уплотнённую сердцевину и накапливают неорганический фосфат (Р;), АДФ, АТФ, Ca2+, серотонин и гистамин.
• λ- Гранулы (200-250 нм) содержат лизосомные ферменты.
• Микропероксисомы - немногочисленные гранулы, обладающие пероксидазной активностью.
Функции
Тромбоциты участвуют в свёртывании крови и восстановлении целостности стенки сосуда. В физиологических условиях тромбоциты не прикрепляются к эндотелию сосуда. При нарушении целостности сосудистой стенки при непосредственном участии тромбоцитов формируется тромб. В частности, тромбоциты высвобождают фибриноген (в дополнение к уже присутствующему в плазме в норме), который с помощью факторов свёртывания конвертируется в фибрин, образующий плотную фиброзную основу, к которой прикрепляется всё больше тромбоцитов и других клеток крови.
Гемопоэз
Гемопоэз - образование клеток крови (кроветворение), происходящее в кроветворных органах. В пренатальном периоде гемопоэз, начинаясь на 3-й неделе развития, последовательно происходит в различных органах. У взрослого человека гемопоэз происходит в костном мозге костей черепа, рёбер, грудины, позвонков, костей таза, эпифизов длинных костей, в лимфоидной ткани. Родоначальница всех форменных элементов крови - стволовая кроветворная клетка.
Кроветворение у эмбриона и плода
У эмбриона и плода последовательно и с частичным перекрыванием по времени возникновения и затухания различают мегалобластическую, гепатоспленотимическую стадии и костномозговое кроветворение.
Мегалобластическая стадия. Во внезародышевой мезодерме желточного мешка в течение 3-й недели формируются скопления мезенхимных клеток - кровяные островки (рис. 6-13). Клетки, расположенные по периферии островка, дифференцируются в эндотелиальные клетки первичных кровеносных сосудов. В центральной части островка образуются первые клетки крови - первичные эритробласты - крупные клетки, содержащие ядро и эмбриональные гемоглобины. Лейкоцитов и тромбоцитов на этой стадии нет. На 12-й неделе кроветворение в желточном мешке заканчивается.
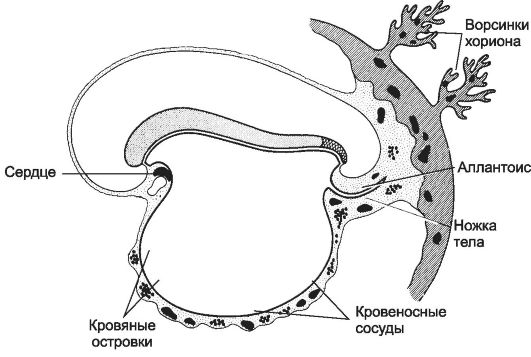 Рис. 6-13. Эмбриональный гемопоэз (19-дневный эмбрион). В
конце 3-й недели кровяные островки присутствуют в стенке желточного
мешка, а также во внезародышевой мезодерме ворсинок хориона и ножке
тела. Островки дают начало первичным клеткам крови и кровеносным
сосудам. В дальнейшем (благодаря объединению сосудов эмбриона и
внеэмбриональных сосудов) устанавливается связь зародыша с плацентой.
[17]
Рис. 6-13. Эмбриональный гемопоэз (19-дневный эмбрион). В
конце 3-й недели кровяные островки присутствуют в стенке желточного
мешка, а также во внезародышевой мезодерме ворсинок хориона и ножке
тела. Островки дают начало первичным клеткам крови и кровеносным
сосудам. В дальнейшем (благодаря объединению сосудов эмбриона и
внеэмбриональных сосудов) устанавливается связь зародыша с плацентой.
[17]
Гепатоспленотимическая стадия начинается на втором месяце развития, когда стволовые кроветворные клетки заселяют печень, селезёнку и тимус.
• Печень. В печени кроветворение начинается на 5-6 неделе развития. Здесь образуются эритроциты, гранулоциты и тромбоциты. К концу 5-го месяца интенсивность гемопоэза в печени уменьшается, но в небольшой степени продолжается ещё несколько недель после рождения.
• Селезёнка. Гемопоэз в селезёнке наиболее выражен с 4 по 8 месяц внутриутробного развития. Здесь образуются эритроциты и небольшое количество гранулоцитов и тромбоцитов. Непосредственно перед рождением важнейшей функцией селезёнки становится образование лимфоцитов.
• Тимус. В вилочковой железе первые лимфоциты появляются на 7-8 неделе. Костномозговое кроветворение. В течение 5-го месяца развития гемопоэз начинается в костном мозге, а к 7-му месяцу костный мозг становится главным органом гемопоэза. После рождения и до полового созревания количество очагов кроветворения в костном мозге уменьшается, хотя костный мозг полностью сохраняет гемопоэтический потенциал. У взрослого человека кроветворение ограничивается костным мозгом и лимфоидной тканью. Когда костный мозг не в состоянии удовлетворить повышенный и длительный запрос на образование клеток крови, гемопоэтическая активность печени, селезёнки и лимфатических узлов может восстановиться (экстрамедуллярный гемопоэз).
Постнатальный гемопоэз
Красный костный мозг (рис. 6-16) содержит в большом количестве созревающие эритроциты, что придаёт костномозговым очагам гемопоэза красный цвет. Строма состоит из ретикулярных клеток с длинными отростками, ретикулиновых волокон, синусоидных капилляров и адипоцитов, составляющих почти половину объёма костного мозга. Клетки стромы костного мозга экспрессируют широкий спектр молекул адгезии, опосредующих связывание стволовых кроветворных клеток с элементами внеклеточного матрикса. Ретикулиновые волокна вместе с отростками ретикулярных клеток формируют трёхмерную сеть и образуют полости, заполненные островками гемопоэтических клеток. Зрелые клетки крови выходят в кровоток через щели в стенке синусоидных капилляров. Костный мозг содержит большое количество макрофагов, расположенных рядом с синусоидами. Помимо кроветворения, в костном мозге, как в селезёнке и печени, происходит удаление из кровотока старых и дефектных клеток крови. Костный мозг играет центральную роль в иммунной защите, т.к. в нём образуются В-лимфоциты, а также присутствует большое количество плазматических клеток, синтезирующих антитела. Жёлтый костный мозг. У взрослых большая часть костного мозга становится неактивной; в нём преобладают жировые клетки. Жёлтый костный мозг, однако,
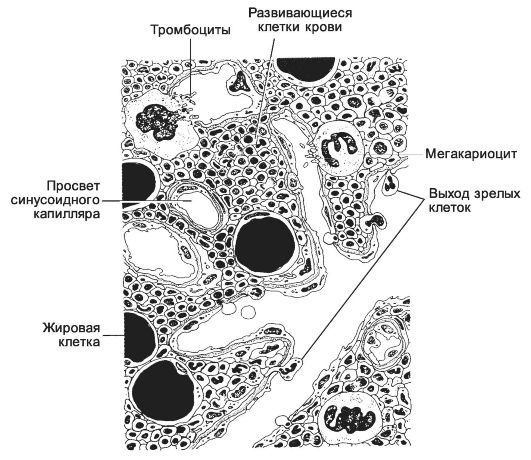 Рис. 6-16. Красный костный мозг. Основу
составляют ретикулярные клетки с длинными отростками и ретикулиновые
волокна. В пространствах между ними располагаются островки
гемопоэтических клеток. Костный мозг пронизан синусоидными капиллярами. К
эндотелию капилляров примыкают макрофаги, образующие длинные отростки. В
большом количестве присутствуют жировые клетки. [17]
Рис. 6-16. Красный костный мозг. Основу
составляют ретикулярные клетки с длинными отростками и ретикулиновые
волокна. В пространствах между ними располагаются островки
гемопоэтических клеток. Костный мозг пронизан синусоидными капиллярами. К
эндотелию капилляров примыкают макрофаги, образующие длинные отростки. В
большом количестве присутствуют жировые клетки. [17]
может восстановить свою активность, если необходимо усилить гемопоэз (например, при хронической гипоксии или выраженных кровотечениях). Стволовая кроветворная клетка морфологически сходна с малым лимфоцитом и способна к дифференцировке во все клетки крови (рис. 6-17). Такая клетка была названа CFU-blast (CFU - Colony Forming Unit, колониеобразующая единица). Стволовая кроветворная клетка постоянно, но редко делится. Дочерние клетки выбирают симметричное или асимметричное деление, т.е. или остаются стволовыми кроветворными клетками, или дифференцируются в полипотентные потомки с их последующей дифференцировкой в клетки крови. Образующиеся
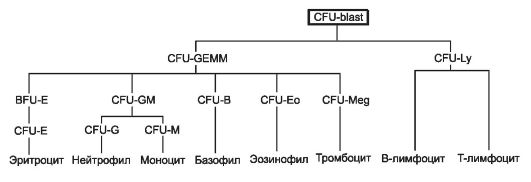 Рис. 6-17. Схема гемопоэза. CFU-blast
-стволовая кроветворная клетка; CFUGEMM - полипотентная
клетка-предшественница миелопоэза; CFU-Ly - полипотентная
клетка-предшественница лимфоцитопоэза; CFU-GM - полипотентная
клетка-предшественница гранулоцитов и моноцитов. Унипотентные
предшественники: BFU-E и CFU-E - эритроцитов; CFU-Eo - эозинофилов;
CFU-M - моноцитов; CFU-G - нейтрофилов, CFU-B - базофилов, CFU-Meg -
тромбоцитов. [17]
Рис. 6-17. Схема гемопоэза. CFU-blast
-стволовая кроветворная клетка; CFUGEMM - полипотентная
клетка-предшественница миелопоэза; CFU-Ly - полипотентная
клетка-предшественница лимфоцитопоэза; CFU-GM - полипотентная
клетка-предшественница гранулоцитов и моноцитов. Унипотентные
предшественники: BFU-E и CFU-E - эритроцитов; CFU-Eo - эозинофилов;
CFU-M - моноцитов; CFU-G - нейтрофилов, CFU-B - базофилов, CFU-Meg -
тромбоцитов. [17]
при делении клетки дифференцируются в пролиферирующие полипотентные клетки-предшественницы (колониеобразующие единицы) лимфоцитопоэза (CFU-Ly) и миелопоэза (CFU-GEMM). В результате деления CFU-Ly и CFU-GEMM их потомки остаются полипотентными или дифференцируются в один из нескольких типов коммитированных унипотентных клеток (колониеобразующих единиц), также активно пролиферирующих, но дифференцирующихся только в одном направлении.
Унипотентные компилированные клетки способны к дифференцировке в один клеточный тип, пролиферируют и в присутствии факторов роста дифференцируются в клетки-предшественницы. Унипотентные клетки морфологически не отличаются от стволовых клеток. Программирование клетки на определённый путь дифференцировки (коммитирование), по-видимому, происходит случайным образом. Клетки-предшественницы - клетки одной линии, различающиеся морфологически и образующиеся последовательно в каждой линии, начинающейся с коммитированной унипотентной клетки и завершающейся формированием зрелой клетки крови.
ЭРИТРОПОЭЗ
Начало эритроидного ряда - взрывообразующая единица эритропоэза (BFU-E) (Burst Forming Unit-E), происходящая из CFU-GEMM. Из BFU-E образуется унипотентная колониеобразующая единица эритропо-
эза (CFU-E). На дальнейших стадиях эритропоэза из CFU-E дифференцируются проэритробласты, эритробласты, ретикулоциты и эритроциты (рис. 6-20). Длительность эритропоэза (от стволовой клетки до эритроцита) - 2 недели.
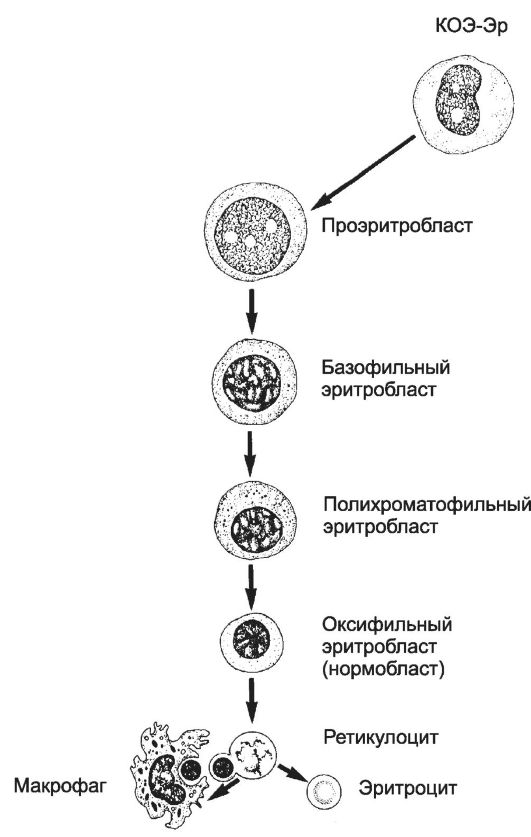 Рис. 6-20. Эритропоэз. Унипотентная
колониеобразующая единица эритропоэза CFU-E даёт начало
проэритробласту. Дальнейшая дифференцировка приводит к уменьшению
размеров клеток и количества органелл, но к увеличению содержания
гемоглобина и потере ядра. При этом из проэритробласта последовательно
дифференцируются базофильный, полихроматофильный, оксифильный
(нормобласт) эритробласт, ретикулоцит, эритроцит. Ранние нормобласты
выталкивают пикнотическое ядро, фагоцитируемое макрофагом. [17]
Рис. 6-20. Эритропоэз. Унипотентная
колониеобразующая единица эритропоэза CFU-E даёт начало
проэритробласту. Дальнейшая дифференцировка приводит к уменьшению
размеров клеток и количества органелл, но к увеличению содержания
гемоглобина и потере ядра. При этом из проэритробласта последовательно
дифференцируются базофильный, полихроматофильный, оксифильный
(нормобласт) эритробласт, ретикулоцит, эритроцит. Ранние нормобласты
выталкивают пикнотическое ядро, фагоцитируемое макрофагом. [17]
Стадии эритропоэза
Взрывообразующая единица эритропоэза (BFU-E) и унипотентная колониеобразующая единица эритропоэза (CFU-E). Отличия взрывообразующей единицы эритропоэза (BFU-E) от унипотентной колониеобразующей единицы эритропоэза (CFU-E) состоят в том, что первая реагируют на ИЛ3, но не чувствительна к эритропоэтину, тогда как пролиферация и дифференцировка CFU-E зависит от эритропоэтина. От клеток в состоянии терминальной дифференцировки BFU-E отделена 12 клеточными поколениями, а от стадии CFU-E до зрелых клеток проходит шесть или меньше делений.
Проэритробласты (рис. 6-20) - первые морфологически опознаваемые предшественники эритроцитов - крупные клетки (диаметр 20- 25 мкм) с многочисленными органеллами, но без гемоглобина (Hb). Бледное ядро расположено центрально. Объём цитоплазмы составляет около 20% общего объёма клетки; в ней присутствует довольно много полирибосом, чем обусловлена базофилия клетки. Проэритробласты подвергаются многократным митозам.
Эритробласты. На дальнейших стадиях дифференцировки происходят уменьшение размера клетки, конденсация хроматина и уменьшение диаметра ядра, прогрессирующая потеря органелл и РНК, постепенное увеличение содержания Hb, элиминация ядра. Последовательно различают эритробласты базофильные, полихроматофильные и оксифильные (нормобласты).
• Базофильный эритробласт несколько меньше (диаметр 16-18 мкм) проэритробласта, содержит ядро с более плотным хроматином. Цитоплазма более базофильна. Клетка сохраняет способность к митозу и активно синтезирует Hb, содержит хорошо развитый белоксинтезирующий аппарат, осуществляющий синтез глобинов для построения Hb. При этом происходит опосредуемый рецепторами эндоцитоз связанного с железом трансферрина. Железо поступает в эритробласт, а свободный трансферрин возвращается в плазму.
• Полихроматофильный эритробласт - клетка диаметром 12-15 мкм, содержит значительное количество Hb. Серый тон цитоплазмы обусловлен базофильным окрашиванием рибосом и оксифильным окрашиванием Hb. Размеры ядра уменьшаются. Клетки продолжают синтезировать Hb и могут делиться.
• Оксифильный эритробласт (нормобласт) имеет небольшие размеры (диаметр 10- 12 мкм) и ацидофильную цитоплазму со следами базофилии. Ядро небольшое, содержит конденсированный хроматин. На этой стадии эритроидные клетки утрачивают способность к делению и выталкивают пикнотическое (дегенерирующее) ядро. Белоксинтезирующий аппарат почти полностью дезинтегрируется.
Ретикулоциты (диаметр 6-8 мкм) содержат остатки рибосом и РНК, формирующие сетеподобные структуры голубого цвета, видимые при окрашивании крезиловым фиолетовым или метиленовым синим. Ретикулоциты выходят в кровоток и составляют до 1% общего числа циркулирующих эритроцитов. После выхода в кровоток в течение первых
24-48 часов ретикулоцит завершает созревание и становится эритроцитом. При этом клетка приобретает форму двояковогнутого диска, а последние сохранившиеся органеллы разрушаются ферментами.
Эритропоэтин
Интенсивность эритропоэза контролирует эритропоэтин. Основной стимул для выработки эритропоэтина - гипоксия (снижение рО2 в тканях, в т.ч. зависящее от числа циркулирующих эритроцитов). Уменьшение рО2 в почке (ренальная гипоксия) стимулирует её интерстициальные клетки к увеличению синтеза и секреции эритропоэтина. Эритропоэтин усиливает пролиферацию колониеобразующей единицы эритропоэза (CFU-E) в костном мозге, что приводит к увеличению количества образующихся эритроцитов и, соответственно, росту рО2 в тканях.
ГРАНУЛОЦИТОПОЭЗ
Гранулоциты образуются в костном мозге. Нейтрофилы происходят из полипотентной колониеобразующей единицы нейтрофилов и мо- ноцитов/макрофагов (CFU-GM), а базофилы и эозинофилы - из унипотентных колониеобразующих единиц базофилов (CFU-B) и эозинофилов (CFU-Eo), соответственно. По мере дифференцировки размеры клеток уменьшаются, хроматин конденсируется, изменяется форма ядра, в цитоплазме накапливаются гранулы (рис. 6-23). При развитии гранулоцита можно выделить 6 морфологически различимых стадий: миелобласт, промиелоцит, миелоцит, метамиелоцит, палочкоядерный и сегментоядерный гранулоциты. Специфические гранулы появляются на стадии миелоцитов; с этого момента клетки называют в соответствии с типом образующихся из них зрелых гранулоцитов. Клеточные деления прекращаются на стадии метамиелоцита. Миелобласт - малодифференцированная клетка диаметром около 15 мкм. Крупное округлое или овальное ядро расположено эксцентрично, содержит 1-3 ядрышка. Цитоплазма слегка базофильна (бледно-голубая), лишена гранул.
Промиелоцит. Миелобласты дают начало промиелоцитам - крупным клеткам (15-24 мкм), содержащим более конденсированный хроматин. Округлое ядро расположено эксцентрично. Цитоплазма содержит азурофильные гранулы.
Миелоцит. Размеры клетки меньше (12-16 мкм), появляется значительное количество специфических гранул, что позволяет различить 3 типа миелоцитов: нейтрофильный, эозинофильный и базофильный. Образование и накопление гранул продолжается в течение последующих трёх клеточных делений. Ядро постепенно приобретает бобовидную форму, хроматин становится конденсированнее.
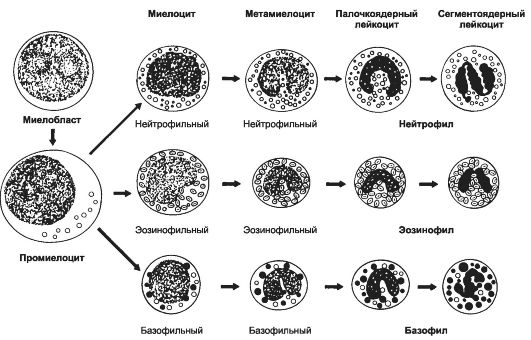 Рис. 6-23. Гранулоцитопоэз. В
ходе дифференцировки предшественников гранулоцитов вьщеляют:
миелобласт, промиелоцит, миелоцит, метамиелоцит, палочкоядерный и
сегментоядерный гранулоцит. По мере дифференцировки уменьшаются размеры
клетки, появляются гранулы в цитоплазме, уплотняется ядро и изменяется
его форма (от округлой к сегментированной). [17]
Рис. 6-23. Гранулоцитопоэз. В
ходе дифференцировки предшественников гранулоцитов вьщеляют:
миелобласт, промиелоцит, миелоцит, метамиелоцит, палочкоядерный и
сегментоядерный гранулоцит. По мере дифференцировки уменьшаются размеры
клетки, появляются гранулы в цитоплазме, уплотняется ядро и изменяется
его форма (от округлой к сегментированной). [17]
Метамиелоцит. В результате делений миелоцитов образуются нейтрофильный, эозинофильный и базофильный метамиелоциты. Размеры этих клеток ещё меньше (12-14 мкм); содержание специфических гранул значительно больше, чем на предыдущей стадии. В ядре появляются глубокие вырезки, хроматин ещё более конденсирован. Способность к митозу утрачивается.
Палочкоядерный гранулоцит. Метамиелоциты дифференцируются в палочкоядерные гранулоциты - клетки, непосредственно предшествующие зрелым формам. Их диаметр составляет 10-12 мкм, ядро имеет подковообразную форму. Эти клетки уже могут выходить в кровоток и составляют 3-5% общего количества циркулирующих лейкоцитов. Сегментоядерный гранулоцит. Палочкоядерные гранулоциты дифференцируются в зрелые формы - сегментоядерные. Сегментированное ядро содержит плотный хроматин.
МОНОЦИТОПОЭЗ
Моноциты и гранулоциты (нейтрофилы) имеют общую клетку-предшественницу - колониеобразующую единицу гранулоцитов (нейтрофилов) и моноцитов (CFU-GM), образующуюся из полипотентной колониеобразующей единицы миелопоэза (CFU-GEMM). CFU-GM даёт начало унипотентным колониеобразующим единицам моноцитов (CFU-M) и гранулоцитов (нейтрофилов) (CFU-G). При развитии моноцитов выделяют две стадии - монобласт и промоноцит. До достижения стадии зрелого моноцита клетки проходят три деления. Постепенно уменьшается размер клеток, в ядре появляются выемки. Все зрелые моноциты покидают костный мозг вскоре после формирования. В течение 2-4 суток моноциты находятся в кровотоке, а затем мигрируют в ткани.
Дифференцировка моноцитов. CD14+-моноциты выходят из кровотока в ткани, где дифференцируются в дендритные клетки и макрофаги, совокупность которых (вместе с моноцитами) составляет систему мононуклеарных фагоцитов. Дендритные антиген-представляющие клетки расположены в коже (внутриэпидермальные дендроциты), фолликулах лимфатических узлов, селезёнки (фолликулярные дендритные клетки). Макрофаги принадлежат к гетерогенной популяции клеток (гистиоциты, звездчатые макрофаги печени, остеокласты, микроглия), экспрессирующих фенотипы, различающиеся по морфологическим и функциональным свойствам.
ТРОМБОЦИТОПОЭЗ
Тромбоцитам дают начало самые крупные (до 100 мкм) клетки костного мозга - мегакариоциты (см. рис. 6-16), их предшественник -
мегакариобласт - потомок унипотентной клетки-предшественницы мегакариоцитов (CFU-Meg), берущей начало от полипотентной колониеобразующей единицы миелопоэза (CFU-GEMM). Для мегакариоцита характерно полиплоидное и дольчатое ядро с диффузно распределённым хроматином. Цитоплазма слабо базофильна, содержит мелкие гранулы и демаркационные мембраны - систему взаимосвязанных пузырьков и трубочек, связанных с клеточной мембраной. Демаркационные мембраны выполняют разграничительную функцию при формировании будущих кровяных пластинок (тромбоцитов) в составе тромбоцитарных полей. Таким образом, тромбоциты формируются путём фрагментации цитоплазмы мегакариоцита (рис. 6-25).
ЛИМФОЦИТОПОЭЗ
Из стволовой кроветворной клетки (CFU-blast) происходит полипотентная колониеобразующая единица лимфоцитопоэза (CFU-Ly). B-лимфоциты образуются в костном мозге, созревание Т-лимфоцитов происходит в тимусе. При образовании лимфоцитов выделяют две ста-
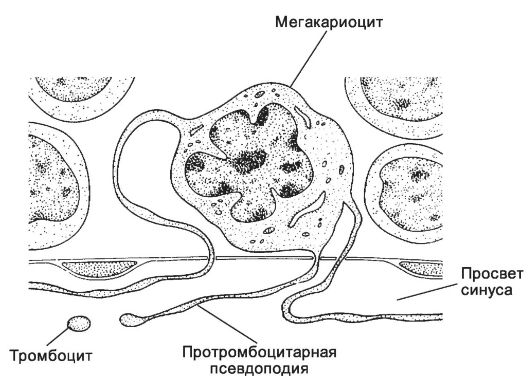 Рис. 6-25. Образование тромбоцитов. Находящийся
в костном мозге мегакариоцит образует содержащие тромбоцитарные поля
протромбоцитарную псевдоподию. Последняя проникает сквозь стенку синуса в
его просвет. От псевдоподии отделяются тромбоциты и поступают в
кровоток. [17]
Рис. 6-25. Образование тромбоцитов. Находящийся
в костном мозге мегакариоцит образует содержащие тромбоцитарные поля
протромбоцитарную псевдоподию. Последняя проникает сквозь стенку синуса в
его просвет. От псевдоподии отделяются тромбоциты и поступают в
кровоток. [17]
дии - лимфобласт и пролимфоцит. Лимфобласт намного крупнее зрелого лимфоцита. Главная особенность лимфоцитопоэза - постепенное и значительное уменьшение клеточного объёма. Однако, многие циркулирующие лимфоциты реагируют на антигенную стимуляцию увеличением объёма клетки, приобретая морфологию лимфобласта. В отличие от других клеток крови, лимфоциты могут пролиферировать и вне костного мозга. Это происходит в тканях иммунной системы в ответ на антигенную стимуляцию.
Дифференцировка B-лимфоцитов. Сигнал для начала дифференцировки поступает от стромальных клеток костного мозга. Выделяют следующие стадии созревания B-лимфоцита; ранний про-B-лимфоцит (проот англ. progenitor, предшественник) → поздний про-B-лимфоцит → большой пре-В-лимфоцит → малый пре-B-лимфоцит → незрелый B- лимфоцит → зрелый B-лимфоцит. Активированный зрелый B-лим- фоцит дифференцируется в лимфобласт и далее - в плазматическую клетку, секретирующую иммуноглобулины.
Дифференцировка T-лимфоцитов происходит в тимусе из клеток-предшественниц, поступающих в вилочковую железу из костного мозга (см. подробнее в главе 11). Зрелые T-лимфоциты покидают тимус, циркулируют в периферической крови и лимфе и оседают в лимфоидных органах.
NK-клетки образуются из полипотентной колониеобразующей единицы лимфоцитопоэза (CFU-Ly) в костном мозге.
ФАКТОРЫ ГЕМОПОЭЗА
Образование клеток крови стимулируют гемопоэтические факторы роста - фактор стволовых клеток (SCF, Stem Cell Factor), колониестимулирующие факторы (CSF) (Colony Stimulating Factor), интерлейкины, эритропоэтин, лептин, тромбопоэтин. На кроветворение влияют фолиевая кислота и витамин B12, участвующие в синтезе ДНК в ходе массового образования новых клеток крови. Дифференцировку кроветворных клеток контролируют транскрипционные факторы.
Возрастные изменения крови
Эритроциты
При рождении и в первые часы жизни количество эритроцитов в крови повышено и составляет 6,0-7,0х1012/л. У новорождённых наблюдают анизоцитоз с преобладанием макроцитов, а также повышенное содержание ретикулоцитов. В течение первых суток постнатального периода количество эритроцитов снижается, к 10-14 суткам до-
стигает уровня взрослого, но продолжает снижаться. Минимальный показатель наблюдается на 3-6-м месяцах жизни (физиологическая анемия), когда снижен уровень эритропоэтина. Это связано с уменьшением синтеза эритропоэтина в печени и началом его выработки в почке. На 3-4-м году жизни количество эритроцитов снижено (ниже, чем у взрослого), т.е. в 1 л их содержится менее 4,5х1012. Содержание эритроцитов достигает нормы взрослого в период полового созревания.
Лейкоциты
Количество лейкоцитов у новорождённых повышено и составляет 10- 30х109/л. Число нейтрофилов составляет 60,5%, эозинофилов - 2%, базофилов - 0,2%, моноцитов - 1,8%, лимфоцитов - 24%. В течение первых двух недель жизни количество лейкоцитов снижается до 9-15х109/л, к 4 годам уменьшается до 7-13х109/л, а к 14 годам достигает уровня, характерного для взрослого. Соотношение нейтрофилов и лимфоцитов меняется, что обусловливает возникновение так называемых физиологических перекрестов.
• Первый перекрест. У новорождённого соотношение содержания этих клеток такое же, как у взрослого. В последующем содержание нейтрофилов уменьшается, а лимфоцитов возрастает, так что на 3-4 сутки их количество уравнивается. В дальнейшем количество нейтрофилов продолжает снижаться и к 1-2 годам достигает 25%. В этом же возрасте количество лимфоцитов составляет 65%.
• Второй перекрест. В течение следующих лет число нейтрофилов постепенно повышается, а лимфоцитов - понижается, так что у четырёхлетних детей эти показатели снова уравниваются и составляют по 35% общего количества лейкоцитов. Количество нейтрофилов продолжает повышаться, а лимфоцитов - снижаться, и к 14 годам эти показатели соответствуют таковым у взрослого.
СОЕДИНИТЕЛЬНЫЕ ТКАНИ
Соединительные ткани обеспечивают поддержание целостности других тканей, формируют строму органов, содержат кровеносные и лимфатические сосуды, участвуют в трофическом обеспечении всех тканей и органов. Среди соединительных тканей выделяют волокнистые ткани (рыхлые и плотные) и ткани со специальными свойствами (например, жировая, ретикулярная). В большинстве органов и между ними рыхлая соединительная ткань выступает в качестве упаковки паренхимы, организуя ложе для её гистологических элементов (строма органов). Плотные соединительные ткани обеспечивают прочность кожи, образуют капсулы органов, позволяют выдерживать значительные механические нагрузки (например, связки и сухожилия).
Межклеточное вещество
В состав всех соединительных тканей входит значительный объём межклеточного вещества (внеклеточный матрикс). Матрикс состоит из основного вещества и погружённых в него волокон различного типа.
ОСНОВНОЕ ВЕЩЕСТВО
Основное вещество - аморфный материал со свойствами геля. Тканевая жидкость связывается с компонентами основного вещества, формируя среду для прохождения молекул через соединительную ткань и для обмена веществ с кровью. Основное вещество содержит гликозаминогликаны, протеогликаны и гликопротеины.
• Гликозаминогликаны - полисахариды, построенные из повторяющихся дисахаридных единиц, одна из которых - обычно уроновая кислота, а другая - аминосахар (N-ацетилгликозамин, N-ацетилгалактозамин). Гликозаминогликаны - кислые (отрицательно заряженные) соединения. Молекулы гликозаминогликанов гидрофильны, они связывают большое количество молекул воды и ионов. Связанные между собой крупные молекулы гликозаминогликанов образуют гель, через который диффундируют метаболиты. К гликозаминогликанам относятся гиалуроновая кислота, хондроитинсульфат, дерматансульфат, кератансульфат, гепарансульфат и гепарин (гепаринсульфат).
• Протеогликаны - волокнистые белки с ковалентно присоединёнными к ним гликозаминогликанами. К протеогликанам, в частности, относятся версикан, агрекан, нейрокан и бревикан.
• Гликопротеины состоят из полипептидных цепей, соединённых с разветвлённы- ми полисахаридами, и связывают клетки с внеклеточным матриксом. Различают гликопротеины, формирующие волокнистые структуры (фибронектин и фибриллин), а также ряд неволокнистых белков (ламинин, тенасцин и энтактин).
ВОЛОКНА
Во внеклеточный матрикс погружены разные типы волокон: построенные из коллагенов коллагеновые и ретикулиновые волокна, а также эластические волокна (в их состав входит эластин и фибриллин).
Коллаген и коллагеновые волокна
Коллагеновые волокна - главный компонент большинства соединительных тканей, а коллаген - наиболее распространённый белок. Коллагены. Молекула коллагена - спираль из трёх про-a-цепей. Длина подобной спирали - 300 нм, диаметр - 1,5 нм. Все типы коллагена содержат области с повторяющейся последовательностью из трёх аминокислот с глицином в третьем положении. Первая аминокислота в такой последовательности может быть любой, вторая - пролин, гидроксипролин или лизин. Благодаря обилию поперечных связей между остатками лизина, коллагеновые волокна обладают высокой прочностью. Известно не менее 27 типов коллагена, по-разному распределяющихся в органах и тканях (табл. 6-11).
Таблица 6-11. Распределение разных коллагенов в тканях и органах
 Образование коллагеновых волокон. На внутриклеточном этапе в
гранулярной эндоплазматической сети происходит синтез и сборка
про-а-цепей. Далее в цистернах комплекса Гольджи осуществляется
гидроксилирование и гликозилирование полипептидов, в результате чего
образуются спирали из трёх проа-цепей (проколлаген). Молекулы проколлагена накапливаются в секреторных гранулах и выделяются во внеклеточное пространство. Вне клетки от молекул проколлагена отщепляются концевые пептиды, образуется тропоколлаген (коллаген).
Из тропоколлагена происходит сборка коллагеновых фибрилл, а из
параллельно расположенных фибрилл - коллагенового волокна.
Образование коллагеновых волокон. На внутриклеточном этапе в
гранулярной эндоплазматической сети происходит синтез и сборка
про-а-цепей. Далее в цистернах комплекса Гольджи осуществляется
гидроксилирование и гликозилирование полипептидов, в результате чего
образуются спирали из трёх проа-цепей (проколлаген). Молекулы проколлагена накапливаются в секреторных гранулах и выделяются во внеклеточное пространство. Вне клетки от молекул проколлагена отщепляются концевые пептиды, образуется тропоколлаген (коллаген).
Из тропоколлагена происходит сборка коллагеновых фибрилл, а из
параллельно расположенных фибрилл - коллагенового волокна.
Фибриллин, эластин и эластические структуры
Эластические структуры (волокна и мембраны) обладают выраженными эластическими свойствами. Эластические волокна присутствуют в эластическом хряще, коже, лёгких, кровеносных сосудах. Окончатые эластические мембраны характерны для крупных артерий. Эластическое волокно (ветвящаяся нить диаметром 0,2-1,0 мкм) состоит из фибриллина и аморфного эластина. Фибробласты и ГМК синтезируют коллаген, эластин и фибриллин в цистернах гранулярной эндоплазматической сети. В комплексе Гольджи происходит упаковка полипептидов в секреторные гранулы, выделяемые во внеклеточную среду, где происходит формирование межмолекулярных связей между молекулами эластина. В результате появляется упругая резиноподобная сеть молекул, способная после деформации восстанавливать исходную форму. Эта сеть и составляет основу эластических структур. Микрофибриллы фибриллина образуются ещё до сборки эластина. После формирования каркаса из фибриллина эластин организуется в волокно.
Коллаген и ретикулиновые волокна
Ретикулиновые волокна - тонкие нити диаметром 0,5-2,0 мкм, состоящие из коллагена типа III, связанного с гликопротеинами и протеогликанами.
БАЗАЛЬНАЯ МЕМБРАНА
Базальная мембрана - особый вид внеклеточного матрикса, имеет вид листа или пластинки толщиной 20-200 нм и состоит из специальных белков, служащих для соединения клеток различного типа (эпителиальных, мышечных, шванновских) с окружающей соединительной тканью. Базальная мембрана состоит из двух слоев - lamina lucida (светлого слоя) толщиной 10-50 нм, примыкающего к плазмолемме, и lamina densa (электронно-плотного слоя, варьирующего по толщине). Основа lamina lucida и lamina densa - трёхмерная сеть, состоящая преимущественно из коллагена типов IV, XV и XVIII, с которым связаны ламинин, энтактин и гепарансульфат протеогликаны.
• Функции. Базальная мембрана объединяет клетки, способствуя их организации в пласт, препятствует инвазии эпителиальных клеток в подлежащую соединительную ткань, фильтрует макромолекулы (например, в почке lamina densa задерживает молекулы с Mr более 50 кД).
• Якорные волокна. Большинство базальных мембран прочно соединено с рыхлой соединительной тканью. Базальные мембраны многослойного эпителия кожи, пищевода, роговицы и амниона короткими (якорными) волокнами связаны с якорными пластинками в подлежащей соединительной ткани. Якорные волокна состоят в основном из коллагена типа VII, якорные пластинки содержат коллаген типа IV. Якорные волокна также соединяют между собой якорные пластинки в строме. В итоге образуется плотная сеть переплетённых волокон, стабилизирующая базальную мембрану в тканях, подверженных значительным воздействиям на сдвиг.
Клетки соединительных тканей
Клетки соединительных тканей разнообразны. Это фибробласты, фиброциты, хондробласты, хондроциты, остеобласты, остеоциты, макрофаги, тучные клетки, лейкоциты, плазмоциты, перициты, адипоциты.
Клетки соединительных тканей подразделяют на две группы - резиденты и иммигранты.
• Резиденты - фибробласты и фиброциты (волокнистая соединительная ткань), хондробласты и хондроциты (хрящевая ткань), остеобласты и остеоциты (костная ткань), тучные клетки, адипоциты, макрофаги.
• Иммигранты - лейкоциты (нейтрофилы, эозинофилы, базофилы, моноциты, лимфоциты). При возникновении очагов воспаления эти клетки выходят из кровотока в соединительную ткань. Лимфоциты, осуществляющие иммунологический надзор, постоянно циркулируют между кровью, соединительными тканями, лимфой.
В зависимости от выполняемой функции клетки соединительных тканей можно разделить на ответственные за синтез молекул внеклеточного вещества, ответственные за накопление и метаболизм жира, клетки с защитными функциями.
Фибробласты и фиброциты
Фибробласт (рис. 6-31А) секретирует компоненты внеклеточного матрикса, способен к пролиферации и миграции. Фибробласт - упло- щённая клетка звездчатой формы, образует широкие клиновидные отростки; содержит крупное овальное ядро с несколькими ядрышками. Размер клетки изменчив. Фибробласт интенсивно синтезирует белок, поэтому его цитоплазма содержит в большом количестве цистерны гранулярной эндоплазматической сети, хорошо выраженный комплекс Гольджи, много митохондрий. Имеются лизосомы и секреторные гранулы, гликоген, многочисленные микрофиламенты и
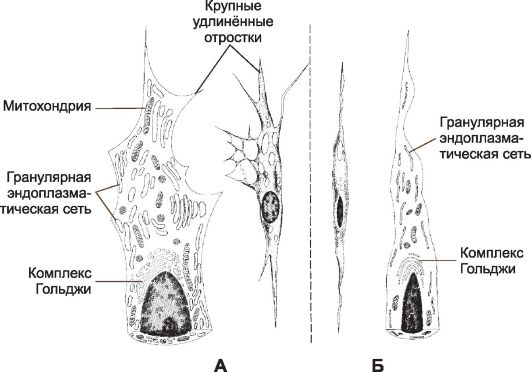 Рис. 6-31. Фибробласт (А) и фиброцит (Б). Фибробласт
(активная форма клетки) содержит хорошо выраженные органеллы:
гранулярную эндоплазматическую сеть, комплекс Гольджи, митохондрии.
Фибробласт образует крупные удлинённые отростки. В фиброците органелл
значительно меньше, клетка лишена отростков и имеет веретеновидную
форму. [17]
Рис. 6-31. Фибробласт (А) и фиброцит (Б). Фибробласт
(активная форма клетки) содержит хорошо выраженные органеллы:
гранулярную эндоплазматическую сеть, комплекс Гольджи, митохондрии.
Фибробласт образует крупные удлинённые отростки. В фиброците органелл
значительно меньше, клетка лишена отростков и имеет веретеновидную
форму. [17]
микротрубочки. К фибробластам относят также липофибробласты и миофибробласты (см. главу 7).
Фибробласты синтезируют коллагены, эластин, фибронектин, гликозаминогликаны, протеогликаны и другие компоненты внеклеточного матрикса. Фибробласты вырабатывают различные цитокины - колониестимулирующий фактор гранулоцитов и макрофагов (GM-CSF), колониестимулирующий фактор гранулоцитов (G-CSF) и колониестимулирующий фактор макрофагов (M-CSF). Фибробласты костного мозга секретируют ИЛ3 и ИЛ7.
Фиброцит (рис. 6-31Б) - зрелая форма фибробласта, присутствующая в плотной оформленной соединительной ткани. Фиброцит имеет веретенообразную форму. Уплотнённое ядро вытянуто и расположено вдоль клетки. Имеются рассеянные цистерны гранулярной эндоплазматической сети, небольшое количество митохондрий. Функция фиброцита заключается в поддержании тканевой структуры путём непрерывного (хотя и медленного) обновления компонентов внеклеточного матрикса.
Липофибробласты содержат многочисленные жировые капли, гранулы гликогена, сократительные белки, накапливают ретиноиды, присутствуют в интерстиции межальвеолярных перегородок лёгких и некоторых других органов. Липофибробласты сходны с адипоцитами, ГМК, миофибробластами, перицитами и жиронакапливающими клетками печени.
Макрофаги
Макрофаг - дифференцированная форма моноцитов. Макрофаги - профессиональные фагоциты, они найдены во всех тканях и органах. Это очень мобильная популяция клеток. Продолжительность жизни - месяцы. Тканевые макрофаги сохраняют некоторую способность к делению. Макрофаги подразделяют на резидентные и подвижные. Среди резидентных макрофагов различают свободные (имеющие округлую форму) и фиксированные макрофаги - звездообразной формы клетки, прикрепляющиеся своими отростками к внеклеточному матриксу или другим клеткам. Подвижные макрофаги - популяция переселяющихся макрофагов.
Строение макрофага (рис. 6-32) зависит от его активности и локализации. Диаметр клетки - около 20 мкм. Ядро неправильной формы, с углублениями. В цитоплазме присутствуют митохондрии, свободные рибосомы, хорошо выраженный комплекс Гольджи, мультивезикулярные тельца, гранулярная эндоплазматическая сеть, лизосомы, фаголизосомы и остаточные тельца, материал которых может выделяться из макрофага путём экзоцитоза. В лизосомах присутствуют бактерицидные агенты (миелопероксидаза, лизоцим, протеиназы, кислые гидролазы, катионные белки, лактоферрин, супероксид дисмутаза - фермент, способствующий образованию H2O2, OH-, O2-).
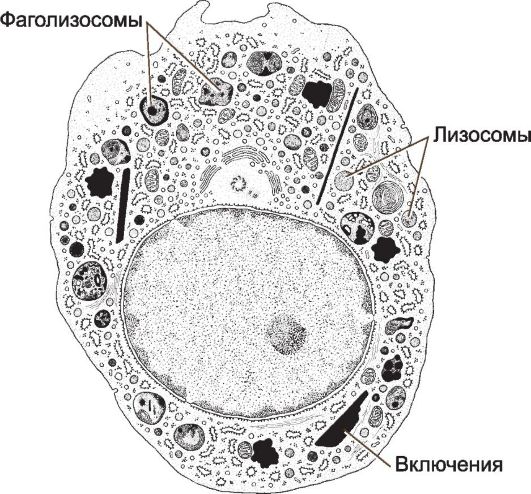 Рис. 6-32. Макрофаг. Ядро
неправильной формы, с выемками. В цитоплазме присутствуют рибосомы,
митохондрии, мультивезикулярные тельца. Хорошо развиты комплекс Гольджи и
гранулярная эндоплазматическая сеть. Имеются многочисленные лизосомы.
Характерно наличие фагосом, фаголизосом, остаточных телец. Клетка
образует цитоплазматические отростки, участвующие в миграции и
фагоцитозе. [17]
Рис. 6-32. Макрофаг. Ядро
неправильной формы, с выемками. В цитоплазме присутствуют рибосомы,
митохондрии, мультивезикулярные тельца. Хорошо развиты комплекс Гольджи и
гранулярная эндоплазматическая сеть. Имеются многочисленные лизосомы.
Характерно наличие фагосом, фаголизосом, остаточных телец. Клетка
образует цитоплазматические отростки, участвующие в миграции и
фагоцитозе. [17]
Под плазмолеммой в большом количестве присутствуют актиновые микрофиламенты, микротрубочки, промежуточные филаменты, необходимые для миграции и фагоцитоза.
Факторы хемотаксиса. Макрофаги мигрируют по градиенту концентрации некоторых факторов, вырабатываемых другими клетками. Факторы хемотаксиса для макрофагов секретируют активированные T-лимфоциты, мигрировавшие в очаг воспаления нейтрофилы. Факторами хемотаксиса для макрофагов служат также компоненты комплемента C5a, C3 и лейкотриен LTB4, бактериальные продукты, лимфокины из активированных лимфоцитов, фрагменты фибронектина. Функции макрофага. Макрофаги - профессиональные фагоциты. Макрофаги фагоцитируют деградированные белки, старые и дефектные эритроциты и другие клетки крови; обломки клеток и тканевого матрикса. Неспецифический фагоцитоз характерен для альвеолярных макрофагов, захватывающих пылевые частицы различной природы, сажу и т.п. Специфический фагоцитоз происходит при взаимодействии макрофага с опсонизированной бактерией.
Система мононуклеарных фагоцитов. Макрофаги соединительной ткани - часть системы мононуклеарных фагоцитов. Клетки системы мононуклеарных фагоцитов отличаются от других фагоцитирующих клеток по трём критериям: имеют морфологию макрофагов, происходят из моноцитов или их предшественников в костном мозге, их фагоцитарную активность модулируют Ig и компоненты комплемента. В систему мононуклеарных фагоцитов входят гистиоциты (тканевые макрофаги), альвеолярные макрофаги, остеокласты, звездчатые макрофаги печени (звездчатые макрофаги), клетки Лангерханса эпидермиса (внутриэпидермальные дендроциты) , клетки Хофбауэра хориона, гигантские клетки инородных тел и, вероятно, клетки микроглии ЦНС.
Тучная клетка
Тучные клетки морфологически и функционально сходны с базофилами крови, но это различные клеточные типы. Тучная клетка, как и базофил, происходит из предшественника в костном мозге, но окончательную дифференцировку проходит в соединительной ткани. Тучные клетки - резидентные клетки соединительной ткани. Их особенно много в коже, в слизистой оболочке органов дыхательной и пищеварительной систем, вокруг кровеносных сосудов. Тучная клетка (рис. 6-34) содержит многочисленные модифицированные лизосомы - крупные метахроматические гранулы. В мембрану клетки встроены различные рецепторы, в том числе рецепторы к Fc-фрагменту IgE. Гранулы тучной клетки. Тучные клетки синтезируют и накапливают в гранулах разнообразные биологически активные вещества, медиаторы и ферменты: гепарин (гепаринсульфат), гистамин, триптазу, химазу, эластазу, дипептидазу, активатор плазминогена, кислые гидролазы, фактор хемотаксиса эозинофилов (ECF), фактор хемотаксиса нейтрофилов (NCF). Основной компонент гранул тучных клеток - отрицательно заряженный сульфатированный гликозаминогликан гепарин, синтезируемый и запасаемый исключительно тучными клетками. Гистамин вызывает сокращение ГМК, гиперсекрецию слизи, увеличение проницаемости сосудов с развитием отёка.
Функции тучной клетки. Тучная клетка участвует в воспалительных и аллергических реакциях. Активация и дегрануляция тучных клеток, как и базофилов, опосредована IgE.
Плазматическая клетка
Плазматическая клетка (плазмоцит) образуется из B-лимфоцита в результате его активации антигеном. Активированный В-лимфоцит делится около 5 дней и, образуя клон, дифференцируется в плазматическую клетку или в В-клетку памяти. Плазматические клетки продуцируют иммуноглобулины и служат главными эффекторными клетками гуморального иммунитета. Плазматическая клетка синтезирует АТ одного типа. Плазматические клетки редко встречаются в периферической крови, в основном они присутствуют в костном мозге,
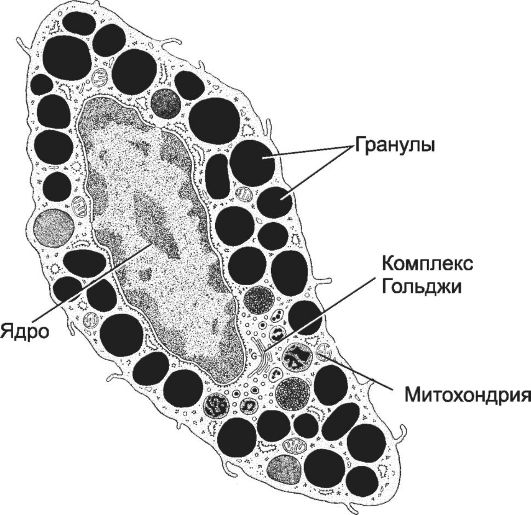 Рис. 6-34. Тучная клетка. Ядро
округлое, умеренно развиты гранулярная эндоплазматическая сеть и
комплекс Гольджи; содержит многочисленные крупные гранулы, варьирующие
по структуре и плотности. [17]
Рис. 6-34. Тучная клетка. Ядро
округлое, умеренно развиты гранулярная эндоплазматическая сеть и
комплекс Гольджи; содержит многочисленные крупные гранулы, варьирующие
по структуре и плотности. [17]
лимфатических узлах и селезёнке, а также в рыхлой соединительной ткани слизистых оболочек.
Плазматическая клетка (рис. 6-35) имеет округлую форму или форму веера, диаметр 8-15 мкм. Плазматическая клетка содержит большое овальное эксцентрически расположенное ядро с характерными глыбками гетерохроматина. Эухроматин занимает меньший объём ядра, но именно с ним связывают транскрипцию генов, кодирующих иммуноглобулины. Отношение объёма ядра к объёму цитоплазмы очень велико и колеблется от 2:1 до 1:1. В цитоплазме - хорошо развитый комплекс Гольджи и масса крупных цистерн гранулярной эндоплазматической сети, концентрически расположенных вокруг ядра. Продолжительность жизни плазматической клетки - 4-5 дней.
Перициты
Перициты - отростчатые клетки, примыкающие снаружи к капиллярам, наиболее многочисленны в посткапиллярных венулах. Овальной формы клетки образуют длинные, расположенные вдоль сосуда пер-
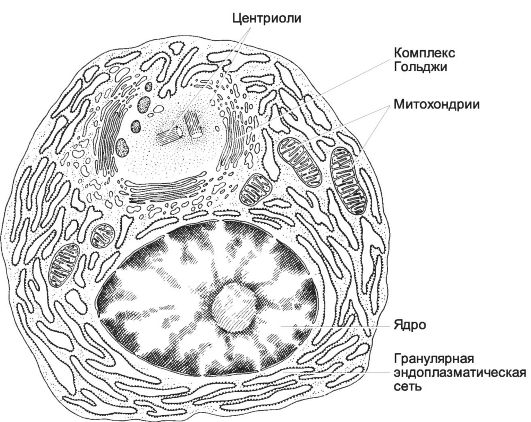 Рис. 6-35 Плазматическая клетка. Хорошо
развитые гранулярная эндоплазматическая сеть и комплекс Гольджи
свидетельствуют об активном синтезе и секреции белка. [17]
Рис. 6-35 Плазматическая клетка. Хорошо
развитые гранулярная эндоплазматическая сеть и комплекс Гольджи
свидетельствуют об активном синтезе и секреции белка. [17]
вичные отростки, от которых под прямым углом отходят более тонкие и короткие вторичные отростки, охватывающие капилляр или посткапиллярную венулу. Для перицита характерны дисковидное ядро, обычный набор органелл, мультивезикулярные тельца, микротрубочки и гликоген. В области, обращённой к стенке сосуда, цитоплазма перицита содержит пузырьки. Около ядра и в отростках присутствуют сократительные белки, в т.ч. актин и миозин. Перициты покрыты базальной мембраной, но тесно связаны с эндотелиальной клеткой, т.к. базальная мембрана между ними может и отсутствовать. Перициты имеют общие свойства с ГМК (экспрессия гладкомышечного актина, виментина) и способны сокращаться в ответ на ангиотензин II, серотонин, ацетилхолин, АТФ, эндотелин-1, регулируя просвет сосуда. При заживлении ран и восстановлении сосудов перициты дифференцируются в ГМК. Наконец, перициты участвуют в фагоцитозе остатков базальной мембраны.
Адипоциты
Среди адипоцитов различают клетки белого и клетки бурого жира. Клетка белого жира. В ходе дифференцировки в цитоплазме мезенхимной клетки появляются капельки жира, сливающиеся по мере увеличения их количества. Дифференцированный адипоцит - крупная округлая клетка диаметром до 120 мкм, содержит одну крупную каплю жира, оттесняющую на периферию цитоплазму и все органеллы. В цитоплазме, узким ободком окружающей каплю жира, находятся сплющенное ядро, свободные рибосомы, гладкая и гранулярная эндоплазматическая сеть, комплекс Гольджи и митохондрии. Адипоциты секретируют гормон лептин, взаимодействие которого с рецепторами нервных клеток вентромедиального и латерального ядер гипоталамуса ведёт к включению центральных механизмов пищевого поведения; лептин противодействует накоплению жировой ткани. Помимо лептина, адипоциты секретируют множество других биологически активных веществ и имеют рецепторы ко многим гормонам. Клетка бурого жира содержит множество мелких жировых капель и крупных митохондрий. В буром адипоците функционирует естественный механизм разобщения окислительного фосфорилирования, что биологически полезно как способ образования тепла. Бурый цвет клетки и ткани в целом обусловлен присутствием железосодержащих пигментов в митохондриях. Активированная гормон-чувствительная липаза гидролизует триглицериды в жирные кислоты и глицерол. Освобождаемые жирные кислоты метаболизируют с образованием тепла. Повышенное теплообразование объясняется наличием во внутренней мембране митохондрий трансмембранного белка термогенина. Термогенин разрешает обратный ток протонов, предварительно транспортированных в интермембранное пространство, без прохождения через систему АТФ-синтетазы. Таким образом, энергия, генерируемая протонным током, не используется для синтеза АТФ, а рассеивается в виде тепла.
Виды соединительных тканей
Различают волокнистые соединительные ткани и соединительные ткани со специальными свойствами. Волокнистые соединительные ткани (в зависимости от количества волокон и основного вещества во внеклеточном матриксе) делят на рыхлую и плотную. В свою очередь, плотная соединительная ткань делится на оформленную и неоформленную, что определяется организацией волокон во внеклеточном матриксе. К соединительным тканям со специальными свойствами относят эмбриональную (мезенхима), жировую и ретикулярную ткани.
ВОЛОКНИСТАЯ СОЕДИНИТЕЛЬНАЯ ТКАНЬ Рыхлая соединительная ткань
Рыхлая (неоформленная) соединительная ткань (рис. 6-37) находится во всех органах, образует их строму и сопровождает сосуды.
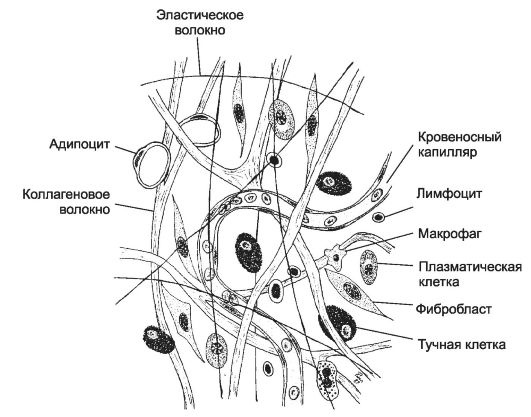 Рис. 6-37. Рыхлая соединительная ткань. Межклеточное
вещество состоит большей частью из основного вещества с хаотично
распределёнными в нём и относительно немногочисленными коллагеновыми и
эластическими волокнами. Характерно клеточное разнообразие (фибробласты,
тучные клетки, различные лейкоциты, адипоциты, макрофаги,
плазматические клетки). [17]
Рис. 6-37. Рыхлая соединительная ткань. Межклеточное
вещество состоит большей частью из основного вещества с хаотично
распределёнными в нём и относительно немногочисленными коллагеновыми и
эластическими волокнами. Характерно клеточное разнообразие (фибробласты,
тучные клетки, различные лейкоциты, адипоциты, макрофаги,
плазматические клетки). [17]
Плотные соединительные ткани
Плотная соединительная ткань содержит большое количество плотно расположенных волокон. Количество основного вещества относительно незначительно.
Плотная неоформленная соединительная ткань состоит из плотно, но беспорядочно расположенных волокон. Между волокнами присутствуют фибробласты (фиброциты), макрофаги, тучные клетки. Такая ткань характерна для собственно кожи, периоста. Плотная оформленная соединительная ткань. Волокна располагаются плотно, образуя параллельно идущие пучки. В узких пространствах между волокнами цепочками выстраиваются фиброциты. Из такой ткани образованы связки, сухожилия и фиброзные мембраны.
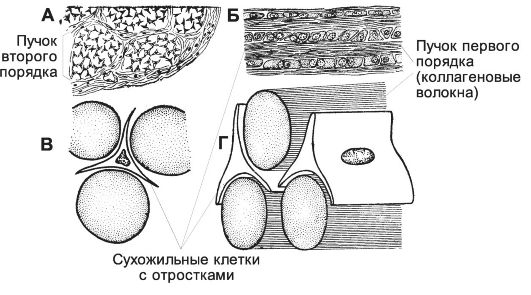 Рис. 6-38. Сухожилие. А - поперечный срез. Б - продольный срез. В и Г - схема строения сухожилия на поперечном и продольном срезах. [17]
Рис. 6-38. Сухожилие. А - поперечный срез. Б - продольный срез. В и Г - схема строения сухожилия на поперечном и продольном срезах. [17]
• Связка (например, ligamenta flava и ligamentum nuchae) состоит из эластина, формирующего толстые волокна. Между ними располагаются тонкие коллагеновые волокна и фиброциты.
• Сухожилие (рис. 6-38) состоит из коллагеновых волокон, формирующих сухожильные пучки I, II и III порядков. Между пучками I порядка расположены ряды сухожильных клеток (фиброцитов) с пластинчатыми отростками. Группы пучков I порядка, окружённые рыхлой соединительной тканью с сосудами и нервами, образуют пучки II порядка. Несколько пучков II порядка объединяются рыхлой соединительной тканью в пучки III порядка. При повреждении сухожилия активированные фиброциты и фибробласты синтезируют коллаген для новых волокон.
• Фиброзные мембраны. Пучки коллагеновых волокон и лежащие между ними фиброциты расположены слоями. В каждом слое волнообразные пучки коллагеновых волокон проходят параллельно в одном направлении, отличном от направлений в соседних слоях. Отдельные пучки волокон переходят из одного слоя в другой, связывая их между собой. К фиброзным мембранам относят фасции, апоневрозы, сухожильный центр диафрагмы, капсулы внутренних органов, твёрдую мозговую оболочку, склеру.
СОЕДИНИТЕЛЬНЫЕ ТКАНИ СО СПЕЦИАЛЬНЫМИ СВОЙСТВАМИ
К соединительным тканям со специальными свойствами отнесены мезенхима, слизистая соединительная ткань, ретикулярная и жировая ткани.
Мезенхима - эмбриональная соединительная ткань - источник клеток всех соединительных тканей. Мезенхимные клетки имеют звездчатую или веретенообразную форму с нежными ветвящимися отростками, формирующими сеть. Гелеобразный внеклеточный материал состоит почти исключительно из основного вещества и минимального количества ретикулиновых волокон.
Слизистая соединительная ткань, или эмбриональная студенистая соединительная ткань присутствует в пупочном канатике, окружая пупочные артерии и вену. Эта ткань состоит из гелеподобного основного вещества, часто называемого вартоновой студенью (вартонов студень). Она заполняет большие межклеточные пространства между тонкими коллагеновыми волокнами (тип I и III) и фибробластоподобными клетками.
Ретикулярная ткань (рис. 6-40) имеет сетевидное строение и состоит из ретикулиновых волокон (коллаген типа III) и ретикулярных клеток, имеющих длинные отростки. Ретикулярные клетки вместе с ретикулиновыми волокнами образуют рыхлую сеть (строму) костного мозга, лимфатических узлов, селезёнки и миндалин.
Стволовая мезенхимная клетка красного костного мозга относится к самообновляющейся клеточной популяции, из которой образуются стромальные клетки, экспрессирующие маркёры стволовых клеток. Стволовая мезенхимная клетка, а также
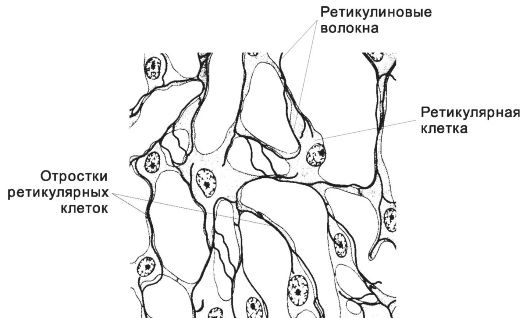 Рис. 6-40. Ретикулярная ткань состоит из ретикулярных клеток и ретикулиновых волокон. [17]
Рис. 6-40. Ретикулярная ткань состоит из ретикулярных клеток и ретикулиновых волокон. [17]
её дочерние стромальные клетки могут дифференцироваться в жировые, костные, хрящевые, мышечные и ретикулярные клетки.
Жировая ткань встречается во многих органах. Различают белую и бурую жировую ткань.
• Белый жир составляет почти всю жировую ткань организма. Участвует в поглощении из крови, синтезе, хранении и мобилизации нейтральных липидов (триглицеридов). На распределение жировой ткани в организме влияют половые гормоны и гормоны коры надпочечников. Жировые клетки (адипоциты) образуют скопления (дольки), разделённые перегородками из рыхлой соединительной ткани. В последней в жировую ткань проходят кровеносные сосуды и нервы. Отдельные жировые клетки окружены сетью ретикулиновых и коллагеновых волокон. В соединительнотканных перегородках присутствуют фибробласты и тучные клетки.
• Бурый жир у новорождённого участвует в терморегуляции. У взрослого бурый жир в небольшом количестве встречается в средостении, вдоль аорты и под кожей между лопатками. Бурая жировая ткань обильно снабжена кровеносными капиллярами, образующими сеть вокруг каждого адипоцита, и имеет выраженную симпатическую иннервацию.
Пигментная ткань - волокнистая (рыхлая или плотная) соединительная ткань, содержащая большое количество пигментных клеток. Это сосудистая оболочка и радужка глаза, дерма в области околососковых кружков, мошонки, вокруг анального отверстия, родинки и родимые пятна.
СКЕЛЕТНЫЕ ТКАНИ
К скелетным (твёрдым) типам тканей внутренней среды относятся хрящевая (хрящ) и костная (кость) ткани.
Хрящевая ткань
Хрящевая ткань состоит из хрящевых клеток (хондроцитов) и межклеточного вещества - хрящевого матрикса. Различают гиалиновый, эластический и волокнистый хрящи. Хрящи не содержат кровеносных сосудов. Основные свойства хряща - прочность и упругость - определяются молекулярной организацией хрящевого матрикса. Хрящ у плода выполняет формообразующую, а в сформированном организме - опорную функции. Хрящ необходим для образования костной ткани путём энхондрального остеогенеза (образования кости на месте хряща).
Гиалиновый хрящ
Гиалиновый хрящ (рис. 6-42) локализуется в рёбрах, суставах, стенке воздухоносных путей. У плода гиалиновый хрящ формирует скелет, а в растущем организме и при переломах кости является местом образования костной ткани.
Гистогенез. Хрящ развивается из мезенхимы. Гистогенез хряща стимулируют тироксин, тестостерон и соматотропин, а угнетают кортизол, гидрокортизон и эстрадиол.
Рост хрящей происходит как изнутри (интерстициальный рост), так и от надхрящницы (аппозиционный рост). Интерстициальный рост обеспечивает пролиферация хондроцитов и увеличение объёма матрикса. Аппозиционный рост - наложение слоёв новообразованной хрящевой ткани по периферии хряща за счёт дифференцировки хрящевых клеток из хондрогенных клеток надхрящницы.
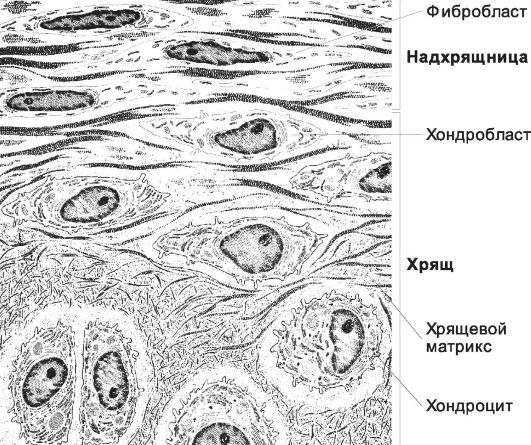 Рис. 6-42. Основные структуры хряща. Снаружи
хрящ покрыт надхрящницей. Под ней расположен молодой хрящ, а глубже -
зрелый хрящ. В хрящевой ткани присутствуют хондроциты, окружённые
хрящевым матриксом. [17]
Рис. 6-42. Основные структуры хряща. Снаружи
хрящ покрыт надхрящницей. Под ней расположен молодой хрящ, а глубже -
зрелый хрящ. В хрящевой ткани присутствуют хондроциты, окружённые
хрящевым матриксом. [17]
Надхрящница. У плода надхрящницу образует слой уплотнённой мезенхимы вокруг хрящевого зачатка. В постнатальном онтогенезе в надхрящнице различают волокнистый наружный слой (коллаген типа I) и клеточный внутренний слой, содержащий хондрогенные клетки. Кровеносные сосуды надхрящницы осуществляют питание хряща. Хондроциты (см. рис. 6-42) - окружённые хрящевым матриксом клетки хрящевой ткани. При развитии хрящевой ткани хондрогенные клетки дифференцируются в хондробласты. Хондробласты пролиферируют и начинают синтез веществ для построения хрящевого матрикса, выделяя их в составе секреторных пузырьков (матриксные пузырьки). В зрелом хряще хондроциты, расположенные ближе к поверхности хряща, имеют овальную форму, их длинная ось расположена параллельно поверхности хряща. В более глубоких слоях хондроциты образуют группы в пределах одной лакуны - так называемые изогенные группы клеток (клон).
Хрящевой матрикс содержит до 75% воды, что позволяет веществам из сосудов надхрящницы диффундировать в матриксе и осуществлять питание хондроцитов. Важное значение для обеспечения прочности и упругости хряща имеют белки хрящевого матрикса. Функционально наиболее значимы коллагены, протеогликаны и хондронектин. Вода и упругость хряща. Молекула протеогликана связывает (структурирует) большой объём воды, по массе намного превышающий её собственный. При сжатии хряща вода вытесняется из областей вокруг сульфатированных и карбоксильных групп протеогликана, группы сближаются, и силы отталкивания между их отрицательными зарядами препятствуют дальнейшему сжатию ткани. Вода возвращается на прежнее место при снятии давления. Таким образом, если коллаген определяет прочность хряща, то протеогликан - его упругость.
Суставной хрящ представлен гиалиновой хрящевой тканью, но не имеет надхрящницы, поэтому этот хрящ не способен к регенерации. Суставной хрящ состоит из трёх нечётко разграниченных зон - наружной, средней и внутренней (рис. 6-48). В наружной зоне мелкие одиночные хондроциты уплощены. В средней зоне продольные ряды клеток расположены цепочками, лежащими перпендикулярно суставной поверхности. Внутренняя зона представлена кальцинированным хрящом, содержащим мелкие хондроциты. Кость примыкает к внутренней зоне, формируя костную пластинку, поддерживающую суставной хрящ. В суставном хряще коллагеновые волокна расположены своеобразно - в виде готических арок, что способствует перераспределению давления, оказываемого на суставную поверхность. Суставной хрящ получает питание из синовиальной жидкости.
Эпифизарная пластинка (см. рис. 6-63). В росте трубчатых костей участвует эпифизарная пластинка, представленная гиалиновым хрящом. Она
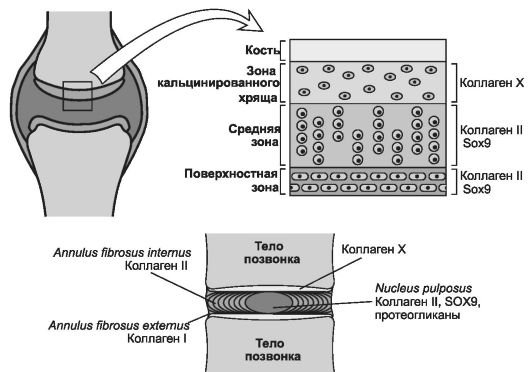 Рис. 6-48. Хрящи суставной и межпозвонкового диска. В
суставном хряще различают три зоны: поверхностная зона содержит плоские
клетки, средняя зона представлена округлыми клетками, организованными в
виде столбиков, или колонок, и узкая минерализованная глубокая зона.
Поверхностная и средняя зона содержат коллаген II типа, а глубокая зона -
коллаген X типа. Nucleus pulposus межпозвонкового диска имеет аналогичную структуру. [119]
Рис. 6-48. Хрящи суставной и межпозвонкового диска. В
суставном хряще различают три зоны: поверхностная зона содержит плоские
клетки, средняя зона представлена округлыми клетками, организованными в
виде столбиков, или колонок, и узкая минерализованная глубокая зона.
Поверхностная и средняя зона содержат коллаген II типа, а глубокая зона -
коллаген X типа. Nucleus pulposus межпозвонкового диска имеет аналогичную структуру. [119]
существует до тех пор, пока полностью не завершится постнатальный рост кости в длину, после чего замещается костной тканью. Эпифизарная пластинка состоит из четырёх зон - резервной (покоящегося хряща); размножения (пролиферирующего молодого хряща); гипертрофии клеток и созревания хряща; оссификации хряща и окостенения.
Эластический хрящ
Эластический хрящ входит в состав ушной раковины, слуховой (евстахиевой) трубы, надгортанника, рожковидных и клиновидных хрящей гортани. Помимо прочности и упругости, эластический хрящ обладает ещё одним свойством - эластичностью. Эластический хрящ принципиально построен так же, как и гиалиновый. Главное отличие - присутствие в хрящевом матриксе сети эластических волокон. По сравнению с гиалиновым, эластический хрящ не обызвествляется.
Волокнистый хрящ
Волокнистый хрящ присутствует в межпозвонковых и суставных дисках, симфизе лонного сочленения, а также в местах перехода сухожилий и связок в гиалиновый хрящ. Надхрящницы нет. Структурно волокнистый хрящ не только занимает промежуточное положение между сухожилием и гиалиновой хрящевой тканью, но и часто граничит с ними или островками входит в состав тех и других. Волокнистый хрящ испытывает значительные механические нагрузки как при сжатии, так и при растяжении. Коллагеновые волокна, формируя пучки, расположены параллельно друг другу. Между ними в полостях (лакунах) лежат более крупные и округлые (по сравнению с фиброцитами) хондроциты - как отдельные, так и образующие изогенные группы. В изогенной группе волокнистого хряща хондроциты расположены цепочкой.
Межпозвонковый диск (см. рис. 6-48). По периферии диска волокнистый хрящ образует концентрические кольца - annulus fibrosus (фиброзное кольцо). Центральная часть диска - студенистое ядро (nucleus pulposus) - заполнена желеобразной массой. В этот жидкий матрикс погружены т.н. пузыревидные клетки, образующие скопления различной величины и формы. Межпозвонковый диск (в первую очередь студенистое ядро) выступает в роли гидравлического амортизатора. С возрастом волокнистый хрящ фиброзного кольца становится тоньше.
Костная ткань
Кости формируют скелет организма, защищают и поддерживают жизненно важные органы, выполняют функцию депо кальция, содержат до 99% всего кальция. Микроскопически различают грубоволокнистую (первичную, или незрелую) и пластинчатую (вторичную, или зрелую) костные ткани. Макроскопически в кости выделяют губчатое и компактное вещество. Костная ткань имеет минерализованный (обызвествлённый, или кальцифицированный) матрикс. В кости присутствуют две линии клеток - созидающая и разрушающая, что отражает постоянную происходящую перестройку костной ткани. Дифферон созидающей линии клеток в костной ткани: остеогенная клетка → остеобласт → остеоцит. Разрушающая линия клеток - остеокласты.
Костный матрикс
Костный матрикс составляет 50% сухого веса кости и состоит из неорганической (50%) и органической (25%) частей и воды (25%). Неорганическая часть содержит два химических элемента - кальций (35%) и фосфор (50%), образующие кристаллы гидроксиапатита, а также вхо-
дящие в состав других неорганических веществ. Кристаллы гидроксиапатита, имеющие стандартный размер 20x5x1,5 нм, соединяются с молекулами коллагена через остеонектин. В состав неорганической части кости также входят бикарбонаты, цитраты, фториды, соли Mg2+, K+, Na+. Органическая часть - коллагены (коллаген типа I - 90-95% и коллаген типа V) и неколлагеновые белки (остеонектин, остеокальцин, протеогликаны, сиалопротеины, морфогенетические белки, протеолипиды, фосфопротеины), а также гликозаминогликаны (хондроитинсульфат, кератансульфат). Органические вещества костного матрикса синтезируют остеобласты.
Остеоид - неминерализованный органический костный матрикс вокруг остеобластов, синтезирующих и секретирующих его компоненты. Позднее остеоид минерализуется, чему предшествует появление в остеоиде выделяемых остеобластами матриксных пузырьков. Окружён- ные мембраной матриксные пузырьки размером от 30 нм до 1 мкм содержат липиды, большое количество Ca2+, различные фосфатазы. В частности, щелочная фосфатаза осуществляет ферментативный гидролиз эфиров фосфорной кислоты с образованием ортофосфата, который взаимодействует с Ca2+, что приводит к образованию осадка в виде аморфного фосфата кальция Ca3(PO4)2 с последующим формированием из него кристаллов гидроксиапатита. Для нормальной минерализации остеоида особенно необходим 1а,25-дигидроксихолекальци- ферол (активная форма витамина D3 кальцитриол).
Клетки костной ткани
Остеогенные клетки происходят из мезенхимы, имеют веретеновидную форму и расположены в периосте и эндосте. При высоком pO2 остеогенные клетки дифференцируются в остеобласты, а при низком pO2 - в хондрогенные клетки.
Остеобласты - неделящиеся отростчатые клетки, имеют кубическую, полигональную или цилиндрическую форму. Ядро расположено эксцентрично, цитоплазма резко базофильна. Остеобласты синтезируют и секретируют вещества костного матрикса. В связи с этим в остеобластах хорошо развиты гранулярная эндоплазматическая сеть и комплекс Гольджи, присутствует множество секреторных гранул, содержащих проколлаген. Проколлаген секретируется практически через всю поверхность клетки, что даёт возможность остеобласту окружить себя матриксом со всех сторон. При помощи отростков остеобласты устанавливают контакты с соседними остеобластами и остеоцитами. Остеоциты (рис. 6-51) - зрелые неделящиеся клетки, расположенные в костных полостях, или лакунах. Тонкие отростки остеоцитов расположены в канальцах, отходящих в разные стороны от костных полостей. Совокупность сообщающихся между собой канальцев и лакун
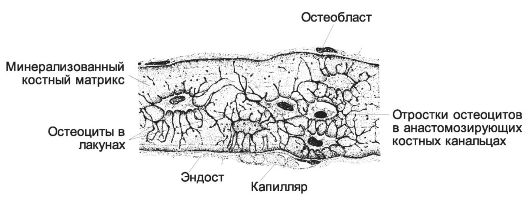 Рис. 6-51. Остеоциты в костной трабекуле. Переплетающиеся
трабекулы губчатой кости содержат остеоциты и окружены снаружи одним
слоем остеобластов. Остеоциты расположены в лакунах. Отростки остеоцитов
проходят в отходящих от лакун костных канальцах. [17]
Рис. 6-51. Остеоциты в костной трабекуле. Переплетающиеся
трабекулы губчатой кости содержат остеоциты и окружены снаружи одним
слоем остеобластов. Остеоциты расположены в лакунах. Отростки остеоцитов
проходят в отходящих от лакун костных канальцах. [17]
составляет лакунарно-канальцевую систему. Остеоциты поддерживают структурную целостность минерализованного матрикса, участвуют в регуляции обмена кальция. Эта функция остеоцитов находится под контролем со стороны Ca2+ плазмы крови и различных гормонов. Остеоциты могут секретировать вещества для образования матрикса новой кости, но эта способность менее выражена, чем у остеобластов. Лакунарно-канальцевая система заполнена тканевой жидкостью, через которую осуществляется обмен веществ между остеоцитами и кровью. В канальцах постоянно циркулирует жидкость, что поддерживает диффузию метаболитов и обмен между лакунами и кровеносными сосудами надкостницы. Разделяющий плазму и лакунарно-канальцевую жидкость барьер называют костной мембраной. Барьер формируют остеобласты и остеоциты.
Остеокласты (рис. 6-54) - крупные многоядерные клетки. Клетка-родоначальница остеокластов - колониеобразующая единица для гранулоцитов и моноцитов (CFU-GM). Остеокласты относят к системе мононуклеарных фагоцитов.
Остеокласты имеют ацидофильную цитоплазму и расположены в области резорбции (разрушения) кости в лакунах Хоушипа. В активированном остеокласте различают гофрированную каёмку, светлую, везикулярную и базальную зоны. Гофрированная каёмка (рис. 6-54) - многочисленные цитоплазматические выросты, направленные к поверхности кости и достигающие её. Через мембрану выростов из остеокласта выделяется большое количество H+ и Cl-, что создаёт и поддерживает в замкнутом пространстве лакуны кислую среду, оптимальную для растворения солей кальция костного матрикса (pH 4.5). Ферменты многочисленных лизосом везикулярной зоны разрушают органическую часть костного матрикса.
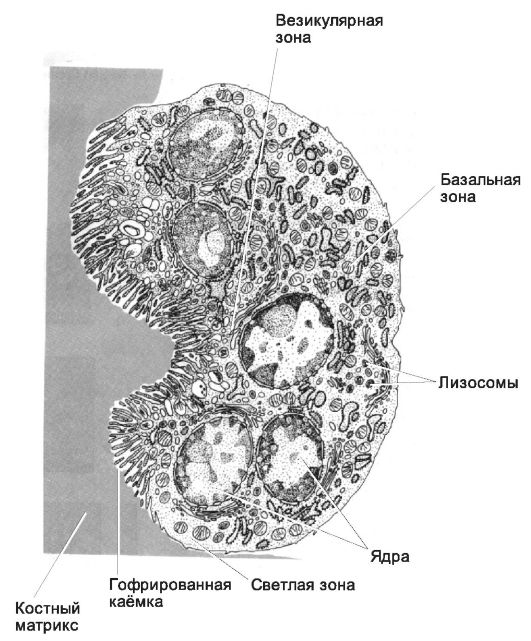 Рис. 6-54. Остеокласт. Многочисленные
цитоплазматические выросты гофрированной каёмки направлены к
поверхности кости. Светлая зона окружает гофрированную каёмку, плотно
прилегая к костному матриксу. В везикулярной зоне расположены лизосомы.
Ядра, митохондрии, цистерны гранулярной эндоплазматической сети и
комплекс Гольджи сосредоточены в базальной зоне. [17]
Рис. 6-54. Остеокласт. Многочисленные
цитоплазматические выросты гофрированной каёмки направлены к
поверхности кости. Светлая зона окружает гофрированную каёмку, плотно
прилегая к костному матриксу. В везикулярной зоне расположены лизосомы.
Ядра, митохондрии, цистерны гранулярной эндоплазматической сети и
комплекс Гольджи сосредоточены в базальной зоне. [17]
Грубоволокнистая костная ткань
Между толстыми пучками беспорядочно расположенных коллагеновых волокон расположены удлинённые лакуны с длинными анастомозирующими канальцами. В лакунах находятся остеоциты. Такая незрелая кость (характерно большое количество протеогликанов и гликопротеинов и низкое содержание минеральных солей) присутствует у плода. У взрослого она сохраняется в местах прикрепления сухожилий к костям, вблизи черепных швов, в зубных альвеолах, в костном лабиринте внутреннего уха. Незрелая кость образуется также при заживлении переломов.
Пластинчатая костная ткань
Зрелая (вторичная), или пластинчатая костная ткань образована костными пластинками. Пластинчатая костная ткань формирует губчатое и компактное вещество кости.
• Губчатое вещество - переплетающиеся костные трабекулы, полости между которыми заполнены костным мозгом. Трабекула состоит из костных пластинок и снаружи окружена одним слоем остеобластов. Трабекулы расположены соответственно направлению сил сжатия и растяжения. Губчатое вещество заполняет эпифизы длинных трубчатых костей и образует внутреннее содержимое коротких и плоских костей скелета.
• Компактное вещество образует диафизы длинных трубчатых костей и слоем различной толщины покрывает все остальные (короткие и плоские) кости скелета. Основная масса компактного вещества состоит из остеонов.
Костная пластинка - слой костного матрикса толщиной 3-7 мкм. Между соседними пластинками в лакунах расположены остеоциты, а в толще пластинки в костных канальцах проходят их отростки. Коллагеновые волокна в пределах пластинки ориентированы упорядоченно и лежат под углом к волокнам соседней пластинки, что обеспечивает значительную прочность пластинчатой кости.
Остеон (рис. 6-56), или хаверсова система - совокупность 4-20 концентрических костных пластинок. В центре остеона расположен хаверсов канал (канал остеона), заполненный рыхлой волокнистой соединительной тканью с кровеносными сосудами и нервными волокнами. Фолькмана каналы (рис. 6-58) связывают каналы остеонов между собой, а также с сосудами и нервами надкостницы. Снаружи остеон ограничен спайной линией (линия цементации), отделяющей его от фрагментов старых остеонов. В ходе образования остеона (рис. 6-57) находящиеся в непосредственной близости от сосуда хаверсова канала остеогенные клетки дифференцируются в остеобласты. Снаружи располагается сформированный остеобластами слой остеоида. В дальнейшем остеоид минерализуется, и остеобласты, окружаемые минерализованным костным матриксом, дифференцируются в остеоциты. Следующий концентрический слой возникает подобным же
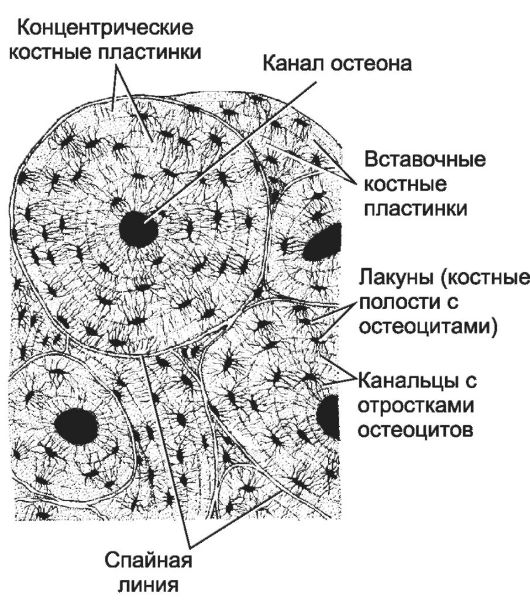 Рис. 6-56. Остеоны в компактной части трубчатой кости. Слой
остеонов компактного вещества трубчатой кости сформирован остеонами
разных генераций, между которыми располагаются остатки старых остеонов в
виде вставочных костных пластинок. [17]
Рис. 6-56. Остеоны в компактной части трубчатой кости. Слой
остеонов компактного вещества трубчатой кости сформирован остеонами
разных генераций, между которыми располагаются остатки старых остеонов в
виде вставочных костных пластинок. [17]
образом изнутри. По наружной поверхности остеоида на границе с минерализованным костным матриксом проходит фронт обызвествления, где начинается процесс отложения минеральных солей. Диаметр остеона (не более 0,4 мм) определяет расстояние, на которое эффективно диффундируют вещества к периферическим остеоцитам остеона по лакунарно-канальцевой системе из центрально расположенного кровеносного сосуда.
Организация пластинчатой костной ткани. В пластинчатой костной ткани (рис. 6-58) упорядоченно расположены остеоциты, коллагеновые волокна, костные пластинки и кровеносные сосуды. Остеоциты лежат в лакунах между соседними пластинками. От лакун в толщу соседних пластинок отходят анастомозирующие костные канальцы, содержащие отростки остеоцитов. Коллагеновые волокна в каждой пластинке проходят параллельно друг другу и под углом к волокнам соседних пластинок. В компактном веществе костные пластинки в основном образуют остеоны, ориентированные вдоль длинной оси трубчатой
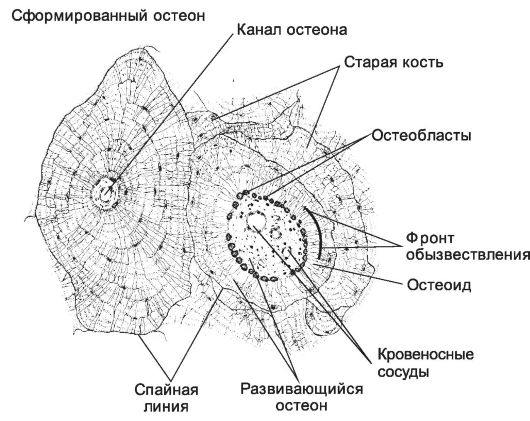 Рис. 6-57. Образование остеона. В
центральной части на месте будущего канала остеона в составе рыхлой
соединительной ткани проходят кровеносные сосуды. Эта центральная часть
окружена слоем остеобластов, снаружи лежит слой остеоида. Следующий слой
остеобластов и соответствующий ему слой остеоида образуется ближе к
центру остеона и имеет меньший диаметр. Сначала обызвествляются
периферические пластинки остеона, а затем и центральные. По мере
обызвествления матрикса остеобласты дифференцируются в остеоциты. [17]
Рис. 6-57. Образование остеона. В
центральной части на месте будущего канала остеона в составе рыхлой
соединительной ткани проходят кровеносные сосуды. Эта центральная часть
окружена слоем остеобластов, снаружи лежит слой остеоида. Следующий слой
остеобластов и соответствующий ему слой остеоида образуется ближе к
центру остеона и имеет меньший диаметр. Сначала обызвествляются
периферические пластинки остеона, а затем и центральные. По мере
обызвествления матрикса остеобласты дифференцируются в остеоциты. [17]
кости. Между остеонами находятся вставочные костные пластинки. Наружные (покрывающие кость) и внутренние (выстилающие полость кости) общие (генеральные) костные пластинки лежат параллельно друг другу. Кровеносные сосуды залегают в каналах остеонов.
Надкостница
Периост покрывает снаружи всю кость, за исключением суставной поверхности. В периосте выделяют два слоя - наружный и внутренний. Толстый наружный слой - волокнистый, представлен плотной соединительной тканью. Остеогенные клетки и остеобласты входят в состав внутреннего (остеогенного) слоя надкостницы. Пучки прободающих коллагеновых волокон (волокна Шарпея), заостряющиеся по направлению к кости и уходящие в её матрикс из надкостницы,
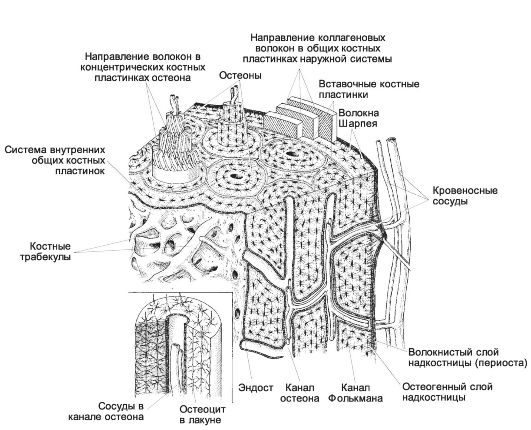 Рис. 6-58. Компактная часть трубчатой кости. Под
надкостницей расположена наружная система общих костных пластинок.
Основной объём компактной части кости занимает слой остеонов. Изнутри к
слою остеонов прилегает внутренняя система общих костных пластинок.
Слева на врезке - остеон. [17]
Рис. 6-58. Компактная часть трубчатой кости. Под
надкостницей расположена наружная система общих костных пластинок.
Основной объём компактной части кости занимает слой остеонов. Изнутри к
слою остеонов прилегает внутренняя система общих костных пластинок.
Слева на врезке - остеон. [17]
обеспечивают прочное прикрепление внутреннего слоя к поверхности кости. Периост - источник остеогенных клеток для развития, роста и регенерации костной ткани.
Эндост - тонкая оболочка, покрывающая трабекулы в губчатом веществе, а также выстилающая кость (со стороны костного мозга) и хаверсовы каналы компактного вещества. Иными словами, эндост присутствует на поверхности всех костных полостей. Эндост состоит из слоя неактивных плоских остеогенных клеток. В период роста и перестройки кости целостность эндоста часто нарушается остеокластами.
ГИСТОГЕНЕЗ КОСТНОЙ ТКАНИ
Различают внутримембранный (прямой) и энхондральный (непрямой) остеогенез.
Внутримембранный остеогенез
Этим способом образуются плоские кости. В участках мезенхимы, содержащих капилляры, группы мезенхимных клеток формируют первичные центры окостенения. Далее мезенхимные клетки дифференцируются в остеобласты.
Остеобласты начинают вырабатывать остеоид. Остеоид минерализуется, и дифференцирующиеся остеоциты оказываются замурованными в лакунах минерализованного костного матрикса. Сформировавшаяся незрелая грубоволокнистая костная ткань существует в форме трабекулы. Отдельные трабекулы, образовавшиеся в различных участках, растут и объединяются друг с другом. Наиболее толстые трабекулы (диаметром свыше 0,4 мм) содержат кровеносный сосуд, расположенный в центральном узком канале, выстланном остеогенными клетками. Поверхность трабекул покрывает слой остеобластов и остеогенных клеток. За счёт этого слоя на поверхности незрелой костной ткани происходит образование костных пластинок. Постепенно остеокласты разрушают первичную кость и на её месте путём аппозиционного роста формируются слои параллельных пластинок, образующих костные трабекулы из зрелой костной ткани. Анастомозирующая сеть костных трабекул формирует губчатое вещество. С утолщением трабекул и уменьшением полостей между ними, вплоть до их исчезновения, губчатое вещество может перестраиваться в компактное, состоящее из остеонов. Длина остеонов плоских костей довольно мала по сравнению с остеонами длинных трубчатых костей. В плоских костях губчатое вещество сохраняется в виде очень тонкого среднего слоя - diploe.
Энхондральный остеогенез
Энхондральный (непрямой) остеогенез (рис. 6-62) происходит в состоящем из гиалинового хряща зачатке будущей кости (хрящевая модель). В ходе этого процесса образуются длинные трубчатые кости. Морфогенетические белки кости (BMP) индуцируют энхондральный остеогенез. В энхондральном остеогенезе: выделяют два этапа: образование первичных, а затем вторичных центров окостенения.
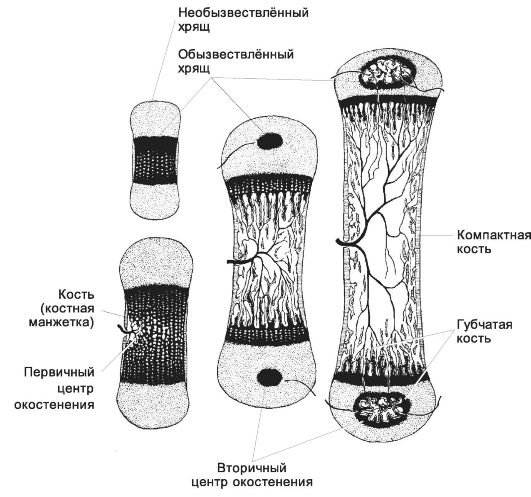 Рис. 6-62. Энхондральный остеогенез. Хрящ
не превращается в кость, а замещается ею. С кровеносными сосудами в
хрящевую модель проникают остеогенные клетки. Остеокласты разбирают
минерализованный хрящевой матрикс, а остеобласты строят костную ткань.
[17]
Рис. 6-62. Энхондральный остеогенез. Хрящ
не превращается в кость, а замещается ею. С кровеносными сосудами в
хрящевую модель проникают остеогенные клетки. Остеокласты разбирают
минерализованный хрящевой матрикс, а остеобласты строят костную ткань.
[17]
Центры окостенения
• Первичный (диафизарный) центр окостенения образуется в ходе следующих событий: усиление кровоснабжения надхрящницы в хрящевой модели → повышение pO2 - коммитирование стволовой клетки скелетных тканей в остеогенном направлении - появление остеобластов - образование грубоволокнистой костной ткани (костная манжетка) в средней части диафиза путём внутримембранного остеогенеза. Параллельно в центральной части хрящевой модели происходят гипертрофия хондроцитов, их дегенерация, обызвествление матрикса, слияние лакун хрящевых клеток и образование полостей. Остеокласты костной манжетки резорбируют первичную костную ткань, что приводит к образованию путей,
по которым кровеносные сосуды, остеогенные и другие клетки мезенхимного происхождения проникают из надкостницы в образованные при гибели хряща полости. Дифференцировка проникших в центр хрящевой модели остеогенных клеток приводит к образованию костной ткани. В диафизе первичная костная ткань замещается компактным веществом. Костномозговая полость формируется в результате активной резорбции остеокластами комплекса «кальцинированный хрящ - кальцинированная кость». Образованная ранее костная манжетка утолщается и растёт по направлению к эпифизам.
• Вторичный (эпифизарный) центр окостенения. В эпифизах оссификация протекает аналогично формированию диафизарного центра окостенения, но на месте первичной костной ткани образуется губчатое вещество. Когда новообразованная костная ткань заполнит весь эпифиз, хрящевая ткань остаётся в виде узких полосок только на поверхности эпифиза (суставной хрящ), а также между эпифизом и диафизом (метафизом) в виде эпифизарной хрящевой пластинки.
Рост трубчатых костей
В удлинении диафиза трубчатых костей участвует эпифизарная пластинка, представленная гиалиновым хрящом (рис. 6-63). Она существует до тех пор, пока полностью не завершится постнатальный рост кости в длину, после чего замещается костной тканью. Эпифизарная пластинка состоит из четырёх зон - резервной (покоящегося хряща); размножения (пролиферирующего молодого хряща); гипертрофии клеток и созревания хряща; кальцификации хряща и окостенения.
• Резервная зона покоящегося хряща расположена в эпифизарной части пластинки. Она состоит из гиалинового хряща, содержащего небольшие хаотично рассеянные хондроциты. Эта зона не участвует в росте эпифизарной пластинки, а служит для фиксации пластинки к эпифизу.
• Зона размножения. В этой зоне находятся многочисленные делящиеся хондроциты. Эти мелкие клетки, укладываясь друг на друга, формируют изогенные группы в виде колонок, расположенных перпендикулярно к плоскости пластинки.
• Зона гипертрофии клеток и созревания хряща. Здесь расположены вышедшие из зоны размножения и также сгруппированные в колонки крупные вакуолизированные клетки, прекратившие митозы. Наиболее зрелые из них, ещё более увеличиваясь в размерах, смещаются ближе к диафизу и активно секретируют щелочную фосфатазу, способствующую накоплению ионов кальция и фосфат ионов. По мере обызвествления хряща третья зона переходит в четвёртую.
• Зона кальцификации хряща, граничащая с диафизом, - очень тонкая; её толщина соответствует диаметру одной-трёх клеток. В этой зоне происходят минерализация хрящевого матрикса и гибель хондроцитов. В формирующиеся полости обызвествлённого хрящевого матрикса со стороны диафиза прорастают кровеносные сосуды с сопровождающими их остеогенными клетками. На месте обызвествлённого хряща формируется костная ткань. Тут же появляются остеокласты, разрушающие комплекс «кальцинированный хрящ-кальцинированная кость».
Суставной хрящ. В постнатальном периоде суставной хрящ длинных трубчатых костей продолжает свой рост (за счёт пролиферации хонд-
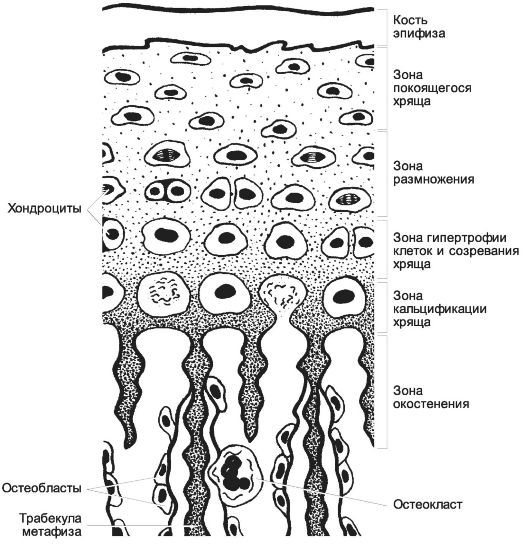 Рис. 6-63. Эпифизарная пластинка. Эпифизарная
часть пластинки образована зоной покоящегося хряща. Она представлена
типичным гиалиновым хрящом. В зоне размножения присутствуют
многочисленные делящиеся хондроциты. Вышедшие из митоза крупные
вакуолизированные хондроциты образуют зону гипертрофии и созревания
хряща. Минерализация хряща и гибель хондроцитов происходят в зоне
кальцификации хряща. В зоне окостенения на месте обызвествлённого хряща
формируется костная ткань. [17]
Рис. 6-63. Эпифизарная пластинка. Эпифизарная
часть пластинки образована зоной покоящегося хряща. Она представлена
типичным гиалиновым хрящом. В зоне размножения присутствуют
многочисленные делящиеся хондроциты. Вышедшие из митоза крупные
вакуолизированные хондроциты образуют зону гипертрофии и созревания
хряща. Минерализация хряща и гибель хондроцитов происходят в зоне
кальцификации хряща. В зоне окостенения на месте обызвествлённого хряща
формируется костная ткань. [17]
роцитов поверхностных слоёв) до момента достижения эпифизами дефинитивных размеров. Таким образом, суставной хрящ обеспечивает рост эпифиза кости так же, как эпифизарная пластинка обеспечивает рост диафиза кости в длину. В коротких костях, не имеющих эпифизарных пластинок, именно суставной хрящ обеспечивает рост кости в длину в целом.
Рост трубчатых костей в ширину происходит благодаря образованию новых слоёв костной ткани (образующихся путём аппозиционного роста) остеогенными клетками надкостницы. С внутренней стороны кость резорбируется остеокластами. В итоге стенка диафиза не утолщается, тогда как костномозговая полость увеличивается. По мере завершения роста кости под надкостницей формируются наружные генеральные пластинки (также по аппозиционному механизму).
Перестройка костной ткани
В костной ткани одновременно и постоянно протекают процессы резорбции старой кости и формирования новой (рис. 6-64). Кость - динамичная структура с постоянно изменяющейся формой и внутренней организацией. Участки кости, испытывающие сжатие, подвергаются резорбции. В итоге происходит перестройка костной ткани, адаптирующая кость к механическим нагрузкам.
• Губчатое вещество кости. У взрослого человека около 4% поверхности губчатого вещества кости вовлечено в процесс активной резорбции, в то же время 10-15% её поверхности покрыто остеоидом.
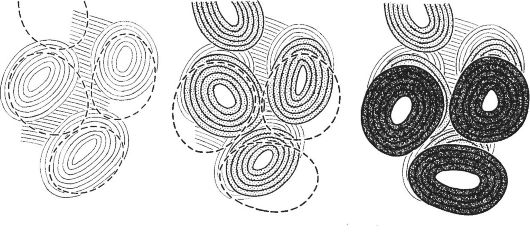
Рис. 6-64. Перестройка пластинчатой костной ткани. Показаны три последовательные генерации остеонов (А, Б, В). Новые остеоны возникают на месте старых. Между остеонами новой генерации видны остатки концентрических костных пластинок старых остеонов, образующие вставочные костные пластинки. [17]
• Остеоны компактного вещества кости не сохраняются в течение всей жизни, а подвержены постоянной резорбции. Их фрагменты всегда присутствуют между сформированными остеонами пластинчатой кости в виде вставочных костных пластинок. В ходе резорбции остеонов образуются полости удлинённой цилиндрической формы, выстланные остеогенными клетками. В этих полостях формируются новые остеоны.
Сращение переломов
В области перелома повреждены ткани, нарушено кровоснабжение, и остеоциты в прилегающих участках остеонов гибнут. Отмирающая кость подвергается резорбции. Между концами отломков формируется новая ткань - костная мозоль (рис. 6-66). Костная мозоль возникает в результате интенсивного размножения остеогенных клеток надкостницы. Часть этих клеток дифференцируется в остеобласты, образующие новые костные трабекулы, прочно прикрепляющиеся к матриксу отломка. Скорость размножения остеогенных клеток в наружной части костной мозоли превышает темпы роста кровеносных сосудов, что и определяет появление хондробластов и образование гиалинового хряща. В дальнейшем (по мере обызвествления) хрящ замещается незрелой грубоволокнистой костной тканью, на месте которой формируется губчатое вещество. После этого костная мозоль перестраивается: губчатое вещество между отломками преобразуется в компактное, и восстанавливается первоначальная конфигурация кости.
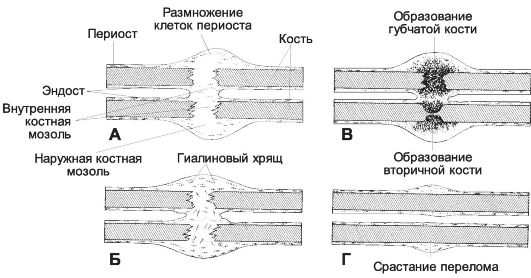 Рис. 6-66. Срастание перелома. Образование костной мозоли путём размножения клеток преимущественно остеогенного слоя надкостницы (А). Появление гиалинового хряща в наружной части костной мозоли и постепенное распространение хряща по всему её объёму (Б). Замещение хряща костью (В). При этом сначала образуется губчатое вещество, позднее перестраивающееся в компактное (Г). [17]
Рис. 6-66. Срастание перелома. Образование костной мозоли путём размножения клеток преимущественно остеогенного слоя надкостницы (А). Появление гиалинового хряща в наружной части костной мозоли и постепенное распространение хряща по всему её объёму (Б). Замещение хряща костью (В). При этом сначала образуется губчатое вещество, позднее перестраивающееся в компактное (Г). [17]
Соединения костей
Различают непрерывные и прерывистые (суставы) соединения костей.
• Непрерывные соединения. К ним относятся синдесмозы, синхондрозы (в том числе симфизы) и синостозы.
♦ Синдесмоз - непрерывное соединение костей при помощи плотной соединительной ткани (соединительнотканная мембрана между лучевой и локтевой костями, швы между костями черепа).
♦ Синхондроз - непрерывное соединение посредством хряща - широко распространён в скелете детей и подростков (соединяет диафиз длинных костей с эпифизом, крестцовые позвонки между собой и т.д.); с возрастом хрящ заменяется костной тканью. У взрослого человека синхондрозы сохраняются в соединениях костей черепа, в грудине (между рукояткой и мечевидным отростком). Симфизы образованы волокнистым хрящом и имеют полость внутри хрящевой пластинки (межпозвонковый симфиз, симфиз рукоятки грудины, лобковый симфиз).
♦ Синостоз - непрерывное соединение костей посредством костной ткани (например, соединение тазовых костей).
• Прерывистые соединения - суставы, или диартрозы. В них суставной хрящ покрывает суставные поверхности. Полость сустава заполнена синовиальной жидкостью. Суставная капсула окружает сустав.
♦ Суставная капсула состоит из двух слоёв: внутреннего (синовиального) и наружного (фиброзного), переходящего в волокнистый слой надкостницы. Фиброзный слой - плотная волокнистая соединительная ткань. Образующие пласты коллагеновые и эластические волокна ориентированы вдоль длинной оси диартроза и соединяют надкостницу одной кости с надкостницей другой. Слой без резкой границы переходит во внутренний (синовиальный) слой. Он образован специализированной соединительной тканью, выстилающей полость сустава. Здесь присутствуют многочисленные кровеносные и лимфатические сосуды, нервные волокна, множество тучных клеток. Содержит коллагеновые и в ряде суставов эластические волокна, а также клетки двух типов. Антигенпредставляющие клетки относятся к системе мононуклеарных фагоцитов, они интенсивно фагоцитируют, имеют хорошо развитый комплекс Гольджи, много лизосом, редкие цистерны гладкой эндоплазматической сети. Синовиальные фибробластоподобные клетки кубической формы имеют хорошо развитую гладкую эндоплазматическую сеть. Разделённые немногими коллагеновыми волокнами, эти клетки образуют почти сплошной слой. Повреждённый синовиальный слой быстро и полностью восстанавливается.
♦ Синовиальная жидкость - прозрачный и вязкий диализат плазмы, в высокой концентрации содержащий сильно полимеризованную гиалуроновую кислоту, продуцируемую клетками синовиального слоя.