Туберкулёз: учебное пособие. - Кошечкин В.А., Иванова З.А. 2007. - 304 с.
|
|
|
|
ГЛАВА 1 ЭТИОЛОГИЯ И ПАТОГЕНЕЗ ТУБЕРКУЛЕЗА
1.1. ХАРАКТЕРИСТИКА МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА
Микобактерии туберкулеза (МБТ) - факультативные внутриклеточные паразиты.
Микобактерии туберкулеза (МБТ) относятся к семейству бактерий Micobacteriacae, порядку Actinomycetalis, роду Mycobacterium. Род Mycobacterium насчитывает свыше 100 видов, большинство из которых являются сапрофитными микроорганизмами, широко распространенными в окружающей среде.
Этимологически слово «микобактерия» происходит из греческих слов myces - гриб и bacterium, bactron - палочка, прутик. Компонент названия «гриб» обусловлен тенденцией этих микроорганизмов образовывать нитчатые и ветвящиеся формы, похожие на плесень.
C позиций клинической медицины микобактерия туберкулеза, открытая немецким ученым Робертом Кохом, является наиболее важным видом актиномицетов, которые объединены в комплекс, включающий M. tuberculosis (МБТ); M. bovis и ее вариант БЦЖ (бацилла Кальметта-Герена); M. africanum и M. microti. Эта группа микобактерий отличается выраженным генетическим сходством.
M. microti считается не патогенной для человека, однако вызывает заболевание у мышей, напоминающее туберкулез. Культура БЦЖ не является патогенной для человека. Микобактерия туберкулеза (МБТ) является до 95% случаев причиной заболевания туберкулезом человека в зависимости от территории проживания. Вместе с тем M. bovis и M. africanum вызывают заболевание у человека, клинически не отличающееся от классического туберкулеза.
Микобактерии, не входящие в комплекс M. Tuberculosis, могут стать причиной микобактериозов. Такие микобактерии объединяют в комплексы, наиболее важными из которых являются: M. avium, M. fortinatum и M. terrae, M. leprae, M. ulcerance.
Представленные в дальнейшем материалы о туберкулезе имеют отношение только к заболеванию, вызываемому M. tuberculosis (МБТ), - бактерии Коха (БК), typus humanus.
Естественный резервуар туберкулезной микобактерии - человек, домашние и дикие животные, птицы.
МБТ внешне представляют собой тонкие изогнутые палочки, стойкие к кислотам, щелочам и высыханию. Наружная оболочка бактерии содержит сложные воска и гликолипиды.
МБТ могут размножаться как в макрофагах, так и вне клеток.
МБТ размножаются относительно медленно. Размножение происходит в основном путем простого клеточного деления. На обогащенных питательных средах МБТ размножаются с периодом удвоения от 18 до 24 ч. Для роста в культуре микобактерий туберкулеза, полученных в клинических условиях, необходимо от 4 до 6 нед.
Генетическая структура МБТ установлена. С нуклеотидной последовательностью МБТ можно ознакомиться в международных банках данных. Нуклеотидная последовательность МБТ (штамм H37Rv) насчитывает 4,411,529 b.p.
Самостоятельным движением МБТ не обладают. Температурные границы роста находятся между 29 и 42 °C (оптимальная - 37-38 °C). МБТ обладают устойчивостью к физическим и химическим агентам; они сохраняют жизнеспособность при очень низких температурах, а повышение до 80°C могут выдерживать в течение 5 мин.
Во внешней среде микобактерия туберкулеза достаточно устойчива. В воде она может сохраняться до 150 дней. Высохшие микобактерии вызывают туберкулез у морских свинок через 1-1,5 года, лиофилизированные и замороженные жизнеспособны до 30 лет.
При интенсивном облучении солнцем и при высокой температуре окружающей среды жизнеспособность МБТ резко снижается; напротив, в темноте и сырости выживаемость их весьма значительна. Вне живого организма они остаются жизнеспособными в течение многих месяцев, в особенности в темных, сырых помещениях.
МБТ выявляются с помощью уникального свойства к окрашиванию (кислотоустойчивости), отличающего их от многих других возбудителей инфекции. Циль (Ziehl) и Нильсен (Neelsen) в 1883 г. разработали специальный контрастный метод окраски МБТ, основанный на свойстве кислотоустойчивости. Препарат, окрашенный при подогревании карболовым фуксином, обесцвечивается раствором серной кислоты и после промывания водой докрашивается
раствором метиленовой синьки (способ Циля-Нильсена). В отличие от некислотоустойчивых бактерий, туберкулезные микобактерии окрашиваются в красный цвет, не обесцвечиваются при действии раствора кислоты и хорошо видны на синем фоне при микроскопии. Способ Циля-Нильсена до сих пор является одним из основных методов окраски МБТ при микроскопии. Более чувствительной, чем кислоустойчивый метод окраски, является окраска аурамином МБТ с последующей флуорисцентной микроскопией (рис. 1-1-1, 1-1-2, см. вклейку).
С липидной фракцией внешней оболочки МБТ связывают устойчивость возбудителей туберкулеза к кислотам, щелочам и спиртам.
Изменчивость морфологии МБТ. Морфология и размеры МБТ не постоянны, это зависит от возраста клеток и особенно от условий существования и состава питательной среды.
Корд-фактор. Липиды поверхностной стенки микобактерий определяют ее вирулентность и способность к образованию в культуре скоплений бактерий в виде кос (корд-фактор).
О корд-факторе было сказано еще Кохом в его начальном сообщении относительно МБТ. Первоначально корд-фактор связывали с вирулентностью МБТ. Способность формировать косы наблюдается среди других микобактерий, имеющих низкую вирулентность или вообще не имеющих ее. Корд-фактор, как было установлено позже, связан с необычным биологическим веществом trehalose 6,6-dimyco- late, которое обладает высокой вирулентностью.
L-формы. Одним из важных видов изменчивости МБТ является формирование L-форм. L-формы характеризуются сниженным уровнем метаболизма, ослабленной вирулентностью. Оставаясь жизнеспособными, они могут длительное время находиться в организме и индуцировать противотуберкулезный иммунитет.
L-формы отличаются выраженными функциональными и морфологическими изменениями. Обнаружено, что трансформация МБТ в L-формы усиливается при длительном влиянии антибактериальной терапии и других факторов, которые нарушают их рост и размножение, образование клеточной мембраны.
Установлено, что в мокроте «абациллярных» больных с деструктивными формами туберкулеза могут находиться L-формы МБТ, способные при соответствующих условиях реверсировать (модифицироваться) в палочковидный вариант, вызывая тем самым реактивацию туберкулезного процесса. Следовательно, абацилли-
рование каверн таких больных еще не означает их стерилизацию в отношении МБТ.
МБТ по своей природе нечувствительны ко многим антибиотикам. Это свойство в первую очередь связано с тем, что высокогидрофобная клеточная поверхность служит своего рода физическим барьером для терапевтических агентов и антибиотиков. Главная причина устойчивости закодирована в структуре генома туберкулезной палочки.
Вместе с тем МБТ могут вырабатывать устойчивость (резистентность) к противотуберкулезным препаратам. Одновременная лекарственная устойчивость МБТ к нескольким препаратам в последние годы значительно снижает эффективность лечения туберкулеза.
В результате современное здравоохранение имеет дело не просто с опасным возбудителем туберкулеза, а с целым набором его штаммов, устойчивых к разным лекарствам. На практике для организации эффективного лечения туберкулеза важно не только обнаружить МБТ, но и параллельно определить их резистентность, причем достаточно быстро - в течение двух-трех дней, чтобы вовремя назначить эффективную химиотерапию.
В конце 80-х гг. прошлого века появился метод, значительно сокращающий время такого анализа. Новая диагностика основана на избирательной амплификации нуклеиновых кислот (ДНК или РНК) in vitro с помощью полимеразной цепной реакции (ПЦР).
Метод ПЦР имеет большие возможности и лежит в основе точной ДНК-диагностики, которая позволяет идентифицировать любой штамм МБТ и определять первопричину той или иной устойчивости к лекарствам.
Лабораторные исследования показали, что возникновение резистентности у M. tuberculosis связано с нуклеотидными заменами (мутациями) в генах, кодирующих различные ферменты, которые непосредственно взаимодействуют с лекарственными средствами.
Резистентность некоторых штаммов МБТ к изониазиду связана с мутациями в гене katG, приводящими к замене некоторых аминокислот в ферментах - каталазе и пероксидазе.
Нечувствительность МБТ к стрептомицину связана с миссенсмутацией в гене rpsL, кодирующем S12 митохондриальный белок, или с нуклеотидными заменами в гене rrs, кодирующем 16S РНК.
Представленные некоторые мутации в геноме микобактерии туберкулеза являются лишь ограниченными примерами формиро-
вания ее резистентности к противотуберкулезным препаратам. На этом основании можно сделать следующий вывод: по мере внедрения в практику химиотерапии туберкулеза новых лекарств в геноме М. tuberculosis будут происходить мутации, приводящие к резистентности ко всем без исключения используемым препаратам, и это обстоятельство необходимо постоянно учитывать в тактике лечения туберкулеза.
1.2. ПУТИ И СПОСОБЫ ЗАРАЖЕНИЯ
ТУБЕРКУЛЕЗОМ
Источник инфекции. Основным источником МБТ является больной туберкулезом человек, распространяющий МБТ (бацилловыделитель).
Очаг туберкулезной инфекции становится опасным в тех случаях, когда больные страдают открытой формой туберкулеза, т.е. выделяют туберкулезные микобактерии. Особое значение при заражении туберкулезом имеет прямой, длительный и тесный контакт здорового человека с бацилловыделителем. Заражение может происходить чаще всего в семье, в месте проживания или в коллективе, в которых находится больной туберкулезом, выделяющий микобактерии. Опасность рассеивания заразного начала устраняется, если бацилловыделитель своевременно выявлен и изолирован.
Возникновение и течение инфекции зависят не только от вирулентности возбудителя, но и состояния устойчивости и реактивности макроорганизма.
Большое значение имеет место проникновения МБТ в организм, где завязывается первичный контакт с микробом (входные ворота инфекции). Различают следующие пути передачи туберкулеза:
1) воздушно-капельный;
2) алиментарный (через пищеварительный тракт);
3) контактный;
4) внутриутробное заражение туберкулезом.
Воздушно-капельный путь заражения туберкулезом
Туберкулезные микобактерии попадают в воздух с капельками при кашле, разговоре и чихании больного с активным туберкулезом. При вдыхании эти зараженные капельки проникают в легкие здоро-
вого человека. Этот способ заражения получил название воздушнокапельной инфекции (рис. 1-2, см. вклейку).
В зависимости от силы кашлевых импульсов и размеров капелек МБТ распространяются в воздухе на различные расстояния: при кашле - до 2 м, при чихании - до 9 м. В среднем частицы мокроты рассеиваются на расстояние 1 м прямо перед больным.
Капельки туберкулезной мокроты, осевшие на пол, высыхают и превращаются в пылинки. Находившиеся в них туберкулезные микобактерии некоторое время остаются в пыли жизнеспособными. Установлено, что к 18-му дню в высушенной мокроте остается 1% живых бактерий. При сильном движении воздуха, подметании пола, перемещении людей пылинки, содержащие туберкулезные микобактерии, поднимаются в воздух, проникают в легкие и вызывают заражение.
Алиментарный путь заражения через пищеварительные пути
Специальные эксперименты на животных показывают, что при алиментарном способе требуется значительно большее количество микобактерий, чем при аэрогенном заражении. Если при вдыхании достаточно одной или двух микобактерий, то для заражения через пищу требуются сотни микробов.
Пути распространения туберкулезных микобактерий в организме человека при алиментарном заражении туберкулезной культурой демонстративно показывают секционные материалы, опубликованные в связи с судебным процессом в Любеке. По ошибке 252 грудным детям при вакцинации per os была введена туберкулезная культура (кильский штамм) вместо БЦЖ. Вследствие заражения умерло от туберкулеза 68 детей, заболел 131 ребенок и 53 остались здоровыми.
При вскрытии трупов 20 умерших детей было установлено, что в большинстве случаев процесс локализовался в органах брюшной полости. Входными воротами инфекции были органы пищеварения.
Одной из особенностей этого пути заражения у маленьких детей является частое поражение туберкулезом мезентериальных лимфатических узлов.
Необходимо иметь в виду, что проникновение туберкулезных микобактерий в кишечник может происходить и при заглатывании больными легочным туберкулезом собственной бациллярной мокроты, что подтверждается при использовании метода флотации промывных вод желудка.
Контактный путь передачи туберкулеза
Описаны случаи заражения через конъюнктиву глаза маленьких детей и взрослых; при этом иногда обнаруживается острый конъюнктивит и воспаление слезного мешочка.
Заражение туберкулезом через кожу встречается редко. Описаны случаи заболеваний туберкулезом доярок при проникновении МБТ через поврежденную кожу рук от больных туберкулезом коров.
Внутриутробное заражение туберкулезом
Возможность заражения туберкулезом плода в период внутриутробной жизни установлена на секции случаями туберкулеза у детей, умерших в первые дни после рождения. Заражение происходит или при поражении туберкулезом плаценты, или при инфицировании поврежденной плаценты во время родов туберкулезной матерью. Такой путь заражения туберкулезом встречается крайне редко.
1.3. ЭТИОЛОГИЯ И ИММУНИТЕТ
Морфологические и биохимические компоненты микробной клетки вызывают различные реакции в организме.
Основными биохимическими компонентами МБТ являются белки, углеводы, липиды.
Белки (туберкулопротеиды) являются основными носителями антигенных свойств МВТ.
Туберкулин - один из туберкулопротеидов, широко используемый в практике для выявления инфицирования МБТ (подробнее см. в разделе 2.3. Туберкулинодиагностика).
Гиперчувствительность замедленного типа (ГЧЗТ)
Вещества, входящие в состав внешней оболочки МБТ, индуцируют специфическую тканевую воспалительную реакцию макроорганизма и образование гранулемы. Одновременно появляется гиперчувствительность замедленного типа (ГЧЗТ), определяемая по реакции на туберкулиновые пробы, и слабое антителообразование.
В основном ГЧЗТ используется для характеристики иммунного ответа IV типа (наличие индурации, развившейся через 48 ч, на участке внутрикожного введения туберкулина) у индивидов, инфициро-
ванных МБТ. Вместе с тем ГЧЗТ связывают с иммунной реакцией на факторы, повреждающие ткани.
Связь между иммунным ответом и патогенезом
Локальные и генерализованные туберкулезные повреждения в организме определяются защитными реакциями, которые производит иммунная система организма против МБТ. При описании этого сложнейшего процесса ограничимся простым перечислением событий, происходящих с момента первичного проникновения МБТ в альвеолы до результатов естественной борьбы между макроорганизмом и МБТ. Этот процесс определяет судьбу, по крайней мере, трети населения мира, которое инфицировано микобактериями туберкулеза.
Цикл развития туберкулеза от инфицирования организма микобактериями туберкулеза до клинических проявлений болезни и распространения МБТ в окружающей среде можно условно разделить на 5 этапов.
Этапы
1. Распространение инфекции (инфицирование).
2. Начало инфекции, пролиферация и диссеминация в инфицированном организме.
3. Развитие иммунной реакции организма.
4. Казеация (развитие казеозного некроза) и ускоренное размножение МБТ.
5. Вторичное распространение инфекции (способность инфицировать, заражать).
Краткое описание каждого этапа Этап 1. Распространение инфекции.
1.1. Больной туберкулезом продуцирует аэрозоли, в которых содержатся МБТ (рис. 1-2, см. вклейку).
1.2. Мелкие частицы аэрозоля высыхают и становятся пылевыми частицами.
1.3. Пылевые частицы, содержащие микобактерии, вдыхаются человеком.
1.4. Частицы проникают через бронхи и скапливаются в альвеолах.
1.5. Микобактерии поглощаются альвеолярными макрофагами неиммунизированного организма.
1.6. Если альвеолярные макрофаги способны уничтожить МБТ, инфекция не развивается.
Этап 2. Начало инфекции, пролиферация и диссеминация.
2.1. МБТ выживают и размножаются в альвеолярных макрофагах.
2.2. Размножающиеся МБТ убивают альвеолярные макрофаги, макрофаги распадаются, высвобожденные хемокины и МБТ взаимодействуют с новыми клетками.
2.3. Вновь сформированные макрофаги и моноциты захватывают и переваривают МБТ.
2.4. Киллерные клетки и T-лимфоциты начинают накапливаться в поврежденных участках.
2.5. МБТ продолжают размножаться, убивая клетки макроорганизма, и распространяться локально (в участке своего первоначального внедрения).
2.6. МБТ транспортируются во внутригрудные лимфатические узлы, откуда распространяются в системные органы.
Этап 3. Развитие иммунного ответа макроорганизма.
Развитие туберкулезного процесса в течение 3-го этапа может происходить в двух вариантах.
Вариант 3.1. У большинства пациентов в течение 3-го этапа появляется достаточная устойчивость, чтобы подавлять развитие туберкулеза на протяжении всей жизни.
3.1.1. Размножение МБТ останавливается, а их количество резко уменьшается.
3.1.2. Первичный фокус и его дочерние фокусы оставляют после себя минимальные остаточные проявления.
3.1.3. Туберкулиновый кожный тест становится положительным. Вариант 3.2 (неблагоприятный). При недостаточно активной
иммунной реакции происходит прогрессирование туберкулезного процесса. Оно чаще наблюдается среди ВИЧ-инфицированных, детей, а также у лиц, предрасположенных к туберкулезу.
У некоторых пациентов возникает реактивация скрытой туберкулезной инфекции. Реактивация может происходить вне легких или в самом легком и закончиться тканевым повреждением, формированием полости распада и вторичным размножением МБТ.
На клеточном уровне неблагоприятный вариант 3-го этапа характеризуется следующими процессами.
3.2.1. Макрофаги передают туберкулезные антигены Т-лимфоцитам; T-лимфоциты высвобождают цитокины.
3.2.2. Цитокины стимулируют продуцирование и активацию макрофагов. В результате формируется защита от повреждения клеток и тканей.
3.2.3. Указанные реакции ограничивают быстрое размножение и/ или уничтожают МБТ, заканчиваются формированием первичного легочного фокуса.
3.2.4. Если макроорганизм не способен создать эффективную защиту от МБТ, первичный очаг прогрессирует.
Этап 4. Казеация и ускоренное размножение МБТ.
4.1. Туберкулезный фокус в легком реактивируется, подвергается некротизированию (казеации) с последующим формированием полости.
4.2. В этот период МБТ, находящиеся во внеклеточном пространстве, размножаются экспоненциально.
Этап 5. Вторичное распространение инфекции.
Пациент откашливает мокроту, содержащую МБТ, другой человек вдыхает их. Таким образом, процесс заражения человека в некоторых случаях приводит к выделению МБТ в окружающую среду, тем самым продолжается распространение МБТ среди окружающих.
Для развития клинических проявлений туберкулеза необходим комплекс факторов. Известно, что у здоровых людей весьма часто обнаруживаются вирулентные микобактерии туберкулеза, однако заболевают туберкулезом далеко не все их носители. Только при наличии сложной комбинации неблагоприятных внешних и внутренних предрасполагающих факторов, резко снижающих сопротивляемость организма, заражение туберкулезными микобактериями может перейти в заболевание туберкулезом. Вместе с тем заражение туберкулезными микобактериями может закончиться так называемой скрытой инфекцией без серьезных последствий.
Скрытая инфекция
Скрытой инфекцией принято считать такой инфекционный процесс, при котором отсутствуют клинические проявления болезни при наличии жизнеспособных микробов в организме. Существование процесса при скрытой инфекции может быть установлено посредством патоморфологического исследования или при помощи иммунобиологических реакций.
Скрытая инфекция при туберкулезе является:
1) следствием неразвившейся первичной инфекции, при которой МБТ продолжают оставаться в организме;
2) результатом незаконченного процесса после перенесенного туберкулеза.
В обоих случаях в организме находятся туберкулезные микобактерии, но условия возникновения скрытой инфекции разные. В первом случае скрытая инфекция возникает при наличии некоторой врожденной устойчивости организма, благодаря чему инфекционный очаг не развивается. Во втором - она наступает вследствие приобретения организмом иммунитета в процессе болезни, когда остается латентный очаг. В обоих случаях способность организма недостаточна, чтобы уничтожить МБТ.
Следовательно, возникновение скрытой инфекции при туберкулезе зависит как от степени вирулентности туберкулезных микобактерий, так и состояния сопротивляемости и иммунобиологической реактивности макроорганизма. Имеет значение и влияние внешней среды на организм.
1.4. ПАТОЛОГИЧЕСКАЯ АНАТОМИЯ ТУБЕРКУЛЕЗА
Легкие - это основной орган, поражаемый при туберкулезе.
Легкие состоят из долей: правое - из трех (верхняя, средняя, нижняя), левое - из двух (верхняя и нижняя). Доли легких делятся на сегменты. В правом и левом легких разделяют 10 сегментов (рис. 1-3). Сегменты состоят из долек. Всего в легких содержится около 1000 долек. В среднем размер дольки 1-1,5 см. Совокупность долек составляет субсегмент. Несколько субсегментов образуют сегмент.
Каждый сегмент легкого имеет свой бронх и свою артерию, причем как бронхи, так и артерии почти параллельны. Сегменты 7 и 8 в левом легком в большинстве случаев имеют общий бронх.
Бронхолегочные сегменты по форме напоминают треугольник, вершиной обращенный медиально, а основанием - к периферической поверхности. Каждый сегмент легкого отделен от соседнего слоем соединительной ткани.
Бронхи. Два главных бронха начинаются от бифуркации трахеи на уровне 4-го грудного позвонка и заканчиваются в соответствующем легком. После входа в легкие бронхи делятся на долевые. Каждый из
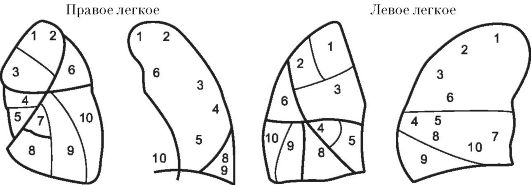 Рис. 1-3. Топография сегментов легких (боковая проекция и вид спереди)
Рис. 1-3. Топография сегментов легких (боковая проекция и вид спереди)
Номенклатура сегментов
Правое легкое | Левое легкое |
Сегменты верхней доли: 1. Верхушечный. 2. Задний. 3. Передний. Сегменты средней доли: 4. Латеральный. 5. Медиальный. Сегменты нижней доли: 6. Верхушечный. 7. Медиальный-базальный. 8. Передний базальный. 9. Латеральный нижний. 10. Задний базальный | Сегменты верхней доли: 1. Верхушечный. 2. Задний. 3. Передний. Сегменты средней доли: 4. Верхнеязычковый. 5. Нижнеязычковый. Сегменты нижней доли: 6. Верхушечный. 7. Медиальный-базальный. 8. Передний базальный. 9. Латеральный базальный. 10. Задний базальный |
них дихотомически делится до концевых (конечных, терминальных) бронхиол (bronchulus terminalis) (рис. 1-4).
Строение легочной паренхимы. Самой мелкой самостоятельной функциональной единицей легочной паренхимы является ацинус (acinus) (рис. 1-4). Это, в известном смысле, легкое в миниатюре диаметром около 1,5 мм.
Ацинус вентилируется конечной бронхиолой (bronchiolus или bronchulus terminalis) - самым мелким разветвлением бронхиального дерева.
Группа ацинусов образует дольку (lobulus), диаметр которой достигает 1-1,5 см.
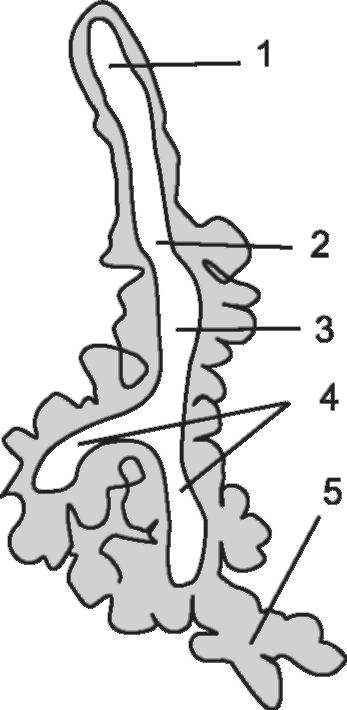 Рис. 1-4. Ацинус:
Рис. 1-4. Ацинус:
1 - конечная бронхиола; 2 - дыхательная бронхиола; 3, 4 - альвеолярные ходы; 5 - альвеолярный мешок. (Розенштраух Л.С. и др., 1987)
Слизистая мембрана, содержащая реснитчатый цилиндрический эпителий, выстилает внутренние стенки бронхов и конечных структур.
Альвеолярные проходы и альвеолы покрыты тонким слоем прозрачного, чешуйчатого эпителия.
Кровеносные сосуды легких. Легочная артерия транспортирует венозную кровь к легким, ее ветви расположены вдоль бронхиальной сети, делясь, повторяют ветвления бронхов. Терминальные отделы легочной артерии заканчиваются густой сетью капиллярных сосудов с последующим формированием венозной сети, которая окружает промежуточные стенки альвеолярных проходов и воздушные ячейки. Обогащенная кислородом кровь возвращается в левое предсердие. Артерии обычно располагаются сверху и сзади бронха, в то время как вены - ниже и впереди его.
Плевра. Каждое легкое окружено серозной оболочкой - плеврой, которая покрывает корень легкого и соответствующие отделы грудной клетки. Та часть мембраны, которая покрывает легкие, называется висцеральной плеврой (pleura visceralis, s. pleura pulmonalis). Она непрерывно переходит на внутренние стенки грудной клетки, где называется париетальной плеврой (pleura parietalis), разделяясь
на реберную (pleura costalis), диафрагмальную (pleura diaphragmatica) и медиастинальную (pleura mediastinalis). Висцеральная плевра очень тонкая, упругая, неразрывно связана со структурой легкого. Париетальная плевра сравнительно толще, имеет малую эластичность и может легко отслаиваться от ребер и межреберных мышц, которые она покрывает.
Лимфатическая система легких. На поверхности легкого сформирована тонкая субплевральная сеть лимфатических сосудов, сообщающаяся посредством пор с плевральной полостью. Паренхима легких содержит два вида лимфатических структур, один из которых формирует сложную сеть, расположенную под слизистой мембраной бронхов, а другой начинается в капиллярах между альвеолярными проходами и альвеолярными мешочками.
Лимфатические сосуды обеих структур заканчиваются в бронхиальных лимфатических узлах корня легкого. Эти узлы, очень многочисленные и часто больших размеров, расположены вокруг бронхов и бифуркации трахеи (рис. 1-5).
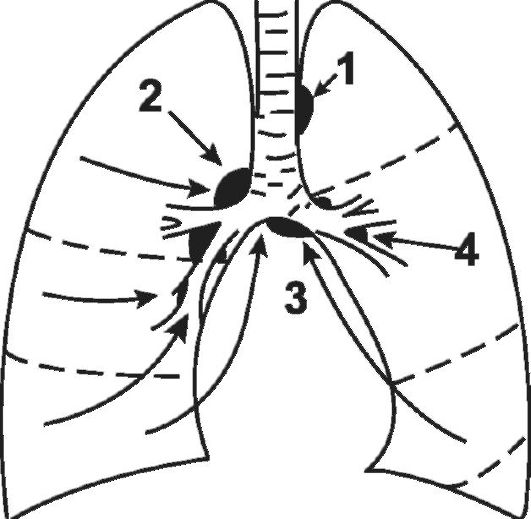 Рис. 1-5. Схема лимфатических узлов средостения и путей оттока лимфы из легких (Розенштраух Л.С. и др., 1987):
Рис. 1-5. Схема лимфатических узлов средостения и путей оттока лимфы из легких (Розенштраух Л.С. и др., 1987):
1 - паратрахеальные узлы; 2 - трахеобронхиальные узлы; 3 - бифуркационные узлы; 4 - бронхопульмональные узлы
Иннервация легких осуществляется симпатическими и парасимпатическими нервами. Симпатические и парасимпатические нервы образуют два сплетения.
1. Переднее легочное сплетение расположено в передних отделах корня легкого и состоит в основном из окончаний глубокого сердечного сплетения.
2. Заднее легочное сплетение расположено в задних отделах корня легкого, в основном состоит из ветвей блуждающего нерва (n. vagus).
Ответвления обоих сплетений следуют вдоль бронхов, а затем распределяются внутри стенок альвеолярных ходов и альвеолярных мешочков.
Средостение. Две плевральные оболочки не соединяются друг с другом, но между ними имеется место, которое содержит все внутригрудные органы, за исключением легких. Это - внутриплевральное пространство, или средостение, которое делится на переднюю, среднюю, заднюю и верхнюю части.
Функции легких. Функции легких тесно связаны с особенностями их строения. Благодаря наличию сотен миллионов альвеол, суммарная поверхность которых достигает 100 м2, и сети капилляров с поверхностью до 80 м2, вместе составляющих альвеолярно-капиллярную перепонку, легкие служат не только для дыхания, но и выделения биологических продуктов, поддержания постоянства температуры тела. Легкие принимают также участие в выработке веществ, участвующих в регуляции свертывания крови, обмена белков, жиров, углеводов.
Туберкулезное воспаление
Туберкулезное воспаление, как и всякое другое, складывается из явлений альтерации, экссудации, пролиферации, приводящих к образованию туберкулезной гранулемы (туберкулезного бугорка) (рис. 1-6-1, 1-6-2, см. вклейку). Название «гранулема» происходит от латинского слова «зерно» - впервые оно было использовано Рудольфом Вирховом (1818) для описания опухолей, которые способны изъязвляться и давать рост грануляционной ткани. Туберкулезная гранулема - не просто скопление клеток, характерных для воспаления, а участок активного действия многочисленных ферментов и цитокинов в очень сложном процессе удаления причинного фактора МБТ.
В формировании туберкулезной гранулемы принимают участие гематогенные (лимфоциты, моноциты, полиморфно-ядерные лейкоциты) и гистиогенные (гистиоциты, макрофаги, фибробласты, ретикулярные клетки, эндотелий кровеносных сосудов, плазматические и тучные клетки) лимфоциты.
Туберкулезная гранулема имеет следующую структуру. В центре ее содержится аморфный тканевой детрит (следствие альтерации и некроза), по периферии частоколом расположен вал из нескольких слоев эпителиоидных клеток. Во внешних слоях бугорка в небольшом количестве обнаруживаются лимфоидные и плазматические клетки. Среди эпителиоидных клеток имеются крупные многоядерные гигантские клетки Пирогова-Лангханса (рис. 1-7, см. вклейку).
Гистогенез туберкулезного бугорка зависит от того, как развивается воспалительный процесс - прогрессирует или, наоборот, регрессирует. При снижении резистентности макроорганизма к туберкулезу происходит прогрессирование туберкулезного воспаления, развивается экссудативная тканевая реакция с появлением творожистого некроза (рис. 1-6а). Творожистый некроз может развиться в бугорке и окружающей его ткани, пропитанной серозно-фибринозным экссудатом.
При дальнейшем прогрессировании специфического туберкулезного воспаления, помимо бугорков, возникают различной величины очаги творожистого некроза (рис. 1-8, см. вклейку). Они могут расплавляться, сливаться в крупные очаги, из которых формируются фокусы с участками казеоза (инфильтраты). Казеоз подвергается разжижению под воздействием протеолитических ферментов и откашливается через бронхи. В этих участках легких появляются полости распада - каверны, а на слизистых оболочках и коже - язвы. Образовавшаяся при распаде казеоза полость (каверна) будет источником диссеминации МБТ в другие отделы легких и образования новых очагов и каверн (рис. 1-17, 1-21).
Особую опасность представляет эрозия кровеносного сосуда, участвующего в кровоснабжении участка казеозного перерождения легочной ткани. При формировании полости кровь из поврежденного сосуда поступает в бронхи, а по ним в другие отделы легких или отхаркивается. При высокой резистентности организма происходит обратное развитие процесса (регрессирование, хронизация заболевания), в результате которого бугорок замещается соединительной тканью, кальцинируется (рис. 1-9, см. вклейку). Эпителиоидные клетки превращаются в фибробласты, аргирофильные волокна коллагенизируются, и бугорок рубцуется. В дальнейшем очаги некроза могут рассосаться, подвергнуться фиброзированию, обызвествлению или окостенению.
Патологическая анатомия первичного туберкулеза легких
Первичный туберкулез развивается после первого контакта макроорганизма с МБТ. Когда частицы воздуха, содержащие МБТ, при вдохе попадают в периферические отделы легких, то они там остаются и медленно размножаются, формируя первичный легочный аффект (очаг). При этом часть микобактерий попадают в лимфу, с которой они транспортируются в близлежащий лимфатический узел. Классическая форма морфологического проявления первичного туберкулеза - первичный туберкулезный комплекс (рис. 1-10, см. вклейку).
В 90% случаев формирование первичного туберкулезного комплекса происходит в верхних и средних отделах легких, но может быть в тонкой кишке, костях и т.д.
В первичном легочном аффекте развивается альвеолит, который быстро сменяется типичным развитием творожистого некроза. В центре первичного аффекта формируется казеоз, по периферии - элементы неспецифического воспаления. Первичный легочный очаг чаще всего располагается непосредственно под плеврой, поэтому в специфический процесс часто вовлекается плевра. В лимфатических сосудах происходит расширение и инфильтрация их стенок и появление бугорков. В регионарных лимфатических узлах возникают элементы воспаления, переходящие в специфические казеозные изменения с некрозом (рис. 1-11).
Перифокальное воспаление вокруг лимфатических узлов распространяется на клетчатку средостения и прилежащую легочную ткань. По тяжести поражения процесс в лимфатических узлах превосходит изменения в области первичного аффекта, поэтому репаративные изменения в лимфатических узлах протекают медленнее.
Динамическое изучение первичных легочных процессов у детей позволило выделить 4 последовательных фазы течения первичного туберкулеза легких (рис. 1-11а, 1-11б, 1-11в, 1-11г):
1) пневмоническая;
2) фаза рассасывания;
3) фаза уплотнения;
4) формирование очага Гона.
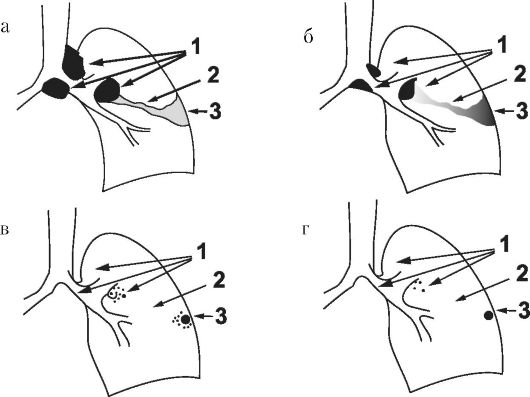 Рис. 1-11. Фазы
течения первичного туберкулеза легких: (а). Первая фаза
(пневмоническая) формирования первичного комплекса (пояснения в тексте);
(б). Вторая фаза (рассасывания); (в). Третья фаза - уплотнение; (г).
Четвертая фаза - формирование очага Гона
Рис. 1-11. Фазы
течения первичного туберкулеза легких: (а). Первая фаза
(пневмоническая) формирования первичного комплекса (пояснения в тексте);
(б). Вторая фаза (рассасывания); (в). Третья фаза - уплотнение; (г).
Четвертая фаза - формирование очага Гона
В первой фазе (пневмонической) определяется очаг бронхолобулярной пневмонии (легочного аффекта) (3) величиной от 1,5-2 до 5 см. Форма легочного аффекта (3) округлая или неправильная, характер неоднородный, контуры размытые (рис. 1-11 а). Одновременно определяются: увеличенные прикорневые лимфатические узлы (1) и усиление бронхо-сосудистого рисунка между очагом и корнем легкого - лимфангит (2).
Воспалительные изменения в легком, в лимфатических узлах (лимфаденит) и лимфатических сосудах (лимфангит) в совокупности называются первичным туберкулезным комплексом. Таким образом, картина первичного туберкулезного комплекса состоит из трех компонентов: изменения в легком (3), лимфангита (2), лимфаденита (1).
Во второй фазе - фаза рассасывания (биполярности) наблюдается уменьшение зоны перифокального воспаления (3), яснее выявляется центрально расположенный казеозный очаг. Уменьшаются
воспалительные изменения в регионарных лимфатических узлах (1) и в районе бронхолегочных сосудов (2) (рис. 1-10б).
В третьей фазе - фазе уплотнения: первичный очаг хорошо очерчен (3), контуры его четкие, по периферии очага имеется начало кальцинации в виде мелких крошек; краевая кальцинация присутствует и в бронхопульмональных лимфатических узлах (1) (рис. 1-11г).
При четвертой фазе на месте очага бронхолобулярной пневмонии (3) кальцинация становится компактной, очаг приобретает округлую форму и ровные четкие контуры, величина его не превышает 3-5 мм. Такое образование называется очагом Гона (рис. 1-11г).
Могут иметь место следующие исходы первичного туберкулезного комплекса:
1) заживление с инкапсуляцией, обызвествлением или окостенением (рис. 1-12, см. вклейку);
2) прогрессирование с развитием различных форм генерализации, присоединением неспецифических осложнений типа ателектаза, пневмосклероза и пр.
При прогрессировании первичного туберкулезного комплекса различают генерализацию (рис. 1-13):
1) гематогенную;
2) лимфогенную;
3) бронхогенную.
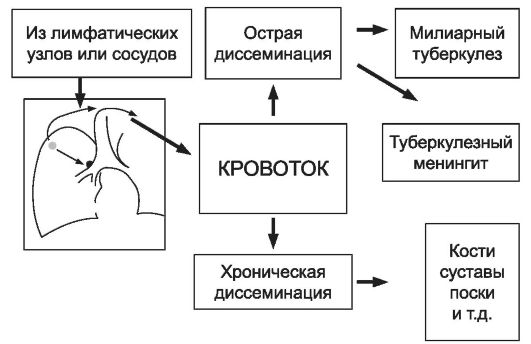 Рис. 1-13. Гематогенная и лимфогематогенная диссеминация МБТ
Рис. 1-13. Гематогенная и лимфогематогенная диссеминация МБТ
Гематогенная генерализация развивается при поступлении микобактерий туберкулеза в кровь. Обязательным условием для гематогенной генерализации является состояние гиперергии. В зависимости от состояния первичного туберкулезного комплекса различают раннюю генерализацию, проявляющуюся в виде:
1) генерализованного милиарного туберкулеза с массивным высыпанием продуктивных или экссудативных узелков во всех органах (рис. 1-14-1, 1-14-2, см. вклейку);
2) очагового туберкулеза с образованием в разных органах до 1 см в диаметре казеозных очагов.
Очаги гематогенной генерализации могут явиться источником развития туберкулеза в различных органах.
Гематогенное распространение микобактерий всегда сочетается с лимфогенным. При этом микобактерии необязательно поступают в кровь одномоментно вследствие прорыва крупного очага некроза. Они могут поступать повторными небольшими порциями, проходя вначале по лимфатическим сосудам. Такой генез дает разные клинико-рентгенологические проявления гематогенно-диссеминированных форм с различным течением, с тяжелым исходом или выздоровлением.
При прогрессировании гематогенно-диссеминированного туберкулеза формируются каверны. Каверны образуются в результате творожистого распада и расплавления некротических масс. При гематогенной форме туберкулеза легких каверны бывают тонкостенными, множественными и располагаются симметрично в обоих легких. В происхождении таких каверн играют роль повреждение кровеносных сосудов, их тромбоз и облитерация. Нарушается питание пораженных участков легких и формируется деструкция по типу трофических язв. С образованием каверн открывается возможность бронхогенного обсеменения здоровых участков легких.
Туберкулезные очаги в лимфатических узлах устойчивы к действию антибактериальных препаратов, являются источником серьезных осложнений: распространения процесса на органы средостения; присоединения вторичной инфекции; развития амилоидоза внутренних органов.
Чаще проявления первичного туберкулеза остаются неактивными (молчащими) в течение десятилетий или всей жизни индивида. Точные механизмы, лежащие в основе этого явления, еще до конца не объяснены. Однако реактивация или реинфекция туберкулеза
могут быть спровоцированы недоеданием, злокачественной болезнью, ВИЧ-инфекцией, использованием иммуносупрессоров и интеркуррентными инфекционными заболеваниями.
Патогенез и патологическая анатомия вторичного туберкулеза
Разделение двух последовательных периодов развития туберкулеза на первичный и вторичный отражает патоморфологическую и клиническую картину болезни.
Послепервичный (вторичный) туберкулез - это определение используется для туберкулеза, который возник в организме, имеющем первичные туберкулезные очаги, ранее излеченные. Возникновение и развитие вторичного туберкулеза может происходить двумя способами:
1) эндогенная суперинфекция (реактивация) остаточных послепервичных очагов (частично кальцинированных лимфатических узлов);
2) экзогенная суперинфекция (реинфекция) - повторное туберкулезное инфицирование. Вторичный туберкулез в 90% случаев является туберкулезом легких. При вторичном туберкулезе начальные признаки часто диагностируются с помощью флюорографии или рентгенографии, которые производятся при профилактическом обследовании у пациентов, не предъявляющих каких-либо жалоб. Эта тенденция - одно из косвенных доказательств, что пациент не ощущает болезни, поскольку туберкулез на начальных этапах развивается бессимптомно. В таких случаях при рентгенологическом обследовании туберкулезные проявления представляют собой фокусы среднего размера в легких или других органах. Однако в легких они встречаются чаще.
Распространение инфекции при прогрессировании вторичного туберкулеза, как правило, идет бронхогенным путем.
Наиболее важным признаком, определяющим, будет ли больной, особенно в старшем возрасте, иметь клинически выраженный туберкулез, является размягчение и разжижение творожистого некротического материала. В этот период происходит быстрое увеличение числа МБТ, которые в этой ситуации начинают размножаться внеклеточно.
Развитие вторичного туберкулеза у взрослых условно можно разделить на этапы (рис. 1-15).
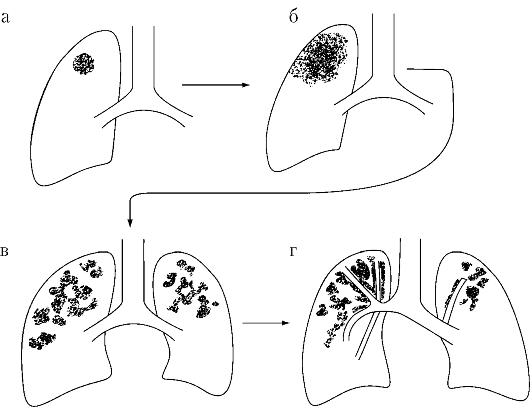 Рис. 1-15. Этапы
развития вторичного туберкулеза у взрослых: а - формирование очагов в
верхних отделах легких у взрослых. Поражения медиастинальных
лимфатических узлов обычно отсутствуют (хотя у африканцев, жителей Азии
или ВИЧ-инфицированных узлы могут быть значительно увеличенными).
Поражения в легких и лимфатических узлах часто уплотняются, процесс
заканчивается формированием кальциноза; б - постепенное распространение в
легких туберкулезных повреждений, формирование казеоза; в - казеоз
(некроз). Жидкие творожистые массы выкашливаются, в результате на этом
месте формируется полость. Диссеминация МБТ из полости приводит к
распространению процесса в противоположное легкое с формированием в нем
полости; г - после одного-двух лет эффективного лечения (если пациент
выживает) на месте специфических поражений развивается фиброз
(рубцевание) полости, смещение средостения и трахеи в сторону наибольших
повреждений.
Рис. 1-15. Этапы
развития вторичного туберкулеза у взрослых: а - формирование очагов в
верхних отделах легких у взрослых. Поражения медиастинальных
лимфатических узлов обычно отсутствуют (хотя у африканцев, жителей Азии
или ВИЧ-инфицированных узлы могут быть значительно увеличенными).
Поражения в легких и лимфатических узлах часто уплотняются, процесс
заканчивается формированием кальциноза; б - постепенное распространение в
легких туберкулезных повреждений, формирование казеоза; в - казеоз
(некроз). Жидкие творожистые массы выкашливаются, в результате на этом
месте формируется полость. Диссеминация МБТ из полости приводит к
распространению процесса в противоположное легкое с формированием в нем
полости; г - после одного-двух лет эффективного лечения (если пациент
выживает) на месте специфических поражений развивается фиброз
(рубцевание) полости, смещение средостения и трахеи в сторону наибольших
повреждений.
Кальцинация начинает формироваться на самых ранних этапах образования туберкулезных очагов, расположенных в верхушках
легких. Вместе с тем полости могут сохраняться. Эта форма хронического туберкулеза является главным источником инфекции.
Разнообразие патоморфологических проявлений в легких явилось основой для классифицирования туберкулеза органов дыхания на формы:
- очаговый туберкулез;
- инфильтративный туберкулез;
- казеозная пневмония;
- туберкулема;
- кавернозный туберкулез;
- фиброзно-кавернозный туберкулез;
- цирротический туберкулез;
- туберкулезный плеврит;
- туберкулез бронхов, трахеи, верхних дыхательных путей;
- туберкулез органов дыхания;
- комбинированный с профессиональными пылевыми заболеваниями легких.
Очаговый туберкулез легких
Очаговый туберкулез легких относится к проявлениям вторичного туберкулеза и представляет собой начальную форму туберкулеза легких у взрослых. К нему относятся: свежий, или мягкоочаговый, туберкулез и фиброзно-очаговый туберкулез, более давний, с очаговыми образованиями не более 1 см в диаметре (рис. 1-16, см. вклейку).
Свежий очаговый туберкулез легких морфологически проявляется развитием эндо- и перибронхита мелких апикальных веточек системы 1-го и 2-го сегментарных бронхов с последующим казеозным некрозом стенок бронхов. Вовлечение в процесс прилежащих альвеол приводит к образованию очага казеозной ацинозной или лобулярной бронхопневмонии.
В течение длительного периода процесс ограничивается территорией ацинуса или дольки. При тенденции к прогрессированию в окружности первоначально возникших очагов появляются новые, развивающиеся путем контакта в пределах того же легочного сегмента. В лимфатических путях, соединительнотканных прослойках, перибронхиальной и периваскулярной тканях отмечается лимфостаз, переходящий на корень легкого.
Типичныйпутьпрогрессированияочаговоготуберкулезалегких - бронхогенный, с развитием новых бронхопневмонических очагов. Поражение лимфатических узлов не характерно.
При благоприятном течении очаги бронхопневмонии подвергаются инкапсуляции, обызвествлению, фиброзу или гиалинозу.
Очаги («реинфекты») при фиброзно-очаговом туберкулезе легких носят характер латентно протекающих, но при неблагоприятных условиях возможно обострение с экссудативной реакцией и ростом зоны некроза.
При туберкулезном поражении бронхиального дерева и попадании МБТ в мокроту возникает открытая форма туберкулеза легких.
При затихании процесса нередко развивается диффузный склероз верхних сегментов.
Инфильтративный туберкулез легких
Инфильтративный туберкулез легких известен давно. T.H. Laenec (1781-1926) на основании секционных данных описал его как желатинозную пневмонию.
Инфильтрат развивается в результате обострения инкапсулированных очагов, которые могут быть не только в легких, но и во внутригрудных лимфатических узлах.
Когда инфильтративный фокус возникает в неизмененной ткани или вокруг свежего очага и слившихся нескольких очагов, развивается перифокальное воспаление.
Инфильтративный туберкулез легких характеризуется развитием воспалительных изменений, преимущественно экссудативного характера, с казеозным некрозом и в сочетании или без деструкции легочной ткани.
Инфильтративный туберкулез легких может быть различного происхождения. У одних больных инфильтративные фокусы развиваются в результате бронхогенного заноса МБТ в здоровую легочную ткань из обострившихся латентных верхушечных очагов. У других - инфильтрат представляет собой перифокальное воспаление на фоне небольших и поэтому трудноопределяемых рентгенологически очагов более давнего происхождения.
Патологоанатомически инфильтративный туберкулез легких характеризуется наличием одного или нескольких мелких, разной давности очагов творожистого некроза с зоной перифокального воспаления, в несколько раз превосходящей их по размерам.
Характер экссудата при этом различный: серозный, серознофибринозный; встречаются десквамативный альвеолит, казеозная инфильтрация. По протяженности процесс может ограничиваться не только долькой, но и занимать всю долю легкого.
Пролиферативная реакция заканчивается развитием соединительной ткани, оставляя после себя фиброзные интерстициальные изменения - индурационное поле.
Исходы инфильтративного туберкулеза легких:
1. Полная резорбция перифокальной зоны или карнификация пораженного участка с инкапсуляцией и обызвествлением казеозных очагов (переход в фиброзно-очаговую форму).
2. Казеация зоны перифокального воспаления, присоединение распада, секвестрации и переход в казеозную пневмонию или острый кавернозный туберкулез легких (рис. 1-17, см. вклейку).
3. При наклонности к казеозному некрозу инфильтрат подвергается полному или частичному распаду. В результате формируется пневмониогенная каверна, размеры которой зависят от объема инфильтративно-пневмонического фокуса и некроза.
Казеозная пневмония возникает чаще всего в результате прогрессирования инфильтративного туберкулеза, но может осложнить течение любой формы туберкулеза легких (рис. 1-18, см. вклейку). Основной морфологический признак казеозной пневмонии - преобладание казеозных изменений над неспецифическими перифокальными. В зависимости от размера пораженного участка легкого различают:
1) ацинозную;
2) лобулярную сливную;
3) сегментарную;
4) лобарную казеозную пневмонию.
При прогрессировании казеозной пневмонии развивается туберкулез легких с многочисленными кавернами.
Туберкулема легких
Туберкулема легких - своеобразное клинико-анатомическое проявление вторичного туберкулеза легких, характеризующееся образованием в легких плотного казеозного фокуса (иногда нескольких) округлой формы, четко отграниченного от окружающей ткани фиброзной капсулой (рис. 1-19, см. вклейку).
Источником формирования туберкулем в основном служат две формы туберкулеза легких: инфильтративная и очаговая. Кроме того, туберкулемы образуются из кавернозного туберкулеза посредством заполнения каверны казеозом.
Заполненные каверны относятся к туберкулемам лишь условно, поскольку заполнение каверны происходит механически, в то время как туберкулемы - это своеобразный феномен в легочной ткани.
Туберкулемы могут быть: а) солитарными (гомогенные); б) слоистого строения на разрезе; в) конгломератными, состоящими из группы очагов с общей капсулой (рис. 1-20, см. вклейку).
Варианты прогрессирования туберкулемы:
1) развитие перифокального воспаления;
2) кавернизация - высвобождение из полости туберкулемы казеозных масс через дренирующий бронх.
Кавернозный туберкулез легких
Кавернозный туберкулез характерен наличием тонкостенной каверны, без перифокального воспаления, с единичными очагами в окружающей легочной ткани (рис. 1-21, см. вклейку).
Кавернозный туберкулез легких возникает:
1) в результате высвобождения казеозных масс из очага инфильтративно-пневмонического туберкулеза легких (пневмониогенная острая каверна);
2) из туберкулемы, путем отторжения казеозных масс. Туберкулезная каверна в легком представляет собой округлое
образование, имеющее капсулу различного размера (2-3 см в диаметре), без перифокального воспаления, с единичными очагами в окружающей легочной ткани. По внутренним границам капсулы расположены остатки казеоза с просветом в центре (рис. 1-21-1, см. вклейку).
Осложнения кавернозного туберкулеза. Для кавернозного туберкулеза легких характерен бронхогенный путь прогрессирования. Из осложнений следует отметить возможность профузных кровотечений. Кавернозный туберкулез легких при дальнейшем течении переходит в фиброзно-кавернозный.
Фиброзно-кавернозный туберкулез легких
Фиброзно-кавернозный туберкулез легких возникает в результате прогрессирования любой формы туберкулеза легких с образованием каверны, в стенке которой выражен фиброзный компонент (рис. 1-21-2, см. вклейку). Конечно, при далеко зашедшей фибрознокавернозной форме не всегда легко определить, какой процесс был ее источником и что послужило причиной ее развития.
Фиброзно-кавернозный туберкулез характеризуется трехслойным строением стенки каверны, включающим: внутренний слой некроза (а); под ним слой туберкулезной (специфической) грануляционной ткани (б) и снаружи неспецифическая грануляционная ткань (в) (рис. 1-21-2, см. вклейку). Переход от кавернозного туберкулеза к
фиброзно-кавернозному морфологически состоит в развитии склеротических изменений как в стенке каверны, так и в окружающей ее легочной ткани. С течением времени изменяются структура стенки и вид каверны. Наружный слой может быть различной толщины, так как в его состав может входить прилегающая к каверне ателектазированная ткань легкого.
Для фиброзно-кавернозного туберкулеза характерны очаги бронхогенного отсева различной давности. Как правило, поражается дренирующий каверну бронх. Развиваются и другие морфологические изменения в легких: пневмосклероз, эмфизема, бронхоэктазы.
Прогрессирование заболевания происходит по контакту и по бронхам в направлении от верхушки легкого к основанию. Поражение бронхиального дерева отмечается во всех случаях фиброзно-кавернозного туберкулеза легких.
Протяженность изменений в легких может быть различной. Процесс бывает односторонним и двусторонним, с наличием одной или множества каверн.
Цирротический туберкулез легких
Циррозы легких представляют собой активную фазу развития туберкулеза легких, возникающую в результате разрастания в легких соединительной ткани. Массивные склеротические изменения развиваются также при карнификации инфильтративно-пневмонических, диссеминированных или фиброзно-кавернозных процессов, фибротизации легочной ткани в результате длительного легочного ателектаза.
Цирротический туберкулез легких представляет собой массивное, диффузного характера разрастание соединительной ткани в сочетании с деформацией легочной ткани и развитием бронхоэктазов. Каверны (полости) деформированы (рис. 1-22, см. вклейку).
При инволюции инфильтрата или фиброзно-кавернозного туберкулеза цирроз может быть односторонним или двусторонним. При значительном объеме склеротических изменений развиваются гипертония малого круга кровообращения, легочное сердце и легочно-сердечная недостаточность. К основным осложнениям относятся также амилоидоз внутренних органов и тромбоэмболия легочной артерии.
Цирротическому процессу в легких сопутствует викарная эмфизема, которая развивается в непораженных отделах легких. Замещение нормальной легочной ткани рубцовой, деформация брон-
хиального просвета нарушают функцию бронхов, приводят к застою в них секрета, в котором размножается микробная флора. Деформация бронхов способствует развитию бронхоэктазов. В условиях пневмосклероза происходят деформация сосудов, сужение и облитерация их просвета.
Структурные изменения бронхов, уменьшение дыхательных экскурсий из-за плевральных сращений и эмфиземы приводят к нарушению функции дыхания. Массовая гибель альвеол и легочных капилляров нарушает альвеолярный газообмен. Развиваются гипоксемия и гипоксия.
Дыхательная недостаточность компенсируется гипертрофией мышцы правых отделов сердца. Когда компенсаторные возможности сердца иссякают, к дыхательной недостаточности присоединяется сердечная - развивается синдром «легочного сердца».
В более поздних стадиях болезни к правожелудочковой недостаточности присоединяется недостаточность левого желудочка. Одной из основных причин смерти больных цирротическим туберкулезом легких является недостаточность кровообращения.
Туберкулезный плеврит
Плеврит - воспаление плевры. Различают две основные формы плеврита: сухой, или фибринозный (pleuritis sicca, fibrinosa), и выпотной, или экссудативный (pleuritis exsudativa).
При туберкулезе плевра вовлекается в воспалительный процесс при проникновении в нее инфекции лимфогенным, гематогенным и контактным путем. Вовлечение плевры в различные патологические процессы обусловлено тесными анатомо-топографическими связями висцеральной и париетальной плевры с легочной тканью, внутригрудными лимфатическими узлами (рис. 1-23). Плевра, обладая барьерной функцией, реагирует на разнообразные патофизиологические сдвиги в организме, в результате чего в ней развиваются воспалительные или аллергические процессы.
Экссудативно-воспалительная реакция плевры связана с повышенной проницаемостью кровеносных и лимфатических капилляров кортикального слоя легких и самой плевры, пропускающих жидкую часть крови в межтканевые щели, поверхностные слои плевры и оттуда, вследствие отрицательного давления, в плевральную щель.
Лимфогенные плевриты. Туберкулезная инфекция может поражать субплевральные лимфатические узлы. Оседая в них, микобак-
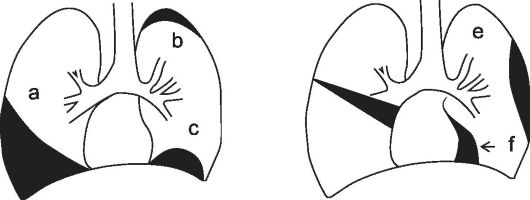 Рис. 1-23. Типичные
локализации выпота в плевральной полости: а) костно-диафрагмальный; b)
диафрагмальный; с) костальный; d) междолевой; e) парамедиастинальный; f)
верхушечный
Рис. 1-23. Типичные
локализации выпота в плевральной полости: а) костно-диафрагмальный; b)
диафрагмальный; с) костальный; d) междолевой; e) парамедиастинальный; f)
верхушечный
терии туберкулеза частично замуровываются и погибают, частично же, сохраняя свою вирулентность, распространяются по лимфатическим путям и вызывают субплевральные кортикальные лимфангиты либо экссудативные плевриты.
Гематогенные плевриты. Возможен гематогенный занос туберкулезной инфекции в плевральную полость с развитием на плевре туберкулезных бугорков. Исходным очагом является активный туберкулезный процесс в прикорневых лимфатических узлах.
Контактный путь распространения инфекции возникает при активном туберкулезе лимфатических узлов средостения с поражением висцеральной плевры.
Фибринозный плеврит (сухой плеврит). При фибринозном плеврите на плевре вначале появляется нежный, легко снимающийся фибринозный налет. В дальнейшем образуется фибринозная пленка желтоватого или желтовато-серого цвета.
Гнойный плеврит (эмпиема плевры) редко с самого начала возникает как гнойный, чаще развивается вслед за серозно-фибринозным воспалением плевры. Процесс обычно бывает односторонним и преимущественно располагается в базальной или задней части полости плевры. Гнойный плеврит наблюдается при прорыве казеозных масс из легкого в полость плевры, бронхоплевральных свищах и т.п.
Геморрагический плеврит сопровождается проникновением в полость плевры экссудата, содержащего значительную примесь эритроцитов.
Исходы плевритов
Фибринозный экссудат в подавляющем большинстве случаев рассасывается лишь частично, а в основном подвергается организации, что ведет к развитию спаек, фиброзному утолщению плевры, облитерации плевральных полостей.
Гнойный экссудат редко подвергается полному рассасыванию, чаще наблюдается инкапсуляция воспалительного выпота (эмпиема).Воспалительный процесс при эмпиеме плевры может переходить на интерстициальную ткань легкого (гнойная пневмония).
Хронические плевриты
Чаще всего хроническое течение плевритов наблюдается при эмпиеме плевры. В этих случаях экссудат сгущается, распадается, превращается в сыровидную массу или кашицу с наличием кристаллов холестерина; микроорганизмы могут исчезнуть. Плевральные листки бывают резко утолщены, плотны, иногда с очаговой петрификацией и даже оссификацией. Значительные отложения известковых масс особенно характерны для туберкулезной эмпиемы. Эмпиема плевры может вести к гнойно-резорбтивной лихора дке, сепсису, истощению, амилоидозу внутренних органов. Иногда затяжное, хроническое течение наблюдается при серозно-фибринозных и фибринозных плевритах.
При острых и хронических плевритах значительное накопление экссудата в плевральной полости вызывает ателектаз легкого и смещение органов средостения в противоположную сторону.
Туберкулез бронхов, трахеи, верхних дыхательных путей
Туберкулез бронхов, трахеи, верхних дыхательных путей и др. (носа, полости рта, глотки) встречается как осложнение других форм первичного и вторичного туберкулеза легких и внутригрудных лимфатических узлов, лишь иногда эти поражения, особенно туберкулез бронхов, бывают изолированными. Патолого-анатомические изменения при туберкулезе бронхов, трахеи, верхних дыхательных путей и др. (носа, полости рта, глотки) характеризуются образованием обычных эпителиоидных бугорков с гигантскими клетками типа Пирогова-Лангханса, с пролиферацией соединительной ткани. Образование очагов некроза, творожистого распада, отеков с наличием МБТ, обнаруженных при гистологическом исследовании, характеризует преимущественно экссудативный тип реакции.
Эпителиоидные бугорки чаще всего лежат поверхностно и непосредственно под эпителием. Вследствие творожистого распада при прогрессирующем развитии инфильтратов, туберкулов, расположенных под эпителием, наступает образование язв.
Процессы заживления патоморфологически характеризуются мощным развитием фиброзной соединительной ткани, прорастающей туберкулезные бугорки и инкапсулирующей их.
1.5. ЭПИДЕМИОЛОГИЯ ТУБЕРКУЛЕЗА
Распространенность туберкулезной инфекции и клинические проявления ее разнообразны. Поэтому понимание эпидемиологии туберкулеза особенно важно, поскольку является основой для разработки мер профилактики, диагностики, лечения, программ борьбы с этим заболеванием для органов здравоохранения.
Задачи эпидемиологии туберкулеза:
1. Определение угрожаемых групп.
2. Масштабы и значение инфекции.
3. Временные характеристики заболевания.
4. География заболеваний.
5. Резервуары и механизмы передачи.
6. Факторы риска: почему одни инфицированные лица заболевают, а другие нет.
Эпидемиологические определения (термины)
Эпидемиологическая обстановка в отношении туберкулеза характеризуется следующими статистическими показателями: инфицированность, заболеваемость, болезненность, смертность.
Инфицированность - процент лиц с положительными реакциями на туберкулин, если они не имеют поствакцинного характера.
Заболеваемость туберкулезом (частота новых случаев) - это число новых случаев активных форм туберкулеза, встречающихся в определенной популяции в течение обозначенного периода времени. Обычно заболеваемость туберкулеза представляется числом случаев на 100 000 населения в год.
Распространенность (болезненность/пораженность) туберкулеза - число больных активным туберкулезом, состоящих на учете на конец года на 100 000 населения; особое значение имеет показа-
тель болезненности открытыми формами туберкулеза легких. Таким образом, распространенность отражает совокупную болезненность туберкулезом. Если бы все новые случаи были быстро излечены, то частота новых случаев и распространенность стали бы близко совпадающими. Но если пациенты не получают лечения или не полностью излечиваются, то накапливаются хронические формы туберкулеза, тем самым формируя различия в частоте новых случаев и распространенности туберкулеза.
Смертность от туберкулеза - число лиц, умерших от туберкулеза на 100 000 населения.
К бактериовыделителям (МБТ+) - открытый туберкулез легких относятся больные туберкулезом легких, у которых в содержимом, полученном из органов дыхания, обнаружены МБТ с помощью микроскопии или с использованием специальных методов окрашивания. Такие случаи также называются бациллярными.
МБТ отрицательный (МБТ-) туберкулез легких, когда при микроскопии мокроты не выявлены микобактерии туберкулеза. В этом случае диагноз туберкулеза устанавливается на основании симптомов, наличия роста МБТ в культуре, изменения на рентгенограмме грудной клетки, отражающих динамику развития болезни, и/или других вспомогательных данных: положительная реакция на туберкулин, эпидемиологические характеристики, для детей - наличие контактов с больным туберкулезом.
Внелегочный туберкулез. К внелегочному относят проявления активного туберкулеза в других органах, вне легких. Большинство пациентов имеют или туберкулез легких, или внелегочный туберкулез; только у небольшого числа больных одновременно наблюдаются сочетанные проявления туберкулеза. Хотя внелегочный туберкулез и туберкулез легких без наличия МБТ в мокроте являются компонентами общей заболеваемости туберкулезом, они менее существенны с эпидемиологической точки зрения по сравнению с МБТ+ случаями, поскольку последние являются инфицирующими факторами туберкулеза.
Ежегодный показатель инфицирования (ЕПИ) является примером новых случаев инфицирования среди туберкулинотрицательных (ранее не инфицированных) представителей данной группы населения, у которых произошел вираж туберкулиновых проб. ЕПИ используется как косвенный или расчетный показатель распространенности МБТ+ (заразных) больных туберкуле-
зом в данной группе населения. Проводя наблюдения за группой лиц, известных как туберкулинотрицательные, и регистрируя частоту появления положительных туберкулиновых тестов среди них, в течение определенного времени делаются попытки оценить общую заболеваемость туберкулезом в данной группе населения и сравнить их с различными информационными базами.
Инфицированные туберкулезом лица - это наличие жизнеспособных микобактерий туберкулеза в организме без клинических признаков заболевания. Большинство практически здоровых лиц, подвергнувшихся инфицированию МБТ, находятся в этом состоянии в течение всей жизни.
Больные туберкулезом - это лица, в организме которых имеются активные, вирулентные МБТ. Обычно это проявляется клиническими симптомами поражения отдельных систем и органов. В большинстве таких случаев туберкулиновый тест резко положительный. Наиболее важным подтверждением туберкулеза является наличие МБТ в мокроте или тканях различных органов.
Для получения сравнительных данных и информационного обеспечения Всемирная организация здравоохранения рекомендует систему классификации больных или лиц, подозрительных на туберкулез и находящихся в контакте с больными туберкулезом.
Информация, собранная при помощи этой классификации, формирует основу для санитарной статистики в мире. За случай туберкулеза принимается заболевание, подтвержденное обнаружением микобактерий туберкулеза, выделенных из очага поражения (с мокротой, мочой и т.д.) или полученных из тканей путем биопсии.
В соответствии с этой классификацией пациенты делятся на 6 групп.
Группа 0. В этой группе регистрируются лица, имеющие отрицательный туберкулиновый тест и не состоящие в контакте с больным туберкулезом.
Группа 1. Подвергнувшиеся туберкулезной инфекции, при отсутствии симптомов инфицирования. Лица, контактирующие с больным туберкулезом, но имеющие отрицательный туберкулиновый тест. Если это ребенок, то должны отсутствовать рентгенологические симптомы в грудной клетке. Может возникнуть необходимость в подтверждении состояния через 3 мес.
Группа 2. Туберкулезное инфицирование есть, но клинических признаков нет. Пациенты с выраженной туберкулиновой реакцией,
при отсутствии клинических, рентгенологических и бактериологических признаков болезни.
Группа 3. Клинически активный туберкулез. Группа включает всех пациентов с клинически активным туберкулезом, у которых результаты обследования подтверждают диагноз; если результаты обследования сомнительны, данный случай следует отнести в группу 5.
Группа 4. Клинически не активный туберкулез. В анамнезе заболевание туберкулезом или патологические, но стабильные рентгенологические признаки в легких, положительный туберкулиновый тест, отрицательные бактериологические тесты (если выполнены) и отсутствие клинических или рентгенологических признаков болезни. Пока активность заболевания не исключена, такой случай должен быть включен в группу 5.
Группа 5. Подозрение на наличие туберкулеза (предполагаемый диагноз). Пациенты, у которых подозревается наличие активного туберкулеза на основании клинических, рентгенологических и/или эпидемиологических данных. Этот статус используется в течение 3 мес, пока не будет установлен точный диагноз.
Общемировая и континентальная эпидемиология туберкулеза. Общее представление о туберкулезе в мире в настоящее время сформировано на основании совокупности прямых наблюдений и расчета, описанного выше показателем ЕПИ. Поскольку туберкулез наиболее распространен в экономически бедных странах, которые, как правило, не имеют эффективной санитарной статистики, многие показатели о состоянии туберкулеза здесь получены косвенным путем.
Из-за неполной регистрации случаев туберкулеза именно в тех регионах, где заболевание наиболее распространено, эти показатели занижены. При рассмотрении тенденции изменений эпидемиологических показателей туберкулеза имеются четкие различия между промышленно развитыми странами, где показатели туберкулеза устойчиво и существенно снизились, и развивающимися, где эти показатели остались устойчивыми или повысились. Снижение показателей распространенности туберкулеза в развивающихся странах явилось результатом расчета относительных показателей при взрывном характере прироста населения.
Общий пул инфицированных и больных туберкулезом в мире растет.