Общая неврология А.С. Никифоров, Е.И. Гусев - 2007г. - 720 с
|
|
|
|
ГЛАВА 13 ВЕГЕТАТИВНАЯ НЕРВНАЯ СИСТЕМА, ЕЕ СТРОЕНИЕ, ФУНКЦИИ
13.1. ОБЩИЕ ПОЛОЖЕНИЯ
Вегетативная нервная система может рассматриваться как комплекс структур, входящих в состав периферического и центрального отделов нервной системы, обеспечивающий регуляцию функций органов и тканей, направленную на поддержание в организме относительного постоянства внутренней среды (гомеостаз). Кроме того, вегетативная нервная система участвует в осуществлении адаптационно-трофических влияний, а также различных форм физической и психической деятельности.
Входящие в состав головного и спинного мозга структуры вегетативной нервной системы составляют центральный ее отдел, остальные - периферический. В центральном отделе принято выделять надсегментарные и сегментарные вегетативные структуры. К надсегментарным относятся участки коры больших полушарий (главным образом располагающиеся медиобазально), а также некоторые образования промежуточного мозга, прежде всего гипоталамуса. Сегментарные структуры центрального отдела вегетативной нервной системы располагаются в стволе головного мозга и в спинном мозге. В периферической нервной системе вегетативная ее часть представлена вегетативными узлами, стволами и сплетениями, афферентными и эфферентными волокнами, а также вегетативными клетками и волокнами, находящимися в составе структур, которые обычно рассматриваются как анимальные (спинномозговые узлы, нервные стволы и пр.), хотя на самом деле имеют смешанный характер.
Среди надсегментарных вегетативных образований особую значимость имеет гипоталамический отдел промежуточного мозга, функция которого в значи- тельной степени контролируется другими структурами головного мозга, в том числе корой больших полушарий. Гипоталамус обеспечивает интеграцию функций анимальной (соматической) и более древней в филогенетическом отношении вегетативной нервной системы.
Вегетативная нервная система известна также как автономная ввиду ее некоторой, хотя и относительной, автономности, или висцеральная в связи с тем, что через посредство ее осуществляется регуляция функций внутренних органов.
13.2. ИСТОРИЯ ВОПРОСА
Первые сведения о структурах и функциях вегетативных структур связаны с именем Галена (ок. 130-ок. 200), так как именно он, изучая черепные нер-
вы, описал блуждающий нерв и пограничный ствол, который им был назван симпатическим. В изданной в 1543 г. книге А. Везалия (1514-1564) «Строение человеческого тела» дано изображение этих образований и описаны ганглии симпатического ствола.
В 1732 г. Дж. Уинслоу (Winslow J., 1669-1760) выделил три группы нервов, ветви которых, оказывая содружественное влияние друг на друга («симпатию»), распространяются на внутренние органы. Термин «вегетативная нервная система» для обозначения нервных структур, регулирующих функцию внутренних органов, ввел в 1807 г. немецкий врач И. Рейль (Reill I.). Французский анатом и физиолог М.Ф. Биша (Bicha M.F., 1771-1802) считал, что рассеянные в разных частях тела симпатические узлы действуют самостоятельно (автономно) и от каждого из них идут ветви, которые соединяют их между собой и обеспечивают их влияние на внутренние органы. В 1800 г. им же было предложено деление нервной системы на вегетативную (растительную) и анимальную (животную). В 1852 г. французский физиолог Клод Бернар (Bernard Claude, 1813-1878) доказал, что раздражение шейного отдела симпатического нервного ствола ведет к расширению сосудов, описав, таким образом, сосудодвигательную функцию симпатических нервов. Он установил также, что укол дна IV желудочка мозга («сахарный укол») изменяет состояние углеводного обмена в организме.
В конце XIX в. английский физиолог Дж. Ленгли (Langley J.N., 1852-1925) ввел термин «автономная нервная система», отметив при этом, что слово «автономная», без сомнения, указывает на большую степень независимости от центральной нервной системы, чем это есть в действительности. На основании морфологических различий, а также признаков функционального антагонизма отдельных вегетативных структур Дж. Ленгли выделил симпатический и парасимпатический отделы автономной нервной системы. Им же было доказано, что в ЦНС существуют центры парасимпатической нервной системы в составе среднего и продолговатого мозга, а также в крестцовых сегментах спинного мозга. В 1898 г. Дж. Ленгли установил в периферической части вегетативной нервной системы (на пути от структур ЦНС к рабочему органу) наличие синаптических аппаратов, расположенных в вегетативных узлах, в которых происходит переключение эфферентных нервных импульсов с нейрона на нейрон. Он отметил, что в составе периферического отдела вегетативной нервной системы есть преганглионарные и постганглионарные нервные волокна и довольно точно описал общий план строения автономной (вегетативной) нервной системы.
В 1901 г. Т. Эллиотт (Elliott T.) высказал предположение о химической передаче нервного импульса в вегетативных узлах, а в 1921 г. в процессе экспериментальных исследований это положение подтвердил австрийский физиолог О. Леви (Loewi O., 1873-1961) и, таким образом, положил начало учению о медиаторах (нейротрансмиттерах). В 1930 г. американский физиолог У. Кеннон (Cannon W., 1871-1945), изучая роль гуморального фактора и вегетативных механизмов в поддержании относительного постоянства внутренней среды организма, ввел термин «гомеостаз», а в 1939 г. установил, что если в функциональном ряду нейронов в одном из звеньев прерывается движение нервных импульсов, то возникающая при этом общая или частичная денервация последующих звеньев цепи вызывает повышение чувствительности всех находящихся в них рецепторов к возбуждающему или тормозящему действию
химических веществ (в том числе медикаментов), обладающих свойствами, подобными соответствующим медиаторам (закон Кеннона-Розенблюта).
Значительна роль в познании функций вегетативной нервной системы немецкого физиолога Э. Геринга (Hering Е., 1834-1918), открывшего синокаротидные рефлексы, и отечественного физиолога Л.А. Орбели (1882-1958), создавшего теорию адаптационно-трофического влияния симпатической нервной системы. Расширению представлений о клинических проявлениях поражения вегетативной нервной системы способствовали многие клиницисты-неврологи, в том числе наши соотечественники М.И. Аствацатуров, Г.И. Маркелов, Н.М. Иценко, И.И. Русецкий, А.М. Гринштейн, Н.И. Гращенков, Н.С. Четвериков, А.М. Вейн.
13.3. СТРОЕНИЕ И ФУНКЦИИ ВЕГЕТАТИВНОЙ НЕРВНОЙ СИСТЕМЫ
С учетом особенностей строения и функции сегментарного отдела вегетативной нервной системы в нем различают преимущественно симпатический и парасимпатический отделы (рис. 13.1). Первый из них обеспечивает главным образом катаболические процессы, второй - анаболические. В состав симпатического и парасимпатического отделов вегетативной нервной системы входят как афферентные, так и эфферентные, а также вставочные структуры. Уже на основании этих данных можно изложить схему построения вегетативного рефлекса.
13.3.1. Дуга вегетативного рефлекса (принципы построения)
Наличие афферентного и эфферентного отделов вегетативной нервной системы, а также ассоциативных (вставочных) образований между ними обеспечивает формирование вегетативных рефлексов, дуги которых замыкаются на спинномозговом либо церебральном уровне. Их афферентное звено представлено рецепторами (главным образом, хеморецепторами), расположенными практически во всех органах и тканях, а также отходящими от них вегетативными волокнами - дендритами первых чувствительных вегетативных нейронов, которые обеспечивают проведение вегетативных импульсов в цент- ростремительном направлении к телам этих нейронов, расположенных в спин- номозговых узлах или в их аналогах, находящихся в составе черепных нервов. Далее вегетативные импульсы, следуя по аксонам первых чувствительных нейронов через задние спинномозговые корешки, входят в спинной или головной мозг и заканчиваются у вставочных (ассоциативных) нейронов, входящих в состав сегментарных вегетативных центров спинного мозга или ствола мозга. Ассоциативные нейроны, в свою очередь, имеют многочисленные вертикальные и горизонтальные межсегментарные связи и находятся под контролем надсег- ментарных вегетативных структур.
Эфферентный отдел дуги вегетативных рефлексов состоит из преганглио- нарных волокон, являющихся аксонами клеток вегетативных центров (ядер) сегментарного отдела центральной нервной системы (ствола мозга, спинного
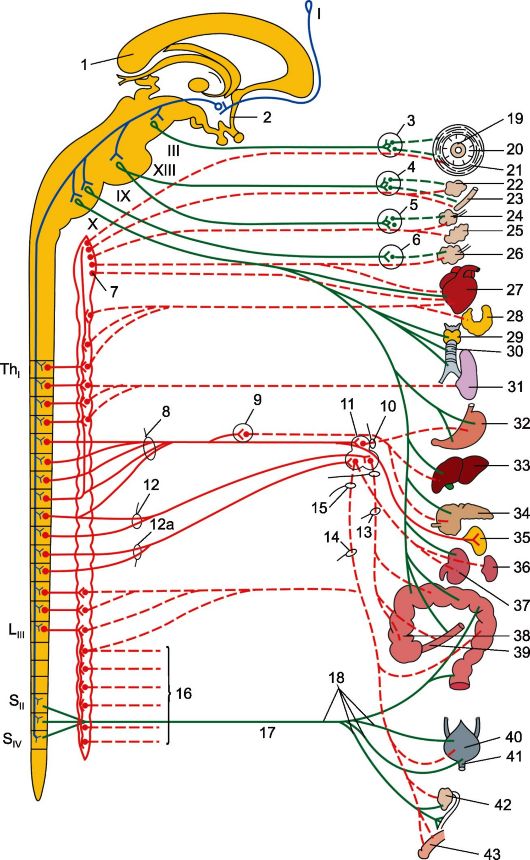
Рис. 13.1. Вегетативная нервная система.
1 - кора большого полушария; 2 - гипоталамус; 3 - ресничный узел; 4 - крылонёб- ный узел; 5 - поднижнечелюстной и подъязычный узлы; 6 - ушной узел; 7 - верхний шейный симпатический узел; 8 - большой внутренностный нерв; 9 - внутренностный узел; 10 - чревное сплетение; 11 - чревные узлы; 12 - малый внутренностный
нерв; 13, 14 - верхнее брыжеечное сплетение; 15 - нижнее брыжеечное сплетение; 16 - аортальное сплетение; 17 - тазовый нерв; 18 - подчревное сплетение; 19 - ресничная мышца, 20 - сфинктер зрачка; 21 - дилататор зрачка; 22 - слезная железа; 23 - железы слизистой оболочки полости носа; 24 - поднижнечелюстная железа; 25 - подъязычная железа; 26 - околоушная железа; 27 - сердце; 28 - щитовидная железа; 29 - гортань; 30 - мышцы трахеи и бронхов; 31 - легкое; 32 - желудок; 33 - печень; 34 - поджелудочная железа; 35 - надпочечник; 36 - селезенка; 37 - почка; 38 - толстая кишка; 39 - тонкая кишка; 40 - детрузор мочевого пузыря; 41 - сфинктер мочевого пузыря; 42 - половые железы; 43 - половые органы.
мозга), которые выходят из мозга в составе передних спинномозговых кореш- ков и достигают определенных периферических вегетативных ганглиев. Здесь вегетативные импульсы переключаются на нейроны, тела которых находятся в ганглиях и далее по постганглиональным волокнам, являющимся аксонами этих нейронов, следуют к иннервируемым органам и тканям.
13.3.2. Афферентные структуры вегетативной нервной системы
Морфологический субстрат афферентной части периферического отдела вегетативной нервной системы не имеет каких-либо принципиальных отличий от афферентной части периферического отдела анимальной нервной системы. Тела первых чувствительных вегетативных нейронов находятся в тех же спинномозговых узлах или являющихся их аналогами узлах черепных нервов, которые содержат и первые нейроны анимальных чувствительных путей. Следовательно, эти узлы являются анимально-вегетативными (соматовегетативными) образованиями, что можно рассматривать как один из фактов, указывающих на нечеткую очерченность границ между анимальными и вегетативными структурами нервной системы.
Тела вторых и последующих чувствительных вегетативных нейронов находятся в спинном мозге или в стволе мозга, их отростки имеют контакты со многими структурами ЦНС, в частности с ядрами промежуточного мозга, прежде всего таламуса и гипоталамуса, а также с другими отделами головного мозга, входящими в лимбико-ретикулярный комплекс. В афферентном звене вегетативной нервной системы можно отметить обилие рецепторов (интерорецепторов, висцерорецепторов), расположенных практически во всех органах и тканях.
13.3.3. Эфферентные структуры вегетативной нервной системы
Если строение афферентной части вегетативного и анимального отделов нервной системы может иметь большое сходство, то эфферентное звено вегетативной нервной системы характеризуют весьма существенные морфологические особенности, при этом они не идентичны в парасимпатическом и симпатическом ее отделах.
13.3.3.1. Строение эфферентного звена парасимпатического отдела вегетативной нервной системы
Центральный отдел парасимпатической нервной системы подразделяется на три части: мезэнцефальную, бульбарную и крестцовую.
Мезэнцефальную часть составляют парные парасимпатические ядра Якубови- ча-Вестфаля-Эдингера, относящиеся к системе глазодвигательных нервов. Периферическая часть мезэнцефального отдела периферической нервной системы состоит из аксонов этого ядра, составляющих парасимпатическую порцию глазодвигательного нерва, который через верхнюю глазничную щель проникает в полость глазницы, при этом включенные в него преганглионарные парасимпа- тические волокна достигают расположенного в клетчатке глазницы ресничного узла (ganglion ciliare), в котором происходит переключение нервных импульсов с нейрона на нейрон. Выходящие из него постганглиональные парасимпатичес- кие волокна участвуют в формировании коротких ресничных нервов (nn. ciliares breves) и заканчиваются в иннервируемых ими гладких мышцах: в мышце, сужи- вающей зрачок (m. sphincter pupille), и в ресничной мышце (m. ciliaris), сокраще- ние которой обеспечивает аккомодацию хрусталика.
К бульбарной части парасимпатической нервной системы относятся три пары парасимпатических ядер - верхнее слюноотделительное, нижнее слюноотделительное и дорсальное. Аксоны клеток этих ядер составляют парасимпатические порции соответственно промежуточного нерва Врисберга (идущего часть пути в составе лицевого нерва), языкоглоточного и блуждающего нервов. Эти парасимпатические структуры указанных черепных нервов состоят из преганг- лионарных волокон, которые заканчиваются в вегетативных узлах. В системе промежуточного и языкоглоточного нервов это крылонёбный (g. pterigopalatum), ушной (g. oticum), подъязычный и поднижнечелюстной узлы (g. sublingualis и g. submandibularis). Отходящие от этих парасимпатических узлов постганглионарные нервные волокна достигают иннервируемых ими слезной железы, слюнных желез и слизистых желез полости носа и рта.
Аксоны дорсального парасимпатического ядра блуждающего нерва выходят из продолговатого мозга в его составе, покидая, таким образом, полость черепа через яремное отверстие. После этого они заканчиваются в многочисленных вегетативных узлах системы блуждающего нерва. Уже на уровне яремного отверстия, где расположены два узла этого нерва (верхний и нижний), часть преганглионарных волокон заканчивается в них. В дальнейшем от верхнего узла отходят постганглионарные волокна, формирующие менингеальные ветви, участвующие в иннервации твердой мозговой оболочки, и ушную ветвь; от нижнего узла блуждающего нерва отходит глоточная ветвь. В дальнейшем от ствола блуждающего нерва отделяются и другие преганглионарные волокна, образующие сердечный депрессивный нерв и частично возвратный нерв гортани; в грудной полости от блуждающего нерва отходят трахеальные, бронхиальные и пищеводные ветви, в брюшной полости - передние и задние желудочные и чревные. Преганглионарные волокна, иннервирующие внутренние органы, заканчиваются в парасимпатических околоорганных и внутриорганных (интрамуральных) узлах,
расположенных в стенках внутренних органов или в непосредственной близости от них. Постганглионарные волокна, отходящие от этих узлов, обеспечивают парасимпатическую иннервацию органов грудной и брюшной полости. Возбуждающее парасимпатическое влияние на эти органы сказывается замед-
лением сердечного ритма, сужением просвета бронхов, усилением перисталь- тики пищевода, желудка и кишечника, повышением секреции желудочного и дуоденального сока и т.д.
Крестцовую часть парасимпатической нервной системы составляют скопления парасимпатических клеток в сером веществе сегментов SII-SIV спинного мозга. Аксоны этих клеток выходят из спинного мозга в составе передних корешков, затем проходят по передним ветвям крестцовых спинномозговых нервов и отделяются от них в виде половых нервов (nn. pudendi), которые принимают участие в формировании нижнего подчревного сплетения и заканчиваются во внутриорганных парасимпатических узлах малого таза. Органы, в которых расположены эти узлы, иннервируются отходящими от них постганглионарными волокнами.
13.3.3.2. Строение эфферентного звена симпатического отдела вегетативной нервной системы
Центральный отдел симпатической вегетативной нервной системы представлен клетками боковых рогов спинного мозга на уровне от VIII шейного до III-IV поясничного его сегментов. Эти вегетативные клетки в совокупности образуют спинномозговой симпатический центр, или columna intermedia (autonomica).
Составляющие спинномозговой симпатический центр клетки Якобсона (мелкие, мультиполярные) связаны с высшими вегетативными центрами, вхо- дящими в систему лимбико-ретикулярного комплекса, которые, в свою очередь, имеют связи с корой больших полушарий и находятся под влиянием исходящей из коры импульсации. Аксоны симпатических клеток Якобсона выходят из спинного мозга в составе передних спинномозговых корешков. В дальнейшем, пройдя через межпозвонковое отверстие в составе спинномозговых нервов, они попадают в их белые соединительные ветви (rami communicantes albi). Каждая белая соединительная ветвь вступает в один из околопозвоночных (паравертебральных) узлов, входящих в состав пограничного симпатического ствола. Здесь часть волокон белой соединительной ветви заканчивается и образует синаптические контакты с симпатическими клетками этих узлов, другая часть волокон проходит через околопозвоночный узел транзитом и достигает клеток других узлов пограничного симпатического ствола или предпозвоночных (превертебральных) симпатических узлов.
Узлы симпатического ствола (околопозвоночные узлы) располагаются цепочкой с обеих сторон позвоночника, между ними проходят межузловые соединительные ветви (rami communicantes interganglionares), и таким образом формируются пограничные симпатические стволы (trunci sympathici dexter et sinister), состоящие из цепи по 17-22 симпатических узла, между которыми имеются и поперечные связи (tracti transversalis). Пограничные симпатические стволы простираются от основания черепа до копчика и имеют 4 отдела: шейный, грудной, поясничный и крестцовый.
Часть лишенных миелиновой оболочки аксонов клеток, расположенных в узлах пограничного симпатического ствола, образует серые соединительные ветви (rami communicantes grisei) и затем вступает в структуры периферической нервной системы: в состав передней ветви спинномозгового нерва, нервного сплетения и периферических нервов подходит к различным тканям, обеспечивая их симпатическую иннервацию. Эта часть осуществляет, в частности,
симпатическую иннервацию пиломоторных мышц, а также потовых и сальных желез. Другая часть постганглионарньх волокон симпатического ствола образует сплетения, распространяющиеся вдоль кровеносных сосудов. Третья часть постганглионарных волокон вместе с преганглионарными волокнами, прошедшими мимо ганглиев симпатического ствола, образует симпатические нервы, направляющиеся главным образом к внутренним органам. По пути следования входящие в их состав преганглионарные волокна заканчиваются в превертебральных симпатических узлах, от которых также отходят постганлионарные волокна, участвующие в иннервации органов и тканей. Шейный отдел симпатического ствола:
1) Шейные симпатические узлы - верхний, средний и нижний. Верхний шейный узел (gangl. cervicale superius) располагается вблизи от затылочной кости на уровне трех первых шейных позвонков вдоль дорсомедиальной поверхности внутренней сонной артерии. Средний шейный узел (gangl. cervicale medium) непостоянный, находится на уровне IV-VI шейных позвонков, впереди подключичной артерии, медиальнее I ребра. Нижний шейный узел (gangl. cervicale inferior) у 75-80% людей сливается с первым (реже - и со вторым) грудным узлом, при этом образуется крупный шейно-грудной узел (gangl. cervicothoracicum), или так называемый звездчатый узел (gangl. stellatum).
На шейном уровне спинного мозга нет боковых рогов и вегетативных клеток, в связи с этим преганглионарные волокна, идущие к шейным ганглиям, представляют собой аксоны симпатических клеток, тела которых располагаются в боковых рогах четырех или пяти верхних грудных сегментов, они входят в шейно-грудной (звездчатый) узел. Часть из этих аксонов заканчивается в этом узле, и идущие по ним нервные импульсы переключаются здесь на следующий нейрон. Другая часть проходит узел симпатического ствола транзитом и идущие по ним импульсы переключаются на следующий симпатический нейрон в расположенных выше среднем или верхнем шейном симпатическом узле.
Отходящие от шейных узлов симпатического ствола постганглионарные волокна отдают ветви, обеспечивающие симпатическую иннервацию органов и тканей шеи и головы. Постганглионарные волокна, отходящие от верхнего шейного узла, формируют сплетения сонных артерий, контролирующие тонус сосудистой стенки этих артерий и их ветвей, а также обеспечивают симпатическую иннервацию потовых желез, гладкой мышцы, расширяющей зрачок (m. dilatator pupillae), глубокой пластины мышцы, поднимающей верхнее веко (lamina profunda m. levator palpebrae superioris), и глазничной мышцы (m. orbitalis). От сплетения сонных артерий отходят и веточки, участвующие в иннервации слезной и слюнных желез, волосяных фолликулов, щитовидной артерии, а также иннервирующие гортань, глотку, участвующие в формировании верхнего сердечного нерва, составляющего часть сердечного сплетения.
Из аксонов нейронов, расположенных в среднем шейном симпатическом узле, формируется средний сердечный нерв, участвующий в формировании сердечного сплетения.
Постганглионарные волокна, отходящие от нижнего шейного симпатического узла или образующегося в связи с его слиянием с верхним грудным узлом шейногрудного, или звездчатого, узла, формируют симпатическое сплетение позвоночной артерии, известное также как позвоночный нерв. Это сплетение окружает позвоночную артерию, вместе с ней проходит через костный канал, образованный отверстиями в поперечных отростках CVI-CII позвонков и через большое затылочное отверстие входит в полость черепа.
2) Грудная часть паравертебрального симпатического ствола состоит из 9-12 узлов. К каждому из них подходит белая соединительная ветвь. Серые соединительные ветви идут ко всем межреберным нервам. Висцеральные ветви от первых четырех узлов направляются к сердцу, легким, плевре, где вместе с ветвями блуждающего нерва образуют соответствующие сплетения. Ветви от 6-9 узлов формируют большой чревный нерв, который проходит в брюшную полость и вступает в чревный узел, являющийся частью комплекса чревного (солнечного) сплетения (plexus coeliacus). Ветви последних 2-3 узлов симпатического ствола образуют малый чревный нерв, часть ветвей которого разветвляется в надпочечном и почечном сплетениях.
3) Поясничная часть паравертебрального симпатического ствола состоит из 2-7 узлов. Белые соединительные ветви подходят лишь к первым 2-3 узлам. Серые соединительные ветви отходят от всех поясничных симпатических узлов к спинномозговым нервам, а висцеральные стволики формируют брюшное аортальное сплетение.
4) Крестцовая часть паравертебрального симпатического ствола состоит из четырех пар крестцовых и одной пары копчиковых ганглиев. Все эти ганглии соединены с крестцовыми спинномозговыми нервами, отдают ветви к органам и сосудисто-нервным сплетениям малого таза.
Превертебральные симпатические узлы отличаются непостоянством формы и величины. Их скопления и сопряженные с ними вегетативные волокна формируют сплетения. Топографически выделяют предпозвоночные сплетения шеи, грудной, брюшной и тазовой полостей. В грудной полости наиболее крупными являются сердечное, а в брюшной - чревное (солнечное), аортальное, брыжеечное, подчревное сплетения.
Из периферических нервов наиболее богаты симпатическими волокнами срединный и седалищный нервы, а также большеберцовый нерв. Поражение их, обычно травматическое, чаще, чем поражение других периферических нервов, вызывает возникновение каузалгии. Боли при каузалгии жгучие, крайне мучительные, трудно локализуемые, имеющие тенденцию распространяться далеко за пределы зоны, иннервируемой пораженным нервом, в которой, кстати, обычно отмечается выраженная гиперпатия. Для больных с каузалгией характерно некоторое облегчение состояния и уменьшение болевых ощущений при увлажнении зоны иннервации (симптом мокрой тряпки).
Симпатическая иннервация тканей туловища и конечностей, а также внутренних органов имеет сегментарный характер, при этом зоны сегментов не соответствуют метамерам, характерным для соматической спинальной ин- нервации. Симпатические сегменты (клетки боковых рогов спинного мозга, составляющие спинномозговой симпатический центр) от CVIII до ThIII обеспечивают симпатическую иннервацию тканей головы и шеи, сегменты ThIV- ThVII - тканей плечевого пояса и руки, сегменты ThVIII ThIX - туловища; наиболее низко расположенные сегменты, в составе которых имеются боковые рога, ThX-ThIII, обеспечивают симпатическую иннервацию органов тазового пояса и ног.
Симпатическая иннервация внутренних органов обеспечивается за счет вегетативных волокон, связанных с определенными сегментами спинного мозга. Возникающие при поражении внутренних органов боли могут иррадиировать в зоны соответствующих этим сегментам дерматомов (зоны Захарьина-Геда). Такие отраженные боли, или гиперестезия, возникают по типу висцеросенсорного рефлекса (рис. 13.2).
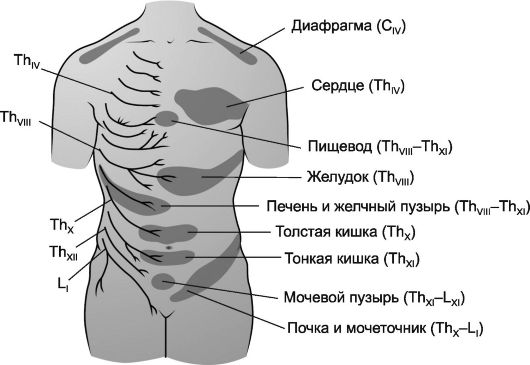
Рис. 13.2. Зоны отраженной боли (зоны Захарьина-Геда) на туловище при заболеваниях внутренних органов - висцеросенсорный рефлекс.
Вегетативные клетки имеют небольшой размер, их волокна безмякотные или с очень тонкой миелиновой оболочкой, относятся к группе В и С. В связи с этим скорость прохождения нервных импульсов в вегетативных волокнах относительно небольшая.
13.3.4. Метасимпатический отдел вегетативной нервной системы
Кроме парасимпатического и симпатического отделов, физиологи выделяют метасимпатический отдел вегетативной нервной системы. Под этим термином подразумевается комплекс микроганглионарных образований, расположенных в стенках внутренних органов, обладающих моторной активностью (сердце, кишечник, мочеточники и др.) и обеспечивающих их автономию. Функция нервных узлов заключается в передаче центральных (симпатических, парасимпатических) влияний к тканям, и, кроме того, они обеспечивают интеграцию информации, поступающей по местным рефлекторным дугам. Метасимпати- ческие структуры представляют собой самостоятельные образования, способные функционировать при полной децентрализии. Несколько (5-7) из относящихся к ним близлежащих узлов объединяются в единый функциональный модуль, основными единицами которого являются клетки-осцилляторы, обеспечи- вающие автономию системы, интернейроны, мотонейроны, чувствительные клетки. Отдельные функциональные модули составляют сплетение, благодаря которому, например, в кишке организуется перистальтическая волна.
Функции метасимпатического отдела вегетативной нервной системы напрямую не зависят от деятельности симпатической или парасимпатической
нервных систем, но могут видоизменяться под их влиянием. Так, например, активация парасимпатического влияния усиливает перистальтику кишечника, а симпатического - ослабляет ее.
13.3.5. Надсегментарные вегетативные структуры
Строго говоря, раздражение любого отдела головного мозга сопровождается каким-либо вегетативным ответом, но в супратенториально расположенных его структурах нет каких-то компактных территорий, которые можно было бы отнести к специализированным вегетативным образованиям. Однако имеются надсегментарные вегетативные структуры большого и промежуточного мозга, оказывающие наиболее существенное, прежде всего интегративное, влияние на состояние вегетативной иннервации органов и тканей.
К таким структурам относится лимбико-ретикулярный комплекс, прежде всего гипоталамус, в котором принято различать передний - трофотропный и задний - эрготропный отделы. Структуры лимбико-ретикулярного комплекса имеют многочисленные прямые и обратные связи с новой корой (neocortex) больших полушарий мозга, которая контролирует и в какой-то степени корригирует их функциональное состояние.
Гипоталамус и другие отделы лимбико-ретикулярного комплекса оказыва- ют глобальное регулирующее влияние на сегментарные отделы вегетативной нервной системы, создают относительный баланс между деятельностью симпатических и парасимпатических структур, направленный на поддержание в организме состояния гомеостаза. Кроме того, гипоталамический отдел мозга, миндалевидный комплекс, старая и древняя кора медиобазальных отделов больших полушарий, извилина гиппокампа и другие отделы лимбико-ретикулярного комплекса осуществляют интеграцию между вегетативными структурами, эндокринной системой и эмоциональной сферой, влияют на формирование мотиваций, эмоций, обеспечение памяти, поведения.
Патология надсегментарных образований может вести к полисистемным реакциям, при которых вегетативные расстройства являются лишь одной из составляющих сложной клинической картины.
13.3.6. Медиаторы и их влияние на состояние вегетативных структур
Проведение импульсов через синаптические аппараты как в центральной, так и в периферической нервных системах осуществляется благодаря медиаторам, или нейротрансмиттерам. В центральной нервной системе медиаторы многочисленны и характер их изучен далеко не во всех синаптических связях. Лучше изучены медиаторы периферических нервных структур, в частности относящихся к вегетативной нервной системе. Следует также обратить внимание на то, что в афферентной (центростремительной, чувствительной) час- ти периферической нервной системы, которую составляют главным образом псевдоуниполярные клетки со своими отростками, синаптические аппараты отсутствуют. В эфферентных структурах (табл. 13.1) анимального (соматичес- кого) отдела периферической нервной системы существуют только нервно-
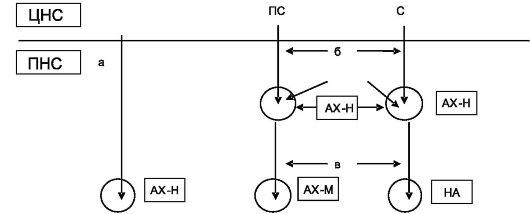
Схема 13.1. Симпатические аппараты и медиаторы периферической нервной системы ЦНС - центральная нервная система; ПНС - периферическая нервная система; ПС - парасимпатические структуры ЦНС; С - симпатические структуры ЦНС; а - соматическое двигательное волокно; б - преганглионарные вегетативные волокна; в - постганглионарные вегетативные волокна; КРУГ - синаптические аппараты; медиаторы: АХ - ацетилхолин; НА - норадреналин.
мышечные синапсы. Медиатором, обеспечивающим проведение нервных импульсов через эти синапсы, является ацетилхолин-Н (АХ-Н), синтезируемый в периферических мотонейронах, расположенных в структурах ЦНС, и поступающий оттуда по их аксонам с аксотоком в синаптические пузырьки, находящиеся вблизи от пресинаптической мембраны.
Эфферентную периферическую часть вегетативной нервной системы составляют выходящие из ЦНС (ствола головного мозга, спинного мозга) преганглионарные волокна, а также вегетативные ганглии, в которых происходит переключение через синаптические аппараты импульсов с преганглионарных волокон на расположенные в ганглиях клетки. В дальнейшем импульсы по отходящим от этих клеток аксонам (постганглионарным волокнам) достигают синапса, обеспечивающего переключение импульса с этих волокон на иннервируемую ткань.
Таким образом, все вегетативные импульсы на пути от ЦНС до иннервируемой ткани проходят через синаптические аппараты дважды. Первый из синапсов находится в парасимпатической или симпатической ганглии, переключение импульса здесь в том и в другом случае обеспечивает тот же медиатор, что и в анимальном нервно-мышечном синапсе, - ацетилхолин-Н (АХ-Н). Вторые, парасимпатический и симпатический, синапсы, в которых импульсы переключаются с постганглионарного волокна на иннервируемую структуру, не идентичны по выделяемому медиатору. Для парасимпатического отдела - это ацетилхолин-М (АХ-М), для симпатического - главным образом норадреналин (НА). Это имеет существенное значение, так как с помощью определенных лекарственных средств можно влиять на проводимость нервных импульсов в зоне перехода их через синапс. К таким лекарственным препаратам относятся Н- и М-холиномиметики и Н- и М-холинолитики, а также адреномиметики и адреноблокаторы. Назначая данные лекарственные средства, необходимо учитывать их действие на синаптические структуры и прогнозировать, какую реакцию на введение каждого из них следует ожидать.
Действие фармпрепарата может сказываться на функции синапсов, относящихся к разным отделам нервной системы, если нейротрансмиссию в них обеспечивает идентичный или близкий по химическому строению медиатор. Так, введение ганглиоблокаторов, являющихся Н-холинолитиками, оказывает блокирующее влияние на проведение импульсов с преганглионарного волокна на находящуюся в ганглии клетку как в симпатических, так и в парасимпатических ганглиях, может также подавлять проведение нервных импульсов через нервно-мышечные синапсы анимального отдела периферической нервной системы.
В некоторых случаях влиять на проведение импульсов через синапс можно и средствами, по-разному влияющими на проводимость синаптических аппаратов. Так, холиномиметический эффект оказывает не только применение холиномиметиков, в частности ацетилхолина, который, кстати, быстро распадается и потому редко применяется в клинической практике, но и антихо- линэстеразных лекарственных средств из группы ингибиторов холинэстеразы (прозерин, галантамин, калемин и т.п.), что ведет к защите от быстрого разру- шения попадающих в синаптическую щель молекул АХ.
Структурам вегетативной нервной системы свойственна способность активно реагировать на многие химические и гуморальные раздражители. Это об- стоятельство определяет лабильность вегетативных функций при малейших изменениях химического состава тканей, в частности крови, под влиянием изменения эндогенных и экзогенных воздействий. Оно же позволяет активно влиять на вегетативный баланс путем введения в организм определенных фар- макологических средств, улучшающих или блокирующих проведение вегетативных импульсов через синаптические аппараты.
Вегетативная нервная система влияет на жизнеспособность организма (табл. 13.1). Она регулирует состояние сердечно-сосудистой, дыхательной, пи- щеварительной, мочеполовой и эндокринной систем, жидких сред, гладкой мускулатуры. В то же время вегетативная система выполняет адаптационно- трофическую функцию, регулирует энергетические ресурсы организма, обеспечивая таким образом все виды физической и психической деятельности, подго- тавливая органы и ткани, в том числе нервную ткань и поперечнополосатую мускулатуру, к оптимальному уровню их активности и успешному выполнению свойственных им функций.
Таблица 13.1. Функции симпатического и парасимпатического отделов вегетативной нервной системы
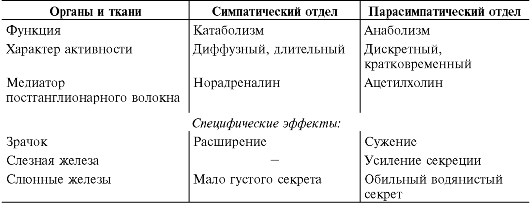
Окончание табл. 13-1
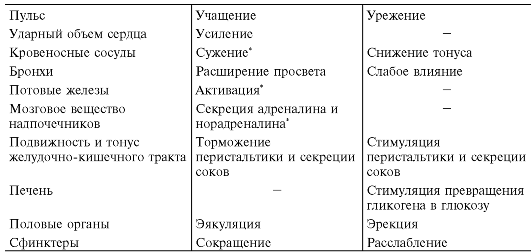
* Для большинства потовых желез, некоторых сосудов и скелетных мышц симпатическим медиатором является ацетилхолин. Мозговое вещество надпочечников иннервируется холинергическими симпатическими нейронами.
В период опасности, напряженной работы вегетативная нервная система призвана удовлетворять возрастающие энергетические потребности организма и осуществляет это путем повышения активности обменных процессов, усиления легочной вентиляции, перевода на более напряженный режим сердечнососудистой и дыхательной систем, изменение гормонального баланса и т.д.
13.3.7. Исследование вегетативных функций
Сведения о вегетативных нарушениях и их локализации могут содействовать решению вопроса о характере и расположении патологического процесса. Иногда особую значимость имеет выявление признаков вегетативного дисбаланса.
Изменение функций гипоталамуса и других надсегментарных структур вегетативной нервной системы ведет к генерализованным вегетативным расстройствам. Поражение вегетативных ядер в стволе мозга и спинном мозге, а также периферических отделов вегетативной нервной системы обычно сопровождается развитием сегментарных вегетативных расстройств в более или менее ограниченной части тела.
При исследовании вегетативной нервной системы следует обратить внимание на телосложение больного, состояние его кожи (гиперемия, бледность, потливость, сальность, гиперкератоз и пр.), ее придатков (облысение, поседение; хрупкость, тусклость, утолщение, деформация ногтей); выраженность подкожного жирового слоя, его распределение; состояние зрачков (деформация, диаметр); слезоотделение; слюноотделение; функцию тазовых органов (императивные позывы на мочеиспускание, недержание мочи, задержки мочи, поносы, запоры). Надо составить представление о характере больного, преобладающем его настроении, самочувствии, работоспособности, степени эмоциональности, способности адаптироваться к изменениям внешней темпера-
туры. Необходимо получить информацию о состоянии соматического статуса больного (частота, лабильность, ритм пульса, артериальное давление, головная боль, ее характер, приступы мигрени в анамнезе, функции дыхательной, пи- щеварительной и других систем), состоянии эндокринной системы, результатах термометрии, лабораторных показателях. Обращают внимание на наличие у больного аллергических проявлений (крапивница, бронхиальная астма, ангионевротические отеки, эссенциальный зуд и пр.), ангиотрофоневрозов, акроангиопатий, симпаталгий, проявлений «морской» болезни при пользовании транспортом, «медвежьей» болезни.
При неврологическом осмотре могут быть выявлены анизокория, расширение или сужение зрачков, не соответствующих имеющейся освещенности, нарушение реакции зрачков на свет, конвергенцию, аккомодацию, тотальная сухожильная гиперрефлексия с возможным расширением рефлексогенных зон, общей двигательной реакцией, изменение местного и рефлекторного дермографизма.
Местный дермографизм вызывается легким штриховым раздражением кожи тупым предметом, например рукояткой неврологического молоточка, закругленным концом стеклянной палочки. В норме при легком раздражении кожи через несколько секунд на ней появляется белая полоска. Если кожное раздражение более интенсивно, возникающая полоска на коже красная. В первом случае - местный дермографизм белый, во втором - местный дермографизм красный.
Если как слабое, так и более интенсивное раздражение кожи вызывает появление местного белого дермографизма, можно говорить о повышенном тонусе сосудов кожи. Если же даже при минимальных по силе штриховых раздражениях кожи возникает местный красный дермографизм, а белый получить не удается, то это свидетельствует о пониженном тонусе сосудов кожи, прежде всего прекапилляров и капилляров. При выраженном снижении их тонуса штриховое раздражение кожи не только ведет к появлению местного красного дермографизма, но и к проникновению плазмы через стенки сосудов. Тогда возможно возникновение отечного, или уртикарного, или возвышенного дермографизма (dermographismus elevatus).
Рефлекторный, или болевой, дермографизм вызывается штриховым раздражением кожи острием иголки или булавки. Рефлекторная дуга его замыкается в сегментарном аппарате спинного мозга. В ответ на болевое раздражение в норме на коже возникает красная полоска шириной в 1-2 мм с узкими белыми краями, которая держится несколько минут.
Если спинной мозг поврежден, то на участках кожи, вегетативная иннервация которых должна обеспечиваться пораженными сегментами, и в расположенных ниже частях тела рефлекторный дермографизм отсутствует. Это обстоятельство может способствовать уточнению верхней границы патологического очага в спинном мозге. Рефлекторный дермографизм исчезает в зонах, иннервируемых пораженными структурами периферической нервной системы.
Определенное топико-диагностическое значение может иметь и состояние пиломоторного (мышечно-волоскового) рефлекса. Его можно вызвать болевым или холодовым раздражением кожи в области трапециевидной мышцы (верхний пиломоторный рефлекс) или в ягодичной области (нижний пиломо- торный рефлекс). Ответной реакцией при этом является возникновение на соответствующей половине тела распространенной пиломоторной реакции в виде «гусиной кожи». Быстрота и интенсивность реакции указывает на степень
возбудимости симпатического отдела вегетативной нервной системы. Дуга пиломоторного рефлекса замыкается в боковых рогах спинного мозга. При поперечных поражениях спинного мозга, вызывая верхний пиломоторный рефлекс, можно отметить, что пиломоторная реакция наблюдается не ниже уровня дерматома, соответствующего верхнему полюсу патологического очага. При вызывании нижнего пиломоторного рефлекса «гусиная кожа» возникает в нижней части тела, распространяясь вверх до нижнего полюса патологического очага в спинном мозге.
Следует иметь в виду, что результаты исследования рефлекторного дермографизма и пиломоторных рефлексов дают лишь ориентировочные сведения о топике патологического очага в спинном мозге. Уточнение локализации патологического очага может обусловить необходимость более полного неврологического осмотра и нередко дополнительных методов обследования (миелография, МРТ-сканирование).
Определенное значение для топической диагностики может иметь выявление местных нарушений потоотделения. Для этого иногда применяется йодно-крахмальная проба Минора . Тело больного смазывается раствором йода в касторовом масле и спирте (iodi puri 16,0; olei risini 100,0; spiriti aetylici 900,0). После того как кожа подсохнет, ее припудривают крахмалом. Затем применяют один из способов, обычно вызывающих усиление потоотделения, при этом вспотевшие участки кожи темнеют, так как выступивший пот содействует реакции крахмала с йодом. Для провокации потоотделения пользуются тремя индикаторами, воздействующими на разные отделы вегетативной нервной системы - различные звенья эфферентной части дуги потоотделительного рефлекса. Прием 1 г аспирина вызывает повышенное потоотделение, вызывая возбуждение центра потоотделения на уровне гипоталамуса. Согревание больного в световой ванне влияет главным образом на спинномозговые центры потоотделения. Подкожное введение 1 мл 1% раствора пилокарпина провоцирует потоотделение, возбуждая периферические окончания постганглионарных вегетативных волокон, расположенных в самих потовых железах.
Для выявления степени возбудимости нервно-мышечных синаптических аппаратов в сердце можно провести ортостатическую и клиностатическую пробы. Ортостатический рефлекс возникает при переходе обследуемого из горизонтального положения в вертикальное. До проведении пробы и в течение первой минуты после перехода больного в вертикальное положения измеряется его пульс. В норме - учащение пульса на 10-12 ударов в мин. Клиностатическая проба проверяется при переходе больного из вертикального положения в горизонтальное. Пульс измеряется также до выполнения пробы и в течение первой минуты после принятия больным горизонтального положения. В норме отмечается замедление пульса на 10-12 ударов в мин.
Проба Льюиса (триада) - комплекс последовательно развивающихся сосудистых реакций на внутрикожное введение двух капель подкисленного 0,01% раствора гистамина. В месте укола в норме происходят следующие реакции: 1) возникает красная точка (ограниченная эритема), обусловленная местным расширением капилляров; 2) вскоре она оказывается на вершине белой папулы (волдыря), возникающей вследствие увеличения проницаемости сосудов кожи; 3) вокруг папулы развивается гиперемия кожи в связи с расширением артериол. Распространение эритемы за пределы папулы может отсутствовать в случае денервации кожи, при этом в течение первых нескольких дней после перерыва периферического нерва он может быть сохранным и исчезает с по-
явлением в нерве дегенеративных изменений. Окружающее папулу наружное красное кольцо обычно отсутствует при синдроме Райли-Дея (семейная дизавтономия). Проба может быть применена и для определения проницаемости сосудов, выявления вегетативных асимметрий. Описал ее английский кардиолог Th. Lewis (1871-1945).
При клиническом обследовании больных могут быть применены и другие методы исследования вегетативной нервной системы, в том числе исследование кожной температуры, чувствительности кожи к ультрафиолетовому облучению, гидрофильности кожи, кожные фармакологические пробы с такими препаратами, как адреналин, ацетилхолин и некоторыми другими вегетотропными средствами, изучение электрокожного сопротивления, глазосердечный рефлекс Даньини-Ашнера, капилляроскопия, плетизмография, рефлексы вегета- тивных сплетений (шейный, эпигастральный) и др. Методика их проведения изложена в специальных и справочных руководствах.
Изучение состояния вегетативных функций может дать важную информацию о наличии у больного функционального или органического поражения нервной системы, нередко способствуя решению вопроса о топическом и нозологическом диагнозе.
Выявление вегетативных асимметрий, выходящих за пределы физиологических колебаний, может рассматриваться как признак диэнцефальной патологии. Локальные изменения вегетативной иннервации могут способствовать топической диагностике некоторых заболеваний спинного мозга и периферической нервной системы. Болезненность и вегетативные расстройства в зонах Захарьина-Геда, носящие отраженный характер, могут указывать на патоло- гию того или иного внутреннего органа. Признаки повышенной возбудимости вегетативной нервной системы, вегетативной лабильности могут быть объективным подтверждением наличия у больного невроза или неврозоподобного состояния. Их выявление подчас играет весьма важную роль при проведении профессионального отбора людей для работы по некоторым специальностям.
Результаты изучения состояния вегетативной нервной системы в какой-то степени позволяют судить о психическом статусе человека, прежде всего его эмоциональной сферы. Такие исследования лежат в основе дисциплины, объединяющей физиологию и психологию и известной как психофизиология, подтверждающей взаимосвязь между психической деятельностью и состоянием вегетативной нервной системы.
13.3.8. Некоторые клинические феномены, зависящие от состояния центральных и периферических структур вегетативной нервной системы
От состояния вегетативной нервной системы зависят функции всех органов и тканей и, следовательно, сердечно-сосудистой, дыхательной, мочеполовой систем, пищеварительного тракта, органов чувств. Она оказывает влияние и на функциональные возможности опорно-двигательного аппарата, регулирует метаболические процессы, обеспечивая относительное постоянство внутренней среды организма, его жизнеспособность. Раздражение или угнетение функций отдельных вегетативных структур ведет к вегетативному
дисбалансу, что в той или иной степени влияет на состояние человека, его здоровье, качество его жизни. В связи с этим стоит лишь подчеркнуть исключительное многообразие клинических проявлений, обусловленных вегетативной дисфункцией, и обратить внимание на то, что возникающими в связи с этим проблемами озабочены представители практически всех клинических дисциплин.
Далее мы имеем возможность остановиться лишь на некоторых клинических феноменах, зависящих от состояния вегетативной нервной системы, с которыми в повседневной работе приходится иметь дело врачу-неврологу (см. также главы 22, 30, 31).
13.3.9. Острая вегетативная дисфункция, проявляющаяся угасанием вегетативных реакций
Вегетативный дисбаланс, как правило, сопровождается клиническими проявлениями, характер которых зависит от его особенностей. Острая вегетативная дисфункция (пандизавтономия) за счет угнетения вегетативных функций обусловлена острым нарушением вегетативной регуляции, проявившимся тотально, во всех тканях и органах. В период этой мультисистемной недостаточности, которая обычно связывается с иммунными нарушениями в периферических миелиновых волокнах, возникают неподвижность и арефлексия зрачков, сухость слизистых оболочек, ортостатическая гипотензия, происходит замедление частоты сердечных сокращений, нарушается перистальтика кишечника, возникает гипотония мочевого пузыря. Сохранными остаются психичес- кие функции, состояние мышц, в том числе и глазодвигательных, координация движений, чувствительность. Возможно изменение сахарной кривой по диабетическому типу, в ЦСЖ - увеличение содержания белка. Острая вегетативная дисфункция может через некоторое время постепенно регрессировать, и в большинстве случаев наступает выздоровление.
13.3.10. Хроническая вегетативная дисфункция
Хроническая вегетативная дисфункция возникает при длительном соблюдении постельного режима или в условиях невесомости. Проявляется в основном головокружением, координаторными расстройствами, которые при возвращении к нормальному режиму постепенно, в течение нескольких суток, уменьшаются. Нарушение вегетативных функций может быть спровоцировано передозировкой некоторых лекарственных средств. Так, передозировка гипо- тензивных препаратов ведет к ортостатической гипотензии; при употреблении препаратов, влияющих на терморегуляцию, возникает изменение вазомоторных реакций и потоотделения.
Некоторые заболевания могут обусловить вторичные вегетативные нарушения. Так, при сахарном диабете и амилоидозе характерны проявления невропатии, при которой возможны тяжелая ортостатическая гипотензия, изменения зрачковых реакций, импотенция, нарушения функции мочевого пузыря. При столбняке возникают артериальная гипертензия, тахикардия, гипергидроз.
13.3.11. Расстройства терморегуляции
Терморегуляцию можно представить как кибернетическую самоуправляющуюся систему, при этом терморегуляторный центр, обеспечивающий совокупность физиологических реакций организма, направленных на поддержание относительного постоянства температуры тела, располагается в гипоталамусе и прилежащих зонах промежуточного мозга. К нему стекается информация от терморецепторов, расположенных в различных органах и тканях. Центр терморегуляции, в свою очередь, через нервные связи, гормоны и другие биологически активные вещества регулирует процессы теплопродукции и теплоотдачи в организме. При расстройстве терморегуляции (в эксперименте на животных - при перерезке ствола мозга) температура тела становится чрезмерно зависимой от температуры окружающей среды (пойкилотермия).
На состояние температуры тела влияют обусловленные разными причинами изменения теплопродукции и теплоотдачи. Если температура тела повышается до 39 ?С, больные обычно испытывают недомогание, сонливость, слабость, головную и мышечные боли. При температуре выше 41,1 ?С у детей часто возникают судороги. Если температура повышается до 42,2 ?С и выше, возможно возникновение необратимых изменений в ткани мозга, по-видимому, вследствие денатурации белков. Температура выше 45,6 ?С несовместима с жизнью. При снижении температуры до 32,8 ?С нарушается сознание, при 28,5 ?С начинается мерцание предсердий, а еще большая гипотермия вызывает фибрилляцию желудочков сердца.
При нарушении функции терморегуляторного центра в преоптической области гипоталамуса (сосудистые расстройства, чаще кровоизлияния, энцефалит, опухоли) возникает эндогенная центральная гипертермия. Для нее характерны изменения суточных колебаний температуры тела, прекращение потоотделения, отсутствие реакции при приеме антипиретических препаратов, нарушение терморегуляции, в частности выраженность снижения температуры тела в ответ на его охлаждение.
Кроме гипертермии, обусловленной нарушением функции терморегуляторного центра, повышенная теплопродукция может быть связана и с другими причинами. Она возможна, в частности, при тиреотоксикозе (температура тела может быть выше нормальной на 0,5-1,1 ?С), повышенной активации мозгового вещества надпочечников, менструациях, климаксе и других состояниях, сопровождающихся эндокринным дисбалансом. Гипертермию может обусловить и чрезвычайная физическая нагрузка. Например, при беге на марафонскую дистанцию температура тела иногда повышается до 39-41 ?С. Причиной гипертермии может быть и снижение теплоотдачи. В связи с этим гипертермия возможна при врожденном отсутствии потовых желез, ихтиозе, распространенных ожогах кожи, а также приеме лекарственных средств, уменьшающих потоотделение (М-холинолитики, ингибиторы МАО, фенотиазины, амфетамины, ЛСД, некоторые гормоны, особенно прогестерон, синтетические нуклеотиды).
Чаще других экзогенной причиной гипертермии бывают инфекционные агенты (бактерии и их эндотоксины, вирусы, спирохеты, дрожжевые грибы). Есть мнение, что все экзогенные пирогены воздействуют на терморегуляторные структуры через вещество-посредник - эндогенный пироген (ЭП), идентич- ный интерлейкину-1, который вырабатывается моноцитами и макрофагами.
В гипоталамусе эндогенный пироген стимулирует синтез простагландинов Е, которые изменяют механизмы теплопродукции и теплоотдачи путем усиления синтеза циклического аденозинмонофосфата. Эндогенный пироген, содержащийся в астроцитах головного мозга, может высвобождаться при кровоизлиянии в мозг, черепно-мозговой травме, вызывая повышение температуры тела, при этом могут активироваться нейроны, ответственные за медленный сон. Последнее обстоятельство объясняет вялость и сонливость при гипертермии, которые можно рассматривать как одну из защитных реакций. При инфекционных процессах или острых воспалениях гипертермия играет важную роль в развитии ответных иммунных реакций, которые могут быть защитными, но иногда и ведущими к нарастанию патологических проявлений.
Перманентная неинфекционная гипертермия (психогенная лихорадка , привычная гипертермия) - перманентный субфебрилитет (37-38 ?С) в течение нескольких недель, реже - нескольких месяцев и даже лет. Температура по- вышается монотонно и не имеет циркадного ритма, сопровождается снижением или прекращением потоотделения, отсутствием реакции на антипиретические препараты (амидопирин и т.п.), нарушением адаптации к внешнему охлаждению. Характерны удовлетворительная переносимость гипертермии, сохранение трудоспособности. Перманентная неинфекционная гипертермия чаще проявляется у детей и молодых женщин в периоды эмоционального напряжения и обычно расценивается как один из признаков синдрома вегетативной дистонии. Однако особенно у лиц старшего возраста она может быть и следствием органического поражения гипоталамуса (опухоль, сосудистые нарушения, особенно кровоизлияние, энцефалит). Вариантом психогенной лихорадки можно, по-видимому, признать синдром Хайнса-Бенника (описал Hines-Bannick M.), возникающий как следствие вегетативного дисбаланса, проявляющегося общей слабостью (астенией), перманентной гипертермией, выраженным гипергидрозом, «гусиной» кожей. Может быть спровоцирован психической травмой.
Температурные кризы (пароксизмальная неинфекционная гипертермия) - вне- запные повышения температуры до 39-41 ?С, сопровождающиеся ознобоподобным состоянием, ощущением внутреннего напряжения, гиперемией лица, тахикардией. Повышенная температура сохраняется несколько часов, после чего обычно возникает ее литическое снижение, сопровождающееся общей слабостью, разбитостью, отмечаемыми в течение нескольких часов. Кризы могут возникать на фоне нормальной температуры тела или длительного субфебрилитета (перманентно-пароксизмальная гипертермия). При них нехарактерны изменения крови, в частности ее лейкоцитарной формулы. Температурные кризы являются одним из возможных проявлений вегетативной дистонии и дисфункции терморегуляторного центра, входящего в состав гипоталамических структур.
Злокачественная гипертермия - группа наследственных состояний, характеризующихся резким повышением температуры тела до 39-42 ?С в ответ на введение ингаляционных анестезирующих средств, а также миорелаксантов, особенно дитилина, при этом отмечается недостаточная релаксация мышц, возник- новение фасцикуляций в ответ на введение дитилина. Тонус жевательных мышц нередко нарастает, создаются трудности для интубации, что может служить поводом к увеличению дозы миорелаксанта и(или) анестетика, ведет к развитию тахикардии и в 75% случаев к генерализованной ригидности мышц (ригидная форма реакции). На этом фоне можно отметить высокую активность
креатинфосфокиназы (КФК) и миоглобинурию, развиваются тяжелый респираторный и метаболический ацидоз и гиперкалиемия, возможно возникновение фибрилляции желудочков, снижается АД, появляется мраморный цианоз, возникает угроза летального исхода.
Риск развития злокачественной гипертермии при ингаляционном наркозе особенно высок у больных, страдающих миопатией Дюшенна, миопатией центрального стержня, миотонией Томсена, хондродистрофической миотонией (синдром Шварца-Джампела). Предполагается, что злокачественная гипертермия связана с накоплением кальция в саркоплазме мышечных волокон. Склонность к злокачественной гипертермии наследуется в большинстве слу- чаев по аутосомно-доминантному типу с различной пенетрантностью патоло- гического гена. Существует и злокачественная гипертермия, наследуемая по рецессивному типу (синдром Короля).
При лабораторных исследованиях в случаях злокачественной гипертермии выявляют признаки дыхательного и метаболического ацидоза, гиперкалиемию и гипермагниемию, повышение содержания в крови лактата и пирувата. Среди поздних осложнений злокачественной гипертермии отмечают массивное набухание скелетных мышц, отек легкого, ДВС-синдром, острую почечную недостаточность.
Нейролептическая злокачественная гипертермия наряду с высокой тем- пературой тела проявляется тахикардией, аритмией, нестабильностью АД, потливостью, цианозом, тахипноэ, при этом возникают нарушение водно- электролитного баланса с повышением концентрации калия в плазме, ацидоз, миоглобинемия, миоглобинурия, повышенная активность КФК, АСТ, АЛТ, появляются признаки ДВС-синдрома. Появляются и нарастают мышечные контрактуры, развивается коматозное состояние. Присоединяются пневмония, олигурия. В патогенезе важна роль нарушения терморегуляции и растормаживания дофаминовой системы туберо-инфундибулярной области гипоталамуса. Смерть наступает чаще через 5-8 дней. При вскрытии обнаруживаются острые дистрофические изменения в мозге и паренхиматозных органах. Синдром развивается вследствие длительного лечения нейролептиками, однако он может развиться у больных шизофренией, не принимавших нейролептиков, редко - у больных паркинсонизмом, длительно принимавших препараты L-ДОФА.
Синдром ознобления - почти постоянное ощущение зябкости во всем теле или в отдельных его частях: в голове, спине и пр., обычно сочетается с се- нестопатиями и проявлениями ипохондрического синдрома, иногда фобиями. Больные опасаются похолодания, сквозняков, обычно носят излишне теплую одежду. Температура тела у них нормальная, в отдельных случаях выявляется перманентная гипертермия. Рассматривается как одно из проявлений вегетативной дистонии с преобладанием активности парасимпатического отдела вегетативной нервной системы.
Для лечения больных с неинфекционной гипертермией целесообразно применение бетаили альфа-адреноблокаторов (фентоламин 25 мг 2-3 раза в день, пирроксан 15 мг 3 раза в день), общеукрепляющее лечение. При устойчивой брадикардии, спастической дискинезии назначают препараты белладонны (беллатаминал, беллоид и т.п.). Больному следует отказаться от курения и злоупотребления алкоголем.
13.3.12. Нарушения слезоотделения
Секреторная функция слезных желез обеспечивается главным образом влиянием на них импульсов, поступающих из парасимпатического слезного ядра, находящегося в мосту мозга вблизи ядра лицевого нерва и получающего стимулирующую импульсацию от структур лимбико-ретикулярного комплекса. От парасимпатического слезного ядра импульсы перемещаются по промежуточному нерву и его ветви - большому каменистому нерву - до парасимпа- тического крылонёбного узла. Аксоны клеток, расположенных в этом ганглии, составляют слезный нерв, который и иннервирует секреторные клетки слезной железы. Симпатические импульсы проходят к слезной железе от шейных сим- патических узлов по волокнам каротидного сплетения и вызывают главным образом вазоконстрикцию в слезных железах. В течение суток слезная железа человека вырабатывает приблизительно 1,2 мл слезной жидкости. Слезоотделение происходит главным образом в периоды бодрствования и угнетается во сне.
Нарушение слезоотделения может быть в форме сухости глаз из-за недостаточности продукции слезной жидкости слезными железами. Чрезмерное слезо- течение (эпифора) чаще сопряжено с нарушением оттока слез в полость носа через носослезный канал.
Сухость (ксерофтальмия, алакримия) глаза может быть следствием поражения самих слезных желез или расстройством их парасимпатической иннервации. Нарушение секреции слезной жидкости - один из характерных признаков синдрома сухих слизистых оболочек Шегрена (H.S. Sjogren), врожденной дизавтономии Райли-Дея, острой преходящей тотальной дизавтономии, синдрома Микулича. Односторонняя ксерофтальмия чаще встречается при поражении лицевого нерва проксимальнее места отхождения от него ветви - большого каменистого нерва. Типичную картину ксерофтальмии, нередко осложняющуюся воспалением тканей глазного яблока, иногда приходится наблюдать у больных, оперированных по поводу невриномы VIII черепного нерва, в процессе которой были рассечены волокна деформированного опухолью лицевого нерва.
При прозоплегии в связи с невропатией лицевого нерва, при которой этот нерв поврежден ниже отхождения от него большого каменистого нерва, обычно имеет место слезотечение, возникающее в результате пареза круговой мышцы глаза, нижнего века и нарушением в связи с этим естественного оттока слезной жидкости через носослезный канал. Та же причина лежит в основе старческого слезотечения, сопряженного со снижением тонуса круговой мышцы глаз, а также вазомоторного ринита, конъюнктивита, приводящих к отеку стенки носослезного канала. Пароксизмальное избыточное слезотечение в связи с отеком стенок носослезного канала при болевом приступе возникает при пучковой боли, приступах вегетативной прозопалгии. Рефлекторным может быть слезотечение, запускаемое раздражением зоны иннервации I ветви тройничного нерва при холодовой эпифоре (слезотечение на морозе), дефиците витамина А, выраженном экзофтальме. Усиленное слезотечение во время еды характерно для синдрома «крокодиловых слез», описанного в 1928 г. Ф.А. Богардом. Этот синдром может быть врожденным или возникает в восстановительной стадии невропатии лицевого нерва. При паркинсонизме слезотечение может быть одним из проявлений общей активации холинергических механизмов, а также следствием гипомимии и редких миганий, что ослабляет возможность оттока слезной жидкости через носослезный канал.
Лечение больных с нарушениями слезотечения зависит от вызывающих их причин. При ксерофтальмии необходимы контроль за состоянием глаза и мероприятия, направленные на поддержание его влажности и профилактики инфицирования, закапывание в глаза масляных растворов, альбуцида и т.п. Последнее время стали пользоваться искусственной слезной жидкостью.
13.3.13. Нарушение слюноотделения
Сухость во рту (гипосаливация , ксеростомия) и избыточное слюноотделение (гиперсаливация, сиалорея) могут быть обусловлены различными причинами. Гипо- и гиперсаливация могут иметь постоянный или пароксизмальный характер,
в ночное время продукция слюны меньше, при приеме и даже при виде пищи, ее запахе количество выделяемой слюны увеличивается. Обычно в сутки вырабатывается от 0,5 до 2 л слюны. Под влиянием парасимпатической импульсации слюнные железы вырабатывают обильную жидкую слюну, тогда как активация симпатической иннервации ведет к выработке более густой слюны.
Гиперсаливация обычна при паркинсонизме, бульбарном и псевдобуль- барном синдроме, детском церебральном параличе; при этих патологических состояниях она может быть обусловлена как гиперпродукцией слюны, так и нарушениями акта глотания, последнее обстоятельство обычно ведет к спонтанному истечению слюны изо рта даже в случаях секреции ее в обычном количестве. Гиперсаливация может быть следствием язвенного стоматита, глистной инвазии, токсикоза беременных, в некоторых случаях она признается психогенной.
Причиной стойкой гипосаливации (ксеростомии) является синдром Шегрена (сухой синдром), при котором одновременно имеют место и ксерофтальмия (сухость глаз), сухость конъюнктивы, слизистой оболочки носа, нарушение функции других слизистых оболочек, припухлость в зоне расположения околоушных слюнных желез. Гипосаливация является признаком глоссодинии, стомалгии, тотальной дизавтономии, она может возникать при сахарном диабете, при заболеваниях желудочно-кишечного тракта, голодании, под влиянием некоторых лекарственных средств (нитразепам, препараты лития, холинолитики, антидепрессанты, антигистаминные средства, диуретики и пр.), во время лучевой терапии. Сухость во рту обычно возникает при волнении в связи с преобладанием симпатических реакций, возможна при депрессивном состоянии.
При нарушении слюноотделения желательно уточнение его причины и после этого проведение возможной патогенетической терапии. В качестве симптоматического средства при гиперсаливации могут применяться холинолитики, при ксеростомии - бромгексин (по 1 таб 3-4 раза в день), пилокарпин (капсулы по 5 мг сублингвально 1 раз в день), никотиновая кислота, препараты витамина А. В качестве заместительного лечения применяется искусственная слюна.
13.3.14. Расстройства потоотделения
Потоотделение является одним из факторов, влияющих на терморегуляцию, и находится в определенной зависимости от состояния терморегуляторного центра, входящего в состав гипоталамуса и оказывающего глобальное
влияние на потовые железы, которые по морфологическим особенностям, расположению и химическому составу выделяемого ими пота дифференцируют на мерокринные и апокриновые, при этом роль последних в возникновении гипергидроза незначительна.
Таким образом, систему терморегуляции составляют в основном определенные структуры гипоталамуса (преоптическая зона гипоталамической области) (Guyton A., 1981), их связи с кожными покровными и расположенными в коже мерокринными потовыми железами. Гипоталамический отдел мозга через вегетативную нервную систему обеспечивает регуляцию теплоот- дачи, контролируя состояние тонуса сосудов кожи и секрецию потовых желез,
при этом большинство потовых желез имеет симпатическую иннервацию, но медиатором подходящих к ним постганглионарных симпатических волокон является ацетилхолин. В постсинаптической мембране мерокринных потовых желез адренергические рецепторы отсутствуют, но и некоторые холинергические рецепторы могут реагировать на циркулирующие в крови адреналин и норадреналин. Принято считать, что двойную холинергическую и адренергическую иннервацию имеют только потовые железы ладоней и подошв. Этим объясняется их повышенная потливость при эмоциогенном стрессе.
Усиление потоотделения может быть нормальной реакцией на внешние раздражители (тепловое воздействие, физическая нагрузка, волнение). Вместе с тем избыточный, устойчивый, локализованный или генерализованный гипергидроз может быть следствием некоторых органических неврологических, эндокринных, онкологических, общесоматических, инфекционных заболеваний. В случаях патологического гипергидроза патофизиологические механизмы различны и определяются особенностями основного заболевания.
Локальный патологический гипергидроз наблюдается относительно редко. В большинстве случаев это так называемый идиопатический гипергидроз, при котором избыточное потоотделение отмечается главным образом на ладонях, стопах, в подмышечной области. Проявляется с 15-30 лет, чаще у женщин. Со временем повышенная потливость может постепенно прекратиться или перейти в хроническую форму. Эта форма локального гипергидроза обычно сочетается с другими признаками вегетативной лабильности, нередко отмечается и у родственников больного.
К локальным относится и гипергидроз, связанный с приемом пищи или горячих напитков, особенно кофе, острых блюд. Пот выступает прежде всего на лбу и на верхней губе. Механизм этой формы гипергидроза не уточнен. Более определенной оказывается причина локального гипергидроза при одной из форм вегетативной прозопалгии - синдроме Байярже-Фрей, описанного французски- ми врачами - в 1847 г. J. Baillarger (1809-1890) и в 1923 г. L. Frey (аурикулотем- поральный синдром), возникающего в результате повреждения ушно-височного нерва в связи с воспалением околоушной слюнной железы. Обязательным про- явлением приступа при этой болезни является гиперемия кожи и усиленное потоотделение в области околоушно-височной области. Возникновение приступов обычно провоцируется приемом горячей пищи, общим перегреванием, курением, физической работой, эмоциональным перенапряжением. Синдром Байяр- же-Фрей может проявляться и у новорожденных, у которых при родоразрешении с применением щипцов был поврежден лицевой нерв.
Синдром барабанной струны характеризуется усиленным потоотделением в области подбородка, обычно в ответ на вкусовое ощущение. Он возникает после операций на поднижнечелюстной железе.
Генерализованный гипергидроз встречается значительно чаще локального. Физиологические механизмы его различны. Вот некоторые из состояний, провоцирующие гипергидроз.
1. Терморегуляторное потоотделение, которое возникает на всем теле в ответ на повышение температуры окружающей среды.
2. Генерализованное избыточное потоотделение может быть следствием психогенного стресса, проявлением гнева и особенно страха, гипергидроз - одно из объективных проявлений ощущаемой пациентом интенсивной боли. Однако при эмоциональных реакциях потоотделение может быть и в ограниченных областях: лицо, ладони, стопы, подмышечные впадины.
3. Инфекционные заболевания и воспалительные процессы, при которых в крови появляются пирогенные вещества, что ведет к формированию триады: гипертермия, озноб, гипергидроз. Нюансы развития и особенности течения составляющих этой триады нередко находятся в зависимости от особенностей инфекции и состояния иммунной системы.
4. Изменения уровня метаболизма при некоторых эндокринных нарушениях: акромегалии, тиреотоксикозе, сахарном диабете, гипогликемии, климактерическом синдроме, феохромоцитоме, гипертермии различного генеза.
5. Онкологические заболевания (прежде всего рак, лимфома, болезнь Ходжкина), при которых в кровь попадают продукты метаболизма и распада опухоли, дающие пирогенный эффект.
Патологические изменения потоотделения возможны при поражениях головного мозга, сопровождающихся нарушением функций его гипоталамического отдела. Провоцировать расстройства потоотделения могут острые нарушения мозгового кровообращения, энцефалиты, объемные патологические процессы в полости черепа. При паркинсонизме нередко отмечается гипергидроз на лице. Гипергидроз центрального генеза характерен для семейной дизавтономии (синдром Райли-Дея).
На состояние потоотделения оказывают влияние многие лекарственные препараты (аспирин, инсулин, некоторые анальгетики, холиномиметики и антихолинестеразные средства - прозерин, калемин и т.п.). Гипергидроз может быть спровоцирован алкоголем, наркотиками, может быть одним из проявлений синдрома отмены, абстинентных реакций. Патологическая потливость являет- ся одним из проявлений отравления фосфорорганическими веществами (ФОВ).
Особое место занимает эссенциальная форма гипергидроза, при которой морфология потовых желез и состав пота не изменены. Этиология этого состояния неизвестна, фармакологическая блокада активности потовых желез не приносит достаточного успеха.
При лечении больных с гипергидрозом могут быть рекомендованы М-холинолитики (циклодол, акинетон и т.п.), малые дозы клофелина, сонапакс, бетаадреноблокаторы. Более эффективны местно применяемые вяжущие средства: растворы перманганата калия, солей алюминия, формалина, таниновой кислоты.
Ангидроз (отсутствие потоотделения) может быть следствием симпатэктомии. Повреждение спинного мозга обычно сопровождается ангидрозом на туловище и конечностях ниже очага поражения. При полном синдроме Горнера наряду с основными признаками (миоз, псевдоптоз, эндофтальм) на лице на стороне поражения обычно можно отметить гиперемию кожи, расширение конъюнктивальных сосудов и ангидроз. Ангидроз может выявляться в зоне, иннервируемой поврежденными периферическими нервами. Ангидроз на туловище
и нижних конечностях может быть и следствием сахарного диабета, в таких случаях больные плохо переносят жару. У них может быть усиленным потоотделение на лице, голове, шее.
13.3.15. Алопеция
Алопеция невротическая (алопеция Михельсона) - облысение, возникающее вследствие нейротрофических расстройств при заболеваниях головного мозга, прежде всего структур диэнцефального отдела мозга. Лечение этой формы нейротрофического процесса не разработано. Алопеция может быть следствием рентгеновского или радиоактивного облучения.
13.3.16. Тошнота и рвота
Тошнота (nausea) - своеобразное тягостное ощущение в глотке, в эпигастральной области надвигающихся позывов к рвоте, признаки начинающейся антиперистальтики. Возникает вследствие возбуждения парасимпатического отдела вегетативной нервной системы, например при чрезмерном раздражении вестибулярного аппарата, блуждающего нерва. Сопровождается бледностью, гипергидрозом, обильным слюноотделением, нередко - брадикардией, артериальной гипотензией.
Рвота (vomitus, emesis) - сложный рефлекторный акт, проявляющийся непроизвольным выбрасыванием, извержением содержимого пищеварительного тракта (главным образом желудка) через рот, реже - через нос. Может быть обусловлен непосредственным раздражением рвотного центра - хеморецепторной зоны, расположенной в покрышке продолговатого мозга (мозговая рвота). Таким раздражающим фактором может быть очаговый патологический процесс (опухоль, цистицеркоз, кровоизлияние и пр.), а также гипоксия, токсическое влияние анестетиков, опиатов и пр.). Мозговая рвота возникает чаще вследствие повышения внутричерепного давления, нередко она проявляется утром натощак, обычно без предвестников и имеет фонтанирующий характер. Причиной мозговой рвоты могут быть энцефалит, менингит, травма мозга, опухоль мозга, острое нарушение мозгового кровообращения, отек мозга, гидроцефалия (все ее формы, кроме викарной, или заместительной).
Психогенная рвота - возможное проявление невротической реакции, невроза, психических расстройств.
Часто причиной рвоты являются различные факторы, вторично раздражающие рецепторы блуждающего нерва на разных уровнях: в диафрагме, органах пищеварительного тракта. В последнем случае афферентную часть рефлекторной дуги составляет главным образом основная, чувствительная порция блуждающего нерва, а эфферентную - двигательные порции тройничного, языкоглоточного и блуждающего нервов. Рвота может быть также следствием перевозбуждения вестибулярного аппарата (морская болезнь, болезнь Меньера и пр.).
Акт рвоты состоит из последовательных сокращений различных мышечных групп (диафрагмы, брюшного пресса, привратника и пр.), при этом опускается надгортанник, приподнимаются гортань и мягкое нёбо, что ведет к изоляции (не всегда достаточной) дыхательных путей от попадания в них рвотных
масс. Рвота может быть защитной реакций пищеварительной системы на по- падание в нее или образование в ней токсичных веществ. При тяжелом общем состоянии больного рвота может обусловить аспирацию дыхательных путей, повторные рвоты - одна из причин обезвоживания организма.
13.3.17. Икота
Икота (singultus) - непроизвольное миоклоническое сокращение дыхательных мышц, имитирующее фиксированный вдох, при этом внезапно дыхательные пути и проходящий по ним поток воздуха перекрываются надгортанником и возникает характерный звук. У здоровых людей икота может быть следствием раздражения диафрагмы, обусловленного перееданием, употреблением охлажденных напитков. В таких случаях икота единичная, кратковременная. Упор- ная икота может быть следствием раздражения нижних отделов ствола мозга при нарушениях мозгового кровообращения, субтенториальной опухоли или травматического повреждения ствола мозга, нарастающей внутричерепной ги- пертензии и в таких случаях является признаком, сигнализирующим об угрозе жизни больного. Опасным может быть и раздражение спинномозгового нерва СIV, а также диафрагмального нерва опухолью щитовидной железы, пищевода, средостения, легких, артериовенозной мальформацией, лимфомой шеи и пр. Причиной икоты могут быть также желудочно-кишечные заболевания, панкреатит, поддиафрагмальный абсцесс, а также интоксикация алкоголем, барбитуратами, наркотическими средствами. Возможна и повторная икота как одно из проявлений невротической реакции.
13.3.18. Расстройства иннервации сердечно-сосудистой системы
Расстройства иннервации сердечной мышцы сказываются на состоянии общей гемодинамики. Отсутствие симпатических влияний на сердечную мышцу ограничивает увеличение ударного объема сердца, а недостаточность влияний блуждающего нерва приводит к появлению тахикардии в покое, при этом возможны различные варианты аритмии, липотимии, синкопальные состояния. Нарушение иннервации сердца у больных сахарным диабетом ведет к аналогичным явлениям. Общие вегетативные расстройства могут сопровождаться приступами падения артериального давления ортостатического характера, возникающими при резких движениях, при попытке больного быстро принять вертикальное положение. Вегетативно-сосудистая дистония может также проявляться лабильностью пульса, изменениями ритма сердечной деятельности, склонностью к ангиоспастическим реакциям, в частности к сосудистым головным болям, вариантом которых являются различные формы мигрени.
У больных с ортостатической гипотензией возможно резкое снижение арте- риального давления под влиянием многих лекарственных препаратов: гипотен- зивных средств, трициклических антидепрессантов, фенотиазинов, вазодилата- торов, диуретиков, инсулина. Денервированное сердце человека функционирует в соответствии с правилом Франка-Старлинга: сила сокращений волокон миокарда пропорциональна первоначальной величине их растяжения.
13.3.19. Нарушение симпатической иннервации гладких мышц глаза (синдром Бернара-Горнера)
Синдром Бернара-Горнера, или синдром Горнера. Симпатическая иннервация гладкой мускулатуры глаза и его придатков обеспечивается нервными импульсами, идущими из ядерных структур задней части гипоталамического отдела мозга, которые по нисходящим проводящим путям проходят через ствол и шейный отдел спинного мозга и заканчиваются в клетках Якобсона, формирующих в боковых рогах CVIII-DI сегментов спинного мозга цилиоспинальный центр Будже-Веллера. От него они по аксонам клеток Якобсона, проходящим через соответствующие передние корешки, спинальные нервы и белые соеди- нительные ветви, попадают в шейный отдел паравертебральной симпатической цепочки, достигая при этом верхнего шейного симпатического узла. Далее импульсы продолжают путь по постганглионарным волокнам, принимающим участие в формировании симпатического сплетения общей и внутренней сонной артерий, и достигают пещеристого синуса. Отсюда они вместе с глазной артерией проникают в глазницу и иннервируют следующие гладкие мышцы: мышцу, расширяющую зрачок, глазничную мышцу и мышцу хряща верхнего века (m. dilatator pupillae, m. orbitalis и m. tarsalis superior).
Нарушение иннервации этих мышц, возникающее при поражении любого участка пути следования к ним симпатических импульсов, идущих от заднего отдела гипоталамуса, ведет к их парезу или параличу. В связи с этим на стороне патологического процесса возникает синдром Горнера, или Клода Берна- ра-Горнера, проявляющийся сужением зрачка (паралитический миоз), небольшим энофтальмом и так называемым псевдоптозом (приспущенностью верхнего века), обусловливающим некоторое сужение глазной щели (рис. 13.3). Ввиду сохранности парасимпатической иннервации сфинктера зрачка на стороне синдрома Горнера реакция зрачка на свет остается сохранной.
В связи с нарушением на гомолатеральной половине лица сосудосуживающих реакций синдром Горнера обычно сопровождается гиперемией конъюнктивы, кожи, возможны также гетерохромия радужки и нарушение потоотделения. Изменение потоотделения на лице может способствовать уточнению топики поражения симпатических структур при синдроме Горнера. При постганглионарной локализации процесса нарушение потоотделения на лице ограничено одной стороной носа и парамедиальным участком лба. Если же потоотделение расстроено на всей половине лица - поражение симпатических структур преганглионарное.
Поскольку птоз верхнего века и сужение зрачка могут иметь различное происхождение, для того чтобы убедиться в том, что в данном случае имеются проявления именно синдрома Горнера, можно проверить реакцию зрачков на закапывание в оба глаза раствора М-холиноблокатора. После этого при синдроме Горнера проявится выраженная анизокория, так как на стороне проявлений этого синдрома расширение зрачка будет отсутствовать или проявится незначительно.
Таким образом, синдром Горнера указывает на нарушение симпатической иннервации гладких мышц глаза и соответствующей половины лица. Он может быть следствием поражения ядер задней части гипоталамуса, центрального симпатического пути на уровне ствола мозга или шейного отдела спинного мозга, цилиоспинального центра, отходящих от него преганглионарных волокон,
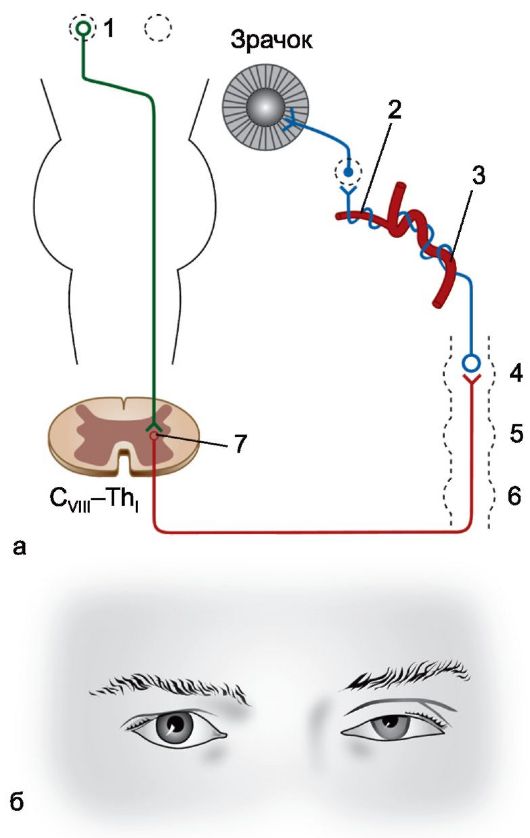
Рис. 13.3. Симпатическая иннервация глаза.
а - схема проводящих путей: 1 - ве- гетативные клетки гипоталамуса; 2 - глазная артерия; 3 - внутренняя сонная артерия; 4, 5 - средний и верхний узлы паравертебральной симпатической цепочки; 6 - звездчатый узел; 7 - тело симпатического нейрона в цилиоспинальном центре спинного мозга; б - внешний вид больного при нарушении симпатической иннервации левого глаза (синдром Бернара- Горнера).
верхнего шейного узла и идущих от него постганглионарных симпатических волокон, формирующих симпатическое сплетение наружной сонной артерии и ее ветвей. Причиной синдрома Горнера могут быть поражения гипоталамуса, ствола мозга, шейного отдела спинного мозга, симпатических структур на шее, сплетения наружной сонной артерии и ее ветвей. Такие поражения могут быть обусловлены травмой указанных структур ЦНС и периферической нервной системы, объемным патологическим процессом, цереброваскулярными заболеваниями, иногда демиелинизацией при рассеянном склерозе. Онкологическим процессом, сопровождающимся развитием синдрома Горнера, может быть рак верхней доли легкого, прорастающий в плевру (рак Панкоста).
13.3.20. Иннервация мочевого пузыря и ее расстройства
Важное практическое значение имеет и выявление нарушений функций мочевого пузыря, возникающее в связи с расстройством его иннервации, которая обеспечивается в основном вегетативной нервной системой (рис. 13.4).
Афферентные соматосенсорные волокна берут начало от проприорецепторов мочевого пузыря, реагирующих на его растяжение. Возникающие в этих рецепторах нервные импульсы через спинномозговые нервы SII-SIV проникают
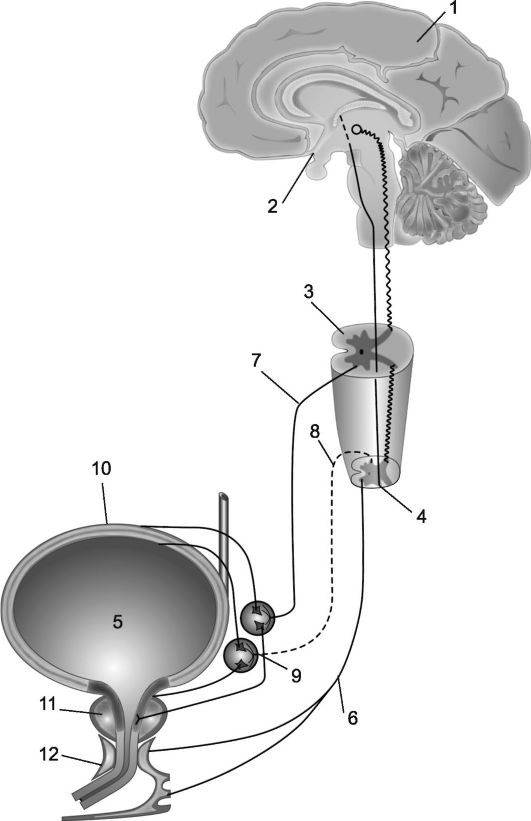
Рис. 13.4. Иннервация мочевого пузыря [по Мюллеру].
1 - парацентральная долька; 2 - гипоталамус; 3 - верхнепоясничный отдел спинного мозга; 4 - нижнекрестцовый отдел спинного мозга; 5 - мочевой пузырь; 6 - половой нерв; 7 - подчревный нерв; 8 - тазовый нерв; 9 - сплетения мочевого пузыря; 10 - детрузор мочевого пузыря; 11 - внутренний сфинктер мочевого пузыря; 12 - наружный сфинктер мочевого пузыря.
в задние канатики спинного мозга, в дальнейшем попадают в ретикулярную формацию ствола мозга и далее - в парацентральные дольки больших полушарий, при этом по пути следования часть этих импульсов переходит на противоположную сторону.
Благодаря информации, идущей по указанным периферическим, спинальным и церебральным структурам к парацентральным долькам, осознается растяжение мочевого пузыря при его заполнении, а наличие неполного пере-
креста этих афферентных путей ведет к тому, что при корковой локализации патологического очага нарушение контроля за тазовыми функциями возникает обычно лишь при поражении обоих парацентральных долек (например, при фалькс-менингиоме).
Эфферентная иннервация мочевого пузыря осуществляется главным образом за счет парацентральных долек, ретикулярной формации ствола мозга и спинальных вегетативных центров: симпатического (нейроны боковых рогов сегментов ThXI-LII) и парасимпатического, расположенного на уровне сегментов спинного мозга SII-SIV. Осознаваемая регуляция мочеиспускания осуществляется главным образом благодаря нервной импульсации, идущей от двигательной зоны коры больших полушарий и ретикулярной формации ствола к мотонейронам передних рогов сегментов SIII-SIV. Понятно, что для обеспечения нервной регуляции мочевого пузыря необходима сохранность проводящих путей, связывающих указанные структуры головного и спинного мозга между собой, а также образований периферической нервной системы, обеспечивающих иннервацию мочевого пузыря.
Преганглионарные волокна, идущие от поясничного симпатического центра тазовых органов (L1-L2), проходят в составе предкрестцового и подчревного нервов транзитом через каудальные отделы симпатических паравертебральных стволов и по поясничным внутренностным нервам (nn. splanchnici lumbales) достигают узлов нижнего брыжеечного сплетения (plexus mesentericus inferior). Идущие от этих узлов постганглионарные волокна принимают участие в формировании нервных сплетений мочевого пузыря и обеспечивают иннервацию прежде всего его внутреннего сфинктера. За счет симпатической стимуляции мочевого пузыря осуществляется сокращение внутреннего сфинктера, образованного гладкими мышцами; при этом по мере наполнения мочевого пузыря происходит растяжение мышцы его стенки - мышцы, выталкивающей мочу (m. detrusor vesicae). Все это обеспечивает удержание мочи, чему способствует и одновременное сокращение наружного поперечнополосатого сфинктера мочевого пузыря, имеющего соматическую иннервацию. Ее осуществляют половые нервы (nn. pudendi), состоящие из аксонов мотонейронов, расположенных в передних рогах SIIISIV сегментов спинного мозга. Через половые нервы проходят также эфферентные импульсы к мышцам тазового дна и встречные проприоцептивные афферентные сигналы от этих мышц.
Парасимпатическую иннервацию тазовых органов осуществляют преганглионарные волокна, идущие от парасимпатического центра мочевого пузыря, расположенного в крестцовом отделе спинного мозга (SI-SIII). Они участвуют в образовании тазового сплетения и достигают интрамуральных (расположенных в стенке мочевого пузыря) ганглиев. Парасимпатическая стимуляция вызывает сокращение гладкой мышцы, образующей тело мочевого пузыря (m. detrusor vesicae), и сопутствующее расслабление его гладких сфинктеров, а также усиление перистальтики кишечника, что создает условия для опорожнения мочевого пузыря. Непроизвольное спонтанное или спровоцированное сокращение детрузора мочевого пузыря (детрузорная гиперактивность) ведет к недержанию мочи. Детрузорная гиперактивность может быть нейрогенно обусловленной (например, при рассеянном склерозе) или идиопатической (при отсутствии выявленной причины).
Задержка мочи (retentio urinae) чаще возникает вследствие поражения спинного мозга выше места расположения спинальных симпатических вегетативных центров (ThXI-LII), ответственных за иннервацию мочевого пузыря.
К задержке мочи ведет диссинергия состояния детрузора и сфинктеров мочевого пузыря (сокращение внутреннего сфинктера и расслабление детрузора). Так
бывает, например, при травматическом поражении спинного мозга, внутри- позвоночной опухоли, рассеянном склерозе. Мочевой пузырь в таких случаях переполняется и дно его может подниматься до уровня пупка и выше. Задержка мочи возможна и вследствие поражения парасимпатической рефлекторной дуги, замыкающейся в крестцовых сегментах спинного мозга и обеспечивающей иннервацию детрузора мочевого пузыря. Причиной пареза или паралича детрузора может быть как поражение указанного уровня спинного мозга, так и расстройство функции составляющих рефлекторную дугу структур периферической нервной системы. В случаях стойкой задержки мочи больные обычно нуждаются в опорожнении мочевого пузыря через катетер. Одновременно с задержкой мочи обычно бывает и невропатическая задержка кала (retencia alvi).
Частичное повреждение спинного мозга выше уровня расположения вегетативных спинальных центров, ответственных за иннервацию мочевого пузыря, может привести к нарушению произвольного контроля за мочеиспусканием и возникновению так называемых императивных позывов на мочеиспускание, при которых больной, ощутив позыв, не в состоянии удерживать мочу. Вероятна большая роль нарушения иннервации наружного сфинктера мочевого пузыря, который в норме может быть до определенной степени контролируем усилием воли. Такие проявления расстройства функций мочевого пузыря возможны, в частности при двустороннем поражении медиальных структур боковых канатиков у больных с интрамедулярной опухолью или рассеянным склерозом.
Патологический процесс, поражающий спинной мозг на уровне расположения в нем симпатических вегетативных центров мочевого пузыря (клеток боковых рогов ThI-LII сегментов спинного мозга) ведет к параличу внутреннего сфинктера мочевого пузыря, тогда как тонус его протрузора при этом оказывается повышенным, в связи с этим возникает постоянное выделение мочи каплями - истинное недержание мочи (incontinentia urinae vera) по мере выработки ее почками, мочевой пузырь при этом практически пустой. Истинное недержание мочи может быть обусловлено спинальным инсультом, травмой спинного мозга или спинальной опухолью на уровне указанных поясничных сегментов. Истинное недержание мочи может быть сопряжено и с поражением структур периферической нервной системы, участвующих в иннервации мочевого пузыря, в частности при сахарном диабете или первичном амилоидозе.
При задержке мочи в связи с поражением структур центральной или пери- ферической нервной системы она накапливается в перерастянутом мочевом пузыре и может создавать в нем настолько высокое давление, что под его влиянием происходит растяжение находящихся в состоянии спастического сокращения внутреннего и наружного сфинктеров мочевого пузыря. В связи с этим через мочеиспускательный канал постоянно каплями или периодически малыми порциями выделяется моча при сохранении переполнения мочевого пузыря - парадоксальное недержание мочи (incontinentia urinae paradoxa), что может быть установлено выявлением при визуальном осмотре, а также при пальпации и перкуссии нижней части живота, выстояния дна мочевого пузыря выше лобка (иногда до пупка).
При поражении парасимпатического спинального центра (сегментов спинного мозга SI-SIII) и соответствующих корешков конского хвоста возможно развитие слабости и одновременное нарушение чувствительности мышцы, выталкивающей мочу (m. detrusor vesicae), при этом возникает задержка мочи.
Однако в таких случаях со временем возможно восстановление рефлекторного опорожнения мочевого пузыря, он начинает функционировать в «автономном» режиме (автономный мочевой пузырь).
Уточнение характера нарушений функции мочевого пузыря может способствовать определению топического и нозологического диагнозов основного заболевания. С целью уточнения особенностей расстройств функций мочевого пузыря наряду с тщательным неврологическим обследованием по показаниям проводится рентгенография верхних мочевых путей, мочевого пузыря и уретры с применением рентгеноконтрастных растворов. Уточнению диагноза могут способствовать результаты урологических обследований, в частности цистоскопия и цистометрия (определение давления в мочевом пузыре во время заполнения его жидкостью или газом). В некоторых случаях может быть информативна электромиография периуретральной поперечнополосатой мускулатуры.