Детские болезни в 2-х томах: том 2 : учебник / Под ред. И.Ю. Мельниковой, - 2009.
|
|
|
|
РАЗДЕЛ VIII ДЕТСКАЯ ОНКОЛОГИЯ
Злокачественный опухоли - редкие болезни детского возраста: заболеваемость ими составляет 11-16 случаев на 100 тыс. детского населения, однако среди причин смертности в экономически развитых странах они занимают второе место у детей старше 5 лет после травм и несчастных случаев. Структура онкологической заболеваемости у детей совершенно отличается от таковой у взрослых, для которых характерны раки (т.е. опухоли эпителиальной природы) различных органов. Детские опухоли в подавляющем большинстве имеют неэпителиальную природу, развиваясь из эмбриональных тканей.
Международная классификация злокачественных опухолей у детей (Лион, 1996)
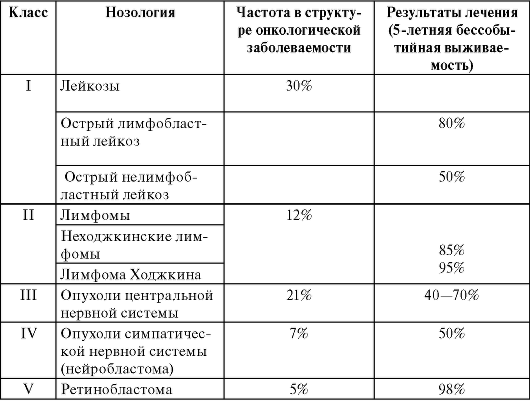
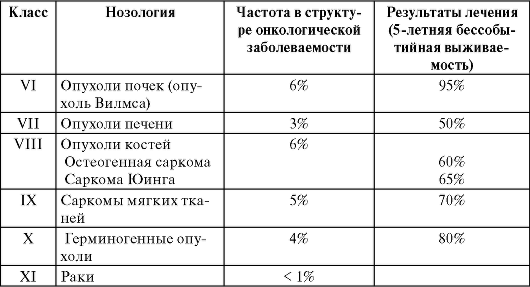 Детская онкология - мультидисциплинарная специальность. Успешное лечение детских злокачественных опухолей требует качественных усилий целой команды специалистов разных профилей, обеспечивающих диагностический и лечебный процесс. Без корректного морфологического диагноза, обеспеченного проведением гистологического, иммуногистохимического и молекулярно-генетического исследований равно как и без квалифицированного обследования, особенно визуализирующих методов (УЗИ, КТ, МРТ, ПЭТ), невозможно применить адекватное лечение и мониторировать его эффективность.
Детская онкология - мультидисциплинарная специальность. Успешное лечение детских злокачественных опухолей требует качественных усилий целой команды специалистов разных профилей, обеспечивающих диагностический и лечебный процесс. Без корректного морфологического диагноза, обеспеченного проведением гистологического, иммуногистохимического и молекулярно-генетического исследований равно как и без квалифицированного обследования, особенно визуализирующих методов (УЗИ, КТ, МРТ, ПЭТ), невозможно применить адекватное лечение и мониторировать его эффективность.
Современное лечение большинства детских злокачественных опухолей осуществляется по протоколам, разработанным для каждой нозологической формы. Практически все детские опухоли в той или иной мере чувствительны к химиотерапии, поэтому главным методом лечения в детской онкологии является многокомпонентная ПХТ. Для ряда опухолей, таких как лейкозы и лимфомы, ПХТ является единственно необходимым и достаточным методом лечения, приводящим к излечению 70-90% больных. Для опухолей ЦНС ведущим является оперативный метод, когда прогноз определяется в первую очередь степенью радикальности удаления опухоли, а ПХТ и ЛТ выполняют адьювантные задачи, существенно улучшая прогноз у этих больных. Излечение детей с опухолью Вилмса и опухолями костей в равной степени зависит от успеха хирургического и химиотерапевтического методов. Современные интенсивные программы
ПХТ являются не только высокоэффективными, но и токсичными. Проведение ПХТ практически всегда сопровождается возникновением неизбежных осложнений: цитопении, инфекции, геморрагический синдром, токсический гепатит, энцефалопатии, почечная недостаточность и другие. Исход лечения зачастую определяется не только грамотным проведением самой ПХТ с соблюдением тайминга и дозировок цитостатиков, но в не меньшей степени качеством сопроводительного лечения: заместительной гемотрансфузионной терапии, энтерального и парентерального питания, антибактериальной, антимикотической и противовирусной терапии, применения иммуноглобулинов и ростовых факторов.
Противоопухолевое лечение, которое получает больной в детском возрасте, может иметь отдаленные последствия и осложнения, которые могут проявиться через многие годы.
Наибольшим неблагоприятным действием в плане возникновения поздних осложнений обладает лучевая терапия.
Однако благодаря современным подходам к лечению опухолей у детей можно уверенно утверждать, что более 70% детей, заболевших злокачественной опухолью, имеют шанс на полное выздоровление.
Глава 1
Опухоли центральной нервной
системы (ЦНС)
Опухоли ЦНС занимают второе место по частоте среди опухолей у детей и составляют около 20%. Классификация опухолей головного мозга основана на гистогенезе тканей головного мозга.
Педиатрическая модификация классификации ВОЗ
 Анапластическая ганглиоглиома
Анапластическая ганглиоглиома
По гистологическим признакам (наличие некрозов, митозов и т д.) дополнительно выделяют степень злокачественности или анаплазии: степень (низкая степень), III-IV (высокая степень). Степень анаплазии определяет биологическое поведение опухолей. Опухоли ЦНС также классифицируют по локализации, выделяют: супратенториальные, инфратенториальные, интраспинальные. У детей старше 1 года преобладают опухоли задней черепной ямки (мозжечок, ствол головного мозга, IV желудочек).
Клиническая картина. Любая опухоль головного мозга имеет злокачественное поведение, так как ее рост происходит в ограничен-
ном объеме, а прогноз и клиническая картина зависят не только от гистологической природы, но и от локализации и размера образования, а также возраста ребенка. Симптомы могут быть вызваны инфильтрацией и сдавлением ткани мозга, а также нарушением ликвородинамики. Соответственно выделяют очаговые симптомы и признаки повышения внутричерепного давления (ВЧД). В зависимости от локализации образования у пациента могут отмечаться судороги (супратенториальные опухоли), атаксия, нистагм (поражение мозжечка), бульбарные расстройства (ствол головного мозга), нарушение зрения, двоение, гемипарез; при интраспинальной локализации - боли в спине, нарушение функции тазовых органов, парапарез. При повышении ВЧД отмечаются утренняя головная боль, рвота, сонливость.
Диагностика включает осмотр офтальмолога и невролога, а также проведение нейровизуализирующих методов исследования. Так как у детей наиболее частыми являются инфратенториальные опухоли, МРТ имеет преимущество перед КТ, проведение которой оправдано только при супратенториальной локализации образования. Эти исследования обязательно должны проводиться с контрастным усилением гадоллиниум-содержащими препаратами. При ряде опухолей головного мозга (ПНЭО и медуллобластома, герминогенные опухоли) возможна нейродиссеменация и необходимо проведение МРТ спинного мозга. В настоящее время дополнительно используется позитронно-эмиссионная томография с метионином (ПЭТ). Гистологическая верификация опухоли необходима и позволяет определить дальнейшую тактику лечения. Основным методом лечения является операция. Если оперативное вмешательство с целью удаления опухоли затруднено из-за связи образования с жизненно важными структурами мозга, показано проведение биопсии опухоли, в том числе с использованием стереотаксической хирургии. В случае значительного увеличения ВЧД до удаления опухоли проводят шунтирование. Для большинства опухолей ЦНС максимальное удаление опухоли существенно улучшает прогноз.
В лечении опухолей ЦНС используют также ЛТ и ПХТ. Облучение не проводится детям младше трех лет независимо от гистологического варианта опухоли в связи с тяжелыми поздними последствиями ЛТ (нарушение роста, интеллектуального развития и т.д.). При проведении ПХТ используются препараты платины, винкристин, этопозид, циклофосфан.
Глиомы низкой степени злокачественности в случае полного удаления опухоли не требуют использования других методов лечения. При тотальном удалении прогноз благоприятный, 5-летняя выживаемость составляет 80-90%. В случае остаточной опухоли или рецидива могут быть использованы лучевая и химиотерапия. Злокачественные глиомы (анапластическая астроцитома, глиобластома) требуют проведения ХТ и локальной ЛТ. 5-летняя выживаемость у пациентов с анапластической астроцитомой составляет 30-45%, с мультиформной глиобластомой - менее 5%.
ПНЭО (или медуллобластома) - самая частая злокачественная опухоль детского возраста. ПНЭО, располагающуюся в задней черепной ямке, традиционно называют медуллобластомой. Среди всех злокачественных опухолей ЦНС имеет самую высокую способность к метастазированию, в том числе и за пределы нервной системы (костный мозг, кости, легкие, печень и.т.д.). Обязательно должна быть проведена МРТ спинного мозга с контрастом вне зависимости от локализации первичной опухоли, исследование ликвора. Показано проведение комплексного лечения. Послеоперационное облучение должно быть краниоспинальным в дозе 35 Гр с увеличением дозы на ложе опухоли до 55Гр с последующей цикловой ПХТ. Для детей младше трех лет разработаны специальные программы лечения без использования ЛТ. Результаты лечения локальных форм достигают 70%, при наличии метастазов - не более 40%.
Герминогенные опухоли. При подозрении на герминогенную опухоль (образование пинеальной области) необходимо определение уровня α-фетопротеина и β-хорионического гонадотропина в ликворе и сыворотке крови. Эти опухоли также способны диссеменировать по спинномозговому каналу и за пределы ЦНС. Оперативное вмешательство показано только при необходимости верификации диагноза (в случае несекретирующей опухоли, т.е. при нормальном уровне α- фетопротеина и β-хорионического гонадотропина), поскольку данные опухоли высоко чувствительны к ЛТ и ПХТ. Отдаленные результаты лечения герминогенных опухолей лучшие среди всех опухолей ЦНС, 5-летняя выживаемость составляет 85-90%.
Опухоли ствола головного мозга. Эту категорию опухолей выделяют из-за особой локализации, т.к. именно локализация определяет особенности лечения и прогноз заболевания. Эти опухоли сдавливают ствол головного мозга, вызывая множественные парезы черепно-мозговых нервов. По гистологическому строению наиболее часто
встречаются глиомы (возможна как низкая, так и высокая степень анаплазии). Тип роста может быть экзофитным или инфильтративным. Возможность удаления опухоли (экзофитный тип роста) существенно улучшает прогноз у таких больных. Остальным пациентам не всегда возможно даже проведение биопсии опухоли. Проводится ЛТ. При гистологической верификации диагноза дополнительно используют ПХТ. Прогноз заболевания неблагоприятный, 5-летняя выживаемость менее 15%.
Опухоли спинного мозга. Они встречаются гораздо реже, чем опухоли головного мозга. Клинические проявления зависят от уровня опухолевого поражения и скорости роста. Основные симптомы: нарушения походки, хромота, боли в спине, расстройства двигательных и чувствительных функций ниже уровня поражения.
Лечение: радикальная операция, локальная ЛТ. При анапластической гистологии - ПХТ.
Прогноз более благоприятный - выживаемость составляет более
75%.
Глава 2
Злокачественные лимфомы
К злокачественным лимфомам относятся болезнь Ходжкина и большая группа заболеваний, объединенных названием «неходжкинские лимфомы».
БОЛЕЗНЬ (ЛИМФОМА) ХОДЖКИНА (ЛИМФОГРАНУЛЕМАТОЗ)
Понятие «Болезнь Ходжкина» (БХ) объединяет 2 заболевания, имеющие различную биологическую природу, проявляющуюся в различной морфологии и иммунофенотипе, а также разные клинические проявления и поведение: Лимфома Ходжкина с нодулярным лимфоцитарным преобладанием (Парагранулема Ходжкина) - моноклональное злокачественное заболевание В-клеточной природы, составляющее не более 5% всех случаев БХ, и классическая Лимфома Ходжкина
Заболеваемость БХ в детском возрасте составляет 0,7-0,8 на 100 тыс. детского населения, что гораздо ниже частоты этого заболевания у взрослых. Мальчики заболевают чаще, чем девочки.
В патогенезе БХ значительную роль играет вирус Эпштейна-Барр (ЭБВ). В настоящее время считается, что БХ - это результат длительно текущей латентной ЭБВ-инфекции. У лиц, инфицированных вирусом приобретенного иммунодефицита, заболеваемость БХ в 3-10 раз выше, чем у неинфицированных.
Клиническая картина
БХ, как правило, типична. Заболевание чаще всего начинается с поражения периферических лимфатических узлов (л/у). Приблизительно у 90% больных отмечается поражение л/у на шее (шейных и надключичных). Пораженные л/у безболезненны, плотноэластичны по консистенции, их увеличение может регистрироваться долгое время, в течение нескольких недель, и часто размеры их могут изменяться. Шейная лимфаденопатия - явление довольно частое в детском возрасте, но, как правило, при воспалительных процессах
чаще вовлекаются верхне-шейные и подчелюстные л/у. Подмышечные л/у вовлекаются в процесс примерно у 20% больных, паховые - в менее чем 5% случаев. Примерно у 60% больных (особенно старшего возраста) поражаются медиастинальные л/у, иногда с возникновением плеврита и контактным вовлечением перикарда, плевры, грудной стенки и ткани легкого. Поддиафрагмальные л/у поражаются реже, и при их вовлечении особых жалоб больные не предъявляют.
При парагранулеме Ходжкина обычно вовлекаются только шейные, подмышечные и паховые л/у. Чаще всего больные имеют 1-2 стадии заболевания, процесс течет медленно и никогда не заканчивается фатально.
Морфологический диагноз
БХ основывается на обнаружении причудливых многоядерных гигантских клеток, так называемых, клеток Рид-Штернберга (Р-Ш) или их одноядерного варианта - клеток Ходжкина (Х), окруженных значительно выраженной реактивной воспалительной клеточной реакцией. Согласно общепринятой «Rye» классификации при классической БХ различают 4 основных гистологических подтипа: лимфоидное преобладание, смешаноклеточный вариант, нодуллярный склероз (grade 1 и grade 2) и лимфоидное истощение. Основную массу составляют больные со смешанноклеточным вариантом и нодулярным склерозом. На долю лимфоидного преобладания и лимфоидного истощения приходится около 10% случаев.
Стадирование
Интенсивность и объем лечения БХ зависит от стадии заболевания. По международной классификации Ann Arbor при БХ различают 4 стадии заболевания.
Стадия I - поражение одной группы л/у или одного экстралимфатического органа (ЭЛО).
Стадия II - поражение двух и более лимфатических зон по одну сторону от диафрагмы или локализованное вовлечение одного ЭЛО и одной или более лимфатических областей по одну сторону от диафрагмы (IIE).
Стадия III - поражение лимфатических областей по обе стороны от диафрагмы, которое может сопровождаться локализованным вовлечением одного ЭЛО (IIIE) или вовлечением селезенки (IIIS), или того и другого (IIIES).
Стадия IV - диссеминированное поражение одного или более экстралимфатических органов или тканей (кроме ситуаций подстадии Е) в сочетании или без вовлечения л/у.
Учитывается также наличие или отсутствие общих, так называемых «В» симптомов: лихорадка, профузные ночные поты, потеря массы тела на 10% и более за последние 6 месяцев. Кожный зуд, который часто встречается у больных с выраженными общими симптомами, не входит в группу В-симптомов. Таким образом, формируются подстадия-А (при отсутствии общих симптомов) и подстадия-В - при их наличии. Наличие В-симптомов ухудшает прогноз заболевания, поэтому дети с одинаковой степенью распространения процесса, но имеющие общие симптомы должны лечиться более интенсивно.
Обследование больного с БХ помимо стандартного «клинического минимума» должно включать.
1. Биопсию наиболее увеличенного периферического л/у с гистологическим и иммуногистохимическим исследованиями. Аспирационной биопсии недостаточно! При отсутствии увеличения периферических л/у - открытая биопсия медиастинальных или абдоминальных л/у.
2. КТ грудной клетки (даже при нормальной Rg), брюшной полости, забрюшинного пространства и носоглотки.
3. ПЭТ всего тела с фторглюкозой (по возможности).
4. Диагностическая лапаротомия выполняется в случае специальных показаний.
5. Трепанобиопсия костного мозга при III-IV стадиях и при наличии общих симптомов.
6. Остеосцинтиграфия (с прицельной Rg выявленных очагов) у больных с «костными» жалобами и у детей с повышенным уровнем щелочной фосфатазы.
7. Сцинтиграфия тела с Ga67.
Лечение
В настоящее время БХ является одной из самых излечимых злокачественных опухолей у детей. В нашей стране используется программа, основанная на многолетнем опыте Немецкого Общества детских онкологов и гематологов. Эта программа предусматривает проведение курсов ПХТ (препаратами винкристин, преднизолон, прокарбазин, адрибластин, этопозид, циклофосфан и дакарбазин), число которых (2-6) зависит от стадии заболевания, и облучение вовлеченных зон в дозе 20-25 Гр. В настоящее время долговременная выживаемость детей с БХ составляет 90-95%.
НЕХОДЖКИНСКИЕ ЛИМФОМЫ (НХЛ)
НХЛ занимают третье по частоте место среди злокачественных опухолей у детей и представляют гетерогенную группу злокачественных клональных опухолей лимфатической системы. Они возникают при пролиферации одной клетки лимфоидного ряда на любом этапе дифференцировки. По гистологической структуре в 97% случаев они имеют диффузный характер поражения. В отличие от взрослых, НХЛ у детей всегда относятся к лимфомам высокой степени злокачественности. Главным методом лечения НХЛ у детей является ПХТ. Детские НХЛ разделяются на 4 большие группы.
1. В-клеточные лимфомы Беркиттовского и не-Беркиттовского типа (около 45%).
2. Лимфобластные лимфомы из клеток - предшественниц Т- и В-лимфоцитов (25%).
3. Диффузные В-крупноклеточные лимфомы (примерно 20%)
4. Крупноклеточные анапластические лимфомы (около 10%) Несмотря на различия в первичной клинической картине, гистологической характеристике, цито- и молекулярной генетике, общими чертами детских НХЛ являются агрессивное клиническое течение, быстрая генерализация с вовлечением костного мозга, ЦНС и костей скелета.
При установлении стадии НХЛ в детской практике применяется система Murphy.
Стадия I. Одиночный узел или одиночная опухоль без местного распространения.
Стадия II. Несколько узлов или экстранодальные проявления по одну сторону от диафрагмы без или с местным распространением. Для В-клеточных и ККАЛ стадия II делится на подстадии:
II R: резектабельная. Опухоль макроскопически полностью удалена;
II NR: нерезектабельная. Опухоль макроскопически полностью не удалена.
Стадия III. Опухоль по обе стороны от диафрагмы. Все опухоли в грудной клетке. Все распространенные опухоли в брюшной полости. Эпидуральные опухоли.
Стадия IV. Независимо от локализации первичной опухоли при вовлечении костного мозга (<25% бластов), ЦНС и/или с поражением скелета.
Острый лимфобластный лейкоз. Более 25% бластов в костном мозге.
При диагностике всех видов НХЛ у детей применяются единые подходы.
1. Открытая биопсия с проведением морфологического, иммунологического, цитогенетического и молекулярно-генетического исследований лимфатических узлов. Диагноз может быть установлен с использованием наименее инвазивных методов: аспирационная биопсия периферических ЛУ или опухолевых масс, исследование ликвора и костного мозга.
2. Rg органов грудной клетки в двух проекциях.
3. УЗИ брюшной полости, малого таза, шейных, аксиллярных и других л/у.
4. КТ грудной, брюшной полости и малого таза.
5. Остеосцинтиграфия выявляет поражение костей скелета.
6. Сцинтиграфия с 67Ga (препаратом, тропным к лимфоидной ткани).
7. ПЭТ с фтор-глюкозой - чувствительный и высокоспецифичный метод диагностики опухолей.
8. Аспирационная биопсия костного мозга из как минимум трех мест, позволяет увеличить вероятность выявления диссеминированных форм заболевания.
9. Спинномозговая пункция с исследованием ликвора - важен клеточный состав осадка, в котором могут быть выявлены бластные клетки.
10. Клинический анализ крови может быть абсолютно нормальным, однако нередко выявляются бластные формы или панцитопения, что может быть косвенным признаком поражения костного мозга.
11. Биохимическое исследование сыворотки крови: уровень лактат-дегидрогеназы (ЛДГ), ее активность определяет группу риска при лечении распространенных В-НХЛ, уровень мочевой кислоты как показателя степени распада опухоли для коррекции инфузионной терапии с целью предотвращения мочекислого инфаркта почек.
12. Сцинтиграфия почек, изотопная ренография - для оценки функции почек перед проведением в дальнейшем нефротоксичной терапии.
В-КЛЕТОЧНЫЕ НХЛ
В-клеточные НХЛ (Лимфома Беркитта, Беркитто-подобные лимфомы) - самый частый вариант НХЛ у детей, характерным признаком которых является обязательная экспрессия поверхностного иммуноглобулина М (sIgM), а также κ- или λ-легких цепей иммуноглобулина. Характерной хромосомной транслокацией является t(8,14)(q24;q32)
В-НХЛ могут быть диагностированы в любом возрасте, однако пик частоты 5-7 лет. Мальчики болеют чаще, чем девочки (3:1).
Клиническая картина
Самой частой первичной локализацией является брюшная полость (60-70%). Опухоль может возникать в любом отделе тонкого и толстого кишечника, однако чаще всего поражаются терминальные отделы подвздошной кишки, илеоцекальный угол и мезентериальные л/у. Манифестация заболевания может быть острой с развитием типичной картины кишечной непроходимости. В этом случае опухоль чаще всего исходит из кишки и имеет небольшие размеры. В большинстве же случаев первыми симптомами являются боли в животе, при осмотре обнаруживается опухоль, чаще всего уже больших размеров, нередко с асцитом. Очагом первичной локализации могут также быть периферические л/у, Вальдейерово кольцо, эпидуральное пространство, однако это встречается значительно реже.
Клиническая картина истинной африканской лимфомы Беркитта отличается от вышеописанной: поражаются лицевой череп (верхняя челюсть вовлекается в процесс в 2 раза чаще, чем нижняя), брюшная полость, почки и ЦНС.
Лечение и прогноз
Операция используется только для диагностики - биопсии опухоли и при картине «острого живота». Но и в этом случае удаление опухоли следует производить только тогда, когда она может быть удалена радикально и без значительного повреждения анатомо-физиологического строения кишечника, т.е. при ее небольших размерах. Во всех остальных случаях следует ограничиться биопсией, поскольку любой объем нерадикальной операции не влияет на прогноз у ребенка с НХЛ. ЛТ в настоящее время исключена из программ лечения детей с В-НХЛ. Главным и высокоэффективным методом лечения В-НХЛ является многокомпонентная интенсивная ПХТ. Поскольку эти опухоли обладают высокой скоростью пролиферации, ХТ проводится короткими интенсивными курсами с минимальными межкурсовыми интервалами. Количество (2-6) и интенсивность блоков ПХТ зависит от стадии заболевания и уровня ЛДГ. Используются следующие химиопрепараты: винкристин, преднизолон, доксорубицин, цитозар дексаметазон, циклофосфан, ифосфамид, метотрексат и этопозид. Обязательны интратекальные введения цитостатиков в каждом блоке ПХТ. В последнее время применяется монокло-
нальное антитело - антиСD20 - ритуксимаб (мабтера). Длительность лечения составляет от 2 до 6 месяцев. Дети с ограниченными стадиями В-НХЛ имеют благоприятный прогноз с уровнем выживаемости 90-95%, при распространенных стадиях выживаемость составляет 70-90%.
ЛИМФОБЛАСТНЫЕ ЛИМФОМЫ (ЛЛ)
Составляют примерно 20-25% всех НХЛ детского возраста. Морфологически они неотличимы от классического ОЛЛ у детей. Около 85% ЛЛ развивается из незрелых Т-клеток, 15% - из клетокпредшественниц В-лимфоцитов. При иммунофенотипировании ЛЛ диагностической является положительная ядерная реакция с антителами к TdT. У 80% больных с Т-ЛЛ выявляются хромосомные транслокации, самой частой из которых является t(11,14) (p13;q11).
Клиническая картина
Характерной первичной локализацией Т-клеточных ЛЛ является средостение, нередко с сопутствующим плевритом. Больные жалуются на одышку, затруднение дыхания, иногда дисфагию. Характерный признак - синдром сдавления верхней полой вены, проявляющийся отеком лица, шеи, верхних конечностей. Компремируя и смещая трахею и главные бронхи, лимфома может стать причиной нарушения бронхиальной проводимости с появлением ателектазов и участков гиповентиляции легких. Это состояние, требующее неотложной помощи и немедленного начала лечения. Часто у этих пациентов имеется увеличение периферических ЛУ выше диафрагмы (шейных, надподключичных, подмышечных). Вовлечение забрюшинных ЛУ встречается реже. Для этого вида лимфомы характерно более частое вовлечение ЦНС, костного мозга и поражение яичек.
ЛЛ из клеток-предшественниц В-ряда представлены в основном либо увеличением периферических ЛУ, либо поражением костей или кожи. Как правило, ЛЛ с В-клеточным иммунофенотипом представляют локальный процесс.
Лечение
Стандартным подходом к лечению Т-ЛЛ и ЛЛ из клеток-предшественниц В-ряда являются программы лечения для ОЛЛ, т.е. классический вариант, состоящий из индукции, консолидации,
реиндукции и длительной поддерживающей терапии. Общая продолжительность лечения составляет 2-2,5 года. Обязательным является ЦНС-направленная терапия: интратекальные введения цитостатиков + краниальное облучение при вовлечении ЦНС (нейролейкемии). В настоящее время с введением в программы лечения высокодозного метотрексата и L-аспарагиназы выживаемость для всех стадий составляет 75-90%.
ДИФФУЗНЫЕ КРУПНОКЛЕТОЧНЫЕ В-ЛИМФОМЫ
(ДККВЛ)
Группа заболеваний, включающая отдельные нозологические формы, которые отличаются вариабельностью клинических проявлений без типичной первичной локализации. ДККВЛ часто могут поражать периферические, медиастинальные и абдоминальные ЛУ. Реже эти лимфомы возникают в костях, коже и мягких тканях. Клинически ДККВЛ могут проявляться как системный процесс с поражением ЛУ самой различной локализации с вовлечением паренхиматозных органов и костей скелета, часто с выраженными В-симптомами.
Первичная медиастинальная ДККВЛ со склерозом
Составляет примерно 25% всех ДККВЛ, с определенной клинической картиной и иммунологическими и генетическими характеристиками. Доказано, что источник ее возникновения - активированные В-клетки тимуса. Клинически заболевание характеризуется увеличением медиастинальных л/у и тимуса, которые представляют собой значительную опухолевую массу с характерными для этой локализации проблемами: сдавлением верхней полой вены и дислокационным синдромом. Костный мозг и ЦНС вовлекаются в процесс редко. Даже при системном программном лечении по программам для В-НХЛ результат лечения у девочек-подростков хуже, чем у остальных больных с ДККВ (выживаемость составляет 66-70%).
КРУПНОКЛЕТОЧНЫЕ АНАПЛАСТИЧЕСКИЕ ЛИМФОМЫ (ККАЛ)
Характеризуются анапластической морфологией, с обязательной мембраноассоциированной экспрессией Ki-1 (CD30) антигена. В
подавляющем большинстве ККАЛ имеют Т-клеточный иммунофенотип, В-фенотип встречается крайне редко. Для ККАЛ характерной является хромосомная транслокация t(2;5)(p23;q35), которая встречается у большинства детей.
Клиническая картина
ККАЛ не имеют характерной локализации, может поражаться практически любая лимфатическая зона, однако часто выявляется увеличение л/у средостения. Но при ККАЛ синдром сдавления верхней полой вены не является частым. Характерно наличие общих симптомов (особенно лихорадки), вовлечение периферических л/у, которые часто выглядят воспаленными и болезненными, нередко поражается кожа. Иммунофенотипирование опухолевой ткани в данном случае имеет решающее значение, главным образом, для дифференциальной диагностики с Т-клеточными лимфомами и болезнью Ходжкина.
Лечение
Проводится по аналогии с лечением В-лимфом. Интенсивность лечения также является стадиозависимой. Выживаемость детей с ККАЛ составляет от 50 до 100% в зависимости от стадии.
Глава 3
Опухоли костей
У детей самые частые злокачественные опухоли костей - остеогенная саркома и саркома Юинга.
ОСТЕОГЕННАЯ САРКОМА (ОС)
Занимает 6-е место среди всех злокачественных опухолей детского возраста, происходит из примитивной кость-формирующей мезенхимы, продуцирует патологическую кость - остеоид. Пик заболеваемости - 10-20 лет.
Факторы, влияющие на развитие заболевания: ионизирующее излучение (сроки заболевания 12-16 лет), болезнь Педжета, доброкачественные опухоли костей, изменения генетического фона (изменения в 13-й паре хромосом, мутация опухоль-супрессирующего гена Р-53, инактивация ряда опухоль-супрессирующих генов).
Стандартные гистологические варианты остеосаркомы - остеобластическая (50%), хондробластическая (25%) и фибробластическая (менее 20%). Редкие варианты: телеангиэктатическая, юкстакортикальная (параоссальная), периоссальная, интраоссальная, мультифокальная, экстраскелетная, мелкоклеточная,
Стадирование
(Enneking WF, Spanier SS, Goodman MA, 1980)
IA Высокодифференцированная опухоль. Очаг ограничен естественным барьером. Отсутствие метастазов.
IB Высокодифференцированная опухоль. Очаг распространяется за пределы естественного барьера. Отсутствие метастазов.
IIA Низкодифференцированная опухоль. Очаг ограничен естественным барьером. Отсутствие метастазов.
IIB Низкодифференцированная опухоль. Очаг распространяется за пределы естественного барьера. Отсутствие метастазов.
III Наличие регионарных и отдаленных метастазов вне зависимости от степени дифференцировки опухоли.
Клиническая картина
Для опухолей костей характерна классическая триада симптомов: боль (в основном по ночам, с постепенным нарастанием интенсивности), увеличение объема и нарушение функции конечности. Длительность анамнеза составляет в среднем 3 месяца.
Локализация: преимущественно метафиз длинных трубчатых костей, около 50% - область коленного сустава (дистальная часть бедра и проксимальная часть большеберцовой кости), реже - проксимальная часть плечевой и бедренной костей, средняя треть бедренной кости. Поражение плоских костей, особенно таза, встречается редко. Основной путь метастазирования - гематогенный, преимущественно, в легкие. К моменту установления диагноза до 20% пациентов уже имеют макрометастазы в легких, выявляемые рентгенологически, но значительно больше пациентов имеют микрометастазы в легких, не выявляемые рутинной рентгенографией (Rg). Лимфогенное распространение редко и связано с плохим прогнозом. Другие зоны метастазирования - кости, плевра, перикард, почки, ЦНС.
ОС обладает локальным агрессивным ростом и может распространяться на эпифиз и близлежащий сустав (чаще всего поражаются коленный и плечевой суставы), и образовывать в костях очаги-сателлиты - «skip»-метастазы.
Диагностика
Обязательными являются Rg очага и легких. Rg-признаки ОС: метафизарная локализация в длинных трубчатых костях, наличие склеротических и литических очагов в кости, наличие васкуляризации и очагов патологического костеобразования в мягких тканях, нарушение целостности надкостницы с образованием «козырька» или «треугольника Кодмена», игольчатый периостит («спикулы»). Морфологическая верификация опухоли проводится с помощью биопсии. Остеосцинтиграфия с Te99 позволяет выявить другие очаги в костях. МРТ очага с контрастированием гадолиниум-содержащими препаратами выявляет более детально поражение кости и окружающих тканей. КТ легких проводится для выявления метастазов. Ангиография в некоторых случаях проводится для выявления вовлечения сосудов при решении вопроса о возможности органосохраняющей операции.
Неблагоприятные факторы прогноза: объем опухолевой массы более 200 мл и плохой гистологический ответ опухоли на предопе-
рационную ПХТ, а также центральная локализация опухоли в связи с невозможностью радикального удаления.
Лечение
Интенсивная ПХТ (пред- и послеоперационная) и обязательное удаление очага (ампутация или органосохраняющая операция с эндопротезированием) с исследованием гистологического ответа опухоли на ПХТ. В лечении ОС используются препараты платины, высокодозный метотрексат, доксорубицин, ифосфамид. Показания к ампутации - поражение сосудисто-нервного пучка, инфицирование места биопсии, слишком молодой возраст больного (при опухоли нижних конечностей), предшествующие операции с обсеменением мягких тканей, большие размеры опухоли с вовлечением мягких тканей. При наличии метастазов в легкие проводится метастазэктомия. Лучевая терапия с лечебной целью не применяется в связи с ее неэффективностью, однако ее можно использовать в качестве паллиативного лечения с противоболевой целью.
Выживаемость при локализованной форме ОС составляет в среднем около 65%. При метастатической ОС выживаемость не превышает 30%.
САРКОМА ЮИНГА (СЮ)
Вторая по частоте злокачественная опухоль костей у детей. Она относится к мелко-круглоклеточным опухолям, имеет нейроэктодермальное происхождение, не продуцирует остеоид. В 85% случаев в опухолевых клетках имеет место хромосомная транслокация t(11,22)(q24,q12).
Пик заболевания - 10-15 лет. Течение очень агрессивное, с быстрым распространением гематогенных метастазов - в легкие, кости, костный мозг, редко - в ЦНС. Лимфогенные метастазы также встречаются редко.
Локализация опухоли: преимущественно плоские кости (таз, лопатка, ребра, позвонки), кости конечностей.
Клиническая картина
Боль, отек, нарушение функции конечностей. Часто течение достаточно острое, с лихорадкой, признаками местного воспаления, напоминающее картину остеомиелита.
Диагностика: Rg очага и легких. Rg-признаки СЮ: деструкция кости («изъеденная молью») без четких границ, может распространяться по костно-мозговому каналу, многослойный линейный («луковичный») периостит, часто - патологический перелом. Мягкотканный компонент однородной структуры без очагов патологического костеобразования.
Биопсия опухоли проводится для верификации диагноза. Иногда возможно получить материал из мягкотканного компонента. Важно, чтобы все места вмешательств (биопсий, дренирования) были включены в дальнейшем в зону облучения или удалены во время операции.
КТ легких, МРТ очага, остеосцинтиграфия, ангиография - методы исследования и цели - такие же как при ОС.
Лечение
Многокомпонентная длительная интенсивная ПХТ (препараты: винкристин, доксорубицин, актиномицин, ифосфамид), по возможности, радикальное удаление опухоли (но без калечащих операций) и облучение первичного очага и/или метастазов. Неблагоприятные прогностические факторы: метастазы в кости, костный мозг, лимфатические узлы, поражение костей таза, объем опухолевой массы более 200 мл. Выживаемость в этих случаях не превышает 10%. При плохом прогнозе применяется высокодозная химиотерапия с трансплантацией аутологичных гемопоэтических стволовых клеток, что значительно улучшает выживаемость, которая составляет более 30%. Выживаемость при локализованной форме заболевания составляет около 50%.
Глава 4
Опухоль Вилмса (нефробластома)
Опухоль Вилмса (ОВ) является эмбриональной опухолью почки у детей младшего возраста. Она занимает 5-е место по частоте среди всех злокачественных опухолей детского возраста. Пик заболеваемости отмечается в возрасте 2-3 лет. ОВ может иметь двусторонний характер поражения, выявляемый в 8% случаев. Пациенты с ОВ имеют нормальный кариотип, но возможны структурные повреждения 11-й хромосомы у ряда пациентов, что имеет прогностическое значение.
Морфология опухоли
Макроскопически опухоль представлена кистами, очагами некрозов и кровоизлияниями. Микроскопически это эмбриональная опухоль и представляет собой сочетание трех клеточных типов: бластемного, стромального и эпителиального. По степени злокачественности и прогнозу ОВ может быть разделена на благоприятный, стандартный и неблагоприятный гистологические варианты в зависимости от преобладающего клеточного компонента.
Клиническая картина
Чаще всего плотно-эластичная опухоль в животе обнаруживается случайно родителями ребенка. Гематурия - один из симптомов ОВ, встречается только у 25% пациентов. Нередко отмечается повышение артериального давления. Общее состояние ребенка практически не изменяется.
Диагностика
УЗИ органов брюшной полости и забрюшинного пространства дает достаточно полную информацию об опухоли, однако необходимо проведение КТ с обязательным контрастным усилением, что позволяет определить характер и степень опухолевого распространения более детально. Rg и КТ легких проводятся для выявления метастазов.
Стадирование
Стадия устанавливается после операции - нефруретерэктомии. Стадия I - опухоль ограничена почкой и полностью удалима. Стадия II - опухоль выходит за пределы почки, но полностью удалима.
Стадия III - опухоль выходит за пределы капсулы почки, неполное удаление опухоли.
Стадия IV - отдаленные метастазы (в легкие, печень, кости, головной мозг и другие органы).
Стадия V - двухсторонняя нефробластома.
Лечение
Более 80% пациентов с ОВ могут быть полностью излечены. Лечение стадиозависимо, используется сочетание оперативного, лучевого и химиотерапевтического методов. Тотальное удаление опухоли с паранефральной клетчаткой является основным моментом в лечении. ЛТ проводится только у пациентов с плохим прогнозом и большим местным и/или метастатическим распространением процесса (пред- и послеоперационная). Пред- и послеоперационная ПХТ в настоящее время является базовым методом терапии, который значительно улучшил результаты лечения. Наиболее эффективными препаратами являются винкристин, дактиномицин, доксорубицин. В группе плохого прогноза дополнительно используются препараты вепезид, карбоплатин, ифосфамид, циклофосфан в режиме интенсивной ПХТ. При наличии метастазов в легкие проводится облучение или метастазэктомия.
Глава 5
Нейробластома
Нейробластома (НБЛ) - эмбриональная опухоль симпатической нервной системы. Она составляет 7-11% от общего числа злокачественных опухолей у детей. У детей первого года жизни НБЛ - самая частая злокачественная опухоль, 90% случаев диагностируется до 5 лет. Типичными источниками опухолевого роста являются симпатический нервный ствол (СНС) на всем его протяжении и мозговое вещество надпочечников. Около 40% опухолей возникают в надпочечниках, 30% исходят из поясничного отдела симпатического ствола, 15% - из грудного отдела, 3% - из тазовых параганглиев, 1% - из шейного отдела. НБЛ отличают ряд специфических, уникальных черт.
1. Способность к спонтанной регрессии. Инволюция злокачественного процесса до полной регрессии может встречаться у грудных детей. Иногда часть таких больных нуждается в минимальной ХТ или ЛТ для «индукции» процесса регрессии.
2. Способность к дифференцировке («созревание») - дифференцировка злокачественных НБЛ в доброкачественные опухоли, что происходит, правда, довольно редко (1:1150).
3. Способность к стремительному агрессивному развитию и бурному метастазированию. Основными факторами, относящимися к несомненным маркерам прогрессии, являются N-myc-амплификация и делеция 1-й пары хромосомы (1р).
Клиническая картина
Зависит от локализации первичной опухоли, наличия и локализации метастазов, количества вазоактивных веществ, продуцируемых опухолью. Основными жалобами являются боль (30-35%), лихорадка (25-30%), потеря веса (20%). Поражение шейно-грудного отдела СНС рано вызывает синдром Горнера. Локализация НБЛ в заднем средостении может стать причиной навязчивого кашля, дыхательных расстройств, деформации грудной стенки, может вызвать дисфагию, а у малышей - частые срыгивания. Поражение костного мозга влечет за собой анемию и геморрагический синдром. Характерен
симптом «очков» с экзофтальмом при поражении ретробульбарного пространства у детей с IV стадией заболевания. Метастазы в кожу имеют синюшно-багровую окраску и плотную консистенцию. При наиболее частой забрюшинной локализации выявляется бугристая, каменистой плотности, практически несмещаемая опухоль. Возможно развитие плегии нижних конечностей при врастании опухоли в спинномозговой канал, что требует ургентной ляминэктомии и декомпрессии.
Возможно повышение артериального давления и возникновение некупируемой диареи.
Более половины больных к моменту диагностики имеют IV стадию процесса, т.е. у них выявляются отдаленные метастазы. Наиболее часто НБЛ метастазирует в лимфатические узлы, костный мозг, кости, печень и головной мозг. Легкие при НБЛ поражаются крайне редко.
Диагностика
Диагноз НБЛ устанавливается по данным биопсии (из очага или метастазов) или при поражении костного мозга в сочетании с повышенным более чем в 3 раза содержанием маркеров опухоли - катехоламинов (КА) или их дериватов: ванилилминдальной (ВМК), гомованилиновой (ГВК) кислот и дофамина (ДА) в крови или в моче, уровни которых повышены у 85% больных. К маркерам НБЛ относится также нейрон-специфичная энолаза (NSE), ее повышение более 80-100 нг/мл свидетельствует о крайне неблагоприятном прогнозе. Повышенные уровни ферритина и лактат-дегидрогеназы отмечаются при распространенных стадиях заболевания и являются отрицательными факторами прогноза.
Схема определения степени распространения опухолевого процесса.
1. Место первичной опухоли - УЗИ, КТ, МРТ (наличие характерных кальцификатов).
2. Остеосцинтиграфия с Те99 и последующая Rg очагов гиперфиксации изотопа.
3. Сцинтиграфия с 123J метайодбензилгуанидином - препаратом, который захватывается клетками, продуцирующими КА.
4. Аспирационная биопсия костного мозга (из 4-8 мест) и трепанбиопсия.
5. Биопсия очагов, подозрительных на метастазы опухоли.
Международная система стадирования нейробластомы (Brodeur и соавт.1988)
СТАДИЯ I | Локализованная опухоль, ограниченная областью возникновения, полное удаление очага с или без микроскопически выявляемой резидуальной опухолью. Л/у не поражены. |
СТАДИЯ IIA | Односторонняя опухоль, удаленная нерадикально, л/у не поражены. |
СТАДИЯ IIIВ | Односторонняя опухоль, удаленная радикально или нерадикально с вовлечением в процесс л/у на стороне поражения. Контралатеральные л/у гистологически не поражены. |
СТАДИЯ III | Опухоль распространяется через среднюю линию (позвоночник) с или без вовлечения региональных л/у с обеих сторон. Или односторонняя опухоль с вовлечением контралатеральных л/у. Или срединно располагающаяся опухоль с двусторонним поражением л/у. |
СТАДИЯ IV | Диссеминированный процесс с метастазами в отдаленные л/у, кости, костный мозг, печень и /или другие органы (за исключением ситуаций, относящихся к IVS стадии) |
СТАДИЯ IVS* | Локализованная первичная опухоль (I или II стадия процесса) с наличием отдаленных метастазов в печень, кожу и / или костный мозг (не >10%). |
* Только для детей до 1 года
Гистология
Для НБЛ характерно образование псевдо-розеток, называемых розетками Homer-Wright, - структур, образованных по периферии ядрами нейробластов с расположенными по центру эозинофильными фибриллами. Характерно наличие кальцификатов. Необходимо проведение иммуногистохимического исследования.
Лечение
Протоколы лечения предусматривают использование ПХТ, ЛТ и операции. Для излечения больных с локализованными стадиями достаточно радикального удаления опухоли. При вовлечении регионарных л/у дополнительно используется ПХТ и облучение очага и вовлеченных узлов. Больные с нерезектабельной опухолью вначале получают предоперационную ПХТ, которая приводит к значительному уменьшению размеров опухоли, иногда даже до возможности ее радикального удаления. В случае неполного удаления показана ЛТ на ложе удаленной опухоли. В современных стандартных режимах ПХТ используются
препараты платины, эпиподофилотоксины (VP-16, VM-26), дакарбазин, адрибластин, циклофосфан, ифосфамид, винкристин. В лечении группы больных с крайне неблагоприятным прогнозом используется мегадозная химиотерапия (мелфалан, вепезид) с (или без) тотальным облучением тела и с аутологичной трансплантацией гемопоэтических стволовых клеток с последующей «дифференцирующей» терапией препаратами 13-цисретиноевой кислоты (роаккутан).
IVS стадия НБЛ встречается только у детей до 1 года. Несмотря на наличие отдаленных метастазов в кожу, печень и костный мозг (не более 10% опухолевых клеток) в этом возрасте очень часто наблюдаются спонтанные регрессии через несколько месяцев от момента диагноза. Первичная локализация чаще всего - надпочечник с малым размером опухоли.
Исход заболевания определяется главным образом стадией заболевания. Выживаемость больных с НБЛ в целом составляет около 50%, по стадиям: I стадия - 100%, II стадия - 94%, III стадия - 60%,
IV стадия - 10-20%, 4S ст - 75%.
Глава 6
Опухоли печени
Первичные опухоли печени занимают третье место по частоте среди абдоминальных опухолей у детей, 80% из них являются злокачественными.
ГЕПАТОБЛАСТОМА (ГБ)
Встречается в возрасте до 5 лет, закладывается в процессе эмбрионального развития. Это преимущественно унифокальная опухоль, часто инкапсулирована, имеет вид дольчатой массы, метастазирует чаще всего в легкие и ворота печени. Редко встречаются метастазы в кости.
ГЕПАТОЦЕЛЛЮЛЯРНАЯ КАРЦИНОМА (ГЦК)
Встречается у детей старше 10 лет и практически не отличается от гепатоцеллюлярного рака взрослых (но часто развивается в отсутствие цирроза печени), располагается мультицентрично, с широкой инвазией печени, также метастазирует в легкие, регионарные лимфоузлы и редко - в кости.
Факторы риска развития ГЦК: вирусные гепатиты В и С, хроническая форма наследственной тирозинемии, длительное использование андрогенных анаболических стероидов.
ХОЛАНГИОКАРЦИНОМА
Очень редко встречается у детей старшего возраста.
Редкие варианты злокачественных опухолей печени: эмбриональная (мезенхимальная) саркома печени, ангиосаркома, рабдомиосаркома, лейомиома, злокачественая тератома, первичная лимфома.
Клиническая картина
Увеличение живота, пальпируемая опухоль, анорексия, тошнота, рвота, лихорадка, бледность, редко - боли. При ГЦК в 25% случаев имеет место желтуха. Клинические симптомы нарастают в течение
1-2 месяцев. У 2% детей с ГБ выявляется преждевременное половое созревание (вследствие продукции опухолью гонадотропина).
Диагностика
Гистологическое исследование опухоли - проводится диагностическая лапаротомия или пункционная биопсия печени. Определение уровня опухолевых маркеров (α-фетопротеина и иногда - хорионического гонадотропина). Проводится в основном для диагностики и мониторинга лечения ГБ. КТ брюшной полости и легких входит в обязательный спектр обследования. Для уточнения характера распространения опухоли проводится ангиография. Дополнительную информацию может дать сцинтиграфия печени с различными изотопами (I131, Au198, Tc99m). В клиническом анализе крови могут выявляться нормохромная, нормоцитарная анемия, тромбоцитоз, полицитемия.
Лечение
Ключевым в лечении является радикальное удаление опухоли при сохранении функции оставшейся части органа. При ГБ дополнительно проводится интенсивная ПХТ (препараты платины, адрибластин), что значительно улучшает выживаемость. При неоперабельных опухолях показана трансплантация печени, используют также криохирургический метод, химиоэмболизацию. Как вспомогательный метод, иногда применяется и лучевая терапия.
Выживаемость при локализованной резектабельной ГБ составляет около 60%. При ГЦК прогноз оптимистичный только в случае радикального удаления локализованной опухоли.
Глава 7
Саркомы мягких тканей
Саркомы мягких тканей (СМТ) - группа злокачественных опухолей, имеющих общий источник - мезенхимальную ткань зародыша (мезодерму), из которой в дальнейшем развиваются мышечная и костная ткани, оболочки внутренних органов, сосудов, нервов и т.д. СМТ могут развиваться в любой части человеческого тела и любом органе - на конечностях, туловище, внутренних органах и т.д. У детей СМТ составляют 4-8% всех злокачественных опухолей.
Клиническая картина
Зависит от локализации опухоли, скорости роста и степени распространения. Общими признаками являются увеличение объема тканей и боль. У маленьких детей поражение орбиты может эмитировать этмоидит (периорбитальный отек, птоз), при опухоли носоглотки возникает обструкция верхних дыхательных путей, дисфагия, носовые кровотечения. При параменингеальных локализациях (опухоли полости носа, параназальных синусов, носоглотки, среднего уха) процесс может распространяться в заднюю черепную ямку и являться причиной парезов черепно-мозговых нервов, положительных менингеальных знаков и явлений компрессии головного мозга. Опухоли конечностей диагностируют при увеличении объема и появлении болей, что часто связывают с травмой и трактуют как гематомы. Урогенитальные локализации СМТ могут проявляться дизурией, гематурией Вагинальные и маточные локализации СМТ манифестируют кровянистыми выделениями из влагалища, часто их диагностируют поздно, когда опухоль в виде гроздевидной массы выбухает из влагалища.
Метастазируют СМТ как лимфогенно - в регионарные лимфатические узлы, так и гематогенно, преимущественно в легкие и кости.
Диагностика
Проводится биопсия опухоли с целью верификации диагноза (гистологическое и иммуногистохимическое исследования). Молекулярно-генетическое исследование выявляет специфические
изменения и несет информацию о прогнозе. КТ и МРТ с контрастированием необходимы для определения размеров опухоли, границ и отношения к окружающим тканям, состояния сосудов и определения подходов для возможного оперативного вмешательства. Rg и КТ легких необходимы для выявления возможных метастазов. С помощью остеосцинтиграфии выявляются метастазы в кости. При параменингеальных поражениях необходимо исследование ликвора.
Стадирование
Стадия (I-IV) определяется размерами первичной опухоли и степенью лимфогенного и гематогенного распространения по системе
TNM.
Лечение
Зависит от гистологического типа опухоли и стадии процесса. Ключевым моментом в лечении является локальный контроль: удаление опухоли в пределах здоровых тканей и облучение резидуальной опухоли при нерадикальной операции. СМТ по-разному чувствительны к химиотерапии. При высокой чувствительности опухоли проводится пред- и послеоперационная ПХТ препаратами: винкристин, ифосфамид, адрибластин, карбоплатин, этопозид. При необходимости производят повторную операцию после проведенной ПХТ для удаления резидуальной опухоли. При неудовлетворительных результатах и IV стадии заболевания используют мегадозную терапию с последующей аутологичной трансплантацией гемопоэтических периферических стволовых клеток или костного мозга.
У детей самая частая СМТ - это рабдомиосаркома (РМС). Опухоль имеет 2 возрастных пика - ранний (до 2 лет) и поздний - (15-19 лет), что отражает наличие двух биологических разновидностей РМС. Возникает в любой части организма, где есть поперечно-полосатая мускулатура. Мальчики болеют чаще, чем девочки - соотношение 1,7 : 1.
Прогностически выделяется три подгруппы.
1. Группа с хорошим прогнозом (ботриоидные и лейомиоматозные формы).
2. Промежуточная - все эмбриональные формы.
3. Группа с плохим прогнозом - альвеолярный тип. Выделяется три гистологических варианта РМС: эмбриональный
(наиболее благоприятный и более чувствительный к ХТ), альвеоляр-
ный и недифференцированный типы. Худший прогноз также имеют параменингеальные РМС. Эти опухоли трудно радикально удалить, с чем связана высокая частота местных рецидивов.
Принципы лечения изложены выше. РМС чаще обладает высокой чувствительностью к ПХТ. Дозы ЛТ зависят от степени радикальности удаления опухоли (32-45Гр).
Долговременная выживаемость больных с локализованными РМС благоприятного гистотипа составляет около 80%.
Глава 8
Ретинобластома
Ретинобластома (РБ) - это врожденная опухоль сетчатки глаза, однако редко диагностируется к моменту рождения ребенка. В 98% случаев РБ диагностируется до пяти лет. Пик диагностики заболевания - 2 года. Заболеваемость одинакова среди мальчиков и девочек. Возможен двусторонний характер поражения, его частота составляет около 25%. У 60% пациентов РБ имеет спорадический характер, причем в большинстве случаев - это односторонние опухоли, наследственные формы РБ чаще билатеральны. При молекулярно-генетическом исследовании выявляются четкие генетические изменения, определен ген РБ (RB1). Пациенты с РБ имеют существенный риск развития вторых опухолей, и в первую очередь, остеогенной саркомы.
Клиническая картина
Одним из первых симптомов опухоли является лейкокория (белый или розовый зрачковый рефлекс) или симптом «кошачьего глаза», который описывается родителями ребенка, как свечение зрачка. Этот симптом появляется тогда, когда опухоль уже достаточно большая. Косоглазие - второй по частоте симптом.
Диагностика
При подозрении на РБ офтальмологическое исследование обоих глаз должно быть произведено под наркозом. Диагноз ставится только клинически. Все внутриглазные процедуры, направленные на получение ткани для гистологического и цитологического исследования, представляют риск распространения опухолевого процесса и являются абсолютно противопоказанными. КТ - обязательный метод исследования, выявляющий характер распространения процесса (интра- и экстраокулярного). МРТ - исследование, дополняющее КТ в оценке поражения зрительного нерва и вовлечения головного мозга.
Дифференциальный диагноз
РБ должна быть отдифференцирована от заболеваний, также вызывающих отслойку сетчатки. Наиболее частыми из них являют-
ся сосудистые аномалии, называемые болезнью Коатса. Картину РБ может симулировать и инфекционное поражение - Toxicara canis. Экстраокулярные РБ следует дифференцировать с рабдомиосаркомами и метастазами нейробластомы. Поражение орбиты и самого глаза возможно при лейкемиях и лимфомах.
Лечение
Тактика лечения РБ зависит от размера и степени распространения опухоли. В настоящее время в лечении РБ используются: оперативный, лучевой и ПХТ методы. Правильное сочетание предложенных методов дает возможность получения хороших результатов. В настоящее время существует тенденция к максимально возможному консервативному лечению с целью сохранения зрения и глаза. Криотерапия и фотокоагуляция - методы локального лечения небольших опухолей. Показаниями к энуклеации являются массивный характер внутриглазного поражения, глаукома, отсутствие зрения и невозможность его восстановления. Для ПХТ используются винкристин, карбоплатин, этопозид. Число курсов (4-8) зависит от степени распространения опухоли. ЛТ в настоящее время имеет ограниченное применение и используется с целью сохранения зрения в случае множественных очагов поражения. Однако преимущества этого метода лечения должны быть взвешены и оценены в связи с неблагоприятными отдаленными последствиями ЛТ (асимметрия лица). Дозы ЛТ колеблются от 35 до 45 Гр.
Прогноз заболевания очень хороший. Выживаемость составляет 98%.
Глава 9
Герминогенные опухоли
Герминогенные опухоли (ГО) развиваются из популяции плюрипотентных зародышевых клеток (ЗК). В период развития эмбриона первоначальные ЗК мигрируют из энтодермы желточного мешка к генитальному гребню в ретроперитонеуме. Здесь из них развиваются половые железы. Если в период этой миграции по каким-то неустановленным причинам происходит нарушение нормального процесса миграции, ЗК могут задерживаться в любом месте своего следования, где в последующем может сформироваться опухоль. ЗК чаще всего могут быть обнаружены в таких областях, как забрюшинное пространство, средостение, пинеальная область (шишковидная железа) и крестцово-копчиковая область. Реже ЗК задерживаются в области влагалища, мочевого пузыря, печени, носоглотки.
ГО составляют 3-8% всех злокачественных опухолей детского возраста. Они могут быть как доброкачественными, так и злокачественными. Эти опухоли в два-три раза чаще встречаются среди девочек, чем мальчиков. Отмечено 2 пика частоты этих опухолей: у детей от 0 до 5 лет, и в период от 12 до 18лет.
Гистогенез
ГО очень часто связаны с различными генетическими аномалиями и нередко сочетаются с другими злокачественными опухолями. Недифференцированные примитивные ЗК, которые не подверглись дифференцировке, могут развиться в герминому (семинома в яичках, дизгерминома в яичниках). Процесс дифференцировки ЗК может идти по эмбриональной и экстраэмбриональной линиям. Дифференцировка по эмбриональной линии дает развитие тератом различной степени зрелости. Злокачественная экстраэмбриональная дифференцировка приводит к развитию хориокарцином и опухолей желточного мешка. Нередко ГО могут содержать клетки различных линий дифференцировки ЗК. Патоморфологическое заключение для герминогенных опухолей должно включать: органную принадлежность, гистологическую структуру, состояние капсулы опухоли (ее целостность), характеристики лимфатической и
сосудистой инвазии, распространение опухоли на окружающие ткани.
Опухолевые маркеры
α-фетопротеин и хориогонический гонадотропин являются маркерами ГО, особенно экстраэмбрионального происхождения. Определение их необходимо как для диагностики, так и при мониторинге лечения.
Клиническая картина
ГО чрезвычайно многообразна и в первую очередь определяется локализацией поражения. Самыми частыми локализациями ГО являются яичники (26%), копчик (27%), яички (18%), головной мозг (15%). Основной симптом - наличие опухоли. Гораздо реже эти опухоли диагностируются в забрюшинном пространстве, средостении, во влагалище, мочевом пузыре, желудке, печени, на шее (в носоглотке).
Диагностика
Начальное обследование выявляет локализацию первичной опухоли, степень распространения опухолевого процесса и наличие отдаленных метастазов.
Рентгенография органов грудной клетки, УЗИ брюшной полости и малого таза - первые необходимые диагностические исследования. Помимо рутинных методов диагностики, КТ органов грудной клетки и брюшной полости с контрастным усилением сегодня является самым информативным и необходимым методом диагностики.
Лечение
В настоящее время в основном используется 2 метода лечения: оперативный и химиотерапевтический. ГО высокочувствительны к ПХТ. В лечении используются препараты платины, ифосфамид, этопозид, блеомицин. Радикальное удаление опухоли улучшает прогноз. ЛТ имеет очень ограниченное применение.
Прогноз
ГО достаточно благоприятный. Долговременная выживаемость пациентов с первичными опухолями яичников составляет 85%, с опухолями крестцово-копчиковой области - 67%, с опухолями
яичек - 90%.
Условные сокращения
КТ - компьютерная томография МРТ - магнитно-резонансная томография Rg - рентгенография ЛУ - лимфатические узлы
Гр - Грей (единица измерения дозы лучевой терапии)
ЛТ - лучевая терапия
ХТ - химиотерапия
ПХТ - полихимиотерапия
ПЭТ - позитронно-эмиссионная томография
ОЛЛ - острый лимфобластный лейкоз