Наглядная детская гастроэнтерология и гепатология : учеб. пособ. - Кильдиярова Р. Р., Лобанов Ю. Ф. 2013. - 124 с. : ил.
|
|
|
|
Глава 4. Заболевания толстой и тонкой кишки
ФУНКЦИОНАЛЬНЫЕ ЗАБОЛЕВАНИЯ КИШЕЧНИКА
Синдром раздраженного кишечника
Коды по МКБ-10
K58. Синдром раздраженного кишечника. K58.0. Синдром раздраженного кишечника с диареей. K58.9. Синдром раздраженного кишечника без диареи. К59.0. Синдром раздраженного кишечника с запором.
Синдром раздраженного кишечника - комплекс функциональных нарушений работы кишечника, наиболее частыми симптомами которого являются нарушение акта дефекации, различные варианты абдоминального болевого синдрома при отсутствии воспалительных или иных органических изменений кишечной трубки.
Синдромом раздраженного кишечника (СРК) страдают от 14 до 48% людей во всем мире. Однако многие пациенты не обращаются за медицинской помощью, поэтому эти показатели можно считать заниженными. Женщины страдают СРК в 2 раза чаще, чем мужчины.
Среди детского населения в США признаки СРК имеют 6% младших и 14% старших школьников, в Италии - 13,9%, в Китае - 13,3% детей. Распространенность СРК у детей в России не уточнена.
Этиология и патогенез
СРК является биопсихосоциальным расстройством, т.е. в основе его развития лежит взаимодействие двух основных патологических механизмов: психосоциального воздействия и сенсорно-моторной дисфункции - нарушений висцеральной чувствительности и двигательной активности кишечника. В патогенезе СРК имеют значение следующие факторы:
• нарушение деятельности центральной и вегетативной нервной системы, приводящее к изменениям моторной функции кишки из-за повышенной чувствительности рецепторов стенки кишки к растяжению. Боли и диспепсические расстройства наблюдаются при более низком пороге возбудимости, чем у здоровых детей;
• недостаток балластных веществ (растительной клетчатки) в питании детей с утратой условного рефлекса на акт дефекации и асинергией мышечных структур тазовой диафрагмы, способствующий снижению эвакуаторной функции кишечника;
• вторичное развитие при хронических гастритах, ЯБ, панкреатитах и др.;
• перенесенные ранее острые кишечные инфекции с развитием кишечного дисбиоза.
Классификация
Согласно Бристольской шкале формы кала у детей старшего возраста и взрослых выделяют 7 типов фекалий (рис. 4-1). Шкалу разработал английский исследователь Х. Мейерс в 1997 г.
Тип стула зависит от времени пребывания его в толстой и прямой кишке. Типы стула 1 и 2 характерны для запора, типы 3 и 4 считаются идеальным стулом (особенно тип 4, так как он легче проходит через прямую кишку в процессе дефекации), типы 5-7 характерны для диареи, особенно последний.
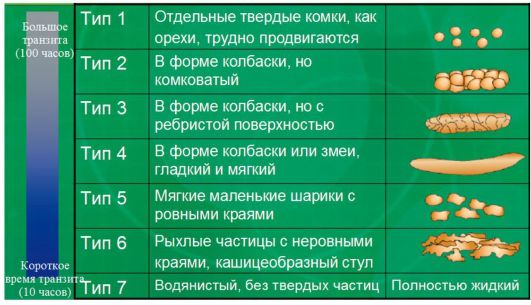
Рис. 4-1. Бристольская шкала формы кала
Предложена следующая классификация СРК (IBS) по преобладающей форме стула:
• СРК с преобладанием запора (IBS-C);
• СРК с преобладанием диареи (IBS-D);
• смешанный СРК (IBS-М);
• неклассифицируемый СРК.
Дефекация у пациентов часто изменяется с течением времени (запор сменяется диареей и наоборот), поэтому предложен термин «перемежающийся СРК» (IBS-A). В настоящее время выделяют постинфекционный СРК (PI-IBS), развившийся после перенесенных острых кишечных инфекций, при котором обнаруживают маркеры инфекций в биоматериалах, полученных от больного, имеется нарушение микрофлоры в кишечнике. Положительный эффект дает лечение антисептиками и пробиотиками. Данный факт крайне важен в педиатрической практике в связи с высокой удельной частотой кишечных инфекций у детей.
Клиническая картина
Диагностическими критериями СРК являются следующие.
Рецидивирующая боль в животе или дискомфорт по крайней мере 3 дня в месяц за последние 3 мес, связанные с двумя или более из следующих ниже признаков:
• улучшением после дефекации;
• началом, связанным с изменением частоты стула;
• началом, связанным с изменением формы стула. Дополнительные симптомы:
• патологическая частота стула (менее 3 раз в неделю или более 3 раз в сутки);
• патологическая форма стула (комковатый/твердый или жидкий/водянистый);
• натуживание при дефекации;
• императивный позыв или чувство неполного опорожнения, выделение слизи и вздутие.

Клиническими признаками СРК также являются изменчивость и многообразие жалоб, отсутствие прогрессирования, нормальные масса тела и общий вид ребенка, усиление
симптомов при стрессе, отсутствие их ночью, связь с другими функциональными расстройствами.
У подростков и юношей могут быть внекишечные симптомы: раннее насыщение, тошнота, чувство переполнения в подложечной области после приема небольшого количества пищи, чувство комка в горле, похолодание конечностей, быстрая утомляемость, плохой сон или сонливость в дневное время, головная боль, дизурические явления. У девочек отмечаются боли в пояснице, дисменорея и др. Эти проявления усугубляют течение СРК и во многом обусловлены психологическими факторами.
Диагностика
Первичные обязательные исследования: общеклинические, печеночные пробы, бактериологический посев кала, анализ кала на скрытую кровь, ректороманоскопия, ультрасонография внутренних органов, эзофагогастродуоденоскопия. В ходе исследований необходимо исключить органическую патологию.
Дифференциальная диагностика
СРК необходимо дифференцировать от хронических воспалительных заболеваний кишечника, инфекционных и паразитарных заболеваний кишечника, синдрома избыточного бактериального роста (СИБР), опухолей и дивертикулов кишечника, ишемического колита, хронического панкреатита.
Эндокринные заболевания, такие как тиреотоксикоз и сахарный диабет с автономной диабетической энтеропатией, могут протекать по типу диарейной формы СРК.
Лечение
Лечение комплексное, с повышением физической активности, психотерапевтическим воздействием.
Назначение миотропных спазмолитиков для лечения СРК является более результативным, чем применение анальгетических препаратов, которые притупляют боль, но не устраняют ее причину. По механизму действия различают нейрои миотропные спазмолитические средства (табл. 4-1).
Таблица 4-1. Классификация спазмолитиков по механизму действия
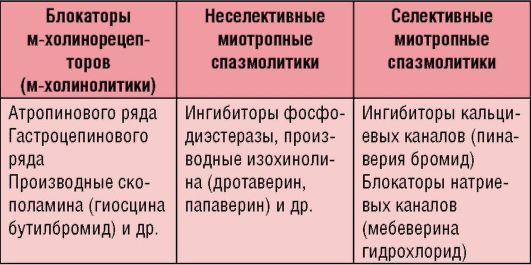
Из миотропных спазмолитиков детям в возрасте от 6 мес до 2 лет назначают внутрь папаверин по 5 мг, 3-4 лет - 5-10 мг, 5-6 лет - 10 мг, 7-9 лет - 10-15 мг, 10-14 лет - 15-20 мг 2 раза в сутки; дротаверин (но-шпа*, спазмол*) детям в возрасте 3-6 лет - по 40-120 мг в 2-3 приема, максимальная суточная доза - 120 мг; 6-18 лет - 80-200 мг в 2-5 приемов, суточная доза - 240 мг. Пинаверия бромид (дицетел*) рекомендуют по 50 мг 3 раза в сутки или по 100 мг 2 раза в сутки детям подросткового возраста. Таблетки не разжевывают, не следует их принимать перед сном.

Блокатор м-холинорецепторов - гиосцина бутилбромид (бускопан*) в суппозиториях и таблетках по 10 мг применяют с 6-летнего возраста по 1-2 таблетки (или по 1-2 ректальных суппозитория) по 10-20 мг 3 раза в сутки. Устраняет спазм, не изменяя нормальную перистальтику кишечника, мебеверин (дюспаталин*, спарекс*) в таблетках по 135 мг и в капсулах ретард по 200 мг, который назначают с 6 лет в дозе 2,5 мг/кг в 2 приема за 20 мин до еды. По достижении эффекта дозу постепенно снижают в течение нескольких недель.
Замедление моторики кишечника можно достичь назначением адсорбентов, например, таких как смектит диоктаэдрический (смекта*, неосмектин*), в то время как применение лоперамида (имодиума*) оправданно только при тяжелой, некупируемой диарее и должно хорошо контролироваться. Лоперамид (имодиум*) в виде таблеток для рассасывания по 2 мг у детей с 2 до 5 лет применяют по 1 мг 3 раза в сутки, 6-8 лет - по 2 мг 2 раза в сутки, 9-12 лет - по 2 мг 3 раза в сутки; курс - 1-3 дня. В состав имодиума плюс* добавлен симетикон.

Антибиотики в лечении диареи не показаны.
При преобладании запора применяют лактулозу (дюфалак*), назначение других слабительных средств не всегда оправданно. Пре- и пробиотики рекомендуют при постинфекционном СРК. Пробиотик с антидиарейным и антитоксическим действиями энтерол* назначают в дозе 250 мг 1 раз в сутки, детям перед употреблением 1 капсулу разводят в 100 мл теплой воды.
При стрессовых ситуациях показаны нейротропные препараты анксиолитического действия с седативным эффектом: феназепам*, сибазон*, нозепам*, лоразепам* и другие, дозу подбирают индивидуально, для подростков РД составляет 0,25-0,3 1-3 раза в сутки. При выраженных симптомах психологической дезадаптации используют амитриптилин и другие антидепрессанты.
У детей чаще используют фитопрепараты - боярышника плодов + бузины черной цветков экстракт + валерианы корневищ с корнями (ново-пассит*). Его назначают с 12 лет по 5-10 мл или по 1 таблетке 3 раза в сутки. Валерианы корневищ с корнями + мелиссы лекарственной травы экстракт + мяту перечную (персен*, персен форте*) детям 3-12 лет назначают по 1 таблетке 1-3 раза в сутки, детям старше 12 лет - по 1 таблетке 3 раза в сутки.
При метеоризме рекомендуют препараты, уменьшающие газообразование в кишечнике, которые ослабляют поверхностное натяжение пузырьков газа, приводят к их разрыву и предотвращают тем самым растяжение кишечной стенки. Могут использоваться симетикон (эспумизан*) и комбинированные препараты: панкреофлат* (фермент + симетикон), юниэнзим* (фермент + сорбент + симетикон), с 12-14 лет - метеоспазмил* (спазмолитик + симетикон).
Панкреофлат* детям старшего возраста назначают по 2-4 таблетки с каждым приемом пищи. Для детей младшего возраста дозу подбирают индивидуально.
При затяжном течении СРК показаны метаболиты и витамины, витаминоподобные средства: тиоктовая кислота (липоевая кислота*, липамид*), α-токоферол*, флавоноид (троксерутин*); препараты кальция и магния: кальций-Э3 Никомед*, кальцевит*, кальций-сандоз форте*, магне В6*, магния оротат (магнерот*).
Если на протяжении 4-6 нед на фоне терапии состояние не нормализуется, проводят дифференциальную диагностику с другими заболеваниями для уточнения характера поражения ЖКТ.
Физиотерапевтическое лечение показано детям с абдоминальными болями в сочетании с диареей. Назначают легкое тепло в виде согревающих компрессов: водных, полуспиртовых, масляных, электрофорез с новокаином, хлористым кальцием, сернокислым цинком; эффективны лечебные грязи. Рекомендуют хвойные, радоновые ванны. По мере стихания болей могут быть использованы импульсные токи Бернара, массаж живота для повышения тонуса мышц передней брюшной стенки. При запоре предпочтение отдается методикам, направленным на нормализацию моторноэвакуаторной функции кишечника, устранение спазма.
Санаторно-курортное лечение осуществляется как в местных, так и в бальнеологических условиях. Наряду с комплексом физиотерапевтических методов большое значение имеет прием минеральных вод. При диарее показаны слабомине-
рализированные воды (1,5-2,0 г/л) типа «Смирновская», «Славяновская», «Ессентуки № 4» из расчета 3 мл/кг массы тела, при запоре - «Ессентуки № 17», «Баталинская» из расчета 3-5 мл на 1 кг массы тела.
Профилактика
Пациентам с СРК необходимо нормализовать режим дня, избегать длительного психического перенапряжения. Важно поддерживать адекватный уровень двигательной активности, привычный режим питания в любых условиях.
Прогноз
Прогноз заболевания благоприятный. Течение болезни хроническое, рецидивирующее, но не прогрессирующее. Лечение оказывается эффективным у 30% пациентов, стойкая ремиссия наблюдается в 10% случаев. Риск развития воспалительных заболеваний кишечника и колоректального рака в этой группе больных такой же, как и в общей популяции.
Функциональные нарушения кишечника
Коды по МКБ-10
K59.0. Функциональная диарея.
K59.1. Функциональный запор.
R15. Недержание кала (функциональный энкопрез).
P78.8. Другие уточненные расстройства системы пищеварения
в перинатальном периоде.
Заболевания данной группы достаточно близки к СРК, однако кардинальным отличием является отсутствие связи болевого синдрома с нарушениями стула.
Функциональными нарушениями кишечника страдают 30-33% детей. Функциональный запор составляет 95% в структуре всех видов запора у детей.

Классификация
Младенческая колика (кишечная колика) характеризуется плачем и беспокойством ребенка в течение 3 ч в сутки и более, не менее 3 дней в неделю на протяжении не менее 1-й недели.
Младенческая дисшизия - затруднение акта дефекации ввиду отсутствия синхронизации работы мышц тазового дна и моторики кишечника.
Функциональная диарея - диарея, не связанная с какимлибо органическим поражением органов пищеварения и не сопровождаемая болевым синдромом.
Функциональный запор (от лат. constipatio, obstipacia - «скопление») - нарушение моторной функции толстой кишки в виде задержки опорожнения на 36 ч и более, затруднение акта дефекации, чувство неполного опорожнения, отхождение малого количества кала повышенной плотности. Частный случай запора (функциональная задержка стула) характеризуется нерегулярной дефекацией при отсутствии перечисленных выше критериев запора. Возможные варианты запора представлены в табл. 4-2.
Таблица 4-2. Классификация запора у детей (Хавкин А.И., 2000)
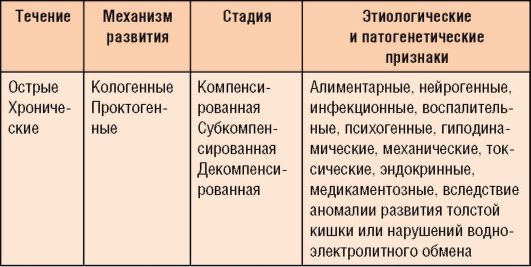
Запор функционального происхождения:
• дискинезии с преобладанием атонии (гипомоторные) или спазма (гипермоторные);
• психогенные;
• условно-рефлекторные;
• при пилороспазме;
• эндокринные (нарушения функций гипофиза, надпочечников, щитовидной и паращитовидной желез).

Функциональный энкопрез - недержание кала, возникающее вследствие психического стресса (испуга, страха, влияния постоянно угнетающих психику впечатлений), систематического подавления позывов на дефекацию, перенесенных в раннем возрасте острых кишечных инфекций или перинатального поражения ЦНС.
Этиология и патогенез
При функциональных расстройствах кишечника, так же как и при других функциональных нарушениях, выделяют три уровня формирования нарушений стула: органный, нервный и психический. Симптомы могут формироваться на любом уровне. Также причины этих расстройств связаны с нарушением нервной или гуморальной регуляции моторики ЖКТ.
В раннем детском возрасте нарушения кишечной моторики могут быть связаны с дисбиотическими нарушениями и частичной недостаточностью ферментов, прежде всего лактазы. Лактазная недостаточность (ЛН) приводит к тому, что гидролиз лактозы осуществляется микрофлорой кишечника, в котором скапливаются осмотически активные вещества и газы, приводящие к метеоризму, коликам, нарушениям стула.
В основе запоров лежат расстройства моторной, всасывательной, секреторной и экскреторной функций толстой
кишки без структурных изменений стенки кишечника
(рис. 4-2).
Гипермоторный (спастический) запор развивается в результате инфекционных заболеваний или психогенных перегрузок, при неврозах, рефлекторных влияниях со стороны других органов, при патологических состояниях, пре-
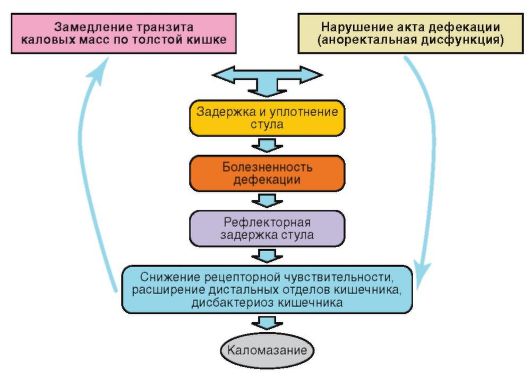
Рис. 4-2. Патогенез функционального запора
пятствующих расслаблению сфинктеров заднего прохода, употреблении пищи, богатой целлюлозой.
Гипомоторный (атонический) запор развивается на фоне рахита, гипотрофии, эндокринной патологии (гипотиреоза), при миатоническом синдроме, а также на фоне малоподвижного образа жизни.
Клиническая картина
Симптоматика при функциональных нарушениях кишечника многообразна, но жалобы должны наблюдаться на протяжении длительного периода времени - 12 мес и более (не обязательно непрерывно!) на протяжении последнего года.
Клиническая картина младенческих кишечных колик у детей:
• дебют плача и беспокойства в возрасте 3-4 нед жизни;
• ежедневный плач в одно и то же время (вечером и ночью - при грудном вскармливании, в течение всего дня и утром - при искусственном);
• длительность кишечных колик составляет 30 мин и более;
• при осмотре - гиперемия лица, ребенок сучит ножками;
• облегчение состояния ребенка отмечается после дефекации или отхождения газов.

Начало младенческой дисшизии - первый месяц жизни. Перед дефекацией ребенок тужится в течение нескольких минут, кричит, плачет, но мягкий стул появляется не ранее чем через 10-15 мин.
У ряда детей различного возраста периодически отмечается диарея без признаков инфекции, без болей (нельзя диагностировать СРК), и при обследовании не удается диагностировать какое-либо заболевание с синдромом мальабсорбции. Такая диарея называется функциональной.
У детей раннего возраста признаком функциональной диареи считается объем стула более 15 г на 1 кг массы тела в сутки. К 3 годам объем стула приближается к таковому у подростков, и диареей считается объем стула, превышающий 200 г/сут. У детей старшего возраста функциональный характер диареи подтверждается не увеличением объема стула, а изменением его характера - жидкого или кашицеобразного, с частотой более 2 раз в день, который может сопровождаться усиленным газообразованием, а позывы на дефекацию нередко носят императивный характер. Хронической считается диарея, продолжающаяся более 3 нед.
Среди функциональных запоров клинически различают гипертонические (спастические) и гипотонические.
При спастическом запоре тонус определенного участка кишки повышен, и каловые массы не могут пройти через это место. Внешне это проявляется в виде очень плотного, «овечьего» кала. При атоническом запоре задержка дефекации достигает 5-7 дней, после которой выделяется неплотный кал большого объема.
Функциональный энкопрез и неврологические, психические нарушения тесно взаимосвязаны.
Диагностика
План исследования включает следующие методы:
• клинический анализ крови и мочи;
• серию копрограмм, анализ кала на яйца глистов и цисты лямблий;
• анализ кала на микрофлору;
• углеводы кала;
• УЗИ внутренних органов, включая органы мочевыводящей системы;
• нейросонографию;
• ректальное исследование;
• рентгенологическое исследование (ирригоскопия, колопроктография, ректороманоскопия, колоноскопия);
• гистологическое исследование;
• неврологическое исследование.
Дифференциальная диагностика
Комплекс исследований у детей, при котором не выявляются изменения, позволяет исключить органическую патологию. У младенцев важно исключить лактазную и другие виды ферментативной недостаточности, гастроинтестинальную аллергию.
С помощью колоноскопии можно дифференцировать воспалительные и ишемические изменения кишечника, эрозии и язвы, полипы, дивертикулы, трещины, геморроидальные узлы и т.д.; с помощью гистологического исследования биоптатов кишечника - аганглиоз, гипоганглиоз, дистрофические изменения. Тщательное неврологическое исследование позволяет выявить нарушение сегментарной иннервации, вегетативной регуляции, в раннем детстве - наличие перинатального поражения ЦНС.
Лечение
Терапию младенцев с функциональными расстройствами кишечника проводят с учетом принципа «не навреди!»: чем меньше вмешательств, тем лучше (рис. 4-3).
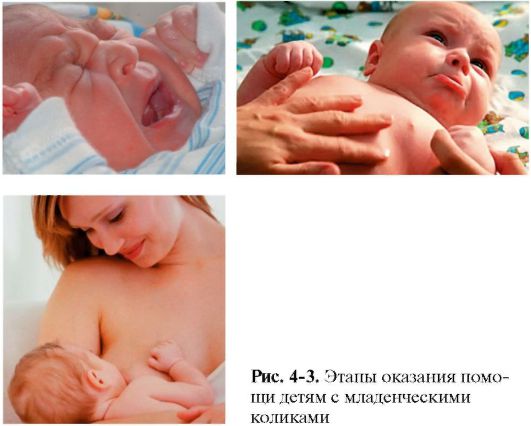
Лечение младенческих колик должно быть:
• индивидуальным;
• направленным на ликвидацию первопричины;
• направленным на коррекцию моторных и функциональных нарушений.
Прежде всего, необходимо создать спокойную обстановку в доме, успокоить родителей, внушив им, что кишечные колики встречаются у большинства младенцев и не представляют угрозы для их жизни и в ближайшее время должны пройти. Рекомендуют длительное ношение ребенка на руках, прижав к животу матери или отца, или положение на животе с согнутыми в коленях ножками (можно на теплой пеленке, грелке), проведение курса общего массажа, массажа живота. Во время и после кормления рекомендуют держать ребенка в полувертикальном положении для устранения аэрофагии. Показаны теплые ванны с отварами трав ромашки, мяты перечной, шалфея, душицы, обладающих спазмолитическим действием.

Применение газоотводных трубочек способствует отхождению газов и купированию боли, особенно оно эффективно при младенческих дисшизиях.
Фармакотерапию младенцев с кишечными коликами используют в последнюю очередь.
Препарат, который разрушает оболочку кишечных газов и облегчает их отхождение, - эмульсия симетикона (эспумизан*, саб симплекс* и др.), РД - 1 мерная ложка 3-5 раз в сутки, можно добавлять в детское питание или питье.
Фитопрепараты с отварами плодов фенхеля обыкновенного, укропа способствуют устранению симптомов метеоризма. Спазмолитики для устранения болей назначают внутрь по 0,5-1,0 мл 2% раствора папаверина гидрохлорида или 2% раствора но-шпы* в 10-15 мл кипяченой воды.

Сорбенты используют при кишечных коликах в сочетании с повышенным газообразованием; пробиотики, не содержащие лактозы и белок коровьего молока, - для коррекции нарушений кишечного микробиоценоза.
Терапия детей более старшего возраста всегда носит комплексный характер. В связи с тем, что в основе функциональных нарушений ЖКТ лежит срыв нервной регуляции органов пищеварения, ее осуществляют в тесной связи с невропатологами.

При функциональной диарее назначают адсорбенты (смекту*), лоперамид (имодиум*) - только при тяжелой, некупируемой диарее.
При метеоризме показан симетикон и комбинированные препараты: панкреофлат*, юниэнзим с МПС*, с 12 лет - метеоспазмил*.
Нормализация микрофлоры кишечника является важной составляющей терапии функциональных заболеваний кишечника (см. «Синдром избыточного бактериального роста»).
В связи с вторичным нарушением процессов переваривания и всасывания может потребоваться включение в состав терапии препаратов панкреатических ферментов (креон 10 000*, панцитрат*, мезим форте*, панзинорм*, панкреатин и др.). Преимущества применения у детей микросферических панкреатических ферментов представлены на рис. 4-4. Помещение
микросфер в рН-чувствительные капсулы защищает их от преждевременной активации в ротовой полости и в пищеводе, где так же как и в ДПК имеет место щелочная среда.
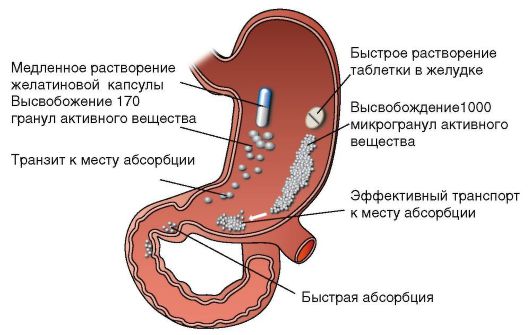
Рис. 4-4. Механизм действия микросферических панкреатических ферментов
Необходимые условия для лечения запора:
• выработать привычку регулярно посещать туалет;
• пользоваться горшком после завтрака;
• поощрять продуктивное посещение туалета;
• не наказывать и не стыдить ребенка.
Показаны ежедневная физическая нагрузка с достаточным пребыванием на свежем воздухе, рациональное питание.
Медикаментозная терапия включает применение слабительных средств, регуляторов моторики ЖКТ, а также пре- и пробиотиков.
Слабительные средства по механизму действия делятся:
• на средства, увеличивающие объем кишечного содержимого (отруби, семена, синтетические вещества);
• вещества, размягчающие каловые массы (жидкий парафин);
• осмотические средства;
• ди- и полисахариды (пребиотики);
• раздражающие или контактные слабительные средства.
В качестве эффективного и безопасного осмотического слабительного средства широко используют препараты лактулозы (дюфалак*, нормазе*, гудлак*), которые обладают пребиотическим действием.
Дюфалак* в виде сиропа выпускается во флаконах по 200, 500 и 1000 мл. Его слабительный эффект обусловлен увеличением объема содержимого толстой кишки примерно на 30% в связи с ростом численности микроорганизмов. Дозу препарата подбирают индивидуально, начиная с 5 мл 1 раз в день. При отсутствии эффекта дозу постепенно увеличивают (на 5 мл каждые 3-4 дня), условно максимальной дозой считают: у детей до 5 лет - 30 мл/сут, у детей 6-12 лет - 40-50 мл/сут, у детей старше 12 лет и подростков - 60 мл/сут. Кратность приема может составлять 1-2, реже 3 раза в день.
Курс лактулозы назначают на 1-2 мес, а при необходимости - и на более длительный срок, отменяют постепенно под контролем частоты и консистенции стула.
К препаратам, вызывающим химическое раздражение рецепторов слизистой оболочки толстой кишки, относится слабительное с мягким действием - бисакодил (дульколакс*). Детям 6-12 лет назначают по 1 таблетке (5 мг) на прием на ночь или за 30 мин до еды, старше 12 лет - по 1-2 таблетке или в виде ректальных суппозиториев (10 мг),
детям в возрасте 6-10 лет - по 1/2 суппозитория, который делят пополам вдоль, старше 10 лет - по 1 суппозиторию.
Натрия пикосульфат (гутталакс*) назначают при атоническом запоре с 4 лет. Для детей от 4 до 10 лет начальная доза - 5-8 капель, в среднем 6-12 капель, старше 10 лет начальная доза - 10 капель, в среднем - 12-24 капли, при тяжелом и стойком запоре - до 30 капель перед сном. Курс лечения - 2-3 нед.
Препарат микролакс* для ректального применения в виде одноразовых тюбиков с полужестким аппликатором по 5 мл используют для проведения микроклизмы. В старшем возрасте аппликатор вводят в прямую кишку на всю длину, детям до 3 лет - наполовину длины. Препарат действует через 5-15 мин, системные побочные эффекты отсутствуют.
При гипермоторном запоре показаны успокаивающие процедуры (теплые ванны, теплый душ, грелка), спазмолитические препараты: папаверин, дротаверин; мебеверин (дюспаталин* - с 6 лет), холинолитический спазмолитик гиосцина бутилбромид (бускопан* - с 6 лет). Рекомендуют слабоминерализованные щелочные минеральные воды («Ессентуки № 4», «Славяновская», «Смирновская», «ВарзиЯтчи» и др.) в негазированном, теплом виде.

При гипомоторном запоре назначают «тренирующие» термоконтрастные клизмы, стимуляцию перистальтики кишечника: электрофорез кальция, антихолинэстеразные препараты (прозерин*, убретид*), амплипульс-терапию, электростимуляцию толстой кишки, рефлексотерапию; газированные воды высокой минерализации: «Ессентуки № 17», «Увинская», «Металлург» в холодном виде назначают 2-3 раза в сутки за 40 мин до еды из расчета 3-5 мл на 1 кг массы тела на прием. Показаны витамины В1 и В6, ноотропы, прокинетики (координакс*, тримедат*).
В качестве вспомогательных средств можно использовать механическую стимуляцию дефекации: газоотводную трубку, глицериновые свечи, массаж кожи вокруг ануса, массаж общий и живота.
Только при недостаточной эффективности этих мер, а также при наличии симптомов каловой интоксикации применяют очистительные клизмы, считающиеся средством скорой помощи.
Профилактика
Больным необходимо соблюдать принципы здорового образа жизни, нормализовать режим дня, избегать стрессов. Важно заниматься физической культурой.
Недопустимы прием лекарственных препаратов, вызывающих дисбиотические нарушения, замедление или ускорение моторной функции (антибиотиков, НПВС, транквилизаторов и др.), перегрузка аудиовизуальной информацией. Имеет значение создание в семье спокойной и доброжелательной обстановки.
Сохранение естественного вскармливания, соблюдение принципов рационального, а лучше функционального питания - главные составляющие профилактики функциональных нарушений кишечника.
Прогноз
Прогноз благоприятный.
СИНДРОМ МАЛЬАБСОРБЦИИ
Коды по МКБ-10
K90. крушение всaсывaния в кишечнике. K90.4. Нарушения всасывания, обусловленные непереносимостью, не классифицированные в других рубриках. K90.8. Другие нарушения всасывания в кишечнике. K90.9. Нарушение всасывания в кишечнике неуточненное. Синдром мальабсорбции - клинический симптомокомплекс, возникающий вследствие нарушения пищеварительнотранспортной функции тонкой кишки, что приводит к метаболическим расстройствам.

Этиология и патогенез
Синдром мальабсорбции может быть:
• врожденным (при целиакии, муковисцидозе);
• приобретенным (при ротавирусных энтеритах, болезни Уиппла, кишечной лимфангиэктазии, тропической спру, синдроме короткой кишки, болезни Крона, злокачественных опухолях тонкой кишки, хроническом панкреатите, циррозе печени и т.д.).
Многообразие этиопатогенетических механизмов нарушений всасывания и переваривания пищи с присущими им заболеваниями представлено на рис. 4-5.
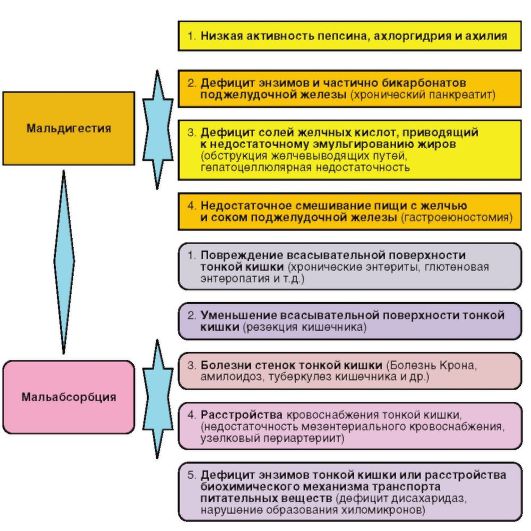
Рис. 4-5. Этиология и патогенез синдрома мальабсорбции
Клиническая картина
Ведущим клиническим симптомом является нарушение дефекации в виде частого жидкого или кашицеобразного стула более 2-3 раз в сутки, а также полифекалия без приме-
си крови и тенезмов. На поверхности каловых масс - жир, каловые массы имеют неприятный запах. Характерно скопление газов в желудке и кишечнике, сопровождаемое вздутием живота (метеоризмом).
Нарушаются переваривание и всасывание белков. Непереваренный белок подвергается гниению под воздействием микрофлоры кишечника, развиваются гнилостная диспепсия, метеоризм. Испражнения имеют неприятный, гнилостный запах, выявляются непереваренные мышечные волокна (креаторея).
В результате нарушения всасывания углеводов при дефиците лактазы лактоза подвергается бактериальному расщеплению в толстой кишке с образованием органических кислот с низкой молекулярной массой (молочной и уксусной кислотой), возбуждающих кишечную моторику и придающих испражнениям кислую реакцию. Каловые массы жидкие, пенистые, с низким рН (бродильная диспепсия).
Выражены общие симптомы: похудение, сухость кожи, мышечная гипотрофия, выпадение волос, ломкость ногтей.

Диагностика
Лабораторно-инструментальные исследования, подтверждающие синдром мальабсорбции, позволяют выявить следующие изменения:
' общий анализ крови - признаки анемии;
• биохимическое исследование крови - снижение содержания общего белка, альбумина, железа, кальция, натрия, хлоридов, глюкозы;
• проба на толерантность к глюкозе - плоскую сахарную кривую, йодокалиевая проба - уменьшение всасывательной функции тонкой кишки;
• копрограмма - стеаторею, креаторею, амилорею, снижение рН кала;
• снижение содержания углеводов в кале;
• УЗИ печени, поджелудочной железы, желчного пузыря и желчевыводящих путей - изменение размеров и структуры паренхимы печени и поджелудочной железы, наличие конкрементов в желчном пузыре, изменение стенок желчного пузыря, нарушение его сократительной способности;
• рентгенологическое исследование тонкой кишки - неравномерный просвет тонкой кишки, беспорядочное утолщение поперечных складок, сегментацию контрастного вещества, ускоренный его пассаж;
• аспирационная биопсия тонкой кишки - атрофию ворсинок, снижение активности лактазы и других ферментов в биоптате.
Лактазная недостаточность
Коды по МКБ-10
Е73.0. Врожденная недостаточность лактазы взрослых (тип с
замедленным началом).
Е73.1. Вторичная недостаточность лактазы.
Лактазная недостаточность (ЛН) - врожденное или приобретенное состояние, характеризуемое снижением активности фермента лактазы в тонкой кишке, протекающее скрыто или манифестно.
ЛН - широко распространенное состояние (рис. 4-6). Наибольшую значимость проблема имеет для детей раннего возраста, так как на первом году жизни грудное молоко и молочные смеси являются основным продуктом питания. Благодаря лактозе обеспечивается около 40% энергетических потребностей ребенка.
Распространенность ЛН в разных регионах мира различна: если в европейских странах она наблюдается у 3-42% населения, то у афроамериканцев и индейцев США, аборигенов Австралии, китайцев и жителей Юго-Восточной Азии - у 80-100% населения. В России ЛН встречается у 16-18% населения (см. рис. 4-6). Непереносимость лактозы увеличивается с возрастом. К примеру, китайцы и японцы на 80-90% теряют способность переваривать лактозу к 3-4 годам. С другой стороны, многие японцы способны переваривать до 200 мл молока без симптомов ЛН.
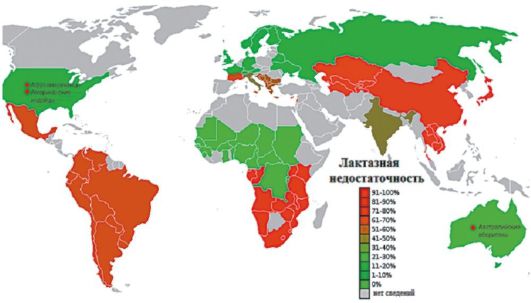
Рис. 4-6. Карта распространенности ЛН
Этиология и патогенез
Лактоза - дисахарид, состоящий из P-D-галактозы и β-Dглюкозы. Расщепление лактозы на моносахариды происходит в пристеночном слое тонкой кишки под действием фермента лактазофлоризингидролазы (лактазы) на глюкозу и галактозу (рис. 4-7, а). Глюкоза - важнейший источник энергии; галактоза же становится составной частью галактолипидов, необходимых для развития ЦНС.
Возникновение первичной врожденной мальабсорбции лактозы (алактазии новорожденных) и первичной врожденной мальабсорбции лактозы с поздним началом (у взрослых) связано с генетически детерминированным нарушением синтеза лактозы. Лактаза кодируется единственным геном, локализованным на хромосоме 2.
Лактазу впервые обнаруживают на 10-12-й неделе гестации, с 24-й недели начинается рост ее активности, который достигает максимума к моменту рождения, особенно в последние недели гестации (рис. 4-7, б). Перечисленные факторы обусловливают ЛН у недоношенных и незрелых детей к моменту рождения.
Выраженное падение активности лактазы происходит к 3-5 годам жизни. Эти закономерности лежат в основе ЛН
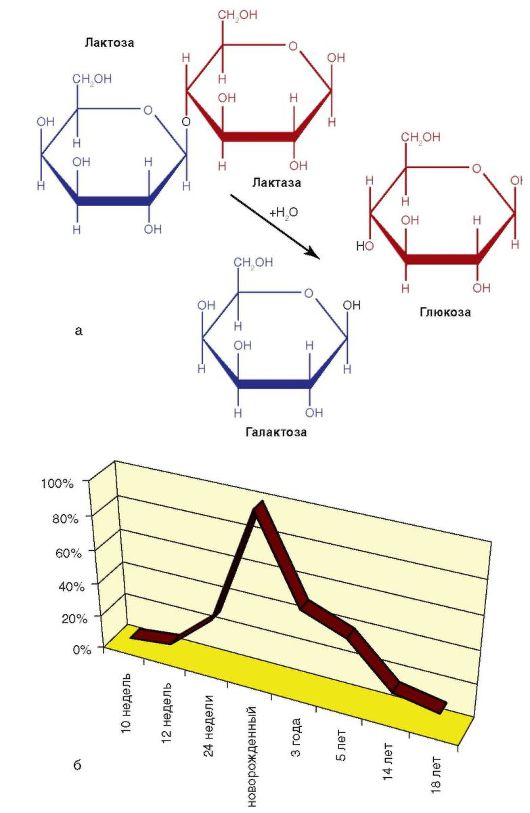
Рис. 4-7. Свойства и активность ферментов лактазы и лактозы: а - формула гидролиза лактозы на галактозу и глюкозу; б - активность лактазы во внутри- и внеутробной жизни ребенка
взрослого типа (конституциональной ЛН), причем темпы снижения активности фермента генетически обусловлены и в большой степени определяются этнической принадлежностью больного.
У большинства кормящих женщин состав молока, выделяющегося в начале и в конце кормления, разный. Переднее молоко богато лактозой, хотя количество лактозы не зависит от рациона матери. Это молоко «набегает» особенно между кормлениями, когда молочные железы не стимулируются сосанием ребенка. Затем, по мере сосания, начинает вытекать более калорийное, жирное, богатое белком заднее молоко, которое поступает из желудка в кишечник ребенка медленнее, и поэтому лактоза успевает переработаться. Более легкое низкокалорийное переднее молоко быстро движется, и часть лактозы может поступить в толстую кишку, не успев подвергнуться расщеплению ферментом лактазой.
Если активность лактазы недостаточна для переваривания всей поступившей в тонкую, а далее толстую кишку лактозы, она становится питательным субстратом для микроорганизмов, которые ферментируют ее до короткоцепочечных жирных кислот, молочной кислоты, углекислого газа, метана,
водорода и воды. Продукты ферментации лактозы - короткоцепочечные жирные кислоты - создают кислую среду, способствующую питанию бифидобактерий. Избыточное поступление лактозы в толстую кишку приводит к количественному и качественному изменению состава микрофлоры и повышению осмотического давления в просвете толстой кишки с развитием клинических проявлений ЛН.
Классификация
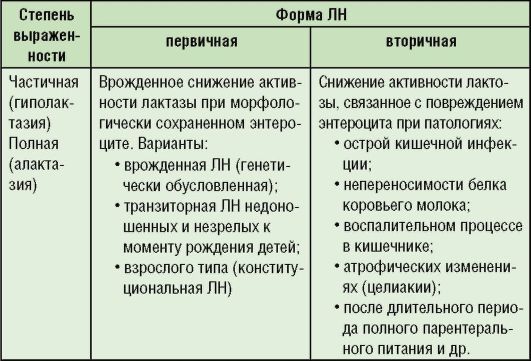
Различают первичную и вторичную формы ЛН (табл. 4-3). Перегрузка лактозой у младенцев на естественном вскармливании - состояние, подобное вторичной ЛН, возникающее при нарушениях режима кормления, кормлении из обеих молочных желез в одно кормление, когда ребенок получает только переднее молоко.
Таблица 4-3. Классификация ЛН
Клиническая картина
Основные проявления ЛН следующие:
• осмотическая (бродильная) диарея после приема молока или содержащих лактозу молочных продуктов (частый, жидкий, пенистый, с кислым запахом стул);
• повышенное газообразование в кишечнике (метеоризм, вздутие кишечника, боли в животе);
• симптомы дегидратации и/или недостаточная прибавка массы тела у детей раннего возраста;
• формирование дисбиотических изменений микрофлоры кишечника.
Тяжесть заболевания определяется выраженностью нарушений нутритивного статуса (гипотрофии), дегидратации, диспепсических симптомов (диареи, болей в животе) и продолжительностью заболевания.
При одной и той же степени недостаточности фермента наблюдается большая вариабельность симптоматики (в том числе в выраженности диареи, метеоризма и болевого синдрома). Однако у каждого конкретного больного наблюдается дозозависимый эффект от количества лактозы в диете - увеличение нагрузки лактозой ведет к более ярким клиническим проявлениям.
Важно помнить, что 5-10% пациентов способны принимать до 250 мл молока без развития клинических симптомов гиполактазии.
Диагностика
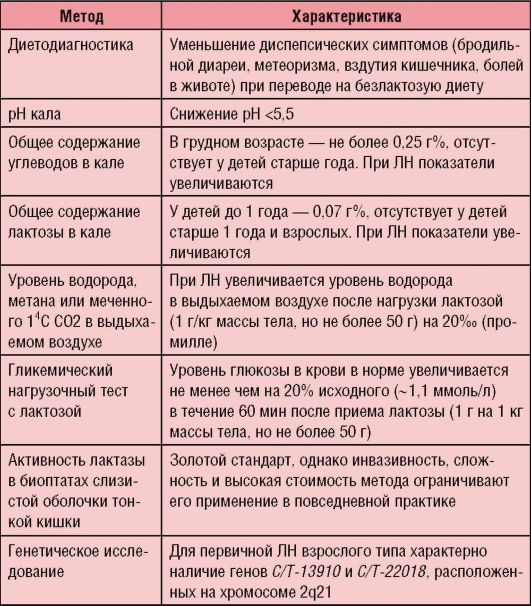
Диагноз ставят на основании характерной клинической картины и подтверждают с помощью дополнительных методов исследования (табл. 4-4).
Таблица 4-4. Методы диагностики лактазной недостаточности
Дифференциальная диагностика
Похожие на ЛН симптомы (рис. 4-8, а) имеют дети с недостаточностью других ферментов - сахаразы, изомальтазы, что объясняется тесной взаимосвязью гидролиза сложных и простых углеводов (рис. 4-8, б, в). Первые симптомы появляются, когда в питание детей включают обычный сахар (когда родители подслащивают блюда прикорма). Редкой и тяжелой патологией является нарушение всасывания моносахаридов - глюкозы и фруктозы, которое проявляется тяжелой диареей сразу же при включении в рацион меда, соков и т.п.
Еще одно редкое заболевание, которое может протекать под маской непереносимости молока, - галактоземия, относящаяся к группе нарушений обмена веществ, в частности обмена галактозы в организме. У таких детей употребление любого продукта, содержащего лактозу (следовательно, и галактозу), вызывает рвоту, желтуху, гипогликемию, глюкозурию. Заболевание проявляется в первые дни жизни.
Лечение
Основной принцип лечения - дифференцированный подход к терапии в зависимости от типа ЛН. Цели лечения:
• оптимизация процессов переваривания и всасывания лактозы;
• поддержание режима сбалансированного питания;
• предупреждение развития осложнений (остеопении, поливитаминной недостаточности).
При первичной ЛН в основе лечения лежит снижение количества лактозы в пище вплоть до полного ее исключения. Параллельно с этим проводят терапию, направленную на коррекцию нарушенной микрофлоры кишечника, и симптоматическое лечение.
При вторичной ЛН в первую очередь уделяют внимание лечению основного заболевания, а снижение количества лактозы в диете является временным мероприятием, которое проводят до восстановления слизистой оболочки тонкой кишки.
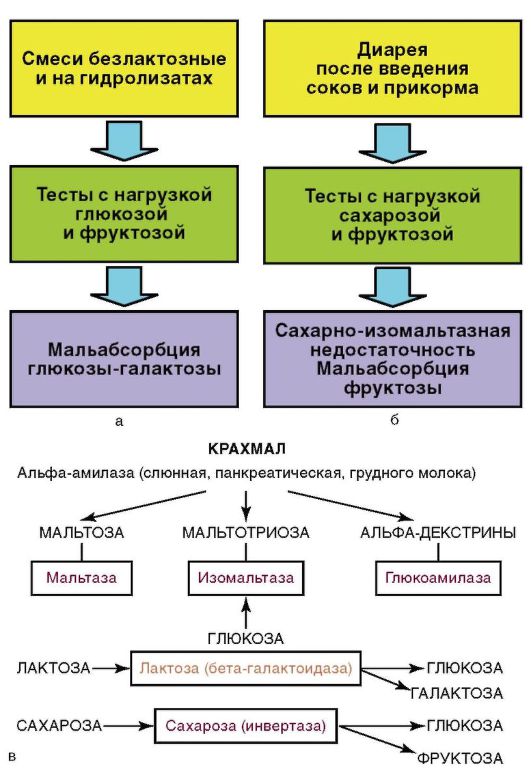
Рис. 4-8. Водянистая «кислая» диарея: а - при ЛН; б - при непереносимости других углеводов; в - взаимосвязь ферментов, осуществляющих переваривание углеводов

С заместительной целью при подтвержденной ЛН назначают ферментативный препарат - лактазу. Отечественные препараты лактазы относятся к биологически активным добавкам. Содержимое капсулы (700 ЕД лактазы) препарата «Лактаза Бэби*» (на 100 мл молока) добавляют в первую порцию предварительно сцеженного молока или молочной смеси. Кормление начинают через несколько минут.
Препарат дают в каждое кормление, которое начинают с порции сцеженного молока с лактозой, а затем ребенка докармливают грудью.

У детей старше года и взрослых при недоступности низколактозного молока также используют фермент лактазу в виде биологически активных добавок (лактазы*, лактазара*) при употреблении в пищу молока и молочных продуктов. Детям от 1 года до 5 лет добавляют в теплую (ниже 55 °C) пищу 1-5 капсулы (в зависимости от количества молока); детям от 5 до 7 лет - 2-7 капсул, если ребенок в состоянии проглотить капсулу или содержимое 2-7 капсул с негорячей пищей.
Необходимо контролировать содержание углеводов в кале. При возобновлении симптомов заболевания, появлении склонности к запору и увеличении содержания лактозы в кале дозу лактазы увеличивают.
У большинства недоношенных с транзиторной ЛН к 3- 4-му месяцу жизни можно вернуться к молочной диете.
При вторичной ЛН симптоматика транзиторная. Пациентам проводят лечение основного заболевания; при восстановлении нормальной структуры и функции слизистой оболочки тонкой кишки активность лактазы восстанавливается. Именно поэтому при разрешении (достижении ремиссии) основного заболевания через 1-3 мес диету расширяют, вводя лактозосодержащие молочные продукты под контролем клинических симптомов (диареи, метеоризма) и экскреции углеводов с калом. При сохранении явлений непереносимости лактозы следует думать о наличии у больного первичной ЛН.
Эффективность лечения включает следующие показатели.
• Клинические признаки: нормализация стула, уменьшение и исчезновение метеоризма и болей в животе.
• Соответствующие возрасту темпы прибавки массы тела, нормальные показатели физического и моторного развития.
• Снижение и нормализация экскреции углеводов с калом.
Профилактика
Непереносимость лактозы - это не повод отказываться от кормления грудью.
Важно сохранение естественного вскармливания при соблюдении некоторых правил. Предупреждение появления симптомов гиполактазии возможно при соблюдении диеты с низким содержанием лактозы или с полным ее отсутствием.
Прогноз
Прогноз при своевременном переводе ребенка на безмолочное питание благоприятный.
Целиакия
Код по МКБ-10
K90.0. Целиакия.
Целиакия - хроническое, генетически детерминированное заболевание (глютеновая болезнь, аутоиммунная Т-клеточноопосредованная энтеропатия, болезнь Ги-Гертера-Гейбнера) со стойкой непереносимостью глютена и синдромом мальабсорбции, связанное с атрофией слизистой оболочки тонкой кишки и отставанием в физическом, интеллектуальном и половом развитии.
Заболеваемость целиакией в мире колеблется примерно 1 случай на 1000 населения. Массовые серологические исследования с последующим гистологическим изучением дуоденальных биоптатов показали, что она достигает уровня 1 случай на 100-200 населения. В европейских странах, США целиакия наблюдается у 0,5-1,0% населения. Соотношение заболевших женщин и мужчин составляет 2:1.
Эпидемиология целиакии напоминает айсберг - имеется гораздо больше невыявленных, чем выявленных случаев. У преобладающего большинства пациентов выявляют внекишечную манифестацию скрытой и субклинической форм: железодефицитную анемию, афтозный стоматит, дерматит Дюринга, остеопороз, задержку физического и полового развития, бесплодие, сахарный диабет 1-го типа и др.
Этиология и патогенез
К глютенам, или белкам злаковых, или проламинам (спирторастворимым протеинам, богатым глютамином и пролином), относятся:
• глиадин пшеницы;
• секалин ржи;
• хордеин ячменя;
• авенин овса (токсичность в настоящее время обсуждается).
Патогенез заболевания до конца не выяснен, но ключевую роль в нем играет иммунный ответ на глютен (рис. 4-9, а). При целиакии нарушена структура HLA-области на хромосоме 6. Наибольший риск связан со специфическими генетическими маркерами, известными как HLA-DQ2 и HLA-DQ8. Имеют место смешанный аутоиммунный, аллергический, наследственный генез (аутосомно-доминантный тип).
Синдром мальабсорбции возникает при резком уменьшении пищеварительной функции тонкой кишки, при атрофии кишечных ворсинок, уменьшении активности кишечных и панкреатических ферментов, нарушении гормональной регуляции пищеварения.
Повреждение гликокаликса, а также щеточной каемки энтероцитов с мембранными ферментами, к которым относятся лактаза, сахараза, мальтаза, изомальтаза и другие, приводит к непереносимости соответствующих пищевых веществ.
Вследствие нарушения трофики ЦНС, аутоиммунных механизмов с поражением гипофиза у части детей развивается снижение уровня соматотропного гормона, что приводит к стойкой задержке роста.
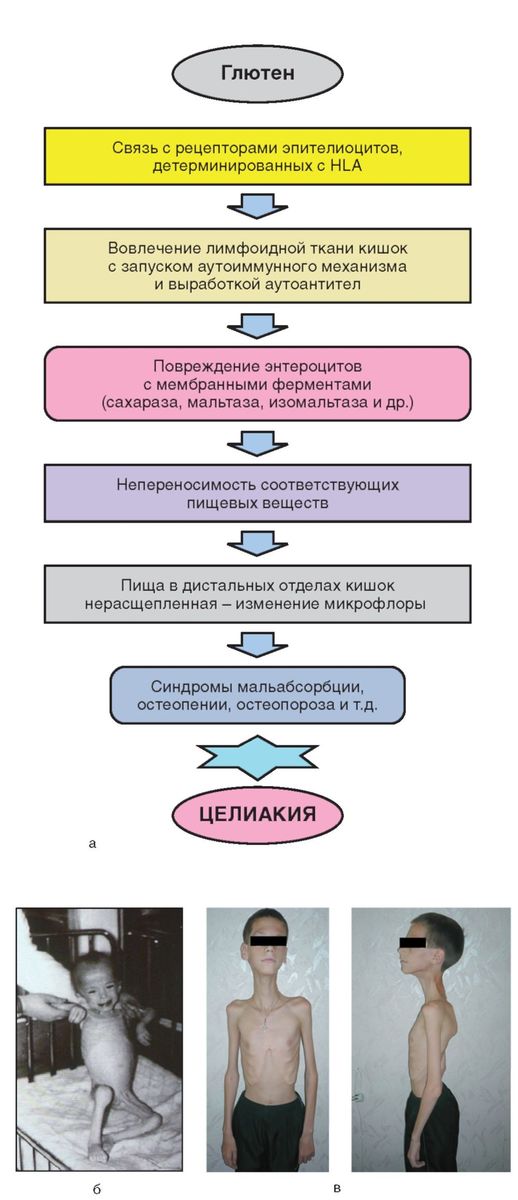
Рис. 4-9. Целиакия: а - схема патогенеза; б, в - внешний вид пациентов раннего и старшего детского возраста
Классификация
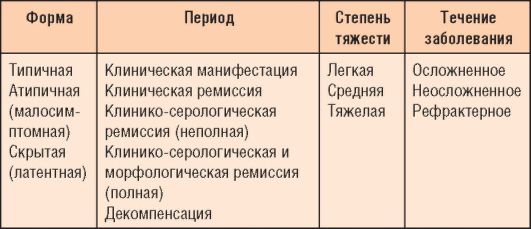
Выделение первичной и вторичной целиакии, а также синдрома целиакии нецелесообразно. Целиакия - всегда первичное заболевание, в истории болезни важно указать дату установления диагноза, что облегчает определение стадии заболевания (табл. 4-5).
Таблица 4-5. Классификация целиакии
Клиническая картина
В типичном случае целиакия манифестирует через 1,5-2 мес после введения злаковых продуктов в рацион питания, как правило, в возрасте 6-8 мес. Нередко провоцирующим фактором является инфекционное заболевание. Характерные симптомы:
• учащение стула, полифекалия, стеаторея;
• увеличение окружности живота на фоне снижения массы тела;
• признаки дистрофии: резкое снижение массы тела, истончение подкожного жирового слоя (рис. 4-9, б, в), снижение мышечного тонуса, утрата ранее приобретенных навыков и умений, гипопротеинемические отеки.
Отмечаются многообразные дефицитные состояния и симптомы: рахитоподобный синдром, синдром остеопении, патологические переломы костей, судорожный синдром, кариес и поражение зубной эмали, раздражительность, агрессивное поведение, анемия, полиурия, полидипсия, дистрофические изменения и ломкость ногтей, повышенная кровоточивость - от мелкоточечных кровоизлияний до тяжелых носовых и маточных кровотечений, нарушение сумеречного зрения, фолликулярный гиперкератоз, витилиго, стойкие фурункулезы, хейлиты, глосситы, рецидивирующие стоматиты, парестезии с потерей чувствительности, выпадение волос и т.д.
Атипичная целиакия характеризуется атрофией слизистой оболочки тонкой кишки, наличием серологических маркеров, однако клинически проявляется каким-либо отдельным симптомом при отсутствии прочих. Могут быть другие варианты атипичной целиакии, но чаще всего ведущими являются анемический синдром, остеопороз, задержка роста.
При латентной целиакии, широко распространенной в европейской популяции, имеет место атрофия слизистой оболочки тонкой кишки различной степени выраженности, определяются серологические маркеры, однако клинические признаки заболевания отсутствуют.
Группы риска по целиакии:
• хроническая диарея и СРК;
• отставание в физическом и/или половом развитии;
• остеопороз;
• железодефицитная или мегалобластическая анемия;
• синдромы Дауна, Вильямса и Шерешевского-Тернера. Детям из групп риска, а также имеющим ассоциированные заболевания, близких родственников (родителей и сибсов), больных целиакией, рекомендуют обследование в целях ее исключения.
Диагностика
HLA-типирование должно являться первым этапом формирования групп риска среди родственников, больных целиакией (группы генетического риска). В дальнейшем
определяют серологические маркеры заболевания (антиаглиадиновые антитела и антитела к трансглютаминазе), что позволяет использовать серологический (второй) этап диагностики для выявления лиц с иммунологическими отклонениями (группы иммунологического риска). В результате морфологического исследования слизистой оболочки тонкой кишки (третий, основной этап диагностики) устанавливают диагноз целиакии. При отрицательных результатах детям (родственникам) рекомендуют дальнейшее динамическое наблюдение.
Серологические методы диагностики целиакии информативны только в активный период заболевания, причем они не являются унифицированными. Предполагается более низкая чувствительность определения аутоантител у детей раннего возраста по сравнению с взрослыми.
При подозрении на целиакию при отсутствии клинических проявлений заболевания и сомнительных данных гистологического и серологического исследований у детей старше 3 лет проводят провокационный тест (нагрузка глютеном). Через 1 мес или раньше в случае появления симптомов заболевания проводят повторные гистологическое и серологическое исследования.
При выявлении анемии может потребоваться углубленное исследование обмена железа, включая общую и латентную железосвязывающую способность сыворотки, уровень трансферрина, сывороточного железа, коэффициент насыщения трансферрином.
В связи с высокой частотой нарушений минерализации костной ткани при целиакии требуется контроль состояния костной ткани: рентгенографическое исследование трубчатых костей, определение костного возраста, биохимические исследования.
Эндоскопические признаки целиакии: отсутствие складок в тонкой кишке (кишка в виде трубы; рис. 4-10, а) и поперечная их исчерченность. Обнаружение этих признаков является поводом для взятия биопсии и проведения гистологического исследования.
Патоморфология
В активном периоде целиакии имеются следующие гистоморфологические признаки.
• Частичная или полная атрофия (значительное снижение высоты) ворсинок вплоть до полного исчезновения (атрофическая энтеропатия; рис. 4-10, б) с увеличением глубины крипт (снижением соотношения «высота ворсинки/глубина крипты» менее 1,5) и уменьшением количества бокаловидных клеток.
• Межэпителиальная лимфоцитарная и лимфоплазмоцитарная инфильтрация собственной пластинки слизистой оболочки тонкой кишки.
• Уменьшение высоты щеточной каемки и т.д. Желательно проведение морфометрии, которая повышает
достоверность диагностики и оценки результатов динамического наблюдения.
Дифференциальная диагностика
Дифференциальную диагностику проводят с кишечной формой муковисцидоза, дисахаридазной недостаточностью, аномалиями ЖКТ. Ложноположительный диагноз целиакии встречается при таких заболеваниях, как функциональная диарея, СРК. Сходная гистологическая картина может наблюдаться при аллергической энтеропатии, белково-калорийной недостаточности питания, тропической спру, лямблиозе, радиационном энтерите, аутоиммунной энтеропатии, иммунодефицитных состояниях, Т-клеточной лимфоме.
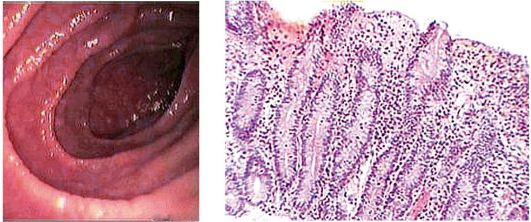
Рис. 4-10. Патоморфология целиакии и хронического атрофического еюнита: а - эндоскопическая картина ДПК при целиакии; б - хронический атрофический еюнит: гиперрегенераторная атрофия слизистой оболочки при целиакии в активной стадии (окраска гематоксилинэозином; χ 100)
Лечение
Разработаны шесть ключевых элементов лечения больных целиакией.
• Консультация с опытным диетологом.
• Образование в отношении болезни.
• Пожизненное соблюдение аглютеновой диеты.
• Диагностика и лечение недостатка питания.
• Доступ к группе поддержки.
• Продолжительное наблюдение мультидисциплинарной группой специалистов.


Медикаментозная терапия при целиакии носит вспомогательный характер, но в ряде случаев может быть жизненно необходимой. В основном она направлена на коррекцию метаболических нарушений, развившихся на фоне синдрома мальабсорбции.
Больным целиакией назначают ферменты: панкреатин (креон*, панцитрат*, ликреаза*) в каждое кормление с индивидуальным подбором дозы (приблизительно 1000 ЕД/кг в сутки липазы), курс - 1-3 мес; при диарее - адсорбентмукоцитопротектор смектит диоктаэдрический (смекта*, неосмектин* ); пробиотики: линекс*, бифиформ*, лактобактерин* и бифидумбактерин* в средних дозах в течение 1-2 мес. Показаны препараты кальция, витамины С, D3, кокарбоксилаза, лечение анемии.
Холестатический синдром может потребовать назначенияпрепаратов урсодезоксихолевой кислоты (урсосан*, урсофальк*).
При среднетяжелой и тяжелой формах требуется стационарное лечение.
При выраженной гипопротеинемии назначают 10% раствор альбумина* в/в капельно, наборы аминокислот, при гипогликемии - препараты калия в 5-10% растворе глюкозы* в/в капельно, при водно-электролитных расстройствах - изотонический раствор натрия хлорида, 4,0-7,5% раствор калия хлорида, 25% раствор сульфата магния. Из анаболиков назначают оротовую кислоту (калия оротат*), глицин*, иногда ретаболил*, при тяжелой форме - глюкокортикоиды (преднизолон по 1-2 мг/кг). L-тироксин* назначают в дозе 25-50 мг/кг, курс - до 1 мес под контролем ТТГ, Т3 и Т4.

Профилактика
Юридические вопросы в отношении целиакии не решены, это касается предоставления инвалидности, безусловного отвода от обязательной службы в рядах вооруженных сил.
Прогноз
Целиакия - на сегодняшний день заболевание, не поддающееся радикальному излечению (хотя достижим высокий уровень качества жизни).
При длительном течении нераспознанной целиакии повышается риск возникновения опухолей ЖКТ и другой локализации, а также ассоциированных с целиакией аутоиммунных заболеваний: сахарного диабета 1-го типа, аутоиммунного
тиреоидита, болезни Аддисона, системной красной волчанки, склеродермии, миастении, ревматоидного артрита, алопеции, аутоиммунного гепатита (АИГ), герпетиформного дерматита, первичного билиарного цирроза печени, атаксии с антителами к клеткам Пуркинье, кардиомиопатий. У 15% больных целиакией риск перехода в гастроинтестинальную карциному или лимфому в 40-100 раз выше по сравнению с общей популяцией.
СИНДРОМ ИЗБЫТОЧНОГО БАКТЕРИАЛЬНОГО РОСТА
СИБР в кишечнике (в англоязычной литературе - bacterial overgrowth) обусловлен нарушением качественного и количественного состава микробного биоценоза кишечника, размножением УПМ в количестве, не свойственном здоровому человеку, - более 105 микробных тел в 1 мл тонкой кишки (рис. 4-11, а). Он представляет собой не самостоятельную нозологическую форму, а синдром. Термин «дисбактериоз» в последние годы использовать не совсем корректно, поскольку он не в полной мере отражает сущность развивающихся нарушений.
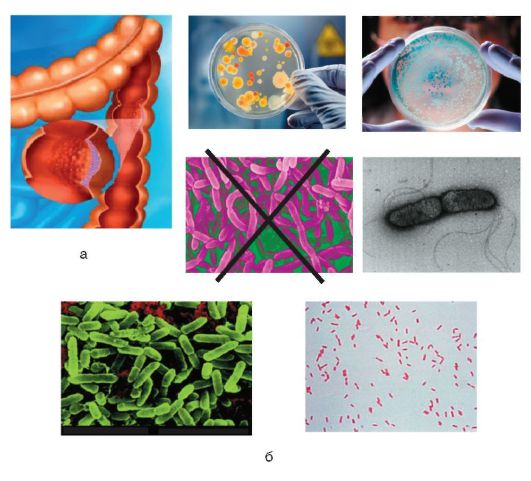
Рис. 4-11. Характеристики СИБР: а - участок тонкой кишки при СИБР; б - разнообразные УПМ при отсутствии бифидобактерий

Этиология и патогенез
С точки зрения микробиологии СИБР характеризуется значительным увеличением общего количества функционально неполноценных кишечных палочек (лактозо-, маннито-, индолоотрицательных), содержанием гемолитических форм Escherichia coli, созданием условий для размножения грибов рода Can dida и других УПМ, а также уменьшением количества анаэробных представителей (особенно бифидобактерий) (рис. 4-11, б). Место про- и пребиотиков в коррекции состава микрофлоры кишечника представлено на рис. 4-12, а.
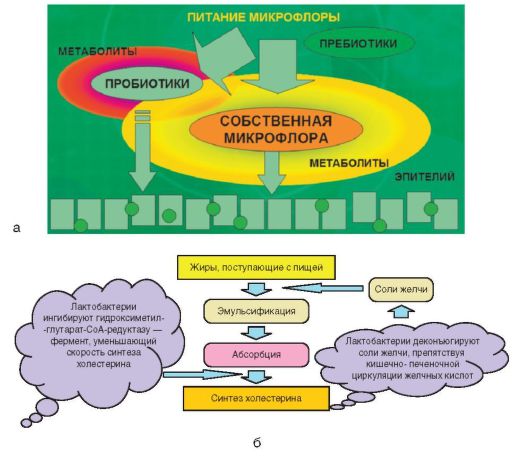
Рис. 4-12. Про- и пребиотики: а - место про- и пребиотиков в коррекции состава микрофлоры кишечника; б - гипохолестеринемическая активность лактобактерий
Доказано, что нарушения обмена холестерина (в том числе ожирение) тесно связаны с нарушением микробного баланса ЖКТ. Механизм снижения содержания холестерина под влиянием действия лактобактерий изображен на рис. 4-12, б.
Фоном для развития СИБР служат различные состояния, сопровождаемые нарушением переваривания пищи, пассажа внутрипросветного содержимого, изменением иммунологической реактивности организма, ятрогенными воздействиями на микрофлору кишечника. При этих состояниях невсосавшиеся питательные вещества служат питательной средой для избыточного размножения бактерий.
В качестве единственной самостоятельной нозологической формы СИБР выступает псевдомембранозный колит, обусловленный избыточным размножением Clostridium difficile - облигатно-анаэробной грамположительной спорообразующей бактерии, обладающей природной устойчивостью к большинству широко применяемых антибиотиков (клиндамицину, ампициллину, цефалоспоринам и др.).
Клиническая картина
СИБР характеризуется различными клиническими проявлениями, наслаивающимися на симптомы основного заболевания.
Избыточное размножение бактерий в тонкой кишке является дополнительным фактором, поддерживающим воспаление слизистой оболочки, снижающим продукцию ферментов (в основном лактазы) и усугубляющим нарушение переваривания и всасывания. Эти изменения обусловливают

развитие таких симптомов, как коликообразные боли в околопупочной области, метеоризм, диарея, похудение.
СИБР играет огромную роль в развитии синдрома экзокринной панкреатической недостаточности за счет разрушения бактериями панкреатических ферментов, развития воспаления в эпителии тонкой кишки с последующим постепенным развитием атрофии слизистой оболочки. При преимущественном вовлечении в процесс толстой кишки пациенты предъявляют жалобы на неоформленный стул, метеоризм, ноющие боли в животе.
Выраженные нарушения равновесия в составе кишечной микрофлоры могут сопровождаться признаками гиповитаминоза В12, В1, В2, РР. У пациента выявляются трещины в углах рта, глоссит, хейлит, поражения кожи (дерматит, нейродермит), железо- и В12-дефицитная анемия. Поскольку микрофлора кишечника служит важным источником викасола, могут наблюдаться нарушения свертывания крови. В результате нарушения обмена желчных кислот развиваются симптомы гипокальциемии (онемение губ, пальцев, остеопороз).
Диагностика
Диагностика СИБР подразумевает анализ картины основного заболевания, выявление возможной причины нарушения микробиоценоза кишечника. Точными методами диагностики СИБР являются аспирация содержимого тонкой кишки с немедленным посевом аспирата на питательную среду, а также неинвазивный дыхательный водородный тест с лактулозой (рис. 4-13, а). В тесте оценивается выдыхаемый воздух после употребления лактозы. Если она метаболизируется быстрее, чем в норме, этот подъем свидетельствует об избыточной концентрации бактерий в тонкой кишке.
Посев кала на дисбактериоз, широко используемый в РФ как метод оценки микробиоценоза кишечника, за рубежом признан неинформативным, поскольку дает представление лишь о микробном составе дистального отдела толстой кишки.
Дополнительные методы могут включать эндоскопическое, рентгенологическое исследования кишечника для выявления нарушений анатомического строения, оценки перистальтики ЖКТ; биопсию тонкой кишки для установления диагноза энтерита, энтеропатии (рис. 4-13, б), диагностики ферментопатий и др.
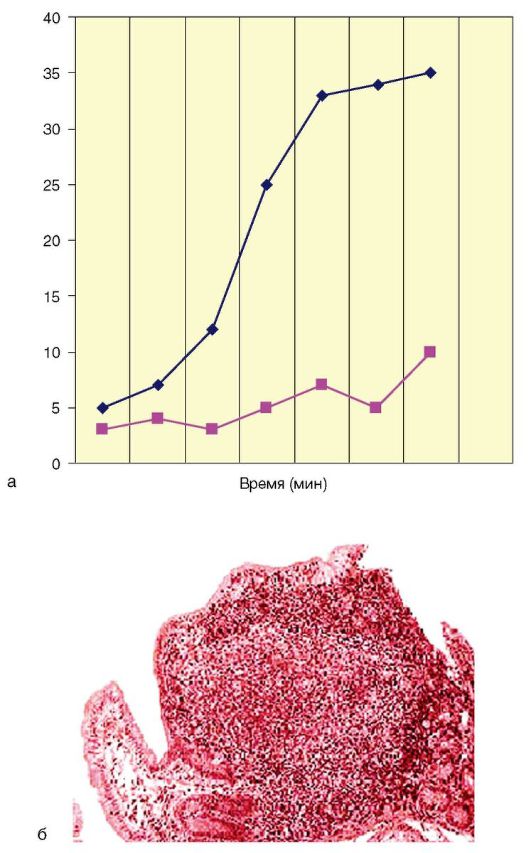
Рис. 4-13. Диагностика СИБР: а - раннее повышение концентрации водорода в выдыхаемом воздухе при СИБРе; б - гиперплазия лимфоидного фолликула при энтеропатии (окраска гематоксилинэозином, χ 50)
Лечение
Диетические предписания необходимо давать с учетом основного заболевания.
Медикаментозное лечение проводят в зависимости от степени дисбактериоза в два этапа:
• I этап - подавление роста УПМ;
• II этап - нормализация кишечной микрофлоры.

Антибактериальная терапия показана крайне редко, только при тяжелых формах СИБР. Назначают метронидазол (трихопол*, флагил*) по 200-400 мг 3 раза в день в течение недели; при его неэффективности детям старшего возраста добавляют тетрациклин по 250 мг 4 раза в день в течение 2 нед. Антибиотики резерва - ципрофлоксацин (ципромед*, ципробай*), суточная доза - 20 мг/кг 2 раза в день, и ванкомицин (ванкоцин*) по 125 мг 4 раза в день, курс - 10-14 дней.
В ряде случаев для подавления УПМ проводят фаготерапию. Бактериофаги используют у новорожденных, применяют внутрь 2-3 раза в сутки за 1-1,5 ч до кормления (предварительно разводят в 2 раза кипяченой водой) или вводят в клизмах 1 раз в сутки. Лечебную микроклизму с бактериофагом проводят через 2 ч после самостоятельного стула или очистительной клизмы.
Бактериофаг стафилококковый* выпускается во флаконах по 50 и 100 мл, в ампулах по 2 мл; детям 0-6 мес назначают внутрь по 5-10 мл и в клизме по 20 мл, 6-12 мес - по 10-15 и 20 мл соответственно, 1-3 лет - по 15-20 и 40 мл, старше 3 лет - внутрь по 50 мл, в клизме - по 50-100 мл. Курс лечения - 5-7 дней, при необходимости через 3-5 дней проводят еще 1-2 курса. Бактериофаг клебсиелл поливалентный очищенный* в ампулах по 5, 10 и 20 мл применяют внутрь в дозе 1,0-1,5 мл/кг в сутки в 1-3 приема и в виде высоких клизм, курсом 10-14 дней. Применяют также бактериофаг коли, интести-бактериофаг, бактериофаг клебсиелл, протейный жидкий во флаконах по 50 и 100 мл, доза - 5-15 мл 3 раза в сутки, курс - 5-10 дней.
Лечение псевдомембранозного колита проводят по определенным схемам и не рассматривают вследствие обособленности этого заболевания.
Дети с небольшими отклонениями биоценоза обычно не нуждаются в подавлении микрофлоры, лечение можно начинать с назначения про- и пребиотиков.
К пробиотикам, содержащим нормальные штаммы кишечных бактерий и используемым с заместительной целью, относят линекс*, бифиформ*, бифидумбактерин* и лактобактерин*, лактобактерии ацидофильные + грибки кефирные (аципол*), бифилиз*, бификол* и др.

Линекс* и бифидумбактерии лонгум + энтерококкус фециум (бифиформ*) - комбинированные препараты в капсулах. Линекс* показан детям с рождения до 2 лет по 1 капсуле, 2-12 лет - по 1-2 капсулы, старше 12 лет - по 2 капсулы 3 раза в сутки. Бифиформ* назначают детям от 2 лет по 2-3 капсулы 2 раза в сутки. Курс лечения - 10-21 день.
Бифидумбактерин форте* детям с рождения до 1 года назначают по 1 пакетику 2-3 раза в сутки, 1-15 лет - по
1 пакетику 3-4 раза в сутки, старше 15 лет - по 2 пакетика 2-3 раза в сутки. Лактобактерии ацидофильные + грибки кефирные (аципол*) в лиофилизате для приготовления раствора, в таблетках, детям 3-12 мес рекомендуют по 1 ч. л. 2-3 раза в сутки, 1-3 лет - по 1 ч. л. 2-4 раза в сутки за 30 мин до приема пищи, с 3 лет - в таблетках.
Лактобактерии ацидофильные (ацилакт*) в таблетках, сухом порошке детям до 6 мес назначают по 5 доз в сутки в
2 приема, старше 6 мес - по 5 доз 2-3 раза в сутки за 30 мин до приема пищи. Бификол* содержит бифидобактерии и кишечные палочки. Препарат назначают детям 6-12 мес - по 2 дозы, 1-3 лет - по 4 дозы, старше 3 лет - по 6 доз 2-3 раза в сутки за 30-40 мин до еды. Курс лечения препаратами - 21 день.
Бактисубтил* (чистая сухая культура бактерий Bacillus cereus в виде спор) в капсулах рекомендуют детям старше
3 лет по 1-2 капсулы 3-4 раза в сутки, цель назначения препарата - селективная деконтаминация, т.е. размножение спор до полной стерилизации кишечника. Курс лечения - 10 дней.

В качестве селективной стимуляции, направленной на активизацию процессов роста и размножения бифидо- и лактофлоры, рекомендуют пребиотики, способствующие восстановлению собственной микрофлоры ребенка: лактулозу, хилак форте*.
Пребиотики - компоненты пищи, которые не перевариваются ферментами человека, не усваиваются в верхних отделах ЖКТ, поэтому достигают кишечника в своем первозданном виде и стимулируют рост естественной микрофлоры кишечника.

С биохимической точки зрения пробиотики - это полисахариды, инулин, лактулоза и некоторые галакто-, фруктозо- и олигосахариды.
Лактулозу (гудлак*, дюфалак*, нормазе*) детям до года назначают внутрь в 1-2 приема по 1,5-3,0 мл/сут, 1-3 года - 5 мл/сут, 3-6 лет - 5-10 мл/сут, 7-14 лет - по 10-15 мл/сут. Курс лечения -3-4 нед и более.
Лактулоза + лигнин гидролизный (лактофильтрум*) - комбинация пребиотика и сорбента, нормализующая микрофлору кишечника и очищающая организм от токсинов и аллергенов. Применяют внутрь 3 раза в день между приемами пищи, детям 7-12 лет назначают по 1-2 таблетки по 500 мг, старше 12 лет и взрослым - по 2-3 таблетки во время еды. Курс лечения - 14 дней.
Хилак форте* стимулирует более 500 видов собственной микрофлоры кишечника, его не назначают одновременно с лактосодержащими препаратами. Детям первых 3 мес жизни - по 15-20 капель, от 3 мес до 1 года - по 15-30 капель, детям 2-14 лет - по 20-40 и 15-18 лет - по 40-60 капель 3 раза в сутки до или во время приема пищи, смешивая с небольшим количеством жидкости (за исключением молока). Форма выпуска - капли во флаконахкапельницах по 30 и 100 мл. Курс лечения - 14 дней и более.

Профилактика
Обязательным условием предупреждения СИБР являются устранение причин, вызвавших его, эффективная терапия основного заболевания.
У детей первого года жизни важным фактором профилактики является сохранение грудного вскармливания или, если это невозможно, использование адаптированных кисломолочных смесей и смесей с пре- и пробиотиками.
Обеспечение современного человека функциональным питанием, т.е. питанием, содержащим полезные микроорганизмы или метаболиты, повышение уровня образования населения в вопросах здорового питания - направления современной профилактической и восстановительной медицины.
Основой предупреждения СИБР являются рациональная антибиотикотерапия и исключение необоснованных случаев назначения антибактериальных средств. Антибактериальную терапию проводят по жизненным показаниям.
Прогноз
Прогноз благоприятный при своевременной коррекции дисбиотических нарушений.
ВОСПАЛИТЕЛЬНЫЕ ЗАБОЛЕВАНИЯ КИШЕЧНИКА
НЯК и болезнь Крона имеют много общих патофизиологических и эпидемиологических характеристик и образуют группу хронических воспалительных заболеваний кишечника, которые иногда сложно дифференцировать. Ключевое отличие в том, что НЯК поражает только толстую кишку, в то время как болезнь Крона может вовлекать весь ЖКТ, начиная от ротовой полости и заканчивая анусом, а также поражать все слои пищеварительной трубки (рис. 4-14).
Географическое, этническое распределение НЯК и болезни Крона очень схожи. При этих заболеваниях признается роль общих генетических механизмов.
Неспецифический язвенный колит
Коды по МКБ-10 K51. Язвенный колит.
K51.0. Язвенный (хронический) энтероколит. K51.1. Язвенный (хронический) илеоколит. K51.2. Язвенный (хронический) проктит. K51.3. Язвенный (хронический) ректосигмоидит. K51.9. Язвенный колит неуточненный.
НЯК - хроническое рецидивирующее заболевание, при котором воспаление имеет диффузный характер и локализуется в пределах слизистой оболочки толстой и прямой
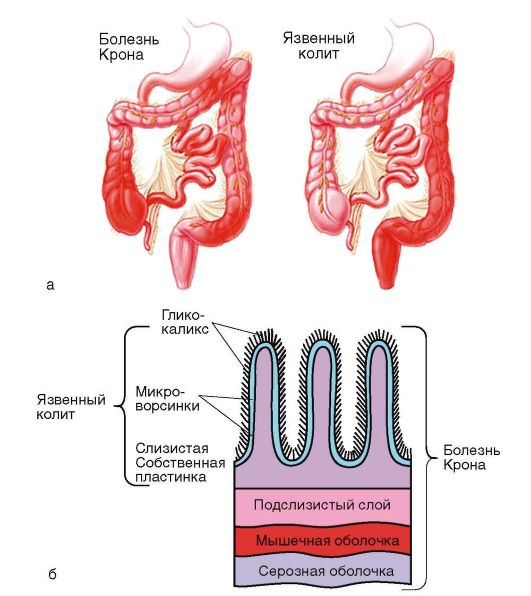
Рис. 4-14. Воспалительные заболевания кишечника: а - наиболее частые локализации патологического процесса; б - глубина поражения стенки пищеварительного тракта при хронических воспалительных заболеваниях кишечника
кишки, сопровождается болями, гемоколитом со слизью и иногда с гноем, прогрессирующим ухудшением состояния.
НЯК обнаруживается у 35-100 человек на каждые 100 000 на-селения индустриально развитых стран, т.е. затрагивает менее 0,1% популяции. У детей НЯК развивается относительно редко, заболеваемость оценивается как 3,4 на 100 000 детского населения. В последние два десятилетия наблюдают рост количества больных НЯК. Соотношение женщин и мужчин составляет 1:1.
К регионам, характеризуемым высокой частотой НЯК, относятся Великобритания, США, Северная Европа, Австралия. Низкая заболеваемость отмечается в Азии, Японии, Южной Америке.

Этиология и патогенез
В настоящее время рассматриваются следующие причины НЯК.
• Генетическая предрасположенность (наличие изменений в хромосомах 6,12, ассоциация с геном IL-1ra).
• Использование НПВС в течение длительного времени.
• Бактерии, вирусы? (роль этих факторов до конца не ясна).
• Пищевая аллергия (молоко и другие продукты), стресс провоцируют первую атаку заболевания или его обострение, но не являются самостоятельными факторами риска развития НЯК.
• Иммунологические нарушения и аутоиммунизация - факторы патогенеза заболевания. При НЯК возникает каскад самоподдерживающихся патологических про-
цессов: сначала неспецифических, затем аутоиммунных, повреждающих прежде всего орган-мишень - кишечник.
Классификация
Классификация НЯК представлена в табл. 4-6.
Таблица 4-6. Рабочая классификация НЯК
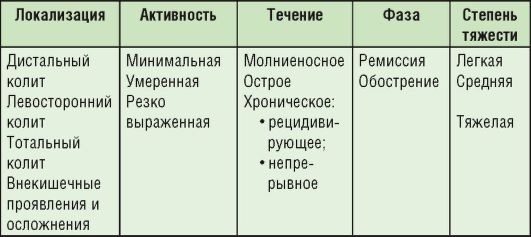
Клиническая картина
Выделяют три ведущих симптома НЯК:
• наличие крови в стуле (гемоколит);
• диарея;
• боли в животе.
Почти в половине случаев заболевание начинается исподволь. Частота стула варьирует от 4-8 до 16-20 раз в сутки и более. Степень процесса определяется как легкая при частоте стула менее 4 раз в сутки, единичных прожилках крови в стуле, нормальной СОЭ, отсутствии системных проявлений. Состояние средней тяжести характеризуется учащенным стулом (более 4 раз в сутки), минимальными системными нарушениями. При тяжелом течении наблюдается дефекация с кровью свыше 6 раз в сутки, отмечаются лихорадка, тахикардия, анемия и повышение СОЭ более 30 мм/ч. Гемоколит сопровождают, а иногда и предшествуют боли в животе, чаще во время еды или перед дефекацией. Боли схваткообразные, локализуются внизу живота, в левой подвздошной области или вокруг пупка.
Различают системные и местные осложнения НЯК (табл. 4-7), причем местные осложнения у детей развиваются редко.
Таблица 4-7. Осложнения НЯК
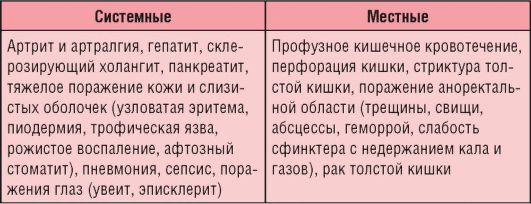
Диагностика
Диагностика заболевания в большинстве случаев не вызывает затруднений.
Для НЯК в клиническом анализе крови характерны признаки воспаления (нейтрофильный лейкоцитоз со сдвигом влево, тромбоцитоз, повышение СОЭ) и анемии (снижение уровня эритроцитов и гемоглобина). В биохимическом анализе крови наблюдаются повышение уровня С-реактивного белка, γ-глобулинов, снижение уровня сывороточного железа, признаки иммунного воспаления (повышены уровни циркулирующих иммунных комплексов, иммуноглобулинов класса G).
Рентгенологически выявляют асимметрию, деформацию или полное исчезновение гаустр. Просвет кишки имеет вид шланга с утолщенными стенками, укороченными отделами, сглаженными анатомическими изгибами.
Решающую роль в подтверждении диагноза НЯК играют колоноскопия или ректороманоскопия с гистологическим исследованием биоптатов. Слизистая оболочка толстой кишки гиперемирована, отечна, легкоранима, появляется ее зернистость (рис. 4-15, а). Сосудистый рисунок не определяется, выражена контактная кровоточивость, обнаруживаются эрозии, язвы, микроабсцессы, псевдополипы.
Диагностическим маркером НЯК является фекальный кальпротектин, при обострении заболевания его уровень повышается более 130 мг/кг стула.
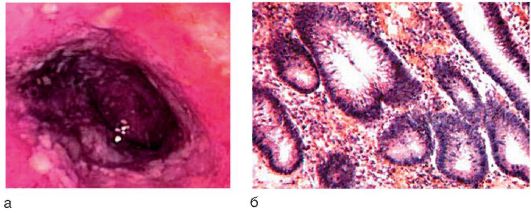
Рис. 4-15. Диагностика воспалительных заболеваний кишечника: а - колоноскопия при НЯК: гипертрофированная остаточная слизистая оболочка, зернистость толстой кишки в очагах атрофии; б - микропрепарат: дисплазия эпителия и многочисленные митозы в криптах (окраска гематоксилин-эозином; χ 100)
Патоморфология
НЯК у детей значительно чаще, чем у взрослых, имеет распространенный характер. Тотальные формы поражения наблюдаются у 60-80% детей и лишь у 20-30% взрослых. При этом прямая кишка меньше вовлечена в воспалительный процесс и может выглядеть малоизмененной.
Патологические изменения в толстой кишке разнообразны - от легкой гиперемии, кровоточивости слизистой оболочки до образования глубоких язв, распространяющихся до серозного слоя.
При гистологическом исследовании выявляются воспаление и некроз, отек слизистой оболочки и подслизистого слоя, расширение капилляров и кровоизлияния в отдельных участках. Клетки эпителия набухшие, переполнены слизью (рис. 4-15, б). Позднее появляются крипт-абсцессы; вскрываясь в полость крипт, они приводят к изъязвлению слизистой оболочки.
Дифференциальная диагностика
Дифференциальную диагностику проводят с болезнью Крона, целиакией, дивертикулитом, опухолями и полипами толстой кишки, туберкулезом кишечника, болезнью Уиппла и др.
В ряде случаев диагноз НЯК может быть выставлен ошибочно. Имитируют это заболевание другие патологии, в частности острые кишечные инфекции (сальмонеллез, дизентерия), протозойные инвазии (амебиаз, лямблиоз), глистные инвазии, болезнь Крона, реже рак толстой кишки.
Для исключения инфекций необходимо получение отрицательных бактериологических посевов кала, отсутствие нарастания титра антител (реакция прямой гемагглютинации - РПГА) к возбудителям в крови. Однако необходимо помнить, что выявление острых кишечных инфекций и нередко гельминтов не исключает диагноз НЯК.
Трудным является проведение дифференциальной диагностики между НЯК и болезнью Крона (см. ниже табл. 4-10).
Лечение
В период незначительного или умеренного обострения возможно амбулаторное лечение.

Назначают антибактериальные препараты - азосоединения сульфапиридина с салициловой кислотой [сульфасалазин, месалазин (салазопиридазин*), салазодиметоксин*] под контролем показателей периферической крови. Сульфасалазин назначают в дозе 30-40 мг/кг в сутки в 3-4 приема: детям 2-5 лет - 1-2 г/сут, 6-10 лет - 2-4 г/сут, старше 10 лет - 2-5 г/сут. Месалазин рекомендуют в суточной дозе 30-40 мг/кг в 3-4 приема. Салазопиридазин* и салазодиметоксин* назначают детям до 5 лет по 500 мг, старше 5 лет - по 750-1500 мг/сут. Полную дозу дают до получения терапевтического эффекта в течение 5-7 дней, затем каждые 2 нед дозу снижают на 1/3 от ее первоначальной величины.
При легкой форме заболевания курс лечения составляет до 2-4 мес, при тяжелой - не менее 6 мес. При дистальном проктите месалазин назначают в свечах по 500 мг 4 раза в сутки или по 1 г 2 раза в сутки, курс лечения - 2-3 мес.
При средней и тяжелой формах заболевания назначают пероральный и парентеральный прием глюкокортикоидов, далее циклоспорин, инфликсимаб в условиях специализированного стационара.
Прием салазопрепаратов сочетают с мексаформом*, интестопаном*, ферментными препаратами (панкреатин, креон 10 000*, панзинорм*, мезим форте*), которые назначают курсами по 2-3 нед.
Фармакологическое действие мексаформа* и интестопана* обусловлено антибактериальным и антипротозойным эффектами. Мексаформ* назначают школьникам по 1-3 таблетки в день, курс лечения - около 3 дней. Интестопан* назначают детям до 2 лет - по 1/4 таблетки на 1 кг массы тела в день в
3-4 приема, старше 2 лет - по 1-2 таблетки 2-4 раза в день, максимальный курс лечения - 10 дней.
Обязательно парентеральное введение комплекса витаминов и микроэлементов.
Для нормализации микрофлоры кишечника назначают пробиотики: линекс*, бифиформ*, колибактерин*, бифидумбактерин*, бификол*, лактобактерин* в общепринятых возрастных дозах на 3-6 нед.

При легкой форме (распространенном проктите или ограниченном проктосигмоидите) назначают микроклизмы с гидрокортизоном (125 мг) или преднизолоном (20 мг) 2 раза в сутки, курс лечения - 7 дней; сульфасалазин в сочетании с местным введением месазалина в свечах или микроклизмах.
При среднетяжелой форме (распространенном проктосигмоидите, реже левостороннем колите) терапию проводят в специализированном стационаре: преднизолон внутрь, микроклизмы с гидрокортизоном или преднизолоном, внутрь длительно сульфасалазин и метронидазол.
При тяжелой форме - терапия в реанимационном отделении, подготовка к хирургическому лечению. Применяют субтотальную колэктомию с наложением первичного анастамоза или илео- и сигмостомы с сохранением возможности восстановления кишечной непрерывности после стихания активности воспаления в прямой кишке. Пирамида лечения пациентов с НЯК представлена на рис. 4-16.
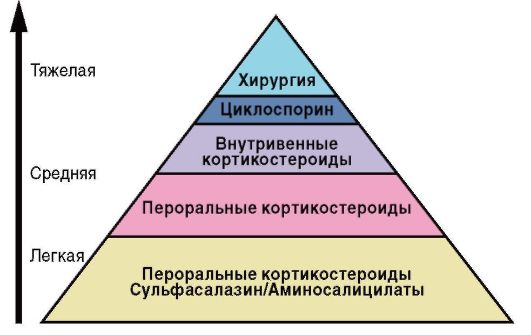
Рис. 4-16. Пирамида лечения при обострении НЯК
Профилактика
Профилактика НЯК представлена ниже.
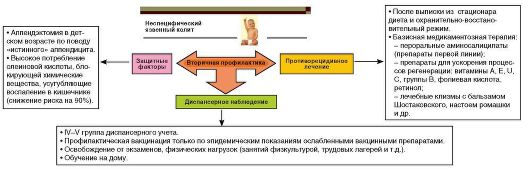
Прогноз
Прогноз для выздоровления неблагоприятный, для жизни - зависит от степени тяжести заболевания, характера течения, наличия осложнений. Показан регулярный эндоскопический контроль изменений слизистой оболочки толстой кишки из-за возможности ее дисплазии. Большинство взрослых пациентов длительно нетрудоспособны, следовательно, нуждаются в оформлении инвалидности.
Болезнь Крона
Коды по МКБ-10
K50. Болезнь Крона (регионарный энтерит). K50.0. Болезнь Крона тонкой кишки. K50.1. Болезнь Крона толстой кишки. K50.8. Другие разновидности болезни Крона. K50.9. Болезнь Крона неуточненная.
Хроническое рецидивирующее заболевание (трансмуральный илеит, терминальный илеит) с воспалительным и гранулематозно-язвенным поражением терминального отдела подвздошной кишки, реже - толстой кишки, характеризуемое болями в животе перед актом дефекации, запором, пониженным питанием. Болезнь названа в честь американского гастроэнтеролога Б. Крона, описавшего ее в 1932 г.
Заболеваемость болезнью Крона составляет 3 случая на 100 000 детского населения. Наиболее часто болезнь встречается у лиц, проживающих в Северной Европе и Северной Америке. Все более часты случаи манифестации болезни у детей в возрасте до 2 лет. Среди заболевших соотношение мальчиков и девочек составляет 1,0:1,1, в то время как среди взрослых чаще болеют мужчины.
Этиология и патогенез
Существуют вирусная, аллергическая, травматическая и инфекционная теории происхождения болезни Крона, однако ни одна из них не получила признания.
Среди причин называются наследственные или генетические вследствие частого выявления болезни у однояйцовых близнецов и у родных братьев. Примерно в 17% случаев больные имеют кровных родственников, также страдающих этим заболеванием. Однако прямая связь с каким-либо HLA-антигеном еще не найдена. Выявлена повышенная частота мутации гена CARDI5. Отягощенность семейного анамнеза отмечается в 26-42% случаев.
Системное поражение органов при болезни Крона наталкивает на подозрение об аутоиммунной природе заболевания. У пациентов обнаруживают патологически высокое количество T-лимфоцитов, антитела к кишечной палочке, белку коровьего молока, липополисахаридам. Из крови больных в периоды обострения выделены иммунные комплексы.
Классификация
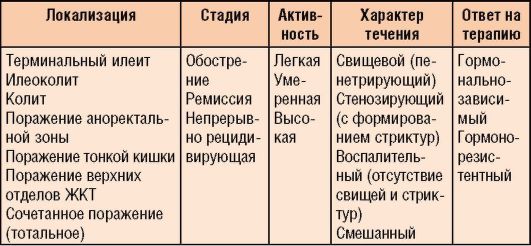
Классификация болезни Крона представлена в табл. 4-8.
Таблица 4-8. Классификация болезни Крона
Клиническая картина
Клиническая картина очень разнообразна и во многом зависит от локализации, тяжести, продолжительности и наличия рецидивов болезни. Для детей характерны более обширные и тяжелые поражения ЖКТ.
Классическая триада: боли в животе, диарея и потеря массы тела - отмечается у 25% больных.
Общие симптомы: слабость, повышенная утомляемость, увеличение температуры тела, часто волнообразного характера.
Кишечные симптомы: боль в животе, часто симулирующая острый аппендицит, диарея, анорексия, тошнота, рвота, вздутие кишечника, потеря массы тела. У детей часто отмечаются абдоминальные боли, а у взрослых - диарея.
Потеря массы тела обусловлена сначала анорексией в результате усиления боли после приема пищи, в запущенных случаях - синдромом мальабсорбции, развивающимся как после хирургических вмешательств, так и в результате распространенности процесса, при котором нарушается всасывание жиров, белков, углеводов, витаминов (A, B12, D) и микроэлементов. Нарушения роста к моменту постановки диагноза болезни Крона отмечаются у 10-40% детей.
Внекишечные проявления: артропатии (артралгия, артрит), узловатая эритема, гангренозная пиодермия, афтозный стоматит, поражения глаз (увеит, ирит, иридоциклит, эписклерит), ревматоидный артрит (серонегативный), анкилозирующий спондилоартрит, сакроилеит, остеопороз, остеомаляция, псориаз и т.д.
Хирургические осложнения представлены на рис. 4-17. Они включают:
• прободение стенки кишки с развитием внутрибрюшинных абсцессов, перитонита, внутренних и наружных свищей, стриктур, брюшных спаек;
• сужение просвета кишки (стриктуры) и кишечная непроходимость;
• гастродуоденальное кровотечение;
• токсический мегаколон;
• абдоминальный инфильтрат;
• анальные трещины;
• свищи (кишечно-кожные, межкишечные).
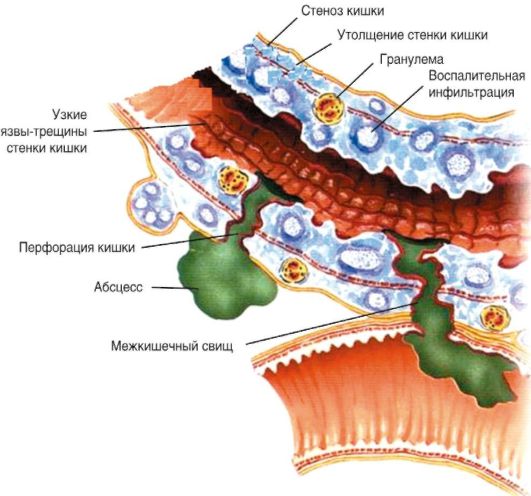
Рис. 4-17. Хирургические осложнения болезни Крона
Диагностика
В анализе крови определяются гиперлейкоцитоз, высокая СОЭ, нормохромно-гипохромная нормоцитарная анемия. Возможны снижение уровня железа, фолиевой кислоты, витамина B12, гипоальбуминемия как результат нарушения всасывания в кишечнике, гиполипидемия, гипокальциемия, повышение С-реактивного белка.
Высокочувствительным и специфичным показателем является уровень кальпротектина в кале. Этот белок продуцируется нейтрофилами слизистой оболочки кишечника. Уровень кальпротектина более 130 мг/кг стула отражает активность воспаления в слизистой оболочке кишечника, а также является предиктором близкого обострения у пациентов с болезнью Крона в фазе ремиссии.
При исследовании желудочной секреции обнаруживают ахлоргидрию.
Золотым стандартом диагностики болезни Крона является илеоколоноскопия (осмотр всей толстой кишки и терминального, или конечного, отдела подвздошной кишки). Обязательным условием является забор не менее 2 биоптатов из отделов толстой кишки и подвздошной кишки (как пораженных, так и интактных) с последующим их гистологическим исследованием.
При эзофагогастродуоденоскопии при болезни Крона с поражением желудка и ДПК обнаруживают регионарное (прерывистое) поражение слизистой оболочки, плотные розоватые возвышения с эрозией в центре на фоне атрофичной слизистой оболочки антрального отдела желудка, полипоподобные изменения слизистой оболочки ДПК, покрытые желтовато-белым налетом (вид булыжной мостовой) (рис. 4-18, а). При биопсии выявляют атрофический гастрит и гранулемы. Характерные для болезни Крона гранулемы (см. рис. 4-17) состоят из эпителиоидных клеток и гигантских многоядерных клеток типа Пирогова-Лангханса.
Наиболее типичной рентгенологической картиной поражения желудка и ДПК являются деформация антрального отдела, инфильтрация и ригидность стенки органа, сужение просвета, вялая перистальтика. Позже складки слизистой оболочки желудка также приобретают вид булыжной мостовой. КТ проводят, когда имеются внутрибрюшинные абсцессы, пальпируемая масса в правой подвздошной области, увеличение лимфатических узлов брыжейки.
Диагноз должен быть подтвержден эндоскопически и морфологически и/или эндоскопически и рентгенологически.
Патоморфология
Патоморфология характеризуется трансмуральным, т.е. затрагивающим все слои пищеварительной трубки, воспалением, лимфаденитом, образованием язв и рубцов стенки кишки. Язвы создают сходство с булыжной мостовой (рис. 4-18, б). Могут встречаться одиночные или многочисленные псевдополипы, которые образуют так называемые мостики. Граница между непораженным и пораженным участками может быть довольно четкой.
При гистологическом исследовании слизистая оболочка замещена отечной грануляционной тканью, инфильтрированной полинуклеарами. В подслизистом слое определяются склероз, отек, обилие сосудов с суженными просветами, скопления эпителиоидных и гигантских клеток без казеозного распада (рис. 4-18, в). Здесь же обнаруживают гранулемы. Мышечный слой утолщен, состоит из мышечных узлов, разделенных интерстициальным склерозом.
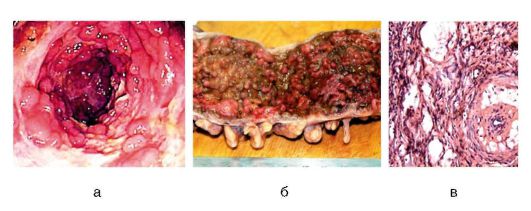
Рис. 4-18. «Булыжная мостовая»: а - ДПК при эндоскопическом исследовании; б - макропрепарат толстой кишки; в - микропрепарат: фиброз тканей, сужение просвета стенок артерии толстой кишки (окраска гематоксилин-эозином; χ 100)
Дифференциальная диагостика
Дифференциальную диагностику болезни Крона проводят с большим количеством инфекционных и неинфекционных хронических диарей, синдромом нарушения всасывания в кишечнике, недостаточностью питания (табл. 4-9).
Таблица 4-9. Дифференциальная диагностика болезни Крона с различными заболеваниями
Гистологическая картина болезни Крона имеет сходство с саркоидозом ввиду наличия характерных гранулем, которые наблюдаются и при туберкулезе. Но, в отличие от последнего, при болезни Крона в бугорках никогда не бывает творожистого распада.
Отличия болезни Крона и НЯК описаны в табл. 4-10.
Таблица 4-10. Дифференциальная диагностика болезни Крона и НЯК
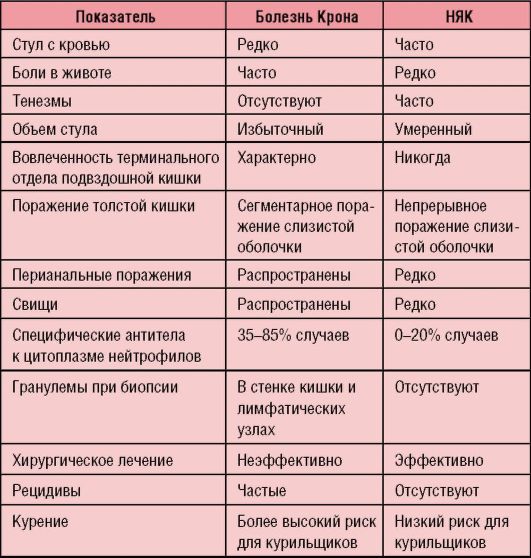
Лечение
Лечение неосложненной болезни Крона с локализацией в желудке и ДПК преимущественно консервативное. Общие принципы терапии следующие.
• Лечение детей должно носить более агрессивный характер с ранним назначением иммуномодуляторов.
• Глюкокортикоиды (преднизолон) применяют только для индукции ремиссии, но не для ее поддержания.
• Энтеральное питание, возможно, более эффективно при впервые выявленной болезни, чем при рецидивирующем течении. При тяжелом течении болезни с развитием гипопротеинемии, электролитных нарушений проводят внутривенные инфузии растворов аминокислот, альбумина, плазмы, электролитов.
Инфликсимаб эффективен как для индукции ремиссии у детей с болезнью Крона, рефрактерной к проводимой терапии, включая рефрактерную свищевую форму, так и для поддержания ремиссии.
В условиях стационара назначают глюкокортикоиды; инфликсимаб (ремикейд*) - селективный антагонист фактора некроза опухоли человека, СД - 5 мг/кг; иммуномодуляторы. При легких и среднетяжелых формах для поддержания ремиссии применяют препараты 5-аминосалициновой кислоты: сульфасалазин, месалазин (салазопиридазин*), салозодиметоксин*.

Для поддержания ремиссии целесообразно применение азатиоприна или 6-меркаптопурина. Препараты рекомендуют на раннем этапе терапии преднизолоном как часть схемы терапии у детей с впервые выявленной болезнью Крона. Для поддержания ремиссии у больных, которые резистентны или не переносят азатиоприн или 6-меркаптопурин, возможно применение метотрексата, при илеоколите - метронидазола (трихопол*, флагил*) по 1,0-1,5 г/сут в сочетании с преднизолоном или салазопиринами.
Назначают успокаивающие и холинолитические средства, ферменты, витамины, антибиотики (в случае присоединения инфекции), симптоматическую терапию.
Хирургическое лечение предпринимается в случаях, когда невозможно исключить опухолевый процесс, при нарушении эвакуации из желудка в результате стеноза или профузном кровотечении.
Профилактика
Первичная профилактика предусматривает рациональное, полноценное, соответствующее возрасту и индивидуальным возможностям ЖКТ питание; предупреждение и последовательное лечение острых кишечных инфекций, паразитарных заболеваний, а также другой патологии органов пищеварения.
Больные дети наблюдаются по IV-V группе диспансерного учета, обучаются на дому, на них оформляется инвалидность.
Прогноз
Прогноз для выздоровления неблагоприятный, для жизни - зависит от тяжести болезни. У детей возможно достижение длительной клинической ремиссии; хирургическое лечение применяют очень редко. У взрослых болезнь имеет рецидивирующее течение, смертность в 2 раза выше по сравнению с таковой в здоровой популяции.