Эндокринная регуляция. Биохимические и физиологические аспекты : учеб. пособие / А.Н. Смирнов ; под ред. В.А. Ткачука - 2009. - 368 с.
|
|
|
|
ГЛАВА 11. ЭНЕРГООБМЕН
МАКРОЭРГИ
Многие реакции биосинтеза, транспорт ионов и сопряженный транспорт ряда низкомолекулярных соединений через мембраны, мышечное сокращение протекают со значительными изменениями свободной энергии. Источниками этой энергии служат так называемые макроэрги - соединения, при гидролизе которых убыль свободной энергии составляет 5 ккал/моль или более. Разность в величинах свободной энергии исходных и конечных продуктов служит движущей силой реакции, и реакция тем интенсивнее, чем выше эта разность. Примеры наиболее распространенных макроэргов и образующихся из них промежуточных соединений представлены на рис. 11-1.
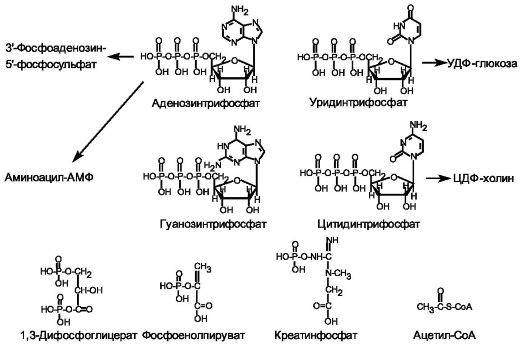 Рис. 11-1. Наиболее распространенные макроэрги
Рис. 11-1. Наиболее распространенные макроэрги
Основная часть макроэргов образуется через аденозинтрифосфат (АТФ), который синтезируется главным образом в митохондриях из аденозиндифосфата (АДФ) и неорганического фосфата за счет энергии, высвобождающейся при окислении кислородом поступающих в митохондрии субстратов. Небольшим, но физиологически важным источником АТФ служит гликолиз. Преобладающими субстратами для образования АТФ в митохондриях служат восстановленный никотинамидадениндинуклеотид (НАДН) и отчасти его фосфорилированный аналог - НАДФН.
Восстановленный НАД образуется преимущественно в митохондриях в цикле лимонной кислоты (цикле Кребса) при окислении ацетата, являющегося общим промежуточным продуктом распада углеводов, липидов и белков, а также в ходе β-окисления жирных кислот. Восстановленный НАДФ образуется при окислении глюкозы по пентозофосфатному пути и малата под действием малик-фермента.
И в реакциях образования восстановленных НАД и НАДФ, и в реакциях окисления этих субстратов с сопряженным фосфорилированием АДФ, и в реакциях гликолиза используется принцип квантования энергии, позволяющий совместить достижение достаточно высокой отдачи энергии в форме макроэргов с достаточно высокой скоростью этих процессов.
Образование АТФ происходит в митохондриях F1F0 АТФ-синтазным комплексом. Движущей силой для синтеза АТФ служит перемещение протонов через данный комплекс по градиенту концентрации извне внутрь митохондрии. Сам градиент концентрации протонов поддерживается цепью переноса электронов за счет энергии окисления НАДН. Комплекс F1F0 (F1 = α3β3γδε; F0 = ab2c10-15) напоминает электродвигатель/электрогенератор, в котором связывание протона субъединицей c комплекса вызывает вращение роторной части комплекса, локализованной во внутренней митохондриальной мембране. Механическая энергия вращения далее преобразуется в химическую энергию эфирной связи фосфата в АТФ каталитическими субъединицами β АТФ-синтазы, опосредованно связанными c субъединицами c. Присоединение и отделение протонов происходят с участием статорной субъединицы α комплекса. На один оборот ротора приходится перемещение 10 -15 протонов и образование до трех молекул АТФ. Ротор может вращаться со скоростью 150 об/сек.
Транспортировка макроэргов в клетке. Скорость доставки макроэргических соединений от места их образования до места потребления
и возвращения продуктов гидролиза АТФ (АДФ, Pi и Н+) к месту биосинтеза АТФ должна быть сопоставима со скоростью гидролиза АТФ АТФазами.
Частичное решение данной проблемы заключается в миграции митохондрий к местам потребления АТФ. Это, однако, не решает проблему полностью, поскольку простая диффузия АТФ и продуктов его гидролиза требовала бы значительных градиентов концентрации этих веществ, сопровождалась бы ингибированием АТФаз продуктами и рассеянием энергии (большим изменением энтальпии, - ΔΗ).
Проблема решается на основе принципа векторного лигандного проведения, заключающегося в создании цепи быстро уравновешивающихся реакций, катализируемых прежде всего креатинкиназой и аденилаткиназой («фосфорильных проводов»). Образующиеся лиганды «толкают» соседние лиганды, что обеспечивает распространение «волны потока» через ферменты (рис. 11-2). Таким образом, лиганды не движутся по всей длине пути переноса энергии, и этот процесс оказывается значительно более быстрым и энергетически выгодным по сравнению с диффузией. При этом градиенты концентраций лигандов оказываются минимальными, т.е. в различных частях клетки уровень АТФ приблизительно одинаков. Данный механизм, очевидно, функционирует не только в цитоплазме, но и внутри митохондрий при обмене нуклеотидов между матриксом, межмембранным пространством и окружающей цитоплазмой.
Креатинкиназа катализирует обратимую реакцию обмена остатками фосфата в парах АТФ - креатин и фосфокреатин - АДФ и служит главной системой транспорта макроэргического фосфата в клетках с высоким энергообменом (скелетная мышца, сердце, мозг, сперматозоиды).
Известно несколько изоформ креатинкиназы (CK), две из которых (мышечного типа, M-CK, и мозгового типа, B-CK) являются раство-
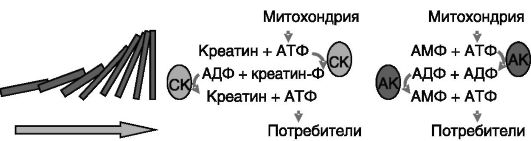 Рис. 11-2. Распространение «волны потока» АТФ: CK - креатинкиназа; AK - аденилаткиназа
Рис. 11-2. Распространение «волны потока» АТФ: CK - креатинкиназа; AK - аденилаткиназа
римыми и локализованы в цитоплазме. Способны формировать гомо- и гетеродимеры MM (скелетная мышца, миокард), MB (миокард) и BB (многие ткани, особенно мозг). Две другие изоформы локализуются на внешней стороне внутренней мембраны митохондрий. СК представляют собой октамеры, построенные из четырех гомодимеров. Саркомерная изоформа (S-MtCK) характерна для сердца и сердечной мышцы, повсеместно распространенная изоформа (U-MtCK) обнаруживается в остальных тканях.
Аденилаткиназа (АК) катализирует обратимую реакцию образования АТФ и АМФ из двух молекул АДФ. Известно не менее пяти изоформ фермента.
Мономерная изоформа AK1 локализована в цитоплазме и является наиболее распространенной. Недостаточность фермента служит одной из причин гемолитической анемии. Цитоплазматическая мономерная изоформа AK5 характерна для мозга. В качестве донора фосфатных групп может использовать АТФ и ГТФ, а акцептора - АМФ и ЦМФ. Изоформы AK3 и AK4 локализуются в матриксе митохондрий, причем AK4 характерна для пирамидальных нейронов гиппокампа. Изоформа 2 локализуется в пространстве между внутренней и наружной мембранами митохондрий. Экспрессируется повсеместно, и особенно интентенсивно - в сердце. В миофибриллах мышечных клеток, а также в других клетках формируют линейные полимерные структуры, структурно обеспечивающие направленный транспорт энергии. Тренировка мышц ведет к повышению активности аденилаткиназы.
Гликолитическая транспортная система. Энергия, затраченная на фосфорилирование глюкозы и фруктозо-6-фосфата, может быть возвращена в форме АТФ в реакции, катализируемой пируваткиназой. Обратимые реакции, катализируемые глицеральдегид-3-фосфатде- гидрогеназой (ГАФДГ) и фосфоглицераткиназой (PGK), могут служить дополнительным путем транспортировки энергии и переноса Pi, NADH и АДФ в митохондрии.
Выявлены адапторные белки или белки лесов, обеспечивающие пространственную организацию ферментов, участвующих в формировании путей транспортировки энергии.
Карбоангидраза (CA) катализирует обратимую реакцию образования из СО2 и воды угольной кислоты, которая дает протоны и HCO3 - для биосинтезов и Н+-АТФаз. Выявлены многочисленные изозимы CA, различающиеся по кинетическим свойствам, регуляции, внутриклеточной локализации. CA I-III локализованы в цито-
плазме, CA IV, IX и XII - на плазматической мембране, CA VA и CA VB - в митохондриях, а CA VI представляет собой секретируемую форму фермента. Кластеризация фермента вдоль мембран и миофибрилл облегчает внутриклеточный транспорт CO2 и H+, и, в частности, обеспечивает однородность pH внутри клетки и удаление протонов от АТФаз.
Полагают, что доставка АТФ облегчается CK, AK и ферментами гликолитического пути, включая гексокиназу (HEX), пируваткиназу (PK), 3-фосфоглицераткиназу (PGK). Удаление АДФ осуществляется CK, AK и PGK. Транспортировка Pi катализируется глицеральдегид-3- фосфатдегидрогеназой (GAPDH). Удаление H+ облегчается CK и CA.
Нуклеозиддифосфаткиназа (NDPK) катализирует обратимую реакцию переноса γ-фосфата с АТФ на нуклеозид-5'-дифосфаты, что обеспечивает необходимый уровень отличных от АТФ нуклеозидтрифосфатов в местах их потребления (синтеза белка, нуклеиновых кислот, сложных липидов, гликогена и т.д.). Выявлено несколько изоформ фермента с локализацией в митохондриях, цитоплазме, плазматической мембране и клеточном ядре.
ИНТЕГРАЛЬНЫЕ ПОКАЗАТЕЛИ ЭНЕРГООБМЕНА
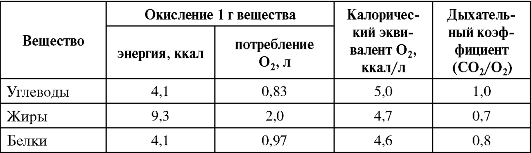
Методами прямой (по выделенному теплу и испаренной воде) и непрямой (по газообмену) калориметрии, а также путем измерения теплотворной способности продуктов питания и экскрементов установлены соотношения между количеством и типом потребляемых продуктов, расходом кислорода и образованием углекислого газа при различных формах активности целого организма (табл. 11-1). Данные подходы применимы и к анализу деятельности отдельных органов и тканей.
Таблица 11-1. Энергетическая ценность питательных веществ
 В
качестве показателя энергетических возможностей организма применяют
факториальный индикатор обмена, равный соотношению энергозатрат при
максимальной активности и в состоянии покоя. У спортсменов этот
показатель выше, чем у нетренированных людей.
В
качестве показателя энергетических возможностей организма применяют
факториальный индикатор обмена, равный соотношению энергозатрат при
максимальной активности и в состоянии покоя. У спортсменов этот
показатель выше, чем у нетренированных людей.
Индуцированный пищей термогенез. Прием пищи сопровождается повышением энергозатрат («специфическое динамическое действие пищи»), которое связано с энергозависимыми процессами всасывания питательных веществ в кишечнике и начальных этапов их метаболизма и запасания. Индуцированный пищей термогенез продолжается несколько часов и на протяжении дня не заканчивается полностью до следующего приема пищи (рис. 11-3). В среднем на индуцированный пищей термогенез затрачивается приблизительно 10% от энергетической ценности пищевых продуктов, причем затраты различаются при приеме разных продуктов: жир - 0-3%; углеводы - 5-10%; белки - 20-30%; алкоголь - 10-30%. Индуцируемый белком повышенный термогенез эффективен в диетах для похудания и сохранения пониженной массы тела по двум причинам: значительная часть энергии белковой пищи рассеивается в виде тепла после еды, а повышение температуры воспринимается как сигнал сытости.
Значительную роль в индуцированном пищей термогенезе играет инсулин. Эта форма термогенеза подавлена у больных с инсулинорезистентностью. По-видимому, основным местом индуцированного
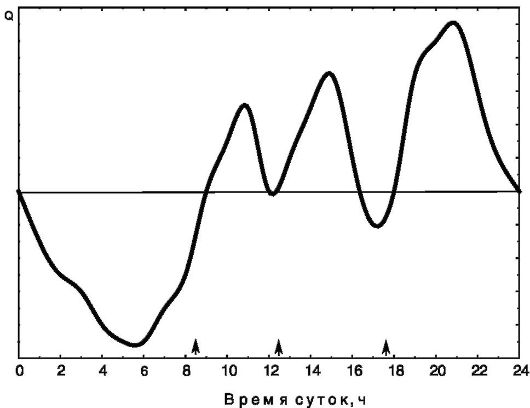 Рис. 11-3. Индуцированный приемами пищи (стрелки) термогенез
Рис. 11-3. Индуцированный приемами пищи (стрелки) термогенез
пищей термогенеза служит скелетная мышца, в которой стимулированный поступающей глюкозой и гормонами желудочно-кишечного тракта инсулин повышает захват глюкозы, ее окисление и отложение в виде гликогена, о чем свидетельствуют данные, полученные при избирательной делеции рецептора инсулина в скелетных мышцах мыши. Другой путь (через гипоталамус) влияния инсулина включает его опосредованное симпатической нервной системой вазодилататорное действие на скелетную мышцу, способствующее захвату глюкозы.
ТЕРМОРЕГУЛЯЦИЯ
Постоянство температуры тела (точнее, его центральной части) дает млекопитающим такое важное преимущество по отношению к пойкилотермным животным, как относительная независимость от температуры окружающей среды. Следует иметь в виду, однако, что изотермия является относительной: во-первых, температура разных частей тела может существенно различаться (от 24,5 °С в коже пальцев ног до 38,5 °С в печени); во-вторых, имеются колебания температуры тела во времени (от 36,4 °С в 3 - 4 часа утра до 37,1 °С к 16 - 18 часам вечера), в зависимости от физической активности, фазы полового цикла (подъем температуры приблизительно на 0,5 °С соответствует овуляции).
Постоянство температуры тела у теплокровных достигается ценой значительно более высоких энергозатрат на выполнение одной и той же физиологической или физической работы по сравнению с холоднокровными животными (рис. 11-4), т.е. с точки зрения энергетики
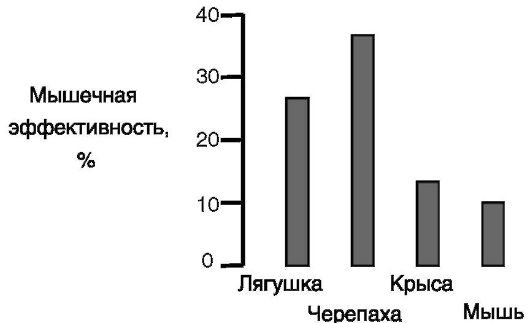 Рис. 11-4. Термодинамическая эффективность скелетных мышц у холоднокровных и теплокровных животных: (работа/ΔH) * 100%
Рис. 11-4. Термодинамическая эффективность скелетных мышц у холоднокровных и теплокровных животных: (работа/ΔH) * 100%
теплокровные являются менее совершенными машинами, и чем мельче животное, тем большую часть потребленной с пищей энергии оно вынуждено затрачивать на поддержание температуры тела.
Источниками тепла служат экзотермические реакции метаболических превращений веществ, которые условно делят на две группы: реакции, ведущие к образованию АТФ («первичное тепло»), и реакции, идущие с расходованием АТФ, такие как реакции биосинтеза, мышечное сокращение, работа ионных насосов и транспортеров и т.д. («вторичное тепло»; рис. 11-5). Оба типа источников тепла могут быть объектами регуляции, обеспечивающей постоянство температуры тела.
Главным сенсором температуры тела служит так называемый гипоталамический термостат - группа нейронов, активность которых чувствительна даже к очень небольшим изменениям температуры крови, поступающей в мозг. Периферические терморецепторы преимущественно участвуют в локальной терморегуляции. Гипоталамический термостат может быть «перенастроен». Например, пирогены при инфекциях и воспалительных процессах, прогестины при беременности или тиреоидные гормоны при холодовой адапта-
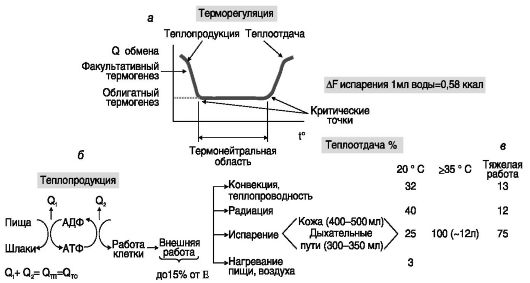 Рис. 11-5. Терморегуляция:
Рис. 11-5. Терморегуляция:
а - энергозатраты при изменениях температуры окружающей среды; б - теплопродукция формируется из первичного тепла (Q1), выделяющегося при образовании макроэргов, и вторичного тепла (Q2), выделяющегося при расходовании макроэргов; в - структура теплоотдачи при разной температуре окружающей среды и работе
ции способны повышать установочную точку поддерживаемой температуры тела.
Постоянство температуры тела при изменениях температуры окружающей среды достигается несколькими механизмами. В так называемой термонейтральной области (см. рис. 11-5) теплопродукция и теплоотдача уравновешены за счет поведенческих (смены места пребывания и позы) и вегетативных (укладка шерсти, изменение характера кровотока) реакций без существенных изменений энергообмена. За пределами термонейтральной области, ограниченной нижней и верхней «критическими точками», поддержание постоянства температуры требует повышения энергозатрат. При повышенной температуре дополнительная энергия расходуется на испарение воды, выделяющейся с потом и/или выдыхаемым воздухом. При пониженной температуре энергозатраты увеличиваются за счет недрожательного и дрожательного термогенеза. У мелких млекопитающих недрожательный термогенез осуществляется преимущественно за счет активизации бурого жира под действием адренергической стимуляции. У более крупных животных, практически лишенных бурого жира, а также у птиц усиление и недрожательного, и дрожательного термогенеза вызывается преимущественно интенсификацией обменных процессов в скелетных мышцах. Энергетически более выгоден недрожательный термогенез в буром жире, поскольку при активации мышц происходит дополнительная потеря тепла через поверхностно расположенные сосуды, снабжающие мышцы кровью. В условиях длительного пребывания животного при повышенной или пониженной температуре происходит адаптация уровня экспрессии ферментов и других белков, участвующих в терморегуляции.
Рассопрягающие белки
Движущей силой биосинтеза АТФ в митохондриях является градиент протонов с двух сторон внутренней мембраны митохондрий, возникающий в результате работы цепи переноса электронов с окисляемых субстратов (например, НАДН) на кислород воздуха. Возвращение протонов извне через внутреннюю мембрану через F0F1- комплекс сопряжено с фосфорилированием АДФ до АТФ, катализируемым АТФ-синтазой. Максимально достижимая степень сопряжения между фосфорилированием АДФ и окислением НАДН равна 3:1. Реально степень сопряжения оказывается более низкой из-за «утечки» протонов через внутреннюю мембрану митохондрий, минуя
комплекс F0F1, что ведет к рассеиванию части энергии протонного градиента в форме тепла. Установлено два основных пути «утечки» протонов: конститутивная простая диффузия через липидный бислой митохондриальной мембраны и регулируемый транспорт посредством рассопрягающих белков (uncoupling proteins, UCPs; рис. 11-6).
Утечка протонов обеспечивает около 20-25% термогенеза в состоянии покоя (основного или стандартного энергообмена). В свободных условиях расход АТФ возрастает, поток протонов через АТФ-синтазу увеличивается, и доля утечки протонов снижается до приблизительно 15-20% от энергообмена. В условиях необходимости повышения термогенеза (выхода гибернантов из спячки, холодовой адаптации) степень разобщения фосфорилирования и окисления возрастает, причем утечка протонов увеличивается преимущественно за счет повышения экспрессии UCP.
Клонировано пять UCPs - UCP1-UCP5. UCP1 экспрессируется исключительно в буром и белом жире, UCP2 экспрессируется многими тканями, включая белый и бурый жир, сердечную и скелетную мышцы, почки, купферовские клетки печени, легкие, плаценту, β-клетки поджелудочной железы, клетки иммунной системы, мозг. UCP3 экспрессируется преимущественно в скелетной мышце и буром жире, а UCP4 и UCP5 - в мозгу. Хотя все указанные белки способны вызывать утечку протонов, лишь в отношении UCP1 строго установлено, что данная способность играет роль в адаптации термогенеза.
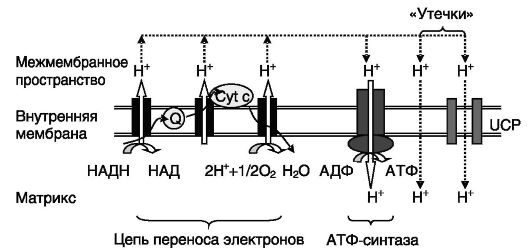 Рис. 11-6. UCPs формируют шунт для протонов в обход АТФ-синтазы, что приводит к рассеиванию части энергии протонного градиента
Рис. 11-6. UCPs формируют шунт для протонов в обход АТФ-синтазы, что приводит к рассеиванию части энергии протонного градиента
Так, у мышей с нокаутированным геном UCP1 возможности холодовой адаптации резко снижены, а у трансгенных мышей с экспрессией UCP1 в белом жире или скелетных мышцах повышается устойчивость к развитию ожирения. Труднее объяснить отсутствие склонности к ожирению у мышей с нокаутированным геном UCP1. Не исключено, что это отчасти связано с компенсаторным повышением экспрессии UCP2 в буром жире.
• Нокаут генов UCP2 и UCP3 у мышей практически не сказывается на энергообмене, хотя их гиперэкспрессия у трансгенных животных сопровождается ожидаемым повышением термогенеза. По-видимому, термогенез не является основной физиологической функцией данных белков, но, судя по характеру регуляции их экспрессии, оба белка связаны с энергообменом. Не исключено, что отсутствие эффекта нокаута UCP2 и UCP3 связано с компенсацией их утраты за счет других источников тепла. Так, одновременный нокаут UCP3 и митохондриальной глицерофосфатдегидрогеназы, обеспечивающей энергетически невыгодную доставку восстановительных эквивалентов (ФАДН2 вместо НАДН Н+) в митохондрии, значительно снижает возможности холодовой адаптации, хотя по отдельности эти мутации оказывают слабое влияние на энергообмен.
На основании того факта, что мыши с нокаутированным геном UCP2 устойчивы к заражению токсоплазмой (внутриклеточный паразит, летальный для интактных животных), а макрофаги генетически модифицированных животных продуцируют повышенное количество ракционноспособных производных кислорода, оказывающих цитотоксическое действие, было высказано предположение о защитной функции UCP2. Известно, что высокое соотношение АТФ/АДФ сопровождается повышенным образованием свободных радикалов, повреждающих клетку. Утечка протонов за счет UCP2 может таким образом защищать клетку от повреждений. Сходную функцию выполняют и другие UCP.
Анализ локализации экспрессии UCP2 в мозгу показал, что этот белок может быть связан с центральными механизмами регуляции энергообмена. Так, UCP2 обнаружен в гипоталамусе (супрахиазматическом, дорсомедиальном, вентромедиальном, аркуатном ядрах), таламусе, стволе (моторном ядре блуждающего нерва), гиппокампе и мозжечке. В пределах гипоталамуса UCP2 обнаруживается в нейронах, связанных с развитием стрессорной реакции, регуляцией пищевого поведения и термопродукции, в частности в кортиколиберин-
ергических нейронах, вазопрессинергических нейронах, нейронах, содержащих нейропептид Y и белок, родственный агути.
У мышей с нокаутированным геном UCP2 наблюдается повышение секреции инсулина и снижение уровня глюкозы в крови. Напротив, гиперэкспрессия UCP2 в β-клетках поджелудочной железы у трансгенных животных сопровождается снижением секреции инсулина. По-видимому, одним из механизмов участия UCP2 в регуляции энергообмена является его негативное влияние на секрецию инсулина, направляющего обменные процессы на запасание, а не на теплопродукцию.
UCP3, возможно, связан с обменом жирных кислот. Экспрессия UCP3 индуцируется голоданием, мышечными нагрузками, тиреоидными гормонами, т.е. факторами, повышающими уровень свободных жирных кислот в крови и утилизацию липидов. Предполагается, что UCP3 может способствовать выведению из митохондрий избытка жирных кислот в нейтральной и анионной форме (которые не могут быть утилизированы в митохондриях из-за отсутствия ацил-CoA-синтазы).
Главным стимулом термогенеза в буром жире служит активация симпатической нервной системы. В результате происходит гипертрофия и гиперплазия бурого жира, увеличиваются его кровоснабжение и метаболизирующая активность. Индукция экспрессии UCP1 в этих условиях играет важнейшую роль в термогенезе. Действие катехоламинов опосредуется в буром жире тремя типами бета-адренорецепторов (βΑΡν), широко распространенными β1 и β2 и специфичными для жировой ткани β3ΑΙΡ. В условиях пониженного термогенеза (при ожирении разной этиологии) экспрессия AR оказывается сниженной, что обусловливает низкую эффективность стимулирующего действия катехоламинов на термогенез. Избирательные агонисты β3ΑΡ способны нормализовать термогенез в этих условиях, в частности, за счет появления бурых адипоцитов среди адипоцитов белого жира и индукции UCP1. Механизм индукции включает высвобождение свободных жирных кислот из триацилглицеридов под действием гормонзависимой липазы, активацию жирными кислотами PPAR и опосредованную другими транскрипционными факторами гормональную индукцию экспрессии UCP1 (рис. 11-7). В отсутствие тиреоидных гормонов норадреналин оказывает весьма слабое (2-3 кратное) стимулирующее действие на экспрессию. Тиреоидные гормоны также практически неэффективны в денервированном буром жире, но при наличии обоих факторов (тиреоидных гормонов и катехоламинов) стимуляция может быть 18 - 20-кратной. Следует отметить синергизм
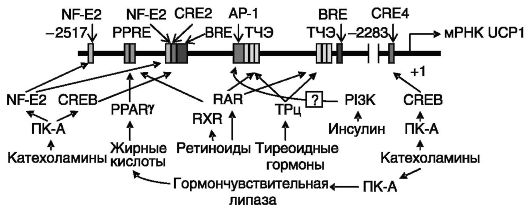 Рис. 11-7. Регуляция
экспрессии рассопрягающего белка UCP1: NF-E2 - ядерный фактор семейства
E2; CREB - белок, связывающий цАМФчувствительный элемент (CRE); RXR -
рецептор X ретиноидов; RAR - рецептор ретиноевой кислоты; тРц - рецептор
тиреоидных гормонов; PI3K - фосфатидилинозитид-3-киназа; PPRE -
PPAR-чувствительный элемент; BRE - регуляторный элемент бурого жира; ТЧЭ
- тиреоидчувствительный элемент
Рис. 11-7. Регуляция
экспрессии рассопрягающего белка UCP1: NF-E2 - ядерный фактор семейства
E2; CREB - белок, связывающий цАМФчувствительный элемент (CRE); RXR -
рецептор X ретиноидов; RAR - рецептор ретиноевой кислоты; тРц - рецептор
тиреоидных гормонов; PI3K - фосфатидилинозитид-3-киназа; PPRE -
PPAR-чувствительный элемент; BRE - регуляторный элемент бурого жира; ТЧЭ
- тиреоидчувствительный элемент
в действии на UCP1 гормонов, обычно оказывающих физиологически противоположные эффекты.
Важно отметить, что экспрессия UCP1 в жировой ткани является необходимым, но не достаточным фактором термогенеза, физиологическим стимулом для которого является активация β-AR.
Тиреоидные гормоны и симпатическая стимуляция бурого жира связаны между собой не только на уровне экспрессии UCP1. При гипотиреозе компенсаторно возрастает активность симпатической нервной системы, повышающей экспрессию в буром жире дейодиназы 2, которая за счет усиленного превращения тироксина в трийодтиронин обеспечивает эффективное действие тиреоидных гормонов даже при снижении их уровня в кровотоке до 30% от нормального. И наоборот, гипертиреоз подавляет активность симпатической нервной системы и, кроме того, индуцирует деградацию дейодиназы 2, ослабляя тем самым синергизм между двумя системами регуляции (рис. 11-8).
ТИРЕОИДНЫЕ ГОРМОНЫ И ЭНЕРГООБМЕН
Стимулирующее действие тиреоидных гормонов на термогенез является эволюционным приобретением млекопитающих. Известно, что гипотиреоз сопровождается пониженным энергообменом, пони-
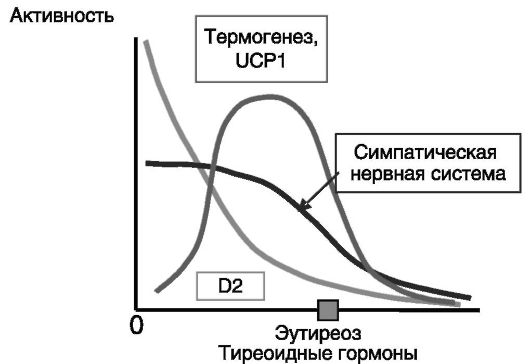 Рис. 11-8. Синергизм тиреоидных гормонов и симпатической стимуляции в индукции термогенеза в буром жире
Рис. 11-8. Синергизм тиреоидных гормонов и симпатической стимуляции в индукции термогенеза в буром жире
женным потреблением кислорода, склонностью к ожирению, понижением пролиферативной активности клеток. И напротив, для гипертиреоза характерны увеличенные энергозатраты и потребление кислорода и как следствие склонность к похуданию. Тиреоидные гормоны действуют на энергообмен на нескольких уровнях. В значительной мере эффекты гормонов связаны с модификациями митохондрий.
Нитроксидсинтаза. Один из установленных путей действия тиреоидных гормонов на функции митохондрий включает подавление экспрессии и ингибирование транслокации в митохондрии нейрональной NOS (nNOS). Образующийся при низком уровне тиреоидных гормонов NO, взаимодействуя с активными формами кислорода, вызывает нитрирование белков транспорта электронов, что ведет к ингибированию дыхания. Введение тиреоидных гормонов стимулирует замену нитрированных переносчиков электронов новосинтезированными белками, что обеспечивает растормаживание цепи переноса электронов и соответствующее увеличение потребления кислорода (рис. 11-9). Известно, что транслокация nNOS в митохондрии обеспечивается ее N-ацилированием и фосфорилированием, а также передислокацией заякоривающих белков.
Биосинтез белков. Тиреоидные гормоны стимулируют экспрессию широкого спектра белков митохондрий, участвующих в транспор-
те электронов и восстанавливающих эквивалентов в митохондрии, кодируемых как геномом митохондрии, так и ядерным геномом. При этом набор таких белков специфичен для определенной ткани.
Например, митохондриальная глицерол-3-фосфатдегидрогеназа, участвующая в транспорте восстанавливающих эквивалентов (Н+, е-) НАД(Ф)Н из цитоплазмы в митохондрию на комплекс III, индуцируется тиреоидными гормонами в скелетной мышце, где этот фермент обеспечивает основную часть переноса восстанавливающих эквивалентов, но не в печени, где транспорт осуществляется преимущественно другим, энергетически более выгодным челночным механизмом, с участием пары субстратов малат-аспартат (с доставкой восстанавливающих эквивалентов на комплекс I). В результате холодовая адаптация под действием тиреоидных гормонов в разных тканях происходит с вовлечением различающихся механизмов.
Индукция тиреоидными гормонами белков происходит в две стадии: на 1-й стадии (приблизительно через 6-8 ч) индуцируется экспрессия ряда генов, белковые продукты которых, как полагают, индуцируют экспрессию генов 2-й волны (приблизительно через 48 ч). Такими посредниками действия тиреоидных гормонов могут служить, в частности, ядерный респираторный фактор 1 (NRF-1) и
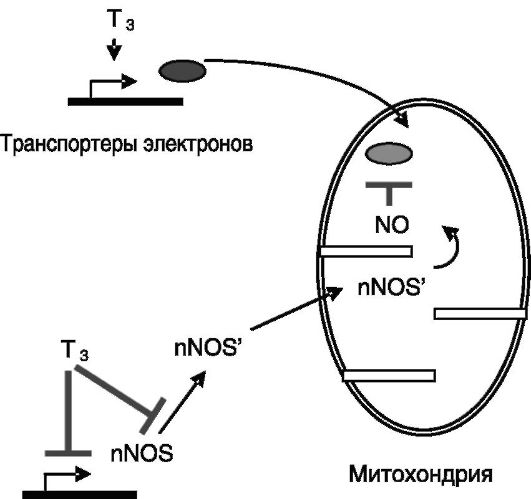 Рис. 11-9. Тиреоидные гормоны снимают ингибирующее действие NOS на дыхательную активность митохондрий
Рис. 11-9. Тиреоидные гормоны снимают ингибирующее действие NOS на дыхательную активность митохондрий
коактиватор 1 альфа PPARγ (PGC-Ια). В промоторах генов этих белков содержатся ГЧЭ, обеспечивающие прямую индукцию транскрипции тиреоидными гормонами, а в промоторах ряда вторичных генов (например, Cyt c, митохондриального транскрипционного фактора A - mtTFA) содержатся элементы, узнаваемые NRF-1, который действует с участием PGC-1a (рис. 11-10).
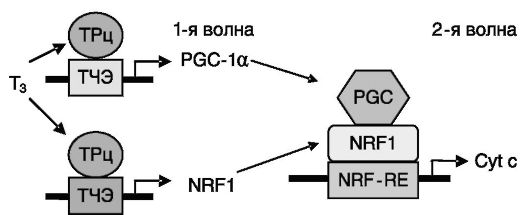 Рис. 11-10. Действие тиреоидных гормонов на многие митохондриальные белки является опосредованным
Рис. 11-10. Действие тиреоидных гормонов на многие митохондриальные белки является опосредованным
Тиреоидные гормоны и ионные насосы. Поиски механизмов, обеспечивающих холодовую адаптацию у крупных животных, практически лишенных бурого жира, показали, что отчасти адаптивное действие тиреоидных гормонов может быть связано со стимуляцией энергозатратной аккумуляции Ca2+ в саркоплазматическом ретикулуме скелетных мышц, причем этот механизм в большей мере связан с медленными мышцами (рис. 11-11). Тиреоидные гормоны стимули-
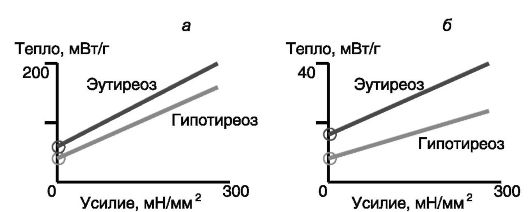 Рис. 11-11. Влияние тиреоидных гормонов на термогенез в покоящейся и работающей быстрой (а; extensor digitorum longus) и медленной (б; soleus) скелетной мышце мыши
Рис. 11-11. Влияние тиреоидных гормонов на термогенез в покоящейся и работающей быстрой (а; extensor digitorum longus) и медленной (б; soleus) скелетной мышце мыши
руют экспрессию зависимой от Ca2+ АТФазы саркоплазматического/ эндоплазматического ретикулума (SERCA1) и одновременно повышают экспрессию рианодиновых рецепторов, обеспечивающих утечку ионов кальция в цитоплазму. Расчеты показывают, что этот эффект тиреоидных гормонов может обеспечивать приблизительно 10% стимулирующего действия гормонов на термогенез в состоянии покоя и что эта доля может возрастать в работающей мышце (ср. наклоны кривых). Интересно отметить, что в отличие от грызунов скелетные мышцы человека содержат активирующую тироксин дейодиназу 2, что позволяет предполагать большую значимость от тиреоидных гормонов мышечного термогенеза у человека по сравнению с грызунами.
Изоформы рецепторов тиреоидных гормонов. Эксперименты с мышами с нокаутированным геном Т-Рца показывают, что через этот рецептор тиреоидные гормоны влияют (повышают) на установочную точку внутренней температуры тела на гипоталамическом уровне. Кроме того, Т-Рца необходим для индукции тиреоидными гормонами термогенеза в буром жире. В отсутствие Т-Рца компенсаторно проявляется другой механизм адаптации к холоду - через повышение термогенеза в скелетных мышцах. Блокировка лигандсвязывающей активности обоих рецепторов тиреоидных гормонов (Т-Рца и Т-Рц β) приводит к утрате толерантности к холоду, т.е. при низкой температуре такие животные не способны компенсаторно увеличивать термогенез до уровня, достаточного для поддержания постоянной температуры тела (рис. 11-12 - 11-14).
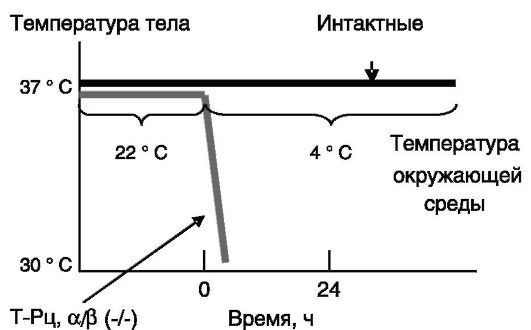 Рис. 11-12. Холодовая
адаптация зависит от тиреоидных гормонов и их рецепторов. Здесь и на
рис. 11-13 и 11-14: Т-Рцα/Р(-/-) - мыши с рецепторами α и β тиреоидных
гормонов, не способными связывать лиганды
Рис. 11-12. Холодовая
адаптация зависит от тиреоидных гормонов и их рецепторов. Здесь и на
рис. 11-13 и 11-14: Т-Рцα/Р(-/-) - мыши с рецепторами α и β тиреоидных
гормонов, не способными связывать лиганды
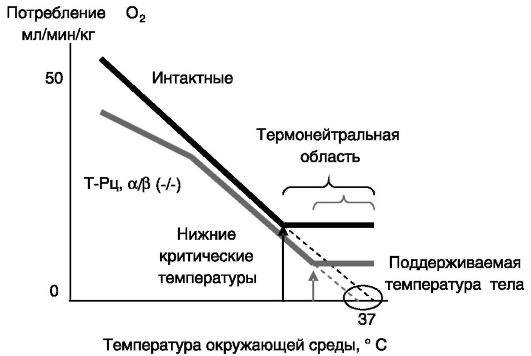 Рис. 11-13. Тиреоидные
гормоны через свои рецепторы повышают установочную точку температуры
тела, увеличивают энергозатраты для поддержания температуры тела и
расширяют термонейтральную область
Рис. 11-13. Тиреоидные
гормоны через свои рецепторы повышают установочную точку температуры
тела, увеличивают энергозатраты для поддержания температуры тела и
расширяют термонейтральную область
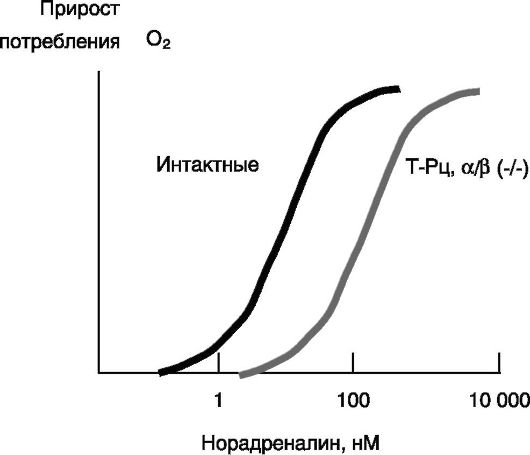 Рис. 11-14. Тиреоидные гормоны через свои рецепторы сенсибилизируют клетки бурого жира к действию норадреналина
Рис. 11-14. Тиреоидные гормоны через свои рецепторы сенсибилизируют клетки бурого жира к действию норадреналина
В буром жире экспрессируются оба рецептора тиреоидных гормонов, Т-Рца и Т-Рцβ. Избирательный агонист Т-Рцβ, GC-1, способен воспроизводить действие T3 на экспрессию рассопрягающего белка UCP-1. Однако индукция UCP-1 не является достаточной для адекватного термогенеза в ответ на адренергическую стимуляцию: только T3, но не GC-1 способен восстанавливать чувствительность бурого жира к норадреналину у гипотиреоидных животных (рис. 11-15). Это означает, что ведущую роль в сенситизации бурого жира к норадреналину играет Т-Рца.
Тиреоидные гормоны наряду с симпатической нервной системой, служат эффекторами в стимулирующем действии лептина на энергообмен.
Локальная продукция T3. Существенную роль в обеспечении тиреоидными гормонами холодовой адаптации играет локальная продукция в буром жире T3 из T4 под действием дейодиназы 2. При нокауте гена данного фермента у мышей способность животных поддерживать температуру тела при охлаждении снижается приблизительно так же, как при нокауте рецепторов тиреоидных гормонов или при гипотиреозе (см. выше), за счет снижения чувствительности бурого жира к адренергической стимуляции. Полагают, что локально образующийся T3 необходим для насыщения Т-Рца, сродство которого к гормону приблизительно в 4 раза ниже, чем сродство Т-Рц β (рис. 11-16).
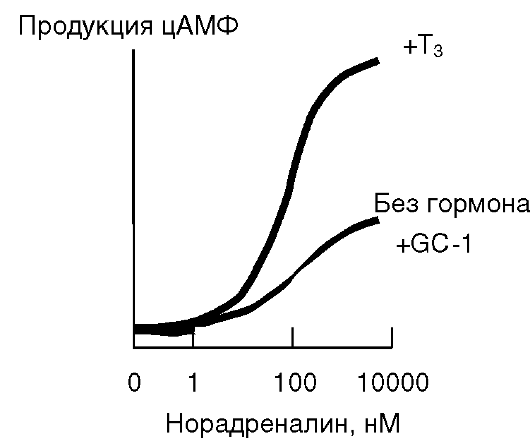 Рис. 11-15. Избирательный агонист Т-Рцβ (GC-1) не воспроизводит действие природного гормона T3 на восстановление чувствительности клеток бурого жира к адренергической стимуляции
Рис. 11-15. Избирательный агонист Т-Рцβ (GC-1) не воспроизводит действие природного гормона T3 на восстановление чувствительности клеток бурого жира к адренергической стимуляции
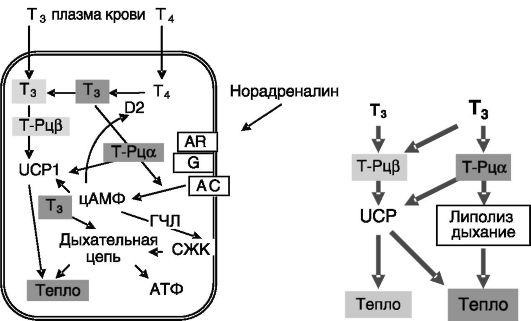 Рис. 11-16. Дейодиназа D2 в клетках бурого жира повышает уровень T3, необходимого для активации Т-Рца, сенсибилизирующего клетки к адренергической стимуляции:
Рис. 11-16. Дейодиназа D2 в клетках бурого жира повышает уровень T3, необходимого для активации Т-Рца, сенсибилизирующего клетки к адренергической стимуляции:
UCP1 - рассопрягающий белок 1; ГЧЛ - гормончувствительная липаза; AR - адренорецепторы (преимущественно подтипа β3); G - Gj-белок; AC - аденилатциклаза
Холодовая адаптация повышает уровень дезубиквитинилирующего фермента-1 , активирующего дейодиназу-2 в буром жире. Это дополняет эффект адренергической стимуляции на биосинтез дейо- диназы-2 de novo, увеличивая локальное образование T3 (рис. 11-17).
Как уже отмечалось, недрожательный термогенез в буром жире энергетически значительно эффективнее дрожательного термогенеза. В связи с этим холодовая адаптация животных с недостаточностью дейодиназы D2 происходит при заметной потере массы тела.
Помимо бурого жира тиреоидные гормоны повышают дыхательную активность митохондрий во многих других типах клеток, прежде всего клетках сердца, печени, скелетных мышц. Поскольку в этих тканях рассопрягающий белок UCP-1 не экспрессируется, а другие белки этого типа выполняют иные функции, то усиленное тиреоидными гормонами дыхание митохондрий ведет к образованию повышенного количества АТФ, который расходуется на усиление функциональной активности органа (например, повышение частоты сердечных сокращений или дрожательный тер-
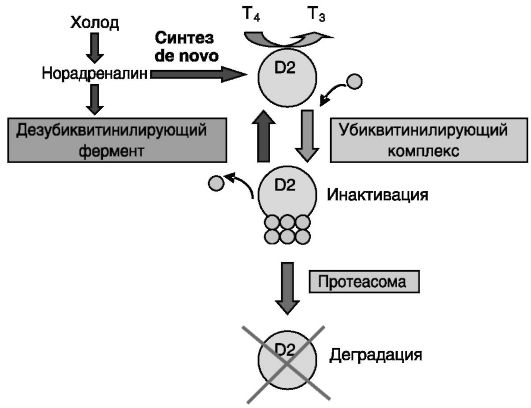 Рис. 11-17. Каталитическая реакция дейодирования T4 стимулирует убиквитинилирование и инактивацию дейодиназы D2
Рис. 11-17. Каталитическая реакция дейодирования T4 стимулирует убиквитинилирование и инактивацию дейодиназы D2
Норадреналин повышает активность дейодиназы D2, индуцируя ее синтез de novo и препятствуя ее деградации в протеасоме путем индукции дезубиквитинилирующего фермента 1. Ub - убиквитин
могенез) или на поддержание энергозатратных «бесполезных» циклов (таких, как перекачка ионов), что в конечном итоге приводит к термогенезу.
ГИПОТАЛАМИЧЕСКАЯ РЕГУЛЯЦИЯ ЭНЕРГООБМЕНА
Интенсивность энергообмена определяется не только температурными условиями окружающей среды, но и доступностью пищи. Так, при голодании в тканях адаптивно снижается экспрессия дейодиназы-2, что приводит к снижению локально образующегося T3 и соответственно уменьшению интенсивности обменных процессов и сохранению питательных веществ в организме. И напротив, увеличивающиеся жировые запасы при избытке пищи стимулируют секрецию адипоцитами лептина, который через активацию симпатико-
адреналовой системы и тиреоидной функции повышает термогенез, что ограничивает дальнейший рост массы тела. Однако связь между терморегуляцией и режимом питания осуществляется не только на уровне периферических тканей, но и на уровне ЦНС (рис. 11-18).
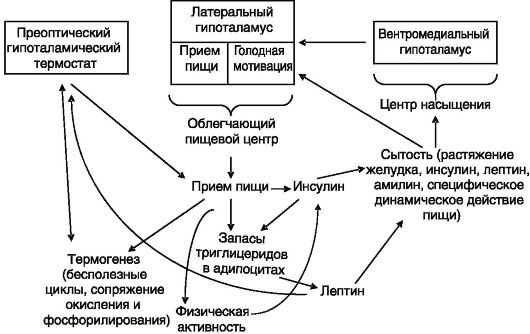 Рис. 11-18. Взаимосвязи центров терморегуляции и пищевого поведения
Рис. 11-18. Взаимосвязи центров терморегуляции и пищевого поведения
Гипоталамическая регуляция аппетита
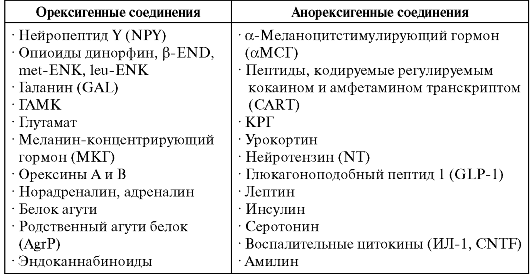
В регуляции пищевого поведения принимает участие целый ряд структур мозга, но базовые процессы протекают в гипоталамусе, куда поступает информация о внешних раздражителях, с рецепторов желудка, об уровне глюкозы и аминокислот в крови, об уровне гормонов и других сигнальных соединений, связанных с пищеварением и энергообменом. Принятие решения об изменении пищевого поведения и реализация этого решения осуществляются с участием множества сигнальных соединений, которые делятся на две основные группы: стимулирующие и подавляющие пищевое поведение (орексигенные и анорексигенные соединения; табл. 11-2).
Области мозга, связанные с регуляцией потребления пищи
Аркуатное ядро (ARC): экспрессирует мРНК многих орексигенных и анорексигенных пептидов. Терминали соответствующих нейронов идут в другие отделы мозга, в частности те, микроинъекции дан-
Таблица 11-2. Орексигенные и анорексигенные соединения
 ных
пептидов в которые вызывают изменения в потреблении пищи. Многие
нейроны ARC экспрессируют одновременно по меньшей мере два регулирующих
потребление пищи пептида (например, NPY и AgrP). Внутри ARC терминали
NPY-ергических нейронов обнаруживаются на телах GAL- и β-END-ергических
нейронов, терминали GAL-ергических нейронов - на телах β-END-ергических
нейронов. ARC не защищено гематоэнцефалическим барьером, что
обеспечивает возможность его регуляции соединениями, поступающими через
кровь и цереброспинальную жидкость.
ных
пептидов в которые вызывают изменения в потреблении пищи. Многие
нейроны ARC экспрессируют одновременно по меньшей мере два регулирующих
потребление пищи пептида (например, NPY и AgrP). Внутри ARC терминали
NPY-ергических нейронов обнаруживаются на телах GAL- и β-END-ергических
нейронов, терминали GAL-ергических нейронов - на телах β-END-ергических
нейронов. ARC не защищено гематоэнцефалическим барьером, что
обеспечивает возможность его регуляции соединениями, поступающими через
кровь и цереброспинальную жидкость.
Вентромедиальное ядро (VMN) и латеральный гипоталамус (LH): VMN чувствительно к орексигенным и анорексигенным соединениям. Его разрушение ведет к гиперфагии и ожирению («центр насыщения»). Терминали из VMN обнаружены в паравентрикулярном и дорзомедиальном ядрах. Через LH проходит переднемозговой пучок. Разрушение LH вызывает временную афагию, а электоростимуляция или микроинъекции орексигенных соединений - повышение потребления пищи («центр питания»).
Дорсомедиальное ядро (DMN): разрушение DMN слабо увеличивает потребление пищи. Микроинъекции орексигенных и анорексигенных соединений соответственно влияют на потребление пищи. Терминали из DMN обнаружены в VMN и паравентрикулярном ядре. Экспрессия NPY в DMN резко возрастает при разрушении VMN и других типах гиперфагии.
Паравентрикулярное ядро (PVN) и околосводный гипоталамус (PFH): чувствительны к микроинъекциям орексигенных и анорексигенных соединений. Разрушение PVN ведет к гиперфагии. PVN - единственная область гипоталамуса, в которой повышается выделение NPY при голодании.
Супрахиазматическое ядро (SCN): повреждения SCN нарушают регулярность приема пищи. Сигналы о светопериодичности направляются через SCN в ARC, VMN, DMN, LH.
Нейроанатомический субстрат контроля аппетита. Рецептивная область для анорексигенных сигналов (лептина, инсулина, КРГ, урокортина, CART) перекрывает рецептивную область для орексигенных сигналов.
Орексигенные сигналы
Нейропептид Y. NPY рассматривается как важнейший организатор пищевого поведения. Кроме гипоталамуса NPY в значительных количествах образуется в стволе мозга (BS). Терминали NPY-нейро- нов BS обнаруживаются в ARC, VMN, DMN, PVN. С NPY совместно образуются другие орексигенные соединения (НА, А, GAL). Эти проекции обеспечивают практически все содержание НА и А и 40 - 50% содержания NPY в гипоталамусе. Хирургическая или химическая блокировка этих путей ведет к гиперфагии. По-видимому, экстрагипоталамический NPY участвует в создании и консолидации нервных стимулов, определяющих суточное потребление пищи.
Микроинъекции NPY в различные области гипоталамуса и экстрагипоталамические структуры стимулируют потребление пищи, что соответствует распределению рецепторов NPY подтипов Y1 и Y5, которые, как полагают, опосредуют стимулирующее действие NPY на прием пищи. Показано, что NPY вызывает длительное синаптическое ингибирование ГАМК-ергической и глутаминергической трансмиссии в ARC. Терминали NPY-нейронов образуют также синапсы на нейронах, продуцирующих орексигенные ПОМК и GAL. Рецепторы NPY Y1 обнаружены на ПОМК- и NPY-продуцирующих нейронах.
Кривая доза-ответ для действия NPY на потребление пищи имеет колоколообразную форму. Введение NPY стимулирует потребление пищи, паттерн и поведенческие особенности которого сходны с естественными, а иммунонейтрализация NPY в темное время суток блокирует ночное потребление пищи. Скорость выделения NPY в PVN во времени совпадает с потреблением пищи, возрастая непосредственно перед едой и снижаясь по мере насыщения. При отсутствии пищи
гиперсекреция NPY сохраняется. Голодание повышает также мРНК рецептора NPY Y1 в гипоталамусе. У мышей ob/ob, db/db и крыс Zucker с ожирением повышены уровень мРНК NPY в ARC, уровень NPY в разных отделах гипоталамуса и секреция NPY в PVN. Сходные изменения предшествуют гиперфагии при введении стрептозотоцина, причем в PVN эти изменения наступают раньше, чем в других отделах гипоталамуса. Гиперфагия при лактации также сопровождается повышением активности NPY-ергической сигнализации в оси ARCPVN. Антагонисты рецепторов Y1 и Y5 снимают ночной и голодный прием пищи. У мышей с недостаточностью Y1 потребление пищи значительно снижено. Нокаут Y5 не влиял на потребление пищи и не влиял на действие NPY, но при этом (как и при нокауте Y1) наблюдалось поздно наступающее ожирение. По-видимому, у таких животных повышаются продукция GAL и чувствительность к нему.
Серотонин снижает выделение NPY и снижает потребление пищи. Антагонисты серотонина действуют противоположным образом. Физиологическое значение этих эффектов остается неясным.
Овариэктомия самок повышает потребление пищи, а введение таким животным эстрогенов восстанавливает данный показатель. При этом кратковременное введение эстрогена ведет к повышению на несколько часов экспрессии NPY в ARC. При длительном введении эстрогена уровень NPY избирательно снижается в PVN и PFH и снижается выделение NPY в PVN. Продуцирующие NPY нейроны содержат Э-Рц. У кастрированных самцов мРНК NPY в ARC снижается, а введение тестостерона восстанавливает экспрессию.
В PVN NPY-нейроны синаптически связаны с КРГ-нейронами. Микроинъекция в PVN NPY индуцирует секрецию АКТГ и кортикостерона. NPY-нейроны в ARC содержат ГК-Рц, и введение адреналэктомированным крысам глюкокортикоида ведет к повышению экспрессии NPY в ARC и повышению потребления пищи. В то же время сама адреналэктомия оказывает слабое влияние на потребление пищи.
У животных, получавших стрептозотоцин, повышается экспрессия и выделение NPY в PVN и развивается гиперфагия, а введение таким животным инсулина нормализует эти показатели. Эффект инсулина наблюдался и in vitro. Вероятно, это один из механизмов установочной точки массы тела.
При инфекциях, травмах развивается анорексия. Это, возможно, связано с действием воспалительных цитокинов. ИЛ-1 снижает пот-
ребление пищи, подавляя эффективность NPY. CNTF снижает экспрессию NPY и уровень Y1.
Недостаточность лептина у мышей ob/ob (мутация гена лептина), нечувствительность к лептину у мышей db/db и у крыс Zucker (fa/fa) (мутации генов рецептора лептина) сопровождаются повышением экспрессии и выделения NPY в гипоталамусе и гиперфагией.
При разрушении VMN развивается гиперфагия. При этом мРНК NPY в ARC и уровень, и выделение NPY в PVN снижены. Но при этом гиперфагия остается зависимой от NPY, поскольку иммунонейтрализация NPY блокирует потребление пищи.
При разрушении VMN микроинъекцией колхицина наступает преходящая (4-5 дней) гиперфагия. Сразу же снижается продукция и выделение NPY в ARC и PVN соответственно. Гиперфагия развивается по меньшей мере отчасти за счет повышения чувствительности к NPY и увеличения рецепторов NPY типа Y1 в гипоталамусе. Параллельно возникает резистентность к лептину. Кроме того, повышается продукция GAL и возрастает чувствительность к нему.
При химической блокировке норадреналинового пучка, идущего из BS, развивается гиперфагия. При этом исчезает подъем продукции лептина после еды в ночное время и возрастает ночная секреция NPY.
Галанин. GAL - 29-членный пептид, микроинъекции которого в PVN, LH, VMN и центральное ядро амигдалы ведут к гиперфагии. Длительность действия небольшая (30 мин), и эффект слабее, чем у NPY. GAL-продуцирующие нейроны обнаружены в нескольких областях гипоталамуса и иннервируют практически весь гипоталамус. GAL- и NPY-продуцирующие нейроны прямо связаны между собой, особенно в ARC и PVN, и, вероятно, GAL участвует в опосредовании эффектов NPY. Терминали GAL-нейронов обнаружены на нейронах, экспрессирующих ПОМК, в ARC. Обработка животных налоксоном (анатагонистом опиатных рецепторов) частично снимает стимулирующее действие GAL на прием пищи. Блокировка α2-AR снижает эффективность GAL. GAL стимулирует выделение НА в PVN. Видимо, норадреналин опосредует отчасти действие GAL.
Опиоиды. ПОМК-продуцирующие нейроны в гипоталамусе локализованы исключительно в ARC и иннервируют VMN, DMN, PVN и другие области гипоталамуса. Микроинъекции β-END и агонистов μ-опиатных рецепторов в эти области стимулируют прием пищи. Нейроны, продуцирующие мет- и лей-энкефалины (met-ENK, leuENK), распространены в гипоталамусе более широко. Сами эти
пептиды неэффективны, но их долгоживущие аналоги, действующие через δ-опиатные рецепторы, стимулируют прием пищи. Инъекции динорфина A 1-17 стимулируют прием пищи через κ-опиатные рецепторы. DYN-продуцирующие нейроны обнаружены в разных областях гипоталамуса. Антагонисты опиоидов, особенно μ- и к-рецепторов, снижают потребление пищи и подавляют индуцированную NPY гиперфагию. Выявлены морфологические связи между нейронами, продуцирующими β-END, GAL и NPY и ГАМК-END. NPY стимулирует выделение β-END в гипоталамусе, но подавляет мРНК ПОМК, а налоксон повышает мРНК NPY в ARC и уровень NPY в DMN. В целом, стимулирующее действие опиоидов на прием пищи кратковременное и относительно слабое.
Меланинконцентрирующий гормон (МКГ). Нейроны, продуцирующие 19-членный МКГ, локализованы в zona incerta и LH, а их проекции обнаружены в гипоталамусе и лимбической системе. Ведение МКГ стимулирует ночное потребление пищи. Голодание повышает экспрессию МКГ. Экспрессия МКГ увеличена у мышей ob/ob. Эффекты МКГ слабее и более кратковременны, чем эффекты NPY. Интересно, что индуцированное МКГ переедание не сопровождается ожирением.
Аминокислоты. Глутамат и ГАМК являются наиболее распространенными нейромедиаторами в гипоталамусе. Оба стимулируют прием пищи. Агонист глутаматных рецепторов NMDA вызывает кратковременную (10 мин) стимуляцию приема пищи только при инъекции в LH. Микроинъекции агониста GABAA в ряд областей гипоталамуса (VMN, DMN, PVN) стимулируют прием пищи в течение 30 мин. ГАМК-ергические окончания обнаружены на β-END-содержащих нейронах в ARC. Но агонист GABAA снижает экспрессию ПОМК и выделение α-МСГ. Обнаружена коэкспрессия ГАМК и NPY, ГАМК и GAL в нейронах ARC. Значительная доля первых проецируется в PVN. Инъекции NPY и агониста ГАМК в PVN оказывают синергичное действие на прием пищи. Не исключается также, что стимуляция приема пищи под действием ГАМК осуществляется за счет тормозного действия ГАМК-ергических нейронов на пути тонического торможения действия NPY.
Гипокретины/орексины. Hcrt1 и Hcrt2, или орексины A и B, продуцируются нейронами в дорзальном и латеральном гипоталамусе и PFH. Терминали обнаружены в ARC, паравентрикулярном ядре таламуса, преоптической области, ядрах перегородки, BS. Внутрижелудочковое
введение этих пептидов, а также микроинъекции в LH, PVN и PFH, но не в VMN и POA, стимулируют потребление пищи. Голодание повышает их экспрессию. Пищевое действие орексинов, по-видимому, определяется рецептором орексинов типа 2. В ARC терминали с орексинами обнаружены на нейронах, коэкспрессирующих NPY и лептин. Вероятно, орексины стимулируют выделение NPY в PVN. И наоборот, терминали с NPY обнаруживаются на нейронах, экспрессирующих орексины, в LH.
Грелин. Этот гормон желудка и нейромедиатор оказывает орексигенное действие. Его концентрация в крови, отражающая преимущественно продукцию желудком, возрастает при голодании и быстро снижается после приема пищи (рис. 11-19). Неизвестно, однако, стимулирует ли пищевое поведение желудочный грелин или грелин, синтезируемый в мозгу.
Анорексигенные сигналы
Пептиды семейства КРГ. КРГ-нейроны, участвующие в регуляции гипофизарного АКТГ, локализованы в PVN. КРГ оказывает также возбуждающее, локомоторное и анксиогеноподобное действие. При инъекциях вызывает анорексию. Основной мишенью анорексигенного действия КРГ является PVN с проведением сигнала через рецепторы КРГ-Рц1 и КРГ-Рц2. Неясно, играет ли КРГ роль в регуляции приема пищи: адреналэктомия, повышающая образования КРГ, не влияет на прием пищи.
Урокортин более эффективно, чем КРГ, подавляет прием пищи за счет большего сродства к КРГ-Рц2 и КРГ-Рц2а. Экспрессирующие
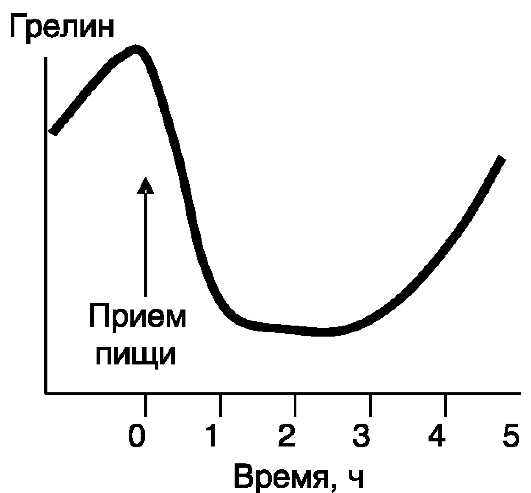 Рис. 11-19. «Голодная» секреция грелина желудком
Рис. 11-19. «Голодная» секреция грелина желудком
урокортин нейроны локализованы в ядре Edinger-Westphal, латеральной верхней оливе, LH и супраоптическом ядре. Микроинъекции урокортина в VMN, но не в PVN тормозят прием пищи. Инфузия антагониста КРГ, КРГ(6-33), значительно снижает массу тела крыс Zucker. При этом прием пищи не снижался.
Нейротензин (NT). NT тормозит спонтанный и индуцированный НА прием пищи. NT-продуцирующие нейроны обнаружены в ARC, PVN, DMN. Эти и соседние области иннервируются NT-продуцирую- щими нейронами (в частности, проекции таких нейронов DMN обнаружены в PVN). У мышей ob/ob уровень мРНК и пептида NT снижен. Концентрация NT снижена также у крыс Zucker (fa/fa).
Глюкагоноподобный пептид 1 (GLP-1). GLP-1 (7-36)амид возникает при процессинге проглюкагона в кишечнике. Иммунореактивный GLP-1 выявлен в нейронах ARC и PVN. Основная часть GLP-1-содер- жащих терминалей в гипоталамусе идет из ядра одиночного тракта. Внутрижелудочковое введение GLP-1 голодным животным снижает прием пищи. У сытых животных антагонист GLP-1 стимулирует прием пищи и ожирение. GLP-1 ослабляет действие NPY, что позволяет предполагать участие NPY в опосредовании действия GLP-1. Эффект, видимо, связан с ингибированием постсинаптического действия NPY в PVN. Показана коэкспрессия мРНК GLP-1 и рецептора лептина в нейронах BS. Антагонист GLP-1 блокировал тормозное действие лептина на потребление пищи. Возможно, GLP-1 служит одним из посредников анорексического действия лептина. Интересно, что при нокауте GLP-1-R изменений в потреблении пищи не наблюдается.
Меланокортин (α-МСГ) и белок агути. У мышей с синдромом ожирения при летальной мутации агути (AY/a) при созревании развиваются ожирение, гиперинсулинемия, гипергликемия, что связано с действием белка агути через меланокортиновые рецепторы MC4. α-МСГ, как полагают, ингибирует потребление пищи через те же рецепторы. MC4-R обнаружены во многих отделах мозга, включая PVN, VMN, DMN. Мутации MC4-R ведут к последствиям, сходным с синдромом ожирения агути. Введение агониста MC4-R снимает гиперфагию, вызванную введением NPY или мутацией в локусе агути (AY). Введение антагониста MC4-R ведет к повышению потребления пищи сытыми животными. У мышей ob/ob и у нормальных голодных мышей экспрессия ПОМК в ARC снижена. Введение таким животным лептина восстанавливает экспрессию ПОМК. Нейроны, экспрессирующие ПОМК, содержат рецепторы лептина. По-видимому,
потребление пищи тонически подавляется системой лептин-ПОМК- αMCT-MC4-R.
В ARC обнаружены нейроны, коэкспрессирующие NPY и ART (ген, кодирующий родственный агути белок, AgrP). Экспрессия AgrP возрастает у мышей ob/ob и db/db. AgrP является сильным антагонистом MC3-R и MC4-R. Возможно, AgrP блокирует тормозное действие a-МСГ в PVN на потребление пищи.
Транскрипт, регулируемый кокаином и амфетамином (CART). Внутрижелудочковое введение CART тормозит потребление пищи. Иммунонейтрализация CART повышает ночной прием пищи. мРНК CART обнаружена в ARC, PVN, SON, VMH, переднем PVN и др. областях. Экспрессия CART при голодании и у fa/fa крыс, и ob/ob мышей снижается в ARC и DMH. Введение лептина мышам ob/ob повышает экспрессию CART в ARC. В PVN обнаружены NPY-терми- нали на экспрессирующих CART нейронах.
Лептин. Введение лептина подавляет потребление пищи с лагпериодом 8 - 10 ч. Активная, длинная форма рецептора лептина (OBRb) экспрессируется в ARC, VMH, PVN, LH, вентральном премамиллярном ядре (PMv), DMN. Микроинъекции лептина в ARC, VMH, LH тормозят потребление пищи. В ARC обнаружена коэкспрессия OB-Rb и NPY. Лептин снижает экспрессию NPY в ARC, DMN, PVN. OB-Rb коэкспрессируется в ряде областей с ПОМК, MCH, GAL, орексинами, GLP-1, что предполагает, что такие нейроны могут быть мишенями для лептина.
У человека циркадный ритм уровня лептина в крови характеризуется базальным уровнем с 8.00 до 12.00 и максимумом между 24.00 и 4.00. Пульсаторный характер с интервалами 44 мин. Циркадные изменения связаны с высотой пульсов.
Лептин ингибирует экспрессию гена NPY и секрецию NPY, а также подавляет стимулирующее аппетит действие экзогенного NPY. Лептин стимулирует экспрессию ПОМК в гипоталамусе и соответственно продукцию α-МСГ. У мышей ob/ob экспрессия ПОМК снижена. Инсулин ингибирует экспрессию NPY и стимулирует экспрессию и секрецию КРГ, который, в свою очередь, индуцирует экспрессию ПОМК и секрецию α-МСГ.
Амилин. Секретируемый β-клетками поджелудочной железы в ответ на прием пищи амилин действует на структуры ромбовидного мозга (ядро одиночного тракта, area postrema (самое заднее поле)), откуда сигнал поступает в латеральный гипоталамус, в результате
чего снижается экспрессия орексигенных соединений орексина и МКГ. На физиологическую значимость этого пути регуляции указывает стимулирующее действие антагонистов рецептора амилина на потребление пищи и отложение жира. При ожирении секреция амилина возрастает.
Обестатин. Этот 23-членный амидированный пептид является продуктом гена грелина, образующимся при протеолитическом процессинге предшественника грелина. Периферическое и центральное введение обестатина оказывает противоположное грелину действие: подавляет потребление пищи, снижает прибавку массы животных, а также замедляет опорожнение желудка и моторику кишечника. В отличие от грелина обестатин не влияет на секрецию СТГ. Предположительно обестатин действует через сиротский рецептор GPR39 класса рецепторов, сопряженных с G-белками, хотя не все экспериментальные данные согласуются с этим предположением. Идентификация обестатина позволяет объяснить тот удивительный факт, что нокаут гена грелина у мыши не сопровождается существенными изменениями в пищевом поведении и массе тела. Вместе с тем уровень обестатина в крови не зависит от пищевого режима, и это ставит под вопрос физиологическую значимость данного пептида.
Ожирение
Избыточное отложение триглицеридов в адипоцитах (ожирение) увеличивает риск смерти человека репродуктивного возраста (20-50 лет) на 50%. Ожирение способствует развитию сердечно-сусудистых заболеваний, сахарного диабета, желчно-каменной болезни, цирроза печени, рака эндометрия и молочной железы (из-за увеличенной ароматизации андрогенов в эстрогены в адипоцитах).
Различают детское и взрослое ожирение. В первом случае к ожирению ведет увеличение количества адипоцитов, вызываемое усиленной дифференцировкой преадипоцитов в адипоциты под действием избыточного потребления/образования жирных кислот в детском возрасте. Одним из сигналов дифференцировки служит активация жирными кислотами PPARγ. Взрослое ожирение связано только с гипертрофией адипоцитов. С точки зрения энергетики, подтверждаемой данными практической медицины, ожирение возникает из-за нарушения баланса между потреблением пищевых продуктов и их расходованием на образование тепла и выполнение физиологической и физической работы (рис. 11-20).
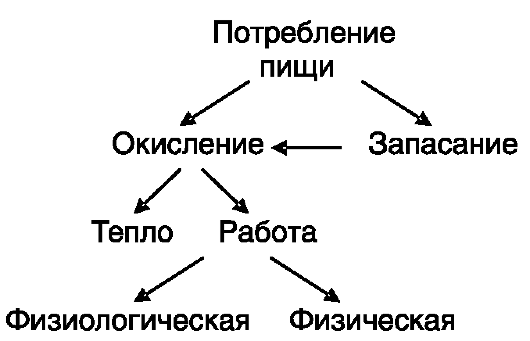 Рис. 11-20. Потребление и расходование пищевых продуктов
Рис. 11-20. Потребление и расходование пищевых продуктов
Дисбаланс может возникнуть вследствие нарушений на любой из стадий. Наиболее частой причиной ожирения служит несоответствие потребления пищи (ее количества и качества) и физической активности. Однажды возникнув, избыток жиров способствует поддержанию нового состояния, в частности, за счет модуляции уровня секретируемого лептина: попытка похудания сопровождается снижением секреции лептина, оказывающего анорексигенное и энергозатратное действие. Аналогичным образом снижение уровня жирных кислот ведет к увеличению секреции инсулина, способствующего увеличению жировых запасов. Как уже упоминалось, к ожирению может вести разрушение у лабораторных животных вентромедиального гипоталамуса, служащего центром «насыщения». В результате развиваются гиперфагия и снижение энергозатрат. К аналогичным последствиям с преобладанием компонентов потребления пищи или расходования энергии ведут инактивирующие мутации системы возникновения/проведения анорексигенных сигналов (например, мутации генов лептина и его рецептора, ob/ob и db/db соответственно) или активирующие мутации системы орексигенной стимуляции (например, «желтое» ожирение, или ожирение агути).
Дисбаланс между потреблением пищи и энергозатратами может возникнуть и на периферии, за счет звеньев запасания, окисления и сопряжения окисления с синтезом и расходом макроэргов. Одним из примеров может служить ожирение при гипотиреозе или инактивирующих мутациях Т-Рц. К настоящему времени выявлены мутации/ полиморфизмы многих десятков генов, ассоциированные с ожирением. В силу полифакторности ожирения его рассматривают не как болезнь, а как симптом.
Рекомендуемая литература
Dimroth P., von Ballmoos C., Meier T. Catalytic and mechanical cycles in F-ATP synthases. Fourth in the Cycles Review Series. EMBO Rep. 2006;7(3):276-282.
Dzeja P.P., Terzic A. Phosphotransfer networks and cellular energetics. J Exp Biol. 2003;206(Pt 12):2039-2047.
Klingenspor M. Cold-induced recruitment of brown adipose tissue thermogenesis. Exp Physiol. 2003;88(1):141-148.
Silva J.E. Thermogenic mechanisms and their hormonal regulation. Physiol Rev. 2006;86(2):435-464.
Villarroya F., Iglesias R., Giralt M. PPARs in the Control of Uncoupling Proteins Gene Expression. PPAR Res. 2007:74364.
Weitzel J.M., Iwen K.A., Seitz H.J. Regulation of mitochondrial biogenesis by thyroid hormone. Exp Physiol. 2003;88(1):121-128.
Westerterp K.R. Diet induced thermogenesis. Nutr Metab (Lond). 2004, 18;1(1):5.
Zhang J.V., Ren P.G., Avsian-Kretchmer O. et al. Obestatin, a peptide encoded by the ghrelin gene, opposes ghrelin's effects on food intake. Science. 2005;310(5750):996-999.