Инфекционные и паразитарные болезни развивающихся стран : учебник для вузов / Под ред. Н.В. Чебышева, С.Г. Пака. - 2008
|
|
|
|
ГЛАВА 4 ГЕЛЬМИНТОЗЫ
4.1. Трематодозы. Общая характеристика трематод
Трематодозы вызываются гельминтами, которые относятся к типу плоских червей - Plathelminthes, классу сосальщиков - Trematoda. Все трематоды - паразиты, локализующиеся в различных органах и тканях человека и животных.
Строение трематод. Тело трематод нерасчлененное, у большинства видов листовидной формы. Длина тела взрослых особей видов, имеющих медицинское значение, колеблется от нескольких миллиметров до 5-8 см. Тело покрыто кожно-мышечным мешком, полости тела нет. Внутренние органы погружены в паренхиму, имеющую преимущественно мезодермальное происхождение. На переднем конце тела находится ротовая присоска. На вентральной поверхности тела расположена брюшная присоска - орган фиксации.
Пищеварительная система трематод начинается ротовым отверстием, расположенным на дне ротовой присоски. Ротовое отверстие ведет в глотку, за которой следует пищевод, переходящий в два слепо заканчивающихся кишечных ствола, у некоторых видов они сильно разветвлены. Анального отверстия нет.
Выделительная система протонефридиального типа состоит из многочисленных терминальных клеток, каждая из которых снабжена пучком ресничек («мерцательным пламенем»). От терминальных клеток отходят тонкие выделительные канальцы, объединяющиеся в более крупные протоки, которые впадают в срединный или боковые собирательные каналы, открывающиеся экскреторным отверстием на заднем конце тела.
Нервная система состоит из окологлоточного нервного кольца с двумя ганглиями и отходящих от них продольных нервных стволов с многочисленными нервами к различным органам.
Половая система в большинстве случаев гермафродитная.
Мужские половые органы состоят из двух семенников, от которых отходят семяпроводы, соединяющиеся в общий семявыносящий проток. Его конечная часть, семяизвергательный канал, переходит в сово-
купительный орган - циррус. Конечная часть семявыносящего протока и циррус заключены в специальный мышечный орган - половую бурсу. В ней находятся также предстательные железы и семенной пузырек. Мужское половое отверстие расположено на брюшной стороне тела.
Женская половая система сосальщиков имеет более сложное строение. Центральным органом ее в большинстве случаев является небольшая полость - оотип, где происходит оплодотворение и завершение формирования яиц, поступающих в него из яичников по яйцеводам. Сперматозоиды проникают в оотип из семяприемника, в котором они скапливаются после копуляции. Из желточника в оотип попадают желточные тела, используемые для формирования запасов питательных веществ и оболочки яиц. В оотип поступает также секрет желез тельца Мелиса, участвующий в формировании яйцевых оболочек и увлажня- ющий поверхность стенок оотипа и матки, что облегчает продвижение яиц к половому отверстию. Яйца, сформировавшиеся в оотипе, поступают в матку и постепенно продвигаются по ней до наружного полового отверстия, через которое они выделяются из тела паразита. У многих трематод от оотипа отходит также Лауреров канал, который открывается на вентральной поверхности тела. Через него удаляется избыток желточных клеток, а иногда он выполняет функцию влагалища, через которое поступают сперматозоиды при копуляции. У трематод происходят самооплодотворение и перекрестное оплодотворение; в последнем случае циррус одной трематоды внедряется в вагину другой особи, и наоборот.
Яйца трематод в большинстве случаев овальные, с крышечкой на одном из полюсов и небольшим бугорком на другом. Цвет их варьирует от бледно-желтого до темно-коричневого.
Биология трематод. Сосальщики являются биогельминтами. Их сложный цикл развития происходит со сменой хозяев: окончательным хозяином являются в основном позвоночные животные, промежуточным - моллюски. В развитии многих трематод принимают участие также дополнительные (вторые промежуточные) хозяева, которыми могут быть рыбы, амфибии и членистоногие (крабы и др.).
Яйца сосальщиков выходят из организма окончательного хозяина во внешнюю среду либо уже зрелыми, либо дозревают в воде, куда попадают с экскрементами. Созревшая личинка (мирацидий) у большинства видов выходит из яйца во внешнюю среду, активно внедряется в ткани соответствующего моллюска. У некоторых видов семейства Opisthorchidae яйцо заглатывается моллюском, и вылупление мирацидия из него происходит только в кишечнике промежуточного хозяина. В моллюске мирацидий развивается в следующую личиночную стадию - спороцисту, которая
представляет собой мешок, заполненный зародышевыми клетками. Из этих клеток путем партеногенеза образуются несколько десятков (иногда свыше ста) редий. Вышедшие из спороцисты редии дают второе поколение редий или образуют личинки следующей стадии - церкарии, которые имеют присоски и длинный хвостовой придаток, с помощью которых они могут активно двигаться. Каждая редия дает от нескольких десятков до нескольких сотен церкариев, которые выходят из моллюсков в воду. Таким образом, из одного яйца, попавшего в моллюска, получается несколько тысяч церкариев.
Церкарии трематод, развивающиеся с одним промежуточным хозяином, попадают из водной среды в организм окончательного хозяина или активно, через неповрежденные кожные покровы (сем. Schistosomatidae), или пассивно (сем. Fasciolidae). В последнем случае вышедший из моллюска церкарий теряет хвост и превращается в инцистированную форму - адолескарий, который заглатывается дефинитивным хозяином, и в его органах развивается в половозрелую форму - мариту. При развитии с дополнительным хозяином церкарии активно в него проникают и инцистируются, образуя метацеркарии. Дефинитивный хозяин заражается ими при употреблении в пищу инвазированных промежуточных хозяев (рыбы или крабов).
4.1.1. Шистосомозы
Шистосомозы (шистосоматозы) - группа тропических трематодозов, которые характеризуются в острой стадии токсико-аллергическими реакциями, а в хронической стадии - явным поражением кишечника или мочеполовой системы за счет паразитирования раздельнополых воз- будителей в мелких венозных кровеносных сосудах (отсюда название - кровяные сосальщики).
4.1.1.1. Мочеполовой шистосомоз
Хронический тропический трематодоз, протекающий с поражением мочеполовых органов.
Этиология. Возбудитель - Schistosoma haematobium. Размеры самца - 10-15 мм, самки -
Кутикула самца вся покрыта шипиками, у самок они имеются только на переднем конце. Глотки нет. Пищевод у самцов и самок сначала
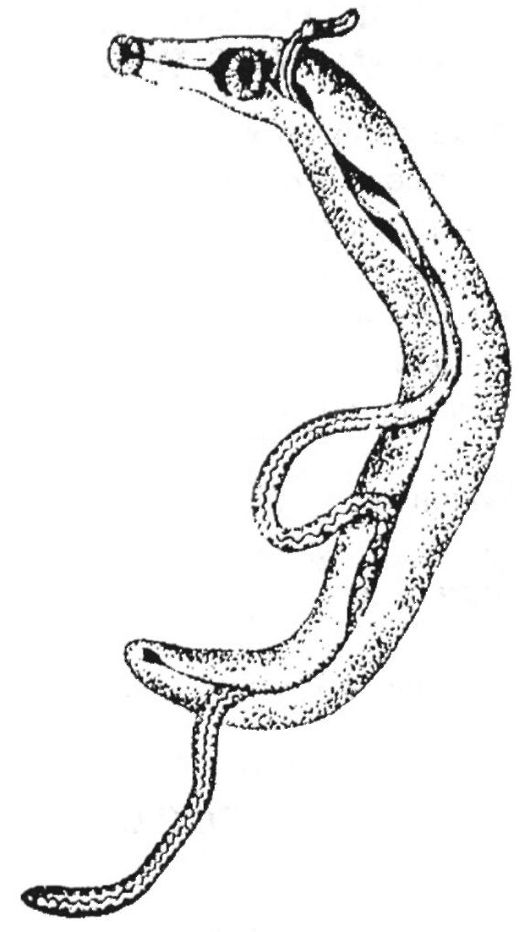
Рис. 4.1. Schistosoma haematobium (самец и самка)
раздваивается на две ветви кишечника, которые затем снова сливаются. Семенников - 4-5, они расположены в передней или задней части тела. Яичник находится у слияния кишечных ветвей, позади него помещаются желточники. Половое отверстие расположено за брюшной присоской. Яйца овальной формы, без крышечки, с характерным для вида терминальным шипом, размер 120-160 χ 40-60 мкм (рис. 4.2).
Возбудители распространены на территории стран тропического и субтропического пояса между 38? с. ш. и 33? ю. ш., в которых, по данным ВОЗ, ежегодно возникает до 200 млн новых случаев заражения. Пораженность шистосомами наиболее высока у лиц в возрасте от 10 до 30 лет. Повышенному риску заражения подвержены сельскохозяйственные рабочие, работ- ники систем орошения. Заболевание широко распространено в большинстве стран Африки и Среднего Востока (Ирак, Сирия, Саудовская Аравия, Израиль, Йемен, Иран, Индия), а также на островах Кипр, Маврикий, Мадагаскар и в Австралии.
По своему социально-экономическому значению среди паразитарных заболеваний шистосомозы занимают второе место в мире после малярии.
Эпидемиология. Шистосомы обитают в мелких венозных кровеносных сосудах мочеполовой системы, в венозных сплетениях малого таза, мочевого пузыря, матки, встречаются в системе воротной вены и разветвлениях брыжеечной вены млекопитающих. Они питаются кровью, частично адсорбируя питательные вещества через кутикулу.
Отложенные яйца мигрируют в мочевой пузырь, дозревают в течение 5-12 дней в тканях хозяина и с мочой выводятся из организма. Окончательное созре-

Рис. 4.2. Яйцо S. haematobium
вание мирацидия происходит в пресной воде при температуре 10-30 ?С. В воде из яиц выходят мирацидии, которые внедряются в пресноводных моллюсков рода Bulinus, где в течение 3-6 недель проходят развитие до церкариев по схеме: мирацидий - материнская спороциста - дочерние спороцисты - церкарии. Церкарии, выйдя из моллюска, способны инвазировать окончательного хозяина в течение 3-х суток. Церкарии внедряются через кожные покровы или слизистую оболочку ротоглоточной полости в организм окончательного хозяина, где превращаются в молодых шистосомул, мигрируют в венозные сосуды мочеполовых органов, развиваются и достигают половой зрелости. Спаривание происходит через 4-5 недель после проникновения в хозяина, затем самки откладывают яйца в мелких венозных сосудах.
С помощью острого шипа и цитолизинов, выделяемых личинками в яйцах, часть яиц проникает через стенки сосудов и ткани слизистой оболочки в просвет мочевого пузыря, откуда они выделяются с мочой. Многие яйца задерживаются в стенке мочевого пузыря и окружающих тканях, вызывая воспаление. Одна пара шистосом продуцирует в сутки 2000-3000 яиц. Продолжительность жизни взрослых шистосом составляет в среднем 5-10 лет (хотя известны случаи паразитирования их у человека на протяжении 15-29 лет).
Патогенез и клиническая картина. Острый период мочеполового шистосомоза совпадает с проникновением церкариев в организм хозяина и миграцией шистосомул по кровеносным сосудам. В этом периоде на стадии внедрения церкариев отмечаются расширение сосудов кожи, покраснение, лихорадка, зуд и отек кожи. Эти явления проходят через 3-4 дня. После первичной реакции и периода относительного благо- получия, длительность которого составляет 3-12 недель, у больного появляются головные боли, слабость, ломота в спине и конечностях, множественные зудящие высыпания типа крапивницы, количество эозинофилов в крови возрастает до 50% и более. Часто увеличиваются печень и селезенка.
В конце острого и начале хронического периодов возникает гематурия, которая чаще бывает терминальной, т.е. кровь в моче появляется в конце мочеиспускания. Больных беспокоят общее недомогание, боли в области мочевого пузыря и промежности; температура тела повышается до 37 ?С и выше, еще больше увеличиваются печень и селезенка. Все эти клинические проявления связаны с реакцией организма человека на внедрение яиц шистосом в ткани мочевого пузыря, половых органов и печени.
Прохождение яиц через стенку мочевого пузыря вызывает гиперемию слизистой оболочки и точечные кровоизлияния. Вокруг погибших яиц в толще стенки мочевого пузыря образуются гранулемы, а на их поверхности - бугорки и полипозные разрастания. Вследствие механического повреждения слизистой проходящими через стенку пузыря яйцами часто присоединяется вторичная инфекция и развивается цистит, приводящий впоследствии к тяжелой деструкции тканей мочевого пузыря, изъязвлению слизистой оболочки. Воспалительный процесс может распространяться вверх по мочеточникам к почкам.
Хронический период заболевания наступает через несколько месяцев после инвазии и может продолжаться несколько лет. Поражение мочеточников сопровождается сужением их дистальных отделов и устья, что приводит к застою мочи, образованию камней и создает условия для развития пиелонефрита и гидронефроза. Поздняя стадия болезни характеризуется развитием фиброза тканей мочевого пузыря и его кальцинацией, что затрудняет прохождение яиц и способствует усилению гранулематозных процессов. Яйца в этих случаях подвергаются обызвествлению. Их скопления образуют видные при цистоскопии так называемые песчаные пятна. В результате меняется форма мочевого пузыря, задерживается моча, повышается внутрипузырное давление. Течение болезни может быть легким, средним и тяжелым. В тяжелых случаях болезнь приводит к инвалидности и преждевременной смерти.
У мужчин заболевание может сопровождаться фиброзом семенных канальцев, орхитом, простатитом, а у женщин - полипозом, изъязвлением слизистой влагалища и шейки матки. Возможно развитие проктита, образование свищей мочевого пузыря. Иногда развиваются псевдоэлефантиаз половых органов, колиты и гепатиты. Поражение легких приводит к гипертензии малого круга кровообращения. Развитие фиброза органов, метаплазии эпителия и иммуносупрессии способствует канцерогенезу. В очагах шистосомозов чаще, чем в других местностях, встречаются опухоли мочеполовой системы.
Дифференциальная диагностика. В эндемичных очагах предварительный диагноз ставится на основании клинических симптомов. Больные жалуются на слабость, недомогание, крапивницу, диуретические расстройства, гематурию, появление капель крови в конце мочеиспускания.
Лабораторная диагностика. Точный диагноз устанавливается при обнаружении яиц шистосом в моче, причем их можно обнаружить лишь через 30-45 дней после заражения. Мочу забирают в часы максимальной экскреции яиц (между 10 и 14 часами). Для овоскопии используют методы концентрации: отстаивания, центрифугирования или фильтрации.
Весьма информативны инструментальные методы диагностики. При цистоскопии выявляются истончение сосудов, побледнение слизистой, деформация и гиперемия устьев мочеточников, скопления погибших и кальцифицированных яиц шистосом, полипозные разрастания.
Также дополнительно используются рентгенологическое исследование и серологические методы (например, ИФА).
Лечение. Лечение больных проводится в стационаре. Препаратом выбора является празиквантель или азинокс в суточной дозе 40 мг/кг в два приема в течение дня. Эффективность препарата составляет 80- 95%. Важное значение в лечении шистосомозов отводится методам симптоматической и патогенетической терапии для улучшения функций пораженных органов и систем. При вторичной инфекции применяются антибиотики. При тяжелом циррозе, тромбозах селезеночных вен, полипозах, стриктурах проводится хирургическое лечение.
Профилактика. Борьба с шистосомозами включает комплекс мероп- риятий, направленных на прекращение передачи инвазии и предупреждение заражения людей:
• своевременное выявление и лечение больных;
• предотвращение попадания яиц шистосом в водоемы, заселенные моллюсками;
• уничтожение моллюсков с помощью моллюскоцидов (фрескон, пентахлорфенолят натрия, медный купорос, эндод и др.);
• расселение в водоемах конкурентов моллюсков и хищников, которые уничтожают яйца моллюсков и их самих;
• использование оросительных систем, снижающих размножение моллюсков;
• очистка и просушка каналов и водоемов;
• ношение защитной одежды (перчатки, резиновые сапоги и др.) при контактах с водой;
• смазывание кожи защитной мазью (40% диметилфталат или дибутилфталат) при купании и работе в воде;
• кипячение или фильтрование воды для питья и хозяйственных нужд;
• активная санитарно-просветительная работа;
• централизованное водоснабжение населения.
Особое значение приобретают меры личной профилактики для туристов и путешественников, находящихся в эндемичных районах. Эти меры подразумевают тщательный выбор мест для купания, избегание заросших растительностью пресноводных водоемов и мест скопления моллюсков.
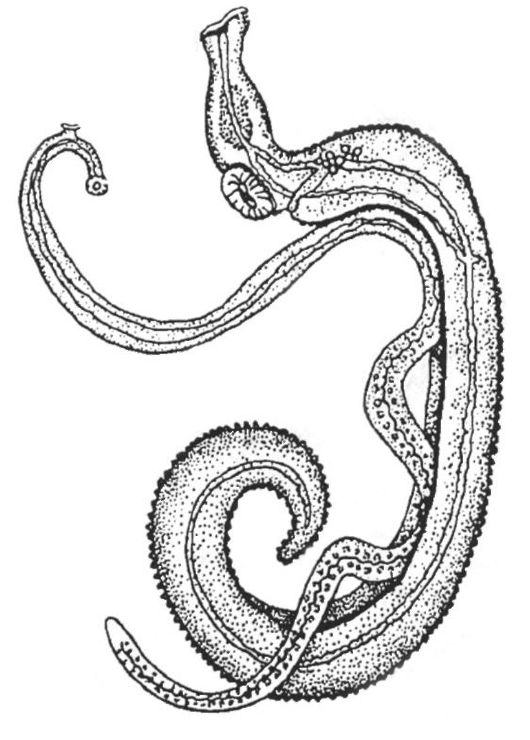
Рис. 4.3.
Schistosoma mansoni (самец и самка)
4.1.1.2. Кишечный шистосомоз Мэнсона
Хронический тропический кишечный трематодоз с преимущественным поражением системы органов пищеварения.
Этиология. Возбудитель - Schistosoma mansoni. Размеры самца 6-14 мм, самки - 12-16 мм (рис. 4.3). Семенники у самцов мелкие, в коли- честве 8-9. Яичник самки расположен в передней части тела. Матка короткая, содержит 1-4 яйца. Яйца овальной формы, с боковым шипом. Размеры яиц 120-160x60-70 мкм (рис. 4.4).
Кишечный шистосомоз широко распространен в странах Африки (Египет, Судан, Замбия, Танзания, Центрально-Африканская Республика, Конго, Камерун, Либерия и др.). В Южной Америке заболевание встречается в Венесуэле, Гвиане, Бразилии, на островах Гаити, Пуэрто-Рико.
Эпидемиология. Цикл развития сходен с жизненным циклом S. haematobium. После активного внедрения церкариев через кожу и сложной миграции шистосомул по лимфатическим и кровеносным сосудам половозрелые гельминты локализуются в разветвлениях воротной вены. Большая их часть мигрирует в мелкие ветви нижней брыжеечной вены, где самки начинают откладывать яйца. С помощью острого шипа и цитолизинов часть яиц проникает через стенку сосудов и ткани слизистой оболочки в просвет кишки и выделяется с калом. Многие яйца паразитов задерживаются в стенке кишечника. Средняя продолжительность жизни самки паразита составляет 3-5 лет, однако отмечены случаи выделения больным яиц кишечных шистосом без повторного заражения более 20 лет.
Патогенез и клиническая картина. Антигены гельминтов оказывают сенсибилизирующее воз- действие на организм хозяина.
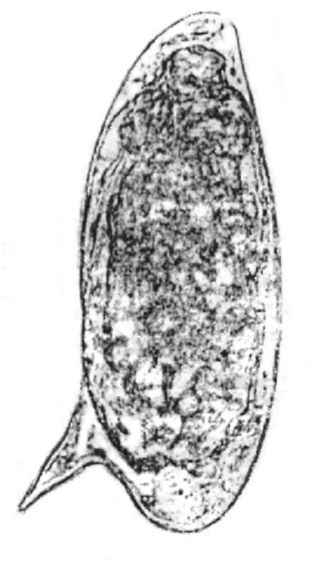
Рис. 4.4
Яйцо S. mansoni
Острая стадия шистосомоза протекает как следствие аллергической перестройки организма. Признаки острого кишечного шистосомоза проявляются через 2-16 (чаще 4-6) недель после заражения. Возникает лихорадка неправильного типа, ухудшается аппетит. Больных беспокоят частый жидкий стул, иногда с примесью крови и слизи, боли в животе. Нередко отмечаются тошнота и рвота. Увеличиваются размеры печени и селезенки. Могут появиться кашель с мокротой, у маленьких детей - одышка, цианоз, тахикардия, гипотония. В крови обнаруживаются эозинофилия и лейкоцитоз. На коже появляется зудящая сыпь, отмечаются локальные отеки кожи. Поражения нервной системы (адинамия, возбуждение, иногда коматозное состояние) отмечаются редко.
В хронической стадии оставшиеся в тканях яйца шистосом служат причиной воспалительных реакций, гранулематозного и фиброзного процессов. Наибольшие патологические изменения развиваются в стенке толстой кишки, в печени и легких. Различают три основные формы хронической стадии кишечного шистосомоза: интерстициальную, гепатоспленомегалическую и легочную. Интерстициальная форма связана с поражением толстого отдела кишечника, особенно его дистальных отделов. Появляется жидкий стул, чередующийся с запорами. Больные жалуются на боли в животе ноющего характера. Часто образуются трещины заднего прохода, развивается геморрой. Гепатоспленомегалия с портальной гипертензией развивается через 5-15 лет после заражения, появляются признаки нарушения функций печени и селезенки: больные жалуются на чувство тяжести и боли в области подреберий, снижение аппетита, похудение, развитие отеков нижних конечностей и асцит. Возникают пищеводные и желудочные кровотечения. При длительном течении болезни развивается цирроз. Дальнейшее развитие патологических процессов приводит к гибели больного от развившейся печеночной недостаточности, тромбоза сосудов печени, кровотечений или в результате острой сердечно-сосудистой декомпенсации. У 5-10% больных развивается легочная форма кишечного шистосомоза. При этом больные жалуются на одышку, повышенную утомляемость, тахикардию, головокружение, боли в области грудной клетки. Образование гранулем и разрастание фиброзной ткани вокруг яиц шистосом, поступающих по воротной системе в печень, создает пресинусоидальный блок, приводящий к развитию портальной гипертензии. Возникает варикозное расширение вен пищевода и желудка, спленомегалия. В условиях застоя в системе воротной вены отмечается занос яиц шистосом в легкие и другие органы. Занос яиц может вызвать поражения червеобразного отростка, желчного пузыря, поджелудочной железы, половых органов, спинного и
редко головного мозга. Как осложнение могут быть кровотечения из вен пищевода, желудочные кровотечения, флегмоны и абсцессы желудка и кишечника, спаечная болезнь, полипоз прямой и сигмовидной кишок, развитие синдрома легочного сердца и др.
Дифференциальная диагностика. Кишечный шистосомоз Мэнсона следует дифференцировать от амебиаза, бактериальной дизентерии, балантидиаза.
Лабораторная диагностика. Паразитологический
диагноз основывается на обнаружении яиц в кале. Для обнаружения яиц
следует делать большие мазки на предметных стеклах. Пробу фекалий из
мазка надо брать с поверхности кала, которая непосредственно
соприкасалась со слизистой кишки, откуда выходили яйца. При
отрицательных результатах копроскопии исследуется ректальная слизь после
дефекации. Применяется также метод обнаружения личинок шистосом в
кале, осно- ванный на их фототропизме. В этом случае фекалии больного
выдерживают в стеклянной колбе в специальных условиях, при которых
через 2 часа и температуре 25 ?С из яиц шистосом вылупляются мирацидии,
которые в силу положительного фототропизма скапливаются на освещенной
поверхности колбы и могут быть выявлены с помощью лупы или
невооруженным глазом. Для выявления неактивного шистосомоза иногда при
ректоскопии производят биопсию кусочка слизистой оболочки кишки на
расстоянии
Лечение. Препаратом выбора является празиквантель или азинокс, которые назначаются в суточной дозе 40 мг/кг в два приема в течение дня (эффективность при инвазии кишечными шистосомами составляет 60%). Высокоэффективным препаратом только для лечения кишечного шистосомоза Мэнсона является оксамнихин. Взрослым препарат назначается внутрь в суточной дозе 15 мг/кг в один прием. Его эффективность достигает 85-95%. Можно также использовать ниридазол в суточной дозе 25 мг/кг курсом лечения 5-7 дней. Важное место в лечении шистосомоза отводится также симптоматической и патогенетической терапии для улучшения функций пораженных органов и систем. При вторичной инфекции можно использовать антибиотики.
Профилактика. Такая же, как и при мочеполовом шистосомозе.
4.1.1.3. Шистосомоз кишечный интеркалярный
Хронический кишечный шистосомоз, распространенный в тропических районах Африки, патогенетически и клинически сходный с кишечным
шистосомозом Мэнсона, но отличающийся от него более доброкачественным течением.
Этиология. Возбудитель - Schistosoma intercalatum, морфологически сходная с S. haematobium. Яйца несколько крупнее. Их размеры 140-
240 χ 50-85 мкм. Яйца выделяются с калом. Болезнь регистрируется в Заире, Габоне, Камеруне, Чаде.
Эпидемиология, патогенез, клиническая картина, лечение и профилактика такие же, как при кишечном шистосомозе Мэнсона.
4.1.1.4. Шистосомоз японский
Хронический тропический трематодоз Юго-Восточной Азии, характеризующийся преимущественным поражением желудоч- но-кишечного тракта и печени.
Этиология. Возбудитель - Schistosoma japonicum. Размеры самца 12-20 мм, самки 12
Эпидемиология. Половозрелые гельминты паразитируют в сосудах системы воротной и мезентериальной вен человека и некоторых домашних и диких животных: крупного и мелкого рогатого скота, собак, кошек, мышей, крыс, кроликов, свиней, обезьян и др. Откладывание яиц начинается самкой через 4 недели после заражения. За сутки каждая самка способна отложить 1500-3000 яиц. Яйца проходят через стенку кишечника и выделяются вместе с калом. В фекалиях яйца появляются через 6-10 недель после заражения. Промежуточные хозяева - мелкие пресноводные моллюски рода Oncomelania. Длительность развития личиночных стадий шисто-
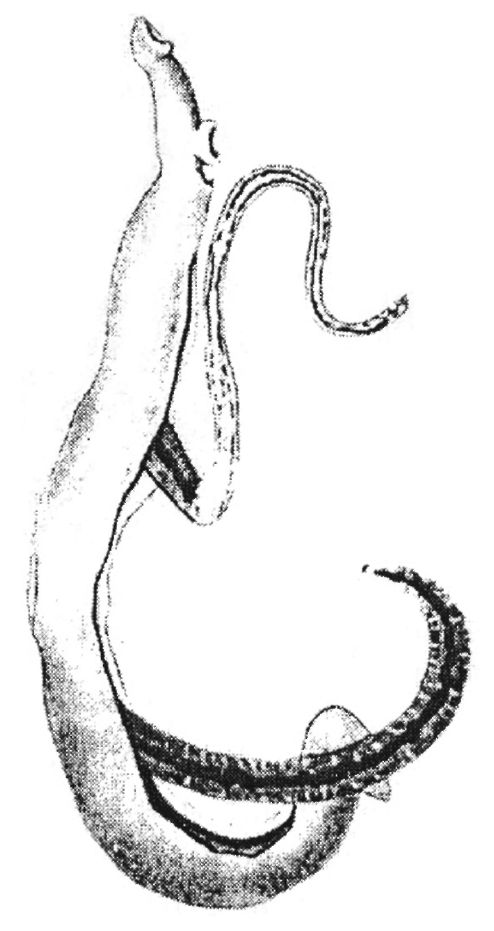
Рис. 4.5. Schistosoma japonicum (самец и самка)
Рис. 4.6. Яйцо S. japonicum
сом в моллюсках составляет 4-12 недель. Церкарии живут в воде до 3-х суток, но сохраняют инвазионную способность лишь первые 30 часов.
Японский шистосомоз регистрируется в странах Азии: Индонезии, Китае, Малайзии, Филиппинах, Японии, Корее. Он распространен как в зоне влажных тропических лесов, так и в субтропических районах. Шистосомоз, встречающийся в Камбодже, Лаосе и Таиланде, называют меконговым. Он чаще встречается у детей до 10 лет.
Патогенез. Патогенез японского шистосомоза во многом сходен с патогенезом S. mansoni. Однако S. japonicum откладывает примерно в 10 раз больше яиц и выделяет их одновременно большими партиями, что приводит к массивному заносу яиц в различные органы: печень, легкие и другие, в которых развиваются тяжелые повреждения сосудов и тканей. Скопления яиц в стенках кишки уже через несколько месяцев начинают обызвествляться, что приводит к формированию гранулем, образование которых сопровождается экссудацией и некрозом. Интенсивная продукция яиц приводит к развитию бурных аллергических реакций. Через 1-7 лет после заражения обычно развивается фиброз печени с портальной гипертензией. Характерным является поражение ЦНС, которое отмеча- ется в 2-4% случаев. При этом развитие гранулем обнаруживается как в сером, так и в белом веществах мозга.
Клиническая картина. В острой фазе болезни при интенсивной инвазии через 2-3 недели после заражения у больных повышается температура тела, появляются высыпания на коже с ангионевротическим отеком. Больных беспокоят головные боли в области живота, понос до 10 раз в сутки со слизью и кровью. В этот период возможно развитие бронхита и бронхопневмонии. Печень и селезенка увеличены. В периферической крови определяется высокая эозинофилия, лейкоцитоз, повышается СОЭ.
В хронический период болезни у больных ведущими являются симптомы, связанные с поражением толстого отдела кишечника. Отмечается диарея с примесью слизи и крови. Иногда развивается кишечная непро- ходимость, обусловленная скоплением яиц. Встречаются тяжелые поражения верхних отделов пищеварительного тракта с образованием язв желудка и двенадцатиперстной кишки, а также со злокачественными образованиями в этих органах. Поражение печени приводит к развитию портальной гипертензии. При поражении ЦНС неврологические симптомы могут появиться уже через 6-8 недель после заражения. Часто регистрируется джексоновская эпилепсия, возможно развитие менингоэнцефалита, параличей. Без проведения лечения и длительном течении болезни развивается кахексия.
Лабораторная диагностика. Диагноз устанавливается при обнаружении яиц в фекалиях теми же методами, что и при кишечном шистосомозе Мэнсона. В позднем периоде во многих случаях решающее значение имеет ректальная биопсия.
Лечение. Прогноз при японском шистосомозе менее благоприятный, чем при других кишечных шистосомозах. В связи с этим празиквантель назначают в повышенной суточной дозе - 60-75 мг/кг и разделяют ее на три приема в течение дня. Эффективность лечения составляет 60%. Необходимо также использовать симптоматическую и патогенетическую терапию.
Профилактика. Такая же, как и при мочеполовом шистосомозе. Кроме того, дополнительно проводятся выявление зараженных домашних животных и их лечение. Фекалии скота на фермах и в местах выпаса зараженных животных должны обеззараживаться. Скот необходимо обеспечивать питьевой водой, свободной от церкариев.
4.1.1.5. Шистосоматидный дерматит (церкариоз)
Шистосоматидный дерматит (церкариоз, зуд купальщиков, водяной зуд, церкарийный дерматит) - паразитарное заболевание, характеризующееся изменениями кожи, вызванными личинками (церкариями) некото- рых видов трематод.
Этиология. Возбудители шистосоматидного дерматита - личинки (церкарии) шистосом семейства Schistosomatidae, паразитирующие во взрослом состоянии в кровеносной системе водоплавающих птиц (уток, чаек, лебедей и др.). Человек не является для них специфическим хозяином. Иногда дерматит может быть вызван церкариями шистосоматид млекопитающих животных (грызунов и др.). В настоящее время насчитывается более 20 видов шистосом, церкарии которых способны проникать через кожу человека.
Эпидемиология. Проникновение церкариев через кожные покровы человека возможно лишь в тех водоемах, в которых содержатся промежуточные хозяева таких шистосом - легочные моллюски. Большинство церкариев гибнет в коже, вызывая воспалительные реакции. Чаще всего шистосоматидные дерматиты вызываются церкариями Tr. ocellata и Tr. stagnicolae.
Яйца трихобильгарций попадают в воду с испражнениями хозяев, из них вылупляются мирацидии, проникающие в моллюсков родов Lymnaea, Planorbis и других, где происходят партеногенетическое раз- множение и развитие личинок до стадии церкария. Церкарии выходят из моллюсков и внедряются через кожные покровы в организм уток и дру-
гих водоплавающих птиц, где продолжается их развитие. Через 2 недели в кровеносной системе хозяев паразиты достигают половой зрелости.
Патогенез. Причиной заражения человека является способность церкарий шистосоматид активно проникать через кожные покровы. Церкарии вызывают механические (часто множественные) поражения кожных покровов и оказывают токсическое и сенсибилизирующее воздействия на организм человека, способствуют заносу вторичной инфекции. Особенно тяжело церкариозы протекают у детей.
В местах внедрения церкариев в кожу человека развиваются отеки с лизисом клеток эпидермиса. По мере миграции церкариев в кориуме возникают инфильтраты из лейкоцитов и лимфоцитов. В результате развившейся иммунологической реакции шистосоматиды в коже человека погибают, и дальнейшее их развитие прекращается.
Клиническая картина. Через 10-15 минут после проникновения в кожу церкариев появляется кожный зуд, а через час после купания на коже возникает пятнистая сыпь, исчезающая через 6-10 часов. У высокочувствительных лиц может возникнуть местная и общая крапивница, аллергический отек и сильный зуд кожи.
При повторном заражении явления дерматита выражены более остро: на коже образуются эритемы и красные папулы, сопровождаю- щиеся сильным кожным зудом. В центре некоторых папул появляются кровоизлияния. Папулы появляются на 2-12-й день после заражения и сохраняются до 2-х недель. Изредка возникают отек кожи и волдыри. Заболевание заканчивается спонтанным выздоровлением. На месте папул в течение нескольких недель сохраняется пигментация.
Дифференциальная диагностика. Основана на появлении характерных изменений кожи при контакте с водой водоемов, где обитают моллюски и утки (купание, рыбная ловля, ирригационные работы и т.д.). Церкариозы дифференцируются с реакциями на укусы насекомых и другими дерматитами.
Осложнения. Прогноз благоприятный.
Лечение. Проводится симптоматическая терапия путем назначения десенсибилизирующих (димедрол внутрь по
Профилактика. В целях личной профилактики церкариозов при кон- тактах с водой водоемов (при купании, стирке белья, играх в воде, рыбной ловле и т.д.) следует:
• избегать заросших водной растительностью мелководных участков водоемов (или их зон), где обитают утки (более безопасны прибрежные зоны, лишенные водной растительности);
• при необходимости длительного пребывания в воде применять защитную одежду и обувь (сапоги, брюки, рубашку), предохраняющие от нападения церкарий шистосоматид;
• после контакта с водой в «подозрительной» зоне водоема тщательно вытереть кожу жестким полотенцем или сухой тканью и быстро сменить промокшую одежду.
Общественная профилактика церкариозов включает:
• оснащение внутренних городских водоемов, где имеется риск заражения людей церкариями, указателями, запрещающими купание и игры в воде;
• регулирование (снижение) численности кряквы в городских водоемах, используемых в рекреационных целях;
• регулярную очистку водоемов (или наиболее посещаемых населением участков водоемов) от водной растительности.
4.1.2. Описторхоз
Описторхоз - биогельминтоз, характеризующийся поражением печени и поджелудочной железы.
Этиология. Возбудителями описторхоза являются два очень близких вида трематод: Opisthorchis felineus и Opisthorchis viverrini. В России возбудителем описторхоза служит О. felineus. Тело описторха плоское, листовидное, суженное спереди; длина 8-14 мм, ширина 1,2-3,5 мм (рис. 4.7). Яйца светло-желтые, очень мелкие (26-30 х 10-15 мкм), с крышечкой на одном полюсе и конусовидным выступом (рис. 4.8).
О. viverrini - двуустка, весьма близкая к О. felineus. Ее размеры 5,4- 10,2 х 0,8-1,9 мм. Пищевод этого паразита в 3 раза длиннее его глот- ки. Яичник многолопастной. Яйца О. viverrini также похожи на яйца О. felineus. Окончательные хозяева - человек, кошка, собака, виверра (сем. Viverridae, отр.хищных млекопитающих). Промежуточныехозяева- различные виды моллюсков рода Codiella и др., дополнительные хозяева - карповые рыбы.
Эпидемиология. Источником заражения являются инвазированные описторхисами люди, а также домашние животные (кошки, свиньи, собаки) и дикие плотоядные, в рацион которых входит рыба.
Заражение человека происходит при употреблении в пищу сырой или необработанной путем нагревания, замораживания или засолки рыбы, содержащей жизнеспособные метацеркарии.
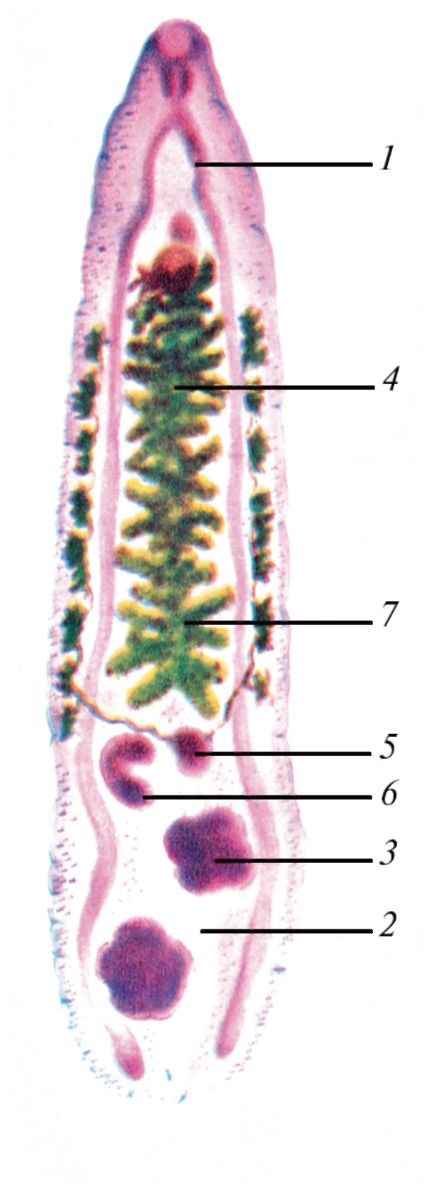
Рис. 4.7. Кошачий сосальщик O.felineus. 1 - ветви кишечника, 2 - выделительный канал, 3 - семенник, 4 - матка, 5 - оотип, 6 - яичник, 7 - матка
Естественная восприимчивость людей к опис- торхозу высокая. Наибольшие показатели заболеваемости регистрируются в возрастной группе от 15 до 50 лет. Несколько чаще болеют мужчины. Заражение, как правило, происходит в летнеосенние месяцы. Часто наблюдаются повторные случаи заражения после излечения. Иммунитет нестойкий. Группу риска представляют новоселы, прибывшие на эндемичные территории и бездумно перенимающие местные традиции употребления в пищу необработанной рыбы.
Описторхоз - один из наиболее распро- страненных биогельминтозов человека в России. Ареал возбудителя простирается от бассейна Енисея до западных границ Европы, но распространение заболевания у человека носит очаговый характер. Крупнейший в мире очаг этого заболевания сформировался в Обь-Иртышском речном бассейне. Здесь регистрируются наиболее высокие показатели заболеваемости населения (до 500 на 100 тыс. населения). Инвазированность сельского населения в Среднем Приобье достигает 90-95%, причем нередко заражены и дети первого года жизни. К 14 годам пораженность детей этим гельминтозом составляет 50-60%, а у взрослого населения она практически стопроцентная.
Очаги описторхоза меньшей напряженности встречаются в бассейнах Волги и Камы, Урала, Дона, Днепра,
Северной Двины и др. Очаги описторхоза, вызываемого О. viverrini, находятся в Таиланде (в некоторых провинциях которого поражено до 80% населения), а также в Лаосе, Индии, на о. Тайвань и в ряде других стран Юго-Восточной Азии. На неэндемичных территориях регистрируются завозные случаи описторхоза и даже групповые заболевания. Фактором заражения в таких случаях служит привезенная зараженная рыба.
Рис. 4.8. Яйцо O.felineus
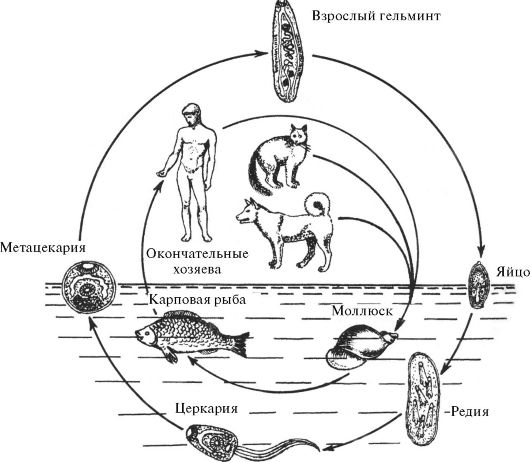
Рис. 4.9. Цикл развития O.felineus
При описторхозе многие инфекционные болезни протекают в более тяжелых формах. У больных описторхозом, перенесших брюшной тиф, в 15 раз чаще формируется хроническое носительство сальмонелл.
О. felineus развивается с тройной сменой хозяев: первого промежу- точного (моллюски), второго промежуточного (рыбы) и окончательного (млекопитающие) (рис. 4.9). К числу окончательных хозяев паразита относятся человек, кошка, собаки, свинья и различные виды диких млекопитающих, в рацион которых входит рыба (лисица, песец, соболь, хорек, выдра, норка, водяная крыса и др.).
Из кишечника окончательных хозяев вполне зрелые яйца описторхисов выделяются в окружающую среду. Яйца паразитов, попавшие в водоем, могут сохранять жизнеспособность 5-6 месяцев. В воде яйцо заглатывается моллюском рода Codiella, в котором из него выходит мира- цидий, превращающийся затем в спороцисту. В ней развиваются редии, проникающие затем в печень моллюска, где они отрождают церкариев.
Все личиночные стадии развиваются из зародышевых клеток партеногенетически (без оплодотворения). При переходе от одной стадии к последующей численность паразитов увеличивается.
Время развития паразитов в моллюске в зависимости от температуры воды может составлять от 2-х до 10-12 месяцев. По достижении инвазионной стадии церкарии выходят из моллюска в воду и при помощи секрета особых желез прикрепляются к коже рыб семейства карповых (линь, язь, елец, сазан, лещ, усач, плотва и др.). Затем они активно внедряются в подкожную клетчатку и мускулатуру, теряют хвост и спустя сутки инцистируются, превращаясь в метацеркариев, размеры которых составляют 0,23-0,37 χ 0,18-0,28 мм. Через 6 недель метацеркарии становятся инвазионными, и содержащая их рыба может служить источником заражения окончательных хозяев.
В кишечнике дефинитивного хозяина под воздействием дуоденального сока личинки освобождаются от оболочек цист и по общему желч- ному протоку мигрируют в печень. Иногда они могут попадать также в поджелудочную железу. Через 3-4 недели от начала заражения окончательных хозяев паразиты достигают половой зрелости и после оплодотворения начинают выделять яйца. Продолжительность жизни кошачьей двуустки может достигать 20-25 лет.
Патогенез. Характер и степень проявления клинических симптомов при описторхозе зависят от интенсивности инвазии и длительности паразитирования, частоты повторных заражений, а также от состояния иммунной системы хозяина. Различают острую и хроническую стадии описторхоза. По течению заболевание может быть стертым или манифестным, а по тяжести - легким, среднетяжелым и тяжелым.
Стертые формы протекают в основном без явных признаков интоксикации и эозинофилией до 30-40%. Такие формы диагностируются, как правило, лишь при случайном выявлении эозинофилии.
В патогенезе острой стадии описторхоза преобладают местные и общие токсико-аллергические действия метаболитов гельминтов на организм хозяина. Вследствие этих аллергических реакций повышается проницаемость сосудов, развиваются периваскулярный отек, мукоидное набухание и эозинофильная инфильтрация стромы разных органов, гиперплазия ретикулярных клеток в регионарных лимфатических узлах; образуются очаги некроза в паренхиме печени.
Питаются гельминты клеточным детритом и эпителиальными секретами. Жизнедеятельность сосальщиков вызывает десквамацию эпителия желчных протоков, вследствие чего развиваются гиперплазия и пролиферация бокаловидных клеток, иногда появляются аденоматоз-
ные изменения и обильное выделение слизи. Образуются кистозные расширения мелких желчных протоков, окруженные пролиферирующей фиброзной тканью. Диффузных поражений печени в большинстве случаев неосложненного описторхоза не возникает. Иногда выявляются небольшие дистрофические изменения цитоплазмы гепатоцитов (мукоидное набухание, избыточное отложение зерен липофусцина и др.).
При хронических поражениях воспалительно-продуктивные процессы приводят к разрастанию соединительной ткани в стенках желчных про- токов печени. Трематоды могут проникать в мелкие желчные протоки, вызывая их закупорку, а иногда и вторичный бактериальный холангит. Могут образовываться желчные камни, вследствие чего возникают приступы желчно-каменной болезни. При тяжелых хронических инвазиях интенсивный фиброз тканей, окружающих желчные протоки, может привести к развитию цирроза печени и даже к портальной гипертензии. Механическое повреждение тканей и раздражение рецепторов желчных протоков вызывают развитие дискинезии желчевыводящих путей. Патологические процессы в поджелудочной железе при описторхозе развиваются вследствие жизнедеятельности самих гельминтов, а также вызываемых ими аллергических реакций, которые приводят к отеку органа и нарушению оттока панкреатического сока. Наиболее часто возникает хронический пролиферативный каналикулит, периканаликулярный фиброз, кистевидные расширения канальцев.
Аденоматозные изменения эпителия желчных и панкреатических протоков могут трансформироваться в холангиокарциному.
Диффузное поражение печени при описторхозе чаще наблюдается у больных с В(Ш) группой крови, а эрозивно-язвенный дуоденит - у людей с 0(1) группой.
Клиническая картина. У неиммунных лиц инкубационный период при описторхозе составляет 2-4 недели. В клиническом течении болезни различают острую и хроническую стадии.
Для легких форм заболевания характерным является внезапное повышение температуры тела до 38 ?С, которая затем держится на субфебрильном уровне в течение 1-2-х недель. Появляются слабость, повышенная утомляемость, в крови определяются умеренно выраженные лейкоцитоз и эозинофилия. Больные жалуются на боли в животе неопределенной локализации, отмечается послабление стула.
Среднетяжелые формы характеризуются лихорадкой различного типа длительностью около 3-х недель с подъемом температуры до 39 ?С и выше, более выраженными лейкоцитозом и эозинофилией, уртикарными высыпаниями на коже, болями в мышцах и суставах. Печень и
селезенка увеличены. Иногда возникают рвота и диарея, бронхит с астматическим компонентом.
При тяжелом течении ярко выражены общетоксические и аллергические явления (высокая температура тела, полиморфные высыпания, головная боль, заторможенность сознания или возбуждение, бессонница). У таких больных ведущими симптомами в клинической картине являются признаки аллергического паренхиматозного гепатита: боли в области правого подреберья, желтуха, увеличение печени, повышенное содержание билирубина и трансаминаз.
У части больных может развиваться эрозивно-язвенный процесс в желудке и двенадцатиперстной кишке. При этом возникают упорные приступообразные боли в правом подреберье и эпигастральной области, тошнота, рвота, вздутие живота, диарея. Понижается кислотность желудочного сока. Рентгенологически выявляется небольших размеров «ниша» и выраженные воспалительные изменения слизистой оболочки кишки.
У некоторых больных появляются кашель, иногда с астматическим компонентом, и боль в грудной клетке при дыхании.
Наиболее тяжело описторхоз протекает при развитии токсико-аллергических поражений ЦНС (вплоть до отека мозга) или миокарда.
В острой стадии заболевания в периферической крови наблюдается лейкоцитоз с эозинофилией (от 10-20 до 60-80%), нередко с развитием лейкемоидной реакции (20-60 х 109/л), увеличение СОЭ. Эти изменения максимально выражены на 2-3-й неделях болезни. При биохимическом исследовании в крови обнаруживается повышение уровней аминотрансфераз, щелочной фосфатазы и прямого билирубина.
Острая стадия заболевания продолжается до двух месяцев, после чего клинические симптомы постепенно исчезают, и болезнь переходит в хроническую стадию, характеризующуюся разнообразными клиническими проявлениями, которые нередко развиваются лишь через несколько лет. У некоторых больных описторхоз может проявляться только симптомами холангита и холецистита, у других - признаками недостаточности пищеварительных ферментов, у третьих - общетоксическими и аллергическими поражениями.
Наиболее часто хроническая стадия заболевания проявляется симптомами поражения гепатобилиарной системы. Больные жалуются на чувство тяжести, распирания в эпигастральной области и правом подреберье, иногда с иррадиацией в спину и левое подреберье. Аппетит снижается, появляются тошнота, рвота, нередки диспепсические расстройства. У большинства больных печень немного увеличена и уплотнена, умеренно
болезненна при пальпации. Однако биохимические показатели функций печени нередко остаются в пределах нормы. Желчный пузырь увеличен, при надавливании болезненный. У больных с гипертоническим и гиперкинетическим типами дискинезии желчевыводящих путей часто выражен синдром желчной (бескаменной) колики, размеры желчного пузыря при этом не увеличены. Температура тела, как правило, не повышается. Во время дуоденального зондирования затруднено получение рефлекса со стороны желчного пузыря. Количество желчи, особенно порции «В», увеличено. При микроскопическом исследовании желчи обнаруживаются лейкоциты и эпителиальные клетки. Методами холецистографии и УЗИ часто определяется дискинезия желчных путей и желчного пузыря.
При поражении поджелудочной железы возникают боли опоясывающего характера с иррадиацией в левую половину грудной клетки, спину, левое плечо. Периодически натощак появляется гипергликемия и снижается содержание пищеварительных ферментов.
У больных хроническим описторхозом нередко нарушаются функции желудка и двенадцатиперстной кишки секреторного и ферментативного характера; развиваются хронический гастрит, дуоденит, гастродуоденит, вплоть до образования язв. Вследствие поражения центральной нервной системы возникают головная боль, головокружение, нарушения сна, эмоциональная неустойчивость, депрессия, раздражительность, частая смена настроения, парестезии, повышенное потоотделение.
При хроническом описторхозе в ряде случаев может отмечаться поражение сердечно-сосудистой системы, проявляющееся болями или неприятными ощущениями за грудиной, сердцебиением. Границы сердца могут быть расширены, тоны приглушены, возникают тахикардия, артериальная гипотензия. На ЭКГ выявляются диффузные дистрофические изменения миокарда.
Нередко течение описторхоза осложняется присоединением вторичной инфекции желчевыводящих путей. У больных повышается температура тела, нарушаются функции печени, она значительно увеличивается в размерах. Иногда наблюдается кратковременная желтуха. При посеве желчи обнаруживается патогенная микрофлора. В крови отмечаются лейкоцитоз, палочкоядерный сдвиг в лейкоцитарной формуле, увеличивается СОЭ, выявляются гиперпротеинемия, гамма-глобулинемия, повышается содержание билирубина, и возрастает активность трансаминаз.
Длительное течение инвазии может приводить к формированию синдрома хронического гепатита, а в последующем - к развитию цирроза печени и даже гепатоцеллюлярной карциномы и рака печени. Именно
поэтому Международным агентством по изучению рака О. viverrini отнесен к первой группе канцерогенов человека.
Дифференциальная диагностика. Полиморфизм клинических симптомов существенно осложняет проведение дифференциальной диагностики описторхоза с рядом других заболеваний. Острую стадию развития описторхоза чаще всего приходится дифференцировать от вирусных гепатитов, тифопаратифозных заболеваний, острого холецистита и острого панкреатита другой этиологии, пищевой токсикоинфекции, миграционной фазы аскаридоза и анкилостомидоза, ОРВИ и др. Хронический описторхоз не имеет существенных клинических отличий от хронического гастрита, гастродуоденита, язвенной болезни, холангита и панкреатита другой этиологии.
При диагностике описторхоза принимаются во внимание данные эпидемиологического анамнеза, свидетельствующие о пребывании больного в эндемичном по описторхозу районе, употреблении им в пищу свежезамороженной, малопросоленной, недостаточно провяленной или прожаренной рыбы семейства карповых.
Лабораторная диагностика. Выявляются признаки острого аллергоза и данные инструментальных методов обследования (УЗИ, холецистография, КТ, МРТ), свидетельствующие о признаках дискинезии желчного пузыря и желчевыводящих путей, снижении выделительной функции печени, расширении желчных протоков, наиболее характерны для острой стадии заболевания. В хронической стадии отмечается умеренная эозинофилия (5-12%), иногда анемия с нормоили макробластическим типом кроветворения. Функции печени (белково-синтетическая, пигментная, антитоксическая) при неосложненном описторхозе остаются в норме или незначительно снижаются. При развитии гепатита, холецистита, холангита отмечается высокая эозинофилия. Появление симптомов желтухи сочетается с повышением активности щелочной фосфатазы при относительно небольшом увеличении уровня АлАТ. О вовлечении в процесс поджелудочной железы свидетельствуют повышение содержания глюкозы в сыворотке крови натощак, измененная кривая при сахарной нагрузке, снижение показателей трипсина, амилазы и липазы в дуоденальном содержимом и повышение их содержания в крови, повышение показателей содержания диастазы в моче. У половины больных отмечается снижение кислотности желудочного сока.
Для серологической диагностики описторхоза применяются иммунологические тест-системы, разработанные фирмой «Вектор-Бест» на основе ИФА, а также РИГА. Однако повышенные титры специфических
антител, определяемые в серологических тестах, не дают основания для установления окончательного диагноза и требуют паразитологического подтверждения.
Окончательный диагноз описторхоза устанавливается при обнаружении в дуоденальном содержимом или в фекалиях яиц кошачьей двуустки, которые начинают выделяться не ранее чем через 4-6 недель после заражения. При малоинтенсивной инвазии перед проведением исследования фекалий целесообразно назначить пациенту желчегонные средства или слепое зондирование по Демьянову, в результате чего повышается вероятность выявления яиц гельминта.
При исследовании фекалий необходимо применять методы обогащения (формалин-эфирный и др.). В случае отрицательного результата исследование фекалий повторяют несколько раз с промежутками 5-7 дней. Исследование дуоденального содержимого необходимо проводить в течение двух часов после его получения, так как при длительном хранении материала в нем происходит лизис яиц.
Осложнения. Чаще развиваются в хронической стадии развития забо- левания. К ним относятся гнойный холангит, флегмона желчного пузыря, хронический гепатит, язвенная болезнь желудка и двенадцатиперстной кишки, острый или хронический панкреатит, механическая желтуха, возможно развитие желчного перитонита при спонтанном разрыве кистозно-измененных желчных протоков, рак печени и желчных протоков. Регистрируются случаи летальных исходов из-за развития острой печеночной недостаточности, но они крайне редки. Прогноз серьезен при развитии гнойных процессов в желчевыделительной системе, при желчных перитонитах и остром панкреатите. Прогноз обычно благоприятный, при развитии холангиокарциномы или рака печени - неблагоприятный.
Лечение. В
большинстве случаев лечение больных описторхозом может быть проведено
амбулаторно. В стационарном лечении нуждаются больные с декомпенсацией
функции органов, больные, имеющие нервно-психические заболевания и с
выраженной клинической симптоматикой острой стадии описторхоза.
Препаратом выбора для лечения описторхоза является празиквантель
(praziquantel, biltricid) или его отечественный аналог - азинокс. Его
назначают в суточной дозе 75 мг/кг сразу после еды, в 3 приема с
интервалом 4-6 часов в течение одного дня. Максимальная разовая доза -
В острой стадии развития заболевания этиотропная терапия проводится после купирования лихорадки, устранения интоксикации и аллергических проявлений. Учитывая полиморфность клинических
проявлений описторхоза и частое сочетание его с другими болезнями, в хронической стадии болезни следует проводить комплексную терапию, направленную на купирование острых состояний и достижение ремиссии сопутствующих заболеваний, а затем проводить специфическое лечение. Эффективность одного курса лечения составляет 96-98% у детей и 86-90% у взрослых. Не рекомендуется назначать препарат детям до 2-х лет, женщинам в I-м триместре беременности. Учитывая частичное выведение препарата из организма с грудным молоком, кормящим женщинам не рекомендуется в день лечения и на следующий день кормить ребенка грудью.
При приеме празиквантеля могут возникать побочные явления: головокружение, головная боль, чувство опьянения, диспепсические расстройства. Эти явления наступают через 30-40 минут после приема, длятся 1-2 часа, слабо выражены и не требуют отмены препарата или медикаментозной коррекции. Учитывая возможность этих явлений специфическое лечение целесообразно назначать на выходные дни, не производить работ, требующих повышенного внимания и быстрых реакций. Категорически противопоказан прием алкоголя в день специфической терапии.
В поздней стадии болезни при развитии холангита и дискинезии желчевыводящих путей назначаются дуоденальные зондирования с введением сульфата магния или сорбита, которые проводят 1-2 раза в неделю в течение 1-2 месяцев. Показаны желчегонные средства, предпочтительно из группы холекинетиков. При болях применяются спазмолитики и анальгетики. В случае присоединения вторичной инфекции желчных путей назначают антибиотики с учетом чувствительности к ним микрофлоры дуоденального содержимого. При развитии анемии, особенно у детей, пациентам назначают полноценную белково-витаминную диету и препараты железа.
С целью контроля эффективности специфического лечения через 3-4 месяца после него проводится трехкратное (с интервалом в 7 дней) контрольное исследование испражнений и дуоденального содержимого.
Профилактика. Основой профилактики заражения описторхозом является исключение из пищи необеззараженной рыбы. Метацеркарии описторхиса мелки и не видны невооруженным глазом. На эндемичных территориях вся рыба семейства карповых подлежит обязательному обеззараживанию путем термической обработки, замораживания или посола.
Комплекс мер профилактики включает также недопущение скармливания собакам, кошкам, свиньям необеззараженной рыбы, защиту водоемов от загрязнения фекалиями, особенно затонов и стариц, так
как в них обитает много моллюсков - промежуточных хозяев кошачьей двуустки.
Необходимо проведение санитарно-просветительной работы, разъяснение недопустимости употребления в пищу сырой, свежемороженой, малосольной, вяленой и недостаточно термически обработанной рыбы.
4.1.3. Клонорхоз
Клонорхоз - биогельминтоз, на ранней стадии проявляющийся аллергическими симптомами, а в хронической стадии протекающий с преимущественным поражением печени и поджелудочной железы.
Этиология. Возбудителем клонорхоза является двуустка китайская - Clonorchis sinensis, имеющая плоское тело, длиной 10-
По строению тела клонорхи сходны с опис- торхами. Отличительными их признаками служат более крупные размеры и более узкий передний конец тела. Семенники клонорхов, в отличие от описторхов, глубоко расчленены, их ветви заходят за кишечные каналы. Отсюда название Clonorchis (греч. klonos - ветвистый, лат. orchis - семенник) (рис. 4.10).
Яйца возбудителя желтовато-коричневого цвета, размером 26-35 χ 17-20 мкм, с крышечкой на одном полюсе и бугорком на другом. Передний конец яйца заметно сужен, выступы по краям крышечки хорошо выражены, что является отличительным признаком от яиц описторхов
(рис. 4.11).

Рис. 4.10. Двуустка китайская (Clonorchis sinensis) (по Г.Г. Смтрнову, 1959).
1 - ротовая присоска;
2 - брюшная присоска;
3 - матка; 4 - оотип;
5 -яичник; 6 - семенники; 7 - выделительный канал
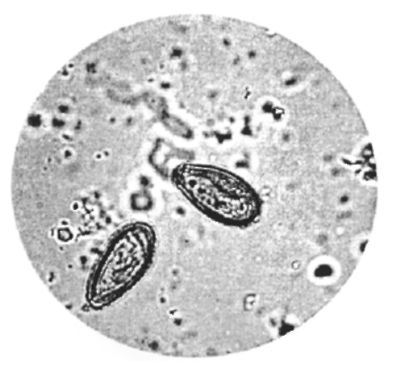
Рис. 4.11. Яйцо Cl.sinensis
Клонорхоз широко распространен в Китае, Японии, Корее и в ряде стран Юго-Восточной Азии. В некоторых эндемичных районах поражено до 80% населения, а в общей сложности клонорхозом инвазированы миллионы людей. В России клонорхоз встречается в бассейне Амура и в Приморье, уровень заболеваемости относительно низок. Однако в нижнем Приамурье (на участке от Хабаровска до Комсомольска-на-Амуре) среди коренного населения (нанайцы) пораженность достигает 25%.
Эпидемиология. Источником инвазии служат зараженные люди, а также собаки, кошки и дикие плотоядные животные. Человек заражается при употреблении в пищу сырой и недостаточно обеззараженной рыбы, а также креветок.
Цикл развития, как и у описторхоз, происходит со сменой трех хозяев. Окончательные хозяева - люди, кошки, собаки, свиньи, выдры, куницы, барсуки, крысы и некоторые другие животные, употребляющие в пищу рыбу. Яйца гельминта, выделяемые с фекалиями, при попадании в воду заглатываются промежуточными хозяевами - моллюсками родов Codiella и др., в теле которых проходит личиночное развитие до стадии церкариев. Церкарии покидают моллюска и проникают в дополнительных хозяев, которыми служат многие виды карповых рыб (карась, язь, лещ, сазан и др.), реже - бычковые и сельдевые; в Китае в число дополнительных хозяев входят также креветки. Церкарии расселяются в мышцах, подкожной клетчатке и других тканях, где примерно в течение 35 дней инцистируются и превращаются в метацеркариев. При попадании метацеркариев в желудочно-кишечный тракт человека или других окончательных хозяев оболочка цисты растворяется, а освободившаяся личинка через желчный проток или по портальным венам попадает в печень, где превращается в половозрелую двуустку, которая через месяц после заражения хозяина начинает откладывать яйца. Развитие личинки до половозрелой стадии может происходить также в протоках поджелудочной железы. Длительность жизни китайской двуустки в организме хозяина может достигать 40 лет.
Патогенез, клиническая картина, осложнения, диагноз и дифференциальный диагноз, лабораторная диагностика при клонорхозе в основном такие же, как и при описторхозе. Более часто, чем при описторхозе, отмечается внезапное начало с выраженными симптомами аллергоза. Внезапно возникает высокая лихорадка постоянного или послабляющего типа с ознобами. Появляются полиморфная сыпь на коже, эозинофильные инфильтраты в легких, бронхит, реактивный плеврит, диф- фузные изменения миокарда, миалгии, артралгии, лимфаденопатия. Примерно у 30% больных увеличивается селезенка. В крови, как пра-
вило, выявляется лейкоцитоз до 20-30 χ 109/л, эозинофилия (до 70%), повышение СОЭ до 30- 40 мм/ч. Окончательный диагноз устанавливается при обнаружении яиц гельминта в дуоденальном содержимом или фекалиях.
Достоверно канцерогенность клонорхов не установлена. Лечение. См. описторхоз.
4.1.4. Фасциолез
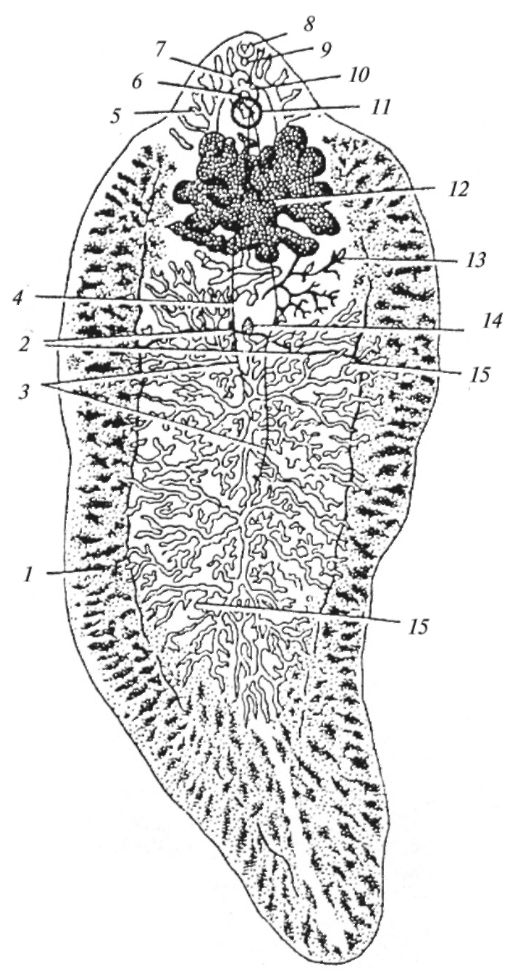
Рис. 4.12. Печеночный сосальщик F.hepatica
1 - желтоточники; 2 - желтлточные протоки; 3 - семяпроводы; 4 - железа Мелиса; 5 - кишечник; 6 - половая сумка; 7 - циррус; 8 - ротовая присоска; 9 - глотка; 10 - женское половое отверстие; 11 - брюшная присоска; 12 - матка; 13 - яичник; 14 - желточный резервуар; 15 - семенники
Фасциолез - биогельминтоз, харак- теризующийся хроническим течением с преимущественным поражением печени и желчевыводящих путей.
Первые сообщения о фасциолезах человека принадлежат Мальпиги (Malpighi, 1698) и П.С. Палласу (1760).
Этиология. Возбудителями фасциолеза являются два вида трематод - Fasciola hepatica и F. gigantica. Последний вид распространен преимущественно в странах с тропическим и субтропическим климатом.
F. hepatica - крупная трематода, размером 20-30 χ 8-12 мм. Кутикула в передней части вооружена шипиками. Головной конец выдается в виде выступа, на котором находятся две присоски.
Внутренние органы фасциолы имеют ветвистое строение. Предглоточная полость и мускулистая глотка вместе с ротовой присоской образуют мощный сосательный аппарат. От короткого пищевода берут начало два кишечных канала, доходящих до заднего конца тела. От каждого из них отходит ряд боковых ветвей, которые в свою очередь разветвляются.
Сложно разветвленные семенники расположены в средней части тела, один позади другого; семяпроводы впереди брюшной присоски впадают в бурсу цирруса, из которой выводится дугообразно изогнутый циррус. Небольшой ветвистый яичник
лежит асимметрично впереди семенников. Протоки желточников, расположенных по сторонам тела, соединяются по средней линии и образуют желточный резервуар, рядом с которым находятся оотип и железа Мелиса. Семяприемника нет. Небольшая петлистая матка лежит между протоками желточников и брюшной присоской (рис.4.12). Яйца крупные, размерами 120-145 χ 70-85 мкм, овальные, желтовато-коричневого цвета, со слабо выраженной крышечкой.
Эпидемиология. F. hepaticci паразитирует в желчных ходах печени многих травоядных животных и изредка у человека. В сутки одна особь откладывает в среднем 25 тыс. яиц. Основным источником заражения служат инвазированные травоядные сельскохозяйственные животные, главным образом крупный рогатый скот. Человек большой роли в эпидемическом процессе фасциолеза не играет, так как является лишь случайным хозяином паразита.
Яйца фасциол зимой в водоемах и на пастбищах сохраняются до 2-х лет. Личинки паразитов, находящиеся в теле моллюсков, могут перезимовывать и выходить из них ранней весной. Адолескарии при 100% относительной влажности переносят температурные колебания в пределах от -18 до +42 ?С; в условиях относительной влажности 25-30% они погибают при 36 ?С. В сухом сене инцистированные адолескарии могут выживать в течение нескольких месяцев, а во влажной почве и воде сохраняются жизнеспособными до 1 года.
Человек заражается при употреблении в пищу дикорастущих растений (кресс-салат водяной, кок-сагыз, дикий лук, щавель), произрастающих в стоячих или медленно текущих водоемах, а также на влажных пастбищах, где могут обитать инвазированные моллюски. Можно заразиться и при питье воды из загрязненных адолескариями водоемов или купании в них, а также при употреблении в пищу обычных огородных овощей (салат, лук), для полива которых использовалась вода из таких источников. Пик заражения приходится на летние месяцы.
Цикл развития (рис. 4.13). Вместе с калом яйца попадают во внешнюю среду. Дальнейшее их развитие происходит в воде. При температуре 20-30 ?С в яйцах через две недели развиваются мирацидии. При более низких температурах развитие яиц замедляется, при температуре выше 40 ?С мирацидии погибают. В темноте яйца развиваются быстрее, но мирацидии из них не выходят. Продолжительность жизни мирацидия в воде составляет не более 2-3 дней. Проникнув во внутренние органы брюхоногих моллюсков Lymnea truncatula и других видов Lymnea, мирацидии превращаются в спороцисты, в которых развиваются редии. В редиях образуются либо второе поколение редий, либо хвостатые цер-
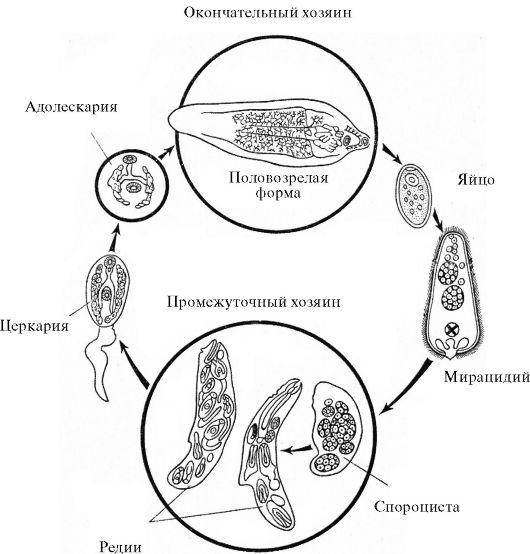
Рис. 4.13. Цикл развития F.hepatica
карии. Они выходят из моллюска через 2-3 месяца после его заражения и в течение ближайших 8 часов инцистируются, прикрепляясь к водным растениям или к поверхностной пленке воды. Инцистированная личинка печеночной двуустки - адолескарий - попадает в желудочно-кишечный тракт окончательного хозяина при питье воды из водоемов, поедании растительности с заливных лугов, либо при использовании зараженной воды для бытовых нужд (мытье овощей и фруктов, полив грядок и т.п.). Попав в кишечник окончательного хозяина с пищей (околоводные и водные растения) или с водой, адолескарии эксцистируются, и личинки проникают через стенку кишечника, мигрируют в брюшную полость, а
затем через капсулу и паренхиму печени - в желчные протоки. Второй путь миграции - гематогенный: через кишечные вены в воротную вену, а затем в желчные протоки печени. От момента попадания адолескариев в организм дефинитивного хозяина до развития половозрелой ста- дии проходит 3-4 месяца. Срок жизни фасциол в организме человека составляет 5 лет и более.
Продвигаясь по печеночной ткани, фасциолы повреждают капилляры, паренхиму, желчные протоки. Образуются ходы, которые в дальнейшем превращаются в фиброзные тяжи. Иногда фасциолы током крови заносятся в другие органы, наиболее часто - в легкие, где инкапсулируются и погибают, не достигая половой зрелости. Кроме того, молодые фасциолы заносят из кишечника в печень микрофлору, вызывающую распад застойной желчи, что обусловливает интоксикацию организма, образование микроабсцессов и микронекрозов.
Фасциолез, вызванный Fasciola hepatica, распространен
в большинстве стран мира. Особенно часто он встречается в тех регионах
Европы, Среднего Востока, Южной Америки и Австралии, где развито
животно- водство. В основном регистрируются спорадические случаи,
однако во Франции, на Кубе, в Иране и Чили были зарегистрированы
вспышки с поражением сотен людей. Описаны вспышки фасциолеза в
Прибалтике, Узбекистане и Грузии. Самая большая известная вспышка
фасциолеза произошла в Иране в
Наиболее интенсивные очаги, связанные с F. gigantica, отмечены во Вьетнаме и в других странах Юго-Восточной Азии, на Гавайских островах и в некоторых странах тропической Африки.
Патогенез. Половозрелые фасциолы, передвигаясь по желчным про- токам, травмируют их и, скапливаясь иногда в большом количестве, закупоривают, нарушая отток желчи. Иногда они проникают в желчный пузырь. Продукты жизнедеятельности паразитов и распада печеночной ткани и желчи, всасываясь в кровь, оказывают общее токсическое действие на весь организм. Нарушаются функции желудочно-кишечного тракта, сердечно-сосудистой, дыхательной, центральной нервной и ретикулоэндотелиальной систем; возникает резкий дефицит витамина А и других витаминов; развивается аллергизация организма.
Нарушению функций желудочно-кишечного тракта и других органов способствуют также патологические рефлексы, возникающие вследствие раздражения нервных окончаний паразитирующими в желчных ходах крупными двуустками.
При длительном течении фасциолеза просвет общего желчного протока часто расширяется, стенки его утолщаются. Происходит аденоматозное расширение желчных протоков, развивается гнойный холангит.
Инкубационный период при фасциолезе продолжается 1-8 недель в зависимости от заражающей дозы и состояния организма болезнь может протекать с различной степенью тяжести.
Клиническая картина. Различают острый и хронический периоды (стадии) заболевания.
Острая (миграционная) стадия сходна с аналогичной при описторхозе, но при фасциолезе у больных чаще развивается аллергический миокардит и в большей степени выражены признаки поражения печени (острый антигенный гепатит). Пациентов беспокоят слабость, недомогание, появляются головные боли, понижается аппетит. Температура субфебрильная или высокая (до 40 ?С), лихорадка носит послабляющий или волнообразный характер. Появляются крапивница, кашель, боли в эпигастральной области, в правом подреберье (чаще приступообразные), тошнота, рвота. У части больных размеры печени увеличиваются, особенно ее левая доля, что приводит к появлению вздутия и болям в эпигастральной области. Постепенно (в течение нескольких недель) эти клинические проявления значительно уменьшаются или даже полностью исчезают.
При исследовании крови в острой стадии развития болезни выявляется выраженный эозинофильный лейкоцитоз (содержание лейкоцитов до 20-60 х 10 /л, эозинофилов - до 85%).
Через 3-6 месяцев после заражения появляются симптомы, свойственные хронической стадии заболевания, которые связаны с органными поражениями печени и желчных путей. Размеры печени вновь увеличи- ваются. При пальпации прощупывается плотный и болезненный нижний ее край. Иногда больных беспокоит сильная приступообразная боль в правом подреберье. Периоды относительного благополучия сменяются периодами обострения, во время которых появляется желтуха при сравнительно невысоких показателях АлАТ и АсАТ и значительном повышении щелочной фосфатазы. По мере прогрессирования нарушений функции печени развиваются гипо- и диспротеинемия, повышается активность трансаминаз. При длительном течении болезни появляются расстройства стула, макроцитарная анемия, гепатит и нарушение питания.
В хронической стадии количество лейкоцитов снижается и часто нормализуется, эозинофилия составляет обычно 7-10%.
В случае вторичного инфицирования желчевыделительной системы бактериальной флорой количество лейкоцитов резко увеличивается, повышается СОЭ. Показателями степени деструктивно-некротичес-
ких и воспалительных изменений в печени служат повышение щелочной фосфатазы, трансаминаз, а также гипопротеинемия и гипоальбуминемия.
При паразитировании единичных фасциол клинические проявления острой стадии могут отсутствовать. В этих случаях болезнь может протекать в инаппарантной форме.
Как казуистика, отмечались случаи проникновения печеночных двуусток в другие органы, сопровождающиеся нарушением их функции. При локализации паразитов в мозге возможны сильная головная боль, эпилептиформные приступы; при попадании в легкие - кашель, кровохарканье; при нахождении в гортани - боль в горле, удушье; в евстахие- вых трубах - боль в ушах, снижение слуха.
Диагностика. Заподозрить фасциолез можно по совокупности данных эпидемиологического анамнеза и клинических симптомов:
- наличие случаев фасциолеза на данной территории;
- употребление в пищу немытой зелени, растущей на незащищенных от фекальных загрязнений переувлажненных берегах водоемов или на заболоченных участках местности;
- острое начало заболевания, лихорадка в сочетании с аллергическими реакциями (отек Квинке, крапивница), боль в правом подреберье или эпигастральной области, увеличение печени, лейкоцитоз, эозинофилия.
Лабораторная диагностика. Уже в острой стадии заболевания информативны серологические методы (РИГА, РИФ, ИФА), однако вследствие недостаточной чувствительности и специфичности они не могут быть использованы для установления окончательного диагноза.
Через 3-4 месяца после заражения диагноз может быть подтвержден обнаружением в дуоденальном содержимом или в фекалиях яиц гельминтов. Паразитологический диагноз фасциолеза представляет опреде- ленные трудности в связи с тем, что паразиты долгое время (3-4 месяца) не откладывают яиц, а также вследствие сравнительно малого числа выделяемых яиц. Поэтому при исследовании фекалий целесообразно использовать методы обогащения.
После употребления в пищу печени крупного рогатого скота, пораженной фасциолами, в фекалиях могут быть обнаружены транзитные яйца. В этих случаях необходимо провести повторные паразитологичес- кие исследования через 3-5 дней после исключения из рациона пациента печени и субпродуктов.
В ряде случаев фасциолы могут обнаруживаться при ультразвуковом исследовании печени, при нахождении гельминтов в желчном пузыре и крупных желчных протоках.
Фасциолез следует дифференцировать с описторхозом, клонорхозом, вирусными гепатитами, лейкозом и заболеваниями желчевыводящих путей другой этиологии.
Осложнения. Гнойный ангиохолангит, абсцессы печени, склерози- руюший холангит, обтурационная желтуха. Прогноз благоприятный. Очень редко (до 0,06% случаев) развивается цирроз печени.
Лечение больных фасциолезом проводится в стационаре. На острый период заболевания назначается постельный режим, диета с ограничением грубой клетчатки и жиров. В острой стадии антигельминтные препараты назначают после купирования лихорадки и аллергических проявлений.
По рекомендациям ВОЗ, препаратом выбора для лечения фасциолеза является триклабендазол, который назначается в дозе 10 мг/кг (в тяжелых случаях 20 мг/кг) на два приема с интервалом 12 часов в течение одного дня.
Используют также празиквантель в тех же дозах, что и при описторхозе. Однако эффективность празиквантела в отношении F. hepatica не превышает 30-40%, а в отношении F. gigantica она сопоставима с эффективностью при лечении описторхоза.
Контроль эффективности лечения проводят через 3 и 6 месяцев после курса терапии путем исследования фекалий или дуоденального содержимого.
Прогноз при своевременном выявлении и лечении благоприятный. При длительном течении инвазии возможно развитие гнойных холангитов и цирроза печени.
Профилактика. В эндемичной по фасциолезу местности воду из непроточных водоемов рекомендуется употреблять для питья только прокипяченной или профильтрованной. Растения, растущие во влажных местах, или огородную зелень, для полива которой использовалась вода из загрязненных фекалиями скота водоемов, перед употреблением в пищу следует отваривать или ошпаривать кипятком.
Следует помнить, что кухня юго-восточных и южных стран с большим объемом свежей зелени, особенно водных растений, представляет опасность заражения фасциолезом при нарушении гигиенических пра- вил приготовления.
Большое значение в профилактике имеют ветеринарные мероприятия, направленные на ликвидацию фасциолеза в хозяйствах: профилактическая дегельминтизация скота, смена пастбищ, скармливание сена с неблагополучных по фасциолезу лугов проводить не ранее чем через 6 месяцев после уборки, когда адолескарии уже погибнут. Борьба
с моллюсками (промежуточными хозяевами фасциол) проводится путем мелиорации заболоченных участков земель. Используют также химические средства борьбы с моллюсками (моллюскоциды). Обязательным компонентом комплекса профилактических мероприятий должна быть санитарно-просветительная работа среди населения, проживающего в эндемичной по фасциолезу местности.
4.1.5. Парагонимоз
Парагонимоз - биогельминтоз, проявляющийся преимущественно поражением органов дыхания. Характеризуется длительным рецидивирующим течением.
Этиология. Возбудитель - легочный сосальщик Paragonimus westermanii и некоторые другие виды семейства Paragonimidae.
P. westermanii - толстая, широкоовальная трематода, красновато- коричневого цвета, по форме напоминающая кофейное зерно. Размеры тела легочной двуустки - 7,5-12 х 4-6 мм при толщине 3,5-5 мм. Кутикула покрыта шипиками; ротовая и брюшная присоски почти одинакового размера. Кишечные ветви извитые и тянутся до конца тела. Два дольчатых семенника находятся в задней трети тела. Дольчатый яичник и петли небольшой матки расположены рядом впереди от семенников. Половые отверстия находятся у заднего края брюшной присоски. Сильно развитые желточники распространены по всему телу от уровня глотки до заднего конца тела сосальщика.
Яйца овальные, золотисто-коричневого цвета, размером 61-81 χ 48- 54 мкм, с толстой оболочкой, крышечкой и небольшим утолщением на противоположном конце. Яйца выделяются незрелыми (рис. 4.14).
Эпидемиология. Источник инвазии - свиньи, собаки, кошки, дикие плотоядные и человек, инвазированные парагонимусом. Пути передачи - пищевой, водный. Факторы передачи - термически необработанное мясо крабов и раков.
При оптимальной температуре (27 ?С) развитие яиц в воде заканчивается через 3 недели. Однако мирацидии могут выходить из них и через несколько месяцев, чему способствует колебание температуры воды. Промежуточными хозяевами являются пресноводные брюхоногие моллюски Melania libertina, M. externa, M. amurensis (Дальний Восток), Ampullara luteosota (Южная Америка) и другие, у которых последовательно развиваются стадии спороцист, редий и церкариев. Церкарии активно проникают в дополнительных хозяев через участки с тонким хитиновым покровом - пресноводных крабов родов Potamon, Eriocheir, Parathelphusa, раков родов Cambaroides, Procambarus и др. (рис. 4.15).
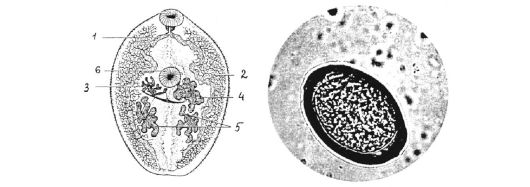
Рис. 4.14. Легочный сосальщик P.westermani и яйцо
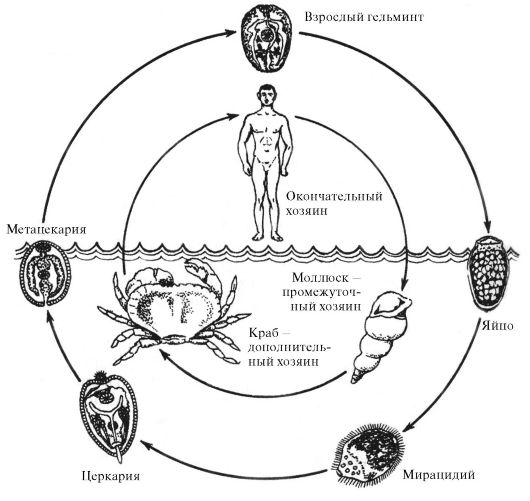
Рис. 4.15. Цикл развития P.westermani
В ракообразных церкарии инцистируются в мышцах и во внутренних органах, где превращаются в метацеркарии, которые становятся инвазионными через 1,5 месяца. В организме одного ракообразного может содержаться несколько сотен метацеркариев. Окончательными хозяевами служат свиньи, собаки, кошки, дикие плотоядные, грызуны (крысы, ондатры) и человек, которые заражаются при поедании крабов и раков в сыром или полусыром виде. Заражение может произойти и через воду, так как при гибели зараженных ракообразных метацеркарии сохраняют жизнеспособность в воде до 25 суток. В двенадцатиперстной кишке окончательных хозяев личинки освобождаются из оболочек, проникают через кишечную стенку в брюшную полость, пробуравливают диафрагму, оба листка плевры и внедряются в легкие. Здесь вокруг паразита формируются фиброзные кисты размером с лесной орех, локализующиеся вблизи корней легких и по периферии легочной ткани. В кисте у человека обычно находится один паразит, реже два. Паразиты достигают половой зрелости и начинают откладывать яйца через 5-6 недель после заражения. Продолжительность жизни паразитов в легких превышает 5 лет.
Парагонимоз распространен преимущественно в странах ЮгоВосточной Азии (Китай, Тайвань, Индокитайский полуостров, Индонезия, Филиппины), а также в Южной Америке (Перу, Эквадор, Колумбия, Венесуэла). В России кроме завозных случаев известны ограниченные очаги парагонимоза в Приморском крае и в Приамурье. В этом регионе заражению способствует употребление в пищу местного блюда - «пьяных крабов», которое готовится из живых крабов или раков, посыпанных солью и залитых красным вином.
Патогенез. В
патогенезе парагонимоза ведущую роль играют токсико- аллергические
реакции и механическое воздействие гельминтов и их яиц на ткани. Во
время миграции личинок паразитов в легкие через диафрагму и другие
органы (печень, поджелудочную железу, почки) в них отмечаются
кровоизлияния, а иногда и некрозы. В легких (особенно в нижних долях)
помимо кровоизлияний образуются эозинофильные инфильтраты и скопления
экссудата. Позднее вокруг паразитов формируются фиброзные кисты
размером от 0,1 до
Клиническая картина. Инкубационный период длится 2-3 недели, при массивной инвазии может сокращаться до нескольких дней.
В остром периоде болезни развиваются признаки тяжелого энтерита, гепатита и доброкачественного асептического перитонита, сопровождающиеся симптомами «острого живота». Затем возникают лихорадка, боли в груди, одышка, кашель с гнойной мокротой, имеющей иногда примесь крови. При физикальном и рентгенологическом исследованиях выявляются экссудативные инфильтраты, а иногда и признаки экссудативного плеврита.
Через 2-3 месяца
болезнь переходит в хроническую стадию, характеризующуюся периодами
ремиссий и обострений, во время которых температура повышается до 38-40
?С, усиливаются боли в груди, головные боли, появляются одышка, кашель
с выделением ржавой мокроты, в которой содержатся яйца гельминта.
Нередко отмечается кровохарканье. При рентгенологическом исследовании
легких определяются слабо выраженные округлые тени диаметром от 5 до
Через 2-4 года клинические проявления болезни постепенно исчезают. После исчезновения симптомов болезни при рентгенологическом исследовании в легких обнаруживаются небольшие изолированные очаги фиброза и единичные или множественные очаги кальцификации диаметром 2-5 мм.
При интенсивной инвазии и многолетнем течении болезни может развиться пневмосклероз и синдром «легочного сердца».
Попадание парагонимусов в ЦНС вызывает развитие симптомов менингита, повышается внутричерепное давление. Возможно развитие атрофии зрительного нерва, парезов, параличей, нарушений чувстви- тельности, эпилепсии. На рентгенограммах головного мозга у таких больных выявляются кальцинированные округлые образования, содержащие погибших гельминтов.
Дифференциальная диагностика. Дифференциальный диагноз проводится с пневмонией, туберкулезом и эхинококкозом легких, а также опухолями. При парагонимозе мозга заболевание дифференцируют с опухолью мозга и менингоэнцефалитом. На паразитарную природу болезни указывает сочетание неврологической симптоматики с характерными изменениями в легких и наличием яиц в мокроте.
Лабораторная диагностика. Диагноз парагонимоза устанавливается на основании эпиданамнеза, клинических данных и результатов лучевых методов исследований (рентгенография, КТ, МРТ), а также при обна-
ружении яиц паразитов в мокроте или испражнениях, куда они попадают при заглатывании мокроты. В ранний период, когда яйца молодыми паразитами еще не выделяются, для диагностики можно использовать ИФА. Однако в России соответствующие коммерческие тест-системы отсутствуют. Можно использовать также внутрикожную аллергическую пробу с антигенами из парагонимусов.
Лечение. Специфическое лечение следует проводить после купиро- вания аллергических проявлений. Препаратом выбора является празиквантель (азинокс), который назначается взрослым в суточной дозе 75 мг/кг в 3 приема в течение одного-двух дней. При поражении ЦНС специфическую терапию следует проводить только в стационаре в связи с возможным развитием отека мозга и повышением внутричерепного давления. Пациентам назначают мочегонные и противосудорожные средства. Единичные кисты удаляют хирургическим способом.
Эффективен также триклабендазол, назначаемый в тех же дозировках, как и при фасциолезе.
С целью контроля эффективности специфического лечения через 2-3 месяца после окончания терапии проводится трехкратное (с интервалом в 7 дней) контрольное исследование мокроты.
Осложнения. При своевременном лечении неосложненных случаев прогноз благоприятный. В случае парагонимоза мозга с множественными кистами прогноз крайне неблагоприятный.
Профилактика. В очагах парагонимоза ракообразных можно есть только после кулинарной обработки, обеспечивающей гибель парагонимусов. В связи с тем что в воде могут содержаться частицы погибших крабов и раков, инвазированных метацеркариями, при купании в открытых пресноводных водоемах следует остерегаться случайного заглатывания воды. Для питья следует использовать только кипяченую или профильтрованную воду. Необходимо обеспечивать охрану водоемов от фекальных загрязнений.
4.2. Цестодозы. Общая характеристика цестод
Цестодозами называются гельминтозы, возбудители которых относятся к классу Cestoidea. Медицинское значение имеют в основном представители двух отрядов: лентецов - Pseudophyllidea и цепней - Cyclophyllidea, относящихся к подклассу настоящих ленточных червей (Eucestoda).
Строение цестод. Тело цестод (от греч. cestos - пояс, лента) обычно лентовидное, сплющенное в дорсовентральном направлении, состоит из
головки
(сколекса), шейки и стробилы, разделенной на членики (проглоттиды).
Длина всей цестоды в зависимости от вида может варьировать от
нескольких миллиметров до
Тело цестод покрыто кожно-мышечным слоем (кожно-мускульным мешком), состоящим из кутикулы и субкутикулы. Кутикула - плотное неклеточное образование на поверхности клеток эпителиальной ткани. Она состоит из трех слоев: наружного, содержащего кератин, среднего - цитоплазматического, богатого белками и липидами, и внутреннего - волокнистого или базального. Кератин вместе с минеральными веществами и белками придает кутикуле механическую прочность; липиды способствуют ее водонепроницаемости. Благодаря устойчивости кутикулы к действию ферментов хозяина и выделению через нее веществ, нейтрализующих влияние ферментов, цестоды могут существовать в агрессивной среде кишечника человека и позвоночных животных. Кутикула покрыта ворсинкоподобными выростами - микротрихиями, которые входят в тесный контакт с микроворсинками слизистой кишечника, что способствует повышению эффективности всасывания питательных веществ. В субкутикуле находится слой клеток погружен- ного эпителия, а также наружный кольцевой и внутренний продольный слои гладких мышечных волокон.
Внутри тело цестод заполнено паренхимой, состоящей из крупных неправильной формы клеток, отростки которых переплетаются между собой. В поверхностных слоях паренхимы находятся одноклеточные кожные железы, а также запасы питательных веществ - белки, липиды и гликоген. Последний имеет большое значение в процессах анаэробного дыхания. Здесь же лежат «известковые тельца», содержащие фосфаты и карбонаты кальция и магния, при участии которых регулируются буферные свойства среды.
В более глубоких слоях паренхимы расположены выделительная, нервная и половая системы. Пищеварительная, дыхательная и крове-
носная системы отсутствуют. Питание осуществляется через покровы тела.
Выделительная система цестод построена по протонефридиальному типу. Она состоит из многочисленных клеток с «мерцательным пламенем» и тонких канальцев, которые, соединяясь между собой, впадают в крупные боковые продольные выводные каналы. Эти каналы в каждом членике соединяются между собой задним поперечным каналом. Когда членик отрывается, боковые выделительные каналы открываются наружу на поверхности отрыва.
Нервная система состоит из продольных нервных стволов, самые крупные из которых - боковые. В сколексе они соединены поперечными комиссурами, которые связаны с довольно сложным головным узлом. Органы чувств не развиты.
Половая система почти у всех цестод гермафродитная. У большинства из них половые органы имеют очень сложное строение. Гермафродитный половой аппарат повторяется в каждой проглоттиде. Первые членики, отпочковывающиеся от шейки, еще не имеют полового аппарата. По мере роста стробилы и удаления члеников от шейки в них формируются органы мужской половой системы, состоящей у большинства видов из многочисленных семенников, которые имеют вид пузырьков, разбросанных в паренхиме членика. От них отходят семявыносящие канальцы, впадающие в семяпровод, заканчивающийся совокупительным органом (cirrus), который находится в половой сумке (bursa cirri). Половая сумка открывается, как правило, на боковой (иногда на вентральной) стороне членика на половом бугорке в специальном углублении, которое называется половой клоакой.
Позднее появляется более сложно устроенная женская половая система. Женское половое отверстие находится в половой клоаке рядом с мужским. Оно ведет в узкий канал влагалища, которое у внутреннего конца образует расширение - семяприемник - и открывается в специальную камеру - оотип. В оотип впадают также протоки яичников (яйцеводы), желточников и тельца Мелиса. Через яйцевод в оотип из яичников поступают яйцевые клетки, а по влагалищу проникают сперматозоиды, накопившиеся в семяприемнике после копуляции. В оотипе происходит оплодотворение яйцеклеток и формирование яиц. Они образуются из питательного материала, поступающего из желточников, а их оболочки создаются из секретов железы Мелиса. Сформированные яйца продвигаются в начинающую развиваться матку. По мере поступления в нее яиц матка увеличивается в размерах и занимает все большую часть объема членика, а гермафродитный половой аппарат постепен-
но редуцируется. Концевые членики стробилы целиком заняты маткой, заполненной огромным количеством яиц.
Членики, содержащие развитые половые органы, называются гермафродитными, а заполненные одной только маткой - зрелыми. У цепней зрелая матка замкнутая. Она не имеет никакого сообщения с половыми путями и наружной средой. Яйца выходят из нее только при отделении конечных проглоттид, которое сопровождается разрушением тканей членика и стенки матки.
У лентецов матка открытая, через ее наружное отверстие яйца попадают в кишечник хозяина, а затем с фекалиями выводятся во внешнюю среду. У лентецов яйца имеют крышечку, подобную яйцам трематод.
Яйца цепней довольно однообразны по своему строению, так что определить их видовую принадлежность при микроскопии часто не представляется возможным. Зрелые яйца овальной или шаровидной формы покрыты чрезвычайно нежной прозрачной наружной оболочкой, сквозь которую хорошо видна находящаяся внутри личинка - онкосфера. Она окружена толстой, радиально исчерченной внутренней оболочкой - эмбриофором, который выполняет основную защитную функцию. Онкосфера имеет шесть эмбриональных крючков, приводимых в движение мышечными клетками. С помощью крючков и секрета железистых клеток личинка проникает в ткани хозяина при миграции. Онкосферы чаще бесцветны, реже окрашены в желтый или желтовато- коричневый цвет. При исследовании фекалий обнаруживаются онкосферы, покрытые лишь эмбриофором, так как наружная оболочка быстро разрушается.
Биология цестод. Цикл развития. Все цестоды - биогельминты; постэмбриональное развитие большинства их видов происходит с двойной (у цепней) или тройной (у лентецов) сменой хозяев.
В кишечнике окончательного хозяина при наличии двух или нескольких червей происходит взаимное оплодотворение между различными особями. Если паразитирует только одна цестода, оплодотворение может происходить между разными ее проглоттидами; возможно самооплодотворение одной и той же проглоттиды. У цепней формирование онкосферы заканчивается в матке; у лентецов оно происходит во внешней среде (обычно в воде). У попавшего в воду зрелого яйца лентеца крышечка открывается, и из него выходит корацидий - шаровидная, свободноплавающая личинка, покрытая слоем ресничных клеток и вооруженная шестью крючьями.
Дальнейшее развитие личинок продолжается в промежуточных хозяевах.
Онкосферы, попавшие с пищей или водой в желудочно-кишечный тракт промежуточного хозяина, освобождаются от эмбриофора, внедряются в кишечную стенку и мигрируют, попадая с кровью в различные внутренние органы, где в зависимости от вида цестоды развиваются в соответствующий тип личинки - ларвоцисты (от лат. larva - личинка и греч. kystis - пузырь). Некоторые из этих ларвоцист (ценуры, эхинокок- ки, альвеококки) в организме промежуточного хозяина могут размножаться бесполым путем.
Основными типами ларвоцист являются:
1. Цистицерк (Cysticercus) - небольшое пузырчатое образование, наполненное жидкостью и содержащее погруженный внутрь сколекс с органами фиксации. При попадании в организм окончательного хозяина сколекс выдвигается из личиночного пузыря подобно тому, как выворачивается ввернутый внутрь палец перчатки. Цистицерк - наиболее распространенная из ларвоцист, встречающихся в тканях позвоночных животных.
2. Цистицеркоид (Cysticercoid) состоит из вздутой пузыревидной части с погруженными в нее сколексом и шейкой и хвостового придатка (церкомера), на котором находятся три пары эмбриональных крючков. Цистицеркоид развивается обычно в организме беспозвоночных проме- жуточных хозяев: ракообразных, клещей, насекомых.
3. Ценур (Coenurus) - пузырчатая ларвоциста со множественными погруженными в нее сколексами, каждый из которых в дальнейшем дает начало отдельной стробиле. Таким образом, из одной онкосферы разви- вается большое число паразитов (бесполое размножение путем почкования). Ценур характерен для рода Malticeps, встречается у овец и некоторых грызунов.
4. Ларвоциста цистного эхинококка (Echinococcus granulosus) - наиболее сложно устроенная личинка цестод. Она представляет собой однокамерный пузырь, заполненный жидкостью. Его внутренняя герминативная оболочка может продуцировать выводковые капсулы с одновременным формированием в них зародышевых сколексов (протосколексов) и вторичных, а затем и третичных пузырей, благодаря чему процесс бесполого размножения приобретает особую интенсивность. В организме промежуточного хозяина эхинококк принимает различные модификации. Паразитирует у млекопитающих.
5. Ларвоциста альвеококка (Echinococcus multilocularis) - конгломерат большого количества мелких, неправильной формы пузырьков, от внешней поверхности которых отпочковываются дочерние пузырьки. В пузырьках развиваются протосколексы. Ларвоциста имеет тенденцию прорастать в соседние ткани.
У низших цестод (лентецов) личинки, паразитирующие в промежуточных хозяевах, удлиненные, по форме напоминающие червей. Основные их формы:
1. Процеркоид (Procercoid) - личиночная стадия лентецов, образующаяся в первом промежуточном хозяине (ракообразном) из корацидия. Длина ее около
2. Плероцеркоид (Plerocercoid) - личиночная стадия лентецов, развивающаяся из процеркоида во втором промежуточном хозяине (рыбе). У некоторых видов лентецов может достигать нескольких десятков сантиметров в длину. На переднем конце тела имеются ботрии.
Дефинитивные хозяева заражаются при питании промежуточными хозяевами, инвазированными плероцеркоидами.
Таким образом, развитие лентецов слагается из пяти фаз:
1) яйцо, эмбриогенез в котором происходит в воде;
2) корацидий, вылупляющийся из яйца и ведущий свободный образ жизни;
3) процеркоид, развивающийся из корацидия в теле веслоногих рачков;
4) плероцеркоид, развивающийся из процеркоида у рыб;
5) взрослая цестода (марита), образующаяся из плероцеркоида в кишечнике теплокровных животных.
4.2.1. Тениаринхоз
Тениаринхоз - биогельминтоз с хроническим течением, характеризующийся преимущественно желудочно-кишечными расстройствами.
Этиология. Возбудитель - цепень бычий, или цепень невооружен- ный, Taenia saginata (прежнее название - Taeniarhynchus saginatus). Слово saginatus (лат. - жирный, пухлый) показывает, что членики цепня невооруженного более толстые, оболочка их более грубая и менее прозрачная, чем у цепня вооруженного (свиного). Стробила цепня невооруженного светло-серого цвета, в длину он достигает 4-12 м, но встречаются и более крупные экземпляры.
Сколекс квадратно-овальной формы, диаметром 1,5-2 мм с четырьмя хорошо развитыми присосками и пигментированным рудиментарным хоботком без крючьев.
Короткая шейка соединяет сколекс со стробилой, которая состоит из 1000-2000 почти квадратных проглоттид. Членики средней части стро-
билы содержат хорошо развитую мужскую и женскую половые системы. Многочисленные семенники расположены в боковых полях членика ближе к брюшной поверхности. Тонкие семяпроводы соединяются в общий семяизвергательный канал, который проходит поперек членика и заканчивается копулятивным органом (циррусом), лежащим в особом мешочке. Половой циррус может выворачиваться наружу через отверстие, которое находится на боку членика на специальном возвышении - половом бугорке. Женская половая система представлена двудольчатым яичником (диагностический признак), который расположен в задней половине проглоттиды. Доля, находящаяся на стороне, соответствующей половому бугорку, под семявыносящим протоком несколько меньше другой доли. Позади яичника, параллельно заднему краю проглоттиды, расположен трубчатый желточник. Посередине и несколько впереди него находится группа мелких желез (тельца Мелиса), в месте расположения которых сливаются проток желточника и яйцевод. Сюда же ведет влагалище, наружное отверстие которого открывается в ямке полового бугорка. По мере созревания членика начинает формироваться матка, которая закладывается в виде продольного стволика, отходящего от места слияния яйцевода и протока желточников. В конечной части стробилы членики несколько суживаются и удлиняются. Они почти полностью заполнены очень развитой замкнутой маткой, от центральной части которой отходят в обе стороны по 17-35 боковых ветвей (рис. 4.16).
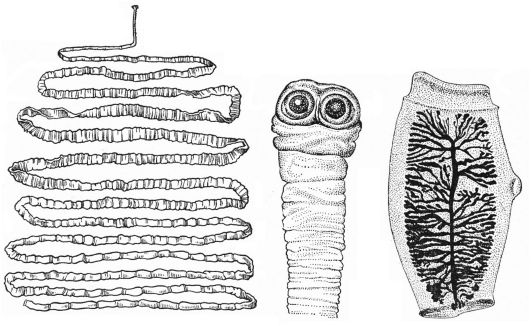
Рис. 4.16. Бычий цепень T.saginatus
Матка наполнена яйцами. Яйца бычьего цепня имеют то же строение, что и цепня свиного; размеры их 28,0-44,0 χ 28,0- 38,0 мкм.
Когда стробила гельминта достигает 5-7 м длины, конечные членики отрываются и вместе с фекалиями или самостоятельно активно выходят наружу. Они выделяются обычно поодиночке, в среднем по 6-8 в течение суток. В каждом членике находится до 175 тыс. яиц. Таким образом, за год человек, инвазированный бычьем цепнем, выделяет около 440 млн яиц. Членики способны активно двигаться. При своем движении в нижних отделах толстой кишки и после выхода из кишечника они выдавливают из матки яйца со зрелыми онкосферами, выходящими всегда через передний край проглоттиды. При этом нежные наружные оболочки яиц разрушаются и освобождают онкосферы, покрытые эмбриофором.
Цистицерки имеют форму овальных пузырьков размером от горошины до зерна фасоли (4-10 мм в поперечнике). Через тонкую, но плотную их стенку просвечивает внутренняя полость, наполненная про- зрачной жидкостью, в которой виден сколекс цепня и зачаток шейки. Продолжительность жизни цистицерков составляет 8-9 месяцев, после чего они дегенерируют и погибают.
Эпидемиология. Источником инвазии служит человек, являющийся единственным дефинитивным хозяином. Механизм заражения - пероральный. Фактором передачи служит мясо крупного рогатого скота и мясные изделия.
Наибольшую опасность в качестве источника инвазии представляют лица, ухаживающие за животными в индивидуальных хозяйствах, а также работники животноводческих ферм: пастухи, доярки, телятницы и пр. При несоблюдении санитарных требований и отсутствии гигиенических навыков они загрязняют своими экскрементами помещения для скота, пастбища, территории ферм и др. Один инвазированный человек, ухаживающий за скотом, может заразить целое стадо животных.
Выделяющиеся в большом количестве с фекалиями онкосферы бычьего цепня длительно сохраняются во внешней среде. При темпе- ратуре 2-5 ?С они остаются живыми в физиологическом растворе 15,5- 16,5 недель, в сточных водах - 16 дней, в жидком навозе - 71 день, в чистой воде - 33 дня, в траве - 159 дней. В сене при температуре от 10 до 30,5 ?С онкосферы остаются жизнеспособными в течение 3-х недель. При колебаниях относительной влажности воздуха от 44 до 96% и температуре от 19 до 37 ?С они сохраняют жизнеспособность 27-29 дней, а при 4 ?С - до 62-64 дней. В условиях Пермской области на поверхности почвы под снегом онкосферы сохранялись живыми в течение всей зимы. В Молдове на поверхности почвы они выживают зимой и весной 5
месяцев, летом - 4 месяца. Наиболее губительны для онкосфер высокая (свыше 30 ?С) и низкая (-20 ?С и ниже) температуры.
Заражение животных происходит обычно на пастбищах. Животные заражаются, заглатывая членики или онкосферы с травой, сеном, водой или подлизывая мочу, находящуюся вблизи фекалий. Но поскольку крупный рогатый скот не имеет склонности к копрофагии, как, например, свиньи, интенсивность инвазии его, как правило, гораздо более низкая, чем инвазированность свиней Т. solium, и может быть незамеченной даже при надлежащем контроле на убойных пунктах.
Чаще заражаются животные в индивидуальных хозяйствах, так как они часто содержатся в худших санитарных условиях, чем животные на фермах. Цистицеркозом наиболее часто поражаются молодые животные (телята в возрасте до двух лет). А поскольку цистицерки в их организме сохраняют инвазионность в течение 11-12 месяцев, то основным путем заражения служит мясо молодых животных. Возможно, что в распространении онкосфер в качестве механических переносчиков могут участвовать мухи и тараканы, в кишечнике которых онкосферы остаются живыми в течение 11 дней.
Механизм заражения человека пероральный. Фактором передачи служит мясо крупного рогатого скота и мясные изделия.
Интенсивность инвазирования населения зависит от многих причин. Главными из них являются: особенности ведения животноводства, эпизоотологическая ситуация по цистицеркозу, эпидемиологическая ситуация по тениаринхозу, обязательность и качество проведения санитарноветеринарной экспертизы мяса и мясных изделий, полнота выявления и эффективность лечения инвазированных и др.
Чаще цистицеркоз животных и тениаринхоз людей встречается в районах, где принято пастбищное и отгонное содержание скота, и население традиционно использует в пищу мясные блюда из термически недостаточно обработанного мяса. В северных районах к таким блюдам относится строганина (ломтики сырого свежезамороженного мяса), в Закавказье - шашлык, гейма, в Средней Азии - бастурма, бичак и др., в Забайкалье готовят позы - блюдо из закопченного в тесте сырого фарша.
Как правило, тениаринхоз регистрируется среди взрослого населения. Женщины заражаются чаще, чем мужчины, так как при приготов- лении пищи они часто пробуют сырой фарш.
В большинстве районов России основное число случаев заражений происходит в осенне-зимний период, во время массового убоя скота. В Якутии и других северных районах свежее мясо едят в основном летом
и ранней осенью, поэтому пик заражений приходится на эти месяцы. У северных оленей цистицерки могут локализоваться в головном мозге, поэтому заражение происходит при употреблении в пищу сырого головного мозга северных оленей, являющегося деликатесом местной кухни северных народностей (рис. 4.17).
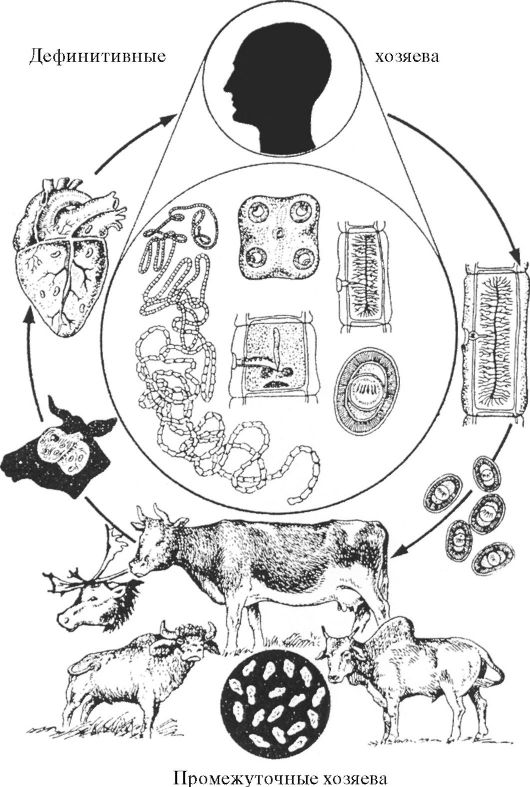
Рис. 4.17. Цикл развития T.saginatus
Заболеваемость тениаринхозом в эндемичных районах обычно носит очаговый характер. Очаги, как правило, формируются в сельской местности с развитым скотоводством. Территориально очаг включает поселок или несколько поселков с общими выпасами. Особенно часто поражаются неблагополучные в санитарном отношении населенные пункты, в которых заражению скота способствует загрязнение территории фекалиями.
Наибольшая
заболеваемость тениаринхозом отмечается в Азербайджане, Армении,
Грузии, Узбекистане, Туркменистане, Кыргызстане, Казахстане,
Таджикистане (в предгорьях Памира). В России эндемичными районами
являются: автономные республики Дагестан, Саха (Якутия) и Бурятия,
Алтайский край, Иркутская, Красноярская, Новосибирская области. В
высокогорных районах эндемичных территорий тениаринхоз встречается чаще,
чем в равнинной местности. Это связано с тем, что при подъеме на
каждые
Тениаринхоз регистрируется на всех обитаемых континентах Земли. Высокая эндемичность (показатель зараженности животных более 10%) отмечается в районах с развитым животноводством в странах Африки к югу от Сахары, в странах Восточного Средиземноморья, Южной Америке и Австралии. Эндемичными остаются Монголия, Китай и ряд стран Юго-Восточной и Южной Азии.
В организм дефинитивного хозяина (человека) - цистицерки невооруженного цепня попадают при употреблении в пищу недостаточно проваренного финнозного мяса животных - промежуточных хозяев этого гельминта. В кишечнике человека сколекс цистицерка выворачивается наподобие пальца перчатки и прикрепляется присосками к слизистой оболочке кишки (обычно двенадцатиперстной) и начинает расти. За сутки стробила паразита удлиняется на 7-10 см. От момента заражения до созревания зрелых члеников проходит около 3-х месяцев. Длительность жизни паразита иногда достигает 20 лет. Бычий цепень, как правило, паразитирует у человека в единственном числе. Отсюда произошло его прежнее название - солитер (от фр. Solitaire - одиночный). Случаи множественной инвазии встречаются редко, обычно в интенсивных эндемических очагах.
Патогенез. Патогенное влияние цепня невооруженного обусловлено действием его присосок и активно подвижных элементов стробилы, которые повреждают слизистую, раздражают рецепторы кишечника и влияют на моторную и секреторную функции желудочно-кишечного
тракта в целом. В результате этого в тонком отделе кишечника возникает катаральное воспаление. Прохождение проглоттид через баугиниевую заслонку может сопровождаться болевым синдромом, напоминающим приступ аппендицита. Боли возникают также при внедрении члеников в червеобразный отросток и развитии воспалительных процессов в его слизистой. Скопление цепней может вызвать закупорку кишечника. Описаны случаи проникновения паразита в желчевыводящие пути и панкреатический проток с последующей их обструкцией. Но чаще дискинезия выводящих путей печени и поджелудочной железы развивается вследствие нервно-рефлекторных воздействий гельминта.
Интенсивное потребление паразитом пищевых веществ, нарушение процессов всасывания в результате механического повреждения слизистой и воспалительных процессов в ней создают дефицит наиболее ценных компонентов питательных веществ, вследствие чего постоянно ощущается чувство голода, повышается потребление пищи, снижается масса тела.
Определенное значение имеет и сенсибилизация организма к продуктам метаболизма паразита.
Постоянное выползание члеников из заднего прохода и их передвижение по коже угнетающе действует на психику больного.
Клиническая картина. Нередко заболевание протекает бессимптомно. В этом случае единственным его проявлением служит обнаружение члеников паразита в фекалиях либо самостоятельное, активное выползание проглоттид через анус.
Чаще всего клинические проявления заболевания наблюдаются после полного развития паразита и по времени совпадают с началом выделения им члеников. Наиболее часто отмечаются диспепсические расстройства. Больные жалуются на тошноту, иногда рвоту, изжогу, изменение аппетита, чувство тяжести и боли в животе, метеоризм, неустойчивый стул. Нередко наблюдается снижение секреции желудочного сока. Закупорка кишечника клубками тениид может привести к развитию симптомов кишечной непроходимости. Иногда при тениаринхозе наблюдается симптомокомплекс, характерный для язвенной болезни двенадцатиперстной кишки или желчной колики.
У детей могут развиваться астеноневротические проявления: повышенная раздражительность, головная боль, обмороки, нарушение сна. Описаны отдельные случаи развития синдрома Меньера и эпилептиформных судорог. У части больных отмечаются общетоксические симптомы: слабость, повышенная утомляемость, снижение работоспособности.
Показатели периферической крови у большинства больных не выходят за границы нормы, иногда могут наблюдаться умеренная эозинофилия, лейкопения, небольшая анемия и повышенная СОЭ.
Лабораторная диагностика. Обычные методы копрологических исследований, применяющиеся для диагностики большинства гельминтозов, при тениаринхозе малоэффективны, так как матка у тениид не имеет выводного отверстия, и некоторая часть яиц попадает в кал лишь при ее разрыве во время отделения члеников.
Наиболее распространенным методом, принятым при массовых обследованиях населения, является опрос о выделении члеников. При тениаринхозе членики обычно выходят днем, совершая активные движения, и продолжают некоторое время перемещаться по телу, вызывая ощущение ползания чего-то липкого и холодного, поэтому они чаще замечаются больными, чем проглоттиды других цестод. Поскольку активно двигающиеся членики оставляют яйца на перианальных кожных складках, для диагностики применяется перианальный соскоб по той же методике, как и при энтеробиозе.
Яйца всех тениид практически неотличимы друг от друга, поэтому дифференциальная диагностика проводится на основании изучения морфологии проглоттид или сколекса гельминта. Членики, сдавленные между предметными стеклами, просматриваются на свет. В членике цепня невооруженного от центрального ствола матки отходит 17-32 боковых ответвлений, а у цепня вооруженного их 8-12. Если матка плохо видна, то перед просмотром членики выдерживают некоторое время в 50% растворе глицерина.
Головка цепня, помещенная между двумя предметными стеклами, рассматривается под малым увеличением микроскопа. Дифференциальнодиагностическим признаком бычьего цепня служит отсутствие крючьев на сколексе. Нередко бычьего цепня можно обнаружить при рентгено- логическом исследовании кишечника с контрастированием; при этом он просматривается в виде бледных длинных полос.
Осложнения. Механическая кишечная непроходимость, перфорация кишечной стенки, аппендицит, холангит, панкреатит. Прогноз, как правило, благоприятный.
Лечение. Для
лечения больных используется никлозамид (фенасал). Препарат
принимается утром натощак или вечером, через 2 часа после легкого
ужина, состоящего из жидкой, обезжиренной пищи. Суточную дозу для
взрослых 2-3 г (8-12 таблеток) принимают за один прием. Детям до 2-х
лет назначают
Эффективным препаратом является также празиквантель (азинокс), который назначается в суточной дозе 25 мг/кг внутрь в один прием. Его эффективность составляет 90%. Контроль за эффективностью дегельминтизации затруднен, так как вследствие разрушения тканей паразита трудно обнаружить его сколекс.
Эффективность лечения контролируют через 1-3 месяца. При появлении члеников паразита проводят повторный курс.
Профилактика. Мероприятия по профилактике и борьбе с тениаринхозом должны быть направлены на обезвреживание источника инвазии, охрану внешней среды от фекального загрязнения и блокирование путей передачи. Выполнение комплекса мер профилактики проводится медицинской и ветеринарной службами при участии административных и хозяйственных структур.
С целью выявления источника инвазии в эндемичных районах проводят массовые гельминтологические обследования населения. Хорошие результаты дает опрос населения на обнаружение члеников паразита. Выявленные больные подлежат дегельминтизации.
С целью
профилактики тениаринхоза в высокоэндемичных его очагах рекомендуется
проводить профилактическое лечение лиц групп риска путем назначения им
Охрана внешней среды от загрязнения онкосферами включает меры по улучшению санитарного состояния населенных пунктов и животноводческих комплексов, предохранение почвы и водоемов от загрязнения их фекалиями человека.
Проводится санитарный контроль за утилизацией экскрементов человека, санитарным состоянием туалетов и сточных вод. Обеспечивается правильное содержание и кормление крупного рогатого скота, предотвращается доступ животных в места, загрязненные фекалиями человека. Для профилактики заражения человека цистицерками следует обеспечить обязательную тщательную ветеринарную экспертизу мяса крупного рогатого скота, особенно скота из индивидуальных хозяйств. При послеубойном осмотре туш исследуются продольные и поперечные разрезы жевательных мышц, мышц языка, сердца, шейных, поясничных и других мышц передней части туловища. При обнаружении более трех цистицерков на площади 40 см2 мышц головы и сердца и на одном из разрезов мышц туловища всю тушу отправляют для технической утилизации или уничтожают. Если при том же количестве цистицерков в мышцах головы и сердца на разрезах мышц туловища цистицерки отсутствуют или обнаруживаются в количестве не более трех, то голову и сердце животного отправляют на утилизацию, а тушу направляют на
вторичную переработку (изготовление фаршевых колбасных изделий или фаршевых консервов). Внутренний жир перетапливают.
Для обеззараживания мяса и мясопродуктов, пораженных цистицерками бычьего цепня, используют замораживание. При снижении температуры в толще мяса до -12 ?С все цистицерки погибают немедленно. При температуре -6...-9 ?С тушу выдерживают в холодильной камере не менее 24 часов.
Головной мозг северных оленей обеззараживается при температуре 10-15 ?С или ниже в течение 2-х суток. Его нагревание до 90-100 ?С (при варке) в течение 5-10 минут приводит к гибели всех цистицерков.
Для обезвреживания говядины от цистицерков ее проваривают. Куски мяса массой до
Допускается обеззараживание говядины путем ее засолки. Куски мяса массой не более
Личная профилактика заключается в исключении из рациона сырого и недостаточно термически обработанного мяса крупного рогатого скота, а также мяса, не прошедшего ветеринарный контроль (неклей- меного).
Большое значение в профилактике имеет санитарно-просветительная работа. Население должно знать, насколько опасно использование в пищу мяса, не прошедшего ветеринарную экспертизу, и какими способами можно надежно обезвредить цистицеркозное мясо.
4.2.2. Тениоз
Тениоз - биогельминтоз, одним из основных клинических проявлений которого является нарушение функций желудочно-кишечного тракта.
Этиология. Возбудитель - цепень вооруженный (свиной) - Taenia solium. Его стробила, состоящая из 800-1000 члеников, достигает 2-3 м в длину (рис. 4.18).
Сколекс диаметром 1-2 мм имеет 4 полусферические боковые мышечные присоски. На верхушке сколекса расположен хоботок, вооруженный 22-23 короткими и длинными хитиновыми крючьями. Крючья эти располагаются в два ряда, чередуясь между собой (отсюда название «вооруженный») (рис. 4.19).
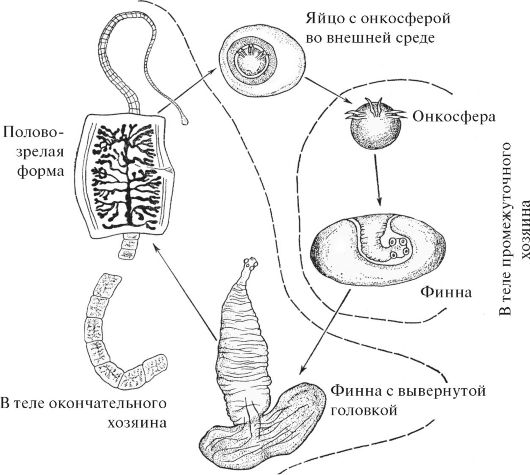
Рис. 4.18. Свиной цепень T.solium
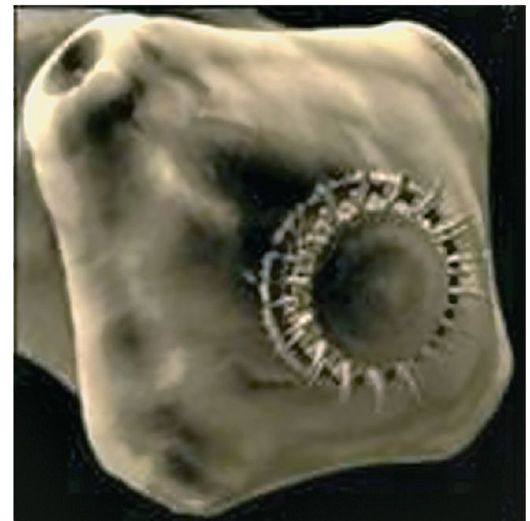
Рис. 4.19. Сколекс T.solium
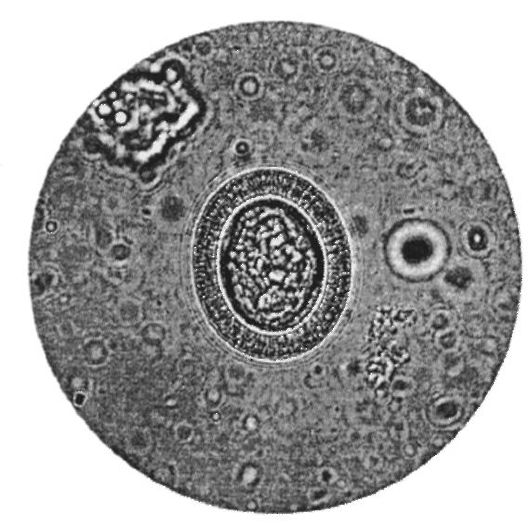
Рис. 4.20. Яйцо T.solium
Прикреплению паразита к слизистой оболочке кишечника хозяина способствует также секрет имеющихся в сколексе желез.
Сколекс со стробилой соединяет небольшая нерасчлененная шейка. Ширина бесполых проглоттид передней части стробилы больше длины. Проглоттиды средней ее части содержат гермафродитные комплексы половой системы. Форма их квадратная, переходящая по мере удаления от переднего конца паразита в удлинен-
но-прямоугольную. Размеры проглоттид составляют 12-15 χ 6-7 мм.
Гермафродитный членик по своему строению сходен с члеником бычьего цепня. Диагностическим признаком служит строение яичника, который в отличие от цепня бычьего имеет маленькую добавочную (третью) дольку, располагающуюся в углу, образованном стволом матки и влагалищем.
В задней части стробилы расположены зрелые членики. Каждый из них заполнен маткой, состоящей из центрального ствола с 8-12 боковыми ответвлениями. Матка, как и у всех цепней закрытого типа (не имеет выводного отверстия), содержит 30 000-50 000 яиц. Яйца свиного цепня имеют то же строение, что и цепня бычьего (рис. 4.20).
Взрослые свиные цепни паразитируют в тонкой кишке человека, который является их единственным дефинитивным хозяином. Отделившиеся от стробилы зрелые членики выделяются наружу только пассивно, с фекалиями больного. Яйца, заключенные в члениках, содержат вполне сформированную личинку, которая не нуждается в дозревании во внешней среде. При отрыве от стробилы часть яиц выдавливается из матки через разрушенный передний край проглоттиды.
Промежуточными хозяевами (рис. 4.21) чаще всего служат домашняя свинья, дикий кабан, медведь, верблюд, реже - собака, кошка, кролик, заяц и др. Они заражаются при заглатывании члеников и онкосфер с пищей или водой. Инвазия свиней часто бывает весьма интенсивной, так как свиньям свойственна копрофагия, при этом они заглатывают целые проглоттиды цепня. В отличие от цепня бычьего личинки цепня вооруженного могут паразитировать и у человека, вызывая тяжелое заболевание - цистицеркоз.
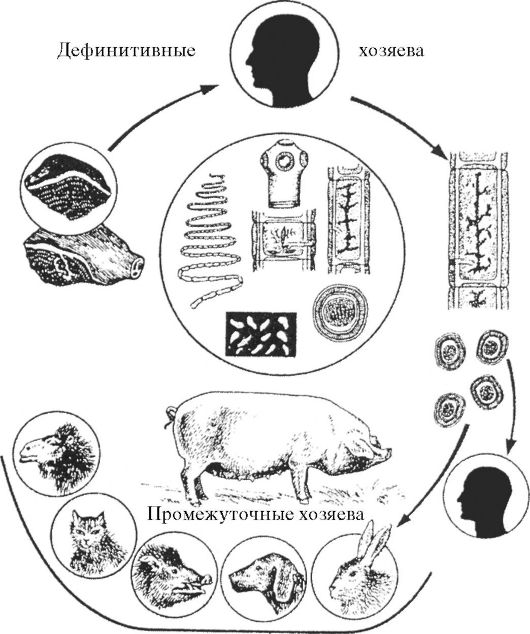
Рис. 4.21. Цикл развития T.solium
В
кишечнике промежуточного хозяина онкосферы с помощью своих крючьев так
же, как и зародыши бычьего цепня, проникают через стенку кишки в
кровеносные сосуды и с током крови разносятся по всему организму. Чаще
всего они локализуются в межклеточной соединительной ткани, где в
течение 60-70 дней после заражения из них формируются пузыревидные
ларвоцисты-цистицерки (Cysticercus cellulosae), имеющие в диаметре 5-8
мм, а в паренхиматозных органах достигающие величины
Окончательный хозяин - человек - заражается при проглатывании цистицерков, находящихся в непроваренном или непрожаренном мясе. В двенадцатиперстной кишке под действием желчи и пищеварительных ферментов сколексы выворачиваются из пузырьков и прикрепляются к слизистой оболочке кишечника, внедряясь в нее своими крючьями. Затем начинается формирование стробилы; через 2-3 месяца после заражения от нее начинают отделяться членики, наполненные зрелыми яйцами. С фекалиями выделяются преимущественно кусочки стробилы, состоящие из 5-6 члеников. Продолжительность жизни цепня вооруженного в кишечнике человека составляет несколько лет.
В настоящее время на территории России отмечаются лишь спорадические случаи заболеваний тениозом. Несколько чаще тениоз встречается в Беларуси и Украине. Тениоз регистрируется во всех странах, где развито свиноводство, в том числе в Индии, Северном Китае, Юго- Восточной Азии, Латинской Америке, Европе и др.
Эпидемиология. Источником заражения является инвазированный человек, выделяющий с фекалиями членики и яйца гельминта. Рассеивание их в окружающей среде приводит к заражению промежуточных хозяев (главным образом, свиней). Этому способствует устойчивость онкосфер к воздействию неблагоприятных факторов внешней среды. Они переносят высыхание до 10 месяцев; в зоне умеренного климата способны перезимовать под снегом, оставаясь жизнеспособными при колебаниях температуры от +4? до -38 ?С. К высоким температурам онкосферы более чувствительны. В воде при температуре 65 ?С они гибнут через 3 минуты. Летом на поверхности почвы солнечные лучи губят их в течение двух суток, но под защитой растительности онкосферы могут выживать до 40 дней.
Люди заражаются при употреблении в пищу недостаточно термически обработанного мяса свиней, иногда мяса диких кабанов и медведей. Поскольку свиньям свойственна копрофагия, их мясо иногда бывает очень интенсивно заражено цистицерками. Именно поэтому при тениозе в желудочно-кишечном тракте человека часто паразитирует много экземпляров цепня свиного.
Больной тениозом представляет непосредственную опасность для окружающих как источник заражения цистицеркозом.
Патогенез. При неосложненном кишечном тениозе в основе патоге- неза лежат те же механизмы, что и при тениаринхозе.
Клиническая картина. Клинические симптомы у этих двух нозологических форм идентичны, однако при тениозе они, как правило, более выражены. В основном возникают диспепсические и неврологические
расстройства: нарушение аппетита, тошнота, рвота, боли в животе, неустойчивый стул, периодические головные боли, головокружение, обморочные состояния, нарушение сна.
Бессимптомные формы тениоза встречаются в 2-3 раза реже, чем при инвазии бычьим цепнем. Во многом это объясняется большей частотой множественных инвазий при тениозе. Однако даже очень интенсивные инвазии (более 100 паразитов) иногда протекают субклинически.
Диагностика. В эндемичном районе наличие инвазии свиным цепнем можно заподозрить при жалобах больного на умеренно выраженные диспепсические расстройства и общетоксические проявления, особенно если в анамнезе имеются сведения об употреблении в пищу недостаточно термически обработанного свиного мяса и сала.
Лабораторная диагностика. Окончательный диагноз тениоза основывается на обнаружении в фекалиях больных зрелых члеников свиного цепня, которые отделяются группами по 5-6 экземпляров, реже поодиночке. Их следует дифференцировать от члеников бычьего цепня. Яйца в фекалиях обнаруживаются не всегда, но значительно чаще, чем яйца цепня бычьего. Тениоз дифференцируют с другими гельминтозами, протекающими с поражением ЖКТ, и прежде всего с тениаринхозом. Если точно установить вид цепня не удается, лечение проводят как при тениозе.
Осложнения. Наиболее часто встречается механическая кишечная непроходимость, перфорация кишечной стенки, аппендицит, холангит, панкреатит. Грозным осложнением является развитие цистицеркоза глаз и мозга. Прогноз, как правило, благоприятный.
Лечение. Лечение тениоза проводится в стационарных условиях и требует особо осторожного подхода ввиду опасности развития цистицеркоза.
Препаратами выбора являются празиквантель (азинокс) и никлозамид (фенасал), назначаемые так же, как и при дифиллоботриозе. При лечении тениоза показано использование солевых слабительных.
Контроль эффективности лечения проводится путем исследования фекалий на наличие члеников через 1-3 месяца после терапии.
Во избежание риска заражения больного и окружающих цистицеркозом необходимо принять все возможные меры для предотвращения загрязнения его испражнениями или рвотными массами белья, предметов обстановки, помещений и уборных. Испражнения больного заливают двойным объемом крутого кипятка и выдерживают в течение 30 минут. Их можно обеззараживать также 10-20% раствором хлорной извести или негашеной известью при экспозиции 5-6 часов. Раковины, краны, ручки дверей и другие предметы следует обрабатывать дезсредствами.
Профилактика. Комплекс профилактических и противоэпидемических мероприятий при тениозе во многом сходен с аналогичными при тениаринхозе. Он включает выявление и лечение всех больных тениозом, санитарное просвещение населения, благоустройство населенных пунктов, обеспечение санитарного надзора за содержанием и убоем свиней, а также ветеринарный контроль мяса.
Метод опроса населения о выделении члеников Т. solium менее эффективен, чем при тениаринхозе, так как членики свиного цепня не обладают активной подвижностью и поэтому реже обнаруживаются.
Учитывая высокую степень устойчивости цистицерков свиного цепня к воздействию низких температур, обеззараживание свиных туш методом замораживания производится при более жестком температурном режиме. Температуру толщи мышц свиной туши необходимо довести до -10 ?С и выдержать тушу при температуре воздуха в камере -12 ?С в течение 10 суток.
4.2.3. Цистицеркоз
Цистицеркоз - биогельминтоз, который вызывается паразитированием в тканях и органах человека личиночной стадии Т. solium - цистицерка (Cysticercus cellulosae). Болезнь проявляется разнообразными симптомами в зависимости от локализации цистицерков. Этиология (см. Тениоз).
Эпидемиология. Эпидемические процессы при цистицеркозе и тениозе едины, так как возбудителями этих инвазий являются разные стадии развития одного и того же паразита. Единственным источником инвазии при цистицеркозе является человек. Географическое распространение цистицеркоза полностью совпадает с распространением тениоза.
Патогенез. Человек заражается цистицеркозом в результате ауто- суперинвазии или заглатывании яиц (онкосфер) Т. solium. При ауто- суперинвазии из кишечника человека зрелые членики забрасываются в желудок, где онкосферы внедряются в капилляры и с током крови заносятся в различные органы и ткани. Примерно через два месяца они превращаются в цистицерков. Цистицерки оказывают механическое воздействие на окружающие ткани, а продукты их жизнедеятельности и распада погибших личинок вызывают токсико-аллергические реакции в организме больного (рис. 4.22). Вокруг цистицерков возникает гра- нулематозная реакция из эозинофилов, лимфоцитов, нейтрофильных лейкоцитов, плазматических и гигантских клеток. При нейроцистицеркозе отмечаются васкулиты, глиальная реакция, иногда обнаруживается картина энцефалита. Постепенно вокруг цистицерка формируется фиброзная капсула (рис. 4.23).
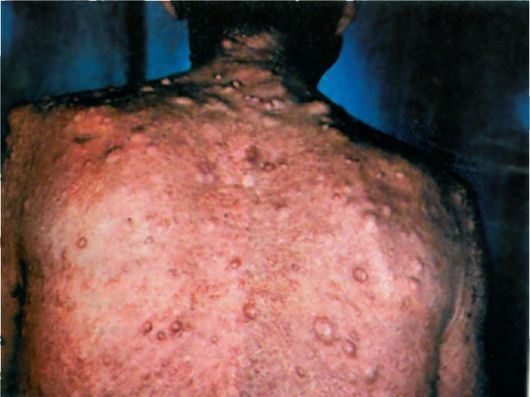
Рис. 4.22. Цистицерки под кожей больного
Рис. 4.23. Цистицерки в мозге
В развитии цистицерка различают стадии жизнеспособного (до 5 лет после заражения), отмирающего и погибшего паразита. На первой стадии воспалительная реакция вокруг цистицерков выражена умеренно. В стадии отмирания происходит набухание и расплавление личинки. Образующиеся при этом продукты распада оказывают более выраженное воздействие на организм хозяина, вследствие чего появляется субфебрильная лихорадка, увеличивается число эозинофилов и лейкоцитов в периферической крови, повышается СОЭ. Капсула, возникающая вокруг паразита, уплотняется. Погибший паразит подвергается обызвествлению. При этом все нарушения тканей, вызванные механи- ческим действием паразита, сохраняются.
Клиническая картина. Клинические проявления цистицеркоза очень разнообразны и зависят от локализации паразитов, их количества, стадии развития и индивидуальной реактивности организма больного.
Цистицерки чаще всего паразитируют в подкожной клетчатке, головном мозге, глазах, мышцах, сердце, печени, легких и брюшине (перечислены в порядке убывания частоты поражений). Возможно пораже- ние сразу нескольких органов.
Наиболее опасна локализация цистицерков в мозге (41-82% случаев) (см. рис. 4.23). При локализации их в больших полушариях появляются симптомы арахноидита. Заболевание начинается с внезапных или постепенно нарастающих приступов повышения внутричерепного дав- ления со светлыми промежутками продолжительностью от нескольких месяцев до нескольких лет. Такие приступы сопровождаются головной болью, рвотой, судорогами, параличами, парезами конечностей, припадками по типу джексоновской эпилепсии. Возможны периодические нарушения в психике в виде галлюцинаторных состояний. Постепенно у больных нарушается память, снижается интеллект. Синдром поражения основания мозга проявляется симптомами развития арахноидита, распространяющегося на черепно-мозговые нервы, ножки мозга, дно III желудочка и т.д. Нарушается отток ликвора с последующим развитием гидроцефалии. Иногда присоединяются мозжечковые расстройства. У половины больных цистицеркозом поражаются глаза (как правило, один глаз). Наиболее часто (в 73,2% случаев), цистицерк локализуется в задней камере глаза.
Вначале, когда паразит попадает под сетчатку, возникает местное кровоизлияние, а затем ее отслойка. Позднее цистицерк проникает в стекловидное тело, в котором может оставаться жизнеспособным в течение нескольких месяцев, обычно не вызывая каких-либо серьезных изменений в стекловидном теле. В некоторых случаях под воздействием продуктов обмена паразита возникает воспалительная реакция, приводящая к помутнению стекловидного тела, развитию ирита и иридоциклита. В случае гибели паразита развиваются тяжелые воспалительные реакции, проявляющиеся эндофтальмитом с последующим фтизисом глазного яблока.
В начальной стадии поражения глаз больные жалуются на возникновение «искр», сеток перед глазами, искажение предметов и постепенное снижение зрения. Впоследствии может наступить слепота. Скорость развития процесса определяется близостью локализации цистицерка к желтому пятну. В редких случаях цистицерк локализуется в передней камере глаза. При этом в течение нескольких недель и даже месяцев не
возникает каких-либо реакций глаза на присутствие цистицерка. При гибели паразита развивается пластический ирит, иридоциклит, помутнение роговицы и жидкости передней камеры глаза, что в конечном итоге может привести к потере глаза.
Довольно часто
(16,2% случаев) цистицерк локализуется в подконъюнктивальном
пространстве, где возникает желтоватая припухлость размером от 3 до
При локализации в подкожной жировой клетчатке век цистицерк может длительное время не вызывать болезненных явлений и не при- влекать внимания больных.
Наиболее доброкачественное течение имеет цистицеркоз подкожной клетчатки (50% случаев). При этом даже высокая интенсивность инвазии не вызывает значительных нарушений функций организма, и больные обычно сохраняют работоспособность.
Диагностика. Диагноз устанавливается на основании анамнести- ческих, клинических, лабораторных и эпидемиологических данных и подтверждается инструментальными и иммунологическими методами исследований (ИФА и др.).
Для идентификации поражений мозга используют КТ и МРТ, ультразвуковое исследование, ангиографию головного мозга. В цереброспинальной жидкости отмечается плеоцитоз с преобладанием эозинофилов и лимфоцитов, повышение уровня белка. В более поздний период, когда цистицерки обызвествляются, их можно выявить с помощью обычных рентгенологических исследований.
При внутриглазной локализации (если среды глаза прозрачны) цистицерк хорошо виден при биомикроскопии или офтальмоскопии, как прозрачное кистозное образование с легкой жемчужной окраской.
В случае помутнения сред глаза и невозможности проведения офтальмоскопии эффективной может оказаться ультразвуковая диагностика.
При цистицеркозе подкожной клетчатки диагноз устанавливается рентгенологически. При необходимости производится биопсия цистицеркозных узлов.
Дифференциальный диагноз цистицеркоза проводится с опухолями, нейроинфекциями, эхинококкозом, при цистицеркозе глаза - с токсокарозом.
Осложнения. Локализация цистицерков в области жизненно важных структур головного мозга может привести к летальному исходу.
Лечение. Для терапевтического лечения больных церебральным цис- тицеркозом применяется празиквантель (азинокс) в суточной дозе 50 мг/кг, назначаемой в 3 приема в течение 14 дней. За 2-3 дня до начала этиотропной терапии и во время ее рекомендуется назначение кортикостероидов в суточной дозе 30-60 мг. Возможно применение албендазола по 15 мг/кг в сутки в течение 30 дней. При необходимости курс терапии может быть проведен повторно через 3-4 недели. В остром периоде цистицеркозного энцефалита перед проведением курса антигельминтных препаратов назначаются противосудорожные средства.
При цистицеркозе других органов возможно проведение 8-дневных курсов албендазола. При подкожном цистицеркозе празиквантель (азинокс) назначают в суточной дозе 60 мг/кг в 3 приема в течение 6 дней. При цистицеркозе глаз этиотропная терапия противопоказана.
Хирургическое удаление цистицерков показано при поражении глаз, а также при цистицеркозе желудочков головного мозга и поражении спинного мозга.
Профилактика такая же, как при тениозе. Учитывая то, что больные цистицеркозом одновременно могут быть инвазированы взрослым свиным цепнем и служить источником инвазии для окружающих, их необходимо обследовать на тениоз.
4.3. Нематодозы. Общая характеристика нематод
Нематодозы - заболевания, вызываемые паразитическими круглыми червями нематодами. Они распространены на всех континентах. В мире инвазировано нематодами около 3-х млрд человек.
Нематоды имеют удлиненную, цилиндрическую форму тела. Поперечное сечение тела круглое. Размеры нематод колеблются от
Снаружи нематоды покрыты кожно-мускульным мешком, образованным кутикулой, гиподермой и одним слоем продольных мышц. Кутикула многослойна, она служит наружным скелетом, защищает тело нематод от механических повреждений и химических воздействий. Под кутикулой залегает гиподерма, представляющая собой симпласт и состоящая из подстилающего кутикулу слоя - субкутикулы и продольных валиков, число которых варьирует от 4 до 16 и более. В гиподерме активно протекают обменные процессы и происходит интенсивный биосинтез. Под гиподермой лежит один слой продольных мышц, разделенных
валиками гиподермы на несколько продольных лент. Движения нематод ограничены. Тело изгибается только в дорсовентральной плоскости благодаря тому, что брюшные и спинные мышечные ленты действуют как антагонисты. Внутри кожно-мускульного мешка находится первичная полость тела, не имеющая специальной выстилки, содержащая полостную жидкость и внутренние органы. Полостная жидкость находится под большим давлением, что создает опору для мускулатуры (гидроскелет) и играет важную роль в обменных процессах. У некоторых нематод эта жидкость токсична.
Пищеварительная, выделительная, нервная и половая системы хорошо развиты. Дыхательная и кровеносная системы отсутствуют.
Пищеварительная система. Пищеварительная система представлена прямой трубкой, которая делится на три отдела - передний, средний и задний. Она начинается ротовым отверстием, расположенным на переднем конце тела. У большинства нематод рот окружен тремя губами. У некоторых видов имеется ротовая капсула, вооруженная зубами, пластинками или другими режущими элементами. За ртом следуют глотка и цилиндрический пищевод, который у некоторых видов имеет одно или два расширения (бульбусы). За пищеводом расположена средняя кишка, переходящая в заднюю, заканчивающаяся анальным отверстием. У некоторых видов нематод анальное отверстие отсутствует.
Выделительная система. Выделительная система представлена 1-2 одноклеточными кожными железами, заменяющими протонефридии. От железы отходят 2 длинных боковых канала, расположенных вдоль всего тела нематоды в боковых валиках гиподермы. Сзади каналы оканчиваются слепо, а в передней части соединяются в один непарный канал, открывающийся наружу, иногда близ переднего конца тела. У нематод имеются особые фагоцитарные клетки (1-2 пары), в которых задержи- ваются и накапливаются различные нерастворимые продукты обмена веществ. Они расположены в полости тела по ходу боковых выделительных каналов в передней трети тела.
Нервная система. Нервная система представлена окологлоточным нервным кольцом, окружающим переднюю часть пищевода. От кольца отходят нервные стволы вперед и назад. Вперед идут 6 коротких нервных веточек. Назад направляются тоже 6 стволов, среди которых наиболее мощные дорзальный и вентральный, проходящие в валиках гиподермы. Оба главных нервных ствола соединяются между собой многочисленными комиссурами, которые имеют вид тонких полуколец, опоясывающих тело попеременно то с правой, то с левой стороны. Органы чувств развиты слабо. Имеются органы осязания и химического чувства.
Половая система. Нематоды раздельнополы и обладают внешним половым диморфизмом. Самки крупнее самцов. У некоторых самцов задний конец закручен на брюшную сторону. У самца имеется один трубчатый семенник, переходящий в семяпровод, после которого следует семяизвергательный канал, открывающийся в задний отдел кишечника. У самцов имеется клоака. Около клоаки у самцов расположены совокупительные спикулы. У некоторых нематод самцы имеют в дополнение к спикулам копулятивную бурсу, представляющую собой расширенные и уплощенные в виде крыльев боковые части заднего конца тела.
У самок половая система парная, трубчатая, состоит из яичников, яйцеводов, маток и влагалища. Самые узкие, слепо замкнутые отделы трубки представляют собой яичники. Они постепенно переходят в более широкие отделы, выполняющие функции яйцеводов. Наиболее широкие отделы матки - соединяются между собой и образуют непарное влагалище, которое открывается наружу на брюшной стороне в передней трети тела нематоды. Для нематод характерны половое размножение и внутреннее оплодотворение.
Развитие. Большинство нематод откладывают яйца, но есть и живо- родящие виды. Формирование и созревание личинок происходит чаще всего во внешней среде. У некоторых видов цикл развития может завершаться в одном организме хозяина. У большинства видов в яйце развивается личинка до инвазионной стадии во внешней среде и выходит из него в кишечнике хозяина, проглотившего яйцо. В процессе развития личинки несколько раз линяют.
Личинки, у ряда нематод, выйдя из яйца во внешней среде, способны вести свободный образ жизни в почве. Различают рабдитовидные и филяриевидные личинки. Рабдитовидные личинки имеют два расшире- ния (бульбуса) в пищеводе, а у филяриевидных - пищевод цилиндрической формы. Личинки могут активно проникать через кожу хозяина, а не только попадать через рот.
Циклы развития нематод разнообразны. Большинство нематод относятся к геогельминтам. Их развитие происходит прямым путем, без смены хозяев. Для личинок многих геогельминтов характерна миграция по органам и тканям хозяина к месту окончательной локализации, где они достигают половой зрелости. Некоторые геогельминты развиваются без миграции личинок. Геогельминты, поражающие человека, не могут паразитировать у животных. Нематодозы, вызываемые этими гельминтами, относят к антропонозным болезням. Другие виды нематод относят к биогельминтам. Их развитие происходит непрямым путем. Они нуждаются в промежуточном хозяине. Ими могут быть кро-
вососущие насекомые, ракообразные, либо один и тот же организм служит последовательно сначала окончательным, а затем промежуточным хозяином.
Заражение человека нематодами-биогельминтами происходит как алиментарным путем при поедании промежуточного хозяина, так и в результате передачи их переносчиком.
Большинство нематод, паразитирующих у человека, в половозрелой стадии обитают в пищеварительной системе человека. Некоторые имеют локализацию в лимфатических узлах и сосудах, в соединительной ткани, под кожей конечностей, в подкожной жировой клетчатке.
4.3.1. Кишечные нематодозы 4.3.1.1. Аскаридоз
Аскаридоз - антропонозное заболевание, геогельминтоз. Взрослые аскариды локализуются в тонком кишечнике человека.
Этиология. Возбудитель аскаридоза - аскарида человеческая, Ascaris lumbricoides. Аскариды - крупные раздельнополые нематоды веретенообразной формы, в живом состоянии розовато-желтого цвета. На головном конце аскариды имеется ротовое отверстие, окруженное тремя губами.
Самки имеют длину 25-40 см, ширину - 5-6 мм. Хвостовой конец самки прямой, имеет конический придаток и 2 крупных сосочка, находящихся на брюшной стороне тела. Кпереди от заднего конца тела находится анус. Вульва открывается в конце передней трети тела самки, где у половозрелых гельминтов имеется кольцевидная перетяжка, служащая местом опоры и охвата задним концом самца тела самки при совокуплении.
Самцы достигают длины 15-25 см, ширины
Оплодотворенные яйца аскариды овальной или округлой формы размерами 0,050-0,070 χ 0,040-0,050 мм, покрыты четырьмя оболочками. Наружная оболочка толстая, фестончатая, прокрашивается пигментами фекалий в коричневый цвет. Зародышевая масса концентрируется в центре яйца, оставляя свободными полюса. Встречаются яйца, лишенные наружной оболочки. При отсутствии самцов в фекалиях больного обнаруживают неоплодотворенные яйца, отличающиеся более крупными раз-
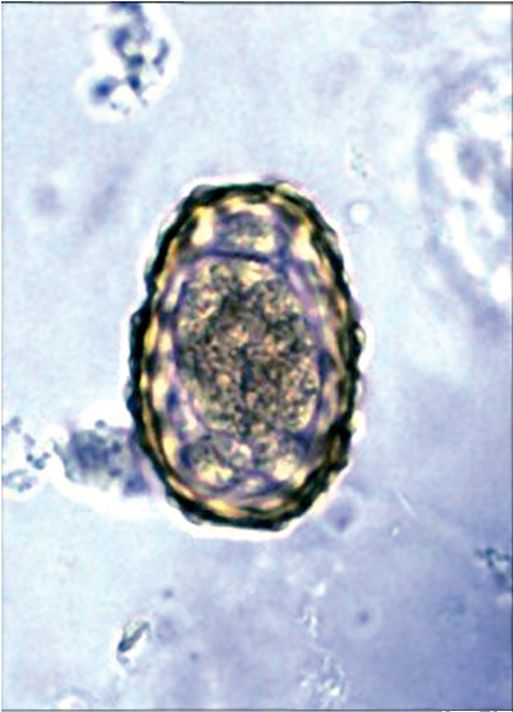
Рис. 4.24. Яйцо аскариды
мерами, неправильной формой и отсутствием зародышевой массы (рис. 4.24).
Цикл развития (рис. 4.25). Человек заражается аскаридозом, проглатывая яйца, содержащие личинки, достигшие инвазионной стадии. В тонком кишечнике человека личинки освобождаются от яйцевых оболочек, проникают сквозь стенку кишечника в кровеносные сосуды и совершают миграцию по кровеносному руслу и тканям хозяина. С током крови они попадают в воротную вену, сосуды печени, нижнюю полую вену, правое предсердие и через легочную артерию в капилляры альвеол легких
(рис. 4.26). Через стенки капилляров личинки проникают в полость альвеол, затем бронхиол и мигрируют по воздухоносным путям. Из трахеи при откашливании с мокротой личинки попадают в глотку, вторично заглатываются и снова оказываются в тонком кишечнике. За время миграции личинки линяют два раза и увеличиваются в размерах с 0,19-0,25 мм до 1,5-2,2 мм. Миграция личинок аскарид длится около двух недель. В кишечнике личинки растут, еще раз линяют и через 2-2,5 месяца становятся половозрелыми. Продолжительность жизни взрослых аскарид около 1 года.
Эпидемиология. Аскаридоз - наиболее распространенный гельминтоз в мире. По данным ВОЗ, в мире аскаридозом заражено более 1,2 млрд человек. Из них ежегодно умирают от этой инвазии примерно 100 тыс. человек. Аскаридоз распространен в 153 из 218 стран мира, расположенных в зонах умеренного, суб- тропического и тропического климата.
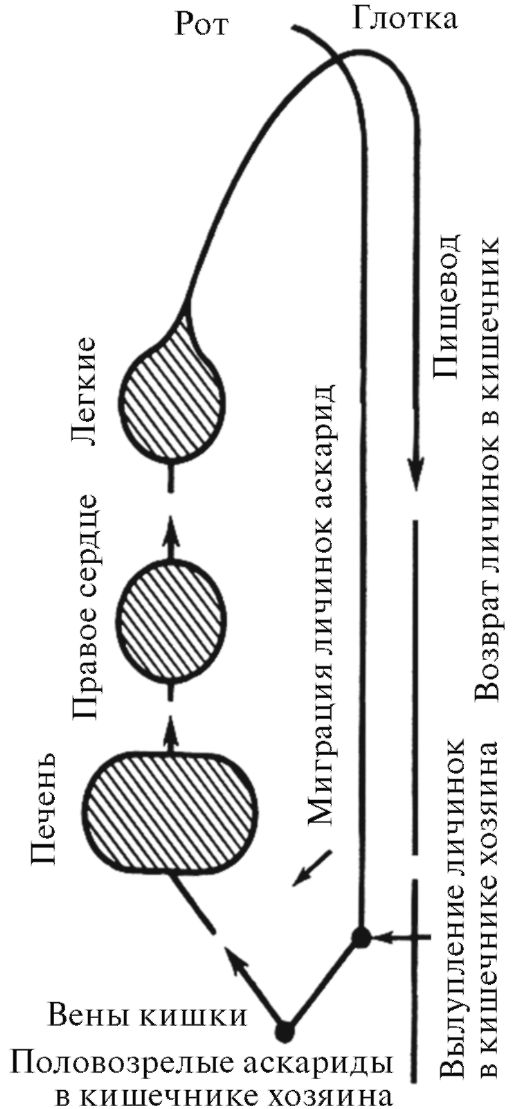
Рис. 4.25. Цикл развития аскариды
Рис. 4.26. Личинка аскариды в легких
Более 50% населения из числа обследованных заражено аскаридозом в Нигерии, Конго, Бразилии, Эквадоре, Ираке, Малайзии, Афганистане, Индонезии. В зонах пустынь, полупустынь и вечной мерзлоты аскари- доз встречается очень редко.
Источник заражения - больной человек, выделяющий во внешнюю среду с экскрементами яйца аскариды.
Самка аскарид в сутки откладывает до 240 000 яиц. Максимальное число яиц выделяется на 5-6 месяцах жизни самки. К 7-му месяцу овуляция заканчивается, и самка перестает выделять яйца.
Для того, чтобы яйца стали инвазионными, необходимы следующие условия: наличие кислорода, влажность не ниже 8%, температура 12- 37 ?С и определенное время. При оптимальных условиях (температура 24-30 ?С и влажность 90-100%) через 2-3 недели в яйце после первой линьки формируется инвазионная личинка, способная заразить человека. Развитие яиц происходит дольше в умеренном и прохладном климате, чем в теплом. При благоприятных условиях яйца могут сохранять жизнеспособность до 10 лет.
В умеренном климате развитие яиц в почве начинается в апреле-мае. Зимой развития яиц не происходит. В мае-июле в яйце сформируются инвазионные личинки. Заражение человека инвазионными яйцами аскарид может произойти в течение всего года, поскольку они устойчивы к внешним воздействиям и длительное время остаются жизнеспособными. Наибольшее число инвазионных яиц накапливается в почве в летне-осенний период, когда происходит массовое заражение населения аскаридозом. Наиболее продолжительный сезон заражения отмечается на юге, а наименее - в северных районах. Наибольшая степень
инвазированности населения взрослыми аскаридами бывает зимой, а наименьшая - в начале лета.
Факторы передачи аскаридоза - почва, загрязненная яйцами аскарид, овощи, ягоды, фрукты, вода. В водоемы могут попадать сточные воды из канализации или фекальные массы из расположенных вблизи уборных. Механическими переносчиками яиц могут быть мухи, тараканы.
Заражение человека происходит при непосредственном контакте с почвой, содержащей инвазионные яйца. При несоблюдении правил личной гигиены яйца из почвы с немытыми руками попадают в рот челове- ка. Заражение может происходить через различные предметы обихода и продукты питания, загрязненные яйцами аскарид. В жилые помещения яйца могут попадать с пылью, заноситься на подошвах обуви.
Очаги аскаридоза разнообразны по интенсивности передачи инвазии, зависящей от степени загрязнения внешней среды инвазионными яйцами аскарид, санитарных условий, гигиенических навыков населения и климатических факторов. Очаги аскаридоза обычно формируются в сельской местности или в тех районах городов, где имеются источники заражения, недостаточное санитарное благоустройство, есть особенности быта и хозяйственной деятельности, способствующие попаданию инвазионных яиц из внешней среды к человеку. Аскаридозом в городах люди болеют чаще всего после возвращения из сельской местности, с садовых участков и дач, где в качестве удобрений иногда используют необеззараженные фекалии человека, а также при употреблении в пищу немытых овощей и фруктов, ягод, привезенных из очагов аскаридоза, и при несоблюдении правил личной гигиены.
Восприимчивость к аскаридозу высокая. В высокоэпидемичных местностях до 90% детей больны аскаридозом. Это объясняется тем, что аскаридоз не оставляет выраженного иммунитета.
Патогенез. Патогенез аскаридоза различен в период миграции личи- нок в крови и пребывания их в органах дыхания и в период паразитирования взрослых гельминтов в тонком кишечнике человека.
В ранней
(миграционной) стадии аскаридоза личинки аскарид выделяют фермент
гиалуронидазу, лизируют стенки сосудов, проникают в кровеносное русло и
с током крови мигрируют по органам и тканям. В начале миграции личинки
очень малы. Они имеют размеры не более
эозинофильных инфильтратов, воспалительных очагов и эозинофилии. Позднее в очагах кровоизлияний образуются очаги воспалений, характерные для бронхопневмонии и острого воспалительного гепатита.
При миграции продукты обмена и распада личинок оказывают сенсибилизирующее действие на организм, что приводит в дальнейшем к развитию аллергических реакций. Могут возникнуть аллергический миокардит, аллергический гепатит, а также изменения в почках, надпочечниках, кишечнике, селезенке.
Тяжелым осложнением аскаридоза является анафилактический шок, приводящий к гибели больного. Признаком анафилаксии может быть увеличение количества тучных клеток на путях миграции личинок (в кишечнике, печени, легких), их дегрануляция, вакуолизация и др.
Во время паразитирования взрослых аскарид в кишечнике сенсибилизация организма продолжается. В патогенезе кишечной фазы основную роль играет интоксикация организма токсическими продуктами жизнедеятельности аскарид, в результате чего возникают нарушения со стороны пищеварительной, нервной, половой и других систем. Гельминты оказывают механическое воздействие на слизистую оболочку кишечника, приводящее к ее изменению: нарушается пристеночное пищеварение, затрудняется всасывание и усвоение белков, жиров, витаминов, уменьшается активность фермента лактазы и др.
Клиническая картина. Миграционная фаза связана с аллергической перестройкой организма. Она может протекать бессимптомно или сопровождаться различными кожными высыпаниями, приступами бронхиальной астмы, эозинофилией, кашлем, насморком, бронхитом, бронхопневмонией. Симптомокомплекс Леффлера сопровождается субфебрильной или умеренно высокой температурой, кашлем, иног- да астматического характера. При миграции личинок аскарид в другие органы создаются условия для присоединения бактериальной инфекции и возникновения осложнений (абсцессы печени).
При миграционной стадии аскаридоза возникают тахикардия, снижение артериального давления. Иногда развиваются панкреатиты и холангиты.
Клиническая картина кишечной стадии аскаридоза разнообразна. Симптомы могут быть выражены слабо, либо, наоборот, заболевание протекает очень тяжело. У детей тяжелые случаи без противоаскаридозного лечения могут заканчиваться летальным исходом.
При кишечной стадии аскаридоза нарушаются функции кишечника, появляются боли в животе, тошнота, рвота, возникает энтероколит, сопровождающийся лихорадкой, появляется снижение веса (рис. 4.27).
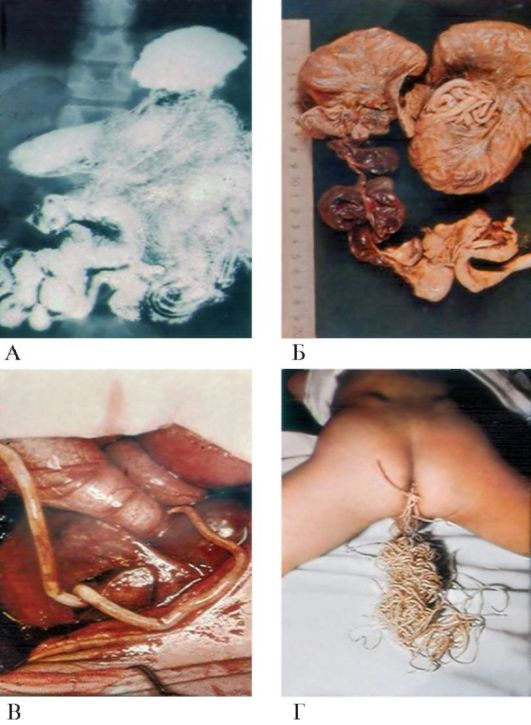
Рис. 4.27. А - рентгеновский снимок кишечника с аскаридами; Б - закупорка кишечника человека клубком аскарид; В - аскарида в печени; Г - аскаридоз у ребенка;
Дифференциальная диагностика. Клинически установить диагноз аскаридоза и дифференцировать его от других кишечных заболеваний сложно.
Лабораторная диагностика. В кишечной стадии диагноз устанавливают по нахождению яиц или аскарид в фекалиях. Учитывают сезон обследования. Максимальное выявление инвазированных лиц происходит в декабре-феврале. При паразитировании в кишечнике только самцов старых или неполовозрелых самок яйца могут отсутствовать.
Диагноз миграционной стадии аскаридоза установить очень сложно. Иногда личинки аскарид могут быть обнаружены при исследовании мокроты.
Осложнения. При интенсивных инвазиях может возникнуть непро- ходимость кишечника, аскаридозный перитонит, закупорка печеночных ходов, протоков поджелудочной железы. Иногда возникают энцефа-
лопатии, вызванные паразитированием аскарид. При проникновении аскарид в дыхательные пути может произойти обтурация и асфиксия. Аскаридоз, сопутствующий другим заболеваниям, утяжеляет их течение. Дизентерия при аскаридозе протекает тяжелее и более длительно. При детских инфекциях, туберкулезе, брюшном тифе часто возникают осложнения и возможен летальный исход.
У человека нет естественного иммунитета против аскаридоза. Приобретенный иммунитет возникает при многократных повторных заражениях. При повторном заражении под действием антител личинки теряют свою активность и гибнут во время миграции. В результате многократных инвазий все личинки могут погибнуть, и кишечная фаза не наступает.
Лечение. Для лечения аскаридоза используют:
- мебендазол (вермокс, антиокс) - взрослым и детям старше 2-х лет 100 мг два раза в сутки в течение 3-х дней (на курс 600 мг);
- албендазол (немозол) - взрослым и детям старше 2-х лет 400 мг однократно;
- карбендацим (медамин) - взрослым и детям из расчета 10 мг/кг/сут в три приема в течение 3-х дней.
Эти препараты противопоказаны во время беременности и кормления грудью.
При необходимости через 2 недели после окончания лечения проводят контроль эффективности лечения. Для этого трижды исследуют кал с интервалом в 2 недели.
Профилактика. Личная профилактика: соблюдение правил личной гигиены, мытье рук, овощей, фруктов, ягод, употребление кипяченой питьевой воды, предохранение пищевых продуктов от мух, тараканов.
Общественная профилактика: выявление больных и массовая дегельминтизация населения, санитарно-просветительская работа, обезвреживание фекалий, используемых как удобрение путем компостирования, охрана окружающей среды от загрязнения (устройство канализации, водопровода).
4.3.1.2. Энтеробиоз
Энтеробиоз - кишечный геогельминтоз. Взрослая острица локализуется в нижнем отделе тонкой и начальном отделе толстой кишки.
Этиология. Возбудитель энтеробиоза - острица, Enterobius vermicularis, мелкие раздельнополые нематоды белого цвета. Длина самки - 9-12 мм, ширина -
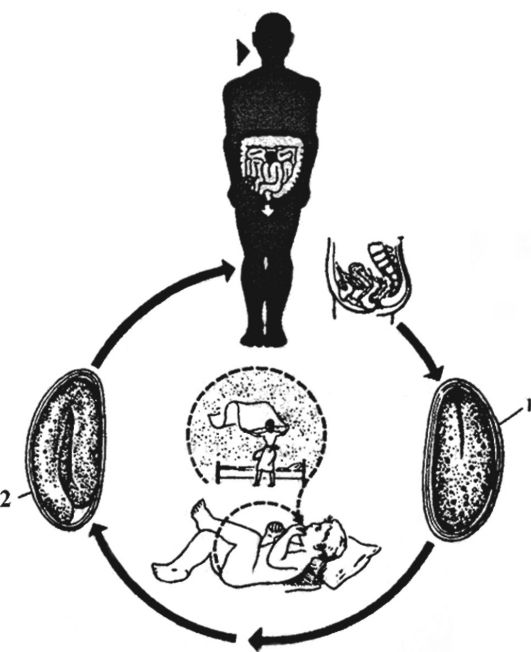
Рис. 4.28. Цикл развития острицы 1 - неинвазионное яйцо острицы; 2 - инвазионное яйцо острицы
конце тела имеется ротовое отверстие, окруженное тремя губами, и везикула (вздутие кутикулы), помогающая гельминту прикрепляться к стенкам кишечника. Задний отдел пищевода имеет шаровидное расширение - бульбус. Кишечник в виде прямой трубки. Матка самки, набитая яйцами, занимает почти все тело червя.
Цикл развития (рис. 4.28). Человек заражается энтеробиозом, про- глатывая инвазионные яйца острицы. Цикл развития происходит без миграции. Из яиц в тонкой кишке выходят личинки, которые с помощью везикулы, плотно прилегающей к тканям хозяина, и благодаря присасывающему действию бульбуса пищевода прикрепляются к слизистой оболочке. Через 12-15 дней личинки становятся половозрелыми. Оплодотворение происходит в кишечнике человека. Сразу после оплодотворения самцы погибают. В матке самки накапливается до
20 тыс. яиц. Сильно растянутая матка сдавливает бульбус, в связи с чем самки не могут удерживаться на слизистой и под действием перистальтики спускаются в нижние отделы кишечника. Во время сна, когда сфинктер расслаблен, самки активно перемещаются вдоль прямой кишки и выползают из анального отверстия. Они откладывают яйца на перианальных складках и после этого погибают. Острицы могут заползать во влагалище, на бедра, нижнюю часть спины. Через 4-6 часов при температуре 36 ?С, влажности 90-100% и наличии кислорода личинки становятся инвазионными. Яйца, попавшие в условия с более низкой температурой, не развиваются. Продолжительность жизни острицы составляет около 30 дней.
Яйца размером 50-60 χ 20-30 мкм покрыты прозрачной оболочкой, ассиметричной формы: одна сторона овала уплощена, другая выпуклая. Внутри находится почти сформированная личинка (рис. 4.29).
Эпидемиология. Энтеробиоз - наиболее широко распространенный гельминтоз. Он встречается повсеместно, но чаще всего в развитых странах умеренного климата. Развитие остриц не зависит от климатических условий. Этим гельминтозом может страдать население как в странах с засушливым, так и с суровым, холодным климатом. В мире энтеробиозом поражено более 350 млн человек. Распространение энтеробиоза связано с интенсивным и экстенсивным загрязнением внешней среды яйцами остриц. Болеют преимущественно дети.
Источником инвазии может быть только человек, больной энтеробиозом.
Самка острицы откладывает около 1500 яиц. При оптимальных условиях период дозревания яиц равен 4-6 часам. Основная особенность энтеробиоза - его контагиозность, обусловленная быстрым созрева- нием яиц, их устойчивостью к действию факторов внешней среды. Интенсивность пораженности людей зависит от уровня санитарной культуры населения.
Механизм передачи заболевания - фекально-оральный. Возможен также контактно-бытовой способ передачи. Заражение человека происходит при проглатывании инвазионных яиц, содержащих подвижные личинки. Яйца могут находиться на различных участках тела, под ногтями, на постельном белье, осаждаться с пылью на предметы обихода и продукты питания, передаваться через рукопожатие.
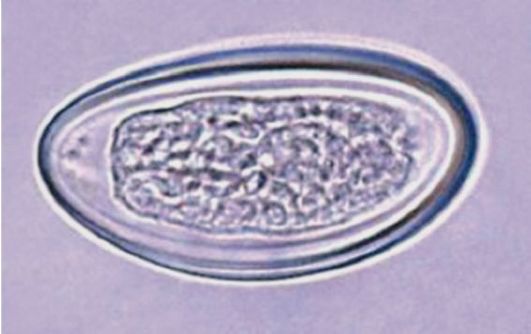
Рис. 4.29. Яйцо острицы
Восприимчивость к энтеробиозу высокая, особенно в детских коллективах. Возможны повторные заражения (аутореинвазии), затрудняющие излечение больных.
Патогенез. Патогенное влияние остриц на организм человека зависит от интенсивности инвазии. Заболевание может протекать бессимптомно или субклинически. Патогенное влияние связано с механическим, токсическим, аллергическим и психогенным действиями гельминтов на организм.
Клиническая картина. К наиболее ранним симптомам заболевания можно отнести зуд в перианальной области, возникающий вечером и ночью. При интенсивной инвазии возникает бессонница, приводящая к нервному истощению больного.
При интенсивной инвазии наблюдается кишечная форма энтеробиоза. Появляются боли в животе, тошнота, диарея, головная боль, головокружение. Острицы могут способствовать развитию аппендицита. Часто возникает дисбактериоз.
Дифференциальная диагностика. Перианальный зуд, основной симптом при энтеробиозе, нужно дифференцировать от зуда при других заболеваниях (геморрой, рак прямой кишки, нейродерматоз, сахарный диабет и др.).
Лабораторная диагностика. Деревянным шпателем или ватным тампоном проводят соскоб с перианальных складок кожи утром до дефекации для обнаружения яиц. Исследование повторяют 3 раза с интервалом в 7-10 дней. Иногда взрослые гельминты могут быть обнаружены на поверхности кала.
Осложнения. Постоянное раздражение кожи вокруг анального отвер- стия приводит к образованию трещин и расчесов, через которые проникает микробная инфекция, что приводит к развитию абсцессов, дерматитов, экзем.
При заползании паразитов в женские половые органы возникают вульвовагиниты. Острицы способствуют проникновению бактериаль- ной инфекции в половые органы.
Лечение. Для лечения энтеробиоза используют следующие препараты:
- пирантел - взрослым и детям с 2-х лет по 10 мг/кг однократно;
- албендазол (немозол) - взрослым и детям старше 2-х лет 400 мг однократно;
- мебендазол (вермокс, антиокс) - взрослым и детям старше 2-х лет 100 мг однократно;
- карбендацим (медамин) - взрослым и детям из расчета 10 мг/кг/сут в три приема в течение одного дня.
Контроль эффективности лечения проводят при затяжном и рецидивирующем течении энтеробиоза. Диагностику проводят обычными методами через 15 дней после окончания лечения.
Профилактика. Личная профилактика: соблюдение правил личной гигиены, особенно чистоты рук; больного ребенка следует укладывать спать в трусах, утром их кипятить и гладить мокрыми. Общественная профилактика: выявление и лечение больных; предупреждение загрязнения яйцами гельминтов помещений детских учреждений, организаций, плавательных бассейнов; проведение санитарно-гигиенических дезинвазивных мероприятий; обучение медицинского и обслуживающего персонала детских коллективов методам профилактики.
4.3.1.3. Трихоцефалез
Трихоцефалез - кишечный геогельминтоз, антропоноз. Взрослый власоглав паразитирует в толстой кишке человека.
Этиология. Возбудитель трихоцефалеза - власоглав (Trichocephalus trichiurus). Власоглавы - мелкие раздельнополые нематоды серого цвета. Длина тела самки составляет 30-55 мм, самца - 30-45 мм. Передний отдел тела власоглава тонкий, волосовидный и составляет 2/3 всей длины. В нем располагается пищевод. Задний отдел утолщен. В нем находятся все основные отделы пищеварительного тракта, у самки видна матка. Задний конец самца завернут в виде спирали.
Яйца власоглава размером 50-54 x 23-26 мкм, имеют форму бочонка или лимона со светлыми пробочками на полюсах. Оболочка яиц гладкая, желтовато-коричневая (рис. 4.30).
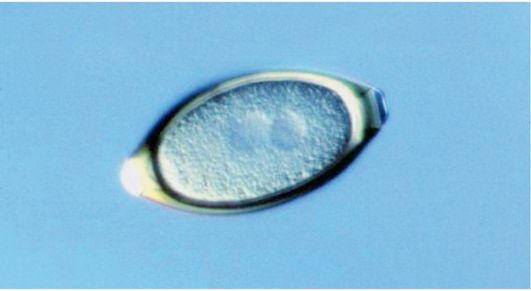
Рис. 4.30. Яйцо власоглава
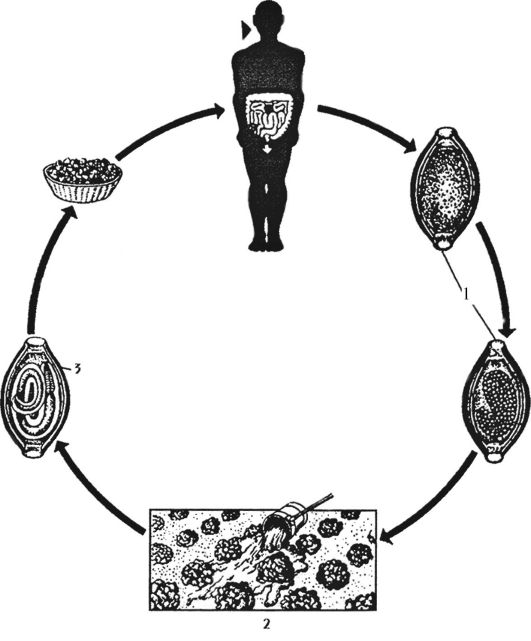
Рис. 4.31. Цикл развития власоглава 1 - яйца власоглава, выделившиеся из кишечника; 2 - почва, в которой происходит вызревание личинок власоглава; 3 - инвазионная личинка власоглава
Цикл развития (рис. 4.31). Человек заражается трихоцефалезом, проглатывая инвазионные яйца власоглава. Цикл развития проходит без миграции. Из инвазионных яиц выходят личинки, которые перемещаются в слепую кишку, где узким передним концом внедряются в слизистую оболочку и остаются там до конца своей жизни. Личинки развиваются около 2-х недель. В течение месяца гельминты достигают
половой зрелости. Они питаются клетками эпителия кишечника и кровью хозяина. Через 6 недель после заражения начинается выделение яиц с фекалиями. Самка в сутки откладывает 1000-3500 яиц. При интенсивной инвазии паразит может обитать в подвздошной и прямой кишках. Продолжительность жизни власоглава составляет 5-6 лет.
Эпидемиология. Трихоцефалез - один из наиболее распространенных гельминтозов. Чаще всего встречается в странах с теплым и влажным климатом. В мире около 800 млн человек поражено трихоцефалезом. В России эта инвазия занимает второе место после аскаридоза.
Источник заражения - больной человек, выделяющий во внешнюю среду яйца с фекалиями.
Яйца власоглава созревают во внешней среде при температуре 15-40 ?С, наличии свободного доступа кислорода, влажности около 100% в течение 17-25 дней. Оптимальная температура для созревания яиц - 26-30 ?С. Яйца власоглава хуже переносят низкие температуры, чем яйца аскариды, но более устойчивы к действию солнечной радиации. В почве яйца сохраняют инвазионность в течение 2-х лет.
Факторы передачи возбудителя трихоцефалеза, механизмы заражения те же, что и при аскаридозе.
Очаги трихоцефалеза различают по степени их экстенсивности, определяемой уровнем пораженности населения. Иногда интенсивные очаги трихоцефалеза формируются в психиатрических больницах.
Патогенез. Слабая инвазия власоглавами не вызывает тяжелых поражений и протекает субклинически. В случаях интенсивной инвазии наблюдаются воспалительная реакция, гиперемия, набухание слизистой кишечника, кровоизлияния, эрозии, эозинофильная и лимфоидная инфильтрации. Эозинофильная воспалительная реакция слизистой кишечника развивается на 7 сутки после заражения как следствие сенсибилизации антигенами паразита. В дальнейшем эти явления стихают. Власоглавы - гематофаги, при интенсивной инвазии развивается анемия.
Клиническая картина трихоцефалеза зависит от интенсивности инвазии. При низкой интенсивности клинические проявления могут отсутствовать. При интенсивной инвазии возникают боли в животе, диарея, повышенная утомляемость, снижение аппетита, анемия, утолщение фаланг пальцев, задержка роста у детей, снижение массы тела, головная боль (рис. 4.32).
Дифференциальная диагностика. Дифференциальную диагностику проводят с другими кишечными гельминтозами.
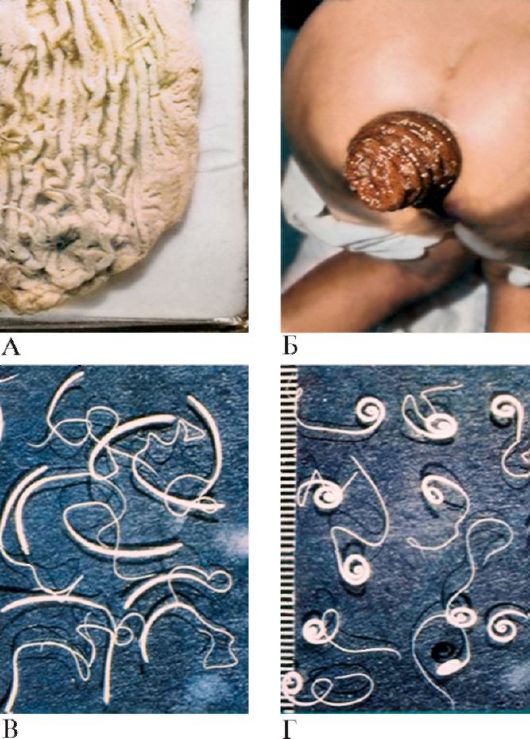
Рис. 4.32. А - власоглавы в слизистой слепой кишки; Б - выпадение прямой кишки при интенсивной инвазии власоглавом; В - самки власоглава; Г - самцы власоглава
Лабораторная диагностика. Диагноз трихоцефалеза ставят при обнаружении яиц в фекалиях методами обогащения. Сезон обследования не имеет значения, так как инвазия продолжается 5 лет при однократном заражении. Взрослые гельминты могут быть обнаружены при колоноскопии.
Осложнения. Проникновение власоглава в аппендикс может быть причиной аппендицита. Могут развиться кахексия, анемия, дисбактериоз, выпадение прямой кишки. При трихоцефалезе тяжело протекают протозойные и бактериальные инфекции.
Лечение. Для лечения трихоцефалеза используют следующие препа- раты:
- албендазол (немозол) - взрослым и детям старше 2-х лет 400 мг однократно;
- мебендазол (вермокс, антиокс) - взрослым и детям старше 2-х лет 100 мг два раза в сутки в течение 3-х дней (на курс 600 мг);
- карбендацим (медамин) - взрослым и детям из расчета 10 мг/кг/сут в три приема в течение 3-х дней.
Все препараты противопоказаны во время беременности и кормления грудью. Для контроля эффективности лечения проводят 3 исследования кала с интервалом в 2 недели через 3-4 недели после проведения терапии.
Профилактика. Меры профилактики трихоцефалеза сходны с мерами, проводимыми при аскаридозе. Необходимо соблюдать правила личной гигиены, мыть овощи и фрукты перед употреблением их в пищу, выявлять и лечить больных, охранять окружающую среду от фекального загрязнения.
4.3.1.4. Анкилостомидозы: анкилостомоз, некатороз
Анкилостомидозы - геогельминтозы. Взрослые гельминты паразитируют в двенадцатиперстной и тощей кишках человека.
Этиология. Анкилостомидозы объединяют два гельминтоза: анки- лостомоз, вызываемый кривоголовкой двенадцатиперстной кишки - Ancylostoma duodenale, и некатороз, вызываемый некатором - Necator americanus.
Эти гельминты сходны по морфологии, циклам развития и действию на организм. Тело нематод розовато-желтоватого цвета, небольших размеров. Самка кривоголовки двенадцатиперстной кишки имеет длину 10-13 мм, а самец - 8-10 мм. Длина самки некатора составляет 9-10 мм, а самца - 5-8 мм. Передний конец тела анкилостомы загнут на вентральную сторону, а у некатора - на дорзальную. Головной конец имеет ротовую капсулу, с помощью нее гельминты прикрепляются к стенке тонкого кишечника. У анкилостомы капсула имеет четыре вентральных и два дорсальных режущих зубца, а у некатора - две режущих пластинки.
Самцы на хвостовом конце имеют колоколовидное расширение кутикулы (половую бурсу). У анкилостомы она крупнее и шире, чем у некатора.
Яйца анкилостом и некатора по строению неразличимы. Они овальной формы, покрыты гладкой, тонкой, бесцветной оболочкой, имеют размеры 66 x 38 мкм. В свежевыделенных яйцах видны 4-8 бластомеров
(рис. 4.33).
Цикл развития (рис. 4.34). Человек заражается анкилостомозом и некаторозом при проникновении инвазионных (филяриевидных) личинок через кожу, например при ходьбе босиком. Заражение анкилостомозом может происходить при проглатывании личинок анкилостом, находящихся в воде или на овощах и фруктах.
При проникновении личинок через кожу дальнейшее их развитие происходит с миграцией. Личинки по венозной системе мигрируют в
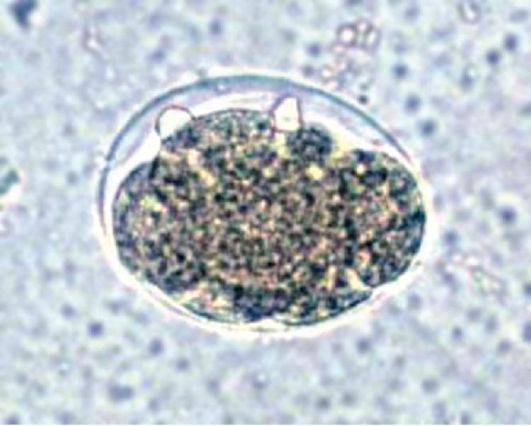
Рис. 4.33. Яйцо анкилостомы
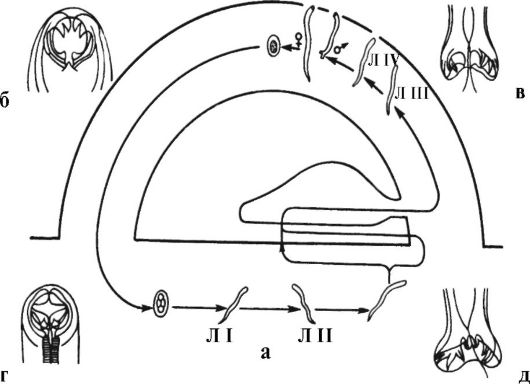
Рис. 4.34. Цикл развития анкилостомид а - цикл развития некатора; б - головной конец тела анкилостомы; в - хвостовой конец тела самца анкилостомы; г - головной конец тела некатора; д - хвостовой конец тела некатора; Л -I, II, III, IV - личинки первой, второй, третьей и четвертой стадий развития
правый желудочек сердца, затем в легкие, выходят в полость альвеол, продвигаются в глотку, ротовую полость и вторично заглатываются. Личинки проходят по пищеводу в желудок и затем оказываются в тонком кишечнике. Через 5-6 недель после внедрения личинок в кожу, миграции и двух линек они становятся половозрелыми гельминтами. После этого срока в фекалиях можно обнаружить яйца.
В северных районах распространения анкилостомидозов с выраженной сменой времен года имеются штаммы анкилостом, личинки которых могут не развиваться в течение 8 месяцев. Затем они продолжают и заканчивают свое развитие. Благодаря этому яйца выходят во внешнюю среду во время, наиболее благоприятное для их развития.
При проникновении личинок анкилостом через рот, миграции не происходит. Личинки сразу же оказываются в кишечнике.
Продолжительность жизни анкилостом - 7-8 лет, а некатора - до 15 лет.
Эпидемиология. Около 25% населения земного шара заражено анки- лостомидозами. Наиболее часто это заболевание встречается в районах с низким уровнем санитарии. Анкилостомидозы - заболевания, распространенные на всех континентах в пределах 45? с. ш. и 30? ю. ш. Около 900 млн человек в мире поражено анкилостомидозами, и ежегодно регистрируется около 450 млн новых случаев заболевания. Чаще всего эти заболевания встречаются в тропических и субтропических странах. Очаги анкилостомидозов имеются в Южной и Центральной Америке, Африке, Индостане, Индокитае и на островах Малайского архипелага. Анкилостомозы встречаются на Кавказе, в Туркмении, Кыргызстане. Некаторозы регистрируются на Черноморском побережье Краснодарского края, на границе с Абхазией. Известны смешанные очаги некаторозов и анкилостомозов в Западной Грузии и Азербайджане.
Источник заражения - инвазированный человек, выделяющий яйца во внешнюю среду.
Самка анкилостомы в сутки выделяет 10-25 тыс. яиц, а некатора - 5-10 тыс. С фекалиями яйца попадают в почву. Развитие личинок происходит при температуре от 14 до 40 ?С. Для развития личинок анкилостом нужна влажность 85-100%, а для некатора - 70-80%. Личинкам требуется доступ свободного кислорода, при 0 ?С они способны сохранять жизнеспособность не более недели. При благоприятных условиях через 1-2 суток в яйцах развиваются рабдитовидные личинки. Они имеют два бульбуса в пищеводе. Эти личинки неинвазионны. Через 7-10 дней после линьки личинки становятся филяриевидными. Они имеют пищевод цилиндрической формы. После второй линьки филяриевидные личинки становятся инвазионными. Личинки могут свободно передвигаться в почве по вертикали и горизонтали.
Основной фактор передачи возбудителя - почва, загрязненная яйцами и личинками гельминтов. Заражение человека происходит чаще всего вследствие проникновения филяриевидных личинок через кожу (перкутанно) при ходьбе босиком. Возможны также трансплацентарный
и трансмаммарный способы заражения. Иногда заражение происходит перорально при употреблении мяса кроликов, ягнят, телят, свиней, а также овощей, фруктов и воды, загрязненных инвазионными личинками гельминтов.
Эпидемические очаги анкилостомозов формируются во влажных тропиках, а некатороза - в странах с субтропическим климатом влажного типа. Интенсивные очаги анкилостомидозов могут формироваться в шахтах, где в условиях повышенной влажности и высоких температур личинки способны быстро развиваться.
Патогенез. Патогенез анкилостомидозов различен в ранней и хро- нической стадиях. На ранней стадии личинки совершают миграцию по органам и тканям хозяина, вызывают аллергические реакции, оказывают сенсибилизирующее действие на организм. По пути миграции личинок, как и при аскаридозе, травмируются ткани дыхательных путей, формируются эозинофильные инфильтраты, возникают кровоизлияния. Длительность ранней стадии составляет 1-2 недели. Кишечная (хроническая) стадия начинается после завершения миграции и проникновения личинок в двенадцатиперстную кишку. С помощью кутикулярных зубов личинки прикрепляются к слизистой оболочке, травмируют сосуды, выделяют антикоагулянты и вызывают сильное кровотечение. Анкилостомы являются гематофагами: за сутки одна особь анкилостомы потребляет 0,16-0,34 мл крови, а некатора - 0,03-0,05 мл. В местах прикрепления анкилостомид образуются изъязвления. Интенсивная инвазия гельминтами способствует развитию гипохромной анемии.
Клиническая картина. Различают три клинические фазы анкилостомидозов.
Первая фаза связана с проникновением личинок через кожу. Эта фаза сопровождается развитием дерматита (папуло-везикулярная сыпь). В коже отмечается нейтрофильная инфильтрация соединительной ткани с наличием лимфоидных и эпителиоидных клеток и фибробластов. Сыпь исчезает через 10-12 дней. При повторных заражениях развиваются крапивница, локальный отек.
Во второй (миграционной) фазе заболевания иногда появляются кашель, охриплость голоса, одышка, повышение температуры. В мокроте и крови увеличивается число эозинофилов, возникают очаговые пневмонии, бронхиты, трахеиты, ларингиты.
Третья, кишечная фаза - длительная, хроническая. Первые симптомы нарушений функций желудочно-кишечного тракта появляются через 30-60 дней после заражения. Выраженность симптомов зависит от числа паразитов. Легкая форма протекает почти бессимптомно.
Возможны неприятные ощущения в эпигастральной области. К концу 12-го месяца развиваются дуодениты с тошнотой, нарушением аппетита и болями в животе.
Тяжелая форма приводит к значительной кровопотере и сопровождается хронической железодефицитной анемией, отдышкой, вялостью, задержкой развития, отеками, диареей с примесью крови и слизи в фекалиях, потерей альбуминов, приводящей к повреждению миокарда и нарушению сердечной деятельности.
У больных черной расы возникает депигментация кожи, связанная с дефицитом железа и гипоальбуминемией.
При инвазии анкилостомами инвазия развивается быстрее и достигает более высокой степени, чем при инвазии некатором.
Осложнения. Декомпенсированная анемия.
Дифференциальная диагностика. Дифференциальная диагностика проводится с другими кишечными гельминтозами, при развитии анемии - с анемиями другой этиологии.
Лабораторная диагностика. Диагноз анкилостомидозов ставят при обнаружении яиц в фекалиях или дуоденальном содержимом. При исследовании фекалий пользуются флотационными методами (по Фюллеборну - через 15-20 мин, по Калантарян - через 10-15 мин). Диагностика видов проводится специальным методом Харада и Мори - культивированием личинок в пробирке на фильтровальной бумаге. При диагностике учитывают эпидемиологические и клинические данные.
Лечение. Для лечения используют следующие препараты:
- албендазол (немозол) - взрослым и детям старше 2-х лет 400 мг однократно;
- мебендазол (вермокс, антиокс) - взрослым и детям старше 2-х лет 100 мг два раза в сутки в течение 3-х дней (на курс 600 мг);
- карбендацим (медамин) - взрослым и детям из расчета 10 мг/кг/сут в три приема в течение 3-х дней;
- пирантел (гельминтокс) - 10 мг/кг (максимально 750 мг для взрослых и детей старше 12 лет) в сутки однократно 3 дня подряд.
При развитии анемии назначают препараты железа и фолиевой кислоты. Для контроля эффективности лечения через месяц после дегельминтизации проводят 3 исследования фекалий с интервалом в 30 дней.
Профилактика. Профилактика анкилостомидозов предполагает выявление и лечение больных, санитарно-гигиенические мероприятия, направленные на охрану окружающей среды от фекального загрязнения, обезвреживание нечистот, ношение обуви в очагах заболеваний, соблюдение правил личной гигиены, мытье овощей и фруктов перед едой.
4.3.1.5. Трихостронгилоидоз
Трихостронгилоидоз - зооноз-геогельминтоз. Человек является факультативным хозяином. Взрослые гельминты локализуются в тонком кишечнике человека.
Этиология. У человека паразитирует в основном Trichostrongylus colubriformis. Трихостронгилиды - мелкие нематоды размером 4-8 x 0,78-1 мм. Ротовое отверстие ограничено тремя губами. У самцов на заднем конце имеется бурса, две буроватые спикулы неравной величины и рулек, направляющий их движение.
Яйца гельминтов овальные, размер 74-80 x 40-43 мкм, покрыты тонкой прозрачной оболочкой, с одним слегка заостренным, а другим - тупым концом.
Цикл развития. Трихостронгилиды паразитируют, как правило, в организме облигатных хозяев - мелкого и крупного рогатого скота и других травоядных млекопитающих. Иногда заражается человек, который является факультативным хозяином для этого гельминта. Человек заражается трихостронгилоидозом при употреблении в пищу растений, загрязненных инвазионными личинками. Развитие происходит без миграции. В кишечнике человека личинки внедряются в слизистую оболочку двенадцатиперстной кишки, развиваются, дважды линяют и превращаются в половозрелых гельминтов. Через 20-30 дней в фекалиях больного можно обнаружить яйца. Продолжительность жизни гельминтов составляет более 8 лет.
Эпидемиология. Роль человека как источника инвазии невелика. Личинки в организм человека попадают довольно редко и в небольшом количестве.
Трихостронгилоидоз встречается в странах с теплым и влажным климатом в Юго-Восточной Азии, Северной Африке, на Ближнем Востоке, в Южной, Центральной и Северной Америке, в Армении, Азербайджане, Узбекистане, в Поволжье, на Дальнем Востоке. Из многочисленных имеющихся видов трихостронгилид у человека была обнаружена инвазия 13 видов. Чаще болеют жители сельской местности с хорошо развитым животноводством. Источник заражения - травоядные животные, крупный и мелкий рогатый скот, загрязняющие яйцами гельминтов пастбища, скотные дворы, стойла. Во внешней среде в яйцах при благоприятных условиях (достаточной влажности, наличии кислорода и оптимальной температуре 30-32 ?С) развиваются личинки. Через 1-3 дня они выходят из яйцевых оболочек, дважды линяют и в течение 4-14 суток превращаются в инвазионных, филяриевидных личинок. В окружающей среде личинки могут выжить в течение 3-4 месяцев. Они могут
осуществлять вертикальную и горизонтальную миграции и сохранять жизнеспособность в почве в течение года. Факторы передачи возбудителя - овощи, фрукты, травы, загрязненные личинками гельминтов во время сельскохозяйственных работ.
Заражение трихостронгилоидозом происходит при употреблении в пищу фруктов, овощей, щавеля и других трав, загрязненных личинками нематод. Человек не играет большой роли в распространении данного заболевания.
Патогенез. Гельминты, проникая в слизистую оболочку двенадцати- перстной и тощей кишок, травмируют ее. Возникают симптомы, обусловленные токсико-сенсибилизирующим действием нематод, а также могут развиваться воспалительные процессы.
Клиническая картина. Интенсивность инвазии у человека, как правило, низкая. Течение бессимптомное или имеет субклиническую форму. При интенсивном заражении преобладают симптомы поражения желудочно-кишечного тракта. Больные отмечают отсутствие аппетита, тошноту, отрыжку, боли в животе, диарею, раздражительность, слабость, похудание. Иногда развиваются гипохромная анемия, лейкоцитоз, эозинофилия.
Дифференциальная диагностика. Дифференциальный диагноз проводят с анкилостомидозами.
Лабораторная диагностика. Диагноз ставят при обнаружении яиц в фекалиях. Применяют метод обогащения, так как интенсивность инвазии низкая. Используют также культивирование личинок на фильтровальной бумаге по методу Харада и Мори. Иногда яйца гельминтов обнаруживают в дуоденальном содержимом.
Осложнения. Сильно выраженная анемия, кахексия.
Лечение. Лечение проводят нематоцидами широкого спектра дейс- твия (албендазол, мебендазол, медамин, пирантел и др.) по тем же схемам, как при аскаридозе.
Профилактика. Профилактика сходна с профилактикой других гео- гельминтозов (аскаридоз, анкилостомидозы и др.).
4.3.1.6. Стронгилоидоз
Стронгилоидоз - геогельминтоз. Взрослые возбудители локализуются в слизистой оболочке тонкого кишечника.
Этиология. Возбудитель стронгилоидоза - угрица кишечная, Strongyloides stercoralis. Взрослые гельминты мелкие, нитевидные. Самки имеют длину
Цилиндрический пищевод занимает 1/4 тела. Яичники двойные, занимают 3/4 длины тела, переходят в парные матки, открывающиеся в непарное влагалище, находящееся на границе передней и средней части тела. В матке располагается цепочка яиц.
Самцы имеют длину
Яйца гельминтов эллипсоидной формы, размером 50 x 30 мкм.
Цикл развития (рис. 4.35). Заражение человека происходит при кон- такте с загрязненной инвазионными личинками почвой и проникновении через кожу или попадании их через рот вместе с пищей и водой.
При проникновении инвазионных (филяриевидных) личинок через кожу дальнейшее их развитие происходит с миграцией, как у личинок аскарид и анкилостомид. Личинки по кровеносным сосудам мигрируют по органам и тканям хозяина и по окончании миграции оказываются в верхних отделах тонкого кишечника, где достигают половой зрелости.
Через 17-28 дней после заражения в фекалиях можно обнаружить личинки гельминтов. Выход личинок из яиц происходит в кишечни- ке. При попадании личинок через рот они проникают через слизистую оболочку ротовой полости в кровеносные сосуды и развиваются также с миграцией, как личинки, проникшие через кожу. Иногда личинки становятся инвазионными до того, как выделятся во внешнюю среду. Это происходит в тех случаях, когда рабдитовидные личинки, вышедшие из яиц, задерживаются в кишечнике больного свыше 24 часов (при запорах). Личинки превращаются в филяриевидные без выхода во внешнюю среду, проникают через слизистую оболочку кишечника в глубь тканей, и, проделав миграцию, попадают в кишечник, вызывая аутосуперинвазию. Самки внедряются в слизистую оболочку тонкого кишечника, самцы находятся в просвете кишечника. Оплодотворение может происходить в легких и кишечнике. Продолжительность жизни гельминтов в кишечнике - несколько месяцев, но аутоинвазия приводит к длительному паразитированию гельминтов у людей (до 30 лет).
Эпидемиология. Стронгилоидоз широко распространен в странах с жарким и влажным климатом. По данным ВОЗ, 35-40 млн человек в мире инвазировано стронгилоидозом. Заболевание встречается в странах Африки (Эфиопия, Мозамбик), Южной Америки (Колумбия, Перу), где зараженность населения достигает 60%. В южных штатах США, в странах Юго-Восточной Азии, Северо-Восточной Австралии зараженность составляет 18%, а в странах Южной и Восточной Африки - от 2,5 до 30%. В районах с умеренным климатом, где низкий уровень санитарной культуры, имеются эндемичные очаги стронгилоидоза, в частности в южных
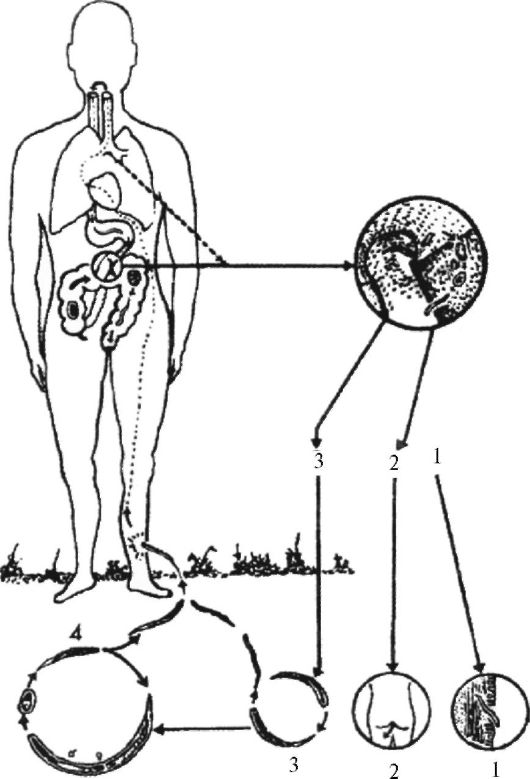
Рис. 4.35. Цикл развития стронгилоидов
1 - рабдитовидные личинки в кишечнике; 2 - рабдитовидные личинки на коже; 3 - превращение рабдитовидных личинок в филяриевидных в почве; 4 - свободноживущее поколение самцов и самок в почве
районах России, западных областях Украины, в Белоруссии, Молдове, на Кавказе и в Средней Азии. Небольшие очаги выявляются в Бельгии, Голландии, Франции, Италии (зараженность населения не превышает доли процента). Сезонность заболевания в странах с умеренным климатом определяется периодом года, когда суточная температура превышает 12?С, и сохраняется достаточная влажность. В осенне-зимний период личинки погибают. В некоторых районах Закавказья, Средней Азии и Казахстана гибель личинок в летнее время обусловлена недостаточной влажностью почвы.
Источник
инвазии - зараженный человек, выделяющий личинки во внешнюю среду.
Редко источником инвазии могут быть собаки, кошки. В их организме могут
развиваться стронгилоиды. Самка угрицы кишечной выделяет в сутки до 50
яиц с уже сформировавшимися рабдитовидными личинками. Личинки выходят
из яиц в кишечнике человека. Вместе с фекалиями рабдитовидные личинки
попадают в почву. Стронгилоиды имеют две формы существования:
паразитическую и свободноживущую. При благоприятных для их развития
условиях (высокой влажности и температуре 26-28 ?С) личинки линяют и
дают начало свободноживущему поколению самцов и самок, обитающих в почве
и способных питаться органическими остатками. Самки стронгилоидов,
живущих в почве, мельче паразитических форм (их длина
Фактор передачи возбудителя - почва, загрязненная личинками, где при оптимальных условиях они остаются живыми в течение 3-4 недель. Заражение человека происходит преимущественно перкутанно, но возможно и перорально, при употреблении немытых овощей, фруктов и ягод, на которых инвазионные личинки выживают в течение 4-5 дней. Возможен контактный путь передачи инвазии, поэтому стронгилоидоз можно отнести к факультативным контагиозным гельминтозам. Так как личинки могут находиться в перианальной области, то чаще таким путем заражаются гомосексуалисты при половых контактах и лица с психическими расстройствами.
Эндемичные очаги находятся в тропиках, субтропиках и странах с умеренным климатом, иногда возникают в горнорудных и каменноугольных шахтах с теплым и влажным микроклиматом.
В группу риска входят пациенты с заболеваниями органов пищеварения, больные туберкулезом, пациенты специализированных интернатов, среди которых возможны «внутрибольничные» вспышки стронгилоидоза.
Патогенез. Патогенез и клинические проявления при стронгилоидозе почти такие же, как при анкилостомидозах.
Клиническая картина. Клинические проявления определяются первичностью или повторностью заражения и наличием или отсутствием аутоинвазии. Слабые инвазии могут протекать бессимптомно. Различиют три варианта инвазий: кишечный, стронгилоидная гиперинвазия и диссеминированный стронгилоидоз. При кишечном стронгилоидозе умеренная инвазия проявляется признаками гастроэнтероколита. Заболевание длится несколько месяцев или лет. В фекалиях и дуоденальном содержимом обнаруживаются только рабдитовидные личинки. Стронгилоидная гиперинвазия характеризуется высокой численностью паразитов. При этом возрастает количество рабдитовидных личинок, превращающихся в филяриевидные во время нахождения их в кишечнике. Если это происходит в легких и желудочно-кишечном тракте, такое состояние обозначается как гиперинвазивный синдром. Диссеминированный стронгилоидоз - системная инвазия, при которой филяриевидные личинки проникают во многие органы и ткани. С этим синдромом часто сочетаются гиперинвазия и аутосуперинвазия, иногда присоединяются бактериальные инфекции. Клинические проявления связаны с кожными, легочными и кишечными симптомами.
В местах внедрения личинок появляется зуд, эритематозные и папулезные высыпания. Сыпь исчезает через 30-40 минут. При повторном заражении или аутоинвазии могут появиться мигрирующие эритематозные, линейные и извилистые папулы, прогрессирующие в «линейную крапивницу». Чаще всего они локализуются на ягодицах, бедрах, в перианальной области. Локальные аллергические дерматиты возникают на коже стоп и пальцев.
Миграция личинок у большинства пациентов проходит бессимптомно. При гиперинвазии возникают кашель с мокротой, бронхоспазм, в легких прослушиваются сухие и влажные хрипы, возникают очаги пневмонии. Характерным признаком ранней стадии стронгилоидоза являются эозинофилия до 30-60%, лейкоцитоз и повышение СОЭ.
Кишечные проявления характеризуются болями в животе, похуданием, тошнотой, рвотой, диареей со слизью и кровью. При длительном течении стронгилоидоза поносы чередуются с запорами, что способс- твует аутоинвазии. Развиваются тяжелая анемия и кахексия.
Гельминты локализуются в двенадцатиперстной кишке, в верхних отделах тощей кишки, иногда проникают в пилорический отдел желудка, слепую и ободочную кишки, желчные и панкреатические протоки.
При интенсивной инвазии слизистая оболочка изъязвляется, может развиться парез кишечника. Нарушения функции кишечника вызываются воспалительной реакцией слизистых оболочек вследствие сенсибили- зирующего влияния антигенов паразита и механического воздействия личинок и самок гельминта. В некоторых случаях отмечается астеноневротический синдром, проявляющийся общей слабостью, нарушением сна, повышенной возбудимостью.
Тяжесть заболевания зависит от состояния иммунной системы пациента. У ослабленных больных со сниженной реактивностью организма вследствие других заболеваний или иммунодефицита субклиническое или бессимптомное течение стронгилоидоза может перейти в гиперинтенсивную или диссеминированную формы.
В эндемичных районах стронгилоидоз является СПИД-ассоциированной инвазией.
Дифферециальная диагностика по клиническим симптомам затруднена вследствие их полиморфизма. В миграционной стадии стронгилоидоз дифференцируют с аскаридозом и анкилостомидозами. Хроническая стадия дифференцируется с язвенной болезнью желудка и двенадцатиперстной кишки.
Лабораторная диагностика. Диагноз ставят при обнаружении личинок в фекалиях при исследовании по методу Бермана и в дуоденальном содержимом. При диагностике учитывают эпидемические и клинические данные.
Осложнения. Язвенные поражения кишечника, перфоративный перитонит, некротический панкреатит, кишечные кровотечения, миокардит, менингоэнцефалит, кахексия и др.
Лечение. В миграционной стадии назначают антигистаминные средс- тва и препараты кальция. В кишечной стадии назначают:
- албендазол (немозолом) - по 400 мг в день за один прием на протяжении 3 суток (для детей 2-х лет и старше);
- карбендацим (медамин) назначают по 10 мг/кг/сут в три приема в течение 3-5 дней;
- ивермектин - назначают в дозе 0,2 мг/кг однократно.
При тяжелом течении инвазии у пациентов с иммунодефицитными состояниями по показаниям проводятся повторные курсы антигельминтной терапии со сменой препаратов.
Контроль эффективности проводят через месяц после лечения, путем проведения трехкратных исследований кала с интервалом в 1-2 дня.
Профилактика. Профилактика стронгилоидоза такая же, как и при анкилостомидозах. Необходимо охранять внешнюю среду от фекаль-
ного загрязнения, избегать контактов с загрязненной почвой, выявлять и лечить больных, соблюдать правила личной гигиены, мыть фрукты и овощи перед употреблением в пищу.
4.3.2. Филяриидозы
Филяриидозы - группа трансмиссивных гельминтозов, распространенных преимущественно в странах с тропическим и субтропическим климатом. Эндемичные очаги филяриидозов лимфатической системы имеются в 73 странах. По данным ВОЗ, этими гельминтозами заражено 120 млн человек, а 1100 млн проживают в зоне риска.
4.3.2.1. Вухерериоз
Вухерериоз - трансмиссивный филяриоз, биогельминтоз, антропоноз. Взрослые особи обитают в лимфатических сосудах, а личинки (микрофилярии) в крови.
Этиология. Возбудитель вухерериоза - Wuchereria bancrofti, имеет
нитевидное тело белого цвета, покрытое гладкой кутикулой, более тонкое
на головном и хвостовом концах. Длина самки составляет 80-100 мм,
ширина - 0,2-0,3 мм, а самцы -
Цикл развития (рис. 4.36). Заражение вухерериозом происходит при укусе человека комарами родов Culex, Anopheles, Aedes или Mansonia. Вухерерия - биогельминт, в цикле ее развития присутствуют окончательный и промежуточный хозяева. Окончательный (дефинитивный) хозяин - человек, промежуточные - комары родов Culex, Anopheles, Aedes или Mansonia.
В момент укуса человека комаром инвазионные личинки (микрофилярии), находящиеся в его ротовых органах, разрывают оболочку хоботка, попадают на кожу и активно внедряются в нее. С током крови они мигрируют в лимфатическую систему, где растут, линяют, а через 3-18 месяцев становятся половозрелыми самцами и самками. Самец и самка располагаются вместе, образуя общий клубок.
Вухерерии являются живородящими. Половозрелые гельминты локализуются в периферических лимфатических сосудах и узлах, где самки рождают живых личинок второй стадии (микрофилярий), покрытых чехликом. Личинки мигрируют из лимфатической системы в кровеносные сосуды. Днем они находятся в крупных кровеносных сосудах (сонная артерия, аорта) и сосудах внутренних органов. Ночью личинки мигрируют в периферические кровеносные сосуды, и поэтому их назы-
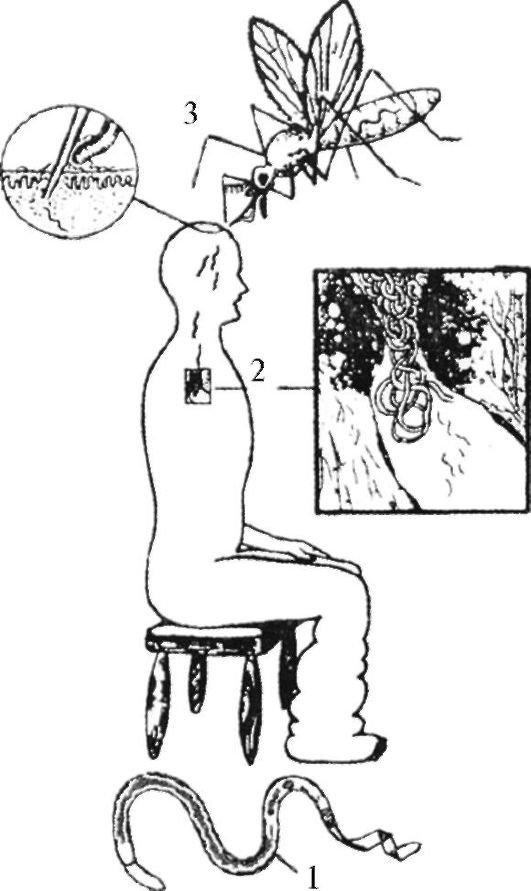
Рис. 4.36. Цикл развития вухерерии 1 - микрофилярия; 2 - взрослые вухерерии в лимфоузлах человека; 3 - комар
вают Microfilaria nocturna (микрофилярии ночные). Суточная миграция личинок связана с ночной активностью комаров (переносчиков возбудителя вухерериоза).
При укусе больного человека самками комаров микрофилярии попадают в пищеварительный тракт насекомого, сбрасывают чехлик, проникают через стенку желудка в полость тела и грудные мышцы. В мышцах личинки дважды линяют, становятся инвазионными личинками четвертой стадии и проникают в ротовой аппарат комара. Продолжительность цикла развития личинок в комаре зависит от температуры и влажности окружающей среды и колеблется от 8 до 35 дней. Оптимальными условиями для развития инвазионных личинок являются температура 29-30 ?С и влажность 70-100%. В теле комара личинки сохраняют жизнеспособ- ность в течение всей жизни.
Продолжительность жизни взрослых гельминтов в организме человека около 17 лет. Микрофилярии сохраняют жизнеспособность в кровеносном русле около 70 дней.
Эпидемиология. Эндемичные очаги вухерериоза встречаются в странах с тропическим и субтропическим климатом. Вухерериоз распространен в Западной и Центральной Африке, Юго-Восточной Азии (Индия, Малайзия, Китай, Япония и др.), Южной и Центральной Америке (Гватемала, Панама, Венесуэла, Бразилия и др.), на островах Тихого и Индийского океанов. В Западном полушарии ареал вухерериоза ограничен 30? с. ш. и 30? ю. ш., а в Восточном полушарии - 41? с. ш. и 28? ю. ш.
Вухерериоз - преимущественно болезнь городского населения. Рост крупных городов, скученность населения, отсутствие санитарного контроля, загрязненные водные резервуары, заброшенные системы водоснабжения и канализации благоприятствуют размножению комаров.
В развивающихся странах Азии и Африки, где осуществляется строительство городов и поселков, зараженность вухерериозом повышается.
Источником распространения заболевания являются зараженные люди. Переносчиком возбудителя в городских условиях чаще всего бывают комары рода Culex. В сельской местности в Африке, Южной Америке и некоторых странах Азии вухерериоз переносят преимущественно комары рода Anopheles, а на островах Тихого океана - рода Aedes. Заражение человека происходит вследствие проникновения инвазионных личинок при укусе комара.
Патогенез. В ранней стадии заболевания появляются признаки токси- ко-аллергических реакций: лихорадка, отеки, высыпания на коже, отмечается эозинофилия крови и т.п. Позднее (через 2-7 лет) развивается воспаление кожных и глубоких лимфатических сосудов. Лимфатические сосуды, в которых находятся взрослые паразиты, расширяются, утолщаются, стенки инфильтрируются лимфоцитами, эозинофилами. Вокруг гельминтов формируются гранулемы. Погибшие гельминты лизируются или кальцифицируются и окружаются фиброзной тканью. На месте гибели может развиться некроз с отеками и гноем. Развиваются грану- лематозный лимфангит и лимфаденит. Лимфатические узлы увеличиваются, становятся болезненными, развивается отек окружающих тканей. Чаще поражаются лимфатические узлы и лимфатические сосуды нижних конечностей и мочеполовых органов. При интенсивной инвазии происходит закупорка лимфатических сосудов, приводящая к нарушению оттока лимфы, в результате чего происходит отек органа (слоновость). Иногда болезнь осложняется присоединением вторичной инфекции.
Клиническая картина. Клинические проявления заболевания зависят от индивидуального иммунного ответа, обусловленного различными факторами - возрастом, степенью заражения и др. Течение данного заболевания полиморфно. Инкубационный период, длящийся от
3-х до 18 месяцев, протекает бессимптомно. У людей, проживающих в эндемичных районах и инфицированных микрофиляриями, симптомы заболевания могут отсутствовать. Это связано с тем, что у коренных жителей данных районов вследствие реинвазии выработался частичный иммунитет. Инкубационный период у местных жителей продолжается 12-18 месяцев. У приезжих неиммунных граждан при слабой инвазии признаком болезни может быть кожный зуд; инкубационный период у них более короткий и длится 3-4 месяца, что соответствует времени от проникновения инвазионных личинок в организм человека до начала рождения микрофилярий половозрелыми самками.
В клиническом течении болезни выделяют острую и хроническую формы.
Для острой формы заболевания характерны аллергические проявления, обусловленные повышенной чувствительностью организма к гельминту. На этой стадии развиваются лимфадениты, лимфангиты в сочетании с лихорадкой и недомоганием. Лимфатическая система поражается чаще у мужчин и проявляется фурункулитами, эпидидимитами, орхитами. Частота обострений аденолимфангита варьирует от 1-2 в год до нескольких в месяц. Во время обострений отмечается лимфатический отек, который постепенно исчезает. С течением времени исчезновение отека происходит неполностью и заболевание переходит в хроническую форму.
Хроническая
форма развивается через 10-15 лет с момента заражения. Она
сопровождается развитием стойких отеков и слоновости (элефантиаза),
возникающих вследствие прогрессирования лимфостаза, пролиферативных
процессов и фиброза в коже и подкожной клетчатке. Размеры пораженных
органов (мошонка, нижние конечности, молочные железы) сильно увеличены.
При элефантиазе мошонки ее масса может достигать 3-4 кг, иногда
При хроническом вухерериозе часто развивается водянка оболочек яичка (гидроцеле). В пунктате жидкости могут быть обнаружены микрофилярии.
Иногда наблюдается хилурия (наличие лимфы в моче), проявляющаяся молочно-белым цветом мочи, хилезная диарея (понос с примесью лимфы). Это приводит к гипопротеинемии из-за потери белков и к снижению веса у больных.
Среди жителей эндемичных очагов вухерериоза в Южной и ЮгоВосточной Азии распространен синдром «тропической легочной эози- нофилии», характеризующийся наличием полилимфаденита, гепатоспленомегалии, субфебрильной лихорадки, ночными приступами кашля,
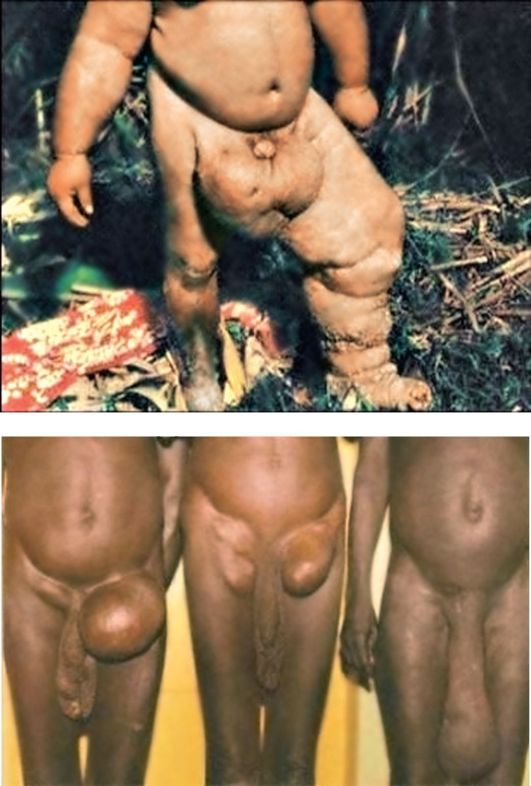
Рис. 4.37, 4.38. Вухерериоз (элефантиаз) - слоновость нижних конечностей
и мошонки
затруднением дыхания, обусловленным бронхоспазмом, сухими хрипами. Отмечаются также увеличение СОЭ и выраженная эозинофилия (до 20-50%). При отсутствии лечения и прогрессировании заболевания развивается фиброз легких.
При длительном течении вухерериоза у больных могут развиться гломерулонефрит, эндомиокардиальный фиброз, поражение глаз (конъюнктивит, иридоциклит) а также присоединиться вторичная инфекция (абсцессы внутренних органов, перитонит).
Дифференциальная диагностика. Вухерериоз дифференцируют с туберкулезом лимфатических узлов, лимфолейкозом, инфекционным мононуклеозом, бубонной формой чумы и другими филяриатозами.
Диагноз ставят на основании эпидемиологического анамнеза, клинических данных, результатов инструментальных и лабораторных методов исследований.
Лабораторная диагностика. Подтверждением диагноза служит нахождение микрофилярий в крови. Исследование крови производят в свежей капле, нанесенной на предметное стекло, под малым увеличением микроскопа (забор крови осуществляют вечером или ночью). Для улучшения диагностики используют метод обогащения. Иногда применяют иммунологические методы, однако они не являются строго специфичными.
Осложнения. Осложнения связаны с поражением лимфатической системы (элефантиаз). Иногда происходит закупорка мочеточников коагулянтами, нарушения функции конечностей при образовании рубцов в области суставов, присоединение вторичной инфекции с развитием острых бактериальных лимфангитов и тромбофлебитов.
Болезнь характеризуется длительным течением. Элефантиаз приводит к потере трудоспособности. Летальные исходы наступают в результате присоединения вторичной инфекции.
Лечение. Лечение вухерериоза комплексное. Его проводят в стаци- онаре. Лечение включает в себя дегельминтизацию, подавление бактериальных инфекций, ослабление аллергической реакции. Часто приходится прибегать к оперативному вмешательству. Лимфадениты лечат антигистаминными препаратами и анальгетиками. Диэтилкарбамазин (ДЭК, дитразин) эффективен в отношении микрофилярий и половозрелых особей (микрофилярии погибают быстро, а половозрелые особи в течение 2-3 недель). В 1-е сутки назначают 50 мг препарата внутрь после еды однократно, на 2-е - по 50 мг 3 раза, а в период с 4-го по 21-й дни лечения - по 2 мг/кг 3 раза в сутки. Максимальная суточная доза - 400 мг. Продолжительность лечения составляет 21 день. Детям препарат назначают по 2 мг/кг 3 раза в сутки в течение 10-14 дней. По клиническим показаниям назначают повторные курсы лечения. В зависимости от эффективности проводят от 3 до 5 курсов лечения с промежутками в 10-12 дней. Массовая гибель микрофилярий в начале лечения может
сопровождаться аллергической реакцией (лихорадка, крапивница, лимфангиты). Для эффективного лечения применяют кортикостероиды. Гидроцеле эффективно лечат хирургическими методами.
Профилактика. Ранняя диагностика и лечение предупреждает развитие элефантиаза. Личная профилактика заключается в индивидуальной защите от укусов комаров. Для этого применяют репелленты, специальные виды одежды, надкроватные пологи. Для борьбы с комарами проводят благоустройство систем канализации и водопроводов в городах и поселках. Уничтожают места выплода комаров с помощью инсектицидов.
Комплекс мер по профилактике включает выявление и лечение больных, а также меры по уничтожению комаров. Проводят массовые обследования населения для выявления лиц с микрофиляриями в крови и последующим их лечением. Для массовой химиопрофилактики лимфатических филяриозов в эндемичных районах используют диэтилкарбамазин (ДЭК). Всем жителям один раз в год назначается в дозе 2 мг/кг внутрь в три приема в течение одного дня.
4.3.2.2. Бругиоз
Бругиоз - трансмиссивный гельминтоз. Взрослые особи обитают в лимфатических сосудах, а личинки (микрофилярии) - в крови.
Этиология. Возбудители бругиоза - Brugia malayi и Brugia timori. У возбудителя малайского бругиоза известны два штамма: периоди- ческий и субпериодический. Самки имеют длину
Цикл развития. Цикл развития бругии почти ничем не отличается от вухерерии. Окончательный хозяин - человек, но могут быть обезьяны, кошки. Переносчики бругиоза - комары рода Anopheles, Mansonia и Aedes.
Эпидемиология. Бругиоз эндемичен только в странах Юго-Восточной Азии, где его ареал совпадает с ареалом вухерериоза: некоторые районы Индии и Китая, Южной Кореи, Вьетнама, на Филиппинах, в Малайзии, Таиланде, Индонезии.
Периодический штамм малайского бругиоза распространен на территории Индокитайского полуострова, в Центральной Индии, Южном Китае, Японии и Индонезии, где бругиоз является антропонозным забо- леванием: окончательный хозяин - человек, а переносчики - комары родов Anopheles, Aedes, Mansonia.
Субпериодический штамм бругии с ночным пиком активности встречается на территории болотистых лесов Малайзии как у человека, так и у обезьян (макак, лори), диких и домашних кошек. Здесь это зоонозная природно-очаговая инвазия, переносчиками являются комары рода Mansonia.
Бругиоз тиморский распространен ограниченно, в Индонезийском архипелаге и на острове Тимор. Здесь это антропоноз с ночной периодичностью появления микрофилярий в периферической крови. Переносчики - комары рода Anopheles.
Источником распространения инвазии являются зараженные люди или обезьяны и кошки. Заражение происходит при укусе окончательного хозяина комаром.
Патогенез и клиническая картина малайского бругиоза очень сходны с таковыми при вухерериозе. При бругиозе чаще возникает изъязвление пораженных лимфатических узлов. Практически отсутствуют поражение половых органов и хилурия. Локализация слоновости отмечается на голенях и предплечьях.
При тиморском бругиозе более часто развиваются абсцессы лимфоузлов, явление слоновости возникают на ногах, как при бругиозе малайском.
Дифференциальная диагностика. Для дифференциального диагноза имеет значение строение заднего конца тела микрофилярий. У личинок под кутикулой виден слой хорошо окрашенных ядер. Расположение этих ядер неодинаково у различных видов филярий. Это позволяет дифференцировать бругий от других видов филярий.
Лабораторная диагностика. Диагноз ставят, как и при вухерериозе, при обнаружении личинок в периферической крови ночью, но они могут быть обнаружены и в дневные часы.
Лечение. Лечение при малайском бругиозе такое же, как при вухерериозе, но аллергические реакции при этом на диэтилкарбамазин (ДЭК) более сильные, что требует снижения доз и применения антигистаминных препаратов. Реакция на ивермектин более слабая, он эффективен в малой дозе (20 мкг/кг).
При тиморском бругиозе лечение ДЭК эффективно, преимуществ у ивермектина перед ДЭК не обнаружено.
Профилактика. Профилактика такая же, как при вухерериозе.
4.3.2.3. Лоалоз
Лоалоз - трансмиссивный биогельминтоз. Половозрелые особи паразитируют в коже, подкожной клетчатке, под конъюнктивой глаза и под серозными оболочками различных органов человека. Личинки (микро- филярии) циркулируют в крови.
Этиология. Возбудитель лоалоза - «африканский глазной червь», - Loa loa, имеет
белое полупрозрачное нитевидное тело. Кутикула гельминтов покрыта
многочисленными округлыми выступами. Самки имеют длину 50-70 мм, ширину
Микрофилярии имеют малозаметный чехлик; их длина 0,25-
Цикл развития (рис. 4.39). Заражение человека лоалозом происходит через укус слепней рода Chrysops. Лоалоз - биогельминтоз, в цикле его развития присутствуют окончательные хозяева - человек, обезъяны, и промежуточные - кровососущие слепни рода uhtysops.
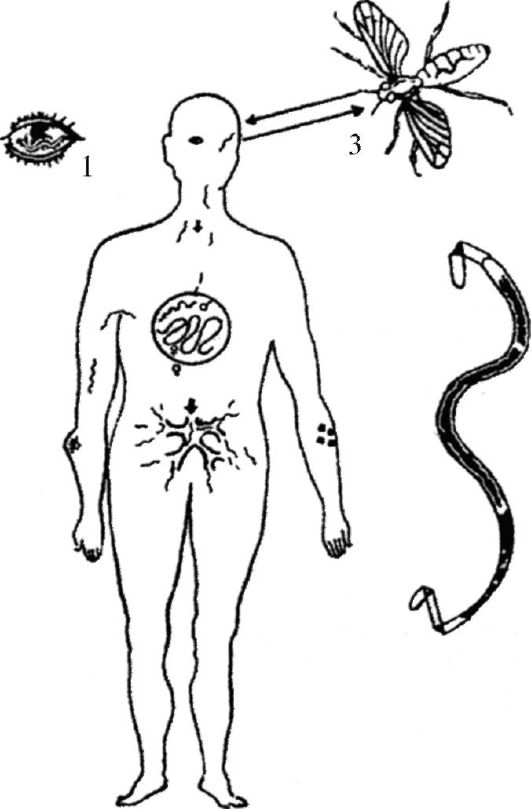
Рис. 4.39. Цикл развития лоа лоа. 1 - миграция гельминта в конъюнктиве глаза; 2 - микрофилярия; 3 - слепень
Слепни обитают в районах густо затененных медленно текущих водоемов. Самки откладывают яйца на листья водных растений. Личинки развиваются в воде, прибрежном иле и влажной почве. Укусы слепней болезненны. При кровососании они поглащают до 300 мг крови, в которой могут оказаться несколько сотен личинок. Микрофилярии проходят цикл развития в грудных мышцах слепня так же, как личинки вухерерий в комарах, и через 10-12 дней достигают инвазионной стадии. Инвазионные личинки мигрируют в ротовой аппарат слепня. Когда слепень кусает человека, инвазионные личинки мигрируют на поверхность кожи и после укуса попадают в кровь. Слепни способны передавать личинок окончательному хозяину в течение 5 дней.
Через 1,5-3 года микрофилярии достигают половой зрелости и начинают отрождать живых личинок. Половозрелые особи мигрируют по подкожной соединительной ткани. Рожденные самкой микрофилярии по лимфатическим и кровеносным сосудам проникают в легкие и там накапливаются. Периодически они мигрируют в периферические кровеносные сосуды. Микрофилярии циркулируют в крови только днем, и поэтому их называют Microfilaria diurna (дневные микрофилярии). Наибольшее количество личинок в периферической крови наблюдается между 8 и 17 часами.
В процессе эволюции произошли взаимные адаптации в цикле развития гельминтов, связанные с жизненной активностью переносчиков.
Переносчики (слепни) являются промежуточными хозяевами. Они активны днем, поэтому в периферической крови окончательного хозяина в это время находится наибольшее количество личинок.
Продолжительность жизни взрослых гельминтов составляет от 4-х до 17 лет.
Эпидемиология. Эндемичные очаги встречаются в лесных зонах Западной и Центральной Африки от 80? с. ш. до 50? ю. ш. Лоаоз распространен в Анголе, Бенине, Гамбии, Габоне, Гане, Заире, Камеруне, Кении, Конго, Либерии, Нигерии, Сенегале, Судане, Танзании, Того, Уганде, Чаде и др.
Источникраспространения лоалоза-больные люди. Специфическим переносчиком лоалоза являются слепни, способные передать возбудителя при укусе.
Патогенез. Инкубационный период длится несколько лет, но иногда сокращается до 4-х месяцев. Микрофилярии могут быть обнаружены в периферической крови через 5-6 месяцев после инвазии.
Патогенное действие обусловлено сенсибилизацией организма человека к продуктам обмена и распада гельминтов. Активное передвижение
филярий (со скоростью
Клиническая картина. Заболевание начинается с аллергических проявлений. Появляются боли в конечностях, крапивница, субфебрильная температура. Течение заболевания может быть бессимптомным до тех пор, пока гельминт не проникнет под конъюнктиву, в глазное яблоко. Могут возникнуть отеки век, сетчатки, зрительного нерва, боли, гиперемия конъюнктивы, ухудшение зрения. Вследствие поражения глаз этого гельминта называют «африканским глазным червем» (рис. 4.40).
Рис. 4.40. Лоа лоа в конъюнктиве глаза
Важным симптомом лоалоза является развитие «калабарского отека». Он появляется на ограниченных участках тела, медленно увеличивается в размерах и медленно рассасывается, кожа над ним обычной окраски. При надавливании на отечную область ямки не остается. Отеки возни- кают в местах локализации филярий в коже и подкожной клетчатке, чаще всего они появляются в областях запястий и локтевых суставов. Локализация отеков непостоянна. Появление отеков может длиться несколько лет. Отеки могут причинять боль, нарушать функции органов, сопровождаться кожным зудом, субфебрильной температурой, кожными высыпаниями.
Со стороны крови наблюдаются эозинофилия, анемия; также наблюдается увеличение и фиброз селезенки.
Миграция гельминтов в уретре вызывает сильные боли, особенно во время мочеиспускания. Вследствие нарушения оттока лимфы у мужчин может развиться гидроцеле.
Проникновение личинок в капилляры мозга вызывает его очаговые поражения, развитие менингита и менингоэнцефалита. Поражение центральной нервной системы может привести к летальному исходу.
Течение заболевания длительное, с чередованием обострений и ремиссий. Прогноз неосложненного лоалоза благоприятный.
Дифференциальная диагностика. Необходимо проводить дифференциальный диагноз с другими филяриатозами.
Лабораторная диагностика связана с обнаружением личинок в мазках и толстой капле крови. Кровь для исследования берут в любое время суток. В эндемичных районах диагноз часто ставится на основании клинических симптомов (наличие «калабарского отека», эозинофилия). Под конъюнктивой гельминты видны невооруженным глазом. При лоалозном энцефалите микрофилярии могут быть обнаружены в спинномозговой жидкости. Иногда используют иммунодиагностику.
Осложнения. Невриты, менингоэнцефалиты, отслойка сетчатки, раз- витие абсцессов, отек гортани, фиброз эндокарда часто встречающиеся осложнения у жителей эндемичных регионов по лоалозу.
Лечение. Лечение проводят в стационаре. Применяют диэтилкар- бамазин по той же схеме, как при вухерериозе. Учитывая выраженную аллергизацию организма продуктами распада гельминтов, одновременно назначают также антигистаминные препараты или глюкокортикоиды.
Из-под конъюнктивы глаза гельминтов удаляют хирургическим путем.
Профилактика. Личная профилактика заключается в защите от напа- дения слепней: ношение плотной одежды, использование репеллентов. Общественная профилактика - выявление и лечение больных, борьба с переносчиками, очистка берегов рек от кустарников, в которых обитают слепни, осушение и обработка инсектицидами заболоченных мест для уничтожения личинок слепней.
4.3.2.4. Онхоцеркоз
Онхоцеркоз - трансмиссивный биогельминтоз. Взрослые особи обитают в подкожной клетчатке человека свободно или внутри капсулы (узла). Микрофилярии скапливаются в коже, в лимфатических узлах.
Этиология. Возбудитель онхоцеркоза - Onchocerca volvulus, белая нитевидная нематода. Самки имеют длину 350-700 мм, ширину - 0,27-
Цикл развития (рис. 4.41). Заражение онхоцеркозом происходит при укусе человека мошкой Simulium. Окончательный хозяин - человек,
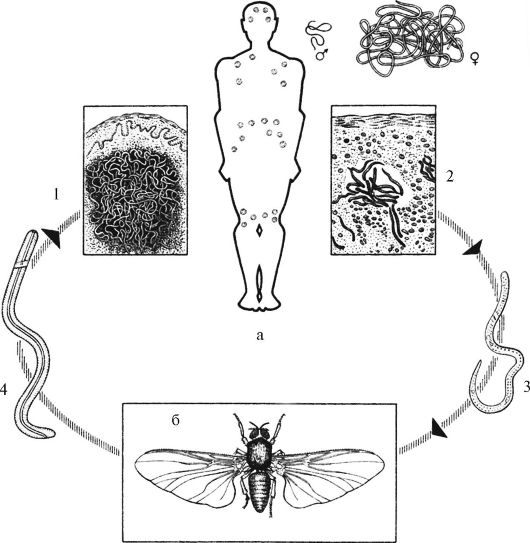
Рис. 4.41. Цикл развития онхоцерков. а - человек - (окончательный хозяин); б - мошка - (промежуточный хозяин); б - подкожный узел, содержащий взрослых нематод; 2 - микрофилярии в коже; 3 - микрофилярия; 4 - инвазионная личинка из промежуточного хозяина
промежуточный хозяин (переносчик) - кровососущие мошки рода Simulium, обитающие вдоль берегов порожистых, чистых, быстро текущих рек и ручьев. Прибрежная растительность служит местом дневного пребывания мошек. Мошки нападают на человека в светлое, наиболее прохладное время суток: с 6 до 10 часов утра и с 16 до 18 часов. Они кусают преимущественно нижние конечности. Днем, когда температура воздуха бывает максимальной, активность мошек снижается.
Жизненный цикл сходен с жизненными циклами других филярий. При укусе больного онхоцеркозом в пищеварительный тракт мошки
попадают микрофилярии, которые через 6-12 дней становятся инвазионными и мигрируют в ее ротовой аппарат. В момент укуса человека личинки активно разрывают оболочку нижней губы мошки, пропадают на кожу и внедряются в нее, мигрируют в лимфатическую систему, затем в подкожную жировую клетчатку, где достигают половой зрелости. Взрослые гельминты находятся в узлах (онхоцеркомах), расположенных под кожей, размером - от горошины до голубиного яйца. Онхоцеркомы - узелки, покрытые соединительнотканной капсулой, содержащие живых и погибших половозрелых гельминтов. Чаще всего узлы располагаются в подмышечной впадине, около суставов (коленный, бедренный), на ребрах, около позвоночника. В каждом узле содержится несколько самок и самцов, переплетенных в клубок. Самка отрождает до 1 млн личинок в год. Первые микрофилярии отрождаются через 10-15 месяцев после заражения. Продолжительность жизни личинок составляет от 6 до 30 месяцев. Микрофилярии располагаются по периферии узлов. Они могут активно проникать в поверхностные слои кожи, лимфатические узлы, в глаза. Взрослые гельминты живут 10-15 лет.
Эпидемиология. Эндемичные очаги онхоцеркоза находятся в странах Африки (Ангола, Бенин, Берег Слоновой Кости, Габон, Гамбия, Гана, Гвинея, Заир, Йемен, Камерун, Конго, Кения, Либерия, Мали, Нигер, Нигерия, Сенегал, Судан, Сьерра-Леоне, Танзания, Того, Уганда, Чад, Эфиопия), Латинской Америки (Венесуэла, Гватемала, Колумбия, Мексика, Эквадор). По данным ВОЗ, в 34 эндемичных странах онхоцеркозом болеют около 18 млн человек, 326 тыс. потеряли зрение в результате этого заболевания.
Очаги
онхоцеркоза обычно формируются в населенных пунктах, расположенных
возле рек, поэтому заболевание называют речной слепотой. От места
выплода мошки могут разлететься на расстояние от 2 до
Источником распространения инвазии являются зараженные люди. В эндемичных по онхоцеркозу районах Западной Африки заболеванию подвержено в основном сельское население. Как правило, поражаются все жители деревни от маленьких детей до стариков. В Африке существуют два типа очагов: лесного и саванного типов. Лесные очаги распространены в местности диффузно. Индекс зараженности мошек не превышает 1,5%. Инвазированное население в этих очагах составляет 20-50%, среди них доля слепых составляет 1-5%.
Очаги саванного типа более интенсивны. Они занимают территории, примыкающие к быстротекущим по каменистым плато речкам. Самые интенсивные в мире очаги онхоцеркоза расположены в западноафри-
канских саваннах, в бассейне реки Вольта. Инфицированность мошек достигает 6%. Пораженность населения онхоцеркозом составляет 80- 90%. Доля слепых среди взрослого населения колеблется от 30 до 50%. Очаги лесного типа могут превращаться в саванные вследствие вырубки лесов.
В Америке очаги онхоцеркоза немногочисленны и не столь интенсивны, как в Африке. Они встречаются в холмистых районах на высоте 600-1200 м над уровнем моря, где площади заняты кофейными плантациями. Рабочие этих плантаций наиболее часто болеют онхоцеркозом. Частота поражений глаз ниже, чем в Африке.
В мире онхоцеркозом поражено около 50 млн человек. Социальноэкономическое значение онхоцеркоза велико: население покидает эндемичные районы с плодородными землями, боясь заражения онхо- церкозом.
В России встречаются единичные завозные случаи онхоцеркоза.
Патогенез. Патогенное действие связано с сенсибилизацией организ- ма человека продуктами обмена и распада паразитов. Организм реагирует аллергическими реакциями на вещества, выделяемые паразитами. Наиболее яркие кожные и глазные проявления возникают в ответ на погибших микрофилярий, а не на живых. Вокруг взрослых паразитов образуется фиброзная капсула, окруженная эозинофилами, лимфоцитами, нейтрофилами. Гельминты постепенно гибнут, что снижает интенсивность инвазии.
Микрофилярии, рожденные половозрелыми самками, мигрируют в соединительную ткань, кожу, лимфатические железы, глаза. Проявления заболевания связаны с локализацией паразитов. Паразитирование гель- минтов в коже приводит к развитию онхоцеркозного дерматита, приводящего к развитию гипер- и депигментированным пятнам, истончению и атрофии кожи, образованию онхоцерком. При проникновении личинок в глаза поражаются сосудистая оболочка глаза, сетчатка, зрительный нерв, что может привести к потере зрения.
Клиническая картина. Инкубационный период длится около 12 месяцев, в некоторых случаях до 20-27 месяцев. Иногда первые признаки болезни могут проявиться через 1,5-2 месяца после заражения.
Клинические проявления онхоцеркоза зависят от степени инфицированности больного. У лиц с низкой инфицированностью единственным проявлением заболевания может быть кожный зуд. В этот период могут появиться субфебрильная температура и эозинофилия в крови. Ранним признаком может быть гиперпигментация кожи. Пятна имеют диаметр от нескольких миллиметров до нескольких сантиметров.
Зуд интенсивен в области бедер и голеней, усиливается в ночное время («филяриозная чесотка»). Он обусловлен поступлением в ткани кожи антигенов личинок гельминтов при их линьке и бывает настолько сильным, что люди кончают жизнь самоубийством. Кроме зуда появляется папулезная сыпь. Папулы могут изъязвляться, медленно заживать и формировать рубцы. Часто присоединяется вторичная инфекция. Кожа утолщается, покрывается морщинками и становится похожей на корку апельсина. У некоторых больных развивается прогрессирующая гипертрофия кожи с потерей ее эластичности («кожа крокодила» или «кожа слона»). Нередко возникает ксеродерма - сухость и шелушение кожи с мозаичным рисунком («кожа ящерицы»).
При длительно текущем дерматите появляется стойкая пятнистая депигментация кожи («кожа леопарда»). Этот признак чаще отмечается на нижних конечностях, половых органах, в паховой и подмышечной областях.
На поздних стадиях развития дерматита происходит атрофия кожи. Некоторые ее участки похожи на мятую папиросную бумагу («расплющенная бумажная кожа», старческий дерматит). Волосяные фолликулы и потовые железы атрофируются полностью. Появляются большие складки кожи, похожие на висячие мешки. Больные молодого возраста с такими изменениями кожи похожи на дряхлых стариков. При локализации поражений в области лица оно приобретает характерный вид, напоминающий морду льва при лепре («львиное лицо»).
На поздней стадии онходерматита с атрофией кожи развиваются псевдоаденокисты. Они встречаются у мужчин и представляют собой большие висячие мешки, содержащие подкожные ткани и лимфатические узлы. Местное население называет их «готентотским фартуком» или «висячим пахом», при локализации в подмышечной области - «висячая подмышка». Часто развиваются паховые и бедренные грыжи, которые весьма распространены в эндемичных по онхоцеркозу районах Африки.
Поражения лимфатической системы проявляются лимфастазом и лимфатическим отеком кожи. Лимфатические узлы увеличены, уплот- нены и безболезненны. Возможно развитие лимфангита, лимфаденита, орхита, гидроцеле.
В Центральной Америке и Мексике у больных моложе 20 лет встречается тяжелая форма онхоцеркозного дерматита, протекающего по типу рецидивирующего рожистого воспаления. На голове, в области шеи, на груди и верхних конечностях появляются темно-бордовые уплотненные и отечные участки кожи. В дерме развиваются грубые деформирующие процессы, сопровождающиеся зудом, отеком век,
светобоязнью, конъюнктивитом, иритом, явлениями общей интоксикации и лихорадкой.
Для
онхоцеркоза характерно развитие онхоцерком - плотных, безболезненных,
округлых или овальных образований, видимых на глаз или определяемых
только путем пальпации. Их размеры варьируют от 0,5 до
У африканцев онхоцеркомы расположены чаще в области таза, особенно над гребнем подвздошной кости, вокруг бедер, над копчиком и крестцом, вокруг коленного сустава, на боковой стенке грудной клетки.
В Центральной Америке онхоцеркомы чаще наблюдаются на верхней половине тела, возле локтевых суставов, более чем в 50% случаев на голове. При локализации онхоцерком в области суставов возможно развитие артритов и тендовагинитов.
Онхоцеркомы образуются лишь у коренных жителей эндемичных районов, у которых уже выработался механизм иммунного ответа на антигены паразита. У неиммунных лиц при длительном течении болезни обнаруживают взрослых онхоцерков, свободно лежащих в подкожной клетчатке.
Наиболее опасно попадание микрофилярий в глаза. Они могут проникать во все его оболочки и среды. Токсико-аллергическое и механическое воздействия вызывают слезотечение, резь в глазах, светобоязнь, гиперемию, отек и пигментацию конъюнктивы. Наиболее характерные повреждения отмечаются в передней камере глаз. Тяжесть поражений прямо пропорциональна числу микрофилярий, находящихся в роговице. Раннее поражение роговицы проявляется точечным кератитом, так называемым снежным помутнением, из-за сходства со снежными хлопьями. Кератит распространяется от периферии к центру, и через некоторое время вся нижняя половина роговицы полностью покрывается сетью кровеносных сосудов - «склеротический конъюнктивит». При онхоцеркозе верхний сегмент роговицы остается чистым вплоть до последней стадии болезни. На роговице образуются язвы, кисты. Спайки, образующиеся в результате воспалительной реакции вокруг гибнущих микрофилярий приводят к изменению формы зрачка, становящегося грушевидным. Хрусталик мутнеет. Патологические процессы в глазу развиваются в течение многих лет и приводят к понижению остроты зрения, а иногда и полной слепоте.
В связи с глубокими поражениями глаз прогноз заболевания серьезный.
Дифференциальная диагностика. Дифференциальную диагностику онходерматита проводят с лепрой, грибковыми заболеваниями кожи,
гиповитаминозами А и В, а также другими филяриатозами. Завозные случаи онхоцеркоза на неэндемичные территории устанавливаются с запозданием. Время от возвращения из тропиков до установления диагноза может составлять 2 года и более.
Диагноз устанавливают на основании комплекса клинических симптомов и эпидемиологического анамнеза.
Лабораторная диагностика. Надежным способом для постановки диагноза является обнаружение микрофилярий в бескровных кусочках кожи, а половозрелых форм - в удаленных онхоцеркомах. При помощи реакции Маззоти удается диагностировать онхоцеркоз в тех случаях, когда другие методы оказались неэффективными.
Осложнения. Серьезными осложнениями онхоцеркоза являются катаракта, глаукома, хориоретинит, атрофия зрительного нерва, слепота.
Лечение. Для лечения используют ивермектин, диэтиларбамазин и антрипол. Ивермектин (мектизан) взрослым назначают однократно из расчета 0,2 мг/кг. В случае возобновления репродуктивной функции у филярий лечение повторяют через 3-4 недели. При приеме лекарства наблюдаются побочные эффекты: головная боль, слабость, лихорадка, боль в животе, миалгия, артралгия, зуд, отеки.
Диэтилкарбамазин (ДЭК) назначается в первый день в дозе 0,5- 1 мг/кг однократно. В последующие 7 дней - по 2-3 мг/кг три раза в сутки. Максимальная суточная доза составляет 400 мг. Препарат оказы- вает действие только на личинок (микрофилярий).
Для уничтожения взрослых
гельминтов после курса ДЭК следует назначить антрипол.
Свежеприготовленный 10% раствор этого препарата вводят внутривенно
медленно. Последующие 5-6 инъекций проводят с недельным интервалом по
При аллергических реакциях назначают антигистаминные препараты, при тяжелых реакциях - кортикостероиды. Онхоцеркозные узлы удаляют оперативным путем.
Профилактика. Для
уменьшения интенсивности очагов онхоцеркоза применяют ларвициды
уничтожающие личинок мошек в местах их выплода. Обработка воды
инсектицидами в течение 20-30 мин приводит к гибели личинок на
протяжении более
При необходимости проживания в эндемичных очагах следует избегать пребывания вне населенного пункта или вне жилых помещений в ранние утренние и вечерние часы. Следует проводить химиопрофилак- тику ивермектином по 0,2 мг/кг внутрь 1 раз в 6 месяцев.
4.3.3. Дракункулез
Дракункулез - биогельминтоз. Половозрелые особи локализуются в подкожной клетчатке, чаще нижних конечностей.
Этиология. Возбудитель дракункулеза - Dracunculus medinensis, ришта, с четко выраженым половым диморфизмом. Нитевидная самка - крупная нематода длиной 30-129 см, шириной 0,5-1,7 мм, самец имеет длину 12-30 мм, ширину 0,2-0,4 мм.
Задний конец самца
загнут на брюшную сторону. На нем находятся 4 пары преанальных и 6 пар
постанальных сосочков, 2 темно-коричневые спикулы длиной 0,49-0,73 мм и
рулек длиной
В процессе длительного развития в организме окончательного хозяина (11-13 месяцев) первичная полость самки почти полностью заполняется матками, набитыми эмбрионами. Отверстие влагалища, прямая кишка и отверстие вульвы атрофируются. Оставшаяся часть кишечной трубки сморщивается и оттесняется в сторону. Личинки выходят через разрывы матки и кутикулы на переднем конце тела.
Цикл развития (рис. 4.42). Дракункулез - биогельминтоз. Окончательный хозяин - человек, иногда животные: собаки, обезьяны. Промежуточные хозяева - пресноводные рачки рода uyclops или Eucyclops.
Человек заражается дракункулезом, заглатывая с водой циклопов, инвазированных зрелыми личинками (микрофиляриями). В желудоч- но-кишечном тракте циклопы перевариваются. Личинки проникают через стенку кишечника и мигрируют по соединительным тканям в направлении нижних конечностей. Через 3 месяца после инвазии про-
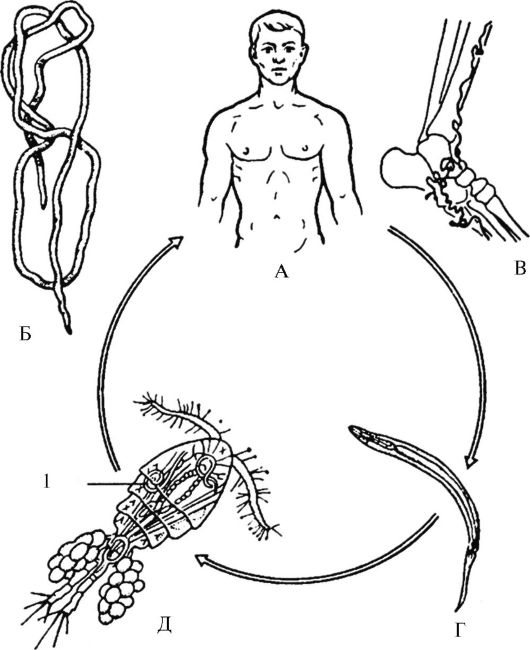
Рис. 4.42. Цикл развития ришты А - окончательный хозяин - (человек); Б - самка; В - локализация паразита в ноге человека (рисунок с рентгенограммы); Г - инвазионная личинка, отрождаемая самкой; Д - циклоп, зараженный личинками; 1 - личинки в полости тела циклопа
исходит оплодотворение самки. После этого самка мигрирует в подкожную клетчатку нижних конечностей, растет, достигая в длину 75-100 см. Примерно через год после проникновения личинок в организм человека в ее матке образуется до 3 млн личинок. Головной конец самки дости- гает кожи, вызывает образование на ней пузыря величиной до 5-8 см в диаметре, заполненного жидкостью. Личинки выходят из половых путей самки через разрыв матки и стенки тела гельминта около его переднего конца. Они выводятся из тела окончательного хозяина через отверстие, образовавшееся на коже под действием секрета специальных желез,
находящихся на переднем конце самки гельминта. Мелкие рабдитовидные личинки с длинным нитевидным концом имеют длину 0,5-0,75 мм, ширину - 15-25 мкм.
При соприкосновении с водой пузырь лопается. Из него высовывается передний конец самки. Выбрасывание личинок из тела ришты происходит благодаря сокращению его мускулатуры при соприкосновении с водой, что, возможно, связано с охлаждением переднего конца гельминта под действием воды. В течение 2-3 недель самка «отрождает» в воду до 3 млн личинок. После этого самки погибают. Они рассасываются или обызвествляются.
Личинки, попавшие в воду, живут в ней в течение 3-6 суток и заглатываются циклопами, в их теле растут, развиваются, дважды линяют и при температуре 25-30 ?С через 12-14 дней достигают инвазионной стадии.
Максимальная продолжительность жизни паразита в теле человека - менее 18 месяцев.
Эпидемиология. Дракункулез распространен в странах с жарким и засушливым климатом, в тропических районах Африки, на юге Аравийского полуострова, на юге Ирана, в Пакистане, Индии, Китае, Южной Америке.
Очаги дракункулеза формируются в местностях, где население употребляет для питья сырую воду из небольших искусственных или естественных непроточных водоемов, в которые жители заходят босиком (в это время самка ришты отрождают в воду личинок). Развитие паразитов происходит синхронно у всех инвазированных людей. Самки становятся способными рожать личинок одновременно почти у всех носителей гельминта. Этим достигается резкое повышение вероятности заражения огромного количества циклопов, а затем и окончательных хозяев в течение небольшого промежутка времени. Такая особенность цикла развития имеет адаптивное значение в зонах с засушливым климатом и редкими дождевыми периодами. В очагах распространения дракункулеза выявляется большое количество людей, пораженных этим гельминтом в течение небольшого временного интервала.
Заражение дракункулезом происходит в результате случайного проглатывания циклопов при питье воды из стоячих открытых водоемов. В организме человека паразит развивается очень медленно. Период эпидемиологической инкубации (срок, прошедший от момента заражения до момента выделения личинок во внешнюю среду) при дракункулезе очень велик и составляет 12 месяцев и более. Инвазированный окончательный хозяин становится источником инвазии только через год после заражения.
Основным источником инвазии является зараженный человек.
Распространение дракункулеза связано с антисанитарными условиями, плохим водоснабжением, отсутствием водопровода и канализации. Дракункулез преобладает в бедных семьях, проживающих в неблагоуст- роенных домах и пьющих сырую грязную воду, использующих фекалии для удобрения огородов.
Большую роль в загрязнении воды личинками ришты играют водоносы, входящие босыми ногами в стоячие водоемы для забора воды, а также верующее население, совершающее в водоемах ритуальное омовение. В результате поступления в водоемы большого количества личинок, наличия множества циклопов и благодаря привычке населения пить сырую воду интенсивность передачи инвазии в очагах дракункулеза велика.
Патогенез. Патогенное действие ришты связано с сенсибилизацией организма продуктами обмена гельминта, механическим повреждением тканей и присоединением вторичной инфекции.
Клиническая картина. О наличии ришты больные узнают через несколько месяцев после заражения, за 8-10 дней до образования пузыря на коже. Первые симптомы сопровождаются выраженными аллергическими реакциями. Возникают зуд, крапивница, тошнота, рвота, астматические явления, лихорадка, опухание суставов, вблизи которых находятся гельминты (рис. 4.43).
Рис. 4.43. Поражение риштой конечности человека
Вскоре после разрыва пузыря аллергические явления прекращаются. Дальнейшее течение инвазии определяется отсутствием или наличием вторичной инфекции.
Специфическими признаками этого заболевания являются эритема, уплотнение кожи, образование пузырьков и язв на месте выхода гель-
минта на поверхность. Первые проявления - формирование маленькой капсулы, превращающейся в пузырь. Пузырь наполнен прозрачной желтоватой жидкостью, которая содержит личинки ришты, лейкоциты, лимфоциты и эозинофилы. Образование пузыря сопровождается зудом и жгучей болью, которые могут ослабеть от холодной воды. Пузырь разрывается при контакте с водой, из него высовывается передний конец самки. На месте пузыря появляется язва, окруженная валиком отечной кожи и покрытая белой некротической массой, которая через несколько дней отторгается. В неосложненных случаях язва быстро заживает. При наличии в организме лишь одного гельминта клинические проявления продолжаются не более 4-6 недель и заканчиваются выздоровлением. Местные поражения локализуются преимущественно на голенях и в области лодыжек (90%), иногда встречаются на других участках тела: на спине, животе, мошонке, ягодицах, молочных железах, языке, плечах.
Тяжесть симптомов зависит от локализации паразита. Более тяжелое течение дракункулеза наблюдается при локализации ришты в области крупных суставов, при гибели паразита, при вторичном бактериальном инфицировании или их сочетании. Чаще возникают одиночные поражения, но известны случаи паразитирования у одного человека до 50 гельминтов. Процесс протекает болезненно и лишает больного трудоспособности на длительное время. Иногда происходит гибель гельминта до отрождения личинок. В этих случаях заболевание протекает бессимптомно.
Диагностика. Диагноз дракункулеза в эндемичных очагах при наличии характерных кожных проявлений не представляет затруднений. Под кожей прощупывается шнуровидное образование. На месте разрыва пузыря можно обнаружить передний конец ришты и ее личинки. Обызвествленные паразиты обнаруживаются при рентгенологическом исследовании.
Вне эндемичных очагов дракункулез необходимо дифференцировать от фурункулеза, абсцесса, флегмоны и выяснить у больного возможность его пребывания в очагах дракункулеза.
Осложнения. При локализации ришты в области суставов развиваются острые артриты, которые в 1% случаев заканчиваются анкилозом. В процесс могут вовлекаться другие крупные суставы и мышцы. Проникновение в место локализации паразита бактериальной инфекции способно вызвать гнойные абсцессы, флегмоны, иногда гангрены, эпидидимит, орхит, сепсис. Случаи столбняка, регистрируемые в эндемичных по дракункулезу районах, возникают вследствие предшествующей инвазии риштой. При отсутствии осложнений прогноз благоприятный.
Лечение. Традиционный способ лечения - наматывание на палочку тела гельминта, по несколько сантиметров в день, избегая его обрыва. При развитии аллергических явлений назначают антигистаминные препараты. Применяют метронидазол в дозе 250 мг x 3 x 10 дней, для детей - 25 мг/кг в три приема, общая суточная доза не должна превышать дозу взрослых. Препараты не уничтожают гельминта, но облегчают его извлечение традиционным способом.
Профилактика. Глобальная программа ликвидации дракункулеза включает:
- обеспечение населения безопасной питьевой водой;
- выделение специальных водоемов для забора питьевой воды и охрана его от загрязнения;
- фильтрацию воды из открытых непроточных водоемов для предупреждения проникновения в нее циклопов;
- выявление и лечение больных;
- предотвращение осеменения водоемов личинками гельминта путем наложения повязки на риштозный пузырь.