Медицинская и клиническая генетика для стоматологов: учебник для вузов / Под ред. О.О. Янушевича., - 2009. - 400 с.
|
|
|
|
ГЛАВА 5. МУЛЬТИФАКТОРИАЛЬНЫЕ БОЛЕЗНИ
Ильяшенко Любовь Дмитриевна
5.1. НАИБОЛЕЕ РАСПРОСТРАНЕННЫЕ НОЗОЛОГИЧЕСКИЕ ФОРМЫ
Возможности новых технологий, а именно молекулярной диагностики, определять предрасположенность к заболеваниям на молекулярно-генетическом уровне резко усилили интерес к генетике наиболее распространенных наследственных заболеваний, приводящих к гибели и инвалидности человека. Это группа мультифактериальных заболеваний , характер наследования которых не может быть объяснен менделевскими законами, законами моногенного наследования (табл. 5.1).
Таблица 5.1. Частота широко распространенных заболеваний мультифакториальной природы
Болезни с наследственной предрасположенностью | Частота(%) |
Ишемическая болезнь сердца | 5-10 |
Гипертоническая болезнь | 10-20 |
Язвенная болезнь желудка и двенадцатиперстной кишки | 2-5 |
Диабет | 1-2 |
Бронхиальная астма | 0,2-0,5 |
Шизофрения | 1-2 |
Эпилепсия | 1 |
Маниакально-депрессивный психоз | 0,5 |
Алкоголизм | 1,4-10 |
Олигофрения (недифференцированная) | 0,5-0,05 |
Расщелина губы и нёба | 0,1-0,2 |
Вывих бедра | 0,5 |
Косолапость | 0,5 |
Анэнцефалия и черепномозговая грыжа | 0,1 |
5.2. ОБЩИЕ И ЧАСТНЫЕ МЕХАНИЗМЫ РЕАЛИЗАЦИИ НАСЛЕДСТВЕННОЙ ПРЕДРАСПОЛОЖЕННОСТИ
Мультифакториальные болезни с наследованием предрасположенности были выделены из группы генных болезней благодаря широким генетико-эпидемиологическим исследованиям в разных популяциях (клинико-генеалогическим, близнецовым, популяционно-статистическим).
В отличие от моногенных болезней, обусловленных одной единственной мутацией, для мультифакториальных заболеваний характерно наследование предрасположенности, зависящей от значительного числа генов с суммарным (аддитивным) эффектом (генетическая компонента) и от факторов внешней среды (средовая компонента) (Фолкнер, 1965).
Генетические факторы (наследственная компонента), представляющие полигенные системы и несущие информацию о предрасположенности, могут быть в виде двух вариантов:
• с пороговым действием;
• без порогового действия.
Полигенные системы предрасположенности без порогового действия предполагают, когда результат действия увеличивается количественно при накоплении патологических генов.
Для реализации полигенной системы предрасположенности с пороговым эффектом в болезнь (утрату ресурсов и функций органов и систем организма) обязательно наличие неблагоприятных факторов окружающей среды, психосоциальных, охарактеризованных клиницистами как «средовые факторы риска» (средовая компонента). Мультифакториальные заболевания возникают и прогрессируют при условии, если суммарный эффект от взаимодействия генетических и средовых факторов (компонент) предрасположенности превышает пороговое значение подверженности. Положение порога на нормальной кривой предрасположенности к заболеванию определяется частотой заболевания в популяции.
Генетическая компонента мультифакториальных заболеваний может быть обусловлена суммарным (аддитивным) действием специфических комбинаций аллелей нескольких генов с незначительным влиянием каждого, либо один ген является главным, а остальные будут иметь модифицирующее влияние. Средовая компонента также
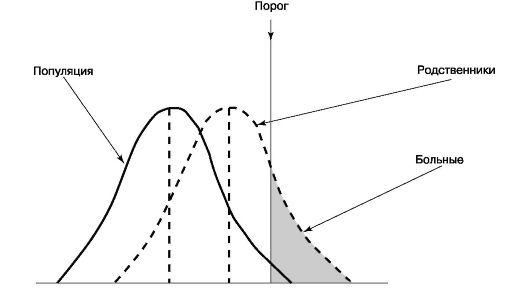 Рис. 5.1. Гипотетические
кривые предрасположенности к мультифакториальному заболеванию в
популяции и у родственников пробандов. По оси абсцисс - степень
предрасположенности (увеличивается справа налево), по оси ординат -
число лиц. Часть серым цветом - больные
Рис. 5.1. Гипотетические
кривые предрасположенности к мультифакториальному заболеванию в
популяции и у родственников пробандов. По оси абсцисс - степень
предрасположенности (увеличивается справа налево), по оси ординат -
число лиц. Часть серым цветом - больные
имеет сложный характер и представляется в виде нескольких компонентов, таких как систематические средовые факторы и случайные.
Сложность генетических и средовых компонент предрасположенности к мультифакториальным заболеваниям, а также сложность их взаимодействия проявляется прежде всего в выраженном клиническом полимофизме этой группы заболеваний, а именно:
• сроки начала;
• полнота и степень выраженности симптомов;
• характер, тяжесть, продолжительность течения;
• толерантность к лечению;
• выход из болезни (выздоровление, инвалидность, смерть). Клиническое многообразие мультифакториальных заболеваний
можно условно разделить на следующие варианты:
• врожденные пороки развития (ВПР);
• системные поражения с хроническим прогрессирующим характером течения;
• а также возможные их сочетания.
Соотносительная роль генетических и средовых факторов (компонент) различна как для конкретной патологии, так и для каждого индивида. Величина предрасположенности может быть различна для индивидов мужского и женского пола, разных конституциональных типов, биохимических, иммунологических характеристик. Например, по ишемической болезни сердца (ИБС) группу риска составляют лица мужского пола гипер- и нормостеники, с коронарным типом личности, повышенным содержанием холестерина липопротеидов низкой плотности, пониженным холестерина липопротеидов высокой плотности, высоким уровнем апоВ, липопротеина L, фибриногена плазмы и гомоцистеина. Но для реализации предложенного генотипа необходимо определенное временное воздействие средовых факторов, таких как курение, высококалорийное питание с высоким содержанием животных жиров, низким растительных жиров, определенный способ приготовления пищи, низкая физическая нагрузка, хронический стресс и др.
При мультифакториальном характере заболевания ожидается уменьшение частоты заболевания с уменьшением степени родства (третьей по сравнению со второй и второй по сравнению с первой).
Частота заболевания будет выше среди родственников больных с более тяжелыми клиническими вариантами данного заболевания, так как степень предрасположенности этих больных должна быть больше, т.е. кривая предрасположенности расположена дальше за порогом.
В то же время несмотря на то что человек глубоко индивидуален по биологическим и психосоциальным факторам, число вариаций ключевых биохимических реакций, важных для гомеостаза, сравнительно ограничено прежде всего генетической конституцией семьи («семейным генофондом»). Исходя из этого анализ модели полигенного наследования предрасположенности показывает, что вероятность мультифакториальных заболеваний среди родственников больных выше, чем в популяции (табл. 5.2). Кривая предрасположенности к заболеванию у родственников имеет характер нормального распределения в популяции, в то же время предрасположенность к заболеванию у родственников больного выше, чем в среднем в популяции, и кривая их предрасположенности сдвинута вправо по сравнению с нормальным распределением (рис. 5.1). Причем она коррелирует с увеличением как числа больных родственников в семье и степенью их родства, так и с тяжестью заболевания родственников.
Таблица 5.2. Увеличение риска иметь больное потомство среди родственников больных по сравнению с общей популяцией
Показатель | Расщелина губы и/или нёба | Косолапость | Стеноз привратника | Грыжа спинного мозга |
Частота в общей популяции Частота среди потомства родственников больного | 0,001 0,001х50 | 0,001 0,001х25 | 0,002 0,002х10 | 0,005 0,005х7 |
Доля идентичных генов у родственников в зависимости от степени родства составляет:
• у родственников I степени родства (родители, сибсы, дети) - 1/2
• у родственников II степени родства (дяди/тети, бабушки/ дедушки, внуки/внучки, полусибсы, племянницы/племянники)-1/4 • у родственников III степени родства (двоюродные сибсы, пра- дедушки/прабабушки, правнуки/правнучки) - 1/8
Мультифакториальные болезни при всем их разнообразии характеризуют следующие общие черты:
• высокая частота популяции;
• несоответствие наследования простым менделевским моделям;
• выраженная внутригенная и межгенная генетическая гетерогенность;
• клинический полиморфизм;
• антиципация - утяжеление клиники в семье по поколениям (как за счет средовой, так и наследственной компонент).
Таблица 5.3. Повышение (%) риска иметь следующего больного ребенка с увеличением числа больных членов семьи
Число больных детей | Расщелина губы и/или нёба | Стеноз привратника | Грыжа спинного мозга |
Один Два | 3-4 10 | 5 10 | 5 10 |
5.3. ФАКТОРЫ И ПРИНЦИПЫ ВЫЯВЛЕНИЯ ЛИЦ С ПОВЫШЕННЫМ РИСКОМ РАЗВИТИЯ БОЛЕЗНЕЙ С НАСЛЕДСТВЕННЫМ ПРЕДРАСПОЛОЖЕНИЕМ
С использованием мультифакториальной модели наследования в 60-70-е годы ХХ в. были получены оценки коэффициентов наследуемости многих хронических заболеваний, что позволило получать оценки повторного риска возникновения заболевания в семьях пробанда для родственников разной степени родства с помощью специальных компьютерных программ.
В России таблицы повторного риска для самых различных семейных ситуаций созданы для многих мультифакториальных заболеваний (сахарного диабета, ишемической болезни сердца, псориаза, расщелины губы/нёба и др.).
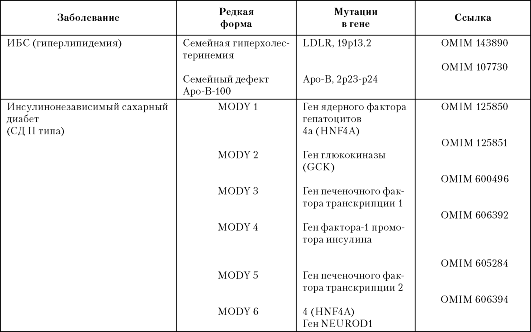
В последующие годы изучение роли наследственности в этиопатогенезе мультифакториальных заболеваний характеризовалось клинико-генетической направленностью. Это позволило исходя из генетической гетерогенности хронических заболеваний выделить в пределах традиционных форм заболеваний ряд редких моногенных форм. Например, из ИБС выделена семейная гиперхолестеринемия, обусловленная дефектом рецепторов липопротеинов низкой плотности (мутации в гене рецепторов ЛПНП), из диабета взрослых - моногенные инсулиннезависимые формы, у молодых МОДИ 1-6, хронического панкреатита - семейный панкреатит (табл. 5.5).
Новые возможности в изучении генетики мультифакториальных заболеваний появились в результате успешной реализации программы «Геном человека». На основе идентификации генов предрасположенности, анализа их взаимодействия в реализации общих метаболических путей и систем возможен переход к этиопатогенетическому лечению этой группы заболеваний их профилактики.
В решении этой труднейшей проблемы наблюдается переход от анализа отдельного гена к анализу большого числа генов среди семейств генов, включенных в общие метаболические пути и системы. От этиологии (специфической мутации) к патогенезу (механизму), от изучения действия гена к познанию регуляции действий гена.
Именно возможности новых технологий, в том числе молекулярной диагностики, определять предрасположенность к заболеваниям на молекулярно-генетическом уровне (в доклинической стадии) обеспечит возможность раннего и рационального лечения заболевания и его профилактики.
Таблица 5.4. Риск развития ишемической болезни сердца (ИБС) у мужчин в зависимости от наличия ИБС у родственников I степени родства
Возраст (годы) | Число здоровых сибсов | Пораженные родители | ||||||||
0 | 1 | 2 | ||||||||
Пораженные сибсы | ||||||||||
0 | 1 | 2 | 0 | 1 | 2 | 0 | 1 | 2 | ||
20-29 | 0 1 2 | 1,7 1,7 1,5 | 8,1 7,4 6,8 | 15,7 14,5 13,5 | 7,7 7,1 6,5 | 15,3 14,1 13,0 | 22,1 20,6 19,2 | 26,9 25,4 24,0 | 30,9 29,7 28,4 | 33,1 32,7 31,6 |
30-39 | 0 1 2 | 2,1 1,9 1,8 | 9,1 8,3 7,6 | 17,2 15,7 14,5 | 9,1 8,3 7,6 | 17,0 15,7 14,4 | 24,3 22,5 20,9 | 29,7 27,8 26,0 | 34,1 32,5 30,8 | 37,3 35,9 34,5 |
40-49 | 0 1 2 | 4,5 4,1 3,8 | 13,4 12,0 10,9 | 22,5 20,2 18,4 | 15,6 13,9 12,5 | 25,1 22,6 20,5 | 32,8 29,8 27,2 | 39,9 36,6 32,6 | 45,7 42,1 38,8 | 50,0 46,8 43,6 |
50-59 | 0 1 2 | 10,2 9,1 8,1 | 20,7 18,1 16,3 | 29,3 26,3 23,7 | 26,5 22,5 20,0 | 36,6 32,3 28,8 | 44,1 39,6 35,8 | 51,7 45,0 39,6 | 58,0 51,6 46,1 | 62,7 56,7 51,4 |
60-69 | 0 1 2 | 16,8 14,7 13,1 | 27,2 24,2 21,8 | 35,4 31,8 28,8 | 36,0 30,6 26,5 | 45,7 39,8 35,2 | 52,7 46,9 42,0 | 60,2 51,7 45,3 | 65,9 57,7 51,2 | 70,1 62,4 56,0 |
20-69 | 0 1 2 | 7,7 6,9 6,2 | 17,6 15,6 11,1 | 26,7 23,9 31,6 | 22,2 19,3 17,1 | 32,3 28,6 25,7 | 39,9 35,9 32,6 | 37,5 41,8 37,1 | 53,8 48,8 43,6 | 58,5 53,5 48,9 |
Значение характеристик пациента как молекулярно-генетических, так и нервно-психических, особенности питания, физических и профессиональных нагрузок, требуют нового осмысления клинико-генеалогических исследований семьи. Именно клиникогенеалогические исследования (составление родословной на базе расширенного анамнеза семьи индивида - пробанда) в сочетании с современными методами исследования (инструментальными, компьютерными, лабораторными, в том числе молекулярно-генетическими) здоровья каждого индивида будет способствовать развитию пациенториентированной модели диагностики, лечения, профилактики мультифакториальных заболеваний, широко распространенных в популяции человека.
5.4. ЭКОГЕНЕТИЧЕСКИЕ БОЛЕЗНИ
Экогенетические реакции, или болезни, представляют собой патологические состояния, возникающие как результат проявления конкретных аллелей гена или изменения экспрессии при влиянии на организм определенных факторов среды.
В процессе эволюции человека среда его обитания постоянно менялась (климат, пища, жилище, одежда), что способствовало формированию биологической природы современного человека как за счет изменения генотипов (мутаций), так и широкой нормы реакции. Оба этих процесса (мутационный, а также широкий балансированный полиморфизм) приводят к изменению темпов изменчивости как на индивидуальном, так и популяционном уровнях. Под действием отбора в окружающей среде выживают и адаптируются популяции в зависимости от их генотипов, формируя биологически-стабильный вид, для которого характерно постоянное равновесие между изменчивостью генотипов и отбором. Биологическая природа человека формировалась в течение миллионов лет, в результате современный человек достаточно хорошо приспособлен к своей среде обитания.
В то же время для современного периода эволюции характерны стремительный темп и огромный объем изменений окружающей среды. Повысился радиационный уровень, изменились среда обитания (отходы производства, транспорта, масштабная циркуляция вирусов и микроорганизмов), а также объем и характер питания (пищевые добавки, пестициды, генетически модифицированные
Таблица 5.5. Редкие моногенные формы, выделенные из группы мультифакториальных заболеваний
 продукты).
Человек в процессе эволюции не соприкасался с многими современными
экогенетическими факторами, соответственно на действие их не было
отбора. Под влиянием экогенетических факторов у современного человека
могут появляться патологические реакции - экогенетические болезни.
продукты).
Человек в процессе эволюции не соприкасался с многими современными
экогенетическими факторами, соответственно на действие их не было
отбора. Под влиянием экогенетических факторов у современного человека
могут появляться патологические реакции - экогенетические болезни.
Предметом экогенетики человека является изучение индивидуальных генотипических особенностей метаболизма химических веществ, реакций на физические факторы, биологические агенты, обусловленные многочисленными вариантами ферментных систем, транспортных белков, антигенов и рецепторов клеток человека. Экогенетика изучает варианты ответов организма разных людей на воздействие факторов окружающей среды, различия в их адаптации.
Экогенетические болезни могут быть обусловлены редкими мутантными аллелями генов или полиморфными системами, определяющими количественные варианты ответа, т.е. могут контролироваться одним геном или несколькими. Соответственно характер распределения данных реакций в потомстве будет соответствовать моноили полигенным моделям наследования. В то же время для проявления патологического ответа необходимо воздействие конкретного средового фактора на данный индивид.
Четко установлена роль полиморфных генных локусов, участвующих как прямо, так и опосредованно в биотрансформации (детоксикации) чужеродных веществ (цитохром Р450, N-ацетилтрансферазы, холинэстеразы, пароксоназы сыворотки, лактазы, глюкоза-6-фос- фатдегидрогеназы, ингибиторов протеаз) в патологических экогенетических реакциях.
Для изучения механизма экогенетических реакций используются как генетические методы (клинико-генеалогический, близнецовый, популяционно-статистический, методы экспериментальной генетики, молекулярно-генетические методы исследования), так и биохимические, токсикологические и фармакологические.
Условно факторы окружающей среды можно разделить на физические, химические и биологические.
Физические факторы
Хорошо известна индивидуальная чувствительность организма человека к теплу, холоду, солнечному свету. Четкие расовые различия установлены в реакции на холодовой фактор. Представители негроидной расы более чувствительны к холоду, чем европеоидной,
возможно, за счет разного уровня теплопродукции и теплоотдачи. Люди с наследственной парамиотией повышенно чувствительны к холоду, сырая, прохладная погода с температурой 10-12 °С вызывает у них тонические спазмы мышц, проходящие под действием тепла.
Имеют место индивидуальные и расовые различия в реакциях на ультрафиолетовые излучения.
Пигментная ксеродерма (1:5-500 тыс.) аутосомно-рецессивного типа наследования является примером высокой чувствительности кожи человека к действию солнечного света. Для клиники заболеваний характерно появление ожогов с последующим их изъязвлением и образованием новообразований под действием солнечного света, развитие катаракты, неврологические нарушения, умственная отсталость. Молекулярно-генетический механизм заключается в мутациях в нескольких генных локусах (не менее 4 типов) Р53, PRb, Р161NК4а, PARF, контролирующих процессы репарации ДНК (экза- и эндонуклиаз, полимеразы, лигазы), что приводит к нарушению процессов репарации ДНК до нормы после повреждения их ультрафиолетовыми лучами. Эти гены клонированы, и возможна преклиническая и дородовая диагностика.
Наследственно детерминированные различия в репарирующих системах могут иметь существенное значение также в проявлениях чувствительности к ионизирующим излучениям.
Химические факторы
Огромное количество новых химических веществ появилось в продуктах и отходах производства, транспорта, в виде лекарственных средств, пищевых добавок и др. В последнее столетие человечество столкнулось с глобальной проблемой загрязнения атмосферы газообразными отходами огромного числа промышленных производств, выхлопными газами транспорта. Образующиеся пылевые частицы, содержащие множество химических соединений, попадают в организм как через легкие, так и слизистые оболочки, кожу и представляют угрозу для здоровья человека, особенно если он занят на соответствующем производстве.
Установлено значение генетической конституции организма человека в развитии экогенетических реакций на загрязнение атмосферы. Примером может служить недостаточность фермента α-антитрипсина. Фермент α-антитрипсин является мощным антипротеиназным ферментом, участвующим в дезактивации эластаз, выделяемых мак-
рофагами и полиморфноядерными лейкоцитами. Наследственный дефицит этого фермента приводит к разрушению межальвеолярных перегородок легких и вследствие этого происходит слияние альвеол в более крупные полости, т.е. к развитию панацинорной энфиземы и хроническому поражению печени. Синтез этого фермента кодируется геном расположенным в 14-й хромосоме. Отмечается значительный популяционный полиморфизм этого белка (около 70 аллелей), а также вариабельность. Наиболее распространенным вариантом является аллель М (80%). Неактивность белка связана с аллелем Z (рецессивный вариант). Фермент, синтезируемый в этом случае, отличается от ММ типа заменой глутаминовой кислоты на лизин в 342-й позиции, что приводит к изменению конформации молекулы белка. В результате этого ZZ форма не может экскретировать фермент печеночными клетками и накапливать в виде эозинофильных включений. Гомозиготы (генотип ZZ - частота 0,05% у европейцев) склонны к развитию хронических заболеваний легких, в том числе энфиземы. Эмфизема легких у этих лиц развивается после 30-40 лет чаще и для нее характерно злокачественное течение. Запыленность воздуха и курение значительно увеличивают риск развития заболевания у этих лиц (в 30 раз). Методы определения недостаточности α-антитрипсина в настоящее время разработаны и должны применяться при профессиональных отборах на соответствующих производствах.
Примеры индивидуальной непереносимости того или иного продукта известны давно, например непереносимость молока, конских бобов, некоторых злаков. Непереносимость лактозы (молока) - галактоземия проявляется в дискомфорте желудочно-кишечного тракта, диарее. Отсутствие выработки фермента лактазы в кишечнике у гомозигот приводит к не расщеплению лактозы, что является субстратом для размножения гнилостной микрофлоры в кишечнике. Мутантные формы гена лактазы встречаются с разной частотой: среди европейцев частота гомозигот составляет 5-10%, восточных народов, афроамериканцев, американских индейцев - 70-100%.
Примером непереносимости пищевых продуктов является целиакия, обусловленная непереносимостью глютена, белка злаков (пшеницы, ржи, ячменя), характеризующаяся развитием атрофии слизистой оболочки тонкой кишки и связанного с ней симптома мальабсорбции. В типичном случае целиакия манифистирует через 1,5-2 мес после введения злаковых продуктов в питание ребенка (в
8-12 мес) с последующим замедлением темпов прибавки веса ребенка, снижением аппетита, эмоциональной лабильностью. В начале заболевания глютен связывается со специфическими рецепторами эпителиоцитов, детерминированными генами HLA, в ответ на действие глютена происходит атрофия ворсинок тонкой кишки, также в процесс активно вовлекается лимфоидная ткань кишки. Предполагается аутосомно-рецессивный тип наследования, в предрасположенности к целиакии участвуют два генных локуса (6р гены GSE,CD). Распространенность предрасположенности к целиакии колеблется в широких пределах 1:500 до 1:2700 (4,6:1000 - Италия до 3,7:1000 - Швеция, 1:476 - Австрия, 1:555 - Ирландия). Крайне редко заболевание встречается в Японии, Китае, Африке. Без продуктов, содержащих глютен, эти дети развиваются нормально, т.е. наиважнейший компонент лечения - пожизненная строгая безглютеновая диета.
Недостаточность фермента глюкозо-6-фосфат - дегидрогеназы (Х-сцепленный рецессивный признак) вызывает гемолиз крови у людей, употребляющих в пищу конские бобы. При постоянном приеме этого продукта вслед за гемолизом следует хроническое поражение почек. Подобную реакцию могут вызывать также и некоторые лекарственные вещества (примахин, сульфаниламидные препараты), промышленные окислители.
Известно около 200 вариантов глюкозо-6-фосфат - дегидрогеназы, лишь некоторые из них вызывают гемолиз эритроцитов. Синтез аномальной молекулы фермента обусловлен структурными мутациями гена. Клинически различают пять форм недостаточности фермента в зависимости от его активности. К первой форме относят недостаточность фермента, который вызывает хроническую несфероцитарную гемолитическую анемию с последующим развитием спленомегалии. Во 2-4-й форме гемолитическая анемия развивается прежде всего при употреблении конских бобов. При недостаточности глюкозо-6-фосфат - дегидрогеназы в эритроцитах нарушается основная функция фермента, поддержание стабильности мембран эритроцитов от повреждающего действия кислорода, устойчивость к воздействию потенциальных окислителей.
Имеются сообщения о различии в чувствительности человека к солям тяжелых металлов (свинец, ртуть, кадмий и др.). У человека существует жесткий генетический контроль метаболизма поступающих в организм химических соединений.
Понятие о экогенетике человека, а также ее основы начали формироваться в средине 50-х годов двадцатого столетия, когда впервые обратили внимание на генетически детерминированные патологические реакции на лекарственные вещества, связанные с недостаточностью ферментов. А. Мотульски (1957) впервые предложил термин «фармакогенетика» для обозначения раздела генетики, изучающего генетический контроль метаболизма лекарств, а также наследственные болезни, возникающие или усиливающиеся при приеме определенных лекарственных веществ (Фогель Ф., 1959).
Биологические факторы
Генетическую природу иммунной системы организма, предназначенной для защиты организма от внешнего (инфекционные болезни) и внутреннего (онкологическое перерождение клетки) повреждающего действия, изучает иммуногенетика.
Иммунная система человека представляет комплекс специализированных лимфоидных органов и диссеминированных клеток. Эти структуры, возникшие в процессе эволюции человека как биологического вида, сформировали механизмы их ответных реакций, обеспечивающих распознавание чужеродных и собственных измененных антигенов (макромолекулы), удаление их из клеток, содержащих их, обеспечивая запоминание контакта с этими антигенами.
Генетическая природа иммунитета и разная степень его выраженности у индивидов является общебиологической закономерностью, обусловленной генетическим полиморфизмом реакций на действие внешних биологических факторов (вирусы, бактерии, грибки) и внутренних (онкологически перерожденные клетки).
Классическим примером генетически детерминированной устойчивости к биологическим агентам служат гемоглобинопатии (серповодноклеточная анемия, талассемии) и энзимопатии (недостаточность глюкозо-6-фосфат - дегидрогеназы). Именно устойчивость лиц с дефектом глюкозо-6-фосфат - дегидрогеназы и гемоглобинопатиями к малярийному плазмодию позволило широкому распространению соответствующих мутаций в ареалах с высокой заболеваемостью малярией (Средиземноморье, Африка).
Распространенные иммунодефицитные состояния могут быть результатом нарушения функций клеточного и гуморального иммунитетов. Они предрасполагают к соответствующим бактериальным, вирусным, грибковым типам инфекций. Хорошо известны факты
различной чувствительности людей при введении одних и тех же доз вакцин: от отсутствия реакции на иммунизацию до клинического проявления инфекции.
В широком понимании все болезни мультифакториальной природы можно рассматривать как экогенетические болезни, так как для их развития необходимо взаимодействие генов предрасположенности и средовых факторов риска. Экогенетические реакции, как и мультифакториальные болезни, являются ответом организма с определенной генетической конституцией на воздействие средовых факторов.
Таким образом, экогенетика является научной основой для обеспечения адаптивной среды для каждого человека: подбор индивидуального рациона и климата, исключение отравления лекарствами, профессиональный отбор, что исключит преждевременную смерть, инвалидизацию, дополнительную госпитализацию человека, а также сохранит его биологическое и социальное здоровье.