Детская урология-андрология: Учеб. пособие. - Разин М.П., Галкин В.Н., Сухих Н.К. 2011. - 128 с.
|
|
|
|
Глава 9. ВОСПАЛИТЕЛЬНЫЕ ЗАБОЛЕВАНИЯ ОРГАНОВ МОЧЕВОЙ СИСТЕМЫ
Воспалительные заболевания органов мочевой системы чрезвычайно распространены в человеческой популяции и, в частности, у детей. Так, из всех заболеваний детского возраста частота разных форм пиелонефрита настолько высока, что уступает это своеобразное лидерство только ОРВИ. В этой главе также освещены наиболее важные особенности таких распространённых воспалительных патологий органов мочевой системы у детей, как цистит и баланопостит.
9.1. ПИЕЛОНЕФРИТ
Пиелонефрит - воспалительное заболевание паренхимы почки и её полостей с преимущественным поражением межуточного вещества мозгового слоя паренхимы и почечных канальцев, обусловленное патогенной флорой. В урологической практике наибольшее значение среди всех гнойных заболеваний почек принадлежит вторичному хроническому обструктивному пиелонефриту, развивающемуся у детей на фоне врождённых обструкций мочевой системы. До недавнего времени в трактовке звеньев патогенеза обструктивного пиелонефрита, осложняющего течение врождённых обструктивных уропатий, большое значение придавали уродинамической концепции. Согласно этой гипотезе обструкция мочевых путей сопровождается нарушением уродинамики. Это приводит к расширению лоханки, повышению внутрилоханочного давления, сдавлению почечной вены и её ветвей, нарушению венозного оттока и проникновению микроорганизмов в почечный кровоток, что создаёт благоприятные условия для развития хронического пиелонефрита. Вместе с тем за последние два десятилетия выявлены другие причины вторичного обструктивного пиелонефрита.
Установлено, что у больных с аномалиями мочевой системы разной формы и локализации выявляются недостаточно дифференцированные, незрелые, неправильно сформированные элементы почечной ткани. Порочно развитые структуры почечной паренхимы, дезори-
ентированные на клеточном уровне, выступают постоянным антигенным стимулятором для собственной иммунной системы ещё до рождения ребёнка. В результате происходит сенсибилизация и активация Т-лимфоцитов и неспецифической защиты организма, а также угнетение гуморального иммунитета, что расценивают как дискоор-динацию иммунного ответа или блок иммуногенеза. После рождения ребёнка воздействие инфекционного (вирусного, бактериального) и антигенного факторов (в результате плановых профилактических прививок) играет решающую роль в клиническом проявлении аномалии в виде хронического пиелонефрита, что позволяет диагностировать порок при целенаправленном и углублённом исследовании. Дальнейшее развитие пиелонефрита обусловлено не только тяжестью аномалии, степенью нарушения уродинамики и гемодинамики; пожалуй, оно в большой мере зависит от типа иммунопатологической реакции, создающей условия для развития хронического воспаления на иммунной основе.
Возникновению вторичного пиелонефрита у детей с врождёнными обструктивными уропатиями способствует расстройство кровообращения в почках, усугубляющееся под действием инфекции. Острые респираторные заболевания и другие инфекции оказывают капилляротоксическое воздействие на богато васкуляризированные органы, в том числе на почки. В них нарушается микроциркуляция (возникают стазы в капиллярах, сладж-синдром, образуются тромбы в венозных сосудах) и повышается проницаемость сосудистой стенки, что способствует оседанию и размножению микроорганизмов в межуточной ткани органа.
Немаловажную роль в развитии пиелонефрита играют анатомо-физиологические особенности почечной ткани, особенно её мозгового вещества. Относительно замедленный кровоток, способствующий оседанию бактерий, высокая осмолярность плазмы крови, повышенная концентрация натрия, мочевины, аммония, глюкозы и других веществ создают благоприятные условия для возникновения инфек-ционно-воспалительного процесса в интерстиции почки. Основные пути инфицирования почки при пиелонефрите:
• гематогенный (более характерен для первичного инфекционного процесса);
• восходящий: интраканаликулярный и уриногенный (более типичен для вторичного инфекционного процесса);
• лимфогенный (реже).
Пиелонефрит развивается при достаточно вирулентной и массивной инфекции, способной преодолеть порог сопротивляемости организма. Особенно часто пиелонефрит у детей вызывают грамотри-цательные бактерии семейства Enterobacteriaceae, первое место среди которых принадлежит Escherichia, выделяемой из мочи 75-90% больных. Патогенные свойства кишечной палочки обусловлены в основном свойствами липополисахарида, а также продуцированием гемолизинов, резистентностью к действию колицинов и способностью внедряться в эпителий мочевого тракта.
Нередко возбудителем пиелонефрита у детей служат стафилококки, зачастую обусловливая тяжёлое течение процесса, особенно в грудном и раннем детском возрасте. В последние годы наметилась определённая тенденция к увеличению удельного веса этого возбудителя в общей структуре уропатогенов. Кроме того, исследования свидетельствуют о большей роли стафилококков в развитии вторичного пиелонефрита по сравнению с первичным.
Видное место среди возбудителей пиелонефрита принадлежит бактериям рода Proteus, выявляемым в моче 8-24% больных. Установлена высокая чувствительность почечной ткани к этому микроорганизму, кроме того, протей способствует камнеобразованию в мочевых путях.
Реже пиелонефрит вызывают клебсиеллы и синегнойная палочка, обладающие высокой устойчивостью к различным антибиотикам; как правило, заболевание у детей протекает тяжело. К ещё более редким возбудителям пиелонефрита у детей принадлежат микоплаз-мы, а также атипичные формы бактерий - протопласты и L-формы, которые чаще всего обусловливают малосимптомное, латентное, субклиническое течение заболевания в детском возрасте.
У некоторых больных пиелонефритом (преимущественно при его хроническом течении) бактериологическое исследование мочи обнаруживает смешанную бактериальную микрофлору, чаще кишечную палочку в ассоциации с другими видами энтеробактерий или кокками. Вообще, для обструктивного пиелонефрита характерен интермиттирующий или даже циклический рост уропатогенной микрофлоры, когда при определённых условиях среды (например, при лечении антибиотиками) "голову поднимают" то одни, то другие микроорганизмы. Сегодня типичен неуклонный рост устойчивости возбудителей пиелонефрита к большинству применяемых антибиотиков, что создаёт дополнительные трудности в лечении больных.
Таким образом, пиелонефрит - полиэтиологическое инфекционно-воспалительное заболевание. Однако инфекционный процесс как основу пиелонефрита необходимо рассматривать с позиций взаимоотношений микроорганизм-хозяин, зависящих от видовых особенностей возбудителей заболевания и индивидуальной реактивности организма, прежде всего от его иммунологической реактивности.
Необходимо отметить, что долгое время роли иммунного фактора в развитии пиелонефрита не придавали должного значения и заболевание рассматривали как местный инфекционно-воспалительный процесс. Мнение о важной роли иммунных нарушений и иммунопатологических реакций в возникновении и развитии пиелонефрита утвердилось далеко не сразу. С учётом незрелости иммунной системы и несовершенства многих её функций в детском возрасте иммунные механизмы в патогенезе пиелонефрита у детей приобретают особую значимость. Следует подчеркнуть, что вторичный хронический обструктивный пиелонефрит у детей с врождёнными обструктивны-ми уропатиями возникает на фоне развившейся иммунологической перестройки организма вследствие нарушения дифференцировки ткани почки и мочеточника.
Литературные данные свидетельствуют о низком уровне местной иммунной защиты в мозговом веществе почки больных пиелонефритом, получившем образное название иммунологической пустыни. Дело в том, что в мозговом веществе почки инактивируются фракции комплемента, в частности фракция С4, подавляется мобилизация лейкоцитов, отмечается неэффективный (незавершённый) фагоцитоз бактерий и угнетение бластной трансформации лейкоцитов, приводящие к быстрому проникновению и пролиферации микроорганизмов в интерстиций. При пиелонефрите повышена экскреция иммуноглобулинов с мочой, в первую очередь секреторной фракции IgA. Содержание секреторного IgA в моче коррелирует с тяжестью течения и активностью пиелонефрита. При тяжёлом течении заболевания наблюдается также выделение с мочой IgM, обладающего большим молекулярным весом и проникающего в мочу из крови только при выраженном инфекционно-воспалительном процессе. По некоторым сведениям, IgA в моче детей до 5 лет часто отсутствует, а созревание местного иммунного ответа служит одним из решающих факторов прекращения рецидивов пиелонефрита у детей более старшего возраста.
Несмотря на некоторую неоднородность литературных сведений, при исследовании иммунитета у этой категории больных получены
убедительные данные о важной роли иммунологических механизмов в генезе пиелонефрита. Для картины иммунологических нарушений у детей с обструктивным пиелонефритом характерно:
• снижение числа Т-лимфоцитов, Т-хелперов (иногда и Т-супрес-соров);
• превышение нормального количества В-лимфоцитов;
• чрезмерное повышение концентрации IgG (а зачастую также IgA и IgM);
• повышение концентрации циркулирующих иммунных комплексов;
• резкое снижение показателей фагоцитоза;
• существенное (в разы и десятки раз) повышение концентраций провоспалительных цитокинов;
• практическое отсутствие в крови интерферона α.
Клиническая картина и диагностика
Для клинической картины пиелонефрита типична фебрильная температура тела больных, всегда выражены и другие симптомы интоксикации (такие как слабость, утомляемость, тошнота и рвота рефлекторного характера), может отмечаться пастозность век и голеней. Дети жалуются на боли в поясничной области, у них возможны эритроцитурия, лейкоцитурия, протеинурия (альбуминурия), определяется нейтрофильный лейкоцитоз со сдвигом лейкоцитарной формулы влево, СОЭ возрастает до 20 мм в час и более, положителен С-реактивный белок, снижаются показатели концентрационной способности почек, характерна гипостенурия и бактериурия. Эти сведения врач получает при полном комплексном обследовании урологического больного, включающем:
• общий анализ крови;
• общий анализ мочи;
• анализ мочи по Зимницкому;
• анализ мочи по Нечипоренко;
• биохимический анализ крови (определение содержания общего белка и белковых фракций, активности АЛТ, АСТ, концентрации мочевины, креатинина, билирубина, глюкозы и электролитов);
• определение минутного диуреза, клубочковой фильтрации, канальцевой реабсорбции;
• анализ мочи на бактериурию;
• бактериологическое исследование мочи с учётом чувствительности микрофлоры к антибиотикам.
В качестве дополнительных методов диагностики показаны:
• УЗИ;
• экскреторная урография;
• микционная уретроцистография;
• уретроцистоскопия;
• регроградная пиелография (по показаниям);
• допплерография (по показаниям).
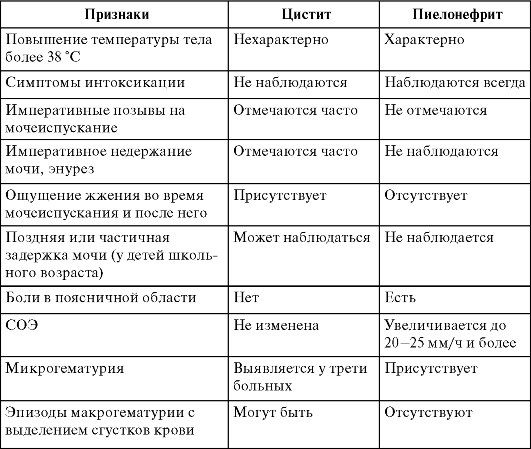
Дифференциальную диагностику пиелонефрита проводят с целым спектром воспалительных заболеваний, из которых наибольшее значение имеют цистит и гломерулонефрит (табл. 3, 4).
Таблица 3. Дифференциально-диагностические критерии цистита и пиелонефрита у детей
Окончание табл. 3
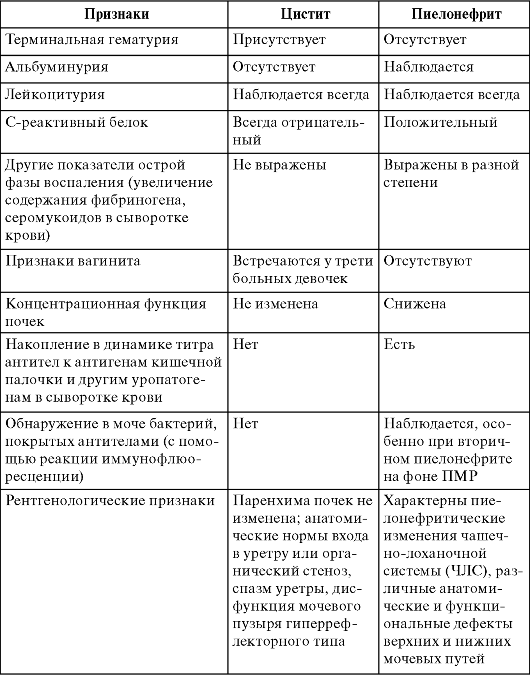
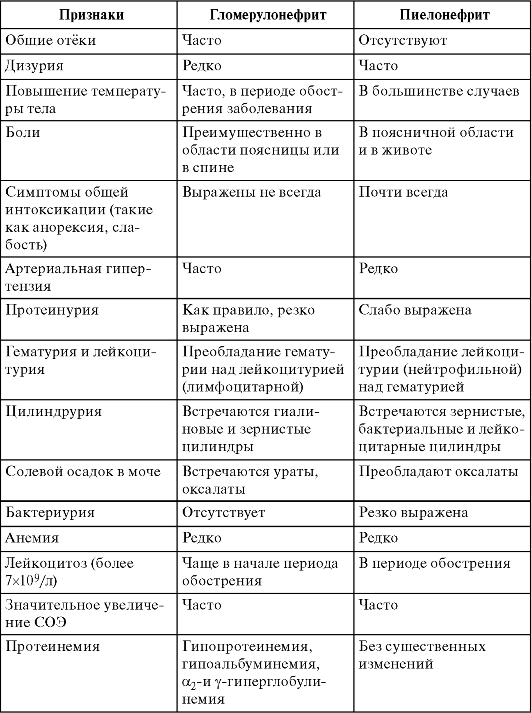
Таблица 4. Дифференциально-диагностические критерии гломерулонефрита и пиелонефрита
Лечение
После оперативной коррекции врождённых обструктивных уропа-тий приступают к лечению обструктивного пиелонефрита. Согласно современному национальному протоколу лечения пиелонефритов у детей (Коровина Н.А., 2007) терапия данного состояния включает:
• диету с небольшим ограничением белка и поваренной соли, исключением из рациона острых, солёных и аллергизирующих блюд;
• приём щелочной минеральной воды в течение 2 недель;
• дезинтоксикационную терапию;
• антибактериальную терапию (сначала - антибиотики с учётом чувствительности возбудителей, затем - уросептики, потом - растительные диуретики);
• десенсибилизирующую терапию;
• мембраностабилизирующую терапию;
• применение стимуляторов энергетического обмена.
Выраженные стабильные изменения показателей иммунологической реактивности при пиелонефрите позволили рекомендовать медикаментозную коррекцию этих нарушений (имунофан*, курсы лечения которым можно проводить 2 раза в год). В последние годы появились сведения о высокой эффективности магнитоинфракрас-ной лазерной терапии (МИЛТ), что связано с её противовоспалительным, противоотёчным, анальгезирующим, антибактериальным, мембраностабилизирующим и иммуномодулирующим действием, улучшением крово- и лимфообращения и стимулированием репа-ративных процессов. У детей с обструктивным пиелонефритом курс МИЛТ состоит из 10 сеансов, проводимых ежедневно 1 раз в день.
9.2. "ГНОЙНАЯ ПОЧКА"
Помимо вышеописанного пиелонефрита в клинической практике у детей встречаются и другие, более злокачественные формы гнойного поражения почек. У взрослых больных они чаще развиваются на фоне мочекаменной болезни (МКБ), у детей это первичные пиелонефриты, но у большинства пациентов пиелонефрит манифестирует на фоне других местных гнойно-воспалительных заболеваний (чаще кожи и подкожной жировой клетчатки), либо такие заболевания у них встречались в недавнем анамнезе (до 2 мес).
Клиническая картина и диагностика
Дети с этими гнойными осложнениями поступают в стационар с клиническими проявлениями острого пиелонефрита, но характерно, что они на протяжении многих дней (несмотря на лечение) высоко лихорадят (около 40 °С), быстро обезвоживаются, у них нарастают одышка и тахикардия, резко выражены другие симптомы интоксикации. Кроме того, у больных данной категории выявляются симптомы, свидетельствующие о переходе серозного пиелонефрита в гнойный:
• лейкоцитурия или пиурия;
• лейкоцитоз >16х109/л;
• сдвиг лейкоцитарной формулы влево: >12 палочкоядерных ней-трофилов;
• разница в сравнительном лейкоцитозе (капли крови из поясничных областей);
• уровень среднемолекулярных олигопептидов в крови повышен более чем в 2-3 раза;
• лейкоцитарный индекс интоксикации повышен более чем в 10 раз;
• косвенные признаки при экскреторной урографии (отсутствие тени большой поясничной мышцы (m. psoas major), увеличенная почка, отсутствие функции почки, "большая белая почка", деформация почки и ЧЛС, неподвижность почки при дыхательной экскурсии - полиграмма);
• анэхогенные зоны при УЗИ;
• резко положительный симптом поколачивания.
В клинической практике встречаются разные формы "гнойной почки", перечисленные в порядке уменьшения распространённости:
• гнойный пиелонефрит;
• апостематозный нефрит - сформировавшиеся под капсулой гнойнички коры почки;
• карбункул почки - некротическое воспаление коркового и в меньшей степени мозгового слоя почки в стадии инфильтрации;
• абсцесс почки (развивается при абсцессе карбункула, при УЗИ заметна чёткая гипоэхогенная зона, иногда видна капсула абсцесса);
• пионефроз - полостное гнойное образование, занимающее всю почку (такая почка не функционирует, при УЗИ почка выглядит как единая полость, внутри которой находится гипоэхогенная взвесь);
• паранефрит - гнойное поражение паранефральной клетчатки.
Лечение
При апостематозном пиелонефрите необходимо интенсивное лечение. До 10 дней возможна консервативная терапия, в остальных случаях детей с апостематозным нефритом и с более выраженными формами гнойного поражения почек оперируют. При апостематозном нефрите выполняют декапсуляцию почки, при карбункуле (абсцессе) почки - декапсуляцию + воронкообразное иссечение гнойника, при паранефрите показано вскрытие и дренирование паранефральной клетчатки, при пионефрозе - нефрэктомия.
9.3. ЦИСТИТ
Циститом называют инфекционно-воспалительное поражение слизистого и подслизистого слоя мочевого пузыря. Заболевание встречается у детей любого возраста и пола, но главным образом у девочек (в 3 раза чаще, чем у мальчиков) в возрасте от 4 до 12 лет. Этому способствуют прежде всего анатомические особенности женской уретры: она более короткая, более прямая, более широкая и открывается ближе к анусу, чем мужская, что создаёт благоприятные условия для распространения микрофлоры кишечника в просвет мочеиспускательного канала. Однако это только одна сторона медали.
Нельзя не учитывать и эндокринных особенностей растущего женского организма. Новорождённая девочка получает достаточное количество эстрогенов от матери трансплацентарно, что ведёт к мно-гослойности эпителия влагалища (до 30-40 слоёв), под ним клетки созревают и ороговевают, а также накапливается гликоген, необходимый палочкам Додерляйна для питания. Эти важные микроорганизмы обнаруживаются во влагалище уже в первые сутки после рождения. Перерабатывая гликоген в молочную кислоту, палочки Додерляйна закисляют среду влагалища, препятствуя появлению там патогенных микроорганизмов. Однако к месячному возрасту материнские эстрогены заканчиваются, до препубертатного периода влагалищный эпителий истончается, и реакция среды становится щелочной (кроме прочего, это ведёт к снижению калибра дис-тальной уретры - функциональная инфравезикальная обструкция). Поскольку местный иммунитет недостаточен, то в этом возрасте у девочек (особенно упитанных) нередки вульвиты и вульвовагиниты, которые зачастую становятся источниками инфицирования нижних мочевых путей.
Итак, инфекция может проникать в мочевой пузырь восходящим путём из аногенитальной области. Среди факторов, способствующих воспалению мочевого пузыря, наиболее существенна способность бактерий к адгезии с уроэпителиальными клетками и их последующее инфицирование, а также нарушение нормальной уродинамики нижних мочевых путей. Обычно возбудителями циститов служат эшерихии, стафилококки и протей.
В зависимости от характера и глубины морфологических изменений выделяют следующие формы острого цистита:
• катаральный;
• геморрагический;
• грануляционный;
• фибринозный;
• язвенный;
• флегмонозный;
• гангренозный.
Соответственно, различают несколько форм хронического цистита (Люлько А.В., 1988):
• катаральный;
• язвенный;
• полипозный;
• кистозный;
• инкрустирующий;
• некротический.
Клиническая картина
Клиническая картина цистита достаточно характерна. У детей часто отмечаются поллакиурия, боли внизу живота с иррадиацией на промежность, императивные позывы на мочеиспускание и императивное недержание мочи, энурез. Однако для них нетипично повышение температуры тела выше 38 °С и другие симптомы интоксикации. Показатели острой фазы у них также не изменены (нормальные СОЭ, уровень фибриногена и серомукоидов, всегда отрицательный С-реактивный белок). Дети могут жаловаться на чувство жжения во время мочеиспускания и после него, у детей школьного возраста нередка задержка мочи. Возможны эпизоды макрогематурии, всегда отмечается лейкоцитурия, у 40% детей - бактериурия, у трети больных девочек присутствуют признаки вагинита.
Диагностика
Достоверных рентгенологических признаков цистита нет, при остром цистите выполнять цистоскопию нельзя, ограничиваются УЗИ почек и мочевого пузыря. При хроническом цистите диагноз верифицируют по данным цистоскопии: определяют форму заболевания, локализацию наибольших изменений, состояние шейки мочевого пузыря и устьев мочеточников. Выполняют бактериологическое исследование мочи, анализ мочи на бактериурию, при латентных формах - анализ мочи по Нечипоренко. При хронических циститах, кроме того, показана микционная цистография. Результаты обследования определяют тактику лечения больных.
Лечение
Лечение цистита включает назначение антибиотиков: как правило, цефалоспоринов II-III поколений (при остром цистите - не более 7 дней) и/или уросептиков (нитрофурановых препаратов, производных налидиксовой кислоты, фуразидина по 7-8 мг/кг в сутки на 4 приёма). При хроническом цистите применяют инстилляции мочевого пузыря антисептиками, а лучше - препаратами, обладающими не только антибактериальным, но и иммуномодулирующим действием (гигаинp, томицид♠). Применяют растительные диуретики, а в последние годы с успехом - препарат канефрон Н*. Показана общеукрепляющая терапия, электрофорез с антибиотиками и тепловые процедуры на область проекции мочевого пузыря, а также инт-раорганная низкоинтенсивная гелий-неоновая лазерная терапия.
9.4. БАЛАНОПОСТИТ
Баланопостит - острое инфекционное воспаление мягких тканей крайней плоти и головки полового члена. У детей встречается серозная или гнойная форма заболевания.
Клиническая картина
Клиническая картина баланопостита весьма специфична: выражены отёк и гиперемия крайней плоти и головки полового члена, характерны жалобы на боли в момент мочеиспускания, возможно выделение гноя из препуциального мешка. Общие воспалительные проявления редки.
Лечение
Если отёк крайней плоти не создаёт препятствий для оттока мочи, то лечение заболевания консервативное. Наружно назначают мази с антибиотиками; тёплые ванночки с растворами нитрофура-ла - фурацилина* и перманганата калия, которые лучше чередовать, каждую по 2 раза в день. Рекомендуют закладывать в препуциальный мешок мазь, содержащую антибиотики (1 раз в сутки на ночь), но обязательно ненасильственно, только при возможности свободного открытия головки полового члена.
Запущенные формы гнойного баланопостита чреваты острой задержкой мочи и/или развитием парафимоза - сдавлением головки полового члена по венечной борозде напряжённой, отёчной тканью крайней плоти. В таких случаях лечебная тактика хирургическая. Ребёнка госпитализируют в хирургический стационар. Чтобы не допустить некроза головки полового члена, нужно рассечь ущемляющее кольцо под аппаратно-масочным наркозом. Оправданны антибиотикотерапия и физиолечение.