Акушерство. Курс лекций: учебное пособие Под ред. А.Н. Стрижакова, А.И. Давыдова. 2009. - 456 с.
|
|
|
|
ЛЕКЦИЯ 10 ВНУТРИУТРОБНЫЕ ИНФЕКЦИИ
Традиционно в отечественной литературе под термином «внутриутробные инфекции» (ВУИ) понимают заболевания, при которых заражение происходит в пренатальном периоде или во время родов и источником является мать. Следует отметить, что внутриутробное заражение ребенка от матери происходит значительно чаще, чем развиваются клинические признаки заболевания. Для обозначения факта внутриутробного заражения в практической медицине используют термин «внутриутробное инфицирование». Термин «внутриутробная инфекция» обычно используется для обозначения клинических проявлений инфекционной болезни плода и новорожденного, выявляемой пренатально или вскоре после рождения.
Частота внутриутробного инфицирования. Согласно обобщенным литературным данным, не менее 10% новорожденных внутриутробно инфицируются различными вирусами и микроорганизмами. Риск внутриутробного инфицирования зависит от типа возбудителя, исходного состояния здоровья беременной женщины и плода, а также от эпидемиологической ситуации в конкретном географическом регионе. Более высокая частота наблюдается при первичном инфицировании беременной женщины, чем при латентной или вторичной вирусной инфекции.
Внутриутробные инфекции являются значимой причиной репродуктивных потерь. Так, частота ранней неонатальной заболеваемости и смертности при ВУИ колеблется от 5,3 до 27,4%, а мертворождаемость достигает 16,8%. В структуре перинатальной смертности на долю инфекции приходится 10,1%. Еще более значительную роль инфекционно-воспалительные заболевания играют в структуре перинатальной заболеваемости, где на их долю приходится 20-38%.
Вместе с тем истинная частота перинатальной патологии, обусловленной инфекционным фактором, остается неуточненной, что обусловлено отсутствием скрининговых исследований, несовпадением частоты инфицированности и непосредственной заболеваемости, частым латентным течением патологического процесса, объективной сложностью антенатальной лабораторной диагностики. В резуль-
тате значительная часть инфекций остается нераспознанной и при статистическом анализе учитывается как следствие осложнений родового акта, внутриутробной асфиксии, синдрома респираторных расстройств и других патологических состояний.
В 95,8% причинами смерти в связи с инфекционным процессом являются состояния, возникающие в перинатальном периоде. Из них наиболее часто отмечают: врожденные пневмонии 47,5%, инфекции, специфичные для перинатального периода 41,6%, и сепсис новорожденных 6,7%.
Этиология. Перечень безусловных возбудителей достаточно обширен и включает в себя десятки видов практически всех классов организмов от вирусов до простейших и грибов.
Доля рождения детей с признаками бактериальных внутриутробных инфекций составляет 20-36%. В настоящее время доказана роль широкого спектра аэробных и анаэробных бактериальных агентов, в первую очередь представителей условно-патогенной микрофлоры: стафилококков, стрептококков, кишечной палочки, клебсиеллы, протея, энтеробактерий, а также неспорообразующих анаэробных микроорганизмов. Следует отметить, что в данной группе пациенток обычно выявляются значительные нарушения в составе микробиоценоза влагалища (у 60-65% обнаруживается кандидозный вульвовагинит или бактериа льный вагиноз).
Классическим примером бактериальной ВУИ является листериоз, возбудителем которого является Listeria monocytogenes - короткие грамположительные палочки (коккобациллы). Среди других бактериальных возбудителей внутриутробной инфекции в последние годы возросла роль стрептококков группы В. Значение их в патологии плода, особенно новорожденных, заметно увеличилось на фоне широкого внедрения в практику антибиотиков аминогликозидов, к которым данные микроорганизмы обладают природной устойчивостью. В настоящее время установлена тесная связь частоты инфекций, вызванных стрептококками группы В у новорожденных, с частотой носительства этих бактерий в половых путях у матерей. Частота выявления носительства стрептококков группы В у беременных колеблется в широких пределах - от 1,5 до 30%. Наиболее опасен массивный очаг (более 105 КОЕ/мл) в цервикальном канале матери. В таких случаях более 60% новорожденных рождаются инфицированными. Клинические проявления инфекций, вызванных у новорожденных этими бактериями, разнообразны - от локальных кожных
до тяжелых молниеносных септических процессов и менингитов, сопровождающихся высокой летальностью (до 80%) у недоношенных новорожденных.
В последние годы в структуре перинатальной патологии возросло значение ссуально-трансмиссивных внутриклеточных инфекционных агентов: микоплазм, уреаплазм и хламидий. Частота внутриутробного инфицирования при генитальном уреа- и микоплазмозе у беременной составляет 40-50%, а при хламидиозе достигает 70,8%.
Значительная часть перинатальных инфекций вызывается различными вирусами, среди которых наиболее важное значение имеют вирусы цитомегалии, простого герпеса, краснухи, энтеровирусы (ECHO, Коксаки), гепатита В, вирус иммунодефицита человека. Кроме того, на увеличение репродуктивных потерь и заболеваемость новорожденных оказывают влияние вирусы гриппа, кори, полиомиелита, папилома- и парвовирус.
В последние годы отмечается рост числа больных с локальными формами герпетических поражений, который определяет тенденцию к увеличению частоты герпетической инфекции новорожденных. Поражение вирусом гениталий выявляется у 7% беременных. Герпес - пример классической хронически протекающей инфекции с пожизненным существованием возбудителя в организме хозяина. Выделено около 70 видов вирусов данной группы, из которых 4 поражают людей: вирус простого герпеса I и II серотипов, вирус варицеллы-зостер, вирус Эпштейна-Барр и цитомегаловирус (клиническое значение имеют все три выделенных штамма - Devis, Kerr и AD189).
Достаточно распространенными в популяции являются и энтеровирусные инфекции. В качестве возбудителей внутриутробных инфекций наибольший интерес представляют эховирусы и вирусы Коксаки. В эксперименте было доказано этиологическое значение вирусов Коксаки типов А13, А3, А6, А7, В4 и В3, а также эховирусов 9 и 11 типов.
Особого внимания заслуживают ретровирусы, вызывающие СПИД. До 50% детей, рожденных от инфицированных ВИЧ матерей, заражаются антенатально, интранатально или в раннем неонатальном периоде. Частота заболевания новорожденных от серопозитивных матерей колеблется в широких пределах - от 7,9 до 40%.
Наибольшее значение среди грибковых возбудителей ВУИ имеют широко распространенные представители грибов рода Candida. Криптококкоз, кокциоидоз, аспергиллез и гистоплазмоз у беремен-
ных чаще возникают на фоне иммунодефицита. Обращает на себя внимание факт резкого возрастания частоты клинических проявлений влагалищного кандидоза во время беременности, которая к III триместру достигает 31-33%. Данный феномен связывают с нарушением усвоения гликогена клетками влагалищного эпителия, а также с усилением образования муцина, предопределяющего за счет эффекта «разведения» снижение концентрации активных факторов местного иммунитета в вагинальном срете - лизоцима, катионных белков, среторных антител и др. Избыток питательных веществ в виде гликогена в сочетании с ослаблением местного иммунитета создают благоприятные условия для реализации патогенного эффекта грибковой флоры. По данным ДНК диагностики, при родах через естественные родовые пути контаминация новорожденных от матерей больных кандидозом приближается к 100% и к завершению неонатального периода спонтанная элиминация грибов наблюдается только в 35% процентах, что позволяет предположить формирование у остальных кандидоносительства. Частота клинически выраженного кандидоза у новорожденных в первые 35 дней приближается к 20-30%, и, несмотря на лечение, через 1 мес он отмечается в каждом пятом наблюдении. Грибковая инфекция не только вызывает оральные, генитальные и кожные проявления кандидоза у новорожденных, но и может приводить к внутриутробному инфицированию плода с формированием системного микоза с глубоким поражением легких, мозга, а также к самопроизвольному прерыванию беременности (чаще во II триместре, в сроки 14-25 нед).
Наконец, перинатальные инфекции вызываются простейшими, трепонемами и риккетсиями. В этой группе наиболее важное значение имеет токсоплазмоз, частота внутриутробного инфицирования при котором составляет около 40%. Кроме того, в последние годы отмечена тенденция возрастания частоты сифилиса. Врожденный сифилис отмечается более чем у 50% новорожденных от больных матерей, которые не получали соответствующего лечения.
Важно отметить, что в большинстве наблюдений внутриутробное инфицирование обусловлено ассоциацией нескольких возбудителей или носит смешанный (вирусно-бактериальный, бактериально-грибковый характеры). В структуре антенатальной смертности вследствие внутриутробной инфекции 27,2% приходится на вирусную инфекцию, 26,3% - на смешанную и 17,5% - на бактериальную.
В 1971 г. была выделена группа инфекций, имеющих, несмотря на выраженные различия в структуре и биологических свойствах возбудителей, сходные клинические проявления и вызывающих у плода стойкие структурные дефекты различных систем органов, наиболее важными из которых являются поражения центральной нервной системы. Для обозначения этой инфекционной группы A.J. Nahmias (1971) была предложена аббревиатура TORCH. Данный комплекс объединяет следующие внутриутробные инфекции: T - токсоплазмоз, R - рубелла (краснуха), C - цитомегаловирусная инфекция, H - герпесвирусная инфекция.
В последние 15 лет наблюдается изменение этиологической структуры перинатальных инфекций. Отчасти это обусловлено расширением возможностей специфической диагностики, в первую очередь микоплазмоза, хламидиоза, цитомегалии, герпетической и стрептококковой В-инфекции и др. Имеет место и истинная смена возбудителей, в частности реже стали встречаться листерии (Айлама-
зян Э.К., 1995).
Несмотря на широкий спектр возбудителей, нельзя не отметить того, что все внутриутробные инфекции имеют общие черты:
• латентное, или стертое, течение, что существенно затрудняет диагностику (особенно при внутриклеточной локализации возбудителя - хламидии, микоплазмы, вирусы и др.) и не позволяет своевременно начать этиотропную терапию;
• активация латентно персистирующей инфекции возможна при любом нарушении гомеостаза у беременной (анемия, гиповитаминоз, переутомление, стрессовые ситуации, декомпенсация экстрагенитального заболевания неинфекционной природы).
ПУТИ ВНУТРИУТРОБНОГО ИНФИЦИРОВАНИЯ И МЕХАНИЗМ ЗАРАЖЕНИЯ ПЛОДА
Внутриутробное инфицирование происходит следующими путями: 'восходящим - при наличии специфического поражения нижних
отделов полового тракта (рис. 34); 'гематогенным (трансплацентарным) - в большинстве случаев обусловлен способностью некоторых микроорганизмов длительно персистировать в лимфоцитах периферической крови;
• трансдецидуальным (трансмуральным) - при наличии инфекции в эндометрии;
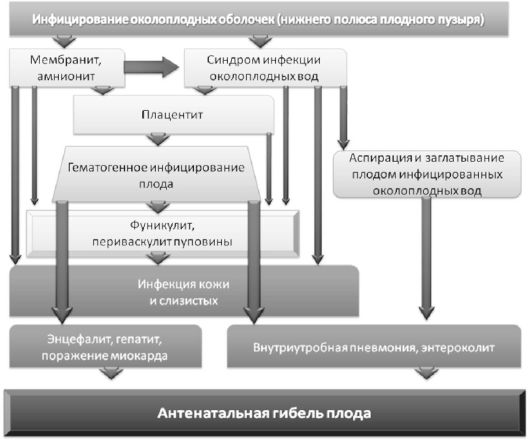 Рис. 34. Патогенез восходящей внутриутробной инфекции
Рис. 34. Патогенез восходящей внутриутробной инфекции
• нисходящим - при локализации воспалительного очага в области придатков матки;
*контагиозным - прямая контаминация новорожденного при прохождении через родовой канал;
• смешанным.
Бактериальная внутриутробная инфекция условно-патогенными микроорганизмами развивается в основном вследствие восходящей инфекции из родовых путей. Этот путь также характерен для микоплазм, хламидий, грибов рода Candida и лишь отдельных вирусов, в частности простого герпеса. Предрасполагающими факторами являются урогенитальные инфекции, истмико-цервикальная недостаточность, частичный разрыв плодных оболочек, несвоевременное излитие вод, биопсия хориона, амниоцентез.
Восходящее инфицирование быстрее всего происходит при повреждении плодных оболочек. Околоплодные воды женщины в поздние сроки беременности обладают антимикробной активностью, которая, однако, выражена слабо и может только задерживать (но
не подавлять) рост микроорганизмов. Бактериостатический эффект весьма непродолжителен (от 3 до 12 ч). Воспалительные изменения в участке оболочек, прилегающем к цервикальному каналу, всегда обнаруживаются раньше, чем в ворсинах плаценты. Из-за низкой вирулентности большинства условно-патогенных микроорганизмов плодные оболочки остаются внешне не поврежденными. В тоже время оболочки оказываются проницаемы для многих условно-патогенных микроорганизмов, поэтому заражение плода может происходить и при целом плодном пузыре. Возбудитель проникает в околоплодные воды, происходит его интенсивное размножение и накопление. Формируется очаг инфекции, и плод оказывается в инфицированной среде. Развивается так называемый синдром инфекции околоплодных вод.
Заражение плода происходит при заглатывании и аспирации им инфицированных вод, что ведет к появлению у новорожденного признаков внутриутробной инфекции (пневмония, энтероколит, везикулез, омфалит, конъюнктивит и др.). Одновременно микроорганизмы, распространяясь по оболочкам или между ними, достигают базальной пластины плаценты (децидуит). Хориальная пластина и элементы пупочного канатика инфицируются при контакте с зараженными околоплодными водами. Дальнейшее распространение воспалительной реакции приводит к развитию хорионита (плацентита), который проявляется лейкоцитарной инфильтрацией интервиллезного пространства и эндоваскулитами в хориальной пластинке. Васкулиты в децидуальной оболочке, стволовых и терминальных ворсинах ведут к облитерации сосудов, появлению инфарктов, кальцинатов, массивных отложений фибриноида, что может проявляться как «преждевременное созревание плаценты».
К проявлениям синдрома «инфекции околоплодных вод», кроме хорионамнионита, относится многоводие, которое может быть выявлено у 5,5-63,6% пациенток уже в конце I триместра беременности. Причиной его развития является изменение соотношения процессов продукции и резорбции околоплодных вод клетками амниотического эпителия на фоне амнионита. Маловодие при внутриутробном инфицировании обычно носит вторичный характер и является проявлением поражения почек (снижение диуреза при плацентарной недостаточности) или мочевыводящих путей плода (обструктивный гидронефроз).
Формирование плацентарной недостаточности. В генезе симптомокомплекса плацентарной недостаточности при ВУИ основная роль принадлежит сосудистым расстройствам (васкулиты и тромбоз сосудов плодовой части плаценты на фоне хорионита (плацентита). Немаловажное значение имеет и изменение морфофункционального состояния клеточных мембран вследствие активации процессов перекисного окисления липидов на фоне плацентита. Основными проявлениями плацентарной недостаточности являются хроническая гипоксия плода и задержка его внутриутробного роста, которая в зависимости от сроков инфицирования носит симметричный (инфицирование до завершения плацентации) или асимметричный характер.
Типичным проявлением внутриутробного инфицирования является невынашивание беременности. В 70% наблюдений самопроизвольное прерывание беременности в поздние сроки и преждевременные роды начинаются с преждевременного разрыва плодных
оболочек и только в 30% - с повышения сократительной активности матки. Преждевременное развитие родовой деятельности и несвоевременный разрыв плодных оболочек обусловлены действием бактериальных фосфолипаз, запускающих простагландиновый каскад, и повреждающим действием воспалительных токсинов на плодные оболочки.
В связи с тем, что фосфолипазы грамотрицательных бактерий способствуют разрушению сурфактанта в легких плода, у новорожденного развиваются респираторные расстройства. Таким образом, выстраиваетсяследующаяпоследовательностьразвитиявосходящего инфицирования: кольпит, цервицит - инфицирование околоплодных вод - поражение эпителия околоплодного пространства - мембранит - амнионит хориальной пластинки - периваскулит пуповины - поражение дыхательных путей, легких, пищеварительного тракта и кожи - антенатальная гибель плода.
При микробиологическом обследовании женщин групп повышенного риска развития ВУИ бактериальной этиологии установлена идентичность видового состава микрофлоры мочеполовых путей женщин и микроорганизмов, выделенных у рожденных ими детей. У новорожденных с клиническими проявлениями ВУИ отмечается массивное обсеменение главным образом внутренних полостей (содержимое желудка, носоглоточные мазки). Посевы мазков с материнской поверхности плаценты и пуповинной крови чаще всего оста-
ются стерильными, а околоплодные воды и плодовая поверхность плаценты имеют наивысший показатель микробной колонизации. Это доказывает преимущественно восходящий путь инфицирования плода и ведущую роль околоплодных вод в заражении плода.
Для гематогенного инфицирования плода наиболее характерно наличие очага в организме матери, расположенного экстрагенитально. Возбудитель, нарушая плацентарный барьер, проникает в кровоток плода. При гематогенном инфицировании нередко возникает генерализованное поражение организма плода - внутриутробный сепсис. Трансплацентарный путь инфицирования имеют все истинные врожденные вирусные инфекции, микоплазмоз, хламидиоз а также такие специфические внутриутробные инфекции, как листериоз, сифилис и токсоплазмоз.
Для гематогенного пути характерно преобладание васкулитов плацентарного ложа матки, затем - развитие интервиллузита, васкулитов хориальной пластинки, далее - флебита и эндартериита пуповины, инфицирование печени, мозга, поражение других органов плода - антенатальная гибель.
Классический вариант гематогенной передачи инфекции плоду из кровеносного русла матери, характерный для истинно-патогенных возбудителей (как вирусной, так и бактериальной или паразитарной флор) при инфекциях, вызванных условно-патогенными микроорганизмами, встречается в наиболее тяжелых случаях и имеет вторичный характер. Этот путь возможен при генерализованной инфекции с массивной бактериемией, когда в результате деструкции ворсин хориона происходит нарушение барьерной функции плаценты.
Для реализации трансдецидуального (трансмурального) пути инфицирования необходимо наличие очага инфекции под эндометрием. Подобный путь инфицирования плода чаще всего имеет место у пациенток, перенесших гнойно-воспалительные заболевания половых органов.
С нисходящим путем внутриутробного инфицирования, при котором проникновение возбудителя к плодному яйцу происходит через маточные трубы, в клинической практике приходится сталкиваться у пациенток с острой хирургической патологией органов брюшной полости, острым или хроническим сальпингоофоритом гонорейной, микоплазменной или хламидийной этиологии. Классическим примером является острый аппендицит, при этом механизм поражения плода напоминает таковой при восходящем инфицировании.
ИММУННАЯ СИСТЕМА ПЛОДА
Зрелый иммунный ответ включает сложную последовательность взаимодействий между несколькими типами клеток. Процесс созревания индивидуальных клеток, участвующих в иммунном ответе, начинается на ранних этапах жизни плода. Клетки-предшественники иммунной системы человека образуются в костном мозге и печени плода. Характерные для Т- и В-лимфоцитов маркеры и антигены гистосовместимости могут быть выявлены на лимфоцитах уже на 8-10 нед беременности. По мере созревания клеток иммунной системы на макрофагах, а также на Т- и В-лимфоцитах появляется все большее число рецепторов и маркеров гистосовместимости, однако полное созревание завершается лишь примерно через 2 года после рождения.
В типичных случаях можно наблюдать ответы на инфекционные агенты, которые проходят через плаценту уже во второй половине беременности. Такого рода иммунный ответ обычно проявляется в форме образования антител класса IgM, однако могут образовываться и антитела класса IgG. Выявление иммунного ответа плода в форме антител IgG является более трудной задачей в связи с наличием пассивных IgG антител матери.
Антитела класса IgG материнского организма начинают проходить через плаценту примерно в середине беременности. Во время родов концентрация IgG в крови у ребенка (в основном иммуноглобулины матери) равна соответствующей концентрации в крови матери или даже превышает ее. Это означает, что у ребенка присутствуют все антитела класса IgG, образованные в организме матери. Антитела класса IgA и IgM материнского организма не проходят через плаценту, и, если антитела этих классов обнаружены у ребенка, это означает, что они образовались в организме ребенка.
Образование антител класса IgA часто не устанавливается полностью к моменту родов. Было показано, что полное развитие этой системы может продолжаться в течение первых семи лет жизни. Таким образом, основным источником иммунитета у плода является перенос материнских IgG-антител через плаценту, хотя уже на достаточно ранних этапах развития его иммунная система способная вырабатывать собственную защиту.
Сложности в изучении и трактовке результатов исследования гуморального и клеточного иммунитета у матери и внутриутробного плода привели к поиску новых решений оценки иммунореактивности
на фоне инфекционного процесса во время беременности. Так, нами проведена оценка ряда про- и противовоспалительных цитокинов (интерферонов, интерлейкинов, фактора некроза опухоли) в различные сроки гестации у внутриутробного плода, матери и новорожденного. Так как цитокины и интерфероны являются универсальными регуляторами всех иммунных реакций, как клеточных, так и гуморальных, их исследование позволяет решить самую важную клиническую проблему - есть ли инфекция у плода и необходимо ли назначать лечение? Доказано, что снижение уровня интерлейки- на-4 в сочетании с увеличением концентрации гамма-интерферона и фактора некроза опухоли в крови матери свидетельствует о наличии внутриутробной инфекции в 86,4%. Подобные исследования позволяют неинвазивно оценивать риск реализации инфекции у новорожденного.
Патогенез. В патогенезе внутриутробного инфицирования плода существенная роль отводится непосредственному взаимодействию возбудителя и плода. Спектр повреждений, обнаруживаемых при внутриутробной инфекции, весьма широк и зависит от особенностей морфогенеза и ответных реакций плода в тот или иной период внутриутробного развития, специфических свойств и продолжительности действия повреждающего фактора.
Связь вирулентности возбудителя и тяжести поражения плода не всегда является прямо пропорциональной. Нередко стерто протекающая или легкая инфекции у матери, вызванная токсоплазмами, листериями, микоплазмами, хламидиями, вирусами или грибами рода Candida, может вести к гибели плода или рождению тяжелобольного ребенка. Данный факт обусловлен тропизмом возбудителей к определенным эмбриональным тканям, а также тем, что клетки плода, обладающие высокой метаболической активностью, представляют собой благоприятную среду для размножения микробов.
Повреждающее действие бактериального инфекционного агента может реализоваться через развитие деструктивного воспалительного процесса в различных органах с формированием структурного или функционального дефекта и путем прямого тератогенного действия с образованием стойких структурных изменений в виде пороков развития. Вирусные агенты обычно вызывают летальные нарушения или дефекты развития за счет подавления митотического деления клеток или при прямом цитотоксическом воздействии. Репарационные процессы, которые развиваются вслед за воспалени-
ем, нередко ведут к склерозированию и кальцификации тканей, что также нарушает процесс гистогенеза.
Период эмбриогенеза охватывает первые 3 мес беременности, причем наиболее чувствительной фазой к воздействию повреждающих факторов являются первые 3-6 нед органогенеза (критический период развития). Во время имплантации значительно повышается чувствительность к действию повреждающих факторов. Инфекционные эмбриопатии, возникающие в это время, характеризуются возникновением уродств (тератогенный эффект), реже наблюдается эмбриотоксическое действие. В первую очередь поражаются ткани, которые на момент действия агента находились в процессе активной дифференцировки. У различных органов периоды закладки не совпадают по времени, поэтому от длительности воздействия повреждающего агента будет зависеть множественность поражения.
С началом раннего фетального периода у плода появляется специфическая чувствительность к возбудителям внутриутробных инфекций. Поражения плода, возникающие в период после 13 нед, носят название «фетопатии». При фетопатиях септической этиологии возможно формирование пороков развития. Морфологической основой для этого служат альтеративные и пролиферативные процессы, приводящие к облитерации или сужению естественных каналов и отверстий. Подобные изменения ведут к нарушению дальнейшего развития уже сформированного органа. Так, инфекция мочевыводящих путей может привести к гидронефрозу, перенесенный менингоэнцефалит - к гидроцефалии на фоне сужения или облитерации сильвиева водопровода.
При инфицировании после 27 нед гестации плод приобретает способность специфически отвечать на внедрение возбудителя инфекции лейкоцитарной инфильтрацией, гуморальными и тканевыми изменениями. Поражающее действие инфекционного агента реализуется в данном случае в виде функциональных дефектов.
Следует отметить и то, что немаловажными звеньями патогенеза ВУИ являются интоксикация продуктами метаболизма инфекционного агента, гипертермия и гипоксемия. Влияние вышеуказанных факторов на внутриутробного плода проявляется задержкой роста и дифференцировки легких, почек и головного мозга, даже при отсутствии других проявлений внутриутробной инфекции.
Клинические признаки внутриутробного инфекционного заболевания у новорожденного или имеются уже при рождении, или прояв-
ляются в течение первых 3 сут жизни (чаще всего на 1-2-е сут). При инфицировании в постнатальном периоде симптомы инфекционного процесса выявляются в более поздние сроки. Возможен более длительный инкубационный период при внутриутробном заражении («поздние» менингиты, остеомиелит, хламидийные поражения и др.) или, напротив, ранние проявления госпитальной инфекции (особенно у недоношенных детей).
Наиболее частым клиническим проявлением бактериальной внутриутробной инфекции у новорожденных в первые дни жизни является так называемый синдром инфицированности. У такого ребенка выявляются общие клинические симптомы, отражающие признаки интоксикации и выражающиеся в общей вялости, снижении мышечного тонуса и рефлексов (в частности, рефлекса сосания), в срыгивании, отказе от груди. Со стороны сердечно-сосудистой системы - глухость тонов сердца, изменения на ЭКГ гипоксического характера. Наблюдаются бледность кожных покровов, нарушение ритма и частоты дыхания, приступы цианоза. Инфицированность может завершиться развитием септического процесса, в реализации которого имеет значение состояние новорожденного в первые часы жизни, и доза возбудителя. Недоношенность, нарушение дыхания и гемодинамики, внутричерепная травма, гипоксия способствуют снижению сопротивляемости организма новорожденного и являются тем благоприятным фоном, на котором инфекция становится выраженной, приобретая характер септического процесса.
Специфические проявления внутриутробных инфекций у новорожденных различны - от легких локальных форм до тяжелых септических.
Клинические проявления врожденного бактериального или микотического поражения кожи у новорожденного могут иметь характер везикулопустулеза. Процент положительных результатов микробиологического исследования содержимого везикул, взятого сразу после рождения ребенка, невысок, поэтому дискутабельным является вопрос о том, относить ли «асептический» везикулез к врожденной инфекции или рассматривать его как проявление бактериальной аллергии с появлением сыпи на коже. Истинный (микробиологически подтвержденный) везикулопустулез проявляется у инфицированных внутриутробно детей обычно к концу 1-х и на 2-е сут жизни, причем возбудителями чаще всего являются стрептокок-
ки групп В и D, эшерихии, дрожжеподобные грибы (Анкирская А.С. и соавт., 1989).
Конъюнктивит, ринит и отит, появившиеся на 1-3-и сут жизни, также могут быть проявлениями внутриутробной инфекции. При врожденном конъюнктивите, кроме микробиологического исследования отделяемого из глаз на условно-патогенные микроорганизмы, необходимо взять мазки для исследования на гонококк.
Внутриутробная пневмония - наиболее часто встречающаяся форма врожденных инфекций новорожденного. У детей с момента рождения наблюдаются признаки дыхательной недостаточности: одышка, цианоз, часто притупление перкуторного звука и мелкопузырчатые влажные хрипы. Рентгенологическое исследование, проведенное в первые часы жизни, подтверждает наличие очагов пневмонии. Врожденная аспирационная пневмония может проявиться и на 2-3-й день жизни. При микробиологическом исследовании аспирата из трахеобронхиальных путей у новорожденных с аспирационной пневмонией чаще всего выделяют грамотрицательные бактерии, тогда как при пневмониях новорожденных, носящих госпитальный характер, чаще всего выделяют золотистый стафилококк. Течение врожденной пневмонии тяжелое, поскольку в результате аспирации выключаются из дыхания обширные участки легкого (нижняя и средняя доли) вследствие обтурации бронхов аспирационными массами - инфицированными околоплодными водами, содержащими примесь мекония, чешуек кожи плода.
Энтероколит у новорожденных также может носить характер внутриутробной инфекции, когда происходит проникновение возбудителя вместе с околоплодными водами в желудочно-кишечный тракт. Для врожденного энтероколита характерны следующие клинические проявления: вялое сосание, срыгивание, вздутие кишечника, увеличение печени и селезенки, расширение венозной сети передней брюшной стенки, частый жидкий стул. Диспепсические явления обычно развиваются на 2-3-и сут жизни. Важное значение имеет микробиологическое исследование кишечного содержимого (признаки нарушения формирования микроценоза кишечника - количественное преобладание клебсиелл, протея, синегнойной палочки).
Поражение центра льной нервной системы при ВУИ у новорожденных может быть как первичным (менингит, энцефалит), так и вторичным, обусловленным интоксикацией. Проникновение возбудите-
ля в мозг плода чаще всего происходит по ликворным путям, поэтому инфекция развивается в оболочках головного и спинного мозга и протекает в виде менингита и менингоэнцефалита. Возникают также изменения в сосудистых сплетениях боковых желудочков мозга, что может сопровождаться развитием врожденной гидроцефалии.
Сепсис у новорожденного трудно диагностировать в связи с низкой реактивностью его организма. В начале заболевания клинические проявления могут быть маловыраженными, возможно наличие только признаков общей интоксикации, без явного очага инфекции (синдром «инфицированности»). Необходимо уделять внимание таким симптомам, как вялость, плохое сосание, срыгивание, замедленное восстановление или вторичное снижение массы тела, задержка заживления пупочной ранки, развитие омфалита. Типичными симптомами инфекционной интоксикации у новорожденного являются нарушения дыхания и тканевого метаболизма. Отмечается бледно-цианотичная, с сероватым оттенком окраска кожных покровов с выраженным сосудистым рисунком (мраморность кожи). Интоксикация сопровождается нарушением экскреторной функции печени, развитием затяжной желтухи. К симптомам сепсиса также относится увеличение селезенки и периферических лимфоузлов. Информативными признаками является отек подкожной клетчатки, гипохромная анемия, нарушение функции почек и печени, водносолевого и белкового обмена (гипопротеинемия) (Анкирская А.С. и
соавт., 1989).
Также следует учитывать неспецифические проявления внутриутробной инфекции. У новорожденных, этой группы нарушаются реакции адаптации таких жизненно важных систем, как центральной нервной, дыхательной, сердечно-сосудистой, эндокринной и иммунной. Часто отмечается низкая оценка по шкале Апгар в первую минуту после рождения. Нередко в раннем неонатальном периоде наблюдаются срывы адаптации в виде гипоксического синдрома, синдрома дыхательных и сердечно-сосудистых расстройств, надпочечниковой и церебральной патологии. Следует иметь в виду и возможность таких проявлений, как врожденная гипотрофия, отечный синдром, гипербилирубинемия, ДВС-синдром крови.
ПРЕНАТАЛЬНАЯ ДИАГНОСТИКА ВНУТРИУТРОБНЫХ ИНФЕКЦИЙ
Учитывая неспецифичность клинических проявлений данной патологии, ее пренатальная диагностика является наиболее сложной.
Наиболее рациональной является поэтапная диагностика внутриутробных инфекций.
На первом этапе на основе сбора анамнестических данных и общего клинического обследования выявляется группа высокого риска по развитию внутриутробных инфекций. В эту группу относят пациенток:
• имеющих экстрагенитальные очаги инфекции, особенно с обострением инфекционного процесса во время беременности, а также перенесших во время беременности острые респираторные вирусные инфекции;
• с ранним началом половой жизни и частой сменой половых партнеров, у которых имелись эпизоды урогенитальных инфекций;
• перенесших воспалительные заболевания матки и ее придатков, кольпиты, заболевания, передаваемые половым путем;
• имевших искусственное прерывание беременности с осложненным течением послеабортного периода;
• с самопроизвольным прерыванием беременности в любые сроки в анамнезе;
• c осложненным течением послеродового периода после предыдущих родов;
• с инфекционно-воспалительными заболеваниями половых органов (кольпит, бактериальный вагиноз) во время беременности;
• c истмико-цервикальной недостаточностью;
• c клиническими признаками многоводия или фетоплацентарной недостаточности.
На втором этапе при помощи комплексного ультразвукового обследования выявляют эхографические маркеры внутриутробных инфекций, а также признаки фетоплацентарной недостаточности и оценивают степень ее тяжести.
Эхографические признаки, указывающие на ВУИ, можно разделить на следующие группы.
1. Патология амниона и хориона: - многоводие или маловодие (может быть диагностировано начиная с конца I триместра беременности);
- гиперэхогенная взвесь в околоплодных водах;
- амниотические тяжи;
- патология ворсинчатого хориона - гипоплазия ворсин (может быть диагностирована в сроки беременности до 8-9 нед и проявляется истончением хориона по всей окружности до 1-3 мм, снижением его эхогенности, прерывистостью и сглаженностью наружного контура);
- плацентит, признаками которого являются отек/утолщение (71,8%), разнородная эхогенность паренхимы плаценты, утол- щение/удвоение контура базальной пластинки, размытость границ долек, неравномерное расширение межворсинчатых пространств и субхориального пространства;
- преждевременное созревание плаценты.
2. Полостные и подкожные отеки:
- неиммунная водянка (подкожный отек и плевральный и/или перикардиальный выпот или асцит);
- гидроторакс;
- двусторонний плевральный выпот.
3. Кальцификаты во внутренних органах плода:
- кальцификаты перивентрикулярной области;
- кальцификаты кишечника;
- паренхиматозные печеночные/селезеночные кальцификаты.
4. Изменение эхогенности внутренних органов плода:
- гиперэхогенный кишечник (признак имеет диагностическое значение после 16 нед беременности);
- пневматоз кишечника (выявляется в 25% наблюдений с ВУИ);
- пузырьки газа в желчном пузыре;
- гиперэхогенные большие почки при нормальных размерах мочевого пузыря;
- двустороннее повышение эхогенности легких (в сочетании с незначительным плевральным выпотом и многоводием является признаком внутриутробной пневмонии).
5. Структурные дефекты (пороки развития внутренних органов плода).
6. Гепатомегалия и спленомегалия.
Обнаружение эхографических маркеров ВУИ не может служить основанием для диагноза. Нами отмечено, что при сочетании трех эхографических признаков и более вероятность реализации внутриутробной инфекции для новорожденного достигает 80%.
При оценке фетометрических параметров осуществляется диагностика синдрома задержки роста плода (СЗРП) и определяется его форма. Допплерометрическое исследование кровотока в сосудах фетоплацентарного комплекса позволяет обнаружить нарушения, которые при ВУИ в первую очередь выявляются в плодово-плацентарном кровотоке. Кардиотокографическое исследование позволяет диагностировать признаки развивающейся гипоксии плода.
Параллельно с ультразвуковой диагностикой проводят комплексное обследование с использованием современных лабораторных методов исследования для выявления возбудителей инфекционных заболеваний в организме женщины.
1. Иммуноферментный анализ, основанный на определении IgM и IgG, специфичных для той или иной инфекции, или антигенов соответствующих возбудителей.
2. Метод молекулярной гибридизации (идентификация фрагментов ДНК или РНК клеток возбудителя).
3. ELISA-метод (определение тест-системой моноклональных антител в жидкостях и средах организма).
4. Бактериоскопическое исследование нативных и окрашенных по Граму мазков из уретры, цервикального канала и влагалища.
5. Бактериологическое исследование с посевом содержимого цервикального канала, уретры и влагалища на жидкие и твердые среды в целях количественного определения представителей аэробных и анаэробных инфекций и чувствительности их к антибактериальным препаратам.
6. Исследование соскоба из цервикального канала методом полимеразной цепной реакции для идентификации возбудителей заболеваний, передаваемых половым путем.
На третьем этапе после применения косвенных методов диагностики и получения данных, свидетельствующих о наличии внутриутробной инфекции, возможно использование методов прямой диагностики ВУИ в материале полученном при биопсии ворсин хориона, амниоцентезе и кордоцентезе.
Для диагностики внутриутробных инфекций в I триместре беременности наиболее удобна аспирационная трансцервикальная биопсия хориальных ворсин. Производится в сроки от 6 до 10 нед беременности под контролем ультразвукового сканирования. Полученный биоптат подвергают бактериологическим и вирусологическим исследованиям, а также проводят кариотипирование. При
обнаружении внутриматочной инфекции следует ставить вопрос о прерывании беременности, так как для инфицирования в ранние сроки характерно образование пороков развития плода.
Начиная с 16-й нед беременности и на протяжении всего II триместра с целью диагностики внутриутробной инфекции используют амниоцентез. Операция проводится в асептических условиях трансвагинальным (через передний или задний свод влагалища или трансцервикально) или трансабдоминальным доступом (применяется чаще). Под контролем ультразвукового сканирования производится пункция амниотической полости в свободном от петель пуповины и мелких частей плода кармане околоплодных вод. Для исследования забираются три пробы околоплодных вод, общим объемом 24 мл, которые в последствии подвергаются микробиологическим, биохимическим и генетическим исследованиям.
Существует ряд тестов, предназначенных для обнаружения возбудителей внутриутробных инфекций в околоплодных водах: газо-жидкостная хроматография амниотической жидкости с целью определения органических кислот (ацетата, сукцината, бутирата, оксалоацетата и др.), что специфично для наличия инфекционных агентов в околоплодных водах.
Используют также и бактериоскопию нативных и окрашенных по Граму мазков околоплодных вод, посев их на жидкие и твердые среды. Обнаружение в посеве этиологически значимых микроорганизмов в количестве, превышающем 5?102 КОЕ/мл, является диагностическим критерием внутриутробной инфекции.
В диагностике вирусных внутриутробных инфекций применяют культивирование вирусных агентов на куриных эмбрионах и полимеразную цепную реакцию.
Важная роль принадлежит серологическим методам исследования, наиболее чувствительным и специфичным из которых является определение моноклональных антител тест-системой ELISA.
Проводится определение активности щелочной фосфатазы лейкоцитов пуповинной крови, подсчет количества тромбоцитов (признаком инфицирования считают тромбоцитопению ниже 150-109/л), соотношения юных форм лейкоцитов и нейтрофилов и радиоизотопное определение β-лактамазы (характерно для инфицирования β- лактамазопродуцирующими микроорганизмами). Кровь подвергают также бактериологическим, вирусологическим и иммунологическим исследованиям.
Доклиническая диагностика ВУИ основана преимущественно на целенаправленном микробиологическом обследовании новорожденных (сразу после рождения) и гистологическом исследовании последа у беременных с повышенным риском развития инфекции у плода.
В противоположность микробиологическим и гистологическим методам иммунологическое исследование новорожденных в момент рождения, в частности определение иммуноглобулинов основных классов в пуповинной крови, не является достаточно информативным для доклинической диагностики ВУИ. Это объясняется тем, что одинаковые показатели иммуноглобулинов G, M, A регистрируются у новорожденных с клиническими проявлениями инфекции и без них. Повышенный уровень IgM и в пуповинной крови отражает имевшую место антигенную стимуляцию в антенатальном периоде, но не всегда свидетельствует о наличии у него инфекционного процесса.
ОСОБЕННОСТИ ОТДЕЛЬНЫХ НОЗОЛОГИЧЕСКИХ ФОРМ ВНУТРИУТРОБНЫХ ИНФЕКЦИЙ
Цитомегаловирус
Цитомегаловирус (ЦМВ) - ДНК-содержащий вирус из семейства герпес-вирусов, повсеместно распространен и может передаваться с различными сретами организма (кровь, моча), но чаще всего при половом контакте. У взрослых инфекция, как правило, протекает без явных клинических проявлений, но возможно и ее мононуклеозоподобное течение.
Заражение ЦМВ происходит при тесном контакте с инфицированным лицом или путем восходящей инфекции от матери к ребенку. Вирус время от времени выделяется со слюной, мочой и выделениями из половых органов и передается при поцелуе, половом сношении или других контактах.
Цитомегаловирус, попав однажды в организм человека, после первичной инфекции не элиминируется во внешнюю среду, а персистирует в нем пожизненно. Длительному латентному течению инфекции способствует внутриклеточное существование вируса, где он надежно защищен от действия специфических антител. Проведенные в России серологические исследования показали, что 90% беременных женщин имеют антитела к ЦМВ, что свидетельствует о крайне высо-
ком уровне вирусоносительства. Во время беременности создаются реальные условия для реактивации инфекции, что связано с гестационными особенностями функционирования системы иммунитета (состояние физиологической иммуносупрессии).
Вероятность внутриутробного инфицирования плода при латентном течении инфекции практически отсутствует, при ее реактивации составляет 0,5-7%, а при первичном инфицировании превышает 40%. В целом частота пренатальной инфекции ЦМВ составляет 5-20 на 1000 живорождений. Пренатальное инфицирование цитомегаловирусом составляет 5% у серопозитивных женщин, до 20% заражений происходит во время родов, а еще 10% детей приобретают инфекцию в раннем постнатальном периоде - чаще всего от матери, через зараженное материнское молоко.
Наиболее частый путь инфицирования - трансплацентарный, реже плод заглатывает инфицированные околоплодные воды при наличии плацентита и хориоамнионита.
Вирус может поразить любой орган плода, включая центральную нервную систему. Инфицирование клеток эпителия характеризуется развитием больших внутриядерных включений (цитомегалические включения). В пораженных тканях наблюдается цитолиз с участками очагового некроза и преимущественно мононуклеарной воспалительной реакцией. Заживление приводит к фиброзу и кальцификации, особенно в субэпендимальной оболочке желудочков мозга и в печени. Тяжелые церебральные осложнения, включая микроцефалию и кальцификацию, обычно являются результатом внутриутробной инфекции в первые 3-4 мес беременности, когда желудочковая система находится в стадии развития.
В связи с поражением на ранних сроках гестации формируются эмбриопатии, развиваются тяжелые нарушения трофики плодного яйца, наступает гибель эмбриона или плода, беременность заканчивается выкидышем. Мертворожденным плодам свойственны тяжелые церебральные нарушения, включая микроцефалию, гидроцефалию и кальцификацию, также могут отмечаться порэнцефалия, кистофиброз поджелудочной железы, цирроз печени, атрезия желчных протоков, кортикальная дисплазия почек.
В более поздние сроки формируются фетопатии с фетоплацентарной недостаточностью, внутриутробной задержкой роста, возникают стигмы дизэмбриогенеза. У новорожденных отмечается поражение эпителия слюнных желез, извитых канальцев почек, бронхов, желч-
ных протоков. По данным комплексного (эхографического, допплерометрического и кардиотокографического) исследования (гормоны - плацентарный лактоген, прогестерон, эстриол, кортизол; содержание АФП) - признаки внутриутробного страдания плода обнаруживаются в 33,9%.
Клинические проявления. У 90-95% детей, инфицированных внутриутробно ЦМВ, при рождении не отмечается никаких симптомов. Большинство из них нормально развивается, но тщательное наблюдение в течение длительного времени указывает, что у 10-30% детей впоследствии отмечаются симптомы незначительных неврологических повреждений - нервная глухота, замедленное развитие или легкая умственная отсталость. Кроме того, возможно специфическое нарушение функции клеточного иммунитета - угнетение активности Т-хелперов, повышение содержания IgM и IgG.
У небольшой части детей с клиническими признаками инфекции последние варьируют от внутриутробной задержки роста (обнаруживается чаще всего как и увеличение печени и селезенки) или вовлечения в процесс отдельного органа до тяжелого, генерализованного, угрожающего жизни заболевания, что бывает редко.
Многие из экстрагенитальных проявлений врожденной цитомегаловирусной инфекции (гепатит, тромбоцитопения, гемолитическая анемия и пневмония) исчезают в течение определенного срока без лечения. Неврологические нарушения необратимы, хотя степень инвалидности бывает различной. Большинство детей с врожденной цитомегаловирусной инфекцией, у которых при рождении отмечаются симптомы поражения нервной системы, страдают серьезными необратимыми неврологическими нарушениями, включая церебральный паралич, эпилепсию, нервную глухоту. Довольно часто встречается хориоретинопатия. Она редко вызывает какой-либо дефект зрения и представляет собой удобный диагностический признак при подозрении на врожденные инфекции, хотя и неотличима от хориоретинопатии в результате токсоплазмоза. Летальность при врожденной цитомегалии - 20-30%.
Профилактика и лечение. На сегодняшний день не разработаны эффективные безопасные вакцины или препараты готовых специфических моноклональных антител. Профилактические мероприятия сводятся к изоляции инфицированных новорожденных и исключению контакта этих новорожденных с серонегативными беременными. Персонал, ухаживающий за ними, работает в перчатках и втором
халате. Как пассивную профилактику можно использовать введение препаратов готовых антител с повышенным содержанием противоцитомегаловирусного IgG.
Несмотря на достигнутые в последнее время успехи в лечении инфекций, вызванных α-герпесвирусами (вирус простого герпеса и вирус варицеллы-зостер), для β-герпесвирусных заболеваний лечение окончательно не разработано. Применяют валацикловир и ганцикловир, однако достаточного опыта их применения у беременных нет. Комплекс лечения включает применение до 14 нед гестации растительных адаптагенов (элеутерококк, женьшень, маточное молочко), витаминов группы В (В1, В6, В12).
Начиная с 15-16 нед в качестве метода паллиативного лечения проводится курс иммуноглобулинотерапии нормальным человеческим иммуноглобулином или препаратами готовых антител с повышенным содержанием противоцитомегаловирусного IgG - противоцитомегаловирусными иммуноглобулинами. При введении препаратов иммуноглобулина организм матери получает готовые антитела (АТ) против ЦМВ. АТ класса IgG активно проходят через плаценту и создают в организме плода пассивный иммунитет. В организме беременной АТ ведут к блокировке внеклеточно расположенных вирусов, создают иммунные комплексы с ними, способствуют элиминации из организма и ограничивают распространение в лимфо- и кровотоке. Проведение иммуноглобулинотерапии проводится с учетом риска аллергических, пирогенных реакций, выработки анти-у-глобулинов, обострения инфекции, т.е. в ситуациях, когда риск неблагоприятного влияния инфекции выше.
Полученные данные о сниженной способности лейкоцитов к продукции α- и у-интерферона у женщин с вирусными инфекциями указывают на целесообразность включения в комплексную терапию беременных с цитомегаловирусной инфекцией иммуномодулирующего и интерферонкорригирующего компонентов. Применяется генно-инженерный рекомбинантный препарат виферон, который представляет собой а2-интерферон, ассоциированный с антиоксидантами. Он обладает интерферонстабилизирующими, иммуномодулирующими и антиоксидантными свойствами.
Новым в лечении герпетических инфекций является использование плазмафереза и эндоваскулярного лазерного облучения крови (ЭЛОК). Лечебная эффективность плазмафереза и ЭЛОК обусловлена детоксикационным эффектом, стимулирующим воздействием на
клеточный и гуморальный иммунитет и реакции неспецифической резистентности, нормализацией коагуляционных и агрегационных свойств крови.
Герпетическая инфекция
Наиболее важную роль играют вирусы семейства Herpesviridae. Вирус простого герпеса (ВПГ) является ДНК-содержащим и входит в одну группу с ЦМВ, вирусом Эпштейна-Барр и вирусом ветряной оспы - опоясывающего лишая. Выделено два его серотипа ВПГ-1 (оролабиальный) и ВПГ-2 (генитальный), однако нет полного соответствия между серотипом и локализацией инфекции. В 20% инфекция новорожденных бывает связана с поражением гениталий ВПГ-1.
Вирус простого герпеса передается различными путями, наибольшее значение имеет половой путь. Поражение вирусом генитального герпеса выявляется у 7% беременных. Герпес у новорожденных регистрируется с частотой 1:2000-1:5000, но, несмотря на относительную редкость неонатального герпеса, тяжесть его проявлений и неблагоприятный прогноз для новорожденного делают весьма актуальной разработку рациональных подходов к диагностике, лечению и в особенности к профилактике этого крайне серьезного заболевания.
Частота обнаружения ВПГ-2 значительно варьирует в зависимости от ряда факторов (возраст, характер половой жизни, социально-культурный уровень населения и т.д.). Так, у подростков младше 15 лет серопозитивные результаты составляют менее 1%, в то время как среди пациенток клиник, специализирующихся по заболеваниям, передающимся половым путем, они колеблются в пределах 46-57%. У беременных специфические антитела к ВПГ-2, например в США, выявляются в среднем у 20-30% женщин.
Клинические проявления первичной инфекции у матери длятся 18-22 дня, с нарастанием симптоматики в течение 1-й нед. Бессимптомное слущивание поврежденного вирусом эпителия наблюдается в течение последующих 2 нед. Общая продолжительность проявлений составляет почти 6 нед. Непервичная генитальная инфекция протекает менее выражено: короче длительность клинических проявлений (около 15 дней), реже наблюдается бессимптомное выделение вируса, а продолжительность его уменьшается до 8 дней. Тяжесть и продолжительность клинических проявлений при рецидивах еще менее выражена, а длительность слущивания поврежденного эпителия составляет всего 4 дня.
Первичный генитальный герпес у матери и обострение хронического процесса являются наиболее опасными для плода. Если интранатально инфицируются 0,5-1,0% новорожденных, то при остром течении или обострении, что проявляется пузырьковыми поражениями кожи и слизистых оболочек гениталий, риск инфицирования плода в родах достигает 40%.
При внутриутробной ВПГ-2 инфекции в большинстве наблюдений инфицирование плода происходит непосредственно перед родами, восходящим путем после разрыва плодных оболочек (критический период 4-6 ч) или во время родов при прохождении через инфицированные родовые пути (85%). Передача инфекции происходит как при наличии очагов повреждения в области шейки матки и вульвы, так и бессимптомном выделении вируса. При восходящем пути инфицирования возбудитель размножается и накапливается в околоплодных водах, отмечается многоводие. После того как произошло инфицирование, вирус может распространяться контактным или гематогенным путями. В 5% встречается трансплацентарное распространение во время беременности.
Поражение плаценты и плода герпетической инфекцией может возникать в любом сроке беременности и приводить к формированию у плода врожденных пороков развития, антенатальной гибели, выкидышу или преждевременным родам. Инфицирование в I триместре приводит к формированию гидроцефалии, пороков сердца, аномалий желудочно-кишечного тракта, часто наступает самопроизвольное прерывание беременности, развивается задержка внутриутробного роста плода. Во II и III триместрах инфекционный процесс ведет к развитию гепатоспеленомегалии, анемии, желтухи, пневмонии, менингоэнцефалита, сепсиса, гипотрофии. Внутриутробное инфицирование на поздних сроках беременности проявляется ранним развитием клинической картины неонатальной инфекции (первые сутки) у детей, рожденных даже в результате кесарева сечения. Обычные проявления герпетической инфекции: поражение кожи, слизистой рта, хориоретинит.
Неонатальная герпесвирусная инфекция проявляется в трех клинических формах.
Локальная форма с поражением кожи и слизистых - 45%. Повреждения кожи и слизистых представляют собой наиболее частую, но и наиболее легкую форму неонатального герпеса. Глаза: кератоконъюнктивит и хориоретинит. Кожа и слизистая рта: везикулы,
эритема, петехии. При отсутствии лечения возможно прогрессирование заболевания с развитием тяжелых осложнений. Смертность составляет около 18%.
Локальная форма с поражением ЦНС (энцефалиты) - 35%. Характерны: лихорадка, вялость, снижение аппетита, синдром угнетения или возбуждения, тремор, судороги. Обнаруживаются выраженные изменения в цереброспинальной жидкости. Смертность при отсутствие терапии - более 50%.
Диссеминированная форма - 20%. При диссеминированной форме неонатального герпеса в процесс обычно вовлекается сразу несколько органов: печень, легкие, кожа, надпочечники. Признаки появляются на 1-2-й нед жизни, включают себя симптомы локализованной формы в сочетании с анорексией, рвотой, летаргией, лихорадкой, желтухой, дыхательными расстройствами, кровотечением, шоком (рис. 35). Появление кровотечения и сосудистого коллапса может быть внезапным и быстро приводит к летальному исходу. Смертность при этой форме крайне высока - 90%. Современная противогерпетическая химиотерапия позволяет значительно улучшить прогноз, но, несмотря на проводимое лечение, риск отдаленных неврологических нарушений остается достаточно высоким.
Выжившие дети в дальнейшем имеют тяжелые осложнения (неврологические расстройства, нарушения зрения, отставание психомоторного развития).
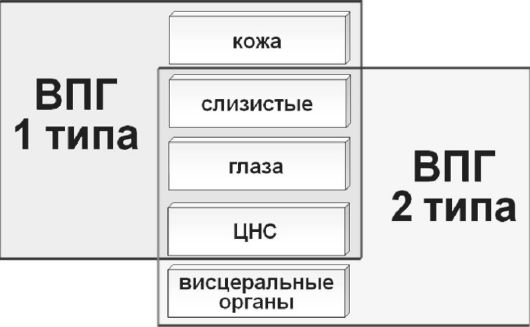 Рис. 35. Тканевой тропизм герпесвирусов
Рис. 35. Тканевой тропизм герпесвирусов
Профилактика, лечение и ведение беременности. Характер профилактических и лечебных мероприятий, а также акушерская тактика зависят от типа, формы (типичная, атипичная, бессимптомная и длительности течения) и наличия поражения гениталий, состояния плодных оболочек.
При первичном инфицировании в ранние сроки беременности необходимо ставить вопрос о ее прерывании. Если же заболевание возникает в поздние сроки или женщина была инфицировна до наступления беременности, профилактические мероприятия заключаются в динамическом эхографическом контроле за развитием и состоянием плода, назначении курсов терапии, включающей метаболический комплекс, стабилизаторы клеточных мембран, унитиол. Вопрос о прерывании беременности решается индивидуально.
Доказано преимущество комплексного лечения герпетических поражений. Основным является химиотерапия препаратами ацикловир или валацикловир. Химиотерапия возможна, начиная с I триместра беременности. Несмотря на недоказанность тератогенного и эмбриотоксического эффектов, назначение ацикловира беременным ограничивают из-за следующих показаний: первичный генитальный герпес, рецидивирующий генитальный герпес (типичная форма), генитальный герпес в сочетании с угрозой прерывания беременности или симптомами ВУИ. У беременных, имеющих частые рецидивы инфекции, проводится перманентное лечение ацикловиром (супрессивная терапия). При осложненном течении герпетической инфекции (пневмония, энцефалит, гепатит, коагулопатия) лечение проводится совместно с инфекционистом.
Одновременно целесообразно назначать иммуноглобулинотерапию, препараты интерферона, «большие» антиоксиданты (витамины Е и С). Следует отметить необходимость лечения сопутствующих герпесу заболеваний (чаще всего хламидиоз, микоплазмоз, трихомониаз, кандидоз, бактериальный вагиноз). Так же как для лечения цитомегалии, в терапии герпетической инфекции нашли свое место плазмаферез и эндоваскулярное лазерное облучение крови. После комплексной терапии частота осложнений для матери и плода снижается в 2-3 раза.
Акушерская тактика ведения женщин с генитальным герпесом зависит от его формы и срока беременности. При первичной инфекции во время беременности (за 1 мес до родов и менее) или рецидиве (за несколько дней до родов) осуществляется химиотерапия,
родоразрешение проводится путем операции кесарева сечения. При наличии генитального герпеса в анамнезе у одного из родителей показано культуральное исследование или ПЦР перед родами. При отрицательном ответе - родоразрешение через родовые пути.
Несмотря на правильно организованную акушерскую помощь, в настоящее время нет условий для полного исключения передачи ВПГ-инфекции от матери к новорожденному. Это обусловлено невозможностью выявления всех женщин с бессимптомно протекающей генитальной герпесной инфекцией. В связи с этим в 70% передача герпесвирусной инфекции новорожденным происходит именно от матерей с бессимптомным течением герпеса.
Краснуха
Роль вируса краснухи как причины врожденных пороков развития была впервые признана в 1941 г. австралийским офтальмологом Norman Gregg. Он впервые описал синдром катаракты, глухоты и врожденного порока сердца у детей, матери которых переболели краснухой во время беременности в Сиднейскую эпидемию 1940 г. Вирус впервые был выделен в культуре тканей в 1962 г. К 1969 г. появилась действенная живая ослабленная вакцина
Вирус краснухи является РНК-содержащим вирусом и относится к группе тогавирусов (микровирусов). Единственным носителем является человек. Вирус краснухи нестоек во внешней среде, распространяется воздушно-капельным путем;для заражения требуется длительный контакт, однократного общения обычно недостаточно, но, поскольку заболевание часто протекает бессимптомно, о контакте может быть неизвестно.
У подавляющего большинства лиц, переболевших краснухой, формируется стойкий иммунитет, однако 0,3-4,25% людей болеют краснухой повторно, так как возможна реактивация ранее перенесенной краснухи или повторная инфекция в результате неполноценности имеющегося гуморального иммунитета. В тоже время, по данным санкт-петербургских исследователей, на практике такие наблюдения фактически не встречаются, и если клинически и серологически исключена острая краснуха, то исключен риск внутриутробного инфицирования. Если имеется высокий или нарастающий титр антител к краснушному антигену, необходимо определение специфических IgM-антител у матери, а при выявлении их - в крови плода, полученной путем кордоцентеза.
Инфицирование плода происходит только от заболевшей матери. Женщинам, переболевшим краснухой, можно рекомендовать беременность не ране чем через 6 мес после выздоровления. Поражение происходит в результате вирусемии и трансплацентарного проникновения вируса.
Одних клинических симптомов для постановки диагноза недостаточно. По той же причине наличие краснухи в анамнезе не свидетельствует о наличии иммунитета. Для доказательства заражения краснухой требуется выделение вируса или соответствующее серологическое исследование.
Критериями диагноза недавно перенесенной краснухи являются:
• выделение вируса краснухи (обычно из глотки);
• повышение титра антител в 4 раза и более;
• наличие специфического для краснухи IgM, который определяется только в течение 4-6 нед после первичной инфекции.
• если диагноз остается под вопросом, особенно если контакт имел место в самые ранние сроки беременности, в 14-20 нед можно провести амниоцентез и попытаться выделить вирус краснухи из амниотической жидкости, что в случае успеха укажет хотя бы на инфицирование плаценты. Отрицательные результаты культивирования вовсе не исключают инфицирования плаценты или плода. Наиболее точным является проведение кордоцентеза.
Краснуха у беременной может иметь следующие исходы:
• отсутствие воздействия на плод;
• инфицирование только плаценты;
• инфицирование плаценты и плода (от бессимптомного течения до поражения многих систем);
• гибель плода (самопроизвольное преждевременное прерывание беременности или мертворождение).
Инфицирование плода может последовать за инфекцией у матери на любом этапе гестации, при этом исход краснухи в большой степени зависит от срока беременности.
Вероятность инфицирования плода в сроке до 8 нед беременности составляет 54%, в 9-12 нед - 34%, 13-24 нед - 10-20% и не более 12% - с конца II триместра. Вирусемия у женщины в первые 8 нед беременности приводит к инфицированию плаценты и самопроизвольному выкидышу или мертворождению; при заражении в середине беременности чаще диагностируется рубеолярная фетопатия у недоношенных новорожденных; при заражении в III триместре краснуха
протекает без врожденных пороков развития как хронический энцефалит и продуктивный лептоменингит у новорожденных.
Клиника врожденной краснухи. Вирус краснухи проявляет исключительный тропизм к молодой эмбриональной ткани, с чем связана эмбриопатия при этом заболевании. Поражение плода вирусом краснухи многообразно. Выделяют «классический синдром врожденной краснухи», который включает триаду наиболее типичных аномалий развития: катаракту с помутнением роговицы, пороки сердца (врожденные дефекты перегородки желудочков - рубеолярная эмбриопатия) и глухоту (геморрагии в мягкие ткани наружного, среднего и внутреннего уха). Синдром врожденной краснухи часто сочетается с интерстициальной продуктивной пневмонией с гигантоклеточным метаморфозом альвеолоцитов.
Помимо классического, существует «расширенный синдром врожденной краснухи», в который, кроме трех названных пороков, входит множество других аномалий развития: микроцефалия, увеличенный родничок, поражение головного мозга, глаукома, расщепление нёба, интерстициальная пневмония, гепатит, поражение вестибулярного аппарата, пороки развития скелета, поражение трубчатых костей, гепатоспленомегалия, пороки развития мочеполовых органов.
До 70% выживших детей с серологическим свидетельством инфекции при рождении практически здоровы, но в течение первых 5 лет жизни более чем у 2/з детей развиваются какие-либо признаки инфекции. Чаще всего это менее очевидные осложнения, которые заключаются в легкой или средней степени глухоты и поражения мозга с задержкой психомоторного развития. К поздним проявлениям краснухи также относят иммунологические дискразии (задержка появления у новорожденного способности к синтезу собственных иммуноглобулинов в ответ на вирусную инфекцию), тугоухость, задержку психомоторного развития, аутизм, мозговые синдромы (склерозирующий панэнцефалит), сахарный диабет.
Среди неонатальных проявлений краснухи наиболее характерна тромбоцитопеническая пурпура, которая сохраняется от 2 нед до 3 мес. Типичны гепатиты с желтухой, гемолитичекая анемия с ретикулоцитозом и деформированными эритроцитами, незаращение переднего родничка с плеоцитозом спинномозговой жидкости, интерстициальная пневмония, поражение трубчатых костей (выявляется рентгенологически и заключается в чередовании участков уплотнения и разрежения кости). Из пороков сердца наиболее частым
является незаращение артериального (боталлова) протока, нередко в сочетании со стенозом легочной артерии. Встречаются также стеноз и коарктация аорты, ДМЖП и ДМПП, транспозиция крупных сосудов; пороки «синего» типа - редко.
Наиболее типичное поражение глаз - катаракта - результат прямого действия вируса краснухи, который может персистировать в хрусталике несколько лет. Катаракта может отсутствовать при рождении и появиться в периоде новорожденности. Глаукома встречается в 10 раз реже. Кроме того, при краснухе могут быть выявлены пигментная ретинопатия, помутнение роговицы, миопия, недоразвитие век.
Самым частым дефектом при врожденной краснухе является глухота, нередко сочетающаяся с вестибулопатией - дефектом кортиева органа.
Чем меньше срок беременности, при котором женщины болеют краснухой, тем чаще проявляется тератогенное действие вируса. Тератогенная опасность краснухи в 1-й мес беременности составляет 35-50% (по некоторым данным, приближается к 100%), во 2-й мес -
25%, в 3-й - 7-10%.
Неблагоприятное влияние краснухи на плод проявляется не только тератогенным действием. Краснушная инфекция в ранний период беременности в 10-40% может вести к спонтанным абортам, в 20% - к мертворождению, 10-25% детей, рожденных живыми, умирают в неонатальном периоде.
Лечение и ведение беременных с краснухой. Для краснухи, как и для других инфекций, вызываемых РНК-вирусами, специфического лечения не существует. Особенности биологии РНК-содержащего вируса (внутриклеточное паразитирование, повреждение цитоплазматических мРНК, быстро приводящее к гибели клетки) не позволяют на данном этапе развития вирусологии создать препарат, избирательно ингибирующий репликацию генома вируса. Перспективным в лечении краснухи является создание препаратов специфических моноклональных антител.
Заболевание краснухой в I триместре беременности, подтвержденное клиническими, эпидемиологическими и лабораторными данными, является показанием для ее прерывания. При контакте беременной с больным краснухой не позднее 10-12 дней необходимо провести серологическое обследование. При серонегативной реакции продолжают тщательное наблюдение и повторное серологическое обследование через 2 нед для выявления бессимптомной инфекции.
Профилактика прежде всего заключается в иммунизации. Вакцинация детей обязательна. Беременные не вакцинируются, так как используется ослабленная живая вакцина и не исключается тератогенный эффект. Рекомендуется скрининговое обследование женщин детородного возраста на наличие антител к антигенам вируса краснухи.
Токсоплазмоз
Toxoplasma gondii относится к простейшим, заражающим у млекопитающих клетки практически любого типа. Этот возбудитель инфекции широко распространен во всем мире, поражает человека и животных, однако окончательный цикл воспроизводства происходит только в кишечнике животных из семейства кошачьих. Ооцисты попадают в организм человека, употребляющего в пищу овощи или другие продукты, зараженные ооцистами из почвы. Вслед за поглощением ооцист в кишечнике высвобождаются трофозоиты. Они проникают в эпителий, где размножаются и затем - через лимфатическую и кровеносную системы - распространяются по всему организму. В организме здорового иммунокомпетентного хозяина размножение трофозоитов ограничивается развитием клеточной иммунной реакции и в меньшей степени продукцией специфических антител. Часть этих организмов предохраняет от иммунной защиты хозяина образование тканевых псевдоцист, представляющих собой внутритканевые скопления организмов, окруженных защитной оболочкой. В этом виде они остаются латентными, но жизнеспособными на всем протяжении жизни хозяина, обычно не вызывая сколько-нибудь значительной иммунной реакции. Если нормальный иммунитет по какой-то причине снижается, инфекция может реактивизироваться.
Другой важный путь заражения - употребление в пищу сырого или не совсем готового мяса от зараженного животного. Этим путем человек чаще всего получает инфекцию при употреблении баранины или свинины. От одного лица к другому инфекция не передается, за исключением передачи через плаценту от матери к плоду при развитии острой инфекции во время беременности. О связи хронической или латентной инфекции с повторными выкидышами убедительных данных нет.
Частота заражения человека Т. gondii в любой популяции зависит от климата, способа приготовления пищи и, кроме того, контактов с кошками. Распространенность выявляемых антител неуклонно
увеличивается с возрастом и колеблется в разных районах мира от 20 и до 80% по отношению к женщинам репродуктивного возраста. Серологические признаки врожденной инфекции отмечаются примерно у 40% детей, матери которых во время беременности перенесли острый токсоплазмоз. Заражение плода возможно только во время паразитемии, т.е. в течение 5-7 дней острого токсоплазмоза. Иными словами, женщина может инфицировать свой плод только однажды - в период острого заболевания при данной беременности; все остальные беременности в этом отношении безопасны для плода.
Частоту врожденного токсоплазмоза определить трудно, поскольку большинство зараженных детей при рождении практически здоровы, а инфекция у матери, как правило, бессимптомна. Имеются данные, что большинство зараженных детей впоследствии страдают от серьезных осложнений этой инфекции, которые могут потребовать специализированного длительного лечения. Теоретический расчетный риск врожденной инфекции, основанный на годовых процентах сероконверсии у женщин детородного возраста, колеблется от 4 до 50 случаев на 10 тыс. рождений живыми детьми.
Клинические проявления инфекции. Клинические проявления инфекции при токсоплазмозе следующие.
'Приобретенный токсоплазмоз. В большинстве случаев заражение человека Т. gondii проходит бессимптомно или не распознается. Самым частым проявлением инфекции является генерализованная лимфаденопатия, которая, хотя и не всегда, сочетается с недомоганием, лихорадкой, болью в горле, головной болью, сыпью. Иногда при этом находят атипичный лимфоцитоз без гетерофильных антител. Инфекция обычно имеет тенденцию к ограничению. В редких более серьезных случаях в инфекционный процесс вовлекаются мозг, миокард, печень или легкие, что требует специфического лечения. Хориоретинит встречается относительно редко и носит обычно односторонний характер. *Врожденный токсоплазмоз. При заражении женщины токсоплазмозом в самом начале беременности риск передачи ее плоду относительно невелик (около 20%), но инфекция в этот период может иметь тяжелые последствия, вплоть до смерти плода. При рождении аномалии выявляются только у 10-20% детей с врожденным токсоплазмозом, большинство детей с тяжелыми нарушениями заражаются в ранние сроки беременности. Тяжелый внутриутробный токсоплазмоз может привести к гибели или
серьезным аномалиям развития плода, в том числе гидроцефалии, формированию кист с кальцификатами или крайнему истончению коры головного мозга с кальцификацией, глиальным пролифератам, продуктивным эндартериитам, развитию генерализованного отека с гидротораксом и асцитом, распространенному воспалению и разрушению тканей различных органов. В последе выявляется хронический виллузит, в строме ворсин - лимфоидная инфильтрация с примесью плазмоцитов. Специфическим признаком является обнаружение возбудителя в виде цист или свободно лежащих форм при окраске по Романовскому-Гимза мазков-отпечатков с материнской поверхности плаценты или из глубины среза плацентарной ткани; окончательный диагноз ставится на основании выявления простейших организмов во внутритканевых псевдоцистах у плода.
• Тяжелый врожденный токсоплазмоз у новорожденных часто представляет собой генерализованное заболевание, проявляющееся в анемии, увеличении печени и селезенки, желтухе, лихорадке и лимфаденопатии. При тщательном исследовании глазного дна у большинства зараженных детей обнаруживаются признаки двустороннего хориоретинита. Вовлечение ЦНС может проявляться в виде внутричерепной кальцификации, судорог, гидроцефалии, микроцефалии или изменений спинномозговой жидкости (в особенности повышенного уровня белка). Примерно у 80% детей с клиническими признаками токсоплазмоза при рождении имеется необратимое повреждение головного мозга и у 50% - ослабление зрения. При заболевании матери токсоплазмозом в более поздние сроки беременности вероятность инфицирования плода выше, но при рождении клинические признаки инфекции в основном не проявляются, а если и имеются, то обычно локализуются в глазном яблоке или центральной нервной системе и у новорожденного часто остаются незамеченными.
Симптомы поражения глаз постепенно проявляются более чем у 80% зараженных детей, хотя их иногда распознают лишь у детей старшего возраста или подростков. Примерно у4 детей в этой группе страдает значительной потерей зрения и столько же рецидивирующим активным хориоретинитом с хотя бы временным расстройством зрения.
Серьезные неврологические нарушения отмечаются реже (<10%), в отдаленном периоде прицельное изучение умственных способ-
ностей показывает ухудшение результатов у большего числа детей. Нередко встречается и частичная потеря слуха.
Профилактика и ведение беременных с токсоплазмозом. Риск инфицирования токсоплазмозом можно снизить следующими способами.
1. Следует избегать употреблять в пищу недожаренное или сырое мясо, особенно свинину или баранину, а также тщательно мыть руки после обработки сырого мяса.
2. Избегать контактов с домашней кошкой во время беременности необязательно, хотя нового животного в это время лучше не заводить. Песок для кошки следует менять чаще и желательно, чтобы это делал кто-нибудь другой. Кормить ее следует только вареным или консервированным мясом.
3. Необходимо хорошо промывать перед едой свежие овощи, чтобы в еду не попала зараженная земля.
4. Следует тщательно мыть руки после работы в саду, особенно перед едой.
Между острым токсоплазмозом у беременной и началом инфекционного процесса у плода проходит значительное время. Если инфекция развивается в первую половину беременности, можно ставить вопрос об искусственном аборте, поскольку риск ее передачи плоду в ранние сроки приближается к 20%, а последствия разрушительны. В поздние сроки беременности осуществляют лечение беременной пириметамином, сульфаниламидами, тиндурином. С успехом применяют макролидный антибиотик спиромицин.
Хламидиоз
Хламидии представляют собой группу облигатных внутриклеточных паразитов, не способных синтезировать АТФ, ГТФ, и ряд ферментативных систем. Возбудитель хламидиоза имеет две формы существования, различающиеся по морфологическим и биологическим свойствам внеклеточную - элементарное тельце (ЭТ) и внутриклеточную - ретикулярное тельце (РТ). ЭТ адаптировано к внеклеточному существованию, является высоко инфекционной формой возбудителя. РТ - форма внутриклеточного существования хламидий, обеспечивающая репродукцию микроба, метаболически активная, имеющая структуру типичных грамотрицательных бактерий. Полный цикл репродукции хламидий равен 48-72 ч.
Хламидии передаются чаще половым путем и поражают преимущественно клетки цилиндрического эпителия. Доказана также воз-
можность распространения хламидий «бытовым» путем, главным образом среди детей раннего возраста.
Клинические проявления хламидиоза. Внедрение хламидий в мочеполовой тракт не всегда сопровождается заметными клиническими проявлениями. Заболевание чаще бывает субманифестным или асимптомным. Половина инфицированных женщин не имеют клинических проявлений. Хламидийные уретриты не имеют специфических проявлений, и больные редко предъявляют жалобы на дизурию. Иногда хламидии могут вызывать экссудативное воспаление протоков и бартолиниевых желез. Цервициты наблюдаются как первичное и наиболее частое проявление хламидийной активности. Выделения из цервикального канала мацерируют многослойный плоский эпителий влагалищной части шейки матки, вызывая его частичную десквамацию. Шейка матки становится отечной, гиперемированной, образуется так называемая гипертрофическая эктопия шейки матки. Хламидийный сальпингит - наиболее частое проявление восходящей хламидийной инфекции. Особенностью хламидийных сальпингитов и сальпингоофоритов является их длительное, подострое, стертое течение без склонности к «утяжелению». Хроническая инфекция может вызывать непроходимость труб, внематочную беременность, бесплодие. У женщин с восходящей хламидийной инфекцией при воспалительных заболеваниях органов малого таза может развиваться перигепатит - синдром Fitz-Hugh-Ciirtis. Этот синдром характеризуется повышением температуры тела, болями в области печени и органов малого таза.
Кроме урогенитального хламидиоза, возможна и экстрагенитальная хламидийная инфекция (офтальмохламидиоз), при этом у 72% больных с офтальмохламидиозом одновременно имеется хламидийная инфекция урогенитального тракта.
Урогенитальный хламидиоз диагностируется у беременных в 3-12%, достигая 33 -74% при хронических воспалительных заболеваниях половых органов, хронических неспецифических заболеваниях легких, отягощенном акушерском анамнезе (мертворождение, внутриутробная пневмония у новорожденного, преждевременные роды, привычное невынашивание беременности).
Беременность при хламидиозе, как правило, протекает с осложнениями. В I триместре характерна угроза прерывания беременности, неразвивающаяся беременность, выкидыши. Частота выкидышей составляет 25%, перинатальные потери при преждевременных родах - до 5,5%.
Хламидиоз ведет не только к привычному невынашиванию беременности, но и внутриутробному инфицированию плода и новорожденного. Хламидии колонизируют главным образом конъюнктивы, носоглотку, дыхательные пути, кишечник, но наиболее характерным считается поражение мягких мозговых оболочек и вещества мозга, где уже макроскопически определяются ватообразные наложения, преимущественно на верхнелатеральных поверхностях полушарий. Гистологически они имеют вид гранулем. Результатом хламидийной инфекции является повышение антенатальной смертности, возникновение трахомоподобных конъюнктивитов и пневмоний у новорожденных. При инфицировании амниотической оболочки развивается многоводие, специфическое поражение плаценты ведет к развитию фетоплацентарной недостаточности (27%), СЗРП и гипоксии плода. Перинатальная смертность при хламидиозе достигает 15,5%, причем удельный вес новорожденных, погибших в постнатальном периоде, составляет больше половины всех перинатальных потерь.
Клинические проявления. У 17-30% беременных хламидиоз протекает латентно или с незначительной симптоматикой. При наличии смешанной инфекции он может быть с полным симптомокомплексом, включающим цервицит с эктопией шейки матки.
Хламидиоз у беременных обычно сочетается с бактериальной и вирусной инфекцией, поэтому инфицирование плода часто происходит за счет совместного воздействия этих возбудителей. Это обусловливает полиморфизм клинических проявлений инфекции у новорожденного, поэтому, наряду с типичными проявлениями хламидийной инфекции (конъюнктивиты, вульвовагиниты, пневмонии), встречаются формы, нехарактерные для хламидиоза (везикулопустулез, омфалит, ринит, сепсис).
Клинические формы проявления внутриутробных инфекционных заболеваний у новорожденных, родившихся от матерей с хламидиозом, делят на три группы: малые формы, тяжелые формы и так называемый синдром инфицированности.
К малым формам относятся:
• конъюнктивиты;
• вульвовагиниты;
• везикулопустулезы, риниты, отиты, омфалиты - при смешанной инфекции.
Тяжелые формы внутриутробного инфицирования у новорожденного при хламидийной инфекции:
• хламидийная пневмония;
• генерализованный воспалительный процесс с развитием сепсиса и наличием нескольких очагов инфекции (пневмония, флебит пупочной вены, менингит, гепатит) - при смешанной инфекции.
При синдроме инфицированности локальные и генерализованные проявления внутриутробной инфекции отсутствуют. Отмечаются нарушения адаптационных процессов у новорожденных, изменение цвета кожи, снижение мышечного тонуса, неустойчивость рефлексов, пролонгированная желтуха, первоначальная потеря массы тела на 10% и более, медленное ее восстановление с повторным падением.
Профилактика и лечение хламидиоза при беременности. Лечение хламидиоза при беременности имеет определенные сложности, что связано с особенностями течения заболевания, сопутствующими нарушениями функции плацентарной системы, возможностью неблагоприятного воздействия на плод традиционных схем лечения.
Антибактериальная терапия проводится препаратами из группы макролидов: джозамицин, азитромицин. В случае индивидуальной непереносимости вышеуказанных препаратов допустимо применение цефалоспоринов III генерации.
Местная терапия. У 95% больных с хламидийной инфекцией имеются различной степени выраженности дисбиотические нарушения микробиоценоза, сопровождающиеся повышением рН вагинального содержимого до 5,9. Кроме того, у больных с урогенитальным хламидиозом часто отмечается значительная контаминация дрожжевыми грибами рода Candida. Эти результаты свидетельствуют о необходимости комбинированного применения антибиотиков, эубиотиков и противомикотических препаратов. Местная терапия включает санацию влагалища с последующим назначением эубиотиков внутрь и местно.
Иммуномодуляторы и интерферонокорректоры. Характерной чертой хламидийной инфекции является изменение функциональной активности иммунной системы, наблюдаются отклонения в уровне циркулирующих иммунных комплексов, угнетение клеточного иммунитета, снижение фагоцитарной активности полинуклеаров крови и макрофагов, угнетение активности неспецифических факторов защиты организма. С целью профилактики иммунных нарушений, сопутствующих хламидиозу, назначаются препараты лактофлоры (бифидобактерии бифидум, высушенные лактобактерии,
флорадофилус), которые не только корректируют микробиоценоз желудочно-кишечного тракта, но посредством стимуляции тимусзависимых зон мезентериальных лимфатических узлов активируют иммунный ответ. Иммуномодулирующими свойствами обладают растительные адаптагены, которые повышают общую неспецифическую резистентность организма к инфекции. С высокой эффективностью применяется препарат рекомбинантного интерферона.
Профилактика нарушений функции фетоплацентарного комплекса. Для улучшения маточно-плацентарного кровотока используют вазоактивные препараты и антиагреганты. В качестве метаболической терапии назначается диета с повышенным содержанием белка, кисломолочных продуктов с одновременным применением энзимных препаратов. В качестве препаратов, активизирующих метаболизм, применяют токоферола ацетат (витамин Е), гепатопротекторные средства.
Сифилис
Врожденный сифилис развивается в результате трансплацентарного распространения Treponema pallidum от матери к плоду. При свежих формах инфекции у матери риск заражения плода относительно высок по сравнению с риском заражения в поздней стадии болезни. Заражаются практически все дети, матери которых страдают во время беременности ранними стадиями нелеченного сифилиса, причем уровень смертности весьма высок. Ранее считалось, что Т. pallidum начинает проникать через плаценту после 18-20 нед беременности, когда исчезает слой клеток Лангерганса. В настоящее время доказано, что трансплацентарное инфицирование плода может иметь место и раньше, но при этом вследствие иммунологической незрелости плода отсутствует типичная реакция на инфекцию. Применение соответствующих методов окрашивания обнаруживает спирохеты у эмбрионов при прерывании беременности в I триместре.
Заражение в раннем фетальном периоде завершается мертворождением с мацерацией и водянкой плода. Обычно выкидыш имеет характерный вид: спавшийся череп, выдающийся живот, гепатоспленомегалия, пузырьковые поражения кожи, СЗРП. Гистологически характерны ареактивные некрозы в органах со скоплением спирохет в виде гнезд или клубочков в центрах некротических очагов. Пролиферативные изменения не свойственны. В последе превалируют очаговый виллузит с характерным эндартериитом по типу обли-
терационной ангиопатии, а также различные варианты незрелости ворсинчатого дерева.
Клинические проявления. Врожденный сифилис является полисистемным заболеванием, значительно различающимся по тяжести и многообразию форм. Развивается у 50% новорожденных, рожденных от матерей с первичным или вторичным нелеченным во время беременности сифилисом (остальные 50% - мертворожденные, глубоко недоношенные и умершие в раннем неонатальном периоде). Его проявления напоминают вторичный сифилис.
Проявления врожденного сифилиса
1. Выкидыш или мертворождение: мацерированный плод, спавшийся череп, выдающийся живот, гепатоспленомегалия, водянка плода, пузырьковые кожные проявления.
2. Водянка плода.
3. Патологически увеличенная плацента (ребенок может быть нормальным, явно инфицированным или мертворожденным).
4. Преждевременные роды.
5. СЗРП.
6. Слизисто-кожные проявления: упорный ринит, макулопапулезная, чешуйчатая или буллезная сыпь, обычно на ладонях и ступнях.
7. Гепатоспленомегалия, лимфаденопатия.
8. Анемия, тромбоцитопения
9. Желтуха (гепатит и/или гемолиз).
10. Костные поражения: симметричный остеохондрит, периостит, остеомиелит длинных костей, черепа, позвоночника и ребер. Типичная рентгенологическая картина, в последствии может развиться псевдопаралич.
11. Поражение центральной нервной системы, обычно бессимптомное. На поражение указывают изменения в спинномозговой жидкости.
Большинство живорожденных детей выглядят здоровыми, у некоторых имеются везикулезно-буллезные высыпания на ладонях и подошвах, однако спустя 4 дня после рождения могут появиться следующие симптомы заболевания:
1) синдром, сходный с гриппом:
- менингеальные симптомы;
- слезотечение (воспаление радужной оболочки);
- отделяемое из носа; слизистые оболочки гиперемированные, отечные, эрозированые;
- ангина (на слизистой глотки имеются папулы);
- генерализованная артралгия (из-за болей отсутствуют активные движения в конечностях - псевдопаралич Парро; на рентгенограмме - явления остеохондрита, часто отмечается периостит, в частности больших берцовых костей (саблевидные голени);
2) увеличение всех групп лимфатических узлов:
- шейные, локтевые, паховые, подмышечные, подколенные;
- гепатоспленомегалия (в тяжелых случаях - анемия, пурпура, желтуха, отеки, гипоальбуминемия);
3) высыпания:
- пятнисто-папулезные;
- слияние папулезных поражений с образованием широких кондилом.
Профилактика. Профилактика врожденного сифилиса сводится к проведению скринингового обследования беременных в целях своевременного выявления больных. При установлении диагноза в I триместре беременности показано ее прерывание в виду того, что инфицирование в ранние сроки беременности приводит к формированию у плода тяжелых поражений. При выявлении сифилиса в поздние сроки беременности проводят лечение, согласно рекомендациям МЗ РФ, по общепринятым схемам в зависимости от стадии течения заболевания.
При подозрении или подтвержденном диагнозе врожденного сифилиса требуется изоляция новорожденного до начала специфической терапии и в течение еще 24 ч с момента ее начала.
Лечение. Специфическую терапию проводят у новорожденных в следующих клинических ситуациях:
• если лечение матери было неадекватным;
• если оно проводилось в последние 4 нед беременности;
• если о нем ничего не известно;
• если для лечения применялись препараты, отличные от пенициллина.
Кроме того, учитывают результаты реагиновых тестов. Более высокий, чем у матери, титр антител указывает на активный инфекционный процесс. Титр антител следует контролировать в динамике, поскольку он может свидетельствовать лишь о трансплацентарном переходе материнских антител к плоду. Если титр антител снижается в первые 8 мес жизни, то новорожденный не
инфицирован. При положительном результате теста лечение проводят в тех наблюдениях, когда нет возможности контролировать титры антител в динамике.
Препаратом выбора для лечения врожденного сифилиса является пенициллин G (прокаинпенициллин, бензатинпенициллин). Расчет суточной дозы препарата производят в зависимости от массы тела новорожденного и его возраста.
Контроль за эффективностью лечения проводят по результатам количественных нетрепонемных тестов, которые проводят в возрасте 3, 6 и 12 мес. На эффективность лечения указывает отрицательный результат тестов. Сохранение и увеличение титра антител требует дальнейшего обследования и проведения повторного лечения.
Вирусный гепатит
Причиной острого вирусного гепатита могут являться по крайней мере пять различных агентов, однако инфекционные поражения печени вызываемые вирусом Эпштейна-Барр, цитомегаловирусом и вирусом желтой лихорадки, считаются отдельными болезнями и обычно не подразумеваются при употреблении термина «острый вирусный гепатит».
Выделяют:
• вирусный гепатит А;
• вирусный гепатит В;
• вирусные гепатиты ни А ни В (спорадический и эпидемический), в том числе гепатит С (HCV);
• вирусный гепатит D (одновременное инфицирование с гепатитом В - ко-инфекция и последовательное инфицирование с гепатитом В - суперинфекция).
Вирус гепатита А (HAV) относится к роду энтеровирусов семейства пикорновирусов. РНК-содержащий вирус, состоит из безоболочечного вириона.
Вирус гепатита В (HBV) является наиболее изученным. Принадлежит к гепадновирусам и имеет более сложное строение, чем вирус гепатита А. Инфекционная частица состоит из сердцевины (кора) и внешней оболочки (капсида). В состав вириона входит кольцевая двухцепочечная ДНК и ДНК-полимераза; репликация вирусных частиц происходит внутри ядер инфицированных гепатоцитов.
По крайней мере четыре различных системы антиген-антитело связаны с вирусом гепатита В.
1. Поверхностный АГ (HBsAg, австралийский АГ) связан с белковой оболочкой вируса. Обнаружение его в плазме крови позволяет диагностировать острый гепатит В и означает, что кровь больного стала потенциальным источником инфицирования. HBsAg выявляется в инкубационном периоде (за 1-6 нед до развития клинических и биохимических признаков болезни) и исчезает при выздоровлении. Соответствующие антитела (анти-HBs) можно обнаружить значит позже, через недели или месяцы после клинического выздоровления, их присутствие указывает на перенесенную инфекцию и относительную защиту в будущем. В 10% HBsAg продолжает обнаруживаться после острой фазы, а соответствующие антитела не появляются - у таких больных обычно развивается хронический гепатит или они становятся бессимптомными носителями вируса.
2. Коровый АГ (HBcAg) ассоциируется с сердцевиной (кором) вириона. Может быть обнаружен в инфицированных клетках печени, а в плазме выявляется лишь в том случае, если с помощью специальных методик разрушают вирусные частицы. Соответствующие антитела (анти-HBc), как правило, обнаруживают в начале периода манифестации; впоследствии их титр постепенно снижается. Наличие АТ-HBc, наряду с АТ-HBs, указывает на предшествующее инфицирование.
3. Антиген е (HBeAg), по-видимому, представляет собой пептид, входящий в состав вирусного кора. Обнаруживается только в HBsAg- положительной плазме. Присутствие свидетельствует об активной репликации вируса и сочетается повышенной инфицирующей способностью крови и вероятностью развития хронического поражения печени.
Вирус гепатита D (HDV, дельта фактор) является уникальным. Его РНК дефектна, вследствие чего данный вирус способен реплицироваться только в присутствии HBV. Гепатит D встречается либо как сочетанная инфекция при остром гепатите В, либо как суперинфекция при достоверно хроническом гепатите В. Инфицированные гепатоциты содержат дельта-частицы, покрытые HBsAg. Клинически инфекция проявляется необычно тяжелым течением острого гепатита В.
Термин «гепатит ни А ни В» (NANB) был предложен для обозначения инфекций не связанных с вирусами А- и В-типа. Относительно недавно идентифицирован специфический одноцепочечный РНКвирус, подобный флавивирусам (вирус гепатита С), являющийся
причиной большинства посттрансфузионных и спорадических случаев гепатита NANB. Особенностью НCV является чрезвычайно высокая гетерогенность его генома. Идентифицировано, как минимум, шесть основных генотипов вируса. АТ к НСV часто появляются в плазме крови через несколько месяцев после острой инфекции. Затем титры постепенно уменьшаются, если только инфекция не становится хронической (что имеет место в 50%). Вирус HCV идентифицируется в плазме с помощью сложной методики, соответствующий АГ выделяется из гепатоцитов.
Вирус гепатита А распространяется преимущественно фекально-оральным путем, также возможно инфицирование через кровь и продукты среции. Источником инфекции является только больной в ранней стадии болезни - вирусоносительство и хронические формы инфекции исключаются. Продромальная (преджелтушная) стадия характеризуется острым повышением температуры, ознобом, головной болью, диспепсическими расстройствами. В этой стадии часто отмечается кожный зуд, что сопровождается увеличением размеров печени, повышением уровня трансфераз в крови за 5-7 дней до появления желтухи. Нередко инфекция протекает бессимптомно.
Вирус гепатита В обычно передается парентерально: через зараженную кровь и ее производные. Возможно инфицирование при нанесении татуировки. Сохраняется высокий процент передачи в среде наркоманов, риск повышен для больных на гемодиализе и больничного персонала, контактирующего с кровью. Встречается непарентеральное распространение половым путем. Хронические носители HBV служат резервуаром инфекции.
Инфицирование HBV сопровождается широким спектром поражений печени - от субклинического носительства до острого и хронического гепатита, цирроза и гепатоцеллюлярной карциномы. Вслед за длительным периодом инкубации (от 6 нед до 6 мес) появляются признаки острой инфекции. Преджелтушный период, в отличие от гепатита А, продолжается дольше и характеризуется постепенным началом с артралгиями, уртикарной сыпью, диспепсическими и астеническими нарушениями, нарастает гепатолиенальный синдром. При тяжелых формах заболевания повышается температура. В крови - повышенные уровни трансаминаз;определяется HBsAg, HBеAg и
АТ-НВс.
С появлением желтухи нарастает интоксикация, диспепсические, астенические проявления, еще более - гепатолиенальный синдром.
Течение желтухи более выражено. При тяжелом течении может развиться геморрагический синдром, острая печеночная энцефалопатия с переходом в кому и даже летальным исходом.
У беременных больных гепатитом В отмечается высокая частота преждевременных родов и гестоза. Более чем у 50% женщин в последе обнаруживаются воспалительные изменения.
Гепатит ни Ани В (NANB) имеет вариант, близкий к гепатиту А, преимущественно распространяющийся в условиях водных вспышек. Вариант, близкий к гепатиту В, обычно с более коротким инкубационным периодом часто ведет к формированию хронических гепатитов.
Наконец, встречаются смешанные варианты инфекции (А и В, В и D, В и ЦМВ, В и ВИЧ).
Средняя продолжительность инкубационного период при заражении гепатитом А - 2-6 нед, гепатитом В - 6-25 нед, ни А ни В - 2-25 нед. Чаще болеют дети и молодые взрослые, однако заболевание может встречаться в любом возрасте.
Вирусный гепатит - наиболее частая причина желтухи во время беременности. Обычно он протекает относительно легко, но при недостаточности питания может встречаться тяжелая эпидемическая форма гепатита ни А ни В. Материнская смертность 0,64-1,79%, однако может достигать 15,6% (Фарбер Н.А. и соавт., 1990). Более тяжело гепатит протекает во второй половине беременности, что связывают с изменениями гормонального фона, более выраженными явлениями холестаза
Врожденный вирусный гепатит возникает редко, при остром или хроническом гепатите В матери во время беременности; также источником внутриутробной инфекции может быть мать с бессимптомной формой гепатита (антигеноносительница). Для фетального гепатита характерен полиморфизм гепатоцитов с образованием многоядерных клеток-симпластов, а также холестазы (внутриклеточные и внутриканальцевые), формирование аденоматозных структур и билиарного некроза при скудной лимфоцитарной инфильтрации портальных трактов. Тяжелый гепатит у матери может вести к антенатальной смерти плода. Макроскопически в последе отмечается желтоватая окраска оболочек, плодной поверхности плаценты, гистологически - у выкидышей регистрируются многочисленные клетки КащенкоХофбауэра в строме ворсин плаценты и оболочек, поглощающие билирубин, при минимальных воспалительных изменениях.
Убедительных данных о тератогенности гепатита в I триместре беременности не имеется. Вирус гепатита В может передаваться новорожденному при родах или реже через плаценту. В I и II триместрах беременности острый гепатит В редко передается плоду (5%). Передача через плаценту окончательно не установлена и наиболее вероятна у матерей, положительных по е-антигенам, которые являются хроническими носителями поверхностного АГ гепатита В (HBsAg), либо заболели гепатитом в III триместре. При заболевании в III триместре вероятность инфицирования плода составляет 60-70%. Чаще всего заражение происходит во время родов вследствие микротрансфузий крови от матери к плоду или в результате контакта ребенка с инфицированными выделениями матери при прохождении через родовые пути. Положительный тест на выявление HBeAg (отражает высокую степень инфицированности) связан с 80-90% вероятностью передачи инфекции плоду. Более 85% новорожденных от таких матерей становятся хроническими носителями. Если у матери обнаруживаются антитела к HBeAg (их наличие свидетельствует о разрешении инфекции), риск инфицирования составляет лишь 25%. Возможно инфицирование в постнатальном периоде (с молоком, слюной)
Инфицированные новорожденные часто становятся носителями НBV и имеют субклиническое нарушение функции печени. Наблюдения явного неонатального гепатита редки.
Прогноз. Гепатит А обычно излечивается спонтанно через 4- 8 нед - в большинстве случаев не требует специального лечения. Ограничение диеты и физической активности не требуется. Частота выкидышей не превышает таковую в популяции. Плод практически не подвержен риску инфицирования и профилактики новорожденному не требуется.
При гепатите В прогноз менее благоприятен, чем при А. Особенно после переливания крови, когда смертность может достигать 10-15%; в 5-10% формируется хроническая форма. Летальность у беременных в 3 раза выше, чем у небеременных. Заболеваемость новорожденных гепатитом - 45-62%.
Самую большую опасность для беременных представляет эпидемический вариант гепатита NANB во II и III триместре беременности. Осложнения: выкидыши, преждевременные роды, высокая материнская летальность, заболеваемость новорожденных и перинатальная смертность.
Профилактика инфицирования и лечение. Личная гигиена помогает предотвратить гепатит А. В случае контакта беременной с больным в течение 7-10 дней следует ввести стандартный γ-глобулин 1,5-3,0 мл однократно в/м. В более поздние сроки применение препарата нецелесообразно.
Для предупреждения гепатита В следует ввести ограничение трансфузий, использование проверенной на HBsAg крови. Требуется скрининг доноров на HCVAg. Стандартный иммуноглобулин обеспечивает защиту против клинически выраженного инфицирования НAV и назначается тем, кто имеет бытовые контакты с установленным носителем.
Вакцинация против HBV приводит к выработке антител у здоровых реципиентов и снижает распространенность гепатитом на 90%. Больные на диализе, с циррозом печени и другими нарушениями иммунитета реагируют на вакцинацию хуже. Небольшая часть здоровых людей не отвечает образованием АТ-HBs.
Предконтактная вакцинация рекомендуется для лиц с высоким риском инфицирования (больные и сотрудники отделений диализа, персонал медицинских учреждений).
Обследование беременных на носительство HBsAg следует проводить уже на ранних сроках беременности.
При гепатите С роль перинатального инфицирования в распространении этой инфекции до конца не определена. Обнаружение РНК вируса гепатита С в сыворотках крови детей на 1-5-й день после рождения делают правомерным предположение о наличии пренатального инфицирования и при этой инфекции. В основе лечения гепатита С лежит интерферонотерапия (интерферон, индукторы интерферона), а также применение противовирусных препаратов.
При легком и среднетяжелом течении гепатита (любого) в I триместре беременности возможно продолжение беременности, так как к моменту родов женщина будет здорова и вероятность врожденных аномалий у ее ребенка не выше, чем у здоровой. При тяжелом течении гепатита после выздоровления в зависимости от особенностей течения инфекции и срока беременности рекомендуется ее прерывание: до 12 нед - медицинский аборт, после 12 нед - интраамниальное введение гипертонического раствора хлорида натрия, простагландина F2a; внутримышечно введением простагландина после предварительного (за 12 ч) расширения шейки матки ламинариями среднего размера.
В лечении важное значение имеет физический покой, сбалансированное питье, лечение угрозы преждевременного прерывания беременности, при возможности - смещение времени физиологических родов, несущие в разгар желтухи не только нежелательную физическую нагрузку, но и внезапную гормональную перестройку, которая может вывести организм из компенсированного относительного равновесия. Показана осторожная инфузионная дезинтоксикационная терапия под контролем диуреза. При задержке жидкости применяют мочегонные препараты. Короткий курс глюкокортикоидов - как составляющая часть комплекса мер по дегидратации при развивающемся отеке мозга. Назначение кортикостероидной терапии нецелесообразно и даже может способствовать нарастанию гепатоцитодистрофии.
Дети, родившиеся от HBsAg-позитивной матери, независимо от наличия у нее в сыворотке крови HВe-антигена или антител, должны получать профилактическое лечение сразу после рождения иммуноглобулином против гепатита В (HBIg), после чего им необходимо провести трехкратную вакцинацию рекомбинантной вакциной против вируса гепатита В. Не рекомендуется изолирование новорожденных от матерей и отказ от грудного вскармливания, особенно после введения HBIg и противовирусной вакцины. Если HBsAg экскретируется с грудным молоком в целях профилактики инфицирования в период новорожденности грудное вскармливание не показано.
Лечение новорожденных с острым гепатитом В симптоматическое при адекватном питании; ни стероиды, ни HBIg не эффективны. Необходима изоляция инфицированного новорожденного и соблюдение крайней осторожности при работе с его кровью и сретами.
ПРЕДГРАВИДАРНАЯ ПОДГОТОВКА И ВЕДЕНИЕ БЕРЕМЕННОСТИ
Таким образом, внутриутробные инфекции представляют серьезную опасность для жизни и здоровья плода и новорожденного, часто имеют неблагоприятные отдаленные последствия. Диагностика и лечение инфекционных заболеваний у беременных представляет значительные трудности, обусловленные стертостью, многообразием и неспецифичностью клинических проявлений, сложностями получения материала для лабораторных исследований, невозможностью широкого применения лечебных препаратов.
В связи с вышеизложенным особое значение приобретают методы профилактики ВУИ, основанные на предупреждении и лечении инфекции у матери. Наиболее перспективным в этом направлении является проведение предгравидарной подготовки супружеских пар с последующим последовательным осуществлением лечебно-диагностических мероприятий во время беременности.
Предгравидарная подготовка должна включать:
• выделение группы риска на основе данных анамнеза и результатов клинического обследования, выявление сопутствующих экстрагенитальных заболеваний;
• комплексное обследование с изучением иммунного, гормонального, микробиологического статуса;
• этиотропную антибактериальную или противовирусную терапию;
• проведение соответствующей коррекции выявленных нарушений микроценоза половых путей с последующим назначением эубиотиков;
• лечение заболеваний с применением иммуностимулирующей и интерферонкорригирующей терапии, а также физиотерапии;
• метаболическую терапию;
• коррекцию нарушений менструального цикла и сопутствующих эндокринопатий;
• лечение полового партнера при наличии заболеваний передаваемых половым путем.
Во время беременности в сроках до 12, а также в 18-20, 28-30 и 37-38 нед у беременных этой группы показана оценка состояния микроценоза влагалища, до 12 нед (далее по показаниям в 18-20 и 37-38 нед) - выявление возбудителей заболеваний, передаваемых половых путем, и определение титра специфических Ig к вирусным и бактериальным агентам. При выявлении инфекций проводится соответствующее лечение, которое подбирается с учетом срока беременности и возможного влияния препаратов на развитие плода.
Регулярное эхографическое, допплерометрическое и кардиотокографическое исследование позволяет своевременно диагностировать формирующуюся фетоплацентарную недостаточность, осуществлять лечение и контроль за его эффективностью.
Проведение предгравидарной подготовки и мероприятий по выявлению угрожаемых по развитию внутриутробных инфекций
позволяет снизить частоту внутриутробных инфекций в 2,4 раза. Одновременно уменьшается число осложнений беременности и родов (особенно преждевременного прерывания беременности, а также фетоплацентарной недостаточности), что способствует снижению общей заболеваемости новорожденных в 1,5 раза.