Клиническая иммунология : учебник / под ред. А.М. Земскова. - 2008. - 432 с.
|
|
|
|
ГЛАВА 9. МОДУЛЯЦИЯ ИММУННОЙ РЕАКТИВНОСТИ
Под модуляцией (коррекцией) понимают стимуляцию заниженных и снижение завышенных значений показателей иммунного статуса. Реализуется четыре основных направления иммунокоррекции:
- коррекция гормонами и медиаторами иммунной системы (тимические факторы, миелопептиды, цитокины типа интерферона, факторов переноса, ИЛ, колониестимулирующих факторов, факторов взаимодействия лимфоцит-макрофаг и др.);
- иммунная инженерия (трансплантация органов и тканей иммунной системы: костный мозг, клетки эмбриональной печени, тимуса, комплекс тимус-грудина и т.д.), введение γ-глобулинов или иммуноглобулинов отдельных классов, плазмы крови);
- коррекция иммуностимуляторами естественного происхождения (вакцины, липополисахариды, бактериальные смеси, а также синтетические препараты - левамизол, диуцифон, полианионы, изоприназин и др.);
- использование лазерного и ультразвукового облучения, сорбционные методы, плазмаферез и др.
9.1. ФАРМАКОЛОГИЧЕСКАЯ МОДУЛЯЦИЯ
Список модуляторов иммунной системы в настоящее время превышает 200 наименований и продолжает увеличиваться. Общепринятой классификации иммунотропных средств пока нет. Существует их деление по индуцируемым эффектам:
Иммунорегуляция - совокупность медикаментозных и немедикаментозных вмешательств, определяющих высоту, интенсивность, продолжительность развития иммунных реакций.
Иммунотерапия - использование с лечебной целью сывороточных, других фармакологических, немедикаментозных воздействий.
Иммуностимуляция - неспецифическое усиление иммунных реакций.
Иммуносупрессия (супрессия) - неспецифическое подавление иммунных реакций.
Иммунокоррекция (модуляция) - исправление дефектного функционирования иммунной системы, проявляющееся в усилении ослабленного или торможении стимулированного иммунитета.
Адъювация - неспецифическое усиление иммунного ответа на конкретный Аг (вакцину, анатоксин).
Иммуноадаптация - комплекс мероприятий по оптимизации иммунных реакций организма при перемене геоклиматических, экологических, световых условий проживания человека.
Иммунореабилитация - система мер по возвращению иммунного ответа к исходному уровню после состязаний, экстремальных физических нагрузок, психоэмоционального напряжения, в результате стрессов у лиц - участников и ликвидаторов последствий техногенных и природных катастроф, после лучевой, химической терапии и др. Иммунопотенцирование - эффект стимуляции или угнетения иммунного ответа в зависимости от времени введения по отношению к Аг.
Иммуностабилизация - обусловленность веществами, стимулирующими только угнетенный и не влияющими на нормальный иммунитет.
Иммунозамещение - использование химических соединений, замещающих дефицит естественных биологических факторов.
По происхождению: из растительного, микробного, животного сырья, синтетические и др. модуляторы.
Требования к модуляторам: минимальная активность; не вызывать побочных действий (злокачественного перерождения клеток) и не потенцировать их свойств у других препаратов; не вызывать аллергизации и индукции аутоиммунных реакций; легко метаболизироваться и выводиться из организма; совместимость с другими препаратами; предпочтительно пероральный способ введения, естественное происхождение, наличие иммуномодулирующих свойств.
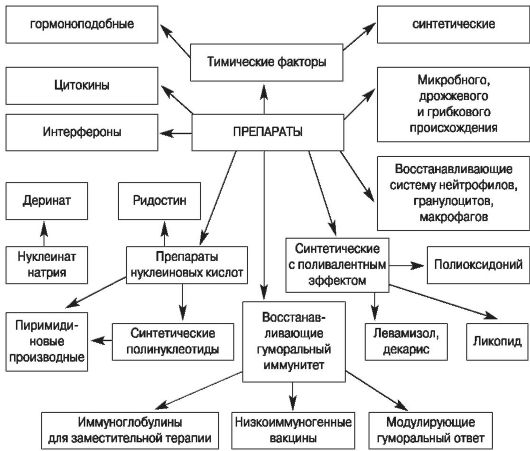 Рис. 10. Классификация
основных иммунотропных препаратов, используемых для восстановления
нормального функционирования дефектной иммунной системы (по Нестерову
И.В. и Сепиашвили Р.И., 2000)
Рис. 10. Классификация
основных иммунотропных препаратов, используемых для восстановления
нормального функционирования дефектной иммунной системы (по Нестерову
И.В. и Сепиашвили Р.И., 2000)
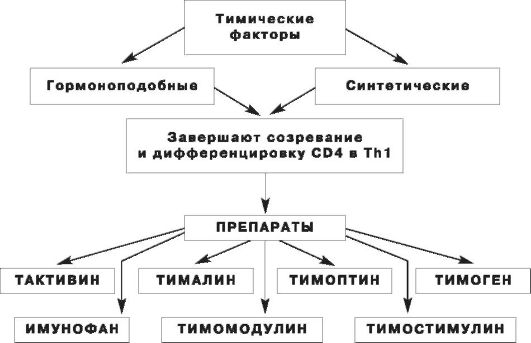 Рис. 11. Характеристики тимусных модуляторов
Рис. 11. Характеристики тимусных модуляторов
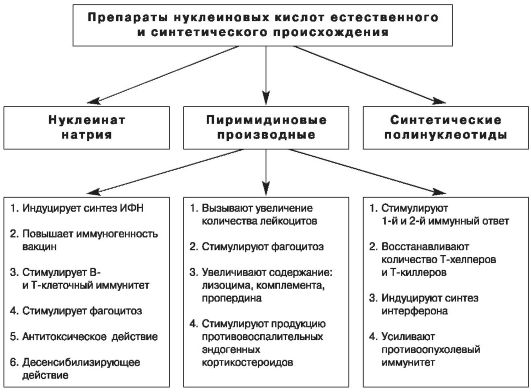 Рис. 12. Характеристики нуклеиновых модуляторов
Рис. 12. Характеристики нуклеиновых модуляторов
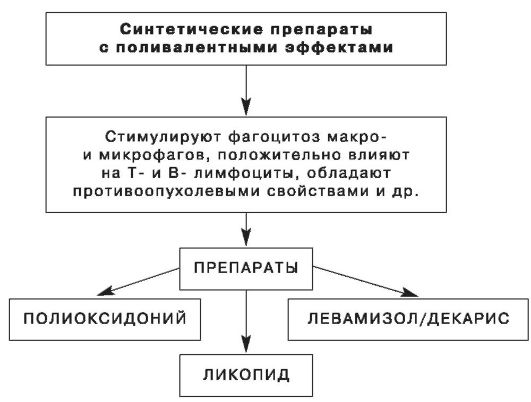 Рис. 13. Характеристики синтетических препаратов (по Б.Н. Райскис и соавт.)
Рис. 13. Характеристики синтетических препаратов (по Б.Н. Райскис и соавт.)
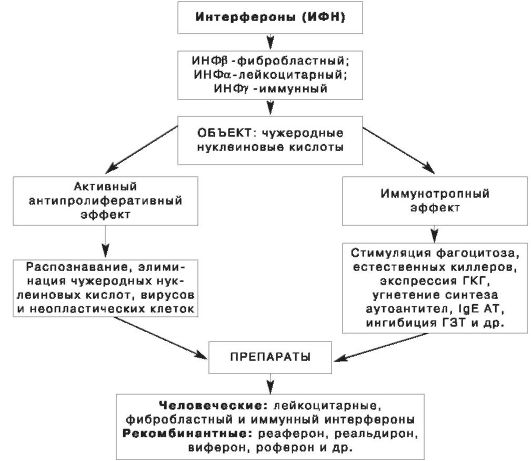 Рис. 14. Характеристики интерферонов (по Б.Н. Райскис и соавт.)
Рис. 14. Характеристики интерферонов (по Б.Н. Райскис и соавт.)
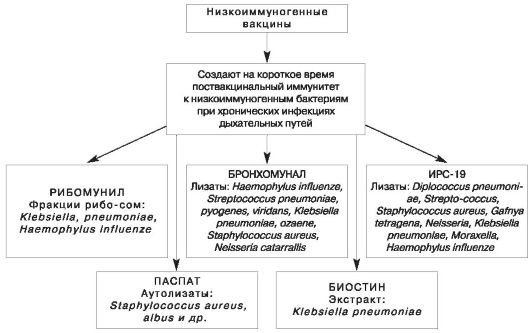 Рис. 15. Характеристики низкоиммуногенных вакцин (по Б.Н. Райскис и соавт.)
Рис. 15. Характеристики низкоиммуногенных вакцин (по Б.Н. Райскис и соавт.)
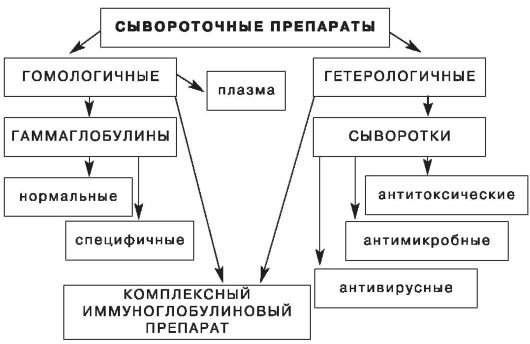 Рис. 16. Характеристики сывороточных препаратов
Рис. 16. Характеристики сывороточных препаратов
9.2. ИММУНОДЕПРЕССИВНЫЕ ПРЕПАРАТЫ, ЦИТОСТАТИКИ
Препараты иммуносупрессорного действия обладают общим свойством подавлять размножение клеток путем блокады или деструкции ядерной ДНК, в результате чего прерывается необходимая для клеточного деления ее репликация. Наиболее широкое применение эти препараты получили в онкологической практике, где они используются как антипролиферативные агенты в больших дозах. Кроме того, их использование необходимо для подавления ответной реакции реципиента при трансплантации органов. Этим удается продлить период приживления трансплантата, предупредить криз отторжения или купировать его. В последние годы иммуносупрессорные препараты также стали использовать в лечении больных аутоиммунными заболеваниями, применяя их в малых дозах длительное время (месяцы, годы). Положительный результат достигается иногда через несколько недель или месяцев от начала терапии.
1. Антиметаболиты
Антагонисты пурина - 6 меркаптопурин (6-МП), азатиоприн. Антагонисты пиримидина - 5-фторурацил, 5-бромдез-оксиуридин. Антагонисты фолиевой кислоты - аминоптерин, метотрексат.
Антиметаболиты имеют структуру, подобную физиологически важным соединениям (аминокислотам, нуклеотидным основаниям, витаминам), но не обладают их свойствами. Включаясь в обмен веществ, они обусловливают синтез соединений, не усваиваемых клеткой и блокирующих определенные реакции обмена веществ.
2. Алкилирующие соединения
Циклофосфан, хлорбутин, сарколизин. In vitro эффективность препаратов этой группы не выражена. Алкилирование происходит только после отщепления циклического фосфорсодержащего соединения. Иными словами, иммуносупрессорный эффект обусловливают не сами препараты, а продукты их деградации в организме.
3. Антибиотики
Наряду с их действием на бактерии, грибы они наделены цитостатическими и иммуносупрессорными свойствами. По механизму действия эти препараты представляют разнородную группу.
В клинике активно применяют митомицин С, дактиномицин, хлорамфеникол, даунорубицин.
4. Алкалоиды
Колхицин, винбластин, винкристин.
5. Другие препараты
L-аспарагиназа - это фермент, вырабатываемый многими организмами. Чаще его получают из кишечной палочки. Применяется при лечении аутоиммунных заболеваний и трансплантации.
Сульфазин, салазопиридазин относятся к группе сульфаниламидных препаратов, в последние годы применяются в комплексном лечении аутоиммунных заболеваний как иммунодепрессоры и противовоспалительные средства.
Циклоспорин представляет собой грибковый метаболит, пептид, состоящий из 11 аминокислот. Имеет несколько разновидностей: А, В, С, F, D, Н и др. Обладает способностью подавлять Т-клеточный иммунитет через супрессию Т-лимфоцитов, не затрагивая В-звено.
Гепарин и аминокапроновая кислота наделены антикомплементарным действием, подавляя комплементзависимые реакции; используются, например, при аутоиммунных гемолитических анемиях.
γ-глобулин - при введении Аг с большими концентрациями этого препарата возможна индукция иммунного паралича.
Ферменты, например, рибонуклеаза, дезоксирибонуклеаза, ксанти-ноксидаза тормозят образование АТ.
Минералокортикоиды (альдостерон) наделены определенными иммуносупрессорными свойствами. Побочные явления наблюдают в 20-30% случаев в виде нефрита, экзантемы.
6. Кортикостероиды
В эту группу входят производные прегнана. Основные мишени препаратов и фармакологическое действие глюкокортикостероидов:
- индукция ферментативной активности;
- углеводный обмен;
- аминокислотный обмен;
- стабилизация клеточных мембран;
- защита лизосомальных мембран;
- торможение диффузии через биомембраны;
- усиление действия катехоламинов;
- торможение синтеза, высвобождение и действие медиаторов при воспалительных процессах и аллергии.
7. Облучение
Действие лучевой терапии основано на ионизации, вызываемой рентгеновскими и γ-лучами с образованием активных радикалов (HO2+, Н+, НзО+) воды внутри клеток. Они и обусловливают изменения нуклеинового обмена, что влечет за собой расстройства обмена белков и функции клеток.
Высокие (летальные) дозы облучения (900-1200 рад) полностью исключают возможность осуществления любой иммунной реакции. Сублетальные дозы (300-500 рад) на длительное время лишают способности к иммунному ответу, в лимфатической ткани подавлены митозы и клетки повреждены, многие клетки некротизированы. Вслед за этим наступает длительный период инактивации митоза и пролиферации. После облучения количество клеток восстанавливается в течение 3 мес, CD19 (В)-лимфоцитов - 6 мес, CD3 (Т)-лимфоцитов - до 12 мес.
8. Антилимфоцитарная сыворотка
Антилимфоцитарная сыворотка (АЛС), антилимфоцитарный γ-глобулин (АЛГ). Эти препараты получают путем гетерологической иммунизации. В качестве Аг используют клетки селезенки, лимфоциты грудного протока, периферической крови, лимфатических узлов.
9. Хирургические методы лечения аутоиммунных заболеваний
Аутоиммунная гемолитическая анемия (спленэктомия), симпатическая офтальмия (энуклеация), аутоиммунный перикардит (перикардэктомия), аутоиммунный тиреоидит (тиреоидэктомия).
10. Показания для применения цитостатиков
- подтвержденный диагноз аутоиммунного заболевания;
- прогрессирующее течение;
- неблагоприятный прогноз;
- ситуация, когда другие терапевтические возможности исчерпаны;
- резистентность к глюкокортикоидам;
- противопоказания к ГКС, например, спленэктомия;
- развитие опасных для жизни осложнений аутоиммунных заболеваний (кровотечение, идиопатическая тромбоцитопеническая пурпура);
- преклонный возраст (по возможности).
11. Противопоказания к иммуносупрессорной терапии
- наличие инфекции (она может выйти из-под контроля);
- предстоящая операция (трансплантация почек);
- недостаточная функция костного мозга (опасен цитостатический эффект иммуносупрессоров);
- снижение функции почек, печени;
- беременность или желание иметь ребенка;
- грубые нарушения в иммунной системе.
Общие принципы назначения терапии
Обычно терапию начинают с больших доз. После достижения желаемого эффекта переходят на поддерживающий курс, составляющий 1/2-1/4 начальной дозы. Эффективность лечения оценивают специфическими для каждой нозоформы параметрами. Принято считать, что продолжительность терапии составляет минимум 3 нед, хотя возможны другие варианты. Исключение составляет метотрексат, который не следует применять свыше 4 нед. При обострении иммунных процессов дозы препаратов увеличивают. Почти все иммуносупрессорные средства применяют в комплексе с гормонами.
Общие побочные действия
1. Нарушение функции костного мозга. В первую очередь повреждаются клетки с высокой митотической активностью (гемопоэтические клетки).
2. Расстройства желудочно-кишечного тракта. Тошнота, рвота, рас-
стройства желудка. Могут быть желудочно-кишечные кровотечения (метотрексат).
3. Предрасположенность к инфекциям. В основе расстройств лежит повреждение кожного и кожно-слизистого барьера, подавление лимфатических защитных механизмов (лейкопения, снижение интенсивности фагоцитоза, угнетение воспалительных процессов), блокирование иммунных механизмов. Эти явления усиливаются при комплексировании с кортикостероидами.
4. Аллергические реакции. Они развиваются после приема АЛС и некоторых других препаратов. Чаще проявляются в виде кожных поражений эозинофилией и лекарственной лихорадкой.
5. Канцерогенный эффект. Помимо основного действия, иммуносупрессорные препараты блокируют механизмы, обеспечивающие элиминацию бластных клеток. Такие клетки, уже прошедшие процесс дифференцировки, не контролируются организмом и могут быть причиной формирования опухолей. Особенно часто эти процессы протекают у больных с «трансплантированными» опухолями.
6. Нарушение репродуктивной функции и тератогенные эффекты.
При назначении алкилирующих соединений существует опасность бесплодия как у женщин, так и у мужчин в 10-70% случаев. При приеме этих препаратов необходимо избегать беременности даже через 6 мес после прекращения курса лечения.
7. Остановка роста. При назначении препаратов детям может произойти задержка роста.
8. Прочие побочные эффекты. Алкилирующие производные индуцируют нарушения сперматогенеза, аменорею, легочные фиброзы. Миелосан - гиперпигментацию, потерю массы тела. Циклофосфамид - выпадение волос, геморрагические циститы. Антиметаболиты - нарушение функции печени. Алкалоиды барвинка - нейротоксическое действие, атаксию, моторные нарушения.
9.3. НЕМЕДИКАМЕНТОЗНАЯ ИММУНОМОДУЛЯЦИЯ
Широкое применение иммунотропных препаратов сдерживается ограниченностью выбора, дефицитом активных средств, в ряде случаев их значительной дороговизной, побочными действиями, нередко тяжелым течением заболеваний, резистентностью к медикаментозной терапии с сопутствующей лекарственной непереносимостью.
Одним из путей выхода из создавшегося положения является использование немедикаментозных воздействий. Известен имму-
ност имулирующий эффект ультразвука, магнитного поля, лазерного облучения, плазмафереза, ультрафиолетового облучения крови, иглорефлексотерапии, электро- и лазероакупунктуры, электромагнитного излучения дециметрового и миллиметрового диапазона. Весьма перспективной является экстракорпоральная иммунофармакотерапия, когда производится активизация стимулятором клеток крови in vitro, затем они отмываются от препарата и реинфузируются больному.
Виды нелекарственной иммуномодуляции представлены на рис. 17. Обозначения: НИЛИ - низкоинтенсивное лазерное излучение, ГБО - гипербарическая оксигенация, УФО крови - ультрафиолетовое облучение крови.
Гемосорбция, как метод извлечения из крови токсичных веществ с помощью активированного угля, в последние годы стала применяться в лечении неспецифических воспалительных заболеваний легких и других болезней. Вероятно, механизм действия гемосорбции основан на изменении функционального состояния рецепторов иммунокомпетентных клеток периферической крови, контактирующих в процессе гемоперфузии с гранулами активированного угля.
Этот метод усовершенствован в плане создания специфических сорбентов, обладающих высоким сродством к определенным патогенным или токсическим компонентам, подлежащим удалению из периферической крови. Наиболее специфическим в этом смысле является метод иммуносорбции, когда специфические АТ к токсичным или вред-
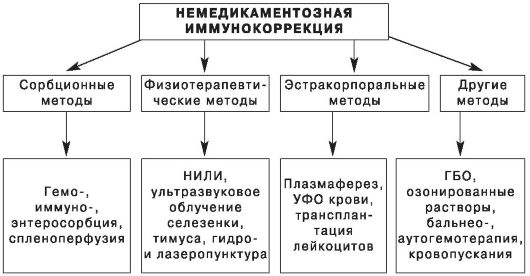 Рис. 17. Немедикаментозная иммунокоррекция
Рис. 17. Немедикаментозная иммунокоррекция
ным веществам в крови фиксированы на нерастворимом носителе, через который перфузируется кровь, содержащая эти вещества.
Энтеросорбция основана на связывании и выведении из желудочно-кишечного тракта с лечебной или профилактической целью экзогенных или эндогенных веществ, надмолекулярных структур и клеток. Необходимо отметить, что по своей эффективности, скорости выведения токсинов и метаболитов энтеросорбция уступает гемо- и иммуносорбции, а также плазмаферезу. Однако ее простота, безвредность и доступность расширяют сферу применения последней.
Спленоперфузия является одним из вариантов немедикаментозной иммунокоррекции. В качестве биологического иммуномодулятора используется ксеноселезенка. Как известно, этот орган играет существенную роль в фагоцитозе, обработке и представлении Аг макрофагами, в Т- и В-клеточных иммунных реакциях, формировании антиинфекционной резистентности, удалении иммунных комплексов, в активации СD8-клеток. Метод заключается в перфузии крови пациента через изолированную ксеноселезенку, чаще селезенку свиньи.
Низкоинтенсивное лазерное излучение нашло широкое терапевтическое применение практически во всех областях медицины.
В спектре действия НИЛИ находятся многочисленные факторы неспецифической антиинфекционной резистентности: лизоцим, система комплемента, фагоцитоз, интерферон; специфические иммунные реакции - антителообразующие клетки, иммуноглобулины, особенно IgG и IgА, СDЗ-лимфоциты, их регуляторные субпопуляции, СD19-клетки и т.д.
Экстракорпоральная иммунофармакотерапия представляет собой активацию каким-либо стимулятором иммунокомпетентных клетокрегуляторов у больного с патологическими процессами in vitro. Эта методика используется в тех случаях, когда у пациента сформирована лекарственная непереносимость к иммунотропным средствам, но и в то же время их назначение является жизненно необходимым. Обычно проведение экстракорпоральной фармакотерапии реализуется при крайне тяжелом состоянии больного для достижения оперативного иммунокорригирующего эффекта.
Плазмаферез - это дробная эксфузия крови, отделение ее клеток от плазмы с последующей реинфузией форменных элементов крови больному. Плазма удаляется и восполняется донорской или плазмоза-
мещ а ющими растворами: низкомолекулярными декстринами, поливинилпирролидоном, 5% альбумином и др.
Иммунокорригирующее действие ЛПФ (лечебный плазмаферез) реализуется следующими механизмами: элиминация избытка ЦИК, в том числе за счет деблокирования естественных путей выведения АТ, Аг, молекул средней массы, продуктов тканевого и клеточного распада; восстановление активности СDЗ-лимфоцитов в результате возможного деблокирования рецепторов и удаления ингибиторов СD8-супрессорной активности; усиление фагоцитарной активности нейтрофилов и альвеолярных макрофагов; нормализация энергетических ферментных систем лимфоцитов; увеличение сниженного количества СDЗ-лимфоцитов, СD8-лимфоцитов, СD4-лимфоци- тов, Т-киллеров, СD19-клеток, иммунных глобулинов основных классов и т.д.
Для усиления положительного действия ЛПФ используют УФОК. Среди множества механизмов этого немедикаментозного воздействия имеют значение: противовоспалительное, десенсибилизирующее, иммуностимулирующее, общеукрепляющее действие; активация клеточного и гуморального звеньев иммунитета, факторов неспецифической антиинфекционной резистентности, увеличение количества СDЗ- и СD19- клеток, повышение их активности, особенно Т-звена; потенцирование синтеза IgM; стимуляция системы комплемента; дезинтоксикационный эффект и т.д.
9.4. КЛАССИФИКАЦИЯ ИММУНОМОДУЛИРУЮЩИХ ВОЗДЕЙСТВИЙ
Классификация иммуномодулирующих воздействий включает:
1. Немедикаментозную иммунокоррекцию;
2. Фармакологическую:
- моноиммунокоррекцию - использование одного препарата;
- комбинированную - одновременное или последовательное применение нескольких модуляторов с различным механизмом действия:
1) местную и общую (сочетание местных и системных модуляторов);
2) активную адъювантную (сочетание вакцин/анатоксинов с адъ- ювантом/модулятором);
3) пассивную адъювантную (сочетание сыворотки/гаммаглобули- на с адъювантом/модулятором);
4) иммуно-метаболическую (сочетание модуляторов с метаболика- ми/адъювантами/антиоксидантами);
5) комплексную (сочетание вакцины/анатоксина с адъювантом/ модулятором и метаболиком/антиоксидантом);
6) альтернативную (сочетание иммунодепрессоров с иммуностимуляторами).
З. Фармако-немедикаментозную (сочетание фармакологических и немедикаментозных воздействий).