Онкология: учебник для вузов / Вельшер Л.З., Матякин Е.Г., Дудицкая Т.К., Поляков Б.И. - 2009. - 512 с.
|
|
|
|
ГЛАВА 9. ОПУХОЛИ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА
Среди опухолей ЖКТ описывают заболевания пищевода, желудка, толстой кишки. Опухоли тонкой кишки представляют собой редкую локализацию и при жизни редко распознаются. Только при далеко зашедших процессах лапаротомия иногда обнаруживает первичный очаг в тонкой кишке. Эти опухоли не являются визуальными, диагностика их довольно трудна. От интуиции врача зависит их своевременное распознавание. В зависимости от локализации образования, формы и скорости его роста развивается соответствующая клиническая картина. Клинические проявления опухолей ЖКТ длительное время бывают не яркими.
Рак пищевода обычно развивается медленно. Экзофитные его формы постепенно вызывают нарушение проходимости пищевода, т.е. дисфагию, которая по степени проявления бывает 4 степеней - от затруднения прохождения твердой пищи до непроходимости для жидкостей, т.е. полной обтурации просвета пищевода. Доброкачественные и экзофитные злокачественные опухоли клинически манифестируют одинаково. Часто эти явления сопровождаются гиперсаливацией, особенно при поражении верхних отделов пищевода. При эндофитных формах роста и изъязвлении опухоли наблюдаются прорастание опухоли в соседние структуры, прорастание возвратного нерва с появлением охриплости из-за неподвижности одной половины гортани. Разрушение стенки бронха сопровождается клинически проявлениями экзофагобронхиального свища.
Симптоматика рака желудка может сводиться в начальных стадиях к незначительным диспептическим проявлениям: после еды тяжесть в эпигастрии, отрыжка, утомляемость, отвращение к некоторым видам пищи, например мясу. Эти явления А.И. Савицкий предложил называть синдромом «малых признаков». Пальпаторно определяемая опухоль в эпигастрии обычно свидетельствует о далеко зашедшем опухолевом процессе.
Наиболее часто при раке ободочной кишки появляется боль в животе, причем при правосторонней локализации опухоли в 2- 3 раза чаще, чем при левосторонней. Может быть и бессимптомное
течение, и появление болей отмечается только при распространении опухоли за стенку кишки, при переходе опухоли на брюшину или соседние органы. В зависимости от локализации опухоли боли могут симулировать различные заболевания органов брюшной полости: хронический аппендицит, холецистит, язвенную болезнь желудка и двенадцатиперстной кишки, хронический аднексит. Для рака восходящего отдела толстой кишки характерно развитие болевого синдрома, приступов лихорадки, с явлениями лейкоцитоза, а также интоксикация и анемия. Нарушается пассаж содержимого кишечника. Поносы чередуются с запорами. К каловым массам могут примешиваться слизь, гной, отторгшиеся опухолевые массы. Развивается картина частичной или полной кишечной непроходимости. Для опухоли левой половины толстой кишки более характерна кишечная непроходимость, воспалительные инфильтраты, кровотечения.
В результате при раке всех отделов ЖКТ могут развиваться похудание, анемия. Последняя при раке желудка имеет природу железодефицитной, из-за недостатка витамина В12. При других локализациях опухолей она является следствием недостатка пластических средств для адекватного гемопоэза и интоксикации (при раке толстой кишки).
Истинную распространенность процесса обычно можно установить только после комплексного обследования. При опухолях ЖКТ особенно четко проявляются признаки объемного поражения полого органа, определяемые при рентгенологическом исследовании. Следует подчеркнуть, что рентгенологическое или эндоскопическое обследование ЖКТ показано при малейшем подозрении на опухоль. Длительное лечение по поводу так называемого «хронического гастрита или колита» создает предпосылки для развития инкурабельного процесса.
В качестве современных диагностических методов используют рентгенографию с контрастом. Пищевод и желудок осматривают при приеме контраста в режиме реального времени, пассаж контраста по тонкой кишке также изучают по мере прохождения преимущественно проксимальных отделов тонкой кишки. Толстый кишечник изучают путем наполнения контрастом с помощью клизмы. Иногда прибегают к приемам двойного контрастирования, когда кроме наполнения кишечника, вводят воздух в брюшную полость, тем самым удается детализировать объем и локализацию опухолевого конгломерата.
Эндоскопическое исследование пищевода, желудка, двенадцатиперстной кишки, толстого кишечника после соответствующей под- готовки стало обязательным способом обследования. Особую ценность при этой методике обследования представляет возможность прицельного забора материала из стенок полого органа в местах с подозрением на опухоль для морфологического исследования. Все шире применяется с диагностической целью эндоскопическое исследование брюшной и плевральной полости, средостения и забрюшинного пространства и др., когда после инсуфляции воздуха становятся обозримыми структуры этих областей.
Ультразвуковое исследование органов брюшной полости, забрюшинного пространства, шейно-надключичных зон является рутин- ным при обследовании по поводу опухоли ЖКТ. При необходимости выполняется КТ или МРТ средостения, печени, почек, легких, головного мозга и др., селективная ангиография сосудов и органов брюшной полости. При возможности используют позитронную эмиссионную томографию для оценки распространенности процесса.
Ведущими локальными факторами прогноза у радикально оперированных больных по поводу рака ЖКТ являются локализация опухоли в органе, степень прорастания стенки, анатомическая форма роста, гистологическое строение и степень дифференцировки, а также состояние регионарных лимфатических узлов.
Со стороны органов головы и шеи, как правило, можно наблюдать изменения только в далеко зашедших стадиях рака ЖКТ, которые проявляются следующими симптомами: бледность кожных покровов и слизистых оболочек вследствие анемии; снижение тургора кожи и сухость слизистых из-за нарушения питания. С одной стороны, появляется ломкость сосудов с мелкими петехиальными кровоизлияниями на слизистой оболочке полости рта из-за недостатка витаминов С и К, с другой стороны, отмечается склонность к тромбо- зу сосудов. Особенно яркими такие проявления бывают при далеко зашедших процессах с явлениями кахексии, нарушениями функции печени и почек. Присоединяются симптомы поражения органов, в которых развиваются метастатические опухоли: печень, почки, легкие, головной мозг. Проведение химиотерапии часто сопровождается появлением в полости рта и глотке эрозивно-язвенных высыпаний. Аналогичные изменения возникают по ходу всего желудочно-кишечного тракта, вызывая соответствующую симптоматику: диарея, кровь в стуле, болевые ощущения по ходу кишечника.
Метастаз Вирхова, обнаруживаемый в левой надключичной области в зоне проекции общего грудного лимфатического протока, свидетельствует о далеко зашедшем процессе с наличием отдаленных метастазов. При паллиативном лечении, наличии гастростомы, еюностомы в полости рта вегетирует патологическая флора - грибковая, гнилостная, но отсутствие питания через естественные пути скоро прекращает ее развитие. Элементарное соблюдение гигиенических мероприятий (чистка зубов, полоскание) способствует этому (см. также раздел «Симптоматическое лечение»).
Из последствий лечения злокачественных опухолей ЖКТ даже при отсутствии признаков рецидива следует остановиться на снижении иммунитета, склонности к простудным заболеваниям с проявлениями, в том числе, в области органов головы и шеи; а также на группе астенических состояний, имеющих различную «окраску». Чаще это эмоциональная лабильность, раздражительность, низкая интеллектуальная продуктивность, неприятное ощущение физической слабости при умственном или незначительном физическом напряжении.
9.1. РАК ПИЩЕВОДА
Рак пищевода занимает 8-е место в общей структуре заболеваемости злокачественными опухолями и 4-е среди новообразований пищеварительного тракта. Рак пищевода - болезнь преимуществен- но пожилых людей, мужчины болеют чаще. Из предрасполагающих факторов обычно называют курение, избыточное употребление алкоголя, недостаточное количество пищи, содержащей поливитамины и микроэлементы. Имеет значение привычка к употреблению очень горячей пищи (страдают верхние отделы пищевода). Эзофагит может стать основанием для развития рака кардиального отдела желудка. К предраковым заболеваниям пищевода относят хронический эзофагит, рубцовые стриктуры, язвы, полипы пищевода. Облигатным предаком является пищевод Барретта. На его фоне развиваются аденокарциномы. Это состояние характеризуется метапластическим замещением плоскоклеточного эпителия пищевода на железистый с формированием структур, соответствующих слизистой оболочке желудка, нередко с явлениями кишечной метаплазии.
На ранней стадии рака пищевода симптомы заболевания могут отсутствовать. К ранним проявлениям рака пищевода относятся
признаки рефлюкс-эзофагита, при котором развивается цилиндроклеточная метаплазия с последующим превращением в рак. Ранним проявлением рака может быть также боль при прохождении пищи по пищеводу из-за образования язв. Позже появляются явления дисфагии - затруднения прохождения пищи по пищеводу. Обычно это уже поздний симптом заболевания, свидетельствующий о значительном местном распространении опухоли с наличием отдаленных метастазов. Для каждого отдела пищевода регионарными считаются определенные группы лимфатических узлов.
Одним из определяющих факторов клинического прогноза является гистологическое строение и степень дифференцировки рака пищевода. В 87-95% случаев в пищеводе развивается плоскоклеточный рак разной степени дифференцировки, в остальных - аденокарцинома. Прогноз ухудшается по мере снижения степени дифференцировки.
Самой частой локализацией (до 60%) рака пищевода является среднегрудной отдел (от бифуркации трахеи до плоскости, расположенной несколько выше пищеводно-желудочного перехода), реже поражаются нижний (нижнегрудной и собственно пищеводно-желудочный переход - до 30%) отдел и верхнегрудной отдел, располагающийся от яремной вырезки до бифуркации трахеи (10%). Уровень расположения опухоли в пищеводе определяет тактику лечения. Обычно верхнюю границу опухоли отмечают при эндоскопическом исследовании по расстоянию от резцов. Локализация опухоли в шейном отделе пищевода, расположенном от нижнего края щитовидного хряща до уровня яремной вырезки, отмечается редко. Этот отдел пищевода чаще поражается при распространении опухолей соседних отделов (гортани, гортаноглотки, щитовидной железы).
В нижнем отделе пищевода чаще развивается аденокарцинома (в пищеводно-желудочном отделе). При нижнегрудной локализации чаще всего применяется хирургическое лечение, при среднегрудной - комбинированное и при верхнегрудной - лучевая терапия.
Различают
следующие анатомические формы роста рака пищевода: с преобладанием
экзофитного роста, с преимущественно эндо- фитным инфильтрирующим
ростом - язвенно-инфильтративный рак и диффузно-инфильтративный.
Экзофитные опухоли в большинстве случаев имеют небольшие размеры (до
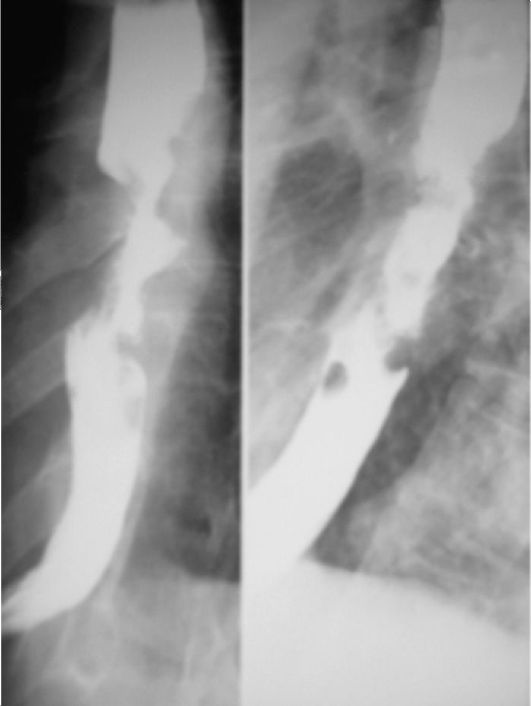
Рис. 9.1. Рак пищевода. Прослеживается неровный контур стенки пищевода в зоне расположения опухоли на фоне контрастного наполнения
Основную
группу составляют больные с эндофитной и язвенноинфильтративной формой
роста, которые одинаково часто встречаются в различных отделах
пищевода, чаще всего прорастают всю стенку пищевода и часто поражают
метастазами регионарные лимфатические узлы. Наименее благоприятно
развивается диффузноинфильтративный рак пищевода. Это опухоли, чаще
всего достигающие размеров
Регионарными для пищевода являются лимфоузлы глубокой шейной цепочки, паратрахеальные и трахеобронхиальные (для шейного отдела пищевода), заднесредостенные и предпозвоночные (для средней трети) и перикардиальные, диафрагмальные, преэзофагеальные (для нижней трети пищевода). Чаще всего поражение лимфоузлов отмечается при прорастании всей стенки пищевода, смешанной и эндофитной формах роста средней и низкой степени дифференцировки. При оценке стадии рака пищевода учитывают
глубину поражения стенки пищевода и поражение лимфатических узлов. Стенка пищевода состоит из следующих слоев: слизистая оболочка, подслизистый, мышечный и соединительнотканный слои, серозная оболочка отсутствует. Рак пищевода может распространяться на органы средостения, трахею, перикард, крупные сосуды. Отдаленные метастазы регистрируются в печени, легких, плевре. Глубину инвазии опухоли и поражение регионарных лимфатических узлов оценивают при ультразвуковом исследовании. Для обнаружения отдаленных метастазов часто используют КТ, но было доказано, что ПЭТ при раке пищевода более информативна для выявления отдаленных метастазов.
Клиническая классификация рака пищевода по системе TNM.
Т - первичная опухоль.
Тх - определить распространенность первичной опухоли невозможно.
Tis - преинвазивная карцинома (carcinoma in situ). T0 - первичная опухоль не определяется.
Т1 - опухоль поражает слизистую оболочку и подслизистый слой.
Т2 - опухоль поражает те же слои + мышечный слой. Т3 - опухоль поражает все указанные выше слои и соединительнотканную пластинку.
Т4 - опухоль поражает прилегающие органы и ткани. N - регионарные лимфатические узлы.
Nx - недостаточно данных для оценки регионарных лимфатических узлов.
N0 - нет признаков поражения регионарных лимфатических узлов.
N1 - обнаружены метастазы в регионарных лимфатических узлах.
М - отдаленные метастазы.
Мх - недостаточно данных для определения отдаленных метастазов.
М0 - нет признаков отдаленных метастазов. М1 - имеются отдаленные метастазы.
Все имеющиеся в арсенале современной онкологии средства терапии рака пищевода можно классифицировать как радикаль- ные и паллиативные. Радикальные методы лечения: хирургический - резекция или экстирпация пищевода с одномоментным или
последующим восстановлением непрерывности пищеварительного тракта - и комбинированный и комплексный подход (адъювантная и неоадъювантная химио- и химиолучевая терапия). Паллиативные методы лечения: хирургический - наложение гастростомы, еюностомия, операции пищеводного шунтирования. Эндоскопическая реканализация пищевода, постановка стента.
При раке внутригрудного отдела пищевода наибольшее распространение получила операция типа Льюиса (одномоментная субтотальная эзофагэктомия, пластика широким желудочным стеблем) с формированием пищеводного соустья с лимфодиссекцией. При локализации опухоли в нижне- и среднегрудном отделах пищевода в настоящее время наиболее распространенной является операция, когда производят субтотальную резекцию или экстирпацию пищевода с одномоментной эзофагопластикой антиили изоперисталь- тической желудочной трубкой, выкроенной из большой кривизны желудка.
Развитие в послеоперационном периоде рефлюкс-эзофагита проявляется довольно часто, что связано с выпадением или повреждением вследствие операции весьма сложного в функциональном отношении замыкательного механизма кардии и заброса кислого содержимого в трансплантат. Определенную роль играет техника наложения эзофагогастроанастомоза. Клинически это осложнение проявляется срыгиванием, изжогой, ощущением жжения за груди- ной, болями при прохождении пищи по пищеводу. По тяжести различают легкий, средней тяжести и тяжелый рефлюкс-эзофагит.
С рефлюкс-эзофагитом часто связан, а иногда является его следствием, рубцовый стеноз анастомоза, клиническим синдромом которого является, дисфагия. Причина ранней послеоперационной дисфагии - анастомозит, в отдаленном периоде это может быть рубцовая стриктура или рецидив рака. Рентгенологически стриктура проявляется стойким, различной степени сужением просвета в области анастомоза, неровностью контуров, супрастенотическим расширением. Это создает серьезные алиментарные нарушения в послеоперационном периоде.
9.2. РАК ЖЕЛУДКА
В Российской Федерации заболеваемость раком желудка занимает 2-е место у мужчин и 3-е у женщин. По частоте инвалидности рак желудка занимает 2-е место после рака молочной железы.
К факторам риска развития рака желудка относятся высокое содержание соли и консервантов в употребляемых продуктах, высококалорийная пища, большое количество нерафинированных жиров, употребление горячей пищи, высокое содержание афлотоксина, нерегулярное питание, а также курение и избыточное употребление алкоголя. Установлено определенное влияние нитрозоаминов, часто эндогенных, на развитие болезни. Синтез нитрозаминов связывают с нарушением кислотности желудка и развитием патогенной флоры, как правило, Helicobacter pylori. Напротив, употребление молока и молочных продуктов, овощей, фруктов и бобовых способствует профилактике рака желудка. При изучении эпидемиологии рака желудка выявлено ведущее значение экзогенных воздействий. Было доказано стремительное снижение заболеваемости раком желудка в странах, где замораживание стало основным методом хранения продуктов. Это связано с уменьшением потребления копченостей, маринадов, соли, нитратов, нитритов.
Основные фоновые заболевания для развития рака желудка: хронический атрофический гастрит, хроническая язва желудка, аденоматозные полипы желудка (рис. 9.2). Отмечена связь частоты рака желудка с инфицированностью Helicobacter pylori, которая часто сопутствует язвенной болезни желудка. Канцерогенное воздействие этой флоры связывают с воспалительными изменениями в желудке, сопровождающимися выраженной пролиферацией интерстициальных клеток. В лечении предопухолевых заболеваний желудка эрадикации Н. pylori придается большое значение. По некоторым данным, с развитием рака желудка связано инфицирование вирусом Эпштейна-Барр. Вирусассоциированные опухоли имеют низкодифференцированную структуру или лимфоэпителиомаподобную (Nakamura S. et al., 1994). Нельзя отрицать и роль наследственных факторов. Отмечено, что у людей с группой крови A(II) заболева- емость на 20% выше, чем у остальных. Эти факты объясняют либо унаследованными особенностями питания, либо сцеплением с соответствующими генами, определяющими группу крови.
Следует заметить, что резекция желудка по любому поводу, в том числе по поводу доброкачественной опухоли, оказывает канцероген-
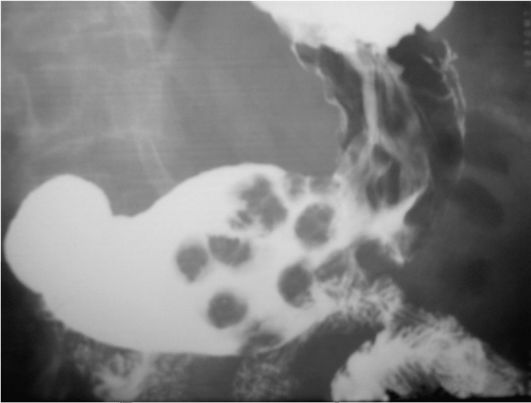
Рис. 9.2. Полипы желудка. Определяются дефекты наполнения желудка на фоне контрастной взвеси
ный эффект, что связывают с сопровождающим исход этой операции снижением кислотности желудка развитием атипичной микрофлоры и метаплазией слизистой оболочки.
Стенка желудка состоит из пяти слоев: слизистого, подслизистого, мышечного, субсерозного и серозного. Процесс канцерогенеза желудка включает в себя целый ряд гистопатологических измене- ний, при которых на первоначально нормальной слизистой оболочке желудка развивается активный хронический гастрит, далее происходят ее атрофия, кишечная метаплазия (I, II и III типа), дисплазия и рак. Механизмы метаплазии возникают на уровне мультипотентных клеток. Она происходит вследствие гибели зрелых клеток с типичной дифференцировкой. Это провоцирует пролиферацию местных стволовых клеток и их атипичную дифференцировку. В желудочном эпителии могут возникнуть три вида метаплазий. I тип - полная, зрелая метаплазия, когда клеточный состав и внешний вид слизистой оболочки желудка приобретает вид тонкокишечной. Менее благоприятна метаплазия II и III типов - неполная, незрелая, толстокишечная, которая связана с более высоким риском малигнизации. Метаплазии I и II типов являются обратимыми, а III типа - необратимой.
95% злокачественных опухолей желудка имеют строение аденокарциномы. Последние имеют разную степень дифференцировки, которая во многом определяет прогноз лечения. Остальные 5% опухолей представлены очень разнообразными по строению опухолями. Отмечается нарастание среди них лимфосарком желудка. Стадию первичного рака желудка оценивают в зависимости от глубины проникновения опухоли. Для точной оценки рN необходимо обширное иссечение лимфоузлов регионарных зон.
Клиническая классификация рака желудка по системе TNM (используется только для верифицированного рака желудка).
Т - первичная опухоль.
Тх - определить распространенность первичной опухоли невозможно.
Tis - преинвазивная карцинома (carcinoma in situ). T0 - первичная опухоль не определяется.
Т1 - опухоль поражает слизистую оболочку и подслизистый слой.
Т2 - опухоль поражает те же слои + мышечный слой слизистой или субсерозный слой.
Т2а - опухоль прорастает в мышечный слой.
Т2Ь - опухоль прорастает субсерозную оболочку.
Т3 - опухоль поражает все указанные выше слои и серозную оболочку (висцеральную брюшину).
Т4 - опухоль поражает прилегающие органы и ткани.
N - регионарные лимфатические узлы.
Nx - недостаточно данных для оценки регионарных лимфатических узлов.
N0 - нет признаков поражения регионарных лимфатических узлов.
N1 - обнаружены от 1 до 6 метастазов в регионарных лимфатических узлах.
N2 - обнаружены от 7 до 15 метастазов в регионарных лимфатических узлах.
N3 - обнаружены более 15 метастатических узлов в регионарных лимфатических узлах.
М - отдаленные метастазы.
Мх - недостаточно данных для определения отдаленных метастазов.
М0 - нет признаков отдаленных метастазов. М1 - имеются отдаленные метастазы.
Большее клиническое значение для прогноза имеет форма роста опухоли. Анатомическая форма роста опухоли тесно связана с глу- биной инвазии стенки желудка. Экзофитные опухоли чаще встречаются в пределах слизистой оболочки желудка, эндофитные - в глубжележащих слоях, прорастая всю его стенку. Пятилетняя выживаемость при экзофитных формах роста опухоли в 2 раза выше, чем при эндофитных. Опухоли с преимущественно экзофитным ростом имеют более благоприятный прогноз в отличие от опухолей с эндофитным ростом. Наименее благоприятная по течению диффузноинфильтративная форма рака желудка отличается бессимптомным или малосимптомным течением. При этой форме роста отмечается своеобразие рентгено-эндоскопических данных - диффузное изменение стенки желудка с развитием ригидности, циркулярное сужение желудка, утолщение стенок и плохое расправление складок на фоне инсуффляции воздуха. Морфологическая картина представлена очагами опухолевых клеток в стенке желудка на фоне интерстициального фиброза.
Локализация процесса в желудке является важным прогностическим критерием. Пятилетняя выживаемость при раке кардиального отдела желудка в 2 раза ниже, чем при раке его выходного отдела. Переход опухоли на пищевод или двенадцатиперстную кишку даже на ранних стадиях процесса после радикального лечения делает прогноз сомнительным. Требуются технически сложные хирургические вмешательства, рецидив таких опухолей отмечен чаще и в более короткие сроки. Регионарными являются лимфоузлы, расположенные вдоль малой и большой кривизны, вдоль левой желудочной, общей печеночной, селезеночной и чревной артерий.
Единственным радикальным методом лечения рака желудка является хирургический метод. При выборе объема операции учитываются все указанные прогностически значимые особенности опухоли. Начальные стадии позволяют выполнить органосохраняющие операции. В последние годы получило распространение комбинированное и комплексное лечение, что существенно повышает показатели 5-летней выживаемости. При III и IVA стадиях применяют комбинированные резекции желудка и гастрэктомию. В неоперабельных случаях используют лучевой и химиотерапевтический методы лечения, как самостоятельно, так и в комбинации с паллиативной целью. Неоперабельный рак желудка часто приводит к необходимости выполнения палли-
ативных операций в виде наложения гастроэнтероанастомоза, гастростомии, еюностомии.
Последствия радикального лечения в значительной степени зависят от объема операции и ее способа. Субтотальная дистальная резекция желудка с анастомозом по способу Бильрот-1 сохраняет пассаж пищи по двенадцатиперстной кишке и сопровождается наименьшей частотой и степенью выраженности функциональных расстройств. В то же время наложение анастомоза этого типа нередко ограничено требованиями абластики. Значительно чаще накладывают анастомоз по способу Бильрот-2. После этой операции в отдаленном периоде чаще возникают тяжелые нарушения функций желудочно-кишечного тракта и метаболические сдвиги в организме больного. К наиболее частым последствиям оперативного лечения рака желудка относятся синдром малого желудка, синдром приводящей петли, рефлюксэзофагит, хронический гастрит культи желудка, анастомозит с последующим исходом в рубцевание, анемия, нарушения функции пищеварения, упадок питания, астенизация нервной системы. Что касается функции пищеварения, снижения массы тела, анемии, астенизации нервной системы, то они встречаются у подавляющего числа больных этой группы.
Комбинированные операции с резекцией смежных органов желудочно-кишечного тракта часто приводят к выраженному нарушению функции пищеварения и требуют длительной адаптации организма к новым условиям.
9.3. КОЛОРЕКТАЛЬНЫЙ РАК
По данным ВОЗ, рак толстой кишки занимает 1-2-е место среди злокачественных новообразований пищеварительного тракта и 5-е среди опухолей других локализаций. Основной контингент - лица трудоспособного возраста от 40 до 60 лет.
Анатомическая форма роста опухоли - важный фактор прогноза. Макроскопически выделяют экзо- и эндофитные раковые опухоли и опухоли со смешанным типом роста. Экзофитные опухоли растут в просвет полого органа (кишки), имеют четкие границы и очень медленно инфильтрируют толщу стенки кишки. Эти опухоли чаще встречаются в правой половине толстой кишки - слепой, восходящей и в печеночном углу. Для эндофитных опухолей характерно разрастание вглубь кишечной стенки и по ее длине, часто опухоли
растут циркулярно, приводя к сужению просвета кишки и кишечной непроходимости. Такие циркулярно растущие опухоли преоблада- ют в левой половине толстой кишки и в поперечной (рис. 9.3, 9.4). Смешанные формы встречаются одинаково часто во всех отделах толстой кишки. Клинический прогноз при эндофитном раке ухудшается в 4 раза.
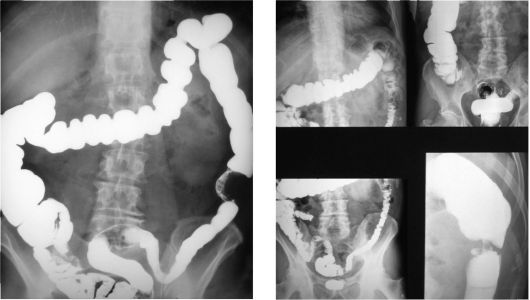
Рис. 9.3. Контрастная ирригогра- Рис. 9.4. Рак селезеночного угла фия толстой кишки. Опухоль (адетолстой кишки нокарцинома) определяется в середине нисходящего отдела толстой кишки
Глубина инвазии опухоли существенно влияет на клинический прогноз больных раком толстой кишки, так же как состояние реги- онарных лимфоузлов. Регионарными лимфоузлами для толстой кишки являются периколярные, периректальные, а также лимфоузлы по ходу сосудов ободочной и прямой кишок. При радикальной операции их удаляют, но метастазы существенно ухудшают прогноз лечения. Прогноз ухудшается по мере снижения степени диффе- ренцировки и наиболее неблагоприятен при слизистых и недифференцированных опухолях. Патоморфологическая классификация
опухоли основывается на изучении удаленного операционного препарата и регионарных лимфатических узлов. Для каждого отдела толстой и прямой кишки регионарными считаются определенные группы лимфатических узлов. До операции проводят ректороманоскопию, колоноскопию с биопсией, КТ и ПЭТ.
Клиническая классификация рака толстой кишки по системе TNM (используется только для верифицированного рака толстой кишки).
Т - первичная опухоль.
Тх - определить распространенность первичной опухоли невозможно.
Tis - преинвазивная карцинома (carcinoma in situ). Опухолевые клетки обнаруживаются в базальной мембране желез или в толще слизистой оболочки.
T0 - первичная опухоль не определяется.
Т1 - опухоль поражает слизистую оболочку и подслизистый слой.
Т2 - опухоль поражает те же слои + мышечный слой слизистой.
Т3 - опухоль поражает субсерозный слой либо распространяется в околокишечную и параректальную клетчатку.
Т4 - опухоль поражает прилегающие органы и ткани и/или проникает через висцеральную брюшину.
N - регионарные лимфатические узлы.
Nx - недостаточно данных для оценки регионарных лимфатических узлов.
N0 - нет признаков поражения регионарных лимфатических узлов.
N1 - обнаружены от 1 до 3 метастазов в регионарных лимфатических узлах.
N2 - обнаружены от 4 и более метастазов в регионарных лимфатических узлах.
М - отдаленные метастазы.
Мх - недостаточно данных для определения отдаленных метастазов.
М0 - нет признаков отдаленных метастазов. М1 - имеются отдаленные метастазы.
Основным методом радикального лечения рака толстой кишки является операция, объем которой зависит от локализации опухо- ли, стадии болезни, анатомической формы роста. При локализации
опухоли
в правой или левой половине ободочной кишки выполняют правоили
левостороннюю гемиколэктомию (при локализации опухоли в слепой кишке
обязательно удаление 10-
R0 - отсутствуют опухолевые клетки по краям резекции.
R1 - неполная резекция, по краю обнаружены микроскопические признаки опухоли.
R2 - неполная резекция, по краю обнаружены макроскопические признаки опухоли.
Примерно у 20-25% больных радикальная операция неосуществима. Им выполняют паллиативные резекции или накладывают колостому.
В последние годы наиболее благоприятные отдаленные результаты получены при комплексном радикальном лечении рака толс- той кишки: предоперационном (реже послеоперационном) лучевом лечении, последующей операции и химиотерапии для подавления и предупреждения метастазов. Применение комплексного лечения повысило 5-летнюю выживаемость приблизительно на 10-20%.
Гистологическое строение опухолей толстой кишки представлено чаще аденокарциномой различной степени дифференцировки и зрелости и плоскоклеточными раками в анальном канале ниже гребешковой линии. По данным ВОЗ, чаще (75%) встречаются высокодифференцированные и средней степени злокачественности
опухоли, реже выявляются низкодифференцированные или недифференцированные.
Злокачественные опухоли анального канала встречаются редко, составляют 1-6% от всех опухолей прямой кишки. В проксимальном отделе заднего прохода имеется три гистологических типа эпителия: железистый, переходный и плоскоклеточный. В дистальном отделе плоскоклеточный эпителий переходит в кожу перианальной области. Опухоли этой области отличаются агрессивным клиническим течением, частыми рецидивами, неблагоприятным прогнозом. Почти в половине случаев опухоли этого отдела прямой кишки имеют строение плоскоклеточного рака. Стандартом лечения при плоско- клеточном раке анального канала является химиолучевая терапия. При отсутствии эффекта от применения консервативных методов лечения выполняется операция. В РОНЦ РАМН применяется также метод терморадиохимиотерапии (т.е. химиолучевая с локальной гипертермией). Этот метод позволяет достигать более часто полной регрессии опухолей, нередко остаточная опухоль невелика и можно выполнить сфинктерсохраняющую операцию.
При наличии отдаленных метастазов колоректального рака, которые наблюдаются очень часто, ведущие специализированные онкологические учреждения обращаются к идее циторедуктивных операций, при этом выполняются, кроме паллиативных операций на первичном очаге, и хирургические вмешательства по поводу метастазов колоректального рака в печень, легкие, яичники и др. Эффективные режимы последующей лекарственной (адъювантной) химиотерапии позволяют значительно продлить жизнь этих больных.