Клиническая иммунология : учебник / под ред. А.М. Земскова. - 2008. - 432 с.
|
|
|
|
ГЛАВА 17. ИММУНОЛОГИЧЕСКИЕ РАССТРОЙСТВА И ИХ КОРРЕКЦИЯ В ДРУГИХ СЛУЧАЯХ*
17.1. При комбинации заболеваний
Сочетание бронхиальной астмы с хроническим аутоиммунным тире-
оидитом. У пациентов с комбинированной патологией отмечается достоверное увеличение уровня ТТГ, ТАТ, IgG, ЦИК и значимое уменьшение содержания Т3, носителей кластеров дифференцировки CD3+, CD4+, CD8+, IgM и IgA.
Ключевыми маркерами иммунных нарушений оказались ТАТ3+ЦИК3+CD43+.
Характер иммунологических расстройств у страдающих только бронхиальной астмой оказался иным. Это было снижение уровня CD3+, CD4+, CD8+, CD19+, IgA с увеличением - IgG, IgM, ЦИК с итоговой ФРИС: IgG2+ЦИК3+IgA2-.
Совпадает в вышеуказанных вариантах формул лишь один показатель из трех ведущих - циркулирующие иммунные комплексы.
У больных с аутоиммунным заболеванием щитовидной железы было зарегистрировано увеличение от уровня нормы ТТГ, ТАТ, IgG и уменьшение соответственно - CD3+, CD4+, CD8+лимфоцитов, IgM и IgA с типовой формулой: ТАТ3+IgM2-CD192+.
Эти данные свидетельствуют о том, что сочетание различных патологических процессов у больных приводит к вариациям иммунных нарушений. Во-первых, это выражается в общем усугублении иммунологических расстройств, а во-вторых, в изменении диагностически значимых параметров. Последнее имеет принципиальное значение для выбора профильной иммунокоррекции.
Наличие у пациентов одновременно хронического обструктивного бронхита и хронического холецистита приводит к избыточному накоплению у пациентов содержания CD4+, CD8+, CD19+- лимфоцитов, IgM, уменьшению концентрации IgA с ФРИС: IgA1-CD191-IgM2+.
В то же время только хронический бронхит характеризуется принципиально иной картиной изменений иммунологической реактивности - по Т-, В-клеткам, CD4+-лимфоцитам, IgA и IgM. Налицо супрессивный профиль иммунного статуса у больных, что подтверждается ФРИС: CD42-CD32-IgM2+.
Другое слагаемое комплексной патологии - хронический холецистит обусловливает активацию иммунной системы по клеткам с
* Глава написана совместно с проф. В.И. Золоедовым
кластерами дифференцировки - CD8+, CD19+, IgM и IgA на фоне накопления IgG.
Диагностически значимыми оказались следующие показатели гуморальной защиты: IgA2+IgG2-IgM3+.
Таким образом, стимуляция иммунологической реактивности у пациентов с хроническим холециститом устранила ее подавление в результате развития хронического воспалительного заболевания легких.
Комбинация мочекаменной болезни с пиелонефритом обусловила типовые изменения иммунолабораторного статуса, свидетельствующие о воспалении, аллергизации, супрессии Т-, дисбалансе В-, подавлении фагоцитарных звеньев иммунитета на фоне накопления образования провоспалительных цитокинов.
Конкретно при данной патологии зарегистрированы вариации лейкоцитов, палочкоядерных и сегментоядерных лимфоцитов, эозинофилов, моноцитов, CD8+-лимфоцитов, IgG, ЦИК, молекул средней массы, фактора некроза опухолей - со стимулирующим вектором и по - CD3+, CD4+- лимфоцитам, IgA, фагоцитарному показателю и фагоцитарному числу, спонтанному тесту с нитросиним тетразолием - с супрессирующей динамикой.
Формула расстройств иммунной системы соответственно включала следующие параметры: CD32-CD82+IgG3+.
При нефролитиазе изменения слагаемых иммунной защиты оказались менее выраженными.
Так, у больных образовывался лейкоцитоз, моноцитоз, недостаточность содержания носителей маркеров CD3+, CD4+, гипоиммуноглобулинемия по IgA и IgM, избыток концентрации ЦИК, снижение поглотительной и метаболической способностей фагоцитов, гиперпродукции ФНО. Иными словами, выраженность воспалительного процесса у данного контингента больных оказалась менее значительной. Это подтверждается составом ФРИС: CD32-CD42-ЦИК2+.
Комбинация хронического обструктивного бронхита с хроническим лимфолейкозом.
У пациентов с ХОБ отмечалась лимфопения, дефицит носителей маркеров CD3+, CD8+, CD19+, а также IgA, снижение величины фаоцитарного числа и гипериммуноглобулинемия по IgM, с ФРИС -
В лимфолейкозе документирована стимуляция уровня лейкоцитов, лимфоцитов, CD3+- и CD19+- клеток, носителей кластера диф-
ференцировки CD8+ с уменьшением фагоцитарного числа и концентрации IgG. ФРИС - CD3;^3+CD83+.
Комбинация обоих заболеваний обусловила следующий характер иммунопатологии - увеличение содержания лейкоцитов, лимфоцитов, CD3+- и CD19+- клеток, носителей маркера CD8+, IgM на фоне дефицита IgG и угнетения поглотительной способности фагоцитов. ФРИС -
Другие комбинации заболеваний также обусловливают изменения состава формул расстройств иммунной системы.
Соответственно, при комбинации бронхиальной астмы с хронической обструктивной болезнью легких ФРИС составили CD42-CD82-
IgG1-, одной ХОБЛ - CD43-CD82-CD33-; одной БА - CD32-CD42-IgA1-.
Во всех случаях наблюдаются различия по одному из слагаемых из трех ключевых.
В то же время динамика составляющих ФРИС у пациентов с язвенной болезнью желудка в сочетании с язвой 12-перстной кишки и отдельными слагаемыми этой комбинации оказалась монотонной, соответственно IgG1+CD3-IgA2-; ЯБЖ - CD31-IgA1-CD193+; ЯБДПК -
CD31-IgG2+IgA2-.
При формировании у больных сложной сочетанной патологии были выявлены следующие ключевые параметры иммунопатологии.
Бронхиальная астма+хронический обструктивный бронхит+ ишемическая болезнь сердца (БА+ХОБ+ИБС) - CD192-CD31-CD41-, БА+ХОБ+гипертоническая болезнь (БА+ХОБ+ГБ) - MСM1+CD32-CD81-, БА+ХОБ+ИБС+ГБ - IgG1-CD31-Лф1-.
Характер иммунных расстройств при сочетанной патологии у часто болеющих детей (ЧБД) представлен в табл. 8.
Таблица 8. Иммунные расстройства при сочетанной патологии у детей
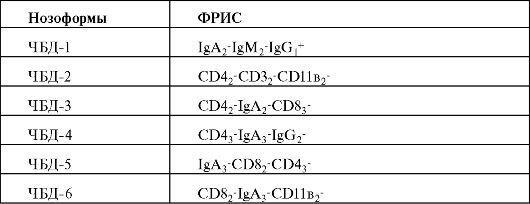 Обозначения: ЧБД-1 - часто болеющие дети без сопутствующей патологии, ЧБД-2 - то же + ЛОР-патологии, ЧБД-3 - то же + аллергия,
Обозначения: ЧБД-1 - часто болеющие дети без сопутствующей патологии, ЧБД-2 - то же + ЛОР-патологии, ЧБД-3 - то же + аллергия,
ЧБД-4 - то же + тимомегалия, ЧБД-5 - то же +ЛОР-патологии и аллергия, ЧБД-6 - то же + аллергия и тимомегалия, CD3, CD4, CD8, CD11в,- кластеры дифференцировки, IgG, IgA и IgM - иммуноглобулины G, А и М, 1,2,3 - степень изменения показателей, «+» - стимуляция, «-» - супрессия.
Данные таблицы демонстрируют существенное влияние сочетанной патологии у детей на формулы расстройств иммунной системы.
Отягощение основной патологии болезнями ЛОР-органов, аллергией, тимомегалией или их комбинациями расширяет спектр пораженных звеньев защитных реакций - от гуморального до клеточного и фагоцитарного. При этом наибольшие изменения наблюдаются при сочетании инфекционного синдрома с аллергией и тимомегалией, а также с аллергией и ЛОР-патологией.
Комбинация хронического аутоиммунного тиреоидита с сахарным диабетом типа 1. У пациентов с ХАИТ наблюдалось снижение уровня CD3+, CD8+-клеток, а увеличение - IgG.
При сахарном диабете 1 типа зарегистрирован дефицит CD3+, CD8+-лимфоцитов, стимуляция количества CD19+-клеток, супрессия фагоцитарного числа и активированного теста с нитросиним тетразолием.
В случае комбинации обеих нозологических форм Т-лимфопения с падением регуляторной субпопуляции CD8+, гипериммуноглобулинемия по IgG, избыток ЦИК, уменьшение фагоцитарного показателя.
Сочетание хронического аутоиммунного тиреоидита с хронической обструктивной болезнью легких. У больных с ХАИТ документировано достоверное снижение содержания лимфоцитов с CD8+-маркером, IgA в сочетании с накоплением ТТГ, ТАТ, IgG, ЦИК, ФНО-α с типовой формулой:ТАТ3+IgG2+CD82- - гиперпродукция антител против тиреоглобулина, гипериммуноглобулинемия по IgG, дефицит числа регуляторных CD8+ -клеток.
При ХОБЛ выявлена принципиально иная динамика показателей - лимфопения, радражение гранулоцитарного ростка, эозинофилия, депрессия CD3+-, дисбаланс CD19+- и фагоцитарного звеньев иммунитета.
ФРИС включала следующие тесты: CD43-CD83+ЦИК3+.
Сочетание обоих заболеваний способствовало увеличению содержания незрелых и зрелых гранулоцитов, эозинофилов, моноцитов, ТТГ, ТАТ, клеток с кластером диффреренцировки CD16+, а также - IgG, ЦИК, МСМ, ФНО, ИЛ-6 и ИЛ-8 на фоне дефицита лимфоцитов с маркерами CD3+, CD4+, CD8+, уменьшению ФП и ФЧ, активации НСТак. с ФРИС: ТАТ3+CD163+ЦИК3+.
У больных из данной группы произошло совмещение патогенеза обоих заболеваний - воспаления, дисфункции щитовидной железы, супрессии клеточной защиты - накопление свидетелей аутоиммунного процесса и токсикоза, угнетение поглотительной и метаболической способности фагоцитов, уменьшение уровня противовоспалительного цитокина ИЛ-4.
17.2. Аллергизация заболеваний
В принципе отягощение патологических процессов аллергией приводит к хронизации основного заболевания и усугублению типовых иммунологических реакций.
Комбинация бронхиальной астмы с псевдоаллергическими реакциями. У больных только с бронхиальной астмой тестируется лейко- и моноцитоз, эозинофилия, накопление зрелых гранулоцитов, ускоренное СОЭ, дефицит CD3-клеток, их регуляторных субпопуляций, увеличение концентрации ЦИК, МСМ, ИЛ-8, сиаловых кислот с потенцированием кислородного метаболизма нейтрофилов, уменьшением фагоцитарного показателя и фагоцитарного числа, провоспалительного ИЛ-4.
В случае присоединения к основному заболеванию псевдоаллергии отмечается дополнительное снижение концентрации гемоглобина, накопление палочкоядерных клеток с характерными изменениями слагаемых иммунного статуса - по лимфоцитам с кластерами дифференцировки - CD3+, CD4+, CD8+, CD16+,
CD19+, IgA, IgM, IgG, ЦИК, МСМ, ФП, ФЧ, НСТсп., НСТак., ИЛ- 4, ИЛ-8.
Соответственно этому варьирует и состав ключевой формулы расстройств иммунной системы.
БА - Л2+CD42-CD32- - лейкоцитоз в сочетании с дефицитом двух Т-зависимых параметров средней выраженности.
БА+ПАР - ПЯ2+CD32ΉСТсп2+ - накопление незрелых гранулоцитов на фоне недостаточности общих CD3-клеток и активации кислородпродуцирующей функции нейтрофилов второй степени.
Налицо изменения характера и усугубление выраженности иммунопатологии за счет развития псевдоаллергических реакций.
Комбинация хронического обструктивного бронхита с псевдоаллергией. Отягощение ХОБ псевдоаллергическими реакциями способствует снижению содержания общих лейкоцитов, IgG и активации кислородпродуцирующей активности нейтрофилов (НСТсп., НСТак.).
Состав ФРИС у больных в обоих случаях отличался по одному слагаемому из трех.
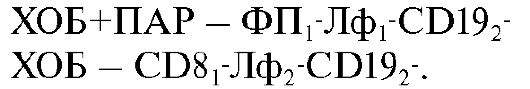 Комбинация бронхиальной астмы с лекарственной непереносимостью.
Комбинация бронхиальной астмы с лекарственной непереносимостью.
Указанное сочетание способствует формированию у больных гипериммуноглобулинемии по IgG и IgA, уменьшению содержания регулирующей субпопуляции CD4+.
Состав ФРИС у пациентов также изменился, соответственно
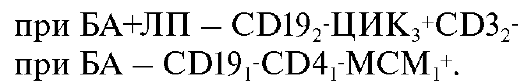 Комбинация глубокой пиодермии с кожным аллергозом. У лиц, страдающих глубокой пиодермией, было документировано достоверное изменение 17 параметров из 25 изученных.
Комбинация глубокой пиодермии с кожным аллергозом. У лиц, страдающих глубокой пиодермией, было документировано достоверное изменение 17 параметров из 25 изученных.
В числе сниженных значились недифференцированные лимфоциты, носители маркеров CD3+, CD4+, CD8+, фагоцитарное число, спонтанный и активированный НСТ-тест в комбинации с увеличением содержания палочкоядерных и сегментоядерных лейкоцитов, CD19+ -клеток, IgG, IgA, IgM, ЦИК, МСМ, ИЛ-6 и ИЛ-8.
У больных с комплексной патологией в числе измененных значились 20 тестов: незрелые и зрелые гранулоциты, эозинофилы, моноциты, CD3+- и CD19+ - лимфоциты, их регуляторные субпопуляции, IgG, IgA, IgM, ЦИК, МСМ, поглотительная и кислородпродуцирующая способность фагоцитов, цитокинов - ФНО-α, ИЛ-4, 6, 8. ФРИС включала: ИЛ-83+ЦИК3+НСТак3-, что маркирует накопление прововоспалительного цитокина, фактора индукции иммунопатологии, стимуляции резервного кислородпродуцирующего механизма нейтрофилов периферической крови.
Таким образом, развитие псевдоаллергии и истинной аллергии является неблагоприятным фоном усугубления и изменения характера иммунопатологии у больных.
17.3. Различные стадии и степени тяжести заболеваний
Указанные факторы также способствуют изменению типовых реакций иммунной системы.
Стадия обострения и ремиссии бронхиальной астмы. В стадии обострения указанного заболевания у пациентов регистрируется стимуляция уровня лейкоцитов, незрелых гранулоцитов, ЦИК, МСМ в сочетании с уменьшением содержания гемоглобина, эритроцитов, CD3+- и CD19+- лимфоцитов, носителей кластеров дифференцировки CD4+- и CD8+- клеток с типовой ФРИС: Л2+CD42-CD32-.
В стадии клинической ремиссии у пациентов сохранились отдельные изменения иммунной системы, т.е. полной коррекции не произошло. Свидетельством этого является ФРИС при выписке больных из стационара: Пя3+CD192-MСM2+.
При проведении иммунотерапии нуклеинатом натрия одних и тех же больных в стадии обострения и ремиссии выявлена смена мишеней действия модулятора: CD33+CD43+Лф2+ на CD33+Э2-ПЯ2-.
В первом случае наблюдалась активация Т-звена иммунитета и лимфопоэза. Во-втором - потенциирование клеточных реакций в сочетании с противоаллергическим и противовоспалительным эффектом.
Стадия обострения и ремиссии рассеянного склероза. У больных с данной патологией в стадии обострения отмечается стимуляция содержания CD3+, CD16+, HLA-DR+, CD19+-клеток, IgM, активация кислородпродуцирующей способности нейтрофилов, фагоцитарного показателя и фагоцитарного числа, снижение количества носителей кластера дифференцировки CD8+.
Таким образом, у пациентов выявлен дисбаланс Т-звена иммунной системы с преимущественным подавлением супрессорных механизмов со стимуляцией В-зависимых реакций, поглотительной и метаболической способности фагоцитов на фоне лейкоцитоза и эозинофилии с типовой ФРИС: IgA1+БФ1-CD33+.
В стадии ремиссии отмечалось накопление CD3+- клеток, естественных киллеров (CD16+), носителей маркеров CD11в+, HLADR+, CD19+, IgA, ЦИК, увеличение фагоцитарного числа с последующей
ФРИС: CD162+HLA-DR2+CD192+.
Указанная формула демонстрирует полную смену ключевых лабораторных параметров в стадии ремиссии бронхиальной астмы.
Стадии цирроза печени также в определенной мере влияют на типовые реакции иммунной системы.
В начальной стадии ФРИС имеет вид - IgG3+CD32-IgA2+. В стадии сформировавшегося цирроза - IgG2+IgA1+CD31- со сменой степени изменений и порядка расположения ключевых параметров. В терминальной стадии - CD32TgA3+Лф2-.
В зависимости от этого менялись и мишени действия однотипной модуляции нуклеинатом натрия, соответственно - РБТЛ3+СЖ2+IgG1-; CD32+(Лф2+Л1+)IgG1- и CD33+Лф3+(Л1+РБТЛ3+).
Острый оофорит и обострение хронического оофорита. Указанные заболевания, с одной стороны, можно с определенной долей условности считать двумя стадиями одного патологического процесса или как варианты разной тяжести течения заболевания.
В стадии острого (первичного) оофорита у больных женщин наблюдалось преобладание лабораторных свидетелей воспаления, сенсибилизации; супрессия Т-звена иммунитета, по клеткам с кластерами дифференцировки CD3+, CD4+, с накоплением - CD8+; активация гуморальных защитных реакций, оцененных образованием иммунных глобулинов IgG, IgA, IgM, уровнем ЦИК с подавлением поглотительной и метаболической способности фагоцитов - по фагоцитарному показателю, фагоцитарному числу, спонтанному, активированному тестам с нитросиним тетразолием на фоне дисбаланса слагаемых цитокинового статуса - снижение противо- и увеличение провоспалительных интерлейкинов.
ФРИС была следующей: Л3+ЦИК3+CD42-.
При обострении хронического оофорита документирована лимфопения, эозинофилия, моноцитоз, уменьшение содержания клеток с маркером CD3+, CD8+, увеличение - CD8+; рост числа ток, гипериммуноглобулинемия по IgG и IgM, избыток содержания ЦИК, дисбаланс фагоцитоза - стимуляция поглотительной и супрессия метаболической способности фагоцитов в сочетании с гиперпродукцией фактора некроза опухолей, ИЛ-6 и ИЛ-8, что в целом свидетельствует об аллергизации, воспалении, подавлении клеточных, активации гуморальных защитных реакций с разнонаправленными изменениями фагоцитарных показателей.
ФРИС включала Э3+IgM3+ИЛ-63+.
Приведенные данные документируют более выраженную несостоятельность иммунной системы при обострении хронического воспаления в женской половой сфере, чем при первичном патологическом процессе.
Таким образом, особенности течения заболеваний, их комбинации, формирование аллергических и псевдоаллергических реак-
ций, локализация, стадия, выраженность иммуно-патологического процесса существенно влияют на изменение иммунологического гомеостаза у больных, что должно учитываться при трактовке данных иммуно-лабораторного обследования пациентов и проведении им направленной иммунокорригирующей терапии.
17.4. Объем хирургического вмешательства
Установлено, что объем хирургического вмешательства влияет на выраженность иммунопатологии и эффективность характера действия иммунотерапии.
Нефролитиаз. Развитие мочекаменной болезни обусловливает у больных увеличение содержания лейкоцитов, моноцитов, ЦИК,ФНО- в сочетании с уменьшением уровня носителей маркеров CD3+, CD4+, IgA и IgM, фагоцитарного показателя и фагоцитарного числа, активированного НСТ-теста.
Ключевыми показателями иммунопатологии оказались: CD32- CD42-ЦИК2+ - недостаточность двух Т-зависимых параметров на фоне избытка ЦИК - провоцирующего фактора аутоагрессии средней выраженности.
Проведение открытой операции вызвало стимуляцию уровня лимфоцитов с маркерами CD8+, CD16+, а также IgG, ЦИК, МСМ, CD4+, CD19+, CD11в+-клеток, ИЛ-4.
В целом у больных произошла негативация иммунологических реакций: лимфопения, рост числа клеток с супрессирующими потенциями, дисбаланс В-звена иммунитета, угнетение фагоцитоза, разнонаправленные изменения цитокинового статуса.
Мишенями операционного вмешательства в иммунной системе оказались нижеследующие тесты: CD83+CD163+ФНО3+ - реализация дерепрессивных тенденций факторов иммунологической реактивности на фоне воспаления.
Дистанционная литотрипсия обеспечивает существенно меньшие изменения иммуно-лабораторных параметров - по лимфоцитам с кластерами дифференцировки CD4+,CD16+, CD11в+, тестами, характеризующими поглотительную и метаблическую способность фагоцитов с ключевой ФМИ: СВ11в2+НСТсп2-CD82-.
Доброкачественная гиперплазия предстательной железы. Данная патология характеризуется накоплением маркеров сенсибилизации и воспаления (эозинофилов, лейкоцитов, моноцитов), угнетением Т-, активацией В-, супрессией фагоцитарного звень-
ев иммунитета, увеличением ИЛ-6 и ИЛ-8 с типовой ФРИС: CD193+НСТак2-CD32-.
Стандартная аденомэктомия обусловливает усугубление дефицита клеточных реакций (CD4+, CD3+), увеличение - числа CD8+, CD16+- клеток с ростом концентрации МСМ и провоспалительного цитокина
ИЛ-8.
ФМИ оперативного вмешательства включала CD82+CD162+MСM2+, что свидетельствует о прогрессировании супрессии иммунологической реактивности и увеличении риска индукции аутоагрессии.
Мобильное действие трансуретральной резекции предстательной железы оказалось существенно ниже. У фоновых значений изменились лишь три показателя - ИЛ-83+CD82+ЦИК2+.