Клиническая генетика : учебник / Н. П. Бочков, В. П. Пузырев, С. А. Смирнихина ; под ред. Н. П. Бочкова. - 4-е изд., доп. и перераб. - 2011. - 592 с. : ил.
|
|
|
|
Глава 9. ЛАБОРАТОРНЫЕ МЕТОДЫ ДИАГНОСТИКИ
ОБЩИЕ ВОПРОСЫ
Многие формы наследственной патологии проявляются настолько специфическим фенотипом, что клинический анализ с синдромологическим подходом позволяет установить точный диагноз. В дополнение к методам клинической диагностики применяют генеалогический метод, который еще больше повышает вероятность правильного диагноза. Однако широкий клинический полиморфизм наследственных болезней, их фенокопии, частичное совпадение симптомов разных заболеваний (наследственных и ненаследственных), необходимость выявления гетерозиготных носителей или носителей балансированных транслокаций и инверсий требуют применения лабораторных методов диагностики, которые при наследственной патологии всегда более точные, чем клинические методы.
Хотя история применения лабораторных методов диагностики наследственных болезней насчитывает почти 100 лет, первая половина этого пути отмечена лишь единичными примерами диагностики отдельных болезней с использованием качественных биохимических реакций (моча) или патогистологических методов. Применение биохимических методов началось с диагностики алкаптонурии в начале XX в., что и позволило А. Гарроду открыть наследственные болезни обмена веществ, обусловленные блоком ферментативной реакции. В 1930-х годах была открыта простая реакция мочи с хлоридом железа (зеленая окраска) при фенилкетонурии. Морфологическими методами подтверждались диагнозы нейрофиброматоза, наследственных кожных болезней (конец XIX в.).
Широкое применение лабораторных методов диагностики наследственных болезней началось в 50-х годах XX в. Это было связано, по-видимому, не только с прогрессом лабораторной диагностики (клинической биохимии, гематологии, цитологии, цитохимии, иммунологии), но и с повышенным интересом в этот период к
* Исправлено и дополнено при участии д-ра мед. наук Т.В. Филипповой.
наследственной патологии. Кроме того, усовершенствование цитогенетических методов в 50-х годах позволило открыть новую группу болезней человека - хромосомные болезни.
Таким образом, генетика человека и медицинская генетика взяли на вооружение многочисленные методы лабораторных исследований (биохимические, иммунологические, цитологические, гематологические, цитогенетические, немного позже и молекулярнобиологические). Это и обусловило формирование клинической генетики как медицинской дисциплины и ее интенсивное развитие.
Лабораторная диагностика наследственных болезней (феноили генотипирование индивидов) может быть направлена на идентификацию одной из трех ступеней болезни. Во-первых, это выявление причины наследственной патологии, или характеристика генотипа, т.е. определение конкретной мутации (генной, хромосомной, геномной). Эти цели достигаются с помощью цитогенетических или молекулярно-генетических методов. Во-вторых, лабораторные (биохимические и иммунологические) методы позволяют регистрировать первичный продукт гена. В-третьих, возможна регистрация специфических метаболитов, возникших в процессе патологического действия мутации. Такая регистрация возможна на уровне жидкостей (крови, мочи, секрета) или клеток. Следовательно, на этой ступени можно применять биохимические, иммунологические и
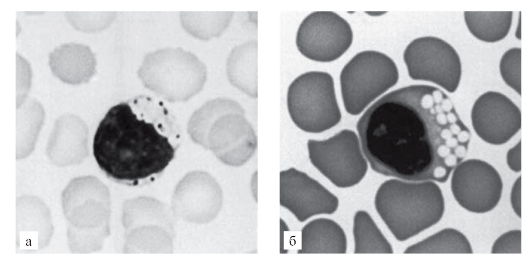
Рис. 9.1. Препараты мазков крови: а - при ганглиозидозе; б - при мукополисахаридозе
цитологические методы, что и нашло подтверждение в клинической практике. Например, иммунологические методы широко применяют для диагностики первичных (наследственных) иммунодефицитов, антигенной несовместимости матери и плода, биохимические - для диагностики наследственных болезней обмена веществ.
Цитологические клинические анализы помогают выявить некоторые наследственные болезни обмена веществ. Например, на рис. 9.1. представлены препараты мазков крови при ганглиозидозе (а) и мукополисахаридозе (б). Эти болезни имеют диагностические цитологические признаки, выявляемые при клинико-лабораторном анализе крови.
ЦИТОГЕНЕТИЧЕСКИЕ МЕТОДЫ
Микроскопические методы изучения хромосом человека применяются с конца XIX в. Соединение цитологического наблюдения хромосом с генетическим анализом сегрегации и сцепления генов привело к рождению цитогенетики. Первоначально цитогенетика концентрировалась на проблемах корреляции генетических и цитологических (хромосомных) признаков. В последующем цитогенетика методически отделилась от генетики. Под термином «цитогенетика» понимают область науки, изучающей структуру и функции хромосом.
Цитогенетические методы предназначены для изучения структуры хромосомного набора или отдельных хромосом. Наиболее распространенный метод в цитогенетике человека - световая микроскопия, а электронная и конфокальная лазерная микроскопия применяется только с исследовательскими целями. Во всей медикогенетической практике используется световая микроскопия (главным образом в проходящем свете), в том числе люминесцентная микроскопия.
Объектом цитогенетических наблюдений могут быть соматические делящиеся, мейотические и интерфазные клетки. Каждый из этих объектов имеет свои преимущества и недостатки. Выбор объекта определяется целью исследования.
Большинство цитогенетических исследований выполняют на соматических клетках, поэтому остановимся на описании этих методов.
Получение препаратов митотических хромосом
Первое условие цитогенетической диагностики - наличие делящихся клеток в материале для цитологического исследования.
Костный мозг, ткани семенника и хорион имеют достаточный митотический индекс для использования в цитогенетике. Однако, как показал опыт, несравненно информативнее исследование на культурах клеток: клетки освобождены от элементов соединительной ткани и хорошо суспендируются. Митотический индекс в культуре клеток много выше, чем в тканях организма.
Культуры клеток можно получать из кусочков кожи (растут фибробласты), костного мозга, эмбриональных тканей, хориона, клеток амниотической жидкости. Наиболее удобным объектом для медицинских генетиков оказалась культура лимфоцитов периферической крови (рис. 9.2). Для ее получения достаточно взять 1-2 мл венозной
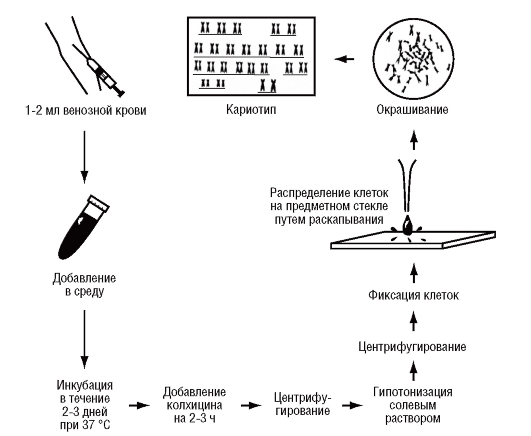
Рис. 9.2. Приготовление цитогенетических препаратов путем культивирования лимфоцитов периферической крови
крови и добавить ее в смесь питательной среды с фитогемагглютинином (белок бобовых растений). Он вызывает иммунную трансформацию и деление лимфоцитов. Продолжительность культивирования составляет 48-72 ч.
Вторым методическим условием цитогенетических исследований является использование колцемида (или колхицина), разрушающего веретено деления и останавливающего клеточное деление на стадии метафазы. Колцемид добавляют в культуры клеток за 2-3 ч до окончания культивирования: митотический индекс в культуре клеток за 2-3 ч повышается в 2-3 раза. Даже без культивирования экспозиция с колцемидом увеличивает число метафаз. Хромосомы в присутствии колцемида укорачиваются в результате продолжающейся конденсации, следовательно, в препарате они легче отделяются одна от другой.
Если необходим детальный анализ определенного района хромосомы, сильно конденсированные хромосомы на стадии метафазы (метод называется метафазным) непригодны для анализа. Клетку нужно зафиксировать на стадии, предшествующей метафазе, когда хромосома редуплицировалась, но еще не полностью конденсировалась. Это стадия прометафазы. Хотя хромосомы на стадии прометафазы плохо разъединены (они еще очень длинные), и в препарате много наложений одной хромосомы на другую, что, безусловно, затрудняет анализ, все же в отдельных клетках можно найти нужный участок, пригодный для анализа. Этот метод (или подход), в отличие от метафазного метода, называют прометафазным, или методом высокоразрешающей цитогенетики. Суть модификации метода состоит в прекращении процесса спирализации и конденсации хромосом в профазе с помощью препаратов, например метатрексата, которые вводят в культуру клеток за несколько часов до фиксации.
Следующее условие для получения хороших метафазных пластинок - гипотонизация клеток (гипотонический шок). Обычно для этого используют гипотонический раствор хлорида калия или цитрата натрия. В гипотоническом растворе клетки набухают, ядерная оболочка разрывается, межхромосомные связи рвутся, и хромосомы свободно плавают в цитоплазме.
Культивирование клеток, применение колцемида и гипотонизация стали условиями, на основе которых сформировались современные цитогенетические методы.
Клеточную суспензию фиксируют смесью метанола и уксусной кислоты (3:1), затем суспензию центрифугируют и меняют фиксатор.
Смесь клеток с фиксатором может сохраняться при температуре +4 °С в течение нескольких недель. При нанесении такой суспензии на чистое предметное стекло метафазная клетка расправляется и в ее пределах располагаются отдельно лежащие хромосомы. При высыхании фиксатора хромосомы прикрепляются к стеклу.
Выше описана методика получения препаратов из культуры лимфоцитов, которая используется наиболее часто. Для диагностических целей можно готовить препараты из хориона, костного мозга, семенников, культуры фибробластов, культуры амниоцитов. Процедуры для каждого объекта отличаются от описанной выше, но общий принцип сохраняется: накопление метафаз, гипотонизация, фиксация, капанье на предметное стекло, окраска, кариотипирование.
Окраска препаратов
Следующая стадия цитогенетических методов - окраска препаратов. Методы окраски бывают простыми, дифференциальными, флюоресцентными.
Наиболее распространен метод окраски по Гимзе, или простая окраска (в русскоязычной литературе распространен также термин «рутинная окраска»). Краситель Гимзы окрашивает все хромосомы равномерно по всей длине (рис. 9.3) При этом контурируются центромера, спутники (иногда со спутничными нитями) и вторичные перетяжки. Механизм связывания красителя
Гимзы хромосомами неясен. Он не является специфичным для какого-либо азотистого основания ДНК.

Рис. 9.3. Метафазная пластинка при простой окраске
При простой окраске возможна только групповая идентификация хромосом, поэтому данный метод используется для ориентировочного определения числовых аномалий кариотипа. Структурные хромосомные аномалии (делеции, транслокации, инверсии), выявляемые при простой окраске, должны быть идентифицированы с помощью дифференциальной окраски.
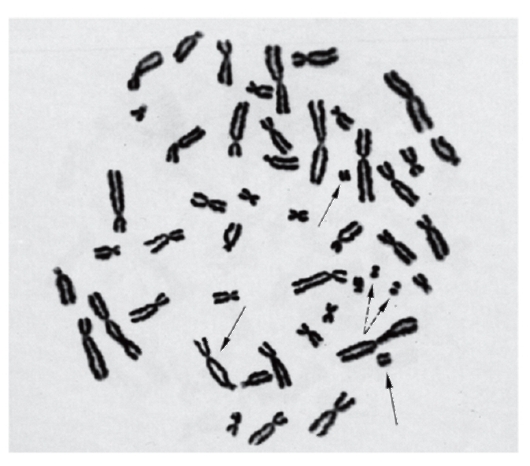
Рис. 9.4. Метафазная пластинка с радиационно-индуцированными хромосомными аберрациями
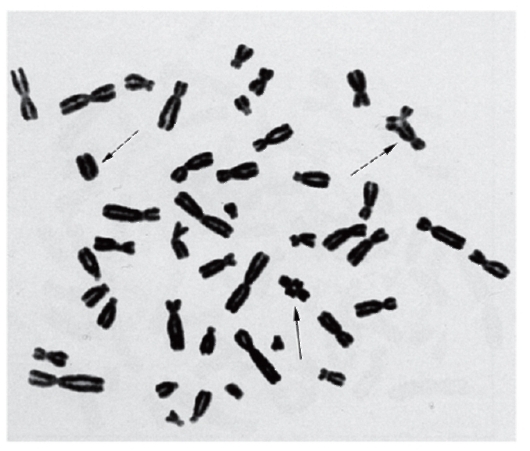
Рис. 9.5. Метафазная пластинка (неполная) с химически-индуцированными аберрациями
Простая окраска широко применяется для изучения хромосомного мутагенеза (учет хромосомных аберраций) при проверке факторов окружающей среды на мутагенность. На рис. 9.4, 9.5 хорошо видны аберрации, возникшие под влиянием радиации и химических мутагенов.
Метод простой окраски хромосом как единственный метод изучения кариотипа человека применялся до начала 70-х годов XX в. С его помощью за 10 лет были открыты основные хромосомные болезни, показана роль хромосомных аномалий в спонтанных абортах, врожденных пороках развития и канцерогенезе, разработаны принципы биологической дозиметрии.
Морфологическая однородность хромосомы по длине на стандартно приготовленных и окрашенных по Гимзе препаратах обманчива. Прогресс цитогенетики человека позволил выявить глубокую линейную дифференцированность не только функции, но и структуры хромосом. В 70-х годах в практику вошли методы дифференциального окрашивания.
Под дифференциальной окрашиваемостью хромосом понимают их способность к избирательному окрашиванию по длине без прижизненной модификации какими-либо воздействиями. Дифференциальное окрашивание хромосом обеспечивается сравнительно простыми температурно-солевыми воздействиями на фиксированные хромосомы. При этом выявляется структурная дифференцировка хромосом по длине, выражающаяся в чередовании эу- и гетерохроматиновых
районов (темные и светлые полосы). Протяженность этих участков специфична для каждой хромосомы, соответствующего плеча и района. Как видно на рисунках 9.6, 9.7, при дифференциальной окраске идентифицируются все хромосомы, плечи и даже определенные районы. Каждая хромосома имеет свой рисунок исчерченности. При дифференциальной окраске метафазных хромосом в
кариотипе можно оценить около 200-400 участков (разрешающая способность метода), на стадии прометафазы - до 2000.

Рис. 9.6. Метафазная пластинка после дифференциальной окраски
Первоначально при специальном окрашивании хромосом использовали флюоресцентное алкилирующее вещество акрихин-иприт. Этот вариант был назван Q-методом, он требует быстрой обработки препарата, что не всегда удобно. Для просмотра препарата надо пользоваться люминесцентным микроскопом.
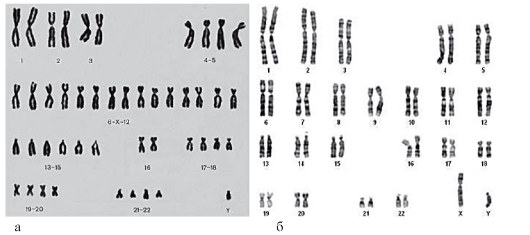
Рис. 9.7. Кариотипы при простой (а) и дифференциальной (б) окраске
В дальнейшем была разработана методика дифференциальной окраски без флюоресцентных
красителей. Наиболее широко используется G-окраска (по Гимзе). Хромосомы нужно предварительно обрабатывать (инкубация в солевом растворе либо обработка протеазой). Предварительная обработка частично нарушает структуру хромосом, в некоторых участках она восстанавливается при окраске, что и придает хромосоме индивидуальную исчерченность. Механизм образования сегментов пока недостаточно ясен. Предполагается, что окрашенные сегменты - это гетерохроматиновые, поздно реплицирующиеся участки хромосом с повторяющимися последовательностями ДНК, а неокрашенные - это эухроматиновые участки, в которых расположены кодирующие последовательности.
Для идентификации хромосом, помимо методов выявления линейной структурной дифференцированности, можно воспользоваться одной из важных характеристик хромосом человека - асинхронностью их репликации по длине. Этот метод разработал талантливый отечественный цитогенетик А.Ф. Захаров о его роли в цитогенетике можно прочитать на компакт-диске. «Рисунки» последовательности репликации (рано или поздно реплицирующиеся участки) специфичны для каждой хромосомы. Для выявления последовательности репликации применяется аналог тимидина - 5-бромдезоксиуридин. Участки хромосомы, включившие этот аналог, окрашиваются плохо. Используя этот метод, можно идентифицировать любую хромосому или хромосомную перестройку.
5-бромдезоксиуридин вводят в культуру на 24 ч и более для дифференциальной окраски сестринских хроматид. Если 5-бромдезоксиуридин ввести на полный клеточный цикл, то вновь образуемая хроматида включит
аналог тимидина и будет окрашиваться слабо. Другая хроматида (старая) окрашивается, как обычно, интенсивно (рис. 9.8). Этот метод позволяет легко выявлять обмены между сестринскими хроматидами, число которых увеличивается при наследственных болезнях с хромосомной нестабильностью (анемия Фанкони, пигментная ксеродерма и др.) (рис. 9.9). Число обменов сестрин-
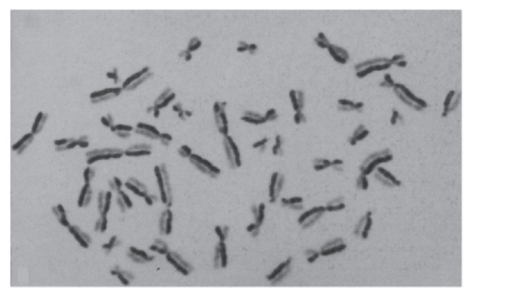
Рис. 9.8. Метафазная пластинка с дифференциальной окраской сестринских хроматид
ских хроматид увеличивается также при мутагенных воздействиях, поэтому метод учета обменов сестринских хроматид широко используется при изучении мутационного процесса у человека.
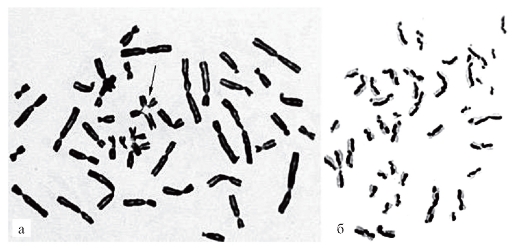
Рис. 9.9. Хроматидные аберрации (а) и сестринские хроматидные обмены (б) при заболеваниях с хромосомной нестабильностью
Молекулярно-цитогенетические методы
Благодаря успехам в молекулярной генетике человека разработан принципиально новый метод изучения хромосом - метод FISH. Принцип этого метода показан на рис. 9.10.
Для изучаемой хромосомы или ее конкретного участка (в связи со специфичностью последовательности оснований ДНК) готовят однонитевой участок ДНК, к которому присоединяется биотин или дигоксигенин. Такой помеченный участок ДНК называется зондом.
На микроскопическом препарате in situ при обработке щелочью хромосомная ДНК денатурируется, т.е. разрываются связи между двумя нитями ДНК.
Зондом обрабатывают препарат. Поскольку последовательность оснований ДНК зонда и соответствующий участок хромосомы взаимно комплементарны, зонд присоединяется к хромосоме. В этом участке происходит ренатурация ДНК.
После этого препарат обрабатывают веществом, которое способно избирательно присоединиться к биотину или дигоксигенину. Для биотина это стрептавидин, для дигоксигенина - антидигоксигениновое антитело. К этим веществам могут быть присоединены в один
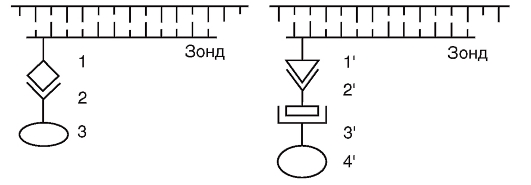
Рис. 9.10. Двойная специфическая флюоресцентная гибридизация in situ (FISH): 1 - биотин; 2 - стрептавидин; 3 - родамин; 1'-дигоксигенин; 2'-антидигоксигениновое антитело; 3', 4'-флюоросцеина изотиоцианат
или два этапа флюоресцентные красители (родамин - красный цвет или флюоресцеина изотиоцианат - зеленый цвет).
С помощью люминесцентного микроскопа окрашенные хромосомы можно увидеть на фоне неокрашенных.
На рисунке 9.10 приведена двойная гибридизация, однако современные методические возможности позволяют увеличить число цветов.
Метод FISH применяется очень широко - от локализации гена до расшифровки сложных перестроек между несколькими хромосомами. Следует подчеркнуть, что сочетание молекулярногенетических и цитологических методов делает почти неограниченными возможности диагностики хромосомных аномалий, как очень сложных, так и очень мелких. Двух- и трехцветная FISH применяется для учета симметричных хромосомных аберраций у лиц, много лет назад получивших дозу ионизирующего излучения. Метод требует меньше времени, чем кариотипирование дифференциально окрашенных метафаз.
В клинической цитогенетике метод FISH занимает все большее место. В случаях сложных хромосомных перестроек, захватывающих более двух хромосом, дифференциальная G-окраска не всегда позволяет идентифицировать измененные сегменты хромосом. В этих случаях применяют трехцветный вариант метода FISH. Например, у ребенка с множественными врожденными аномалиями при G-анализе обнаружены сложные перестройки в 6 хромосомах (1, 4, 7, 8, 9 и 12) с 10 разрывами. Полная идентификация разрывов возможна только с помощью FISH-окраски.
Метод FISH можно применять для диагностики анеуплоидий в интерфазных ядрах. Принцип метода в этом варианте такой же, как и для метафазных пластинок, описанный выше. Например, специфичный для хромосомы 21 зонд ДНК, соединенный с биотином, гибридизируется с денатурированными клетками из амниотической жидкости на предметном стекле. В норме, т.е. если у плода есть дисомия по хромосоме 21, в ядре будут видны 2 флюоресцирующие соответствующим цветом точки. Если плод трисомный, то в ядре будут видны 3 точки (рис. 9.11). Такой методический прием называют интерфазной цитогенетикой. Метод прост, экономичен, анализ занимает всего несколько часов.
Метод CGH (comparative genome hybridization). Область использования - онкологическая цитогенетика, назначение - определение районов хромосом, которые делетируются или амплифицируются в определенном типе опухоли. Районы делеций, как правило, содержат гены-супрессоры опухолевого роста, а районы амплификации - онкогены. Таким образом, метод используется в большей степени для картирования и клонирования генов, вовлеченных в канцерогенез. Иногда достаточно сложно получить хромосомные препараты хорошего качества из солидной опухоли или у пациентов с гематологическими онкологическими заболеваниями. В связи с этим был разработан оригинальный метод косвенного анализа хромо-
сом в опухоли. Суть метода CGH состоит в том, что из опухоли выделяют ДНК и метят ее определенным флюорохромом. ДНК, выделенную из нормальной ткани, метят другим флюорохромом. Хромосомные препараты приготавливают стандартным способом из лимфоцитов периферической крови контрольного индивида. Меченую ДНК из опухоли и неизмененной ткани гибридизуют с хромосомным препаратом. По интенсивности свечения метки определяют области делеций и амплификаций. Область разрешения -
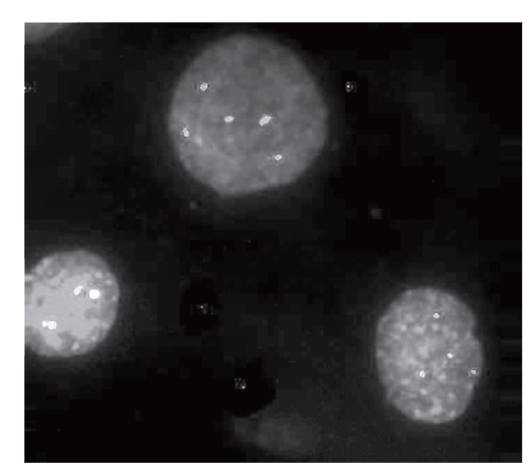
Рис. 9.11. Флюоресцентная гибридизация in situ (FISH). Вверху ядро с трисомией по хромосоме 6 и дисомией по хромосоме 8
5-10 млн пар нуклеотидов. Для обработки данных используют программы компьютерного анализа хромосом.
Спектроскопический анализ хромосом (SKY). При этом методе используются флюоресцентные красители, имеющие сродство к определенным участкам хромосом. При использовании набора специфических зондов с разными красителями каждая пара хромосом имеет свои уникальные спектральные характеристики. Особенность метода - использование интерферометра, аналогичного используемым для измерения спектра астрономических объектов. Незначительные вариации в спектральном составе, не различимые человеческим глазом, учитываются при компьютерной обработке, и затем программа назначает каждой паре хромосом легко распознаваемые цвета. Результат в виде цветного изображения чаще используется в цифровой форме. Анализ кариотипа значительно облегчается, поскольку гомологичные хромосомы имеют один и тот же цвет, а аберрации становятся легкоразличимыми. Кроме того, спектральное кариотипирование используется для выявления транслокаций, не распознаваемых традиционными методами. Область использования метода - онкоцитогенетика. Благодаря такому подходу удается точно описать множественные структурные перестройки хромосом, происходящие в опухолевых клетках.
В клинической цитогенетике удается определять очень незначительные по величине транслокации, инсерции и маленькие маркерные хромосомы. Однако использование метода ограничено высокой стоимостью оборудования для анализа. Более подробные сведения о цитогенетических методах см. на компакт-диске в статье «Современная клиническая цитогенетика» и в статье Н.Б. Рубцова и Т.В. Карамышевой «Прямая и обратная цитогенетка».
Показания для проведения цитогенетических исследований
Показания для цитогенетического исследования достаточно широкие, особенно при акушерско-гинекологической и детской патологии. Ниже приводится перечень (возможно, неполный) состояний, при которых для диагностики надо иметь результаты цитогенетического исследования у пациента (пробанда) и в случае необходимости у его родственников:
- Подозрение на хромосомную болезнь по клинической симптоматике (для подтверждения диагноза).
- Наличие у ребенка множественных врожденных пороков развития, не относящихся к генному синдрому.
- Многократные (более двух) спонтанные аборты, мертворождения или рождения детей с врожденными пороками развития.
- Нарушение репродуктивной функции неясного генеза у женщин и мужчин (первичная аменорея, бесплодный брак и др.).
- Существенная задержка умственного и физического развития у ребенка.
- Пренатальная диагностика (по возрасту, в связи с наличием транслокации у родителей, при рождении предыдущего ребенка с хромосомной болезнью).
- Подозрение на синдромы с хромосомной нестабильностью (учет хромосомных аберраций и сестринских хроматид).
- Лейкозы (для дифференциальной диагностики, оценки эффективности лечения и прогноза).
- Оценка мутагенных воздействий (радиационных, химических).
Медицинских ограничений для применения цитогенетических методов нет. Однако необходимо помнить, что эти методы трудоемкие, дорогие, их назначение наугад не оправдано (по принципу «если неясно, то давайте назначим»). Правильнее назначать цитогенетическое исследование по рекомендации врача-генетика после проведения медико-генетического консультирования.
Опыт работы зарубежных медицинских учреждений показал необходимость создания цитогенетических лабораторий при больших многопрофильных больницах и медико-генетических консультациях, комплексно обслуживающих какой-либо район или город. В России цитогенетические исследования проводятся в медико-генетических кабинетах и медико-генетических консультациях.
БИОХИМИЧЕСКИЕ МЕТОДЫ
Биохимические методы в лабораторной диагностике наследственных болезней применяются с начала XX в. Биохимические показатели (первичный белковый продукт гена, накопление патологических метаболитов внутри клетки и во внеклеточных жидкостях) лучше отражают сущность болезни, чем клинические симптомы, не только в диагностическом, ноив генетическом аспекте. Значимость биохимических методов повышалась по мере описания наследственных болезней и совершенствования этих методов (электрофорез, хроматография, спектроскопия и др.). В 80-х годах ХХ в. был выделен целый
раздел - наследственные болезни обмена веществ, т.е. заболевания с различными биохимическими нарушениями.
Биохимические методы направлены на выявление биохимического фенотипа организма. Уровни, на которых оценивается фенотип, могут быть разными: от первичного продукта гена (полипептидной цепи) до конечных метаболитов в крови, моче или поте. Биохимические методы чрезвычайно многообразны, и их значение в диагностике наследственных болезней постоянно возрастает. Разработка молекулярно-генетических методов диагностики наследственных болезней частично снизила интерес к биохимическим исследованиям, но вскоре стало ясно, что в большинстве случаев указанные методы дополняют друг друга, поскольку молекулярно-генетически описывается генотип, а биохимически - фенотип. Болезнь - это в конечном счете фенотип. В связи с этим, несмотря на сложность, а иногда и дороговизну биохимических методов, им принадлежит ведущая роль в диагностике моногенных наследственных болезней. Современные высокоточные технологии (высокоэффективная жидкостная хроматография, хроматомасс-спектрометрия, газовая хроматография, тандемная спектрометрия) позволяют идентифицировать любые метаболиты, специфичные для конкретной наследственной болезни.
На первый взгляд может показаться, что самым точным методом диагностики является определение мутации на уровне ДНК. Однако это не всегда так. Реализация действия гена - сложный процесс, поэтому «нормальная» структура гена, а точнее, необнаружение мутации, не всегда бывает полной гарантией нормального биохимического фенотипа.
Принципы биохимической диагностики наследственных болезней менялись в процессе развития генетики человека и биохимии. Так, до 50-х годов XX в. диагностика была направлена на поиски специфичных для каждой болезни метаболитов в моче (алкаптонурия, фенилкетонурия). С 50-х до 70-х годов упор в диагностике был сделан на выявление энзимопатий. Разумеется, поиски метаболитов в конечных реакциях при этом не исключались. Наконец, с 70-х годов главным объектом при диагностике стали белки разных групп. К настоящему времени все эти объекты являются предметом биохимической диагностики.
Оценка метаболитов в биологических жидкостях - необходимый этап диагностики аминоацидопатий, органических ацидурий, муко-
полисахаридозов, митохондриальных и пероксисомных болезней, дефектов метаболизма пуринов и пиримидинов и т.д. Для этих целей используют методы качественного химического анализа, спектрофотометрические методы количественной оценки соединений, а также различные виды хроматографии.
Хроматографические методы анализа играют важнейшую роль в диагностике наследственных болезней обмена. Это обусловлено тем, что современный арсенал хроматографических технологий чрезвычайно широк и позволяет эффективно и информативно разделять сложные многокомпонентные смеси, к которым в том числе относится и биологический материал. Для количественного анализа маркеров-метаболитов наследственных болезней обмена успешно применяются такие хроматографические методы, как газовая и высокоэффективная жидкостная хроматография, а также хроматомасс-спектрометрия. Газовая и высокоэффективная жидкостная хроматография являются универсальными методами разделения сложных смесей соединений, отличаются высокой чувствительностью и воспроизводимостью. В обоих случаях разделение осуществляется в результате различного взаимодействия компонентов смеси с неподвижной и подвижной фазами хроматографической колонки. Для газовой хроматографии подвижной фазой является газноситель, для жидкостной хроматографии - жидкость (элюент). Выход каждого соединения фиксируется детектором прибора, сигнал которого преобразуется в пики на хроматограмме. Каждый пик характеризуется временем удерживания и площадью. Следует отметить, что газовая хроматография проводится, как правило, в высокотемпературном режиме, поэтому ограничением для ее применения является термическая неустойчивость соединений. Для высокоэффективной жидкостной хроматографии не существует подобных ограничений, так как в этом случае анализ проводится в мягких условиях.
Масс-спектрометрия - аналитический метод, с помощью которого можно получать как качественную (структура), так и количественную (молекулярная масса или концентрация) информацию от анализируемых молекул после их преобразования в ионы. Существенное отличие масс-спектрометрии от других аналитических физикохимических методов состоит в том, что в масс-спектрометре определяются непосредственно масса молекул и их фрагментов. Результаты представляются графически (так называемый масс-спектр). Иногда невозможно анализировать многокомпонентные, сложные смеси молекул без их предварительного разделения. Разделить молекулы
можно либо хроматографически (жидкостная или газовая хроматография), либо использовать два последовательно соединенных массспектрометра - тандемная масс-спектрометрия.
Тандемная масс-спектрометрия позволяет охарактеризовать структуру, молекулярную массу и провести количественную оценку 3000 соединений одновременно. При этом не требуется длительной подготовки проб для проведения анализа (как, например, для газовой хроматографии), а время исследования занимает несколько секунд. Нозологические формы наследственных болезней обмена, которые можно диагностировать с использованием тандемной массспектрометрии, приведены в табл. 9.1.
Таблица 9.1. Заболевания, диагностируемые с помощью тандемной массспектрометрии
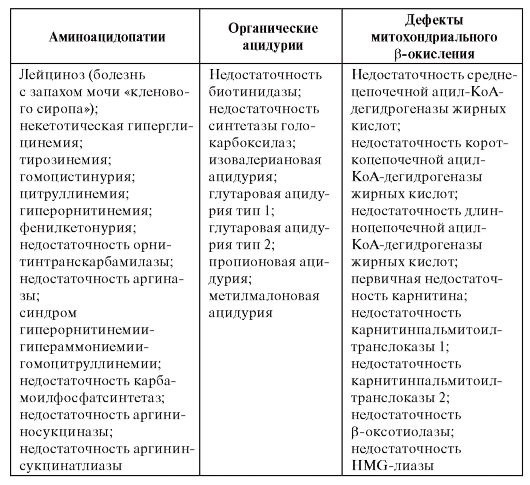
Тандемная масс-спектрометрия является одним из перспективных направлений в развитии программ диагностики наследственных болезней обмена, поскольку позволяет количественно и в микроколичествах биологического материала определять множество метаболитов. В настоящее время в некоторых странах данный метод применяется для массового скрининга новорожденных. Для более подробного ознакомления см. статью Г.В. Байдакой и Е.Ю. Захаровой «Тандемная масс-спектрометрия с ионизацией в электроспрее: принцип метода и применение для диагностики наследственных болезней обмена» на компакт-диске.
В связи с многообразием биохимических методов, применяемых в лабораторной диагностике наследственных болезней, в использовании этих методов должна быть определенная система. У пробанда или члена его семьи нереально исключить все наследственные болезни, которые могут быть в поле зрения при обследовании. Если применять максимально возможное число методов диагностики, то каждое обследование станет очень трудоемким и долгим. Исходная схема обследования строится на клинической картине болезни, генеалогических сведениях и биохимической стратегии, которые позволяют определить ход обследования на основе поэтапного исключения определенных классов наследственных болезней обмена (просеивающий метод).
Необходимо подчеркнуть, что биохимические методы (в отличие от цитогенетических) многоступенчаты. Для их проведения требуется аппаратура разных классов. Материалом для биохимической диагностики могут быть моча, пот, плазма и сыворотка крови, форменные элементы крови, культуры клеток (фибробласты, лимфоциты), биоптаты мышц. При использовании просеивающего метода в биохимической диагностике можно выделить два уровня: первичный и уточняющий. Каждый из этих уровней может быть по-разному «нагружен» реакциями в зависимости от возможностей лаборатории.
Основная цель первичной диагностики заключается в том, чтобы выявить здоровых людей и отобрать пациентов для последующего уточнения диагноза. В таких программах первичной диагностики в качестве материала используются моча и небольшое количество крови. Программы первичной биохимической диагностики наследственных болезней могут быть массовыми и селективными. Массовые просеивающие программы в диагностике фенилкетонурии, врожденного гипотиреоза, адреногенитального синдрома, врожденных аномалий развития нервной трубки и болезни Дауна описаны в главе 11.
Селективные диагностические программы предусматривают проверку биохимических аномалий обмена (моча, кровь) у пациентов с подозрением на генные наследственные болезни. Фактически такие программы должны функционировать в каждой большой больнице. Показания для их применения достаточно широкие, стоимость каждого анализа невысокая.
В селективных программах могут использоваться простые качественные реакции (например, тест с хлоридом железа для выявления фенилкетонурии или с динитрофенилгидразином для выявления кетокислот) или более точные методы, позволяющие обнаруживать большие группы отклонений. Газовая хроматография применяется для выявления наследственных болезней обмена органических кислот, ряда аминоацидопатий. С помощью электрофореза гемоглобинов диагностируют все заболевания из группы гемоглобинопатий. На рисунке 9.12 представлены результаты биохимической диагностики лизинурической непереносимости белка.
Нередко приходится углублять биохимический анализ от количественного определения метаболита до определения активности фер-
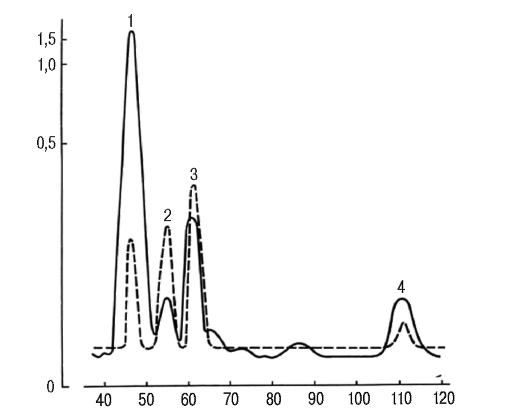
Рис. 9.12. Количественное содержание диаминокислот в образце суточной мочи больного с лизинурической непереносимостью белка. Выполнено на аминокислотном анализаторе: по оси абсцисс - время элюирования, мин; по оси ординат - концентрация, мкМ; сплошная линия - больной; пунктирная линия - норма, 1 - лизин; 2 - гистидин; 3 - аммиак; 4 - аргинин
мента (использование нативных тканей или культивированных клеток), например, с помощью спектрофлуориометрии.
В современных условиях очень многие этапы биохимической диагностики осуществляются автоматически, в частности аминоанализаторами.
Селективные диагностические программы обеспечивают только предположительное выявление больных с наследственными болезнями обмена веществ. Методы подтверждающей диагностики включают количественное определение метаболитов, исследование их кинетики, энзимодиагностику, ДНК-диагностику (табл. 9.2).
Таблица 9.2. Методы подтверждающей диагностики
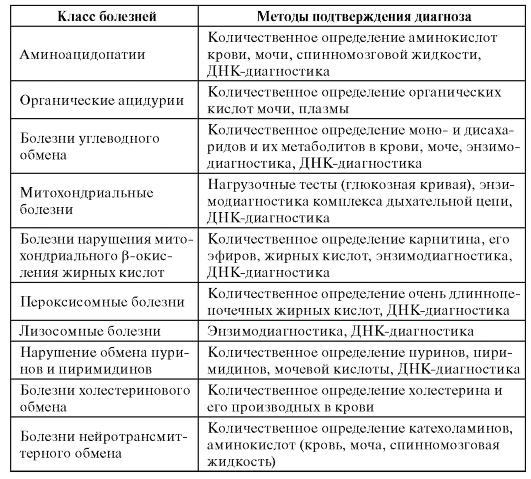
Как видно из табл. 9.2, методы подтверждения диагноза многообразны и специфичны для разных классов болезней.
Показаниями для применения биохимических методов диагностики у новорожденных являются судороги, кома, рвота, гипотония, желтуха, специфический запах мочи и пота, ацидоз, нарушенное кислотно-основное равновесие, остановка роста. У детей биохимические методы используют во всех случаях подозрения на наследственные болезни обмена веществ (задержка физического и умственного развития, потеря приобретенных функций, клиническая картина, специфичная для какой-либо наследственной болезни).
Биохимические методы применяют для диагностики наследственных болезней и гетерозиготных состояний у взрослых (гепатолентикулярная дегенерация, недостаточность α1-антитрипсина, недостаточность Г6ФДГ и т.д.). Для диагностики многих болезней биохимические методы заменяют молекулярно-генетическими в связи с их большей точностью или экономичностью. Более подробную информацию по диагностике болезней накопления можно найти в статье Е.Ю. Захаровой и др. «Лабораторная диагностикализосомных болезней накопления» на компакт-диске.
МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКИЕ МЕТОДЫ
Общие процедуры
Молекулярно-генетические методы - большая и разнообразная группа методов, в конечном счете предназначенных для выявления вариаций в структуре исследуемого участка ДНК (аллеля, гена, региона хромосомы) вплоть до расшифровки первичной последовательности оснований. В основе этих методов лежат манипуляции с ДНК и РНК. В результате бурного развития молекулярной генетики человека в 70-80-х годах XX в. и последующего успешного изучения генома человека молекулярно-генетические методы прочно вошли в медико-генетическую практику. Для идентификации и поиска ДНКполиморфизмов (мутаций) применяются уже более 100 разных методов. Однако широко используется только незначительная их часть.
Ниже схематично описаны основные этапы и варианты молекулярно-генетических методов. Освоение этих методов, как и других методов лабораторной диагностики, требует специальной подготовки в соответствующих лабораториях.
Получение образцов ДНК (или РНК) - первый этап всех методов. Он включает выделение всей ДНК (тотальной или геномной) из
клеток или накопление определенных фрагментов, которые предполагается анализировать с помощью ПЦР.
Источником геномной ДНК могут быть любые ядросодержащие клетки. Выделенная из клеток ДНК представляет собой весь геном организма, поэтому такие образцы называют геномной ДНК. На практике чаще используют периферическую кровь (лейкоциты), хорион, амниотические клетки, культуры фибробластов. Для одного анализа необходимо иметь (в зависимости от используемого метода) от нескольких нанограммов до нескольких микрограммов ДНК. Для этого требуется небольшое количество биологического материала, например 20-40 мг хориона, 1 мл крови, 5-10 мг культуры клеток. При использовании некоторых методов достаточно иметь одну каплю крови или соскоб эпителия со слизистой оболочки щеки либо несколько волосяных луковиц. Возможность проведения молекулярно-генетического анализа с небольшим количеством легкодоступного биологического материала - преимущество методов этой группы. Можно добавить, что выделенная ДНК одинаково пригодна для проведения различных вариантов методов и может долго сохраняться в замороженном виде.
В большинстве случаев для успешной диагностики болезни или гетерозиготного состояния достаточно исследовать небольшой фрагмент генома. Необходимо получить достаточное количество таких фрагментов, т.е. амплифицировать (умножить) их. Ранее решение этой задачи было трудоемким: создание рекомбинантной плазмиды
введение плазмиды в бактериальную клетку размножение бактериальных клеток - выделение заданных фрагментов ДНК. Теперь накопление нужных фрагментов ДНК обеспечивает ПЦР. Открытие этой реакции совершило революцию в изучении генома человека и молекулярно-генетической диагностике наследственных болезней.
ПЦР - метод амплификации ДНК in vitro. За несколько часов можно размножить определенную последовательность ДНК в количестве, превышающем исходное в миллион раз и более. Следовательно, исходно требуется незначительное количество материала. Для проведения ПЦР нужно знать нуклеотидную последовательность амплифицируемого фрагмента.
В соответствии с нуклеотидной последовательностью концов 5' и 3' исследуемого участка синтезируется два олигонуклеотидных праймера (затравки). Длина праймеров составляет 20-30 нуклеотидов.
Процесс амплификации состоит в повторяющихся циклах. Каждый цикл включает 3 стадии: температурную денатурацию
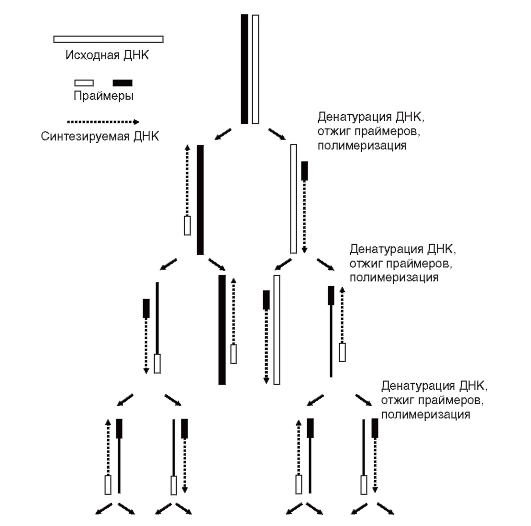
Рис. 9.13. Полимеразная цепная реакция (ПЦР)
ДНК (разделение двухцепочечной ДНК на одноцепочечные молекулы) - присоединение праймеров к комплементарным последовательностям одноцепочечных молекул (отжиг) - синтез полинуклеотидных цепей на одноцепочечных молекулах в границах присоединенных праймеров с помощью полимеразы (рис. 9.13). О ПЦР можно подробнее прочитать в на компакт-диске в статье С.С. Охапкиной «ПЦР - основа современной генодиагностики».
Рестрикция ДНК на фрагменты - необходимый этап молекулярногенетической диагностики, осуществляется рестриктазами, относящимися к группе бактериальных эндонуклеаз. В генетике человека используют несколько десятков разных рестриктаз (EcoRI, RsaI, HpaII, Ksp22I и др.). Они способны разрывать двухцепочечную ДНК в пределах строго определенных для каждого фрагмента последовательностей нуклеотидов протяженностью 4-6 пар оснований (редко больше). При обработке геномной ДНК определенной рестриктазой
получается закономерный для данного фермента набор фрагментов различной длины.
Электрофорез фрагментов ДНК обеспечивает разделение этих фрагментов при их распределении на поверхности агарозного или полиакриламидного геля. Фрагменты ДНК движутся в геле, помещенном в постоянное электрическое поле, от отрицательного полюса к положительному в зависимости от размеров (чем больше относительная молекулярная масса фрагмента, тем медленнее он движется в электрическом поле). После окончания электрофореза каждый фрагмент ДНК занимает определенное положение в виде дискретной полосы в конкретном месте геля. Длину каждого фрагмента можно определить путем сравнения пройденного фрагментом расстояния с расстоянием, пройденным стандартным образцом ДНК с известными размерами.
Визуализация и идентификация фрагментов ДНК в геле становятся либо конечным этапом диагностики, либо элементом дальнейшего анализа.
Визуализация фрагментов ДНК после ПЦР осуществляется сравнительно легко. После окончания ПЦР проводят электрофорез в агарозном геле, после чего гель обрабатывают этидия бромидом, который связывается с ДНК. При ультрафиолетовом облучении поверхности геля выявляется свечение в красной области спектра.
Разработаны и другие методы окраски ПЦР-фрагментов. В некоторых вариантах методов возможна автоматическая регистрация результатов.
Идентификацию конкретных фрагментов в геле среди геномной ДНК провести труднее. Из-за больших размеров генома человека после рестрикции образуется так много рестриктных фрагментов, что агарозный гель после электрофореза и окраски этидия бромидом в ультрафиолетовых лучах выглядит более или менее равномерно окрашенным, поэтому специфические фрагменты ДНК выявляют путем блот-гибридизации по Саузерну. Эта методика состоит из следующих этапов (рис. 9.14).
- После окончания электрофореза гель помещают в раствор основания (щелочи), в котором двухцепочечные фрагменты ДНК теряют связи и становятся одноцепочечными.
- Перенос ДНК с геля на нитроцеллюлозный или нейлоновый фильтр производится в буферном растворе. Непосредственно на поверхность геля кладут фильтр и стопку фильтровальной бумаги. В результате капиллярного эффекта создается ток буфера, перпендикулярный плоскости геля. Вымываемая из
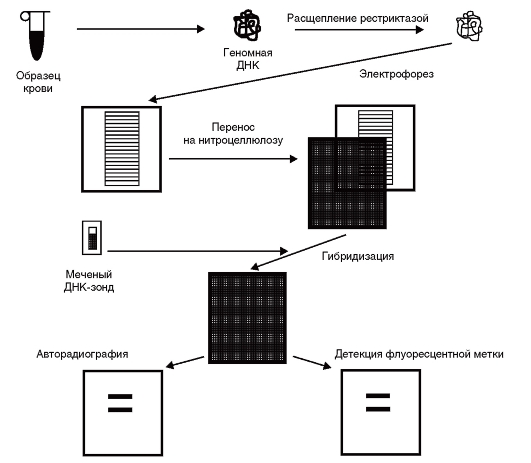
Рис. 9.14. Блот-гибридизация по Саузерну
геля ДНК задерживается фильтром и практически полностью оказывается на его поверхности. После переноса одноцепочечные нити фиксируют на фильтре. Расположение фрагментов на фильтре точно соответствует их расположению в геле. - Для того чтобы визуально выявить нужные фрагменты (фиксированная на фильтре ДНК не видна), проводят гибридизацию со специфическим по нуклеотидной последовательности меченым радионуклидом или флюоресцентной меткой олигонуклеотидным синтетическим зондом (такой зонд состоит из 16-30 пар оснований) либо клонированным фрагментом ДНК. Нуклеотидная последовательность зонда должна быть
полностью или частично комплементарна изучаемому участку геномной ДНК.
- При инкубации фильтра с раствором, содержащим меченый зонд, происходит гибридизация комплементарных цепей ДНК зонда и фрагмента на фильтре. Неспецифически связанные молекулы зонда отмываются с помощью специальной процедуры. Радиоактивно меченные участки выявляют путем экспонирования фильтра с рентгеновской пленкой (ауторадиография). После проявления на пленке видны полосы меченной зондом ДНК. Нерадиоактивные метки визуализируют с помощью флюоресценции или опосредованно с помощью антител.
Методы ДНК-диагностики наследственных болезней
ДНК-диагностика бывает подтверждающей , пресимптоматической, пренатальной, а также ДНК-диагностикой носительства.
Принципиально различают прямую и косвенную ДНКдиагностику моногенных наследственных болезней. Прямые методы возможны лишь при условии, что ген заболевания клонирован, известна его экзон-интронная организация или нуклеотидная последовательность полноразмерной комплементарной ДНК. При прямой диагностике предметом анализа являются мутации гена.
Однако для ряда наследственных заболеваний ген не клонирован или заболевание является генетически гетерогенным, т.е. обусловлено повреждениями в разных генах, либо молекулярная организация гена не позволяет использовать прямые методы. Эти трудности можно преодолеть с помощью косвенных методов ДНК-диагностики, основанных на использовании сцепленных с геном полиморфных маркеров. В этом случае определяется гаплотип хромосомы, несущей мутантный ген в семьях высокого риска, т.е. у родителей больного и его ближайших родственников. Такой подход возможен практически для всех моногенных заболеваний с известной локализацией гена.
Прямые методы диагностики мутаций
В ДНК-диагностике в настоящее время используются два типа прямых методов. Проще всего обнаруживаются мутации, изменяющие длину амплифицированных фрагментов ДНК, которые выявляются при электрофоретическом анализе.
Методы детекции известных мутаций. Если мутации известны, то можно их выявлять либо с помощью ферментов-рестриктаз, которые
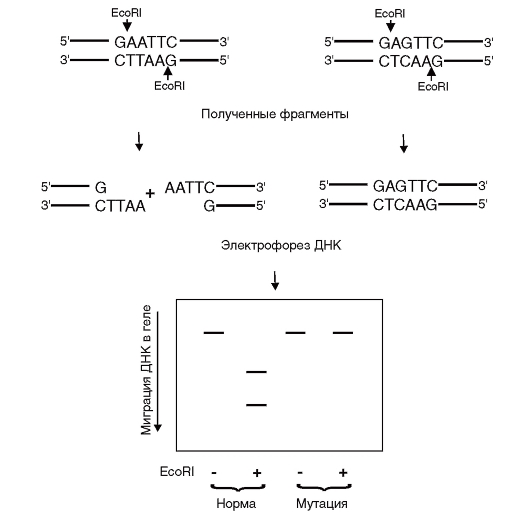
Рис. 9.15. Рестрикционный анализ с ферментом EcoRI
распознают строго определенные нуклеотидные последовательности, либо на основе ДНК-гибридизации.
Рестрикционный анализ - наиболее простой метод прямой детекции мутаций (рис. 9.15). Его суть состоит в том, что рестрикционные эндонуклеазы (бактериальные ферменты) разрезают двойную нить ДНК в определенных последовательностях из 4-8 нуклеотидов. Разрезанные участки мутантной ДНК, отличающиеся по длине от нормальных участков, выявляются на электрофореграмме. Если в состав сайта рестрикции входит полиморфный нуклеотид, эту мутацию можно выявить абсолютно достоверно. Если полиморфные
нуклеотиды лежат в неузнаваемых рестриктазой участках, то метод рестрикционного анализа неприменим.
Аллельспецифичная ПЦР используется для выявления точковых мутаций, небольших делеций и инсерций в исследуемых генах. ПЦР позволяет многократно увеличить уникальную последовательность ДНК, а затем проанализировать ее на предмет мутации. С помощью специфических олигонуклеотидных праймеров проводят амплификацию кодирующих участков геномной ДНК.
На рисунке 9.16 представлены результаты ДНК-диагностики в семье с мальчиком, страдающим муковисцидозом. Молекулярная структура этого гена хорошо известна. ПЦР-амплификация проведена по участку (сайту) расположения мутации F508 в гене муковисцидоза у детей и родителей. Как видно из электрофоретической картины, отец, мать и дочь (они здоровы) имеют две полосы (98 и 95 пар нуклеотидов), следовательно, они гетерозиготы. У больного мальчика одна полоса (95 пар нуклеотидов), т.е. он гомозиготен по мутантному аллелю F508. Обычно параллельно ставят реакции с праймерами, соответствующими мутантному и нормальному аллелям. Использование нормального праймера служит положительным контролем, свидетельствующим о нормальном ходе амплификации.
В 1988 г. был предложен еще один метод обнаружения мутаций - мультиплексная ПЦР. Метод позволяет проводить одновременно несколько амплификаций в одной пробирке. Это осуществляется путем добавления в реакцию сразу нескольких пар праймеров.
Мультиплексная ПЦР нашла применение во многих областях медицины: детекция мутаций, скрининг, обнаружение полиморфизмов, диагностика инфекционных заболеваний. За счет одновременного проведения нескольких реакций в одной пробирке данный метод позволяет экономить время и деньги. Однако, несмотря на явные преимущества, мультиплексная ПЦР требует длительной оптимизации протокола (подбор температур отжига праймеров, концентрации реактивов, параметров амплификации), что
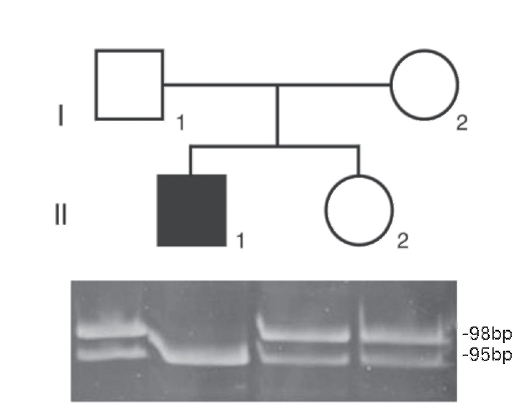
Рис. 9.16. ДНК-диагностика муковисцидоза с помощью технологии полимеразной цепной реакции (ПЦР) в сайте ∆F508. Объяснение в тексте
ограничивает ее широкое применение. Информация о методе мультиплексной ПЦР более подробно изложена на компакт-диске в статье А.В. Полякова с соавт. «Применение мультиплексной полимеразной цепной реакции для диагностики наследственных заболеваний».
Наряду с двумя разобранными выше прямыми методами детекции известных мутаций есть еще несколько методов, не менее точных, но более трудоемких. Это гибридизация с аллельспецифичными олигонуклеотидами, аллельспецифичная лигазная реакция, минисеквенирование, пиросеквенирование. Характеристики этих методов можно найти в специальной литературе.
В начале 90-х годов ХХ в. был предложен принципиально новый подход в диагностике заболеваний с помощью ПЦР - изобретена ПЦР в реальном времени. Суть метода заключается в том, что благодаря добавлению в пробирку специальных флуорофоров можно обнаруживать ПЦР-продукт на протяжении всей амплификации. Флуорофор встраивается в двухцепочечную ДНК и приобретает способность флюоресцировать, что детектируется прибором. Чем больше синтезировано ПЦР-продуктов, тем более интенсивная наблюдается флюоресценция.
Другой подход заключается в том, что к олигонуклеотиду прикрепляют флуорофор и гаситель флюоресценции. Если происходит гибридизация, то флуорофор отделяется от гасителя и фиксируется флюоресценция.
ПЦР в реальном времени позволяет не только обнаруживать ПЦРпродукт еще во время амплификации, но также и определять его количество и исходную концентрацию ДНК. Данный метод в основном применяют для оценки экспрессии генов. Для этого из ткани выделяют РНК, проводят реакцию обратной транскрипции (синтез кДНК) и далее ПЦР в реальном времени.
Новые технологии позволяют проводить синтез кДНК и ПЦР одновременно. Из преимуществ можно отметить высокую чувствительность метода, небольшое количество требуемой РНК (или кДНК), отсутствие необходимости проводить электрофорез после реакции, возможность одновременно проводить несколько сотен реакций на одном приборе. Из недостатков метода следует отметить следующее: он существенно дороже обычной ПЦР, требователен к качеству матрицы, позволяет амплифицировать лишь небольшие фрагменты ДНК.
В целом же ПЦР в реальном времени постепенно вытесняет обычную ПЦР. На сегодняшний день данный метод является одним из самых используемых.
В последнее время эпигенетическим процессам придают большое значение в этиологии многих болезней, в том числе и наследственных. Такие заболевания, как синдром Прадера-Вилли, Ангельмана, Беквита-Видемана, связывают с нарушением метилирования. Нарушение метилирования является также диагностическим критерием для многих онкологических заболеваний. В связи с этим была предложена качественная реакция для определения метилирования - метилсцецифическая ПЦР. Суть этой реакции состоит в следующем. ДНК обрабатывают бисульфитом натрия, в результате чего все неметилированные остатки цитозина конвертируются в урацил, а метилированные не изменяются. После этого проводят ПЦР с праймерами, соответствующими метилированной и неметилированной последовательности. По тому, с какой парой праймеров происходит амплификация, можно судить о метилировании. Из недостатков можно отметить сложность в подборе праймеров, неполную конверсию, возможность оценки только единичных CpG-динуклеотидов. Однако метод относительно дешев, специфичен и прост, что позволяет его широко использовать в диагностике злокачественных новообразований и болезней импринтинга.
Чувствительность и специфичность прямых методов диагностики высокие. Наиболее распространены три метода: рестрикционный анализ, аллельспецифичная ПЦР и ПЦР в реальном времени. Врачлаборант или исследователь в каждом случае останавливается на каком-то методе, а потом может перейти на другой. Все методы очень точные. Они позволяют однозначно определять мутацию ДНК, даже если разница составляет одно основание.
Методы мутационного скрининга. Если характер мутации неизвестен, а клиническая картина заболевания позволяет предположить, в каких генах могла произойти мутация, то в лабораторной диагностике применяются следующие методы мутационного скрининга:
• анализ перестроек ДНК-блотингом по Саузерну;
• анализ полиморфизма конформации одноцепочечной ДНК;
• электрофорез двухцепочечной ДНК в градиенте денатуранта;
• гетеродуплексный анализ;
• денатурирующая высокоэффективная жидкостная хроматография;
• химическое обнаружение неспаренных нуклеотидов;
Чувствительность скрининговых методов обнаружения мутаций не абсолютна. Однако соотношение между их информативностью и стоимостью достаточно высокое, поэтому они широко используются в практике. В то же время их отрицательная сила невелика, т.е. если не обнаружено изменений, это не значит, что их на самом деле нет.
Ниже будут приведены характеристики некоторых методов мутационного скрининга.
SSСР (Single Strand Conformation Polymorphism) - метод анализа конформационного полиморфизма однонитевой ДНК - основан на регистрации различий в электрофоретической подвижности однонитевых ДНК, одинаковых по величине, но различающихся вследствие нуклеотидных замен по пространственной организации молекул (рис. 9.17). Конформация небольших однонитевых ДНК зависит от нуклеотидной последовательности, поэтому замена даже одно-
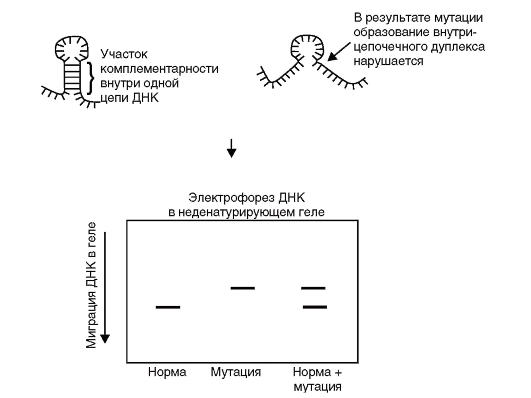
Рис. 9.17. Анализ полиморфизма конформации (SSСР) одноцепочечной
ДНК.
го нуклеотида приводит к изменению пространственной структуры. Метод включает амплификацию фрагментов ДНК размером до 300 пар нуклеотидов, денатурацию продуктов ПЦР и высокоразрешающий электрофорез в полиакриламидном геле.
Конформационный метод выявления точковых мутаций получил широкое распространение вследствие относительной простоты и способности обнаруживать любые типы замен. Ограничением является размер исследуемого фрагмента ДНК, так как высокая эффективность детекции мутаций, составляющая 80-90%, показана при длине фрагментов менее 200 пар нуклеотидов, а для фрагментов более 400 пар нуклеотидов вероятность обнаружения мутаций уменьшается до 50%.
В настоящее время разрешающая способность метода значительно повышена. В частности, разработаны подходы для идентификации точковых мутаций методом SSCP-анализа в амплифицированных фрагментах ДНК размером до 800 пар нуклеотидов. Для этого используется полиакриламидный гель с низким pH.
НА (Heteroduplex Analysis) - гетеродуплексный анализ позволяет выявлять мутации, находящиеся в гетерозиготном состоянии, а также инсерции и делеции. Принцип этого метода заключается в следующем.
При амплификации фрагментов генов гетерозигот, последующей денатурации и медленной ренатурации полученных продуктов ПЦР в амплификационной смеси наряду с двумя типами гомодуплексов образуются гетеродуплексы между нормальной и мутантной цепями ДНК (рис. 9.18). Такие гетеродуплексные молекулы отличаются по электрофоретической подвижности от гомодуплексов из-за конформационных особенностей в местах несовпадения нуклеотидов, поскольку электрофоретическая подвижность гетеродуплексов значительно ниже, чем гомодуплексов. Эти различия обнаруживаются при электрофорезе в обычном полиакриламидном геле.
Наиболее распространенный способ скрининга мутаций - комбинация анализа гетеродуплексов и метода однонитевого конформационного полиморфизма, позволяющая выявить точковые мутации почти в 100% случаев и не требующая больших затрат времени.
DGGE (Denaturating Gradient Gel Electrophoresis) - денатурирующий градиентный гель-электрофорез (рис. 9.19). ДНК-дуплексы подвергаются миграции в геле с градиентом денатурирующих условий (можно использовать и температурный градиент). Миграция продолжается до тех пор, пока ДНК-дуплексы не достигают в геле точки плавления
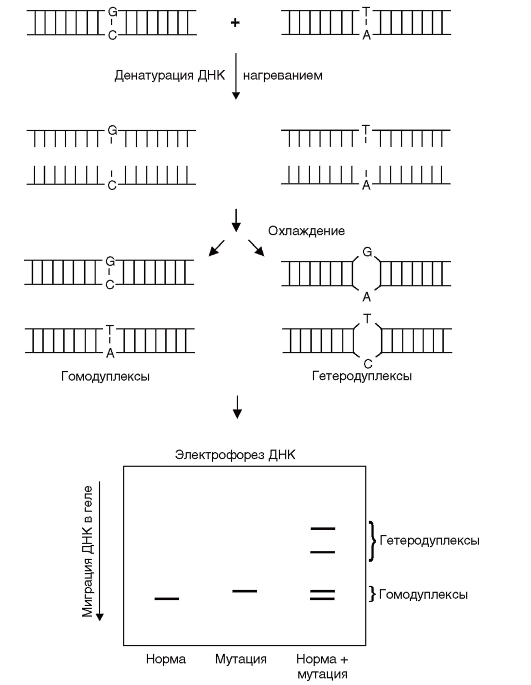
Рис. 9.18. Гетеродуплексный анализ (НА)
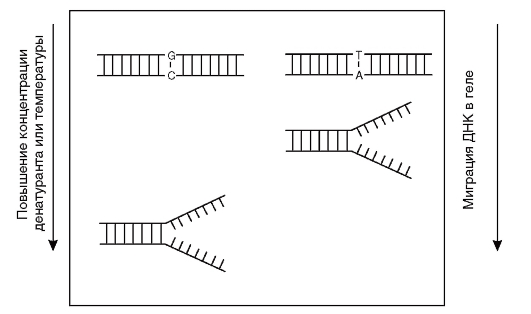
Рис. 9.19. Электрофорез в градиенте денатуранта (DGGE)
и не разделяются, после чего миграция фрагментов останавливается. Однонуклеотидные различия в нормальной и тестируемой ДНК выявляются по различной электрофоретической подвижности в геле. Высокая чувствительность метода (95%) достигается благодаря специфическим праймерам с так называемым GC-зажимом, представленным чередованием гуанина и цитозина в пределах до 20 нуклеотидов. В результате температура плавления продукта амплификации сильно увеличивается, что повышает эффективность определения мутации. Однако праймеры с GС-зажимом достаточно дороги, поэтому применение метода ограничено.
ССМ (Chemical Cleavage of Mismatch) - метод химического расщепления неспаренных оснований. Метод основан на гибридизации радиоактивно меченой ДНК-пробы с тестируемой ДНК. Места ошибок затем выявляют с помощью серии химических реакций (модификация с использованием тетрахлорида осмия), которые происходят с однонитевой ДНК в сайтах неправильного спаривания. Этот метод можно применять для тестирования фрагментов ДНК размером до 1000 пар нуклеотидов, он выявляет локализацию ошибки и довольно чувствителен. Однако метод не нашел широкого распространения вследствие токсичности химических реагентов и методической сложности. Подобное расщепление неспаренных нуклеотидов может быть и энзиматическим, что позволяет исключить использование
токсичных химикатов. Метод основан на расщеплении неспаренных оснований в гетеродуплексе, образуемом между тестируемой ДНК и нормальной последовательностью посредством таких ферментов, как резолваза фага Т4 или эндонуклеаза VII. Однако этот метод еще более «капризный», чем ССМ.
Заключительный этап анализа мутаций - их секвенирование, т.е. определение нуклеотидной последовательности фрагмента ДНК, показавшего аномальную электрофоретическую подвижность. Последовательность нуклеотидов этого фрагмента сравнивается с нормой, в результате чего патология приобретает свою окончательную характеристику.
Метод секвенирования является «золотым стандартом» молекулярной генетики. Поиск новых, редких и подтверждение известных мутаций можно провести с помощью этого метода. Диагностика многих наследственных заболеваний включает проведение секвенирования: предрасположенность к раку яичников и молочной железы (BRCA1 и BRCA2), нейрофиброматоз, фенилкетонурия, муковисцидоз и другие. При отсутствии мажорных мутаций, приводящих к наследственному заболеванию, часто секвенируют ген на предмет новых мутаций. Для некоторых генов, имеющих небольшие размеры, прямое секвенирование с успехом применяется как основной метод сканирования мутаций. Так, в частности, особенно удобным оказалось его применение для детекции мутаций в сравнительно небольших генах, таких, как ген фактора IX свертывания крови (гемофилия В).
Любые типы мутаций можно обнаружить путем прямого секвенирования мутантной ДНК или отдельных экзонов. Первичный поиск нарушений в кодирующих областях гена часто осуществляют именно таким образом.
Разработанные в последние годы модификации методов ПЦР значительно облегчили секвенирование амплифицированных фрагментов и повысили эффективность секвенирования. Так, в частности, предложен вариант асимметричной ПЦР, когда при амплификации концентрация одного из олигопраймеров в несколько десятков раз превосходит концентрацию другого праймера, в результате чего синтезируется преимущественно только одна, нужная для секвенирования цепочка ДНК.
Один из существенных недостатков технологии секвенирования - его дороговизна. Однако применение новых методик позволяет из года в год снижать стоимость секвенирования.
В настоящее время всё большее распространение получают секвенаторы нового поколения, которые обеспечивают параллельное секвенирование сотен тысяч последовательностей. В подавляющем большинстве случаев это дорогостоящее оборудование используется в научных целях. Однако стремительное развитие данного научнотехнического направления приводит к неуклонному повышению производительности и снижению стоимости оборудования и проведения анализа. В ближайшие годы можно ожидать применения секвенаторов в клинических целях - для неинвазивной пренатальной диагностики, быстрого и недорогого определения всех известных моногенных заболеваний, определения сотен полиморфизмов, связанных с рисками многофакторных болезней.
В табл. 9.3 представлены характеристики разных скрининговых методов ДНК-диагностики. Врач лаборант-генетик заранее определяет стратегию поиска в соответствии с оснащенностью лаборатории.
Таблица 9.3. Эффективность основных скрининговых методов ДНК-диагностики
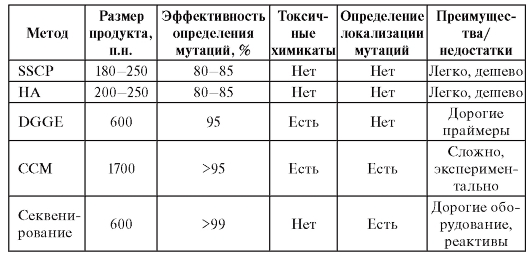
Примечание. CCM - метод химического расщепления неспаренных оснований (Chemical Cleavage of Mismatch); DGGE - денатурирующий градиентный гель-электрофорез (Denaturating Gradient Gel Electrophoresis); HA - гетеродуплексный анализ (Heteroduplex Analysis); SSCР - метод анализа конформационного полиморфизма однонитевой ДНК (Single Strand Conformation Polymorphism); п.н. - пар нуклеотидов.
Многие мутации прерывают синтез белкового продукта. В этих случаях образуются укороченные полипептидные цепи, функционально незначимые. Для диагностики таких мутаций можно применять метод трансляции белкового продукта. Он проводится in vitro на основе полученной специфической мРНК с добавлением лизата ретикулоцитов (в нем содержатся все необходимые компоненты для синтеза белка). В этой системе синтезируется белковый продукт соответствующего гена. Продукт трансляции анализируют с помощью электрофореза. Изменение электрофоретической подвижности белка свидетельствует о наличии мутации (нонсенс-мутация, нарушение сплайсинга РНК, сдвиг рамки считывания), приводящей к обрыву синтеза полипептидной цепочки.
В связи с бурно развивающимся направлением по изучению генетического полиморфизма и его роли в предрасположенности к многофакторным заболеваниям разработаны или усовершенствованы новые методы детекции разных вариантов генетических полиморфизмов. К ним можно отнести следующие методы, которые предназначены для автоматического или полуавтоматического исследования часто встречающихся полиморфизмов:
• денатурирующая жидкостная хроматография высокого разрешения - DHPLC (Denaturation High Performance Liquid Chromatography);
• методы биочипов и др.
Метод DHPLC фактически является вариантом метода гетеродуплексного анализа ДНК с последующим автоматическим учетом результатов с помощью жидкостного хроматографа. Его чувствительность и специфичность близки к 100%. Этот метод позволяет определять ОНП, делеции и инсерции длиной до 1500 п.о. в течение 2-3 мин. Его широко применяют для генотипирования ОНП и в других разделах изучения генетического полиморфизма, в том числе для картирования генов.
Методы биочипов в последние годы заняли существенное место в разнонаправленных молекулярно-биологических исследованиях.
Чипы представляют собой миниатюрные гелевые пластинки с многочисленными правильно расположенными углублениями или ячейками на стекле или какой-либо мембране. В углубления (ячейки) помещаются иммобилизованные зонды: ДНК, РНК, белки, клетки. В зависимости от этих зондов различают: ДНК-чипы, РНК-чипы, белковые микрочипы, клеточные микрочипы.
В клинической и медико-генетической практике наибольшее распространение получили ДНК-чипы. Они используются для анализа спектра мутаций или аллельных вариантов разных генов. Ячейки чипа заполняются (иммобилизуются) ДНК-зондами применительно к поставленной задаче исследования. Микрочиповая технология позволяет проводить реакцию в микрообъемах, а, следовательно, требуется незначительное количество материала, и в то же время проводить многосторонний анализ многих чипов одного и того же объекта. Выбор зондов для иммобилизации и их расположение в чипе программирует исследователь.
Чувствительность метода высокая, сопоставимая с другими ДНКовыми методами диагностики. С помощью ДНК-чипов можно анализировать транслокации, дупликации, делеции, как протяженные, так и короткие. ДНК-чипы могут содержать несколько сотен ДНК-зондов, что очень важно либо для массовых популяционных исследований одного гена, либо для исследований сотен тысяч генов одного индивида.
Технология приготовления микрочипов в настоящее время коммерциализирована, и многочисленные фирмы (в том числе в России) могут по заказу подготовить любой вариант чипа.
Интерес к использованию микрочипов в исследовательской практике в последнее время снизился, а в клинической практике повышается, особенно в связи с поиском ассоциаций генетических полиморфизмов с заболеваниями (предсказательная медицинская практика). Создаются биочипы для диагностики конкретных заболеваний, для поиска полиморфных систем генов детоксикации и фармакогенетически оправданного лекарственного лечения лейкозов, туберкулеза, бронхиальной астмы. Для более подробного ознакомления см. статью М.В. Голубенко с соавт. «ДНК-чет для исследования структуры наследственной предрасположенности к сердечно-сосудистым заболеваниям» на компакт-диске.
Другие методы или варианты вышеописанных методов распознавания мутаций (метод поверхностного плазмонового резонанса - surface plasmon resonance, метод масс-спектрометрии, метод «жидких биочипов», секвенирование ДНК с помощью нанопор), хотя и точные, но трудоемкие, и в клинической практике используются только в узких целях (см. раздел по биохимической диагностике).
Косвенное выявление мутаций
Когда нуклеотидная последовательность гена еще неизвестна и вместе с тем имеется информация об относительном положении гена
на генетической карте, применяют косвенное выявление мутаций. Фактически это соответствует диагностике с помощью метода сцепления генов.
Косвенная ДНК-диагностика, по существу, сводится к анализу полиморфных генетических маркеров у больных и здоровых членов семьи. Эти маркеры должны быть расположены в том же хромосомном регионе, где и ген болезни, т.е. они сцеплены. Такими маркерами могут быть участки ДНК, существующие в популяции в нескольких аллельных вариантах. Различия могут быть по составу нуклеотидов, по числу динуклеотидных повторов. На основе вариабельности состава маркерных участков ДНК можно дифференцировать материнское или отцовское происхождение конкретного варианта маркера, сцепленного с геном болезни. Сцепление означает, что маркер и ген болезни располагаются близко друг к другу; они передаются в составе одного хромосомного сегмента. Благодаря анализу полиморфных генетических маркеров можно проследить в ряду поколений наследование каждой из родительских хромосом.
Технические приемы в косвенной диагностике те же самые, что и в прямой (получение ДНК, рестрикция, электрофорез и т.д.). Естественно, к этому добавляется математический анализ сцепления признаков.
Использование косвенных подходов оказалось возможным благодаря существованию в геноме полиморфных участков (локусов) ДНК. Нуклеотидные замены достаточно часто встречаются в некодирующих участках ДНК. Значительное число нуклеотидных замен приводит к изменению мест рестрикции. Эти изменения можно выявить с помощью блот-гибридизации по Саузерну, поскольку изменяется длина рестриктных фрагментов. Эта разновидность полиморфизма ДНК получила название полиморфизма по длине рестриктных фрагментов.
Расположенный вблизи изучаемого гена или внутри него полиморфный сайт может служить маркером аллельных вариантов этого гена, в том числе маркером патологических мутаций.
Полиморфизм, обусловленный нуклеотидными заменами или делециями, как правило, диаллелен, а, значит, его информационная ценность ограничена. Более информативны кластеры тандемных повторов, которые обусловливают полиморфизм по количеству копий (VNTR - variable number of tandem repeats), так называемый полиморфизм мини- и микросателлитных последовательностей.
Микросателлиты - короткие тандемные повторы, обычно двугексануклеотидные. Самый распространенный из них - CA-повтор. Показано, что кластеры СА-повторов встречаются в среднем 1 на 30 000 пар нуклеотидов. Они локализованы, как правило, в некодирующих районах ДНК. Блоки СА-повторов имеют менделевское наследование в семьях и не обнаруживают новых мутаций (рис. 9.20). Немаловажным положительным фактором является относительная простота обнаружения таких повторов в геноме человека. Кроме СА-повторов, достаточно распространены GA-повторы и другие кластеры тандемных повторов (ТТТА)хп, (TCTA)xn, (TTTC)xn, также обнаруживающие вариабельность по числу повторов. Широкая распростра-
ненность в геноме (частота различных микросателлитов, взятых вместе, составляет 1 на 6000 пар нуклеотидов) и высокий уровень полиморфизма делают микро- и мини-сателлиты идеальными полиморфными маркерами для картирования генов наследственных заболеваний и проведения косвенной ДНК-диагностики.
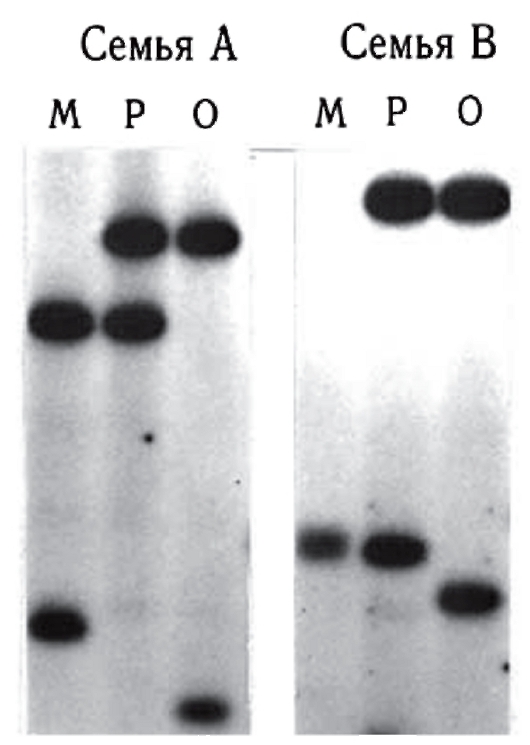
Рис. 9.20. Семейный анализ фрагментов ДНК с помощью блотгибридизации по Саузерну: М - мать, Р - ребенок, О - отец
Полиморфные ДНК-маркеры и интегральная карта их расположения позволяют определить и проследить в поколениях хромосому, несущую патологический ген, а также подробнейшим образом охарактеризовать определенный хромосомный район, выявить субмикроскопические перестройки, определить наименьший район их перекрывания и локализовать ген-кандидат, ответственный за заболевание.
Основной недостаток косвенных методов диагностики - обязательное предварительное изучение генотипа (гаплотипа) хотя бы одного пораженного родственника. В случае отсутствия пораженных
родственников, доступных для обследования, диагностика (за редким исключением) становится невозможной.
Итак, существует достаточно много молекулярно-генетических методов диагностики наследственных болезней. Эти методы оказались настолько универсальными, что нашли применение не только в медицинской генетике, но и диагностике инфекционных заболеваний. Каждый из представленных в табл. 9.4 методов имеет много вариантов. Одни и те же болезни можно диагностировать разными методами. Можно диагностировать болезнь даже в трудных случаях (невозможность обследования родителей, малое количество биологического материала, отсутствие сведений о гене и т.д.).
Таблица 9.4. Сравнительные характеристики прямых и непрямых методов ДНК-диагностики
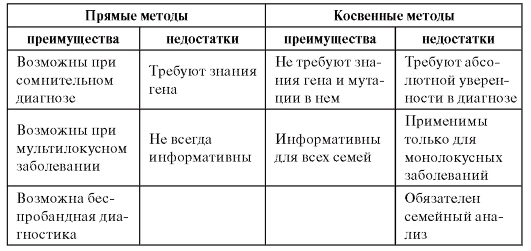
Вся методология молекулярно-генетической диагностики наследственных болезней представлена на рис. 9.21 в виде алгоритма.
Поскольку генодиагностика проводится в специализированных, хорошо оснащенных лабораториях и сопряжена с немалыми расходами, для проведения анализа должны быть строгие клинические показания. Лечащий врач и врач-генетик совместно составляют схему обследования больного. Такое взаимодействие, как правило, обеспечивает успех.
Автоматизация существующих методов и разработка принципиально новых подходов к изучению структуры нуклеиновых кислот
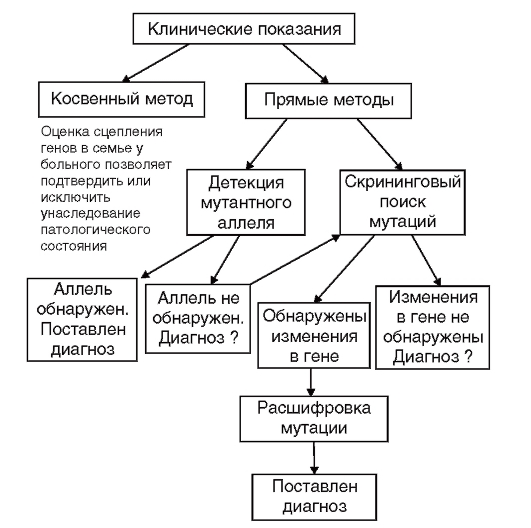
Рис. 9.21. Алгоритм генодиагностики наследственных заболеваний
наряду с ускоренными темпами изучения генома человека и клонирования генов, ответственных за развитие моногенной патологии, позволяют прогнозировать появление в недалеком будущем средств диагностики большинства известных наследственных болезней человека.
КЛЮЧЕВЫЕ СЛОВА И ПОНЯТИЯ
Асинхронность репликации ДНК Блот-гибридизация по Саузерну Высокоразрешающие цитогенетические методы Диагностика путем анализа полиморфизма по длине рестриктных фрагментов
Диагностика путем секвенирования гена Интерфазная цитогенетика
Лабораторная идентификация ступеней болезни Массовые просеивающие программы Материал для цитогенетических методов Методические условия цитогенетических исследований Олигонуклеотидные зонды Показания для биохимических исследований Показания для цитогенетических исследований Полимеразная цепная реакция
Принципы биохимической диагностики наследственных болезней
Просеивающий подход
Прямая детекция мутаций (варианты)
Селективные диагностические программы
Специфические зонды ДНК
Сущность молекулярно-генетической диагностики Метод флюоресцентной гибридизации in situ
РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА
Байдакова Г.В., Букина А.М., Гончаров В.М. и др. Диагностика наследственных болезней обмена веществ на основе сочетания методов тандемной масс-спектрометрии и энзимодиагностики // Медицинская генетика. - 2005. - Т. 4. - № 1. - С. 28-32.
Генетический паспорт - основа индивидуальной предиктивной медицины / под ред. В.С. Баранова. - СПб.: Изд-во Н-Л, 2009. - 527 с.
Захаров А.Ф., Бенюш В.А., Кулешов Н.П. Хромосомы человека: Атлас. - М.: Медицина, 1982. - 263 с.
Иллариошкин С.Н. ДНК-диагностика и медико-генетическое консультирование. - М.: МИА, 2002. - 591 с.
Клиническая биохимия / под ред. В.А. Ткачука. - М.: ГЭОТАР-
Медиа, 2008. - 264 с.
Коряков Д.Е., Жимулев И.Ф. Хромосомы. Структура и функции. -
Новосибирск: Изд-во СО РАН, 2009. - 258 c.
Краснопольская К.Д. Наследственные болезни обмена веществ. Справочное пособие для врачей. - М.: РОО Центр социальной адаптации и реабилитации детей «Фохат», 2005. - 364 с.: ил.
ПЦР в реальном времени / под ред. Д.В. Ребрикова. - 2-е изд., доп. и перераб. - М.: Бином. Лаборатория знаний, 2009. - 221 с.
Рубцов Н.Б. Методы работы с хромосомами млекопитающих: учебн. пос. - Новосибирск: Новосиб. гос. ун-т., 2006. - 152 с.
Свердлов Е.Д. Взгляд на жизнь через окно генома: Т. 1. Очерки структурной молекулярной генетики. - М.: Наука, 2009. - 525 с.