Биологическая химия с упражнениями и задачами : учебник / под ред. чл.-корр. РАМН С.Е. Северина. - 2011. - 624 с.: ил.
|
|
|
|
МОДУЛЬ 12 ОБЕЗВРЕЖИВАНИЕ ТОКСИЧЕСКИХ ВЕЩЕСТВ В ПЕЧЕНИ
Темы
12.1. Механизмы обезвреживания токсических веществ
12.2. Обезвреживание продуктов катаболизма аминокислот в кишечнике
12.3. Биотрансформация лекарств
12.4. Метаболизм и обезвреживание этанола
12.5. Химический канцерогенез
Цели изучения Уметь:
1. Объяснять молекулярные механизмы детоксикационной функции печени на примерах обезвреживания нормальных метаболитов и ксенобиотиков.
2. Объяснять молекулярные механизмы трансформации лекарственных веществ, явления привыкания к лекарствам, индивидуальную чувствительность к ним, прогнозировать последствия применения лекарственных препаратов.
3. Объяснять молекулярные механизмы токсического действия этанола и продуктов его метаболизма.
4. Объяснять молекулярные механизмы химического канцерогенеза.
Знать:
1. Основные функции печени.
2. Основные компоненты и этапы обезвреживания нормальных метаболитов и ксенобиотиков: связывание, транспорт и выведение.
3. Видовые, генетические, возрастные особенности системы обезвреживания.
4. Метаболизм этанола и его действие на организм.
5. Основы метаболизма лекарственных препаратов.
6. Основы химического канцерогенеза.
ТЕМА 12.1. МЕХАНИЗМЫ ОБЕЗВРЕЖИВАНИЯ ТОКСИЧЕСКИХ ВЕЩЕСТВ
Соединения, поступающие в организм с пищей, через кожу или легкие и не используемые организмом для энергетических и пластических целей, называются чужеродными веществами или ксенобиотиками. Они,
как правило, гидрофобны, токсичны и должны удаляться из организма. Для снижения их токсичности и повышения растворимости они подвергаются детоксикации, которая заключается в их химической модификации, и удаляются из организма (рис. 12.1). Обезвреживанию подвергаются также токсические вещества, образующиеся в организме: NH3, пептидные и стероидные гормоны, катехоламины, продукты катаболизма гема, продукты гниения аминокислот в кишечнике. Лекарственные вещества в редких случаях используются организмом в качестве субстратов, большая их часть, выполнив свою функцию, которая заключается во взаимодействии с белками или ферментами, должны быть удалены из организма. Они могут, в зависимости от их структуры, выводиться из организма как в неизмененном виде, так и в модифицированном.
Обезвреживание токсических веществ происходит путем химической модификации в две фазы:
• в реакциях первой фазы гидрофобное вещество модифицируется, причем чаще всего происходит его гидроксилирование;
• во вторую фазу происходит реакция конъюгации.
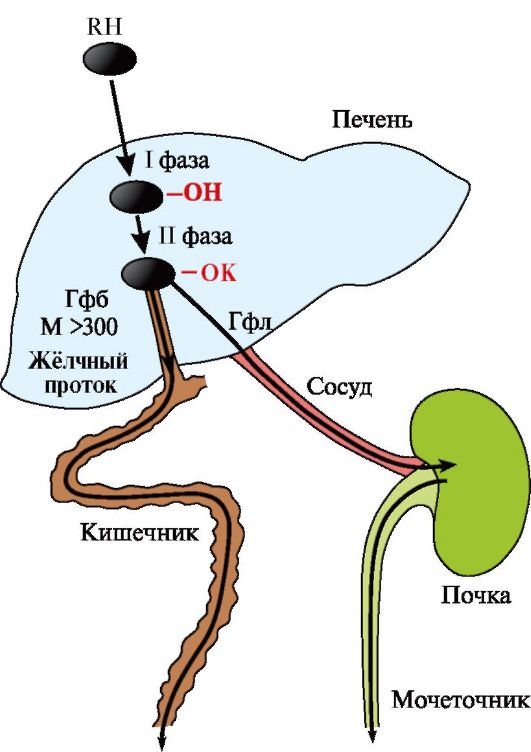 Рис. 12.1. Метаболизм и выведение ксенобиотиков из организма:
Рис. 12.1. Метаболизм и выведение ксенобиотиков из организма:
Ксб - ксенобиотик; К - радикал, используемый при конъюгации (глутатион, глюкуронил и др.); Гфб - гидрофобные и Гфл - гидрофильные метаболиты ксенобиотиков; М - молекулярная масса
Первая фаза обезвреживания
Эта фаза обязательна для гидрофобных веществ, так как они плохо выводятся из организма и могут накапливаться в тканях, богатых липидами (жировая клетчатка, мембраны клеток, нервная система). В этой фазе вещества подвергаются таким изменениям, как гидроксилирование, восстановление, сульфоокисление, дезаминирование, гидролиз и др.
В мембранах эндоплазматического ретикулума (ЭР) практически всех тканей локализована система микросомального (монооксигеназного) окисления (СМО), отвечающая за течение первой фазы обезвреживания. В эксперименте при выделении ЭР из клеток мембрана распадается на части, каждая из которых образует замкнутый пузырек - микросому. Микросомы сохраняют большинство морфологических и функциональных характеристик интактных мембран ЭР, в частности, они содержат активные ферменты, участвующие в реакциях обезвреживания. Эта система наиболее активна в печени. В клетках некоторых тканей (например, кора надпочечников) окислительная система локализована в мембранах митохондрий.
Основные ферменты, участвующие в работе окислительной системы: гемопротеин - цитохром Р450, цитохром Р450-редуктаза - флавопротеин (коферменты FAD и FMN) (рис. 12.2).
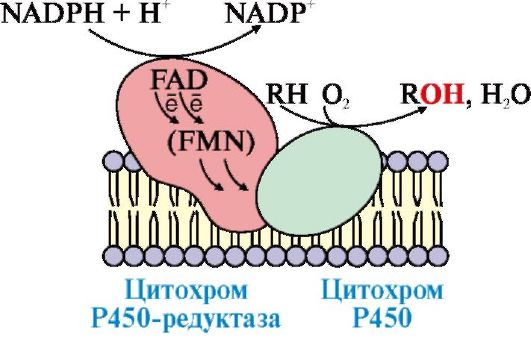 Рис. 12.2. Структурная организация монооксигеназной системы:
Рис. 12.2. Структурная организация монооксигеназной системы:
RH - субстрат цитохрома Р450; стрелками показаны реакции переноса электронов. Донором электронов является NADPH, который окисляется цитохром Р450-редуктазой
Цитохром Р450 может связывать в активном центре липофильное вещество RH и молекулу кислорода. Один атом кислорода принимает два электрона 2ё и переходит в форму О2-. Донором электронов и протонов является NADFН+Н+, который окисляет цитохром Р450-редуктазой; О2- взаимодействует с протонами и образуется вода: О2-+ 2Н+→ Н2О. Второй атом кислорода включается в гидроксильную группу вещества R-OH.
Суммарное уравнение реакции гидроксилирования вещества RH ферментами микросомального окисления
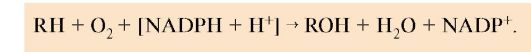 В
результате гидроксилирования повышается растворимость гидрофобного
соединения, что снижает его токсичность и облегчает дальнейшую
инактивацию и выведение из организма.
В
результате гидроксилирования повышается растворимость гидрофобного
соединения, что снижает его токсичность и облегчает дальнейшую
инактивацию и выведение из организма.
Цитохром Р450 обладает относительной субстратной специфичностью. Известно много изоформ Р450, каждая из них может взаимодействовать с разными, но сходными по строению ксенобиотиками. Субстратами Р450 могут быть как экзо-, так и эндогенные липофильные вещества, а продукты их превращений могут входить в пути нормального метаболизма. Цитохромы Р450 участвуют в биотрансформации многих лекарств, которые, будучи гидрофобными, не могут быть выведены из организма в неизменном виде.
Вторая фаза обезвреживания - коньюгация
Конъюгация - это присоединение к функциональным группам, образовавшимся в первой фазе или уже имеющимся у ксенобиотиков, других молекул или групп, увеличивающих гидрофильность и уменьшающих их токсичность.
Конъюгация может происходить с:
• глицином,
• глюкуронатом,
• сульфатом,
• ацетататом,
• метильной группой,
• глутатионом.
В этой фазе участвуют ферменты трансферазы, которые присоединяют различные конъюгаты к гидрофильным группам обезвреживаемых веществ. Полученный продукт, как правило, хорошо растворим и легко удаляется из организма с желчью и мочой.
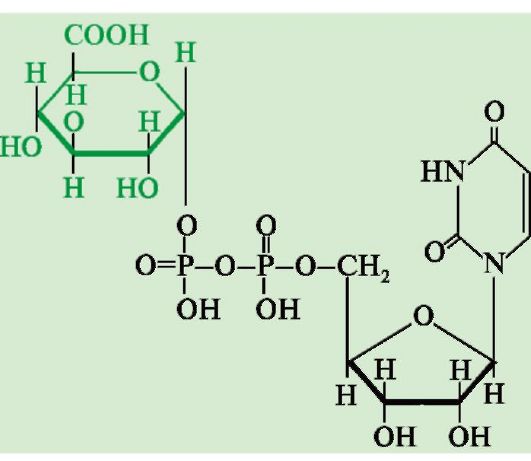
Например, УДФ-глюкуронилтрансферазы, локализованные в основном в ЭР, присоединяют к молекуле обезвреживаемого вещества остаток глюкуроновой кислоты (активная форма - УДФ-глюкуронат).

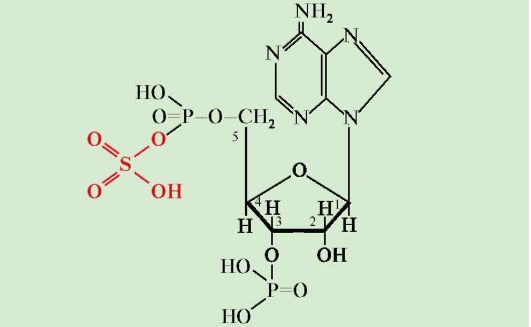
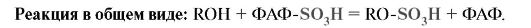 Особое место среди ферментов, участвующих в обезвреживании ксенобиотиков, нормальных метаболитов, лекарств, занимают глутатионтрансферазы (ГТазы).
Известно множество изоферментов ГТазы с различной субстратной
специфичностью. Для работы ферментов требуется глутатион (ГSH).
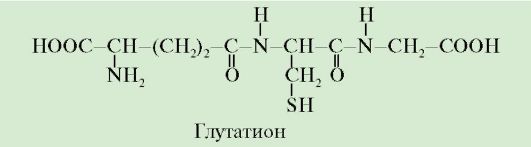
Глутатион - это трипептид глу-цис-гли, остаток глутаминовой кислоты
присоединен к цистеину карбоксильной группой радикала.
Особое место среди ферментов, участвующих в обезвреживании ксенобиотиков, нормальных метаболитов, лекарств, занимают глутатионтрансферазы (ГТазы).
Известно множество изоферментов ГТазы с различной субстратной
специфичностью. Для работы ферментов требуется глутатион (ГSH).
Глутатион - это трипептид глу-цис-гли, остаток глутаминовой кислоты
присоединен к цистеину карбоксильной группой радикала.
 ГТазы
- универсальные ферменты, функционирующие у всех животных и человека, и
имеющиеся во всех тканях. ГТазы играют важную роль в обезвреживании
собственных метаболитов: некоторых стероидных гормонов, простагландинов,
билирубина, желчных кислот, продуктов перекисного окисления липидов.
ГТазы
- универсальные ферменты, функционирующие у всех животных и человека, и
имеющиеся во всех тканях. ГТазы играют важную роль в обезвреживании
собственных метаболитов: некоторых стероидных гормонов, простагландинов,
билирубина, желчных кислот, продуктов перекисного окисления липидов.
Обезвреживание ксенобиотиков с участием ГТазы происходит тремя путями:
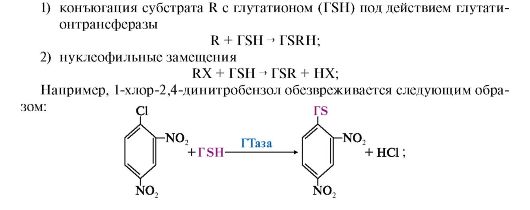 3) восстановление органических пероксидов до спиртов под действием глутатионпероксидазы:
3) восстановление органических пероксидов до спиртов под действием глутатионпероксидазы:
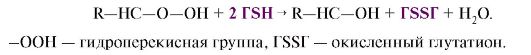 Обезвреживание
ксенобиотиков с участием цитохрома Р450 иногда приводит к образованию
метаболитов не менее, а более токсичных, чем исходные. Эти токсические
вещества обезвреживаются глутатионтрансферазой (ГТазой).
Обезвреживание
ксенобиотиков с участием цитохрома Р450 иногда приводит к образованию
метаболитов не менее, а более токсичных, чем исходные. Эти токсические
вещества обезвреживаются глутатионтрансферазой (ГТазой).
ГТаза - индуцируемый фермент, его синтез индуцируется при приеме этанола, снотворных препаратов - производных барбитуровой кислоты и т.д.
ТЕМА 12.2. ОБЕЗВРЕЖИВАНИЕ ПРОДУКТОВ КАТАБОЛИЗМА АМИНОКИСЛОТ В КИШЕЧНИКЕ
Аминокислоты, не всосавшиеся в клетки кишечника, используются микрофлорой толстой кишки. Ферменты микроорганизмов расщепляют аминокислоты и превращают их в амины, фенолы, индол, скатол, сероводород и другие, токсичные для организма соединения. Этот процесс называют гниением белков в кишечнике. В основе его лежат реакции декарбоксилирования и дезаминирования аминокислот. Продукты гниения частично всасываются в нижних отделах тонкой кишки и с током крови поступают в печень и другие ткани, где могут оказывать токсическое действие.
1. Образование и обезвреживание и-крезола и фенола. Под действием ферментов бактерий из аминокислоты тирозина могут образовываться фенол или крезол путем отщепления боковых цепей (рис. 12.3).
Часть этих соединений попадает в кровоток и по воротной вене поступает в печень, где подвергаются конъюгации двух видов:
• с сульфатом в составе (ФАФС),
• с глюкуроновой кислотой в составе УДФ-глюкуроната.
Реакции конъюгации фенола и крезола с ФАФС катализирует фермент сульфотрансфераза (рис. 12.4).
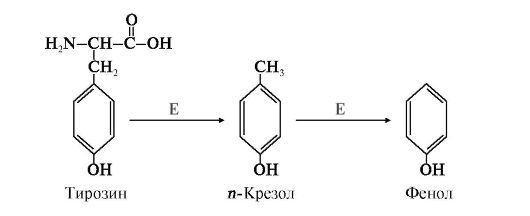 Рис. 12.3. Катаболизм тирозина под действием бактерий:
Рис. 12.3. Катаболизм тирозина под действием бактерий:
Е - бактериальные ферменты
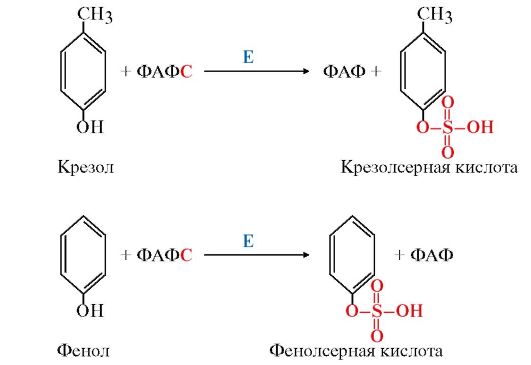 Рис. 12.4. Конъюгация фенола и крезола с ФАФС:
Рис. 12.4. Конъюгация фенола и крезола с ФАФС:
Е - сульфотрансфераза
Конъюгация фенола и крезола с глюкуроновой кислотой происходит при участии фермента УДФ-глюкуронилтрансферазы. Продукты конъюгации - фенолглюкуронат и крезолглюкуронат хорошо растворимы в воде и выводятся с мочой. Повышение количества конъюгатов глюкуроновой кислоты с фенолом и крезолом в моче обнаруживается при усилении гниения белков в кишечнике.
2. Образование и обезвреживание индола и скатола. В кишечнике из аминокислоты триптофан микроорганизмы образуют индол и скатол. Бактерии отщепляют карбоксильную и α-амино-группу триптофана, оставляя нетронутым гетероциклический радикал. Индол образуется в результате отщепления бактериями боковой цепи с образованием серина или аланина
(рис. 12.5).
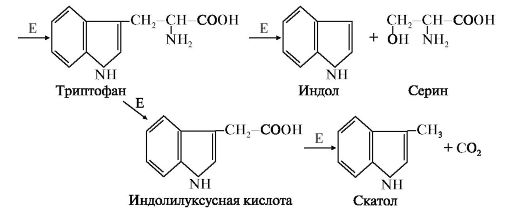 Рис. 12.5. Катаболизм триптофана под действием бактерий:
Рис. 12.5. Катаболизм триптофана под действием бактерий:
Е - бактериальные ферменты
Скатол и индол обладают гидрофобными свойствами и обезвреживаются в печени в два этапа:
- сначала в результате микросомального окисления они приобретают гидроксильную группу, индол превращается в индоксил;
- затем индоксил вступает в реакцию конъюгации с ФАФС, образуя индоксилсерную кислоту, калиевая соль которой получила название животного индикана. Анализ последнего в моче использовали для оценки детоксикационной функции печени (рис. 12.6).
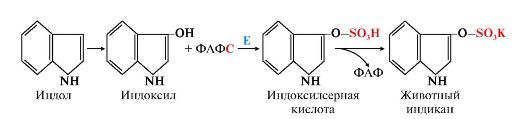 Рис. 12.6. Участие сульфотрансферазы в обезвреживании индола:
Рис. 12.6. Участие сульфотрансферазы в обезвреживании индола:
Е - сульфотрансфераза
ТЕМА 12.3. БИОТРАНСФОРМАЦИЯ ЛЕКАРСТВ
Действие на организм большинства лекарств должно быть строго дозировано и прекращается через определенное время после их приема. Прекращение действия может быть результатом выведения лекарства из организма в неизменном виде (что характерно для гидрофильных соединений) или лекарственные препараты подвергаются химической модификации (биотрансформации) и в виде продуктов экскретируются из организма.
Результатом биотрансформации лекарственных веществ являются:
1) инактивация лекарственных веществ, т.е. снижение их фармакологической активности_(фенобарбитал, нитриты, эфедрин и др.);
2) повышение активности лекарственных веществ (бутадион, метилдофа, норморфин, ловастатин и др.);
3) появление метаболитов, оказывающих токсическое действие на организм (фенацетин, сульфаниламиды).
Инактивация лекарственных веществ часто происходит в два этапа.
Первый этап - химическая модификация под действием ферментов монооксигеназной системы эндоплазматического ретикулума (микросомального окисления) (рис. 12.7).
Второй этап - конъюгация (связывание) лекарственных веществ (как подвергшихся каким-либо превращениям на первом этапе, так и нативных препаратов).
Конъюгация может происходить с глицином, ацетатом, глюкуронатом, сульфатом, глутатионом и др.
Глицин может присоединяться по карбоксильной группе, глюкуроновая кислота по ОН-группе, а ацетильный остаток ацетил-КоА по NН2-группе.
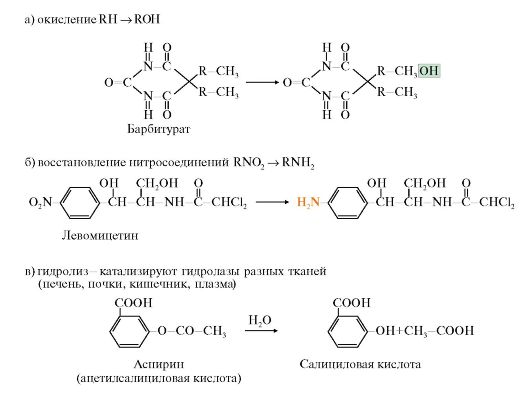 Рис. 12.7. Варианты химических модификаций:
Рис. 12.7. Варианты химических модификаций:
а - окисление RH ROH; б - восстановление нитросоединений RNO2 RNH2; в - гидролиз
Реакции конъюгации катализируют соответствующие ферменты класса трансфераз (рис. 12.8).
Дозы некоторых лекарств при систематическом приеме необходимо увеличивать, так как их действие на организм ослабляется. Это происходит потому, что эти лекарства, как и другие чужеродные соединения, индуцируют синтез ферментов монооксигенезной системы и реакций конъюгации.
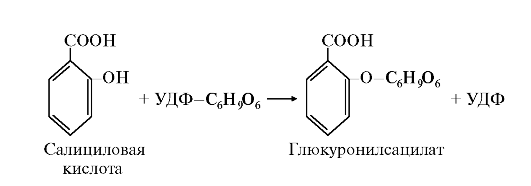 Рис. 12.8. Конъюгация УДФГК с салициловой кислотой
Рис. 12.8. Конъюгация УДФГК с салициловой кислотой
Это обстоятельство лежит в основе привыкания к лекарственным препаратам и некоторым ядам. Кроме того, особое значение имеет широкая субстратная специфичность ферментов системы обезвреживания. В настоящее время известно несколько тысяч соединений, которые могут модифицироваться в организме при участии этой системы.
ТЕМА 12.4. МЕТАБОЛИЗМ И ОБЕЗВРЕЖИВАНИЕ
ЭТАНОЛА
Этанол может синтезироваться в организме человека или поступает с пищей. Эндогенный этиловый спирт содержится в крови в концентрации 0,0004 до 0,001 г/л. Источниками этанола являются:
• превращение глюкозы: Глюкоза Пируват →Ацетальдегид →Этанол;
• спиртовое брожение углеводов микрофлорой кишечника и дыхательных путей.
Источником экзогенного этанола для человека служат спиртные напитки и даже некоторые пищевые продукты (соки, кефир, хлеб). Экзогенный этанол быстро всасывается в желудке (20-30%) и в тонком кишечнике (70-80%), достигая через 30-60 минут максимальной концентрации в крови. Метаболизм (окисление) этанола начинается уже в слизистой оболочке рта и продолжается во многих органах, но главным образом в печени (до 70-95% окисляемого этанола).
Возможные реакции окисления этанола и ацетальдегида представлены ниже. При малых и умеренных дозах этанол окисляется с участием NAD-зави- симых ферментов (рис. 12.9).
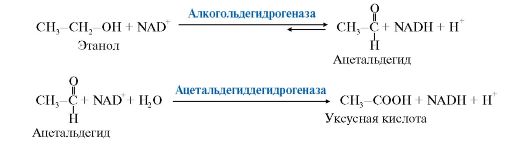 Рис. 12.9. Окисление этанола с участием NAD-зависимых дегидрогеназ
Рис. 12.9. Окисление этанола с участием NAD-зависимых дегидрогеназ
Уксусная кислота превращается в ацетил-КоА, который является конечным продуктом метаболизма этанола. Ацетил-КоА окисляется в цитратном цикле до СО2, а при его избытке у больных, страдающих хроническим алкоголизмом, используется в печени для синтеза жирных кислот, жира и холестерина. Около 10% экзогенного этанола выводится в неизменном виде с выдыхаемым воздухом, мочой, потом.
Биологические эффекты этанола неспецифичны и многогранны: физико-химические, мембранотропные, метаболические, наркотические, токсические и канцерогенные. Этанол как амфифильное вещество усиливает
проницаемость гематоэнцефалического барьера для других веществ, проникает в мозг, нарушает структуру и функции мембран и вызывает изменение метаболизма практически во всех органах. Однако еще более выраженное токсическое действие оказывает продукт метаболизма этанола - ацетальдегид.
Ацетальдегид способен взаимодействовать с функциональными группами (NH2, SH, ОН) белков, ферментов, рецепторов, глутатиона, нарушая их функции, что может вызывать рак полости рта, глотки и мочевых путей. Ацетальдегид ингибирует NADH-дегидрогеназу и снижает способность гемоглобина переносить кислород, что приводит к нарушению энергетического обмена и синтеза АТФ. При хроническом алкоголизме ацетальдегид вступает в реакции с дофамином и серотонином, образуя алкогольные опиоиды, реагирующие с опиатными рецепторами и являющиеся факторами развития алкогольной эйфории и влечения к алкоголю. Один из таких опиоидов выделяется с мочой и служит клинико-биохимическим маркером систематического употребления алкоголя.
При употреблении больших количеств этанола (для барбитуратов есть свой Р450) индуцируется особая микросомальная этанолокисляющая система (МЭОС), в которой главную роль играет цитохром Р450 II Е1 - один из изоферментов цитохрома Р450. В этой ситуации окисление этанола происходит следующим образом:
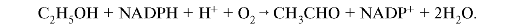 Ацетальдегид далее окисляется ацетальдегиддегидрогеназой (кофермент FAD).
Ацетальдегид далее окисляется ацетальдегиддегидрогеназой (кофермент FAD).
Кроме того, цитохром P450 II E1 катализирует образование активных (токсических) форм кислорода, которые стимулируют перекисное окисление липидов и вызывают повреждения мембран многих органов.
Цитохром Р450 II E, как и другие цитохромы Р450, не обладает абсолютной специфичностью и может с меньшей скоростью катализировать реакции с другими веществами, в том числе лекарствами, вызывая их биотрансформацию. У лиц, страдающих алкоголизмом, этанол увеличивает активность «своего» цитохрома P450 по отношению к этанолу путем индукции. И поэтому из-за относительной специфичности этого фермента биотрансформация лекарственных веществ протекает также более активно и эффективность действия принимаемых препаратов снижается. В результате окисления этанола и ацетальдегида алкогольдегидрогеназой и ацетальдегиддегидрогеназой, повышается содержание NADH который вызывает разнообразные метаболические эффекты: лактоацидоз, угнетение глюконеогенеза, гипогликемию, снижение активности ферментов цитратного цикла и нарушение энергетического обмена.
Последствием воздействия этанола и ацетальдегида являются нарушения обмена белков, липидов, углеводов, биогенных аминов, нейропептидов, а также заболевания внутренних органов (висцеральный алкоголизм) и поражение нервной системы с формированием алкогольной зависимости и алкогольной толерантности к этанолу.
ТЕМА 12.5. ХИМИЧЕСКИЙ КАНЦЕРОГЕНЕЗ
1. В основе химического канцерогенеза лежат повреждения ДНК под действием химических канцерогенов. Полициклические ароматические углеводороды, ароматические амины (например, 2-нафтиламин), нитрозамины, которые содержатся в каменноугольной смоле, табачном дыме, в загрязненном воздухе больших городов и в пищевых продуктах, подвергнутых обжариванию на углях или копчению, не являются канцерогенами, но превращаются в них, подвергаясь «обезвреживанию» в печени ферментами монооксигеназной системы. Наиболее часто встречающиеся проканцерогены приведены в табл. 12.1.
Таблица 12.1. Некоторые химические канцерогены
Класс соединений | Представители | Источники |
Полициклические ароматические углеводороды | Бензантрацен, метилхолантрен, диметилбензантрацен | Выхлопные газы, продукты горения, сигаретный дым, коксохимическое производство |
Ароматические амины | Метиламинобензол нафтиламин | Производство красителей |
Диоксины | Тетрахлорбензодиоксин | Производство дефолиантов и ростовых веществ, целлюлозобумажная промышленность, хлорирование воды, горящие свалки |
Микотоксины | Афлатоксин В1 | Плесневые грибы |
Нитрозамины | Диметилнитрозоамин, диэтилнитрозоамин | Образуются при употреблении нитратсодержащих продуктов |
Известны сотни генов (протоонкогены), мутации в которых могут способствовать превращению нормальной клетки в опухолевую. Протоонкоген - ген, содержащий информацию о белке, регулирующем нормальную пролиферацию клеток, и способный в результате изменения структуры превращаться в онкоген. Онкоген - ген, экспрессия которого приводит к неконтролируемой пролиферации клеток. Для превращения протоонгкогена в онкоген требуются определенные изменения в его регуляторной или структурной части.
Канцерогенами могут быть как органические, так и неорганические молекулы, т.е. канцерогенность не связана с какой-либо определенной структурной особенностью.
Например, полициклический углеводород бензантрацен в организме подвергается гидроксилированию, в качестве промежуточного продукта образуется эпоксид, который является канцерогеном.
Ковалентная модификация гуанина в ДНК под действием нитрозаминов (образование N7-метилгуанина или Об-метилгуанина) приводит к разрыву водородной связи между G-C в цепях ДНК и последующему изменению первичной структуры ДНК и нарушению взаимодействия ДНК с белками.
Канцерогеном неорганической природы могут быть нитраты в высоких концентрациях. Эти соединения широко распространены в воде и почве, попадая туда из различных источников, в том числе в составе удобрений. В организм человека поступают с пищей (молоко, консервы, фрукты, овощи) и в виде лекарств. Нитраты и особенно нитриты являются сильными окислителями. В процессе метаболизма азот нитратов присоединяет в ходе последовательных реакций восьми электронов. Промежуточные продукты этих реакций могут участвовать в реакциях окисления
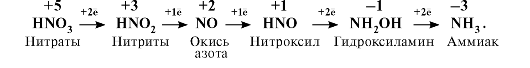 Окисляемыми
субстратами могут быть все железосодержащие гемопротеины: Hb, цитохромы
ЦПЭ, цитохромы монооксигеназной системы эндоплазматического ретикулума.
Окисляемыми
субстратами могут быть все железосодержащие гемопротеины: Hb, цитохромы
ЦПЭ, цитохромы монооксигеназной системы эндоплазматического ретикулума.
В организме из азотистой кислоты (HNO2) и вторичных аминов структуры R2NH образуются нитрозамины R2N-N=O, которые являются достаточно сильными мутагенами, вызывая алкилирование (например, метилирование) азотистых оснований ДНК. Нитриты превращают также остаток цитозина в цепи ДНК в урацил, и пара GC превращается в UC.
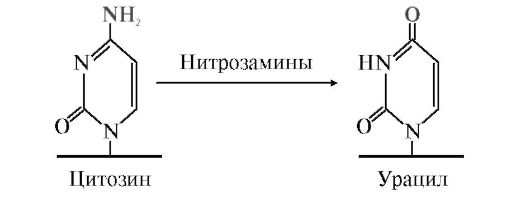 В
ходе репликации мутантной ДНК U образует комплементарную пару UA,
которая в ходе следующей репликации преобразуется в пару АТ. Если
мутация произошла в протоонкогене белка, ответственного за регуляцию
клеточного цикла, то это может привести к нарушению его структуры,
неконтролируемому делению клеток и развитию опухоли.
В
ходе репликации мутантной ДНК U образует комплементарную пару UA,
которая в ходе следующей репликации преобразуется в пару АТ. Если
мутация произошла в протоонкогене белка, ответственного за регуляцию
клеточного цикла, то это может привести к нарушению его структуры,
неконтролируемому делению клеток и развитию опухоли.
Нитраты и промежуточные продукты их превращений снижают активность некоторых ферментов антиоксидантной защиты, что приводит к накоплению активных форм кислорода и активации перекисного окисления липидов.
Ароматические амины. Ароматические амины - это вещества, которые используются в производстве анилиновых красителей и резиновой промышленности, одно из этих веществ - 2-нафтиламин - в печени в ходе первой фазы обезвреживания превращается в канцероген - 2-амино-1-нафтол. Однако в печени он быстро конъюгирует с ФАФС и превращается в нейтральный продукт. При выведении с мочой часть конъюгатов гидролизуется, в результате чего снова образуется канцероген, который может со временем вызвать развитие рака мочевого пузыря (рис. 12.10).
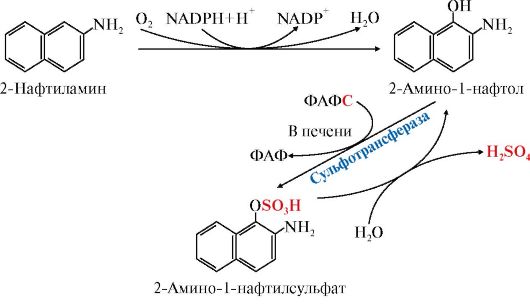 Рис. 12.10. Метаболизм 2-нафтиламина
Рис. 12.10. Метаболизм 2-нафтиламина
Афлатоксины - это метаболиты некоторых видов плесневых грибов, например Aspergillus flavus, которые развиваются при неправильном хранении зерновых продуктов, круп и орехов. Афлатоксин В1 в результате химической модификации превращается в печени в эпоксид, который является концерогеном и вызывает развитие рака печени (рис. 12.11).
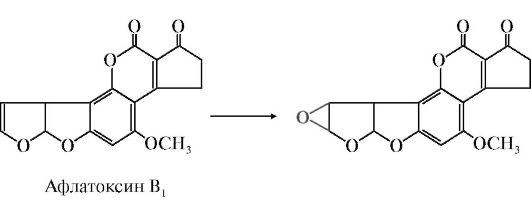 Рис. 12.11. Окисление афлатоксина В
Рис. 12.11. Окисление афлатоксина В
ЗАДАНИЯ ДЛЯ ВНЕАУДИТОРНОЙ РАБОТЫ
1. На химическом предприятии произошло испарение небольших количеств бензола, который вместе с вдыхаемым воздухом попал в организм нескольких рабочих. Опишите механизмы, с помощью которых организм будет избавляться от токсических веществ. Для этого:
а) укажите фазы обезвреживания токсических веществ;
б) напишите реакции обезвреживания бензола, назовите ферменты и коферменты.
2. Табл. 12.2. перенесите в тетрадь, запомните название ферментов, напишите названия активных форм и формулы метаболитов, используемых для конъюгации.
Таблица 12.2. Основные виды конъюгации
Фермент | Метаболит, используемый для конъюгации | Активная форма |
Глутатионтрансферазы | ||
УДФ-глюкуронилтрансферазы | ||
Сульфотрансферазы | ||
Ацетилтрансферазы | ||
Метилтрансферазы |
3. Напишите и выучите формулу глюкуроновой кислоты, укажите веществопредшественник.
4. В процессе гниения белков, происходящего под влиянием микрофлоры толстого кишечника, образуются ядовитые продукты, например индол:
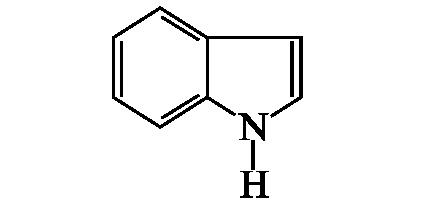 а) назовите, из какой аминокислоты образуется индол;
а) назовите, из какой аминокислоты образуется индол;
б) напишите формулами реакции обезвреживания этого соединения;
в) укажите другое известное вам токсическое соединение, которое образуется из этой же аминокислоты под действием кишечных бактерий;
г) напишите реакции обезвреживания этого вещества.
5. Напишите реакции инактивации фенобарбитала, назовите ферменты.
6. Первый этап инактивации аспирина завершается образованием салициловой и уксусной кислот. Напишите реакции второго этапа обезвреживания (конъюгации), назовите фермент.
7. Составьте перечень продуктов метаболизма этанола, которые вызывают метаболические, токсические, наркотические и канцерогенные эффекты и приводят к поражениям внутренних органов и нервной системы.
ЗАДАНИЯ ДЛЯ САМОКОНТРОЛЯ
1. Выберите правильные ответы.
В печени происходит обезвреживание:
A. NH3
Б. Крезола
B. Ксенобиотиков Г. Индола
Д. Адреналина
2. Выберите правильные ответы.
В функционировании микросомальной системы окисления принимают участие:
A. Цитохром Р450-редуктаза
Б. О2
B. Цитохром Р450 Г. NADPH
Д. СО2
3. Выберите один наиболее полный ответ. В печени происходят реакции:
A. Конъюгации с участием УДФ-глюкуроната Б. Гидроксилирования ксенобиотиков
B. Конъюгации с ФАФС
Г. Обезвреживания токсических веществ Д. Конъюгации с глутатионом
4. Выберите правильные ответы. Во второй фазе обезвреживания:
A. Участвуют глюкуронилтрансферазы
Б. Используется 5-фосфоаденозин-5'-фосфосульфат
B. Образуются растворимые конъюгаты Г. Участвуют ацетилтрансферазы
Д. Могут образовываться канцерогены
5. Выберите правильный ответ. Глутатионтрансферазы:
A. Функционируют в составе монооксигеназной системы
Б. Связывают липофильные вещества и предотвращают их внедрение в липидный бислой мембран
B. Восстанавливают глутатион с участием кофермента NADHP Г. Локализованы во всех тканях
Д. Локализованы в мембранном слое эндоплазматического ретикулума
6. Выберите правильные ответы. Субстратами цитохрома Р450 могут быть:
A. Эндогенные гидрофильные вещества Б. Гидрофобные ксенобиотики
B. Экзогенные гидрофобные вещества Г. Лекарства
Д. Эндогенные гидрофобные вещества
7. Выберите правильные ответы. Изоформы цитохрома Р450 различаются по:
A. Первичной структуре
Б. Субстратной специфичности
B. Локализации
Г. Строению небелковой части Д. Строению активного центра
8. Выберите правильный ответ. Сульфотрансферазы:
A. В качестве субстрата используют SAM
Б. Катализируют перенос метильной группы
B. Обладают абсолютной специфичностью
Г. Входят в состав микросомальной системы окисления Д. Катализируют реакции с участием 3'-фосфоаденозин-5'-фосфо- сульфата
9. Выберите правильные ответы. Глутатион (ГSH):
A. Трипептид Цис-Цис-Гли Б. Содержит остаток цистеина
B. Участвует в реакциях, катализируемых глутатионтрансферазой Г. В окисленной форме имеет дисульфидный мостик
Д. Окисляется ферментом глутатионпероксидазой
10. Выберите правил ьн ый от вет. Источником афлатоксина являются:
A. Выхлопные газы
Б. Анилиновые красители
B. Нитратсодержащие продукты Г. Плесневые грибы
Д. Табачный дым
11. Установите правильную последовательность событий. При обезвреживании 2-нафтиламина происходит:
A. Реакции микросомального окисления 2-нафтиламина
Б. Синтез конъюгатов 2-амино-1-нафтола с серной кислотой
B. Гидролиз части конъюгатов в мочевом пузыре бактериальными ферментами
Г. Поступление в организм человека проканцерогена 2-нафтиламина Д. Взаимодействие 2-амино-1-нафтола с ДНК клеток и их опухолевое перерождение
ЭТАЛОНЫ ОТВЕТОВ К «ЗАДАНИЯМ ДЛЯ САМОКОНТРОЛЯ»
1. А, Б, В, Г
2. А, Б, В, Г
3. Г
4. А, Б, В, Г
5. Д
6. Б, В, Г, Д
7. А, Б, Д
8. Д
9. Б, В, Г, Д
10. Г
11. Г→А→Б→В→Д
ОСНОВНЫЕ ТЕРМИНЫ И ПОНЯТИЯ
1. Ксенобиотики
2. Микросомальная система окисления и процессы конъюгации
3. Цитохром Р450
4. Продукты гниения в кишечнике
5. Токсические эффекты этанола
6. Биотрансформация лекарств
7. Химический канцерогенез
ЗАДАНИЯ ДЛЯ АУДИТОРНОЙ РАБОТЫ
Решите задачи
1. У пациентов, длительно употребляющих алкоголь, наблюдается снижение эффективности действия лекарств, а также наркотических средств при хирургическом вмешательстве. Почему изменяется скорость биотрансформации лекарственных веществ у этих людей? Для ответа:
а) напишите реакции катаболизма этанола в печени;
б) объясните, как влияет этанол на активность микросомального окисления в печени.
2. В загрязненном воздухе городов, каменноугольной смоле и табачном дыме содержатся полициклические углеводороды, которые могут провоцировать возникновение онкологических заболеваний. Укажите, какой конечный метаболит образуется в организме из полициклических углеводородов при участии микросомальной системы окисления? Объясните механизм его канцерогенного действия. Для этого:
а) напишите схему катаболизма полициклических углеводородов;
б) назовите компонент клетки, на который оказывает действие продукт этого процесса.
3. Царь Митридат (Крымское царство) систематически принимал небольшие дозы растительных ядов, чтобы избежать острого отравления. На чем основан «эффект Митридата»? Для ответа:
а) назовите этапы обезвреживания веществ в печени;
б) напишите схему обезвреживания токсических веществ (в общем виде), укажите ферменты, коферменты;
в) объясните, почему систематический прием небольших доз растительных ядов позволяет избежать острого отравления.
4. Водно-нитратная метгемоглобинемия - заболевание, которое развивается при употреблении воды, содержащей большое количество нитратов. У грудных детей возможен летальный исход при выраженных явлениях тканевой гипоксии (синюшность губ и кожных покровов, одышка).
Нарушение каких биохимических процессов лежит в основе развития метгемоглобинемии?
Для ответа на вопрос:
а) напишите схему метаболизма нитратов в организме человека;
б) укажите, на структуру каких соединений в организме ребенка влияют продукты метаболизма нитратов;
в) объясните, почему у детей наблюдается гипоксия.
5. При неправильном хранении круп, зерна и орехов в них развиваются плесени рода Aspergillus flavus, продуктом жизнедеятельности которых является афлатоксин В1, вызывающий развитие первичного рака печени:
а) назовите канцерогенный метаболит, образующийся в печени из афлатоксина В1;
б) объясните биохимические основы канцерогенного эффекта афлатоксина В1.
6. В течение многих лет в качестве жаропонижающего и болеутоляющего средства использовали фенацетин. В организме человека он метаболизируется следующим образом:
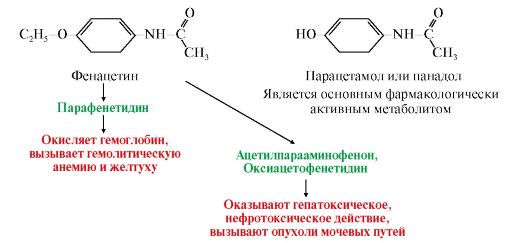 При
длительном использовании фенацетин вызывает указанные побочные эффекты и
даже онкологические заболевания, поэтому его производство прекращено.
Парацетамол менее токсичен и в терапевтических дозах редко вызывает
осложнения. Он быстрее метаболизируется в печени и выводится с мочой:
При
длительном использовании фенацетин вызывает указанные побочные эффекты и
даже онкологические заболевания, поэтому его производство прекращено.
Парацетамол менее токсичен и в терапевтических дозах редко вызывает
осложнения. Он быстрее метаболизируется в печени и выводится с мочой:
а) рассмотрите формулы лекарств и объясните, почему парацетамол менее токсичен и быстрее выводится из организма. Напишите реакцию обезвреживания парацетамола;
б) назовите продукт окисления гемоглобина, образующийся при длительном лечении фенацетином или при отравлении большими дозами парацетамола.
7. При длительном лечении туберкулеза изониазидом этот лекарственный препарат вызывает побочные эффекты и осложнения (например, невриты, поражения зрительного нерва), связанные со следующими реакциями:
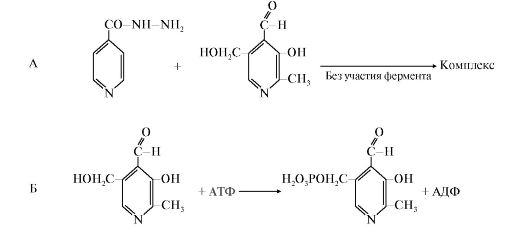 Объясните возникновение этих осложнений. Для этого:
Объясните возникновение этих осложнений. Для этого:
а) назовите соединения, формулы которых представлены в уравнениях; укажите биологическое значение этих соединений;
б) назовите фермент, катализирующий вторую реакцию и его класс;
в) укажите, какие нарушения биохимических процессов могут возникать в организме пациентов в результате указанных реакций с изониазидом;
г) назовите, какой витамин необходимо назначать пациентам при длительном лечении изониазидом.