Патологическая анатомия : учебник / А. И. Струков, В. В. Серов. - 5-е изд., стер. - М.: Литтерра, 2010. - 848 с. : ил.
|
|
|
|
ИНФЕКЦИОННЫЕ БОЛЕЗНИ
Инфекционными называют болезни, вызываемые инфекционными агентами - вирусами, бактериями, грибами. При внедрении в организм простейших и глистов говорят об инвазионных заболеваниях.
Некоторые инфекционные заболевания в настоящее время ликвидированы, однако многие, особенно вирусные, представляют еще значительную угрозу населению. Кроме того, сохранились еще эндемические очаги ряда инфекционных болезней, которые при скорости, присущей современным средствам передвижения, могут легко переноситься в другие страны.
Инфекционный процесс очень сложный, и его развитие определяют как особенности возбудителя, так и реактивное состояние макроорганизма. Особенности микроорганизма - возбудителя инфекционного заболевания - определяются не только его строением, химической структурой, антигенными свойствами, но и характером взаимодействия с организмом хозяина. Результат этого взаимодействия в значительной мере зависит от состояния систем защиты организма - фагоцитарной (нейтрофилы и моноцитарные фагоциты) и иммунной, особенно системы гуморального иммунитета.
Сосуществование микро- и макроорганизма может быть 3 видов: 1) симбиоз - сосуществование микроба и макроорганизма в интересах каждого (например, кишечная палочка в кишечнике); 2) комменсализм (от франц. commensal - сотрапезник), при котором микроб и макроорганизм не оказывают взаимного влияния друг на друга; 3) паразитизм - жизнь микроба за счет макроорганизма, что ведет к развитию болезни. Под влиянием различных экзогенных и эндогенных факторов взаимоотношения между микро- и макроорганизмом могут быть нарушены в пользу микроорганизма, который приобретает патогенные свойства. В этих условиях индифферентный комменсал, или безвредный симбионт, становится паразитом и вызывает заболевание. Такие ситуации возникают при лечении многими препаратами, но прежде всего антибиотиками, которые нарушают установившееся равновесие микробной флоры. Инфекционная болезнь может быть и результатом ослабления фагоцитарной и иммунной систем организма, что встречается, например, при лечении иммунодепрессантами и цитостатическими средствами.
Большинство возбудителей болезней попадает в организм человека из внешней среды через входные ворота, например через кишечник, с пищей, через легкие с вдыхаемым воздухом, при укусах насекомых, через поврежденную кожу или слизистые оболочки и т.д. В таких случаях говорят об экзогенной инфекции.
Однако заражение может быть эндогенным, тогда речь идет об эндогенной инфекции, или аутоинфекции.
Различные инфекционные агенты вызывают разные тканевые реакции, что особенно демонстративно при бактериальных и вирусных инфекциях. Бактерии, проникнув в ткани, вызывают обычно воспаление. Вирусы, подчиняя клетки хозяина механизму своего размножения (репродукции), могут вести к дистрофии и некрозу клеток, а также к их пролиферации и трансформации; воспалительная реакция в значительной мере вторична.
При инфекционном процессе независимо от характера возбудителя появляются иммунные реакции, направленные на разрушение и элиминацию инфекта. Циркулирующие в крови антитела образуются в ответ на антигенную стимуляцию иммунной системы. Соединения антигена с антителом в присутствии комплемента производят антимикробное и антитоксическое действие, обеспечивающее послеинфекционный гуморальный иммунитет. В то же время длительное антигенное воздействие при инфекционном заболевании ведет к сенсибилизации организма, появлению реакций гиперчувствительности как немедленного, так и замедленного (аллергические реакции) типа. Из этого следует, что тканевые повреждения при инфекционных заболеваниях могут развиваться не только под воздействием инфекта, но и в связи с реакциями гиперчувствительности.
Клинико-морфологическая характеристика. Для инфекционных заболеваний характерен ряд общих признаков:
1. Каждое инфекционное заболевание имеет своего возбудителя, который выявляется в крови или экскретах больного.
2. Возбудитель инфекционной болезни имеет входные ворота, характерные для каждой инфекции.
3. При инфекционной болезни наблюдается образование первичного аффекта (очага), который обычно появляется во входных воротах. Первичный аффект представляет собой очаг воспаления. При лимфогенном распространении инфекции возникает воспаление как отводящих лимфатических сосудов (лимфангит), так и регионарных лимфатических узлов (лимфаденит). Сочетание первичного аффекта, лимфангита и лимфаденита при инфекционном заболевании позволяет говорить о первичном инфекционном комплексе. При одних инфекциях он выражен (туберкулез, сифилис, туляремия), при других - фактически не возникает, процесс сразу принимает генерализованный характер (сыпной и возвратный тифы, малярия).
4. Путь распространения инфекции из первичного очага или комплекса может быть лимфогенным, гематогенным, интраканаликулярным, периневральным или контактным.
5. Каждая инфекционная болезнь характеризуется местными изменениями, которые развиваются в определенной ткани или органе (в толстой кишке при дизентерии, в клетках передних рогов спинного мозга при полиомиелите, в стенках мелких сосудов при сыпном тифе) и в той или иной степени типичны для данной болезни.
6. При инфекционных болезнях развивается ряд общих изменений: кожные высыпания, васкулиты, гиперпластические процессы в лимфатических узлах, селезенке, костном мозге, воспалительные процессы в межуточной ткани и дистрофические изменения в паренхиматозных органах.
Инфекционная болезнь чаще протекает циклически. В ее течении выделяют инкубационный, продромальный периоды и период основных проявлений болезни (фазы нарастания симптомов болезни, разгара и ее угасания). Инфекционное заболевание может закончиться выздоровлением, принять хроническое течение, быть причиной бациллоносительства. Очень часто она сопровождается различными осложнениями, которые могут стать причиной смерти.
Классификация. Инфекционные болезни разделяют по нескольким признакам.
По биологическому признаку: 1) антропонозы - инфекционные болезни, встречающиеся только у человека; 2) антропозоонозы - инфекционные болезни, возникающие у человека и животных; 3) биоценозы - группа антропонозов и антропозоонозов, передающихся через укусы насекомых, являющихся местом размножения возбудителя.
По этиологическому признаку: 1) вирусные инфекции; 2) риккетсиозы; 3) бактериальные инфекции; 4) грибковые; 5) протозойные; 6) паразитарные. Инфекции могут быть экзогенными или эндогенными. В дальнейшем все инфекционные болезни будут описаны по этиологическому признаку.
По механизму передачи: 1) кишечные инфекции, возникающие при попадании инфекта в пищеварительный тракт через рот; 2) инфекции дыхательных путей, передающиеся воздушно-капельным путем; 3) «кровяные инфекции» (трансмиссивные), передающиеся через кровососущих членистоногих; 4) инфекции наружных покровов, клетчатки и мышц тела (заражение происходит через воздействие каких-либо инфицированных факторов внешней среды; травма инфицированным предметом); 5) инфекции с различными механизмами передачи.
По характеру клинико-анатомических проявлений различают инфекции с преимущественным поражением: 1) покровов (кожи и ее придатков, наружных слизистых оболочек), клетчатки и мышц тела; 2) дыхательных путей; 3) пищеварительного тракта; 4) нервной системы; 5 сердечнососудистой системы; 6) системы крови и других тканей внутренней среды организма; 7) мочеполовых путей.
По характеру течения различают инфекции: 1) острые; 2) хронические; 3) латентные (скрытые); 4) медленные.
Вирусные болезни
Вирусные болезни разнообразны, что определяется прежде всего разнообразием вирусов, которые обладают высокой контагиозностью и способны вызывать эпидемии и пандемии. Разнообразно и течение вирусных инфекций. Они могут быть не только острыми и хроническими, но и латентными (скрытыми) и медленными, которым уделяется особое внимание. Медленные вирусные инфекции имеют длительный (иногда многолетний) инкубационный период, характеризуются персистированием и накоплением возбудителя в организме, прогрессирующим длительным течением заболевания, заканчивающимся в большинстве случаев смертью. Разнообразие вирусных инфекций определяется также их способностью избирательно поражать клетки определенных органов и тканей (тропизм вирусов). Проникновение вируса в клетку обусловлено, с одной стороны, характером рецепторов оболочки клетки (гликопротеиды или липопротеиды), а с другой - особенностями «фермента проникновения» вируса. Так, вирусы гриппа и аденовирусы, содержащие специфические ферменты (нейраминидаза, муциназа), реагируют с гликопротеидными (полисахаридными) рецепторами и легко проникают в цитоплазму и ядро эпителиальных клеток дыхательных путей. Вирус полиомиелита реагирует с липопротеидными рецепторами, имеющими сродство с богатой липидами мозговой тканью, и проникают в цитоплазму нейрона. Ферменты клетки разрушают белки-капсомеры вируса, вследствие чего происходит высвобождение в цитоплазму вирусной нуклеиновой кислоты и включение ее в ультраструктуры клетки-хозяина.
Морфологические проявления взаимоотношений вируса с клеткоймишенью разнообразны: 1) цитолитическое действие вируса (грипп, вирусный гепатит А); 2) интеграция вируса с геномом клетки без выраженной ее деструкции (вирусный гепатит В); 3) пролиферация клетокмишеней (парагрипп, натуральная оспа); 4) гигантоклеточная трансформация (корь, респираторно-синцитиальная инфекция); 5) образование телец - включений (грипп, аденовирусная инфекция, бешенство). При этом следует помнить, что интеграция вируса с геномом клетки может быть основой онкогенного действия ряда вирусов.
Острые респираторные вирусные инфекции
Острые респираторные вирусные инфекции (ОРВИ) - группа клинически и морфологически сходных острых воспалительных заболеваний органов дыхания, вызываемых гшевмотропными вирусами. Эти инфекции широко распространены и в развитых странах суммарно превышают заболеваемость другими инфекциями. ОРВИ чаще появляются в холодное время года и протекают в виде спорадических случаев, эпидемий и пандемий.
Среди ОРВИ наибольшее значение имеют грипп, парагрипп, аденовирусная и респираторно-синцитиальная инфекции.
Грипп
Грипп (от франц. grippe - схватывать) - ОРВИ, вызываемая вирусами гриппа. Кроме человека, им болеют многие млекопитающие (лошади, свиньи, собаки, рогатый скот) и птицы. Источником заболевания людей является только больной человек. Возможна гибридизация вирусов животных и человека, что ведет к изменчивости возбудителя и появлению пандемически опасных штаммов.
Этиология. Возбудители гриппа - 1шевмотропные РНК-содержащие вирусы трех антигенно обусловленных серологических вариантов: A (A1, A2), В и С, относящихся к семейству Orthomyxoviridae. Частицы вируса гриппа (вирионы) округлой формы, диаметром 80-100 нм, состоят из молекулы РНК, окруженной липогликопротеидной оболочкой (капсидом). Благодаря наличию специфических рецепторов капсид обеспечивается адсорбция вируса на эпителиальных клетках. С помощью нейраминидазы вирус растворяет оболочку и проникает внутрь клетки хозяина. РНК-полимераза активирует репродукцию вируса.
Патогенез. Инфекция распространяется воздушно-капельным путем. Инкубационный период длится 2-4 дня. Первичная адсорбция, внедрение и размножение вируса происходят в клетках бронхиолярного и альвеолярного эпителия, в эндотелии капилляров, что ведет к первичной вирусемии. Репродукция вируса в эпителиальных клетках бронхиол и легких сопровождается их гибелью и высвобождением возбудителя, который заселяет эпителий бронхов и трахеи. Острый бронхит и трахеит являются первыми клиническими признаками начала заболевания. Вирус гриппа оказывает цитопатическое (цитолитическое) влияние на эпителий бронхов и трахеи, вызывает его дистрофию, некроз, десквамацию. Нарушение целостности эпителиального барьера бронхов и трахеи определяет возникновение вторичной вирусемии и возможность проявления ряда свойств вируса. Среди них наибольшее значение в патогенезе гриппа имеют вазопатическое (вазопаралитическое) действие (полнокровие, стазы, плазмо- и геморрагия) и угнетение защитных систем организма - нейтрофилов (подавление фагоцитоза), моноцитарных фагоцитов (подавление хемотаксиса и фагоцитоза), иммунной системы (развитие аллергии, появление токсических иммунных комплексов). Вазопатическое и иммунодепрессивное действие вируса гриппа определяют присоединение вторичной инфекции, характер местных (ринит, фарингит, трахеит, бронхит, пневмония) и общих (дисциркуляторные расстройства, дистрофия паренхиматозных элементов, воспаление) изменений.
Внедрение вируса не всегда ведет к развитию острого инфекционного процесса. Возможны латентные (бессимптомные) и хронические формы болезни, которые имеют большое значение, особенно в перинатальной патологии.
Патологическая анатомия. Изменения при гриппе различны и зависят от тяжести его течения, которая определяется типом возбудителя (грипп А2 всегда течет тяжелее), силы его воздействия, состояния макроорганизма
и присоединения вторичной инфекции. Различают легкую (амбулаторную), средней тяжести и тяжелую формы гриппа.
Легкая форма гриппа характеризуется поражением слизистой оболочки верхних дыхательных путей, где развивается острый катаральный риноларинготрахеобронхит. Слизистая оболочка становится набухшей, гиперемированной, с избыточным серозно-слизистым отделяемым. Микроскопически на фоне полнокровия, отека и лимфоидно-клеточной инфильтрации субэпителиального слоя отмечаются гидропическая дистрофия клеток мерцательного эпителия, потеря ими ресничек; усиливается секреторная активность бокаловидных клеток и серозно-слизистых желез, многие клетки эпителия десквамируются. Характерно наличие в цитоплазме эпителиальных клеток базофильных и оксифильных (фуксинофильных) включений. Мелкие базофильные включения представляют собой микроколонии вируса гриппа, что подтверждается методом флюоресцирующих антител (рис. 250). Оксифильные включения являются продуктом реакции клетки на внедрение вируса и появляются вследствие очаговой деструкции ее органелл. Цитоплазматические включения и антиген гриппа могут быть обнаружены в мазках-отпечатках со слизистой оболочки носа в самой ранней стадии гриппа, что имеет значение для его диагностики. Легкая форма гриппа течет благоприятно, заканчивается через 5-6 дней полным восстановлением слизистой оболочки верхних дыхательных путей и выздоровлением.
Грипп средней тяжести протекает с вовлечением в патологический процесс слизистой оболочки не только верхних дыхательных путей, но и мелких бронхов, бронхиол, а также легочной паренхимы. В трахее и бронхах развивается серозно-геморрагическое воспаление, иногда с очагами некроза слизистой оболочки (некротический трахеит, см. рис. 250). Эпи-
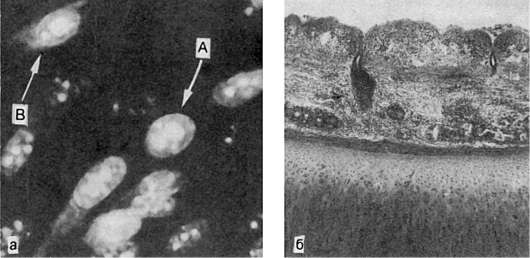 Рис. 250. Грипп:
Рис. 250. Грипп:
а - специфическая люминесценция вируса в ядрах (А) и перинуклеарной зоне (В); б - некротический трахеит
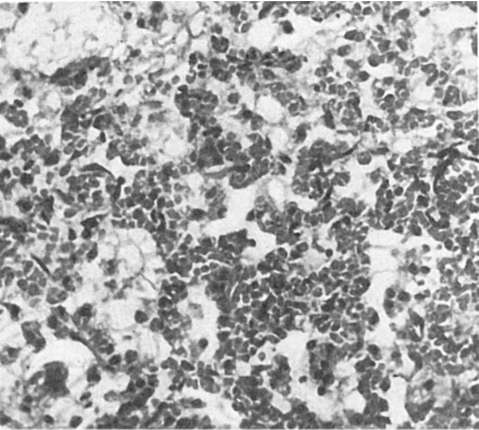 Рис. 251. Гриппозная пневмония
Рис. 251. Гриппозная пневмония
телиальные клетки слущиваются на значительном протяжении в виде пластов, заполняя просвет бронхов, что ведет к развитию очагов ателектаза и острой эмфиземы легких. На фоне полнокровия, участков ателектаза и острой эмфиземы появляются очаги гриппозной пневмонии (рис. 251): в альвеолах видны серозный экссудат, альвеолярные макрофаги, десквамированные клетки альвеолярного эпителия, эритроциты, единичные нейтрофилы; межальвеолярные перегородки утолщены за счет пролиферации септальных клеток и инфильтрации
лимфоидными клетками, иногда обнаруживаются гиалиновые мембраны. В ряде случаев пневмония имеет характер геморрагической. В цитоплазме бронхиального и альвеолярного эпителия имеются включения вируса. Воспалительные, некробиотические и десквамативные процессы в легких сочетаются с регенераторными.
Течение гриппа средней тяжести в целом благоприятное: выздоровление наступает через 3-4 нед. У ослабленных людей, стариков, детей, а также больных сердечно-сосудистыми заболеваниями пневмония может приобрести затяжное течение, явиться причиной сердечно-легочной недостаточности и смерти.
Тяжелая форма гриппа имеет две разновидности: первая обусловлена выраженной общей интоксикацией, вторая - легочными осложнениями в связи с присоединением вторичной инфекции.
При тяжелом гриппе с выраженной общей интоксикацией на первый план выступает цито- и вазопатическое действие вируса. В трахее и бронхах возникают серозно-геморрагическое воспаление и некроз. В легких на фоне расстройств кровообращения и массивных кровоизлияний имеется множество мелких (ацинозных, дольковых) очагов серозногеморрагической пневмонии, чередующихся с фокусами острой эмфиземы и ателектаза. В случаях молниеносного течения гриппа возможен токсический геморрагический отек легких. Кровоизлияния появляются и за пределами легких: в головном мозге, внутренних органах, серозных и слизистых оболочках, коже. Нередко такие больные погибают на 4-5-й день заболевания от кровоизлияний в жизненно важные центры или дыхательной недостаточности.
Тяжелый грипп с легочными осложнениями обусловлен присоединением вторичной инфекции (стафилококк, стрептококк, пневмококк, синегнойная палочка), которая существенно меняет характер морфологических изменений в органах дыхания. Обычно степень воспалительных и
деструктивных изменений нарастает от трахеи к легким, но в наиболее тяжелых случаях в гортани и трахее находят фибринозно-геморрагическое воспаление с обширными участками некроза в слизистой оболочке и образованием язв. Развивается деструктивный анбронхит, что ведет к формированию острых бронхоэктазов, очагов ателектаза и острой эмфиземы. Характерна бронхопневмония (ацинозная, дольковая, сливная дольковая) с наклонностью к абсцедированию, некрозу, кровоизлияниям. В клетках эпителия определяются цитоплазматические включения и антиген вируса, в срезах легких - колонии микробов. Легкие увеличены в объеме, на разрезе пестрого вида - «большое пестрое гриппозное легкое». Нередко в процесс вовлекается плевра, появляется серозный или фибринозный плеврит. Возможно развитие эмпиемы плевры, которая может осложниться гнойным перикардитом и гнойным медиастинитом.
При гриппе во внутренних органах наблюдается сочетание дистрофических и воспалительных изменений с циркуляторными расстройствами. В сердце, печени и почках, помимо полнокровия и петехиальных кровоизлияний, находят белковую и жировую дистрофию паренхиматозных элементов; воспалительные изменения возникают редко и в основном при наличии легочных осложнений (пневмонии). Дистрофические изменения клеток интрамуральных ганглиев сердца могут явиться причиной острой сердечной недостаточности.
В головном мозге при тяжелой форме гриппа циркуляторные расстройства ведут к острому набуханию его вещества, сопровождающемуся вклиниванием миндалин мозжечка в большое затылочное отверстие, и смерти больных. Иногда встречается серозный менингит, который может сочетаться с энцефалитом. Для гриппозного энцефалита характерны периваскулярные лимфоцитарные инфильтраты, нейроглиальные узелки, дистрофические изменения нервных клеток, множество мелких кровоизлияний. Дистрофические и воспалительные изменения наблюдаются также в узлах блуждающего и симпатического нервов, а также в стволах периферических нервов.
В венах конечностей, надпочечников, почек, мозговых синусах воспалительные изменения сочетаются с образованием тромбов - тромбофлебитов, а в артериях очаговый лизис внутренней эластической мембраны сочетается с утолщением интимы и пристеночными тромбами - тромбартериитом.
Особенности течения гриппа у детей. У детей раннего возраста заболевание протекает тяжелее, чем у взрослых; часто развиваются легочные и внелегочные осложнения. Отмечается преобладание общей интоксикации с поражением нервной системы, обилием петехий во внутренних органах, серозных и слизистых оболочках. Местные изменения иногда сопровождаются катаральным воспалением и отеком слизистой оболочки гортани, сужением ее просвета (ложный круп) и асфиксией.
Осложнения. Они наблюдаются главным образом в легких. Карнификация экссудата, облитерирующий бронхит и бронхиолит, склероз стенки
бронхов ведут к развитию бронхоэктазов, пневмофиброза, хронической обструктивной эмфиземы, хронической пневмонии, легочно-сердечной недостаточности. У детей бронхоэктатическая болезнь в 75% наблюдений связана с тяжелым гриппом в раннем возрасте. Осложнения, возникающие в нервной системе (энцефалит, арахноидит, неврит), способствуют инвалидизации больных.
Смерть при гриппе наступает от интоксикации, кровоизлияний в жизненно важные центры (головной мозг), от легочных осложнений (пневмония, эмпиема плевры), сердечной или сердечно-легочной недостаточности. Большую опасность грипп представляет для маленьких детей, стариков и больных сердечнососудистыми заболеваниями.
Парагрипп
Парагрипп (от греч. рага - возле, около) - гриппоподобное острое инфекционное заболевание, вызываемое вирусами парагриппа; характеризуется преимущественным поражением дыхательных путей и умеренной интоксикацией. Распространен повсеместно, составляет около 20% от общего числа ОРВИ. В эпидемии гриппа нередко является сопутствующим заболеванием. Болеют люди разного возраста, но преимущественно дети.
Этиология и патогенез. Возбудители парагриппа - пневмотропные РНК-содержащие вирусы типов 1-4, относятся к семейству Paramyxoviridae. Вирусы имеют форму неправильных сфер диаметром 150-300 нм или длинных спиралей. Капсид вируса содержит фактор, вызывающий образование многоядерных клеточных симпластов. Вирусы парагриппа менее агрессивны по сравнению с вирусами гриппа. Патогенез парагриппа сходен с таковым при гриппе, однако интоксикация выражена меньше и течение заболевания более легкое. Парагрипп, вызванный вирусами типов 1 и 2, протекает как легкая форма гриппа, однако при этом часто возникают острый ларингит и отек гортани, осложняющиеся ложным крупом и асфиксией. Вирус парагриппа типа 3 ведет к поражению нижних дыхательных путей, а вирус типа 4 вызывает интоксикацию. Показана возможность размножения вируса парагриппа в клетках эпендимы и сосудистых сплетений головного мозга.
Патологическая анатомия. Изменения органов дыхания при парагриппе сходны с описываемыми при гриппе, но выражены в меньшей степени. Характерным является пролиферация эпителия трахеи и бронхов с появлением полиморфных клеток, имеющих одно или несколько пузырьковидных пикнотичных ядер. Такие клетки образуют подушкообразные разрастания. Такие же многоядерные клетки встречаются при поражении легких в серозно-десквамативном экссудате. Интерстициальная клеточная реакция в легких выражена умеренно, а кровоизлияния редки. Возможно развитие менингоэнцефалита.
Осложнения парагриппа наблюдаются при присоединении вторичной инфекции. Наиболее часто развиваются бронхопневмония, ангина, синуситы, отит, евстахеит.
Смерть больных при неосложненном парагриппе может наступить от асфиксии, обусловленной ложным крупом, или вирусной пневмонии, при присоединении вторичной инфекции - от легочных осложнений. Парагрипп опасен для детей раннего возраста в связи с возможностью генерализации инфекции.
Респираторно-синцитиальная инфекция
Респираторно-синцитиальная инфекция (PC-инфекция) - острое респираторное инфекционное заболевание, вызываемое респираторносинцитиальным вирусом (PC-вирусом); обладает высокой контагиозностью и нередко носит эпидемический характер.
PC-инфекцией болеет не только человек, но и некоторые животные (шимпанзе).
Этиология и патогенез. PC-вирус относится к РНК-содержащим вирусам из семейства Paramyxoviridae и обладает способностью формировать в культуре гигантские клетки и синцитий, имеет диаметр 90-120 нм. Патогенез РС-инфекции сходен с патогенезом гриппа и парагриппа. Первоначально поражаются легкие, позже - верхние дыхательные пути, что чаще встречается у детей младшего возраста. У детей старшего возраста и у взрослых поражаются только верхние дыхательные пути, и заболевание протекает легко. Возможна генерализация инфекции, которая встречается в основном у детей первых месяцев жизни.
Патологическая анатомия. При PC-инфекции находят ларинготрахеобронхит, бронхиолит и бронхопневмонию. Морфологической особенностью является пролиферация эпителия трахеи, бронхов, бронхиол, альвеолярных ходов в виде сосочков или пластов из нескольких клеток. Эпителиальные пролифераты, как и экссудат, могут вести к обструкции бронхиального дерева и развитию очагов острой эмфиземы и ателектаза легких. Клеточная инфильтрация интерстициальной ткани легких резко выражена и нередко сочетается с деструктивными изменениями стенок альвеол. При бронхопневмонии в воспалительном экссудате обнаруживается большое число крупных клеток, образующих симпласты. В альвеолярных симпластах и сосочковых разрастаниях бронхов методом иммуно-люминесценции определяется PC-антиген. В легких случаях PC-инфекции изменения ограничиваются катаральным воспалением верхних дыхательных путей.
При генерализации инфекции выявляют характерные изменения во внутренних органах: в кишечнике, печени, поджелудочной железе, почках клеточная воспалительная инфильтрация сочетается с сосочковыми разрастаниями эпителия, в центральной нервной системе - с очаговой пролиферацией эпендимы.
Осложнения. Преимущественно легочные в связи с присоединением вторичной инфекции.
Смерть в тяжелых случаях наступает от пневмонии, легочных осложнений, обусловленных вторичной инфекцией, а также генерализации инфекции.
Аденовирусная инфекция
Аденовирусная инфекция - острое респираторное заболевание, вызываемое аденовирусами; характеризуется поражением дыхательных путей, конъюнктивы, лимфоидной ткани зева и глотки, реже - кишечника и лимфатических узлов брюшной полости.
Этиология и патогенез. Аденовирусы - группа ДНК-содержащих вирусов, образующих в клетках внутриядерные включения. Диаметр вирионов составляет 70-90 нм, они содержат двунитчатую ДНК. В капсиде отсутствуют углеводы, липиды и ферменты. Инфекция передается преимущественно воздушно-капельным путем, источником заражения являются больной человек и носители. Адсорбированный вирус проникает в эпителиальную клетку путем пиноцитоза, вирусная ДНК транспортируется в ядро, где происходит репродукция вируса. Цитопатическое действие вируса проявляется в формировании внутриядерных включений, состоящих из вирусных частиц, что определяет в итоге лизис клетки. Выход вируса из клеток при их гибели ведет к интоксикации, которая выражена в меньшей степени, чем при гриппе. Возможны генерализация процесса с поражением многих органов и тканей, а также присоединение вторичной инфекции.
Патологическая анатомия. Выраженность изменений при аденовирусной инфекции зависит от тяжести ее течения. При легкой форме возникают острое катаральное воспаление верхних дыхательных путей (острый риноларинготрахеобронхит), глотки (острый фарингит), регионарный лимфаденит и острый конъюнктивит. Слизистая оболочка верхних дыхательных путей гиперемирована, отечна, с петехиальными кровоизлияниями, лимфогистиоцитарной инфильтрацией и выраженной десквамацией эпителиальных клеток. В цитоплазме десквамированных клеток находят фуксинофильные включения, увеличенные в размерах ядра содержат включения аденовируса. Такие аденовирусные клетки (рис. 252) являются маркером аденовирусной инфекции. У детей до 1 года нередко возникает пневмония, связанная со специфическим действием аденовируса - аденовирусная пневмония (см. рис. 252). В экссудате, который состоит из белковых масс с незначительным числом макрофагов, лимфоидных клеток, нейтрофилов и альвеолярного эпителия, обнаруживаются аденовирусные клетки. В межальвеолярных перегородках среди пролиферирующих септальных клеток также встречаются аденовирусные клетки. Иногда в альвеолах образуются гиалиновые мембраны.
Тяжелая форма заболевания обусловлена генерализацией вируса или присоединением вторичной инфекции. При генерализации инфекции вирусы размножаются в эпителиальных элементах кишечника, печени, почек, поджелудочной железы, ганглиозных клетках головного мозга, при этом образуются аденовирусные клетки. В этих органах развиваются расстройства кровообращения и воспаление. Присоединение вторичной инфекции меняет характер морфологических изменений в органах, присоединяются нагноение и некроз.
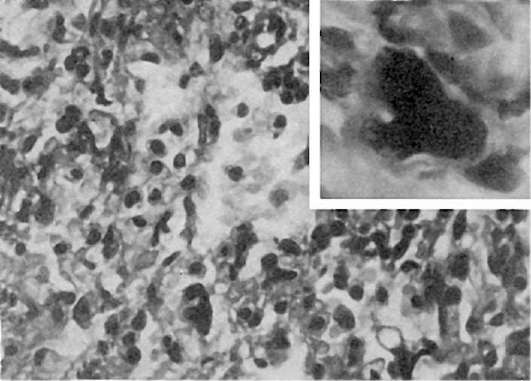 Рис. 252. Аденовирусная инфекция. Вверху справа - аденовирусная клетка
Рис. 252. Аденовирусная инфекция. Вверху справа - аденовирусная клетка
Осложнения. Отит, синусит, ангина, пневмония, развитие которых связано с присоединением вторичной инфекции.
Смерть может наступить от аденовирусной пневмонии, легочных осложнений в связи с присоединением бактериальной инфекции или от распространенных поражений внутренних органов (особенно головного мозга) при генерализации инфекции.
СПИД
СПИД (синдром приобретенного иммунодефицита) - заболевание, вызываемое вирусом иммунодефицита человека (ВИЧ). Свое название получило в связи с развивающимся в финале заболевания тотальным угнетением иммунной системы, сопровождающимся развитием оппортунистических инфекций и опухолей (саркома Капоши, злокачественные лимфомы). Оппортунистическими называют инфекции, вызываемые условно-патогенными (маловирулентными) возбудителями, заражение которыми у здорового человека не сопровождается патологическими изменениями. СПИД всегда заканчивается летально.
Эпидемиология. Первые случаи СПИДа появились в США в 1979 г., но официально заболевание зарегестрировано лишь два года спустя. В последующие годы распространение СПИДа получило характер пандемии. К марту 1988 г. было зарегистрировано 81 433 случая заболевания в 133 странах, однако, поскольку диагностируется лишь небольшой процент случаев СПИДа, по мнению ВОЗ, реальная цифра больных - 250 тыс. Общее количество инфицированных 5-10 млн, из них к 1991 г. заболеет не менее 1 млн человек. Большая часть больных выявлена в США, странах Западной Европы, Африке. В Центральной Африке создалось катастрофическое положение, так как в отдельных ее регионах инфици-
ровано 5-20% взрослого населения. Примерно через каждые 8-10 мес число больных СПИД удваивается, из них половина умирает в течение 5 лет. Среди заболевших преобладают лица в возрасте 20-50 лет (пик заболевания приходится на 30-40 лет); нередко болеют дети.
Источником заражения является больной человек и вирусоноситель. Наибольшая концентрация вируса обнаруживается в крови, сперме, спинномозговой жидкости, в меньших количествах вирус выявляется в слезах, в слюне, цервикальном и вагинальном секретах больных. В настоящее время доказаны 3 пути передачи вируса: 1) половой (при гомосексуальных и гетеросексуальных контактах); 2) посредством парентерального введения вируса с препаратами крови или при использовании инфицированных инструментов; 3) от матери ребенку - транспланцентарный или с молоком. Другие пути передачи вируса (воздушно-капельный, контактно-бытовой, фекально-оральный, трансмиссивный - через укус кровососущих насекомых) убедительных доказательств не получили.
Среди населения США, Канады, а также европейских стран четко определяются контингенты населения, в которых заболеваемость СПИДом особенно высока, что позволило выделить группы риска. К ним отнесены: 1) гомосексуалисты; 2) наркоманы, пользующиеся внутривенным введением наркотиков; 3) больные гемофилией; 4) реципиенты крови; 5) гетеросексуальные партнеры больных СПИДом и вирусоносителей, а также лиц, входящих в группы риска; 6) дети, родители которых принадлежат к одной из групп риска.
Для пандемии СПИДа характерна неравномерность географического, расового и полового распределения случаев заболевания. В США и других промышленно развитых странах с большим числом заболевших основные пути распространения вируса - гомосексуализм и внутривенное применение наркотиков, причем среди больных примерно в 10- 15 раз больше мужчин. В Центральной, Восточной и Южной Африке, а также некоторых странах Карибского бассейна СПИД распространяется преимущественно гетеросексуальным путем, при этом число заболевших мужчин и женщин примерно одинаково. В этих районах также высока роль перинатальной (от матери ребенку) передачи вируса, а также заражение с донорской кровью. В Восточной Европе, на Ближнем Востоке, в Азии зарегистрировано немного случаев СПИДа. В этих регионах зарегистрированы случаи заражения при половых контактах и внутривенных инъекциях, в некоторых случаях заболевание было вызвано импортированной донорской кровью и кровепродуктами. Современная эпидемиологическая ситуация по СПИДу не дает оптимистического прогноза на будущее.
Этиология. Вирус СПИДа впервые выделили в 1983 г. независимо друг от друга Л. Монтанье (Франция) и Р. Галло (США). Им оказался вирус из семейства Т-лимфотропных ретровирусов, который в 1986 г. был назван «ВИЧ». В последнее время этот вирус стали обозначать ВИЧ-1, так как был выявлен другой вирус-ВИЧ-2 (вирус «африканского СПИДа»),
который чаще обнаруживается у аборигенов Западной Африки. Обнаружено много различных штаммов вируса благодаря его феноменальной склонности к мутациям. Диаметр зрелых вирусных частиц 100-140 мкм. Нуклеоид содержит две молекулы РНК (геном вируса) и обратную транскриптазу. Капсид содержит два гликопротеида - 41 и 120, причем последний обеспечивает специфическое связывание вируса с клетками, несущими на своей поверхности антиген СД4. Такими клетками являются прежде всего Т4-лимфоциты (хелперы), в меньшей степени - моноциты и макрофаги, а также микроглия. ВИЧ нестоек во внешней среде и гибнет при температуре 56 °С в течение 30 мин, при 70-80 °C - в течение 10 мин, быстро инактивируется этиловым спиртом, ацетоном, эфиром, 1% раствором глютаральдегида и др., но относительно устойчив к действию ионизирующей радиации и ультрафиолетовому облучению.
Происхождение вируса спорно. Наиболее доказательной считается «теория африканского происхождения», согласно которой ВИЧ в течение длительного времени существовал в Центральной Африке, где СПИД носил характер эндемического заболевания. В середине 70-х годов нашего столетия в связи с усиленной миграцией населения из Центральной Африки, обусловленной засухой и голодом, ВИЧ был завезен в США и Западную Европу, где он долго циркулировал среди гомосексуалистов, а затем стал распространяться среди других слоев населения.
Патогенез. При заражении ВИЧ попадает в кровь непосредственно (при инъекциях) либо через поврежденные слизистые оболочки половых путей (при половом контакте) и связывается с клетками, к которым обладает тропизмом. При взаимодействии вируса с клеткой-мишенью его оболочка сливается с клеточной мембраной, вирус оказывается внутри клетки. С РНК вируса с помощью обратной транскриптазы снимается ДНК-копия (провирус), которая встраивается в хромосомную ДНК клетки-мишени. Вирусный генетический материал остается в клетке пожизненно, при делении клетки он передается ее потомству. ВИЧ ведет себя различно в зависимости от типа зараженной клетки, уровня ее активности, а также от состояния иммунной системы. В Т4-лимфоцитах он может находится в латентном состоянии неопределенно долго, чем объясняется возможность длительного латентного вирусоносительства при СПИДе. Активация Т4-лимфоцитов (например, при инифицировании другим агентом) может спровоцировать бурную репликацию ВИЧ, что ведет к массовой гибели клеток. В моноцитах и макрофагах репликация происходит очень медленно, без выраженного цитопатического действия, но изменяя функциональное состояние клетки. Разнообразное поведение вируса в клетке-мишени определяется сложной организацией его генома, в состав которого входят не только структурные гены (с ними связан синтез вирусспецифичных белков), но и регуляторные гены, взаимодействие которых определяет начало репликации и ее интенсивность. Сложные механизмы регуляции репликации ВИЧ находятся в тесном взаимодействии с метаболизмом клетки-хозяина.
Ведущим звеном в развитии иммунодефицита считают поражение Т4- лимфоцитов (хелперов), которое подтверждается у больных СПИДом прогрессирующей лимфопенией. Не только уменьшается количество Т-хелперов, но и снижается отношение Т4/Т8 (хелперно-супрессорное отношение), которое при СПИДе всегда меньше 1. Снижение T4/T8 является главной особенностью иммунологического дефекта при СПИДе и определяется при всех его клинических вариантах.
Механизм гибели Т4-лимфоцитов нельзя сводить только к цитопатическому действию вируса. Большое значение имеет образование нежизнеспособных многоядерных клеточных симпластов, связанных с зараженной клеткой, причем одна зараженная клетка может связывать до 500 нормальных. Экспрессируемые на поверхности инфицированных клеток вирусные антигены стимулируют иммунный ответ в виде продукции анти-ВИЧ-антител и цитотоксических лимфоцитов, которые обусловливают цитолиз как поврежденных, так и неповрежденных Т4-клеток. Гибель непораженных Т4-лимфоцитов связана с их способностью связывать свободные молекулы вирусного гликопротеина, отделившегося от зараженных клеток и циркулирующих в крови. В последнее вре.мя установлено, что ВИЧ не только приводит к уменьшению количества Т4-лимфоцитов, но и вызывает выделение оставшегося растворимого фактора супрессии, в результате чего Т4-клетки теряют способность осуществлять узнавание антигена.
Количественные и качественные изменения Т4-лимфоцитов, которые являются «дирижерами» иммунного процесса, а также повреждение вирусом макрофагов приводят к грубому полому в первую очередь клеточного, а также и гуморального иммунитета. Повреждение клеточного иммунитета у больных СПИДом проявляется резким снижением, а в финале заболевания и полной утратой реакций ГЗТ на различные антигены, как и снижение реакции бласттрансформации in vitro. Повреждение гуморального иммунитета представлено неспецифической поликлональной активацией В-клеток, сопровождающейся повышением уровня сывороточных иммуноглобулинов. Однако способность формировать специфический гуморальный ответ снижается по мере прогрессирования заболевания. В финале развивается угнетение и гуморального звена иммунитета.
Особенности взаимодействия ВИЧ с клеткой, а также раннее и прогрессирующее повреждение иммунной системы приводят к тому, что организм оказывается неспособным элиминировать ВИЧ и противостоять вторичной инфекции. Он становится беззащитным в отношении воздействия многих вирусов, грибов, некоторых бактерий (в частности, микобактерий туберкулеза). Ведущими в клинике СПИДа становятся оппортунистические инфекции и опухоли.
Периоды течения СПИДа и их морфология. Полагают, что все инфицированные ВИЧ рано или поздно заболевают СПИДом. Заболевание развивается длительное время (от 1 года до 15 лет), медленно прогрессирует, проходя несколько периодов (стадий), имеющих определенное клиниче-
ское и морфологическое выражение. Среди периодов СПИДа различают: 1) инкубационный; 2) персистирующей генерализованной лимфоаденопатии; 3) пре-СПИД, или СПИД-ассоциированньгй комплекс; 4) СПИД (схема XXIII).
Инкубационный период, его продолжительность зависит от путей и характера заражения, величины инфицирующей дозы, первоначального состояния иммунной системы; он может длиться от нескольких недель до 10-15 лет. В этот период можно установить сам факт инфицирования при определении в крови антигена или анти-ВИЧ-антител. Количество антигена вируса в крови в первое время резко увеличивается, затем, начиная с 6-8-й недели, когда появляются анти-ВИЧ-антитела, снижается, т.е. происходит сероконверсия. Некоторые исследователи выделяют сероконверсию в самостоятельный период СПИДа.
В большинстве случаев в инкубационный период симптомов заболевания нет, однако у некоторых отмечается синдром, похожий на мононуклеоз: лихорадка, увеличение различных групп лимфатических узлов,
Схема XXIII. Периоды СПИД
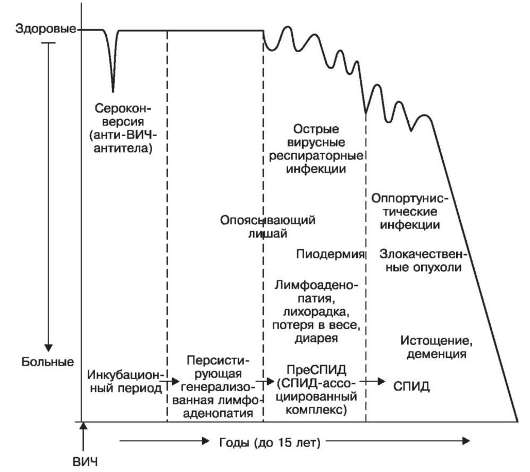 иногда острый энцефалит. Но проявления этого синдрома проходят обычо в течение нескольких недель.
иногда острый энцефалит. Но проявления этого синдрома проходят обычо в течение нескольких недель.
Второй период - период персистирующей генерализованной лимфоаденопатии - характеризуется стойким, в течение нескольких месяцев, увеличением различных групп лимфатических узлов. В основе лимфоаденопатии лежит неспецифическая гиперреактивность В-клеток, проявляющаяся фолликулярной гиперплазией лимфатических узлов (увеличение лимфоидных фолликулов и их светлых центров). Длительность стадии - 3-5 лет.
Третий период заболевания, возникающий на фоне умеренного иммунодефицита, называют преСПИД, или СПИД-ассоциированным комплексом. Для него характерны лихорадка, лимфоаденопатия, диарея, незначительная потеря массы тела. На этом фоне появляется наклонность к развитию вторичных инфекций - острых вирусных респираторных инфекций, опоясывающего лишая, пиодермии и др. Этот период длится несколько лет.
Четвертый период заболевания, который продолжается около двух лет, - это период синдрома приобретенного иммунодефицита (СПИД). Для него характерны оппортунистические инфекции и опухоли, истощение и деменция. В этот финальный период, как правило, снижается количество анти-ВИЧ-антител (они могут вообще не определяться), а количество вирусных антигенов нарастает, что необходимо учитывать при диагностике
СПИДа.
Патологическая анатомия. Происходят изменения лимфатических узлов, характерные поражения ЦНС и изменения, типичные для оппортунистических инфекций и опухолей. Фолликулярная гиперплазия лимфатических узлов сменяется полным истощением их лимфоидной ткани (рис. 253). Лимфатические узлы резко уменьшаются, определяются с трудом. Поражение ЦНС представлено ВИЧ-энцефаломиелитом, при этом основные изменения находят главным образом в белом веществе и подкорковых узлах мозга. При микроскопическом исследовании находят микроглиальные узелки, многоядерные симпласты, в которых удается обнаружить частицы ВИЧ. В боковых и задних столбах спинного мозга определяются очаги размягчения и вакуолизация белого вещества. Благодаря демиелинизации белое вещество приобретает сероватый оттенок. Для оппортунистических инфекций при СПИДе характерно тяжелое рецидивирующее течение, часто с генерализацией процесса и устойчивостью к проводимой терапии. Оппортунистические инфекции могут вызываться простейшими (пневмоцисты, токсоплазмы, криптоспоридии), грибами (рода Candida, криптококки), вирусами (цитомегаловирусы, герпетические вирусы, некоторые вирусы медленных инфекций), бактериями (Mycobacterium avium intracellulare, легионелла, сальмонелла). Одна из самых частых и характерных инфекций при СПИДе вызывается пневмоцистами. Она приводит к развитию тяжелой пневмонии с образованием в альвеолах большого количества пенистых эозинофильных масс, в ко-
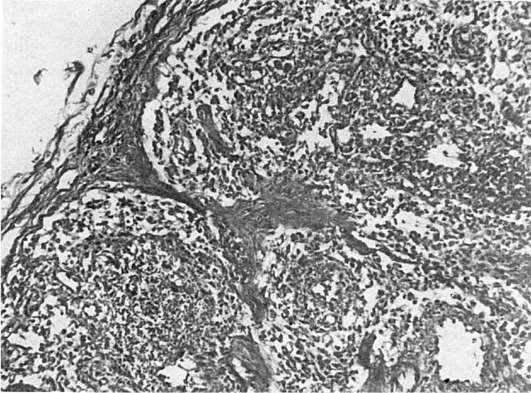 Рис. 253. Истощение лимфоидной ткани лимфатического узла при СПИДе
Рис. 253. Истощение лимфоидной ткани лимфатического узла при СПИДе
торых выявляются пневмоцисты. Довольно часто возникает и токсоплазменная инфекция, при которой находят энцефалит; для него характерны фокусы некроза и абсцедирования. При криптоспоридиозе поражается кишечник, развиваются энтериты и колиты, проявляющиеся длительной профузной диареей. Среди поражений грибами часто отмечается кандидоз с вовлечением пищевода, трахеи, бронхов, легких, а также криптококков, склонный к диссеминации процесса. Из вирусных инфекций наиболее типична цитомегаловирусная с развитием ринита, пневмонита, колита, энцефалита. Герпетической инфекции свойственно длительное поражение слизистых оболочек и кожи. Среди бактериальных инфекций наиболее характерна атипичная микобактериальная инфекция Mycobacteria avium intracellulare, которая приводит к развитию диссеминированного процесса с поражением лимфатических узлов и внутренних органов.
Злокачественные опухоли при СПИДе встречаются в 40% случаев. Наиболее характерными являются саркома Капоши (у 30% больных) и злокачественные лимфомы.
Саркома Капоши (множественная идиопатическая геморрагическая саркома) - редкое заболевание, возникающее обычно у мужчин старше 60 лет, характеризуется медленным довольно доброкачественным течением. Проявляется багрово-красными пятнами, бляшками и узлами, расположенными обычно на коже дистальных отделов нижних конечностей. Характерны изъязвления. Возможна самопроизвольная инволюция с возникновением на месте опухоли рубцов и депигментированных пятен. Микроскопически опухоль состоит из множества новообразованных
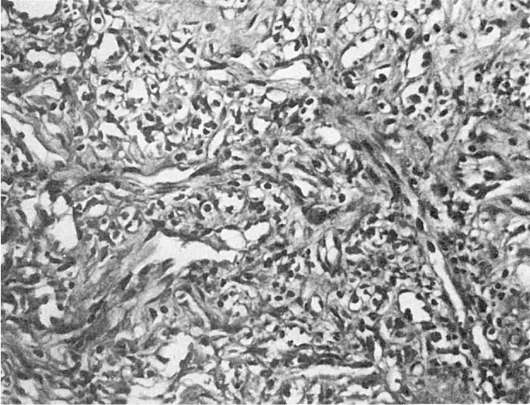 Рис. 254. Саркома Капоши у больного СПИДом. Поражение кожи
Рис. 254. Саркома Капоши у больного СПИДом. Поражение кожи
хаотично расположенных тонкостенных сосудов с хорошо определяемым эндотелием и пучков веретенообразных клеток (рис. 254). В рыхлой строме часто видны кровоизлияния и скопления гемосидерина. У больных СПИДом саркома Капоши имеет злокачественный характер и отличается от классического варианта генерализацией процесса с поражением лимфатических узлов, желудочно-кишечного тракта, легких и других внутренних органов.
Злокачественные лимфомы при СПИДе преимущественно В-клеточные. Часто встречается лимфома Беркитта (см. Лимфомы).
Многообразие оппортунистических инфекций, часто сочетающихся между собой, а также с опухолями, делает клиническую картину СПИДа чрезвычайно полиморфной. В связи с этим выделяют несколько наиболее типичных клинических вариантов СПИДа: легочный, синдром поражения центральной нервной системы, желудочно-кишечный синдром, лихорадку неясного генеза.
Легочный вариант - самый частый (у 80% больных). Он представлен сочетанием пневмоцистной пневмонии, цитомегаловирусной и атипичной микобактериальной инфекции и саркомы Капоши. Синдром поражения центральной нервной системы включает ВИЧ-энцефалит, поражения, связанные с токсоплазмозом, криптококкозом и цитомегаловирусной инфекцией, а также лимфому; приводит к развитию деменции. Желудочнокишечный синдром - это сочетание кандидоза, цитомегаловирусной инфекции, криптоспоридиоза и атипичной микобактериальной инфекции;
сопровождается диареей и развитием в финале кахексии. Лихорадка неясного генеза; в ряде случаев удается обнаружить атипичную микобактериальную инфекцию или злокачественную лимфому.
Причины смерти. Смерть наступает чаще от оппортунистических инфекций и генерализации опухолей. В развитых странах 50% больных умирают в течение 18 мес со дня постановки диагноза и 80% - в течение 36 мес. Летальность достигает 100%.
Натуральная оспа
Натуральная оспа (variola vera, лат. variolus - пестрый) - острое контагиозное вирусное заболевание из группы карантинных инфекций с поражением легких, кожи и реже других органов. Оспа ликвидирована во всем мире, но это не исключает случаи заражения.
Этиология и патогенез. Возбудителем оспы является ДНК-содержащий вирус (Poxvirus variola). Колонии вируса видны под световым микроскопом в виде элементарных телец. Тельца Пашена представляют собой мелкие кокковидные образования, тельца Гуарниери - более крупные образования. Источник инфекции - больной человек. Заражение происходит воздушно-капельным и контактным путем. Входными воротами чаще являются органы дыхания, где появляется первичное поражение. Из места первичного поражения вирус в короткие сроки распространяется в организме, как следствие вирусемии возникают множественные вторичные поражения, которые особенно выражены в коже.
Патологическая анатомия. При натуральной оспе поражаются кожа и дыхательные пути, наиболее типично поражение кожи. Различают три основные формы натуральной оспы: папулопустулезную, геморрагическую и вариолоид.
Папулопустулезная форма характеризуется появлением на коже папулопустулезной сыпи, особенно обильной на лице, волосистой части головы, шее, груди, спине. Самые ранние изменения возникают в дерме в виде полнокровия, отека, незначительной периваскулярной клеточной инфильтрации. Вслед за этим наступает пролиферация, набухание, гидропическая дистрофия клеток росткового (мальпигиева) слоя эпидермиса, которая сменяется его баллонной дистрофией, или «баллонирующей дегенерацией» эпидермиса (рис. 255). Баллонообразные клетки сливаются и образуют пузырьки, разделенные на камеры тяжами эпителиальных клеток; клетки, входящие в эти тяжи, сдавливаются, подвергаются дистрофии, ядра их сморщиваются (ретикулярная дегенерация). Макроскопически эти образования вначале имеют вид папул, затем превращаются в везикулы и гнойнички - пустулы (рис. 256). На 3-й неделе пустулы заживают, оставляя рубчики разных размеров в зависимости от глубины деструктивного процесса.
Геморрагическая форма характеризуется присоединением к папулам и пустулам кровоизлияний, сопровождается отеком кожи, полнокровием. На коже появляются сливные и крупнопятнистые кровоизлияния, мно-
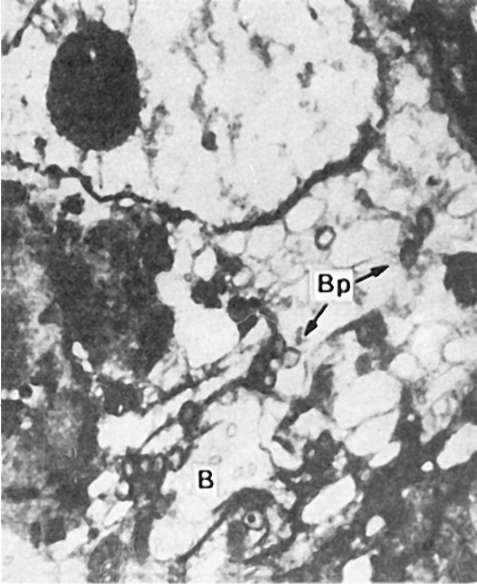 Рис. 255. Натуральная
оспа. Баллонная дистрофия эпидермиса: цитоплазма заполнена огромными
вакуолями (В), в которых находятся частицы вируса (Вр); ультраструктуры
клетки разрушены. х1 000 000 (по Девису и др.)
Рис. 255. Натуральная
оспа. Баллонная дистрофия эпидермиса: цитоплазма заполнена огромными
вакуолями (В), в которых находятся частицы вируса (Вр); ультраструктуры
клетки разрушены. х1 000 000 (по Девису и др.)
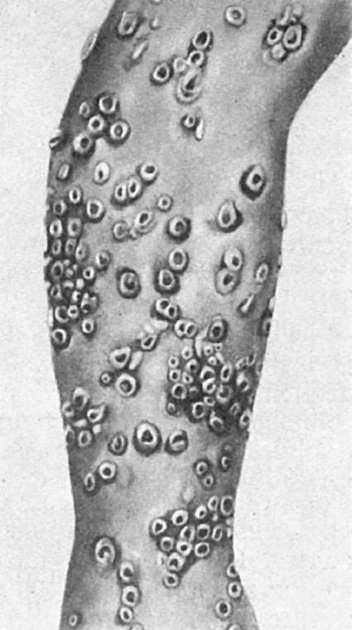 Рис. 256. Изменения кожи при оспе
Рис. 256. Изменения кожи при оспе
жество пузырей, которые лопаются, что ведет к образованию кровоточащих дефектов кожи («черная оспа»). Для этой формы характерно очень тяжелое течение, исходом которого становится смерть больных. Важное клинико-эпидемиологическое значение имеет так называемая оспенная пурпура - форма натуральной оспы, протекающая как острый сепсис и всегда быстро заканчивающаяся гибелью больных.
Вариолоид - легкая форма натуральной оспы, которая может протекать как с сыпью, так и без нее. Она наблюдается у ревакцинированных лиц, нередко в период инкубации. Заболевание заканчивается благоприятно, но может провоцировать скрыто протекающие болезни крови, сердца, легких и др.
Характерные для оспы изменения встречаются в слизистой оболочке дыхательных путей и легких. В слизистой оболочке трахеи и бронхов на фоне катаральных изменений образуются везикулы и пустулы. В легких могут возникать очажки некроза. В слизистой оболочке полости рта, пищевода, кишечника, влагалища также могут развиваться оспенные пустулы с изъязвлением. В яичках нередко появляются очаги некроза («некротический» орхит). Иногда очаги некроза встречаются и в костном мозге эпифизов трубчатых костей (оспенный остеомиелит). Селезенка резко увеличена, полнокровна; микроскопически в ней обнаруживаются миелоз, кровоизлияния, очаги некроза. Лимфатические узлы увеличены, в них отмечают гиперплазию фолликулов и фокусы некроза.
Осложнения. Очень опасны осложнения, связанные с развитием оспенных гнойников в конъюнктиве глаза, что может привести к разрушению роговицы и слепоте. Поражение слизистой оболочки среднего уха приводит к глухоте. Оспенные пустулы могут быть источником флегмоны кожи. В легких развиваются абсцессы, гангрена.
Смерть больных оспой наступает от оспенного токсикоза, сепсиса или от осложнений в связи с присоединившейся бактериальной инфекцией.
Бешенство
Бешенство (rabies, от лат. rabere - бесноватый), водобоязнь, гидрофобия (от греч. hydor - вода, hobos - боязнь) - острое инфекционное заболевание, которым болеют люди и животные (антропозооноз), характеризуется поражением центральной нервной системы.
Этиология и патогенез. Возбудителем болезни является вирус бешенства из семейства рабдовирусов, патогенный для человека и большинства теплокровных животных. Заражение человека происходит при укусе больным животным. Кожная рана считается входными воротами инфекции. Из раны вирус, обладающий нейротропностью, распространяется по периневральным пространствам, достигает нервных клеток головного и спинного мозга, внедряется в них и репродуцируется. Инкубационный период длится 30-40 дней. Продолжительность болезни - 5-7 дней. В течение заболевания различают стадию предвестников, возбуждения и паралитическую. В момент начала заболевания в области укуса, который к этому времени заживает рубцом, нередко вспыхивает экссудативное воспаление, а в периферических нервах той же области обнаруживаются воспалительные инфильтраты и распад миелиновых оболочек.
Патологическая анатомия. Характерные для бешенства изменения выявляются главным образом в головном мозге, который становится отечным, полнокровным, иногда с мелкими кровоизлияниями в области продолговатого мозга. Характерные изменения, которые находят лишь при микроскопическом исследовании, касаются нервных клеток стволовой части головного мозга, стенок III желудочка мозга и гиппокампа. В результате репродукции вируса бешенства в нервных клетках развиваются хроматолиз, гидропия, завершающиеся некрозом. Вокруг погибших нервных клеток, мелких сосудов обнаруживаются скопления микроглиальных и лимфоидных клеток, образующих узелки бешенства. Их особенно много в продолговатом мозге, области водопровода большого мозга (сильвиев водопровод), но они встречаются и в других отделах нервной системы. Иногда появляются мелкие кровоизлияния. Описанные изменения в головном мозге соответствуют картине энцефалита. Аналогичные изменения встречаются и в спинном мозге, особенно шейном утолщении. В узлах вегетативной нервной системы также происходит гибель нервных клеток, вокруг них отмечается усиленная пролиферация сателлитов, клеток лимфоидного типа - образуются узелки бешенства. Особенно резко эти изменения выражены в тройничном (так называемом гассеровом) и верхних шейных симпатических узлах.
Большое диагностическое значение имеет обнаружение в нервных клетках гиппокампа, реже в других отделах головного мозга так называемых телец Бабеша-Негри, представленных эозинофильными округлыми образованиями (включениями) в цитоплазме.
В слюнных железах при бешенстве встречаются круглоклеточные инфильтраты вокруг сосудов, в нервных узлах желез - узелки бешенства. В других органах наблюдаются дистрофические изменения.
Смерть при нелеченом бешенстве и без применения антирабической сыворотки наблюдается в 100% случаев. Больные, прошедшие курс антирабических прививок, остаются здоровыми. Однако возможно развитие прививочных осложнений: менингоэнцефалита, восходящего паралича Ландри, параличей отдельных нервов, психических расстройств.
Риккетсиозы
Риккетсиозы - группа болезней, вызываемых микроорганизмами рода риккетсий, которых в настоящее время причисляют к бактериям. Однако некоторые особенности риккетсий (паразитирование в клетках эндотелия и мезотелия), как и эпидемиологические и клинико-морфологические особенности вызываемых ими заболеваний, позволяют говорить об особой группе болезней - риккетсиозах. В естественных условиях риккетсиозы наблюдаются у кровососущих членистоногих (вши, блохи, клещи), у некоторых диких и домашних животных и, наконец, у людей. Резервуар риккетсиозной инфекции в природе образуют клещи, дикие и домашние животные. Больной человек является источником инфекции только при таких риккетсиозах, как эпидемический сыпной тиф и волынская лихорадка. Все остальные риккетсиозы являются эндемическими инфекциями и наблюдаются исключительно в районах соответствующих энзоотии (природные очаги инфекции).
Классификация. П.Ф. Здродовский и Е.А. Голиневич (1972) предложили единую номенклатуру риккетсиозов, в которую включено 11 групп: 1) вшивый, или эпидемический, сыпной тиф и спорадический сыпной тиф, или болезнь Брилла-Цинссера; 2) эндемический, или крысиный, сыпной тиф; 3) пятнистая лихорадка Скалистых гор; 4) марсельская лихорадка; 5) клещевой сыпной тиф; 6) североавстралийский тиф; 7) везикулярный, или осповидный, риккетсиоз; 8) лихорадка цуцугамуши; 9) Ку-лихорадка; 10) волынская лихорадка; 11) клещевой пароксизмальный риккетсиоз. В патологии человека особенно большое значение имеют эпидемический сыпной тиф, спорадический сыпной тиф и Кулихорадка.
Эпидемический сыпной тиф
Эпидемический сыпной тиф (typhus exanthematicus) - острое лихорадочное риккетсиозное заболевание, характеризующееся поражением мелких сосудов, головного мозга, токсикозом, распространенной розеолезно-
петехиальной сыпью. Заболевание чаще наблюдается в возрасте от 20 до 40 лет, реже - в пожилом возрасте и совсем редко - у детей. Несколько чаще болеют мужчины.
Этиология и патогенез. Вызывают сыпной тиф риккетсии Провацека-да Роха-Лима. Источником заболевания и резервуаром риккетсии является больной человек, а переносчиком их от больного к здоровому - платяная (иногда головная) вошь. Она заражается от больного тифом человека, а затем, при укусе здоровых, через свои фекалии распространяет риккетсии при расчесе кожи. После инкубационного периода, продолжающегося 10-12 дней, начинается лихорадочный период заболевания, сопровождающийся генерализованным токсико-паралитическим поражением микроциркуляторного русла, особенно выраженным в продолговатом мозге (рис. 257), что ведет к падению артериального давления. Эти явления усиливаются, когда в результате внедрения в эндотелий мелких сосудов и размножения в нем риккетсии развивается генерализованный васкулит с преимущественным поражением центральной нервной системы, особенно продолговатого мозга и кожи. На высоте лихорадочного периода (на 2-3-й недели болезни) в связи с поражением продолговатого мозга могут развиваться нарушения глотания и дыхания (бульварные явления). Распространенные васкулиты в сочетании с расстройствами нервной трофики понижают устойчивость тканей, у больных легко возникают некрозы тканей, пролежни. Поражения симпатической нервной системы и надпочечников усиливают гипотонию, сопровождаются нарушением сердечной деятельности, которая может привести к летальному исходу.
Патологическая анатомия. Основные изменения при сыпном тифе выявляются только с помощью микроскопа. При вскрытии трупов умерших от сыпного тифа диагноз можно поставить только предположительно. На коже обнаруживаются следы сыпи в виде пятен и точек коричневого и красного цвета. Особенно характерно наличие конъюнктивальной сыпи, которая постоянно отмечается на 2-4-й неделе болезни. Вещество мозга
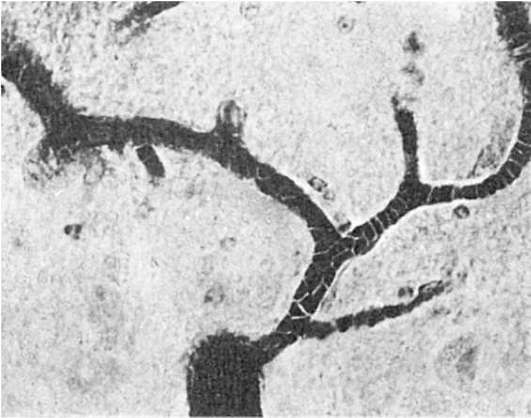 Рис. 257. Стаз в сосудах микроциркуляторного русла с агрегацией эритроцитов при экспериментальном сыпном тифе (препарат А.П. Авцына)
Рис. 257. Стаз в сосудах микроциркуляторного русла с агрегацией эритроцитов при экспериментальном сыпном тифе (препарат А.П. Авцына)
полнокровное, мягкие оболочки тусклые (серозный менингит), селезенка увеличена (масса ее 300-500 г), мягкая, полнокровная, ткань ее дает небольшой соскоб пульпы на разрезе. В других органах отмечаются дистрофические изменения.
При микроскопическом исследовании органов, особенно ЦНС и кожи, обнаруживаются изменения каппиляров и артериол, характерные для сыпнотифозного васкулита. Вначале наблюдают набухание, деструкцию, слущивание эндотелия и формирование тромбов (пристеночных или обтурирующих). Затем нарастает пролиферация эндотелия, адвентициальных и периадвентициальных клеток, вокруг сосудов появляются лимфоциты и единичные нейтрофилы; в стенке сосудов развивается очаговый некроз. Изменения в сосудах могут варьировать как по интенсивности, так и по степени участия пролиферативных, некробиотических или тромботических процессов. Исходя из этого, выделяют несколько видов сыпнотифозного васкулита: бородавчатый эндоваскулит, пролиферативный заскулит, некротический васкулит. Часто можно говорить о сыпнотифозном деструктивно-пролиферативном эндотромбоваскулите. Следует отметить, что очаги эндо- и периваскулярной инфильтрации имеют вид узелков, которые были впервые обнаружены при сыпном тифе в ЦНС Л.В. Поповым (1875). В последующем узелки признаны наиболее характерными, для сыпного тифа образованиями и названы сыпнотифозными гранулемами Попова (рис. 258).
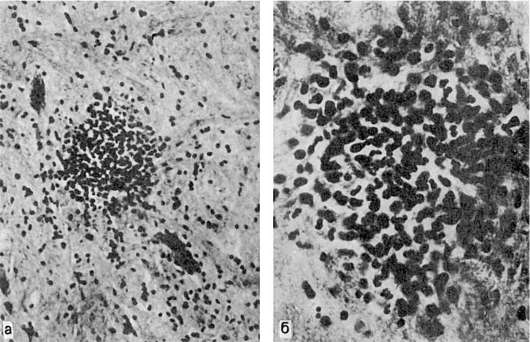 Рис. 258. Узелок Попова в продолговатом мозге при сыпном тифе (препарат А.П. Авцына):
Рис. 258. Узелок Попова в продолговатом мозге при сыпном тифе (препарат А.П. Авцына):
а - малое увеличение; б - большое увеличение
Сыпнотифозные гранулемы обнаруживаются во всех системах и органах, за исключением печени, селезенки, лимфатических узлов и костного мозга, но строение гранулем и характер васкулитов различны в разных органах. В головном мозге гранулемы окружаются широкой зоной пролиферирующих клеток микроглии (глиогранулематоз сосуда). В коже в образовании гранулемы принимают участие эндо- и перителий капилляров и адвентициальные клетки артериол и венул, а также окружающие сосуд лимфоидные клетки, единичные нейтрофилы. Просвет сосуда в центре сформированной гранулемы, как в мозге, так и в коже, распознается с трудом или совсем теряется в массе пролиферирующих клеток. В симпатической нервной системе сыпнотифозные гранулемы образуются так же, как и в головном мозге.
Сыпнотифозная сыпь (экзантема) появляется в коже на 3-5-й день лихорадочного периода болезни. Морфологически она характеризуется описанными выше изменениями сосудов микроциркуляторного русла и мелких артерий с образованием гранулем. При преобладании некротических васкулитов в коже могут появляться геморрагии (петехии), что обычно наблюдается при тяжелом течении сыпного тифа. В головном мозге сыпнотифозные узелки образуются обычно на 2-й неделе и исчезают в начале 6-й недели заболевания. Они обнаруживаются в мосту и ножках мозга, подкорковых ганглиях, продолговатом мозге (особенно часто на уровне нижних олив), задней доли гипофиза. В белом веществе полушарий большого мозга узелки отсутствуют. Кроме того, в ткани головного мозга наблюдаются гиперемия, стазы, периваскулярные (главным образом перивенозные) муфты из плазматических клеток, очаговая пролиферация микроглии. Альтеративные изменения нервных клеток не достигают большой степени. На основании этих изменений можно говорить о развитии при сыпном тифе энцефалита, который сочетается с серозным менингитом.
В симпатической нервной системе развиваются воспалительные изменения с образованием узелков и инфильтратов из лимфоидных клеток, гиперемия, нервные клетки подвергаются значительным изменениям - сыпнотифозный ганглионит. Воспалительные явления обнаруживаются и в периферической нервной системе - неврит.
Сердце при сыпном тифе поражается постоянно, что выражается развитием дистрофических изменений миокарда или интерстициального миокардита, который проявляется в очаговой, реже диффузной, инфильтрации стромы плазматическими клетками, лимфоцитами, образованием гранулем. Выраженность миокардита может быть различной. Артерии крупного, среднего и мелкого калибров при сыпном тифе часто вовлекаются в процесс: наблюдаются некроз эндотелия, иногда сегментарные некрозы мышечной оболочки, что ведет к пристеночному или обтурирующему тромбозу и развитию локальных гемодинамических нарушений: гангрены конечностей, очагов некроза в головном мозге, сетчатке глаза.
В эндокринных железах отмечаются различные изменения. В щитовидной железе развивается межуточное воспаление, в надпочечниках - эндо- и периваскулиты, тромбоэндоваскулиты, типичные для сыпного тифа. Кроме того, в ткани надпочечников наблюдаются очаги некроза, кровоизлияния в мозговом слое. В остальных органах могут встречаться межуточные гистиолимфоцитарные и плазмоклеточные инфильтраты, кровоизлияния.
Осложнения сыпного тифа многообразны и связаны с изменениями сосудов и нервной системы. Часто развиваются трофические нарушения. В коже от небольшого давления возникают очаги некроза на выступающих участках кожи, пролежни. При подавлении секреции слюнных желез в связи с поражением шейных симпатических ганглиев создаются условия для развития вторичной инфекции: развиваются гнойные паротит и отит, заканчивающиеся сепсисом. При подкожных инъекциях лекарств появляются очаги некроза подкожного жира - олеогранулемы (некроз жира может происходить и спонтанно). В результате нарушений кровообращения (васкулиты) и в связи с ослаблением деятельности сердца (миокардит) развиваются бронхит, пневмония.
Смерть при сыпном тифе наступает вследствие сердечной недостаточности или от осложнений. Наибольшая летальность отмечается у людей старше 40 лет. Сыпной тиф у детей протекает легко и дает небольшую летальность.
Спорадический сыпной тиф
Спорадический сыпной тиф (болезнь Брилла-Цинссера) - разновидность сыпного тифа, этиологически тождественная эпидемическому сыпному тифу. Он встречается среди населения, в прошлом болевшего эпидемическим сыпным тифом, и рассматривается как его повторный рецидив. Спорадический сыпной тиф отличается появлением одиночных случаев заболевания, преимущественно у людей старше 45 лет, доброкачественным течением, отсутствием вшивости и высоким титром антител к специфическим антигенам риккетсий Провацека. Клинические проявления и характер морфологических изменений аналогичны таковым при эпидемическом сыпном тифе, но выражены слабее. Летальность небольшая.
Появление случаев спорадического тифа свидетельствует о существовании у людей, перенесших эпидемический сыпной тиф, резервуара риккетсий Провацека и возможности рецидивирования у них заболевания через много лет (Здродовский П.Ф., 1972). При наличии завшивленности в окружении больного спорадическим сыпным тифом возможна вспышка эпидемического сыпного тифа.
Ку-лихорадка
Ку-лихорадка - пневмориккетсиоз. Отличается высокой контагиозностью, острым лихорадочным течением и развитием пневмонии. Встречается во многих странах, в том числе и на территории СССР.
Этиология и патогенез. Ку-лихорадка вызывается риккетсией Бернета. Передается воздушно-капельным, алиментарным или контактным путем.
Морфологическая картина. В острых случаях развивается интерстициальная пневмония, которая иногда может принять затяжное течение и привести к летальному исходу. На вскрытии умерших в таких случаях находят, помимо интерстициальной, фокусы очаговой пневмонии с явлениями карнификации, васкулиты, гиперплазию лимфатических узлов с образованием в них многочисленных эпителиоидно- и плазмоклеточных узелков.
Болезни, вызываемые бактериями
Болезни, вызываемые бактериями, чрезвычайно разнообразны, что определяется особенностью возбудителя, способом заражения, аффинностью клеток и тканей в отношении инфекта, характером реакции макроорганизма на инфект и т.д. Описываемые ниже заболевания являются иллюстрацией разнообразия бактериальных инфекций.
Брюшной тиф
Брюшной тиф - острое инфекционное заболевание из группы кишечных; типичный антропоноз. Возможны эпидемии, но в настоящее время заболевание имеет обычно спорадический характер и довольно легкое течение.
Этиология и патогенез. Вызывается брюшнотифозной палочкой (Salmonella typhi). Источником заражения является больной человек или бациллоноситель, в выделениях которого (кал, моча, пот) содержатся микробы. Заражение происходит парентерально. Инкубационный период 10-14 дней. В нижнем отделе тонкой кишки бактерии размножаются, выделяют эндотоксины. Из кишки по лимфатическим путям они поступают в групповые лимфатические фолликулы (так называемые пейеровы бляшки) и солитарные фолликулы, а затем в регионарные лимфатические узлы. Преодолев лимфатический барьер, возбудитель поступает в кровь. Развивается бактериемия, особенно отчетливо выраженная в течение 1-й недели болезни, когда брюшнотифозную палочку можно выделить из крови (гемокультура). С бактериемией связаны генерализация инфекта и становление иммунитета. Начиная со 2-й недели с помощью реакции агглютинации (реакция Видаля) в крови определяются антитела к возбудителю. С бактериемией связана и элиминация возбудителя, который со 2-й недели болезни выделяется с потом, молоком (у лактирующих женщин), мочой, калом, желчью. В этот период больной особенно заразен. В желчных путях (желчи) бактерии брюшного тифа находят наиболее благоприятные условия существования и усиленно размножаются (бактериохолия). Выделяясь с желчью в просвет тонкой кишки, бактерии вызывают гиперергическую реакцию в сенсибилизированных при первой встрече (заражение) и генерализации инфекта (бактериемия) групповых
лимфатических и солитарных фолликулах, которая завершается некрозом лимфатического аппарата кишки. Доказаны цитолитический эффект сальмонелл в отношении микроворсинок кишечного эпителия и интерцеллюлярный путь их миграции в слизистой оболочке.
Патологическая анатомия. Изменения при брюшном тифе делят на местные и общие.
Местные изменения. Они возникают в слизистой оболочке и лимфатическом аппарате - групповых лимфатических и солитарных фолликулах кишечника. В тех случаях, когда они преобладают в тонкой кишке, говорят об илеотифе, в толстой кишке - о колотифе, в тонкой и толстой кишках - об илеоколотифе. Однако наиболее характерные изменения развиваются в пейеровых бляшках подвздошной кишки (илеотиф). Эти изменения проходят 5 стадий (периодов): мозговидного набухания, некроза, образования язв, чистых язв и заживления. Каждая стадия занимает примерно неделю болезни.
В стадии мозговидного набухания групповые фолликулы увеличиваются, выступают над поверхностью слизистой оболочки, на их поверхности образуются борозды и извилины, что напоминает поверхность мозга (рис. 259). На разрезе они серо-красные, сочные. В основе мозговидного набухания лежит пролиферация моноцитов, гистиоцитов и ретикулярных клеток, которые вытесняют лимфоциты. Эти клетки выходят за пределы групповых фолликулов и слизистой оболочки, проникают в мышечный слой и достигают иногда серозного покрова. Многие из пролиферирую-
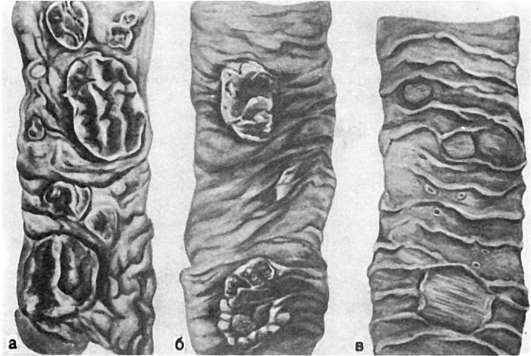 Рис. 259. Брюшной тиф:
Рис. 259. Брюшной тиф:
а - мозговидное набухание групповых фолликулов (так называемых пейеровых бляшек); б - некроз групповых фолликулов; в - чистые язвы
щих клеток, особенно моноциты, превращаются в макрофаги (большие клетки со светлой цитоплазмой), фагоцитирующие брюшнотифозные палочки. Такие макрофаги называют брюшнотифозными клетками, которые образуют скопления, или брюшнотифозные гранулемы (рис. 260). Аналогичные изменения развиваются в солитарных фолликулах. Мозговидное набухание групповых и солитарных фолликулов сочетается с катаральным энтеритом.
В основе стадии некроза групповых фолликулов лежит некроз брюшнотифозных гранулем. Некроз начинается в поверхностных слоях групповых фолликулов и постепенно углубляется, достигая иногда мышечного слоя и даже брюшины (см. рис. 259). Вокруг некротических масс возникает демаркационное воспаление. Омертвевшая ткань имбибируется желчью и приобретает зеленоватую окраску. Такие же изменения наблюдаются и в солитарных фолликулах. В интрамуральных нервных ганглиях отмечаются дистрофические изменения нервных клеток и волокон. Переход в стадию образования язв связан с секвестрацией и отторжением некротических масс. Раньше всего язвы, которые называют «грязными», появляются в нижнем отрезке подвздошной кишки, затем - в вышележащих отделах. В этой стадии появляется опасность внутрикишечных кровотечений, реже - перфорации стенки кишки.
В стадии чистых язв последние меняют свой вид: они расположены по длиннику кишки, края ровные, слегка закругленные, дно чистое, образовано мышечным слоем, реже серозной оболочкой (см. рис. 259). В этой стадии велика опасность перфорации стенки кишки.
Стадия заживления язв завершается образованием на их месте нежных рубчиков; лимфоидная ткань кишки частично или полностью восстанавливается, становится лишь слегка пигментированной.
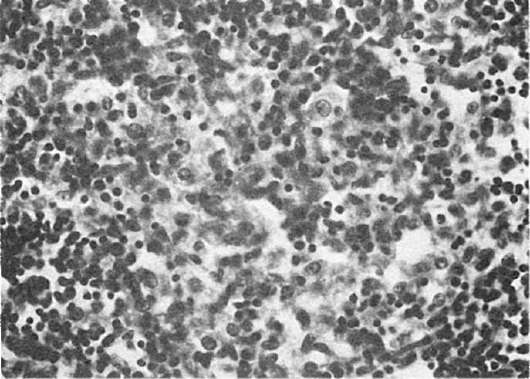 Рис. 260. Брюшной тиф. Гранулема из крупных макрофагальных (брюшнотифозных) клеток при мозговидном набухании групповых фолликулов
Рис. 260. Брюшной тиф. Гранулема из крупных макрофагальных (брюшнотифозных) клеток при мозговидном набухании групповых фолликулов
В лимфатических узлах брыжейки, особенно илеоцекального угла, отмечаются изменения, развивающиеся в той же последовательности, что и в лимфатическом аппарате кишки. Сначала они увеличиваются за счет полнокровия, пролиферации моноцитарных фагоцитов и ретикулярных клеток, вытесняющих лимфоциты. Затем появляются брюшнотифозные гранулемы, происходят их некроз, организация и петрификация некротических масс.
Разграничение местных изменений при брюшном тифе на стадии условно, так как нередко можно видеть одновременно сочетание изменений, характерных для двух-трех стадий. Чем проксимальнее расположены изменения, тем они «моложе», чем дистальнее, ближе к илеоцекальному углу, тем «старее». Судить на основании патологоанатомических данных о стадии брюшного тифа следует по наиболее «старым» изменениям, наблюдаемым в нижнем отделе подвздошной кишки.
Общие изменения. При брюшном тифе имеются как типичные только для него изменения, так и характерные для любого инфекционного заболевания. К первым относятся сыпь, образование брюшнотифозных гранулем в разных органах, ко вторым - гиперпластические процессы в органах лимфатической системы и дистрофические изменения в паренхиматозных органах.
Брюшнотифозная сыпь появляется на 7-11-й день болезни на коже туловища, прежде всего на животе. Она имеет розеолезно-папулезный характер, слегка возвышается над поверхностью кожи и исчезает при давлении. Гистологически главным образом в сосочковом слое кожи находят гиперемию сосудов, лимфоидные воспалительные инфильтраты; эпидермис разрыхлен, с явлениями гиперкератоза (в экзантеме можно обнаружить брюшнотифозные палочки). Образование брюшнотифозных гранулем выражено в селезенке, лимфатических узлах, костном мозге, легких, желчном пузыре, почках.
Иногда характерные кишечные изменения при брюшном тифе уступают внекишечным гранулематозным изменениям, причем из внекишечных очагов поражения высеваются брюшнотифозные палочки. Если эти специфические для брюшного тифа изменения доминируют в легких и развивается своеобразная брюшнотифозная пневмония, говорят о пневмотифе (Ю.М. Лозовский, 1948), если они обнаруживаются в желчных путях при относительно интактном кишечнике - о холанготифе (Абрикосов А.И., 1927).
Селезенка при брюшном тифе, как правило, увеличена в 3-4 раза, капсула напряжена, ткань темно-красного цвета, дает обильный соскоб пульпы. Отмечаются гиперплазия красной пульпы, пролиферация моноцитарных элементов и ретикулярных клеток с образованием брюшнотифозных гранулем. В миокарде, печени, почках находят дистрофические изменения. В ряде случаев развивается холецистит.
Осложнения. Среди кишечных осложнений наиболее часты и опасны внутрикишечные кровотечения и прободение язвы. Кровотечение возникает обычно на 3-й неделе и может быть смертельным. Прободение язвы
обнаруживается чаще на 4-й неделе болезни. В таких случаях находят проникновение брюшнотифозных гранулем в глубокие отделы мышечного слоя кишки и некроз достигает брюшины. Прободение язвы ведет к перитониту. Причиной его могут быть также некротические изменения брыжеечных лимфатических узлов и надрыв капсулы селезенки (при расположении некротизирующихся брюшнотифозных гранулем под капсулой).
Среди внекишечных осложнений наибольшее значение имеют пневмония, гнойный перихондрит гортани, восковидные некрозы прямых мышц живота, остеомиелит, внутримышечные абсцессы.
Пневмония обычно вызывается пневмококком, стафилококком (брюшнотифозная пневмония наблюдается редко). Это очаговая пневмония с поражением нижних долей. Гнойный перихондрит гортани с развитием пролежней у входа в пищевод возникает у ослабленных больных. Восковидный некроз прямых мышц живота - довольно частая находка. Гнойный остеомиелит и внутримышечные абсцессы - поздние осложнения брюшного тифа. Брюшнотифозный сепсис встречается редко, при этом местные (кишечные) изменения могут отсутствовать (typhus sine typho).
Смерть больных брюшным тифом наступает обычно от осложнений (внутрикишечное кровотечение, перитонит, пневмония, сепсис).
Сальмонеллезы
Сальмонеллезы - кишечные инфекции, вызываемые сальмонеллами; относятся к антропозоонозам и встречаются как у человека, так и у многих животных.
Этиология и патогенез. Среди сальмонелл наибольшее значение в патологии человека имеют Salmonella typhimurium, Salmonella enteritidis (Gartneri), Salmonella cholerae suis. Инфекция передается пищевым путем. Источник заражения - больные люди, носители, мясо скота и птицы при несоблюдении правил забоя и хранения, куриные яйца. Патогенез в значительной мере определяется особенностями возбудителя, количеством эндотоксина, освобождающегося при распаде сальмонелл в кишечнике и характеризующегося пирогенным, цитотоксическим и вазопаралитическим действием. В одних случаях развиваются острый гастроэнтерит, резкие сосудистые расстройства, коллапс; в других случаях сальмонеллез подобен брюшному тифу. Сальмонеллез может присоединяться к другим инфекциям (дизентерия, возвратный тиф) и утяжелять их течение.
Патологическая анатомия. Различают 3 формы сальмонеллеза: интестинальную (токсическую), септическую и брюшнотифозную.
Интестинальная форма развивается обычно при пищевом отравлении. Для нее характерна картина острейшего гастроэнтерита, приводящего к резкому обезвоживанию организма. Заболевание сходно с холерой, поэтому его называют домашней холерой (cholera nostras).
Септическая форма отличается от интестинальной тем, что при незначительно выраженных изменениях в тонкой кишке (гиперемия, отек, гиперплазия лимфатического аппарата) имеется гематогенная генерали-
зация возбудителя с образованием во многих органах (легких, головном мозге) метастатических гнойников. Брюшнотифозная форма (паратифы А и В по старой терминологии) напоминает брюшной тиф и вызывается Salmonella paratyphi A и Salmonella Schottmulleri. В кишечнике, лимфатических узлах, селезенке появляются изменения, сходные с наблюдающимися при брюшном тифе, но более слабо выраженные. Поэтому кишечные осложнения (кровотечение, прободение язвы) встречаются редко.
Осложнения. При сальмонеллезах возможны токсико-инфекционньгй шок, гнойные осложнения, дисбактериоз при неадекватном лечении.
Дизентерия
Дизентерия (от греч. dys - расстройство и enteron - кишечник) - острое кишечное инфекционное заболевание с преимущественным поражением толстой кишки и явлениями интоксикации.
Этиология и патогенез. Вызывается группой родственных бактерий - шигелл с нередкой сменой их видов. Путь заражения фекальнооральный. Инкубационный период до 3 сут. Бактерии находят наиболее благоприятные условия для своего развития в толстой кишке. Доказано, что местом жизнедеятельности и размножения шигелл является эпителий
слизистой оболочки толстой кишки (рис. 261), где они недоступны для лейкоцитов, антител, антибиотиков. Цитопатическим действием шигелл на клетки эпителия объясняются деструкция и десквамация последних, развитие десквамативного катара толстой кишки в начальной стадии болезни. С высвобождением энтеротоксина при гибели эпителия осуществляется вазонейропаралитическое его действие (паралич кровеносных сосудов, повреждение интрамуральных нервных ганглиев кишки). Деструкция эпителия слизистой оболочки и паралич кровеносных сосудов кишки, с которым связано усиление экссудации, определяют смену катара фибринозным воспалением и развитием язв при отторжении фибринозных пленок и некротических масс слизистой оболочки. Таким образом, характер морфологических изменений толстой кишки при дизентерии в значительной
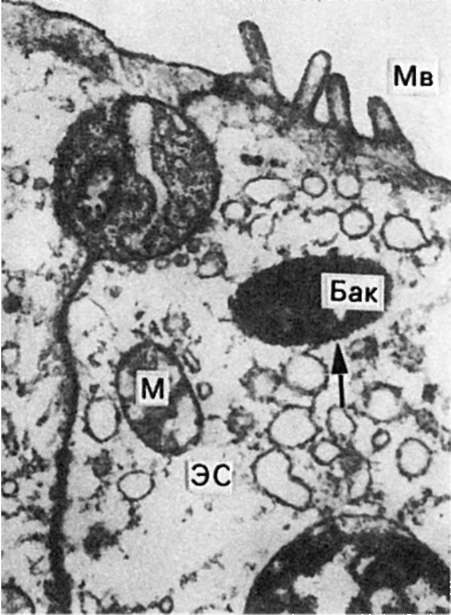 Рис. 261. Дизентерия.
Шигелла (Бак) в эпителиальной клетке кишки; клетка в состоянии глубокой
дистрофии; расширение и вакуолизация канальцев эндоплазматической сети
(ЭС), деструкция митохондрий (М) и микроворсинок (Мв). х8000 (по Такеуши
и др.)
Рис. 261. Дизентерия.
Шигелла (Бак) в эпителиальной клетке кишки; клетка в состоянии глубокой
дистрофии; расширение и вакуолизация канальцев эндоплазматической сети
(ЭС), деструкция митохондрий (М) и микроворсинок (Мв). х8000 (по Такеуши
и др.)
мере объясняется как внутриэпителиальным обитанием шигелл, так и вазонейропаралитическим действием их токсина. Определенное значение имеет и возраст больного.
Патологическая анатомия. При дизентерии наблюдаются изменения местного и общего характера.
Местные изменения. Изменения местного характера развиваются в слизистой толстой кишки, главным образом в прямой и сигмовидной. Степень этих изменений по направлению к слепой кишке убывает. Возникает колит, в развитии которого различают 4 стадии: катарального колита, фибринозного колита, образования язв (язвенного колита) и заживления язв.
Стадия катарального колита (продолжительность 2-3 дня) характеризуется гиперемией и набуханием слизистой оболочки кишки, в которой встречаются поверхностные участки некроза и кровоизлияния. Просвет кишки в связи со спазмом мышечного слоя сужен. Микроскопически обнаруживаются слущивание эпителия, в цитоплазме которого находят шигеллы (рис. 262), гиперемию, отек, кровоизлияния и очаги некроза слизистой оболочки, лейкоцитарные инфильтраты в строме.
В стадии фибринозного, чаще дифтеритического, колита (продолжительность 5-10 дней), которая сменяет катар слизистой оболочки, на вершине ее складок и между складками появляется фибринозная пленка коричнево-зеленого цвета (рис. 263). Стенка кишки утолщена, просвет резко сужен.
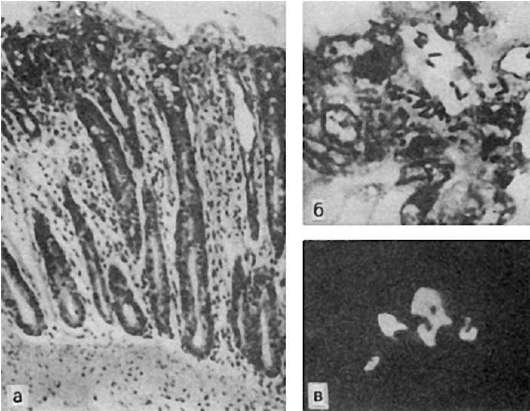 Рис. 262. Дизентерия. Катаральный колит (по М.В. Войно-Ясенецкому):
Рис. 262. Дизентерия. Катаральный колит (по М.В. Войно-Ясенецкому):
а - десквамация покровного эпителия слизистой оболочки, клеточная инфильтрация стромы; б - возбудители дизентерии в эпителии слизистой оболочки; в - люминесценция возбудителей дизентерии после обработки срезов специфической сывороткой
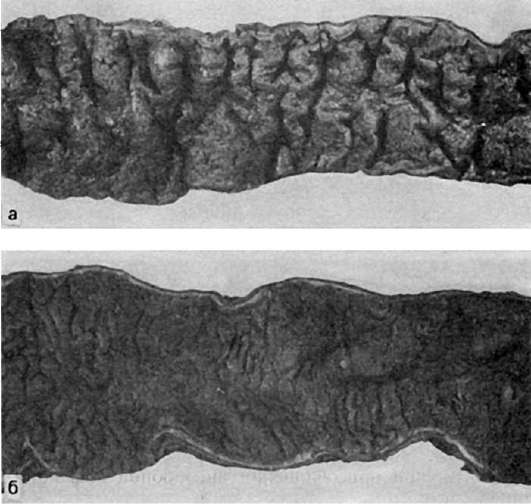 Рис. 263. Дифтеритический (а) и язвенный (б) колит при дизентерии
Рис. 263. Дифтеритический (а) и язвенный (б) колит при дизентерии
При гистологическом исследовании виден проникающий на различную глубину некроз слизистой оболочки, некротические массы пронизаны нитями фибрина.
Слизистая оболочка по периферии некротических очагов, как и подслизистый слой, отечна, инфильтрирована лейкоцитами, с фокусами геморрагии. В нервных приборах кишки - подслизистом (так называемом меисснеровском) и межмышечном (так называемом ауэрбаховом) сплетениях - обнаруживаются дистрофические и некротические изменения (вакуолизация, кариолиз нервных клеток, распад нервных волокон с размножением леммоцитов).
При дифтеритическом воспалении некротические изменения могут прогрессировать; при присоединении анаэробной инфекции в таких случаях дизентерии развивается гангрена стенки кишки (гангренозный колит при дизентерии).
Стадия образования язв, т.е. язвенного колита (см. рис. 263), появляется на 10-12-й день болезни. Язвы возникают прежде всего в прямой и сигмовидной кишках в связи с отторжением фибринозных пленок и некротических масс, имеют неправильные очертания и разную глубину. С образованием язв связана возможность кровотечения и перфорации стенки кишки.
Стадия заживления язв характеризуется процессами регенерации и продолжается в течение 3-4-й недели болезни. Дефекты слизистой обо-
лочки заполняются грануляционной тканью, которая созревает. При незначительных дефектах регенерация может быть полной; при глубокой и распространенной деструкции слизистой оболочки образуются рубцы, приводящие к сужению просвета кишки. Возможно вялое заживление язв, при этом появляются псевдополипы слизистой оболочки. В таких случаях говорят о хронической дизентерии, хотя ряд исследователей понятие хронической дизентерии отвергает, считая такой колит постдизентерийным. Однако у таких больных из краев язв удается высеять дизентерийные бактерии и обнаружить положительную реакцию агглютинации с дизентерийным антигеном.
Классическая схема стадийных изменений слизистой оболочки толстой кишки в ряде случаев нарушается, иногда изменения могут ограничиваться только стадией катарального колита - катаральная дизентерия (абортивная форма). У детей на фоне катарального воспаления слизистой оболочки могут возникать резкие изменения лимфатического аппарата кишки. Происходит гиперплазия клеток солитарных фолликулов, они увеличиваются в размерах и выступают над поверхностью слизистой оболочки (фолликулярный колит). Центральные участки фолликулов могут подвергнуться некрозу и гнойному расплавлению, на поверхности фолликулов появляются язвочки (фолликулярно-язвенный колит).
В регионарных лимфатических узлах при дизентерии возникает воспаление - лимфаденит с явлениями миелоидной метаплазии.
Общие изменения. Каких-либо характерных черт общие изменения не имеют. В селезенке происходит гиперплазия лимфоидных клеток, она увеличивается, но незначительно. В сердце и печени часто наблюдается жировая дистрофия, в печени, кроме того, возможны мелкоочаговые некрозы. В почках нередко наблюдается некроз эпителия канальцев. Часто возникают нарушения минерального обмена, что ведет к появлению известковых метастазов, образованию микро- и макролитов.
Осложнения связаны прежде всего с язвенными изменениями толстой кишки. Это - перфорация (микроперфорация) язвы с развитием парапроктита или перитонита, флегмона кишки, реже - внутрикишечное кровотечение, рубцовые стенозы кишки. Среди внекишечных осложнений встречаются бронхопневмония, пиелит и пиелонефрит, серозные (токсические) артриты, пилефлебитические абсцессы печени, амилоидоз, интоксикация, истощение.
Смерть больных дизентерией наступает от кишечных или внекишечных осложнений.
Иерсиниоз
Иерсиниоз - острое инфекционное заболевание, характеризующееся поражением желудка и кишечника с наклонностью к генерализации процесса и поражением различных органов.
Иерсиниоз относится к зоонозам. В природе существует естественный резервуар заболевания (грызуны, кошки, собаки, свиньи, крупный и
мелкий рогатый скот). Источником заражения могут быть больные иерсиниозом и носители. Чаще болеют дети.
Этиология и патогенез. Возбудитель заболевания - Yersinia enterocolitica. Путь заражения обычно алиментарный через зараженные овощи, фрукты, мясо, молоко. В развитии заболевания выделяют несколько фаз. После заражения инфект преодолевает желудочный барьер, проникает в слизистую оболочку тонкой кишки, вызывает энтерит. Затем иерсинии лимфогенно проникают в мезентериальные лимфатические узлы, где размножаются и накапливаются, - развивается мезентериальный лимфаденит. Далее происходит прорыв бактерий из лимфатической системы в кровь, что ведет к диссеминации инфекции, поражению внутренних органов, интоксикации. Адекватная иммунная реакция на возбудитель обычно ведет к выздоровлению.
Патологическая анатомия. Выделяют 3 клинико-морфологические его формы: абдоминальную (гастроэнтероколит), аппендикулярную и септическую.
Абдоминальная форма может быть представлена гастроэнтероколитом, энтероколитом или энтеритом, реже острым гастритом. Доминирует терминальный катаральный или катарально-язвенный энтерит. Слизистая оболочка терминального отдела подвздошной кишки отечна, просвет ее сужен, в области гиперплазированных групповых лимфоидных фолликулов определяются округлые язвы. Иногда в процесс вовлекается слепая кишка, где обнаруживают изменения типа псевдомембранозного колита. Характерна инфильтрация всех слоев стенки кишки нейтрофилами, мононуклеарными клетками, эозинофилами, плазматическими клетками. В дне язв находят иерсинии и полиморфно-ядерные лейкоциты.
Мезентериальные лимфатические узлы увеличены в размерах, спаяны в пакеты, ткань их инфильтрирована полиморфно-ядерными лейкоцитами, эозинофилами, гистиоцитами; иногда определяются микроабсцессы.
Печень увеличена, гепатоциты подвергаются дистрофическим изменениям, изредка развивается острый гепатит. Селезенка гиперплазирована (масса увеличена в 1,5-2 раза), с большими зародышевыми центрами в лимфоидных фолликулах и редукцией лимфоидной ткани. Очень часты иммунокомплексные поражения сосудов - васкулиты, тромбоваскулиты, фибриноидный некроз. Следствием системных васкулитов является сыпь, которая отмечается у больных иерсиниозом в 95% случаев, иногда гломерулонефрит.
При аппендикулярной форме, которая некоторыми авторами рассматривается как вариант абдоминальной, обнаруживают любые формы острого аппендицита, сочетающегося с терминальным илеитом и брыжеечным мезаденитом. В стенке червеобразного отростка находят обильную инфильтрацию полиморфно-ядерными лейкоцитами, эозинофилами, гистиоцитами, иногда иерсиниозные гранулемы из макрофагов, эпителиоидных клеток и единичных гигантских клеток типа Пирогова-Лангханса; для гранулем характерны кариорексис и гнойное расплавление.
Септическая форма заболевания протекает по типу септицемии; в 50% случаев она заканчивается летально.
Осложнения. Они имеют инфекционно-аллергический характер. В раннем периоде болезни возможны перфорация язв кишечника с развитием перитонита, желтуха, пневмония. В позднем периоде чаще находят полиартрит, узелковую эритему, синдром Рейтера, миокардит. Осложнения пролонгируют течение заболевания, которое может занимать несколько месяцев.
Исход обычно благоприятный, но заболевание может рецидивировать, принимать хронический характер. Смертельный исход отмечается в основном при септической форме.
Холера
Холера (от древнеевр. choul ran - дурная болезнь или греч. chole - желчь и rheo - течь) - острейшее инфекционное заболевание с преимущественным поражением желудка и тонкой кишки. Холера относится к группе карантинных, или конвенционных, инфекций и чрезвычайно контагиозна. Это - строгий антропоноз.
Этиология. Возбудителем является вибрион, выделенный Р. Кохом в 1884 г. Наибольшее значение имеет вибрион азиатской холеры Коха и вибрион Эль-Тор (Эль-Тор - карантинный пункт в Египте, где в 1906 г. был выделен новый тип вибриона, считавшийся ранее условно-патогенным). Вибрион Эль-Тор по сравнению с вибрионом Коха вызывает более легкие формы заболевания, дает меньшую летальность.
Эпидемиология и патогенез. Распространение холеры имеет характер эпидемий и пандемий. За последние 150 лет было 7 пандемий холеры. Седьмая пандемия началась в 1961 г. в Индонезии (Сулавеси), распространившись впоследствии на страны Азии, Европы и Африки. Она связана с вибрионом Эль-Тор, который по сравнению с вибрионом азиатской холеры более устойчив, обитает как в пресной, так и в морской воде и дольше переживает во внешней среде.
Источником заражения является больной холерой или вибриононоситель, резервуаром возбудителя - вода. Заражение энтеральное и происходит обычно при питье инфицированной воды. Инкубационный период длится 3-5 сут. «Щелочелюбивые» вибрионы, преодолев кислотный барьер желудка (у добровольцев холеру удавалось вызвать лишь после нейтрализации желудочного сока), находят оптимальную среду обитания в тонкой кишке. Здесь они размножаются и выделяют экзотоксин (холероген). Под действием экзотоксина эпителий слизистой оболочки секретирует большое количество изотонической жидкости. Обильная секреция жидкости происходит в результате взаимодействия холерогена с ферментными системами клетки; при этом имеет значение блокада «натриевого насоса» клетки, что нарушает обратное всасывание жидкости из просвета кишки. С обильной секрецией жидкости и нарушением обратного ее всасывания связана профузная диарея. В развитии диареи имеет значение
повреждение клеточных и сосудистых мембран, что ведет к повышению тканево-сосудистой проницаемости, причем повреждение мембран связано с наличием у вибриона муциназы (мембранно-фильтрационная теория патогенеза). Профузная диарея приводит к быстрой потере воды и электролитов (натрия, калия, бикарбонатов), а обезвоживание - к гиповолемическому шоку и обменному ацидозу, сгущению крови и гипоксии, нарастающей олигурии и падению температуры тела - алгидный (от лат. algor - холод) период холеры. Прогрессирующий эксикоз и нарушение электролитного баланса играют ведущую роль в возникновении холерной комы.
Патологическая анатомия. В развитии холеры различают 3 стадии (периоды): холерный энтерит, холерный гастроэнтерит и алгидный период.
Холерный энтерит имеет серозный или серозно-геморрагический характер. Слизистая оболочка становится набухшей, отечной и полнокровной; отмечается гиперсекреция бокаловидных клеток, цитоплазматические мембраны которых разрываются и секрет выбрасывается в просвет кишки. На этом фоне появляются единичные или множественные кровоизлияния. Энтерит (особенно вызванный вибрионом Эль-Тор) при своевременном лечении нередко заканчивается выздоровлением, однако он может смениться вторым периодом болезни - холерным гастроэнтеритом.
При холерном гастроэнтерите явления энтерита нарастают, эпителиальные клетки вакуолизируются и теряют микроворсинки; некоторые из них погибают и десквамируются. К энтериту присоединяются серозный или серозно-геморрагический гастрит. Прогрессирующее обезвоживание в этот период связано не только с диареей, но и рвотой.
В алгидный период морфологические изменения выражены наиболее отчетливо (рис. 264). В тонкой кишке отмечаются резкое полнокровие, отек, некроз и слущивание эпителиальных клеток ворсин, инфильтрация слизистой оболочки лимфоцитами, плазматическими клетками, нейтрофилами, очаги кровоизлияний. Петли кишки растянуты, в просвете их содержится большое количество (3-4 л) бесцветной жидкости без запаха, которая имеет вид рисового отвара. В этой жидкости удается обнаружить вибрионы. Серозная оболочка кишки сухая, с точечными кровоизлияниями, матовая, окрашена в розово-желтый цвет. Между петлями тонкой кишки обнаруживается прозрачная, липкая, тянущаяся в виде нитей слизь.
Проявления эксикоза ярко выражены и обнаруживаются как при осмотре, так и при внутреннем исследовании трупа. Трупное окоченение наступает быстро и сохраняется в течение нескольких дней. В результате этого мышцы резко контурированы («поза гладиатора»). Кожа, как правило, сухая, морщинистая, особенно на пальцах рук («руки прачки»). Вследствие быстро наступающего трупного окоченения она иногда напоминает гусиную. Слизистые оболочки, подкожная клетчатка, мышцы сухие, причем мышцы становятся темно-красными. Кровь в венах густая
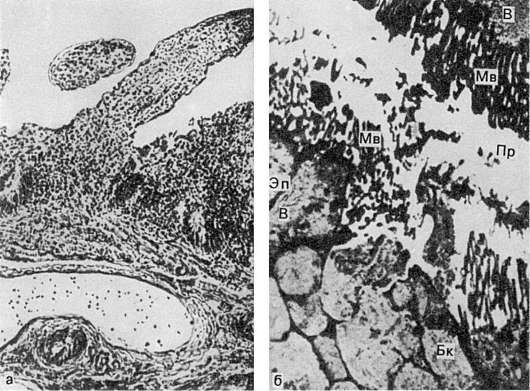 Рис. 264. Холера. Энтерит (энтеробиопсия):
Рис. 264. Холера. Энтерит (энтеробиопсия):
а - полнокровие, отек, слущивание эпителиальных клеток ворсин, клеточная инфильтрация стромы (препарат А.К. Агеева); б - гомогенизация цитоплазмы клеток кишечного эпителия (Эп), множественные вакуоли (В); разрушение и слущивание микроворсинок (Мв); Бк - гиперсекретирующая бокаловидная клетка. Пр - просвет кишки. х10 000 (по А.А. Авакяну и др.)
и темная. Серозные оболочки также сухие, покрыты липкой, прозрачной слизью, которая тянется в виде нитей. С обезвоживанием связаны изменения многих внутренних органов - селезенки, печени, желчного пузыря, почек, миокарда, головного мозга. Селезенка уменьшается, капсула ее морщиниста, фолликулы атрофичны, отмечается гемосидероз пульпы. В печени развиваются дистрофия гепатоцитов и очаговые некрозы паренхимы; желчеобразование нарушается. Желчный пузырь растянут прозрачной светлой желчью («белая желчь»). В почках отмечают некроз эпителия канальцев главных отделов нефрона, т.е. изменения, наблюдаемые при олигурии или острой почечной недостаточности. В миокарде, головном мозге имеются дистрофические и некробиотические изменения.
Осложнения. Выделяют специфические и неспецифические осложнения холеры. К специфическим осложнениям относятся холерный тифоид и постхолерная уремия. Холерный тифоид развивается как гиперергическая реакция на повторное поступление вибрионов. Не исключено значение и патогенной флоры кишечника. Клинико-морфологические проявления алгидного периода при тифоиде исчезают. Основные изменения наблю-
даются в толстой кишке и представлены дифтеритическим колитом, похожим на дизентерийный. Селезенка увеличивается, помимо гиперплазии пульпы в ней находят инфаркты. В печени появляются множественные различной величины очаги некроза в связи с тромбозом междольковых сосудов. Изменения почек характеризуются подострим, экстракапиллярным гломерулонефритом или некрозом эпителия почечных канальцев. Эти изменения обусловливают развитие уремии при холерном тифоиде.
Постхолерная уремия - своеобразное осложнение посталгидной холеры, при котором в корковом веществе почек появляются множественные инфарктоподобные некрозы.
К неспецифическим осложнениям холеры относятся пневмония, абсцессы, флегмона, рожа, сепсис.
Смерть больных холерой обычно наступает в алгидный период от обезвоживания, комы, уремии, интоксикации. В настоящее время в связи с ранним и адекватным лечением (введение воды и электролитов, прием антибиотиков) летальность при холерном алгиде значительно снижена.
Возможна смерть и от осложнений холеры, среди которых наиболее частым является уремия.
Чума
Чума (pestis) - острейшее инфекционное заболевание из группы карантинных (конвенционных) болезней.
Этиология. Вызывается палочкой чумы (Yersinia pestis), которая является аэробом и факультативным анаэробом, выделяет фибринолизин и гиалуронидазу и персистирует в полиморфно-ядерных лейкоцитах и макрофагах. Антигены ее близки антигенам тканей человека.
Эпидемиология и патогенез. Для чумы характерны эпидемии и пандемии с огромной летальностью. Однако встречаются спорадические случаи и доброкачественные формы. Чума - типичный антропозооноз. Источником заражения и резервуаром возбудителя чумы являются дикие животные, главным образом грызуны (суслики, тарбаганы, тушканчики, белки, крысы и др.), из домашних животных - кошки, верблюды. Среди грызунов нередки эпидемии (энзоотии) чумы, которые имеют характер геморрагической септицемии. Возможны два пути заражения человека: чаще от больных грызунов при укусе блох (бубонная или кожно-бубонная чума), реже - воздушно-капельным путем от больного человека с чумной пневмонией (первично-легочная чума). Инкубационный период длится от нескольких часов до 6 сут.
От места заражения при укусе блохи возбудитель распространяется лимфогенно, в регионарном лимфатическом узле развивается воспаление - лимфаденит (первичный чумной бубон первого порядка). При дальнейшем лимфогенном распространении появляются первичные бубоны второго, третьего порядка и т.д. Однако независимо от формы чумы для нее наиболее характерна гематогенная генерализация возбудителя. Заболевание течет, как сепсис (геморрагическая септицемия), что объясня-
ют недостаточностью при чуме фагоцитарной реакции (эндоцитобиоз) и гуморального иммунитета (антитела вырабатываются крайне медленно и не достигают высоких титров). Возможно, это связано с тем, что палочка чумы обладает антигенной близостью к клеткам человеческого тела.
С особенностями иммунитета (подавление фагоцитоза) и возбудителя (наличие в палочке чумы гиалуронидазы и фибринолизина) связаны также характер и динамика тканевых изменений - серозно-геморрагическое воспаление, сменяемое геморрагически-некротическим и гнойным, как реакция на некроз.
Патологическая анатомия. Различают бубонную, кожно-бубонную (кожную), первично-легочную и первично-септическую формы чумы.
Бубонная чума характеризуется увеличением регионарных по отношению к воротам инфекции лимфатических узлов (чаще - паховые, реже - подмышечные, шейные). Такие лимфатические узлы имеют название первичных чумных бубонов первого порядка. Они могут быть единичными (рис. 265) или множественными. Бубоны достигают 5-8 см в диаметре; лимфатические узлы спаяны, тестоватой консистенции, неподвижны, на разрезе темно-красного цвета, с очагами некроза. Ткань, окружающая бубоны, отечна. При микроскопическом исследовании определяется картина острейшего серозно-геморрагического лимфаденита: ткань лимфатического узла пропитана кровью и серозной жидкостью, в которой содержится масса микробов, отмечается пролиферация ретикулярных клеток. На этом фоне появляются очаги некроза, лимфаденит становится геморрагически-некротическим. Как реакция на некроз развиваются гнойное воспаление и расплавление ткани лимфатического узла, появляются язвы. При благоприятном исходе язвы рубцуются. Однако чаще первичные бубоны первого порядка становятся источником лимфогенного и гематогенного распространения инфекции.
При лимфогенном распространении появляются новые бубоны (первичные бубоны второго, третьего порядка и т.д.), где отмечаются те же
 Рис. 265. Чума. Бубон правого плеча
Рис. 265. Чума. Бубон правого плеча
морфологические изменения, что и в регионарном лимфатическом узле. Гематогенное распространение ведет к быстрому развитию чумной бактериемии и септицемии, которые проявляются сыпью, множественными геморрагиями, гематогенным поражением лимфатических узлов, селезенки, вторичной чумной пневмонией, дистрофией и некрозом паренхиматозных органов.
Сыпь может быть представлена пустулами, папулами, эритемой, но с обязательными геморрагическим и некротическим компонентами, нередко с образованием язв. Множественные геморрагии отмечаются как в серозных, так и слизистых оболочках. При гематогенном поражении лимфатических узлов появляются вторичные бубоны (серозно-геморрагический, геморрагически-некротический лимфаденит). Селезенка септическая, резко увеличена (в 2-4 раза), дряблая, дает обильный соскоб пульпы, с очагами некроза и лейкоцитарной реакцией на некроз. Вторичная чумная пневмония, развивающаяся в результате гематогенного (эмболического) заноса инфекции, имеет очаговый характер. В легких в связи с серозногеморрагическим воспалением появляются множественные темно-красные очаги с участками некроза, где обнаруживается огромное количество возбудителя. Больные вторичной чумной пневмонией могут быть источником воздушно-капельной инфекции, т.е. возникновения первично-легочной чумы. Дистрофические и некротические изменения касаются многих паренхиматозных органов - сердца, печени, почек и т.д.
Кожно-бубонная (кожная) форма чумы отличается от бубонной тем, что при ней, помимо бубона, развиваются изменения в месте заражения, т.е. развивается первичный аффект. Он представлен «чумной фликтеной» (пузырек с серозно-геморрагическим содержимым) либо чумным геморрагическим карбункулом. Между первичным аффектом и бубоном появляется лимфангит. На месте карбункула отмечаются отек, уплотнение кожи, которая становится темно-красной; на разрезе видно кровянистое пропитывание всех слоев кожи, очаги некроза, окруженные скоплениями лейкоцитов. В дальнейшем карбункул изъязвляется. Развивается септицемия с теми же изменениями в органах, что и при бубонной чуме.
Первично-легочная чума чрезвычайно контагиозна. Продолжительность заболевания 2-3 дня. Возникает долевая пневмония, как правило, поражена плевра - плевропневмония. На разрезе ткань легкого серо-желтая, плеврит серозно-геморрагический. В начале заболевания отмечается полнокровие ткани, в просвете альвеол содержится серозно-геморрагический экссудат; в дальнейшем присоединяются стазы, кровоизлияния, очаги некроза и вторичного нагноения. Выражены явления тяжелой интоксикации. Во внутренних органах, слизистых оболочках, коже обнаруживаются множественные кровоизлияния.
Первично-септическая чума характеризуется картиной сепсиса без видимых входных ворот инфекции. Течение болезни крайне тяжелое.
Для установления диагноза чумы у секционного стола обязательны бактериоскопическое и последующее бактериологическое исследование с высевом культуры палочки чумы, а также проверка диагноза с помощью
биологического опыта - введение материала, взятого на вскрытии, животным (в случае чумы смерть животных наступает на 3-6-й день опыта от геморрагической септицемии). При вскрытии трупов соблюдаются особые меры предосторожности.
Осложнения. При чуме они обычно смертельны. При бубонной, кожнобубонной и первично-септической формах чумы больные умирают от септицемии или кахексии - чумного маразма, при первично-легочной чуме - от интоксикации или легочных осложнений.
Туляремия
Туляремия - инфекционное природно-очаговое заболевание из группы бактериальных антропозоонозов, протекающее остро или хронически.
Этиология. Заболевание вызывается Francisella tularense, открытой Г. Мак-Коем и Ч. Чепином (1912) на берегах озера Туларе в Калифорнии, откуда и произошло его название.
Эпидемиология и патогенез. Резервуаром возбудителя являются грызуны (главным образом водяные крысы, зайцы, дикие кролики, белки, полевые мыши), среди которых периодически появляются чумоподобные эпидемии. Передается туляремия от животных контактным, воздушнокапельным, водным и пищевым путем, а также через кровососущих насекомых (клещи). Заражение от больных людей практически не встречается. Болезнь имеет обычно профессиональный характер и встречается в виде промысловых эпидемий у охотников. Возможны спорадические случаи. Инкубационный период 3-8 сут. Патогенез туляремии имеет много общего с чумой («доброкачественная чума»). В месте внедрения возбудителя может возникать первичный аффект (пустула, изъязвление). Однако обычно первичный аффект не возникает, бактерии лимфогенно достигают регионарных лимфатических узлов (чаще подмышечных или паховых), где развивается воспаление, образуются первичные туляремийные бубоны. Распространяется инфекция лимфогенно и гематогенно, но генерализация инфекции при туляремии происходит на фоне иммунных реакций, о чем свидетельствует раннее формирование туляремийных гранулем.
Патологическая анатомия. Различают бубонную, легочную и тифоидную формы туляремии. При бубонной форме могут быть выражены все компоненты первичного туляремийного комплекса, но особенно они характерны для язвенно-бубонного варианта этой формы. На месте внедрения инфекта (обычно на пальцах правой руки) появляется пустула, а затем язва. При гистологическом исследовании, помимо некроза эпидермиса, в дерме обнаруживаются туляремийные гранулемы. Они состоят из эпителиоидных, лимфоидных, гигантских клеток, полиморфно-ядерных лейкоцитов; в центре гранулем определяется некроз. Туляремийные гранулемы напоминают туберкулезные и отличаются от них лишь наклонностью к нагноению. В туляремийных бубонах, которые представляют собой увеличенные и спаянные лимфатические узлы, образуются гранулемы
описанного выше строения, очаги некроза и нагноения. Если нагноение выражено резко, появляются свищи, длительно не заживающие язвы, на месте которых образуются рубцы. Заболевание принимает в таких случаях хроническое течение. При генерализации процесса гранулемы и очаги нагноения появляются в разных органах: селезенке, печени, костном мозге, легких, эндокринных органах. Селезенка при этом увеличивается и напоминает септическую. При хроническом течении заболевания в тканях находят туляремийные гранулемы и склероз.
Легочная форма туляремии (при воздушно-капельном заражении) характеризуется первичной туляремийной пневмонией и лимфаденитом регионарных лимфатических узлов. Очаги уплотнения в легком напоминают очаги творожистого некроза при туберкулезе. В этих очагах обнаруживают скопления серозно-фибринозного или серозно-геморрагического экссудата с участками некроза, а также гранулематоз. В лимфатических узлах также определяются гранулемы, очаги некроза и нагноения.
Тифоидная форма характеризуется септицемией с множественными геморрагиями в органах без местных кожных изменений и изменений лимфатических узлов. В таких случаях лишь бактериологическое исследование и биологический опыт (заражение животных материалом от трупа) позволяют поставить диагноз.
Смерть при туляремии чаще наступает при тифоидной (сепсис) и легочной (пневмония) формах.
Бруцеллез
Бруцеллез - инфекционное заболевание из группы бактериальных антропозоонозов, имеющее острое, подострое и хроническое течение.
Этиология. В человеческой патологии бруцеллез равнозначен мальтийской лихорадке, или болезни Банга. Заболевание и возбудитель - Brucella - названы по имени Д. Брюса, нашедшего в 1866 г. в козьем молоке возбудитель мальтийской лихорадки (Brucella melitensis), или козье-овечий тип бруцеллы. В ветеринарии бруцеллез отождествляют с инфекционным абортом крупного рогатого скота и свиней. Возбудитель аборта крупного рогатого скота (Brucella abortus), или коровий тип бруцеллы, открыт в 1897 г. Б. Бангом, а возбудитель аборта свиней (Brucella suis), или свиной тип бруцеллы, - в 1914 г. Дж. Траумом. Все три вида возбудителя, которые объединены в настоящее время в одну группу бруцелл, патогенны для человека.
Эпидемиология и патогенез. При заражении человека бруцеллой коровьего или свиного типа чаще наблюдается спорадический бруцеллез, а бруцеллой козье-овечьего типа - эпидемический. Заражение происходит через кожу, слизистые оболочки дыхательных путей или алиментарным путем при употреблении молока и молочных продуктов. Заболевание имеет чаще всего профессиональный характер (болеют работники животноводства). Инкубационный период длится 1-3 нед. В месте входных ворот инфекции изменения не развиваются. Возбудитель накапливается в
регионарных лимфатических узлах, после чего происходит гематогенная его генерализация. Заболевание протекает на фоне сенсибилизации организма бруцеллами, причем иммунологический ответ в разные периоды болезни выражен различно.
Патологическая анатомия. Изменения при бруцеллезе в острой, подострой и хронической стадиях различны.
Острая стадия характеризуется острым началом и септическим течением (1-2 мес). Для нее характерна гиперергическая реакция в ответ на генерализацию инфекции. Эта реакция проявляется увеличением селезенки, печени, лимфатических узлов в связи с гиперплазией лимфоидных и эндотелиальных элементов, пролиферативными васкулитами с тромбозом и явлениями повышенной сосудистой проницаемости. Развивается геморрагический диатез. В паренхиматозных органах появляются дистрофические изменения и серозное воспаление.
В подострой стадии (3-4-е месяцы болезни) преобладают реакции гиперчувствительности замедленного типа, в различных органах появляются бруцеллезные гранулемы. Они состоят из эпителиоидных и гигантских клеток типа Пирогова-Лангханса с примесью плазматических клеток и эозинофилов. В бруцеллезной гранулеме в отличие от туберкулезной, которую она напоминает, много сосудов, эпителиоидные клетки располагаются беспорядочно, а центральный некроз развивается редко. Помимо гранулематоза для этой стадии характерно развитие аллергического продуктивно-деструктивного васкулита, который имеет системный характер. При преобладании сосудистых изменений в том или ином органе наблюдаются локальные проявления бруцеллеза. Наиболее часто поражаются печень (гепатит), сердце (полипозно-язвенный эндокардит, продуктивный миокардит), головной мозг и его оболочки (энцефаломиелит, экссудативно-продуктивный менингит), почки (гломерулонефрит). В селезенке, как правило, отмечаются гиперплазия пульпы, образование гранулем, что ведет к ее увеличению.
Хроническая стадия наблюдается в случаях длительного (более года) течения болезни. Для нее характерны выраженная продуктивная реакция с образованием гранулем, васкулиты, дистрофия, атрофия и склероз паренхиматозных органов. При снижении резистентности организма хронический бруцеллез протекает как затяжной сепсис и сопровождается развитием кахексии.
В этой стадии отчетливо выражены локальные (органные) поражения, поэтому различают несколько клинико-морфологических форм хронического бруцеллеза: сердечно-сосудистую, нервную (нейробруцеллез), гепатолиенальную, урогенитальную и костно-суставную.
При сердечно-сосудистой форме развивается полипозно-язвенный эндокардит аортальных клапанов, напоминающий изменения при бактериальном (затяжном септическом) эндокардите. С клапанных наложений высевают бруцеллы. Эндокардит сочетается с продуктивным миокардитом. В строме миокарда появляются гранулемы, а в разветвлениях ве-
нечных артерий - продуктивное воспаление, тромбоз (тромбоваскулит). При длительном течении развиваются аортальный порок сердца, кардиосклероз.
Нервная форма (нейробруцеллез) характеризуется менингоэнцефалитом, в основе которого лежит продуктивно-деструктивный васкулит с глиальной реакцией. В тех случаях, когда присоединяется тромбоз сосудов, появляются очаги размягчения мозга, кровоизлияния, кисты.
При гепатолиенальной форме преобладают изменения печени и селезенки с исходом в цирроз печени и спленомегалию, сопровождающиеся желтухой и геморрагическим диатезом.
Для урогенитальной формы характерно развитие специфического орхита и эпидидимита с исходом в атрофию яичек и их придатков (бруцеллезные оофориты наблюдаются редко).
При костно-суставной форме гранулематозный процесс преобладает в мышцах, сухожилиях, апоневрозах, в капсуле и синовиальной оболочке суставов, в костном мозге. Развиваются остеомиелит трубчатых и плоских костей, периоститы и артриты с деструкцией костей и суставов. Возможна и смешанная форма хронического бруцеллеза.
Смерть в острой стадии бруцеллеза может наступить от сепсиса. В подострой и хронической стадиях она обусловлена локальными поражениями.
Сибирская язва
Сибирская язва - острое инфекционное заболевание из группы бактериальных антропозоонозов.
Этиология. Заболевание вызывается спороносной и устойчивой во внешней среде сибиреязвенной палочкой (Вас. anthracis), которая впервые выделена в чистой культуре Р. Кохом (1876).
Эпидемиология и патогенез. Помимо человека, болеют преимущественно домашние животные (лошадь, крупный и мелкий рогатый скот). Заражение человека от больных животных происходит различными путями. Если заражение осуществляется через кожу, возникает кожная форма, алиментарным путем - кишечная форма, а при вдыхании воздуха, содержащего споры возбудителя сибирской язвы, - первично-легочная форма заболевания. Инкубационный период составляет 2-3 сут. Болезнь имеет выраженный профессиональный характер. После проникновения в организм сибиреязвенная бактерия образует капсулу, что препятствует фагоцитозу и становлению иммунитета. В месте внедрения возбудитель вызывает отрицательный лейкотаксис и развитие серозно-геморрагического воспаления. Распространение инфекции сначала лимфогенное с накоплением инфекта в регионарных лимфатических узлах, затем гематогенное, что ведет к бактериемии и сепсису.
Патологическая анатомия. Различают кожную, кишечную, первичнолегочную и первично-септическую формы сибирской язвы.
Кожная форма встречается наиболее часто. На месте внедрения возбудителя (лицо, шея, конечности, реже туловище) появляется небольшое красное пятно, в центре которого образуется пузырек с серозно-геморрагической жидкостью. Вскоре центральная часть его некротизируется, становится черной, похожей на уголь, - образуется сибиреязвенный карбункул. В его основе лежит острейшее серозногеморрагическое воспаление. В отечных тканях, окружающих карбункул, определяется огромное число бактерий, причем явления фагоцитоза отсутствуют, лейкоцитов в экссудате крайне мало. Почти одновременно с карбункулом развивается регионарный серозно-геморрагический лимфаденит. Лимфатические узлы резко увеличены, на разрезе темно-красного цвета. Отмечаются резкое полнокровие, отек и геморрагическое пропитывание их ткани, в которой находят огромные скопления микробов. Рыхлая клетчатка вокруг лимфатических узлов также отечна, с участками геморрагии. В большинстве случаев кожная форма заканчивается выздоровлением. Однако в четверти случаев развивается сибиреязвенный сепсис.
Конъюнктивальная (форма как разновидность кожной возникает при попадании спор в конъюнктиву и сопровождается серозно-геморрагическим воспалением тканей глаза (офтальмит), отеком окружающей его клетчатки.
При кишечной форме болезни в нижнем отделе подвздошной кишки появляются обширные участки геморрагической инфильтрации и язвы, развивается серозно-геморрагическое воспаление кишки. В лимфатических узлах брыжейки также находят картину серозно-геморрагического воспаления, которое распространяется на окружающую их клетчатку. Лимфатические узлы, как и брыжейки, отечны, пропитаны кровью. В брюшной полости накапливается серозно-геморрагический выпот. Как правило, кишечная форма осложняется сепсисом.
Первично-легочная форма характеризуется геморрагическим трахеитом, бронхитом и серозно-геморрагической очаговой или сливной пневмонией. Лимфатические узлы корней легких увеличены, отечны, с очагами кровоизлияний, что связано с серозно-геморрагическим воспалением. Первично-легочная форма, как правило, осложняется сепсисом.
Для первично-септической формы характерны общие проявления инфекции при отсутствии местных изменений. Эти общие проявления однозначны как при первичном сибиреязвенном сепсисе, так и при вторичном, осложняющем кожную, кишечную или первично-легочную форму заболевания. При вскрытии умерших от сибиреязвенного сепсиса находят увеличенную селезенку, она дряблая, на разрезе темно-вишневого цвета, почти черная, дает обильный соскоб пульпы. В мазках с поверхности разреза селезенки обнаруживают огромное число сибиреязвенных палочек. Особенно характерно развитие геморрагического менингоэнцефалита (рис. 266). Мягкие мозговые оболочки на своде и основании мозга отечны, пропитаны кровью, имеют темно-красный цвет («красный чепец»). Картина напоминает травматическое повреждение мозга.
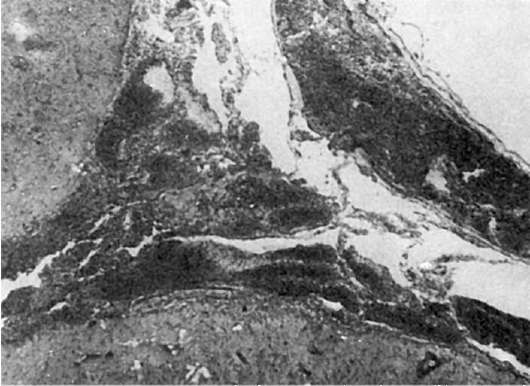 Рис. 266. Сибирская язва. Геморрагический менингоэнцефалит. Мягкая мозговая оболочка пропитана кровью
Рис. 266. Сибирская язва. Геморрагический менингоэнцефалит. Мягкая мозговая оболочка пропитана кровью
При гистологическом исследовании обнаруживают серозно-геморрагическое воспаление оболочек и ткани мозга с разрушением стенок мелких сосудов, разрывом их, скоплением в просвете сосудов огромного числа сибиреязвенных микробов. «Заселение» сосудов (капилляров, артериол) сибиреязвенными бактериями наблюдается повсеместно, а не только в головном мозге и его оболочках.
Смерть больных сибирской язвой наступает от сепсиса. На вскрытии диагноз сибирской язвы должен быть подтвержден результатами бактериоскопического исследования.
Возвратный тиф
Возвратный тиф (typhus recurrens) - острое инфекционное заболевание, характеризуется острым началом, регулярными приступами лихорадки, интоксикацией, головными и мышечными болями, гепатолиенальным синдромом.
Этиология и патогенез. Вызывается спирохетой возвратного тифа (Borellia recurrentis), которую в 1873 г. обнаружил О. Обермейер в крови больных. Возбудитель размножается в клетках системы моноцитарных фагоцитов, его эндотоксин обладает нейротропным (ЦНС) и вазопаралитическим действием. Возвратный тиф передается от человека человеку через укусы насекомых, чаще вшей, у которых спирохета размножается в полостях тела и гемолимфе и не выделяется в окружающую среду. Внедрение спирохет происходит при расчесах, сопровождающихся раздавливанием вши. Инкубационный период от 3 до 30 дней. В конце его возбудитель попадает в кровь, где высвобождается эндотоксин. Во время
приступов лихорадки спирохеты свободно циркулируют в крови, а затем исчезают, причем те из них, которые обнаруживаются в крови при очередном приступе, отличаются по своим антигенным свойствам. Основное значение в возврате приступов лихорадки имеет персистенция возбудителя в макрофагах. Иммунитет после перенесенного возвратного тифа стойкий и длительный.
Патологическая анатомия. Изменения при возвратном тифе изучены главным образом отечественными исследователями (Никифоров М.Н., 1887; Войно-Ясенецкий М.В., 1964). Наиболее характерные изменения возникают в селезенке. Она увеличивается, масса ее достигает 400-600 г, консистенция плотная, капсула напряжена, иногда покрыта фибринозным налетом; в редких случаях наблюдаются разрывы селезенки с массивным кровотечением. В пульпе появляются мелкие серо-белые или желтые очажки, которые хорошо видны на разрезе. Под капсулой обнаруживаются инфарктоподобные очаги некроза, обусловленные поражением сосудов (некроз стенки, тромбоз).
При микроскопическом исследовании отмечается гиперплазия фолликулов селезенки с распадом лимфоцитов и замещением их нейтрофилами. Особенно отчетливо эти изменения выражены в конце приступа, когда происходит фагоцитоз спирохет. Очаги некроза фолликулов селезенки называют милиарными некрозами (см. рис. 44). В дальнейшем в участках некроза фолликулов происходит полная регенерация лимфоидной ткани или развиваются рубчики.
В печени и почках наблюдаются дистрофические изменения, иногда кровоизлияния. В миокарде находят дистрофию мышечных волокон и пролиферацию клеток стромы. В стенках мелких сосудов разных органов встречаются деструктивные изменения.
Осложнения. Осложнением возвратного тифа, ведущим часто к гибели больных, является разрыв селезенки. У истощенных больных наблюдаются пневмония, перихондриты ребер. При присоединении сальмонеллеза болезнь приобретает характер сепсиса с появлением множества гнойничков в почках, развитием желтухи и т.д.
Туберкулез
Туберкулез - хроническое инфекционное заболевание, при котором могут поражаться все органы человека, но чаще легкие.
Туберкулез продолжает оставаться достаточно распространенным заболеванием. Во всем мире ежегодно заболевают туберкулезом 2-3 млн, а умирает 3-5 млн человек; общее количество больных достигает 15- 20 млн, причем половина из них старше 45 лет. 75% всех больных и умерших от туберкулеза приходятся на развивающиеся страны Азии, Африки и Южной Америки, где туберкулез должен быть отнесен к эпидемическим заболеваниям без тенденции к уменьшению. Борьбу с туберкулезом осуществляет ВОЗ в порядке международного сотрудничества.
Туберкулез имеет ряд особенностей, отличающих его от других инфекций.
Они представлены: 1) убиквитарностью (от лат. ubique - повсюду) инфекции в эпидемиологическом, клиническом и морфологическом отношении; 2) двуликостью туберкулеза, который в зависимости от соотношения иммунитета и аллергии может быть проявлением как инфицированности, так и болезни; 3) полиморфизмом клинико-морфологических проявлений; 4) хроническим волнообразным течением - чередованием вспышек и ремиссий заболевания.
Этиология и патогенез. Вызывает туберкулез микобактерия туберкулеза, открытая Кохом в 1882 г. Различают 4 типа микобактерий: человеческий, бычий, птичий и холоднокровных. Для человека патогенны два первых типа. Для микобактерий туберкулеза характерны: оптимальный рост в условиях большого насыщения тканей кислородом и вместе с тем возможность роста при его отсутствии (факультативный анаэроб); крайне выраженная изменчивость - ветвистые, коккообразные, L-формы, которые под влиянием химиопрепаратов могут терять клеточную стенку и длительно персистировать в организме.
Патогенез туберкулеза сводится к проникновению микобактерий в организм и взаимодействию с ним, его тканями и органами. Возникновение, течение и исход туберкулеза в значительной степени обусловлены иммунным состоянием организма, его реактивностью. Реактивность определяет необычное разнообразие клинико-морфологических проявлений туберкулеза, что составляет одну из ярких его особенностей как болезни и создает большие трудности в клинической диагностике.
Патологическая анатомия. Различают три основных вида клиникоморфологических проявлений туберкулеза: первичный, гематогенный и вторичный туберкулез.
Первичный туберкулез
Первичный туберкулез характеризуется: 1) развитием заболевания в период инфицирования, т.е. при первой встрече организма с инфектом; 2) сенсибилизацией и аллергией, реакциями гиперчувствительности немедленного типа; 3) преобладанием экссудативно-некротических изменений; 4) наклонностью к гематогенной и лимфогенной (лимфожелезистой) генерализации; 5) параспецифическими реакциями в виде васкулитов, артритов, серозитов и т.д.
Как правило, путь заражения аэрогенный, возможен и алиментарный путь. Болеют преимущественно дети, но в настоящее время в связи с успешной профилактикой туберкулеза у детей первичный туберкулез наблюдается у подростков и взрослых.
Патологическая анатомия. Морфологическим выражением первичного туберкулеза является первичный туберкулезный комплекс (схема XXIV). Он состоит из трех компонентов (рис. 267): очага поражения в органе - первичного очага или аффекта, туберкулезного воспаления отводящих лимфатических сосудов - лимфангита и туберкулезного воспаления регионарных лимфатических узлов - лимфаденита.
Схема XXIV. Варианты течения первичного туберкулеза
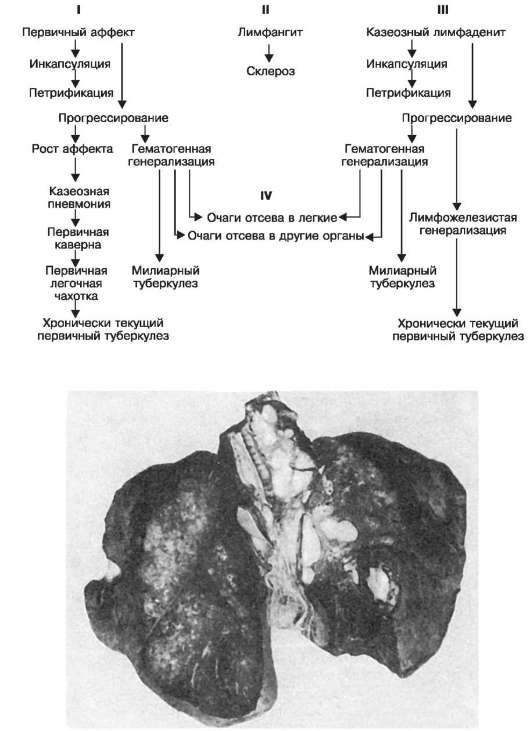 Рис. 267. Первичный туберкулезный комплекс. Первичный аффект в нижней доле правого легкого, туберкулезный лимфангит и казеозный лимфаденит
Рис. 267. Первичный туберкулезный комплекс. Первичный аффект в нижней доле правого легкого, туберкулезный лимфангит и казеозный лимфаденит
При аэрогенном заражении в легких первичный туберкулезный очаг (аффект) возникает субплеврально в наиболее хорошо аэрируемых сегментах, чаще правого легкого - III, VIII, IX, X (особенно часто в III). Он представлен фокусом экссудативного воспаления, причем экссудат быстро подвергается некрозу. Образуется очаг казеозной пневмонии, окруженный зоной перифокального воспаления. Размеры аффекта различны: иногда это альвеолит, едва различимый микроскопически, но чаще воспаление охватывает ацинус или дольку, реже - сегмент и в очень редких случаях - всю долю. В казеозных массах первичного аффекта длительное время сохраняются эластические и аргирофильные волокна каркаса легкого. Постоянно наблюдается вовлечение в воспалительный процесс плевры с развитием фибринозного или серозно-фибринозного плеврита.
Очень быстро специфический воспалительный процесс распространяется на прилежащие к первичному очагу лимфатические сосуды - развивается туберкулезный лимфангит. Он представлен лимфостазом и формированием по ходу лимфатических сосудов в периваскулярной отечной ткани туберкулезных бугорков. Образуется как бы дорожка от первичного очага к прикорневым лимфатическим узлам.
В дальнейшем воспалительный процесс довольно быстро переходит на регионарные бронхопульмональные, бронхиальные и бифуркационные лимфатические узлы, в которых развивается специфический воспалительный процесс с быстро наступающим казеозным некрозом. Возникает тотальный казеозный туберкулезный лимфаденит. Лимфатические узлы увеличиваются в несколько раз и на разрезе представлены казеозными массами. Изменения в регионарных лимфатических узлах всегда более значительны по сравнению с первичным аффектом.
В клетчатке средостения, прилежащей к казеозно-измененным лимфатическим узлам, развивается выраженное в той или иной степени перифокальное воспаление, в наиболее тяжелых случаях встречаются даже очаги творожистого некроза.
При алиментарном заражении первичный туберкулезный комплекс развивается в кишечнике и также состоит из трех компонентов. В лимфоидной ткани нижнего отдела тощей или слепой кишки формируются туберкулезные бугорки с некрозом и последующим образованием в слизистой оболочке язвы, которая и рассматривается как первичный аффект. Далее возникают туберкулезный лимфангит с появлением бугорков по ходу лимфатических сосудов и казеозный лимфаденит регионарных к первичному аффекту лимфатических узлов. Аналогичным образом проявляется первичный туберкулезный комплекс в миндалине (первичный аффект в миндалине, лимфангит и казеозный некроз лимфатических узлов шеи), коже (язва в коже, лимфангит, регионарный казеозный лимфаденит).
Возможны 3 варианта течения первичного туберкулеза: 1) затухание первичного туберкулеза и заживление очагов первичного комплекса;
2) прогрессирование первичного туберкулеза с генерализацией процесса;
3) хроническое течение (хронически текущий первичный туберкулез, см.
схему XXIV).
Затухание первичного туберкулеза и заживление очагов первичного комплекса. Эти процессы начинаются в первичном легочном очаге. Первоначально рассасывается перифокальное воспаление, экссудативная тканевая реакция сменяется продуктивной: вокруг очага казеозной пневмонии образуется вал из эпителиоидных и лимфоидных клеток, как бы отграничивающий очаг от окружающей легочной ткани. Кнаружи от этого вала появляются фиброзирующиеся туберкулезные гранулемы. Вокруг первичного аффекта формируется капсула, наружные слои которой состоят из рыхлой соединительной ткани с наличием мелких сосудов, окруженных клетками лимфоидного типа. Внутренний слой капсулы, прилежащий непосредственно к казеозным массам, постепенно обогащается волокнистыми структурами и сливается с наружным. Со стороны наружного слоя капсулы первичного аффекта врастают сосуды, которые могут достигать внутренних слоев капсулы и вступать в непосредственный контакт с казеозными массами. Последние постепенно обезвоживаются, становятся плотными, обызвествляются (петрификация). С течением времени во внутреннем слое, соприкасающемся с обызвествленными казеозными массами, появляются многоядерные клетки, рассасывающие обызвествленные казеозные массы. На их месте путем метаплазии образуются костные балки с клетками костного мозга в межбалочных пространствах. Так, петрифицированный первичный очаг превращается в оссифицированный. Такой заживший первичный очаг называют по имени описавшего его чешского патолога очагом Гона.
На месте туберкулезного лимфангита в результате фиброзирования туберкулезных гранулем образуется фиброзный тяж. Заживление в лимфатических узлах происходит так же, как и в легочном очаге. Однако в связи с большими размерами поражения в лимфатических узлах оно протекает медленнее, чем в легочном очаге. Очаг казеоза в лимфатическом узле постепенно обезвоживается, обызвествляется и окостеневает.
Обызвествленные очаги в легких обнаруживаются у многих практически здоровых людей. В возрасте до 10 лет они встречаются в 6% вскрытий, от 10 до 15 лет - в 25%, от 20 до 30 лет - в 45%, а после 40 лет - почти у всех людей. Таким образом, попадание туберкулезных микобактерий в организм человека ведет не только к заболеванию, но и к инфицированию, которое может оказать благоприятное влияние на становление иммунитета и предупреждение нового заражения. Доказано, что противотуберкулезный иммунитет является инфекционным, нестерильным, т.е. он осуществляется в организме при наличии слабовирулентных микобактерий. Их удается выделить даже из обызвествленных очагов первичного туберкулезного комплекса. Практически уже давно проводится вакцинация новорожденных и детей младшего возраста вакциной БЦЖ, приготовленной из ослабленных туберкулезных микобактерий. Обязательное введение противотуберкулезной вакцинации привело к тому, что в последние годы резко снизилась инфицированность в детском возрасте, оно отодвинуло сроки заражения людей более старших возрастных групп, защитные силы которых выражены в гораздо большей степени. Однако следует учитывать, что в казеозных обызвествленных и даже частично оссифицированных массах скапливаются маловирулентные микобактерий или их L-формы, которые могут проявлять свою жизнедеятельность при ослаблении защитных сил организма.
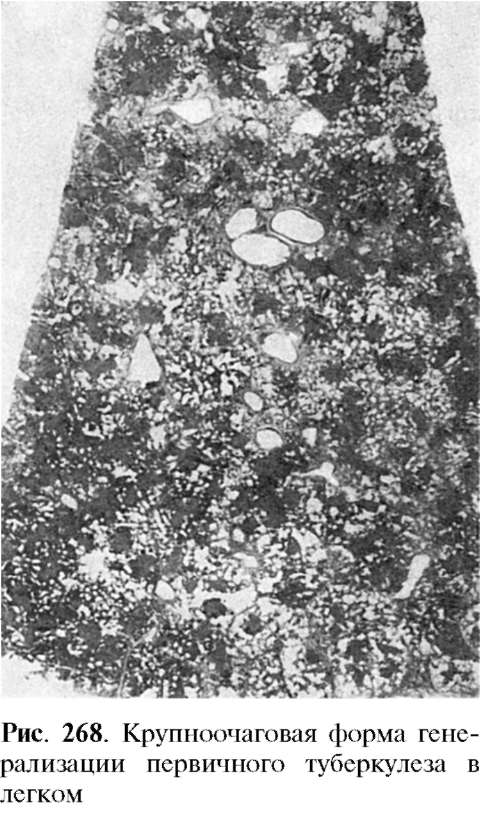 В
кишечнике на месте первичной язвы при заживлении образуется рубчик, а в
лимфатических узлах - петрификаты. Оссификация их протекает очень
медленно.
В
кишечнике на месте первичной язвы при заживлении образуется рубчик, а в
лимфатических узлах - петрификаты. Оссификация их протекает очень
медленно.
Прогрессирование первичного туберкулеза с генерализацией процесса. Оно проявляется в 4 формах: гематогенной, лимфогенной (лимфожелезистой), росте первичного аффекта и смешанной.
Гематогенная форма прогрессирования (генерализация) при первичном туберкулезе развивается в связи с ранним попаданием микобактерий в кровь (диссеминация) из первичного аффекта или из казеозно-измененных лимфатических узлов. Микобактерий оседают в различных органах и вызывают образование в них бугорков размером от милиарных (просовидных) - милиарный туберкулез (см. рис. 71) до крупных очагов величиной с горошину и более. В связи с этим различают милиарную
и крупноочаговую формы гематогенной генерализации (рис. 268). Особенно опасно высыпание милиарных туберкулезных бугорков в мягких мозговых оболочках с развитием туберкулезного лептоменингита. Иногда при гематогенной генерализации появляются единичные разной величины отсевы в различные органы, в том числе в верхушки легких (очаги Симона), которые спустя много лет после затихания первичной инфекции дают начало туберкулезному поражению в месте локализации этого очага отсева.
Лимфогенная (лимфожелезистая)1 форма прогрессирования (генерализации) при первичном туберкулезе проявляется вовлечением в процесс специфического воспаления бронхиальных, бифуркационных, околотрахеальных, над-и подключичных, шейных и других лимфатических узлов. Особенно большое значение в клинике приобретает туберкулезный бронхоаденит. В тех случаях, когда пакеты лимфатических узлов напоминают опухоль, говорят об опухолевидном бронхоадените. При этом казеозноизмененные увеличенные лимфатические узлы сдавливают просветы бронхов, что ведет к развитию очагов ателектаза легких и пневмонии.
1 Это устаревшее название связано с ранее принятым неправильным обозначением лимфатических узлов «железами».
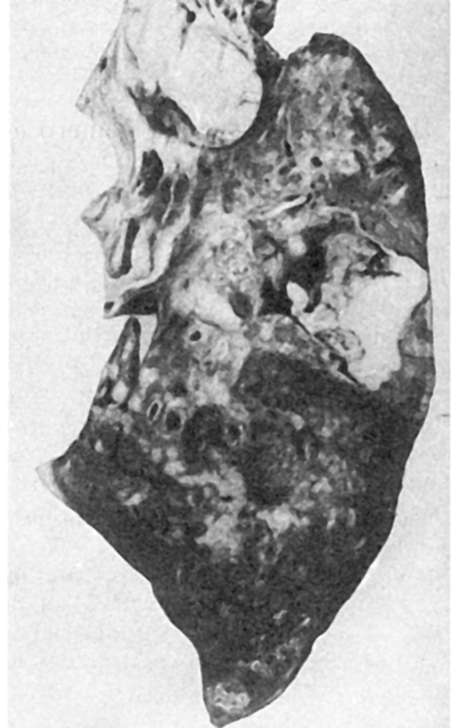 Рис. 269. Распад первичного аффекта и начало образования каверны
Рис. 269. Распад первичного аффекта и начало образования каверны
При первичном кишечном туберкулезе лимфогенная (лимфожелезистая) генерализация ведет к увеличению всех групп мезентериальных лимфатических узлов. Развивается туберкулезный мезаденит, который может доминировать в клинической картине заболевания.
Рост первичного аффекта - наиболее тяжелая форма прогрессирования первичного туберкулеза. При ней наступает казеозный некроз зоны перифокального воспаления, вокруг первичного аффекта образуются свежие участки экссудативного воспаления, подвергающиеся омертвению и сливающиеся между собой. Первичный очаг из ацинозного превращается в лобулярный, затем в сливной лобулярный, сегментарный, лобарный - возникает лобарная казеозная пневмония. Это самая тяжелая форма первичного туберкулеза, быстро заканчиваю- щаяся гибелью больного («скоро- течная чахотка»). В других случаях
первичный очаг лобулярнои или сегментарной казеознои пневмонии расплавляется и на его месте образуется первичная легочная каверна (рис. 269). Процесс принимает хроническое течение, развивается первичная легочная чахотка, напоминающая вторичный фиброзно-кавернозный туберкулез, но отличающаяся от него наличием казеозного бронхоаденита.
Первичный кишечный аффект растет за счет увеличения туберкулезной язвы, обычно в области слепой кишки. Появляются ограниченный туберкулезный перитонит, спайки, пакеты казеозно-измененных илеоцекальных лимфатических узлов. Образуется плотный конгломерат тканей, который клинически иногда принимается за опухоль (опухолевидный первичный кишечный туберкулез). Процесс имеет обычно хроническое течение.
Смешанная форма прогрессирования при первичном туберкулезе наблюдается при ослаблении организма после перенесенных острых инфекций, например кори, при авитаминозах, голодании и т.д. В таких случаях обнаруживаются крупный первичный аффект, казеозный бронхоаденит, нередко осложненный расплавлением некротических масс и образованием свищей. В обоих легких и во всех органах видны многочисленные туберкулезные высыпания.
Обострение туберкулеза со стороны заживших петрифицированных лимфатических узлов наблюдается при длительном применении стероидных гормонов
и иммунодепрессантов, снижающих сопротивляемость организма. Развивается массивный туберкулезный бронхоаденит с лимфогенной и гематогенной генерализацией, очень слабовыраженными общими явлениями и незначительной клеточной реакцией. Этот так называемый лекарственный (стероидный) туберкулез рассматривается как выражение эндогенной инфекции.
Исходы прогрессирующего первичного туберкулеза различны. В неблагоприятных случаях смерть больного наступает от общей генерализации процесса и туберкулезного менингита. При благоприятном течении заболевания и применении эффективных лекарственных препаратов прогрессирование первичного туберкулеза может быть приостановлено, удается перевести экссудативную реакцию в продуктивную, вызвать инкапсуляцию и обызвествление очагов первичного комплекса и рубцевание его отсевов.
Хроническое течение (хронически текущий первичный туберкулез). Оно
возникает прежде всего в тех случаях, когда при зажившем первичном аффекте воспалительный специфический процесс в лимфожелезистом компоненте первичного комплекса принимает медленно прогрессирующее течение с чередованием вспышек и затиханий. При этом наступает сенсибилизация организма - повышается его чувствительность ко всякого рода неспецифическим воздействиям. Повышенная реактивность организма клинически выявляется кожными туберкулиновыми пробами и появлением в тканях и органах параспецифических изменений (Струков А.И., 1948), под которыми понимают различные мезенхимальные клеточные реакции в виде диффузной или узелковой пролиферации лимфоцитов и макрофагов, гиперпластических процессов в кроветворной ткани, фибриноидных изменений соединительной ткани и стенок артериол в органах, диспротеиноз, иногда даже развитие амилоидоза.
Параспецифические реакции, протекающие по типу гиперчувствительности немедленного или замедленного типа, в суставах придают хроническому первичному туберкулезу большое сходство с ревматизмом и описаны под названием ревматизма Понсе.
О хронически текущем первичном туберкулезе говорят также тогда, когда образуется первичная легочная каверна и развивается первичная легочная чахотка (см. схему XXIV).
Гематогенный туберкулез
Гематогенный туберкулез объединяет ряд проявлений заболевания, возникающего и развивающегося в организме человека через значительный срок после перенесенной первичной инфекции, и представляет собой послепервичный туберкулез. В этих случаях речь идет о людях, клинически выздоровевших от первичного туберкулеза, но сохранивших повышенную чувствительность к туберкулину и выработавших значительный иммунитет к туберкулезной микобактерии. Гематогенным туберкулез возникает у тех больных, у которых первичная инфекция оставила изменения в виде очагов отсевов в различные органы или не вполне заживших фокусов в
лимфатических узлах. Эти очаги долгое время могут оставаться латентными, их обострение происходит под влиянием каких-либо неблагоприятных факторов при наличии повышенной реактивности (повышенная чувствительность к туберкулину на фоне выработанного иммунитета к микобактерии). Поэтому при гематогенном туберкулезе преобладает продуктивная тканевая реакция (гранулема), выражена наклонность к гематогенной генерализации, которая ведет к поражению различных органов и тканей.
Выделяют три разновидности гематогенного туберкулеза (схема XXV): 1) генерализованный гематогенный туберкулез; 2) гематогенный туберкулез с преимущественным поражением легких; 3) гематогенный туберкулез с преимущественными внелегочными поражениями.
Генерализованный гематогенный туберкулез. Встречается в настоящее время крайне редко, представляет собой наиболее тяжелую форму заболевания с равномерным высыпанием во многих органах туберкулезных бугорков и очагов. В одних случаях во всех органах формируются некротические очажки без пролиферативной или со слабовыраженной экссудативной реакцией (так называемый некротический вид генерализованного туберкулеза). Это острейший туберкулезный сепсис. В других случаях во всех органах появляются мелкие милиарные продуктивные бугорки. Эту форму обозначают как острый общий милиарный туберкулез. Она часто заканчивается менингитом. Наконец, в некоторых случаях наблюдается острый общий крупноочаговый туберкулез, который встречается обычно у ослабленных больных и характеризуется образованием в разных органах крупных (диаметром до 1 см) туберкулезных очагов (рис. 270).
В каждом случае генерализованного гематогенного туберкулеза необходимо найти очаг, являющийся источником обсеменения; обычно им оказывается не вполне заживший очаг периода первичной инфекции в лимфатическом узле, половых органах, костной системе и т.д.
Гематогенный туберкулез с преимущественным поражением легких. Характеризуется преобладанием в легких высыпаний, в то время как в других органах они отсутствуют или единичны. При наличии в легких множества мелких милиарных бугорков говорят о милиарном туберкулезе легких (рис. 271), который по течению может быть как острым, так и хроническим.
Схема XXV. Основные разновидности гематогенного туберкулеза
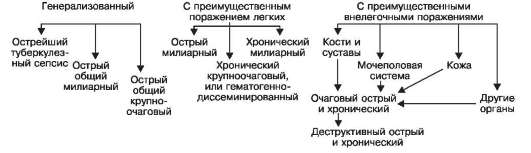
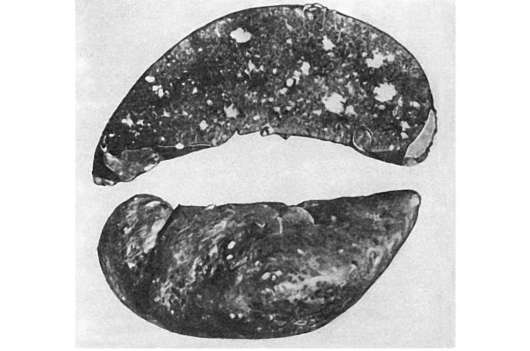 Рис. 270. Изменения селезенки при крупноочаговой генерализации гематогенного туберкулеза
Рис. 270. Изменения селезенки при крупноочаговой генерализации гематогенного туберкулеза
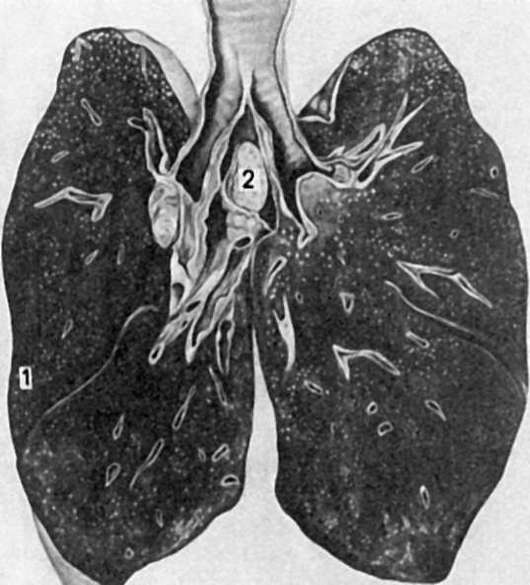 Рис. 271. Милиарный туберкулез легких:
Рис. 271. Милиарный туберкулез легких:
1, 2 - элементы зажившего первичного комплекса
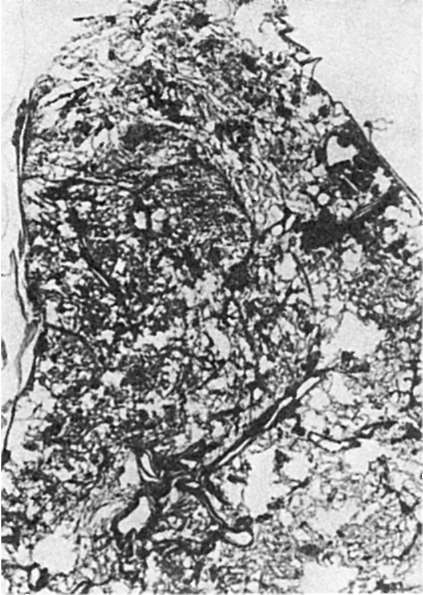 Рис. 272. Хронический крупноочаговый (гематогенно-диссеминированный) туберкулез легких
Рис. 272. Хронический крупноочаговый (гематогенно-диссеминированный) туберкулез легких
При остром милиарном туберкулезе, который встречается редко, легкие бывают вздутыми, пушистыми; в них, как песчинки, прощупываются мелкие бугорки, которые всегда более густо рассеяны в верхних их сегментах, чем в нижних. Нередко эта форма туберкулеза заканчивается менингитом. При хроническом милиарном туберкулезе возможны рубцевание бугорков и развитие стойкой эмфиземы легких, в связи с чем усиливается нагрузка на сердце и наблюдается гипертрофия правого желудочка - легочное сердце. Выделяют, кроме того, хронический крупноочаговый, или гематогенно-диссеминированный, туберкулез легких, который встречается у взрослых людей. Для него характерны преимущественно кортикоплевральная локализация очагов
в обоих легких и продуктивная тканевая реакция (рис. 272), развитие сетчатого пневмосклероза, эмфиземы, легочного сердца и наличие внелегочного туберкулезного очага.
Гематогенный туберкулез с преимущественными внелегочными поражениями. Развивается из очагов-отсевов, занесенных в тот или иной орган гематогенным путем в периоде первичной инфекции. Поражаются преимущественно кости скелета (костно-суставной туберкулез) и мочеполовая система (туберкулез почек, половых органов), кожа и другие органы. Различают очаговую и деструктивную формы, которые могут иметь острое и хроническое течение (см. схему XXV), т.е. формы туберкулеза становятся фазами его развития.
Туберкулез костей и суставов встречается чаще у детей, реже у взрослых. Развивается из очагов отсевов в костном мозге (туберкулезный остеомиелит). Излюбленной локализацией являются тела позвонков (туберкулезный спондилит, рис. 273, см. на цв. вкл.), эпифизы костей, образующих тазобедренный (туберкулезный коксит) и коленный (туберкулезный го- нит) суставы. Диафизы поражаются редко. Синовиальные оболочки вовлекаются в процесс вторично при переходе его с эпифиза кости на ткани сустава. Наиболее опасными при туберкулезе костей и суставов являются образование секвестров, т.е. участков омертвения кости, ее разрушение, образование горба и деформация суставов. С кости специфический процесс распространяется на прилежащие к суставам мягкие ткани, что ведет к появлению натечных абсцессов и свищей.
Туберкулез почек бывает обычно односторонним, чаще проявляется у молодых людей в период полового созревания, а также в пожилом возрасте. Ранние очаги возникают в корковом слое, при прогрессировании процесса они появляются в сосочках пирамид; здесь начинается деструктивный процесс с образованием полостей (рис. 274, см. на цв. вкл.). Вне каверн интерстиций почечной ткани инфильтрирован лимфоцитами, гистиоцитами с примесью эпителиоидных клеток (хронический интерстициальный нефрит - рис. 274, см. на цв. вкл.). Закрытие просвета мочеточника казеозными массами приводит к развитию пионефроза. Постепенно специфический воспалительный процесс переходит на мочевыводящие пути, мочевой пузырь, предстательную железу, придаток яичка. У женщин поражаются слизистая оболочка матки, трубы, редко яичники.
При гематогенном туберкулезе поражаются также эндокринные железы, ЦНС, печень, серозные оболочки (в последних туберкулез может возникать и в результате перехода специфического процесса с пораженных лимфатических узлов.
Вторичный туберкулез
Вторичный, реинфекционный, туберкулез развивается в организме взрослого человека, перенесшего ранее первичную инфекцию, которая обеспечила ему относительный иммунитет, но не оградила от возможности повторного заболевания - послепервичного туберкулеза. Для него характерны: 1) избирательно легочная локализация процесса; 2) контактное и интраканаликулярное (бронхиальное дерево, желудочно-кишечный тракт) распространение; 3) смена клинико-морфологических форм, которые являются фазами туберкулезного процесса в легких.
В отношении происхождения вторичного туберкулеза существуют две теории: экзогенного происхождения, т.е. нового заражения, и эндогенного происхождения. Тот факт, что анатомические находки позволяют проследить длинную цепь событий, начиная от очагов первичной инфекции до образования свежих очагов реинфектов, позволяет большинству исследователей присоединиться к теории их эндогенного происхождения.
Патологическая анатомия. Различают 8 форм вторичного туберкулеза, каждая из которых представляет собой дальнейшее развитие предшествующей ей формы (схема XXVI). В связи с этим формы вторичного туберкулеза являются одновременно и фазами его развития (формы-фазы). Среди форм-фаз вторичного туберкулеза различают: 1) острый очаговый; 2) фиброзно-очаговый; 3) инфильтративный; 4) туберкулему; 5) казеозную пневмонию; 6) острый кавернозный; 7) фиброзно-кавернозный; 8) цирротический.
Острый очаговый туберкулез встречается у людей в возрасте 20-25 лет и старше. Морфологически он характеризуется наличием в I и II сегментах правого (реже левого) легкого одного или двух очагов. Они получили название очагов реинфекта Абрикосова. А.И. Абрикосов в 1904 г. впервые показал, что эти начальные проявления вторичного туберкулеза состоят
Схема XXVI. Формы-фазы вторичного туберкулеза легких
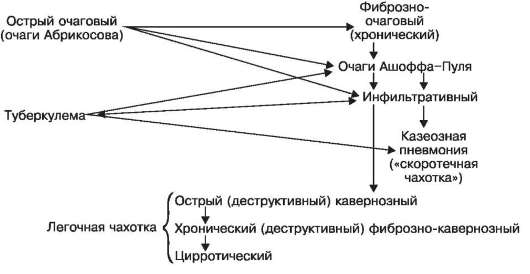 из специфического эндобронхита, мезобронхита и панбронхита внутридолькового
бронха. Специфический процесс по бронхиолам переходит на легочную
паренхиму, вследствие чего развивается ацинозная или лобулярная творожистая бронхопневмония, вокруг
которой быстро формируется вал эпителиоидных клеток с примесью
лимфоидных и гигантских клеток Пирогова-Лангханса. В лимфатических узлах
корня легкого развивается реактивный неспецифический процесс. При
своевременном лечении, а в большом числе случаев спонтанно, процесс
затихает, экссудативная тканевая реакция сменяется продуктивной, очаги
казеозного некроза инкапсулируются и петрифицируются, появляются
ашофф-пулевские очаги реинфекта и процесс на этом может закончиться.
из специфического эндобронхита, мезобронхита и панбронхита внутридолькового
бронха. Специфический процесс по бронхиолам переходит на легочную
паренхиму, вследствие чего развивается ацинозная или лобулярная творожистая бронхопневмония, вокруг
которой быстро формируется вал эпителиоидных клеток с примесью
лимфоидных и гигантских клеток Пирогова-Лангханса. В лимфатических узлах
корня легкого развивается реактивный неспецифический процесс. При
своевременном лечении, а в большом числе случаев спонтанно, процесс
затихает, экссудативная тканевая реакция сменяется продуктивной, очаги
казеозного некроза инкапсулируются и петрифицируются, появляются
ашофф-пулевские очаги реинфекта и процесс на этом может закончиться.
Фиброзно-очаговый туберкулез представляет собой ту фазу течения острого очагового туберкулеза, когда после периода затихания болезни (заживления очагов Абрикосова) процесс снова вспыхивает. При заживлении очагов Абрикосова появляются довольно крупные инкапсулированные и частично петрифицированные очаги, описанные немецкими учеными Л. Ашоффом и Х. Пулем (ашофф-пулевские очаги). Им придается значение в обострении процесса, которое характеризуется возникновением ацинозных, лобулярных очагов казеозной пневмонии, которые снова инкапсулируются, частично петрифицируются и превращаются в ашофф-пулевские. Однако склонность к обострению сохраняется. Процесс остается односторонним, не выходит за пределы I и II сегментов. Следует помнить, что в I и II сегментах среди осумкованных и обызвествленных очагов туберкулеза есть не только ашофф-пулевские (зажившие очаги Абрикосова), но и те, которые представляют собой исход гематогенных отсевов в период первичной инфекции. Они описаны Г. Симоном и носят его имя. Симоновские очаги мельче ашофф-пулевских и в верхушках легких располагаются симметрично.
Инфильтративный туберкулез развивается при прогрессировании острого очагового или обострении фиброзно-очагового туберкулеза, причем экссудативные изменения вокруг казеозных очагов выходят за пределы дольки и даже сегмента. Перифокальное воспаление преобладает над казеозными изменениями, которые могут быть незначительными. Такой очаг называют очагом-инфильтратом Ассманна-Редекера (по имени ученых, впервые описавших его рентгенологическую картину). Неспецифическое перифокальное воспаление может рассасываться, и тогда в период заживления остаются только один или два нерассосавшихся небольших казеозных фокуса, которые в дальнейшем инкапсулируются, и заболевание снова приобретает характер фиброзно-очагового туберкулеза. В тех случаях, когда перифокальное воспаление охватывает всю долю, говорят о лобите как об острой форме инфильтративного туберкулеза.
Туберкулема - форма вторичного туберкулеза, возникающая как своеобразная фаза эволюции инфильтративного туберкулеза, когда перифокальное воспаление рассасывается и остается очаг творожистого некроза, окруженный капсулой (рис. 275). Туберкулема достигает 2-5 см в диаметре, расположена в I или II сегменте, чаще справа. Нередко при рентгенологическом обследовании вследствие довольно хорошо очерченных границ ее ошибочно принимают за периферический рак легкого.
Казеозная пневмония обычно наблюдается при прогрессировании инфильтративного туберкулеза, в результате чего казеозные изменения начинают преобладать над перифокальными. Образуются ацинозные,
лобулярные, сегментарные казеознопневмонические очаги, которые при слиянии могут занимать более крупные участки легких и даже всю долю. Лобарный характер имеет казеозная пневмония, развившаяся на фоне лобита. Казеозная пневмония наблюдается обычно у ослабленных больных и всегда на фоне более старых изменений (фиброзно-очагового, инфильтративно-пневмонического туберкулеза или туберкулемы). Она нередко возникает в терминальном периоде любой формы туберкулеза, чему способствует ослабление защитных сил организма. Легкое при казеозной пневмонии увеличено, плотное, на разрезе желтой окраски, на плевре фибринозные наложения. В настоящее время казеоз- ная пневмония встречается редко.
 Острый кавернозный туберкулез -
форма вторичного туберкулеза, для которой характерно быстрое
образование полости распада, а затем каверны на месте очага-инфильтрата
или туберкулемы (рис. 276). Полость распада возникает в результате
гнойного расплавления и разжижения казеозных масс, которые с
микобактериями выделяются вместе с мокротой. Это создает большую
опасность бронхогенного обсеменения легких, а также выделения
микобактерий в окружающую среду. Образующаяся при этом каверна
локализуется обычно в I или II сегменте (на месте очагов, из которых она
развилась), имеет овальную или округлую форму, диаметром 2-5 см,
сообщается с просветом сегментарного бронха. Стенка каверны неоднородна:
внутренний слой ее состоит из казеоз- ных масс, наружный - из уплот- ненной в результате воспаления легочной ткани (см. рис. 276).
Острый кавернозный туберкулез -
форма вторичного туберкулеза, для которой характерно быстрое
образование полости распада, а затем каверны на месте очага-инфильтрата
или туберкулемы (рис. 276). Полость распада возникает в результате
гнойного расплавления и разжижения казеозных масс, которые с
микобактериями выделяются вместе с мокротой. Это создает большую
опасность бронхогенного обсеменения легких, а также выделения
микобактерий в окружающую среду. Образующаяся при этом каверна
локализуется обычно в I или II сегменте (на месте очагов, из которых она
развилась), имеет овальную или округлую форму, диаметром 2-5 см,
сообщается с просветом сегментарного бронха. Стенка каверны неоднородна:
внутренний слой ее состоит из казеоз- ных масс, наружный - из уплот- ненной в результате воспаления легочной ткани (см. рис. 276).
Фиброзно-кавернозный туберкулез (рис. 277), или хроническая легочная чахотка, возникает из острого кавернозного туберкулеза в тех случаях, когда процесс принимает хроническое течение. Стенка каверны плотная и имеет три слоя: внутренний - пиогенный (некротический), богатый распадающимися лейкоцитами; средний - слой туберкулезной грануляционной ткани; наружный - соединительнотканный, причем среди прослоек соединительной ткани видны участки ателектазов легкого. Внутренняя поверхность неровная, с пересекающими полость каверны балками; каждая балка представляет собой облитерированный бронх или тромбированный сосуд. Изменения более выражены в одном, чаще в правом, легком. В I и II сегментах изменения более старые, плевра утолщена. Каверна занимает один или оба сегмента. Вокруг нее определяются разнообразные очаги (в зависимости от типа тканевой реакции), бронхоэктазы. Процесс постепенно распространяется в апико-каудальном направлении, спускается с верхних сегментов на нижние как контактным путем, так и по бронхам, занимая все новые участки легкого. Поэтому наиболее старые изменения при фиброзно-кавернозном туберкулезе наблюдаются в верхних отделах легких, а наиболее свежие - в нижних. С течением времени процесс переходит по бронхам на противоположное
 Рис. 277. Фиброзно-кавернозный туберкулез легких
Рис. 277. Фиброзно-кавернозный туберкулез легких
легкое. Раньше всего бронхогенные метастатические очаги в нем возникают в III сегменте, где появляются ацинозные и лобулярные туберкулезные очаги. При их распаде возможны образование каверн и дальнейшее бронхогенное распространение процесса.
Цирротический туберкулез рассматривается как вариант развития фиброзно-кавернозного туберкулеза, когда в пораженных легких вокруг каверн происходит мощное развитие соединительной ткани, на месте зажившей каверны образуется линейный рубец, появляются плевральные сращения, легкие деформируются, становятся плотными и малоподвижными, появляются многочисленные бронхоэктазы.
При вторичном легочном туберкулезе в силу того, что инфекция распространяется, как правило, интраканаликулярным (бронхиальное дерево, желудочно-кишечный тракт) или контактным путем, может развиваться специфическое поражение бронхов, трахеи, гортани, полости рта, кишечника. Гематогенное распространение отмечается редко, оно возможно в терминальном периоде болезни при снижении защитных сил организма. В этих случаях находят туберкулезный менингит, органные внелегочные и другие поражения.
Осложнения туберкулеза многообразны и упоминались при описании отдельных его форм. При первичном туберкулезе могут развиться туберкулезный менингит, плеврит, перикардит, перитонит. При костном туберкулезе наблюдаются секвестры, деформации, поражение мягких тканей, абсцессы и свищи. При вторичном туберкулезе наибольшее число осложнений связано с каверной: кровотечения, прорыв содержимого каверны в плевральную полость, что приводит к пневмотораксу и гнойному плевриту (эмпиема плевры). В связи с длительным течением заболевания
любая форма туберкулеза может осложниться амилоидозом (особенно часто он наблюдается при фиброзно-кавернозном туберкулезе).
Причина смерти больных легочным туберкулезом в настоящее время заключается в легочно-сердечной недостаточности, кровотечениях, амилоидозе и осложнениях послеоперационного периода у больных с тяжелым кавернозным процессом.
Патоморфоз туберкулеза
За последние годы клиническая и морфологическая картина туберкулеза в экономически развитых странах значительно изменилась. Изменения обусловлены главным образом социальным прогрессом, достижениями лекарственной и антибактериальной терапии и рассматриваются как естественный и индуцированный патоморфоз. Наблюдается резкое снижение и практически исчезновение прогрессирующих форм заболевания: первичного туберкулеза, гематогенного туберкулеза, казеозной пневмонии. К числу общих для всех клинико-анатомических форм признаков современного туберкулеза относят уменьшение специфических экссудативных изменений (рис. 278) и генерализации процесса, усиление неспецифического компонента туберкулезного воспаления и фибропластической реакции.
 Рис. 278. Патоморфоз туберкулеза. Очищенная каверна, превратившаяся в кисту (препарат И.П. Соловьевой)
Рис. 278. Патоморфоз туберкулеза. Очищенная каверна, превратившаяся в кисту (препарат И.П. Соловьевой)
Сифилис
Сифилис (syphilis, по имени пастуха Сифилиуса, героя поэмы врача Дж. Фракасторо; вероятно, от греч. sys - свинья + hilos - друг), или люэс - хроническое инфекционное венерическое заболевание, характеризующееся поражением кожи, слизистых оболочек, внутренних органов, костей, нервной системы с последовательной сменой стадий (периодов) болезни.
Этиология и патогенез. Возбудитель заболевания - бледная трепонема (Treponema allidum), открыта в 1905 г. Ф. Шаудином и Э. Гоффманом. Трепонема - анаэроб, занимает среднее положение между бактериями и простейшими; существуют и L-формы, с которыми связывают серорезистентность у ряда больных. Проникновение возбудителя в организм происходит через поврежденный эпидермис или эпителий слизистой оболочки. Заражение осуществляется половым, реже - внеполовым путем (бытовой или профессиональный сифилис). Это так называемый приобретенный сифилис. Кроме того, выделяют врожденный сифилис, возникающий при внутриутробном заражении плода. Развитию морфологических и клинических проявлений приобретенного сифилиса предшествует инкубационныгй период, продолжающийся в среднем 3 нед. Трепонема быстро внедряется в лимфатические сосуды, регионарные (паховые при половом заражении) лимфатические узлы, а затем попадает в ток крови и распространяется по организму. Все тканевые изменения, развивающиеся при сифилисе, по существу определяются измененной реактивностью организма. Они отражают 3 периода сифилиса - первичный, вторичный и третичный (гуммозный). Первичный период сифилиса возникает на фоне нарастающей сенсибилизации, вторичный период соответствует проявлениям гиперергии (реакции гиперчувствительности немедленного типа) и протекает с явлениями генерализации инфекции, третичный период развивается на фоне становления иммунитета и проявлений гиперчувствительности замедленного типа; поражения при нем носят локальный характер.
Патологическая анатомия. Изменения при сифилисе отличаются большим разнообразием и зависят от периода болезни.
Первичный период сифилиса характеризуется образованием во входных воротах инфекции затвердения, на месте которого вскоре появляется безболезненная округлая язва с гладким лакированным дном и ровными, хрящевидной консистенции, краями. Так образуется первичный сифилитический аффект - твердый шанкр, или твердая язва (ulcus durum). Локализация первичного аффекта при половом заражении - половые органы (головка полового члена, малые и большие срамные губы), при внеполовом - слизистая оболочка полости рта, пальцы рук (у акушеров, патологоанатомов). Очень быстро в процесс вовлекаются отводящие лимфатические сосуды и регионарные лимфатические узлы, которые увеличиваются, становятся плотными и в сочетании с первичным аффектом образуют первичный сифилитический комплекс. В твердом шанкре воспа-
лительный инфильтрат по краям язвы и в области дна состоит из лимфоидных и плазматических клеток с примесью небольшого числа нейтрофилов и эгштелиоидных клеток. Между клетками обнаруживается большое число трепонем. Инфильтрат располагается главным образом вокруг мелких сосудов, в которых наблюдается пролиферация эндотелия, вплоть до полного закрытия просвета. Среди клеток появляются прослойки зрелой соединительной ткани, происходит рубцевание и через 2-3 мес на месте первичного аффекта образуется небольшой, лишенный пигмента рубчик. В регионарных лимфатических узлах находят гиперплазию фолликулов, десквамацию и пролиферацию эндотелия синусов и сосудов; происходит склероз лимфатического узла.
Вторичный период сифилиса (период гиперергии и генерализации) наступает приблизительно через 6-10 нед после заражения и характеризуется появлением сифилидов - множественных воспалительных очагов на коже и слизистых оболочках. В зависимости от интенсивности воспаления и преобладания экссудативных или некробиотических процессов различают несколько разновидностей сифилидов: розеолы, папулы и пустулы. Общими для всех сифилидов являются очаговый отек кожи и слизистых оболочек, разрыхление эпителиального покрова, гиперемия сосудов, воспалительная инфильтрация вокруг них, некроз стенок. Сифилиды богаты трепонемами, которые при изъязвлении папул или пустул могут попадать во внешнюю среду, поэтому вторичный период очень заразен. В увеличенных лимфатических узлах отмечаются отек, гиперплазия, очаги некроза, скопления трепонем. После заживления сифилидов (через 3-6 нед от начала высыпаний) остаются небольшие беспигментные рубчики, иногда исчезающие.
Третичный период наступает через 3-6 лет после заражения, проявляется в виде хронического диффузного интерстициального воспаления и образования гумм.
Хроническое диффузное интерстициальное воспаление отмечается в печени, легких, стенке аорты, ткани яичек. По ходу сосудов наблюдаются клеточные инфильтраты, состоящие главным образом из лимфоидных и плазматических клеток, наблюдаются продуктивный эндартериит и лимфангит. В дальнейшем в пораженных органах развивается сифилитический цирроз, который особенно ярко выражен в печени, которая становится дольчатой, бугристой.
Гумма - очаг сифилитического продуктивно-некротического воспаления (см. Воспаление), сифилитическая гранулема (см. рис. 73). Гуммы могут быть одиночными (солитарные) и множественными. Чаще всего они встречаются в печени, коже, мягких тканях. С течением времени некротические массы гуммы подвергаются рубцеванию, иногда обызвествляются.
Висцеральный сифилис
При висцеральном сифилисе поражаются внутренние органы, чаще в третичный период заболевания. Могут вовлекаться в процесс многие ор-
ганы (сердце и сосуды, органы пищеварения, дыхания, молочные железы, нервная система и др.), но наибольшее значение в клинике висцерального сифилиса имеет поражение сердечно-сосудистой системы; велико также значение сифилиса центральной нервной системы (нейросифилис).
Поражение сердца при висцеральном сифилисе может проявляться в виде гуммозного и хронического межуточного миокардита и заканчивается развитием массивного кардиосклероза. Поражаются артерии разного калибра, возникает продуктивный артериит, заканчивающийся артериосклерозом. Чаще других артерий вовлекается аорта. Развивается сифилитический мезаортит (нередко через 15-20 лет после заражения), обычно у мужчин в возрасте 40-60 лет. Процесс локализуется в восходящей части и дуге аорты, чаще непосредственно над клапанами. На интиме аорты появляются белесоватые бугристости с рубцовыми втяжениями, придающими аорте вид шагреневой кожи (рис. 279). Если присоединяется атеросклероз, то картина специфических изменений затушевывается. В типичных случаях изменения резко обрываются в дуге или в нисходящей части аорты. Брюшная аорта поражается очень редко.
При сифилитическом мезаортите в стенке аорты обнаруживается воспалительныгй процесс, распространяющийся со стороны vasa vasorum и адвентиции на среднюю оболочку. Здесь имеются скопления лимфоидных, плазматических клеток, гигантских клеток типа Пирогова-Лангханса, фибробластов, иногда мелкие очажки некроза (см. рис. 279). Воспалительный инфильтрат разрушает эластические волокна средней оболочки,
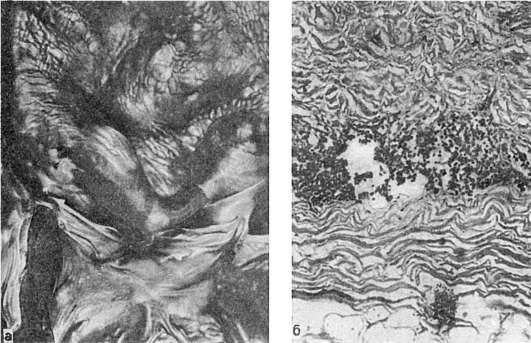 Рис. 279. Сифилитический мезаортит:
Рис. 279. Сифилитический мезаортит:
а - внешний вид аорты; б - микроскопическая картина
в ней появляются поля соединительной ткани с обрывками эластических волокон. Прочность стенки аорты уменьшается, просвет ее расширяется - образуется сифилитическая аневризма аорты. Аневризма восходящей части и дуги аорты, увеличиваясь в вентральном направлении, может вызывать узуру грудины и прилежащих частей ребер, выпячиваться через кожу и перфорировать ее.
Со стенки аорты воспаление может перейти на аортальный клапан и его заслонки. Они становятся белесоватыми, деформируются вследствие грубого рубцевания, характерного для сифилиса, срастаются между собой, что приводит к сифилитическому аортальному пороку. Он нередко комбинируется с аневризмой восходящей части аорты. Возможны и другие осложнения сифилитического мезаортита. Нередко гуммозный инфильтрат переходит на венечные артерии сердца. Вокруг их устьев возникает специфическое воспаление, происходит рубцевание, что приводит к сужению устьев венечных артерий и к коронарной недостаточности.
Нейросифилис представляет собой сифилитический процесс в нервной системе. Он может наблюдаться в любом периоде заболевания, но чаще в третичном. Различают гуммозную и простую формы сифилиса нервной системы, сосудистые поражения, прогрессивный паралич и спинную сухотку. Гуммы в головном мозге имеют характерное для них строение, размеры их различны - от просовидного узелка до голубиного яйца. Иногда находят диффузные гуммозные разрастания с поражением ткани мозга и его оболочек. Простая форма сифилитического поражения выражается воспалительными лимфоцитарными инфильтратами как в ткани мозга, так и в его оболочках. Сосудистые поражения при нейросифилисе могут проявляться сифилитическим облитерирующим эндартериитом и эндофлебитом. Вследствие циркуляторных нарушений в ткани головного и спинного мозга образуются очаги размягчения.
Прогрессивный паралич представляет собой позднее проявление сифилиса и характеризуется уменьшением массы головного мозга, истончением извилин, атрофией подкорковых узлов и мозжечка. Эпендима желудочков приобретает зернистый вид. При микроскопическом исследовании в ткани мозга обнаруживают воспалительные и дистрофические изменения, гибель нервных клеток, участки демиелинизации, нарушение архитектоники мозговой ткани. Отмечается пролиферация глии, причем клетки микроглии представлены палочковидными формами. В мягкой оболочке головного и спинного мозга также находят воспалительные изменения. В спинном мозге поражаются задние, реже - боковые столбы.
Спинная сухотка (tabes dorsalis) - позднее проявление сифилиса, при котором поражается спинной мозг. На поперечных срезах его задние столбы выглядят истонченными и имеют серую окраску. Обычно дистрофический процесс начинается в верхнепоясничном отделе спинного мозга и касается вначале клиновидных пучков (пучки Бурдаха), а в дальнейшем распространяется на задние столбы; задние корешки спинного мозга истончаются. В задних столбах миелиновые оболочки распадаются, высвобождаются нейтральные жиры, которые поглощаются глиозными
элементами, макрофагами и транспортируются в адвентициальные сосудистые пространства.
В мягкой мозговой оболочке спинного мозга находят воспалительные изменения. В участках воспаления и в веществе спинного мозга находят бледные трепонемы.
Врожденный сифилис
Врожденный сифилис развивается при внутриутробном заражении плода через плаценту от больной сифилисом матери. Этот вид сифилиса подразделяют на 3 формы: 1) сифилис мертворожденных недоношенных плодов; 2) ранний врожденный сифилис новорожденных и грудных детей; 3) поздний врожденный сифилис детей дошкольного и школьного возраста, а также взрослых. Тканевые изменения при врожденном сифилисе разнообразны. Одни из них вызываются самой трепонемой, другие являются результатом задержки или нарушения развития (дисплазии) органов под влиянием возбудителя сифилиса.
При сифилисе мертворожденных недоношенных плодов смерть плода обычно наступает между VI и VII лунным месяцем в утробе матери. Это приводит к преждевременным родам мацерированным плодом. Причиной смерти является токсическое действие трепонемы.
Ранний врожденный сифилис проявляется чаще всего на протяжении первых двух месяцев жизни. При нем поражаются почки, легкие, печень, кости, ЦНС. В коже появляются сифилиды папулезного и пустулезного характера. В легких развивается интерстициальная сифилитическая пневмония, ведущая к уплотнению ткани легкого с развитием в нем склеротических изменений. На разрезе легкие принимают белесоватый вид, что дало повод Р. Вирхову назвать этот процесс белой пневмонией. Поражение печени имеет характер интерстициального гепатита (рис. 280) с гибелью гепатоцитов, межуточной круглоклеточной инфильтрацией, образованием милиарных гумм и склерозом. На разрезе она приобретает коричневатый цвет («кремневая печень»). В костях нарушается процесс предварительного обызвествления эпифизарного хряща и новообразования костной ткани; он сочетается с воспалительными изменениями в прилежащих к эпифизу отделах кости и сифилитическим эндопериваскулитом. Этот процесс развивается на границе диафиза и нижнего эпифиза бедра, в ребрах и грудине и носит название сифилитического остеохондрита. Границы кости и хряща имеют вид не ровной, а зазубренной линии. В ЦНС возникают сосудистые воспалительные изменения, поражение как вещества мозга, так и мозговых оболочек - сифилитический энцефалит и менингит. При раннем врожденном сифилисе к описанным выше изменениям органов может присоединяться высыпание мелких очажков, состоящих из подвергшейся некрозу ткани органа и распадающихся лейкоцитов; эти очажки, содержащие много трепонем, называют милиарными гуммами.
Поздний врожденный сифилис характеризуется деформацией зубов, в основе которой лежат гипоплазия эмали и образование полулунной выемки на обоих верхних центральных резцах или же на одном из них с
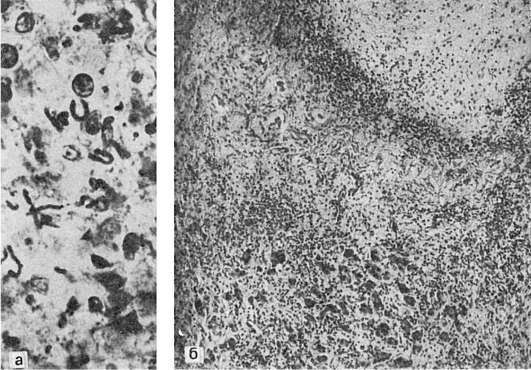 Рис. 280. Печень при врожденном сифилисе (препарат А.В. Цинзерлинга):
Рис. 280. Печень при врожденном сифилисе (препарат А.В. Цинзерлинга):
а - скопления трепонем (импрегнация серебром по Левадити); б - интерстициальный гепатит, склероз (портальный) печени
последующим искривлением. Зубы становятся бочкообразными: на уровне шейки зуб шире, чем на свободном крае; размеры зубов уменьшены - зубы Гетчинсона. Развиваются паренхиматозный кератит, глухота, которые в сочетании с измененными зубами составляют так называемую триаду Гетчинсона, характерную для позднего врожденного сифилиса. Изменения в органах сходны с проявлениями приобретенного сифилиса третичного периода. Отличия касаются вилочковой железы, в которой могут встречаться полости, наполненные серозной жидкостью с примесью нейтрофилов и лимфоцитов. Полости окружены валом из эпителиоидных клеток и носят название абсцессов Дюбуа.
Плацента при сифилисе роженицы изменена: ее масса увеличена (до 2250 г вместо 600 г), цвет желтовато-серый, консистенция кожистая. В ней обнаруживаются отек, клеточная инфильтрация, резкая гиперплазия ворсин, иногда в них образуются обсцессы; в стенках сосудов отмечаются воспалительные изменения.
Сепсис
Сепсис (от греч. sepsis - гниение) - общее инфекционное заболевание, возникающее в связи с существованием в организме очага инфекции и имеющее ряд отличий от других инфекционных болезней. Сепсис от-
личают этиологические, эпидемиологические, клинические, иммунологические и патологоанатомические особенности.
Этиологические особенности сепсиса заключаются в том, что его могут вызывать самые разнообразные возбудители: стафилококк, стрептококк, пневмококк, менингококк, синегнойная палочка, микобактерия туберкулеза, брюшнотифозная палочка, грибы и другие инфекты (кроме вирусов). Таким образом, сепсис полиэтиологичен.
В эпидемиологическом отношении сепсис не является заразной болезнью, он не воспроизводится в эксперименте.
Клиническое своеобразие сепсиса как инфекции состоит в том, что независимо от характера возбудителя проявления болезни остаются трафаретными, они обусловлены генерализацией инфекции и неадекватной реакцией организма на инфект. В течении заболевания отсутствует цикличность, столь характерная для многих инфекционных заболеваний. Сепсис не имеет определенных сроков инкубации. Ему свойственны разные сроки течения - от нескольких дней до нескольких месяцев и даже лет, в связи с чем выделяют острейший, острый, подострый и хронический сепсис.
Иммунологическая особенность сепсиса состоит в том, что иммунитет при нем не вырабатывается, организм в условиях повышенной реактивной готовности реагирует на инфекционный возбудитель неадекватно, преобладают гиперергические реакции.
Патологоанатомические особенности сепсиса сводятся к тому, чго местные и общие изменения при нем не имеют каких-либо специфических особенностей, тогда как при других инфекциях (сыпной и брюшной тифы, скарлатина, дизентерия и др.) эти изменения достаточно характерны.
Сепсис является одной из наиболее тяжелых и довольно частых инфекций. При нем отмечается высокая летальность. В последнее десятилетие заболевания сепсисом участились, что связывают с появлением устойчивых к антибиотикам штаммов бактерий и аутоинфекций в результате применения цитостатических препаратов, ведущих к недостаточности иммунной системы.
Патогенез. Для возникновения заболевания необходима бактериемия, что, однако, является только одной из предпосылок для развития сепсиса. Бактериемия наблюдается при ряде болезней (например, при брюшном тифе, туберкулезе и др.), но не ведет к развитию сепсиса. До недавнего времени считалось, что сепсис является выражением особого вида реакции организма на микроб, а не каких-то особых свойств инфекта, поэтому-то он и представляет собой не инфекцию в этиологическом смысле, а определенную форму развития в организме разных инфекций. В настоящее время эта реактологическая теория патогенеза сепсиса (Абрикосов А.И., 1944; Давыдовский И.В., 1956), согласно которой ведущая роль в его развитии принадлежит состоянию организма, а не микробу, встречает возражения. Доказано, что при сепсисе велика роль не только меняющейся реактивности макроорганизма, но и само-
го инфекта. Сепсис рассматривается как особая форма взаимодействия макро- и микроорганизма, при этом воздействию инфекта и реакции на него организма придается равное значение. Гиперергическая реакция организма на инфект и отсутствие иммунитета объясняют генерализацию инфекции, ациклическое течение сепсиса, преобладание реакций общего плана и утрату способности локализовать инфекцию.
Патологическая анатомия. При сепсисе различают местные и общие изменения. Местные изменения развиваются в очаге внедрения инфекции (входные ворота) или в отдалении от него. Образуется септический очаг, который представляет собой фокус гнойного воспаления (в некоторых случаях септический очаг отсутствует). Из септического очага инфекция быстро распространяется по лимфатическим и кровеносным сосудам. Распространение инфекции по лимфатической системе ведет к развитию лимфангита, лимфотромбоза и лимфаденита, а распространение ее по кровеносной системе (по венам) - к развитию флебита и тромбофлебита. Нередко возникает гнойный тромбофлебит, что ведет к расплавлению тромбов и тромбобактериальной эмболии.
Общие изменения при сепсисе имеют характер дистрофических, воспалительных и гиперпластических. Дистрофические изменения развиваются в паренхиматозных органах (печень, почки, миокард, мышцы, ЦНС) и проявляются различными видами дистрофии и некробиозом, которые нередко завершаются некрозом.
Воспалительные изменения представлены межуточными процессами (межуточный септический нефрит, гепатит, миокардит - рис. 281). На клапанах сердца может возникать острый полипозно-язвенный эндокардит (рис. 282) с расплавлением ткани и отрывом клапанов. Воспалительные изменения возникают в сосудах (васкулиты), что обусловливает появление множественных геморрагии. Однако геморрагический синдром
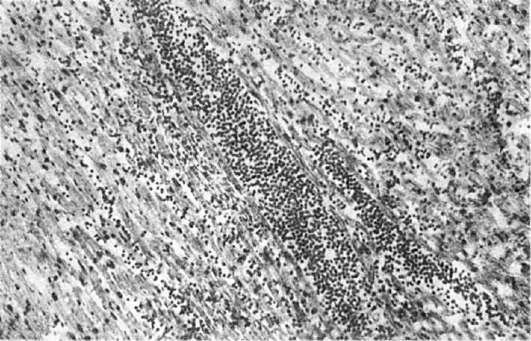 Рис. 281. Сепсис. Межуточный экссудативный миокардит
Рис. 281. Сепсис. Межуточный экссудативный миокардит
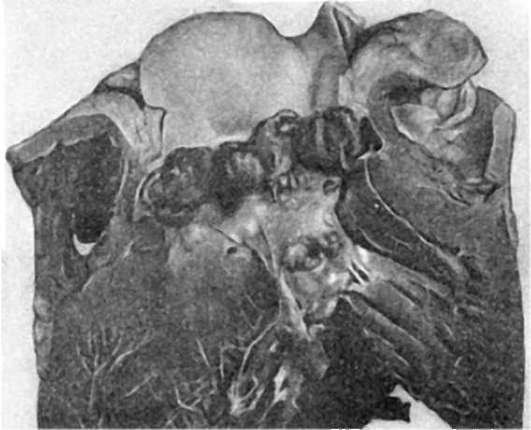 Рис. 282. Острый септический полипозно-язвенный эндокардит
Рис. 282. Острый септический полипозно-язвенный эндокардит
связан при сепсисе не только с васкулитами, но и с интоксикацией, повышенной сосудисто-тканевой проницаемостью, анемией и т.д.
Гиперпластические процессы при сепсисе наблюдаются главным образом в кроветворной и лимфатической (иммунокомпетентной) тканях. Происходит гиперплазия костного мозга плоских костей. Желтый костный мозг трубчатых костей становится красным, в крови увеличивается количество лейкоцитов, иногда появляются молодые формы лейкоцитов, развивается так называемая лейкемоидная реакция. Гиперплазия лимфатической ткани приводит к увеличению размеров лимфатических узлов, селезенки, которая становится не только резко увеличенной, но и дряблой, на разрезе имеет красный цвет и дает обильный соскоб пульпы (септическая селезенка). Гиперпластические процессы в гистиоцитарномакрофагальной системе объясняют увеличение печени. В связи с гемолитическим действием некоторых бактериальных токсинов при сепсисе может возникнуть гемолитическая желтуха.
Классификация. При классификации сепсиса необходимо учитывать ряд признаков: 1) этиологический; 2) характер входных ворот инфекции (локализация септического очага); 3) клинико-морфологические.
По этиологическому признаку выделяют следующие виды сепсиса: стрептококковый, стафилококковый, пневмококковый, гонококковый, синегнойный, колибациллярный, брюшнотифозный, сибиреязвенный, туберкулезный, сифилитический, грибковый и др. Особенно большое значение в развитии сепсиса имеют стафилококк и синегнойная палочка, а также ассоциация этих микробов. Это связано с широким и недостаточно рациональным применением в клинике антибиотиков, причем в больших дозах, а также цитостатических препаратов.
В зависимости от характера входных ворот инфекции (локализации септического очага) различают терапевтический (параинфекционный), тонзиллогенный, хирургический, маточный, отогенный, одонтогенный, пупочный, криптогенный сепсис. Криптогенным (от греч. kryptos - тай-
ный, скрытый) называют сепсис при отсутствии септического очага. Следует иметь в виду, что септический очаг не всегда локализуется в воротах инфекции и может находиться в отдалении от них (например, случаи сепсиса, развивающегося из абсцессов печени после бывшего ранее гнойного аппендицита или язвенного колита).
По клинико-морфологическим признакам выделяют 4 клинико-анатомические формы сепсиса: септицемию, септикопиемию, септический (бактериальный) эндокардит и хрониосепсис.
Септицемия
Септицемия - форма сепсиса, для которой характерны выраженный токсикоз (высокая температура, затемненное сознание), повышенная реактивность организма (гиперергия), отсутствие гнойных метастазов и быстрое течение.
Развитие септицемии часто связано со стрептококком. При вскрытии умерших от септицемии септический очаг, как правило, отсутствует или выражен слабо (входные ворота инфекции не обнаруживаются). Кожа и склеры нередко желтушны (гемолитическая желтуха), отчетливо выражены признаки геморрагического синдрома в виде петехиальной сыпи на коже, кровоизлияний в серозных и слизистых оболочках, во внутренних органах. Характерна гиперплазия лимфоидной и кроветворной тканей. В связи с этим резко увеличиваются селезенка, которая дает обильный соскоб пульпы (септическая селезенка), и лимфатические узлы. В селезенке и лимфатических узлах находят не только пролиферацию лимфоидных и ретикулярных клеток, но и скопления зрелых и незрелых форм клеток гемопоэза. В костном мозге плоских костей и диафизах трубчатых костей отмечается усиленное кроветворение с образованием большого числа юных форм. Появляются также очаги внекостно-мозгового кроветворения. В паренхиматозных органах - сердце, печени, почках - развивается межуточное воспаление (см. рис. 281). Строма этих органов отечна и инфильтрирована нейтрофилами, лимфоцитами, гистиоцитами. Для септицемии характерны повышение сосудисто-тканевой проницаемости, развитие фибриноидных изменений стенок сосудов, аллергических васкулитов, с чем в значительной мере связаны проявления геморрагического синдрома.
Септикопиемия
Септикопиемия - форма сепсиса, при котором ведущими являются гнойные процессы в воротах инфекции и бактериальная эмболия («метастазирование гноя») с образованием гнойников во многих органах и тканях; в отличие от септицемии признаки гиперергии проявляются весьма умеренно, поэтому заболевание не имеет бурного течения. Главная роль в развитии септикопиемии принадлежит стафилококку и синегнойной палочке.
При вскрытии умерших от септикопиемии, как правило, находят септический очаг, обычно расположенный в воротах инфекции, с гнойным
лимфангитом и лимфаденитом, причем ткань лимфатического узла нередко подвергается гнойному расплавлению. В области септического очага обнаруживается также гнойный тромбофлебит, который является источником тромбобактериальной эмболии. В связи с тем что источники последней появляются чаще в венах большого круга кровообращения, первые метастатические гнойники появляются в легких (рис. 283). Затем при вовлечении в процесс легочных вен (тромбофлебит легочных вен) гнойники появляются в органах системы большого круга кровообращения - в печени (абсцессы печени), почках (гнойничковый нефрит), подкожной клетчатке, костном мозге (гнойный остеомиелит), в синовиальных оболочках (гнойный артрит), клапанах сердца (острый септический полипозно-язвенный эндокардит, см. рис. 282). Гнойники могут распространяться на соседние ткани. Например, при абсцессе легкого развиваются гнойный плеврит и перикардит, при метастатическом абсцессе печени - гнойный перитонит; гнойники почки осложняются пери- и паранефритом, гнойники кожи - флегмоной и т.д. Гиперпластические процессы в лимфатической (иммунокомпетентной) и кроветворной тканях выражены слабее, чем при септицемии. Поэтому лимфатические узлы резко не увеличиваются, однако селезенка может быть типично септической, причем в пульпе ее обнаруживается большое число лейкоцитов (септический лейкоцитоз селезенки). В костном мозге омоложение его клеточного состава встречается редко. Межуточные воспалительные реакции в паренхиматозных органах весьма умеренны или отсутствуют.
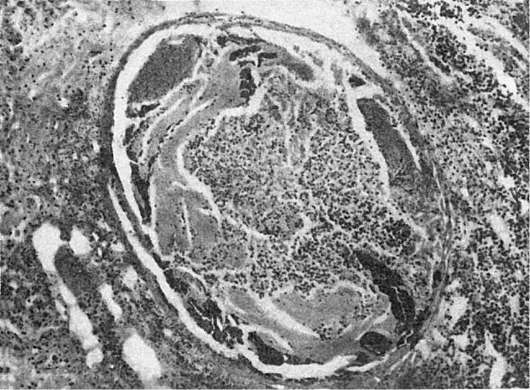 Рис. 283. Тромбобактериальный эмбол в ветви легочной артерии при септикопиемии (препарат А.В. Цинзерлинга)
Рис. 283. Тромбобактериальный эмбол в ветви легочной артерии при септикопиемии (препарат А.В. Цинзерлинга)
Септический (бактериальный) эндокардит
Септический (бактериальный) эндокардит - особая форма сепсиса, для которой характерно септическое поражение клапанов сердца.
При септическом эндокардите выражена гиперергия, в связи с чем его можно рассматривать как бактериальную септицемию. Поскольку септический очаг находится на клапанах сердца, гиперергическому повреждению подвергается прежде всего сердечно-сосудистая система, что определяет своеобразие клинических и патологоанатомических проявлений этого заболевания.
Этиология и патогенез. В настоящее время наиболее частыми возбудителями бактериального эндокардита стали белый и золотистый стафилококк, зеленящий стрептококк (преимущественно L-формы и мутанты), энтерококк. Возросло значение грамотрицательных бактерий - кишечной и синегнойной палочек, клебсиеллы, протея, а также патогенных грибов. Взгляды на патогенез бактериального эндокардита за последние 40 лет подверглись значительной эволюции. Еще в 1942 г. А.И. Абрикосов считал эндокардит (sepsis lenta) гиперергической формой сепсиса. Вскоре на смену этому взгляду пришел диаметрально противоположный: большинство исследователей стали рассматривать септический эндокардит как проявление гиперергии, как септицемию с септическим очагом на клапанах сердца. В настоящее время характер гиперергии расшифрован. Показано, что в ее основе лежат реакции гиперчувствительности, обусловленные воздействием циркулирующих в крови токсических иммунных комплексов, которые содержат антиген возбудителя. С циркулирующими иммунными комплексами связывают многие проявления септического эндокардита: генерализованные васкулиты, резкое повышение сосудистой проницаемости, тромбоэмболический синдром, клеточные реакции стромы и др.
Классификация. Септический (бактериальный) эндокардит разделяют по характеру течения и наличию или отсутствию фонового заболевания.
Исходя из характера течения заболевания выделяют острый, подострый и затяжной (хронический) септический эндокардит. Продолжительность острого септического эндокардита составляет около 2 нед, подострого - до 3 мес, затяжного - многие месяцы и годы.
В настоящее время преобладают подострые и затяжные формы, острые почти исчезли.
В зависимости от наличия или отсутствия фонового заболевания септический эндокардит (особенно подострыи и затяжной) делят на два вида: 1) развивающийся на измененных (порочных) клапанах - вторичный септический эндокардит; 2) возникающий на интактных клапанах - первичный септический эндокардит, описанный в 1949 г. Б.А. Черногубовым (болезнь Черногубова). Вторичный септический эндокардит, по данным вскрытий, наблюдается в 70-80% случаев и преимущественно на фоне ревматического порока сердца; редко он развивается на фоне атеросклеротического, сифилитического или врожденного (тетрада Фалло, сохра-
нившийся артериальный проток и др.) порока. Первичный септический эндокардит отмечают в 20-30% случаев, причем в последнее десятилетие развитие его резко возросло.
Патологическая анатомия. Достаточно характерна и проявляется преимущественно изменениями в сердце, сосудах, селезенке и почках, а также рядом так называемых периферических признаков. Эти изменения сочетаются с тромбоэмболиями, инфарктами и множественными геморрагиями.
Основные изменения касаются клапанов сердца. Преобладает изолированный эндокардит, который, по данным вскрытий, встречается в 60- 75% случаев. В 50% случаев поражаются только аортальные клапаны, в 10-15% - митральный клапан, в 25-30% - аортальный и митральный клапаны, в 5% - другие клапаны. Следовательно, септический эндокардит очень часто (в 75-80%) развивается на аортальных клапанах. Как на склерозированных, так и на несклерозированных клапанах возникает полипозно-язвенный эндокардит (рис. 284). При этом обычно на склерозированных клапанах появляются обширные тромботические наложения в виде полипов, которые легко крошатся и рано пропитываются известью, что весьма характерно для этого заболевания. После удаления этих наложений обнаруживаются язвенные дефекты в склерозированных и деформированных створках клапанов, иногда поверхностные, иногда с нарушением целости клапана, образованием острых аневризм створок или массивным их разрушением. Тромботические наложения располагаются не только на створках, но и на пристеночном эндокарде, а при поражении аортальных клапанов распространяются на интиму аорты.
При микроскопическом исследовании удается установить, что процесс начинается с образования очагов некроза ткани клапана, вокруг которых наблюдается инфильтрация из лимфоидных клеток, гистиоцитов, многоядерных макрофагов, нейтрофилы отсутствуют или их очень мало.
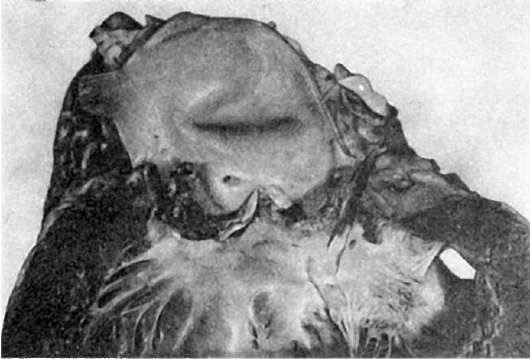 Рис. 284. Хронический полипозно-язвенный эндокардит
Рис. 284. Хронический полипозно-язвенный эндокардит
Среди клеток инфильтрата встречаются колонии бактерий. В участках некроза появляются массивные тромботические наложения, которые организуются. Разрастающаяся грануляционная ткань при созревании деформирует створки, что ведет к формированию порока сердца. Если эндокардит развился на порочных клапанах, то склероз их усиливается. В миокарде отмечается гипертрофия мышечных волокон, выраженность которой в стенках той или иной полости сердца зависит от характера порока. В межуточной ткани миокарда встречаются гистиолимфоцитарные инфильтраты и узелки, напоминающие ашофф-талалаевские гранулемы. В сосудах миокарда обнаруживают плазматическое пропитывание и фибри-ноидный некроз стенок, эндо- и периваскулиты.
В сосудистой системе, особенно в микроциркуляторном русле, находят распространенные альтеративно-продуктивные изменения. Они представлены плазморрагией и фибриноидным некрозом стенок капилляров, артериол и вен, эндо- и периваскулитами. Воспалительные изменения в стенках артерий мелкого и среднего калибра приводят к развитию аневризм, разрыв которых может оказаться смертельным (например, кровоизлияние в ткань головного озга). Преобладают явления повышенной сосудистой проницаемости, с которыми в значительной мере связано развитие геморрагического синдрома. Появляются множественные петехиальные кровоизлияния на коже, в серозных и слизистых оболочках, а также в конъюнктиве глаз.
Селезенка в результате длительной гиперплазии пульпы, как правило, увеличена, с инфарктами различной давности (рис. 285). В почках развивается иммунокомплексный диффузный гломерулонефрит. Нередко наблюдаются инфаркты и рубцы после них. Во многих органах обнаруживают межуточные воспалительные процессы, васкулиты, кровоизлияния, инфаркты. В головном мозге, в частности, на почве сосудистых изменений (васкулиты, аневризмы) и тромбоэмболии возникают очаги размягчения и кровоизлияния. Среди так называемых периферических признаков септического эндокардита характерными считаются: 1) петехиальные кровоизлияния в конъюнктиве глаз у внутреннего угла нижнего века (пятна Лукина-Либмана); 2) узелковые утолщения на ладонных поверхностях кистей (узелки Ослера); 3) утолщения ногтевых фаланг («барабанные палочки»); 4) очаги некроза в подкожной жировой клетчатке; 5) кровоиз-
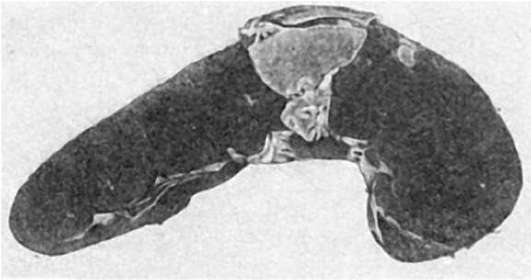 Рис. 285. Инфаркт селезенки при хроническом септическом эндокардите
Рис. 285. Инфаркт селезенки при хроническом септическом эндокардите
лияния в кожу и подкожную клетчатку (пятна Джейнуэя); 6) желтуха. В настоящее время из периферических признаков септического эндокардита постоянно встречаются лишь узелки Ослера.
Тромбоэмболические осложнения находят исключительно часто, так как источник тромбоэмболии - тромбоэндокардит - в подавляющем большинстве случаев локализуется в левом сердце. Тромбоэмболии нередко принимают распространенный характер и доминируют в клинической картине болезни. В этих случаях говорят о тромбоэмболическом синдроме. На почве эмболии могут развиваться инфаркты в легких, селезенке, почках, сетчатке глаза, некрозы кожи, гангрена конечностей, кишок, очаги размягчения в мозге. Несмотря на наличие в тромбоэмболах стрептококков, нагноение в тканях отсутствует, что свидетельствует о гиперергической реакции организма при септическом эндокардите.
Патоморфоз. За последние десятилетия произошли значительные изменения в клинической и морфологической картине (патоморфоз) септического эндокардита. До применения антибиотиков септический эндокардит относился к числу крайне тяжелых болезней, неизбежно ведущих к смерти. Лечение массивными дозами антибиотиков приводит к ликвидации септического процесса на клапанах, ускоряет созревание грануляций в ткани створок клапанов и тем самым избавляет организм от септического очага, но способствует деформации клапанов, развитию или усилению предсуществовавшего порока сердца. Через несколько лет после начала лечения обычно появляются признаки сердечной декомпенсации, которые приводят к смерти. При вскрытии умерших от декомпенсации сердца после излечения от септического процесса находят чаще аортальный или аортально-митральный порок сердца с резко выраженной деформацией клапанов, перфорацией створок и заслонок и тяжелые дистрофические изменения миокарда. Патоморфоз септического эндокардита касается также его этиологии (преобладание стафилококка и грамотрицательных бактерий), структуры (учащение первичного септического эндокардита), клиники, морфологии, осложнений.
Хрониосепсис
Хрониосепсис характеризуется наличием длительно не заживающего септического очага и обширных нагноений. Такие септические очаги находят в кариозных зубах, миндалинах, однако чаще ими являются обширные нагноения, возникающие после ранений. Гной и продукты распада тканей всасываются, ведут к интоксикации, нарастающему истощению и развитию амилоидоза. В годы войны случаи хрониосепсиса наблюдались довольно часто. Существует мнение (Давыдовский И.В., 1944), что подобные состояния не являются сепсисом, а представляют собой гнойнорезорбтивную лихорадку, ведущую к травматическому истощению.
Изменения в органах и тканях при хрониосепсисе носят в основном атрофический характер. Выражены истощение, обезвоживание. Селезенка уменьшается. В печени, миокарде, поперечнополосатой мускулатуре обнаруживается бурая атрофия.
Грибковые заболевания (микозы)
Микозы - большая группа заболеваний с разнообразными клиникоморфологическими проявлениями. При одних микозах происходит экзогенное заражение, при других - эндогенное, т.е. развивается аутоинфекция под влиянием тех или иных неблагоприятных факторов. В связи с этим целесообразно разделить все микозы на экзогенные и эндогенные. К экзогенным микозам относят трихофитию, паршу, актиномикоз, нокардиоз, кокцидиоидомикоз, риноспоридиоз и гистоплазмоз. При этих заболеваниях обнаружение в тканях гриба (мицелий, органы плодоношения, споры) позволяет ставить диагноз. В группу эндогенных микозов включают кандидозы, европейский бластомикоз, аспергиллез, пенициллез, мукормикоз. Возбудители этих микозов часто находятся в качестве сапрофитов на слизистых оболочках здоровых людей, не вызывая изменений (миконосительство). Однако под влиянием неблагоприятных факторов возникает дисбактериоз и грибы проявляют патогенное действие. Отмечаемое за последнее десятилетие увеличение заболеваемости микозами происходит главным образом за счет форм, развивающихся на почве дисбактериоза при лечении иммунодепрессантами и цитостатическими препаратами.
Различают грибковые заболевания кожи - дерматомикозы и внутренних органов - висцеральные микозы.
Дерматомикозы
Дерматомикозы разделяют на три группы: эпидермомикозы, поверхностные и глубокие дерматомикозы.
Эпидермомикозы характеризуются поражением эпидермиса и вызываются эпидермофитами различных видов. Наиболее частыми формами этой группы микозов являются отрубевидный (разноцветный) лишай и эпидермофития. При поверхностных дерматомикозах основные изменения развиваются в эпидермисе, хотя дерма не остается интактной. Наибольшее практическое значение имеют трихофития и парша. Глубокие дерматомикозы характеризуются поражением главным образом собственно дермы, но страдает также и эпидермис.
Висцеральные микозы
Висцеральные микозы, т.е. грибковые поражения внутренних органов, весьма разнообразны. Чаще они вызываются дрожжевыми и дрожжеподобными плесневыми грибами, актиномицетами и др. Однако в редких случаях, например при трихофитии, парше, поражение внутренних органов могут вызвать некоторые поверхностные дерматофиты. Эти тяжелые формы заболевания, встречающиеся у ослабленных людей, сопровождаются кахексией и обычно заканчиваются смертью.
Классификация. По этиологическому принципу висцеральные микозы делят на 4 группы: 1) заболевания, вызываемые лучистыми грибами: актиномикоз, нокардиоз (стрептотрихоз); 2) заболевания, вызываемые
дрожжеподобными и дрожжевыми грибами: кандидоз, бластомикозы; 3) заболевания, вызываемые плесневыми грибами: аспергиллез, пенициллез, мукормикоз; 4) заболевания, вызываемые другими грибами: кокцидиоидомикоз, риноспоридиоз, споротрихоз, гистоплазмоз.
Заболевания, вызываемые лучистыми грибами
Актиномикоз - висцеральный микоз, характеризующийся хроническим течением, образованием гнойников и гранулем. Вызывается анаэробным лучистым грибом Actinomyces Israeli, попадающим в организм чаще всего через пищеварительный тракт или дыхательные пути. Возбудитель находят в кариозных зубах, криптах миндалин у здоровых людей, поэтому считают, что эндогенный способ заражения является наиболее вероятным. Большое значение в развитии актиномикоза имеют травма и проникновение гриба с инородными телами. Различают первичные (локальные) и вторичные проявления актиномикоза. Вторичный актиномикоз возникает при переходе процесса с соседнего органа, ткани или при распространении гриба гематогенным путем - генерализованный актиномикоз.
Патологическая анатомия. При попадании гриба в ткань вокруг него развиваются гиперемия, стаз, затем появляются усиленная эмиграция нейтрофилов и формирование небольшого гнойника. Вокруг него происходит пролиферация макрофагов, молодых соединительнотканных элементов, плазматических клеток, появляются ксантомные клетки, новообразованные сосуды. Образуется актиномикотическая гранулема. По соседству с ней образуются новые гранулемы, они сливаются. Так формируются иногда обширные очаги актиномикотического поражения (инфильтрации) ткани, в которых участки гнойного расплавления окружены созревающими грануляциями и зрелой соединительной тканью. Очаги актиномикоза плотны, на разрезе желто-зеленоватой окраски, множество мелких гнойничков придает ткани сотовидное строение. В гное видны белые крупинки - друзы актиномицета (рис. 286). Друзы состоят из многочисленных коротких палочковидных элементов гриба, прикреплен-
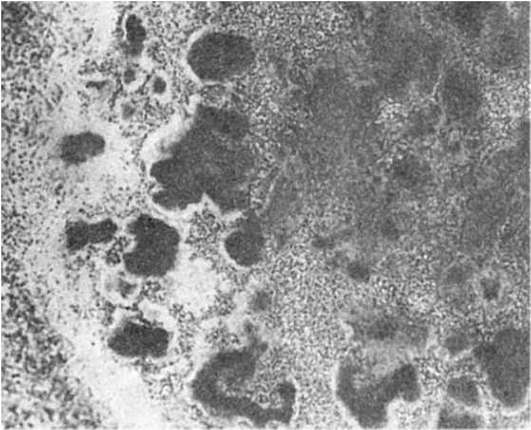 Рис. 286. Актиномикоз. Друзы актиномицета в гное
Рис. 286. Актиномикоз. Друзы актиномицета в гное
ных одним концом к гомогенному центру, который представляет собой конгломерат из переплетающегося мицелия. Считают, что в образовании друз принимают участие преципитирующие белки тканей.
Заболевание течет длительно, причем распространение актиномикотического инфильтрата происходит по клетчатке и соединительнотканным прослойкам органов и тканей. Он всегда направляется к свободной поверхности органов или тканей, где открывается свищами. В одних случаях преобладает разрушение ткани с образованием крупных гнойников (деструктивная форма), в других разрастание соединительной ткани сочетается с деструктивными изменениями (деструктивно-пролиферативная форма). В зависимости от локализации актиномикоз делят на шейнолицевой (наиболее частое проявление), актиномикоз легких и органов грудной клетки, абдоминальный, костно-суставной и мышечный, актиномикоз кожи, нервной системы и других органов.
Наиболее тяжелым осложнением актиномикоза является амилоидоз.
Заболевания, вызываемые дрожжеподобными и дрожжевыми грибами
Кандидоз (кандидамикоз, монилиаз, оидиомикоз), или молочница, - одно из наиболее распространенных и частых проявлений висцеральных микозов. Вызывается дрожжеподобными грибами рода Candida, главным образом Candida albicans. Эти грибы спор не образуют, размножаются почкованием, причем дрожжевые клетки располагаются в виде нитей псевдомицелия, хорошо выявляемых с помощью ШИК-реакции. Принято различать кандиданосительство и кандидоз как заболевание.
Кандидоз - один из ярких примеров аутоинфекции, возникающей под влиянием каких-либо факторов, чаще всего неправильного применения антибиотиков и кортикостероидов; при этом большое значение имеет повышенная чувствительность организма к продуктам жизнедеятельности гриба. Различают кандидоз первичный, наблюдающийся обычно у маленьких детей без провоцирующих факторов, и вторичный - после каких-либо воздействий на организм (вирусная инфекция).
Патологическая анатомия. Кандидоз встречается в виде локальной (например, кандидоз кожи, слизистых оболочек пищеварительного тракта, мочевых путей и почек, легких, раневых поверхностей и др.) и генерализованной форм.
При локальном кандидозе наиболее часто поражаются слизистые обо- лочки, покрытые многослойным плоским эпителием. Это объясняется известным тропизмом гриба к эпителию, богатому гликогеном, каковым и является многослойный плоский эпителий. В слизистой оболочке гриб растет поверхностно, при этом появляются буроватые наложения, состоящие из переплетающихся нитей псевдомицелия, слущенных клеток эпителия и нейтрофилов. При проникновении гриба в толщу слизистой оболочки появляются фокусы ее некроза. Некротические участки отграничиваются от здоровой ткани демаркационным валом нейтрофилов. Прорастание псевдомицелия в просвет сосуда обусловливает развитие метастазов. Во внутренних органах вокруг грибов появляется клеточный
инфильтрат, также состоящий преимущественно из распадающихся нейтрофилов, как бы нанизанных на нити псевдомицелия. У ослабленных больных очажки имеют не гнойный, а некротический характер. При недостаточной сопротивляемости организма по периферии лейкоцитарного инфильтрата образуется вал из грануляционной ткани, в которой грибы обнаруживаются редко. Если заболевание растягивается во времени, преобладает продуктивная реакция, появляются гранулемы, состоящие главным образом из макрофагов, фибробластов и гигантских многоядерных клеток, содержащих в цитоплазме обрывки нитей и почкующиеся формы гриба.
При кандидозе пищеварительного тракта поражаются все его отделы. Кандидоз пищевода наиболее часто встречается в раннем детском возрасте. На слизистой оболочке пищевода образуются пленки, которые в ряде случаев почти полностью закрывают его просвет. Поражения желудка встречаются сравнительно редко. Однако грибы могут обнаруживаться при язвенной болезни в дне язвы и быть источником генерализованного кандидоза. Поражение кишечника (рис. 287) представлено язвами и псевдомембранозными наложениями.
Кандидоз мочевыводящих путей и почек возникает восходящим путем и не имеет каких-либо специфических черт. В корковом слое почек появляются мелкие гнойнички, очаги некроза или гранулемы, содержащие элементы гриба. Проникновение грибов в просвет канальцев может вести к появлению грибов в моче, что имеет диагностическое значение.
Кандидоз легких обычно сочетается с тяжелым и распространенным кандидозом пищеварительного тракта; реже он протекает изолированно. При остром течении заболевания появляются мелкие очажки фибринозного воспаления с некрозом в центре. В дальнейшем происходят нагноение этих очажков и образование полостей. При затянувшемся течении
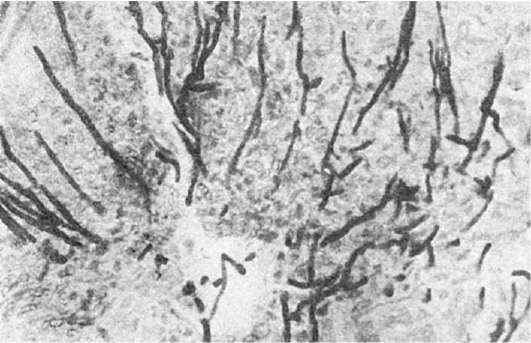 Рис. 287. Кандидоз. Грибковый колит. Врастание гриба Candida в ткань фолликула толстой кишки
Рис. 287. Кандидоз. Грибковый колит. Врастание гриба Candida в ткань фолликула толстой кишки
вокруг очажков некроза и пневмонии возникает продуктивная тканевая реакция, появляется грануляционная ткань, и процесс заканчивается фиброзом. Мелкие бронхи при кандидозе легких поражаются постоянно, в их просвете видны нити гриба и обильный лейкоцитарный экссудат. Грибы могут прорасти стенку бронха, что ведет в тяжелых случаях к ее некрозу. Поражение верхних дыхательных путей встречается сравнительно редко.
О генерализованном кандидозе говорят в тех случаях, когда грибы из первичных очагов попадают в кровяное русло, в результате чего в органах и тканях (головном мозге и его оболочках, сердце, легких, почках) появляются метастатические очаги. Речь идет о кандидозной септикопиемии (см. Сепсис).
Бластомикоз - группа заболеваний кожи и внутренних органов, вызываемых бластомицетами - дрожжеподобными грибами. Выделяют несколько видов бластомикоза, среди которых наибольшее значение имеет европейский бластомикоз Бруссе-Бушке (криптококкоз, торулез).
Заболевания, вызываемые плесневыми грибами
Аспергиллез - заболевание, встречающееся у человека, животных и птиц. Оно вызывается несколькими видами Aspergillus (чаще Aspergillus fumigatus), которые, являясь аэробами, широко распространены в природе и постоянно вегетируют в почве. Аспергиллез наблюдается обычно у лиц, которые подвергаются массивному воздействию продуктов, содержащих грибы. Так, аспергиллез легких особенно часто встречается у людей определенных профессий, например у вскармливающих голубей (изо рта человека непосредственно в клюв голубя), у чесальщиков волос. Чаще встречается аэрогенное заражение. Аспергиллез как аутоинфекция развивается у больных, получающих большие дозы антибиотиков, стероидные гормоны и цитостатические средства.
Патологическая анатомия. Наиболее характерен легочный аспергиллез - первый легочный микоз человека, который описали Слайтер (1847) и Р. Вирхов (1851). Различают 4 типа легочного аспергиллеза как самостоятельного заболевания: 1) негнойный легочный аспергиллез, при котором образуются серо-бурые плотные очаги с белесоватым центром, где среди инфильтрата определяются скопления гриба; 2) гнойный легочный аспергиллез, которому свойственно образование очагов некроза и нагноения; 3) аспергиллез-мицетома - своеобразная форма поражения, при которой имеется бронхоэктатическая полость или легочный абсцесс. Возбудитель растет по внутренней поверхности полости, образует толстые, сморщенные мембраны, которые слущиваются в просвет полости; 4) туберкулоидный легочный аспергиллез, характеризующийся появлением узелков, сходных с туберкулезными.
Аспергиллез нередко присоединяется к хроническим легочным заболеваниям: бронхиту, бронхоэктатической болезни, абсцессу, раку легкого, фиброзно-кавернозному туберкулезу. В этих случаях стенка бронха, каверны оказываются как бы выстланными тонким слоем плесени. В та-
ких случаях можно говорить о сапрофитном существовании аспергиллеза на определенной патологической основе.
Заболевания, вызываемые другими грибами
Из других висцеральных микозов встречаются, но редко кокцидиоидомикоз, гистоплазмоз, риноспоридиоз и споротрихоз.
Болезни, вызываемые простейшими и гельминтами
Болезни, вызываемые простейшими и гельминтами, называют инвазионными. Эта группа болезней велика и разнообразна. Наибольшее значение среди заболеваний, вызываемых простейшими, имеют малярия, амебиаз и балантидиаз, а среди заболеваний, вызываемых гельминтами, - эхинококкоз, цистицеркоз, описторхоз и шистосомоз.
Малярия
Малярия (от лат. mala aria - плохой воздух) - острое или хроническое рецидивирующее инфекционное заболевание, имеющее различные клинические формы в зависимости от срока созревания возбудителя; характеризуется лихорадочными пароксизмами, гипохромной анемией, увеличением селезенки и печени.
Этиология и патогенез. Заболевание вызывается несколькими видами простейших рода Plasmodium (впервые плазмодий малярии был обнаружен в эритроцитах А. Лавераном в 1880 г.). Попав в кровь при укусе комара, плазмодии проделывают сложный цикл развития, паразитируют в эритроцитах человека, размножаясь бесполым путем, который называют шизогонией. Шизонты паразита накапливают в цитоплазме частицы темно-бурого пигмента - гемомеланина. При гемолизе паразиты и гемомеланин высвобождаются из эритроцита, причем пигмент фагоцитируется клетками макрофагальной системы, а шизонты вновь внедряются в эритроциты. В связи с этим развиваются надпеченочная (гемолитическая) анемия, гемомеланоз и гемосидероз элементов ретикуло-эндотелиальной системы, завершающийся склерозом. В периоды гемолитических кризов появляются острые сосудистые расстройства (стаз, диапедезные кровоизлияния). В связи с персистирующей антигенемией при малярии в крови появляются токсические иммунные комплексы. С их воздействием связано поражение микроциркуляторного русла (повышение проницаемости, геморрагии), а также развитие гломерулонефрита.
Патологическая анатомия. В связи с существованием нескольких видов малярийного плазмодия, различающихся по срокам их созревания, выделяют трехдневную, четырехдневную и тропическую формы малярии.
При трехдневной малярии, наиболее частой, в связи с разрушением эритроцитов развивается анемия, тяжесть которой усугубляется свойством плазмодиев трехдневной малярии поселяться в молодых эритроцитах - ретикулоцитах (Войно-Ясенецкий М.В., 1950). Высвобождающиеся при распаде эритроцитов продукты, особенно гемомеланин, захватываются
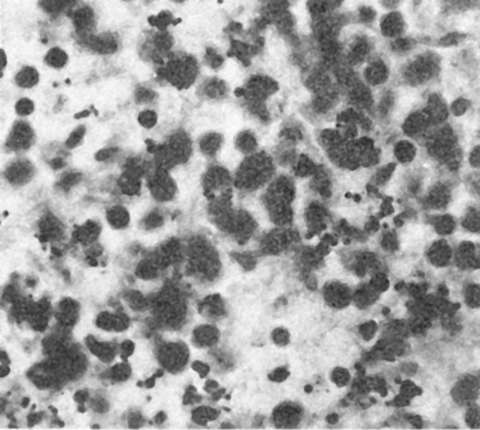 Рис. 288. Малярия. Зерна гемомеланина в макрофагах селезенки
Рис. 288. Малярия. Зерна гемомеланина в макрофагах селезенки
клетками макрофагальной системы, что приводит к увеличению селезенки и печени, гиперплазии костного мозга. Органы, загруженные пигментом, приобретают темно-серую, а иногда черную окраску. Селезенка увеличивается особенно быстро, вначале в результате полнокровия, а затем - гиперплазии клеток, фагоцитирующих пигмент (рис. 288). Пульпа ее становится темной, почти черной. В острой стадии малярии селезенка мягкая, полнокровная, в хронической - плотная вследствие развивающегося склероза; масса ее достигает 3-5 кг (малярийная спленомегалия). Печень - увеличена,
полнокровна, на разрезе серо-черная. Отчетливо выражена гиперплазия звездчатых ретикулоэндотелиоцитов с отложением в их цитоплазме гемомеланина. При хронической малярии отмечаются огрубение стромы печени и разрастание в ней соединительной ткани. Костный мозг плоских и трубчатых костей имеет темно-серую окраску, отмечается гиперплазия его клеток и отложение в них пигмента. Встречаются участки аплазии костного мозга. Гемомеланоз органов гистиоцитарно-макрофагальной системы сочетается с их гемосидерозом. Развивается надпеченочная (гемолитическая) желтуха. Патологическая анатомия четырехдневной малярии подобна таковой при трехдневной малярии.
При тропической малярии изменения, с одной стороны, имеют много общего с описанными при трехдневной форме, с другой - отличаются некоторыми особенностями. Они объясняются тем, что эритроциты, содержащие дозревающие шизонты тропической малярии, скапливаются в терминальных участках кровяного русла, что ведет к развитию паразитарных стазов. В местах скопления дозревающих шизонтов в период деления их на мерозоиты происходит фагоцитоз нейтрофилами и макрофагами как зараженных эритроцитов и незрелых шизонтов, так и продуктов распада и пигмента, появляющихся после деления плазмодиев (ВойноЯсенецкий М.В., 1950). С паразитарными стазами связаны опасные для жизни изменения головного мозга, которые определяют развитие малярийной комы. Кора и другие участки серого вещества головного мозга имеют в таких случаях темную коричнево-серую (дымчатую) окраску. В белом веществе встречаются многочисленные точечные кровоизлияния, которые окружают сосуды, заполненные агглютинированными эритроцитами с паразитами в цитоплазме или гиалиновыми тромбами. Вокруг таких сосудов, помимо кровоизлияний, появляются очаги некроза мозговой ткани. На границе некроза и кровоизлияния через 2 сут от начала
комы находят реактивное разрастание клеток глии, что ведет к формированию своеобразных узелков - так называемых гранулем Дюрка.
Осложнением острой малярии может быть гломерулонефрит, хронической - истощение, амилоидоз.
Смерть наблюдается обычно при тропической малярии, осложненной комой.
Амебиаз
Амебиаз, или амебная дизентерия, - хроническое протозойное заболевание, в основе которого лежит хронический рецидивирующий язвенный колит.
Этиология и патогенез. Амебиаз вызывается простейшим из класса корненожек - Entamoeba histolytica. Возбудитель открыт Ф.А. Лешом (1875) в испражнениях больных амебиазом. Заболевание встречается главным образом в странах с жарким климатом, а в СССР - республиках Средней Азии. Заражение происходит алиментарным путем инцистированными амебами, защищенными от действия пищеварительных соков особой оболочкой, которая расплавляется в слепой кишке, где и наблюдаются обычно наиболее выраженные морфологические изменения.
Гистологические свойства амебы объясняют глубокое ее проникновение в стенку кишки и образование незаживающих язв. У некоторых лиц отмечается носительство амеб в кишечнике.
Патологическая анатомия. Попадая в стенку толстой кишки, амеба и продукты ее жизнедеятельности вызывают отек и гистолиз, некроз слизистой оболочки, образование язв. Некротически-язвенные изменения наиболее часто и резко выражены в слепой кишке (хронический язвенный колит). Однако нередки случаи, когда язвы образуются на всем протяжении толстой кишки и даже в подвздошной кишке. При микроскопическом исследовании видно, что участки некроза слизистой оболочки несколько выбухают над ее поверхностью, они окрашены в грязно-серый или зеленоватый цвет. Зона некроза проникает глубоко в подслизистый и мышечный слои. При образовании язвы края ее становятся подрытыми и нависают над дном. По мере прогрессирования некроза размеры язвы увеличиваются. Амеб находят на границе между омертвевшими и сохранившимися тканями. Характерно, что клеточная реакция в стенке кишки выражена слабо. Однако по мере присоединения вторичной инфекции возникает инфильтрат из нейтрофилов, появляется гной. Иногда развиваются флегмонозная и гангренозная формы колита. Глубокие язвы заживают рубцом. Характерны рецидивы заболевания.
Регионарные лимфатические узлы несколько увеличены, но амебы в них не обнаруживаются; амебы обычно находят в кровеносных сосудах стенки кишки.
Осложнения амебиаза делят на кишечные и внекишечные. Из кишечных наиболее опасны прободение язвы, кровотечение, образование стенозирующих рубцов после заживления язв, развитие воспалительных
инфильтратов вокруг пораженной кишки, которые нередко симулируют опухоль. Из внекишечных осложнений наиболее опасным является развитие абсцесса печени.
Балантидиаз
Балантидиаз - инфекционное протозойное заболевание, характеризующееся развитием хронического язвенного колита. Редко отмечается изолированное поражение червеобразного отростка.
Этиология и патогенез. Возбудителем балантидиаза является инфузория Balantidium coli, описанная Р. Мальмстеном в 1857 г. Основной источник инфекции - свиньи, а также больной балантидиазом человек. Передается инфекция через загрязненную воду и контактным путем. Наблюдается заболевание чаще среди людей, занимающихся свиноводством. Проникнув в организм через рот, балантидии накапливаются преимущественно в слепой кишке, реже - в нижнем отделе тонкой кишки. Размножаясь в просвете кишки, они могут не вызывать симптомов болезни, что рассматривается как носительство. При внедрении балантидии в слизистую оболочку кишки, чему способствует выделяемая ими гиалуронидаза, образуются характерные язвы.
Патологическая анатомия. Изменения при балантидиазе сходны с таковыми при амебиазе, однако при балантидиазе, который встречается значительно реже амебиаза, поражение кишки не столь резко выражено. Вначале наблюдается поражение поверхностных слоев слизистой оболочки с образованием эрозий. В дальнейшем, по мере проникновения балантидии в подслизистый слой, развиваются язвы, которые имеют разную величину и форму, края их подрыты, на дне видны серо-грязные остатки некротических масс. Балантидии обнаруживаются обычно по соседству с очагами некроза, а также в криптах и толще слизистой оболочки вдали от язв. Они могут проникать в мышечный слой, в просвет лимфатических и кровеносных сосудов. Местные клеточные реакции при балантидиазе выражены слабо, среди клеток инфильтрата преобладают эозинофилы.
Осложнения. Важнейшее из осложнений балантидиаза - прободение язвы с развитием перитонита. Присоединение к язвенному процессу вторичной инфекции может привести к септикопиемии.
Эхинококкоз
Эхинококкоз (от греч. echinos - еж, kokkos - зерно) - гельминтоз из группы цестодозов, характеризующийся образованием эхинококковых кист в различных органах.
Этиология, эпидемиология и патогенез. Наибольшее значение в патологии человека и животных имеют Echinococcus granulosus, вызывающий гидатидозную форму эхинококкоза, и Echinococcus multilocularis, вызывающий альвеолярную форму эхинококкоза, или альвеококкоз. Гидатидозный эхинококкоз встречается чаще, чем альвеококкоз.
В развитии гидатидозного эхинококкоза у человека большая роль принадлежит облигатному хозяину половозрелого ленточного червя: в природе - плотоядным животным (волки, шакалы и др.), в культурных очагах - собаке. У них паразит обитает в кишечнике. Личинка альвеококка, отличающаяся от личинки гидатидозного эхинококка, обнаруживается у грызунов и человека. Охота и скотоводство на пастбищах, загрязненных фекалиями зараженных хищников, приводят к заражению скота (коровы, олени и др.), поедающего загрязненную траву, и собак, которым скармливают внутренности убитых диких животных. Это обусловливает появление смешанных очагов инвазии. Заражение человека происходит в очагах инвазии при тесном контакте с зараженными собаками, при разделке туш пораженных животных, пользовании загрязненными природными водоисточниками. Следует подчеркнуть, что альвеококкоз характеризуется определенной географической патологией. В нашей стране он чаще наблюдается в Якутии, Казахстане, очень редко - в Европейской части СССР. Очаги альвеококкоза встречаются также в некоторых странах Европы.
Патологическая анатомия. При гидатидозном эхинококкозе в органах появляются пузыри (или один пузырь) той или иной величины (от ореха до головы взрослого человека). Они имеют беловатую слоистую хитиновую оболочку и заполнены прозрачной бесцветной жидкостью. В жидкости белок отсутствует, но содержится янтарная кислота. Из внутреннего герминативного слоя оболочки пузыря возникают дочерние пузыри со сколексами. Эти дочерние пузыри заполняют камеру материнского пузыря (однокамерный эхинококк). Ткань органа, в котором развивается однокамерный эхинококк, подвергается атрофии. На границе с эхинококком разрастается соединительная ткань, образуя вокруг пузыря капсулу. В капсуле обнаруживаются сосуды с утолщенными стенками и очаги клеточной инфильтрации с примесью эозинофилов. В участках капсулы, прилегающей непосредственно к хитиновой оболочке, появляются гигантские клетки инородных тел, фагоцитирующие элементы этой оболочки. Чаще эхинококковый пузырь обнаруживается в печени, легких, почках, реже - в других органах.
При альвеококкозе онкосферы дают начало развитию сразу нескольких пузырей, причем вокруг них появляются очаги некроза. В пузырях альвеококкоза образуются выросты цитоплазмы, и рост пузырей происходит путем почкования наружу, а не внутрь материнского пузыря, как это имеет место при однокамерном эхинококке. В результате этого при альвеококкозе образуются все новые и новые пузыри, проникающие в ткань, что ведет к ее разрушению. Поэтому альвеококк называют также многокамерным эхинококком. Следовательно, рост альвеококка имеет инфильтрирующий характер и подобен росту злокачественного новообразования. Выделяющиеся из пузырьков токсические вещества вызывают в окружающих тканях некроз и продуктивную реакцию. В грануляционной ткани много эозинофилов и гигантских клеток инородных тел, фагоцитирующих оболочки погибших пузырьков (рис. 289).
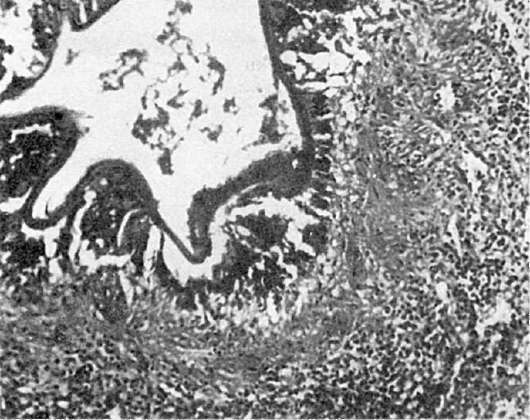 Рис. 289. Альвеококкоз. Среди некротических масс - пузыри эхинококка, окруженные зоной продуктивного воспаления
Рис. 289. Альвеококкоз. Среди некротических масс - пузыри эхинококка, окруженные зоной продуктивного воспаления
Первично альвеококк чаще встречается в печени: реже - в других органах. В печени он занимает целую долю, очень плотен (плотность доски), на разрезе имеет пористый вид с прослойками плотной соединительной ткани. В центре узла иногда образуется полость распада. Альвеококк склонен к гематогенному и лимфогенному метастазированию. Гематогенные метастазы альвеококка при первичной локализации его в печени появляются в легких, затем в органах большого круга кровообращения - почках, головном мозге, сердце и др. В связи с этим клинически альвеококк ведет себя как злокачественная опухоль.
Осложнения. При эхинококкозе осложнения чаще связаны с ростом пузыря в печени или метастазами альвеококка. Возможно развитие амилоидоза.
Цистицеркоз
Цистицеркоз - хронический гельминтоз из группы цестодозов, который вызывается цистицерками вооруженного (свиного) цепня (солитера).
Этиология, эпидемиология, патогенез. Цистицерк является личиночной стадией (финной) свиного цепня. Заболевание развивается у людей, а также у некоторых животных (свиньи, собаки, кошки), являющихся промежуточными хозяевами паразита и его финнозной стадии. Животные заражаются, поедая каловые массы человека, содержащие яйца гельминта. Человек заражается при употреблении в пищу мяса свиней, в котором паразитирует цистицерк. Развитие финны во взрослого паразита происходит в кишечнике человека. При паразитировании свиного солитера в кишечнике у человека может развиться цистицеркоз. Это происходит при
попадании яиц солитера в желудок, где их оболочка растворяется, зародыши проникают через стенку желудка в просвет сосудов, переносятся в различные ткани и органы, где и превращаются в цистицерки.
Патологическая анатомия. Цистицерки обнаруживаются в самых разнообразных органах, но чаще всего в головном мозге, глазе, мышцах, подкожной клетчатке. В мягких мозговых оболочках основания головного мозга наблюдается ветвистый (рацемозный) цистицерк. Наиболее опасен цистицерк головного мозга и глаза.
При микроскопическом исследовании цистицерк имеет вид пузырька величиной с горошину. От его стенки внутрь отходит головка с шейкой. Вокруг цистицерка развивается воспалительная реакция. Инфильтрат состоит из лимфоцитов, плазматических клеток, фибробластов, эозинофилов. Вокруг инфильтрата постепенно появляется молодая соединительная ткань, которая созревает и образует вокруг цистицерка капсулу. В головном мозге в формировании капсулы вокруг цистицерка принимают участие клетки микроглии. С течением времени цистицерк погибает и обызвествляется.
Описторхоз
Описторхоз - заболевание человека и млекопитающих из группы трематодозов. Первое описание морфологии описторхоза принадлежит русскому патологоанатому К.Н. Виноградову (1891).
Этиология, эпидемиология, патогенез. Для человека наибольшее значение имеет инвазия Opistorchia felineus (двуустка кошачья). Человек и плотоядные животные, зараженные описторхозом, являются источником инвазии для моллюсков битиний, которые заглатывают яйца паразита, попавшие в воду с фекалиями больных людей и животных. В организме моллюсков размножаются личиночные стадии гельминта, что заканчивается выходом в воду церкариев. Они проникают через кожу рыб в их подкожную клетчатку и мышцы, превращаясь здесь в метацеркариев. Заражение описторхозом человека и млекопитающих происходит при употреблении в пищу сырой рыбы с личинками гельминта (метацеркариями). Оптимальной средой обитания для двуусток становятся желчные пути.
Патологическая анатомия. Основные изменения развиваются в желчных путях и паренхиме печени. Во внутрипеченочных желчных протоках, где находится большое число паразитов, развивается воспаление - холангит. Стенки протоков инфильтрированы лимфоидными элементами, плазматическими клетками, эозинофилами. Эпителий образует реактивные разрастания с формированием железистых структур в подэпителиальном слое. В исходе развиваются склероз стенок протоков и перидуктальный склероз. В паренхиме печени появляются участки некроза, которые замещаются разрастающейся соединительной тканью. Склеротические изменения в печени имеют очаговый характер и связаны с преимущественной локализацией паразитов в желчных путях. В стенке желчного пузыря также возникает воспаление - холецистит.
В поджелудочной железе отмечаются расширение протоков, в которых находят скопления гельминтов, гиперплазия слизистой оболочки, воспалительные инфильтраты в стенке протоков и строме железы - панкреатит.
Осложнения. Присоединение вторичной инфекции желчных путей приводит к развитию гнойного холангита и холангиолита. При длительном течении описторхоза возможен цирроз печени. В результате длительной и извращенной пролиферации эпителия желчных путей иногда развивается холангиоцеллюлярный рак печени.
Шистосомоз
Шистосомоз - хронический гельминтоз, вызываемый трематодами рода Schistosoma, с преимущественным поражением мочеполовой системы и кишечника.
Этиология. Возбудителем этого гельминта у человека являются Schistosoma haematobium (мочеполовой шистосомоз), Schistosoma mansoni (кишечный шистосомоз) и Schistosoma japonicum (японский шистосомоз с явлениями аллергии, развитием колита, гепатита, цирроза печени). Шистосомоз мочеполовой системы, который впервые был обнаружен Бильгарцом, получил название бильгарциоза.
Эпидемиология и патогенез. Яйца паразита проделывают свой цикл развития в организме пресноводных моллюсков до стадии церкариев, которые и внедряются через кожу в организм человека. Церкарии очень быстро созревают и превращаются в шистосомулы, проникающие в периферические вены, где и образуются половозрелые особи. Отсюда оплодотворенные самки направляются к месту излюбленного обитания: вены таза, мезентериальные и геморроидальные вены, а также в стенку толстой кишки. Здесь самки откладывают яйца, что вызывает повреждение ткани. Часть яиц выделяется с мочой и калом во внешнюю среду, являясь источником распространения гельминтоза. Очаги уринарного шистосомоза находятся главным образом в Африке: кишечного - в Южной и Центральной Америке, Африке, японского - в Японии и странах ЮгоВосточной Азии.
Патологическая анатомия. Наиболее часто встречается уринарный шистосомоз, при котором поражается мочевой пузырь. В ранний период болезни в поверхностных слоях слизистой оболочки мочевого пузыря развиваются воспаление, кровоизлияния, слущивание эпителиального покрова. Затем изменения распространяются на более глубокие слои стенки. В подслизистом слое вокруг яиц шистосом появляются лейкоцитарные инфильтраты, они охватывают всю толщину слизистой оболочки, в которой образуются язвы. Со временем экссудативная тканевая реакция сменяется продуктивной, вокруг яиц формируется грануляционная ткань с большим числом эпителиоидных клеток, образуется шистосомная гранулема (рис. 290). Процесс приобретает хроническое течение, исходом которого являются склероз и деформация стенки пузыря. Погибшие яйца
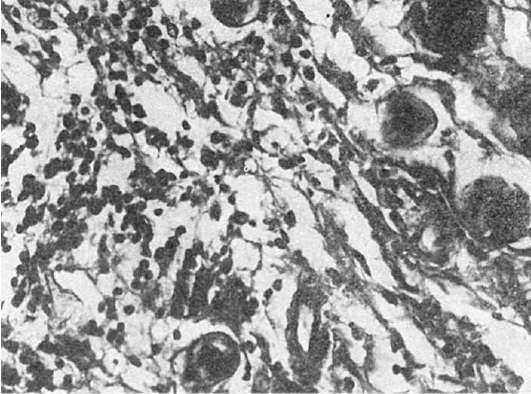 Рис. 290. Уринарный шистосомоз. Яйца паразита в шистосомной гранулеме
Рис. 290. Уринарный шистосомоз. Яйца паразита в шистосомной гранулеме
обызвествляются. Распространение паразита в вены малого таза ведет к возникновению очагов поражения в предстательной железе, придатке яичка. При медленном заживлении язв мочевого пузыря возможно развитие в нем рака.
При кишечном ишстосомозе в толстой кишке развиваются те же воспалительные изменения (шистосомозный колит), завершающиеся склерозом стенки кишки. Встречаются случаи шистосомозного аппендицита.
Возможно гематогенное распространение процесса: паразиты заносятся в печень, легкие, головной мозг и на месте их внедрения возникают воспалительные инфильтраты, образуется грануляционная ткань (гранулемы), развивается склероз.