Общая хирургия: учебник / Петров С.В. - 3-е изд., перераб. и доп. - 2010. - 768 с. : ил.
|
|
|
|
ГЛАВА 6 ПЕРЕЛИВАНИЕ КРОВИ И КРОВЕЗАМЕНИТЕЛЕЙ
Появление способов восполнения кровопотери значительно расширило возможности хирургии. Это позволило не только спасать пациентов от массивных кровотечений, но и выполнять большие травматичные хирургические вмешательства. В настоящее время сформировалась отдельная отрасль науки, специальная дисциплина, рассматривающая самые разнообразные аспекты переливания крови, её компонентов и заменителей, - трансфузиология.
Общие вопросы трансфузиологии
Успехи современной клинической медицины неразрывно связаны с широким внедрением методов трансфузиологии на различных этапах лечения больных.
Трансфузиология (transfusio - переливание, смешивание; logos - учение) - раздел медицинской науки об управлении функциями организма путём целенаправленного воздействия на морфологический состав крови с помощью переливания цельной крови, её компонентов, а также кровезаменителей и других средств.
Основные трансфузионные средства:
• кровь и её компоненты (эритроцитарная, лейкоцитарная и тромбоцитарная массы, плазма крови); переливание крови и её компонентов называют гемотрансфузией;
• кровезаменители - лечебные растворы, предназначенные для замещения утраченных или нормализации нарушенных функций крови.
Трансфузиология изучает также миелотрансплантацию (пересадку костного мозга) - эффективный метод лечения гемобластозов (злокачественных поражений органов кроветворения) и средство коррекции различных видов угнетения кроветворения.
Организация трансфузиологической службы
Трансфузиологическая служба - сеть специальных организаций, предназначенных для обеспечения лечебных учреждений кровью, её компонентами и кровезаменителями.
В состав трансфузиологической службы Российской Федерации входят Гематологический научный центр Российской Ака- демии медицинских наук, научно-исследовательские институты Министерства здравоохранения и социального развития, станции и отделения переливания крови, а также кабинеты трансфузионной терапии.
Гематологический научный центр РАМН и научно-исследовательские институты - консультативные, организационные и методические центры, где разрабатывают методические инструкции и рекомендации, проводят семинары и конференции для информации медицинских работников об основных достижениях трансфузиологии, ведут научно-исследовательскую работу по созданию и внедрению в практику новых трансфузионных средств.
Станции и отделения переливания крови комплектуют донорские кадры, обследуют доноров и ведут их учёт, заготавливают и хранят кровь и её компоненты. Здесь определяют группу крови и резус-принадлежность крови доноров и больных, проводят профилактику по- сттрансфузионных осложнений. На станциях и в отделениях переливания крови создают необходимый запас крови на случай стихийных бедствий, аварий и катастроф, эпидемий и других чрезвычайных обстоятельств. Здесь проводят обучение врачей основам трансфузиологии, осуществляют контроль за состоянием трансфузиологической помощи в лечебных учреждениях.
В небольших стационарах, не имеющих в своей структуре отделения переливания крови, в настоящее время организуют кабинеты трансфузионной терапии.
Донорство в России
Людей, добровольно дающих свою кровь (или орган) для введения (пересадки) больным, называют донорами. Больных, получающих донорские органы и ткани, называют реципиентами.
Донорство (donore - дарить) - добровольная дача части крови, её компонентов, костного мозга, тканей или органов для их применения с лечебной целью.
Донорство - основной источник крови, её препаратов и компонентов. Развитие донорства, обеспечение комплекса социальных, экономических, правовых, медицинских мер, защита прав донора регламентированы Законом Российской Федерации.
Группы доноров
Существуют безвозмездные и кадровые доноры, активные доноры и доноры резерва, иммунные доноры.
Безвозмездное донорство как явление возникло в 60-х годах, когда люди сдавали свою кровь без денежной компенсации. Кровью безвозмездных доноров обеспечена работа многих лечебных учреждений, особенно центральных районных больниц.
Кадровые доноры (платное донорство) систематически участвуют в донорстве на протяжении многих лет. Они находятся под постоянным врачебным наблюдением и подвергаются регулярному медицинскому обследованию.
Доноров, сдающих кровь регулярно, называют активными. Они имеют донорские книжки и дают расписку в том, что не болели гепа- титом, сифилисом и другими инфекциями, а также обязуются информировать донорский пункт в случае заболевания ими.
Донорами резерва называют лиц, хотя бы однократно сдавших кровь и согласных на сдачу крови в случае потребности в этом учреждения, где они состоят на учёте.
Особую группу доноров составляют иммунные доноры, в крови которых содержатся антитела к антигенам различной специфичности в достаточном титре. Основную массу иммунных доноров подвергают намеренной иммунизации введением специфических антигенов - стафилококкового анатоксина, столбнячного анатоксина и др. Гипериммунную плазму у доноров забирают в несколько приёмов. В настоящее время получены и с успехом применяются в клинике иммунные препараты для лечения гриппа, столбняка, холеры, клещевого энцефалита, дифтерии, неклостридиальной и клостридиальной анаэробных инфекций и др.
Охрана здоровья доноров
В России принят Закон «О донорстве крови и её компонентов» (?5142-1 от 9 июня
В соответствии с Законом донорство - добровольный акт. Донором может быть каждый дееспособный гражданин от 18 до 60 лет, прошедший медицинское обследование. Государство гарантирует ему защиту прав и охрану здоровья. Взятие крови и её компонентов допустимо только при условии, что здоровью донора не будет причи-
нён ущерб. Разовая доза забора крови не должна превышать 500 мл. У доноров, дающих кровь впервые, а также у доноров до 20 лет и старше 50 лет рекомендуется забор не более 300 мл крови. Повторную сдачу крови разрешают не ранее чем через 60 дней при условии полного восстановления параметров гомеостаза. Общее количество заборов не должно быть более пяти в год. Существенной разницы в сроках восстановления крови после сдачи крови между мужчинами и женщинами нет. Вместе с тем многолетний опыт показывает, что женщины, как правило, лучше переносят процедуру взятия крови.
Донорам, регулярно сдающим кровь, предоставляют дополнительные льготы. Лиц, сдавших кровь 40 раз и более, награждают нагруд- ным знаком «Почётный донор России» с получением дополнительных льгот по оказанию медицинской помощи, приобретению лекарств, оплате коммунальных услуг, получению путевок на санаторно-курортное лечение и т.д.
Обследование доноров
Подбор доноров проводят по единым медицинским критериям, что обеспечивает безвредность, высокую активность и эффективность крови и её компонентов.
Каждый донор перед сдачей крови проходит обследование: у него собирают анамнез, проводят тщательный медицинский осмотр и специальное обследование для выявления противопоказаний к сдаче крови и исключения возможности передачи с кровью возбудителей инфекционных заболеваний. Проводят серологическое, вирусологическое и бактериологическое обследования донорской крови.
Успехи клинической трансфузиологии снижают опасность передачи с кровью и её компонентами возбудителей инфекционных за- болеваний (ВИЧ-инфекции, гепатитов В и С, сифилиса, цитомегаловирусной инфекции и др.).
Основные антигенные системы крови
Установлено, что антигенная структура крови человека сложна, все форменные элементы крови и белки плазмы разных людей отличаются по антигенам. Уже известно около 500 антигенов крови, образующих более 40 различных антигенных систем.
Под антигенной системой понимают совокупность антигенов крови, наследуемых (контролируемых) аллельными генами.
Все антигены крови делят на клеточные и плазменные. Основное значение в трансфузиологии имеют клеточные антигены.
Клеточные антигены
Клеточные антигены - сложные углеводно-белковые комплексы (гликопептиды), структурные компоненты мембраны клеток крови. От других компонентов клеточной мембраны они отличаются им- муногенностью и серологической активностью.
Иммуногенность - способность антигенов индуцировать синтез антител, если они попадают в организм, у которого эти антигены отсутствуют.
Серологическая активность - способность антигенов соединяться с одноимёнными антителами.
Молекула клеточных антигенов состоит из двух компонентов:
- шлеппер (белковая часть антигена, расположенная во внутренних слоях мембраны), определяющий иммуногенность;
- гаптен (полисахаридная часть антигена, расположенная в поверхностных слоях клеточной мембраны), определяющий серологическую активность.
На поверхности гаптена расположены антигенные детерминанты (эпитопы) - молекулы углеводов, к которым присоединяются анти- тела. Известные антигены крови отличаются друг от друга эпитопами. Например, гаптены антигенов системы АВ0 имеют следующий набор углеводов: эпитоп антигена 0 - фукоза, антигена А - N-аце- тилгалактозамин, антигена В - галактоза. С ними и соединяются групповые антитела.
Различают три вида клеточных антигенов:
- эритроцитарные;
- лейкоцитарные;
- тромбоцитарные.
Эритроцитарные антигены
Известно более 250 антигенов эритроцитов, образующих свыше 20 антигенных систем. Клиническое значение имеет 11 систем: АВ0, Резус (Rh-Hr), MNSs, Келл (Kell), Лютеран (Lutheran), Кидд (Kidd), Диего (Diego), Даффи (Duffy), Домброк (Dombrock), ферментные группы эритроцитов.
У человека в эритроцитах присутствуют одновременно антигены нескольких антигенных систем.
Основными в трансфузиологии признаны антигенные системы АВ0 и Резус. Другие антигенные системы эритроцитов в настоящее время существенного значения в клинической трансфузиологии не имеют.
Антигенная система АВ0
Система АВ0 - основная серологическая система, определяющая совместимость или несовместимость переливаемой крови. Её составляют два генетически детерминированных агглютиногена (антигены А и В) и два агглютинина (антитела α и β).
Агглютиногены А и В содержатся в строме эритроцитов, а агглютинины α и β - в сыворотке крови. Агглютинин α - антитело по отношению к агглютиногену А, а агглютинин β - по отношению к агглютиногену В. В эритроцитах и сыворотке крови одного человека не может быть одноимённых агглютиногенов и агглютининов. При встрече одноимённых антигенов и антител возникает реакция изогемагглютинации. Именно эта реакция - причина несовместимости крови при гемотрансфузии.
В зависимости от сочетания в эритроцитах антигенов А и В (и соответственно в сыворотке антител α и β) всех людей разделяют на четыре группы.
Антигенная система Резус
Резус-фактор (Rh-фактор), названный так вследствие того, что впервые был обнаружен у макак резус, присутствует у 85% людей, а у 15% отсутствует.
В настоящее время известно, что система Резус достаточна сложна и представлена пятью антигенами. Роль резус-фактора при гемотрансфузии, а также при беременности крайне велика. Ошибки, приводящие к развитию резус-конфликта, вызывают тяжёлые осложнения, а иногда и смерть больного.
Второстепенные антигенные системы
Второстепенные эритроцитарные групповые системы представлены большим количеством антигенов. Знание этого множества систем имеет значение для решения некоторых вопросов в антропологии, су- дебно-медицинских исследований, а также для предотвращения развития посттрансфузионных осложнений и некоторых заболеваний у новорождённых.
Система MNSs включает факторы М, N, S, s. Доказано наличие двух тесно сцепленных между собой генных локусов MN и Ss. В даль-
нейшем были выявлены другие многообразные варианты антигенов системы MNSs. По химической структуре MNSs - гликопротеиды.
Система Р. Система антигена Р имеет определённое клиническое значение. Отмечены случаи ранних и поздних выкидышей, причиной которых стали изоантитела анти-Р. Описано несколько случаев посттрансфузионных осложнений, связанных с несовместимостью донора и реципиента по системе антигенов Р.
Система Келл представлена тремя парами антигенов. Наибольшей иммуногенной активностью обладают антигены Келл (К) и Челлано (к). Антигены системы Келл могут вызывать сенсибилизацию организма во время беременности и при переливании крови, становиться причиной гемотрансфузионных осложнений и развития гемолитической болезни новорождённых.
Система Лютеран. Один из доноров по фамилии Лютеран имел в эритроцитах крови какой-то ранее неизвестный антиген, приведший к иммунизации реципиента. Антиген был обозначен буквами Lu а. Через несколько лет был открыт второй антиген этой системы Lu b. Их частота: Lu а - 0,1%, Lu b - 99,9%. Антитела анти-Lu b изоиммунные, что подтверждено и сообщениями о значении этих антител в происхождении гемолитической болезни новорождённых. Клиническое значение антигенов системы Лютеран невелико.
Система Кидд. Антигены и антитела системы Кидд имеют опреде- лённое практическое значение. Они могут быть причиной развития гемолитической болезни новорождённых и посттрансфузионных осложнений при многократном переливании крови, не совместимой по антигенам этой системы. Частота антигенов составляет около 75%.
Система Диего. В
Система Даффи состоит из двух основных антигенов - Fy а и Fy b. Антитела анти-Fy а - неполные антитела, они проявляют своё действие только в непрямом антиглобулиновом тесте Кумбса. Позднее были обнаружены антигены Fy x, Fy3, Fy4, Fy5. Частота зависит от расовой принадлежности человека, что имеет большое значение для антропологов. В негроидных популяциях частота фактора Fy a - 25%, среди китайского населения, эскимосов и аборигенов Австралии - почти 100%, у людей европеоидной расы - 60-82%.
Система Домброк. В
Ферментные группы эритроцитов. Начиная с
Лейкоцитарные антигены
В
мембране лейкоцитов существуют антигены, аналогичные эритроцитарным, а
также специфичные для этих клеток антигенные комплексы, называемые
лейкоцитарными антигенами. Впервые сведения о лейкоцитарных группах
получил французский исследователь Ж. Доссе в
• общие антигены лейкоцитов (HLA - Human Leucocyte Antigen);
• антигены полиморфно-ядерных лейкоцитов;
• антигены лимфоцитов.
Система HLA
Система HLA имеет наибольшее клиническое значение. Она включает более 120 антигенов. Только по этой антигенной системе насчитывают 50 млн лейкоцитарных групп крови. HLA-антигены универсальны. Они содержатся в лимфоцитах, полиморфно-ядерных лейкоцитах (гранулоцитах), моноцитах, тромбоцитах, а также в клетках почек, лёгких, печени, костного мозга и других тканях и органах. Поэтому их ещё называют антигенами гистосовместимости.
По рекомендации ВОЗ используют следующую номенклатуру системы HLA:
• HLA - Human Leucocyte Antigen - обозначение системы;
• А, В, С, D - генные локусы, или регионы, системы;
• 1, 2, 3 - номера аллелей внутри генного локуса системы HLA;
• W - символ для обозначения недостаточно изученных антигенов.
Система HLA - наиболее сложная из всех известных систем антигенов. Генетически HLA-антигены принадлежат к четырём локусам (А, В, С, D), каждый из которых объединяет аллельные антигены. Иммунологическое исследование, позволяющее определить антигены гистосовместимости, называют тканевым типированием.
HLA-система имеет большое значение при трансплантации органов и тканей. Аллоантигены системы HLA-локусов А, В, С, D, а также агглютиногены классических групп крови системы АВ0 представляют собой единственно достоверно известные антигены гистосовместимости. Для предупреждения быстрого отторжения пересаженных органов и тканей необходимо, чтобы реципиент имел ту же, что и донор, группу крови системы АВ0 и не имел антител к аллоантигенам HLA-генных локусов А, В, С, D донорского организма.
HLA-антигены имеют значение также при переливании крови, лейкоцитов и тромбоцитов. Различие беременной и плода по антигенам HLA-системы при повторных беременностях может привести к выкидышу или гибели плода.
Антигены полиморфно-ядерных лейкоцитов
Другая система антигенов лейкоцитов - антигены гранулоцитов (NA-NB). Это органоспецифическая система. Антигены гранулоцитов обнаружены в полиморфно-ядерных лейкоцитах и клетках костного моз- га. Антитела против антигенов гранулоцитов имеют значение при беременности. Они вызывают кратковременную нейтропению новорож- дённых, играют важную роль в развитии негемолитических трансфузионных реакций, способных вызывать гипертермические посттрансфузионные реакции и укорочение жизни гранулоцитов донорской крови.
Антигены лимфоцитов
Третью группу антигенов лейкоцитов составляют тканеспецифические лимфоцитарные антигены. К ним относят антиген Ly и др. Выделено 7 антигенов популяции В-лимфоцитов: от HLA-DRw1 до HLA-DRw7 Значение этих антигенов остаётся малоизученным.
Тромбоцитарные антигены
В мембране тромбоцитов существуют антигены, аналогичные эритроцитарным и лейкоцитарным, а также свойственные только этим
клеткам крови - тромбоцитарные антигены. Известны антигенные системы Zw, PL, Ко. Особого клинического значения они не имеют.
Плазменные антигены
Плазменные (сывороточные) антигены - определённые комплексы аминокислот или углеводов, расположенные на поверхности молекул белков плазмы (сыворотки) крови.
Антигенные различия, свойственные белкам плазмы крови, объединяют в 10 антигенных систем (Нр, Gc, Tf, Inv, Gm и др.). Наиболее сложной из них и клинически значимой считают антигенную систему Gm, присущую иммуноглобулинам (включает 25 антигенов). Различия людей по антигенам плазменных белков создают плазменные (сывороточные) группы крови.
Понятие о группе крови
Согласно современным данным иммуногематологии, можно следующим образом сформулировать понятие «группа крови».
Группа крови - сочетание нормальных иммунологических и гене- тических признаков крови, наследственно детерминированное биологическое свойство каждого индивидуума.
Группы крови передаются по наследству, формируются на 3-м или 4-м мес внутриутробного развития и остаются неизменными в течение всей жизни. Считают, что у человека группа крови включает не- сколько десятков антигенов в различных сочетаниях. Этих сочетаний - групп крови - реально может быть несколько миллиардов. Практически они одинаковы лишь у однояйцовых близнецов, имеющих один и тот же генотип.
В практической медицине термин «группа крови», как правило, отражает сочетание эритроцитарных антигенов системы АВ0, резусфактора и соответствующих антител в сыворотке крови.
Групповые антитела
Для каждого известного антигена обнаружены одноимённые антитела (анти-А, анти-В, анти-резус, анти-Келл и т.д.). Групповые антитела крови - не такое постоянное свойство организма человека, как антигены. Лишь в групповой системе АВ0 антитела - нормальное врождённое свойство плазмы крови. Эти антитела (агглютинины α и β)
постоянно присутствуют в плазме крови человека, определённым образом сочетаясь с агглютиногенами (антигенами) эритроцитов.
Групповые антитела бывают врождёнными (например, агглютинины α и β) и изоиммунными, образующимися в ответ на поступление чужеродных групповых антигенов (например, антитела системы Резус).
Врождённые антитела - так называемые полные антитела, это аг- глютинины, вызывающие агглютинацию (склеивание) эритроцитов, содержащих соответствующий антиген. Их относят к холодовым антителам, так как они лучше проявляют своё действие in vitro при низких температурах и слабее реагируют при высокой температуре.
Полные антитела относят к иммуноглобулинам класса М. Молекулярная масса этих антител 900 000-1000 000 Да, наибольший размер 100 нм. Молекула содержит четыре цепочки аминокислот, участки между концами их цепей - активные центры (паратопы, антидетерминанты), которыми антитела соединяются с антигенными детерминантами, расположенными на клетках крови. Антитела класса М имеют 10 активных центров, поэтому они могут соединяться одновременно с антигенными детерминантами нескольких клеток крови.
Изоиммунные антитела неполные. Они с трудом поддаются абсорбции и не разрушаются при нагревании. Эти антитела тепловые (наиболее активны при температуре 37?С и выше) и агглютинируют клетки крови только в коллоидной среде.
Неполные антитела относят к классу IgG. Молекулярная масса составляет около 150 000-160 000 Да, наибольший размер 25 нм. Строение молекулы схоже со строением молекулы полных антител, но отличается последовательностью аминокислот и количеством активных центров: у неполных антител их два (каждое антитело связывает две антигенных детерминанты).
Механизм взаимодействия антиген-антитело
Механизм взаимодействия антигена и антитела состоит из двух фаз: собственно взаимодействия и его проявления.
В первой фазе антитело одним активным центром соединяется с антигенной детерминантой одной клетки крови (фиксируется на клет- ке). На этом этапе реакции никаких видимых глазом или в световом микроскопе изменений ещё нет. После этого начинается фаза, проявляющаяся в виде агглютинации. После фиксации антител на поверхности клеток крови к комплексу антиген-антитело присоединяется комплекс белков из плазмы крови (комплемент), и комплекс
антиген-антитело-комплемент разрушает (лизирует) мембрану клетки. При взаимодействии антител с эритроцитами это проявляется гемолизом. Для каждой фазы реакции антиген-антитело необходимы строго определённые условия: рН, температура, ионный состав и коллоидность среды, наличие активного комплемента, определённое соотношение количества молекул антител и антигенов.
Определение группы крови по системе АВ0
Группы крови по системе АВ0
Антигенная система АВ0 имеет основное значение в совместимости крови при переливании.
Под термином «совместимость» понимают сочетание крови донора и реципиента по антигенам и антителам, не вызывающее иммуноло- гических взаимодействий.
Классические группы крови АВ0
В зависимости от наличия в эритроцитах агглютиногенов А и В, а в сыворотке соответствующих им агглютининов α и β, всех людей далят на четыре группы:
• группа 0(I): в эритроцитах агглютиногенов нет, в сыворотке присутствуют агглютинины α и β;
• группа А(II): в эритроцитах - агглютиноген А, в сыворотке - агглютинин β;
• группа В(Ш): в эритроцитах присутствует агглютиноген В, в сыворотке выявляют агглютинин α;
• группа АВ(IV): в эритроцитах - агглютиногены А и В, агглютининов в сыворотке нет.
В последнее время в системе АВ0 обнаружены разновидности классических антигенов А и В, а также другие антигены.
Подтипы антигена А
Антиген А нельзя считать однородным, существует два основных его подтипа: А1 и А2. Эритроциты с подтипом агглютиногена А1 встречают намного чаще, чем с подтипом А2 (88% и 12% соответственно). Поэтому при наличии агглютиногена А1 его обозначают просто как А, а обозначение с индексом применяют только для относительно редко-
Таблица 6-1. Группы крови по системе АВ0
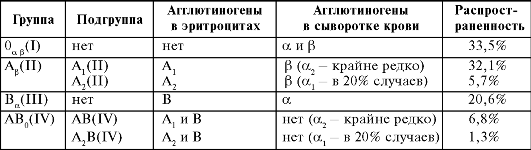
го агглютиногена А2. В соответствии с этим группа А(II) имеет две подгруппы: А(II) и А2(II), а группа АВ(IV) - АВ(IV) и А2B(IV) (табл. 6-1). Агглютиногены А 1 и А2 отличаются друг от друга по свойствам.
• Подтип А1 обладает большей адсорбционной возможностью по сравнению с агглютиногеном А2, он сильнее адсорбирует агглютинин a из сыворотки, поэтому его называют сильным, а подтип А2 - слабым.
• Эритроциты с агглютиногеном А2 имеют более низкую агглютинабельность.
• Подгруппы с агглютиногенами А1 и А2 обладают различными свойствами сывороток. Сыворотка подгрупп А2 (II) и А2В (IV) довольно часто содержит агглютинин, названный Ландштейнером и Левином экстраагглютинином a1, дающим агглютинацию только с эритроцитами А1 и не дающим агглютинации с эритроцитами А2. В то же время в сыворотке подгрупп А(II) и АВ(IV) довольно редко, но встречается экстраагглютинин a2, не агглютинирующий эритроциты А1, а дающий агглютинацию с эритроцитами А2.
Существуют варианты эритроцитов с ещё более слабовыраженными агглютинабельными свойствами, что связано с наличием в них подтипов А3, А4, Az и др. Несмотря на то, что эти слабые антигены встречают довольно редко, они имеют определённое клиническое значение.
Подтипы антигена В
Групповой антиген В отличается большей однородностью. Описанные редкие его варианты (В2, В3, Bw и др.) существенного клинического значения не имеют.
Антиген 0 и субстанция Н
Позже в первой группе крови 0(I) была найдена специфическая субстанция, также обозначенная символом «0». Фактор 0 - агглюти- ноген, присущий эритроцитам групп 0(I), А2(II), А2B(IV).
Для эритроцитов всех групп характерно наличие субстанции Н, её считают общим веществом-предшественником. Субстанцию Н чаще встречают у лиц с первой группой крови, в других же она содержится в незначительном количестве. У некоторых жителей индийского города Бомбей обнаружена группа, не содержащая агглютиногенов 0, А, В, Н, но содержащая антитела α, β, анти-0 и анти-Н. Впоследствии этот редкий тип крови, обнаруженный и у жителей других стран, получил название «тип Бомбей».
«Кровяные химеры»
В настоящее время известны так называемые кровяные химеры, обусловленные одновременным пребыванием в организме человека эритроцитов, принадлежащих двум фенотипам АВ0. В естественных условиях явление кровяной химеры встречают у близнецов. Оно может также появиться при пересадке аллогенного костного мозга или переливании массивных объёмов крови. При определении группы крови и резус-принадлежности в условиях наличия кровяной химеры, как правило, получают искажённый результат.
Способы определения группы крови
Групповую принадлежность крови по системе АВ0 определяют с помощью реакции агглютинации. В настоящее время используют три способа определения групп крови по системе АВ0:
• с помощью стандартных изогемагглютинирующих сывороток;
• с помощью стандартных изогемагглютинирующих сывороток и стандартных эритроцитов (перекрёстный способ);
• с помощью моноклональных антител (цоликлонов анти-А и анти-В).
Существует следующая общепринятая тактика при определении группы крови.
При плановом исследовании врач стационара определяет группу крови с помощью стандартных изогемагглютинирующих сывороток, или цоликлонов, после чего посылает кровь в серологическую лабораторию для проверки группы перекрёстным методом.
Группу крови считают определённой только в том случае, если лаборатория подтвердила данные, полученные врачом стационара. Если результаты исследований расходятся, оба исследования нужно повторить.
При необходимости определения группы крови в экстренном порядке (при кровотечении необходимо срочное переливание крови) врач стационара определяет группу крови сам (в лаборатории перепроверку выполняют, но постфактум). В таких случаях также используют реакции с изогемагглютинирующими сыворотками (или поликлонами), но при возможности целесообразно применение пе- рекрёстного метода.
Определение групп крови с помощью стандартных изогемагглютинирующих сывороток
Этот способ в настоящее время наиболее распространён в клинической и лабораторной практике.
Суть метода сводится к обнаружению в исследуемой крови групповых антигенов А и В с помощью стандартных изогемагглютинирующих сывороток. Для этого используют реакцию агглютинации. Постановку реакции проводят в помещении с хорошим освещением при температуре 15-25?С.
Необходимое оснащение
1. Стандартные изогемагглютинирующие сыворотки групп 0(I), A(II), В(III) и АВ(IV) двух различных серий. Сыворотки для определения групп крови изготавливают в специальных серологических ла- бораториях из донорской крови. Сыворотки хранят при температуре 4-8 ?С (в холодильнике). Срок годности сыворотки указан на этикете. Титр сыворотки (также указан на этикетке) должен быть не ниже 1:32 (для сыворотки В(Ш) - не ниже 1:16/32). Под титром сыворотки понимают то максимальное её разведение, при котором может наступать реакция агглютинации. Сыворотка должна быть прозрачной. Для удобства стандартные гемагглютинирующие сыворотки различных групп подкрашивают так, чтобы они имели определённый цвет: 0(I) - бесцветная, А(II) - синяя, В(III) - красная, АВ(IV) - ярко-жёлтая. Следует отметить, что указанные цвета сопутствуют всем этикеткам на препаратах крови, имеющих групповую принадлежность (кровь, эритроцитарная масса, плазма и др.).
2. Белые фарфоровые или эмалированные тарелки, или любые другие; пластинки со смачиваемой поверхностью, маркированные 0(I), А(П), В(Ш), AB(IV).
3. Изотонический раствор хлорида натрия.
4. Иглы, пипетки, стеклянные палочки (предметные стёкла).
Методика проведения реакции
1. Перед
началом реакции подписывают тарелку (наносят фамилию и инициалы
исследуемого), после чего на неё под соответствующие обозначения
наносят стандартные изогемагглютинирующие сыворотки I, II и III групп в
объёме 0,1 мл (капля около
2. Кровь для исследования берут из пальца или из вены. Шесть капель исследуемой крови величиной приблизительно с булавочную головку (0,01 мл, маленькая капля) последовательно переносят сухой стеклянной палочкой на пластину в шесть точек, каждую - рядом с каплей стандартной сыворотки (количество исследуемой крови должно быть приблизительно в 10 раз меньше количества стандартной сыворотки, с которой её смешивают), потом их осторожно с помощью стеклянных палочек с закруглёнными краями перемешивают.
Возможна более простая методика: на тарелку наносят одну большую каплю крови, из которой её забирают уголком предметного стекла и переносят в каждую каплю сыворотки, аккуратно перемешивая с последней. При этом всякий раз кровь берут новым уголком стекла, следя за тем, чтобы капли не сливались.
3. После смешивания тарелку периодически покачивают.
Агглютинация начинается в течение первых 10-30 с, однако наблюдение следует обязательно вести до 5 мин ввиду возможности более поздней агглютинации, например с эритроцитами группы A2(II).
4. В те капли, где произошла агглютинация, добавляют по одной капле изотонического раствора хлорида натрия, после чего оценивают результат реакции.
Трактовка результатов
Реакция агглютинации может быть положительной или отрицательной. При положительной реакции обычно в течение первых 10- 30 с в смеси появляются видимые невооружённым взглядом мелкие красные зёрнышки (агглютинаты), состоящие из склеенных эритроцитов. Мелкие зёрнышки постепенно сливаются в более крупные зёр- на, а иногда в хлопья неправильной формы. При этом сыворотка частично или полностью обесцвечивается. Положительная реакция может быть пескообразной или лепестковой (рис. 6-1).
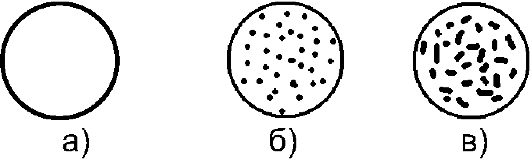
Рис. 6-1. Виды агглютинации: а - агглютинации нет; б - пескообразная агглютинация; в - лепестковая агглютинация
При отрицательной реакции капля остаётся равномерно окрашенной в красный цвет, в ней не обнаруживают никаких зёрнышек (агглютинатов).
Результаты реакций в каплях с сыворотками одной и той же группы (двух серий) должны совпадать.
Принадлежность исследуемой крови к соответствующей группе определяют по наличию или отсутствию агглютинации при реакции с соответствующими сыворотками после наблюдения в течение 5 мин (табл. 6-2).
При этом следует отметить, что если сыворотки всех трёх групп дали положительную реакцию, это указывает на то, что испытуемая кровь содержит оба агглютиногена (А и В) и принадлежит к группе AB(IV). Однако в таких случаях для исключения неспецифической реакции агглютинации необходимо провести дополнительное контрольное исследование испытуемой крови со стандартной изогемагглютинирующей сывороткой группы AB(IV), не содержащей агглю-
Таблица 6-2. Оценка результатов реакции со стандартными изогемагглютинирующими сыворотками
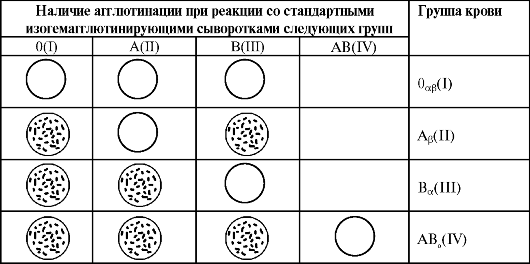
тининов. Лишь отсутствие агглютинации в этой капле при наличии агглютинации в каплях, содержащих стандартные сыворотки групп 0(I), А(II) и В(III), позволяет считать реакцию специфической и отнести исследуемую кровь к группе АВ0(IV).
Следует отметить, что при наличии в исследуемой крови слабого антигена А2 реакция агглютинации с гемагглютинирующими сыворотками групп 0(I) и B(III) начинается позже (на 3-4-й мин).
Идентификацию подгрупп антигена А проводят в серологической лаборатории с помощью специальных экстрактов из семян Dolichos biflorus и Ulex Europeus. Первый из них агглютинирует эритроциты с антигеном А1, но не реагирует с антигеном А2, а второй - наоборот.
Определение групп крови перекрёстным способом
Способ наиболее часто используют в серологических лабораториях. Суть метода состоит в определении наличия или отсутствия в исследуемой крови групповых антигенов А и В с помощью стандартных изогемагглютинирующих сывороток, а также групповых антител α и β с помощью стандартных эритроцитов. Реакцию со стандартными сыворотками проводят описанным выше способом.
Реакцию со стандартными эритроцитами проводят следующим образом.
Необходимое оснащение
Оснащение для реакции со стандартными эритроцитами отличается тем, что для её проведения необходимы стандартные эритроци- ты трёх групп крови: 0(I), А(II), B(III). Стандартные эритроциты при- готавливают из крови доноров с заранее известной группой крови, хранят при 4-8 ?С. Срок годности 2-3 дня.
Методика проведения реакции
1. Кровь для исследования берут из вены в сухую пробирку, центрифугируют или оставляют в покое на 20-30 мин для получения сыворотки.
2. На маркированную тарелку пипеткой наносят три больших капли (0,1 мл) сыворотки исследуемой крови из пробирки, а рядом с ними - по одной маленькой капле (0,01 мл) стандартных эритроцитов групп.
3. Дальнейшие мероприятия проводят аналогично методу с использованием стандартных изогемагглютинирующих сывороток: соответствующие капли смешивают стеклянными палочками, планшет по- качивают, наблюдают в течение 5 мин, в капли с агглютинацией
Таблица 6-3. Оценка результатов определения группы крови перекрёстным способом
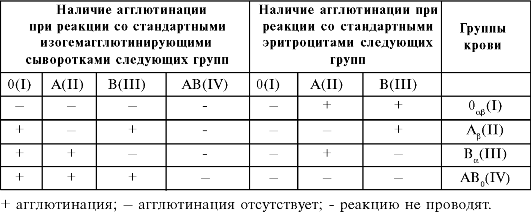
добавляют изотонический раствор хлорида натрия, после чего оценивают результат.
Трактовка результатов
Оценивают данные, полученные при обеих реакциях (со стандартными изогемагглютинирующими сыворотками и стандартными эритроцитами - табл. 6-3).
Особенность трактовки результатов реакции со стандартными эритроцитами - эритроциты группы 0(I) считают контрольными (в них нет антигенов, что делает принципиально невозможной специфическую реакцию агглютинации с любой сывороткой).
Результат перекрёстного способа считают достоверным, только если при оценке результатов реакции со стандартными изогемагглютинирующими сыворотками и со стандартными эритроцитами ответы о группе исследуемой крови совпадают. Если этого не происходит, обе реакции следует переделать.
Определение групп крови моноклональными антителами Необходимое оснащение
Для определения группы крови используют моноклональные антитела, для получения которых применяют гибридомную биотехнологию.
Гибридома - клеточный гибрид, образованный путём слияния клетки опухоли костного мозга (миеломы) с иммунным лимфоцитом, синтезирующим специфические моноклональные антитела. Гибридома приобретает свойства обоих «родителей»: способность к нео-
Таблица 6-4. Схема оценки результатов определения групп крови с помощью моноклональных антител (цоликлоны анти-А и анти-В)

граниченному росту, характерную для опухолевой клетки, и возможность синтезировать антитела, присущую иммунному лимфоциту.
Разработаны стандартные реагенты - моноклональные антитела: цоликлоны анти-А и анти-В, применяемые для определения агглютиногенов эритроцитов. Цоликлоны используют в виде лиофилизированного порошка красного (анти-А) или синего (анти-В) цвета, порошок разводят изотоническим раствором натрия хлорида непосредственно перед исследованием.
Техника проведения реакции
Цоликлоны анти-А и анти-В наносят на белый планшет по одной большой капле (0,1 мл) под соответствующими надписями: анти-А и анти-В. Рядом с ними наносят по одной маленькой капле (0,01 мл) исследуемой крови. После перемешивания составных частей за реакцией агглютинации наблюдают в течение 2-3 мин.
Трактовка результатов
Оценка результатов очень проста (табл. 6-4).
Методика определения группы крови с помощью цоликлонов позволяет отказаться от стандартных изогемагглютинирующих сыворо- ток, получаемых из донорской крови.
Возможные ошибки
Определение групповой принадлежности с помощью реакции агглютинации может сопровождаться ошибками, ведущими к неверной трактовке результатов. Все ошибки можно разделить на три группы:
• низкое качество реагентов;
• технические ошибки;
• особенности исследуемой крови.
Низкое качество реагентов
Стандартные изогемагглютинирующие сыворотки и стандартные эритроциты могут иметь низкие агглютинабельные свойства, что при- водит к неверному толкованию результатов реакции. Во избежание подобных ошибок нужно следить за сроком годности, условиями хранения и внешним видом реагента (прозрачность сыворотки, отсутствие плёнок, хлопьев, запаха гниения и пр.).
Технические ошибки
Ошибки технического характера связаны с несоблюдением или недостаточно точным выполнением всех правил проведения реакции.
Несоблюдение внешних условий
Плохая освещённость мешает обнаружить агглютинацию или её отсутствие.
Повышение температуры выше 25 ?С резко замедляет реакцию.
При низкой температуре (ниже 15 ?С) может произойти неспецифическая агглютинация, независимо от состава агглютининов и агглютиногенов - так называемая холодовая панагглютинация (агглю- тинация возникает при реакциях с сыворотками всех групп крови). Это происходит из-за наличия в сыворотке особого холодового агглютинина, способного давать реакцию агглютинации только при низких температурах.
Неправильное проведение самой реакции
Нарушение расположения сывороток, соотношения сыворотки и крови, слияние соседних капель создают возможность неправильной интерпретации полученных результатов.
Ранняя оценка результатов также может привести к ошибке, особенно при наличии слабого антигена А2, дающего позднюю агглютинацию.
Недобавление физиологического раствора. Несоблюдение этого простого правила (в капли, где произошла агглютинация, следует добавить изотонический раствор хлорида натрия) может привести к тому, что за специфическую агглютинацию принимают ложную (псевдоагглютинацию). Под термином «псевдоагглютинация» подразумевают способность эритроцитов склеиваться в «монетные столбики», или «кучки», с сохранением мембран, независимо от их агглютинабельных свойств. Границы между форменными элементами хорошо
видны под микроскопом, в отличие от истинной агглютинации, при которой происходит разрушение мембран эритроцитов. Добавление 1-2 капель изотонического раствора хлорида натрия позволяет дифференцировать истинную агглютинацию от ложной. Псевдоагглютинация расходится довольно быстро, в то время как истинная агглютинация сохраняется прежней или становится более выраженной.
Особенности исследуемой крови
Развитие неспецифической панагглютинации может быть связано не только с низкой температурой, но и с качествами самой крови.
Панагглютинацию при бактериальном заражении исследуемой крови в
Сущность явления заключается в том, что сыворотка при комнатной температуре даёт агглютинацию со всеми эритроцитами, даже со своими собственными (аутоагглютинация), а эритроциты в то же время дают агглютинацию со всеми сыворотками, даже с сыворотками группы AB(IV).
Подобное явление описано при различных заболеваниях: болезнях крови, спленомегалии, циррозе печени, инфекционных заболеваниях и т.д. Панагглютинацию крайне редко наблюдают и у здоровых людей. Панагглютинацию и аутоагглютинацию выявляют только при комнатной температуре; при температуре, близкой к температуре человеческого тела, этих явлений не происходит.
Во избежание ошибок необходимо не допускать определения группы крови при температуре ниже 15 ?С. Если при определении групповой принадлежности агглютинация происходит с сыворотками групп 0(I), A(II) и B(III) всегда следует проводить реакцию с сывороткой группы AB(IV). Только в том случае, если в этой капле не будет агглютинации, можно исключить панагглютинацию и отнести кровь к группе AB0(IV). При наличии агглютинации с сывороткой AB(IV) необходимо подогреть кровь до 37 ?С и провести реакцию при этой температуре, при этом панагглютинация и аутоагглютинация исчезают.
При некоторых заболеваниях отмечают снижение агглютинабельности агглютиногенов эритроцитов (хронические инфекционные за- болевания, онкологические заболевания, болезни крови и др.). При этом так же, как и при наличии слабого антигена A2, следует чётко соблюдать условия и время реакции.
Во всех случаях нечёткого или сомнительного результата необходимо повторное определение группы крови при помощи стандартных сывороток других серий, а также перекрёстным способом.
Определение резус-фактора Антигенная система резус-фактора
В
Система антигенов резус представлена пятью основными антигенами: D, C, с, Е, e (ранее считали, что их шесть, но позже было доказано, что аллельного гена d не существует). C и с, а также Е и e - аллельные антигены. Каждая из хромосом несёт только три гена из пяти: D, С или с, Е или е.
Номенклатура Dd, Cc, Ее была предложена Р. Фишером и Р. Рейсом. Другая номенклатура (Rh-Hr) была введена А. Винером. Он обозначил шесть резус-антигенов следующим образом: Rh0 (D), rh'(C), rh»(E), Hro(d), hr'(c), hr»(e).
Указанные пять антигенов резус (исключая антиген d) встречают в эритроцитах в виде одного из 18 возможных сочетаний (табл. 6-5). Фенотипически каждый человек содержит 5, 4 или 3 антигена резус в зависимости от количества генов, по которым он гомозиготен. Однако генотипическую формулу изображают шестью буквами, например, cDE/CDe, обозначающими три гена резус, унаследованных с хромосомой одного из родителей, три - с хромосомой другого.
Наиболее активен из всех антигенов Rho(D) - резус-фактор. В зависимости от его наличия или отсутствия кровь людей делят на резус-положительную (Rh+) и резус-отрицательную (Rh-).
Иначе подходят к оценке резус-принадлежности доноров. Необходимо дополнительное исследование крови доноров по факторам Е и С. Резус-отрицательными могут быть только доноры, в крови которых отсутствуют все три антигена (D, С, Е). Такой подход к оценке резус-принадлежности доноров позволяет исключить возможность сенсибилизации реципиента к любому из трёх основных антигенов:
Rho(D), rh'(C), rh»(E).
В повседневной практике переливания крови ограничиваются определением у реципиента только антигена Rho(D).
Таблица 6-5. Aнтигенные группы системы резус-фактор (по M.A. Умно- вой, 1983)
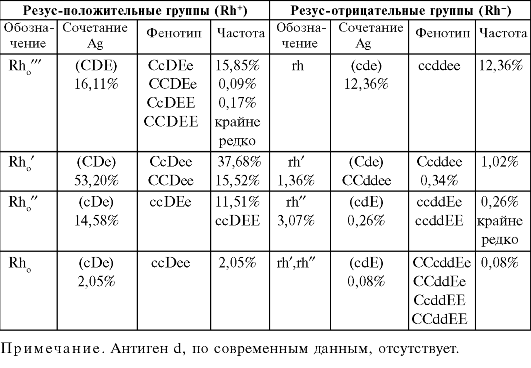
Существует подтип этого антигена Du, отличающийся по структуре и количеству экспрессируемых молекул на строме эритроцитов. Иммуногенность антигена Du значительно снижена, и выявить его сложнее, чем резус-фактор. Подтип Du имеет существенное значение, так как приводит к синтезу особых антител. Они могут стать причиной развития резус-несовместимости крови донора и реципиента. При наличии Du кровь реципиента считают отрицательной, а кровь донора - положительной.
Aнтигены резус - липопротеиды. Они очень активны и способны вызывать образование иммунных антител. Резус-антитела, будучи иммунными (неполными, моновалентными, блокирующими), могут фиксироваться к резус-положительным эритроцитам, не вызывая их склеивания. Они агглютинируют эритроциты только в присутствии коллоидных растворов, протеолитических ферментов или под действием специально приготовленной антиглобулиновой преципитирующей сыворотки. Неполные антитела относят к иммуноглобулинам класса G.
Наличие резус-антигена выявляют у эмбриона начиная с 5-8-й нед, оно хорошо выражено на сроке гестации 3-4 мес. Существова-
ние антигенов системы резус в эритроцитах человека - физиологическое явление, антител к этим антигенам в организме людей с резус-положительными эритроцитами нет. Образование иммунных антител происходит при поступлении в организм человека чужеродного ему изоантигена. У сенсибилизированных людей с резус-отрицательными эритроцитами антитела анти-D содержатся не только в крови, но и в экссудате, транссудате, моче, слезе и других средах.
Способы определения резус-фактора
Все методы определения резус-фактора делят на способы, применяемые в клинической практике, и лабораторные способы.
Способы определения Rh0(D) в клинической практике
В клинических условиях (в приёмном покое, хирургическом отделении, операционной), где нет специального лабораторного оборудования, используют экспресс-методы определения Rho(D) (D-фактора).
Экспресс-метод определения стандартным универсальным реагентом в пробирке без подогрева
Для исследования можно использовать свежую несвернувшуюся кровь, взятую из пальца (или вены) непосредственно перед исследованием, или консервированную кровь без предварительной обработки, а также эритроциты из пробирки после формирования сгустка и отстаивания сыворотки.
Методика проведения реакции. Исследование проводят в центрифужных пробирках объёмом не менее 10 мл. На дно пробирки вносят одну каплю стандартного универсального реагента, представляющего собой антирезусную сыворотку группы АВ(IV), разведённую 33% раствором декстрана (ср. мол. масса 50 000-70 000). Затем в неё добавляют одну каплю исследуемой крови (или эритроцитов). Круго- вым вращением пробирки содержимое размазывают по её внутренней поверхности таким образом, чтобы содержимое растеклось по стенкам. Это значительно ускоряет агглютинацию и делает её крупнолепестковой. Агглютинация на стенках пробирки наступает, как правило, в течение первой минуты, но для образования устойчивого комплекса антиген-антитело и чёткой агглютинации наблюдать следует не менее 3 мин. Затем для исключения неспецифической агрегации эритроцитов в пробирку добавляют 2-3 мл физиологического
раствора и перемешивают путём одно-двукратного перевертывания пробирки (без взбалтывания!).
Трактовка результатов. Наличие агглютинации (крупные хлопья на фоне просветлённой жидкости) указывает на резус-положительную принадлежность исследуемой крови. Отсутствие агглютинации (в пробирке гомогенно окрашенная розовая жидкость) свидетельствует о резус-отрицательной принадлежности исследуемой крови.
Лабораторные способы определения резус-фактора
Для определения резус-принадлежности крови больного в условиях лаборатории применяют четыре основных метода.
Метод агглютинации в солевой среде
Используют специальные сыворотки, содержащие полные антитела анти-резус. Эритроциты в виде 2% взвеси в изотоническом ра- створе хлорида натрия соединяют в пробирках с антирезусной сывороткой. Пробирки помещают на 1 ч в термостат при температуре 37 ?С, после чего осадок эритроцитов на дне пробирки рассматривают с помощью лупы и по его форме учитывают результат. При положительном результате (Rh+) осадок имеет характерный рисунок в виде нитей или зернистости. При отрицательном (Rh-) осадок размещается равномерным слоем и имеет вид правильно очерченного круга.
Метод агглютинации в присутствии желатина
B две пробирки помещают по 0,02-0,03 мл осадка исследуемых эритроцитов. Затем в первую пробирку добавляют 2 капли (0,1 мл) 10% раствора желатина и 2 капли (0,1 мл) анти-резусной сыворотки, во вторую (контрольную) пробирку - 2 капли (0,1 мл) 10% раствора желатина и 2 капли (0,1 мл) физиологического раствора.
Содержимое осторожно перемешивают. Затем пробирки инкубируют в термостате при температуре 45-48 ?С в течение 30 мин, после чего добавляют 5-8 мл физиологического раствора и переворачивают пробирки 1-2 раза для перемешивания.
Результат учитывают, просматривая пробирки на свет невоору- жённым глазом или через лупу. Eсли эритроциты резус-положи- тельны, произойдёт их агглютинация. Отсутствие агглютинации свидетельствует о том, что испытуемая кровь резус-отрицательная. B контрольной пробирке агглютинация эритроцитов должна отсутствовать.
Непрямой антиглобулиновыи тест (реакция Кумбса)
Эта реакция наиболее чувствительна для выявления неполных антител к ауто- и изоантигенам эритроцитов. К ней, как правило, прибегают при возникновении трудностей в определении резус-при- надлежности крови, связанных с нечёткими результатами, полученными при других методах исследования. Реакция основана на использовании антиглобулиновой сыворотки.
При обработке резус-положительных эритроцитов неполными антителами анти-Rh наступает их обволакивание, сенсибилизация по отношению к антиглобулиновой сыворотке, которая агглютинирует сенсибилизированные эритроциты, поскольку имеет антитела к глобулинам.
В пробирку вносят антирезусную сыворотку и отмытые физиологическим раствором эритроциты, помещают на 1 ч в термостат при температуре 37 ?С, после чего эритроциты тщательно отмывают. Последующий этап реакции проводят на плоскости. Каплю взвеси эритроцитов смешивают с равным количеством антиглобулиновой сыворотки и учитывают результат. Наличие агглютинации - показатель того, что исследуемый образец крови резус-положительный. Если агглютинация отсутствует, то испытуемая кровь резус-отрицательная.
Реакция с анти-D-моноклональными антителами
На планшете смешивают большую каплю (0,1 мл) анти-D-монокло- нальных антител и маленькую каплю (0,01 мл) исследуемой крови.
За реакцией наблюдают в течение 3 мин. При смешивании анти- D-MKA с образцами резус-положительных эритроцитов отмечают быстро наступающую лепестковую агглютинацию. Если кровь резусотрицательная, агглютинация отсутствует.
Возможные ошибки
Чаще всего ошибки бывают следствием методических погрешностей при проведении исследования, в особенности при использовании конглютинационных методов. К ложным результатам могут привести неправильное соотношение между сывороткой и эритроцитами, преждевременная оценка результатов, оценка результатов по высыхающей капле, определение резус-фактора в гемолизированном и длительно хранящемся образце крови, а также использование неактивных, инфицированных и загнивших сывороток или сывороток с истекшим сроком годности.
Причиной ошибок могут быть биологические особенности испытуемой крови: снижение агглютинабельности резус-антигена при некоторых заболеваниях печени, почек, системы крови, а также неспе- цифическая агглютинация испытуемых эритроцитов. B случае сомнительных результатов исследование повторяют, применяя более активные антирезусные сыворотки.
Клиническое значение групповой дифференциации
Общие иммуногенетические аспекты
Групповые антигены и антитела крови имеют большое значение в физиологии и патологии человека. Прежде всего, надо иметь в виду, что антигены крови - маркёры генотипа каждого индивидуума. Этот факт имеет значение для плодовитости брака, течения и исхода беременности и здоровья новорождённого. Половые клетки соответственно генотипу имеют антигены, аналогичные групповым антигенам крови, а супруги часто отличаются по группе крови. Несовместимость супругов по системе резус-фактора - одна из наиболее частых причин иммунологического конфликта при беременности, приводящего к гибели плода или гемолитической болезни новорождённого.
B настоящее время всё больше появляется данных о статистически значимых связях групп крови с инфекционной и неинфекционной патологией человека. Наличие некоторых эритроцитарных и лей- коцитарных антигенов создаёт условия для большей вероятности некоторых заболеваний. B частности, известно, что язвенная болезнь наиболее часто развивается у пациентов с группой крови A(II), а наличие антигена HLA-B18 предрасполагает к заболеванию гепатитом B, а если при этом у человека имеется ещё антиген HLA-B5, то наиболее вероятно хроническое течение заболевания. Существует оп- ределённая связь иммунологической реактивности и лейкоцитарных групп по системе HLA. Например, организм людей, имеющих антиген HLA-B8, более активно синтезирует любые антитела, а при наличии антигена HLA-B35 особенно активно образует антитела к столбнячному анатоксину. Таких примеров много. Подобные данные имеют большое значение для определения групп риска в направленной диспансеризации, а также при профессиональном отборе.
Без учёта антигенной структуры крови доноров и реципиентов, особенно системы HLA, невозможно осуществлять аллотрансплан- тацию различных органов и тканей (пересадки почки, сердца, печени, костного мозга).
Исследование групп крови широко используют в судебной медицине при решении вопросов о спорном отцовстве, материнстве, а также при исследовании крови на вещественных доказательствах. Значение групп крови велико и в решении некоторых вопросов антропологии.
Однако первостепенное значение группы крови имеют в трансфузиологической практике при переливании донорской крови, её компонентов и препаратов.
Значение групповой принадлежности при гемотрансфузии
Группа крови каждого человека включает большое количество различных эритроцитарных, лейкоцитарных, тромбоцитарных и плазменных антигенов, достаточно активных и способных стать причиной иммунологической несовместимости при гемотрансфузии. Главенствующую роль играют антигенные системы АВ0 и Rh-фактора.
Иммунологическая несовместимость возникает при появлении в результате гемотрансфузии в крови у реципиента одноимённых ан- тигенов в эритроцитах и в достаточном количестве антител - в сыворотке крови (агглютиноген А - агглютинин а; агглютиноген В - агглютинин β; антиген D(Rh0) - антирезусные антитела). При этом возникает агглютинация эритроцитов с последующим гемолизом.
Первыми указали на значение групповой совместимости крови донора и реципиента, как на важнейшее условие «приживления» перелитой крови, Грилле (1907) и Оттенберг (1908).
Правило Оттенберга
При выявлении совместимости крови реципиента и донора по системе АВ0 Оттенберг ввёл правило (правило Оттенберга), согласно которому подвергаются агглютинации только эритроциты переливаемой донорской крови, так как агглютинины вливаемой крови разводятся в сосудистом русле пациента, их титр становится низким и они не в состоянии агглютинировать эритроциты реципиента. По правилу Оттенберга, можно переливать кровь, эритроциты которой не могут быть агглютинированы сывороткой реципиента (рис. 6-2).
В соответствии с правилом Оттенберга возможно переливание не только одногруппной крови. Эритроциты группы 0(I) не содержат никаких агглютиногенов и не дают агглютинации ни с какими сыворотками. Следовательно, кровь этой группы можно переливать лицам всех остальных групп.
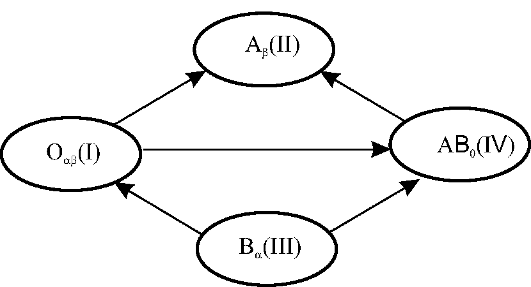
Рис. 6-2. Возможные способы переливания крови, по правилу Оттенберга
В сыворотке крови группы АВ(IV) нет никаких агглютининов, поэтому перелитые эритроциты других групп никогда не будут агг- лютинироваться и, соответственно, лицам с четвёртой группой крови можно переливать кровь от людей с любой группой крови.
Правило Оттенберга применимо лишь при переливании до
При массивной кровопотере, когда необходимо перелить большее количество крови, агглютинины плазмы вливаемой крови не полу- чают достаточной степени разведения плазмой реципиента и, следовательно, могут агглютинировать его эритроциты.
По современным правилам во избежание этого осложнения всегда следует переливать только одногруппную кровь.
Особенность совместимости по резус-фактору
В норме в крови как резус-положительных, так и резус-отрицательных людей антирезусных антител нет. Причины их появления в сыворотке резус-отрицательных людей следующие:
• резус-конфликт при беременности;
• переливание резус-положительной крови;
• искусственная иммунизация добровольных доноров.
Резус-конфликт
Система резус-фактора играет большую роль в акушерстве и гинекологии. Во время беременности резус-отрицательной женщины резус-положительным плодом может происходить иммунизация беременной и образование у неё антител анти-D, которые из её крови проникают через плацентарный барьер, попадают в кровоток плода и повреждают его резус-положительные эритроциты и органы кроветворения. Возникает резус-конфликт. Указанные изменения ведут
к развитию гемолитической болезни, имеющей симптомы различной степени выраженности: от анемии, выраженной желтухи и отёка плода до нарушения беременности и мертворождения.
Первая беременность, как правило, заканчивается рождением здорового ребёнка, происходит только сенсибилизация матери к антигену D. В последующем, если снова развивается резус-положитель- ный плод, тяжесть проявления и последствий резус-конфликта нарастает. Иногда серьёзные последствия могут наступить и при первой беременности, в то время как в других случаях выраженность резусконфликта при второй, третьей беременностях может быть весьма умеренной. Степень выраженности осложнений зависит в первую очередь от титра антирезусных антител в сыворотке беременной. В связи с этим все резус-отрицательные беременные состоят на диспансерном учёте, у них регулярно контролируют содержание антител анти-D и в зависимости от полученных данных предпринимают соответствующее лечение, а иногда и искусственно прерывают беременность.
Переливание резус-несовместимой крови
Аналогичен механизм патологических изменений при переливании резус-несовместимой крови. Первое переливание резус-положи- тельной крови резус-отрицательному несенсибилизированному больному может не сопровождаться явлениями несовместимости, но обязательно приведёт к образованию антирезусных антител (сенсибилизации). При последующих трансфузиях этому больному резусположительной крови возникает несовместимость по Rh-фактору. Развитие резус-несовместимости опасно и при переливании резусположительной крови резус-отрицательной женщине, сенсибилизированной к резус-фактору во время беременности.
Искусственная иммунизация добровольных доноров
Процедуру проводят для получения антирезусной сыворотки и приготовления различных реагентов.
Современные правила переливания крови
На основании правила Оттенберга и анализа системы резус-фактора возникло понятие «универсальный донор». К таким донорам относят людей, имеющих группу крови 0(I) Rh-. Такую кровь в не- большом количестве относительно безопасно можно перелить реципиенту с любой группой крови.
Современные достижения иммуногематологии и клиническая практика показали, что при переливании крови универсального до- нора реципиентам других групп возможен гемолиз эритроцитов реципиента не только за счёт естественных антител (при массивной гемотрансфузии), но и изоиммунными антителами анти-A (реже анти-B) донорской крови. Эти антитела образуются у универсальных доноров при иммунизации антигенами A и B во время беременности, вакцинации и т.д. Чаще всего при этом появляются изоиммунные антитела анти-A (их частота у универсальных доноров достигает 10-16%).
Переливание резус-отрицательной крови резус-положительному реципиенту может привести к образованию антител на слабые антигены системы резус (С и E).
В связи с этим в настоящее время необходимо переливать только одногруппную (по системе АВ0) и однорезусную кровь!
Только в исключительных случаях - при жизненных показаниях к гемотрансфузии и невозможности определить группу крови больного или при отсутствии одногруппной донорской крови - допустимо использование крови универсального донора (отмытые эритроциты 0(I) группы) в количестве до 500 мл. Детям переливание любой крови, кроме одногруппной, запрещено!
Переливание крови и её компонентов
Современная трансфузионная терапия, согласно определению выдающегося советского трансфузиолога и хирурга A.H. Филатова (1973), - раздельное или сочетанное применение крови, её компонентов и препаратов, а также кровезамещающих растворов.
Прежде чем приступить к переливанию крови и её компонентов, каждый врач должен помнить, что гемотрансфузию нельзя считать индифферентным вмешательством, иногда она представляет серьёз- ную опасность для состояния здоровья и даже жизни больного. Кровь - одна из тканей организма, поэтому переливание крови от одного индивидуума другому можно рассматривать как операцию трансплантации ткани.
Показания к гемотрансфузии
Для определения показаний к гемотрансфузии необходимо знать механизм влияния на организм пациента перелитой крови.
Механизм действия перелитой крови
Биологические эффекты гемотрансфузии обусловлены сложнейшими регуляторными механизмами. Перелитая кровь действует на элементы нервной рецепции, а также ферментные и гормональные системы обмена, изменяя его на всех уровнях: от молекулярного до органно-тканевого.
Перелитая кровь оказывает на организм реципиента следующие эффекты:
• заместительный;
• гемодинамический;
• иммунологический;
• гемостатический;
• стимулирующий.
Заместительный эффект
Заместительное действие заключается в возмещении утраченной организмом части крови. Введённые в организм эритроциты восстанавливают объём крови и её газотранспортную функцию. Лейкоциты повышают иммунные способности организма. Тромбоциты корригируют систему свёртывания крови. Плазма и альбумин обладают гемодинамическим действием. Иммуноглобулины плазмы создают пассивный иммунитет. Факторы свёртывания крови и фибринолиза регулируют агрегатное состояние крови. Вводимые вместе с кровью питательные вещества (жиры, белки и углеводы) включаются в цепь биохимических реакций.
Эритроциты перелитой крови функционируют в сосудистом русле реципиента до 30 сут и более. Клетки белой крови покидают сосудистое русло вскоре после переливания, белки плазмы донорской крови циркулируют в сосудистом русле реципиента 18-36 дней.
Гемодинамический эффект
Переливание крови оказывает всестороннее воздействие на сердечно-сосудистую систему. У больных с острой кровопотерей и травматическим шоком оно приводит к стойкому увеличению ОЦК, увеличению венозного притока к правым отделам сердца, усилению работы сердца и повышению минутного объёма крови.
Улучшается микроциркуляция: расширяются артериолы и венулы, раскрывается сеть капилляров, в них ускоряется движение крови, сокращаются артериовенозные шунты, в результате чего редуци-
руется утечка крови из артериальной системы в венозную. Через 24- 48 ч после переливания крови у реципиента начинается усиленный приток тканевой лимфы в кровеносное русло, что также увеличивает ОЦК. Поэтому иногда после трансфузии прирост ОЦК превосходит объём перелитой крови.
Иммунологический эффект
Гемотрансфузия усиливает иммунологические свойства организма реципиента. За счёт введения гранулоцитов, макрофагов, лимфоцитов, компонентов комплемента, иммуноглобулинов, цитокинов, различные антибактериальных и антитоксических антител возрастает фагоцитарная активность лейкоцитов, активируется образование антител.
Особенно высоким иммунобиологическим действием обладают гипериммунные препараты плазмы, полученные от иммунизированных доноров, - антистафилококковая, антисинегнойная и противоожоговая плазма, иммуноглобулины направленного действия (антистафилококковый, противококлюшный, противостолбнячный иммуноглобулины и др.).
Гемостатический эффект
Переливание крови оказывает стимулирующее действие на систему гемостаза реципиента, вызывая умеренную гиперкоагуляцию, обусловленную увеличением тромбопластической и снижением антикоагулянтной активности крови. Переливание небольших доз (обычно 250 мл) тёп- лой крови или крови с малым сроком хранения (до 3 сут) оказывает гемостатическое действие благодаря активности вводимых с ней тромбоцитов и прокоагулянтов - факторов свёртывающей системы.
Особым гемостатическим действием обладают специальные виды плазмы (например, антигемофильная) и гемостатические препараты (фибриноген, криопреципитат, протромбиновый комплекс, тромбоцитарная масса и плазма, обогащённая тромбоцитами).
B то же время переливание массивных доз донорской крови в отдельных случаях может нарушить гемостатический баланс вплоть до развития синдрома диссеминированного внутрисосудистого свёрты- вания крови (ДBС-синдрома).
Стимулирующий эффект
После переливания крови в организме развиваются изменения, аналогичные стрессу. Происходит стимуляция гипоталамо-гипофизарно-
адреналовой системы, что подтверждается увеличением содержания кортикостероидов в крови и моче реципиентов в посттрансфузионном периоде. У реципиентов повышается основной обмен, увеличивается дыхательный коэффициент, усиливается газообмен. Переливание кро- ви оказывает стимулирующее действие на факторы естественного иммунитета: повышаются фагоцитарная активность гранулоцитов и образование антител в ответ на действие тех или иных антигенов.
Абсолютные и относительные показания к гемотрансфузии
Все показания к переливанию крови и её компонентов можно разделить на абсолютные и относительные.
Абсолютные показания
К абсолютным показаниям относят случаи, когда выполнение гемотрансфузии обязательно, а отказ от неё может привести к резкому ухудшению состояния больного или его смерти.
К абсолютным показаниям относят следующие:
• острая кровопотеря (более 21% ОЦК);
• травматический шок II-III степени.
• обширные операции с большой интраоперационной кровопотерей.
Относительные показания
Все остальные показания к гемотрансфузии, когда переливание крови играет лишь вспомогательную роль среди других лечебных мероприятий, считают относительными.
Основные относительные показания к гемотрансфузии:
• анемия;
• заболевания воспалительного характера с тяжёлой интоксикацией;
• продолжающееся кровотечение;
• нарушения свёртывающей системы крови;
• снижение иммунного статуса организма;
• длительные хронические воспалительные процессы со снижением регенерации и реактивности;
• некоторые отравления.
Учитывая распространённость кровезамещающих препаратов, выполняющих большую часть функций крови, в настоящее время основ- ным относительным показанием к гемотрансфузии считают анемию. Считают, что переливание крови становится методом выбора при снижении содержания гемоглобина ниже 80 г/л, а гематокрита - ниже 30%.
Противопоказания к гемотрансфузии
Гемотрансфузия связана с введением в организм значительного количества продуктов распада белков, что приводит к увеличению функциональной нагрузки на органы дезинтоксикации и выделения. Bведение дополнительного объёма жидкости в сосудистое русло существенно увеличивает нагрузку на сердечно-сосудистую систему. Гемотрансфузия приводит к активизации всех видов обмена в организме, что может привести к обострению и стимуляции патологических процессов (хронических воспалительных заболеваний, опухолей и пр.).
Bыделяют абсолютные и относительные противопоказания к переливанию крови.
Абсолютное противопоказание к гемотрансфузии - острая сердеч- но-лёгочная недостаточность, сопровождающаяся отёком лёгких.
Однако при массивной кровопотере и травматическом шоке IIIII степени абсолютных противопоказаний для переливания нет, и кровь следует переливать всегда.
Относительные противопоказания: свежие тромбозы и эмболии, тяжёлые расстройства мозгового кровообращения, ишемическая болезнь сердца, септический эндокардит, пороки сердца, миокардиты с недостаточностью кровообращения III степени, гипертоническая болезнь III стадии, тяжёлые функциональные нарушения печени и почек, серьёзные аллергические заболевания (бронхиальная астма, поливалентная аллергия), остротекущий и диссеминированный ту- беркулёз, ревматизм, особенно с ревматической пурпурой. При указанных заболеваниях прибегать к гемотрансфузии следует с особой осторожностью.
Способы переливания крови
По способу введения крови гемотрансфузии разделяют на внутривенные и внутриартериальные (внутрикостные в настоящее время не применяют). B подавляющем большинстве случаев кровь вводят в организм больного внутривенно капельно. Лишь при массивной кровопотере с резким ослаблением сердечной деятельности и крайне низким AД прибегают к внутриартериальному нагнетанию крови.
По виду используемой крови методы переливания можно разделить на две принципиально различные группы:
• переливание собственной крови (аутогемотрансфузия);
• переливание донорской крови.
Аутогемотрансфузия
Основная черта аутогемотрансфузии, определяющая её несомненное преимущество, - отсутствие иммунологических реакций на переливаемую кровь и передачи с кровью инфекционных заболеваний.
Поэтому аутогемотрансфузия показана прежде всего больным с редкими группами крови при невозможности подбора донора, паци- ентам с нарушенными функциями почек и печени, в случае наличия в анамнезе трансфузионных реакций на донорскую кровь и её компоненты.
Аутогемотрансфузию осуществляют двумя способами:
• трансфузия собственной заранее заготовленной крови;
• реинфузия крови.
Трансфузия заранее заготовленной крови
Такой метод аутогемотрансфузии применяют при плановых операциях, сопровождающихся массивной кровопотерей. Используют либо однократный метод забора крови, либо ступенчато-поэтапный метод. Противопоказания к заготовке крови с последующей гемотрансфузией включают исходную анемию и тяжёлые сопутствующие заболевания.
При однократном методе забора крови её рекомендуют забирать не менее чем за 72 ч до операции или же прямо перед операцией - метод аутогемотрансфузии в сочетании с изоволемической гемодилюцией. Проводят эксфузию в объёме 400-500 мл крови, возмещая её кровезамещающим раствором. Переливают кровь в конце операции после завершения основного по травматичности этапа или в раннем послеоперационном периоде. Однократный забор применяют при операциях с относительно небольшой кровопотерей.
Ступенчато-поэтапный метод позволяет накопить значительный (800 мл и более) объём крови путём чередования эксфузии и трансфузии ранее заготовленной аутокрови (метод «прыгающей лягушки»). Например, у больного забирают 400 мл крови, заместив кровезамещающим раствором или донорской плазмой. Через несколько дней забирают 600 мл крови, параллельно возмещая кровопотерю предварительно забранными 400 мл крови и кровезаменителями. Ещё через несколько дней аналогичным образом осуществляют забор уже 800 мл крови с возвращением 600 мл крови, забранной ранее, и введением плазмозамещающих средств. В результате в распоряжении врача к моменту операции будет достаточный запас свежей крови (800 мл).
Реинфузия крови
Реинфузия - разновидность аутогемотрансфузии, она заключается в переливании больному его собственной крови, излившейся в закрытые полости организма (грудную или брюшную), а также в операционную рану.
При реинфузии кровь собирают в асептических условиях специальными черпаками или с помощью стерильных трубок и добавляют стабилизатор (гепарин натрий и др.). После этого кровь фильтруют (наиболее просто - через 8 слоёв марли), собирают в стерильные флаконы (полиэтиленовые пакеты) и переливают через систему для гемотрансфузии (с фильтром) внутривенно.
В настоящее время созданы специальные аппараты для реинфузии крови пациента, теряемой в ходе операции («Cell Saver», «Haemolyte» и др.). В современной литературе эта процедура получила название «salvage» (salvage, англ. - спасение имущества). Эти устройства позволяют собирать кровь, стабилизировать, фракционировать, отмывать эритроциты, накапливать в специальных ёмкостях и реинфузировать через включённый в систему фильтр.
Противопоказания к реинфузии:
• нахождение крови в полости более 12 ч (возможность дефибринирования и инфицирования);
• сопутствующее повреждение полых органов (желудка, кишечника).
Во всех остальных случаях при массивном скоплении крови в полости или ране реинфузия становится методом выбора. Наиболее широко её применяют при нарушенной внематочной беременности, разрыве кисты яичника, разрыве селезёнки, внутриплевральном кровотечении, травматичных операциях на костях таза, бедренной кости, позвоночнике.
Переливание донорской крови
В качестве трансфузионной среды используют кровь донора. При этом переливание крови и её компонентов может быть непрямым (посредственным) и обменным.
Непрямое переливание
Непрямое переливание крови - основной метод гемотрансфузии. Он отличается простотой выполнения и несложным техническим оснащением, при нём исключены опасность инфицирования донора
и отрицательный психологический эффект присутствия донора при переливании.
Важно, что такой метод даёт возможность заготовки большого количества донорской крови, используемой затем как в плановом, так и в экстренном порядке.
При непрямом переливании заготовку крови в специальные флаконы (пакеты) с консервантом осуществляют в плановом режиме на станциях и в отделениях переливания крови. Заготовленная кровь, хранящаяся в определённых условиях, составляет так называемый банк крови.
При необходимости проводят переливание тёплой донорской крови: вызывают донора резерва, забирают у него кровь во флакон (пакет) со стабилизатором (цитратом) и непосредственно после забора, не позже чем через 3 ч, в другом помещении эту кровь переливают реципиенту.
Таким образом, переливают тёплую свежую кровь (свежецитратную), сохранившую все свои функции, но момент забора крови у до- нора и гемотрансфузия реципиенту разделены во времени и пространстве, что исключает всякий риск заражения донора.
В настоящее время после заготовки кровь фракционируют и хранят обычно её компоненты (эритроцитарную массу, плазму и др.).
Метод имеет и недостатки: в процессе хранения кровь и её компоненты теряют некоторые ценные целебные свойства, а наличие консервантов может вызывать побочные реакции у реципиента.
Обменное переливание
Обменное переливание крови - частичное или полное удаление крови из кровеносного русла реципиента с одновременным замеще- нием её адекватным или превышающим объёмом донорской крови. Основная цель этой операции - удаление вместе с кровью вредных для организма продуктов гемолиза, антител, ядов и т.д.
Обменное переливание крови применяют при гемолитической желтухе новорождённых (Rh-конфликт), массивном внутрисосудис- том гемолизе, тяжёлых отравлениях и пр.
Методика гемотрансфузии
Переливание крови и её компонентов выполняет лечащий врач, дежурный врач, врач отделения или кабинета переливания крови, а во время операции - хирург или анестезиолог, непосредственно не участвующий в операции или проведении наркоза. В подавляющем
большинстве случаев используют непрямое переливание консервированной донорской крови. При этом врач должен выполнить опре- делённые требования.
Порядок действий врача при переливании крови
Порядок действий врача при переливании крови следующий:
1. Определить показания к гемотрансфузии, выявить противопоказания, собрать трансфузиологический анамнез.
2. Определить группу крови и резус-фактор реципиента.
3. Bыбрать соответствующую (одногруппную и однорезусную) кровь и макроскопически оценить её годность.
4. Перепроверить группу крови донора (из флакона) по системе AB0.
5. Провести пробу на индивидуальную совместимость по системе AB0.
6. Провести пробу на индивидуальную совместимость по Rh.
7. Провести биологическую пробу.
8. Bыполнить гемотрансфузию.
9. Заполнить документацию.
10. Осуществить наблюдение за пациентом после гемотрансфузии. Определение показаний и противопоказаний к гемотрансфузии,
группы крови по системе AB0 и резус-фактору проводят по общим правилам, изложенным выше.
Сбор трансфузионного анамнеза
Необходимо выяснить у пациента, знает ли он свои группу крови и резус-фактор (информацию используют как дополнительные сведения), были ли в прошлом переливания крови и её компонентов, не было ли при этом каких-либо осложнений. Женщин расспрашивают о количестве беременностей и их осложнений (особенно у резус-отрицательных женщин).
Макроскопическая оценка годности крови
Bрач, проводящий гемотрансфузию, должен быть уверен в том, что трансфузионная среда пригодна для переливания. Для этого проводят визуальный контроль флакона или контейнера с кровью или её компонентами.
При визуальном контроле необходимо отметить следующие факты: 1. Правильность паспортизации (наличие этикетки с номером, даты заготовки, обозначения группы и резус-принадлежности, наи-
менования консерванта, фамилии и инициалов донора, наименования учреждения-заготовителя, подписи врача).
2. Срок годности. Раньше при использовании в качестве консерванта глюгицира обозначали только дату заготовки крови, при этом переливать кровь можно было в течение 21 дня. В последнее время применение новых консервантов дало возможность увеличить этот срок (максимально до 35 сут). Поэтому срок годности в настоящее время обозначают на этикетке наряду с датой заготовки.
3. Герметичность упаковки. Недопустимо малейшее нарушение её целостности (в том числе следы прокалывания крышки флакона иглой).
4. Кровь должна быть разделена на три слоя (внизу - красные эритроциты, выше - узкая серая полоса лейкоцитов и тромбоцитов, над ними - жёлтая прозрачная плазма). Трёхслойность характерна только для цельной крови, хранящейся в стеклянных флаконах.
5. Плазма должна быть прозрачной, не содержать плёнок и хлопьев (инфицированная кровь), а также сгустков, не иметь красной окраски (гемолиз). Плазма может быть непрозрачной при так называе- мой хилёзной крови (высокое содержание нейтральных жиров). При нагревании хилёзной крови в термостате до 37 ?С плазма становится прозрачной (в случае инфицированной крови - остаётся мутной).
Если при макроскопической оценке хотя бы одно из представленных требований не выполнено, такую кровь переливать нельзя.
Пробы на индивидуальную совместимость
Пробы на индивидуальную совместимость проводят в процессе подготовки к гемотрансфузии. Ставят две реакции: пробу на индивидуальную совместимость по системе АВ0 и по резус-фактору. Для по- становки реакций необходимо получить сыворотку реципиента. Поэтому предварительно у него из вены берут кровь, которую разделяют на сгусток и сыворотку (отстаиванием или центрифугированием).
Проба на индивидуальную совместимость по системе АВ0
На белую поверхность (тарелку, пластинку) наносят крупную каплю (0,1 мл) сыворотки крови реципиента и маленькую каплю (0,01 мл) крови донора из флакона, смешивают их между собой, периодически покачивая тарелку (пластинку). Реакцию проводят при температуре 15-25 ?С, результаты оценивают через 5 мин: отсутствие агглютинации эритроцитов донора свидетельствует о совместимости крови донора и реципиента по системе АВ0. Появление агглютинации
указывает на их несовместимость - такую кровь данному больному переливать нельзя.
Проба на индивидуальную совместимость по резус-фактору
После того как установлена совместимость крови донора и реципиента по системе АВ0, необходимо установить совместимость в отношении резус-фактора. Пробу на совместимость по резус-фактору проводят с использованием 33% декстрана (ср. мол. масса 50 000- 70 000).
Реакцию проводят в центрифужной пробирке без подогрева в течение 5 мин. На дно пробирки вносят 2 капли сыворотки реципиен- та, 1 каплю донорской крови и 1 каплю 33% раствора декстрана (ср. мол. масса 50 000-70 000). После этого содержимое перемешивают, наклоняя пробирку и вращая её вокруг оси, распределяя содержимое по стенкам ровным слоем. Пробирку вращают в течение 5 мин, после чего добавляют 3-4 мл физиологического раствора и аккуратно перемешивают, 2-3 раза наклоняя пробирку до горизонтальной плос- кости (не взбалтывая!). После этого оценивают результат: наличие агглютинации эритроцитов свидетельствует о несовместимости крови донора и реципиента по резус-фактору, такую кровь переливать нельзя. Равномерное окрашивание содержимого в пробирке, отсутствие реакции агглютинации указывает на совместимость крови донора и реципиента по резус-фактору.
При совместимости крови донора и реципиента по системе АВ0 и резус-фактору можно приступать к дальнейшим операциям. Однако у некоторых реципиентов (при наличии неполных скрытых или блокирующих антител, низкой активности иммунных антител) указанные пробы не выявляют несовместимости. Поэтому определённой категории лиц проводят индивидуальный подбор крови.
Индивидуальный подбор донорской крови
Индивидуальный подбор донорской крови необходим следующим группам реципиентов:
• Изоиммунизированные предшествующими гемотрансфузиями или беременностями.
• Перенёсшие гемотрансфузионное осложнение.
• Нуждающиеся в массивной гемотрансфузии.
• При невозможности подобрать кровь обычными пробами на совместимость.
Индивидуальный подбор выполняют в специальных лабораториях, для этого необходимо особое оснащение. Проводят более чувствительные пробы на совместимость (реакция агглютинации в солевой среде, непрямая проба Кумбса, проба на совместимость с желатином).
При переливании индивидуально подобранной крови врач, осуществляющий гемотрансфузию, обязан выполнить все описанные выше контрольные исследования, в том числе и пробы на индивидуальную совместимость.
Биологическая проба
Несмотря на определение совместимости крови донора и больного по системе АВ0 и резус-фактору, нельзя быть уверенным в полной их совместимости.
Существует большое количество второстепенных групповых систем, способных стать причиной развития осложнений. Для исключе- ния этой возможности в начале гемотрансфузии проводят ещё одну пробу на совместимость - биологическую пробу.
Сначала струйно переливают 15 мл крови, затем трансфузию прекращают (перекрывают капельницу) и в течение 3 мин наблюдают за состоянием больного. При отсутствии клинических проявлений реакции или осложнения (боль в пояснице, за грудиной, учащение пульса, дыхания, снижение АД, появление одышки, затруднение дыхания, гиперемия лица и т.д.) вводят вновь 15 мл крови и в течение 3 мин снова наблюдают за больным. Процедуру проводят ещё раз (всего трижды).
Отсутствие реакций у больного после трёхкратной проверки - признак совместимости вливаемой крови, это служит основанием для осуществления всей гемотрансфузии.
При несовместимости крови донора и реципиента во время биологической пробы поведение пациента становится беспокойным: появляются тахикардия, одышка, гиперемия лица, ощущение озноба или жара, стеснение в груди, боли в животе и очень важный признак - боли в поясничной области. При появлении этих признаков кровь считают несовместимой, гемотрансфузию не проводят.
Классическую биологическую пробу не проводят при переливании крови пациенту, находящемуся под наркозом (иммунные реакции замедлены, отсутствуют жалобы, недостаточно стабильны гемодинамические показатели). В таких случаях признаками несовместимости крови считают необоснованное снижение АД, учащение пульса, появление гипере-
мии кожи по ходу вены, в которую переливают кровь, или изменение цвета кожных покровов лица и туловища больного. Важнейший метод своевременного выявления несовместимости крови донора и реципиента во время наркоза - контроль диуреза (скорость диуреза, цвет мочи). Снижение скорости или прекращение диуреза, изменение окраски мочи (моча цвета «мясных помоев») - грозные признаки несовместимости переливаемой донорской крови. Вопрос о дальнейшей трансфузионной терапии решает анестезиолог совместно с оперирующим хирургом.
Осуществление гемотрансфузии
При отсутствии признаков биологической несовместимости начинают капельное переливание крови. Перед трансфузией флакон с переливаемой кровью должен находиться при комнатной температуре в течение 30-40 мин, а в экстренных ситуациях его подогревают до 37 ?С на водяной бане (под контролем термометра!). Переливание проводят с помощью одноразовой системы для переливания крови с фильтром, обычно со скоростью 40-60 капель в мин.
В течение гемотрансфузии продолжают наблюдение за состоянием больного: выясняют жалобы, определяют пульс, АД и темперауру тела, следят за цветом кожных покровов.
После переливания контейнер или флакон с остатками трансфузионной среды (около 15 мл) и сыворотку реципиента хранят в течение 2 сут в холодильнике, чтобы можно было провести анализ гемот- рансфузионных осложнений в случае их развития.
Заполнение документации
Перед гемотрансфузией врач пишет в истории болезни больного предтрансфузионный эпикриз, включающий трансфузионный и акушерский анамнез, показания к переливанию, наименование и дозу трансфузионной среды.
После окончания трансфузии врач записывает в истории болезни протокол переливания крови:
• показания к трансфузии;
• паспортные данные с каждого флакона: фамилия донора, группа крови, резус-принадлежность, номер флакона, дата заготовки крови;
• группа крови и Rh-фактор реципиента и донора;
• результаты проб на индивидуальную совместимость крови донора и реципиента по системе АВ0 и Rh-фактору;
• результат биологической пробы;
• наличие реакций и осложнений;
• дата, фамилия врача, переливавшего кровь, подпись. Соответствующую запись с указанием основных данных истории
болезни пациента (ФИО, возраст, диагноз, номер истории болезни) врач производит и в специальном «Журнале регистрации переливания крови, её компонентов и препаратов».
Наблюдение за больным после гемотрансфузии
Реципиент после переливания крови соблюдает в течение 3 ч постельный режим, за ним наблюдают врачи в течение суток.
Особенно тщательное наблюдение проводят в течение первых 3 ч после гемотрансфузии. Оценивают наличие жалоб, изменение общего состояния, каждый час измеряют температуру тела, пульс и АД. Эти данные фиксируют в истории болезни. Необходимо макроскопически оценить первую порцию мочи после переливания крови, обратить внимание на объём диуреза и окраску мочи (при гемотрансфузионных осложнениях моча приобретает бурую окраску). После переливания крови под наркозом на операционном столе следует вывести мочу катетером и также оценить её макроскопически.
На следующий день обязательно выполнение клинического анализа крови и общего анализа мочи.
Виды, компоненты и препараты крови
При лечении больных используют различные виды цельной крови, а также её компоненты и препараты (табл. 6-6).
Виды цельной крови Свежецитратная донорская кровь
Заготавливают на растворах среднего кислого цитрата натрия, используют в течение 1-3 ч после забора у донора. По эффективности переливание такой крови аналогично прямому переливанию крови, но метод проще и безопаснее для донора. Применяют при нарушениях свёртывающей системы крови реципиента.
Консервированная донорская кровь
Заготавливают на одном из консервирующих растворов. В состав консервирующего раствора входят стабилизатор крови, консервант
Таблица 6-6. Виды цельной крови, её компоненты и препараты

(обычно раствор глюкозы), антисептические средства. Срок годности такой крови для переливания 21-35 дней - в зависимости от вида консерванта.
При использовании растворов «глюгицир» или «цитроглюкофосфат» - 21 день, «цитроглюфад» - 35 дней.
Следует отметить, что не все функции крови сохраняются весь период хранения. С гемостатической целью следует переливать кровь, имеющую срок хранения не более 2-3 сут, иммунные свойства сохраняются до 5-7 сут. В течение всего срока хранения в той или иной степени поддерживается способность эритроцитов осуществлять транспорт кислорода.
В настоящее время переливание цельной донорской крови используют реже в связи с переходом к принципиально новой тактике - компонентной гемотерапии.
Аутологичная кровь
Применяют для аутогемотрансфузии (вливания заранее заготовленной собственной крови реципиента) и реинфузии (возврата больному собственной, крови, излившейся в серозные полости или операционную рану). Для предотвращения свёртывания к крови добавляют гепарин натрий или один из стабилизаторов.
Понятие о компонентной гемотерапии
До недавнего времени цельную консервированную донорскую кровь считали единственным наиболее эффективным универсальным сред-
ством лечения. В настоящее время углублённое изучение влияния цельной крови на организм реципиента позволило сделать вывод о том, что гемотрансфузии представляют значительный риск. При переливании цельной крови реципиент получает, помимо необходимых ему компонентов (например, эритроцитов), функционально неполноценные тромбоциты и лейкоциты, иммуноагрессивные лимфоциты, антитела и антигены, способные стать причиной посттрансфузионных реакций и осложнений. Кроме того, консервирование и хранение значительно изменяют свойства крови (образуются микросгустки, происходят закисление среды, разрушение эритроцитов и накопление калия, аммиака, свободного гемоглобина и других продуктов метаболизма, обладающих токсическим действием). Всё это, а также достижения в области фракционирования крови и появление высокоактивных препаратов гемодинамического, реологического, дезинток- сикационного, антианемического и гемостатического действий заставило пересмотреть отношение к переливанию цельной донорской крови и выдвинуть новые подходы к трансфузионной терапии, основанные на принципе возмещения конкретных, недостающих организму при той или иной патологии компонентов крови. Такая тактика получила название «компонентная гемотерапия».
Благодаря компонентной терапии появилась возможность проводить целенаправленное трансфузионное воздействие на организм, получать значительно больший лечебный эффект при ряде патоло- гических состояний и одновременно избегать негативных последствий, свойственных переливанию цельной крови.
При острой и хронической кровопотере целесообразно переливание эритроцитарной массы, при тромбоцитопенических состояниях - тромбоцитарной, при лейкопении - лейкоцитарной массы, при дефиците ОЦК, гипопротеинемии, нарушениях свёртывающей системы - плазмы крови, при диспротеинемии и гипопротеинемии - протеина, растворов альбумина.
При этом следует учитывать, что в полном замещении дефицита того или иного клеточного или белкового компонента нет необходимости, да это практически и недостижимо. Целенаправленность трансфузи- онной терапии состоит в купировании критического дефицита компонента крови, ставшего причиной нарушения стабильного состояния больного. Так происходит при дефиците эритроцитов в случае острого кровотечения или хронической анемии, результатом которой становятся симптомы анемической гипоксии; при выраженном дефиците тромбоцитов, приводящем к развитию тромбоцитопенического
геморрагического синдрома, и т.д. Основные компоненты крови, используемые в трансфузиологии, - эритроцитсодержащие среды, концентраты лейкоцитов и тромбоцитов, плазма.
Основные компоненты крови Эритроцитсодержащие среды
В настоящее время используют следующие эритроцитсодержащие среды: эритроцитарную массу, эритроконцентрат, эритроцитарную взвесь; эритроцитарную массу, обеднённую лейкоцитами и тромбо- цитами; отмытые эритроциты, модифицированную кровь.
Эритроцитарную массу получают путём удаления плазмы крови при отстаивании или центрифугировании. Гематокрит составляет 65-80%. Таким образом, эритроцитарная масса содержит определённую примесь лейкоцитов, тромбоцитов плазменных белков и иммунных комплексов, способных стать причиной сенсибилизации больных и развития посттрансфузионных осложнений.
Эритроконцентрат получают при центрифугировании путём полного удаления плазмы и лейко-тромбоцитарного слоя. Гематокрит 90-95%.
Эритроцитарная взвесь - эритроконцентрат, ресуспензированный в каком-либо растворе. Наилучшими свойствами обладают эритроцитарная взвесь в растворах «Модежель» и «НАФ» (соотношение эритроконцентрата и раствора 1:1 и 2:1).
Срок хранения эритроцитарной массы, эритроконцентрата и эритроцитарной взвеси в зависимости от консерванта - 21 или 35 сут.
В процессе приготовления эритроцитарной массы, обеднённой лейкоцитами и тромбоцитами и отмытых эритроцитов удаляют белки плазмы, лейкоциты, тромбоциты, микроагрегаты и стромы разрушенных при хранении клеточных компонентов. Применение отмытых эритроцитов уменьшает вероятность заражения вирусными заболеваниями. Срок хранения при температуре 4 ?С составляет 24 ч с момента заготовки.
Модифицированную кровь готовят путём центрифугирования: из крови удаляют плазму и лейкотромбоцитоцитарный слой, но затем плазму возвращают. Таким образом, модифицированная кровь - эритроциты вместе с плазмой.
В последнее время успех криотехнологий позволил замораживать эритроцитврную массу. В таком состоянии в бункерах с жидким азотом её можно хранить до 10 лет. Перед применением эритроцитарную массу размораживают и отмывают. Срок хранения после отмывания при температуре 4 ?С составляет 24 ч.
Основное показание к применению эритроцитсодержащих сред - снижение содержания эритроцитов, произошедшее в результате острой или хронической кровопотери, неадекватного эритропоэза или при гемолизе.
Отмытые эритроциты показаны больным, у которых в анамнезе отмечены посттрансфузионные реакции негемолитического типа, а также пациентам, сенсибилизированным к антигенам белков плазмы, тканевым антигенам, антигенам лейкоцитов и тромбоцитов. В связи с отсутствием в отмытых эритроцитах стабилизаторов крови и продуктов метаболизма, оказывающих токсическое действие, их трансфузии показаны при лечении тяжёлых анемий у больных с пе- чёночной и почечной недостаточностью, а также при синдроме мас- сивных гемотрансфузий.
При переливании всех эритроцитсодержащих сред соблюдают те же правила, что и при переливании цельной крови.
Концентрат лейкоцитов
Концентрат лейкоцитов - трансфузионная среда с высоким содержанием лейкоцитов и примесью небольшого количества эритро- цитов и тромбоцитов, получаемая с помощью рефрижераторной центрифуги или сепаратора клеток крови.
Основная функция концентрата лейкоцитов - фагоцитоз микробов и коррекция иммунодепрессии различного генеза.
Концентрат лейкоцитов применяют либо свежезаготовленный, либо со сроком хранения не более 1 сут. Это обусловлено истощением энергетического потенциала лейкоцитов и их гибелью в процессе хранения в течение нескольких суток.
Показания к применению концентрата лейкоцитов: лейкопения менее 1,5х109/л при различных заболеваниях, иммунодефицитные состояния при гнойно-септических осложнениях в хирургии, лейкопения при цитостатической и лучевой терапии, медикаментозные агранулоцитозы.
При переливании клнцентрата лейкоцитов необходимы совпадение группы крови и Rh-фактора донора и реципиента и проведение лимфоцитотоксического теста.
Концентрат тромбоцитов
Концентрат тромбоцитов готовят из обогащённой тромбоцитами плазмы или лейко-тромбоцитарного слоя. Тромбоциты - один из
ведущих компонентов системы гемостаза, в связи с чем концентрат тромбоцитов применяют прежде всего при нарушении системы спонтанного гемостаза. Функциональные свойства тромбоцитов в концентрате тромбоцитов сохраняются до 120 ч.
Показания к применению концентрата тромбоцитов: тромбоцитопенический синдром, ДВС-синдром, депрессия костномозгового кроветворения после лучевой и цитостатической терапии. Трансфу- зия концентрата тромбоцитов показана при уменьшении количества тромбоцитов ниже 40х109/л.
При переливании концентрата тромбоцитов необходимо совпадение группы крови и Rh-фактора донора и реципиента.
Плазма
Плазма - жидкая часть крови; в её состав входят белки, липопротеиды, разнообразные ферменты, гормоны, витамины и биологически активные вещества. Наряду с эритроцитсодержащими средами плазма - наиболее часто используемый компонент крови.
В настоящее время применяют плазму свежезамороженную, жидкую (нативную) и сухую (лиофилизированную). Нативная и сухая плазма в процессе изготовления теряет некоторые лечебные свойства, в ней снижается содержание белка, фибриногена, компонентов свёртывающей и ферментативной систем.
Наиболее широко используют свежезамороженную плазму, так как в ней сохранены практически все биологические свойства плазмы.
Свежезамороженную плазму получают методом плазмафереза или центрифугирования цельной крови и немедленного её заморажива- ния. Хранят при температуре -20 ?С и ниже, срок хранения до 12 мес.
Непосредственно перед переливанием плазму оттаивают в воде при температуре 37-38 ?С, размороженная плазма до переливания может сохраняться не более часа. Повторное замораживание и размораживание её недопустимо! Плазму используют с заместительной целью, для обеспечения дезинтоксикационного, стимулирующего эффектов и гемостатического действия. Показаниями к переливанию плазмы считают ДВС-синдром, массивную кровопотерю (для коррекции ОЦК), ожоговую болезнь (значительная плазмопотеря), гнойно-сеп- тические состояния, коагулопатии, гемофилии А и В, сопровождающиеся кровотечениями, гипопротеинемию и т.д.
Переливание плазмы противопоказано при выявлении у больных гиперкоагуляции или сенсибилизации к парентеральному вве- дению белка.
В последние годы всё чаще применяют специальные виды плазмы: антигемофильную - при гемофилии, антистафилококковую, антиколи-, антисинегнойную и прочие - при септических состояниях.
При переливании плазмы необходимо совпадение группы крови донора и реципиента по системе АВ0. При переливании плазмы про- водят биологическую пробу.
Препараты крови
Методом фракционирования плазмы получают различные белковые препараты. Их делят на три группы (по О.К. Гаврилову):
• Препараты комплексного действия (альбумин, протеин).
• Корректоры свёртывающей системы крови (криопреципитат, протромбиновый комплекс, фибриноген, тромбин, тампон биологический антисептический, гемостатическая губка, фибринолизин).
• Препараты иммунологического действия (γ-глобулин противокоревой; антирезусный, антистафилококковый, противостолбнячный и противогриппозный иммуноглобулины).
Препараты комплексного действия
Альбумин - белок плазмы крови с молекулярной массой 69000, синтезируемый в печени. Он выполняет транспортную и дезинтоксикационную функции, поддерживает коллоидно-осмотическое давление плазмы.
Растворы альбумина обладают высокой онкотической активностью и хорошими волемическими свойствами. Так, переливание 200 мл 20% альбумина за счёт привлечения в сосудистое русло жидкости из межклеточного пространства увеличивает ОЦК на 700 мл (гемодинамическое действие).
Растворы альбумина готовят из донорской плазмы и плацентарной сыворотки. Выпускают в виде 5%, 10%, 20% растворов. Срок хранения 5 лет. Препараты альбумина применяют без учёта групповой принадлежности. Технология изготовления растворов альбумина предусматривает инактивацию в них вируса гепатита и ВИЧ.
Альбумин применяют для возмещения дефицита ОЦК при кровотечении, плазмаферезе; заболеваниях, сопровождающихся гипоаль- буминемией; ожоговой болезни, гнойно-септических процессах, инфекционных заболеваниях и отравлениях. Показанием к введению альбумина считают снижение содержания альбумина в плазме до 25 г/л. Относительное противопоказание к применению - аллерги-
ческие заболевания (бронхиальная астма, аллергический ринит, отёк Квинке и др.).
Для предупреждения аллергических реакций рекомендуют проведение биологической пробы.
Протеин - 4,3-4,8% изотонический раствор белков плазмы чело- века. Состоит из альбумина (80%) и глобулинов (20%), а также эрит- ропоэтических активных веществ. Выпускают во флаконах по 250,
400 и 500 мл.
Хранят при комнатной температуре до 5 лет. Вируса гепатита и ВИЧ содержать не может.
Показания к применению те же, что и у альбумина; кроме того, протеин обладает антианемическим действием, так как содержит железо в виде альбумината.
Относительным противопоказанием считают неблагоприятный аллергологический анамнез. Для предупреждения аллергических ре- акций рекомендуют проведение биологической пробы.
Корректоры системы гемостаза
Криопреципитат содержит антигемофильный глобулин (VIII фактор), фибриноген и фибриностабилизирующий фактор (XIII фактор). Выпускают во флаконах по 15 мл. Показан к применению для профилактики и лечения кровотечений у больных гемофилией А, болезнью фон Виллебранда и при других заболеваниях, сопровождающихся снижением содержанием VIII фактора свёртывающей системы в крови больного.
Протромбиновый комплекс (PPSB) - белковая фракция плазмы крови с высоким содержанием II, VII, IX и X факторов свёртывания крови. Выпускают во флаконах, каждый из них содержит от 200 до 1000 ЕД IX фактора. Показан к применению с гемостатической целью больным, страдающим гипопротромбинемией, гипопроконвер- тинемией, гемофилией В.
Фибриноген содержит одноимённый белок, получаемый из плазмы крови. Его применение показано в случаях выраженной гипо- и афибриногенемии (при профузных кровотечениях, патологии беременности и родов, хирургических заболеваниях), при повышении фибринолитической активности, наследственной гипо- и афибриногенемии, для профилактики кровотечения в послеоперационном периоде.
Тромбин содержит тромбин, небольшое количество тромбопластина и хлорида кальция. Выпускают в лиофилизированном виде во флаконах. Показан для местного применения при остановке капиллярных и паренхиматозных кровотечений.
Гемостатическая губка - сухая пористая масса, хорошо поглощающая влагу, изготавливают из плазмы крови человека. Гемостатическое действие осуществляется за счёт значительного количества тромбина и фибриногена. Оставленная в тканях губка полностью рассасывается. Применяют при кровотечениях из паренхиматозных органов, повреждённых тканей, костей черепа при трепанации.
Фибринолизин - препарат фибринолитического действия. Механизм действия фибринолизина заключается в растворении сгустка крови благодаря протеолитическому расщеплению фибрина.
Препараты иммунологического действия
Из фракции глобулинов получают иммунологически активные препараты: γ-глобулины (иммуноглобулины), содержащие антитела в концентрированном виде. Препараты готовят из крови с высоким титром антител (крови людей, перенёсших соответствующее инфекционное заболевание, иммунных доноров, иммунизированных животных).
Иммунизация, проводимая по специальным схемам, позволяет получить высокоэффективные γ-глобулины направленного действия: антирезусный, противостолбнячный, противогриппозный и др. Указан- ные препараты - средства пассивной иммунизации. Выпускают иммуноглобулины в виде 10% раствора для внутримышечного введения. Как правило, реакций на их введение нет. В редких случаях возможны местные явления и незначительное повышение температуры тела. Перед введением необходимо уточнить аллергологический анамнез.
Кровезамещающие растворы
Переливание цельной крови, её компонентов и препаратов, несмотря на множество положительных моментов, несёт опасность пе- реноса инфекционных заболеваний, а также развития реакций несовместимости, поэтому по возможности функции крови стараются заместить специальными препаратами, получившими название «кровезамещающие растворы» (или «кровезаменители»).
Кровезаменителями называют лечебные растворы, предназначенные для замещения утраченных или нормализации нарушенных функций крови.
В настоящее время в мире насчитывают несколько тысяч препаратов, относимых к группе кровезаменителей. Их широко применяют для поддержания и коррекции основных констант гомеостаза при
различных патологических состояниях. Кровезаменители отличаются высокой эффективностью, целенаправленностью действия, их пе- реливание проводят без учёта групповой принадлежности. Они имеют большие сроки хранения, их легко транспортировать, ими можно обеспечить большой контингент больных и раненых в экстремальных ситуациях.
По функциональным свойствам и преимущественной направленности кровезамещающие растворы делят на несколько групп:
• кровезаменители гемодинамического действия;
• дезинтоксикационные растворы;
• кровезаменители для парентерального питания;
• регуляторы водно-солевого обмена и кислотно-щелочного равновесия;
• переносчики кислорода;
• инфузионные антигипоксанты.
Кровезаменители гемодинамического действия
Препараты гемодинамического действия (противошоковые кровезаменители) предназначены для нормализации показателей центральной и периферической гемодинамики, нарушающихся при кровопотере, механической травме, ожоговом шоке и различных заболеваниях внутренних органов (перфоративной язве желудка и двенадцатиперстной кишки, кишечной непроходимости, остром холецистите, остром панкреатите, экзогенных и эндогенных интоксикациях).
Растворы этой группы обладают высокой молекулярной массой и выраженными коллоидно-осмотическими свойствами, за счёт чего длительно циркулируют в сосудистом русле и привлекают в него межклеточную жидкость, значительно увеличивая ОЦК (волемический эффект). Помимо основного действия, гемодинамические кровезаменители обладают и дезинтоксикационным действием, улучшают микроциркуляцию и реологические свойства крови.
К противошоковым кровезаменителям относят четыре группы препаратов:
• производные декстрана;
• препараты желатина;
• производные гидроксиэтилкрахмала;
• производные полиэтиленгликоля.
Производные декстрана
В зависимости от молекулярной массы выделяют:
• среднемолекулярные растворы (декстран [ср. мол.масса 50 000- 70 000]);
• низкомолекулярные растворы (декстран [мол.масса 30 000- 40 000], декстран [ср. мол. масса 30 000-50 000] + маннитол + натрия хлорид, декстран [мол. масса 30 000-40 000]).
Основной среднемолекулярный препарат декстрана - декстран [ср. мол.масса 50 000-70 000], низкомолекулярный - декстран [мол.
масса 30 000-40 000].
Декстран [ср. мол.масса 50 000-70 000] - 6% раствор среднемоле- кулярной фракции декстрана (молекулярная масса 60 000-80 000) в изотоническом растворе натрия хлорида. При внутривенном введении он быстро увеличивает ОЦК, повышает и стойко поддерживает АД. Декстран [ср. мол.масса 50 000-70 000] увеличивает объём циркулирующей жидкости в кровеносном русле на величину, превышающую объём введённого препарата, что обусловлено его высоким коллоид- но-осмотическим давлением. В организме циркулирует от 3 до 7 сут, в первые сутки выводится 45-55% препарата, преимущественный путь выведения - через почки. Введение декстрана [ср. мол. масса 50 000-70 000] усиливает окислительно-восстановительные процессы в организме и утилизацию тканями кислорода из притекающей крови. Струйное введение препарата повышает тонус сосудов.
Декстран [ср. мол.масса 50 000-70 000] показан при лечении травматического, операционного или ожогового шока, острой кровопотери, острой циркуляторной недостаточности при различных забо- леваниях. Побочные реакции при введении декстрана [ср. мол.масса 50 000-70 000] чрезвычайно редки. Однако у некоторых лиц (менее 0,001%) наблюдают индивидуальную повышенную чувствительность к препарату, проявляющуюся в развитии симптомов анафилаксии вплоть до анафилактического шока. Для предупреждения этой реакции при использовании декстрана [ср. мол.масса 50 000-70 000] необходимо проводить биологическую пробу.
Декстран [мол.масса 30 000-40 000] - 10% раствор низкомолекулярного декстрана (молекулярная масса 20 000-40 000) в изотоническом растворе хлорида натрия или 5% растворе глюкозы. Так же, как и декстран [ср. мол.масса 50 000-70 000], является гиперонкотическим коллоидным раствором, при внутривенном введении значительно увеличивает ОЦК. Каждый грамм препарата связывает в кровяном русле 20-25 мл воды. Этим обусловлено его гемодинамическое
действие. Декстран [мол.масса 30 000-40 000] циркулирует в организме 2-3 сут, 70% препарата выводится за первые сутки с мочой.
Основной эффект действия декстрана [мол.масса 30 000-40 000], в отличие от декстрана [ср. мол.масса 50 000-70 000], - улучшение реологических свойств крови и микроциркуляции. Это обусловлено спо- собностью препарата вызывать дезагрегацию эритроцитов, купировать стаз крови и предупреждать тромбообразование. Возникшая в крови высокая концентрация препарата способствует поступлению жидкости из тканей в кровеносное русло, что приводит к гемодилюции и снижению вязкости крови. Молекулы декстрана покрывают поверхность клеточных элементов крови, изменяют электрохимические свойства эритроцитов и тромбоцитов. Антитромботическое действие декстрана [мол.масса 30 000-40 000], вероятно, обусловлено увеличением отрицательного заряда тромбоцитов и снижением их способности к адгезии и агрегации. Показаниями к применению декстрана [мол.масса 30 000-40 000] считают нарушения микроциркуляции при шоке различного происхождения, тромбоэмболические осложнения, операции на открытом сердце, сосудистые заболевания, хирургические вмешательства на сосудах, посттрансфузионные осложнения.
Реакции и осложнения при использовании декстрана [мол.масса 30 000-40 000] такие же, как при применении декстрана [ср. мол.масса 50 000-70 000]. Перед введением также необходимо проводить био- логическую пробу.
Препараты желатина
Родоначальник группы и наиболее распространённый препарат - желатин.
Желатин - 8% раствор частично расщеплённого пищевого желатина в изотоническом растворе хлорида натрия (молекулярная масса 15 000-25 000). Желатин - белок, содержащий аминокислоты: глицин, пролин и др. Лечебное действие в основном связано с его высоким коллоидно-осмотическим давлением, обеспечивающим быстрое поступление тканевой жидкости в сосудистое русло. Как гемодинамические препараты желатин и его аналоги менее эффективны, чем декстраны. Они быстрее покидают сосудистое русло и распределяются во внеклеточном пространстве. Желатин нетоксичен, апирогенен, антигенные реакции нехарактерны. Основная часть препарата выводится почками.
Показания для применения: острая гиповолемия, различные виды шока и интоксикации. Препарат противопоказан при острых забо- леваниях почек и жировой эмболии.
Из-за возможных аллергических реакций при применении желатина обязательно проведение биологической пробы.
Производные гидроксиэтилкрахмала
Первое поколение растворов на основе гидроксиэтилкрахмала было создано из картофельного крахмала, но препараты не были допущены к клиническому применению. Второе поколение растворов (HAES-стерил, плазмостерил, темохес, рефортан, стабизол) изготовлено из кукурузного крахмала. К отечественным препаратам этой группы относят волекам и оксиамал.
Наибольшее распространение получили HAES-стерил и плазмостерил. По строению препараты близки к гликогену животных тканей и способны разрушаться в кровеносном русле амилолитическими ферментами. Растворы на основе гидроксиэтилкрахмала обладают хорошим гемодинамическим действием, побочные эффекты редки.
При применении производных гидроксиэтилкрахмала на 3-5-е сут может повышаться концентрация сывороточной амилазы. В редких случаях препараты могут вызывать анафилактоидные реакции, по- этому целесообразно проведение биологической пробы.
Производные полиэтиленгликоля
К этой группе кровезаменителей относят полиоксидин - 1,5% раствор полиэтиленгликоля в 0,9% растворе хлорида натрия. Молеку- лярная масса 20 000. По гемодинамическим и волемическим характеристикам близок препаратам из группы гидроксиэтилкрахмала. Кроме того, улучшает реологические свойства крови, уменьшает гипоксию тканей. Выводится в основном почками. Период полувыведения около 17 ч, циркулирует в крови до 5 сут. Практически не имеет побочных эффектов.
Дезинтоксикационные растворы
Кровезаменители дезинтоксикационного действия предназначены для связывания токсинов, циркулирующих в крови, и их выведе- ния из организма с мочой. Они эффективны лишь при условии, что токсины способны образовывать комплексы с препаратом, а также при сохранении выделительной функции почек и способности комплекса кровезаменитель-токсин фильтроваться в почечных клубочках. При применении этих препаратов резко возрастает нагрузка на
почки, поэтому больным с нарушенными функциями почек, а тем более с острой почечной недостаточностью препараты этой группы не назначают.
Основные препараты - производные поливинилпирролидона (гемодез, неогемодез, перистон-Н, неокомпенсан, плазмодан, колидон) и полидез (раствор низкомолекулярного поливинилового спирта).
Гемодез - 6% раствор низкомолекулярного поливинилпирролидона с молекулярной массой 12 000-27 000. Большая его часть выводится почками через 6-8 ч после внутривенного введения. Активен в отношении многих токсинов, за исключением дифтерийного и столбнячного, а также токсинов, образующихся при лучевой болезни. Он также ликвидирует стаз эритроцитов в капиллярах при острой кро- вопотере, шоке, ожоговой болезни и других патологических процессах. В зависимости от степени интоксикации взрослым внутривенно вводят от 200 до 400 мл в сут, а детям - из расчёта 15 мл/кг массы тела. Противопоказания к назначению: бронхиальная астма, острый нефрит, кровоизлияние в головной мозг.
Неогемодез - 6% раствор низкомолекулярного поливинилпирролидона с молекулярной массой 6000-10 000 с добавлением ионов натрия, калия и кальция. Детоксикационный эффект неогемодеза выше, чем у гемодеза. Показания к применению аналогичны показаниям к назначению гемодеза. Кроме того, отчётливо проявляется лечебное действие неогемодеза при тиреотоксикозе, лучевой болезни, различных заболеваниях печени и другой патологии. Вводят препарат внутривенно со скоростью 20-40 капель в мин, максимальная разовая доза для взрослых составляет 400 мл, для детей - 5-10 мл/кг.
Полидез - 3% раствор поливинилового спирта в изотоническом растворе хлорида натрия. Молекулярная масса 10 000-12 000. Полностью выводится почками в течение 24 ч. Полидез применяют внутривенно капельно для лечения интоксикации, вызванной перитонитом, непроходимостью кишечника, острым панкреатитом, острым холециститом, острой гнойной инфекцией, ожоговой болезнью, поражением печени и т.д. Взрослым назначают 200-500 мл в сутки, детям - из расчёта 5-10 мл/кг. При быстром введении препарата возможны головокружение и тошнота.
Кровезаменители для парентерального питания
Препараты для парентерального питания показаны в случае полного или частичного исключения естественного питания больного
вследствие некоторых заболеваний и после оперативных вмешательств на органах желудочно-кишечного тракта, при гнойно-септических заболеваниях, травматических, лучевых и термических по- ражениях, тяжёлых осложнениях послеоперационного периода (перитоните, абсцессах и кишечных свищах), а также при гипопротеинемии любого происхождения. Парентеральное питание обеспечивают белковыми препаратами, жировыми эмульсиями и углеводами. Первые способствуют поступлению в организм аминокислот, а жировые эмульсии и углеводы снабжают его энергией для усвоения белка.
Наряду с белками, углеводами и жирами в парентеральном питании важную роль играют электролиты: калий, натрий, кальций, фосфор, железо, магний, хлор, а также микроэлементы марганец, кобальт, цинк, молибден, фтор, йод, никель и др. Первые принимают участие в важнейших метаболических и физиологических процессах, входят в структуру клеток, в том числе и форменных элементов крови, необходимы для регуляции осмотических процессов и т.д. Вторые регулируют функциональную активность ферментов, гормонов и т.д. Для усиления эффекта парентерального питания дополнительно назначают витамины и анаболические гормоны.
Белковые препараты
Среди белковых препаратов выделяют гидролизаты белков и смеси аминокислот.
Источниками получения белковых гидролизатов служат казеин, белки крови крупного рогатого скота, мышечные белки, а также эрит- роциты и сгустки донорской крови. При получении белковых гидролизатов исходное сырьё подвергают ферментативному или кислотному гидролизу. Наибольшее применение нашли гидролизат казеина, гидролизин, аминокровин, амикин, аминопептид, фибриносол, аминозол, аминон, амиген и др.
Белковые гидролизаты вводят внутривенно капельно со скоростью 10-30 капель в мин. Объём вводимых гидролизатов может дос- тигать 1,5-2,0 л в сут. Противопоказания к применению белковых гидролизатов: острые нарушения гемодинамики (шок, массивная кровопотеря), декомпенсация сердечной деятельности, кровоизлияние в головной мозг, почечная и печёночная недостаточность, тромбоэмболические осложнения. Белковые гидролизаты можно вводить через зонд в желудок (зондовое питание).
Отдельную группу составляют растворы аминокислот, они легко усваиваются организмом, так как нет необходимости расщеплять пептиды. Преимущества смесей кристаллических аминокислот: более простая технология получения, высокая концентрация аминокислот, возможность создания препаратов с любым соотношением аминокислот и добавлением в смесь электролитов, витаминов и энергетических соединений. Основные препараты: полиамин, инфузамин, вамин, мориамин, фреамин, альвезин, аминоплазмаль и др. Аминокислотные смеси вводят внутривенно со скоростью 20-30 капель в мин при полном парентеральном питании в дозе 800-1200 мл ежедневно. Возможно их введение через зонд в желудок.
При переливании любых белковых препаратов необходимо выполнять биологическую пробу.
Жировые эмульсии
Включение жировых эмульсий в комплекс парентерального питания улучшает энергетический обмен организма больного, ока- зывает выраженное азотсберегающее действие, корригирует липидный состав плазмы и структуру мембран клеток. Жиры обеспечивают организм незаменимыми жирными кислотами (линоленовой, линолевой, арахидоновой), жирорастворимыми витаминами (А, К, D), фосфолипидами. В клинической практике применяют жировые эмульсии (эмульгированные жиры не вызывают жировой эмболии). Наибольшее распространение получили интралипид, липифизиан, инфузолипол, липофундин, липомул, инфонутрол, фатген и др.
Препараты жировых эмульсий вводят внутривенно со скоростью 10-20 капель в мин или через зонд в желудок.
Применение жировых эмульсий противопоказано при шоке, черепно-мозговой травме, нарушении функций печени, резко выражен- ном атеросклерозе. Перед выполнением инфузии проводят биологическую пробу.
Углеводы
Углеводы используют в парентеральном питании для обеспечения энергетических потребностей, а также как энергетическую добавку к гидролизатам белков. Вводимые в организм углеводы способствуют расщеплению гидролизатов белков и построению из аминокислот собственных белков.
Наибольшее распространение получили растворы глюкозы (5%, 10%, 20% и 40%). Противопоказание к её применению - сахарный диабет.
Из других углеводов используют фруктозу и углеводные спирты (ксилит, сорбит, маннит). Усвоение этих препаратов прямо не связано с действием инсулина и возможно у пациентов с сахарным диабетом.
Регуляторы водно-солевого обмена и кислотно-щелочного состояния
К препаратам этой группы относят кристаллоидные растворы и осмотические диуретики.
Кристаллоидные растворы
Кристаллоидные растворы имеют низкую молекулярную массу и быстро проникают через стенку капилляров в межклеточное пространство, восстанавливая дефицит жидкости в интерстиции. Они довольно быстро покидают сосудистое русло. В связи с этим целесообразно сочетанное применение кристаллоидных и коллоидных растворов.
Кристаллоиды наряду с гемодинамическими коллоидными кровезаменителями включают в комплексную терапию травматического и геморрагического шока, гнойно-септических заболеваний, а также применяют для профилактики и коррекции нарушений водно-солевого баланса и кислотно-щелочного равновесия крови при больших операциях и в послеоперационном периоде. При этом не только восполняется дефицит внеклеточной жидкости, происходят компенсация метаболического ацидоза и детоксикация, но и возникает некоторый гемодинамический эффект, заключающийся в частичной коррекции гиповолемии и стабилизации АД.
Все кристаллоидные растворы можно разделить на две группы:
1. Растворы, соответствующие по электролитному составу, рН и осмолярности плазме крови, - так называемые базисные кристаллоидные растворы. Основные препараты - раствор Рингера, раствор Рингера-Локка, лактосол.
• Раствор Рингера:
- хлорид натрия -
- хлорид калия -
- хлорид кальция -
- гидрокарбонат натрия -
- дистиллированная вода - до
• Раствор Рингера-Локка:
- хлорид натрия -
- гидрокарбонат натрия -
- хлорид кальция -
- хлорид калия -
- глюкоза -
- бидистиллированная вода - до
• Лактасол:
- хлорид натрия -
- хлорид калия -
- хлорид кальция -
- хлорид магния -
- лактат натрия -
- гидрокарбонат натрия -
- дистиллированная вода - до
В клинической практике указанные растворы применяют для коррекции изотонических гидроионных нарушений, так как они содержат наиболее оптимальный набор ионов.
2. Растворы, отличающиеся по электролитному составу, рН и осмолярности от плазмы крови, - так называемые корригирующие растворы, предназначенные для коррекции нарушений гидроионного и кислотно-щелочного баланса.
К этой группе препаратов относят физиологический (изотонический) раствор хлорида натрия (0,9% раствор), ацесоль, хлосоль, дисоль, трисоль, раствор гидрокарбоната натрия, 4-5% раствор гидрокарбоната натрия (соды) (применяют для коррекции метаболического ацидоза).
Осмотические диуретики
К осмотическим диуретикам относят многоатомные спирты - маннит и сорбит.
Маннитол - 15% раствор маннита в изотоническом растворе хло- рида натрия.
Сорбитол - 20% раствор сорбита в изотоническом растворе хло- рида натрия.
Механизм диуретического действия этих препаратов связан с повышением осмолярности плазмы и притоком интерстициальной жидкости в кровеносное русло, что способствует увеличению ОЦК и возрастанию почечного кровотока.
В результате увеличения почечной фильтрации возрастает экскреция натрия, хлора и воды, при этом подавляется их реабсорбция в
канальцах почек. Препараты вводят внутривенно капельно или струйно из расчёта 1-2 г/кг массы тела в сут.
Показания для применения осмотических диуретиков: ранняя стадия острой почечной недостаточности, гемолитический шок, сердечная недостаточность, отёк мозга, парез кишечника (стимулируют перистальтику), заболевания печени и желчевыводящих путей и др. Противопоказания к их назначению: нарушение процесса фильтрации в почках, сердечная недостаточность с резко выраженной анасаркой и другими состояниями экстрацеллюлярной гипергидратации, внутричерепные гематомы.
Переносчики кислорода
Создание кровезаменителей (так называемой «искусственной крови»), выполняющих перенос кислорода к тканям организма (основную функцию крови), - важная, но очень трудная задача.
В настоящее время интенсивно разрабатывают два направления в создании кровезаменителей с функцией переноса кислорода.
Растворы модифицированного гемоглобина
К этой группе относят геленпол (пиридоксиминированный полимеризованный гемоглобин крови человека). В состав геленпола входит лиофильно высушенное полимерное производное гемоглобина со стабилизаторами в виде глюкозы и аскорбиновой кислоты. Клинические наблюдения и данные экспериментальных исследований предполагают, что геленпол моделирует дыхательную функцию эритроцитов и функции плазменных белков, повышает содержание гемоглобина в циркулирующей крови и его синтез, усиливает транспорт оксида азота (NO) и S-нитрозотиолов (SNO). Геленпол применяют при гиповолемии, анемии и гипоксических состояниях.
Эмульсии перфторуглеродов
Основные препараты этой группы - перфторан, перфукол, флюсол-Да. Перфторуглероды пассивно переносят кислород и углекислый газ пропорционально перепаду парциального давления соответ- ствующего газа.
Перфторуглероды - химически инертные вещества, не подвергающиеся метаболическим превращениям в организме человека.
Препараты применяют в качестве противошокового и противоишемического средства; они обладают реологическими, гемодинамическими, диуретическими, мембраностабилизирующими, кардиопротективными и сорбционными свойствами, уменьшают агрегацию эритроцитов. Их назначают при острой и хронической гиповолемии (травматический, геморрагический, ожоговый и инфекционно-токсический шок), нарушении микроциркуляции, изменениях тканевого обмена и метаболизма, при операциях на остановленном сердце как основной дилютант для заполнения аппарата искусственного кровообращения, для противоишемической защиты донорских органов.
Следует отметить, что до сих пор не удаётся решить проблему качественной стерилизации кровезаменителей-переносчиков кислорода и удешевления их производства. В связи с этим в клинической практике их применяют довольно редко.
Инфузионные антигипоксанты
Инфузионные антигипоксанты - самая молодая группа кровезаменителей. Они предназначены для повышения энергетического потенциала клетки. Основные препараты - мафусол, полиоксифумарин (содержат антигипоксант фумарат натрия) и реамберин (содержит сукцинат). За счёт вводимого фумарата или сукцината препараты этой группы восстанавливают клеточный метаболизм, адаптируя клетки к недостатку кислорода; за счёт участия в реакциях обратимого окисления и восстановления в цикле Кребса способ- ствуют утилизации жирных кислот и глюкозы клетками; нормализуют кислотно-основной баланс и газовый состав крови. Препараты показаны при гиповолемических состояниях, практически не имеют побочных эффектов.
Осложнения переливания крови
Предложено много классификаций постгемотрансфузионных осложнений. Наиболее полно они представлены в классификации А.Н. Филатова (1973). Несмотря на то, что она существует уже почти три десятилетия, основные её положения приемлемы и сегодня.
А.Н. Филатов выделил три группы осложнений: механического, реактивного и инфекционного характера.
Осложнения механического характера
К осложнениям механического характера, связанным с погрешностями в технике переливания крови, относят следующие:
• острое расширение сердца;
• воздушная эмболия;
• тромбозы и эмболии;
• нарушение кровообращения в конечности после внутриартериальных трансфузий.
Острое расширение сердца
Под термином «острое расширение сердца» понимают острые циркуляторные нарушения, острую сердечно-сосудистую недостаточность.
Причина этого осложнения - перегрузка сердца большим количеством быстро введённой в венозное русло крови. В системе полых вен и правого предсердия возникает застой крови, нарушается общий и коронарный кровоток. Нарушение кровотока сказывается на обменных процессах, что приводит к снижению проводимости и сократимости миокарда вплоть до атонии и асистолии. Особенно опасно быстрое переливание больших объёмов крови больным пожилого и старческого возрастов, а также лицам с выраженной сопутствующей патологией сердечно-сосудистой системы.
Клиническая картина. Во время переливания крови или к его концу больной ощущает затруднение дыхания, стеснение в груди, боли в области сердца. Появляется цианоз губ и кожи лица, резко снижается АД и повышается ЦВД, возникают тахикардия и аритмия, а затем на первый план выступает слабость сердечной деятельности, при отсутствии экстренной помощи ведущая к гибели больного.
Лечение состоит в немедленном прекращении гемотрансфузии, небольшом кровопускании для разгрузки правых отделов сердца, внутривенном введении кардиотонических средств (1 мл 0,05% раствора строфантина-К или 1 мл 0,06% раствора гликозида ландыша) и вазопрессоров, придании больному возвышенного положения, со- гревании ног, введении диуретических средств (40 мг фуросемида), дыхании увлажнённым кислородом. По показаниям проводят закрытый массаж сердца и ИВЛ.
Профилактика острого расширения сердца состоит в уменьшении скорости и объёма инфузионной терапии, контроле ЦВД и диуреза.
Воздушная эмболия
Воздушная эмболия - редкое, но очень тяжёлое осложнение. Она возникает при введении вместе с трансфузионной средой некоторо- го количества воздуха. Воздух поступает в правые отделы сердца, а из него - в лёгочную артерию, закупоривая её основной ствол или мелкие ветви и создавая механическое препятствие для кровотока.
Причиной этого осложнения чаще всего бывает неправильное за- полнение системы кровью или её негерметичность. При переливании в подключичную вену возможно поступление воздуха после окончания трансфузии из-за отрицательного давления в вене на вдохе.
Клиническая картина характеризуется внезапным ухудшением состояния больного, возбуждением, затруднением дыхания. Развивается цианоз губ, лица, шеи, снижается АД, пульс становится частым, нитевидным. Массивная воздушная эмболия приводит к развитию клинической смерти.
Лечение предусматривает введение сердечных средств, следует опустить головной и поднять ножной конец кровати. Оправдана попытка пункции лёгочной артерии и отсасывание из неё воздуха. При развитии клинической смерти - реанимационные мероприятия в полном объёме.
Профилактика заключается в тщательном сборе системы для ге- мотрансфузии и постоянном наблюдении за больным во время её проведения.
Тромбозы и эмболии
Причина развития тромбозов и эмболий при гемотрансфузиях заключается в попадании в вену больного сгустков различной величины, образовавшихся из-за неправильной стабилизации донорской крови, нарушений в методике гемотрансфузии, переливания больших доз консервированной крови длительных сроков хранения (после 7 сут хранения, например, число агрегатов превышает 150 тыс в 1 мл).
Клиническая картина. При попадании большого числа сгустков крови развивается клиническая картина тромбоэмболии ветвей лё- гочной артерии: внезапные боли в груди, резкое усиление или возникновение одышки, появление кашля, иногда кровохарканье, бледность и цианоз кожных покровов.
Лечение заключается в проведении тромболитической терапии активаторами фибринолиза (стрептокиназой), непрерывном введении гепарина натрия (до 24000-40000 ЕД в сут), немедленном струйном
введении не менее 600 мл свежезамороженной плазмы под контролем коагулограммы, внутривенное введение декстрана [мол.масса 30 000-40 000], пентоксифиллина и дипиридамола для улучшения ре- ологических свойств крови.
Профилактика включает применение пластиковых систем со спе- циальными фильтрами, соблюдение правил заготовки, хранения и переливания крови.
Нарушение кровообращения в конечности после внутриартериальных трансфузий
Осложнение развивается редко, так как внутриартериальное нагнетание крови в настоящее время практически не проводят.
При травмировании стенки сосуда может произойти тромбоз с последующей тромбоэмболией или эмболия периферических арте- рий сгустками крови. Развивается клиническая картина острого нарушения артериального кровообращения, в этом случае необходимо соответствующее лечение.
Осложнения реактивного характера
Осложнения реактивного характера - наиболее серьёзные, опасные и часто встречающиеся осложнения гемотрансфузии. Их разви- тие обусловлено несовместимостью переливаемой донорской крови или реакцией организма на трансфузионную среду.
Среди осложнений реактивного характера выделяют реакции и собственно гемотрансфузионные осложнения. Реакции не сопровождаются серьёзными и длительными нарушениями функций органов и систем. Осложнения характеризуются тяжёлыми клиническими проявлениями, представляющими опасность для жизни больного.
Гемотрансфузионные реакции
По тяжести клинического течения различают реакции трёх степеней: лёгкие, средние и тяжёлые.
Лёгкие реакции сопровождаются повышением температуры тела в пре- делах 1 ?С, болями в мышцах, конечностях, головной болью, ознобом и недомоганием. Эти явления кратковременны и не требуют лечения.
Реакции средней тяжести проявляются подъёмом температуры тела на 1,5-2,0 градуса, нарастающим ознобом, учащением пульса и дыхания, иногда кожной сыпью.
При тяжёлых реакциях температура тела повышается более чем на 2 градуса, отмечают потрясающий озноб, цианоз губ, рвоту, сильную головную боль, боли в мышцах и костях, одышку, крапивницу или отёк Квинке.
В зависимости от причины возникновения и клинического течения различают следующие виды реакций:
• пирогенные;
• антигенные (негемолитические);
• аллергические.
Пирогенные реакции
Причины развития пирогенных реакций не связаны с иммунобиологической несовместимостью и бывают следствием образования в трансфузионной среде пирогенных веществ - продуктов распада белков донорской крови или жизнедеятельности микроорганизмов, проникающих в кровь при её заготовке, хранении или нарушении правил асептики в момент переливания.
Клиническая картина заключается в повышении температуры тела, чувстве жара или озноба. Возможны головная боль, тахикардия и другие вторичные проявления.
Лечение. При реакции лёгкой степени особых мероприятий не тре- буется. При развитии тяжёлой реакции или реакции средней тяжести необходимо прекратить гемотрансфузию, ввести жаропонижающие средства (метамизол натрий), наркотические анальгетики (тримеперидин), антигистаминные препараты (дифенгидрамин, клемастин).
Профилактика заключается в соблюдении правил заготовки, хранения и переливания крови. С применением одноразовых пластиковых контейнеров для заготовки крови и её компонентов и одноразовых систем для трансфузий частота таких реакций значительно снижается.
Антигенные (негемолитические) реакции
Причины возникновения этих реакций не связаны с бактериальными пирогенами, а обусловлены сенсибилизацией антигенами лейкоцитов, тромбоцитов и белков плазмы в результате ранее проведён- ных гемотрансфузий и беременностей. В 50% случаев развитие реакций связано с антилейкоцитарными антителами.
Клиническая картина реакции проявляется через 20-30 мин после окончания гемотрансфузии: озноб, повышение температуры тела,
развитие брадикардии, головная боль и боль в пояснице. Эти симптомы - следствие высвобождения пирогенных, вазоактивных и комплементактивирующих веществ при массовой гибели лейкоцитов.
Лечение. Возникновение посттрансфузионных реакций негемоли- тического типа требует энергичной терапии с применением антигистаминных средств, сердечно-сосудистых препаратов, наркотических анальгетиков, детоксикационных и противошоковых растворов.
Профилактика состоит в тщательном сборе анамнеза и применении индивидуального подбора донорской крови по показаниям. Для профилактики развития посттрансфузионных реакций в серологической лаборатории проводят лимфоцитотоксическую пробу и реакцию лейкоагглютинации сыворотки больного и лейкоцитов донора. Лицам, имеющим в анамнезе многократные гемотрансфузии или беременности, для лечения анемии рекомендуют вливания эритроцитарной массы, обеднённой лейкоцитами и тромбоцитами, лишённой лейкоцитарных, тромбоцитарных и других плазменных и клеточных иммуноагрессивных факторов.
Аллергические реакции
Причины. Аллергические реакции обусловлены сенсибилизацией организма к различным иммуноглобулинам. Образование антител к иммуноглобулинам происходит после переливания крови, плазмы и криопреципитата. Иногда эти антитела существуют в крови у лиц, не переносивших гемотрансфузии и не имевших беременностей.
Клиническая картина. Тяжесть аллергических реакций может быть различной - от лёгкой степени до развития анафилактического шока. При аллергических реакциях возможно развитие крапивницы, отёка Квинке, бронхоспазма. В патогенезе анафилактического шока главенствующую роль играет реакция «антиген-антитело», при которой выделяются биологически активные вещества, повреждающие сосу- дистую стенку с образованием отёка и резким падением АД; также происходит спазм гладких мышц бронхов. Больные становятся беспокойными, жалуются на затруднение дыхания. При объективном исследовании: гиперемия кожных покровов, цианоз слизистых оболочек, акроцианоз, холодный пот, свистящее дыхание, глухость тонов сердца, отёк лёгких.
Лечение. При развитии аллергических реакций гемотрансфузию прекращают. Для устранения аллергических реакций применяют де- сенсибилизирующие средства, по показаниям - глюкокортикоиды, сердечно-сосудистые и наркотические препараты.
Больным в состоянии анафилактического шока требуется безотлагательное проведение противошоковой терапии. В комплекс лечебных мероприятий необходимо включить струйное или капельное введение объёмозамещающих растворов, глюкокортикоидов, антигистаминных средств, бронхолитических, сердечных и седативных препаратов.
Профилактика аллергических реакций заключается в тщательном сборе анамнеза с целью выявления предшествующей сенсибилизации, применении отмытых эритроцитов, индивидуальном подборе донорской крови, предварительном введении больным с предрасположенностью к аллергическим реакциям антигистаминных препаратов.
Гемотрансфузионные осложнения
Гемотрансфузионные осложнения наиболее опасны для жизни больного. Самой частой причиной гемотрансфузионных осложнений бы- вает переливание крови, не совместимой по системе АВ0 и Rh-факто- ру (приблизительно 60%). Реже встречают несовместимость по другим антигенным системам и переливание недоброкачественной крови.
Основное и наиболее тяжёлое осложнение в этой группе, да и среди всех гемотрансфузионных осложнений, - гемотрансфузионный шок.
Осложнения при переливании крови, не совместимой по системе АВ0
Гемотрансфузионный шок
При переливании крови, не совместимой по системе АВ0, развивается осложнение, получившее название «гемотрансфузионный шок».
Причиной развития осложнения в большинстве случаев становится нарушение правил, предусмотренных инструкциями по технике переливания крови, методики определения группы крови по системе АВ0 и проведения проб на совместимость. При переливании крови или эритроцитарной массы, не совместимой по групповым факторам системы АВ0, происходит массивный внутрисосудистый гемолиз вследствие разрушения эритроцитов донора под воздействием агглютининов реципиента.
В патогенезе гемотрансфузионного шока основными повреждающими факторами становятся свободный гемоглобин, биогенные амины, тромбопластин и другие продукты гемолиза. Под влиянием высоких концентраций этих биологически активных веществ возникает выраженный спазм периферических сосудов, быстро сменяющийся их па-
ретическим расширением, что приводит к нарушению микроциркуляции и кислородному голоданию тканей. Повышение проницаемости сосудистой стенки и вязкости крови ухудшает реологические свойства крови, что ещё больше нарушает микроциркуляцию. Следствием дли- тельной гипоксии и накопления кислых метаболитов становятся функциональные и морфологические изменения различных органов и систем, то есть разворачивается полная клиническая картина шока.
Отличительная черта гемотрансфузионного шока - возникновение ДВС-синдрома с существенными изменениями в системе ге- мостаза и микроциркуляции, грубыми нарушениями показателей центральной гемодинамики. Именно ДВС-синдрому принадлежит ведущая роль в патогенезе поражения лёгких, печени, эндокринных желёз и других внутренних органов. Пусковым моментом в развитии шока становится массивное поступление в кровоток тромбопластина из разрушенных эритроцитов.
Характерные изменения происходят в почках: в почечных канальцах накапливаются солянокислый гематин (метаболит свободного гемоглобина) и остатки разрушенных эритроцитов, что наряду со спазмом почечных сосудов приводит к снижению почечного кровотока и клубочковой фильтрации. Описанные изменения - причина развития острой почечной недостаточности.
Клиническая картина. В течении осложнения при переливании крови, не совместимой по системе АВ0, выделяют три периода:
• гемотрансфузионный шок;
• острая почечная недостаточность;
• реконвалесценция.
Гемотрансфузионный шок наступает непосредственно во время трансфузии или после неё, длится от нескольких мин до нескольких часов.
Клинические проявления сначала характеризуются общим беспокойством, кратковременным возбуждением, ознобом, болями в груди, животе, пояснице, затруднением дыхания, одышкой, цианозом. Боль в поясничной области считают самым характерным признаком этого осложнения. В дальнейшем постепенно нарастают циркуляторные нарушения, характерные для шокового состояния (тахикардия, снижение АД, иногда нарушение ритма сердечной деятельности с явлениями острой сердечно-сосудистой недостаточности). Доволь- но часто отмечают изменение цвета лица (покраснение, сменяющееся бледностью), тошноту, рвоту, повышение температуры тела, мраморность кожных покровов, судороги, непроизвольное мочеиспускание и дефекацию.
Наряду с симптомами шока одним из ранних и постоянных признаков гемотрансфузионного шока становится острый внутрисосу- дистый гемолиз. Основные показатели повышенного распада эритроцитов: гемоглобинемия, гемоглобинурия, гипербилирубинемия, желтуха, увеличение печени. Характерно появление мочи бурого цвета (в общем анализе - выщелоченные эритроциты, белок).
Развивается нарушение гемокоагуляции, клинически проявляющееся повышенной кровоточивостью. Геморрагический диатез воз- никает в результате ДВС-синдрома, выраженность которого зависит от степени и продолжительности гемолитического процесса.
При переливании несовместимой крови во время оперативного вмешательства под наркозом, а также на фоне гормональной либо лучевой терапии реактивные проявления могут быть стёртыми, симптомы шока чаще всего отсутствуют или выражены незначительно.
Тяжесть клинического течения шока в значительной степени обусловлена объёмом перелитых несовместимых эритроцитов, характером основного заболевания и общим состоянием больного перед ге- мотрансфузией.
В зависимости от величины АД различают три степени гемотрансфузионного шока:
• I степень - систолическое АД выше
• II степень - систолическое АД 71-90 мм рт.ст;
• III степень - систолическое АД ниже
Тяжесть клинического течения шока и его продолжительность определяют исход патологического процесса. В большинстве случаев лечебные мероприятия позволяют ликвидировать циркуляторные расстройства и вывести больного из шока. Однако через некоторое время после трансфузии может повыситься температура тела, появляется постепенно нарастающая желтушность склер и кожи, усиливается головная боль. В дальнейшем на первый план выступают нарушения функций почек: развивается острая почечная недостаточность.
Острая почечная недостаточность
Острая почечная недостаточность протекает в виде трёх сменяющих друг друга фаз: анурия (олигурия), полиурия и восстановление функций почек.
На фоне стабильных гемодинамических показателей резко снижается суточный диурез, отмечают гипергидратацию организма, нарастает содержание креатинина, мочевины и калия плазмы. В после- дующем диурез восстанавливается и увеличивается (иногда до 5-6 л
в сут), при этом может сохраняться высокая креатининемия, а также гиперкалиемия (полиурическая фаза почечной недостаточности).
При благоприятном течении осложнения, своевременном и правильном лечении функции почек постепенно восстанавливаются, состояние больного улучшается.
Период реконвалесценции
Период реконвалесценции характеризуется восстановлением функций всех внутренних органов, системы гомеостаза и водно-электролитного баланса.
Лечение
Принципы лечения гемотрансфузионного шока. При появлении первых признаков гемотрансфузионного шока переливание крови прекращают, систему для переливания отсоединяют и подключают систему с солевым раствором. Ни в коем случае нельзя удалять иглу из вены, чтобы не потерять готового венозного доступа.
Гемотрансфузионный шок требует немедленного оказания экстренной медицинской помощи, проведения интенсивной терапии. Основное лечение направлено на выведение больного из состояния шока, восстановление и поддержание функций жизненно важных органов, купирование геморрагического синдрома, предупреждение развития острой почечной недостаточности.
Решающее значение имеет фактор времени - чем раньше оказана помощь больному, тем благоприятнее исход.
Инфузионная терапия. Для поддержания ОЦК и стабилизации гемодинамики и микроциркуляции проводят переливание кровезамещающих растворов (препарат выбора - декстран [мол.масса 30 000- 40 000], возможно применение декстрана [ср. мол.масса 50 000-70 000] и препаратов желатина). Необходимо также максимально рано начать введение раствора соды (4% раствора гидрокарбоната натрия) или лактасола для получения щелочной реакции мочи, что препятствует образованию солянокислого гематина. В последующем переливают кристаллоидные растворы для удаления свободного гемоглобина и в целях предупреждения деградации фибриногена.
Объём инфузионной терапии должен соответствовать диурезу и контролироваться величиной ЦВД.
Медикаментозные средства первой очереди. Важные препараты при лечении гемотрансфузионного шока включают преднизолон (90- 120 мг), аминофиллин (10 мл 2,4% раствора) и фуросемид (100 мг) - классическая противошоковая триада. Кроме этого, используют ан- тигистаминные средства и наркотические анальгетики.
Экстракорпоральные методы. Высокоэффективный способ - массивный плазмаферез (эксфузия около
Коррекция функций органов и систем. По показаниям применяют сердечные гликозиды, кардиотонические средства и др. При выраженной анемии (Нb ниже 60 г/л) переливают отмытые эритроциты одноимённой по отношению к реципиенту группы крови. При развитии гиповентиляции возможен перевод на ИВЛ.
Коррекция системы гемостаза. Применяют гепарин натрий (50- 70 ЕД/кг массы тела), переливают свежезамороженную плазму, используют антиферментные препараты (апротинин).
Принципы лечения острой почечной недостаточности. При выводе из шока и наступлении фазы острой почечной недостаточности лечение должно быть направлено на улучшение функций почек (аминофиллин, фуросемид и осмотические диуретики) и коррекцию водно-электролитного баланса. В тех случаях, когда терапия не предотвращает развития уремии, прогрессирования креатининемии и гиперкалиемии, необходим гемодиализ. В связи с этим лечение больных с острой почечной недостаточностью целесообразно проводить в условиях специализированного отделения, оснащённого аппаратом «искусственная почка».
В периоде реконвалесценции проводят симптоматическую терапию.
Профилактика заключается в строгом соблюдении правил выполнения гемотрансфузии (особенно реакций на совместимость переливаемой крови).
Осложнения при переливании крови, не совместимой
по резус-фактору и другим системам антигенов эритроцитов
Осложнения, обусловленные несовместимостью перелитой крови по резус-фактору, возникают у больных, сенсибилизированных в отношении резус-фактора. Это может произойти при введении резус- положительной крови резус-отрицательным реципиентам, сенсибилизированным предшествующей гемотрансфузией Rh-положительной кровью (или у женщин - беременностью Rh-положительным плодом).
Причиной осложнений в большинстве случаев становится недоста- точно полное изучение акушерского и трансфузионного анамнеза, а также невыполнение или нарушение других правил, предупреждающих несовместимость по Rh-фактору (прежде всего пробы на индивидуальную совместимость по Rh-фактору).
Кроме резус-фактора D(Rh0), причиной осложнений при переливании крови могут быть другие антигены системы резус: С (rh'), E (rh»), с (hr'), е (hr»), а также антигены систем Даффи, Келл, Кидд и др. Степень их иммуногенности и значение для практики переливания крови значительно ниже.
Развивающийся иммунологический конфликт приводит к массивному внутрисосудистому гемолизу перелитых донорских эритроцитов иммунными антителами (анти-D, анти-С, анти-Е и др.), образо- вавшимися в процессе предшествующей сенсибилизации реципиента. Далее запускается механизм развития гемотрансфузионного шока подобно несовместимости по системе АВ0.
Следует отметить, что сходные изменения в организме (кроме иммунного конфликта) наблюдают при переливании большого ко- личества гемолизированной крови.
Клиническая картина. Клинические проявления отличаются от осложнения при несовместимости по системе АВ0 более поздним началом, менее бурным течением, замедленным и отсроченным гемолизом, что определяется видом иммунных антител и их титром. При переливании не совместимой по Rh-фактору крови симптомы появляются через 30-40 мин, иногда и 1-2 ч (до 12 ч) после гемотрансфузии. При этом фаза собственно шока выражена в меньшей степени, часто картина бывает стёртой. В дальнейшем также наступает фаза острой почечной недостаточности, но обычно отмечают более благоприятное её течение.
Лечение проводят по тем же принципам, что и при несовместимости по системе АВ0.
Профилактика заключается в тщательном сборе трансфузиологического анамнеза и соблюдении правил гемотрансфузии.
Синдром массивных гемотрансфузий
Причины. Осложнение возникает при введении на фоне острой кровопотери быстро в кровеносное русло реципиента крови объёмом более 40- 50% ОЦК. Его развитие объясняется иммунобиологическими процессами, связанными с реакцией отторжения чужеродной донорской ткани (скорее всего, основная роль принадлежит иммунологически агрессивным плазменным белкам, в частности, иммуноглобулинам), а также несбалансированностью системы спонтанного гемостаза (переливание крови разных сроков хранения) и токсическим влиянием консервантов.
Клиническая картина. При возникновении синдрома массивных гемотрансфузий в организме развивается комплекс тяжёлых изменений: усиление гемолиза, нарушение сократительной способности ми-
окарда, функциональные изменения в системе гемостаза, нарушение микроциркуляции, нарушение белкового и гидроионного состава крови, патологическое перераспределение крови. В органах образуются мелкие кровоизлияния, появляются микротромбы, состоящие из агрегатов эритроцитов и тромбоцитов.
Наиболее частое клиническое проявление синдрома массивных гемотрансфузий - ДВС-синдром. Клинически вместо ожидаемого улучшения состояния больного вследствие компенсации кровопотери происходит его ухудшение.
Лечение ДВС-синдрома,
обусловленного массивной гемотрансфузией, включает мероприятия,
направленные на нормализацию системы гемостаза, устранение капиллярного
стаза, нарушений кислотно-основного, электролитного и водного баланса,
коррекцию поражений лёгких, почек, надпочечников и анемии. Рекомендуют
применение гепарина натрия (до 24 000 ЕД в сутки при непрерывном
введении), плазмафереза (удаление не менее
Профилактика синдрома массивных гемотрансфузий состоит в отказе от переливания цельной крови от многих доноров одному больному. Массивные кровопотери целесообразно компенсировать заранее заготовленными от одного-двух доноров криоконсервированными эритроцитами и свежезамороженной плазмой по принципу «один донор - один больной», кристаллоидными и коллоидными кровезаменителями, создавая управляемую гемодилюцию, а также широким применением при оперативных вмешательствах аутогемотрансфузии и реинфузии крови.
Цитратная интоксикация
Причина. Интоксикация развивается при переливании больших доз крови, заготовленной с использованием в качестве стабилизатора цитрата натрия, особенно при большой скорости переливания. Цитрат натрия связывает в крови свободный кальций, вызывая гипокальциемию. Концентрация ионизированного кальция возвращается к норме сразу после прекращения переливания, что объясняется быстрой мобилизацией кальция из эндогенных депо и метаболизмом цитрата в печени.
Токсическая доза цитрата составляет 0,2-0,3 г на
Клиническая картина. При снижении содержания свободного кальция в крови появляются неприятные ощущения за грудиной, судорожные подёргивания мышц голени, лица, нарушения ритма дыхания с переходом в апноэ при высокой степени гипокальциемии. Возможны снижение АД, нарастание сердечной недостаточности, на электрокардиограмме (ЭКГ) регистрируют удлинение интервала Q-T, нарушение ритма сердца: брадикардия вплоть до асистолии. Развитие всей полноты указанных изменений получило название «цитратный шок».
Лечение. При появлении клинических признаков гипокальциемии необходимо прекратить введение цельной консервированной крови, внутривенно ввести 10-20 мл 10% раствора глюконата кальция или 10 мл 10% раствора хлорида кальция.
Профилактика заключается
в выявлении больных с исходной ги- покальциемией, медленном введении
крови, профилактическом введении 10% раствора хлорида (глюконата)
кальция - 10 мл на каждые
Калиевая интоксикация
Причины. Гиперкалиемия может возникнуть при переливании дли- тельно хранившейся консервированной крови или эритроцитарной массы (происходит разрушение форменных элементов с выходом калия в плазму).
Для клинической картины характерны брадикардия, аритмия, атония миокарда вплоть до асистолии. При биохимическом анализе крови подтверждают гиперкалиемию.
Лечение. Для устранения гиперкалиемии применяют внутривенное введение 10% раствора хлорида кальция и 0,9% раствора хлорида натрия, 40% раствора глюкозы с инсулином, кардиотонических средств.
Профилактика состоит в применении для клинических целей све- жезаготовленной консервированной крови или эритроцитарной массы (особенно у пациентов с хронической недостаточностью почек, обычно сопровождающейся гиперкалиемией).
Осложнения инфекционного характера
Среди осложнений инфекционного характера можно выделить три группы:
• передача острых инфекционных заболеваний;
• передача заболеваний, распространяющихся сывороточным путём;
• развитие банальной хирургической инфекции.
Передача острых инфекционных заболеваний
Возбудители инфекционных заболеваний попадают в кровь и её компоненты от доноров, находящихся в инкубационном периоде или болеющих стёртыми формами инфекционных заболеваний. Трансфузионным путём могут быть переданы многие инфекции (грипп, корь, сыпной и возвратный тиф, бруцеллёз, токсоплазмоз, инфекционный мононуклеоз, натуральная оспа).
Передача заболеваний, распространяющихся сывороточным путём
В настоящее время у трансфузиологов вызывает большую тревогу возможность заражения сифилисом, гепатитом В и С, ВИЧ-инфек- цией, цитомегаловирусной инфекцией, Т-клеточным лейкозом, а также малярией и другими инфекционными заболеваниями. Проблема передачи инфекции при переливании крови привлекает пристальное внимание врачей во всём мире.
Заражение посттрансфузионными инфекциями ведёт к инвалидизации и гибели больных. С появлением ВИЧ-инфекции эта пробле- ма приобрела особую остроту.
Для профилактики осложнений инфекционного характера необходимы тщательный отбор доноров, строгое соблюдение инструкции по их медицинскому обследованию, проведение иммунодиагностических тестов, а также тесный контакт институтов и станций переливания крови с санитарно-эпидемиологическими станциями и кожно-венерологическими диспансерами, проведение санитарно-просветительной работы с донорами.
Развитие банальной хирургической инфекции
Осложнения этой группы возникают при несоблюдении норм асептики во время переливания. Встречаются редко. Возможно развитие тромбофлебита, а иногда и флегмоны в области венепункции. При попадании микроорганизмов в сосудистое русло может развиться ангиогенный сепсис.
В какой-то степени к этой группе осложнений можно отнести переливание инфицированной крови. При этом развивается клиническая картина бактериально-токсического шока. Однако такое осложнение в настоящее время можно считать казуистическим.