Лучевая диагностика и терапия: учебное пособие / С.К. Терновой, В.Е. Синицын. - 2010. - 304 с: ил.
|
|
|
|
ГЛАВА 8 СЕРДЕЧНО-СОСУДИСТАЯ СИСТЕМА
Для изучения сердца и крупных сосудов широко применяются все известные диагностические методы: ЭхоКГ, радионуклидные методы, КТ, МРТ и ангио- и коронароангиография.
Методы лучевой диагностики могут быть использованы для исследования положения, формы, величины и функции камер сер- дца, перфузии и жизнеспособности миокарда, строения коронарных артерий и крупных магистральных сосудов, а также особенностей кровотока в них.
8.1. НОРМАЛЬНАЯ АНАТОМИЯ
На рентгенограмме грудной клетки большая часть срединной тени является суммарным изображением собственно сердца и крупных кровеносных сосудов. Сердце представлено в виде косо расположенного неправильного эллипса, большая часть которого находится в стороне левого легочного поля (рис. 8-1).
Срединная тень на рентгенограммах однородна, поэтому определение анатомических элементов проводится по краевым выступам («дугам»). Во фронтальной проекции по правому контуру срединной тени различают две тени - верхнюю, образованную верхней полой веной, и нижнюю, сформированную краем правого предсердия. Слева различают четыре дуги (сверху вниз), образованные последовательно аортой, легочной артерией, ушком левого предсердия и левым желудочком.
На рентгенограмме в боковой проекции можно рассмотреть все части аорты (восходящую часть, дугу и нисходящую часть) и контуры камер сердца. Боковую рентгенографию выполняют после контрастирования глотком бариевой взвеси.
Новые технологии (УЗИ, МСКТ, МРТ) существенно расширили возможности исследования сердца и сосудов.
В настоящее время эхокардиография (ЭхоКГ) в различных плоскостях стала основным методом исследования сердца. Она поз-
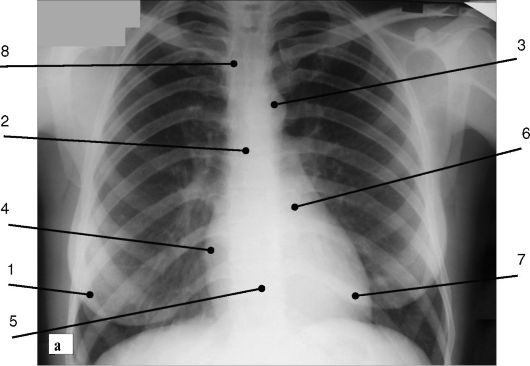
Рис. 8-1. Рентгенограмма сердца в прямой (а) и косой (б) проекциях: 1 - тень молочной железы; 2 - восходящая аорта; 3 - дуга аорты; 4 - правое предсердие; 5 - правый желудочек; 6 - левое предсердие; 7 - левый желу- дочек; 8 - верхняя полая вена
воляет получить изображение всех его структур (за исключением коронарных артерий). Естественными ограничениями метода явля- ются плохое «ультразвуковое окно» у тучных пациентов и узкий сектор обзора. Эхокардиограммы сердца можно выполнять в разных сечениях (например, двухили четырехкамерном). ЭхоКГ дает возможность изучать работу сердца в реальном масштабе времени (рис. 8-2).
Использование допплерографии помогает измерить скорость и характер движения крови в полостях сердца и сосудах.
При наличии плохого «ультразвукового окна» у пациента приходится прибегать к чреспищеводной ЭхоКГ. Методика не сложна для выполнения и дает хорошие результаты. Для ее применения нужен специальный датчик, который вводится в пищевод и опускается до уровня сердца.
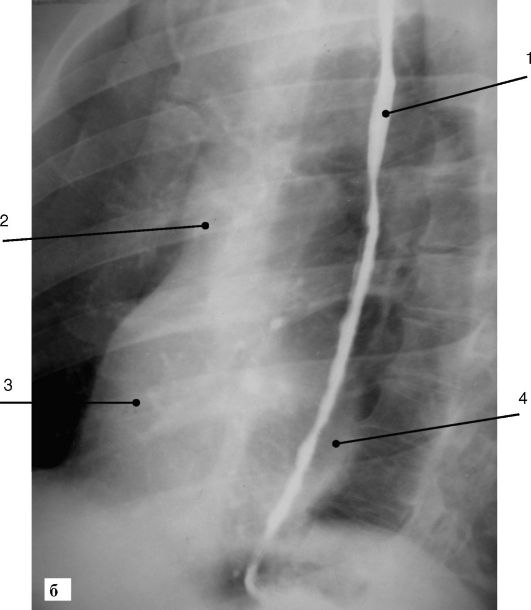
Рис. 8-1. Рентгенограмма сердца в прямой (а) и косой (б) проекциях (окончание):
1 - контрастированный пищевод; 2 - восходящая аорта; 3 - правый желудочек; 4 - левое предсердие
В крупных кардиохирургических клиниках в сложных случаях применяется методика внутрисосудистого исследования коронарных сосудов. Это исследование выполняется во время коронарографии и позволяет визуализировать мельчайшие детали стенки сосуда. Особенно важна эта методика для своевременного выявления осложнений внутрисосудистых манипуляций.
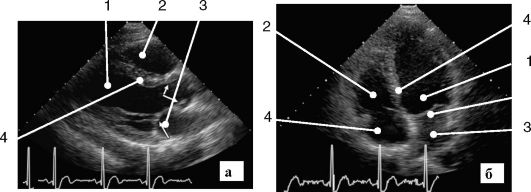
Рис. 8-2. Эхокардиограмма:
а - двухкамерное сечение; б - парастернальное сечение по длинной оси левого желудочка;
1 - левый желудочек; 2 - правый желудочек; 3 - левое предсердие; 4 - межжелудочковая перегородка; 5 - митральный клапан
С помощью ЭхоКГ можно выявлять дефекты межпредсердной и межжелудочковой перегородок и поражения клапанов сердца, гипертрофию миокарда, постинфарктные рубцы и тромбы, опухоли сердца и многие другие заболевания.
Методика селективной ангиографии коронарных сосудов (коронароангиография - КАГ) остается «золотым стандартом» диагностики патологии коронарных сосудов.
Для проведения КАГ катетер подводят в корень аорты и затем селективно вводят контрастное вещество в коронарные артерии (рис. 8-3). Исследование может быть расширено контрастированием левого желудочка для оценки его морфологии и сократимости миокарда (вентрикулография). Во время выполнения ангиографии возможно проводить баллонную дилатацию стенозов, открывать окклюзии и устанавливать внутрисосудистые стенты.
Для исследования крупных сосудов всегда применяется введение контрастного вещества внутрь изучаемого сосуда. При ангиографии это достигается пункцией бедренной (или лучевой, плечевой) арте- рии и введением в просвет сосуда специального тонкого длинного катетера. Катетер продвигается к интересующему врача сосуду, и в него быстро вводится небольшое (40-70 мл) количество контрастного вещества.
В момент введения контраста проводится быстрая серийная съемка. На серии ангиограмм отображается интересующий сосуд
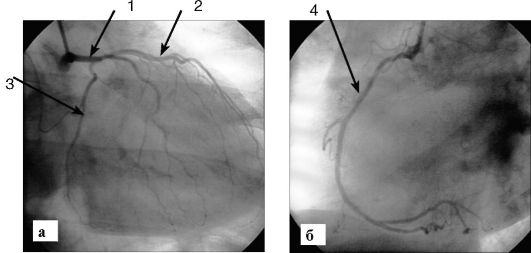
Рис. 8-3. Коронарограмма:
а - 1 - ствол левой коронарной артерии; 2 - передняя нисходящая артерия; 3 - огибающая артерия; б - 4 - правая коронарная артерия; 5 - катетер
или сосудистый бассейн, который исследуется. В норме артериальные сосуды имеют четкие, ровные контуры, их просвет постепенно сужается к периферии. В последние годы ангиографию применяют реже в связи с развитием КТ-ангиографии.
Применение МСКТ в кардиологии позволяет более быстро и точно проводить диагностику заболеваний сердечно-сосудистой системы. В некоторых случаях можно выявлять заболевания коронарных сосудов на доклинической фазе. Это позволяет проводить скрининг ишемической болезни сердца как основной причины смертности в группах высокого риска.
Исследование сердца при МСКТ проводится с болюсным введением 80-120 мл контрастного вещества в локтевую вену с кардио- синхронизацией.
На компьютерных томограммах видны все отделы сердца (предсердия, желудочки, миокард, клапаны, хорды, папиллярные мышцы, коронарные артерии и пр.) (рис. 8-4).
Изучая левый желудочек в систолу и диастолу, можно измерить фракцию выброса желудочков и изучить их сократительную спо- собность.
С помощью МРТ сердца можно получить очень важные, порой недостижимые при использовании других методов, данные (рис. 8-5).
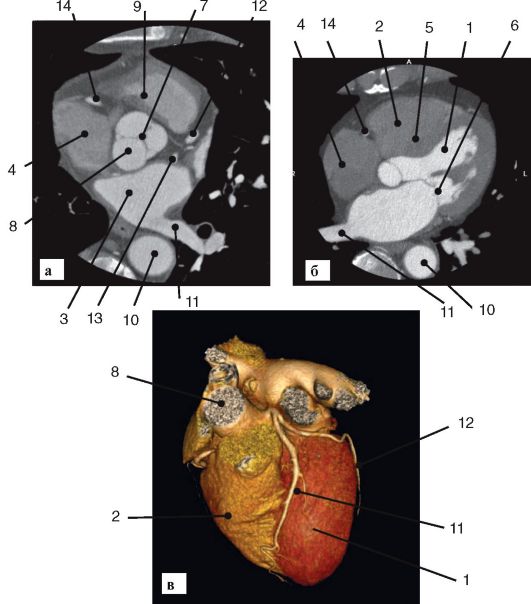
Рис. 8-4. КТ сердца. Норма:
а - поперечный срез через корень аорты; б - поперечный срез через желудочки, реконструкция; в - трехмерная реконструкция сердца и коронарных артерий;
1 - левый желудочек; 2 - правый желудочек; 3 - левое предсердие; 4 - правое предсердие; 5 - межжелудочковая перегородка; 6 - митральный клапан; 7 - аортальный клапан; 8 - восходящая аорта; 9 - конус- ная часть правого желудочка; 10 - нисходящая аорта; 11 - ле__ная вена;
12 - передняя нисходящая артерия; 13 - огибающая артерия; 14 - фрагмент правой коронарной артерии
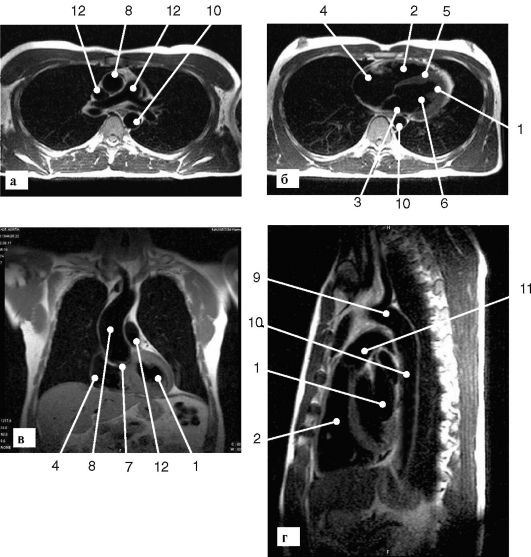
Рис. 8-5. МРТ сердца:
а - поперечный срез на уровне ствола легочной артерии; б - поперечный срез на уровне желудочков; в - сагиттальный срез через левый желудочек; г - фронтальный срез через желудочки и восходящую аорту; 1 - левый желудочек; 2 - правый желудочек; 3 - левое предсердие; 4 - правое предсердие; 5 - межжелудочковая перегородка; 6 - митральный клапан; 7 - аортальный клапан; 8 - восходящая аорта; 9 - дуга аорты; 10 - нисходящая аорта; 11 - легочная артерия; 12 - верхняя полая вена
Для правильного выполнения исследования и трактовки результатов необходимо хорошо ориентироваться не только в анатомии, но и в физиологии сердца. Исследование сердца можно выполнять только на высокопольных магнитах (1,5-3 Тл), с использованием синхронизации с ЭКГ. МРТ используют для дифференциальной диагностики кардиологических заболеваний в сложных случаях и для уточнения данных ЭхоКГ. Используя методику «кино-МРТ», получают изображения сердца в различные фазы сердечного цикла. Это позволяет оценить скорость и характер кровотока в камерах сердца и магистральных сосудах. Существуют более сложные МР-методики оценки перфузии и жизнеспособности миокарда, для чего внутривенно вводятся контрастные вещества на основе гадолиния.
Важные сведения по перфузии миокарда и функции левого желудочка обеспечивают радионуклидные исследования.
Такие методики, как радионуклидная вентрикулография, радионуклидная ангиография, перфузионная сцинтиграфия миокарда с использованием РФП, меченных технецием или таллием, позволяют решать важные вопросы оценки перфузии миокарда при болезнях сердца и коронарных сосудов. Исследования перфузии необходимо выполнять до и после физической нагрузки.
8.2. СЕМИОТИКА ИЗМЕНЕНИЙ КАМЕР СЕРДЦА НА ЛУЧЕВЫХ ИЗОБРАЖЕНИЯХ
Несмотря на быстрый прогресс современных методов диагностики, классическое рентгенологическое исследование сердца не потеряло своей актуальности.
Рентгенологическое исследование в нескольких проекциях дает возможность косвенно судить о размерах отдельных камер сердца.
Увеличение левого желудочка обусловлено его гипертрофией либо дилатацией. При рентгенографии в прямой проекции опре- деляется увеличение и удлинение его тени, а верхушка желудочка расположена ниже, чем обычно. При этом тень сердца выходит за пределы левой срединно-ключичной линии (рис. 8-6). В боковой проекции при увеличении левого желудочка тень последнего заходит за тень заполненного барием пищевода и суживает заднее ретрокардиальное пространство. Конфигурацию сердца с признаками
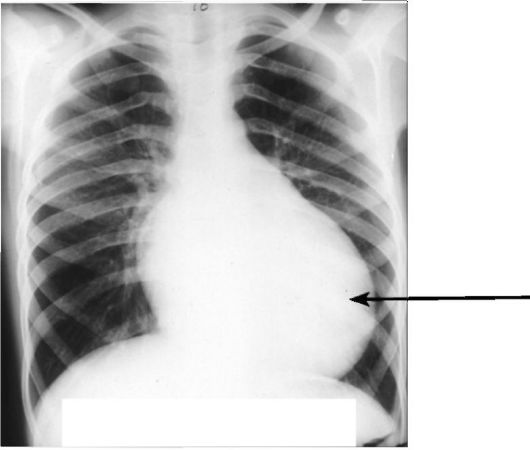
Рис. 8-6. Рентгенограмма сердца при увеличении левого желудочка. Аортальная конфигурация сердца.
Прямая проекция. Граница ЛЖ выходит за левую срединно-ключичную линию, кардио-торакальный индекс превышает 50%. Верхушка желудочка расширена, закруглена (стрелка)
расширенного левого желудочка и тени восходящего отдела грудной аорты называют «аортальной». Такие изменения встречаются при пороках аортального клапана, стенозе устья аорты, артериальной гипертонии и кардиомиопатии.
Увеличенное левое предсердие определяется при смещении им контрастированного пищевода кзади, а левого главного бронха - кверху. Симптом «двойного контура» визуализируется при появлении контура левого предсердия позади правого. Признаки венозного полнокровия в малом круге кровообращения определяются в виде расширения ствола и ветвей легочной артерии. Конфигурация сердца в виде увеличения левого предсердия и легочной гипертензии (рис. 8-7) называется «митральной». Самой частой причиной мит- ральной конфигурации являются пороки митрального клапана либо нарушение диастолической функции из-за изменений в самом миокарде.
Правый желудочек увеличивается при ревматических пороках трехстворчатого клапана, а также вторичной его недостаточности, связанной с перегрузкой правых отделов сердца. Рентгенологически при увеличении правого желудочка уменьшается свободное рет-
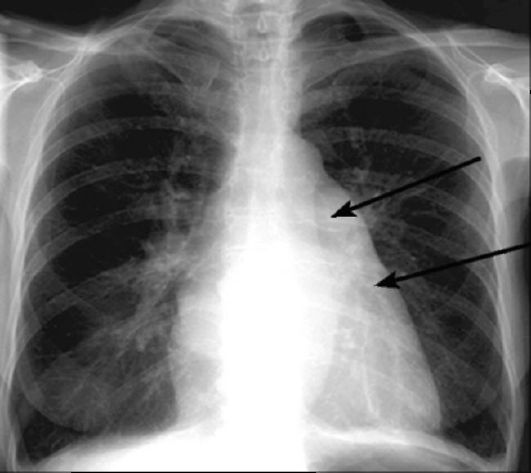
Рис. 8-7. Рентгенограмма сердца при увеличении левого предсердия. Митральная конфигурация сердца. Прямая проекция. Увеличены дуги левого предсердия (стрелка) и легочной артерии (короткая стрелка). Справа на фоне тени правого предсердия видна тень края левого предсердия
ростернальное пространство и увеличивается более чем на треть поверхность его соприкосновения с грудиной. Эти изменения видны на боковых или косых снимках. В прямой проекции расширенный правый желудочек сдвигает левый контур тени сердца латерально и вверх, тогда как увеличенный левый желудочек ее одновременно вниз и латерально, отмечается расширение легочной артерии (рис. 8-8).
Правое предсердие редко увеличивается изолированно. При этом на прямой рентгенограмме отмечается смещение нижнего правого контура сердца вправо. Наиболее частой причиной увеличения правого предсердия является недостаточность трехстворчатого клапана и сброс крови «слева направо» при дефектах межпредсердной перегородки.
При недостаточности кровообращения по большому и малому кругу вследствие различных сердечно-сосудистых заболеваний увеличиваются все камеры сердца, что приводит к формированию «трапециевидной» конфигурации. Следует помнить, что увеличение всех отделов сердца может имитировать наличие жидкости в околосердечной сумке при перикардите и сердечной недостаточности
(рис. 8-9).
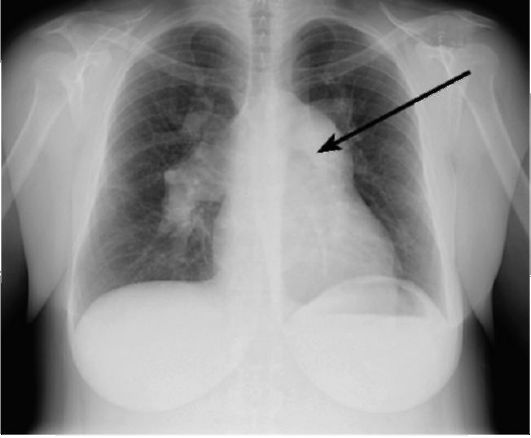
Рис. 8-8. Увеличение правых отделов сердца при легочной гипертензии. Прямая проекция. Признаки увеличения легочной артерии (стрелка)
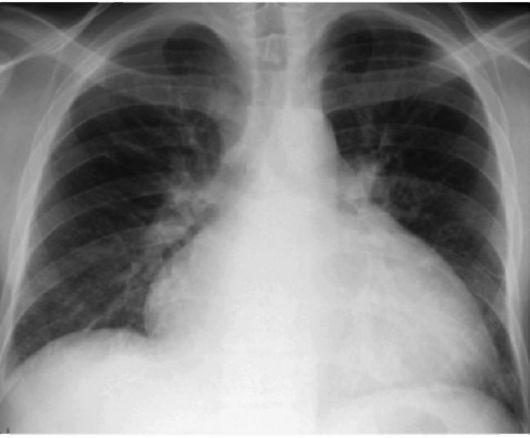
Рис. 8-9. «Трапециевидная» конфигурация тени сердца: кардиомегалия при тяжелой сердечной недостаточности. Тень сердца расширена в обе стороны
8.3. ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА (ВПС)
Многочисленные ВПС с практической точки зрения можно разделить на ряд групп: врожденные пороки сердца без цианоза, пороки с цианозом, а также ВПС с увеличенным, нормальным или сниженным кровотоком в малом круге кровообращения.
8.3.1. Врожденные пороки сердца без цианоза
К врожденным порокам сердца без цианоза с нормальным или повышенным легочным кровообращением относятся дефекты межжелудочковой или межпредсердной перегородок, открытый артериальный проток, коарктация аорты, стенозы устья аорты и ствола легочной артерии.
При дефекте межжелудочковой перегородки (ДМЖП) клиническая и радиологическая картина определяются размером и локализацией дефекта, количеством сброса крови в правый желудочек, давле- нием в правых отделах сердца и степенью легочной гипертензии. При небольших дефектах рентгенологическая картина может оставаться нормальной. При значительных дефектах и большом сбросе крови слева направо отмечается увеличение правых отделов сердца и ствола легочной артерии.
Такие ультразвуковые методы исследования, как эхокардиография и допплерокардиография, позволяют непосредственно визуа- лизировать дефект перегородки и оценить степень нарушения кровотока (рис. 8-10). Немаловажным преимуществом этих методов является возможность количественной оценки степени увеличения и гипертрофии желудочков.
При сомнительных ультразвуковых данных диагностический алгоритм может быть пополнен мультиспиральной КТ, МРТ либо зондированием камер сердца.
Небольшие дефекты межпредсердной перегородки (ДМЖП) могут не сопровождаться нарушением гемодинамики, в связи с чем пороки долгое время остаются нераспознанными. При больших дефектах кровь сбрасывается из левого предсердия в правое предсердие и затем из правого желудочка в малый круг. Это приводит к увеличению правых отделов сердца и появлению на рентгенограммах признаков усиления легочного рисунка за счет сосудистого компонента. Ультразвуковые методы диагностики, в том числе и чреспищеводная эхокардиография, играют ведущую роль в постановке правильного диагноза.
Нередко с ДМЖП сочетаются пороки, связанные с частичным аномальным дренажем легочных вен. К ним относятся, например, впадение правой верхней легочной вены в верхнюю полую вену или правой нижней легочной вены в нижнюю полую вену.
Если в первые сутки после рождения артериальный проток, обеспечивающий во внутриутробном периоде кровоток из легочной артерии в аорту, не закрывается, то развивается открытый артериальный проток (ОАП). При таком пороке кровь сбрасывается из аорты в легочную артерию, увеличивается легочный кровоток, что приводит к перегрузке левых отделов сердца. При рентгенологическом исследовании обнаруживаются признаки усиления кровотока в малом круге, расширение ствола
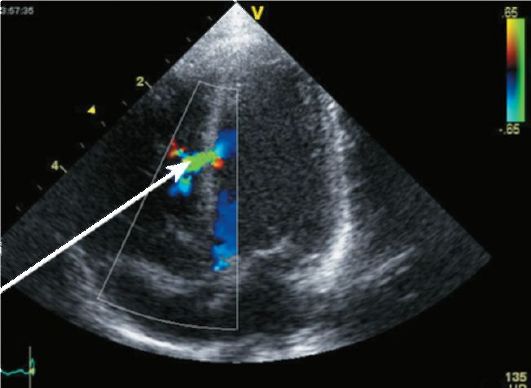
Рис. 8-10. Трансторакальная эхокардиография. Дефект межжелудочковой перегородки. Дуплексное исследование.
Видно отверстие в межжелудочковой перегородке (стрелка), через которое в правый желудочек сбрасывается кровь
легочной артерии, увеличение левого предсердия, левого желудочка и поперечника дуги аорты. Оптимальным методом лучевой диагностики является допплерография, которая дает возможность визуализиро- вать кровоток через ОАП и оценить его объем.
8.3.2. Врожденная патология магистральных сосудов
Коарктация аорты представляет собой врожденное сужение грудного отдела аорты. Обычно сужение возникает несколько ниже места отхождения левой подключичной артерии на уровне артериального протока. Коарктация аорты является одной из причин развития вторичной артериальной гипертензии.
На рентгенограммах видны признаки расширения и гипертрофии левого желудочка, расширение тени восходящего отдела грудной аорты и ее локальное сужение в области перешейка. При длительном давлении расширенных коллатеральных межреберных артерий могут обнаруживаться узурации по нижним краям ребер. Лучше всего коарктация аорты визуализируется при ультразвуковом исследовании, а также при КТ и МРТ (рис. 8-11).
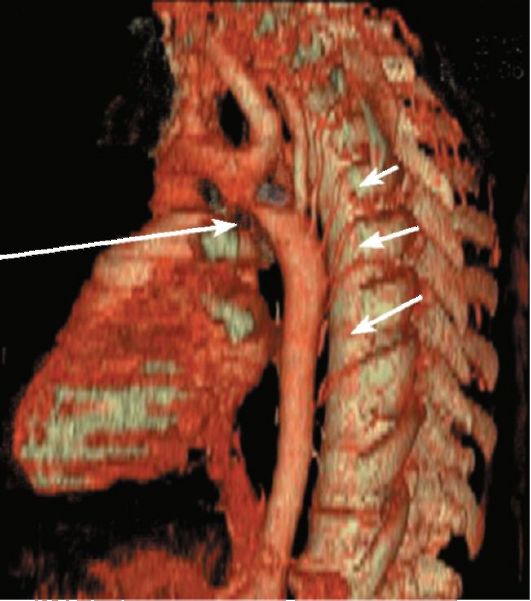
Рис. 8-11. Коарктация грудной аорты: КТ-ангиография при коарктации аорты. Трехмерная реконструкция. Отчетливо виден участок коарктации (стрелка), множественные расширенные реберные артерии (маленькие стрелки)
Врожденные стенозы устья аорты и легочной артерии могут быть изолированными либо сочетаться с другими пороками. Врожденные стенозы устья аорты в большинстве случаев развиваются на уровне клапанов и мало чем отличаются по своему течению от приобретенных стенозов. На рентгенограммах отмечается расширение левого желудочка и восходящей части дуги аорты. При надклапанном или подклапанном формировании сужения эти признаки, как правило, отсутствуют. Детальное строение клапана и причина возникновения стеноза лучше всего видны при ультразвуковых исследованиях сердца.
8.3.3. Врожденные пороки сердца с цианозом и нормальным легочным кровообращением
Для тетрады Фалло характерны четыре составляющих: стеноз выносящего тракта правого желудочка, дефект межжелудочковой перегородки, правостороннее расположение аорты и гипертрофия миокарда правого желудочка. Сердце на рентгенограммах имеет характерную конфигурацию в виде «сапожка». Такая картина обусловлена тем, что тень магистральных сосудов сужена, имеется вогнутость в проекции ствола легочной артерии, а верхушка сердца смещена кверху из-за ротации вследствие расширения правого желудочка (рис. 8-12). Оптимальный объем информации можно получить при использовании ультразвуковых методов исследования.
Атрезия трехстворчатого клапана характеризуется отсутствием сообщения между правым предсердием и правым желудочком. Жизнеспособность организма при такой патологии может обеспечиваться только при нали-
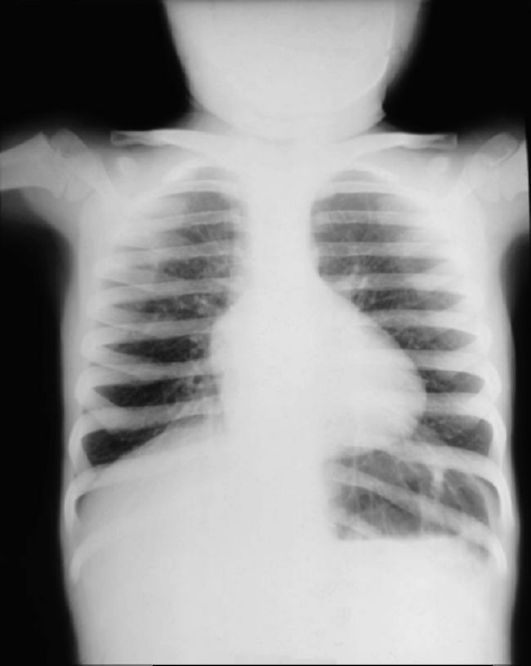
Рис. 8-12. Тетрада Фалло: рентгенограмма грудной клетки. Из-за увеличения правых отделов и приподнятости верхушки левого желудочка сердце имеет форму «сапожка»
чии сброса крови справа налево через дефект межпредсердной или межжелудочковой перегородки. При рентгенографии грудной клетки тень сердца имеет нормальные или уменьшенные размеры, а легочный рисунок обеднен за счет уменьшенного кровотока в малом круге. Окончательный диагноз устанавливается с помощью ультразвуковых исследований и зондирования полостей сердца.
Аномалия Эбштейна обусловлена дислокацией и нарушением строения трехстворчатого клапана, что приводит к выраженной клапанной недостаточности. Нередко имеет место сочетание данной аномалии с дефектом межпредсердной перегородки. На рентгенограммах органов грудной клетки отмечаются обеднение кровоснабжения легких и увеличение сердца за счет правых отделов, из-за чего тень сердца приобретает форму «коробочки». Точная диагностика проводится на основе анализа данных эходопплерографии (рис. 8-13)
или МРТ.
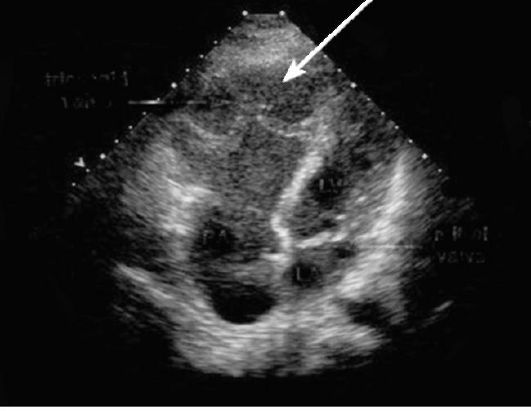
Рис. 8-13. Эхокардиограмма при аномалии Эбштейна. Полость пра- вого желудочка расширена, в глубине ее виден трехстворчатый клапан (стрелки)
8.3.4. Врожденные пороки сердца с цианозом и повышенным легочным кровообращением
Полная транспозиция магистральных сосудов проявляется цианозом в первые часы жизни новорожденного. При этой аномалии, нередко сочетающейся с другими пороками развития, восходящий отдел грудной аорты с коронарными артериями отходит от правого желудочка, а легочная артерия - от левого. Жизнь ребенка возможна лишь при наличии шунтирования крови между левыми и правыми отделами сердца. При рентгенографии отсутствует обычная тень от дуги аорты и нередко отмечается асимметрия размеров ветвей легочных артерий. Детальную информацию можно получить с помощью эхокардиографии, МРТ, МСКТ (рис. 8-14) или зондирования сердца.
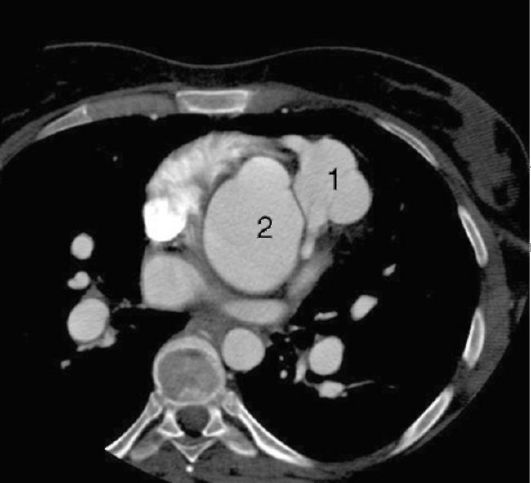
Рис. 8-14. КТ-ангиография при транспозиции магистральных арте- рий. Обратное расположение восходящей аорты (1) и ствола легочной артерии (2)
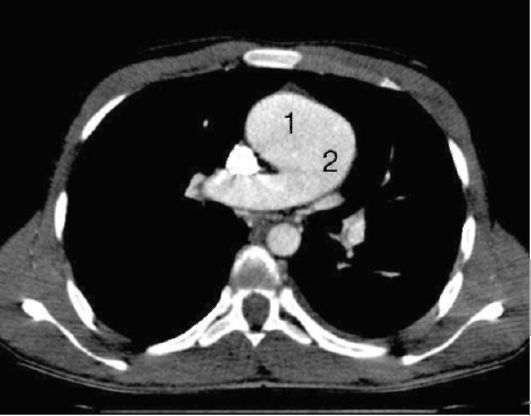
Рис. 8-15. КТ-ангиография. Поперечный срез. Общий артериальный ствол. Отсутствует разделение восходящей аорты (1) и легочного ствола (2)
Общий артериальный ствол возникает вследствие нарушения дифференциации выходящих из сердца сосудов на аорту и легочную артерию. При этой аномалии из обоих желудочков отходит единый ствол, снаб- жающий кровью как большой, так и малый круг кровообращения. Обычно наряду с общим артериальным стволом имеется высокий дефект межжелудочковой перегородки, через который идет смешивание артериальной и венозной крови. При рентгенологическом исследовании определяются кардиомегалия, расширение тени отходящих от ствола сосудов и признаки избыточного легочного кровотока. Наиболее информативными лучевыми методами для постановки точного диагноза являются ультразвуковые методы исследования, МРТ, МСКТ (рис. 8-15) или ангиография.
Примерно в 1% случаев могут иметь место различные варианты отхождения коронарных артерий от синусов Вальсальвы. Чаще всего они представляют собой обычные варианты развития. В детском возрасте такие изменения хорошо видны при ультразвуковом исследовании, тогда как у взрослых наиболее информативна КТ-коронарография.
Изредка крупные сосуды аномально охватывают «сосудистыми кольцами» трахею и пищевод. Если такие кольца неполные, то кли-
ническая картина, как правило, отсутствует. При наличии замкнутого хвоста могут появиться симптомы сдавливания трахеи и пищевода. Примером такой аномалии может быть левосторонняя дуга аорты с аберантной правой подключичной или безымянной артерией.
8.4. ПРИОБРЕТЕННЫЕ БОЛЕЗНИ СЕРДЦА
Приобретенные болезни сердца, такие, как ишемическая болезнь, пороки клапанов, различные виды кардиомиопатий, заболевания аорты и сосудов, являются основными причинами смертности во всем мире. Поэтому правильное и своевременное применение методов лучевой диагностики, в том числе и на доклиническом этапе, позволяет вовремя установить диагноз и оказать пациенту адекватную помощь.
8.4.1. Пороки митрального клапана
Органические изменения в клапанах сердца возникают вследствие заболеваний (ревматизма, атеросклероза, эндокардита) или травм. Проявление и диагностика приобретенных пороков сердца обусловлены скоростью развития болезни и ведущим признаком - стенозом или недостаточностью клапана.
Первое место по частоте среди причин возникновения пороков клапанов сердца принадлежит митральному клапану.
Недостаточность митрального клапана развивается в результате ревматизма, бактериального эндокардита, дисфункции папиллярных мышц, дилятации и гипертрофии левого желудочка.
Стеноз левого атриовентрикулярного отверстия встречается значительно реже и обычно обусловлен ревматическим поражением либо имеет врожденное происхождение.
Пороки митрального клапана приводят к формированию так называемой митральной конфигурации сердца. Рентгенологические признаки увеличения как левого предсердия, так и левого желудочка чаще всего отражают наличие митральной недостаточности. При остром развитии митральной недостаточности могут визуализироваться рентгенологические признаки отека легкого.
«Золотым» стандартом в диагностике пороков митрального клапана являются эхокардиография и допплерография, позволяющие не
только хорошо визуализировать структуру клапанов, но и изучить состояние миокарда, оценить степень стеноза или регургитации, а также определить размеры камер сердца (рис. 8-16). В сложных случаях применяют МРТ или зондирование сердца.
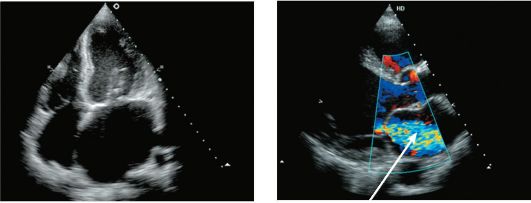
Рис. 8-16. Эхокардиография при пороках митрального клапана: а - стеноз левого атриовентрикулярного отверстия. Диастола. 1 - ЛЖ. 2 - ПЖ. Стрелкой указаны утолщенные створки митрального клапана с ограниченным раскрытием;
б - цветовое допплеровское исследование при митральной недостаточности. Систола. Поток митральной регургитации распространяется в левое предсердие (указан стрелкой)
8.4.2. Пороки аортального клапана
Стеноз устья аорты обычно возникает как осложнение ревмокардита или атеросклероза. При ревматической этиологии стеноз нередко сочетается с недостаточностью аортального клапана. При этом в стенках аортального клапана зачастую откладывается кальций.
На рентгенограммах визуализируется «аортальная» конфигурация сердца, развивающаяся вследствие дилатации и гипертрофии левого желудочка.
Методами выбора в диагностике пороков аортального клапана (стеноза и недостаточности) являются эхокардиография и допплерография, дающие возможность не только увидеть анатомию и оценить функцию створок клапана, но и измерить площадь отверстия клапана и градиент давления в нем (рис. 8-17).
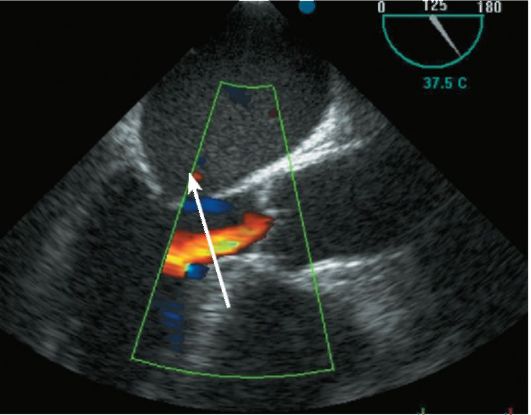
Рис. 8-17. Эходопплерография при недостаточности аортального клапана. Стрелкой указан ретроградный поток крови через закрытые створки аортального клапана в диастолу (стрелка)
8.4.3. Пороки трехстворчатого клапана и клапана легочной артерии
Пороки трехстворчатого клапана редко развиваются изолированно и, как правило, являются следствием ревмокардита. При исследовании больных с пороками трехстворчатого клапана обычно отмеча- ется увеличение правого предсердия.
При пороке клапана легочной артерии всегда обнаруживаются признаки расширения и гипертрофии правого желудочка. При сте- нозе клапана, под влиянием высокоскоростного потока крови, сразу после места сужения возникает расширение легочной артерии и ее левой ветви.
8.4.4. Болезни миокарда
Кардиомиопатии развиваются вследствие острых и хронических миокардитов, а также при коллагенозах, саркоидозе, гемохроматозе, васкулитах, амилоидозе и других заболеваниях. Возможно развитие кардиомиопатии и на фоне токсического воздействия, например алкоголя и лекарственных средств.
Дилатационная кардиомиопатия сопровождается расширением камер сердца и снижением сократительной функции миокарда, что
сопровождается недостаточностью кровообращения в малом круге. При рентгенографии обычно визуализируются признаки застоя или отека легких. Ультразвуковые методы, а также КТ и МРТ дают точную информацию о состоянии камер сердца и степени нарушения сократительной функции миокарда (рис. 8-18).
Гипертрофическая кардиомиопатия характеризуется ассиметричной или симметричной гипертрофией различных участков миокарда без очевидных причин. Для диагностики этого вида кардиомиопатий наиболее информативными являются двухмерная эхокардиография и МРТ (рис. 8-19).
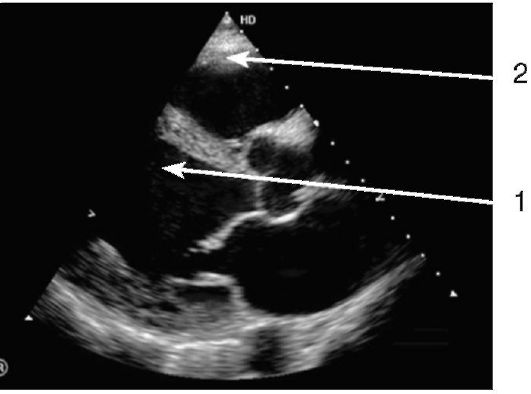
Рис. 8-18. Эхокардиография у пациента с дилатационной кардиомиопатией. Определяется выраженное увеличение полости левого желудочка. ЛЖ - 1, ПЖ - 2. При исследовании в режиме реального времени опре- делялось снижение сократительной функции миокарда
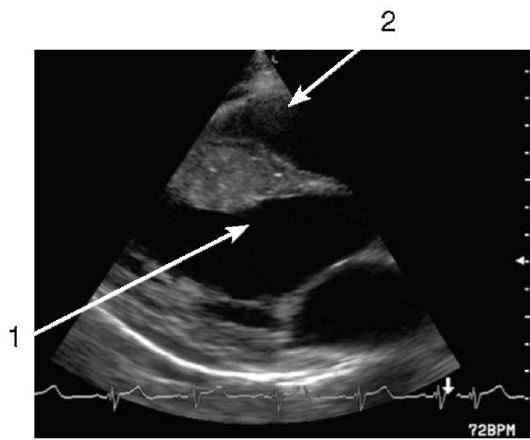
Рис. 8-19. Эхокардиограмма при гипертрофической кардиомиопатии. ЛЖ - 1, ПЖ - 2. Утолщенная межжелудочковая перегородка указана стрелкой
Рестриктивная кардиомиопатия сопровождается нарушением диастолического расслабления желудочков, фиброзом миокарда и эндо- карда. Рентгенологически определяется увеличение обоих предсердий при нормальных размерах желудочков.
Для морфологической верификации отдельных видов кардиомиопатий и миокардитов иногда необходимо выполнение эндомио- кардиальной биопсии при ангиографическом зондировании камер сердца.
8.4.5. Ишемическая болезнь сердца (ИБС) и коронарный атеросклероз
Снижение кровотока по коронарным артериям, сопровождающееся ухудшением питания сердечной мышцы, ведет к развитию ишемической болезни сердца. Самым грозным осложнением ИБС является инфаркт миокарда.
В большинстве случаев причиной сужения коронарных артерий являются атеросклеротические бляшки. Так называемые неослож- ненные, стабильные атеросклеротические бляшки не приводят к возникновению гемодинамических нарушений и длительное время себя не проявляют.
Клинические признаки ИБС возникают в тех случаях, когда атеросклеротические бляшки перекрывают более 70% диаметра коронарного сосуда или занимают более 50% его площади. При физических или эмоциональных нагрузках, приводящих к повышенному потреблению кислорода, возникают эпизоды ишемии миокарда. Длительный спазм коронарного сосуда вызывает инфаркт миокарда. К острому инфаркту миокарда может привести разрыв или эрозия бляшки, сопровождающиеся тромбозом сосуда.
При стабильной ИБС, а также в неотложных ситуациях самым высокоинформативным и надежным методом лучевой диагностики является коронароангиография (КАГ). Метод дает возможность обнаружить стеноз в коронарных сосудах и определить его степень (рис. 8-20).
В случаях значительного сужения сосуда КАГ используется для проведения эндоваскулярного баллонного расширения места стеноза и установки внутрикоронарного стента (рис. 8-21).
При хронической ИБС в целях определения перфузии и жизнеспособности сердечной мышцы применяется радионуклидная сцинтиграфия миокарда в покое и после нагрузки. При наличии преходящих дефектов перфузии сцинтиграфия после велоэргометрии позволяет выявить зоны нарушения перфузии, невидимые при исследовании в покое (рис. 8-22).
К концу первых суток от момента развития острого инфаркта миокарда сцинтиграфия после внутривенного введения технеция 99м- пирофосфата дает возможность визуализировать очаги накопления радиофармпрепарата в очагах некроза сердечной мышцы. Однако изза сомнительных результатов, получаемых в первые сутки развития патологического процесса, этот метод не стал ведущим в экстренной диагностике инфаркта миокарда.
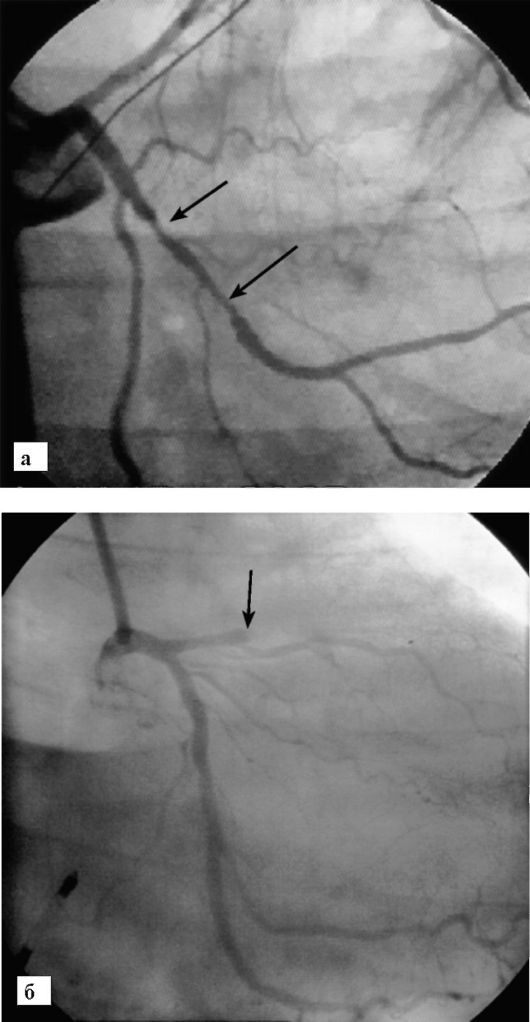
Рис. 8-20. Коронарография при стенозах и окклюзиях венечных сосудов (указаны стрелками):
а - протяженный стеноз огибающей артерии; б - окклюзия передней межжелудочковой ветви
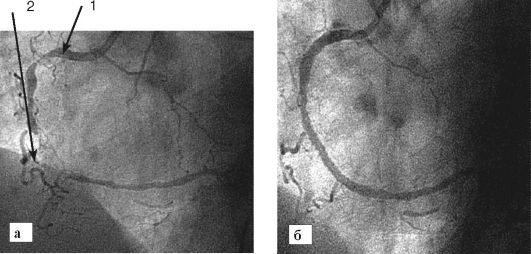
Рис. 8-21. Устранение стеноза (1) и окклюзии (2) правой коронарной артерии с помощью стентирования:
а - ангиограмма до вмешательства; б - после стентирования
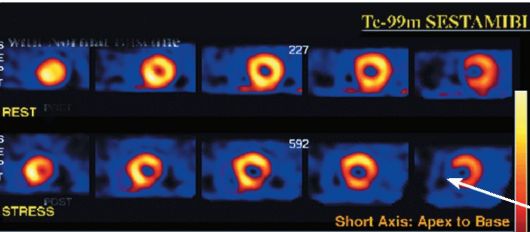
Рис. 8-22. Сцинтиграфия миокарда с Тс99т SESTAMBI у пациента с ИБС. В верхнем ряду - сцинтиграммы ЛЖ в покое. Распределение радиофармпре- парата равномерное. В нижнем ряду показаны сцинтиграммы после теста с физической нагрузкой, на которых отмечается появление дефекта перфузии в области боковой стенки ЛЖ (стрелка)
В последние годы для выявления участков некроза и воспаления в миокарде на ранних стадиях инфаркта начали использовать специальные методики МРТ после внутривенного введения контрастных препаратов, содержащих гадолиний. Эти методики применяют в специализированных клиниках.
В связи с широкой распространенностью ишемической болезни сердца, ее скрытым течением и в целях доклинической диагностики коронарного атеросклероза у пациентов с высоким риском развития коронарных осложнений в настоящее время используется мультиспиральная КТ, проводимая с кардиосинхронизацией. Это простая и эффективная методика, при которой не требуется введение контрастного препарата, может быть выполнена любым пациентам, вне зависимости от их веса, физической тренированности, пола и возраста. При помощи этого метода рентгенологи могут обнаружить обызвествленные бляшки и оценить количество кальция в коронарных сосудах. «Мягкие» бляшки, не содержащие кальция, при такой методике не визуализируются и могут быть обнаружены только при мультиспиральной коронарографии при болюсном введении контрастного препарата (рис. 8-23).
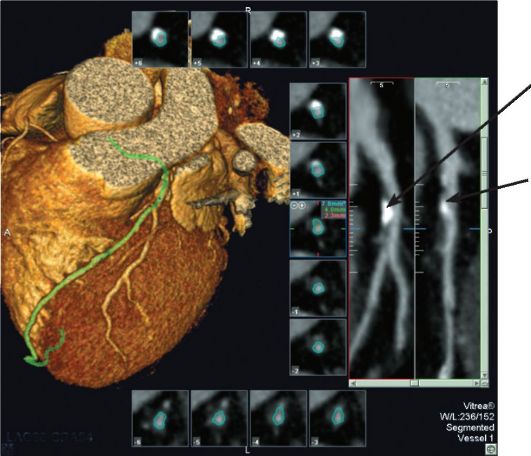
Рис. 8-23. МСКТ-ангиография. Трехмерная реконструкция сердца и коронарных артерий. Проведена линия по ходу передней межжелудочковой ветви, соответственно которой слева построено сечение сосуда, заполненного кон- трастным веществом. Отчетливо видна частично кальцинированная атеро- склеротическая бляшка, суживающая просвет сосуда (стрелка)
8.5. ОПУХОЛИ СЕРДЦА
Новообразования сердца относятся к редкой патологии и при рентгенологических исследованиях, как правило, не визуализируются. Зачастую опухоли сердца длительное время протекают бессимптом- но и впервые диагностируются лишь при проведении ЭхоКГ.
Различают первичные и вторичные (метастатические) опухоли сердца. Первичные опухоли в основном представлены доброкачественными новообразованиями: миксомами, фибромами, липомами и рабдимиомами. Самой распространенной доброкачественной опухолью является миксома. Опухоль обычно располагается в области межпредсердной перегородки и имеет шаровидную или овальную форму. В настоящее время диагностика миксом не представляет трудностей, поскольку опухоль хорошо визуализируется в виде дви- жущегося объемного образования с отличной от крови акустической плотностью при эхокардиографии (рис. 8-24), а также в виде дефекта наполнения на фоне яркого сигнала от движущейся крови при МРТ. Высокоинформативной при миксомах сердца является и мультиспиральная КТ, однако только на фоне введенного контрастного препарата.
Злокачественные первичные опухоли сердца (ангиосаркомы) встречаются редко, локализуются в основном в правом предсердии и быстро вовлекают в процесс правый желудочек и перикард, вызывая выпот в полость последнего. Диагностика этих опухолей ничем не отличается от диагностики доброкачественных новообразований.
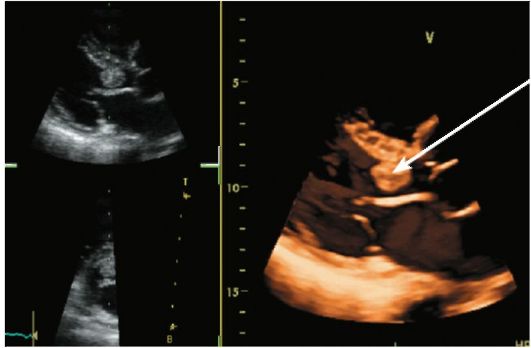
Рис. 8-24. Миксома левого предсердия. При двухмерной и трехмерной эхокардиографии видна миксома левого предсердия (стрелка)
8.6. БОЛЕЗНИ ПЕРИКАРДА
Экссудат или транссудат в полости перикарда появляется в основном в результате сердечно-сосудистых заболеваний (инфаркт, сердечно-сосудистая недостаточность), инфекций (перикардит), метаболических или эндокринных расстройств (уремия, гипотиреоз). Кроме того, выпот может образовываться при опухолевом процессе, после лучевой терапии, а также в результате хирургических вмешательств.
Наличие значительного количества жидкости в перикардиальной полости рентгенологически проявляется равномерным расширением тени сердца, без признаков преобладания увеличения какого-либо из отделов сердца. Небольшое количество выпота может быть обнаружено только при ультразвуковой диагностике (рис. 8-25) либо при
КТ или МРТ.
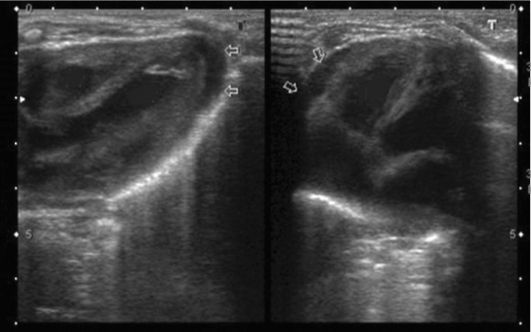
Рис. 8-25. Эхокардиография при экссудативном перикардите. Перед правым и за левым желудочком определяется свободное эхонегативное пространство (стрелки)
В случае возникновения фиброза или кальциноза перикарда может развиться констриктивный перикардит, приводящий к нарушению заполнения желудочков кровью. Рентгенологически он проявляется наличием уплотненной или обызвествленной линии по периферии сердечной тени, с характерным началом из атриовентрикулярных борозд. Лучше всего подобные изменения видны при
КТ (рис. 8-26).
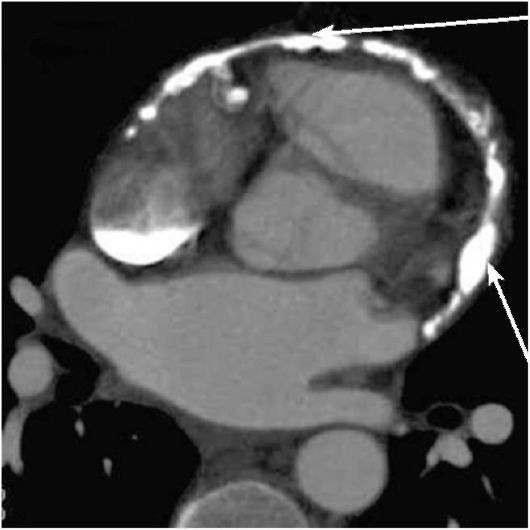
Рис. 8-26. МСКТ при констриктивном перикардите. На поперечном срезе хорошо видны утолщенные, неравномерно кальцинированные листки перикарда (стрелки)
Нередко в перикарде локализуются тонкостенные кисты, заполненные серозной жидкостью (перикардиальные кисты) и имеющие сообщение с перикардиальной полостью. Большие кисты могут быть обнаружены при рентгенографии, чаще всего в области правого кардиодиафрагмального угла. Для дифференциальной диагностики кисты перикарда с липомой или другой опухолью необходимо провести КТили МРТ-исследование.
Наиболее часто встречающейся злокачественной опухолью перикарда является мезотелиома, которая в большинстве случаев дает геморрагический выпот в плевральную полость. Опухолевую природу экссудата в таких случаях позволяет установить КТ с введением контрастного препарата и забор жидкости для цитологического исследования.
8.7. БОЛЕЗНИ СОСУДОВ
В течение многих десятилетий единственным методом диагностики патологии сосудов была рентгеновская ангиография.
В последние годы для выявления патологии сосудов начали широко применяться менее инвазивные лучевые методы, такие, как ультразвуковая диагностика, КТ-ангиография и МР-ангиография.
Цветовое допплеровское и дуплексное ультразвуковое исследование позволяет не только визуализировать и оценивать состояние стенки и интимы сосудов, но и проводить количественный анализ показателей кровотока.
При мультиспиральной КТА появилась возможность изучать состояние артериальных и венозных сосудов в разные фазы прохождения по ним контрастного препарата.
Возможности МРА практически идентичны таковым при МСКТ, однако отсутствие ионизирующего излучения делает МРА более предпочтительной при обследованиях детей.
Необходимо отметить, что с внедрением указанных методов роль прямой рентгеновской ангиографии в диагностике сосудистой патологии снизилась. В настоящее время в подавляющем большинстве случаев ангиография используется для проведения баллонной ангиопластики, стентирования, эмболизации и других лечебных мероприятий.
8.8 АНЕВРИЗМЫ И РАССЛОЕНИЯ АОРТЫ
Аневризмы аорты бывают истинными и ложными. Разрывы аневризм аорты приводят к кровопотере, часто несовместимой с жизнью.
Истинные аневризмы распространяются на все слои стенки аорты и в большинстве случаев являются следствием атеросклероза. В молодом возрасте встречаются врожденные нарушения строения аорты (синдром Морфана или Элерса-Данло). Причиной развития аневризмы могут быть грибковые поражения, сифилис и артерииты.
Ложные аневризмы развиваются при разрывах интимы и медии, что приводит к ассиметричному выбуханию стенки аорты. В основ- ном ложные аневризмы развиваются при травмах, инфекционных процессах, после оперативных вмешательств, а также как следствие атеросклероза. Локальный разрыв оболочек приводит к образованию двух просветов в аорте - истинного и ложного. Ложный просвет, как правило, тромбируется, однако при сохранении его связи с истинным просветом кровоток может сохраняться.
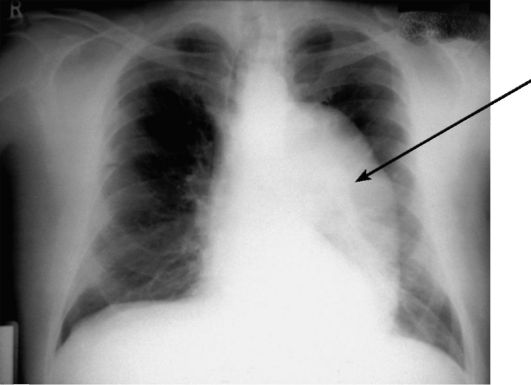
Рис. 8-27. Рентгенограмма грудной клетки при аневризме нисходящей аорты. Нисходящая аорта расширена и отклонена влево (стрелка), что приводит к выраженному изменению конфигурации тени сердца и средостения на снимке
Согласно классификации De Backey расслаивающие аневризмы аорты бывают трех типов: I - расслоение восходящей и нисходящей аорты, II - расслоение восходящей аорты и III - расслоение нис- ходящей аорты.
В большинстве случаев аневризмы грудной аорты можно выявить при рентгенографии (рис. 8-27), но этот метод не позволяет видеть внутреннюю структуру аневризмы.
Если раньше для окончательной диагностики аневризм и расслоений аорты применялась только аортография, то в последнее десятилетие самыми быстрыми и информативными методами лучевой диагностики стали КТА и МРА. С их помощью можно оценить не только состояние стенок аорты, но и определить наличие тромбоза, хода отслоившейся интимы по отношению к коронарным артериям и другим ветвям аорты (рис. 8-28).
В неотложных случаях, при подозрении на расслаивающую аневризму и необходимости решения вопроса о срочном оперативном вмешательстве, в первую очередь необходимо выполнить КТА или прямую аортографию.
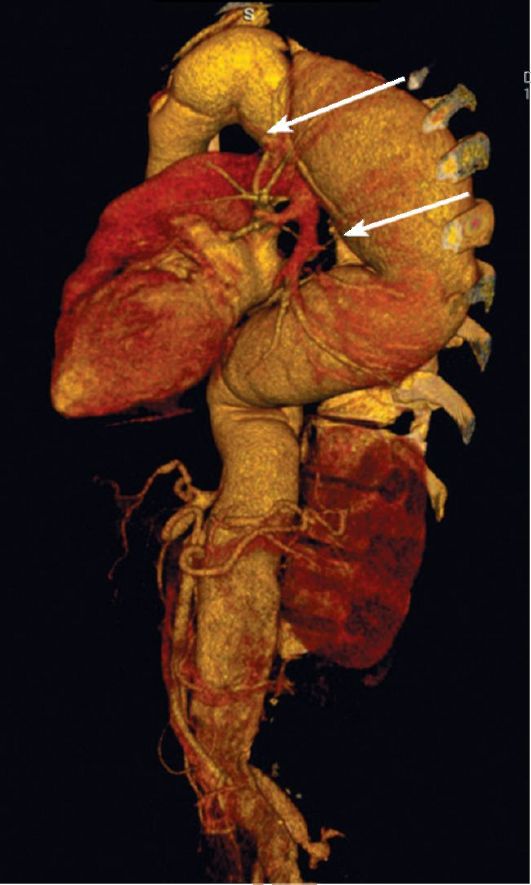
Рис. 8-28. КТ-ангиография при расслаивающей торакоабдоминальной аневризме. Трехмерная реконструкция, показывающая протяженность расслоения и переход его на брюшную аорту. Линия отслоившейся интимы указана стрелкой
8.9. ОККЛЮЗИОННЫЕ ПОРАЖЕНИЯ ПЕРИФЕРИЧЕСКИХ АРТЕРИЙ
Стеноз и окклюзии периферических артерий развиваются на фоне атеросклероза, сахарного диабета, облитерирующего тромбоангиита, аорто-артериита и различных васкулитов.
Окклюзионно-стенотический процесс может быть острым или хроническим. Острые окклюзии чаще всего возникают при эмбо-
лиях или тромбозах, однако могут быть следствием спазма, внешней компрессии и расслоения стенок артериальных сосудов. Первичным методом диагностики болезней периферических артерий являются сонография и допплерография. «Золотым стандартом» лучевой диагностики является прямая артериография, когда на уровне окклюзии виден «обрыв» контрастированного просвета артерии. В настоящее время уровень окклюзии может диагностироваться и при мультиспиральной КТА (рис. 8-29), что во многих случаях позволяет избежать инвазивного диагностического вмешательства.
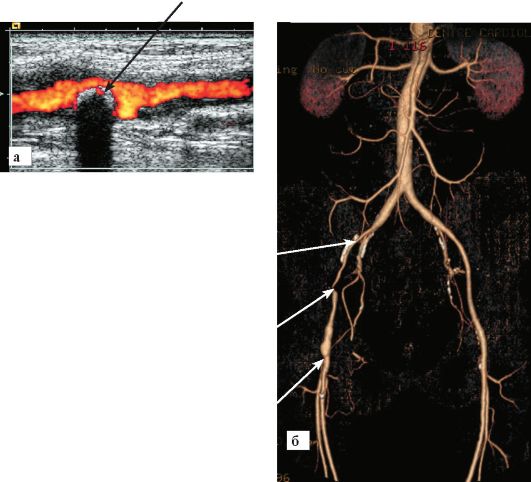
Рис. 8.29. Неинвазивные методы диагностики окклюзионных поражений артерий:
а - дуплексное исследование бедренной артерии. Видна кальцинированная бляшка (стрелка) с изъязвленной поверхностью, суживающая просвет сосуда; б - МСКТ-ангиография. Большое поле изображения позволяет видеть множественные сужения подвздошных и бедренных артерий (стрелки)
Значимые для гемодинамики хронические стенозы и окклюзии периферических артерий в основном развиваются на фоне атероск- лероза и проявляются клинической симптоматикой ишемии в виде различных функциональных расстройств и боли. При сужении,
например, проксимального отдела подключичной артерии может возникнуть синдром «обкрадывания» с возникновением обратного кровотока в позвоночной артерии и развитием недостаточности мозгового кровообращения. Стеноз в чревном стволе и верхнебрыжеечной артерии проявляется симптомами мезентериальной ишемии («брюшная жаба»).
Для хронической формы окклюзионной болезни характерно развитие множественных коллатералей, при помощи которых организм частично компенсирует недостаточность кровообращения.
В отличие от атеросклероза воспалительные процессы являются причиной окклюзионных процессов в артериях лишь в 5% случаев. Чаще всего в клинической практике практические врачи сталкиваются с облитерирующим тромбангиитом (болезнью Бюргера), при котором первично поражаются периферические артерии малого и среднего калибра у молодых мужчин.
Артерии дуги аорты, легочной артерии и брюшного отдела аорты поражаются при артериите Такаясу.
Кроме этого стенозы и окклюзии могут вызываться узелковым и гигантоклеточным артериитом, туберкулезом, сифилисом и другими инфекционными процессами.
Основным методом скрининга в диагностике патологии периферических артерий являются ультразвуковое исследование с допплерографией. Однако для целенаправленного планирования хирургического или интервенционного эндоваскулярного вмешательства необходимо проведение прямой ангиографии или МСКТангиографии, дающих комплексное представление о состоянии всех артерий и коллатералей исследуемой области. Основными симптомами атеросклероза аорты и периферических артерий, выявляемыми при ангиографии, являются неровность стенок сосудов и сужение их просвета. Сами бляшки при ангиографии не обнаруживаются. Одновременно с диагностикой возможно вос- становление проходимости сосуда при использовании эндоваскулярных технологий: тромболизиса, ангиопластики, стентирования (рис. 8-30).
За последние годы большой прогресс в диагностике заболеваний сосудов достигнут благодаря использованию МСКТА, позволяющей не только получать аналогичную прямой ангиографии информацию, но и визуализировать и определять характер самой бляшки.
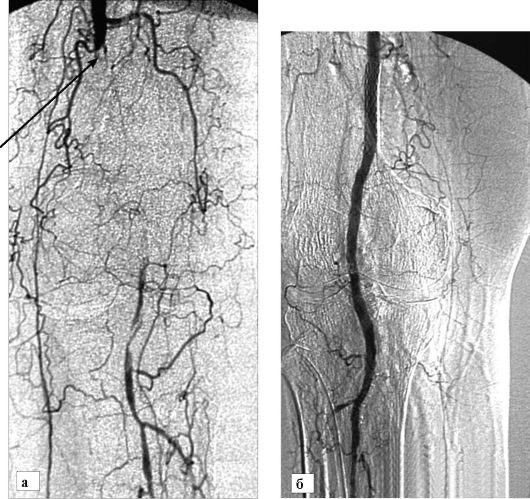
Рис. 8-30. Ангиография бедренной и подколенной артерии: а - виден «обрыв» просвета бедренной артерии в нижней трети (стрелка). Имеется выраженная сеть коллатералей; б - ангиография, выполненная после открытия окклюзии и стентирования (стент указан стрелкой) пораженного участка. Полное восстановление кровотока по сосуду
8.10. АНОМАЛИИ СТРОЕНИЯ СОСУДОВ
(МАЛЬФОРМАЦИИ)
Мальформации сосудов бывают врожденными и приобретенными. К врожденным аномалиям относятся гемангиомы, артериове- нозные мальформации (АВМ), капиллярные и венозные ангиомы,
артериовенозные фистулы. Более половины врожденных мальформаций встречается в головном и спинном мозге. В остальных случаях пороки развития сосудов локализуются в других анатомических областях.
Артериовенозные фистулы или шунты, образующиеся после травм или в результате новообразований печени или почек, относятся к приобретенным мальформациям.
Ведущую роль в диагностике аномалий развития сосудов играет КТ- и МР-ангиография.
Эндоваскулярные процедуры с закрытием при помощи специальных спиралей и пломбирующих средств кровотока к питающему сосуду позволяют избежать необходимости проведения открытых оперативных вмешательств (рис. 8-31).
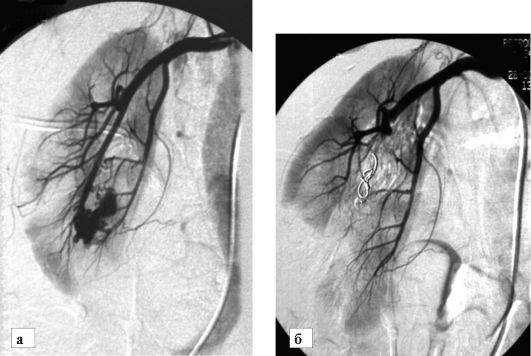
Рис. 8-31. Диагностика и лечение артериовенозной фистулы правой почки: а - на ангиограмме визуализируется сеть расширенных сосудов, образо- вавшихся в результате врожденной артериовенозной фистулы; б - после эмболизации микроспиралями (указаны стрелкой) контрастирование патологических сосудов исчезло
8.11. БОЛЕЗНИ ВЕН
Тромбоз глубоких вен - наиболее часто встречающаяся в клинической практике патология венозных сосудов. Основными факторами риска развития этого заболевания являются расстройства свертывающей системы крови, длительная иммобилизация, травмы, пожилой возраст пациента, опухолевые процессы и различного рода хирургические вмешательства. При тромбозе глубоких вен резко возрастает угроза легочной эмболии, венозной гангрены с последующей потерей конечности, тромбоза нижней полой вены, развития кожных трофических изменений.
Основным лучевым методом диагностики патологии вен является ультразвуковая диагностика с допплерографией. Метод позволяет определить наличие тромба в просвете вены, а также выяснить причину отсутствия или снижения венозного кровотока (рис. 8-32).
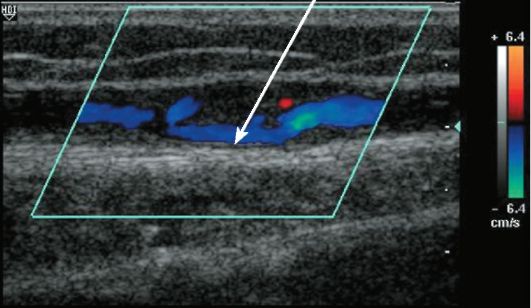
Рис. 8-32. Дуплексное исследование при тромбозе бедренной вены. Синим цветом кодируется кровоток в сосуде. Внутри просвета вены видны тромботические массы (стрелки)
Вопросы и задания
1. Как проявляется увеличение левого предсердия на рентгенограммах грудной клетки?
2. Укажите основной метод диагностики клапанных пороков сердца.
3. С какой целью пациентам с ИБС чаще всего назначают радионуклидные исследования?
4. Каким образом возможно проведение неинвазивной коронарографии?
5. Укажите основной симптом расслоения аорты.