Руководство к практическим занятиям по гинекологии: Учебное пособие / Под ред. В.Е. Радзинского. - 2007. - 600 с. : ил.
|
|
|
|
ГЛАВА 6 ДОБРОКАЧЕСТВЕННЫЕ ОПУХОЛИ И ПРЕДРАКОВЫЕ ЗАБОЛЕВАНИЯ ЖЕНСКИХ ПОЛОВЫХ ОРГАНОВ
6.1. КИСТЫ ПОЛОВЫХ ОРГАНОВ
Что такое киста?
Киста (от греч. kystos - пузырь; англ. - cyst) - тонкостенная патологическая полость, заполненная жидким содержимым. Кисты встречаются во всех отделах мочеполового тракта женщины.
Какие бывают кисты?
Различают кисты ретенционные (лат. retentio - задержка), которые образуются из-за задержки секрета в результате облитерации выводного протока железы, рамолиционные (лат. ramollitio - размягчение) - от распада тканей (при кровоизлияниях, некрозах); эмбриональные (морганиевы гидатиды) и паразитарные (эхинококковая киста).
За счет чего киста увеличивается в размерах?
Увеличение кисты происходит за счет накопления секрета, стенка же кисты, подвергаясь давлению изнутри, растягивается, истончается, эпителий атрофируется и исчезает.
Каково различие между кистами и истинными опухолями?
Различие между кистами и истинными опухолями состоит в том, что последние увеличиваются за счет клеточной пролиферации, а кисты - за счет объема жидкого содержимого.
Какие бывают кисты в области наружных половых органов?
Кисты в области наружных половых органов могут возникать в сальных и потовых железах. Они имеют небольшие размеры - 2-3 см в диаметре. Кисты, развивающиеся из сальных желез, называются атеромами. Небольшие кисты могут появиться из парауретральных желез, располагаясь сбоку от уретры. Крайне редко встречается киста из влагалищного отростка брюшины, когда в эмбриональном
периоде этот отросток не подвергается обратному развитию и образуется полость, называемая дивертикулом Нука. Эта киста располагается в верхней трети большой половой губы, доходит до пахового канала, имеет продолговатую форму, иногда ее размер достигает 7-8 см. Она подлежит оперативному лечению.
Какая киста наружных половых органов имеет наибольшее практическое значение?
Наиболее
часто в области наружных половых органов встречаются кисты больших
желез преддверия влагалища (бартолиновых желез). Эта киста развивается в
результате закупорки, стенозирования или заращения выводного протока
железы. Содержимое кисты прозрачное, тягучее, желтоватой или
коричневатой окраски, размер кисты - от 3 до
Какова клиника кисты большой железы преддверия?
Киста большой железы преддверия влагалища может быть односторонней и двусторонней, располагается в толще нижней трети больших половых губ.
При небольших размерах кисты больные жалоб не предъявляют и за медицинской помощью не обращаются, при больших ее размерах отмечают чувство тяжести в области наружных половых органов, затруднение при ходьбе и половом акте.
Каково лечение кисты большой железы преддверия влагалища?
Лечение оперативное.
Какие методы оперативного лечения применяют?
Первый метод - вылущивание кисты острым путем из ее ложа (рис. 6.1). В проекции кисты делают разрез с внутренней поверхности большой половой губы в нижней ее трети (анатомическое расположение барто- линовой железы). При вылущивании необходимо тщательно удалить всю капсулу, так как при оставлении части ее возникает рецидив. Ложе удаленной кисты зашивают погружными кетгутовыми швами, края раны - отдельными узловатыми кетгутовыми швами.
Второй метод - марсупиализация (восстановление проходимости) выводного протока бартолиновой железы (рис. 6.2). После разреза в
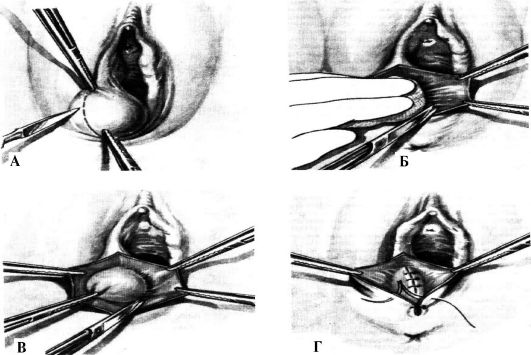
Рис. 6.1. Удаление кисты большой железы преддверия: А - разрез кнаружи от малой половой губы; Б - натяжение и пересечение соединительнотканных тяжей клетчатки; В - продолжение выделения кисты; Г - зашивание кожи

Рис. 6.2. Восстановление проходимости выводного протока большой железы преддверия: А - начало операции; Б - соединение стенки кисты с краями
кожной раны
капсуле кисты иссекают «окошко» и края капсулы отдельными кетгутовыми швами соединяют с краями кожной раны. Таким образом восстанавливают проходимость выводного протока железы, наружное отверстие которого постепенно, в течение 3-5 нед, уменьшается до нормальных размеров.
6.1.1. Кисты влагалища
Кисты на стенке влагалища встречаются редко - в 1-2% случаев. Слизистая влагалища желез не имеет, но кисты могут развиваться из продуцирующих секрет остатков мезонефрального протока (гартнеровы ходы).
Какова локализация кист влагалища?
Кисты влагалища обычно располагаются вдоль боковых стенок влагалища, чаще - в верхнем его отделе.
Какова клиническая характеристика кист влагалища?
Как правило, кисты влагалища однокамерные, редко - многокамерные, округлой формы, с гладкой поверхностью мягкоили тугоэластической консистенции. Содержимое кист - прозрачная слизистая жидкость, иногда коричневатая в результате кровоизлияния.
Величина ретенционных кист влагалища колеблется от 1 до 9-10 см в диаметре.
Что такое киста гартнерова хода?
Это киста, возникшая из остатка мезо- нефрального (вольфова) протока, имеет продолговатую форму, может достигать больших размеров, уходя глубоко в параметральную клетчатку, что необходимо помнить при операции удаления этих кист (рис. 6.3).
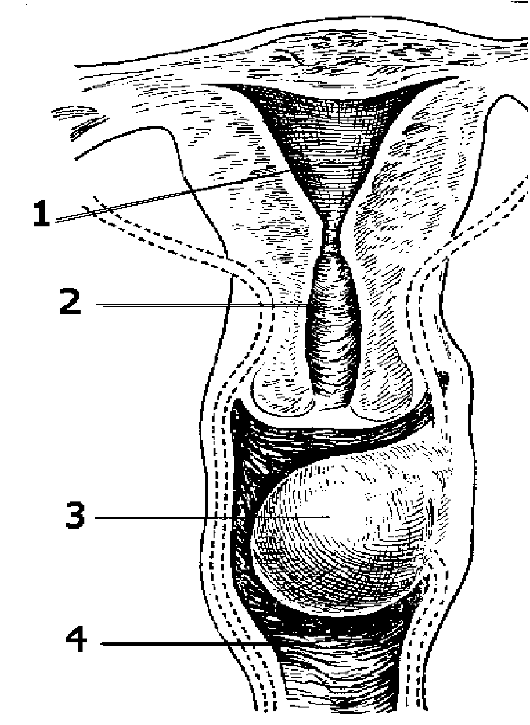
Рис. 6.3. Киста влагалища из гартнерова хода: 1 - полость матки; 2 - цервикальный канал; 3 - киста; 4 - влагалище
Какова симптоматология кист влагалища?
Обычно течение бессимптомное, лишь при больших размерах кисты отмечаются затруднение и болезненные ощущения при половом акте.
Каковы методы диагностики кист влагалища?
Диагностика кист влагалища проста. Диагноз ставят на основании данных влагалищного исследования и осмотра в зеркалах. Дифференцировать кисты влагалища следует от опущения стенок влагалища и заболеваний мочевыделительной системы (дивертикул уретры).
Каковы методы лечения кист влагалища?
Лечение кист влагалища только хирургическое - вылущивание кисты.
6.1.2. Кисты шейки матки
Каковы особенности кист шейки матки?
Кисты шейки матки по происхождению ретенционные, обычно имеют небольшие размеры - от 0,2 до
ретенционная киста - из гартнерова хода, при которой производят операцию вылущивания кисты, при этом следует помнить об опасности повреждения маточных сосудов и мочеточника, так как такая киста нередко проникает в широкую маточную связку.
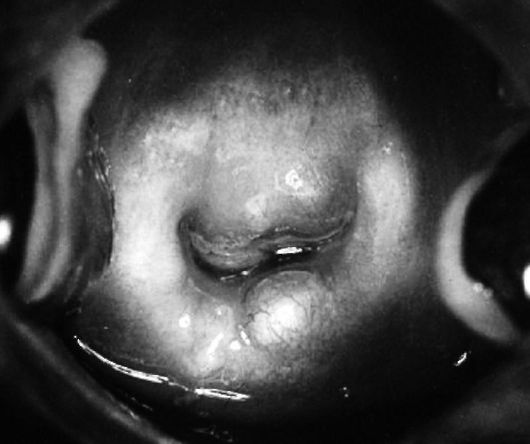
Рис. 6.4. Кисты шейки матки
Каковы методы лечения кист шейки матки?
При небольших размерах кист можно ограничиться наблюдением, при значительных размерах проводят крио- и лазердеструкцию, в настоящее время отдают предпочтение радиохирургическому методу.
6.1.3. Кисты маточных труб
Эти кисты практического значения не имеют. Нередко обнаруживаются во время операции на ампулярных отделах труб маленькие кисты - морганиевы гидатиды, которые происходят из остатков гартнерова хода. Удаляют их попутно при операциях на трубах и яичниках.
6.2. ДОБРОКАЧЕСТВЕННЫЕ ОПУХОЛИ И ОПУХОЛЕВИДНЫЕ ОБРАЗОВАНИЯ ЯИЧНИКОВ
Опухоли яичников - часто встречающаяся гинекологическая патология, занимающая второе место среди опухолей женских половых органов. Частота опухолей яичников, составляемая 6-11%, за последние 10 лет увеличилась до 19-25%. Большинство новообразований яичников являются доброкачественными. На их долю приходится около 75-87% всех истинных опухолей яичников. До 11% чревосечений, выполняемых в гинекологических стационарах, предпринимаются по поводу опухолей и кист яичников или их осложнений.
Какая классификация опухолей яичников
в настоящее время является общепризнанной?
С целью унификации диагнозов опухолей и патологических процессов яичников рекомендуется пользоваться классификацией, разработанной Международным комитетом ВОЗ (1977). Эта гистологическая классификация предусматривает деление опухолей внутри каждого гистологического типа на доброкачественные, пограничные и злокачественные формы.
В клинической практике наибольшее значение имеет классификация по Пфанненштилю (табл. 6.1).
Таблица 6.1. Классификация опухолей яичников по Пфанненштилю
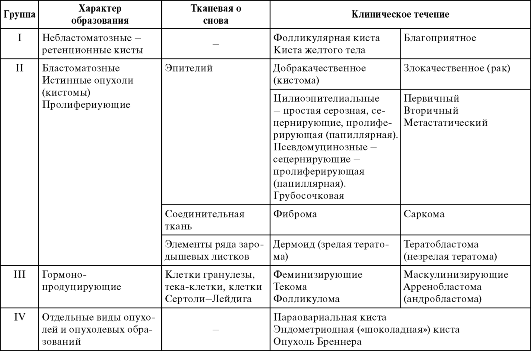
В клинической практике наибольшее значение имеют эпителиальные опухоли, опухоли стромы полового тяжа, герминогенные и метастатические опухоли.
Чем объясняется разнообразие опухолей яичников?
Многообразие опухолей яичников обусловлено тем, что в морфологическом отношении в строении яичника принимают участие следующие ткани:
- эпителиальная;
- соединительнотканная;
- нервная;
- сосудистая.
Кроме вышеперечисленных структур, основой опухоли яичника может быть эпителий, имплантируемый из матки, а также яйцеклетка, которая содержит элементы экто-, мезо- и эндодермы. Поэтому опухоли яичника могут быть смешанными.
6.2.1. Кисты яичников
Кисты яичников (лат. - cysta ovarii; англ. - ovarian cyst) преимущественно являются ретенционными. Они развиваются из фолликулов и желтых тел.
Какова этиология кист яичников?
Существуют две основные теории возникновения ретенционных кист яичников.
Первая теория объясняет их появление изменениями, связанными с воспалением придатков матки (51,6% случаев). Большое значение при этом имеют застойная гиперемия тазовых органов и развитие явлений периоофорита. Кроме того, гиперемия наблюдается в физиологических условиях в связи с менструальным циклом (овуляция, фаза развития желтого тела); с беременностью, родами, послеродовым периодом и лактацией; причинами могут быть прерванное половое сношение (coitus interruptus), ненаступление оргазма при выраженном половом возбуждении, а также опухоли матки (миома) в 34,2% случаев.
Вторая теория - гормональная - нарушение гормонального баланса в организме больной.
Каков патогенез возникновения кист яичника?
Развитие кист может происходить различными путями. В одних случаях имеют место нарушение соотношения между ЛГ и ФСГ, повышение ФСГ, нарушение овуляции при фолликулярных кистах (недостаток в организме лютеинизирующего гормона), а кисты желтого тела развиваются при избыточной продукции лютеинизирующего гормона гипофиза. В других случаях кисты возникают на фоне застойной гиперемии, в третьих - происходит утолщение белочной оболочки яичника, вследствие чего созревший фолликул не может вскрыться.
Что такое фолликулярная киста яичника?
Это однокамерное образование, возникшее вследствие того, что граафов фолликул не вскрылся, полость его наполняется прозрачной жидкостью, которая является продуктом жизнедеятельности гранулезных клеток (рис. 6.5).
Наличие фолликулярной кисты не нарушает процессов созревания яйцеклетки и овуляции в остальных фолликулах.
Какова клиническая характеристика кисты?
Фолликулярная киста наблюдается наиболее часто. При небольших размерах она бессимптомна, может достигать размера до
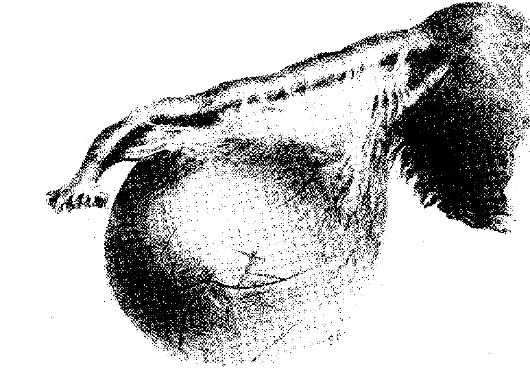
Рис. 6.5. Фолликулярная киста яичника
Каковы методы диагностики кист яичника?
Диагностика основана на данных бимануального исследования, УЗИ, лапароскопии, компьютерной томографии, РМР.
Каково лечение фолликулярной кисты яичника?
Лечение хирургическое. Производят резекцию яичника в пределах здоровых тканей, что особенно важно у женщин репродуктивного возраста (вылущивание кисты). В настоящее время эти операции проводят лапароскопическим методом.
Что такое киста желтого тела?
Кисты желтого тела (рис. 6.6) в отличие от фолликулярных встречаются значительно реже. Развитие их связано с тем, что после овуляции полость фолликула не спадается и не заполняется целиком лютеино- выми клетками, как это бывает в норме, а остается существовать и растягивается серозной жидкостью. Стенка кисты состоит из нескольких рядов лютеиновых и текалютеиновых клеток. По мере роста кисты происходит атрофия лютеиновых клеток и кистозных элементов внутренней стенки. Киста желтого тела гормонально неактивна.
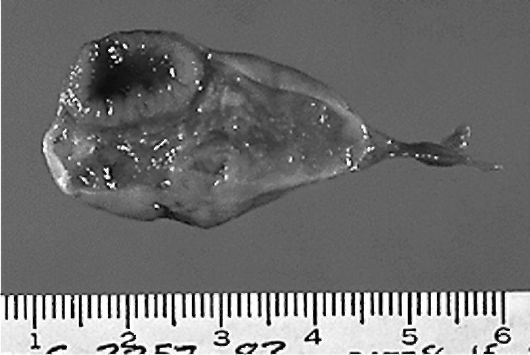
Рис. 6.6. Киста желтого тела яичника
Какова клиническая характеристика кисты желтого тела?
Киста обычно односторонняя, небольших размеров - 3-4 см в диаметре, тугоэластической консистенции, безболезненна. На разрезе отмечается фестончатость желтой или оранжевой окраски. Лютеиновая
ткань кисты претерпевает обычные для желтого тела циклические изменения. В связи с этим в фазе васкуляризации желтого тела возникают кровотечения в полость кисты. Как правило, киста появляется и увеличивается во 2-й фазе менструального цикла.
Какова симптоматика кисты желтого тела?
Возникают симптомы ранних сроков беременности - задержка менструации, нагрубание молочных желез; при влагалищном исследовании отмечают увеличение размеров матки, появление кровяных выделений из половых путей. На этом этапе необходимо проводить дифференциальный диагноз с беременностью, как маточной, так и внематочной. Уточняют диагноз при исследовании мочи на β-ХГЧ, который при кисте желтого тела не обнаруживается. Для постановки диагноза, как правило, достаточно бимануального исследования, УЗИ.
Какова тактика врача при обнаружении у больной кисты желтого тела?
Тактика выжидательная. Как правило, кисты желтого тела подвергаются обратному развитию. Если этого не наблюдается или имеется тенденция к увеличению кисты, показана операция, во время которой производят резекцию яичника в пределах здоровых тканей. Кисты желтого тела, как и фолликулярные, могут рецидивировать.
Каковы осложнения кист яичника?
К осложнениям кист яичника относятся перекрут ножки кисты, нагноение кисты, разрыв капсулы.
Прогноз при фолликулярных кистах и кистах желтого тела благоприятный.
Что такое текалютеиновые кисты?
Текалютеиновые кисты формируются под влиянием стимулирующего действия хорионического гонадотропина, содержащего большое коли- чество лютеинизирующего гормона, на текаткань фолликулов. Они двусторонние, достигают гигантских размеров, являются спутниками таких заболеваний, как болезни трофобласта. По мере лечения основного заболевания текалютеиновые кисты рассасываются и поэтому не подлежат хирургическому лечению.
6.2.2. Параовариальная киста
Параовариальная киста образуется из эпиофорона - надяичникова придатка (параовария), остатка мезонефрального протока.
Какова характеристика параовариальной кисты?
Киста чаще всего однокамерная, тонкостенная, располагается межсвязочно, содержимое прозрачное, жидкое, бедное белками, не содержит муцина. По объему параовариальная киста может быть от нескольких сантиметров в диаметре до размеров головки новорожденного. Форма шаровидная или овоидная (рис. 6.7). Яичник в патологический процесс не вовлекается, маточная труба чаще всего бывает распластана на поверхности кисты. Стенка параовариальной кисты состоит из соединительной ткани, внутренняя поверхность гладкая, выстлана однослойным цилиндрическим или плоским эпителием.
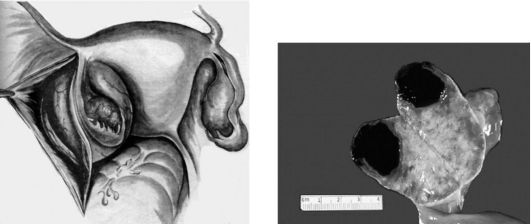
Рис. 6.7. Параовариальная киста
Каковы клиника и диагностика параовариальной кисты?
Встречается обычно в возрасте 20-30 лет и составляет около 10% всех опухолей и опухолевидных образований яичника. При небольших размерах киста никак не проявляется. При значительных размерах появляются симптомы - боль внизу живота и в крестце, дизурические явления. Развивается киста медленно, малигнизация исключительно редка. При бимануальном исследовании определяется кистозное обра-
зование, ограниченно подвижное вследствие интралигаментарного расположения. На нижнем полюсе кисты иногда удается пропальпировать яичник. Диагноз уточняют при ультразвуковом исследовании.
Каково лечение параовариальной кисты?
Лечение кисты хирургическое. Операция заключается в вылущивании кисты. Маточная труба и яичник сохраняются. Рецидивов параовариальной кисты не бывает. Прогноз благоприятный.
6.2.3. Доброкачественные опухоли яичников
Каков патогенез доброкачественных опухолей яичников?
Вопросы этиологии и патогенеза опухолей яичников являются дискутабельными, однако в настоящее время считается, что опухоли яичников относятся к полиэтилогичным заболеваниям. В патогенезе существенную роль играют изменения в гормональной, иммунной и эндокринной системах:
- в системе гипоталамус-гипофиз-яичники наблюдается угнетение секреции ЛГ в течение всего менструального цикла, ФСГ - в периовуляторный период и различное у всех больных изменение секреции эстрадиола;
- в системе протеолиза отмечена активация трипсино- и химотрипсиноподобных протеаз, лизосомальных протеаз.
В иммунной системе констатировано уменьшение общего содержания и функциональных способностей Т- и В-лимфоцитов.
В возникновении опухолей имеет значение также изменение чувствительности тканей к действию нормальных концентраций гормонов (патология рецепторного аппарата). Кроме того, снижение функции эпифиза может служить причиной возникновения гиперпластических процессов в яичниках.
Какие существуют факторы риска развития опухолей яичников?
В развитии опухолей яичников имеют значение некоторые факторы риска: генетическая предрасположенность, нарушение менструальной функции, бесплодие, раннее либо позднее наступление менархе, ран-
няя - до 45 лет или поздняя - после 50 лет менопауза, сопутствующие заболевания: миома матки, генитальный эндометриоз, хроническое воспаление придатков матки.
Что такое цистаденома (кистома) яичника?
Цистаденома (cystadenoma), или кистома - истинная опухоль яичника - объемное образование с выраженной капсулой, эпителиальной выстилкой; в отличие от кист яичников способна к пролиферации и бластоматозному росту (озлокачествлению).
Что такое «анатомическая» и «хирургическая» ножки опухоли?
В состав «анатомической» ножки входят собственная связка яичника, воронкотазовая связка, мезосальпинкс.
«Хирургическая» ножка - образование, которое приходится пересекать во время операции при удалении опухоли; в ее состав входят анатомическая ножка и чаще всего растянутая в длину маточная труба (рис. 6.8).
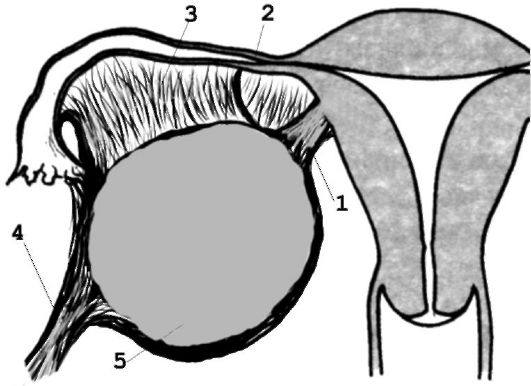
Рис. 6.8. «Анатомическая» ножка опухоли яичника: 1 - собственная связка яичника; 2 - маточная труба; 3 - дупликатура широкой связки; 4 - воронкотазовая связка; 5 - опухоль яичника.
Каковы основные жалобы больных с опухолями яичников?
Для опухолей яичников характерно длительное бессимптомное течение. Ведущий симптом при опухолях яичников - боли различной интенсивности внизу живота, реже выявляются нарушения менс-
труальной и детородной функций. При больших размерах опухоли увеличивается объем живота, нарушаются функций соседних органов (учащенное мочеиспускание, запоры), появляются отеки нижних конечностей. Наиболее яркая клиническая картина наблюдается при осложненном течении опухолей яичников: перекрут ножки опухоли, разрыв капсулы, нагноение, кровоизлияние в капсулу.
Клинические проявления гормонально-активных опухолей яичников обусловлены гиперэстрогенией либо гиперандрогенией (нару- шения менструального цикла, бесплодие, маточные кровотечения). Иногда опухоль обнаруживается больной или врачом при отсутствии каких-либо болезненных проявлений.
Какие существуют методы диагностики опухолей яичников?
Основными методами диагностики опухолей яичников являются двуручное гинекологическое и ректоабдоминальное исследования, дополнительными - проба с пулевыми щипцами, УЗИ (УЗИ должно осуществляться трансабдоминальным и трансвагинальным датчиками). В случаях, подозрительных на злокачественный процесс, эхографию целесообразно дополнять допплерометрией, которая позволяет в цвете выявлять сосудистое строение опухоли и определять особенности кровотока в сосудах, дифференцируя тем самым доброкачественный и злокачественный характер образования. Производят компьютерную томографию, магнитно-резонансную томографию, РО-тест (тест на опухолевый рост), определение уровня онкомаркеров (СА-125), лапароскопию, цитологическое исследование асцитической жидкости, полученной при пункции брюшной полости через задний свод влагалища, рентгенологическое и эндоскопическое обследование желудочно-кишечного тракта; урологическое обследование (цистоскопия, внутривенная урография); для решения вопроса о распространенности процесса при злокачественных опухолях применяют лимфо- и ангиографию.
С какой целью проводят обследование желудочнокишечного тракта у больных с опухолями яичников?
Обследование желудочно-кишечного тракта необходимо для исключения метастатического поражения яичников (опухоль Кру- кенберга).
С какими заболеваниями необходимо дифференцировать опухоли яичников?
Опухоли яичников в первую очередь дифференцируют от кист яичников, субсерозной миомы матки, воспалительных поражений придатков матки, дистопированной почки, опухолей кишечника, мочевого пузыря, от забрюшинных новообразований. Особо следует помнить об опухоли Крукенберга - метастатическом поражении яичника при первичном раке желудка: опухоль яичника часто выявляется до установления основного диагноза.
Какие существуют эпителиальные опухоли яичников?
К эпителиальным опухолям яичников относятся серозные, муцинозные, эндометриоидные, светлоклеточные, а также опухоли Бреннера.
Как классифицируют серозные опухоли яичников?
К серозным опухолям яичников относятся простая серозная цистаденома, папиллярная цистаденома и муцинозная цистаденома.
В чем заключаются особенности клинического течения простой серозной цистаденомы?
Простая серозная цистаденома (кистома) покрыта низким кубическим эпителием, расположена сбоку от матки или в заднем своде, чаще с одной стороны, овальной формы, тугоэластической консистенции, не достигает больших размеров, подвижна, с гладкой поверхностью, безболезненна. Внутренняя поверхность ее выстлана реснитчатым эпителием, напоминающим трубный. Из-за наличия ресничек их раньше обозначали как «цилиоэпителиальные» кисты. Встречаются у женщин всех возрастов, но чаще в 41-50 лет. Среди клинических симптомов довольно часто встречаются боли внизу живота и пояснице. Крайне редко данная опухоль озлокачествляется.
Каковы особенности папиллярной цистаденомы?
Реснитчатый эпителий, выстилающий внутреннюю поверхность капсулы, обладает склонностью к пролиферации и образованию мягких крошащихся сосочков. Эти разрастания напоминают цветную капусту. Иногда множественные сосочки заполняют всю полость (эндофитный рост) или прорастают через капсулу на наружную ее поверхность (экзофитный рост) (рис. 6.9). Опухоль заполнена серозным содержимым, располагается сбоку от матки, чаще двусторонняя, овальной формы,

Рис. 6.9. Папиллярная цистаденома
эластической консистенции, с гладкой поверхностью, обычно небольших размеров, подвижная, безболезненная, может сопровождаться асцитом. Часто перерождается в рак, так как клетки опухоли обладают большой степенью пролиферации.
Каковы особенности муцинозной цистаденомы?
Типичной формой для муцинозных опухолей является многокамерное образование круглой или овальной формы, бугристое, с различной толщиной стенок (рис. 6.10). Внутренняя поверхность капсулы выстлана эпителием типа цервикального, способным продуцировать характерное слизеобразное содержимое - муцин.
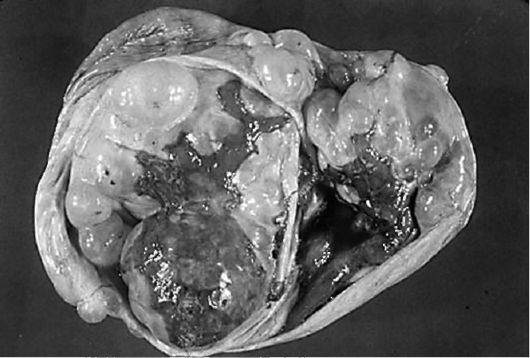
Рис. 6.10. Муцинозная цистаденома
Опухоль может достигать больших и даже гигантских размеров; описаны опухоли массой до
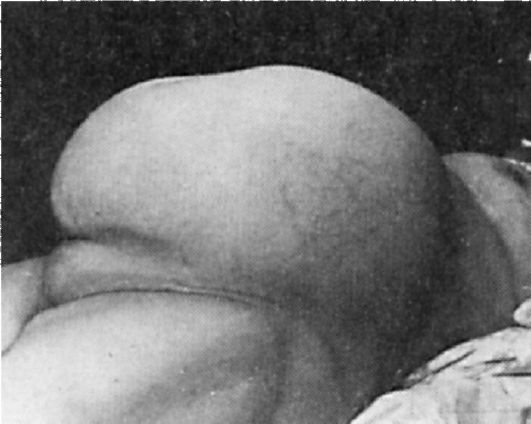
Рис. 6.11. Внешний вид больной с гигантской муцинозной цистаденомой яичника
Каков объем хирургического вмешательства при эпителиальных опухолях яичников?
Лечение опухолей яичников оперативное. Объем операций зависит от возраста больной и характера поражения. Особое значение для решения вопроса об объеме операции имеет срочное гистологическое исследо- вание, особенно в детском и подростковом возрасте.
При муцинозной цистаденоме у женщин до 40 лет удаляют придатки с одной стороны, у пациенток старше 40 лет - с обеих сторон.
При серозной цистаденоме объем операции заключается в удалении придатков матки. Папиллярная цистаденома вследствие выраженности пролиферативных процессов требует более радикальной операции. При поражении одного яичника в случаях, когда папиллярные разрастания располагаются лишь на внутренней поверхности капсулы опухоли, допустимо (в зависимости от возраста) удаление придатков пораженной стороны.
При поражении обоих яичников производят надвлагалищную ампутацию матки с придатками с обеих сторон. Если папиллярные разрастания обнаруживаются на поверхности капсулы, дополнительно резецируют сальник и в последующем назначают химиотерапию.
Что такое муциноматоз брюшины?
Муциноматоз брюшины (псевдомиксома брюшины) - это специфическое осложнение течения муцинозных опухолей яичников. Источниками муциноматоза брюшины чаще всего являются муцинозные цистаденомы и цистаденокарциномы, а также кисты или дивертикулы червеобразного отростка (рис. 6.12).

Рис. 6.12. Муцинозные массы, удаленные из брюшной полости при псевдомиксоме брюшины, возникшей в результате разрыва муцинозной цистаденомы
яичника
Псевдомиксома брюшины - тяжелое, трудно распознаваемое заболевание, по своей природе всегда являющееся результатом попадания слизи из какой-либо первичной опухоли, чаше всего новообразования яичника.
Что такое опухоль Бреннера?
Опухоли Бреннера встречаются довольно редко, в пределах 0,5% по отношению ко всем первичным опухолям яичников. Преобладают доброкачественные варианты, но встречаются и злокачественные формы. Наиболее распространен крупноклеточный солидный гормонально-неактивный вариант опухоли Бреннера. Все остальные
типы
опухоли Бреннера гормонально активны, что подтверждается появлением у
пожилых женщин гиперплазии эндометрия, дисгормональных пролифератов в
матке и молочных железах. Макроскопически опухоль Бреннера
разнообразна, ее размеры - от 2 до
Какие новообразования относятся к опухолям стромы полового тяжа?
К опухолям стромы полового тяжа относятся гранулезостромальные клеточные опухоли (гранулезоклеточная опухоль и группа теком-фибром) и андробластомы. Это гормонально-активные опухоли, которые по клиническому течению разделяются на феминизирующие (гранулезоклеточная и текома) и маскулинизирующие (андробластома).
Каковы клинические особенности феминизирующих опухолей в различные возрастные периоды жизни женщины?
Феминизирующие опухоли встречаются в любом возрасте: гранулезоклеточная - чаще у детей и молодых людей, текома - в пре- или постменопаузе. Гранулезоклеточная опухоль развивается из гранулезной ткани, сходной по строению с зернистым эпителием зреющего фолликула. Текома состоит из клеток, похожих на клетки тека, зреющих и атрезирующих фолликулов. Клинические проявления связаны с гормональной активностью этих опухолей. У девочек наблюдается клиническая картина преждевременного полового развития, появляются нерегулярные кровянистые выделения из половых путей при незначи- тельном развитии вторичных половых признаков; определяются признаки эстрогенного влияния - цианотичность вульвы, складчатость влагалища, увеличение матки, появление симптома «зрачка». У этих пациенток в то же время не отмечается ускорения соматического развития. Костный возраст, масса и рост соответствуют календарному.
В репродуктивном периоде наблюдается нарушение менструальной функции по типу дисфункциональных маточных кровотечений. Возникновение феминизирующих опухолей в пожилом возрасте
приводит к «омоложению» больной, появлению кровяных выделений из половых путей и признаков эстрогенного влияния. В эндометрии развивается железистая гиперплазия, а под влиянием длительной гиперэстрогении возможно возникновение рака эндометрия. Чаще эти опухоли расположены в боковом своде, односторонние, овальной формы, плотные, различных размеров - от горошины до головы взрослого человека, подвижные, безболезненные. Макроскопически гормонально-активные опухоли на разрезе имеют выраженную дольчатость и желтый цвет, очаговые кровоизлияния и некрозы.
Какой объем оперативного вмешательства выполняют у больных с феминизирующими опухолями яичников?
Лечение феминизирующих опухолей - только оперативное. Объем операции зависит от возраста больной, состояния второго яичника. Необходимо срочное гистологическое исследование удаленного пре- парата. У девочек при гранулезоклеточной опухоли удаляют только пораженный яичник, если нет поражения лимфатических узлов. Требуется тщательное наблюдение за девочкой: при малейшем росте второго яичника необходимо его удаление. У пациенток репродуктивного периода также надо стремиться к минимальному объе- му - удалению придатков пораженной стороны. В пожилом и старческом возрасте выполняют операцию в объеме надвлагалищной ампутации матки с придатками.
Что такое фиброма яичника?
Фиброма яичника - опухоль из соединительной ткани - относится к группе теком-фибром, редко встречающихся и не проявляю- щих гормональной активности (рис. 6.13). Поражается в основном контингент пожилых женщин, у которых такая опухоль вызывает асцит, иногда гидроторакс и анемию (синдром Мейгса; Joe Meigs, 1892-1966). Фибромы чаще всего односторонние, самой различной величины, плотной консистенции, округлой или овальной
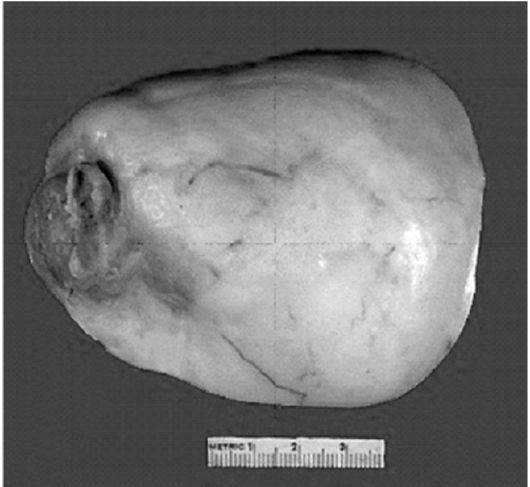
Рис. 6.13. Фиброма яичника
формы, на разрезе волокнистого строения, перламутрового вида; встречаются очаги обызвествления, отека, распада и кровоизлияний. Причина накопления жидкости в серозных полостях при фиброме окончательно не установлена.
Течение доброкачественное, лечение оперативное в объеме удаления придатков пораженной стороны.
Что характерно для андробластомы?
Андробластома - маскулинизирующая гормонпродуцирующая опухоль, содержащая клетки Сертоли-Лейдига (хилюсные и стромальные клетки) (рис. 6.14). Образующиеся при этом в избытке андрогены угнетают функцию гипофиза, и по принципу «обратной связи» в организме снижается выработка эстрогенов. Встречается у пациенток 20-35 лет. Основной клинический признак - дефеминизация: на фоне общего здоровья возникают аменорея, бесплодие, уменьшаются молочные железы, а затем возникают признаки омужествления: грубеет тембр голоса, появляется оволосение по мужскому типу, снижается либидо, уменьшается подкожная жировая клетчатка, возникает гипертрофия клитора, контуры тела и лица приобретают мужские черты. Симптомы развиваются постепенно.
Каковы клинические особенности течения андробластомы?
Клинические проявления в большей мере зависят от возраста. В возрасте до полового созревания опухоль встречается крайне редко и распознать ее очень трудно, так как симптомов дефеминизации при этом отметить не удается. В репродуктивном периоде пациентка обращается
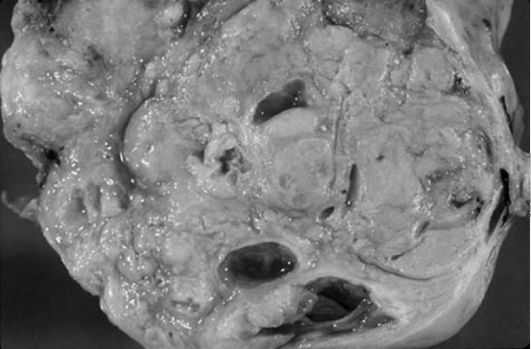
Рис. 6.14. Андробластома
к врачу, как правило, по поводу аменореи и бесплодия. В период климактерии и постменопаузы женщину редко беспокоят признаки дефеминизации, которые в большинстве случаев принимают за проявление возрастного характера, и лишь при возникновении симптомов маскулинизации пациентки обращаются к врачу. Опухоль растет медленно, поэтому больные годами являются носительницами такого образования, а более раннее обращение к врачу связано с болями внизу живота.
При
гинекологическом исследовании определяется опухоль, расположенная
сбоку от матки, односторонняя, овальной формы, плотная, небольших
размеров, подвижная, безболезненная. Величина опухоли варьирует от 2 до
Каков объем операции при андробластоме?
При андробластоме достаточно удалить опухоль в пределах здоровой ткани яичника у лиц репродуктивного возраста. У пациенток старшего возраста показано удаление придатков пораженной стороны. При злокачественном характере показана пангистерэктомия с резекцией сальника. После удаления опухоли функции организма женщины восстанавливаются в такой же последовательности, в какой развивались симптомы заболевания, хотя огрубение голоса, увеличение клитора и гирсутизм могут сохраниться на всю жизнь. Облик женщины меняется очень быстро. Восстанавливаются менструальная и репродуктивная функции. Прогноз в большинстве случаев благоприятный.
Какие существуют герминогенные опухоли?
Различают зрелые (доброкачественные) тератомы и незрелые (злокачественные) тератомы (тератобластомы), которые происходят из какого-либо или из всех трех зародышевых листков (эктодерма, мезодерма, эндодерма); в отдельную подгруппу выделяют дисгерминомы.
В чем заключаются особенности клинического течения зрелой тератомы?
Зрелая тератома (дермоидная киста) - одна из наиболее распространенных опухолей яичников в детском и юношеском возрасте (рис. 6.15). Эта опухоль встречается даже у новорожденных, что косвенно свидетельствует о тератогенном происхождении этих опухолей или их развитии из остатков эмбриональных тканей.

Рис. 6.15. Зрелая тератома
Зрелые тератомы располагаются обычно спереди и сбоку от матки, чаще они односторонние, округлой формы, неравномерной плотно- эластической консистенции, с гладкой поверхностью, редко достигают размеров больше 13-15 см в диаметре, безболезненны; за счет длинной «ножки» обладают повышенной подвижностью и склонностью к ее перекруту. Содержимое тератомы - сало, волосы, зубы, хрящ (ткани эктодермального происхождения).
Какой объем операции выполняют при зрелой тератоме?
Лечение зрелых тератом хирургическое - удаление придатков пораженной стороны; у девочек - резекция яичника в пределах здоровых тканей. Прогноз благоприятный. Злокачественное перерождение отмечается лишь в 1,7% наблюдений.
Что такое дисгерминома?
Дисгерминома - злокачественная опухоль, относящаяся к группе герминогенных (зародышевых) новообразований. Дисгерминома яичника аналогична семиноме яичка, развивается из половых клеток, не подвергающихся дифференцировке.
Дисгерминомы растут и метастазируют быстро, возраст пациенток молодой, чаще страдают инфантильные женщины с замедленным половым развитием и с признаками псевдогермафродитизма. Встречаются такие опухоли сравнительно редко, составляя от 0,6 до 5% случаев всех опухолей яичников.
Какова клиническая картина при дисгерминоме?
Жалобы больных неопределенные, иногда появляются тупые тянущие боли внизу живота, учащенное мочеиспускание, общее недомогание, слабость, сонливость. Девочки из резвых и шаловливых становятся вялыми и тихими. Отмечается быстрая утомляемость. Опухолевый рост сопровождается расстройством менструального цикла: длительная аменорея (4-6 мес.) может сменяться маточными кровотечениями. В незапущенных случаях картина крови обычно без особых изменений. При появлении распада в опухоли и быстром ее распространении возникает незначительное повышение вечерней температуры, уве- личивается СОЭ, в картине крови появляется сдвиг лейкоцитарной формулы влево.
При гинекологическом осмотре определяется опухоль, расположенная позади матки, чаще односторонняя (двусторонние опухоли встречаются в 8-12% наблюдений), округлой формы, плотная, бугристая, разнообразной величины (чаще достигает больших размеров); в начале развития опухоль подвижная, безболезненная. Дисгерминома характеризуется быстрым ростом, способностью к сращиваниям с прилежащими органами (маткой, петлями кишечника) и быстрому метастазированию в парааортальные лимфоузлы, в лимфоузлы по ходу нижней полой вены, околопочечные лимфоузлы и в отдаленные органы (легкие, мозг).
Прогноз при дисгерминомах различный. У детей они протекают более доброкачественно, чем у взрослых. «Чистые» формы дисгермином обладают высокой радиочувствительностью (рентгенотающие опухоли), поэтому полное излечение даже при наличии метастазов реально.
Какое лечение показано при дисгерминоме?
Лечение опухоли - только хирургическое с последующей лучевой терапией. При односторонней опухоли без признаков распространения за пределы пораженного яичника можно ограничиться удалением придатков. Во время операции необходимо очень бережное обращение с опухолью. Нарушение целости капсулы резко ухудшает прогноз заболевания.
При распространении опухоли за пределы одного яичника показана более радикальная операция - удаление придатков и матки с последующей рентгенотерапией. Как первичная опухоль, так и метастатические узлы хорошо поддаются рентгенотерапии. При правильном лечении возможно полное выздоровление.
Какие возможны осложнения
при доброкачественных опухолях яичников?
K числу осложнений при опухолях яичника относятся: перекрут ножки опухоли (рис. 6.16), разрыв капсулы, кровоизлияние в капсулу, злокачественное перерождение.
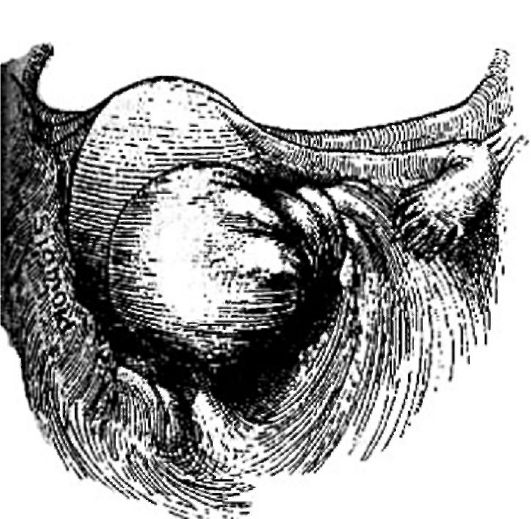
Рис. 6.16. Перекрут ножки опухоли яичника
Какова клиническая картина перекрута ножки опухоли яичника?
Больную беспокоят резкие боли внизу живота, тошнота, рвота, повышение температуры, лейкоцитоз крови, учащение пульса, парез и вздутие кишечника, напряжение мышц передней брюшной стенки; нередко начало заболевания связано с физической нагрузкой.
При гинекологическом исследовании в области придатков определяется опухолевидное образование, болезненное при пальпации и попытке его смещения.
Какое лечение применяют
при перекруте ножки кисты яичника?
Показано срочное оперативное лечение. Промедление может привести к некрозу кисты, кровоизлиянию в капсулу с последующим ее разрывом, нагноению и развитию перитонита.
Каким образом решается проблема улучшения репродуктивного здоровья женщин с опухолями яичников?
Улучшение репродуктивного здоровья женщин с опухолями яичников предусматривает трехэтапный подход к решению этой проблемы. 1-й этап - универсальная подготовка к оперативному лечению:
- исключение инфекционного агента (микробиологическое исследование); элиминация инфекта (бетадин, наксоджин), восстановление нормобиоценоза влагалища (эубиотики, актимель, дюфалак);
- оценка иммунореактивности организма (ЭЛИ-П-ТЕСТ), деблокирование иммунной системы, иммунокоррекция;
- гормональные исследования, ТФД, выявление нарушений и их возможная коррекция (дюфастон, регулон).
2-й этап- оперативное лечение:
- органосохраняющий принцип (резекция яичника, односторонняя аднексэктомия.
3-й этап:
- ранняя активизация (ЛФК, дыхательная гимнастика);
- профилактика послеоперационных осложнений;
- физиотерапия (СМТ, переменное магнитное поле, фонофорез лекарственными веществами);
- улучшение кровотока и метаболизма клеток, усиление фагоцитоза и ферментативной активности, улучшение процессов репарации;
- восстановление двухфазного менструального цикла (гормональная терапия);
- восстановление нарушений в системе гипоталамус-гипофиз- яичники;
- поддержка нормобиоценоза влагалища;
- иммуномодуляция (иммунотерапия, энзимотерапия);
- репродуктивное планирование (контрацепция).
Каковы особенности диагностики
и лечения опухолей яичников у девочек?
1. Быстрый рост опухоли, обусловленный активными обменными процессами растущего организма.
2. Отсутствие интралигаментарного расположения опухолей.
3. Редко встречающиеся двусторонние опухоли.
4. Асимметрия объема и функциональной активности правого и левого яичников.
5. Воспалительных изменений в малом тазу, которые часто сопровождают опухоли яичников у взрослых; у девочек, как правило, не бывает.
6. Наиболее распространенное осложнение - перекрут ножки опухоли.
Принципы лечения опухолей яичников те же, что и у взрослых женщин, но следует учесть ряд следующих обстоятельств.
1. При обнаружении опухоли яичника у девочек операция должна быть проведена незамедлительно.
2. Гистологическая экспресс-диагностика обязательна.
3. При морфологическом подтверждении доброкачественности патологического процесса операцию выполняют в объеме удаления опухоли в пределах здоровых тканей; операция максимально щадящая.
4. При злокачественном опухолевом процессе показаны оперативное вмешательство в объеме надвлагалищной ампутации матки с придатками и экстирпация большого сальника.
6.3. ПРЕДРАКОВЫЕ ЗАБОЛЕВАНИЯ НАРУЖНЫХ ПОЛОВЫХ ОРГАНОВ, ВЛАГАЛИЩА И ШЕЙКИ МАТКИ
Проблема предраковых заболеваний женских половых органов чрезвычайно важна. Пока точно не известны причины возникновения и механизмы развития злокачественных опухолей, поэтому действенную профилактику их можно проводить главным образом путем раннего выявления и лечения так называемых предраковых заболеваний.
Развитию злокачественных опухолей гениталий, как правило, предшествуют различные патологические состояния органов и систем, на фоне которых нередко развиваются злокачественные опухоли.
Впервые термин «предрак» был введен в
Понятие «предрак» хорошо объясняется теорией канцерогенеза, согласно которой предрак является одним из фазовых состояний в общем процессе канцерогенеза.
На какие две группы делят предраковые заболевания вульвы, влагалища и шейки матки?
Предраковые заболевания вульвы, влагалища и шейки матки делят на факультативные и облигатные.
Что относят к факультативным предраковым заболеваниям вульвы?
К этим заболеваниям относят:
- остроконечные кондиломы;
- крауроз;
- лейкоплакию.
Что такое остроконечные кондиломы?
Остроконечные кондиломы представляют собой бородавчатые выступы или их сливающиеся поверхности. Они имеют вирусную этиологию (отсюда англ. аббревиатура «HPV» - human papilloma virus), обычно встречаются в молодом возрасте, нередко проявляются и начинают расти во время беременности, а после беременности часто полностью исчезают спонтанно без лечения.
Что такое крауроз?
Крауроз (греч. krauros - сухой, хрупкий) представляет собой атрофический процесс многослойного плоского эпителия, который приводит к диффузной атрофии вульвы, полному исчезновению клитора, больших и малых половых губ со склерозированием входа во влагалище.
Что такое лейкоплакия?
Лейкоплакия (от греч. leukos - белый, plax, plakos - пластина) характеризуется гиперплазией эпителия в сочетании с лимфогистиоцитарной инфильтрацией подэпителиальной ткани. Выражается в появлении белесоватых сливающихся бляшек на клиторе, малых губах.
Каковы этиология и патогенез крауроза и лейкоплакии вульвы?
В основе крауроза и лейкоплакии лежат сложные нейроэндокринные и обменные нарушения, реализующиеся вегетоневротическими реак- циями. У больных часто снижается функция коры надпочечников, уменьшается количество кортикостероидов и эстрогенов в тканях вульвы, в результате чего изменяется гормонорецепция вульвы.
Чем характеризуется клиническое течение крауроза и лейкоплакии вульвы?
Заболевание начинается незаметно, в легких формах не сопровождается никакими симптомами и обнаруживается только при профилактических осмотрах. Лейкоплакия клинически часто сочетается с краурозом, но может быть и самостоятельным заболеванием. Симптомы заболевания сходны. Лейкоплакия и крауроз сопровождаются зудом вульвы преимущественно в ночное время, появляются парестезии (онемение, «ползание мурашек», чувство жжения). Продолжительный, многолетний зуд нередко бывает столь мучительным, что приводит к невротическим расстройствам (депрессия, повышенная раздражительность и даже суицидальные попытки), лишает больную сна, снижает трудоспособность. Появление столь мучительного зуда объясняется нарушением трофики тканей, разрастанием свободных нервных окончаний, лишенных глиального покрова. Упорный зуд приводит к расчесам, ссадинам, трещинам и в конечном итоге к воспалению вульвы.
Каковы методы диагностики крауроза и лейкоплакии вульвы?
Диагностика крауроза и лейкоплакии вульвы основывается на данных анамнеза (время появления зуда, его интенсивность, сопутствующие и предшествующие зуду заболевания, эффективность проводимого ранее лечения), соматического обследования больной. Обязательны повторные исследования мазков на флору из цервикального канала, влагалища и уретры. Осмотр желательно дополнить кольпоскопией, что позволяет более правильно оценить макроскопические изменения, выявить изменения, обусловленные инфекцией, выбрать участки, подозрительные на малигнизацию, для прицельной биопсии.
Какова кольпоскопическая картина при краурозе и лейкоплакии вульвы?
При краурозе слизистая оболочка имеет цвет от желтоватого до кирпичного. Проба Шиллера отрицательная или слабоположительная, что говорит об отсутствии гликогена в клетках поверхностного эпителия. На белесоватой или желтоватой поверхности хорошо видны капилляры в виде красной крапчатости.
Кольпоскопия лейкоплакии имеет характерную картину. Ороговевшая поверхность малопрозрачна; в зависимости от ее толщины лейкоплакия выглядит как простое белое пятно или образует
белую бугристую поверхность с отсутствием сосудов. Часто границы лейкоплакии имеют вид географической карты (т.е. четко очерченные, но неправильной формы). Проба Шиллера также отрицательная.
С какими заболеваниями следует проводить дифференциальный диагноз лейкоплакии и крауроза вульвы?
Дифференциальный диагноз проводят с патологическими процессами, имеющими сходную клиническую картину: красным плоским лишаем, кандидозом вульвы, витилиго, эссенциальным зудом, чесоткой и др.
Как лечить крауроз и лейкоплакию вульвы?
Крауроз и лейкоплакия имеют хроническое длительное течение. Показано местное применение гормональных средств, содержащих эстриол (овестин), в виде мазей, кремов, вагинальных свечей; мази с глюкокортикоидами - 1% и 2,5% гидрокортизоновая мазь, 0,5% преднизолоновая, фторокорт, синалар (синафлан, флюоцинолон ацетонид) и др., с ментолом и анестезином, с витамином А.
Применяют физиотерапевтические методы - ультразвук, который снижает возбудимость вегетативной нервной системы, блокирует проведение патологических импульсов, оказывает механическое (микро- массаж), рассасывающее и противовоспалительное действие на ткани, стимулирует функцию яичников. На курс - 15-20 процедур; фонофорез гидрокортизона на область вульвы, паховую и перианальную области (фибринолитический, трофический, вазотропный эффект).
В особо упорных случаях применяют спиртоновокаиновые блокады и оксигенотерапию. Спиртоновокаиновый раствор (100 мл 0,25% раствора новокаина и 30 мл 96% спирта) после предварительной анес- тезии кожи вводят в ишиоректальное пространство, где он блокирует патологические импульсы, улучшает трофику. Проводят 2-5 блокад с интервалом 1 нед.
Эффективным методом лечения дистрофических процессов наружных половых органов стала криотерапия (аэрозольный метод) и лазертерапия, которая не дает опасных кровотечений, при этом быстрее про- исходит заживление раны, яснее отграничивается очаг деструкции от окружающих тканей. Кроме того, используют радиоволновую пунктуру пораженных участков с последующими аппликациями 100% экстракта листа чайного дерева и удаление участков крауроза с помощью петлевой насадки аппарата «Сургитрон».
Что относят к истинным (облигатным) предраковым заболеваниям вульвы и чем они характеризуются?
К истинным (облигатным) предраковым заболеваниям вульвы относят дисплазию и лейкоплакию с атипией. Дисплазия вуль- вы - это атипия многослойного плоского эпителия вульвы с нарушением слоистости, но без включения в процесс поверхностного слоя и проникновения процесса через базальную мембрану. Различают дисплазию слабой, умеренной и тяжелой степени, а также локальную и диффузную.
Лейкоплакия вульвы с атипией - это гиперкератоз с атипией.
В чем состоит лечение дисплазии вульвы?
При выявлении локальной дисплазии в репродуктивном возрасте показаны иссечение в пределах здоровых тканей (лучше радиоволновым методом) для тотального гистологического исследования биоптата, криодеструкция или лечение газовым лазером (СО2), что позволяет получить хороший косметический эффект.
При диффузных формах дисплазии в репродуктивном периоде, а также при всех разновидностях дисплазии в пре- и постменопаузе методом выбора является простая вульвэктомия.
Вульвэктомия показана также в случае отсутствия эффекта от консервативного лечения и там, где не исключена возможность развития рака в измененных краурозом тканях.
Что относят к факультативным (фоновым) заболеваниям влагалища?
К факультативным заболеваниям влагалища относят:
- лейкоплакию;
- папиллому.
Что относят к облигатным (истинным) предраковым заболеваниям влагалища?
К таким заболеваниям относят дисплазию, которая в зависимости от выраженности патологических изменений в поверхностном пласте многослойного плоского эпителия делится на легкую, умеренную и тяжелую.
Каковы проявления и методы лечения фоновых и истинных предраковых заболеваний влагалища?
Клиническое течение вышеуказанных заболеваний, как правило, медленное. Чаще всего больные не предъявляют жалоб. Боли возникают при сочетании с воспалительными процессами. Выявляются эти заболевания чаще на профилактических осмотрах. Лечение лейкоплакии влагалища оперативное с последующим гистологическим исследованием материала. Наиболее целесообразна криотерапия. При дисплазии оптимальными современными методами лечения являются радиоволновая хирургия и криодеструкция.
Что относят к факультативным (фоновым) заболеваниям шейки матки?
К факультативным заболеваниям шейки матки относятся:
- истинная эрозия (травматическое или инфекционное поражение эпителия шейки матки, характеризующееся его локальным отсутствием);
- эктопия;
- эрозированный эктропион (выворот слизистой оболочки цервикального канала в результате рубцовой деформации шейки матки);
- лейкоплакия;
- полип.
Неправильным является проведение аналогии между эктопией и эрозией, так как имеются коренные различия в патогенезе этих двух состояний.
Что такое эктопия?
Смещение высокого цилиндрического эпителия на участок влагалищной части шейки матки за пределы наружного зева называется эктопией. Эктопия на шейке матки наблюдается у 10-15% женщин моложе 30 лет. Посттравматическая эктопия (эрозированный эктропион) возникает после травмы шейки матки в родах или во время аборта.
При физиологической эктопии у новорожденных, девочек и молодых женщин граница между высоким цилиндрическим и многослойным плоским эпителием располагается кнаружи от наружного зева. В период полового созревания под влиянием половых гормонов происходят
изменения в составных компонентах шейки с появлением на влагалищной ее части в области наружного зева высокого цилиндрического эпителия, что сопровождается образованием эктопии.
Как выглядит эктопия при осмотре шейки матки при помощи зеркал?
При осмотре невооруженным глазом эктопия имеет ярко-красный цвет, зернистую поверхность. Форма и величина эктопий различны. Они могут располагаться вокруг цервикального канала, реже - только на передней или задней губе шейки матки. Для эктопий характерны так называемые «контактные» кровотечения.
Эктопия может возникнуть на неизмененной и деформированной шейке матки. Последний вариант более опасен в смысле малигнизации из-за нарушения трофики тканей и иннервации.
Какова кольпоскопическая характеристика эктопии?
При кольпоскопии эктопия отличается по цвету и рельефу от слизистой оболочки, покрытой многослойным плоским эпителием. Она представляет собой гроздьевидные скопления мелких шаровидных или продолговатых сосочков насыщенного красного цвета. Ярко-красный цвет эктопии обусловлен просвечиванием многочисленных сосудов через однослойный цилиндрический эпителий. Иногда наблюдаются островки эктопии, окруженные многослойным плоским эпителием и изолированные от наружного зева. Картина эктопии хорошо выявля- ется при нанесении на ее поверхность раствора 3% уксусной кислоты, которая вызывает сокращение сосудов. При этом сосочки становятся более рельефными, бледными и стекловидными, напоминая гроздь винограда.
Обнаруживаются сосочковые разрастания, в которых видны сосудистые петли. Иногда более светлые овальные участки окружены темноокрашенным валом плоского или метапластически измененного эпителия (устья открытых желез). При возникновении репаративных процессов в псевдоэрозии наблюдается плоскоклеточная метаплазия.
Что такое метаплазия?
Метаплазия - замещение однослойного цилиндрического эпителия многослойным плоским эпителием (не путать с неоплазией!)
Какова цитологическая
и гистологическая картина эктопии?
При цитологическом исследовании часто обнаруживаются клетки плоского эпителия, иногда слущенные с поверхности эктопии клетки высокого цилиндрического эпителия (вытянутой формы с ядрами, расположенными у основания), а также единичные, отдельно расположенные ядра, эритроциты и лейкоциты.
При гистологическом исследовании различают железистые, папиллярные эктопии и эктопии с плоскоклеточной метаплазией.
Для железистой эктопии (псевдоэрозии) характерно наличие железистых образований в подэпителиальной ткани. Высокий цилиндрический эпителий выстилает ветвящиеся железистые ходы - «эрозивные» железы, вокруг которых нередко отмечается воспалительная инфильтрация.
При папиллярной эктопии строма разрастается с формированием сосочков различной величины, покрытых однослойным высоким цилиндрическим эпителием (рис. 6.17). В каждом сосочке содержится концевая сосудистая петля.
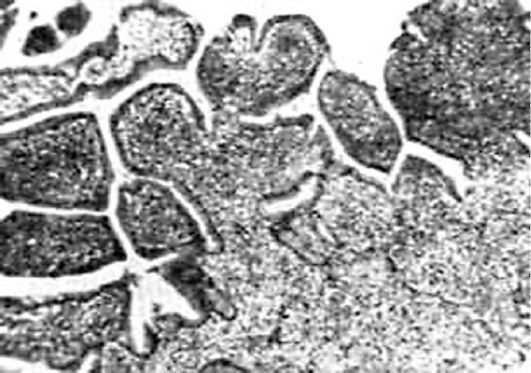
Рис. 6.17. Папиллярная псевдоэрозия
При заживлении эктопии на ее наружной поверхности и в «эрозионных» железах появляются резервные клетки, метапластически измененные клеточные элементы и образуется многослойный плоский эпителий. Замещение цилиндрического эпителия многослойным плоским - обязательный этап в течении эктопии.
Как происходит замещение эктопированного эпителия?
Замещение высокого цилиндрического эпителия может происходить двумя путями:
- за счет регенерации многослойного плоского эпителия с периферии;
- путем резервно-клеточной метаплазии, которая является преобладающей.
Что такое наботова киста?
Развитие наботовых кист связано с особенностями репаративного процесса, при котором метапластически измененный или многослойный плоский эпителий перекрывает устья открытых желез, что приводит к скоплению слизи в ветвящихся железистых ходах и образованию ретенционных кист. Размеры этих кист различные, чаще они мелкие, имеют вид желтоватых бугорков.
Что такое зона трансформации?
Зона трансформации - зона превращения, или зона перестройки, является признаком заживления эктопии и состоит из участков многослойного плоского эпителия, островков эктопии, открытых протоков желез, кистозно-расширенных желез, сосудов, островков многослойного плоского эпителия.
Какова кольпоскопическая картина зоны трансформации?
При кольпоскопии различают незаконченную и законченную зоны трансформации. Для незаконченной зоны трансформации характер- ны языковидные образования либо отдельные островки незрелого метапластически измененного эпителия белесоватого цвета с гладкой поверхностью, устья выводных протоков желез и остатки эктопии вокруг зева. При законченной зоне трансформации влагалищная порция шейки матки полностью покрыта многослойным плоским эпителием, под которым определяются железы и ретенционные кисты (ovula Nabothii).
Чем характеризуется цитологическая и гистологическая картина зоны трансформации?
При цитологическом исследовании незаконченной зоны трансформации обнаруживаются клетки всех слоев плоского эпителия и клеточные элементы метапластически измененного эпителия. При закон-
ченной зоне трансформации определяется цитологическая картина, характерная для слизистой оболочки неизмененной шейки матки.
При гистологическом исследовании законченной зоны трансформации поверхность шейки матки покрыта многослойным плоским эпителием, под которым располагаются железы различной формы и величины, включая кистозно-расширенные. В просвете желез содержится слизистый секрет, выводные протоки желез закрыты (закрытые железы).
Нередко можно наблюдать, как метапластически измененный плоский эпителий внедряется в просвет «эрозивных» желез и частично или полностью заполняет их просвет.
Каково лечение эктопии шейки матки?
Неосложненная эктопия шейки матки является вариантом нормы для девушек-подростков и молодых женщин в возрасте до 25 лет (так называемая врожденная эктопия шейки матки). Это, как правило, временное состояние шейки матки, не приводящее к малигнизации.
На фоне эктопии могут возникать патологические процессы шейки матки: экзо- и эндоцервициты, лейкоплакия шейки матки, плоские кондиломы, диспластическеи изменения. В этих случаях диагностику и лечение проводят по правилам для каждой нозологии.
Что такое лейкоплакия шейки матки?
Лейкоплакия - патологический процесс, характеризующийся ороговением поверхностных отделов многослойного плоского эпителия шейки матки.
Каковы этиология и патогенез лейкоплакии?
В этиологии лейкоплакии шейки матки принято выделять следующие группы факторов:
- эндогенные (нарушение гормонального гомеостаза, изменения иммунного статуса);
- экзогенные (инфекционные, химические, травматические).
Возникновению лейкоплакии шейки матки у женщин репродуктивного возраста предшествуют перенесенные воспалительные процессы матки и придатков на фоне нарушения менструальной функции по
типу олигоменореи у 35,5% больных и по типу неполноценной лютеиновой фазы цикла - у 65%.
Большую роль в возникновении лейкоплакии шейки матки играют также химические и травматические воздействия. Доказано, что более 2/ больных лейкоплакией шейки матки ранее получали интенсивное и неадекватное медикаментозное лечение по поводу псевдоэрозии шейки матки, а 33% пациенток с клинически выраженной лейкоплакией ранее перенесли диатермокоагуляцию.
Таким образом, к группе риска по возникновению лейкоплакии шейки матки следует относить пациенток с нарушениями менструального цикла, перенесенными воспалительными заболеваниями половых органов, рецидивирующими эктопиями (псевдоэрозиями) шейки матки в анамнезе.
Какова клиника лейкоплакии шейки матки?
В большинстве случаев жалобы отсутствуют. Лишь незначительное число женщин предъявляют жалобы на обильные бели и контактные кровянистые выделения.
На чем основывается диагностика лейкоплакии шейки матки?
Диагностика лейкоплакии шейки матки включает клинические, кольпоскопические, цитологические и морфологические методы. Наиболее информативными являются расширенная кольпоскопия и морфологические методы исследования. Перспективны исследования ВПЧ (Digene-test: определение суммарного количества онкогенных штаммов более 104).
Что позволяет уточнить расширенная кольпоскопия?
Расширенная кольпоскопия позволяет уточнить размеры и характер лейкоплакии, оценить состояние покровного эпителия влагалищной части шейки матки.
Что является основным методом диагностики лейкоплакии шейки матки?
Основной метод диагностики лейкоплакии шейки матки - морфологическое исследование биоптата. Для качественного его выполнения необходимо применять прицельную ножевую биопсию под контролем кольпоскопии из пораженных участков шейки матки. Более опти-
мальным является удаление всего патологически измененного участка радиоволновым ножом, что позволяет провести серийное гистологическое исследование всех удаленных тканей.
Одновременно с биопсией производят выскабливание слизистой оболочки цервикального канала. Необходимость ревизии цервикального канала обусловлена тем, что патологический процесс может развиться не только на влагалищной части шейки матки, влагалище и вульве, но и в участках плоскоклеточной метаплазии слизистой оболочки цервикального канала.
Чем характеризуется морфологическая картина лейкоплакии шейки матки?
Для морфологической картины этого заболевания характерны:
- утолщение покровного эпителия, в основном за счет увеличения числа клеток шиповидного слоя с сохранением их комплексности; оно может быть обусловлено акантозом - погружением эпителиальных пластов в подэпителиальную соединительную ткань;
- наличие рогового слоя на поверхности эпителия, который в норме отсутствует;
- наличие зернистого слоя, который расположен под роговым и представлен 2-3 рядами клеток, цитоплазма которых заполнена умеренным количеством базофильных гранул;
- рассеянная или очаговая лимфоидная инфильтрация подэпителиальной соединительной ткани.
Как лечить лейкоплакии?
Основной принцип лечения - удаление лейкоплакии в пределах здоровой ткани. Удалить ее можно, применив диатермокаутеризацию, криогенное воздействие, радиоволновую эксцизию, высокоинтенсивное лазерное излучение. Наиболее эффективны два последних метода.
Следует подчеркнуть, что при сочетании лейкоплакии шейки матки с воспалительными процессами вульвы и влагалища различной этио- логии сначала необходимо устранить воспалительный процесс.
Одним из наиболее современных и эффективных методов лечения лейкоплакии шейки матки является применение высокоинтенсивного лазера. Достоинством СО2-лазера является его способность бескон- тактно, безболезненно, асептично, бескровно испарять, сжигать и коагулировать патологические ткани, образуя на раневой поверхности
тонкую коагуляционную пленку, препятствующую проникновению инфекции в подлежащие ткани.
Как правило, лазеркоагуляцию проводят амбулаторно без предварительного обезболивания в первой половине цикла (на 4-7-й день).
Достоинством радиоволновой эксцизии является прежде всего онкобезопасность: всю иссеченную ткань подвергают гистологичес- кому исследованию; второе преимущество - отсутствие ожоговых изменений в подлежащих тканях - «холодная» резекция радиоволной не оставляет «угольного» струпа, заживление происходит под тонкой фибриновой пленкой.
Какова этиология полипа цервикального канала?
Причины возникновения полипов до конца не установлены. Определенную роль в их образовании играют гормональные наруше- ния, воспалительные процессы слизистой оболочки цервикального канала.
Какова характеристика полипов цервикального канала?
Полипы эндоцервикса редко бывают множественными, обычно они одиночные. Величина и форма их разнообразны: преимущественно они небольшие (диаметр 0,2-0,4 см), овальные или круглые, реже языкообразной или гроздьевидной формы, свисают во влагалище. Поверхность полипов гладкая, консистенция мягкая, но может быть и более плотной, что обусловлено большим содержанием фиброзной ткани. При осмотре в зеркалах полипы обнаруживают в области наружного зева, они хорошо видны невооруженным глазом. Полипы имеют темно-розовый цвет, что обусловлено просвечиванием сосудов через покровный цилиндрический эпителий. При нарушении кровообращения они могут принимать темно-фиолетовую окраску. Реже поверхность полипа бывает белесой, что связано с нахождением на ней плоского многослойного эпителия. Основание полипов представляет собой тонкую либо широкую ножку.
Каковы методы лечения полипа цервикального канала?
Лечение полипа состоит в его удалении (полипэктомия) с последующим раздельным выскабливанием слизистой цервикального канала и стенок полости матки. Уменьшение числа рецидивов достигается эндоско- пическим контролем (цервикоскопия, гистероскопия) и коагуляцией ножки полипа одним из методов.
Что такое эктропион шейки матки
и какова его клиническая характеристика?
Под эктропионом понимают выворот слизистой оболочки цервикального канала, возникший вследствие травмы шейки матки в родах. Реже эта травма наблюдается во время аборта.
При эктропионе больные в основном жалуются на бели, боли в пояснице и внизу живота, нарушение менструальной функции в виде меноррагий, обусловленных, как правило, сопутствующими, хроническими эндоцервицитом и эндометритом.
Диагностика деформации шейки матки нетрудна, однако выворот слизистой оболочки цервикального канала иногда расценивают как псевдоэрозию и проводят неадекватное лечение.
Наиболее эффективным методом лечения эктропиона шейки матки является реконструктивно-пластическая операция методом расслоения по В.И. Ельцову-Стрелкову, восстанавливающая анатомию шейки матки до внутреннего зева.
Какова техника реконструктивно-пластической операции методом расслоения по В.И. Ельцову-Стрелкову?
1-й этап операции (рис. 6.18, А). Рассечение влагалищной части шейки матки до внутреннего зева. Шейку матки обнажают при помощи зеркал, фиксируют за переднюю и заднюю губы пулевыми щипцами и максимально низводят. Иссекают рубцовую или патологически измененную ткань, расположенную на боковых стенках шейки матки. В результате этого шейка матки разделяется на передний и задний лоскуты.
2-й этап операции
(рис. 6.18, Б). Расслоение шейки матки. Острым путем производят
расслоение переднего лоскута шейки матки от наружного зева параллельно
продольной оси до внутреннего зева. Получают два листка - внутренний и
наружный. При гипертрофии или цервикозе шейки матки одновременно
иссекают измененные ткани. Верхний листок отсепаровывают так, чтобы
слизистая оболочка канала шейки матки вместе с мышечным слоем была
толщиной не менее 5-
3-й этап операции (рис. 6.18, В). Формирование канала шейки матки. Внутренние листки, т.е. слизистую цервикального канала с мышечным слоем, формируют так, чтобы после их сшивания образовался цервикальный канал веретенообразной формы с внутренним
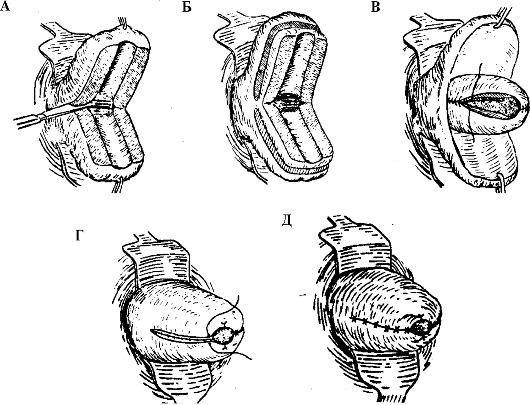
Рис. 6.18. Этапы реконструктивно-пластической операции методом расслоения по В.И. Ельцову-Стрелкову (А-Д, пояснения в тексте)
зевом диаметром 3-4 мм. Листки соединяют друг с другом отдельными швами таким образом, чтобы узлы были погружены в просвет вновь сформированного канала шейки матки.
4-й этап операции (рис. 6.18, Г). Формирование наружного зева. На данном этапе операции наружные листки слизистой влагалищной порции шейки матки подшивают к вновь сформированному каналу в области наружного зева соответственно на 12 и 6 ч по циферблату. Боковые поверхности наружных листков слизистой влагалищной порции шейки матки соединяют между собой на 3 и 9 ч по циферблату отдельными швами, после чего заканчивают формирование наружного зева шейки матки.
5-й этап операции (рис. 6.18, Д). Окончательное формирование шейки матки. На края разрезов накладывают отдельные швы так, чтобы края слизистой были хорошо кооптированы. Шейка матки приобретает коническую или субконическую форму с округлым наружным зевом.
Что относят к истинным (облигатным) предраковым заболеваниям шейки матки?
К истинному предраку шейки матки относят дисплазию; более правильным считают термин «цервикальная интраэпителиальная неоплазия» (cervical intraepithelial neoplasia - CIN) с выделением трех степеней тяжести: I и II степени соответствуют легкой и умеренной дисплазии, III степень включает одновременно тяжелую дисплазию и преинвазивную карциному.
Каковы этиология и патогенез истинного предракового заболевания шейки матки?
В возникновении истинного предракового состояния шейки матки большое значение придается родовой травме либо травме после аборта. У больных этой группы нарушается трофика тканей и иннервации, у каждой седьмой женщины рак шейки матки возникает на фоне травмы, резкой деформации шейки [Серебров А.И., 1962]. Известно, что в основе всех злокачественных опухолей лежит сочетание дегенеративных и регенеративных процессов, вызванных хроническим воспалением, дистрофией, травмой, застойными явлениями.
Какие факторы имеют значение
в возникновении патологии шейки матки?
Важную роль в развитии истинного предракового заболевания играют гормональные нарушения. У больных с предопухолевыми заболеваниями шейки матки повышается гонадотропная функция, нарушается метаболизм эстрогенов с преобладанием содержания эстрадиола.
В возникновении патологии шейки матки большое значение имеет фактор смегмы у сексуального партнера. Установлено, что смегма, накапливающаяся под крайней плотью, содержит канцерогенные вещества, и при недостаточной опрятности полового партнера она попадает на шейку матки женщины. В мусульманских странах, где принято совершать обрезание крайней плоти, раком шейки матки болеют значительно реже, чем в христианских.
В развитии предраковых и раковых заболеваний шейки матки играют роль инфекционные процессы, вызванные вирусом герпеса типа 2 и особенно вирусом папилломы человека (см. главу 5).
Возникновение и развитие опухолевых процессов в значительной степени связано также с нарушениями в системе иммунной защиты. В противоопухолевой защите важную роль играют естественные проти-
воопухолевые антитела, обладающие цитотоксическими свойствами. Определенный интерес представляет взаимосвязь между микробиоценозом влагалища и состоянием эпителия слизистой оболочки шейки матки. С одной стороны, существуют данные о возможном участии в патогенезе неоплазии шейки матки вирусов, хламидий, простейших и неспецифической бактериальной флоры. С другой стороны, патологически измененный эпителий приводит к нарушению одного из физиологических барьеров, обеспечивающих инфекционную резистентность.
Развитие предопухолевых заболеваний шейки матки может быть связано с некоторыми профессиональными факторами. Так, у женщин, работающих в горнорудной и нефтеперерабатывающей промышленности, на табачном производстве, эти заболевания встречаются гораздо чаще.
В возникновении предрака и рака шейки матки определенную роль играют наследственные факторы. Риск заболевания шейки матки у женщин с семейной отягощенностью в 1,6 раза выше по сравнению с женщинами без этой предрасположенности.
Какова клиника дисплазии?
Дисплазия шейки матки не имеет клинических проявлений, особенно если она возникает не на фоне эктопии (псевдоэрозии), лейкоплакии, а на визуально непораженной шейке матки. Иногда первым сигналом о наличии предрака или начальной стадии рака шейки матки могут быть данные цитологического исследования содержимого влагалища и цервикального канала (англ. Pap-smear test).
У молодых женщин диспластические изменения эпителия отмечаются преимущественно на влагалищной части шейки матки, особенно в зоне трансформации, после 40 лет - в цервикальном канале, при этом патологический процесс может быть изолированным или с одновременным поражением и влагалищной части шейки матки.
Какие женщины относятся к группе риска по развитию истинного предракового заболевания шейки матки?
К группе риска относятся:
- больные с хроническими воспалительными заболеваниями влагалищной части шейки матки и цервикального канала;
- женщины, которым ранее проводили лечение влагалищной части шейки матки (консервативное, тот или иной вид коагуляции, хирургическое лечение);
- больные, у которых возник рецидив заболевания;
- больные со старыми разрывами шейки матки;
- женщинысзаболеваниями,сопровождающимисягормо-нальны- ми нарушениями.
Каковы методы диагностики дисплазии шейки матки?
Для своевременной диагностики предраковых заболеваний необходимо использовать возможности комплексного обследования больной. Комплексное обследование женщин с целью выявления предраковых заболеваний шейки матки включает сбор анамнеза, выявление жалоб, оценку общего статуса больной, осмотр влагалищной части шейки матки, бимануальное, бактериоскопическое и бактериологическое исследование, а также целый ряд дополнительных методов исследования: кольпоскопию, цитологическое исследование мазков с поверхности шейки матки и из цервикального канала, пробы Шиллера или Деражне (прижизненная окраска слизистой оболочки шейки матки гематоксилином, при этом нормальный многослойный плоский эпителий окрашивается в нежно-фиолетовый цвет, а опухолевые очаги - в синий). CIN может быть обнаружена как при исследовании визуально неизмененной шейки матки, так и сочетаться с фоновыми ее заболеваниями, чаще всего с эктопией (псевдоэрозией).
На что следует обращать особое внимание при сборе анамнеза?
Собирая анамнез, необходимо уточнить следующие данные: число беременностей (родов, абортов), течение послеродового периода, осложнения после абортов, наличие родовой или послеабортной травмы и восстановление шейки матки, гинекологические заболевания и методы их лечения (особое внимание обращают на перенесенные заболевания влагалищной части шейки матки), обследование, проведенное ранее для уточнения диагноза, характер и длительность лечения (применение мазевых тампонов, прижигающих медикаментозных средств, диатермокоагуляции и других методов лечения), наличие гормональных нарушений, продолжительность заболевания, характер лечения и его эффективность, а также наличие или отсутствие рецидивов после лечения.
Что можно наблюдать при осмотре шейки матки при помощи зеркал?
У одних больных можно наблюдать очаговую гиперемию («красное пятно»), неравномерную окраску, местами белесоватую, с шероховатой поверхностью (преимущественно на передней губе) либо эктопию различной величины, у других - неизмененную влагалищную часть шейки матки, поскольку дисплазия локализуется в слизистой оболочке цервикального канала.
Какие дополнительные методы исследования применяют при подозрении на CIN?
Дополнительными методами являются цитологическое исследование поверхностного соскоба с шейки матки и из цервикального канала, расширенная кольпоскопия, прицельная биопсия.
Какова кольпоскопическая картина дисплазии шейки матки?
Необходимо отметить определенные трудности кольпоскопической диагностики диспластических изменений шейки матки, так как кольпоскопическая картина весьма разнообразна. Характерный признак дисплазии - наличие атипической зоны трансформации. В понятие «атипическая зона трансформации» включают различные сочетания кольпоскопических картин атипического эпителия (лейкоплакия, основа лейкоплакии с образованием полей, немые йоднегативные, ацетобелые участки). Кольпоскопическая картина атипического эпителия характеризуется нарушением гликогенообразования и возникновением дискератозов. На фоне зоны трансформации с открытыми и закрытыми железами, эпителиального пласта неравномерной толщины имеются различные сочетания лейкоплакии, ее основы, немых йоднегативных участков. На фоне атипической зоны трансформации могут наблюдаться дисплазия, преинвазивная карцинома и инвазивный рак. Для диагностирования предраковых состояний шейки матки может быть использована и кольпомикроскопия.
Какова цитологическая картина шеечных мазков при дисплазии шейки матки?
Цитологическое исследование шеечных мазков характеризуется наличием клеток с дискариозом. В зависимости от выраженности увеличения ядерно-цитоплазматического соотношения и других структурных изменений (форма ядер, содержание и распределение хроматина, вклю-
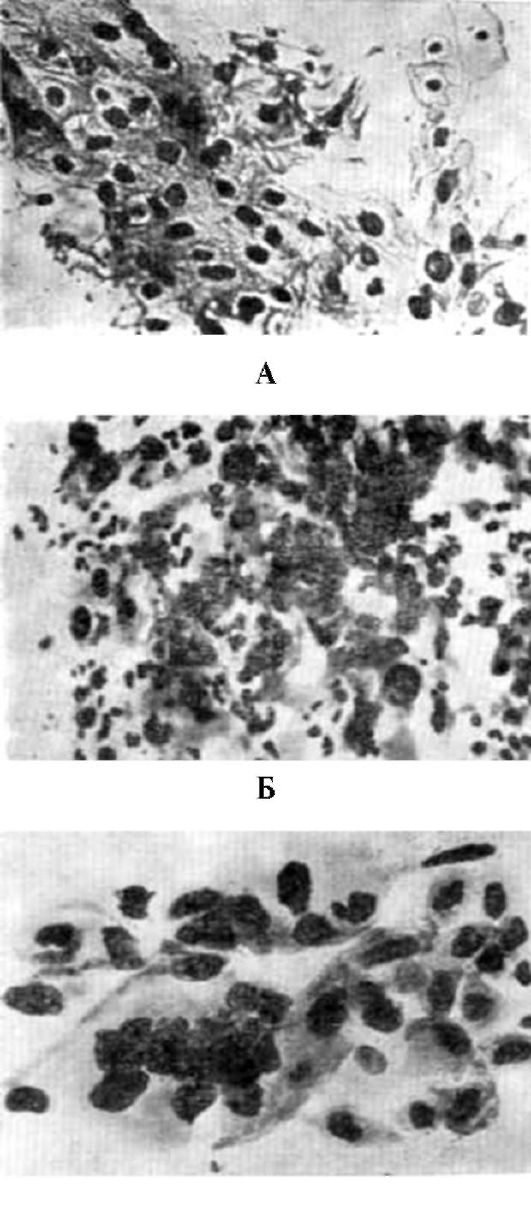
Рис. 6.19. А - слабая дисплазия, Б - умеренная дисплазия, В - тяжелая дисплазия
чения в цитоплазме) различают 3 степени дискариоза - легкую, умеренную и тяжелую, при этом считается, что клеточные элементы с легким и умеренным дискариозом свойственны соответственно легкой и умеренной дисплазии, с тяжелым дискариозом - тяжелой дисплазии, а также преинвазивной карциноме (рис. 6.19 А, Б, В). При исследовании мазков с поверхности влагалищной части шейки матки при легкой дисплазии отмечаются преимущественно пролиферация клеток базального и парабазального слоев, единичные клеточные элементы с признаками дискариоза.
Какова морфологическая картина дисплазии шейки матки?
Для дисплазии характерно изменение размеров и формы клеток и ядер: их гиперхроматизм, усиление митотической активности, включая увеличение числа и расширение спектра патологических митозов, нарушение ядерно-цитоплазматического соотношения, акантоз, инфильтрация лимфоцитами и гистиоцитами в сочетании с патологическим ангиогенезом в подэпителиальной строме. Процессы дезорганизации ткани стромы возникают уже на ранних стадиях неопластического процесса и прогрессируют по мере усиления тяжести патологии, происходят снижение содержания гликопротеидов в структурах базальной мембраны, деполяризация гликозаминогликанов, усиление функциональной активности фибробластов, уменьшение миграции тучных клеток, а также угнетение синтеза гепарина.
При CIN I степени тяжести (легкая дисплазия) изменения наблюдаются в нижней трети эпителия, при CIN II (умеренная диспла- зия) - в нижних двух третях эпителия, при CIN III (тяжелая дисплазия и преинвазивная карцинома) - почти во всем или во всем эпителии.
В чем заключается лечение CIN?
Лечение должно быть радикальным и, по возможности, бережным - радиоволновая, электроэксцизия шейки матки или ее ножевая ампутация.
Гистерэктомию выполняют только при наличии сопутствующих заболеваний, например при миоме матки.
Какова тактика врача после проведенного лечения?
После лечения требуется контроль, который заключается в повторном цитокольпоскопическом обследовании больной через 1,5-2 мес. после операции. Диспансерное наблюдение осуществляют в течение 3 лет после проведенного лечения. С диспансерного учета больную можно снять только при условии полной эпителизации шейки матки неизмененным плоским эпителием.
Каковы исходы CIN?
Дисплазия эпителия шейки матки является пограничным состоянием, способным к регрессии, стабилизации и прогрессии - переходу в преинвазивный или инвазивный рак.
В чем состоит профилактика рака шейки матки?
Для успешной профилактики рака шейки матки необходимы массовые и регулярные осмотры женщин старше 20 лет с их обязательным цитологическим обследованием (Pap-smear test) и радикальным лечением выявленных патологических процессов.
6.4. МИОМА МАТКИ
Что такое миома матки?
Миома матки - доброкачественная опухоль, относится к стромальным опухолям, которые образуются в результате гипертрофии и пролиферации элементов соединительной и мышечной ткани. Миома матки является опухолью моноклонального происхождения. Опухоль растет
как генетически аномальный клон клеток, происходящих из одной первичной клетки, которая в результате произошедшей в ней мутации приобрела способность нерегулированного роста. Факторы, запускающие этот механизм, передаются только потомкам, поэтому множественные миомы в одной матке клонально не связаны, что обусловливает и различный темп роста миоматозных узлов.
Как часто встречается миома матки среди гинекологических больных?
Результаты популяционных исследований свидетельствуют о том, что миома встречается у 15-17% женщин старше 30 лет - до постменопаузы. В постменопаузе, как правило, происходит обратное развитие опухоли. Среди гинекологических больных миома матки наблюдается у 10-27%, а при профилактических осмотрах эту опухоль впервые выявляют у 1-2,5% женщин. В гинекологических хирургических стационарах оперативное вмешательство по поводу миомы матки производят более чем у 50% больных.
Изучение преморбидного фона этих больных показывает, что все они в детстве перенесли много различных инфекций. Почти 1/3 больных с миомой перенесли ранее воспаление придатков матки. Генеративная функция снижена: половина больных страдают первичным бесплодием или имеют малое число беременностей. Менструальный цикл при миоме матки может быть овуляторным. Такие женщины беременеют и рожают, но у многих отмечают ановуляцию или неполноценность второй фазы цикла. Бесплодие может быть обусловлено также расположением узлов в трубных углах матки. Нередки привычные выкидыши.
Какие факторы риска способствуют возникновению миомы матки?
В настоящее время к основным факторам риска, способствующим возникновению миомы матки, относят: позднее менархе, обильные менструации, высокую частоту медицинских абортов, наличие экстрагенитальной патологии (особенно сердечно-сосудистой) и гинекологических заболеваний. Кроме того, при оценке риска возникновения миомы матки прослеживается генетическая предрасположенность к развитию данного заболевания
Каковы основные причины возникновения миомы матки?
Вопрос о причинах возникновения миомы матки до настоящего времени окончательно не решен. Патогенез миомы матки остается спорным и вызывает много вопросов.
Одно из центральных мест в проблеме патогенеза миомы матки занимает вопрос об особенностях гормонального статуса и функциональном состоянии репродуктивной системы по мере развития заболевания.
До настоящего времени существует традиционное мнение о ведущей роли эстрогенов в патогенезе миом. Уменьшение объема миоматозных узлов и значительное снижение содержания рецепторов эстрогенов в миометрии и тканях миомы после длительного лечения агонистами гонадолиберина подтверждают это мнение.
Развитие и рост миомы во многом обусловливаются состоянием рецепторного аппарата матки. Нарушение рецепторного аппарата могут способствовать изменения характера роста опухоли (быстрый, медленный).
У больных с миомой матки наблюдаются выраженные изменения гемодинамики малого таза, что является одним из факторов, способствующих более благоприятному развитию опухоли.
В генезе миомы матки играют роль изменения иммунологической реактивности организма, особенно при наличии хронических очагов инфекции.
Какие факторы играют роль в развитии миомы матки?
Таким образом, патогенез миомы матки очень сложен. В развитии заболевания играют существенную роль нарушения гипоталамо-гипофизарной системы, функции яичников, надпочечников, щитовидной железы.
По мере развития миомы матки на первый план начинают выступать более глубокие нарушения функции многих эндокринных желез, играющих важную роль в развитии этой опухоли.
В патогенезе миомы матки важная роль отводится нарушениям функции яичников, подтверждением чему служат обнаруженные мелкокистозные изменения яичников у 50-60% женщин в этой группе больных.
Как классифицируют миому матки?
Опухоль возникает межмышечно, затем в зависимости от направления роста развиваются интерстициальные - интрамуральные, межмышечные (в толще стенки матки), подбрюшинные (субсерозные), растущие в сторону брюшной полости, и подслизистые, растущие в сторону слизистой оболочки матки, узлы опухоли. Вокруг миоматозного узла образуется капсула из мышечных и соединительнотканных элементов стенки матки. Капсула подбрюшинных узлов образована также за счет брюшинного покрова матки. Подслизистые узлы имеют капсулу из мышечного слоя и слизистой оболочки матки.
Подслизистые узлы встречаются примерно у каждой десятой больной с миомой матки. Эти формы опухоли различаются не только клинически, но также морфологически и гистохимически. В подслизистых узлах активность обменных процессов выше, что обеспечивает более быстрый их рост.
Наиболее часто (80%) встречаются множественные миомы матки с различным числом и расположением узлов неодинаковой величины и формы. Значительно реже имеют место одиночные подбрюшин-
ные или интерстициальные узлы. Миоматозные узлы, располагающиеся ближе к внутреннему зеву матки, могут расти по направ- лению к боковой стенке малого таза, располагаясь между листками широкой связки - интралигаментарно (рис. 6.20, 6.21).
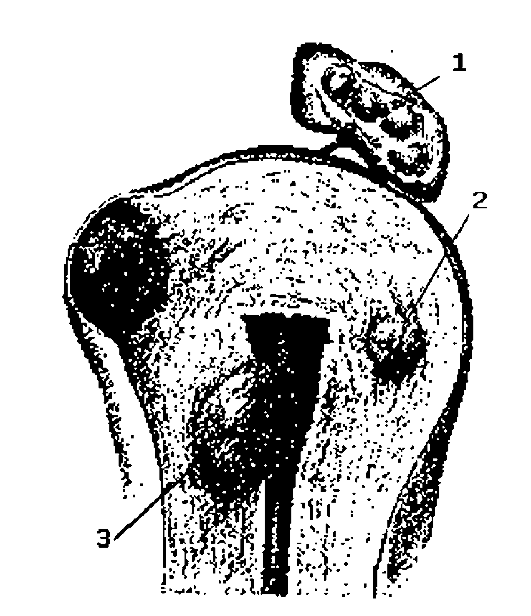
Рис. 6.20. Типичные локализации миом матки: 1 - субсерозный узел;
2 - интерстициальный узел; 3 - интерстициальный с центростремительным ростом
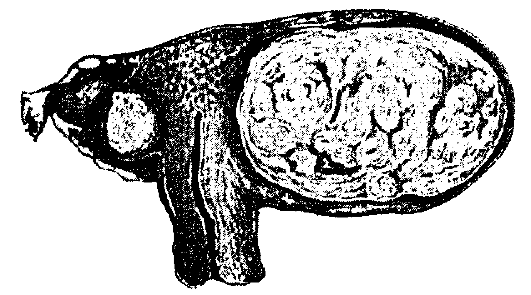
Рис. 6.21. Интралигаментарный миоматозный узел
От чего зависят жалобы больных при миоме матки?
Жалобы больных зависят от многих факторов: локализации и величины опухоли, вторичных изменений в миоматозных узлах, продолжительности заболевания, наличия сопутствующих изменений в половых органах и т. д. Преобладание тех или иных факторов отражается на симптоматике заболевания.
Каковы основные клинические симптомы при миоме матки?
Жалобы больных зависят от многих факторов: локализации и величины опухоли, вторичных изменений в миоматозных узлах, продолжительности заболевания, наличия сопутствующих изменений в половых органах и т. д. Преобладание тех или иных факторов отражается на симптоматике заболевания. Основными симптомами являются кровотечение, боли, сдавление соседних органов, рост опухоли.
Чем обусловлены кровотечения у больных с миомой матки, а также характер кровотечений у женщин репродуктивного и постменопаузального возраста?
Кровотечения чаще носят характер гиперполименореи. При наличии множественной миомы матки с интерстициальным расположением узлов происходят растяжение полости матки и увеличение менструирующей поверхности. Вследствие этого увеличивается количество крови, теряемой во время менструации. Кроме того, нарушается сократительная способность матки. Особенно сильные кровотечения возникают при миомах матки с центрипетальным ростом и подслизистым расположением узлов. Для такого расположения миом характерны не только длительные менструации, но и наличие межменструальных кровотечений. Ациклические кровотечения при миоме матки могут быть обусловлены нарушением функции яичников, что подтверждается нередко выявляемой гипер- плазией эндометрия. Маточное кровотечение может быть обусловлено также сопутствующей патологией: стромальной гиперплазией яичников, их кистозной дегенерацией, воспалением придатков матки, внутренним эндометриозом, гормонпродуцирующими опухолями яичников.
Появление кровотечения у женщин с миомой матки в постменопаузе почти всегда свидетельствует о патологии яичников (феминизирующая опухоль, стромальная гиперплазия яичника) или эндометрия (рак, гиперплазия, полипоз). Болевой синдром вызыван натяжением связочного аппарата матки, растяжением ее брюшинного покрова, а также давлением растущей опухоли на окружающие органы.
Чем обусловлены мено- и метроррагии у больных миомой матки?
Меноррагии у больных миомой матки могут быть обусловлены увеличением внутренней поверхности, с которой происходит десквамация эндометрия во время менструации, неполноценностью миометрия и сосудов, расположенных в мышечном слое, гиперплазией эндометрия и повышением его фибринолитической активности.
Длительные и обильные менструации нередко бывают связаны с сопутствующим эндометриозом. Достаточно часто маточные кровотечения зависят от топографического расположения миоматозных узлов в матке, они могут наблюдаться при интерстициальном и особенно при субмукозном расположении опухоли.
Чем обусловлено давление на соседние органы у больных с миомой матки?
Давление на соседние органы зависит от расположения и направления роста узлов. Так, исходящие из передней стенки матки узлы даже небольших размеров давят на мочевой пузырь, вызывая дизурические явления. Интралигаментарно расположенные опухоли вызывают сдав- ление мочеточников с последующим развитием гидроуретера, гидронефроза и пиелонефрита. Давление на прямую кишку обусловливает нарушения функции желудочно-кишечного тракта.
Чем обусловлен болевой синдром у больных миомой матки?
При миоме матки с центрипетальным ростом и подслизистым расположением узла боли могут быть схваткообразными. Подслизистые миоматозные узлы на ножке иногда появляются во влагалище, что сопровождается резкими болями и усилением кровотечения.
Миомы матки, как правило, растут медленно (не более 4 нед в год). Быстрое увеличение опухоли подозрительно в отношении саркоматозного роста, хотя это происходит редко (2%).
Какие осложнения возникают при миоме матки?
Наиболее частым осложнением миомы матки является нарушение питания субсерозного узла с последующим некрозом, реже возникают перекрут ножки подбрюшинного узла, острое кровотечение, сопровож- дающееся стойкой анемией больной. Такое осложнение, как выворот
матки при рождающемся субмукозном узле, встречается крайне редко. Злокачественное перерождение составляет, по данным некоторых авторов, до 2%.
Что такое субмукозная миома матки?
Субмукозная миома матки берет свое начало из глубокого слоя миометрия и растет в сторону эндометрия (рис. 6.22, А). Часто узлы опухоли связаны с миометрием только тонкой ножкой, поэтому могут далеко выдаваться в полость матки и даже выпадать через цервикальный канал (родившийся субмукозный узел).
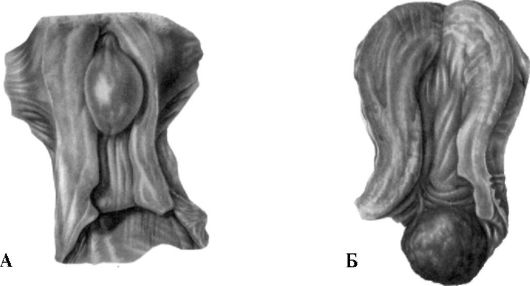
Рис. 6.22. Субмукозная миома: А - у дна матки; Б - рождающаяся
Существуют ли особенности развития и клиники при субмукозной миоме матки?
Как правило, субмукозные миомы матки быстрее растут и часто сопровождаются изменениями покрывающего их эндометрия и кро- вотечениями. При рождающемся субмукозном узле (рис. 6.22, Б) боли носят схваткообразный характер.
Каким образом производят удаление рождающегося или родившегося субмукозного миоматозного узла?
Рождающийся или родившийся субмукозный миоматозный узел захватывают крепкими щипцами и пытаются открутить его медленными ненасильственными вращениями в одну и ту же сторону до полного отторжения. При необходимости основание узла может быть рассечено длинными ножницами. После удаления родившегося субмукозного узла показано выскабливание слизистой тела матки.
Каков дифференциальный диагноз рождающегося субмукозного узла?
Рождающийся субмукозный узел дифференцируют от аборта в ходу или полипа шейки матки.
Какие методы диагностики применяют при миоме матки?
У большинства больных поставить диагноз миомы матки не представляет больших затруднений, так как при обычном гинекологическом исследовании определяется увеличенная в размерах, подвижная, безболезненная матка плотной консистенции с узловатой поверхностью. В настоящее время для определения размеров матки, локализации узлов и состояния яичников широко используют ультразвуковое сканирование. Уточнить диагноз позволяют такие методы исследования, как зондирование матки с последующим раздельным диагностическим выскабливанием слизистой оболочки цервикального канала и слизистой оболочки полости матки, гистеросальпингография, гистероскопия.
При неясном диагнозе обследование больной заканчивают проведением лапароскопии, с помощью которой можно уточнить диагноз миомы, определить характер изменений в придатках, а при необходимости взять кусочек ткани для патоморфологического исследования.
С чем следует дифференцировать миому матки?
Миому матки следует дифференцировать от рака или саркомы тела матки, от доброкачественной или злокачественной опухоли, исходящей из яичника, от воспалительных опухолевидных образований придатков матки, от беременности.
При дифференциальной диагностике между миомой матки и беременностью прежде всего следует обратить внимание на плотную консистенцию матки, узловатую поверхность опухоли, наличие длительных и обильных менструаций, что позволяет исключить беременность. Кроме того, глубокое изучение анамнеза, учет вероятных и предположительных признаков беременности, положительная реакция на хорионический гонадотропин, ультразвуковое исследование помогают уточнить диагноз.
С каким еще заболеванием проводят дифференциальную диагностику миомы матки?
При дифференциальной диагностике миомы матки (чаще субсерозное расположение узла) и кистомы яичника следует обратить внимание на консистенцию опухоли, подвижность, бугристую поверхность образования. Ультразвуковое исследование, диагностическая лапароскопия - основные методы для уточнения диагноза.
При дифференциальной диагностике миомы матки и саркомы матки обращают на себя внимание быстрый рост опухоли, возраст больной, жалобы больной на бели гнилостного характера, боли в нижних отделах живота, значительное похудание, анемия, не связанная с кровотечением, ухудшение общего состояния больной. Следует иметь в виду, что эти заболевания могут сочетаться. Большую помощь в диагностике оказывают ангиография, лимфография, хромоцистоскопия, экскреторная урография, радиоизотопная ренография.
От чего зависит метод лечения миомы матки? Какие существуют методы лечения миом матки?
Метод лечения обусловлен конкретными симптомами, размером, количеством и локализацией лейомиом, а также возрастом пациентки, заинтересованностью в сохранении фертильности [Brosens I., 1999]. Имеют значение также технические навыки, опыт и квалификация хирурга. Лечение может быть медикаментозным, хирургическим или с применением малоинвазивных технологий (эмболизация маточных артерий и миолиз).
Какие существуют современные тенденции в лечении миомы матки?
Современными тенденциями в лечении миомы матки являются:
- более активная тактика ведения больных;
- рост органосохраняющих операций;
- более широкое применение медикаментозного лечения;
- внедрение малоинвазивных технологий.
Каковы принципы лечения и показания
к медикаментозному лечению миомы матки?
Принципы медикаментозного лечения лейомиомы матки основаны на концепции о гормональнозависимом характере этой опухоли и использовании средств, тормозящих ее развитие [Nowak R.A., 2000].
Медикаментозное лечение направлено на торможение роста опухоли, уменьшение размеров матки, регресс клинических симптомов, сохранение репродуктивной функции у пациенток фертильного возраста, улучшение качества жизни [Manyonda I., 2004].
Показания к медикаментозному лечению больных лейомиомой матки:
- величина опухоли, увеличивающая размер матки менее чем до 12-13 нед беременности;
- интрамуральное и субсерозное расположение узлов (на широком основании);
- наличие противопоказаний к оперативному лечению;
- в качестве адъювантной терапии;
- отсутствие маточных кровотечений, приводящих к анемии.
Какие препараты являются основой медикаментозного лечения миомы матки?
Основой консервативной терапии миомы матки являются гормональные препараты. Механизм действия препаратов, применяемых для лечения миомы матки, в основном заключается во временном и обратимом угнетении функции яичников. Противоопухолевое действие гестагенов проявляется в снижении митотической активности клеток опухоли, что способствует торможению ее роста.
От чего зависит выбор препарата
для медикаментозного лечения миомы матки?
Выбор препаратов зависит от возраста больной, особенностей анамнеза (наличие роста миоматозных узлов во время беременности), переносимости лекарственных средств, наличия сопутствующей гинекологической и соматической патологии.
Каков механизм действия агонистов ГнРГ при медикаментозном лечении миомы матки?
Агонисты ГнРГ широко используются для лечения миомы матки в качестве неоадъювантного лечения и в виде длительной монотера- пии (по определенным показаниям). Механизм действия основан на десенситизации гонадотрофов аденогипофиза, блокаде секреции гонадотропинов и яичниковых гормонов, что вызывает состояние «обратимой медикаментозной гонадэктомии». Стойкая аменорея, индуцированная этими препаратами, приводит к повышению гемоглобина, к увеличению плотности микрососудов, что важно для пациенток с меноррагиями.
Какие препараты являются препаратами выбора при неоадъювантном лечении агонистами ГнРГ?
Неоадъювантное лечение: длительность курса лечения составляет 3-4 мес., введение препарата начинают в первые 5 дней менструального цикла, 1 раз в 28-30 дней.
- гозерелин (золадекс) - подкожно по 3,6 мг;
- декапептил депо (трипторелин) - внутримышечно по 3,75 мг;
- трипторелин (диферелин) - внутримышечно по 3,75 мг;
- бусерелин - внутримышечно по 3,75 мг;
- лейпрорелин (люкрин-депо) внутримышечно или подкожно по 3,75 мг.
Какие препараты являются препаратами выбора при монотерапии агонистами ГнРГ?
Монотерапия - длительность курса лечения составляет 6 мес. 1 раз в 28-30 дней. Возможны долгосрочные курсы с перерывом на 3 мес. или добавлением «возвратной» терапии препаратами для заместительной гормонотерапии (с целью купирования побочных эффектов, связанных с гипоэстрогенией); наилучшим препаратом является тиболон по 1 таблетке в день непрерывно в течение 3-6 мес.
Каков механизм действия антипрогестагенов при медикаментозном лечении миомы матки?
Антипрогестагены. Механизм действия: вызывают блокаду эффектов эндогенного стероида, конкурируя с прогестероном на уровне клеток-мишеней за взаимодействие с рецепторами. Длительность курса лечения - 3-6 мес. Используют в качестве неоадъювантного лечения и монотерапии (возможны повторные курсы лечения):
- мифепристон - перорально по 50 мг в день (возможно 25 мг), непрерывно. Побочные эффекты в виде тошноты, атипических приливов - кратковременны и слабо выражены.
Каков механизм действия антигонадотропных средств при медикаментозном лечении миомы матки?
Антигонадотропные средства. Механизм действия основан на подавлении максимальных выбросов ЛГ и ФСГ, что вызывает хроническую ановуляцию и на конкурентном ингибировании андрогенных, прогес- тероновых и эстрогенных (только даназол) рецепторов. Длительность курса составляет 3-6 мес. (возможно до 12 мес.).
Даназол перорально по 1 капсуле (100 или 200 мг) 4 или 2 раза в сутки (суточная доза 400 мг) в течение 3-6 мес., реже 12 мес. Стартовая доза обычно составляет 200 мг 2 раза в сутки и может быть увеличена в зависимости от клинической симптоматики.
Гестринон (неместран) перорально, стартовая доза по 2,5 мг (в некоторых случаях 5 мг) 2 раза в неделю. Продолжительность лечения - 3-6 мес.
Побочные эффекты андрогенного характера (у 40-72% больных) органичивают использование антигонадотропных средств.
Каков механизм действия прогестагенов и показания при медикаментозном лечении миомы матки?
Прогестагены малоэффективны при лечении миомы матки. Рекомендуется использовать их при сочетании миомы матки небольших раз- меров и гиперпластического процесса эндометрия. Наиболее эффективным методом терапии в этом случае среди других прогестагенов является внутриматочная гормональная система «Мирена» (ВМК с левоноргестрелом), выделяющая левоноргестрел в полость матки по 20 мкг в сутки. Динамический контроль (ультразвуковое исследование) необходимо проводить каждые 4-6 мес. на протяжении всего курса лечения. Осложнения и побочные эффекты: «прорывные» маточные кровотечения, рост миоматозных узлов.
Какие существуют методы хирургического лечения миом матки?
К хирургическим методам лечения относятся радикальные - гистерэктомия и органосохраняющие операции - миомэктомия с использованием различных доступов (гистероскопическим, лапароскопическим и абдоминальным).
Каковы показания к оперативному лечению миом матки?
Показания к хирургическому лечению следующие.
1. Субмукозная миома матки с обильными длительными менструациями или ациклические кровотечения, приводящие к анемизации больной (уточнение состояния эндометрия обязательно для исключения малигнизации). Такие миомы вызывают обильные кровотечения, приводящие к резкой анемизации больной. Нередко при этом матка не достигает больших размеров, а в некоторых случаях лишь слегка увеличена. Эти больные нуждаются в незамедлительном оперативном
лечении. Срочная помощь требуется при рождении подслизистого миоматозного узла, так как это сопровождается резкими схваткообразными болями и обильным кровотечением. При этом происходят сглаживание и раскрытие шейки матки, как при родах. Узел выполняет шейку матки или рождается во влагалище.
2. Большие размеры опухоли (свыше 15 нед беременности) даже в отсутствие жалоб. Опухоли такого размера нарушают анатомические взаимоотношения в малом тазу и брюшной полости.
3. Размер опухоли, соответствующий 12-13 нед беременности, при наличии симптомов сдавления соседних органов.
4. Рост опухоли более 4 нед в год.
5. Подбрюшинный узел на ножке. Такой узел подлежит удалению, поскольку появляется опасность перекрута его ножки, что может вызвать необходимость срочного оперативного вмешательства.
6. Некроз миоматозного узла. Некротические изменения обусловлены нарушением питания опухоли. Некроз миомы матки сопровождается, как правило, острыми болями, напряжением передней брюшной стенки, повышением температуры тела и лейкоцитозом. Чаще всего некрозу подвергаются подслизистые узлы миомы. Интерстициальные и подбрюшинные узлы нередко некротизируются во время беременности, в послеродовом или послеабортном периоде.
7. Интралигаментарное расположение узлов миомы, приводящее к появлению болей вследствие сдавления нервных сплетений и нарушению функции почек при сдавлении мочеточников.
8. Шеечные узлы миомы матки, исходящие из влагалищной части шейки матки.
9. Сочетание миомы матки с другими патологическими изменениями половых органов: рецидивирующей гиперплазией эндометрия, опухолью яичника, опущением и выпадением матки.
10. Бесплодие.
Устанавливая показания, нужно учитывать, все факторы, так как операцию
выполняют по относительным показаниям и она не всегда приводит к
восстановлению генеративной функции, особенно необходимо удаление узлов
свыше
Характер и объем оперативного вмешательства должны определяться хирургом строго индивидуально с учетом общего состояния и возраста больной. Очень важны не только правильное установление показаний к оперативному лечению, но и выбор наиболее рациональной методики и оптимального объема оперативного вмешательства.
Каков объем операций при миоме матки?
Характер и объем оперативного вмешательства должны определяться хирургом строго индивидуально с учетом общего состояния и возраста больной. Важны не только правильное установление показаний к оперативному лечению, но и выбор наиболее рациональной методики и оптимального объема оперативного вмешательства.
Какие виды операций применяют при миоме матки?
Органосохраняющие и органоуносящие.
Что относится к органосохраняющим операциям?
Консервативная миомэктомия - для сохранения генеративной или менструальной функции женщины. При миоме матки выполняют следующие консервативные операции: энуклеацию узлов матки, дефундацию и высокую ампутацию матки, аутотрансплантацию эндометрия, миомэктомию по методике Слепых с сохранением магистральных маточных сосудов, пластические операции по Александрову.
Гистерорезектоскопия. Проводят женщинам, желающим сохранить репродуктивную функцию, в возрасте до 38 лет при единичном миоматозном узле с субмукозной локализацией.
Какое реабилитационное лечение проводят после органосохраняющих операций?
Реабилитация после консервативной миомэктомии: электрофорез йода и цинка; общие радоновые ванны и влагалищные орошения. Одно из основных механизмов действия радоновой воды - седативное влияние на центральную и вегетативную нервные системы. При лечении больных миомой матки радоновой водой происходят восстановление нормальных гипоталамо-гипофизарно-яичниковых взаимоотношений, рецепции эндо- и миометрия, а также ликвидация воспаления, отека и венозного застоя.
Какие операции относят к органоуносящим?
При сочетании миомы матки и пролапса гениталий выполняют органоуносящие операции - экстирпацию матки влагалищным путем с последующей пластикой передней и задней стенок влагалища.
Какие операции при миоме матки относятся к радикальным?
К радикальным относятся операции:
1. Надвлагалищная ампутация матки.
2. Надвлагалищная ампутация матки с иссечением слизистой оболочки цервикального канала. Данная операция предложена на кафедре акушерства и гинекологии РУДН. Используется при сочетании миомы матки с эндометриозом.
3. Экстирпация матки (гистерэктомия) - выполняют при сочетании миомы матки с заболеванием шейки матки или при низко расположенных миоматозных узлах (интралигаментарное расположение узлов), когда технически произвести надвлагалищную ампутацию матки не представляется возможным.
4. Удаление рождающегося или родившегося субмукозного миоматозного узла: узел захватывают крепкими щипцами и пытаются открутить его медленными вращениями в одну и ту же сторону до полного отторжения. После удаления родившегося субмукозного узла показано выскабливание слизистой оболочки тела матки.
Каковы преимущества лапароскопии при консервативной миомэктомии или надвлагалищной ампутации матки?
В последнее время такие операции, как консервативная миомэктомия или надвлагалищная ампутация матки, выполняют при помощи лапароскопии. Преимуществами этого метода являются значительное уменьшение операционной травмы (нет разреза передней брюшной стенки), значительно менее выраженный в последующем спаечный процесс, хороший косметический эффект, более легкое течение послеоперационного периода, быстрое восстановление работоспособности.
Каковы преимущества влагалищной гистерэктомии?
1. Отсутствие рубца на передней брюшной стенке.
2. Обеспечение оперативного доступа минуя брюшную полость.
3. Низкая частота послеоперационных осложнений.
Каковы современные технологии радикального лечения миом матки?
Наиболее эффективным методом удаления матки является влагалищная гистерэктомия. Современные технологии радикального лечения миом матки существенно расширились за счет эмболизации маточных
артерий (ЭМА), ультразвуковой, лазерной вапоризации отдельных узлов. Все эти методы позволяют сохранить матку и в дальнейшем осуществить детородную функцию.
Каковы показания для эмболизации маточных артерий при миоме матки?
Показания к ЭМА:
- размеры лейомиомы матки, соответствующие 16-18 нед беременности при всех локализациях (за исключением субсерозных узлов на ножке);
- «симптомная» миома матки;
- в качестве неоадъювантного метода (с целью коррекции анемии);
- реализованная репродуктивная функция.
Каковы преимущества эмболизации маточных артерий (ЭМА) по сравнению с медикаментозным лечением миомы матки?
Преимущества ЭМА по сравнению с медикаментозным лечением:
- одномоментность воздействия;
- сохранение длительного эффекта процедуры и отсутствие рецидивов;
- более высокая эффективность в отношении регресса клинических симптомов и размеров миомы матки;
- отсутствие серьезных побочных эффектов;
- возможность проведения больным с экстрагенитальной патологией.
Каковы преимущества эмболизации
маточных артерий по сравнению
с хирургическим лечением миомы матки?
Преимущества ЭМА по сравнению с хирургическим лечением:
- сохранение матки;
- отсутствие интраоперационной кровопотери;
- одновременное влияние на все миоматозные узлы;
- отсутствие комбинированного эндотрахеального наркоза;
- более короткий срок пребывания в стационаре;
- меньший риск осложнений.
Какие вопросы могут возникнуть при оперативном лечении больных с миомой матки?
При оперативном лечении таких больных возникает ряд вопросов. Прежде всего, необходимо решить - полным или частичным должно быть удаление матки, яичников, маточных труб и каким доступом производить операцию - абдоминальным, вагинальным или методом хирургической лапароскопии.
Больным с миомой матки производят радикальные и консервативные операции. К каждому из этих методов имеются показания и противопоказания. Операции по поводу миомы матки выполняют в экстренном и плановом порядке. Экстренные показания возникают при кровотечении, связанном с опасностью для жизни больной, перекруте ножки миоматозного узла, некрозе или нагноении миоматозного узла. Во всех этих случаях показана срочная операция. Противопоказанием к операции является только агональное состояние больной.
Чем следует руководствоваться
при выборе объема оперативного лечения
при миоме матки?
При решении вопроса об объеме операции, т. е. ампутации или экстирпации, следует руководствоваться состоянием шейки матки. Неизмененную шейку удалять не следует. Возможно лечение патологических изменений шейки матки перед операцией. Обследование больных в отдаленные сроки показывает, что после надвлагалищной ампутации матки патологические изменения шейки матки обнаруживаются именно у тех женщин, у которых к моменту операции уже имели место те или иные ее изменения. При надвлагалищной ампутации матки или ее экстирпации вопрос об оставлении или удалении маточных труб решается индивидуально в каждом случае. Если маточные трубы натянуты на узлах опухоли или имеет место воспалительный процесс в них, то маточные трубы следует удалить. Во всех остальных случаях эти трубы нужно сохранить, так как их удаление в какой-то мере нарушает иннервацию и кровоснабжение яичников и приводит к более быстрому угасанию их функции.
6.5. ГИПЕРПЛАСТИЧЕСКИЕ ПРОЦЕССЫ ЭНДОМЕТРИЯ
Гиперпластические процессы эндометрия (ГПЭ) - распространенная гинекологическая патология, частота которой существенно увеличивается к менопаузе.
Каковы причины возникновения ГПЭ?
Эндометрий является органом-мишенью для половых гормонов из-за присутствия в нем специфических рецепторов. Сбалансированное гормональное воздействие через цитоплазматические и ядерные рецепторы обеспечивает физиологические циклические превращения слизистой оболочки матки. Нарушение гормонального статуса женщины может приводить к изменению роста и дифференцировки клеточных элементов эндометрия и повлечь за собой развитие гиперпластических процессов.
ГПЭ развиваются, как правило, на фоне абсолютной или относительной гиперэстрогении и значительно реже - при ненарушенных гормональных соотношениях.
К возникновению ГПЭ у женщин различного возраста приводят следующие факторы:
- нарушения центральной регуляции репродуктивной системы, вызывающие недостаточность лютеиновой фазы и ановуляцию;
- гиперпластические процессы в яичниках (стромальная гиперплазия, текаматоз, фолликулярная киста с гиперплазией тека и/или гранулезных клеток);
- гормональные опухоли яичников (гранулезоклеточные, текаклеточные и др.);
- нарушения тканевой рецепции, жирового обмена, метаболизма половых гормонов при патологии гепатобилиарной системы и желудочно-кишечного тракта, иммунитета и функции щитовидной железы.
Каков патогенез ГПЭ?
В патогенезе ГПЭ основную роль играют избыток эстрогенов и дефицит прогестерона.
Особая роль в патогенезе ГПЭ принадлежит изменению функциональной активности лизосомного аппарата эндометрия, в частности
состоянию лизосомных мембран, а также активности протеолитических ферментов.
В патогенезе ГПЭ большое значение имеют рецепторы эндометрия и чувствительность их к эстрогенам и прогестерону.
Каковы изменения в иммунной системе при ГПЭ?
При ГПЭ происходит изменение основных показателей иммунной системы: достоверное увеличение процентного содержания Т-лимфоцитов; относительное количественное увеличение Т-супрессоров и соответственно снижение коэффициента Т-хелпе- ры/Т-супрессоры; снижение фагоцитарной активности нейтрофилов и фагоцитарного индекса.
Установлено, что один из факторов роста - эпидермальный, связываясь со специфическими рецепторами, обусловливает синтез ДНК и митотическую активность эндометриальных клеток, т. е. их пролиферацию. Инсулиноподобный фактор роста-1 обнаружен в эндометрии и участвует в процессах роста клеток и их дифференцировке.
Какова роль избытка жировой ткани в патогенезе ГПЭ?
Определенную роль в патогенезе гиперплазии эндометрия играют ожирение и гипергликемия. Следствием этого является внегонадное образование эстрогенов из андрогенов в жировой ткани. Установлено, что содержание эстрадиола и глобулинов, связывающих половые стероиды, у женщин с нормальной или сниженной массой тела на 27-43% ниже. Изучение роли рецепторов эндометрия к яичниковым гормонам показало, что в эндометрии здоровых женщин содержание рецепторов эстрадиола достоверно ниже, чем при железисто-кистозной гиперплазии.
Часто наблюдаемое в клинической практике сочетание патологии эндометрия с дисгормональными изменениями в молочной железе и миомой матки указывает на общность патологических процессов, вызванных нарушением гормонального баланса. По мнению ряда авторов, предрак и рак эндометрия развиваются у женщин определенного типа, имеющих на протяжении жизни длительные периоды гиперэстрогении. Это позволило Я.В. Бохману (1977) отнести больных с эндокринно-обменным синдромом и наличием патологии эндомет- рия к первому патогенетическому варианту. При обследовании таких больных выявляется простая железистая или атипическая гиперплазия
эндометрия. Данный синдром часто наблюдается и при высокодифференцированной аденокарциноме тела матки. Ко второму патогенетическому варианту (больные без выраженного нейроэндокринного синдрома) чаще относятся больные с эндометриальными полипами. Выделение патогенетических вариантов позволяет более дифференцированно подходить к лечению гормонами.
Какие гистологические типы гиперплазии эндометрия выделяют?
Гистологическая классификация ВОЗ (1975) выделяет 3 основных вида гиперпластических процессов в эндометрии: полипы, эндометриальная гиперплазия и атипичная гиперплазия эндометрия.
В литературе обычно применяют следующую классификацию:
- железисто-кистозная гиперплазия эндометрия;
- полипы эндометрия (железистые и железисто-кистозные);
- атипическая гиперплазия эндометрия (синонимы - аденоматоз, аденоматозная гиперплазия очаговая либо диффузная, включающая и аденоматозные полипы).
Каковы морфологические особенности железисто-кистозной гиперплазии эндометрия?
Эндометрий утолщен, отсутствует разделение на компактный и спонгиозный слои, нарушается правильность распределения желез в строме, характерны кистовидно-расширенные железы. Количество желез не увеличивается, но в связи с усиленной пролиферацией железы приобретают извитую форму, и на срезе, проходящем через
отдельные витки одной и той же
железистой трубочки, создается впечатление большого количества желез. Кистовидное расширение желез при железисто-кистозной гиперплазии происходит вследствие разной интенсивности пролиферации эпителия на отдельных участках желез и различий в степени пролиферации стромы. В строме, как правило, клубков спиральных артерий не наблюдается (рис. 6.23).
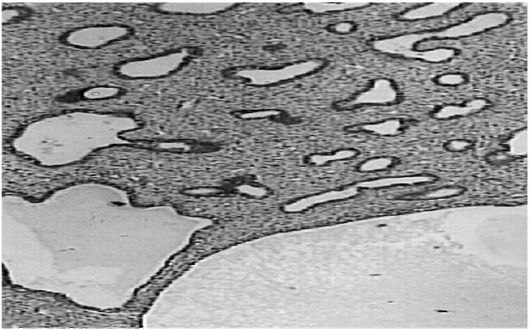
Рис. 6.23. Смешанная форма желе зисто-кистозной гиперплазии эндо метрия.
Каковы морфологические особенности эндометриального полипа?
Полип тела матки представляет собой локальное, экзофитно растущее образование, исходящее из ткани базального слоя эндометрия. Наиболее частой локализацией полипов эндометрия являются дно тела матки и устья маточных труб. Форма полипов различная - от шаровидной, грушевидной или грибовидной до вытянутой, цилиндрической. Размеры полипа от 0,3-1,0 см до больших экзофитных образований, заполняющих всю полость матки и проникающих через цервикальный канал во влагалище (рис. 6.24).
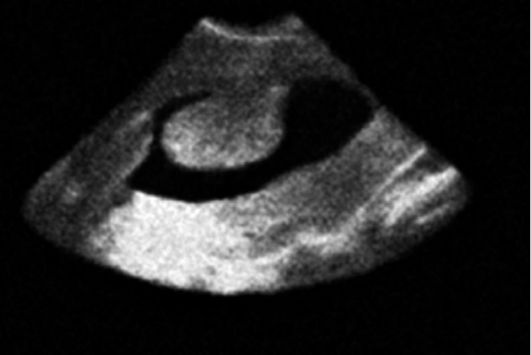
Рис. 6.24. Полип эндометрия с визуализацией его ножки.
Какие полипы выделяют по гистологическому типу?
По гистологическому строению выделяют два типа полипов эндометрия: полипы, содержащие элементы функционирующего эндометрия, которые реагируют на действие эстрогенов и прогестерона, как и окружающая их ткань эндометрия, и полипы, состоящие из незрелого эндометрия базального слоя, они гормонально малоактивны. Строма в полипах первого типа такая же, как и в гиперплазированном эндометрии, и их целесообразнее относить к полиповидной форме гиперплазии эндометрия. Строма в полипах второго типа состоит из фиброзных и гладкомышечных элементов, и этот тип полипа относят к истинным железистым полипам.
Чем характеризуются железистые полипы?
Железистые полипы отличаются от гиперплазированного эндометрия особенностями строения желез и стромы. Железы в полипе располагаются неравномерно, беспорядочно, имеют различную величину и форму. Одни железы узкие, другие расширенные и даже кистовидные, у третьих - пиловидная извитая форма. Железы выстланы обычно высокопризматическим эпителием индифферентного или пролиферативного типа, а в кистовидных железах эпителий приобретает уплощенную, изоили низкопризматическую форму.
Для железистых полипов эндометрия характерно строение кровеносных сосудов, они обычно имеют утолщенные склерозированные стенки, а в основании полипов могут образовывать клубки.
Каковы морфологические особенности атипической гиперплазии эндометрия?
При гистологическом исследовании характерными для атипической гиперплазии эндометрия являются следующие признаки:
- увеличенное количество желез;
- нарушение полярности расположения клеток;
- сближение желез с узкими прослойками стромы между ними (спинка к спинке);
- значительное преобладание железистых элементов над стромальными;
- ветвление (почкование) желез;
- микрофолликулярный тип строения желез (когда вокруг крупной железы располагаются мелкие дочерние железы микрофол- ликулярного типа);
- повышенная извитость желез;
- неправильная форма желез;
- истинные сосочки в железах (в просвет желез выступают сосочки, имеющие фиброзную ножку), иногда могут наблюдаться и ложные сосочки, состоящие из нагромождающихся эпителиальных клеток;
- структуры «железа в железе» возникают за счет поперечных срезов внутрижелезистых сосочковых разрастаний;
- внутрижелезистые эпителиальные мостики;
- кривообразные структуры.
Что относится к предраковым заболеваниям эндометрия?
К предраковым заболеваниям эндометрия относятся: атипическая гиперплазия эндометрия (аденоматоз) и аденоматозные полипы в любом возрасте, рецидивирующая железистая гиперплазия эндометрия, особенно в перименопаузальном и постменопаузальном периодах; железистая гиперплазия эндометрия в сочетании с нейрообменно-эндокринной патологией (ожирение, сахарный диабет), гипертонической болезнью.
Какие больные могут быть отнесены к группе риска по развитию предрака эндометрия?
К группе риска по развитию предраковых состояний эндометрия могут быть отнесены женщины, имеющие:
- ановуляторные маточные кровотечения;
- позднее, после 50 лет, наступление менопаузы;
- ожирение;
- сахарный диабет;
- гипертоническую болезнь.
Каковы проявления ГПЭ?
Основными жалобами больных являются:
- нарушения менструальной функции (или кровянистые выделения из половых путей в менопаузе);
- жалобы, обусловленные обменными и эндокринными нарушениями.
В репродуктивном возрасте больные обычно жалуются на кровянистые выделения из половых путей в межменструальном периоде, а также до или после менструации. Для всех ГПЭ характерны нарушения менструального цикла.
В пременопаузальном периоде женщин беспокоят нерегулярные обильные менструации с последующими длительными мажущими кровянистыми выделениями. В менопаузе больные отмечают скудные кратковременные или длительные кровянистые выделения. Наиболее характерные жалобы при наличии обменных и эндокринных нарушений - головные боли, избыточная прибавка массы тела, гипертрихоз, нарушения сна, периодически возникающая жажда, розовые стрии, пониженная работоспособность, раздражительность.
Клинике ГПЭ часто присущи проявления гипертонической болезни, сахарного диабета, ожирения, т. е. метаболических нарушений, являющихся фоном для развития пролиферативных процессов в органах-мишенях.
Какие методы применяют для диагностики ГПЭ?
Наиболее достоверным и объективным методом диагностики является гистологическое исследование слизистой из цервикального канала и тела матки, полученной методом аспирационной биопсии или при раз- дельном лечебно-диагностическом выскабливании. Информативность исследования повышается, если его проводят под контролем гистероскопии.
С какой целью применяют гистероскопию?
Особое место в диагностике внутриматочной патологии занимает гистероскопия, которая позволяет более детально изучить состояние эндометрия, провести четкую топическую диагностику и проконтро- лировать результаты корригирующей терапии.
Наиболее часто используют жидкостную гистероскопию (изотонический раствор натрия хлорида, 5% раствор глюкозы, дистиллированная вода, декстраны), которая позволяет выполнить ряд внутри- маточных операций и использовать электро- и лазерную хирургию. Контрольное гистероскопическое исследование дает также возможность оценить качество произведенного выскабливания с прицельным удалением остатков гиперплазированного эндометрия или полипов, выявить сопутствующую внутриматочную патологию (внутренний эндометриоз, миоматозные узлы с подслизистым или центрипетальным ростом и др.).
Какое значение имеет ультразвуковое исследование в диагностике патологии эндометрия?
УЗИ позволяет косвенно судить о состоянии эндометрия, ориентируясь на толщину и структуру срединного М-эха. Эндометрий имеет четкие очертания и большую акустическую плотность по сравнению с миомет- рием, занимая серединное положение параллельно внешнему контуру матки. При нормальном менструальном цикле толщина эндометрия зависит от фазы цикла, постепенно возрастая от 3-4 мм в первой фазе до 12-15 мм - во второй фазе цикла. Гиперплазия эндометрия обусловливает значительное увеличение этих показателей. Полипы эндо-
метрия,
как правило, визуализируются на эхограммах в виде округлых или
удлиненных овальных образований с четким контуром и тонким
эхонегативным ободком («гало») на фоне расширенной полости матки. В
постменопаузе увеличение размера срединного М-эха до
Каковы признаки ГПЭ при гистерографии?
Гиперплазированный эндометрий и полипы на гистерограммах проявляются в виде зазубренности или фестончатости контуров стенок полости матки, особенно у дна, или дефектов наполнения. Это иссле- дование проводят на 7-8-й день цикла, используя водорастворимые контрастные вещества (верографин, урографин, уротраст).
Какова роль цитологического исследования аспирата эндометрия в диагностике ГПЭ?
Цитологическое исследование аспирата из полости матки позволяет определить выраженность пролиферативных изменений эндометрия, но не дает четкого представления о его патоморфологической структу- ре. Этот метод можно рекомендовать в качестве скрининга патологии эндометрия и его состояния на фоне гормональной терапии, однако цитологическое исследование аспирата нельзя рассматривать как альтернативу гистологическому исследованию. Последнее производят или при взятии соскоба слизистой оболочки матки специальными приспособлениями без расширения цервикального канала (эндосэмплер) амбулаторно, или при гистероскопии и раздельном диагностическом выскабливании.
Какова лечебная тактика при ГПЭ?
Лечебная тактика при гиперпластических процессах зависит от патоморфологической характеристики эндометрия, возраста больной, этиологии и патогенеза заболевания, сопутствующей генитальной и экстрагенитальной патологии.
У больных с ГПЭ первый этап лечения осуществляют путем лечебно-диагностического выскабливания слизистой оболочки матки с гистероскопическим контролем.
Терапия в различные возрастные периоды складывается из остановки кровотечения и профилактики рецидива гиперпластического процесса, сохранения ритмичной менструальноподобной реакции
(до 50 лет) или стойкого прекращения менструаций. Гормональная терапия железистой гиперплазии и полипов эндометрия в этой возрастной группе предусматривает применение прогестагенов, например дюфастона.
Помимо прогестагенов, для лечения гиперпластических процессов эндометрия у больных этого возраста успешно используют агонисты ГнРГ.
Каков механизм действия аналогов гонадолиберина?
В норме гонадолиберин секретируется в гипоталамусе в импульсном режиме. Импульсное воздействие гонадолиберина активирует гонадотропные клетки гипофиза и стимулирует секрецию ЛГ и ФСГ. Напротив, непрерывное воздействие гонадолиберина приводит к подавлению секреции ЛГ и ФСГ. В результате снижается секреция эстрогенов в яичниках; прекращаются менструации, атрофируется эндометрий. После отмены лечения импульсный режим секреции гонадолиберина восстанавливается, также возобновляется и менстру- альный цикл.
Какие аналоги гонадолиберина применяют при лечении ГПЭ?
Для лечения ГПЭ применяют следующие аналоги гонадолиберина: бусерелин, декапептил, золадекс, диферелин, гозерелин.
Какова тактика лечения больных с железисто-кистозной гиперплазией?
У больных репродуктивного возраста гормональное лечение направлено на сохранение менструальной функции и коррекцию ановуляции путем циклической секреторной трансформации эндометрия. Предложено несколько схем лечения больных с железисто-кистозной гиперплазией эндометрия.
Схема 1 - эстроген-гестагены по 1 таблетке на ночь с 5-го по 25-й день цикла, затем 7-дневный перерыв. Курс лечения 3-6 мес. Предпочтительнее назначение трехфазных оральных контрацептивов - три-регол.
Схема 2 - 17-ОПК по 1 мл (125 мг) 12,5% раствора на 12-14-17-й день цикла в течение 4-6 мес. под контролем тестов функциональной диагностики (или по 250 мг на 14-й и 16-й день цикла).
Схема 3 - дюфастон по 20 мг в сутки ежедневно либо с 16-го по 25-й день менструального цикла в течение 4-6 мес.
У женщин молодого возраста второй этап лечения подразумевает профилактику рецидивов ГПЭ с последующим восстановлением овуляторного менструального цикла.
В пременопаузальном периоде второй этап терапии преследует цель профилактики рецидива ГПЭ с сохранением ритмичной менструальноподобной реакции или стойким прекращением менструации (для этой цели используют андрогены, прогестагены в непрерывном режиме в течение 6-9 мес.).
Особого внимания заслуживают ГПЭ в постменопаузальном периоде, причиной которых в основном бывают гормонально-активные структуры яичников (стромальная гиперплазия, текаматоз, тека- и гранулезоклеточные опухоли) или обменно-эндокринные нарушения (ожирение, диэнцефальная патология).
Лечение больных после удаления эндометриальных полипов заключается в назначении прогестагенов либо антигонадотропных препаратов или агонистов гонадолиберинов в течение 6 мес.
Какова медикаментозная терапия
при выявлении аденоматоза эндометрия?
Лечение больных с аденоматозными изменениями эндометрия проводят, как правило, прогестагенами в непрерывном режиме или реже - по контрацептивной схеме в течение 6 мес. и более. В перименопаузальном периоде аденоматозная гиперплазия эндометрия требует назначения более высоких доз и желательно парентерального введения (17-ОПК, депо-провера, депостат).
В последние годы наряду с прогестагенами при лечении аденоматозной ГПЭ стали широко использовать препараты с выраженным антигонадотропным эффектом - даназол и гестринон, которые принято назначать в непрерывном режиме в течение 6 мес. Эти лекарственные средства целесообразно также принимать при сочетании ГПЭ с миомой матки небольших размеров и внутренним эндометриозом у молодых пациенток.
Для оценки эффективности гормональной терапии гиперпластических процессов эндометрия через 3 мес. от начала лечения показано контрольное обследование, включающее эхографию, изучение цитологии аспирата из полости матки. Кроме того, после окончания лечения (через 6 мес.) необходимо гистологическое исследование слизистой оболочки матки.
Какова медикаментозная терапия при выявлении атипической формы ГПЭ?
Лечение больных с атипической формой ГПЭ. В репродуктивном периоде на первом этапе лечения обычно используют 17-ОПК в непрерывном режиме по 500 мг 3 раза в неделю в течение 3 мес., затем по 500 мг 2 раза в неделю - на протяжении 3 мес.
На 2-м этапе назначают эстроген-гестагенные препараты по контрацептивной схеме в течение 6 мес.
3-й этап состоит в стимуляции овуляции.
В ходе лечения необходимо каждые 3-4 мес. выполнять контрольную аспирационную биопсию.
У больных в пре- и постменопаузе назначают 17-ОПК по 500 мг 3 раза в неделю в течение 3 мес., затем по 500 мг 2 раза в неделю в течение 3 мес., затем по 500 мг 1 раз в неделю еще в течение 3 мес.
Суммарная доза 17-ОПК при лечении атипичной ГПЭ составляет
Для лечения атипичной ГПЭ возможно также использование МПА (депо-провера) по 200-400 мг в/м 1 раз в 7-10 дней в течение 6 мес.
Как оценивают результаты лечения ГПЭ?
Если после проведенного ранее диагностического выскабливания под контролем гистероскопии и последующей гормональной терапии у больной вновь диагностирована гиперплазия эндометрия, то следует говорить о его рецидиве. Рецидив ГПЭ свидетельствует скорее всего о недостаточной терапии либо о гормонально-активных структурах в яичниках, что требует уточнения их состояния путем эндоскопической биопсии или резекции. Отсутствие морфологических изменений в яичниках позволяет продолжить гормональную терапию более высокими дозами препаратов. Рецидив ГПЭ, а также сочетание этой патологии с миомой матки и/или внутренним эндометриозом у больных в перименопаузальном периоде требуют расширения показаний к оперативному лечению (электроили лазерная аблация эндометрия, криодеструкция слизистой оболочки матки, лапароскопическая аднексэктомия, экстирпация матки с придатками).
При рецидивирующих полипах эндометрия зачастую необходимо эндоскопическое хирургическое воздействие на зону роста (ножка полипа), а именно - криодеструкция, лазервапоризация или резек- тоскопия.
Повторное возникновение аденоматозных изменений эндометрия, несмотря на адекватную гормональную терапию, требует расширения показаний к оперативному лечению (эндоскопическая аблация эндо- метрия, резекция яичников, экстирпация матки с придатками).
Каковы показания к хирургическому лечению?
Показаниями к хирургическому лечению являются:
- рецидивирующая ГПЭ на фоне метаболических нарушений в сочетании с миомой матки, аденомиозом;
- атипичная ГПЭ, особенно в сочетании с миомой матки, аденомиозом;
- неэффективность гормонотерапии, невозможность наблюдения за больной;
- аличие атипичной ГПЭ у больных старше 50 лет.
Как осуществляют диспансерное наблюдение за больными с гиперпластическими процессами?
Все больные с гиперпластическими процессами должны находиться на диспансерном учете с длительностью наблюдения не менее 5 лет. Контроль за результатами лечения осуществляют через 3 и 6 мес. путем цитологического исследования аспирата из полости матки и динамического эхографического скрининг-контроля.
По окончании гормональной терапии необходимо произвести аспирационную биопсию эндометрия с морфологическим исследованием.