Эндокринология : учебник. И.И. Дедов - 2009. - 432 с.: ил.
|
|
|
|
ГЛАВА 5 РЕПРОДУКТИВНАЯ ЭНДОКРИНОЛОГИЯ ЖЕНСКОГО ПОЛА
5.1. АНАТОМИЯ И ФИЗИОЛОГИЯ ЖЕНСКОЙ РЕПРОДУКТИВНОЙ СИСТЕМЫ
Яичник (ovarium, oophoron) - парный орган женской репродуктивной системы и одновременно железа внутренней секреции (рис. 5.1). Масса яичника в норме не превышает 5-8 г, размеры составляют 2,5-5,5 см в длину, 1,5-3,0 см в ширину и до 2 см в толщину. Яичник состоит из двух слоев: коркового вещества, покрытого белочной оболочкой, и мозгового. Корковое вещество образовано фолликулами различной степени зрелости.
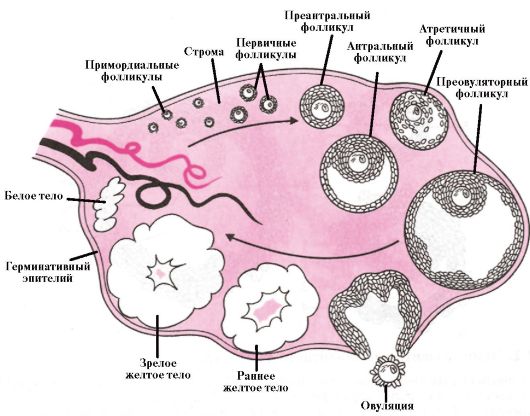 Рис. 5.1. Яичник: процессы, происходящие в течение овуляторного цикла
Рис. 5.1. Яичник: процессы, происходящие в течение овуляторного цикла
Основными стероидными гормонами, секретируемыми яичниками, являются эстрогены и прогестерон, а также андрогены. Эстрогены представлены эстрадиолом, эстроном и эстриолом. Эстрадиол (Е2) секретируется преимущественно клетками гранулезы. Эстрон (E1) образуется путем периферической ароматизации эстрадиола; эстриол (Е3) синтезируется яичниками в следовых количествах; основным источником эстриола является гидроксилирование эстрадиола и эстрона в печени. Основным прогестагенным гормоном (прогестином) является прогестерон, который секретируется преимущественно желтым телом. Основным яичниковым андрогеном, который секретируется клетками теки, является андростендион. В норме большая часть андрогенов в женском организме имеет надпочечниковое происхождение.
Исходными соединениями для синтеза эстрогенов и прогестерона является холестерин. Биосинтез половых гормонов происходит аналогично биосинтезу кортикостероидов. Стероидные гормоны яичников так же, как и надпочечников, практически не накапливаются в клетках, а секретируются в процессе синтеза. В кровеносном русле значительная часть стероидов связывается с транспортными белками: эстрогены - с глобулином, связывающим половые гормоны (ГСПГ), прогестерон - с кортизолсвязывающим глобулином (транскортином). Механизм действия эстрогенов, прогестинов и андрогенов аналогичен таковому у других стероидных гормонов. Основными метаболитами эстрогенов являются катехолэстрогены (2-оксиэстрон, 2-метоксиэс- трон, 17-эпистриол), обладающие слабой эстрогенной активностью; основным метаболитом прогестерона является прегнандиол.
До начала пубертатного периода в яичниках происходит независимый от гонадотропинов очень медленный рост первичных фолликулов. Дальнейшее развитие зрелых фолликулов возможно лишь под действием гормонов гипофиза: фолликулостимулирующего (ФСГ) и лютеинизирующего (ЛГ), продукция которых, в свою очередь, регулируется гонадолиберином гипоталамуса. В овариальном цикле различают две фазы - фолликулярную и лютеиновую, которые разделены двумя событиями - овуляцией и менструацией (рис. 5.2).
В фолликулярной фазе секреция ФСГ гипофизом стимулирует процессы роста и развития первичных фолликулов, а также выработку эстрогенов клетками фолликулярного эпителия. Предовуляторный выброс гонадотропинов определяет сам процесс овуляции. Овуляторный выброс ЛГ и в меньшей степени ФСГ обусловлен сенси-
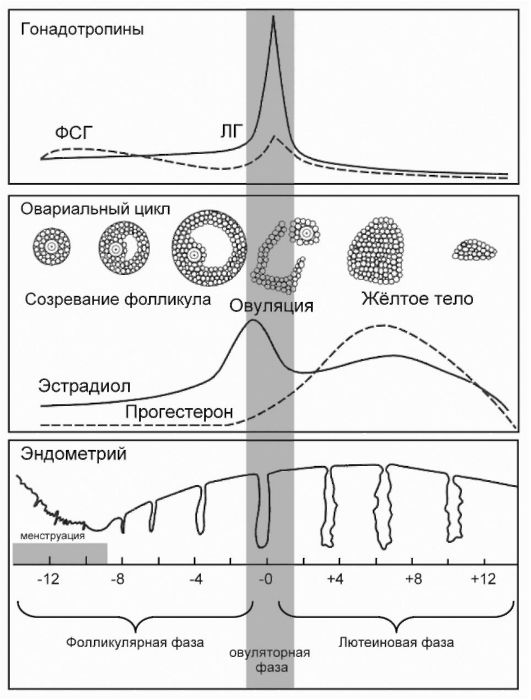 Рис. 5.2. Циклические изменения в репродуктивной системе у женщины на протяжении менструального цикла
Рис. 5.2. Циклические изменения в репродуктивной системе у женщины на протяжении менструального цикла
билизацией гипофиза к действию гонадолиберина и связан с резким падением уровня эстрадиола в течение 24 ч, предшествующих овуляции, а также с существованием механизма положительной обратной связи сверхвысоких концентраций эстрогенов и уровня ЛГ.
Под влиянием овуляторного увеличения уровня ЛГ происходит формирование желтого тела, которое начинает продуцировать прогестерон. Последний ингибирует рост и развитие новых фолликулов, а также участвует в подготовке эндометрия к внедрению оплодотворенной яйцеклетки. Плато сывороточной концентрации прогестерона соответствует плато ректальной (базальной) температуры (37,2-37,5 °С), что лежит в основе одного из методов диагности-
ки произошедшей овуляции. Если в дальнейшем оплодотворение не происходит, через 10-12 дней наступает регресс желтого тела, если же оплодотворенная яйцеклетка внедрилась в эндометрий и образующаяся бластула стала синтезировать хорионический гонадотропин (ХГ), желтое тело становится желтым телом беременности.
Длительность овариального (менструального) цикла в норме варьирует от 21 до 35 дней. Самым распространенным считается 28-днев- ный цикл, существующий в течение длительного времени только у 30-40 % женщин. В менструальном цикле различают три периода, или фазы: менструальная (фаза десквамации эндометрия), которой заканчивается предыдущий цикл, постменструальная (фаза пролиферации эндометрия), предменструальная (функциональная, или секреторная фаза). Границей между двумя последними фазами является овуляция. Отсчет дней менструального цикла начинается с первого дня менструации.
5.2. МЕТОДЫ ОБСЛЕДОВАНИЯ В ГИНЕКОЛОГИЧЕСКОЙ ЭНДОКРИНОЛОГИИ
5.2.1. Физикальные методы
Включают гинекологический и общий осмотр, c оценкой типа телосложения, выраженности и распределения жировой клетчатки, состояния молочных желез, характера оволосения. При опросе выясняется возраст менархе, наличие или отсутствие нарушений менструального цикла, длительность и характер менструальных выделений, продолжительность менструального цикла. Выясняют число беременностей, срок наступления беременности от начала половой жизни без контрацепции, течение беременности и родов. В целом, нормальное наступление и течение беременности, которая заканчивается рождением здорового ребенка, практически исключает наличие у пациентки как минимум тяжелой эндокринной патологии. Эти данные позволяют анамнестически сориентироваться в отношении начала того или иного эндокринного заболевания.
5.2.2. Лабораторные методы
При рождении ребенка с неправильным строением наружных гениталий, во всех случаях первичной аменореи, а также для диагностики
хромосомных болезней, большинство из которых протекает с нарушением полового развития, обязательно исследование кариотипа.
Лабораторная диагностика при заболеваниях репродуктивной системы у женщин подразумевает исследование содержания яичниковых и надпочечниковых стероидных гормонов, а также гонадотропинов (ЛГ и ФСГ) и пролактина. При регулярном менструальном цикле или олигоменорее исследование базальных уровней гонадотропинов должно проводиться на 5-7 день менструального цикла (в ранней фолликулярной фазе). Полученные данные в подавляющем большинстве случаев позволяют дифференцировать гипер-, гипоили нормогонадотропные состояния. Первичный гипогонадизм (синдром истощения яичников, менопауза, овариэктомия) характеризуется высокими уровнями ФСГ и ЛГ и низким - эстрадиола. При вторичном (гипофизарном) гипогонадизме снижено содержание как гонадотропинов, так и эстрадиола. Для оценки функциональной активности желтого тела рекомендуется определение уровня прогестерона в крови в лютеиновой фазе цикла. Для диагностики типа гиперандрогении при вирильном синдроме проводится определение в плазме дегидроэпиандростеронасульфата (ДЭАС) и тестостерона, а также 17-гид- роксипрогестерона для диагностики врожденной дисфункции коры надпочечников (см. п. 4.6).
В отдельных относительно редких случаях для определения характера нарушений и функционального состояния репродуктивной системы используют фармакологические пробы. К ним относится проба с хорионическим гонадотропином (ХГ), которая в рамках дифференциальной диагностики первичного и вторичного гипогонадизма позволяет оценить реакцию яичников на гонадотропную стимуляцию. Для дифференциальной диагностики гипоталамического и гипофизарного гипогонадизма может использоваться проба с аналогами гонадотропин-рилизинг-гормона (бусерелин, трипторелин).
5.2.3. Инструментальные методы
В связи с неинвазивностью, безопасностью и доступностью наибольшее распространение в гинекологии получило ультразвуковое исследование, которое помимо визуализации яичников и других органов малого таза позволяет проводить контроль за ростом и созреванием фолликула, оценивать толщину эндометрия, выявлять и наблюдать опухолевидные образования яичников. Кроме того, широко используются эндоскопические методы (кольпоскопия, гистероскопия и ла-
пароскопия), которые применяются не только для диагностики, но и для лечения различных гинекологических заболеваний.
5.3. АМЕНОРЕЯ
Аменореей обозначают отсутствие менструаций у женщин репродуктивного возраста. Под первичной аменореей понимают отсутствие менструаций у девушек старше 16 лет, под вторичной аменореей - прекращение менструаций на срок более 6 месяцев у женщин с ранее установленным менструальным циклом. Для обозначения скудных менструаций используется термин опсоменорея; под олигоменореей подразумевают редкие нерегулярные менструации (менее 9 в году). Физиологическая аменорея имеет место во время беременности и в постменопаузе.
Табл. 5.1. Аменорея
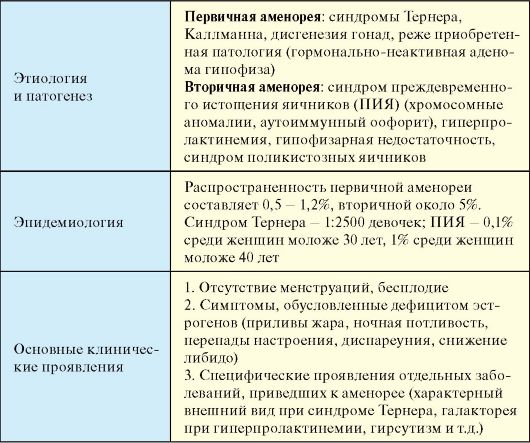 Окончание табл. 5.1
Окончание табл. 5.1
 Этиология и патогенез
Этиология и патогенез
Широко варьируют от наследственных синдромов (Тернера, Каллманна) до приобретенных заболеваний (пролактинома, нервная анорексия), при этом этиология частично перекрывается для первичной и вторичной аменореи, то есть одно и тоже заболевание (например, крупная опухоль гипофиза, вызывающая гипопитуитаризм) может быть причиной как первичной, так и вторичной аменореи. Наиболее частыми причинами первичной аменореи (> 60 % случаев) является недостаточность яичников и пороки развития матки (табл. 5.2).
Табл. 5.2. Некоторые заболевания,
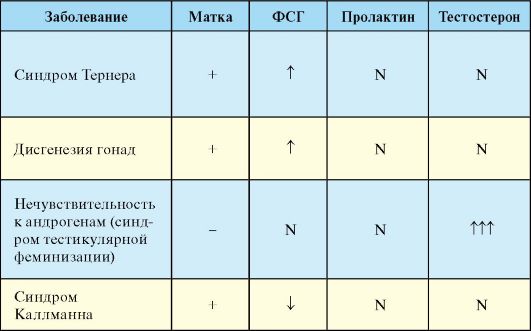 (+/-) - есть/нет (присутствует/отсутствует); ↑, ↓ - повышение/понижение (уровня гормона), N - норма.
(+/-) - есть/нет (присутствует/отсутствует); ↑, ↓ - повышение/понижение (уровня гормона), N - норма.
Табл. 5.3. Некоторые заболевания,
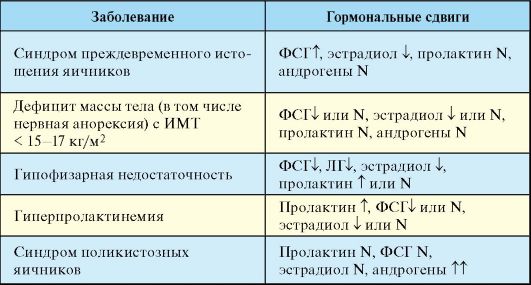 протекающие с первичной аменореей
протекающие с первичной аменореей
 протекающие со вторичной аменореей
протекающие со вторичной аменореей
 Большая
часть случаев вторичной аменореи связана с гиперпролактинемией (15-30
%) (табл. 5.3), гиперандрогенией различного генеза, синдромом
преждевременного истощения яичников (10 %).
Большая
часть случаев вторичной аменореи связана с гиперпролактинемией (15-30
%) (табл. 5.3), гиперандрогенией различного генеза, синдромом
преждевременного истощения яичников (10 %).
Эпидемиология
Распространенность первичной аменореи составляет 0,5-1,2 %, вторичной около 5 %. Распространенность синдрома Тернера - 1:2500 девочек, преждевременного истощения яичников (ПИЯ) - 0,1 % среди женщин моложе 30 лет и 1 % среди женщин моложе 40 лет. В структуре ПИЯ 60 % приходится на генетические нарушения (ломкая Х-хромосома, мутация гена рецептора ФСГ или ЛГ), 20 % на аутоиммунный оофорит.
Клинические проявления
♦ Отсутствие менструаций, бесплодие. Последнее определяется как ненаступление беременности на протяжении одного года регулярной половой жизни (в среднем 2 раза в неделю) без контрацепции. Вероятность спонтанного наступления беременности при ПИЯ составляет 5 %.
♦ Симптомы, обусловленные дефицитом эстрогенов при первичной аменорее, отсутствуют и встречаются у 75 % женщин со вторичной аменореей. К ним относятся приливы жара, ночная потливость, перепады настроения, диспареуния, снижение либидо.
♦ Специфические проявления отдельных заболеваний, приведших к аменорее (характерный внешний вид при синдроме Тернера, галакторея при гиперпролактинемии, гирсутизм и т.д).
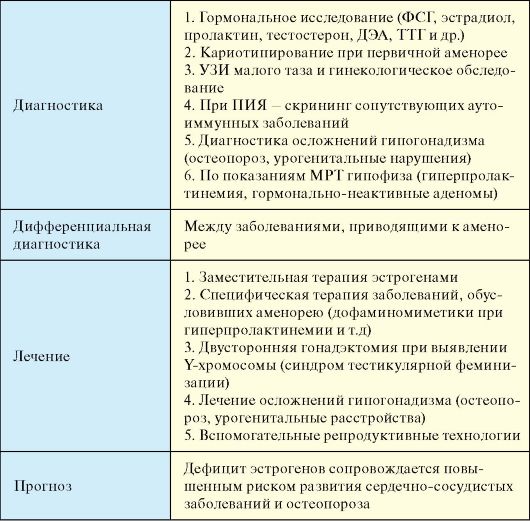
Диагностика
1. Гормональное исследование (рис. 5.3). Диагноз первичного гипогонадизма подтверждается двукратным выявлением повышенного уровня ФСГ (> 30 мЕд/л). Кроме того, при этом повышен уровень ЛГ и снижен уровень эстрадиола. Для вторичного гипогонадизма характерен низкий уровень гонадотропинов и эстрадиола. Всем пациенткам со вторичной аменорей показано определение уровня пролактина и ТТГ, по показаниям - ДЭА и тестостерона.
2. Кариотипирование показано всем женщинам с первичной аменореей.
3. УЗИ малого таза и гинекологическое обследование.
4. При ПИЯ показан скрининг сопутствующих аутоиммунных заболеваний, в первую очередь, определение уровня ТТГ.
5. Диагностика осложнений гипогонадизма, к которым относятся остеопороз (костная денситометрия), урогенитальные нарушения.
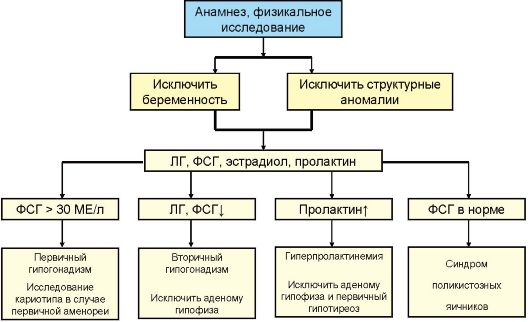 Рис. 5.3. Алгоритм обследования женщин с аменореей
Рис. 5.3. Алгоритм обследования женщин с аменореей
6. По показаниям МРТ гипофиза (гиперпролактинемия, гормонально-неактивные аденомы).
Дифференциальная диагностика
Проводится между многочисленными заболеваниями, приводящими к аменорее.
Лечение
♦ Заместительная терапия эстрогенами (за исключением случаев отсутствия матки - в комбинации с гестагенами) показана при первичном и вторичном гипогонадизме. Она проводится минимум вплоть до возраста, соответствующего естественному наступлению менопаузы (около 50 лет).
♦ Специфическая терапия заболеваний, обусловивших аменорею (дофаминомиметики при гиперпролактинемии, хирургическое лечение при гормонально-неактивных аденомах гипофиза, антиандрогенная терапия и т.д).
♦ При выявлении Y-хромосомы (синдром тестикулярной феминизации) показана двусторонняя гонадэктомия с целью предупреждения развития гонадобластомы.
♦ Лечение осложнений гипогонадизма (остеопороз, урогенитальные расстройства).
♦ Вспомогательные репродуктивные технологии (экстракорпоральное оплодотворение) при многих заболеваниях, протекающих с первичной и вторичной аменореей, позволяют планировать беременность.
Прогноз
Зависит от заболевания, приведшего к аменорее. Смертность среди женщин с гипогонадизмом различного генеза существенно выше, чем в общей популяции. Дефицит эстрогенов сопровождается повышенным риском развития сердечно-сосудистых заболеваний и остеопороза.
5.4. КЛИМАКТЕРИЧЕСКИЙ СИНДРОМ
Климактерический период - физиологический период жизни, обусловленный возрастными инволютивными изменениями репродуктивной системы. В нем выделяют следующие этапы: пременопаузу - период, предшествующий менопаузе (около 2-5 лет), менопаузу - последнее менструальное кровотечение, постменопаузу - период жизни, наступающий спустя год после менопаузы.
Этиология и патогенез
Одной из возможных причин снижения функции яичников в пременопаузе является уменьшение в них количества рецепторов к гонадотропинам, в результате чего происходит постепенное снижение продукции эстрадиола, прогестерона, андростендиона и тестостерона; яичники уменьшаются в 2-3 раза. Выпадение трофических эффектов эстрадиола на мочеполовую систему и кости приводит к развитию осложнений, к которым относится атрофический вагинит, мочепузырные расстройства и остеопороз. С наступлением менопаузы развиваются атерогенные изменения липидного спектра, способствующие развитию атеросклероза.
Эпидемиология
Как правило, менопауза наступает в возрасте между 45 и 55 годами (чаще в 50-51 год). У курящих женщин менопауза наступает в среднем на 2 года раньше.
Табл. 5.4. Климактерический синдром
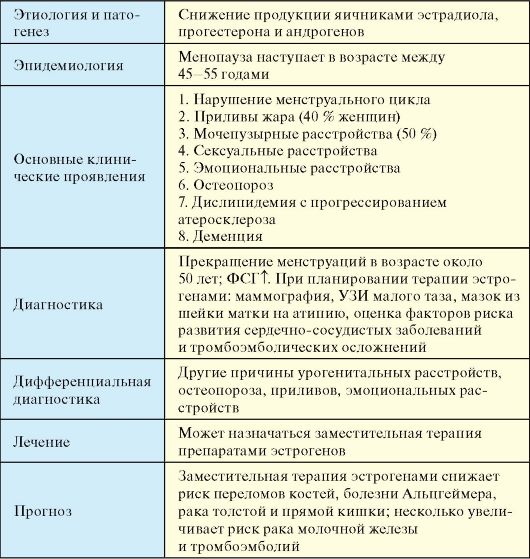 Клинические проявления
Клинические проявления
1. Нарушение менструального цикла у 90 % женщин начинается уже примерно за 4 года до менопаузы.
2. Приливы жара (40 % женщин) часто сочетаются с потливостью и покраснением кожи и в большинстве случаев заканчиваются спустя 5 лет после менопаузы.
3. Мочепузырные расстройства (50 %) вследствие атрофии уретры и шейки мочевого пузыря проявляются недержанием мочи (при кашле, смехе, быстрой ходьбе), частыми циститами и пиелонефритами.
4. Сексуальные расстройства: снижение либидо, сухость влагалища, диспареуния.
5. Эмоциональные расстройства: раздражительность, перепады настроения, депрессия, фобии.
6. Остеопороз, сопровождающийся повышенным риском переломов костей.
7. Осложнения атеросклероза, в первую очередь, ИБС.
8. Деменция; у женщин болезнь Альцгеймера развивается в 2-3 раза чаще, чем у мужчин и в ее патогенезе придается значение дефициту эстрогенов.
Диагностика
Прекращение менструаций у женщин в возрасте около 50 лет обычно само по себе свидетельствует о наступлении постменопаузы. В ряде случаев факт ее наступления нужно подтверждать при гормональном исследовании, которое выявляет повышенный уровень ФСГ и сниженный уровень эстрадиола. Степень повышения уровня ФСГ не коррелирует с выраженностью постменопаузальных симптомов и осложнений. Если женщине планируется назначение заместительной гормональной терапии эстрогенами, предварительно необходимо провести следующие обследования: маммография, УЗИ малого таза, мазок из шейки матки на атипию, оценка факторов риска развития сердечно-сосудистых заболеваний и тромбоэмболических осложнений.
Дифференциальная диагностика
Другие причины урогенитальных заболеваний, остеопороза, приливов, эмоциональных расстройств.
Лечение
Заместительная терапия эстрогенами может назначаться с целью купирования симптомов (приливы, урогенитальные симптомы, атрофический вагинит), а также с целью предотвращения отдаленных осложнений, характерных для климактерического синдрома (остеопороз, ИБС, деменция). Эстрогены (при наличии матки - в комбинации с прогестинами) могут назначаться в виде таблеток, накожных пластырей и вагинальных свечей. При помощи эстрогенов обычно достаточно легко купируются такие симптомы как приливы, сухость влагалища и урогенитальные расстройства. В тоже время единое мне-
ние о целесообразности длительной заместительной терапии эстрогенами в постменопаузе отсутствует.
Прогноз
Заместительная терапия эстрогенами в постменопаузе позволяет на 50 % снизить риск переломов костей, болезни Альцгеймера, а также рака толстой и прямой кишки. Существуют данные о небольшом повышении риска рака молочной железы и тромбоэмболий.
5.5. СИНДРОМ ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ
Синдром поликистозных яичников (СПЯ) - гетерогенный клинический синдром, характеризующийся гиперандрогенией и овуляторной дисфункцией (табл. 5.5). Впервые СПЯ описан Д. Штейном и Д. Левенталем в 1935 г.
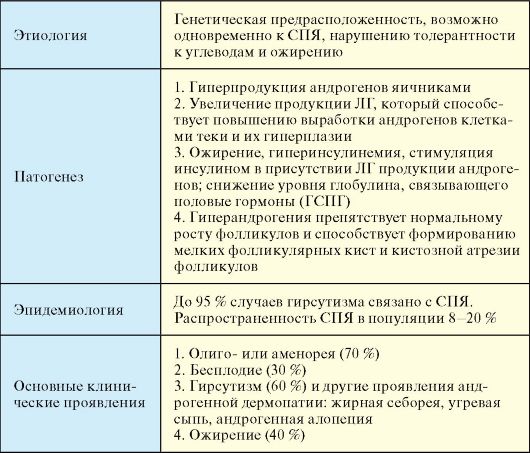
Табл. 5.5. Синдром поликистозных яичников
 Окончание табл. 5.5
Окончание табл. 5.5
 Этиология
Этиология
Большое значение имеет генетическая предрасположенность; предполагается полигенный характер наследования. Среди генов кандидатов рассматриваются гены, участвующие в биосинтезе инсулина и стероидных гормонов: INS, VNTR, CYP11 и другие. Вероятно, генетическая предрасположенность к СПЯ сходна с таковой для сахарного диабета 2 типа (СД-2) и ожирения (см. п. 7.6). Семейный анамнез большинства пациенток к СПЯ отягощен по ожирению, СД-2 и другим компонентам так называемого метаболического синдрома (см. п. 11.2).
Патогенез
1. В основе патогенеза лежит гиперпродукция андрогенов яичниками; наряду с этим в избыточных количествах могут продуцироваться и надпочечниковые андрогены. Причина нарушения функции яичников не вполне понятна. Так, описано нарушение активности фермента P450c17α, но, вероятно, это не первичный дефект, а маркер повышения стероидпродуцирующей активности яичника.
2. При СПЯ определяется повышение частоты и амплитуды продукции гонадотропин-рилизинг-гормона, в результате чего повышается продукция ЛГ; вероятно это является следствием ановуляции и низкого уровня прогестерона. Избыток ЛГ способствует повышению продукции андрогенов клетками теки и их гиперплазии.
3. У большинства пациентов с СПЯ имеется той или иной выраженности ожирение и, как следствие, гиперинсулинемия. Рецепторы инсулина и ИРФ-1 обнаруживаются в строме яичника, при этом инсулин в присутствии ЛГ может стимулировать продукцию андрогенов. Кроме того, инсулин способствует снижению уровня глобулина, связывающего половые гормоны (ГСПГ), что усугубляет гиперандрогению, т.к. способствует увеличению уровня свободных фракций андрогенов и эстрогенов (рис. 5.4).
4. Гиперандрогения препятствует нормальному росту фолликулов и способствует формированию мелких фолликулярных кист и кистозной атрезии фолликулов (поликистоз). При СПЯ происходит 3-6-кратное увеличение размеров яичников; у большинства пациентов выявляется склерозирование и значительное утолщение белочной оболочки.
Эпидемиология
Является одной из самых частых эндокринопатий у женщин репродуктивного возраста. До 95 % случаев гирсутизма у женщин связано с СПЯ. Распространенность СПЯ в популяции варьирует от 8 % (если
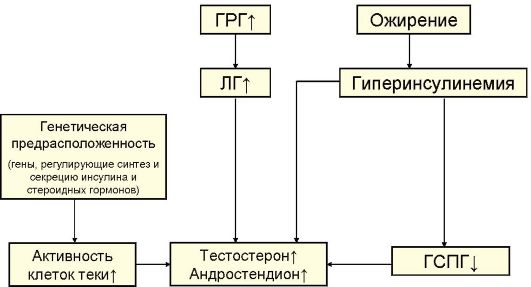 Рис. 5.4. Патогенез синдрома поликистозных яичников
Рис. 5.4. Патогенез синдрома поликистозных яичников
для диагностики использовать только данные клинической картины) и до 20 % (если использовать данные УЗИ).
Клинические проявления
♦ Клиническая картина значительно варьирует; заболевание, как правило, начинается в молодом возрасте, по времени совпадает с менархе, началом половой жизни, беременностью, значительной прибавкой веса.
♦ Олигоили аменорея (70 %) является следствием ановуляции. Обычно появляются задержки цикла до 3-6 месяцев, выделения становятся скудными; встречаются дисфункциональные маточные кровотечения.
♦ Бесплодие (30 %) как следствие хронической ановуляции.
♦ Гирсутизм (60 %) - избыточный рост волос в андроген-зависимых зонах. Могут наблюдаться и другие проявления андрогенной дермопатии: жирная себорея, угревая сыпь, андрогенная алопеция. Из других проявлений вирильного синдрома при СПЯ у 40 % больных при гинекологическом осмотре обнаруживается гипертрофия клитора.
♦ Ожирение (40 %); при усилении ожирения происходит усугубление выраженности других симптомов, поскольку усиление инсулинорезистентности способствует повышению уровня андрогенов.
Диагностика
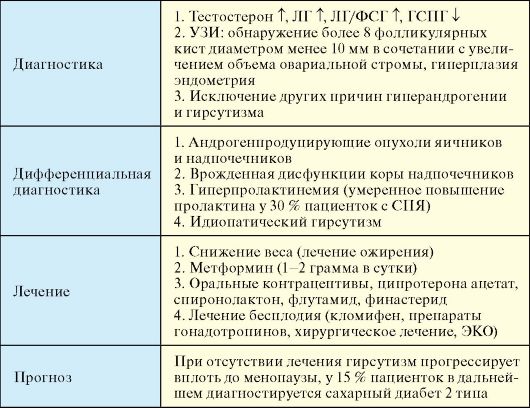
1. Уровень тестостерона чаще умеренно повышен, но у многих женщин с СПЯ остается в пределах нормы и не всегда коррелирует с выраженностью гирсутизма.
2. Уровень ЛГ повышен у 50-70 % женщин, при этом характерно увеличение соотношения ЛГ/ФСГ (>3) (в последнее время не рассматривается как диагностический критерий).
3. Уровень ГСПГ снижен у 50 % женщин.
4. Наиболее ценным инструментальным исследованием в диагностике СПЯ является УЗИ малого таза трансвагинальным датчиком. Ультразвуковым критерием СПЯ является обнаружение более 8 фолликулярных кист диаметром менее 10 мм в сочетании с увеличением объема овариальной стромы (рис. 5.5). Кроме того, обнаруживается гиперплазия эндометрия (толщина >10 мм).
5. С целью диагностики сахарного диабета или нарушения толерантности к углеводам необходимо определение уровня гликемии и, при необходимости, проведение орального глюкозотолерантного
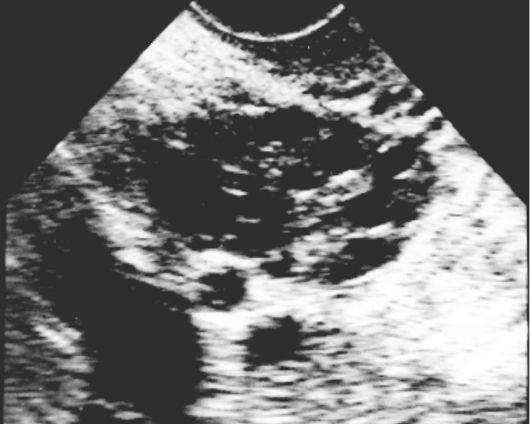 Рис. 5.5. Увеличение яичника, большое количество эхонегативных включений. Синдром поликистозных яичников (трансвагинальная эхограмма)
Рис. 5.5. Увеличение яичника, большое количество эхонегативных включений. Синдром поликистозных яичников (трансвагинальная эхограмма)
теста. Считается, что диагноз СПЯ может быть установлен при наличии 2-х из 3-х следующих признаков: ановуляция (бесплодие), лабораторно подтвержденная гиперандрогения, ультразвуковые признаки поликистозного изменения яичников.
Дифференциальная диагностика
1. Андрогенпродуцирующие опухоли яичников являются достаточно редким заболеванием. Для них характерно быстро прогрессирующий и тяжелый гирсутизм, вирилизация и значительное повышение уровня тестостерона (> 5-10 нмоль/л). Для крайне редко встречающихся андрогенпродуцирующих опухолей надпочечников характерна аналогичная симптоматика в сочетании со значительным повышением уровня ДЭА и андростендиона.
2. Для исключения врожденной дисфункции коры надпочечников (п. 4.6) проводится определение уровня 17-гидроксипрогестерона и ДЭА, при необходимости - проба с 1-24АКТГ.
3. Гиперпролактинемия может первично обусловливать сходную клиническую картину (см. п. 2.4), наряду с этим умеренное повышение уровня пролактина встречается у 30 % пациенток с СПЯ.
4. Идиопатический гирсутизм - состояние, при котором у женщин развиваются гирсутизм и гипертрихоз на фоне неизмененного менструального цикла и сохранения фертильности.
5. Бесплодие и нарушение менструальной функции другого генеза. Лечение
1. Снижение веса (лечение ожирения). Зачастую нормализация менструальной и овуляторной функций, а также регресс гирсутизма происходит за счет одной только нормализации массы тела.
2. Среди сенситайзеров инсулина свою эффективность показал метформин (см. п. 7.6). Назначение препарата (1-2 грамма в сутки) целесообразно при клинических и лабораторных данных, свидетельствующих об инсулинорезистентности, при этом следует помнить, что метформин противопоказан при беременности.
3. Антиандрогенная терапия:
- оральные контрацептивы. Их эстрогеновый компонент подавляет продукцию андрогенов в яичнике и приводит к повышению уровня ГСПГ, а гестагенный компонент подавляет продукцию ЛГ. Чаще всего назначается фиксированная комбинация этинилэстрадиола с ципротероном ацетатом, который обладает антиандрогенной активностью;
- ципротерона ацетат является блокатором андрогеновых рецепторов (25-100 мг во второй фазе цикла, как правило, в комбинации с эстрогенами);
- спиронолактон, обладающий слабой антиандрогенной активностью (может назначаться в дозе 50-200 мг в день);
- флутамид (125 мг в сутки) обладает выраженной антиандрогенной активностью, но из-за возможных тяжелых побочных эффектов для лечения СПЯ используется редко;
- финастерид (5 мг в сутки) является ингибитором 5α-редуктазы.
4. Лечение бесплодия:
- кломифена цитрат (25-150 мг с 5 дня менструального цикла в течение 5 дней) снижает влияние эстрогенов на гипофиз и способствует повышению продукции ФСГ, стимулирующего рост фолликулов. Овуляция на фоне терапии кломифеном развивается у 80 % пациенток, беременность - у 65 %;
- препараты гонадотропинов (рекомбинантный человеческий ФСГ) используется при неэффективности кломифена. Овуляции удается достичь в 94 % случаев, беременность после
нескольких курсов введения препарата наступает в 40 % случаев;
- хирургическое лечение подразумевает лапароскопическую диатермию или лазерный дриллинг. В прошлом хирургическое лечение чаще всего подразумевало открытую секторальную резекцию яичников. Механизм временного восстановления овуляторной функции в результате таких операций не вполне понятен. Овуляция после операции восстанавливается у 90 % женщин, беременность в ближайшие 8 месяцев наступает у 80 %;
- экстракорпоральное оплодотворение.
Прогноз
Развивающийся при СПЯ гирсутизм при отсутствии лечения постепенно прогрессирует вплоть до менопаузального возраста, после чего начинает спонтанно разрешаться. У 15 % женщин с СПЯ в дальнейшем развивается сахарный диабет 2 типа; с повышенной частотой развивается артериальная гипертензия и дислипидемии.