Атлас по физиологии. В двух томах. Том 1: учеб. пособие / А. Г. Камкин, И. С. Киселева - 2010. - 408 с. : ил.
|
|
|
|
Глава 4. Физиология мышц
Общие представления о строении различных мышц
Многие клетки обладают ограниченной способностью преобразовывать химическую энергию в механическую силу и движение, но только в мышечных волокнах этот процесс занял главное место. Основная функция этих специализированных клеток состоит в генерировании силы и движений, которые организм использует, чтобы регулировать внутреннюю среду и перемещаться во внешнем пространстве.
На основании структуры, сократительных свойств и механизмов регуляции различают три вида мышечной ткани:
1) скелетные мышцы;
2) гладкая мускулатура;
3) сердечная мышца (миокард).
Скелетные мышцы, как следует из их названия, прикреплены, как правило, к костям скелета; благодаря сокращениям этих мышц поддерживается положение скелета в пространстве и происходят его движения. Сокращения возникают под влиянием импульсов от нервных клеток и обычно бывают произвольными.
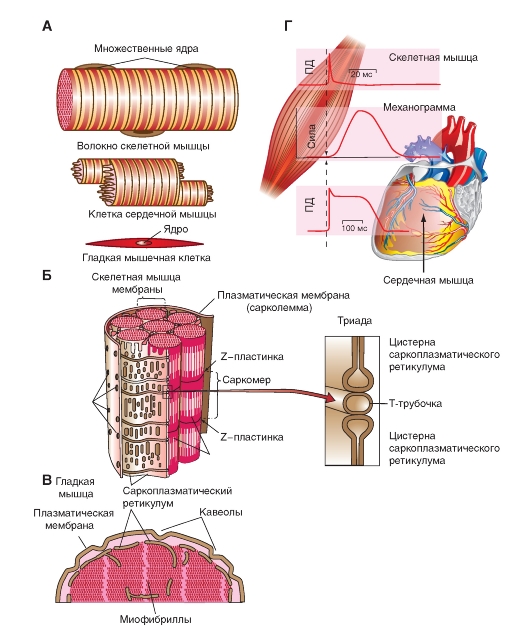
На рисунке 4-1 А представлены волокна скелетной мышцы (верхняя панель), клетка сердечной мышцы (средняя панель) и клетка гладкой мышцы (нижняя панель). Клетка скелетной мышцы называется мышечным волокном. В процессе эмбрионального развития каждое мышечное волокно формируется путем слияния многих недифференцированных одноядерных клеток (миобластов) в одну цилиндрическую многоядерную клетку. Дифференцировка скелетных мышц завершается примерно к моменту рождения. В период от младенческого до взрослого состояния организма размеры дифференцированных мышечных волокон продолжают увеличиваться, но новые волокна из миобластов не образуются. У взрослого человека диаметр мышечных волокон достигает 10-100 мкм, длина - до 20 см.
Если в постнатальный период происходит повреждение скелетных мышечных волокон, они не могут замещаться путем деления сохранившихся волокон, однако новые волокна образуются из недифференцированных клеток, так называемых клеток-сателлитов, расположенных рядом с мышечными волокнами и подвергающихся дифференцировке аналогично эмбриональным миобластам. Возможности формирования новых волокон в скелетной мышце значительны, однако после сильного повреждения она целиком уже не восстанавливается. Важную роль в компенсации
утраченной мышечной ткани играет увеличение неповрежденных мышечных волокон.
На рисунке рис. 4-1 А, Г представлена также сердечная мышца (миокард), которая обеспечивает работу сердца.
Слои гладких мышц находятся в стенках полых внутренних органов и трубчатых образований: желудка, кишечника, мочевого пузыря, матки, кровеносных сосудов, бронхов. В результате сокращений гладких мышц проталкивается содержимое полых органов, регулируется ток жидкости в сосудах и протоках путем изменений их диаметра. Маленькие пучки гладкомышечных клеток находятся также в коже около волосяных сумок и в радужной оболочке глаза. Сокращениями гладких мышц управляет вегетативная нервная система, гормоны, аутокринные / паракринные факторы, другие местные химические сигналы. Некоторые гладкие мышцы спонтанно сокращаются даже при отсутствии сигналов. В отличие от скелетных мышц, гладкая мускулатура не имеет произвольной регуляции.
Несмотря на существенные различия между этими тремя видами мышц, у них сходный механизм генерирования силы. Сначала будут рассмотрены скелетные мышцы, затем гладкая мускулатура. Сердечная мышца характеризуется сочетанием ряда свойств двух первых видов мышц.
Наиболее примечательная характеристика волокон скелетной, а также сердечной мышц при изучении с помощью светового микроскопа - чередование светлых и темных полос, поперечных по отношению к длинной оси волокна. Благодаря этой особенности оба типа мышц относят к поперечнополосатым мышцам (рис. 4-1 А, верхняя и средняя панели). В гладкой мышце такая картина отсутствует (рис. 4-1 А, нижняя панель).
В скелетной мышце толстые и тонкие филаменты образуют периодический рисунок вдоль каждой миофибриллы. Регулярно повторяющийся элемент этого рисунка известен как саркомер (от греч. sarco - мышца, mere - маленький) (увеличенный фрагмент на рис. 4-1 Б). Каждый саркомер включает в себя триаду:
1) цистерну саркоплазматического ретикулума;
2) поперечную тубулу;
3) еще одну цистерну саркоплазматического ретикулума (рис. 4-1 Б).
На рисунке 4-1 В представлено строение гладкой мышцы, которое отличается от скелетной.
Совмещенный рисунок 4-1 Г демонстрирует синхронную запись потенциалов действия, а также механограмму скелетной мышцы и мышцы сердца.
Рис. 4-1. Организация волокон и филаментов в скелетной и гладкой мышцах
Типы мышц
Существуют три типа мышц: скелетные, гладкие и миокард. Скелетные мышцы прикреплены к костям, осуществляя их поддержку и движение. Гладкая мускулатура окружает полые и трубчатые органы. Сердечная мышца (миокард) обеспечивает работу сердца.
Скелетные мышцы
1. Скелетные мышцы состоят из цилиндрических мышечных волокон (клеток); каждый конец мышцы соединен посредством сухожилий с костями.
2. Волокна скелетных мышц характеризуются периодическим чередованием светлых и темных полос, отражающих пространственную организацию толстых и тонких филаментов в миофибриллах.
3. Тонкие филаменты, содержащие актин, прикреплены на обоих краях саркомера к Z-поло- сам; свободные концы тонких филаментов частично перекрываются с миозинсодержащими толстыми филаментами в А-полосе центральной части саркомера.
4. Во время активного укорочения скелетного мышечного волокна тонкие филаменты подтягиваются по направлению к центру саркомера в результате движений миозиновых поперечных мостиков, которые связываются с актином:
- две глобулярные головки каждого поперечного мостика содержат участок связывания с актином, а также фермент, расщепляющий АТФ;
- каждый рабочий цикл поперечного мостика состоит из четырех стадий. Во время сокращения поперечные мостики совершают повторные циклы, каждый из которых обеспечивает очень маленькое продвижение тонких филаментов;
- АТФ выполняет во время мышечного сокращения три функции.
5. В покоящейся мышце прикрепление поперечных мостиков к актину заблокировано молекулами тропомиозина, контактирующими с субъединицами актина тонких филаментов.
6. Сокращение инициируется в результате повышения цитоплазматической концентрации Са2+. При связывании ионов Са2+ с тропонином изменяется его конформация, благодаря чему тропомиозин смещается, открывая доступ к участкам связывания на молекулах актина; поперечные мостики связываются с тонкими филаментами:
- повышение цитоплазматической концентрации Са2+ запускается потенциалом действия
плазматической мембраны. Потенциал действия распространяется вглубь волокна вдоль поперечных трубочек к саркоплазматическому ретикулуму и вызывает высвобождение Са2+ из ретикулума;
- расслабление мышечного волокна после сокращения происходит в результате активного обратного транспорта Са2+ из цитоплазмы в саркоплазматический ретикулум.
7. Окончания двигательного аксона образуют нервно-мышечные соединения с мышечными волокнами двигательной единицы соответствующего мотонейрона. Каждое мышечное волокно иннервируется ветвью только одного мотонейрона:
- АЦХ, высвобождаемый из двигательных нервных окончаний при поступлении потенциала действия мотонейрона, связывается с рецепторами двигательной концевой пластинки мышечной мембраны; открываются ионные каналы, пропускающие Na+ и К+, благодаря чему концевая пластинка деполяризуется;
- одного потенциала действия мотонейрона достаточно, чтобы вызвать потенциал действия в волокне скелетной мышцы.
8. Существует определенная последовательность процессов, ведущих к сокращению скелетного мышечного волокна.
9. Понятие «сокращение» относится к включению рабочего цикла поперечных мостиков. Изменяется ли при этом длина мышцы, зависит от действия на нее внешних сил.
10. При активации мышечного волокна возможны три типа сокращения:
- изометрическое сокращение, когда мышца генерирует напряжение, но ее длина не меняется;
- изотоническое сокращение, когда мышца укорачивается, перемещая нагрузку;
- удлиняющее сокращение, когда внешняя нагрузка заставляет мышцу удлиняться во время сократительной активности.
11. Повышение частоты потенциалов действия мышечного волокна сопровождается увеличением механической реакции (напряжения или укорочения) до тех пор, пока не будет достигнут максимальный уровень тетанического напряжения.
12. Максимальное изометрическое тетаническое напряжение развивается в случае оптимальной длины саркомера Lо. При растяжении волокна более его оптимальной длины или уменьшении длины волокна менее Lо генерируемое им напряжение падает.
13. Скорость укорочения мышечного волокна снижается при повышении нагрузки. Максимальная скорость соответствует нулевой нагрузке.
14. АТФ образуется в мышечных волокнах следующими способами: перенос фосфата с креатинфосфата к АДФ; окислительное фосфорилирование АДФ в митохондриях; субстратное фосфорилирование АДФ в процессе гликолиза.
15. В начале физического упражнения главным источником энергии служит мышечный гликоген. При более длительном упражнении энергия образуется в основном за счет глюкозы и жирных кислот, поступающих с кровью; по мере дальнейшего продолжения физической деятельности возрастает роль жирных кислот. Когда интенсивность физической работы превысит ~70% от максимума, все более значительную часть образующейся АТФ начинает обеспечивать гликолиз.
16. Мышечное утомление обусловлено рядом факторов, включая изменения кислотности внутриклеточной среды, уменьшение запасов гликогена, нарушение электромеханического сопряжения, но не истощение АТФ.
17. Различают три типа скелетных мышечных волокон в зависимости от максимальной скорости укорочения и преобладающего способа образования АТФ: медленные оксидативные, быстрые оксидативные и быстрые гликолитические:
- разная максимальная скорость укорочения быстрых и медленных волокон обусловлена различиями АТФазы миозина: высокой и низкой АТФазной активности соответствуют быстрые и медленные волокна;
- быстрые гликолитические волокна имеют в среднем больший диаметр, чем оксидативные, и потому развивают более значительное напряжение, однако быстрее утомляются.
18. Все мышечные волокна одной двигательной единицы принадлежат к одному и тому же типу; большинство мышц содержат все три типа двигательных единиц.
19. Известны характеристики трех типов скелетных мышечных волокон.
20. Напряжение целой мышцы зависит от величины напряжения, развиваемого каждым волокном, и от количества активных волокон в мышце.
21. Мышцы, выполняющие тонкие движения, состоят из двигательных единиц с небольшим числом волокон, тогда как большие мышцы, обеспечивающие поддержание позы тела, состоят из гораздо более крупных двигательных единиц.
22. Быстрые гликолитические двигательные единицы содержат волокна большего диаметра и, кроме того, их двигательные единицы имеют более значительное число волокон.
23. Повышение мышечного напряжения происходит прежде всего путем увеличения количества активных двигательных единиц, т.е. их вовлечения. В начале сокращения первыми вовлекаются медленные оксидативные двигательные единицы, затем быстрые оксидативные и, наконец, уже при очень интенсивном сокращении, быстрые гликолитические единицы.
24. Вовлечение двигательных единиц сопровождается повышением скорости, с которой мышца перемещает нагрузку.
25. Силу и утомляемость мышцы можно изменить посредством тренировки:
- продолжительныеупражнения низкой интенсивности повышают способность мышечных волокон к образованию АТФ окислительным (аэробным) путем. Это происходит благодаря увеличению количества митохондрий и кровеносных сосудов в мышце. В итоге возрастает выносливость мышцы;
- кратковременные упражнения высокой интенсивности увеличивают диаметр волокон вследствие повышения синтеза актина и миозина. В итоге возрастает мышечная сила.
26. Движения суставов осуществляются посредством двух антагонистических групп мышц: сгибателей и разгибателей.
27. Мышцы вместе с костями представляют собой системы рычагов; чтобы конечность могла удержать груз, изометрическое напряжение мышцы должно существенно превысить массу этого груза, зато скорость перемещения плеча рычага гораздо больше, чем скорость укорочения мышцы.
Гладкие мышцы
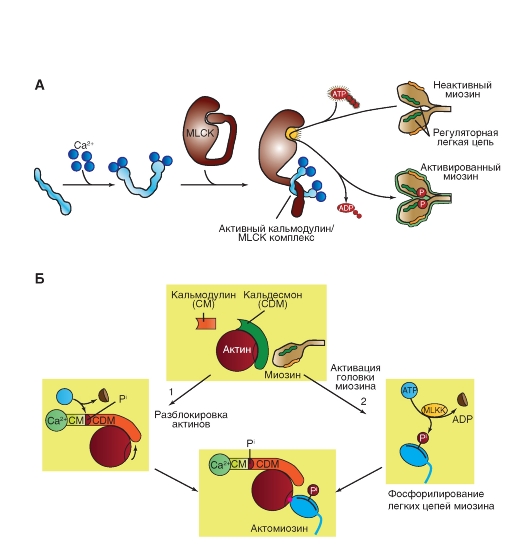
1. Гладкие мышцы можно классифицировать на две большие группы: унитарные гладкие мышцы и мультиунитарные гладкие мышцы.
2. Гладкомышечные волокна - веретенообразные клетки без поперечной исчерченности, с одним ядром, способны к делению. Они содержат актиновые и миозиновые филаменты и сокращаются посредством механизма скользящих нитей.
3. Повышение концентрации Са2+ в цитоплазме ведет к связывания Са2+ с кальмодулином. Затем комплекс Са2+-кальмодулин связывается с киназой легких цепей миозина, активируя этот фермент, фосфорилирующий миозин. Только после фосфорилирования
гладкомышечный миозин может связываться с актином и осуществлять циклические движения поперечных мостиков.
4. Миозин гладких мышц гидролизует АТФ с относительно низкой скоростью, поэтому гладкие мышцы укорачиваются гораздо медленнее, чем поперечно-полосатые. Однако напряжение в расчете на единицу площади поперечного сечения для гладкой мышцы такое же, как для поперечно-полосатой.
5. Ионы Са2+, инициирующие сокращение гладкой мышцы, поступают из двух источников: саркоплазматического ретикулума и внеклеточной среды. В результате открывания кальциевых каналов плазматической мембраны и саркоплазматического ретикулума, которое опосредуется различными факторами, Са2+ поступает в цитоплазму.
6. Большинство стимулирующих факторов повышают цитоплазматическую концентрацию Са2+ не настолько, чтобы произошла активация всех поперечных мостиков клетки. Именно поэтому факторы, повышающие концентрацию Са2+ в цитоплазме, могут усиливать напряжение гладкой мышцы.
7. Существуют определенные типы стимулов, вызывающих сокращение гладкой мышцы благодаря открыванию кальциевых каналов плазматической мембраны и саркоплазматического ретикулума.
8. В плазматической мембране большинства гладкомышечных клеток (но не всех) при ее деполяризации могут генерироваться потенциалы действия. Восходящая фаза потенциала действия гладкой мышцы обусловлена входом Са2+ в клетку через открывшиеся кальциевые каналы.
9. В некоторыхгладких мышцах потенциалы действия генерируются спонтанно, при отсутствии внешних стимулов. Это происходит благодаря тому, что в плазматической мембране периодически возникают пейсмекерные потенциалы, деполяризующие мембрану до порогового уровня.
10. Гладкомышечные клетки лишены специализированных концевых пластинок. Некоторые гладкомышечные волокна подвергаются действию нейромедиаторов, высвобождаемых из варикозных утолщений одиночной ветви нерва, причем каждое волокно может находиться под влиянием нейромедиаторов более чем одного нейрона. Действие нейромедиаторов на сокращения гладких мышц может быть возбуждающим либо тормозным.
Мышца сердца
1. Потенциалы действия с быстрым ответом регистрируются от предсердных и желудочковых волокон миокарда и от специализированных волокон проводящей системы желудочков (волокна Пуркинье). Потенциал действия характеризуется большой амплитудой, крутым нарастанием и относительно длинным плато.
2. Потенциалы действия с медленным ответом регистрируются в клетках SA- и AV-узлов и в аномальных кардиомиоцитах, которые были частично деполяризованы. Потенциал действия характеризуется менее негативным потенциалом покоя, меньшей амплитудой, менее крутым нарастанием и более коротким плато, чем потенциал действия с быстрым ответом. Нарастание генерируется за счет активации Са2+-каналов.
3. Потенциалы действия характеризуются эффективным рефрактерным периодом (фаза абсолютной рефрактерности).
4. Автоматия характерна для некоторых клеток SA- и AV-узлов и для клеток проводящей системы желудочков. Признаком автоматии служит медленная деполяризация мембраны в течение фазы 4 (медленная диастолическая деполяризация).
5. В норме SA-узел инициирует импульс, вызывающий сокращение сердца. Этот импульс распространяется из SA-узла по ткани предсердий и в конечном счете достигает AV-узла. После задержки в AV-узле сердечный импульс распространяется по желудочкам.
6. Увеличение длины волокон миокарда, как бывает при увеличенном желудочковом наполнении (при преднагрузке) во время диастолы, вызывает более сильное сокращение желудочков. Соотношение между длиной волокон и силой сокращения известно как соотношение Франка-Старлинга или как закон сердца Франка-Старлинга.
7. Несмотря на то, что миокард состоит из отдельных клеток, отделенных друг от друга мембранами, кардиомиоциты, из которых состоят желудочки, сокращаются почти в унисон, как и кардиомиоциты предсердий. Миокард функционирует как синцитий с реакцией типа «все или ничего» при возбуждении. Проведение возбуждения от клетки к клетке осуществляется через высоко проницаемые контакты - gap junctions, которыми соединены цитозоли смежных клеток.
Рис. 4-2. Общие представления о строении различных мышц (см. табл.)
8. При возбуждении потенциалуправляемые кальциевые каналы открываются, и внеклеточный Са2+ поступает в клетку. Приток Са2+ способствует высвобождению Са2+ из саркоплазматического ретикулума. Возросшая концентрация внутриклеточного Са2+ вызывает сокращение миофиламентов. Расслабление сопровождается восстановлением концентрации внутриклеточного Са2+ до уровня в состоянии покоя путем активного закачивания Са2+ назад в саркоплазматический ретикулум и обмена Са2+ на внеклеточный Na+ через сарколемму.
9. Скорость и сила сокращений зависят от внутриклеточной концентрации свободных ионов
кальция. Сила и скорость обратно пропорциональны друг другу, так что при отсутствии нагрузки скорость максимальна. Во время изоволюмического сокращения, когда нет внешнего укорочения, общая нагрузка максимальна, а скорость равна нулю.
10. При сокращении желудочков растягивание мышечных волокон кровью во время его наполнения служит преднагрузкой. Постнагрузкой является аортальное давление, преодолевая которое левый желудочек выталкивает кровь.
11. Сократительная способность отражает работу сердца при заданных величинах преднагрузки и постнагрузки.
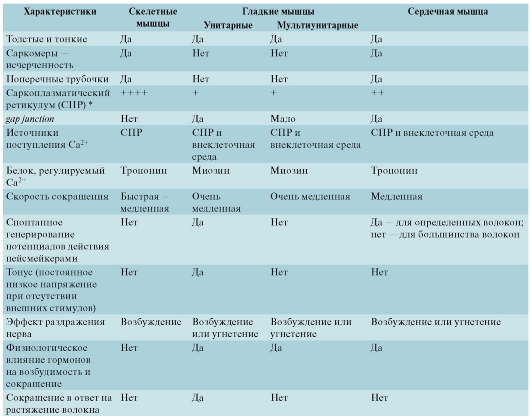
* Число знаков «плюс» (+) указывает на относительные размеры саркоплазматического ретикулума в мышцах конкретного типа.
Физиология скелетных мышц
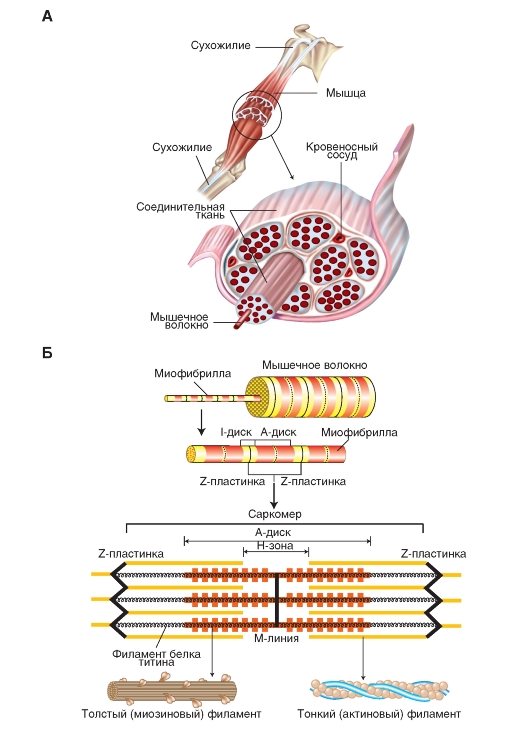
Понятие скелетная, или поперечно-полосатая мышца относится к группе мышечных волокон, связанных соединительной тканью (рис. 4-3 А). Обычно мышцы прикреплены к костям пучками коллагеновых волокон - сухожилиями, находящимися на обоих концах мышцы. В некоторых мышцах одиночные волокна имеют такую же протяженность, как и вся мышца, но в большинстве случаев волокна короче и часто располагаются под углом к продольной оси мышцы. Есть очень длинные сухожилия, они прикреплены к кости, удаленной от конца мышцы. Например, некоторые мышцы, осуществляющие движения пальцев рук, находятся в предплечье; шевеля пальцами, мы чувствуем, как двигаются мышцы кисти. Эти мышцы соединены с пальцами посредством длинных сухожилий.
При изучении с помощью светового микроскопа, основной характеристикой волокон скелетной мышцы оказалось чередование светлых и темных полос, поперечных по отношению к длинной оси волокна. Поэтому скелетные мышцы были названы поперечно-полосатыми.
Поперечная исчерченность волокон скелетной мышцы обусловлена особым распределением в их цитоплазме многочисленных толстых и тонких «нитей» (филаментов), объединяющихся в цилиндрические пучки диаметром 1-2 мкм - миофибриллы (рис. 4-3 Б). Мышечное волокно практически заполнено миофибриллами, они тянутся по всей его длине и на обоих его концах соединены с сухожилиями.
Толстые и тонкие филаменты образуют периодический рисунок вдоль каждой миофибриллы. Толстые филаменты состоят почти целиком из сократительного белка миозина. Тонкие филаменты (их толщина равна примерно половине диаметра толстого филамента) содержат сократительный белок актин, а также два других белка - тропонин
и тропомиозин, играющих важную роль в регуляции сокращения (см. ниже).
Толстые филаменты сосредоточены в средней части каждого саркомера, где они лежат параллельно друг другу; эта область выглядит как широкая темная (анизотропная) полоса, называемая А-полосой. В обеих половинах саркомера находится по набору тонких филаментов. Один конец каждого из них прикреплен к так называемой Z-пластинке (или Z-линии, или Z-полосе) - сети из переплетающихся белковых молекул, - а другой конец перекрывается с толстыми филаментами. Саркомер ограничен двумя последовательно расположенными Z-полосами. Таким образом, тонкие филаменты двух соседних саркомеров закреплены на двух сторонах каждой Z-полосы.
Светлая (изотропная) полоса - так называемая I-полоса - расположена между краями А-полос двух соседних саркомеров и состоит из тех участков тонких филаментов, которые не перекрываются с толстыми филаментами. Z-полоса делит I-полосу пополам.
В пределах А-полосы каждого саркомера различают еще две полоски. В центре А-полосы видна узкая светлая полоска - Н-зона. Она соответствует промежутку между противостоящими друг другу концами двух наборов тонких филаментов каждого саркомера, т.е. включает только центральные части толстых филаментов. Посередине Н-зоны находится совсем тонкая темная М-линия. Это сеть белков, соединяющих центральные части толстых филаментов. Кроме того, от Z-полосы к М-линии идут филаменты белка титина, связанные одновременно с белками М-линии и с толстыми филаментами. М-линия и титиновые филаменты поддерживают упорядоченную организацию толстых филаментов в середине каждого саркомера. Таким образом, толстые и тонкие филаменты не являются свободными, незакрепленными внутриклеточными структурами.
Рис. 4-3. Структура скелетных мышц.
А - организация цилиндрических волокон в скелетной мышце, прикрепленной к костям сухожилиями. Б - структурная организация филаментов в волокне скелетной мышцы, создающая картину поперечных полос. Показаны многочисленные миофибриллы в одиночном мышечном волокне, а также организация толстых и тонких филаментов в саркомере
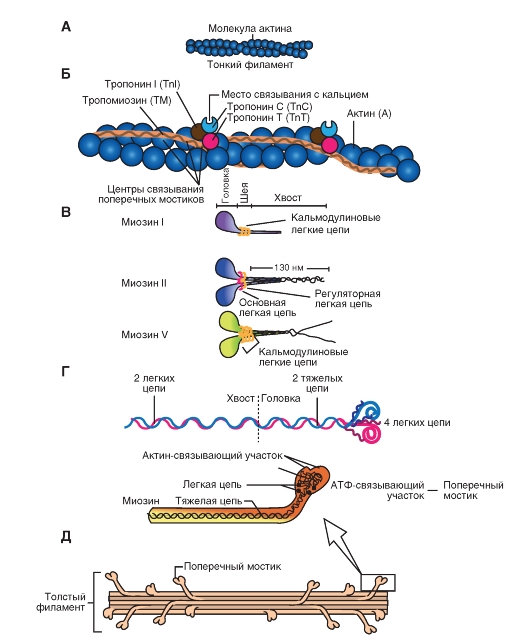
Молекула актина
Это глобулярный белок, состоящий из одного полипептида, который полимеризуется с другими молекулами актина и образует две цепи, обвивающие друг друга (рис. 4-4 А). Такая двойная спираль представляет собой остов тонкого филамента. На каждой молекуле актина есть участок связывания миозина. В покоящемся мышечном волокне взаимодействие между актином и миозином предотвращают два белка - тропонин и тропомиозин (рис. 4-4 Б).
Тропомиозин - стержневидная молекула из двух полипептидов, обвивающихся друг около друга; молекула соответствует в длину примерно семи мономерам актина. Цепи из молекул тропомиозина, уложенные конец в конец, располагаются вдоль всего тонкого филамента. Молекулы тропомиозина частично прикрывают участки связывания каждой молекулы актина, мешая контакту миозина с актином. В таком блокирующем положении молекула тропомиозина удерживается тропонином.
Тропонин - гетеротримерный белок. Он состоит из тропонина Т (отвечает за связывание с одиночной молекулой тропомиозина), тропонина С (связывает ион Са2+) и тропонина I (связывает актин и ингибирует сокращение). Каждая молекула тропомиозина связана с одной гетеротримерной молекулой тропонина, которая регулирует доступ к участкам связывания миозина на семи мономерах актина, прилегающих к молекуле тропомиозина.
Миозин
Это единое название большой семьи протеинов, имеющих определенные отличия в клетках разных тканей. Миозин присутствует у всех эукариотов. Около 60 лет назад было известно два типа миозина, которые сейчас называют миозин I и миозин II. Миозин II был первым из числа открытых миозинов, и именно он принимает участие в мышечном сокращении. Позднее были открыты миозин I и миозин V (рис. 4-4 В). В последнее время показано, что миозин II участвует в мышечном сокращении, тогда как миозин I и миозин V вовлечены в работу подмембранного (кортикального) цитоскелета. В настоящее время идентифицировано более 10 классов миозина. На рисунке 4-4 Г показано два варианта схемы строения миозина, который состоит из головки, шейки и хвоста. Молекула миозина состоит из двух больших полипептидов (тяжелых цепей) и четырех меньших (легких цепей). Эти полипептиды составляют молекулу с двумя глобулярными «головками», которые содержат оба вида цепей, и длинным стержнем («хвостом») из двух переплетенных тяжелых цепей. Хвост каждой молекулы миозина располагается вдоль оси толстого филамента, а две глобулярные головки выступают по бокам, их иначе называют поперечными мостиками. На каждой глобулярной головке находятся по два участка связывания: для актина и для АТФ. Участки связывания АТФ обладают также свойствами фермента АТФазы, гидролизующей связанную молекулу АТФ.
На рисунке 4-4 Д представлена упаковка молекул миозина. Выступающие головки миозина и есть поперечные мостики.
Рис. 4-4. Строение актина и миозина
Саркоплазматический ретикулум
В состоянии покоя в мышечном волокне концентрация свободного, ионизированного Са2+ в цитоплазме вокруг толстых и тонких филаментов очень низка, около 10-7 моль/л. При такой концентрации ионы Са2+ занимают очень небольшое количество участков связывания на молекулах тропонина (тропонина С), поэтому тропомиозин блокирует связывание с актином поперечных мостиков. После потенциала действия концентрация ионов Са2+ в цитоплазме быстро возрастает, и они связываются с тропонином, устраняя блокирующий эффект тропомиозина и инициируя цикл поперечных мостиков. Источником поступления Са2+ в цитоплазму служит саркоплазматический ретикулум мышечного волокна.
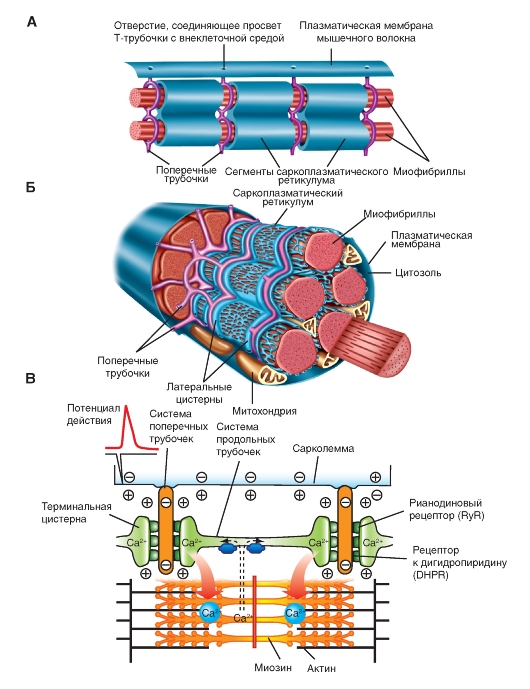
Саркоплазматический ретикулум мышц гомологичен эндоплазматическому ретикулуму других клеток. Он располагается вокруг каждой миофибриллы наподобие «рваного рукава», сегментами которого окружены А- и I-полосы. Концевые части каждого сегмента расширяются в виде так называемых латеральных мешков (терминальных цистерн), соединенных друг с другом серией более тонких трубок. В латеральных мешках депонируется Са2+, высвобождающийся после возбуждения плазматической мембраны (рис. 4-5 А).
Отдельную систему составляют поперечные трубочки (Т-трубочки), которые пересекают мышечное волокно на границе полос А-I, проходят между латеральными мешками двух смежных саркомеров и выходят на поверхность волокна, составляя единое целое с плазматической мембраной. Просвет Т-трубочки заполнен внеклеточной жидкостью, окружающей мышечное волокно (рис. 4-5 Б). Мембрана Т-трубочек, так же как плазматическая мембрана, способна к проведению потенциала действия. Возникнув в
плазматической мембране (рис. 4-5 В), потенциал действия быстро распространяется по поверхности волокна и по мембране Т-трубочек вглубь клетки. Достигнув области Т-трубочек, прилегающей к латеральным мешкам, потенциал действия активирует потенциалзависимые «воротные» белки мембраны Т-трубочек, физически или химически сопряженные с кальциевыми каналами мембраны латеральных мешков. Таким образом, деполяризация мембраны Т-трубочек, обусловленная потенциалом действия, приводит к открыванию кальциевых каналов мембраны латеральных мешков, содержащих Са2+ в высокой концентрации, и ионы Са2+ выходят в цитоплазму. Повышение цитоплазматического уровня Са2+ обычно бывает достаточным для активации всех поперечных мостиков мышечного волокна.
Процесс сокращения продолжается, пока ионы Са2+ связаны с тропонином, т.е. до тех пор, пока их концентрация в цитоплазме не вернется к низкому исходному значению. Мембрана саркоплазматического ретикулума содержит Са-АТФазу - интегральный белок, осуществляющий активный транспорт Са2+ из цитоплазмы обратно в полость саркоплазматического ретикулума. Как только что говорилось, Са2+ высвобождается из ретикулума в результате распространения потенциала действия по Т-трубочкам; для возвращения Са2+ в ретикулум нужно гораздо больше времени, чем для его выхода. Именно поэтому, повышенная концентрация Са2+ в цитоплазме сохраняется в течение некоторого времени, и сокращение мышечного волокна продолжается после завершения потенциала действия.
Подведем итог. Сокращение обусловлено высвобождением ионов Са2+, хранящихся в саркоплазматическом ретикулуме. Когда Са2+ поступает обратно в ретикулум, сокращение заканчивается и начинается расслабление.
Рис. 4-5. Саркоплазматический ретикулум и его роль в механизме сокращения мышцы.
А - схема организации саркоплазматического ретикулума, поперечных трубочек и миофибрилл. Б - схема анатомической структуры поперечных трубочек и саркоплазматического ретикулума в индивидуальном волокне скелетной мышцы. В - роль саркоплазматического ретикулума в механизме сокращения скелетной мышцы
Электромеханическое сопряжение
Это последовательность процессов, в результате которых потенциал действия плазматической мембраны мышечного волокна приводит к запуску сокращения мышцы или к так называемому циклу поперечных мостиков, который будет продемонстрирован далее.
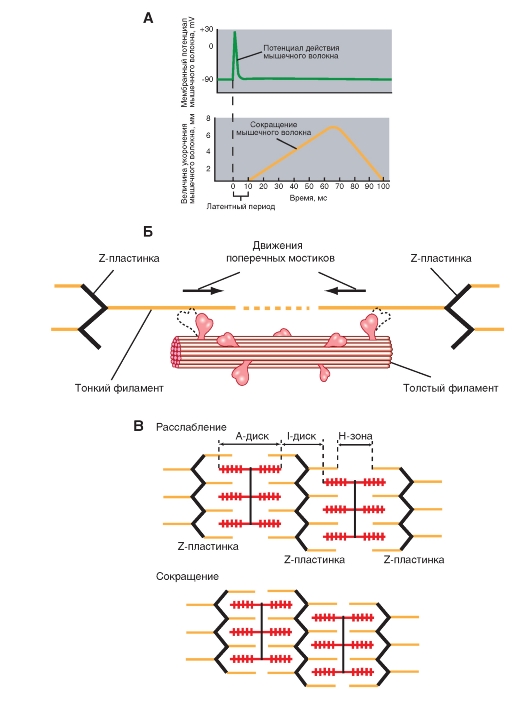
Плазматическая мембрана скелетных мышц электрически возбудима и способна генерировать распространяющийся потенциал действия посредством механизма, аналогичного тому, который действует в нервных клетках. Потенциал действия в волокне скелетной мышцы длится 1-2 мс и заканчивается раньше, чем появятся какие-либо признаки механической активности (рис. 4-6 А). Начавшаяся механическая активность может продолжаться более 100 мс. Электрическая активность плазматической мембраны не оказывает прямого влияния на сократительные белки, а вызывает повышение цитоплазматической концентрации ионов Са2+, которые продолжают активировать сократительный аппарат и после прекращения электрического процесса.
Сокращение мышц
В физиологии мышц термин «сокращение» не обязательно следует понимать как «укорочение». Прежде всего, рассматривается факт активации поперечных мостиков - участков генерирования силы в мышечном волокне. После сокращения механизм, инициирующий развитие силы, выключается.
Силу, с которой мышца, при ее сокращении, действует на предмет, называют мышечным напряжением (tension); сила действия предмета (обычно его массы) на мышцу - это нагрузка (load). Силы мышечного напряжения и нагрузки противодействуют друг другу. Приведет ли сила, генерируемая мышечным волокном, к его укорочению, зависит от относительных величин напряжения и
нагрузки. Чтобы мышечное волокно укоротилось и таким образом переместило нагрузку, его напряжение должно быть больше противодействующей нагрузки.
Если мышца развивает напряжение, но не укорачивается (и не удлиняется), сокращение называют изометрическим (длина мышцы постоянна). Такое сокращение происходит, когда мышца удерживает нагрузку в постоянном положении либо развивает силу по отношению к нагрузке, масса которой больше, чем мышечное напряжение. Если мышца укорачивается, а нагрузка на нее остается постоянной, сокращение называют изотоническим (напряжение мышцы постоянно).
Модель скользящих нитей
При укорочении волокна каждый поперечный мостик, прикрепившийся к тонкому филаменту, совершает поворот наподобие вращения лодочного весла. Вращательные движения множества поперечных мостиков подтягивают тонкие филаменты от обоих краев А-полосы к ее середине, и саркомер укорачивается (рис. 4-6 Б). Один «гребок» поперечного мостика создает очень маленькое перемещение тонкого филамента относительно толстого. Однако, за весь период активного состояния (возбуждения) мышечного волокна каждый поперечный мостик повторяет свое вращательное движение много раз, обеспечивая значительное смещение миофиламентов. Детальный молекулярный механизм этого явления будет рассматриваться далее.
Во время генерирования силы, укорачивающей мышечное волокно, перекрывающиеся толстые и тонкие филаменты каждого саркомера, подтягиваемые движениями поперечных мостиков, сдвигаются друг относительно друга. Длина толстых и тонких филаментов при укорочении саркомера не изменяется (рис. 4-6 В). Этот механизм мышечного сокращения известен как модель скользящих нитей.
Рис. 4-6. Феномен электромеханического сопряжения.
А - соотношение между временным ходом потенциала действия в мышечном волокне и возникающим в результате этого сокращением мышечного волокна с последующим его расслаблением. Б - поперечные мостики толстых филаментов, связываясь с актином тонких филаментов, подвергаются конформационному изменению, благодаря которому тонкие филаменты подтягиваются к середине саркомера. (На схеме изображены лишь два из примерно 200 поперечных мостиков каждого толстого филамента). В - модель скользящих нитей. Скольжение перекрывающихся толстых и тонких филаментов друг относительно друга приводит к укорочению миофибриллы без изменений длины филаментов. I-диск и Н-зона при этом уменьшаются
Специфические белки скелетной мышцы
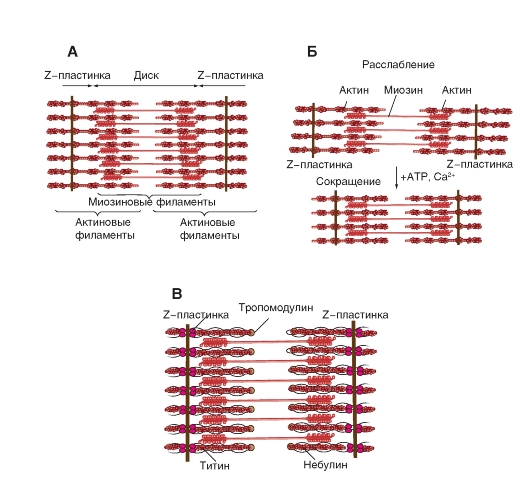
Как было отмечено, толстые и тонкие филаменты образуют периодический рисунок вдоль каждой миофибриллы. Регулярно повторяющийся элемент - саркомер. Толстые филаменты состоят почти целиком из сократительного белка миозина. Тонкие филаменты содержат сократительный белок актин, тропонин и тропомиозин. Толстые филаменты сосредоточены в средней части каждого саркомера, где они лежат параллельно друг другу. Эта область имеет вид широкой темной полосы, называемой А-полосой (рис. 4-7 А). В обеих половинах саркомера находится по набору тонких филаментов. Один конец каждого из них прикреплен к так называемой Z-полосе (или Z-линии) - сети из переплетающихся белковых молекул. Другой конец перекрывается с толстыми филаментами. Саркомер ограничен двумя последовательно расположенными Z-полосами. Таким образом, тонкие филаменты двух соседних саркомеров закреплены на двух сторонах каждой Z-полосы. Светлая полоса - I-полоса, расположена между краями А-полос двух соседних саркомеров и состоит из тех участков тонких филаментов, которые не перекрываются с толстыми филаментами. Z-полоса делит I-полосу пополам.
Два конца каждого толстого филамента молекулы миозина ориентированы в противоположных направлениях так, что концы их хвостов направлены по отношению к центру филамента (рис. 4-7 Б). Благодаря этому при гребковых движениях поперечных мостиков прикрепившиеся к ним тонкие
филаменты левой и правой половины саркомера проталкиваются к его середине, в результате саркомер укорачивается. То есть во время генерирования силы, укорачивающей мышечное волокно, перекрывающиеся толстые и тонкие филаменты каждого саркомера сдвигаются друг относительно друга, подтягиваемые движениями поперечных мостиков. Длина толстых и тонких филаментов при укорочении саркомера не изменяется
(рис. 4-7 Б).
Известно, что в пределах А-полосы каждого саркомера различаются еще две полоски. В центре А-полосы видна узкая светлая полоска - Н-зона. Она соответствует промежутку между противостоящими друг другу концами двух наборов тонких филаментов каждого саркомера, т.е. включает только центральные части толстых филаментов. Посередине Н-зоны находится совсем тонкая темная М-линия. Это сеть белков, соединяющих центральные части толстых филаментов. На рис. 4-7 В показаны известные в настоящее время дополнительные белки. От Z-полосы к М-линии идут филаменты белка титина, связанные одновременно с белками М-линии и с толстыми филаментами. М-линия и титиновые филаменты поддерживают упорядоченную организацию толстых филаментов в середине каждого саркомера. Таким образом, толстые и тонкие филаменты не являются свободными, незакрепленными внутриклеточными структурами. Кроме того, на рис. 4-7 В показан белок CapZ, определяющий стабилизацию филаментов актина. Показан также тропомодулин. На рисунке представлен и гигантский протеин - небулин.
Рис. 4-7. Строение скелетной мышцы в норме (А), на фоне расслабления (Б) и сокращения (В). Дополнительные белки, найденные в скелетной мышце (Г)
Молекула актина и миозина
Тонкий филамент (рис. 4-8 А) состоит из актина, тропомиозина и тропонина. Основа тонкого филамента - двойная закрученная цепь α- спирального полимера молекулы актина. Иначе говоря, это две цепи, закрученные относительно друг друга. Такая двойная спираль представляет собой остов тонкого филамента. Каждый спиральный оборот единичной нити филамента, или F-актин, состоит из 13 единичных мономеров в виде глобул и равен в длину примерно 70 нм. На каждой единичной молекуле актина есть участок связывания миозина. F-актин связан с двумя важнейшими регуляторными актинсвязывающими белками - тропомиозином и тропонином. Эти белки в покоящемся мышечном волокне предотвращают взаимодействие между актином и миозином. Коротко, молекулы тропомиозина частично закрывают участки связывания каждой единичной молекулы актина, мешая контакту миозина с актином. В таком состоянии блокирования участков связывания каждой единичной молекулы актина молекула тропомиозина удерживает тропонин. Рассмотрим тропомиозин и тропонин подробнее.
Тропомиозин - длинная молекула, состоящая из двух полипептидов, обвивающих друг друга. Молекула тропомиозина соответствует в длину примерно семи мономерам актина. Цепи из молекул тропомиозина, уложенные конец в конец, располагаются вдоль всего тонкого филамента. Молекулы тропомиозина частично прикрывают участки связывания каждой молекулы актина, блокируя возможность контакта миозина с актином. В таком блокирующем положении молекула тропомиозина удерживается тропонином.
Тропонин - гетеротримерный белок. Он состоит из тропонина Т, который отвечает за связывание с одиночной молекулой тропомиозина, тропонина С, который связывает ион Са2+, и тропонина I, который связывает актин и ингибирует сокращение. Каждая молекула тропомиози-
на связана с одной гетеротримерной молекулой тропонина, регулирующей доступ к участкам связывания миозина на семи мономерах актина, прилегающих к молекуле тропомиозина.
Молекула миозина (рис. 4-8 Б) - единое название большой семьи протеинов, имеющих определенные отличия в клетках разных тканей. В мышечном сокращении участвует миозин II, открытый первым из числа всех миозинов. В целом, молекула миозина II состоит из двух больших полипептидов (так называемых тяжелых цепей) и четырех меньших (так называемых легких цепей). У миозина II две тяжелые цепи составляют молекулу, содержащую две глобулярные «головки» (по одной у каждого полипептида) и соответственно две незакрученные «шейки». В некоторой литературе шейку тяжелой цепи переводят как «плечо молекулы миозина». Далее два больших полипептида, т.е. две тяжелые цепи, начинают закручиваться относительно друг друга. Их начальный регион закручивания получил название «шарнирный регион тяжелых цепей». Затем следует длинный стержень из двух переплетенных тяжелых цепей, получивший название «хвост». Хвост каждой молекулы миозина располагается вдоль оси толстого филамента, а две глобулярные головки вместе с шейками и шарнирным регионом, выступающие по бокам, иначе называют «поперечными мостиками». На каждой глобулярной головке у миозина II находятся по две легких цепи. Одна - так называемая легкая регуляторная цепь, другая - легкая основная цепь. Легкая основная цепь участвует в стабилизации головки миозина. Легкая регуляторная цепь регулирует активность фермента АТФазы миозина, гидролизующей связанную молекулу АТФ. Действие легкой регуляторной цепи миозина заключается в изменении регуляции посредством фосфорилирования с помощью Са2+-зависимой или Са2+-независимой киназ.
Взаимодействие тонкого филамента и одиночной пары головок от миозина толстого филамента показано на рис. 4-8 В.
Рис. 4-8. Молекулярная организация тонких и толстых филаментов.
А - тонкий филамент. Б - молекула миозина. В - взаимодействие тонкого и толстого филамента
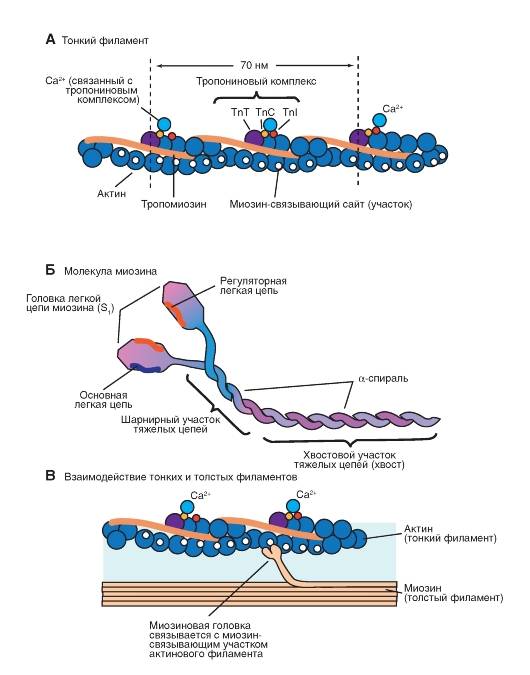
Взаимодействие актина и миозина
Рассмотрим вопрос, что позволяет поперечным мостикам, т.е. глобулярным головкам (вместе с шейками и шарнирным регионом), связываться с актином и начинать совершать определенное движение. Если говорить предельно коротко, то в основе мышечного сокращения лежит цикл, в котором головки миозина II связываются с участками связывания актина. Эти поперечные мостики создают искривление, что соответствует перемещению молекулы, после чего головки миозина отделяются от актина. Для этих циклов берется энергия гидролиза АТФ. Мышцы имеют механизмы регуляции циклов поперечных мостиков. Увеличение [Ca2+]in инициирует продолжение формирования циклов поперечных мостиков. При возбуждении происходит увеличение [Ca2+]in от уровня покоя (10-7 М и меньше) до более чем 10-5 М.
Начнем с того, что потенциал действия в волокне скелетной мышцы длится 1-2 мс и заканчивается раньше, чем появятся какие-либо признаки механической активности. Начавшаяся механическая активность может продолжаться более 100 мс. Электрическая активность плазматической мембраны не оказывает прямого влияния на сократительные белки, а вызывает повышение цитоплазматической концентрации ионов Са2+, которые продолжают активировать сократительный аппарат и после прекращения электрического процесса. То есть сокращение обусловлено высвобождением ионов Са2+, хранящихся в саркоплазматическом ретикулуме. Когда Са2+
поступает обратно в ретикулум, сокращение заканчивается и начинается расслабление. Источником энергии для кальциевого насоса служит АТФ: это одна из трех главных функций АТФ в мышечном сокращении.
Итак, сокращение инициируется в результате увеличения [Ca2+]in. Молекула гетеротримерного тропонина содержит ключевой Ca2+-сенситивный регулятор - тропонин С. Каждая молекула тропонина С в скелетной мышце имеет два высокоаффинных Ca2+-связывающих места, которые участвуют в связывании тропонина С с тонким филаментом. Связывание Ca2+ в этих высокоаффинных местах постоянно и не меняется в течение активности мышцы. Каждая молекула тропонина С в скелетной мышце имеет также два дополнительных низкоаффинных Ca2+-связывающих места. Взаимодействие Ca2+ с ними индуцирует конформационные изменения в тропониновом комплексе, приводящие к двум эффектам. Первый эффект заключается в том, что С-терминаль ингибиторного тропонина I двигается в направлении от центра связывания актина с миозином (расположенном на актине), тем самым осуществляя движение молекулы тропомиозина также в сторону от центра связывания актина с миозином (расположенном на актине). Другой эффект осуществляется через тропонин Т, и заключается в выталкивании тропомиозина от центра связывания актина с миозином в так называемый актиновый желобок. Это приводит к тому, что центр связывания с миозином на актине открывается, и головка миозина может взаимодействовать с актином, создавая цикл поперечных мостиков.
Рис. 4-9. Принципы взаимодействия актина и миозина в скелетной и сердечной мышцах
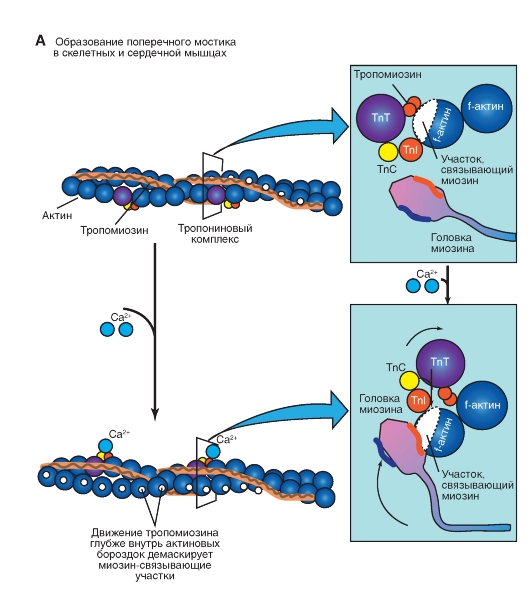
Механизм сокращения
Последовательность событий, начиная от связывания поперечного мостика с тонким филаментом и до момента, когда система готова к повторению процесса, называется рабочим циклом поперечных мостиков. Каждый цикл состоит из четырех основных фаз. Фаза 1 - головка миозина прочно связана с молекулой актина в актомиозиновый комплекс. Для отделения головки миозина в цитозоле необходим АТФ, и его подход к миозину показан стрелкой на схеме. Фаза 2 - если головка миозина связывается с АТФ, то уменьшается аффинность головки миозина к актину. Из-за уменьшения аффинности головка миозина отделяется от молекулы актина. При устранении действия на головку миозина АТФ цикл продолжается дальше. В мышце это происходит, исключительно, благодаря расщеплению АТФ до АДФ+Рi в результате работы фермента АТФазы миозина. Этот шаг зависит от наличия Mg2+. Фаза 3 - если на головке миозина после расщепления АТФ на АДФ и Pi оба, АДФ и Pi, связаны. При этом головка миозина выпрямляется. Аффинность образования актомиозинового комплекса опять повышается, и головка миозина может вновь присоединить молекулу актина со слабой связью. Фаза 4 - инициация слабой связи переходит быстро в более сильную связь с головкой миозина, нагруженной АДФ. Переход в это состояние представляет собой собственно ступень генерации силы. Этот процесс объясняют вращением головки миозина, благодаря которой поворот миозина осуществляет сдвиг на шаг филамент актина.
В цикле поперечных мостиков АТФ выполняет две разные роли:
1) гидролиз АТФ поставляет энергию для движения поперечного мостика;
2) связывание (но не гидролиз) АТФ с миозином сопровождается отделением миозина от актина и создает возможность повторения цикла поперечных мостиков.
Химические и физические явления во время четырех стадий цикла поперечных мостиков можно представить иначе. Молекула АТФ, связанная с миозином, расщепляется с освобождением химической энергии и образованием высокоэнергетической конформации миозина поперечного мостика; с этой формой миозина (М*) остаются связанными продукты гидролиза АТФ-АДФ и неорганический фосфат (Pi).
Энергию активной конформации миозина можно сравнить с потенциальной энергией растянутой пружины.
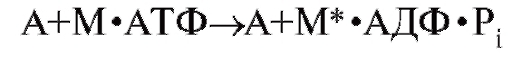
Гидролиз АТФ.
Далее происходит связывание высокоэнергетической формы миозина с актином (А) тонкого филамента:
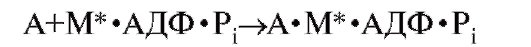
Связывание актина.
При связывании высокоэнергетической формы миозина с актином запускается освобождение напряженной конформации высокоэнергетического поперечного мостика; в результате связанный с актином поперечный мостик совершает свое вращательное движение и одновременно теряет АДФ и Pi.
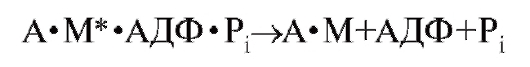
Движение поперечного мостика.
Процесс последовательного получения и освобождения энергии миозином можно сравнить с работой мышеловки. В ней энергия запасается при растягивании пружины (в мышце - при гидролизе АТФ), а освобождается при отпускании пружины (в мышце - при связывании миозина с актином).
Во время движения поперечного мостика миозин очень прочно прикреплен к актину; только после разрыва этой связи он может снова получить энергию и повторить цикл. Связь между актином и миозином разрывается при соединении с миозином новой молекулы АТФ.
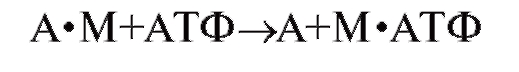
Диссоциация поперечного мостика от актина.
Обеспечиваемое АТФ разделение актина и миозина - пример аллостерической регуляции активности белка. Связывание АТФ с одним участком миозина снижает сродство его молекулы к актину, связанному с другим участком. Следовательно, АТФ действует как модулятор, регулирующий связывание актина с миозином. Отметим, что на этой стадии АТФ не расщепляется, т.е. служит не источником энергии, а только модулирующей молекулой, которая обеспечивает аллостерическую модуляцию миозиновой головки и тем самым ослабляет связь миозина с актином.
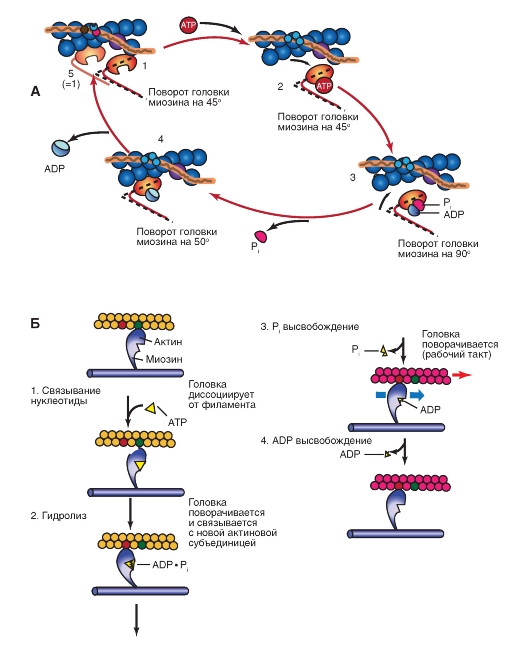
Рис. 4-10. Механизм сокращения. Представлен рабочий цикл поперечных мостиков - головки миозина (вместе с шейкой и шарнирным регионом).
На панели (А) процесс представлен в виде замкнутого цикла из четырех фаз. На панели (Б) процесс представлен в виде последовательных шагов более детально
Одиночное сокращение мышцы
Если мышца развивает напряжение, но не укорачивается (и не удлиняется), сокращение называется изометрическим (длина мышцы постоянна). Такое сокращение происходит, когда мышца удерживает нагрузку в постоянном положении, либо развивает силу по отношению к нагрузке, масса которой больше, чем мышечное напряжение. Если мышца укорачивается, а нагрузка на нее остается постоянной, сокращение называется изотоническим (напряжение мышцы постоянно).
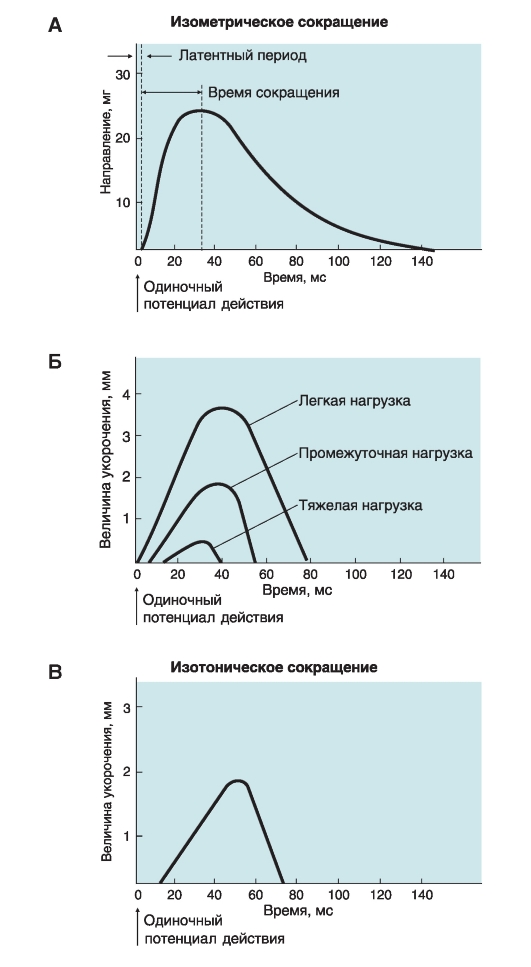
Механический ответ отдельного мышечного волокна на одиночный потенциал действия называется одиночным сокращением (twitch). Основные характеристики одиночного изометрического сокращения показаны на рис. 4-11 А. Начало мышечного напряжения запаздывает на несколько миллисекунд по отношению к потенциалу действия. В течение этого латентного периода проходят все этапы электромеханического сопряжения. Интервал от начала развития напряжения до момента его максимума это время сокращения. Оно различно для разных типов волокон скелетных мышц. Время сокращения быстрых волокон не превышает 10 мс, тогда как для более медленных волокон оно не меньше 100 мс. Длительность сокращения определяется тем, как долго цитоплазматическая концентрация Са2+ остается повышенной, обеспечивая продолжение циклической активности поперечных мостиков. Время сокращения обусловлено активностью Са-АТФазы саркоплазматического ретикулума, которая в быстрых волокнах выше, чем в медленных.
Характеристики изотонического сокращения зависят также от массы поднимаемой нагрузки (рис. 4-11 Б), а именно, при более тяжелой нагрузке:
1) латентный период продолжительнее;
2) скорость укорочения (величина укорочения мышцы в единицу времени), длительность сокращения и величина укорочения мышцы - меньше.
Сравнение одиночных сокращений одного и того же мышечного волокна при разных режимах его деятельности показывает (рис. 4-11 В), что латентный период больше для изотонического сокращения, чем для изометрического, тогда как длительность механического процесса меньше в случае изотонического сокращения (т.е. при укорочении), чем изометрического (т.е. при генерировании силы).
Рассмотрим подробнее последовательность явлений во время изотонического одиночного сокращения. При возбуждении мышечного волокна поперечные мостики начинают развивать силу, однако укорочение не начнется, пока мышечное напряжение не превысит нагрузку на волокно. Таким образом, укорочению предшествует период изометрического сокращения, в течение которого возрастает напряжение. Чем тяжелее нагрузка, тем больше потребуется времени, чтобы напряжение сравнялось с величиной нагрузки и началось укорочение. Если нагрузку повышать, то, в конце концов, мышечное волокно не сможет ее поднять, скорость и степень укорочения будут равны нулю и сокращение станет полностью изометрическим.
Заметим, что силу, с которой мышца при ее сокращении действует на предмет, называют мышечным напряжением (tension). Сила действия предмета (обычно его массы) на мышцу - это нагрузка (load). Кривая мышечного сокращения в отечественной литературе издревле называется «механограммой», т.е. записью механической активности мышцы. В мировой литературе обычно применяют понятия resting tension (force) для описания силы, с которой покоящаяся мышца действует на предмет (в mN), и active tension (force) для описания силы, с которой мышца при ее сокращении действует на предмет.
Силы мышечного напряжения и нагрузки противодействуют друг другу. Приведет ли сила, генерируемая мышечным волокном, к его укорочению, зависит от относительных величин напряжения и нагрузки. Чтобы мышечное волокно укоротилось и, таким образом, переместило нагрузку, его напряжение должно быть больше противодействующей нагрузки.
Рис. 4-11. Одиночное мышечное сокращение.
А - одиночное изометрическое сокращение волокна скелетной мышцы после одного потенциала действия. Б - одиночные изотонические сокращения при разных нагрузках. Величина, скорость и продолжительность укорочения уменьшаются с увеличением нагрузки, тогда как интервал времени от стимула до начала укорочения возрастает с увеличением нагрузки. В - одиночное изотоническое сокращение волокна скелетной мышцы после одного потенциала действия
Виды мышечных сокращений
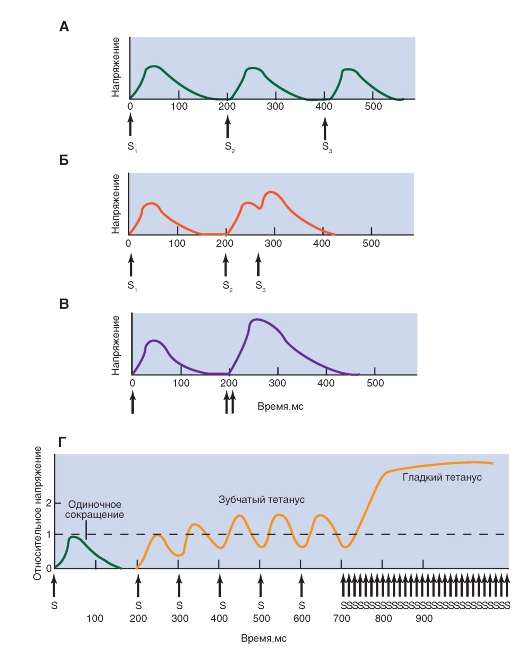
Поскольку длительность одного потенциала действия в скелетном мышечном волокне составляет 1-2 мс, а одиночное сокращение может продолжаться 100 мс, момент инициации второго потенциала действия может попасть на период механической активности. На рисунке 4-12 А- В представлены изометрические сокращения мышечного волокна в ответ на три последовательных стимула. Изометрическое сокращение в ответ на первый стимул S1 продолжалось 150 мс (рис. 4-12 А). Второй стимул S2, поданный через 200 мс после S1, когда мышечное волокно уже полностью расслабилось, вызвал второе сокращение, идентичное первому, а третий стимул S3 с таким же интервалом - третье идентичное сокращение. На рисунке 4-12 Б интервал S1-S2 остался равным 200 мс, а третий стимул был подан через 60 мс после S2, когда механический ответ на S2 начал снижаться, но еще не закончился. Стимул S3 вызвал сократительный ответ, максимальное напряжение которого превысило ответ на S2. На рисунке 4-12 В интервал S2-S3 был уменьшен до 10 мс, и максимальный механический ответ увеличился еще больше, причем ответ на S3 оказался слитным продолжением ответа на S2.
Увеличение мышечного напряжения при последовательных потенциалах действия, возникающих до окончания фазы механической активности, называется суммацией. При слиянии одиночных сокращений во время ритмического раздражения наблюдается тетанус (тетаническое сокращение). При низких частотах раздражения механический ответ может быть волнообразным, так как волокно частично расслабляется в промежутках между стимулами; это зубчатый тетанус. Если частоту раздражения повысить, получается гладкий тетанус, без осцилляций (рис. 4-12 Г).
По мере повышения частоты потенциалов действия величина напряжения возрастает в результате суммации до тех пор, пока гладкий тетанус не достигнет максимума, после которого напряжение не будет увеличиваться при дальнейшем повышении частоты раздражения.
Чтобы объяснить причинысуммации, нужнорассмотреть, какие процессы происходят в мышечных волокнах. Но сначала следует получить сведения об упругих свойствах мышцы. Мышца содержит пассивные упругие элементы (участки толстых и тонких филаментов, а также сухожилия), последовательно соединенные с сократительными элементами (генерирующими силу). Последовательные
упругие элементы действуют как пружины, через которые активная сила, генерируемая поперечными мостиками, передается к нагрузке. Временной ход напряжения при изометрическом сокращении включает период, необходимый для растяжения последовательных упругих элементов.
Напряжение мышечного волокна в конкретный момент времени зависит от следующих факторов:
1) число поперечных мостиков, прикрепленных к актину и находящихся на 2-й стадии цикла поперечных мостиков в каждом саркомере;
2) сила, создаваемая каждым поперечным мостиком;
3) длительность активного состояния поперечных мостиков.
Один потенциал действия вызывает в мышечном волокне высвобождение такого количества Са2+, которое достаточно для насыщения тропонина, поэтому все участки связывания миозина на тонких филаментах изначально доступны. Однако связывание высокоэнергетической формы поперечных мостиков с этими участками (1-я стадия цикла поперечного мостика) занимает некоторое время, а кроме того, как было отмечено выше, необходимо время для растяжения последовательных упругих элементов. В результате, несмотря на изначальную доступность всех участков связывания при одиночном сокращении, максимальное напряжение развивается не сразу. Еще одно обстоятельство: почти сразу после высвобождения ионов Са2+ начинается их обратный перенос в саркоплазматический ретикулум, так что концентрация Са2+ в цитоплазме постепенно снижается относительно прежнего высокого уровня и, следовательно, на актиновых нитях остается все меньше участков связывания миозина, способных взаимодействовать с поперечными мостиками.
Иная ситуация во время тетанического сокращения. Каждый очередной потенциал действия вызывает высвобождение Са2+ из саркоплазматического ретикулума раньше, чем заканчивается обратный перенос всех ионов Са2+, находящихся в цитоплазме после предыдущего потенциала действия. Благодаря этому устойчиво поддерживается повышенная цитоплазматическая концентрация Са2+ и, значит, не уменьшается количество доступных для связывания с миозином участков на актиновых филаментах. В итоге количество доступных для связывания участков остается на максимальном уровне, циклическая активность поперечных мостиков обеспечивает достаточное растяжение последовательных упругих элементов и передачу максимального напряжения к концам мышечного волокна.
Рис. 4-12. Соотношение между частотой и напряжением.
А-В - суммация сокращений в результате уменьшения промежутков времени между стимулами S2 и S3. Г - изометрические сокращения, вызванные серией стимулов с частотой 10/с (зубчатый тетанус) и 100/с (слитный тетанус); для сравнения показано одиночное сокращение
Соотношение между нагрузкой и скоростью укорочения
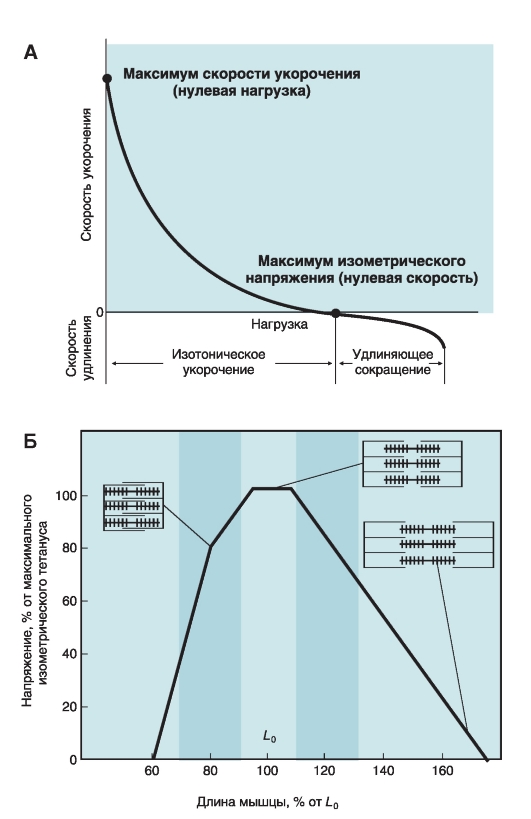
Скорость укорочения мышечного волокна уменьшается при увеличении нагрузки (рис. 4-13 А). Скорость укорочения максимальна при отсутствии нагрузки и равна нулю, когда нагрузка соответствует силе максимального изометрического напряжения. Если нагрузка станет больше, чем максимальное изометрическое напряжение, будет происходить удлинение мышечного волокна со скоростью, возрастающей с увеличением нагрузки; при очень большой нагрузке волокно разорвется.
Скорость укорочения определяется частотой повторения рабочих циклов каждого поперечного мостика и в конечном итоге частотой расщепления молекул АТФ, поскольку в каждом цикле поперечного мостика расщепляется одна молекула АТФ. Если нагрузка на поперечный мостик увеличивается, молекулы АТФ подвергаются гидролизу реже (по ряду причин) и, следовательно, снижается скорость укорочения.
Соотношение между длиной мышцы и ее напряжением
Пассивные упругие свойства расслабленной мышцы обусловлены, главным образом, особенностями организации белка титина, молекула которого одним концом прикреплена к Z-поло- се, другим - к толстому филаменту, и действует подобно пружине. По мере растяжения мышцы пассивное напряжение расслабленного волокна возрастает, но не за счет активных движений поперечных мостиков, а благодаря растягиванию титиновых нитей. Если растянутое волокно отпустить, его длина вернется к равновесному состоянию, также как сокращается в аналогичной ситуации полоска резины. Растяжение приводит не только к пассивному напряжению мышечного волокна, но и к изменению его активного напряжения при сокращении. Поэтому сила, генерируемая во время сокращения, зависит от исходной длины мышечного волокна. Это проиллюстрировано экспериментом, когда мышечное волокно растягивают, и при каждой длине регистрируют величину активного напряжения в ответ на стимулы (рис. 4-13 Б). Длина, при которой волокно генерирует наибольшее активное изометрическое напряжение, называется оптимальной длиной,
При длине мышечного волокна, равной 60% от Lo, волокно не генерирует напряжения в ответ
на стимул. По мере растяжения волокна от этого исходного уровня активное изометрическое напряжение возрастает при каждом значении длины вплоть до максимума при длине Lo. В ходе дальнейшего удлинения волокна его напряжение падает. При длине, составляющей 175% и более от Lo, волокно не реагирует на раздражение.
Когда скелетные мышцы расслаблены, длина большинства их волокон приближается к Lo и, следовательно, оптимальна для генерирования силы. Длина расслабленных волокон меняется под действием нагрузки или в результате растягивания, обусловленного сокращением других мышц, однако пассивное изменение длины расслабленных волокон ограничено, поскольку мышцы прикреплены к костям. Пассивное изменение длины редко превышает 30%, а часто бывает гораздо меньше. В этом диапазоне значений исходной длины активное напряжение мышцы никогда не становится ниже половины напряжения, развиваемого при Lo (рис. 4-13 Б).
Соотношение между исходной длиной волокна и его способностью развивать активное напряжение во время сокращения можно объяснить с позиций модели скользящих нитей. При растяжении расслабленного мышечного волокна происходит вытягивание тонких филаментов из пучков толстых филаментов, так что зона перекрывания уменьшается. Если волокно растянуто до 1,75 Lo, филаменты уже не перекрываются. Поперечные мостики не могут связываться с актином, и напряжение не развивается. При меньшем растяжении (постепенное изменение длины от 1,75 Lo до Lo) зона перекрывания филаментов увеличивается, и напряжение, развиваемое при стимуляции, возрастает прямо пропорционально увеличению количества поперечных мостиков в зоне перекрывания. Самая большая зона перекрывания бывает при длине Lo; тогда к тонким филаментам может прикрепляться наибольшее количество поперечных мостиков, и генерируемое напряжение максимально.
Если длина волокна меньше Lo, развиваемое напряжение снижается ввиду ряда обстоятельств. Во-первых, пучки тонких филаментов с противоположных концов саркомера начинают взаимно перекрываться, мешая прикреплению поперечных мостиков и развитию силы. Во-вторых, по неясным пока причинам при уменьшении длины волокна снижается сродство тропонина к Са2+ и, следовательно, на тонких филаментах уменьшается количество участков, доступных для связывания с поперечными мостиками.
Рис. 4-13. Два основных соотношения: нагрузка - скорость укорочения мышцы, длина - напряжение мышцы.
А - скорость укорочения и удлинения волокна скелетной мышцы в зависимости от нагрузки. Отметим, что сила, действующая на поперечные мостики во время удлиняющего сокращения больше, чем максимальное изометрическое напряжение. Б - изменения активного изометрического тетанического напряжения в зависимости от длины мышечного волокна. Голубая область соответствует физиологическому диапазону значений длины волокон в мышце, прикрепленной к кости
Функциональная роль АТФ в процессе сокращения скелетной мышцы
1. В результате вызываемого миозином гидролиза АТФ поперечные мостики получают энергию для развития тянущего усилия.
2. Связывание АТФ с миозином сопровождается отсоединением поперечных мостиков, прикрепленных к актину.
3. Гидролиз АТФ под действием Са-АТФазы саркоплазматического ретикулума поставляет энергию для активного транспорта Са2+ в латеральные мешки саркоплазматического ретикулума, что приводит к снижению цитоплазматического Са2+ до исходного уровня. Соответственно сокращение завершается, и мышечное волокно расслабляется.
В скелетных мышцах при их переходе от состояния покоя к сократительной активности - в 20 раз (или даже в несколько сотен раз) резко одномоментно повышается скорость расщепления АТФ. Небольшой запас АТФ в скелетной мышце достаточен лишь для нескольких одиночных сокращений. Чтобы поддерживать длительное сокращение, молекулы АТФ должны образовываться в процессе метаболизма с такой же скоростью, с какой они расщепляются во время сокращения.
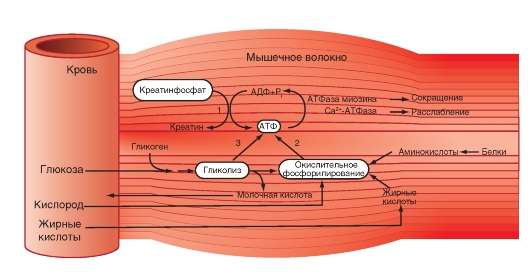
Существуют три способа образования АТФ во время сокращения мышечного волокна (рис. 4-14):
1) фосфорилирование АДФ путем переноса фосфатной группы от креатинфосфата;
2) окислительное фосфорилирование АДФ в мито - хондриях;
3) фосфорилирование АДФ в процессе гликолиза в цитоплазме.
Благодаря фосфорилированию АДФ креатинфосфатом обеспечивается очень быстрое образование АТФ в самом начале сокращения:
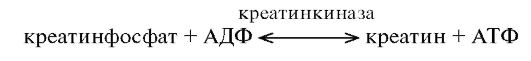
В течение периода покоя концентрация креатинфосфата в мышечном волокне возрастает до уровня, примерно в пять раз превышающего содержание АТФ. В начале сокращения, когда начинаются снижение концентрации АТФ и увеличение концентрации АДФ вследствие расщепления АТФ под действием АТФазы миозина, реакция сдвигается в сторону образования АТФ за счет креатинфосфата. При этом переход энергии совершается с такой большой скоростью, что в начале сокращения
концентрация АТФ в мышечном волокне изменяется мало, в то время как концентрация креатинфосфата падает быстро.
Хотя АТФ образуется за счет креатинфосфата очень быстро, посредством единственной ферментативной реакции, количество АТФ лимитировано исходной концентрацией креатинфосфата в клетке. Чтобы мышечное сокращение могло продолжаться дольше нескольких секунд, необходимо участие двух других, упоминавшихся выше, источников образования АТФ. После начала сокращения, обеспечиваемого за счет использования креатинфосфата, подключаются более медленные, требующие участия многих ферментов пути окислительного фосфорилирования и гликолиза, благодаря которым скорость образования АТФ увеличивается до уровня, соответствующего скорости расщепления АТФ.
При умеренной мышечной активности АТФ образуется преимущественно путем окислительного фосфорилирования, и в течение первых 5-10 мин главным ресурсом для этого служит гликоген. В последующие ~30 мин доминирующими становятся источники энергии, доставляемые кровью, причем глюкоза и жирные кислоты участвуют примерно в одинаковой мере. На более поздних этапах сокращения преобладает утилизация жирных кислот, а глюкоза расходуется меньше.
Если интенсивность мышечной работы такова, что скорость расщепления АТФ превышает 70% от ее максимального уровня, существенно возрастает вклад гликолиза в образование АТФ. Глюкоза для этого процесса поступает из двух источников: из крови или за счет запасов гликогена в мышечных волокнах. По мере усиления мышечной активности увеличивается доля АТФ, обеспечиваемая путем анаэробного процесса - гликолиза; соответственно образуется больше молочной кислоты.
По окончании мышечной работы запасы богатых энергией соединений (креатинфосфата и гликогена) в мышце снижены. Для восстановления запасов обоих соединений нужна энергия, поэтому мышца, уже находясь в состоянии покоя, продолжает некоторое время усиленно потреблять кислород. Благодаря усиленному потреблению кислорода в период после мышечной работы покрывается так называемый кислородный долг; и интенсивное образование АТФ путем окислительного фосфорилирования направлено на восстановление энергетических ресурсов в виде креатинфосфата и гликогена.
Рис. 4-14. Энергетический метаболизм скелетной мышцы.
Три ресурса для образования АТФ во время мышечного сокращения: 1 - креатинфосфат; 2 - окислительное фосфорилирование; 3 - гликолиз
Типы волокон скелетных мышц
Волокна скелетных мышц неодинаковы по своим механическим и метаболическим особенностям. Типы волокон различаются на основе следующих характеристик:
1) в зависимости от максимальной скорости укорочения - волокна быстрые и медленные;
2) в зависимости от главного пути образования АТФ - волокна оксидативные и гликолитические.
Быстрые и медленные мышечные волокна содержат изоферменты миозина, расщепляющие АТФ с разной максимальной скоростью, чему соответствует различная максимальная скорость рабочего цикла поперечных мостиков и, следовательно, разная максимальная скорость укорочения волокна. Высокая АТФазная активность миозина свойственна быстрым волокнам, более низкая АТФазная активность - медленным волокнам. Хотя в быстрых волокнах скорость рабочего цикла примерно в 4 раза выше, чем в медленных, поперечные мостики обоих типов генерируют одинаковую силу.
Другой подход к классификации волокон скелетных мышц основан на различиях ферментативных механизмов синтеза АТФ. В некоторых волокнах много митохондрий и, следовательно, обеспечивается высокий уровень окислительного фосфорилирования; это оксидативные волокна. Количество образующейся в них АТФ зависит от снабжения мышцы кровью, с которой поступают молекулы кислорода, и богатых энергией соединений. Волокна этого типа окружены многочисленными капиллярами. Кроме того, в них присутствует связывающий кислород белок - миоглобин, который увеличивает скорость диффузии кислорода, а также выполняет функцию кратковременного кислородного депо в мышечной ткани. Благодаря значительному содержанию миоглобина оксидативные волокна окрашены в темно-красный цвет; их часто называют красными мышечными волокнами.
В гликолитических волокнах, наоборот, мало митохондрий, но высокое содержание ферментов гликолиза и большие запасы гликогена. Эти волокна окружены относительно небольшим числом капилляров, и миоглобина в их ткани немного, что соответствует ограниченному использованию кислорода. Вследствие недостатка
миоглобина гликолитические волокна выглядят светлыми и получили название белых мышечных волокон.
На основании двух рассмотренных характеристик (скорость укорочения и тип метаболизма) можно выделить три типа волокон скелетных мышц.
1. Медленные оксидативные волокна (тип I) - низкая активность миозиновой АТФазы и высокая окислительная способность (рис. 4-15 А).
2. Быстрые оксидативные волокна (тип IIа) - высокая активность миозиновой АТФазы и высокая окислительная способность (рис. 4-15 Б).
3. Быстрые гликолитические волокна (тип IIб) - высокая активность миозиновой АТФазы и высокая гликолитическая способность
(рис. 4-15 В).
Отметим, что не обнаружен четвертый теоретически возможный вариант - медленные гликолитические волокна.
Волокна варьируют не только по своим биохимическим особенностям, но и по размерам: у гликолитических волокон диаметр существенно больше, чем у оксидативных. Это сказывается на величине развиваемого ими напряжения. Что касается числа толстых и тонких филаментов на единицу площади поперечного сечения, то оно примерно одинаково для всех типов скелетных мышечных волокон. Таким образом, чем больше диаметр волокна, тем большее число параллельно задействованных толстых и тонких филаментов участвует в генерировании силы, и тем больше максимальное напряжение мышечного волокна. Отсюда следует, что гликолитическое волокно, которое имеет больший диаметр, развивает в среднем более значительное напряжение, по сравнению с напряжением оксидативного волокна.
Кроме того, рассмотренные три типа мышечных волокон характеризуются разной устойчивостью к утомлению. Быстрые гликолитические волокна утомляются через короткое время, тогда как медленные оксидативные волокна очень выносливы, что позволяет им длительно поддерживать сократительную активность практически при постоянном уровне напряжения. Быстрые оксидативные волокна занимают промежуточное место по способности противостоять развитию утомления.
Характеристики трех типов волокон скелетных мышц обобщены в табл. 4-1.
Рис. 4-15. Типы волокон скелетных мышц. Скорость развития утомления в волокнах трех типов.
Каждая вертикальная линия соответствует сократительному ответу на короткое тетаническое раздражение. Сократительные ответы в период между 9-й и 60-й мин пропущены
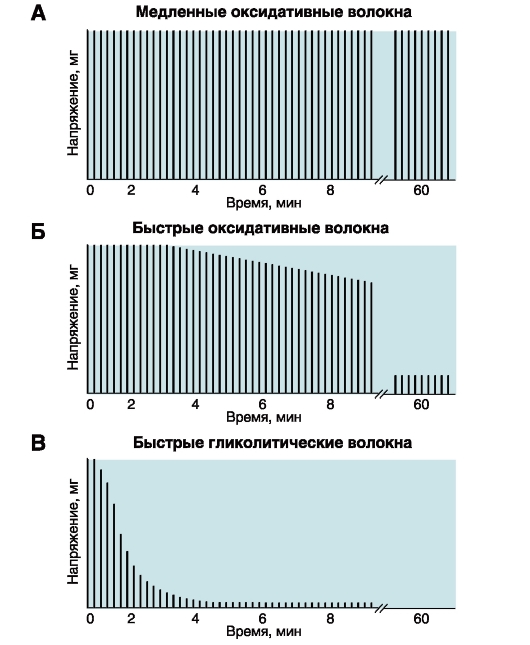
Таблица 4-1. Характеристики трех типов волокон скелетных мышц

Напряжение мышцы
Силу, с которой мышца при ее сокращении действует на предмет, называют мышечным напряжением (tension); сила действия предмета (обычно его масса) на мышцу - это нагрузка (load). Если мышце задать фоновую нагрузку, как обычно осуществляют при измерениях, то эту фоновую нагрузку называют preload - преднагрузкой или предрастяжением. Часто это пишут в русскоязычном написании - «прелод». Силы мышечного напряжения и нагрузки противодействуют друг другу. Приведет ли сила, генерируемая мышечным волокном, к его укорочению, зависит от относительных величин напряжения и нагрузки. Чтобы мышечное волокно укоротилось и таким образом переместило нагрузку, его напряжение должно быть больше противодействующей нагрузки.
Если мышца развивает напряжение, но не укорачивается (и не удлиняется), сокращение называют изометрическим (длина мышцы постоянна) (рис. 4-16 А). Такое сокращение происходит, когда мышца удерживает нагрузку в постоянном положении либо развивает силу по отношению к нагрузке, масса которой больше, чем мышечное напряжение. Если мышца укорачивается, а нагрузка на нее остается постоянной, сокращение называют изотоническим (напряжение мышцы постоянно) (рис. 4-16 Б).
Третий тип сокращения - удлиняющее сокращение (эксцентрическое сокращение), когда действующая на мышцу нагрузка больше, чем напряжение, развиваемое поперечными мостиками. В такой ситуации нагрузка растягивает мышцу, несмотря на противодействующую силу, создаваемую движениями поперечных мостиков. Эксцентрическое сокращение происходит, если поддерживаемый мышцей объект смещается вниз (примеры: человек садится из положения стоя или спускается вниз по
лестнице). Следует подчеркнуть, что в подобных условиях удлинение мышечных волокон не активный процесс, осуществляемый сократительными белками, а результат действия на мышцу внешней силы. При отсутствии внешней силы, удлиняющей мышцу, волокно при его стимуляции будет только укорачиваться, но не удлиняться. Все три типа сокращения (изометрическое, изотоническое и эксцентрическое) - это естественные события повседневной деятельности.
При каждом типе сокращения поперечные мостики ритмически повторяют цикл, состоящий из четырех стадий. На 2-й стадии изотонического сокращения поперечные мостики, связанные с актином, совершают вращательное движение, заставляя саркомеры укорачиваться. По-другому происходит при изометрическом сокращении: изза нагрузки, действующей на мышцу, связанные с актином поперечные мостики не могут сдвинуть тонкие филаменты, но передают им силу - изометрическое напряжение. Во время 2-й стадии эксцентрического сокращения поперечные мостики испытывают действие нагрузки, которая тянет их назад к Z-пластинке, при этом они остаются прикрепленными к актину и развивают усилие. Стадии 1, 3 и 4 проходят одинаково при всех трех типах сокращений. Таким образом, при каждом типе сокращения сократительные белки претерпевают одинаковые химические изменения. Конечный результат (укорочение, отсутствие изменений длины или удлинение) определяется величиной нагрузки на мышцу.
На рисунке 4-16 В показана зависимость «длина-tension» при изометрическом сокращении, а на рис. 4-16 Г только «активный» фрагмент этой зависимости, т.е. разница между «пассивной» кривой и общей кривой. Далее показаны (рис. 4-16 Д) характерные кривые, отражающие зависимость «нагрузка-скорость».
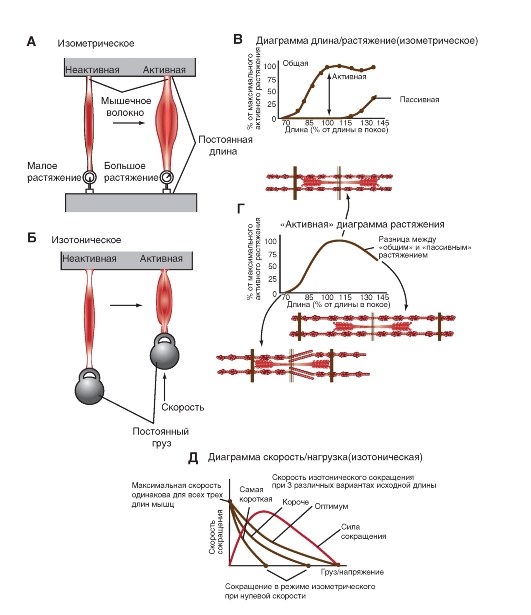
Рис. 4-16. Изометрическое и изотоническое сокращение.
А - экспериментальный препарат для изучения мышечных сокращений в изометрических условиях. Б - экспериментальный препарат для изучения мышечных сокращений в изотонических условиях. В - пассивная кривая, демонстрирующая мышечное напряжение (tension), которое измеряется при различных длинах мышцы перед сокращением. Суммарная кривая, демонстрирующая мышечное напряжение (tension), которая измеряется при различных длинах мышцы в течение сокращения. Г - активное мышечное напряжение (active tension) представляет собой разницу между суммарным и пассивным мышечным напряжением на панели (С). Д - три кривые голубого цвета показывают, что скорость укорочения мышцы быстрее, если мышца натянута массой
Опорно-двигательный аппарат
Сокращающаяся мышца передает усилие костям через сухожилия. Если усилие достаточно, то при укорочении мышцы кости перемещаются. При сокращении мышца развивает только тянущее усилие, так что кости, к которым она прикреплена, по мере ее укорочения подтягиваются друг к другу. При этом может происходить сгибание конечности в суставе (флексия) или разгибание (экстензия) - выпрямление конечности (рис. 4- 17 А). В этих противоположно направленных движениях должны участвовать, по крайней мере, две разные мышцы - сгибатель и разгибатель. Мышечные группы, осуществляющие движения сустава в противоположных направлениях, называют антагонистами. Как показано на рис. 4-17 А, при сокращении двуглавой мышцы плеча (m. biceps) рука сгибается в локтевом суставе, тогда как сокращение мышцы-антагониста - трехглавой мышцы плеча (m. triceps) заставляет руку разгибаться. Обе мышцы создают при сокращении только тянущее усилие по отношению к предплечью.
Группы мышц-антагонистов необходимы не только для сгибания и разгибания, но и для движения конечностей в стороны или для вращения. Некоторые мышцы при сокращении могут создавать два типа движения в зависимости от сократительной активности других мышц, действующих на ту же конечность. Например, при сокращении икроножной мышцы (m. gastrocnemius) нога сгибается в колене, например, во время ходьбы (рис. 4-17 Б). Однако, если икроножная мышца сокращается одновременно с четырехглавой мышцей бедра (m. quadriceps femoris), которая выпрямляет ногу в голени, коленный сустав не может согнуться, так что движение возможно только в голеностопном суставе. Происходит разгибание стопы, т.е. человек приподнимается на кончиках пальцев ног - «встает на цыпочки».
Мышцы, кости и суставы тела представляют собой системы рычагов. Принцип действия рычага можно проиллюстрировать на примере сгибания предплечья (рис. 4-17 В): двуглавая мышца оказывает тянущее усилие, направленное вверх, на участок предплечья примерно на расстоянии 5 см от локтевого сустава. В рассматриваемом примере кисть руки удерживает нагрузку 10 кг, т.е. на расстоянии примерно 35 см от локтя действует направленная вниз сила величиной 10 кг. Согласно законам физики, предплечье находится в состоянии механического равновесия (т.е. суммарная сила, действующая на систему, равна нулю), когда произведение направленной вниз силы (10 кг) на расстояние от места ее приложения до локтя (35 см) равно произведению изометрического напряжения мышцы (Х) на расстояние от нее до локтя (5 см). Итак, 10х35=5хХ; отсюда Х=70 кг. Отметим, что работа этой системы механически невыгодна, поскольку сила, развиваемая мышцей, гораздо больше, чем масса удерживаемой нагрузки (10 кг).
Однако механически невыгодные условия работы большинства механизмов мышечных рычагов компенсируются за счет повышения маневренности. На рисунке 4-17 показано, что укорочению двуглавой мышцы на 1 см соответствует перемещение кисти на расстояние 7 см. Поскольку укорочение мышцы на 1 см и перемещение кисти на 7 см совершаются за одно и то же время, скорость движения кисти в семь раз больше, чем скорость укорочения мышцы. Система рычагов играет роль усилителя, благодаря которому небольшие относительно медленные движения двуглавой мышцы преобразуются в более быстрые движения кисти. Так мяч, брошенный подающим игроком баскетбольной команды, летит со скоростью 90-100 миль/ч (примерно 150-160 км/ч), хотя мышцы игрока укорачиваются во много раз медленнее.
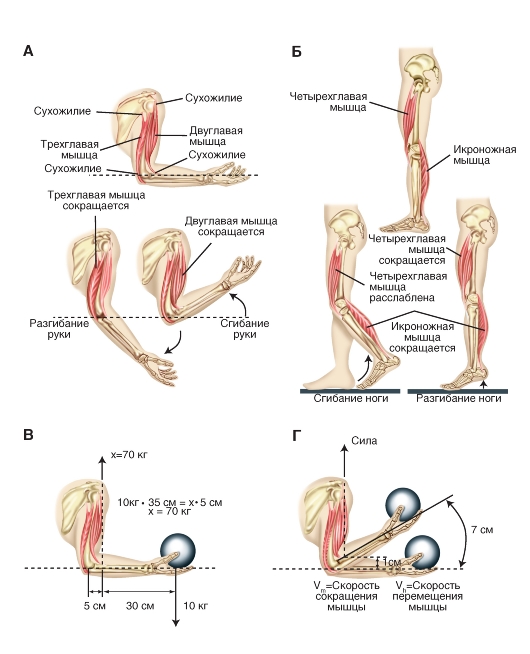
Рис. 4-17. Мышцы и кости действуют как система рычагов.
А - мышцы-антагонисты, осуществляющие сгибание и разгибание предплечья. Б - сокращение икроножной мышцы приводит к сгибанию нижней конечности, когда четырехглавая мышца бедра расслаблена, или к разгибанию, когда последняя сокращается, не позволяя коленному суставу сгибаться. В - механическое равновесие сил, действующих на предплечье, когда рука держит груз 10 кг. Г - рычажная система руки действует как усилитель по отношению к скорости сокращения двуглавой мышцы плеча, увеличивая скорость перемещения кисти. Система является также усилителем диапазона перемещений кисти (при укорочении мышцы на 1 см кисть перемещается на 7 см)
Нервно-мышечное соединение
Сигналом длязапускасокращения служит потенциал действия плазматической мембраны волокна скелетной мышцы. В скелетных мышцах потенциалы действия можно вызвать только одним способом - раздражением нервных волокон.
Волокна скелетных мышц иннервируются аксонами нервных клеток, называемых мотонейронами (или соматическими эфферентными нейронами). Тела этих клеток расположены в стволе мозга или в спинном мозге. Аксоны мотонейронов покрыты миелиновой оболочкой, а их диаметр больше, чем у других аксонов, поэтому они проводят потенциалы действия с высокой скоростью, обеспечивая поступление сигналов из ЦНС к волокнам скелетных мышц лишь с минимальной задержкой.
Войдя в мышцу, аксон мотонейрона разделяется на множество ветвей, каждая из которых образует одно соединение с мышечным волокном. Один мотонейрон иннервирует много мышечных волокон, но каждым мышечным волокном управляет ветвь только от одного мотонейрона. Мотонейрон вместе с мышечными волокнами, которые он иннервирует, составляет двигательную единицу. Мышечные волокна одной двигательной единицы находятся в одной и той же мышце, но не в виде компактной группы, а рассеяны по мышце. Когда в мотонейроне возникает потенциал действия, все мышечные волокна его двигательной единицы получают стимул к сокращению.
При подходе аксона к поверхности мышечного волокна миелиновая оболочка заканчивается, и аксон образует терминальную часть (нервное окончание) в виде нескольких коротких отростков, располагающихся в желобках на поверхности мышечного волокна. Область плазматической мембраны мышечного волокна, лежащая непосредственно под нервным окончанием, обладает особыми свойствами и называется двигательной концевой пластинкой. Структура, состоящая из нервного окончания и двигательной концевой пластинки, известна как нервно-мышечное соединение (нервно-мышечный синапс).
Терминали аксонов мотонейрона (двигательные нервные окончания) содержат везикулы, заполненные АЦХ. Поступающий от мотонейрона потенциал действия деполяризует плазматическую мембрану нервного окончания, вследствие чего открываются потенциалуправляемые Са2+-каналы, и в нервное окончание входит Са2+ из внеклеточной среды. Ионы Са2+ связываются с белками,
обеспечивающими слияние мембраны везикул с плазматической мембраной нервного окончания, и происходит освобождение АЦХ в синаптическую щель, разделяющую нервное окончание и двигательную концевую пластинку. Молекулы АЦХ диффундируют от нервного окончания к двигательной концевой пластинке, где они связываются с ацетилхолиновыми рецепторами никотинового типа, при этом открываются ионные каналы, проницаемые как для Na+, так и для K+. Из-за разницы трансмембранных электрохимических градиентов этих ионов, входящий в мышечное волокно поток Na+ больше, чем выходящий поток К+, благодаря чему возникает местная деполяризация двигательной концевой пластинки - потенциал концевой пластинки (ПКП). ПКП аналогичен ВПСП в межнейронных синапсах. Однако амплитуда одиночного ПКП существенно выше, чем амплитуда ВПСП, потому что в нервно-мышечном соединении высвобождаемый нейромедиатор попадает на более обширную поверхность, где он связывается с гораздо большим количеством рецепторов, и где, следовательно, открывается намного больше ионных каналов. По этой причине амплитуда одиночного ПКП обычно бывает более чем достаточной для того, чтобы в смежной с концевой пластинкой области плазматической мышечной мембраны возник местный электрический ток, инициирующий потенциал действия. Затем потенциал действия распространяется по поверхности мышечного волокна посредством такого же механизма, что и в мембране аксона. Большинство нервно-мышечных соединений расположено в срединной части мышечного волокна, откуда возникший потенциал действия распространяется к обоим концам волокна. В скелетной мышце человека никогда не возникают тормозные потенциалы. Все нервномышечные соединения - возбуждающие.
Наряду с рецепторами АЦХ на двигательной концевой пластинке присутствует фермент ацетихолинэстераза (АЦХ-эстераза), которая расщепляет АЦХ. По мере того как концентрация свободного АЦХ снижается вследствие его расщепления АЦХ-эстеразой, уменьшается количество АЦХ, способного связываться с рецепторами. Когда не остается рецепторов, связанных с АЦХ, ионные каналы концевой пластинки становятся закрытыми. Деполяризация концевой пластинки завершается, мембранный потенциал возвращается к уровню покоя, и концевая пластинка вновь способна отвечать на АЦХ, высвобождаемый при поступлении к нервному окончанию следующего потенциала действия.
Рис. 4-18. Возбуждение мембраны мышечного волокна: нервно-мышечное соединение

Электромеханическое сопряжение
Ранние исследования изолированного сердца позволили обнаружить, что для сокращения сердечной мышцы необходимы оптимальные концентрации Na+, K+ и Ca2+. Без Na+ сердце невозбудимо, оно не станет биться, так как потенциал действия зависит от внеклеточных ионов натрия. Напротив, потенциал покоящейся мембраны не зависит от трансмембранного градиента ионов Na+. В нормальных условиях внеклеточная концентрация K+ составляет около 4 мМ. Снижение концентрации внеклеточного K+ не оказывает большого влияния на возбуждение и сокращение сердечной мышцы. Однако увеличение концентрации внеклеточного K+ до достаточно высоких уровней вызывает деполяризацию, потерю возбудимости клеток миокарда и остановку сердца в диастоле. Ca2+ также существенно важен для сердечных сокращений. Удаление Ca2+ из внеклеточной жидкости приводит к уменьшению силы сердечных сокращений и последующей остановке сердца в диастоле. Напротив, увеличение концентрации внеклеточного Ca2+ усиливает сердечные сокращения, а очень высокие концентрации Ca2+ приводят к остановке сердца в систоле. Свободный внутриклеточный Ca2+ служит ионом, отвечающим за сократительную способность миокарда.
На двух панелях рисунка показаны механизмы электромеханического сопряжения в сердце, описанные ниже. Возбуждение сердечной мышцы начинается, когда волна возбуждения быстро распространяется вдоль сарколеммы клеток миокарда от клетки к клетке через щелевые контакты. Возбуждение также распространяется внутрь клеток через поперечные трубки, которые инвагинированы в сердечные волокна на Z-полосах. Электростимуляция в области Z-по- лосы или аппликация ионизированного Са2+ в области Z-полосы сердечных волокон, освобожденных от оболочки (с удаленными сарколеммами), вызывает локальное сокращение соседних миофибрилл. Во время плато потенциала действия повышается проницаемость сарколеммы для Са2+. Са2+ входит в клетку по его электрохимическому градиенту через кальциевые каналы сарколеммы и ее инвагинаций, т.е. через мембраны Т-системы.
Считается, что открытие кальциевых каналов происходит в результате фосфорилирования протеинов каналов с помощью циклической аденозинмонофосфатзависимой протеинкиназы (цАМФзависимой протеинкиназы). Первоначальным источником внеклеточного Са2+ служит интерстициальная жидкость (10-3 М Са2+). Некоторое
количество Са2+ может также быть связано с сарколеммой и с гликокаликсом, мукополисахаридом, покрывающим сарколемму. Количество кальция, попадающего внутрь клетки из внеклеточного пространства, недостаточно для того, чтобы вызвать сокращение миофибрилл. Вошедший внутрь кальций («запускающий или триггерный» Са2+) запускает высвобождение Са2+ из саркоплазматического ретикулума (где есть запас внутриклеточного Са2+). Концентрация свободного Са2+ в цитоплазме возрастает от уровня покоя (resting level) примерно в 10-7 М до уровней от 10-6 до 10-5 М во время возбуждения. Затем Са2+ связывается с белком тропонином С. Кальциево-тропониновый комплекс взаимодействует с тропомиозином, чтобы снять блок с активных участков между актиновыми и миозиновыми филаментами. Это снятие блока позволяет образовываться циклическим поперечным связям между актином и миозином и, следовательно, позволяет миофибриллам сокращаться.
Механизмы, повышающие концентрацию Са2+ в цитозоли, увеличивают развиваемую силу сердечных сокращений (active force), а механизмы, которые снижают концентрацию Са2+ в цитозоли, уменьшают ее. Например, катехоламины увеличивают поступление Са2+ в клетку путем фосфорилирования каналов через цАМФ-зависимую протеинкиназу. К тому же катехоламины, подобно другим агонистам, увеличивают силу сердечных сокращений путем повышения чувствительности сократительного механизма к Са2+. Повышение концентрации внеклеточного Са2+ или уменьшение градиента Na+ через сарколемму также приводит к увеличению концентрации Са2+ в цитозоле.
Градиент натрия может быть понижен путем увеличения внутриклеточной концентрации Na+ или путем понижения внеклеточной концентрации Na+. Сердечные гликозиды повышают внутриклеточную концентрацию Na+ путем «отравления» Na+/К+-АТФазы, что приводит к аккумуляции Na+ в клетках. Повышение концентрации Na+ в цитозоле изменяет направление Na+/Са2+-обменника (Na+/Ca2+-exchanger) на противоположное, так что из клетки удаляется меньше Са2+. Пониженная концентрация внеклеточного Na+ служит причиной того, что меньше Na+ входит в клетку, и, таким образом, меньше Na+ заменяется на Са2+.
Достигнутое механическое напряжение (tension) уменьшается за счет снижения концентрации внеклеточного Са2+, увеличения трансмембранного градиента Na+ или применения блокаторов Са2+- каналов, которые препятствуют входу Са2+ в клетки миокарда.
Рис. 4-19. Электромеханическое сопряжение в сердце
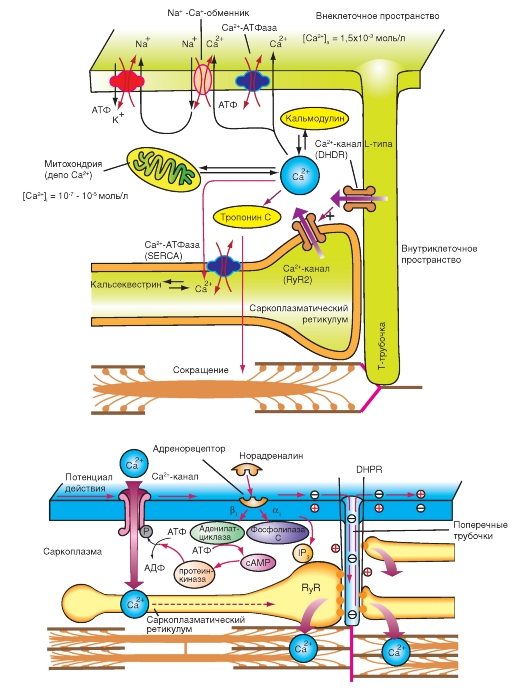
Физиология гладких мышц
Гладкое мышечное волокно - это веретеновидная клетка диаметром от 2 до 10 мкм. В отличие от многоядерных волокон скелетных мышц, которые после завершения дифференцировки уже не могут делиться, гладкие мышечные волокна обладают единственным ядром и способны к делению на протяжении всей жизни организма. Деление начинается в ответ на разнообразные паракринные сигналы, часто - на повреждение ткани.
Значительное разнообразие факторов, модифицирующих сократительную деятельность гладких мышц различных органов, затрудняет классификацию гладких мышечных волокон. Однако есть общий принцип, основанный на электрических характеристиках плазматической мембраны. В соответствии с этим принципом большинство гладких мышц можно отнести к одному из двух типов: унитарные гладкие мышцы (single-unit smooth muscles) с волокнами, связанными в единое целое (рис. 4-20 А), клетки которых взаимодействуют через gap junction, и мультиунитарные гладкие мышцы (multiunit smooth muscles) с индивидуальной иннервацией волокон (рис. 4-20 Б).
Унитарные гладкие мышцы
В мышцах этого типа активность (электрическая и механическая) осуществляется разными клетками синхронно, т.е. на стимулы мышца реагирует как единое целое. Это обусловлено тем, что мышечные волокна связаны друг с другом gap junction (щелевыми контактами), через которые потенциал действия может посредством локальных токов распространяться от одной клетки в соседние. Таким образом, электрическая активность, возникшая в любой клетке унитарных гладких мышц, передается ко всем волокнам (рис. 4-20 А).
Некоторые волокна унитарных гладких мышц обладают пейсмекерными свойствами. В них спонтанно возникают потенциалы действия, которые проводятся через gap junction к волокнам, не обладающим такой активностью. Большинство клеток унитарных гладких мышц не являются пейсмекерными.
На сократительную активность унитарных гладких мышц оказывают влияние электрическая активность нервов, гормоны, локальные факторы;
эти влияния опосредуются механизмами, рассмотренными выше применительно к деятельности всей гладкой мускулатуры. Характер иннервации унитарных гладких мышц существенно варьирует в разных органах. Во многих случаях нервные окончания сосредоточены в тех областях мышцы, где находятся пейсмекерные клетки. Активность всей мышцы может регулироваться посредством изменений частоты потенциалов действия пейсмекерных клеток.
Еще одна особенность унитарных гладких мышц состоит в том, что часто ее волокна сокращаются в ответ на растяжение. Сокращения возникают при растяжении стенок многих полых органов (например, матки), когда возрастает объем их внутреннего содержимого.
Примеры унитарных гладких мышц: мышцы стенок желудочно-кишечного тракта, матки, тонких кровеносных сосудов.
Мультиунитарные гладкие мышцы
Между клетками мультиунитарных гладких мышц мало gap junction, каждое волокно действует независимо от соседних, и мышца ведет себя как множество самостоятельных элементов. Мультиунитарные гладкие мышцы обильно снабжены ветвлениями вегетативных нервов (рис. 4-20 Б). Общий ответ всей мышцы зависит от количества активированных волокон и от частоты нервных импульсов. Хотя поступающие нервные импульсы сопровождаются деполяризацией и сократительными ответами волокон, потенциалы действия в мультиунитарных гладких мышцах, как правило, не генерируются. Сократительная активность мультиунитарных гладких мышц усиливается либо ослабевает в результате поступления с кровью гормонов, однако мультиунитарные гладкие мышцы не сокращаются при растяжении. Примеры мультиунитарных гладких мышц: мышцы в стенках бронхов и крупных артерий и др.
Следует подчеркнуть, что большинство гладких мышц не обладают свойствами исключительно унитарных либо мультиунитарных гладких мышц. В действительности существует непрерывное множество вариаций гладких мышц с разными сочетаниями свойств того и другого типа; унитарные гладкие мышцы и мультиунитарные гладкие мышцы - это две крайности.
Рис. 4-20. Структура гладких мышц
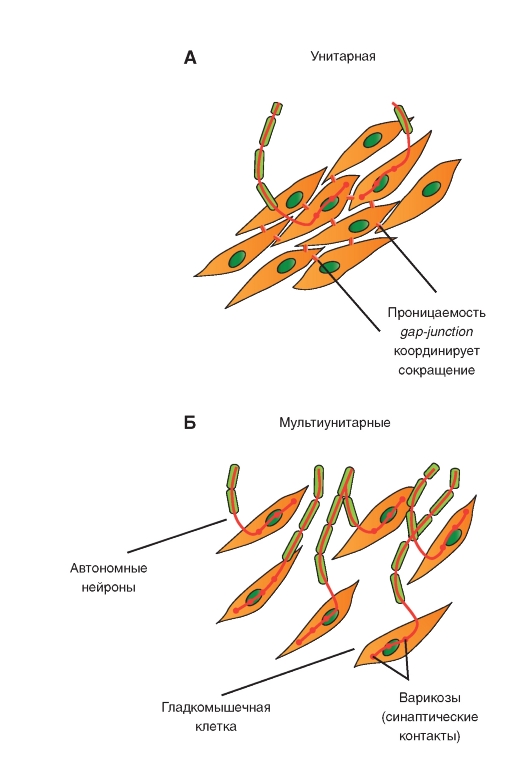
Потенциалы гладких мышц
Некоторые типы гладких мышечных волокон генерируют потенциалы действия спонтанно, при отсутствии всякого нейрогенного или гормонального воздействия. Потенциал покоя плазматической мембраны таких волокон не поддерживается на постоянном уровне, а подвергается постепенной деполяризации до тех пор, пока он не достигнет порогового уровня и не произойдет генерирование потенциала действия. После реполяризации мембраны вновь начинается ее деполяризация (рис. 4-21), так что возникает серия потенциалов действия, вызывающая тоническую сократительную активность. Спонтанные сдвиги потенциала, деполяризующие мембрану до порогового уровня, называются пейсмекерными потенциалами. (Как показано в других главах, часть волокон сердечной мышцы и некоторые типы нейронов ЦНС тоже обладают пейсмекерными потенциалами и могут спонтанно генерировать потенциалы действия при отсутствии внешних стимулов).
Интересно, что в гладких мышцах, способных к генерированию потенциалов действия, переносчиками положительных зарядов в клетку в фазу нарастания потенциала действия служат ионы Са2+, а не Na+, т.е. при деполяризации мембраны открываются потенциалзависимые кальциевые каналы, и потенциалы действия в гладкой мускулатуре имеют кальциевую природу, а не натриевую.
В отличие от поперечно-полосатой мышцы, в гладкой мышце цитоплазматическая концентра-
ция Са2+ может увеличиваться (или уменьшаться) в результате градуальных деполяризационных (или гиперполяризационных) сдвигов мембранного потенциала, увеличивающих (или уменьшающих) число открытых кальциевых каналов плазматической мембраны.
Какую роль в электромеханическом сопряжении играет внеклеточный Са2+? В плазматической мембране гладких мышечных клеток находятся кальциевые каналы двух типов - потенциалзависимые и управляемые химическими посредниками. Поскольку концентрация Са2+ во внеклеточной жидкости в 10 000 раз выше, чем в цитоплазме, открывание кальциевых каналов плазматической мембраны сопровождается входом Са2+ в клетку. Благодаря небольшим размерам волокна, вошедшие ионы Са2+ быстро достигают путем диффузии внутриклеточных участков связывания.
Еще одно различие заключается в том, что если в скелетной мышце одиночный потенциал действия высвобождает достаточное количество Са2+ для включения всех поперечных мостиков волокна, то в гладкой мышце в ответ на большинство стимулов активируется только часть поперечных мостиков. Именно поэтому, гладкое мышечное волокно генерирует напряжение постепенно, по мере изменения цитоплазматической концентрации Са2+. Чем значительнее прирост концентрации Са2+, тем большее число поперечных мостиков активируется, и тем больше генерируемое напряжение.
Рис. 4-21. Электрические потенциалы гладких мышц
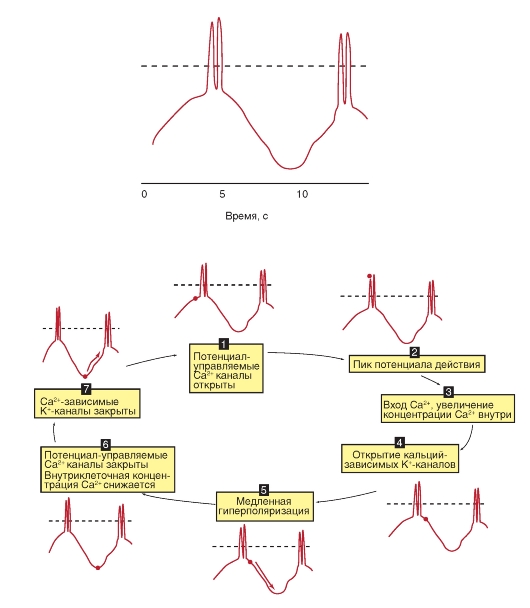
Источники поступления кальция в цитоплазму
Повышение концентрации Са2+ в цитоплазме, благодаря чему инициируется сокращение гладкой мышцы, обеспечивается из двух источников: (1) саркоплазматического ретикулума и (2) внеклеточной среды, из которой Са2+ входит в клетку через кальциевые каналы плазматической мембраны. Относительный вклад этих двух источников Са2+ варьирует для разных гладких мышц. Некоторые из них в большей мере зависят от внеклеточной концентрации Са2+, другие - от Са2+, депонированного в саркоплазматическом ретикулуме.
Саркоплазматический ретикулум гладких мышц
Что касается саркоплазматического ретикулума, то в гладкой мышце он развит слабее, чем в скелетной мышце, и не имеет специфической организации, которая коррелировала бы с расположением толстых и тонких филаментов (рис. 4- 22 А). Кроме того, в гладкой мышце отсутствуют Т-трубочки, соединенные с плазматической мембраной. Поскольку диаметр гладкого мышечного волокна невелик, а сокращение развивается медленно, нет функциональной необходимости в быстром распространении возбуждающего сигнала вглубь волокна. Вместе с тем между участками плазматической мембраны и саркоплазматического ретикулума наблюдаются особые структуры,
аналогичные специализированным контактам между мембранами Т-трубочек и латеральных мешков в поперечно-полосатых волокнах. Эти структуры осуществляют сопряжение между потенциалом действия плазматической мембраны и высвобождением Са2+ из саркоплазматического ретикулума. В инициации высвобождения Са2+ из областей саркоплазматического ретикулума, находящихся в центре волокна, участвуют вторичные посредники, высвобождаемые плазматической мембраной или образующиеся в цитоплазме в ответ на связывание внеклеточных химических медиаторов с рецепторами плазматической мембраны (рис. 4-22 В).
В некоторых гладких мышцах концентрация Са2+ достаточна для поддержания активности поперечных мостиков на определенном низком уровне даже при отсутствии внешних стимулов. Такое явление носит название тонус гладкой мускулатуры. Интенсивность тонуса изменяют факторы, воздействующие на цитоплазматическую концентрацию Са2+.
Удаление Са2+ из цитоплазмы, необходимое для того, чтобы волокно расслабилось, происходит посредством активного транспорта Са2+ обратно в саркоплазматический ретикулум, а также через плазматическую мембрану во внеклеточную среду. Скорость удаления Са2+ в гладкой мышце гораздо меньше, чем в скелетной. Отсюда и разная продолжительность одиночного сокращения - несколько секунд для гладкой мышцы и доли секунды для скелетной.
Механизмы обмена кальцием представлены на
рис. 4-22 Г.
Рис. 4-22. Саркоплазматический ретикулyм гладких мышц.
А - структура саркоплазматического ретикулума. Б - источники поступления кальция через ионные каналы. В - источники поступления кальция через насосы и обменники
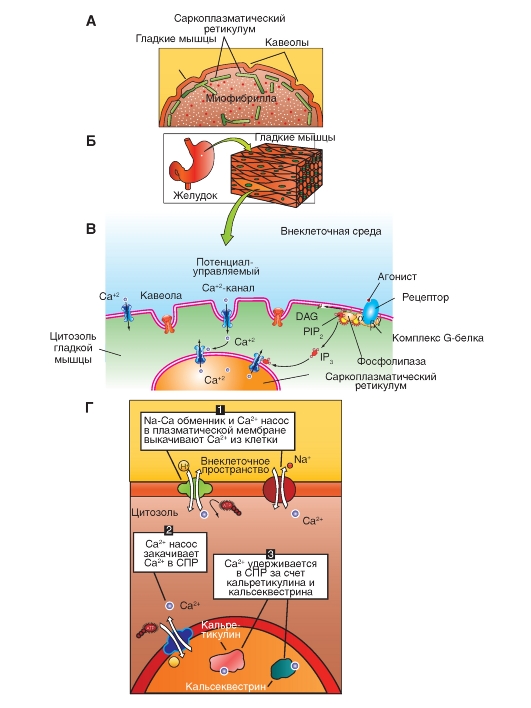
Сокращения гладких мышц
В цитоплазме гладких мышечных волокон присутствуют два вида филаментов: толстые миозинсодержащие и тонкие актинсодержащие. Тонкие филаменты прикреплены либо к плазматической мембране, либо к цитоплазматическим структурам - так называемым плотным тельцам (функциональные аналоги Z-полос поперечно-полосатых волокон). В расслабленном гладком мышечном волокне филаменты обоего вида ориентированы под косым углом к длинной оси клетки. Во время укорочения волокна участки плазматической мембраны, находящиеся между точками прикрепления актина, выбухают. Толстые и тонкие филаменты не объединены в миофибриллы, как в поперечно-полосатых мышцах, и не образуют регулярно повторяющихся саркомеров, поэтому не наблюдается поперечная исчерченность. Тем не менее сокращение гладких мышц происходит посредством механизма скользящих нитей.
Концентрация миозина в гладкой мышце составляет лишь около одной трети от его содержания в поперечно-полосатой мышце, в то время как содержание актина может быть в два раза больше. Несмотря на эти различия, максимальное напряжение на единицу площади поперечного сечения, развиваемое гладкими и скелетными мышцами, схоже.
Соотношение между изометрическим напряжением и длиной для гладких мышечных волокон количественно такое же, как для волокон скелетной мышцы. При оптимальной длине волокна развивается максимальное напряжение, а при сдвигах длины в обе стороны от ее оптимального значения напряжение уменьшается. Однако гладкая мышца, по сравнению со скелетной мышцей, способна развивать напряжение в более широком диапазоне значений длины. Это важное адаптационное свойство, если учесть, что большинство гладких мышц входит в состав стенок полых органов, при изменении объема которых меняется и длина мышечных волокон. Даже при относительно большом увеличении объема, как, например, при заполнении мочевого пузыря, гладкие мышечные волокна в его стенках сохраняют в определенной мере способность к развитию напряжения; в поперечно-полосатых волокнах подобное растяжение могло бы привести к расхождению толстых и тонких филаментов за пределы зоны их перекрывания.
Так же как в поперечно-полосатой мышце, в гладких мышечных волокнах сократительная активность регулируется изменениями цитоплазматической концентрации ионов Са2+. Однако эти два типа мышц существенно различаются по механизму влияния Са2+ на активность поперечных мостиков и изменений концентрации Са2+ в ответ на стимуляцию.
Рис. 4-23. В гладкой мышце толстые и тонкие филаменты ориентированы под углом к осям волокна и прикреплены к плазматической мембране или к плотным тельцам в цитоплазме. При активации мышечных клеток толстые и тонкие филаменты скользят друг относительно друга так, что клетки укорачиваются и утолщаются
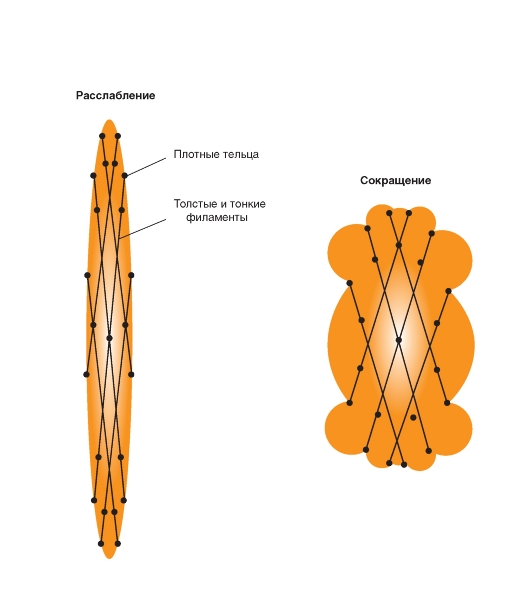
Активация поперечных мостиков
В тонких филаментах гладких мышц нет связывающего Са2+-белка тропонина С, который опосредует триггерную роль Са2+ по отношению к активности поперечных мостиков в скелетной мышце и в миокарде. Вместо этого цикл поперечных мостиков в гладкой мышце контролируется Са2+-регулируемым ферментом, фосфорилирующим миозин. Только фосфорилированная форма миозина в гладкой мышце может связываться с актином и обеспечивать циклы движений поперечных мостиков.
Рассмотрим процесс сокращения гладкой мышцы в деталях. Увеличение уровня Са2+ в цитоплазме инициирует медленную цепь событий, приводящих, с одной стороны, к освобождению активного центра связывания с миозином на актине и, с другой стороны, к увеличению активности АТФазы миозина, и без этого увеличения активности АТФазы миозина в гладкой мышце сокращение не может начаться.
Первая фаза процесса активации головки миозина заключается в связывании 4 ионов Са2+ с кальмодулином (СаМ), который в этом смысле очень похож на тропонин С поперечно-полосатой мышцы. Далее комплекс Са2+-СаМ активирует фермент, называемый киназой легкой цепи миозина (КЛЦМ) (myosin light chain kinase, MLCK). КЛЦМ содержит АТФ-связывающий домен и активный центр, обеспечивающий перенос фосфата с АТФ на белок-акцептор. По этому механизму КЛЦМ, в свою очередь, фосфорилирует легкую регуляторную цепь, ассоциированную с головкой молекулы миозина II. Фосфорилирование легкой цепи меняет конформацию головки миозина II, которая достаточно изменена увеличением своей АТФазной активности, что и позволяет ей взаимодействовать с актином. То есть система работает как молекулярный мотор (рис. 4-23 А).
На рисунке 4-23 Б представлены два независимых каскада, приводящих к сокращению гладкой мышцы. Каскад (1) включает механизм освобождения от блокирования активного центра актина, с которым должен связаться миозин. Каскад (2) включает механизм активации головки миозина. Итог этих двух каскадов состоит в формировании актомиозинового комплекса.
Рассмотрим первый каскад освобождения от блокирования активного центра актина. Два белка, кальдесмон и кальпомин, блокируют возможность связи актина с миозином. Оба представляют собой Са2+-СаМ, связывающие протеины, и оба связывают актин. С одной стороны, Са2+ связывается с СаМ, и комплекс Са2+-СаМ действует двояко на кальпонин. Первый эффект - комплекс Са2+-СаМ связывается с кальпонином. Второй эффект - комплекс Са2+-СаМ активирует Са2+-СаМ-зависимую протеинкиназу, которая фосфорилирует кальпонин. Оба эффекта уменьшают ингибирование кальпонином АТФазной
активности миозина. Кальдесмон также ингибирует АТФазную активность миозина гладкой мышцы. С другой стороны, Са2+ связывается с СаМ, а комплекс Са2+-СаМ связывается через Pi с кальдесмоном, что сдвигает последний от центра связывания актина с миозином. Центр связывания на актине открывается.
Рассмотрим второй каскад, который представлен на панели А. Первая фаза процесса активации головки миозина заключается в связывании четырех ионов Са2+ с СаМ. Сформировавшийся комплекс Са2+-СаМ активирует КЛЦМ. КЛЦМ фосфорилирует легкую регуляторную цепь, ассоциированную с головкой молекулы миозина II. Фосфорилирование легкой цепи меняет конформацию головки миозина II, которая достаточно изменена увеличением своей АТФазной активности, что и позволяет ей взаимодействовать с актином.
В итоге актомиозиновый комплекс оказывается сформированным.
Гладкомышечная изоформа АТФазы миозина характеризуется очень низкой максимальной активностью, примерно в 10-100 раз ниже, чем активность АТФазы миозина скелетной мышцы. Поскольку от скорости гидролиза АТФ зависит скорость циклических движений поперечных мостиков и соответственно скорость укорочения, гладкая мышца сокращается гораздо медленнее, чем скелетная. Кроме того, гладкая мышца не утомляется во время продолжительной активности.
Чтобы после сокращения гладкая мышца расслабилась, необходимо дефосфорилирование миозина, так как дефосфорилированный миозин не может быть связан с актином. Этот процесс катализируется фосфатазой легких цепей миозина, активной в течение всего времени покоя и сокращения гладкой мышцы. При повышении цитоплазматической концентрации Са2+ скорость фосфорилирования миозина активной киназой становится выше, чем скорость его дефосфорилирования фосфатазой, и количество фосфорилированного миозина в клетке возрастает, обеспечивая развитие напряжения. Когда концентрация Са2+ в цитоплазме снижается, скорость дефосфорилирования становится выше, чем скорость фосфорилирования, количество фосфорилированного миозина падает, и гладкая мышца расслабляется.
При сохранении повышенного уровня цитоплазматического Са2+ скорость гидролиза АТФ миозином поперечных мостиков падает, несмотря на сохраняющееся изометрическое напряжение. Если фосфорилированный поперечный мостик, прикрепленный к актину, подвергается дефосфорилированию, он окажется в состоянии стойкого ригидного напряжения, оставаясь неподвижным. Когда такие дефосфорилированные поперечные мостики связываются с АТФ, они диссоциируют от актина гораздо медленнее. Таким образом, обеспечивается способность гладкой мышцы длительно поддерживать напряжение при невысоком потреблении АТФ.